Урок 24. строение атома. опыты резерфорда – Физика – 11 класс
Физика, 11 класс
Урок №24. Строение атома. Опыты Резерфорда
На уроке рассматриваются: понятия атомное ядро, опыты Резерфорда, планетарная модель строения атома; сравниваются модели атома Томсона и Резерфорда, даны некоторые сведения о фактах, подтверждающих сложное строение атома, о работах учёных по созданию модели строения атома.
Атомное ядро — тело малых размеров, в котором сконцентрирована почти вся масса и весь положительный заряд атома.
Размеры ядра: диаметр порядка 10-12—10-13 см (у разных ядер диаметры различны).
Размер атома: примерно 10-8 см, т. е. от 10 до 100 тысяч раз превышает размеры ядра.
Планетарная модель атома Резерфорда: в целом атом нейтрален, в центре атома расположено положительно заряжённое ядро, в котором сосредоточена почти вся масса атома, электроны движутся по орбитам вокруг ядра, заряд ядра, как и число электронов в атоме, равен порядковому номеру элемента в периодической системе Д.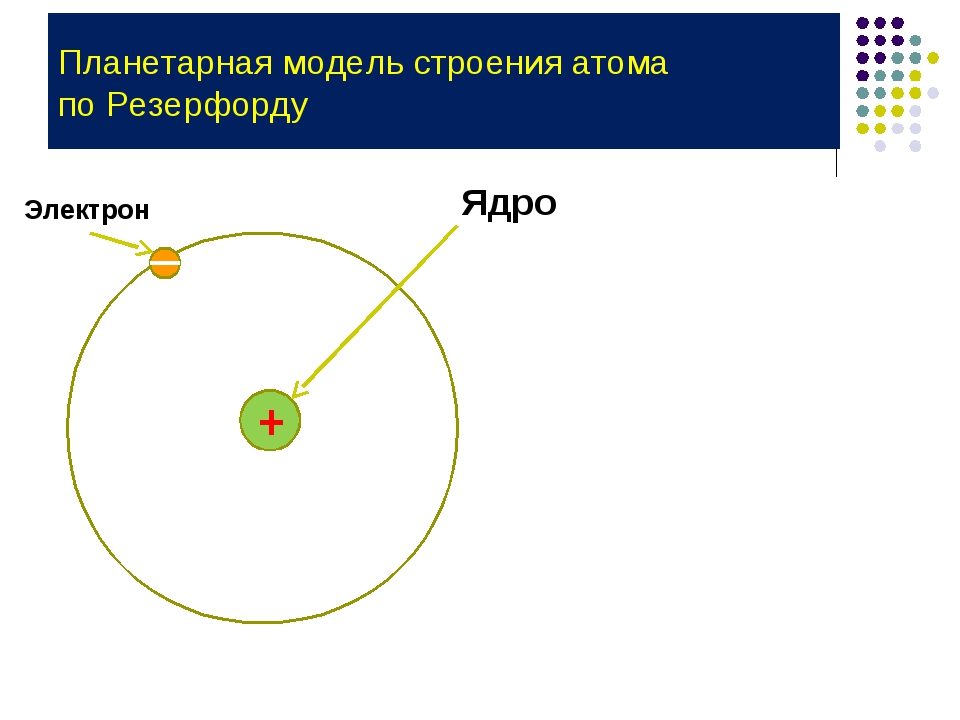
Ядро атома водорода названо протоном и рассматривается как элементарная частица.
Ядро атома водорода имеет положительный заряд, равный по модулю заряду электрона, и массу, примерно в 1836,1 раза больше массы электрона.
Частота излучений атома водорода составляет ряд серий: серия Бальмера, серия Лаймана, серия Пашена и другие, каждая из которых образуется в процессе перехода атома в одно из энергетических состояний.
Обязательная литература по теме урока:
- Мякишев Г.Я., Буховцев Б.Б., Сотский Н.Н. Физика.11 класс. Учебник для общеобразовательных организаций М.: Просвещение, 2017. – С. 279 – 283.
- Степанова Г.Н. (сост.) Сборник задач по физике для 10-11 классов общеобразовательных учреждений.5-е изд., доп. — М.: «Просвещение», 1999 — С. 221-222
- Анциферов Л.И., Физика: электродинамика и квантовая физика. 11кл. Учебник для общеобразовательных учреждений. – М.: Мнемозина, 2001. – С. 270-274.
- Рымкевич А.
 П. Физика. Задачник. 10-11 классы. – М.: Дрофа, 2013. — С. 155 – 156.
П. Физика. Задачник. 10-11 классы. – М.: Дрофа, 2013. — С. 155 – 156. - Кикоин А. К. За пределы таблицы //Квант. — 1991. — № 1. — С. 38,39,42-44
Основное содержание урока
Долгое время, физика накапливала факты о свойстве вещества для полного представления о строении атома. И только в XIX веке изучение атомического строения вещества существенно сдвинулось с точки покоя.
Большую роль в развитии атомистической теории сыграл выдающийся русский химик Дмитрий Иванович Менделеев, разработавший в 1869 году периодическую систему элементов, в которой впервые был поставлен вопрос о единой природе атомов.
Важным свидетельством сложной структуры атомов явились исследования спектров, излучаемые веществом, которые привели к открытию линейчатых спектров атомов. В начале XIX века в излучении атома водорода были открыты спектральные линии в видимой части спектра.
Идеи электронной структуры атома теоретически и гипотетически формулировались учёными. В 1896 году Хендрик Лоренц создал электронную теорию о том, что электроны являются частью атома.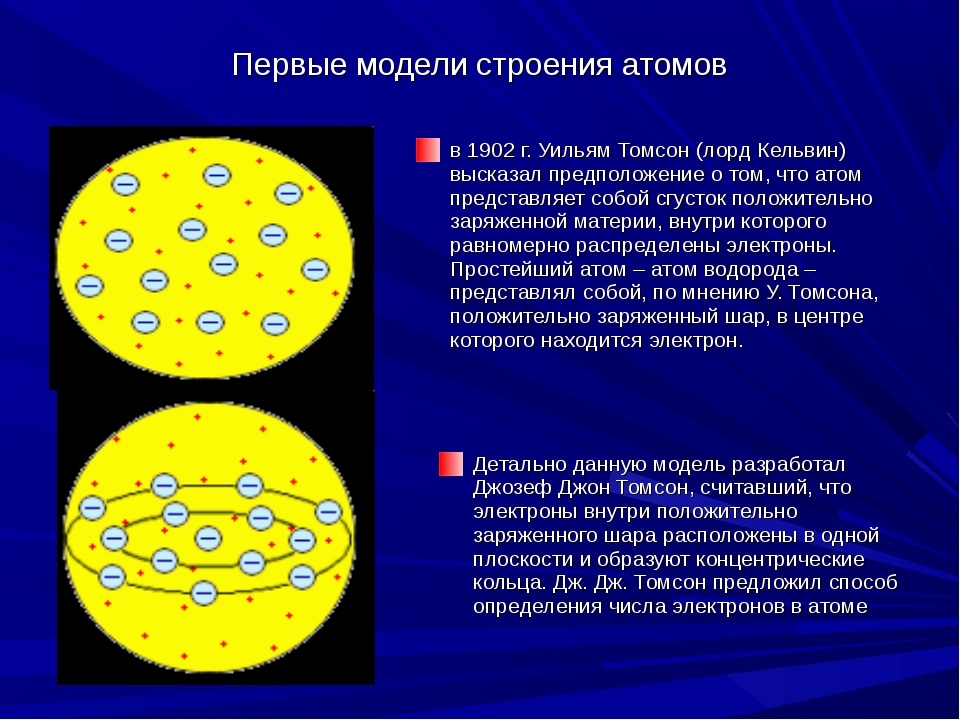 Эту гипотезу в 1897 году подтвердили эксперименты Джозефа Джона Томсона. Им был сформулирован вывод о том, что существуют частицы с наименьшим отрицательным зарядом – электроны и они являются частью атомов.
Эту гипотезу в 1897 году подтвердили эксперименты Джозефа Джона Томсона. Им был сформулирован вывод о том, что существуют частицы с наименьшим отрицательным зарядом – электроны и они являются частью атомов.
По мысли Томсона, положительный заряд занимает весь объём атома и распределён он в этом сферическом объёме равномерно. У более сложных атомов в положительно заряжённом шаре есть несколько электронов, так что атом подобен кексу, в котором роль изюма играют электроны. Распространённый термин этой модели – «Пудинг с изюмом» или «Булочка с изюмом».
Таким образом, к началу XX века учёные сделали вывод о том, что атомы материи имеют сложную внутреннюю структуру. Они являются электрически нейтральными системами, а носителями отрицательного заряда атомов являются лёгкие электроны, масса которых составляет лишь малую долю массы атомов. Однако модель атома Томсона находилась в полном противоречии с экспериментами по изучению распределения положительных зарядов.
Электрон – наименьшая электроотрицательная заряжённая элементарная частица
Масса покоя электрона me = 9,1·10
– отношение заряда электрона к его массе.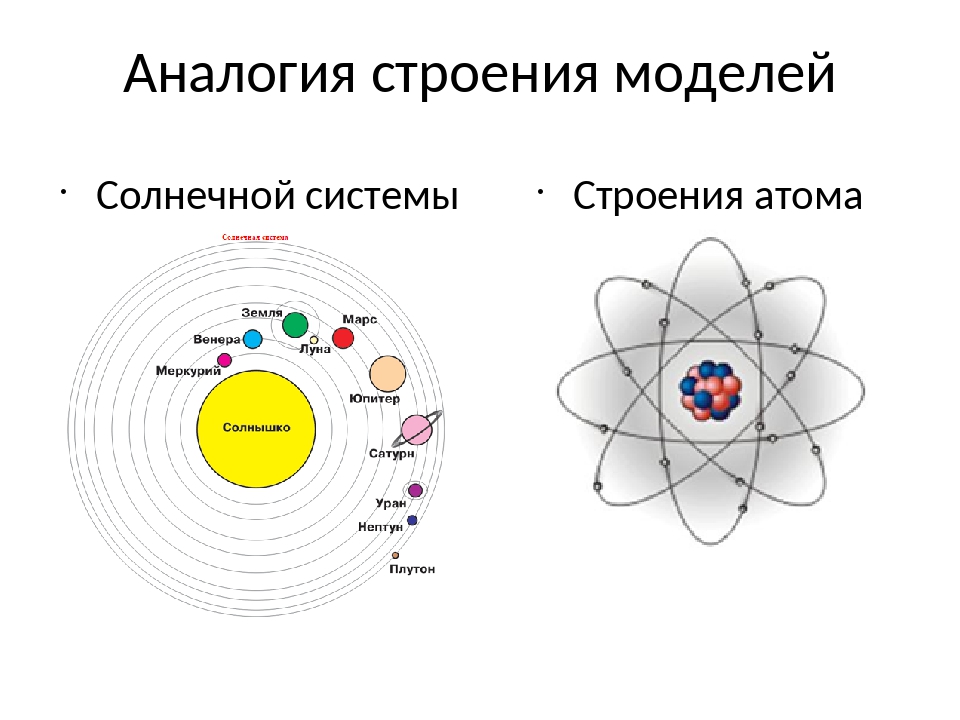
Немецкий физик Филипп фон Ленард в 1903 году проводил опыты, в которых пучок быстрых электронов легко проходил через тонкую металлическую фольгу. На основании этого Ленард предположил, что атом состоит из нейтральных частиц или нейтральных дуплетов с совмещённым положительным и отрицательным зарядами, рассредоточенными в атоме, где большая площадь представляет собой пустоту.
В 1904 году японский физик Хентаро Нагаока выдвинул гипотезу о том, что атом состоит из тяжелого положительно заряженного ядра, окруженного кольцами из большого числа электронов, колебания которых и являются причиной испускания атомных спектров, по аналогии с теорией устойчивости колец Сатурна.
Но в физике уже более 200 лет существует главное правило: окончательный выбор между гипотезами может быть сделан только на основе опыта. Эксперименты, проведенные в первый раз Эрнестом Резерфордом, сыграли решающую роль в понимании структуры атома.
30.08.1871 г. – 19.10.1937 г.
Эрнест Резерфорд
Британский физик новозеландского происхождения
Лауреат Нобелевской премии по химии 1908 года
Для экспериментального изучения распределения положительного заряда, а значит, и массы внутри атома Эрнест Резерфорд в 1906 г.
Эти частицы возникают при распаде, например, радия и некоторых других радиоактивных элементов. Сами же α-частицы – это ионизированные атомы гелия, положительный заряд гелия в два раза больше заряда электрона +2He. Этими частицами Резерфорд бомбардировал атомы тяжёлых элементов (золото, медь и др.). Если бы электроны были равномерно распределены по всему объёму атома (по модели атома Томсона), электроны не могли бы заметно изменять траекторию α –частиц, так как размеры и масса электронов в 8000 раз меньше массы α-частиц. Точно так же камушек в несколько десятков граммов при столкновении с автомобилем не может изменить его скорость.
Изменение направления движения α-частиц может вызвать только массивная часть атома, при этом положительно заряжённая. Весь прибор размещался в сосуде, из которого был откачан воздух. Радиоактивный препарат, помещался внутри свинцового цилиндра, вдоль которого был высверлен узкий канал.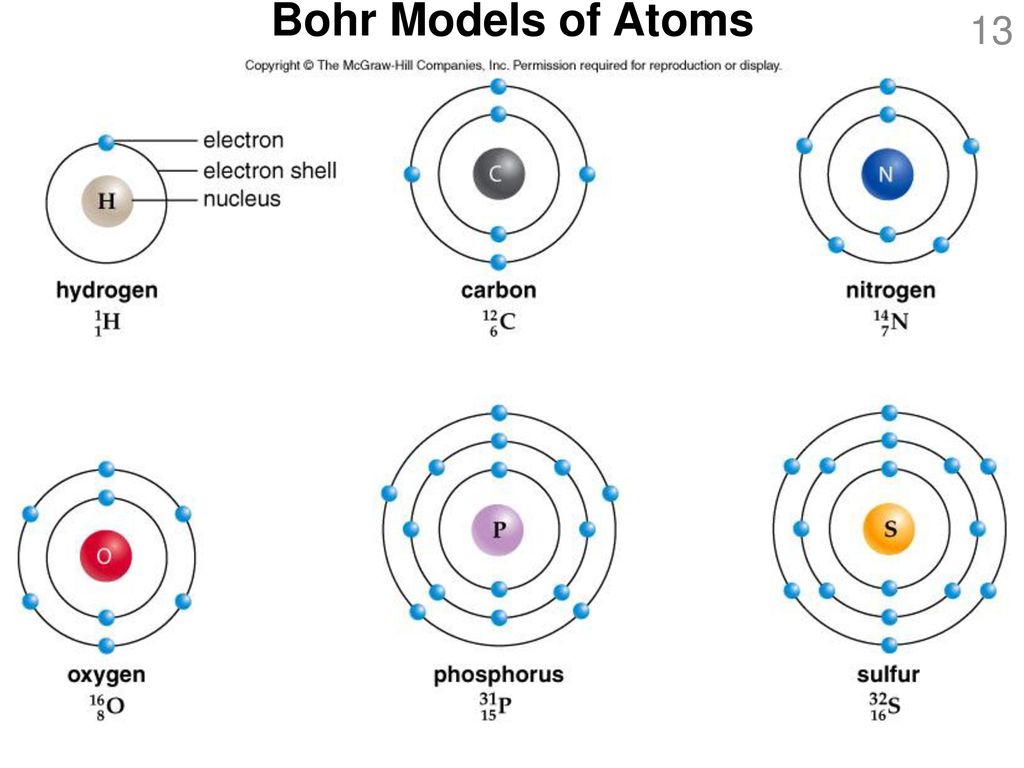 Пучок α -частиц из канала падал на тонкую фольгу из тяжёлого металла. После рассеяния α-частицы попадали на полупрозрачный экран, покрытый сульфидом цинка. Столкновение каждой частицы с экраном сопровождалось сцинтилляцией (вспышкой света), которую можно было наблюдать в микроскоп.
Пучок α -частиц из канала падал на тонкую фольгу из тяжёлого металла. После рассеяния α-частицы попадали на полупрозрачный экран, покрытый сульфидом цинка. Столкновение каждой частицы с экраном сопровождалось сцинтилляцией (вспышкой света), которую можно было наблюдать в микроскоп.
Чтобы обнаружить отклонение α-частиц на большие углы Резерфорд окружил фольгу экранами. Сотрудники Резерфорда вели счёт α-частиц, попадающих в регистрирующее устройство при отклонении их на от первоначального направления на определённый угол φ (фи). Данные из серии опытов, за определённый период времени, приведены в таблице:
Угол отклонения α-частиц φ, ° | 15 | 60 | 105 | 150 | 180 |
Число частиц N | 132000 | 477 | 70 | 33 | 1-3 |
Отсюда можно сделать вывод: такое поведение α-частиц возможно только в том случае, если они упруго взаимодействуют с массивным положительно заряжённым телом малых по сравнению с атомом размеров.
Позднее Резерфорд признался, что, предложив своим ученикам провести эксперимент по наблюдению за рассеянием α-частиц, он сам не верил в положительный результат. Он сравнил такой эффект с 15-дюймовым снарядом, как если бы его выстрелили в кусок тонкой бумаги, а снаряд возвратился бы и нанёс обратный удар.
Резерфорд понял, что α-частица могла быть отброшена назад лишь в том случае, если положительный заряд атома и его масса сконцентрированы в очень малой области пространства. Так Резерфорд пришел к мысли о существовании атомного ядра.
Подсчитывая число α-частиц, рассеянных на различные углы, Резерфорд смог оценить размеры ядра. Оказалось, что ядро имеет диаметр порядка 10-12—10-13 см (у разных ядер диаметры различны). Размер же самого атома 10-8 см, то есть от 10 до 100 тысяч раз превышает размеры ядра. Впоследствии удалось определить и заряд ядра.
Планетарная модель атома Резерфорда: в целом атом нейтрален, в центре атома расположено положительно заряженное ядро, в котором сосредоточена почти вся масса атома.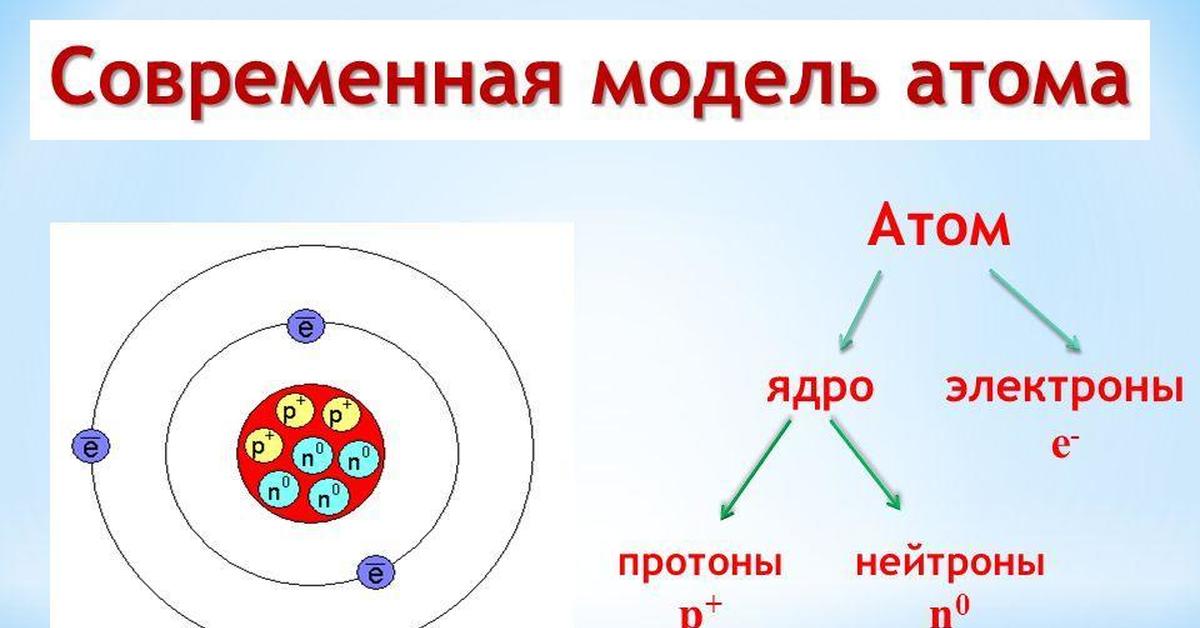
Электроны движутся вокруг ядра, подобно тому как планеты обращаются вокруг Солнца.
Такой характер движения электронов определяется действием кулоновских сил притяжения со стороны ядра.
Закон Кулона:
qα — заряд α-частицы;
q — положительный заряд атома;
r — его радиус;
— коэффициент пропорциональности.
Ядро атома водорода имеет положительный заряд, который по модулю равен заряду электрона, и массу, примерно в 1836,1 раза больше массы электрона.
Размер атома водорода — это радиус орбиты его электрона
Простая и наглядная планетарная модель атома имеет прямое экспериментальное обоснование. Она кажется совершенно необходимой для объяснения опытов по рассеиванию α-частиц. Но на основе этой модели нельзя объяснить факт существования атома, его устойчивость. Ведь движение электронов по орбитам происходит с ускорением.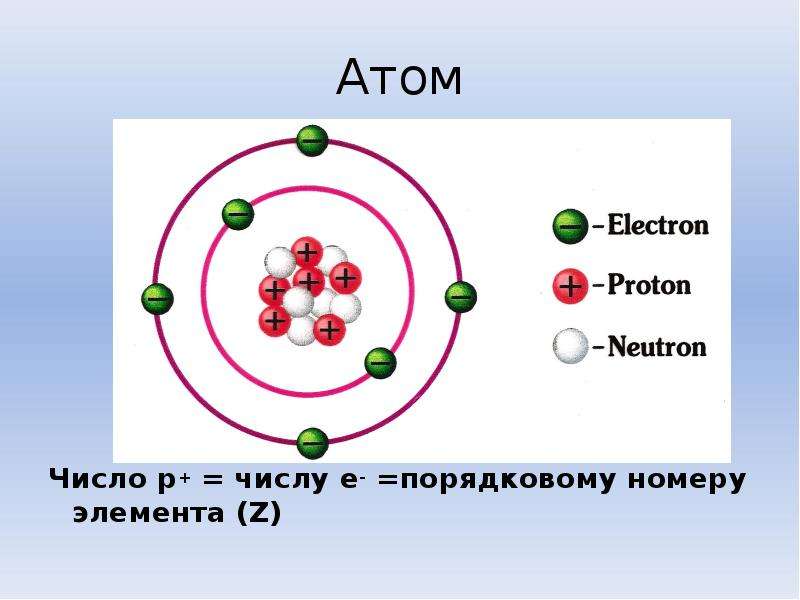 Ускоренно движущийся заряд должен излучать электромагнитные волны с частотой, равной частоте его обращения вокруг ядра. Электроны должны приближаться к ядру, подобно тому как спутник приближается к Земле при торможении в верхних слоях атмосферы. Атом должен прекратить свое существование. В действительности ничего подобного не происходит. Атомы устойчивы и в невозбужденном состоянии могут существовать неограниченно долго, совершенно не излучая электромагнитные волны
Ускоренно движущийся заряд должен излучать электромагнитные волны с частотой, равной частоте его обращения вокруг ядра. Электроны должны приближаться к ядру, подобно тому как спутник приближается к Земле при торможении в верхних слоях атмосферы. Атом должен прекратить свое существование. В действительности ничего подобного не происходит. Атомы устойчивы и в невозбужденном состоянии могут существовать неограниченно долго, совершенно не излучая электромагнитные волны
В начале XX века было уже известно, что вещество излучает свет конкретных длин волн в определенных, очень узких спектральных интервалах – спектральных линиях, все линии имеют конечную длину.
Линейчатые спектры дают все вещества в газообразном атомарном (но не молекулярном состоянии). Классическим примером линейчатого спектра является спектр атома водорода.
Швейцарский физик и математикИоганн Якоб Бальмер определил, что в видимой части спектра атома водорода имеются четыре линии, соответствующие длинам волн: λ1 = 434 нм; λ2 = 486 нм; λ3 = 410 нм; λ4 = 656 нм
Частота излучений атома водорода составляет ряд серий, каждая из которых образуется в процессе перехода атома в одно из энергетических состояний, переходов электрона с верхних энергетических уровней на нижние уровни.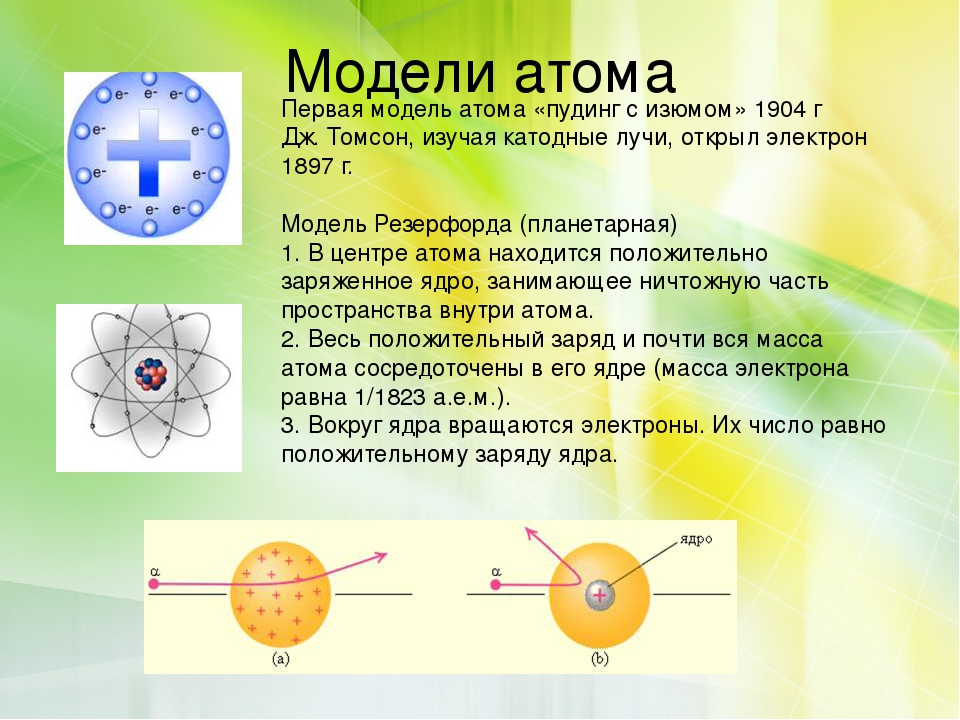
На рисунке можно увидеть переходы электрона на другой энергетический уровень, частоты излучения которого находятся в видимой области спектра.
Серию уровней назвали в честь швейцарского учителя Иоганна Бальмера, который ещё в 1885 году основываясь на результатах экспериментов вывел формулу для определения частот видимой части спектра водорода:
где Z – число протонов в атоме или порядковый номер в периодической таблице Менделеева;
n и m (целое число – 1, 2, 3, 4, 5, и так далее) – энергетические уровни, где m > n.
В этой формуле v — не частота, которая измеряется в с-1, а волновое число, которое равно обратному значению длины волны 1/λ и которое измеряется в м-1.
R — это постоянная Ридберга (для данного вещества), которая определена из спектральных данных, учитывая, что скорость распространения видимого излучения составляет:
Не согласующийся с опытом вывод о неизбежной гибели атома вследствие потери энергии на излучение — это результат применения законов классической физики к явлениям, происходящим внутри атома. Отсюда следует, что к таким явлениям законы классической физики неприменимы. Все выводы об устойчивости атома и спектре, которые излучает атом будут подтверждены Нильсом Бором в 1913 году.
Отсюда следует, что к таким явлениям законы классической физики неприменимы. Все выводы об устойчивости атома и спектре, которые излучает атом будут подтверждены Нильсом Бором в 1913 году.
Рассмотрим задачи тренировочного блока урока.
1. Формула Бальмера – Ридберга для водорода приводится в виде:
Коэффициент RH носит название постоянной Ридберга для водорода и его можно вычислить из данной формулы. Полученный результат равен _______·107 м-1, если известно, что при переходе атома водорода из четвёртого энергетического состояния во второе происходит излучение с длиной волны 486,13 нм.
Дано:
m = 4
n = 2
RH – ?
Решение:
Постоянная Ридберга для водорода:
Выведем постоянную Ридберга RH из формулы Бальмера – Ридберга:
Подставим известные значения в формулу:
Ответ:
2. Рассчитайте на какое наименьшее расстояние α-частица может приблизиться к ядру атома золота, двигаясь по прямой, проходящей через центр ядра. Масса α-частицы, её заряд, скорость движения и заряд ядра золота приведены в таблице:
Масса α-частицы, её заряд, скорость движения и заряд ядра золота приведены в таблице:
Масса α-частицы, кг | Заряд α-частицы, Кл | Скорость движения α-частицы, м/с | Заряд ядра золота, Кл | Расстояние сближения, м |
6,6·10-27 | 3,2·10-19 | 1,9·107 | 1,3·10-17 | ? |
По закону сохранения энергии максимальная кинетическая энергия α-частицы будет равна максимальной потенциальной энергии взаимодействия частицы с ядром атома золота:
Потенциальная энергия кулоновского взаимодействия зарядов.
Для определения наименьшего расстояния между α-частицей и ядра атома золота используем формулу взаимодействия заряжённых частиц – закон Кулона:
— коэффициент пропорциональности.
Чтобы определить силу взаимодействия зарядов на кратчайшем расстоянии, запишем II закон Ньютона, устанавливающий зависимость силы от ускорения, для движения тела движущегося по окружности с центростремительным ускорением:
Приравняем выражения для силы взаимодействия двух точечных зарядов:
Отсюда выразим расстояние сближения двух зарядов, считая его радиусом от центра ядра золота до точки сближения с α-частицей:
Подставим числовые значения в полученную формулу:
Ответ:
Масса α-частицы, кг | Заряд α-частицы, Кл | Скорость движения α-частицы, м/с | Заряд ядра золота, Кл | Расстояние сближения, м |
6,6·10-27 | 3,2·10-19 | 1,9·107 | 1,3·10-17 | 3,1·10-14 |
Строение атома.
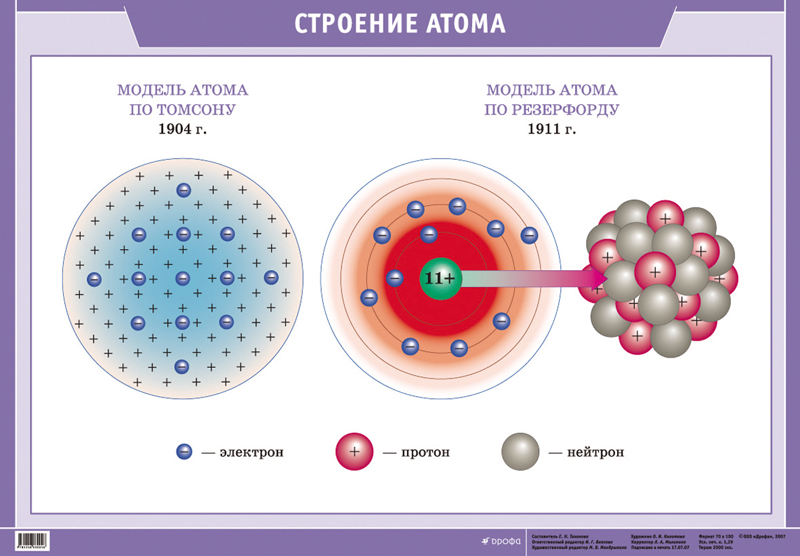 Модель томпсона. Опыты Резерфорда. Планетарная модель
Модель томпсона. Опыты Резерфорда. Планетарная модель
Автор статьи — профессиональный репетитор, автор учебных пособий для подготовки к ЕГЭ Игорь Вячеславович Яковлев
Темы кодификатора ЕГЭ: планетарная модель атома.Атомы каждого химического элемента имеют строго индивидуальный линейчатый спектр, присущий только данному элементу и не меняющийся от опыта к опыту. Как это можно объяснить? Как вывести формулу, дающую весь набор частот атомного спектра? Чтобы сделать это, нужно узнать, как устроен атом.
Модель Томсона
Первую модель строения атома придумал английский физик Джозеф Джон Томсон (удостоенный Нобелевской премии за открытие электрона). В конечном счёте она оказалась неверной, но сыграла важную роль, будучи стимулом последующих экспериментальных исследований Резерфорда. Физики называли модель Томсона «пудинг с изюмом».
Согласно Томсону атом представляет собой шар размером порядка см. По этому шару некоторым образом распределён положительный заряд, а внутри шара, подобно изюминкам, находятся электроны (рис. 1).
По этому шару некоторым образом распределён положительный заряд, а внутри шара, подобно изюминкам, находятся электроны (рис. 1).
Рис. 1. Модель атома Томсона
Суммарный заряд электронов в точности равен положительному заряду шара, поэтому атом в целом электрически нейтрален.
Излучение атомов объясняется колебаниями электронов около положений равновесия (как вы помните, любой ускоренно движущийся заряд излучает электромагнитные волны). Однако вся совокупность экспериментальных данных по атомным спектрам не укладывалась в модель Томсона. Например, для некоторых химических элементов были подобраны формулы, хорошо описывающие их спектры, но эти формулы из модели Томсона никак не следовали.
Опыты Резерфорда
Верна ли модель Томсона? Как в действительности распределены положительные и отрицательные заряды внутри атома? Чтобы ответить на эти вопросы, нужен был эксперимент, позволяющий проникнуть внутрь атома. Ученик Томсона, знаменитый английский физик Эрнест Резерфорд предложил с этой целью бомбардировать атом высокоэнергетичными ?-частицами и смотреть, как они будут отклоняться положительным зарядом атома.
Ученик Томсона, знаменитый английский физик Эрнест Резерфорд предложил с этой целью бомбардировать атом высокоэнергетичными ?-частицами и смотреть, как они будут отклоняться положительным зарядом атома.
Что такое -частицы? Потоки этих частиц — так называемые «альфа-лучи» — были обнаружены при радиоактивном распаде некоторых элементов (например, радия). В результате тщательных исследований, проведённых опять-таки Резерфордом, было установлено, что каждая -частица имеет положительный заряд, равный по модулю удвоенному заряду электрона, и массу, превышающую массу электрона примерно в раз. То есть, -частица оказалась полностью ионизованным (лишённым электронов) атомом гелия.
Резерфорд говорил об -частицах как об ионах гелия; сейчас мы знаем, что это ядра гелия.
Но в те времена об атомных ядрах ещё ничего не знали — о них Резерфорду лишь предстояло догадаться, глядя на результаты своих знаменитых опытов!
Энергия -частиц очень велика — достаточно сказать, что скорость их вылета из радиоактивного образца составляет примерно скорости света. Поэтому интересно было выяснить, на какие углы будут отклоняться столь мощные «снаряды» при рассеянии на отдельных атомах, а точнее — на их положительных зарядах.
Поэтому интересно было выяснить, на какие углы будут отклоняться столь мощные «снаряды» при рассеянии на отдельных атомах, а точнее — на их положительных зарядах.
Пучок -частиц направлялся на тончайшую золотую фольгу. Как гласит история, Резерфорд не сомневался в том, что углы отклонения должны быть весьма малы: имея столь огромную энергию, -частицы должны проходить сквозь фольгу как нож сквозь масло. Только «для очистки совести», на всякий случай, он попросил учеников посмотреть, не возникает ли рассеяния -частиц на большие углы.
Каково же было всеобщее удивление, когда такие частицы обнаружились! Да, как и следовало ожидать, подавляющая доля -частиц отклонялась несущественно. Но совсем небольшая их часть (примерно одна частица из нескольких тысяч) отклонялась на угол, больший (рис. 2).
Рис. 2. Рассеяние -частиц на атомах
Эти отклонения казались совершенно невероятными. По словам Резерфорда, дело выглядело так, словно артиллерийский снаряд налетел на кусок бумаги и от удара повернул назад.
А «бумагой» в образном сравнении Резерфорда служил атом, устроенный согласно модели Томсона. Действительно, допустим, что положительный заряд атома «размазан» по всему атому, то есть шару радиусом см. Этот положительный заряд создаёт электрическое поле, тормозящее и отклоняющее -частицы. Вблизи атома потенциал данного поля:
Расчёты, однако, показывают, что такое поле оказывается слишком слабым — его тормозящего действия никак не хватит для того, чтобы остановить -частицу и отбросить её назад!
Таким образом, наличие -частиц, отброшенных фольгой, опровергло модель Томсона. Что же было предложено взамен?
Планетарная модель атома
Чтобы отбросить -частицу, положительный заряд атома должен создавать куда более сильное электрическое поле, чем то, которое получается в модели Томсона. А чтобы создать такое поле, положительный заряд должен быть сосредоточен в области, гораздо меньшей размера атома.
Размер этой области можно вычислить. Если положительный заряд занимает область размером , то вблизи заряда создаётся электрическое поле с потенциалом
Если положительный заряд занимает область размером , то вблизи заряда создаётся электрическое поле с потенциалом
Зная кинетическую энергию -частицы, можно найти величину тормозящего потенциала , а затем и размер положительно заряженной области. Вычисления, проведённые Резерфордом, дали следующий результат:
см.
Эта величина на пять порядков (в сто тысяч раз!) меньше размера атома. Так на смену модели Томсона пришла планетарная модель атома (рис. 3).
Рис. 3. Планетарная модель атома
В центре атома находится крошечное положительно заряженное ядро, вокруг которого, словно планеты вокруг Солнца, движутся электроны. Между ядром и электронами действуют силы кулоновского притяжения, но упасть на ядро электроны не могут за счёт своего движения — точно так же, как и планеты не падают на Солнце, хоть и притягиваются к нему.
Заряд ядра по модулю равен суммарному заряду электронов, так что атом в целом электрически нейтрален. Однако электроны могут быть выбиты из своих орбит и покинуть атом — тогда атом превращается в положительно заряженный ион.
Однако электроны могут быть выбиты из своих орбит и покинуть атом — тогда атом превращается в положительно заряженный ион.
Масса электронов составляет очень малую часть общей массы атома. Например, в атоме водорода всего один электрон, и его масса в раз меньше массы ядра. Следовательно, почти вся масса атома сосредоточена в ядре — и это при том, что ядро в сто тысяч раз меньше самого атома.
Чтобы лучше почувствовать соотношение масштабов атома и ядра, представьте себе, что атом стал размером с Останкинскую телебашню ( м). Тогда ядро окажется горошиной размером мм, лежащей у вас на ладони. И тем не менее, почти вся масса атома заключена в этой горошине!
Вот таким удивительным объектом оказался атом. Однако планетарная модель атома, объяснив результаты опытов Резерфорда по рассеянию -частиц, оказалась лишь первым шагом на пути к пониманию внутриатомных процессов. А именно, планетарная модель приводила к одному серьёзному противоречию, и преодоление этого противоречия Нильсом Бором положило начало физике атома. Читаем следующий листок!
Читаем следующий листок!
Модели строения атомов
Первые сведения о сложном строении атома были получены при изучении процессов прохождения электрического тока через жидкости. В тридцатых годах XIX в. опыты выдающегося физика М. Фарадея навели на мысль о том, что электричество существует в виде отдельных единичных зарядов.
Открытие самопроизвольного распада атомов некоторых элементов, названное радиоактивностью, стало прямым доказательством сложности строения атома. В 1902 году английские учёные Эрнест Резерфорд и Фредерик Содди доказали, что при радиоактивном распаде атом урана превращается в два атома – атом тория и атом гелия. Это означало, что атомы не являются неизменными, неразрушимыми частицами.
Модель атома Резерфорда
Исследуя прохождение узкого пучка альфа-частиц через тонкие слои вещества, Резерфорд обнаружил, что большинство альфа-частиц проходит сквозь металлическую фольгу, состоящую из множества тысяч слоёв атомов, не отклоняясь от первоначального направления, не испытывая рассеяния, как будто бы на их пути не было никаких препятствий. Однако некоторые частицы отклонялись на большие углы, испытав действие больших сил.
Однако некоторые частицы отклонялись на большие углы, испытав действие больших сил.
На основании результатов опытов по наблюдению рассеивания альфа-частиц в веществе Резерфорд предложил планетарную модель строения атома. Согласно этой модели строение атома подобно строению солнечной системы. В центре каждого атома имеется положительно заряженное ядро радиусом ≈ 10-10м подобно планетам обращаются отрицательно заряженные электроны. Почти вся масса сосредоточена в атомном ядре. Альфа-частицы могут без рассеяния проходить через тысячи слоёв атомов так, как большая часть пространства внутри атомов пуста, а столкновения с лёгкими электронами почти не влияют на движение тяжёлой альфа-частицы. Рассеяние альфа-частиц происходит при столкновениях с атомными ядрами.
Модель атома Резерфорда не смогла объяснить все свойства атомов.
Согласно законам классической физики атом из положительно заряженного ядра и электронов, обращающимся по круговым орбитам, должен излучать электромагнитные волны. Излучение электромагнитных волн должно приводить к уменьшению запаса потенциальной энергии в системе ядро – электрон, к постепенному уменьшению радиуса орбиты электрона и падению электрона на ядро. Однако атомы обычно не излучают электромагнитные волны, электроны не падают на атомные ядра, то есть атомы устойчивы.
Излучение электромагнитных волн должно приводить к уменьшению запаса потенциальной энергии в системе ядро – электрон, к постепенному уменьшению радиуса орбиты электрона и падению электрона на ядро. Однако атомы обычно не излучают электромагнитные волны, электроны не падают на атомные ядра, то есть атомы устойчивы.
Квантовые постулаты Н. Бора
Для объяснения устойчивости атомов Нильс Бор предложил отказаться от привычных классических представлений и законов при объяснении свойств атомов.
Основные свойства атомов получают последовательное качественное объяснение на основе принятия квантовых постулатов Н. Бора.
1. Электрон вращается вокруг ядра только по строго определенным (стационарным) круговым орбитам.
2. Атомная система может находиться лишь в определённых стационарных или квантовых состояниях, каждому из которых соответствует определённая энергия Е. Атом не излучает энергию в стационарных состояниях.
Стационарное состояние атома с минимальным запасом энергии называется основным состоянием, все остальные состояния называются возбуждёнными (квантовыми) состояниями. В основном состоянии атом может находиться бесконечно долго, время жизни атома в возбуждённом состоянии длится 10-9-10-7 секунды.
3. Излучение или поглощение энергии происходит только при переходе атома из одного стационарного состояния в другое. Энергия кванта электромагнитного излучения при переходе из стационарного состояния с энергией Еm в состояние с энергией Еnравна разности энергий атома в двух квантовых состояниях:
∆Е = Еm – Еn = hv,
где v – частота излучения, h = 2ph = 6,62 ∙ 10-34 Дж ∙с.
Квантовая модель строения атома
В дальнейшем некоторые положения теории Н.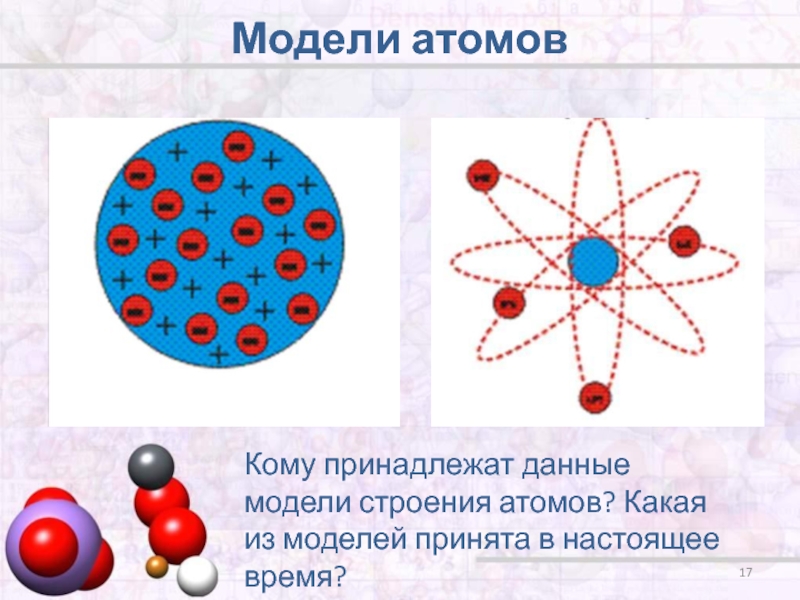 Бора были дополнены и переосмыслены. Наиболее значительным изменением стало введение понятие об электронном облаке, которое сменило понятие об электроне только как частице. Позже теорию Бора сменила квантовая теория, которая учитывает волновые свойства электрона и других элементарных частиц, образующих атом.
Бора были дополнены и переосмыслены. Наиболее значительным изменением стало введение понятие об электронном облаке, которое сменило понятие об электроне только как частице. Позже теорию Бора сменила квантовая теория, которая учитывает волновые свойства электрона и других элементарных частиц, образующих атом.
Основой современной теории строения атома является планетарная модель, дополненная и усовершенствованная. Согласно данной теории, ядро атома состоит из протонов (положительно заряженных частиц) и нейронов (не имеющих заряда частиц). А вокруг ядра по неопределённым траекториям движутся электроны (отрицательно заряженные частицы).
Остались вопросы? Хотите знать больше о моделях строения атома?
Чтобы получить помощь репетитора – зарегистрируйтесь.
Первый урок – бесплатно!
Зарегистрироваться
© blog.tutoronline.ru,
при полном или частичном копировании материала ссылка на первоисточник обязательна.
3. Строение атома
В результате открытия в 1911 г. Э. Резерфордом
атомного ядра образовалась новая концепция строения материи: атом состоит из
массивного положительно заряженного атомного ядра, окруженного электронными
оболочками. Положительный заряд атомного ядра определяет суммарное число
электронов в атомных оболочках. В целом атом является электрически нейтральной
системой. Н. Бор, 1913 г.: «Квантовая теория строения атомов. 1. Среди мыслимых состояний движения атомной системы имеется ряд так называемых стационарных состояний, относительно которых предполагается, что движение частиц в этих состояниях, подчиняясь в значительном объеме классическим механическим законам, отличается, однако, своеобразной механически необъяснимой устойчивостью, в результате которой следует, что всякое остаточное изменение движения системы должно состоять в полном переходе из одного состояния в другое. 2. В самих стационарных состояниях, в противоречие с классической электромагнитной теорией, излучения не происходит, однако процесс перехода между двумя стационарными состояниями может сопровождаться электромагнитным излучением, обладающим теми же свойствами, как излучение, посылаемое на основании классической теории электрической частицей, совершающей гармонические колебания с постоянной частотой. Эта частота ν не находится, однако, в простом отношении к движению частиц атома и определяется условием hν = E’ – E” где
h –
постоянная Планка, E’
и
E” –
значение атомной энергии в двух стационарных состояниях, образующих начальное и
конечное состоянии процесса излучения. Электрон согласно модели Н. Бора в атоме водорода вращается вокруг ядра по классическим траекториям, не излучая энергию, если на его орбите укладывается целое число длин волн де Бройля nλ = 2πrn, n = 1, 2, 3… Разным разрешённым орбитам n соответствуют разные энергии электронов En n = 1, 2, 3… Радиус первой боровской орбиты атома водорода r1 ≈ 0.53·10-8см. Электромагнитное взаимодействие электронов и атомных ядер определяет энергию связи и размеры атомов, размеры молекулярных структур. Э. Резерфорд, 1914 г.: «Из рассмотрения атомов водорода и гелия, где водород имеет один
электрон, а гелий – два, очевидно, что число электронов не может быть всегда
точно равно половине атомного веса. Размеры атома составляют несколько ангстрем (1 Å = 10–8 см). Химические свойства атомов,
способность атомов образовывать различные химические соединения – молекулы
определяются внешней электронной оболочкой атома и зависят от числа электронов в
ней. Z + N = A. Атомные ядра обладают магнитными моментами, которые измеряются в ядерных магнетонах где mp – масса протона. где me – масса электрона. Магнитные момента атомов в тысячи раз больше магнитных моментов ядер. Таблица 1 Характеристики протона, нейтрона и электрона
Протон, нейтрон и электрон являются фермионами, имеют спин J = 1/2 и подчиняются принципу Паули. Нейтрон имеет массу на 1.3 МэВ больше, чем протон, поэтому в свободном состоянии он распадается на протон p, электрон e− и электронное антинейтрино | |||
Строение атома
Открытие сложного строения атома — важнейший этап становления современной физики, наложивший отпечаток на все ее дальнейшее развитие. В процессе создания количественной теории строения атома, позволившей объяснить атомные спектры, были открыты новые законы движения микрочастиц — законы квантовой механики.
Модель Томсона
Хотя слово атом в первоначальном значении — частица, которая не делится на меньшие части, согласно научным представлениям он состоит из более мелких частиц, которые называют субатомными частицами. Атом состоит из электронов, протонов, все атомы, кроме водорода-1, содержат также нейтроны. Не сразу ученые пришли к правильным представлениям о строении атома. Первая модель атома была предложена английским физиком Дж. Дж. Томсоном, открывшим электрон. По мысли Томсона, положительный заряд атома занимает весь объем атома и распределен в этом объеме с постоянной плотностью. Простейший атом — атом водорода — представляет собой положительно заряженный шар радиусом около 10-8 см, внутри которого находится электрон. У более сложных атомов в положительно заряженном шаре находятся несколько электронов.
Однако модель Томсона оказалась в полном противоречии с известными уже к тому времени свойствами атома, главным из которых является устойчивость.
Атом состоит из электронов, протонов, все атомы, кроме водорода-1, содержат также нейтроны. Не сразу ученые пришли к правильным представлениям о строении атома. Первая модель атома была предложена английским физиком Дж. Дж. Томсоном, открывшим электрон. По мысли Томсона, положительный заряд атома занимает весь объем атома и распределен в этом объеме с постоянной плотностью. Простейший атом — атом водорода — представляет собой положительно заряженный шар радиусом около 10-8 см, внутри которого находится электрон. У более сложных атомов в положительно заряженном шаре находятся несколько электронов.
Однако модель Томсона оказалась в полном противоречии с известными уже к тому времени свойствами атома, главным из которых является устойчивость.
Опыт Резерфорда
Масса электронов в несколько тысяч раз меньше массы атомов. Так как атом в целом нейтрален, то, следовательно, основная масса атома приходится на его положительно заряженную часть.
Для экспериментального исследования распределения положительного заряда, а значит, и массы внутри атома Эрнест Резерфорд предложил в 1906 г.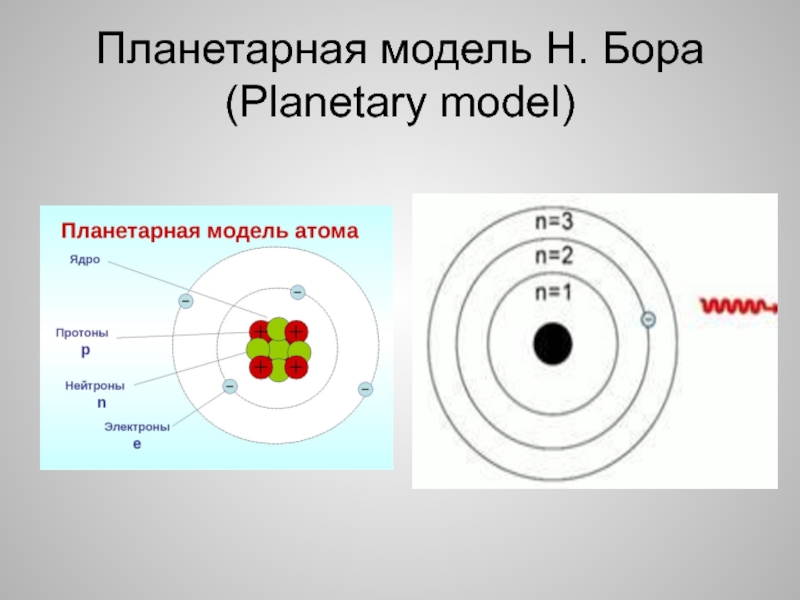 применить зондирование атома с помощью α-частиц. Эти частица возникают при распаде радия и некоторых других элементов. Их масса примерно в 8000 раз больше массы электрона, а положительный заряд равен по модулю удвоенному заряду электрона. Это не что иное, как полностью ионизированные атомы гелия. Скорость α-частиц очень велика: они составляет 1/15 скорости света.
Этими частицами Резерфорд бомбардировал атомы тяжелых элементов. Электроны вследствие своей малой массы не могут заметно изменить траекторию α-частицы.
Рассеяние (изменение направления движения) α-частиц может вызвать только положительно заряженная часть атома. Таким образом, по рассеянию α-частиц можно определить характер распределения положительного заряда и массы внутри атома.
Модифицируя экспериментальную установку, Резерфорд попытался обнаружить отклонение α-частиц на бо́льшие углы. Для этого он окружил фольгу сцинтилляционными экранами и определил число вспышек на каждом экране. Совершенно неожиданно оказалось, что небольшое число α-частиц (примерно одно из двух тысяч) отклонилось на углы, большие 90º.
применить зондирование атома с помощью α-частиц. Эти частица возникают при распаде радия и некоторых других элементов. Их масса примерно в 8000 раз больше массы электрона, а положительный заряд равен по модулю удвоенному заряду электрона. Это не что иное, как полностью ионизированные атомы гелия. Скорость α-частиц очень велика: они составляет 1/15 скорости света.
Этими частицами Резерфорд бомбардировал атомы тяжелых элементов. Электроны вследствие своей малой массы не могут заметно изменить траекторию α-частицы.
Рассеяние (изменение направления движения) α-частиц может вызвать только положительно заряженная часть атома. Таким образом, по рассеянию α-частиц можно определить характер распределения положительного заряда и массы внутри атома.
Модифицируя экспериментальную установку, Резерфорд попытался обнаружить отклонение α-частиц на бо́льшие углы. Для этого он окружил фольгу сцинтилляционными экранами и определил число вспышек на каждом экране. Совершенно неожиданно оказалось, что небольшое число α-частиц (примерно одно из двух тысяч) отклонилось на углы, большие 90º. Позднее Резерфорд признался, что, предложив своим ученикам провести эксперимент по наблюдению за рассеянием α-частиц на бо́льшие углы, он сам не верил в положительный результат. «Это почти столь же невероятно, — говорил Резерфорд, — как если бы вы выстрелили 15-дюймовым снарядом в кусок тонкой бумаги, а снаряд возвратился бы к вам и нанес вам удар».
Позднее Резерфорд признался, что, предложив своим ученикам провести эксперимент по наблюдению за рассеянием α-частиц на бо́льшие углы, он сам не верил в положительный результат. «Это почти столь же невероятно, — говорил Резерфорд, — как если бы вы выстрелили 15-дюймовым снарядом в кусок тонкой бумаги, а снаряд возвратился бы к вам и нанес вам удар».
Другие заметки по физике
Планетарная модель строения атома. Методические материалы
Цифровой ресурс может использоваться для обучения в рамках программы основной и средней школы (базового уровня).
Компьютерная программа представляет собой демонстрацию по теме «Строение атома». Приводится информация о классическом опыте Резерфорда по зондированию атома с помощью α-частиц, приводятся примеры строения атомов шести различных химических элементов.
Краткая теория
Первые прямые эксперименты по исследованию внутренней структуры атомов были выполнены Э.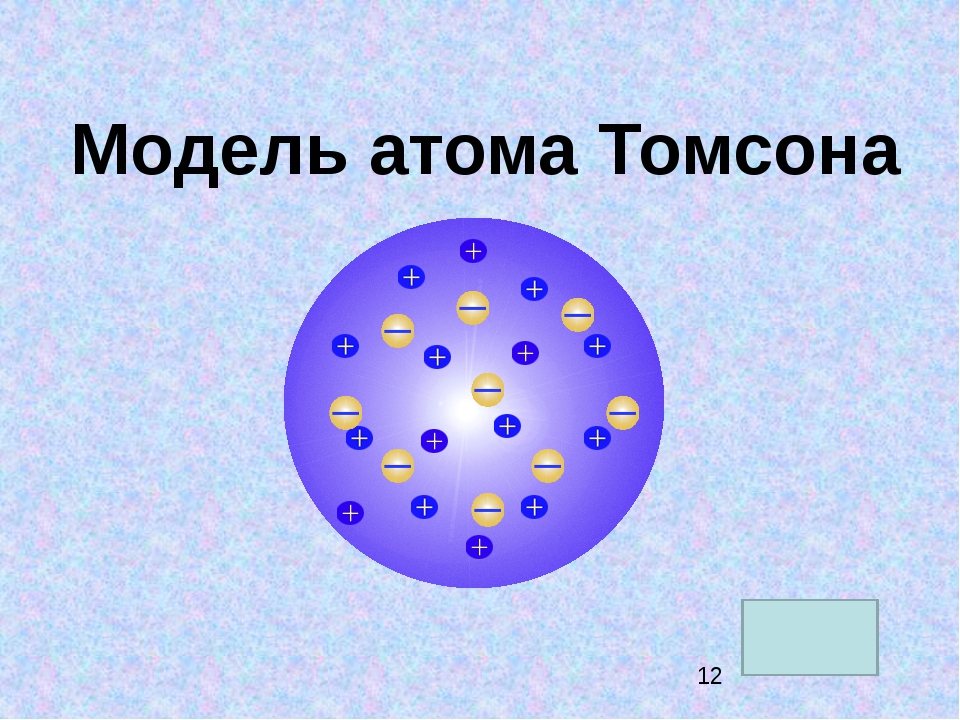 Резерфордом и его сотрудниками Э. Марсденом и Х. Гейгером в 1909–1911 годах.
Резерфордом и его сотрудниками Э. Марсденом и Х. Гейгером в 1909–1911 годах.
Резерфорд предложил применить зондирование атома с помощью α-частиц, которые возникают при радиоактивном распаде радия и некоторых других элементов. Масса α-частиц приблизительно в 7300 раз больше массы электрона, а положительный заряд равен удвоенному элементарному заряду. В своих опытах Резерфорд использовал α-частицы с кинетической энергией около 5 МэВ (скорость таких частиц очень велика – порядка 107 м/с, но все же значительно меньше скорости света).
α-частицы – это полностью ионизированные атомы гелия. Они были открыты Резерфордом в 1899 году при изучении явления радиоактивности. Этими частицами Резерфорд бомбардировал атомы тяжелых элементов (золото, серебро, медь и др.). Электроны, входящие в состав атомов, вследствие малой массы не могут заметно изменить траекторию α-частицы. Рассеяние, то есть изменение направления движения α-частиц, может вызвать только тяжелая положительно заряженная часть атома.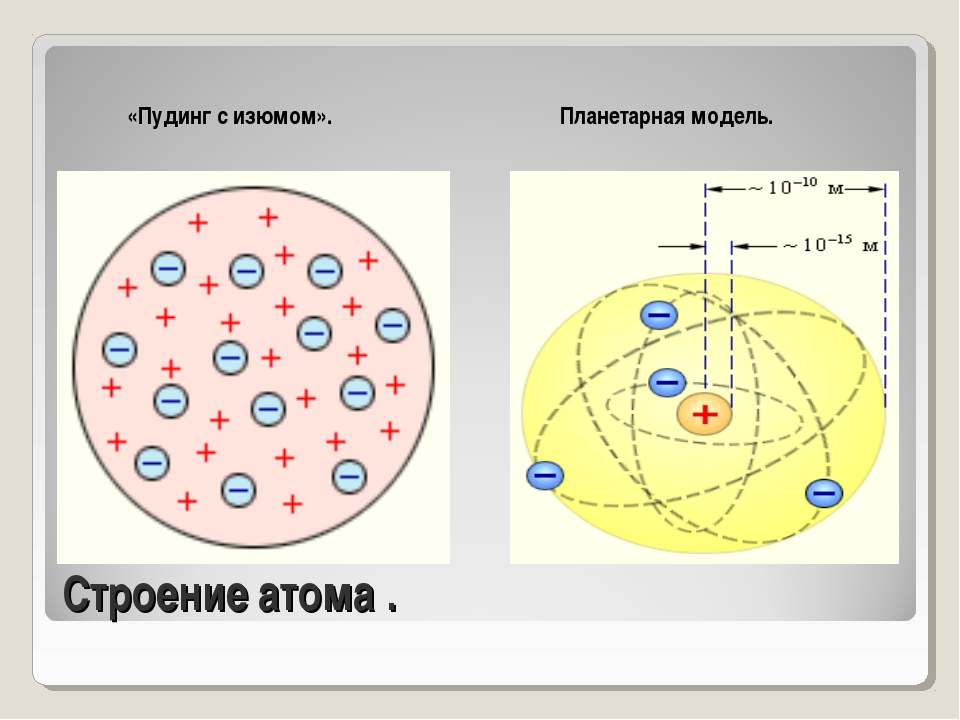
Опыты Резерфорда и его сотрудников привели к выводу о том, что в центре атома находится плотное положительно заряженное ядро, диаметр которого не превышает 10–14–10–15 м. Это ядро занимает только 10–12 часть полного объема атома, но содержит весь положительный заряд и не менее 99,95 % его массы. Заряд ядра должен быть равен суммарному заряду всех электронов, входящих в состав атома.
Опираясь на классические представления о движении микрочастиц, Резерфорд предложил планетарную модель атома. Согласно этой модели, в центре атома располагается положительно заряженное ядро, в котором сосредоточена почти вся масса атома. Атом в целом нейтрален. Вокруг ядра, подобно планетам, под действием кулоновских сил со стороны ядра вращаются электроны. Находиться в состоянии покоя электроны не могут, так как они упали бы на ядро.
|
Рис. |
Планетарная модель атома, предложенная Резерфордом, явилась крупным шагом вперед в развитии знаний о строении атома. Она была совершенно необходимой для объяснения опытов по рассеянию α-частиц, однако оказалась неспособной объяснить сам факт длительного существования атома, т. е. его устойчивость. По законам классической электродинамики, движущийся с ускорением заряд должен излучать электромагнитные волны, уносящие энергию. За короткое время (порядка 10–8 с) все электроны в атоме Резерфорда должны растратить всю свою энергию и упасть на ядро. То, что этого не происходит в устойчивых состояниях атома, показывает, что внутренние процессы в атоме не подчиняются классическим законам.
Работа с моделью
Демонстрация состоит из семи экранов. Модель может быть использована в режиме ручного переключения кадров и в режиме автоматической демонстрации ().
Рекомендации по применению модели
Данная модель может быть применена в качестве иллюстрации на уроках изучения нового материала в 9 и 11 классах по теме «Строение атома». На примере этой модели можно рассмотреть с учащимися планетарные модели строения атома различных химических элементов.
Пример планирования урока с использованием модели
Тема «Строение атома»
Цель урока: рассмотреть модель атома Томпсона, на опыте Резерфорда обосновать не состоятельность модели атома Томпсона, дать планетарную модель атома, рассмотреть модели атомов различных химических элементов, ввести понятие иона.
|
|||||||||||||||||||||||||
|
Таблица 1. |
Примеры вопросов и заданий
-
В томсоновской модели атома водорода предполагалось, что положительный заряд e, равный по модулю заряду электрона, равномерно распределен внутри шара радиусом R = 10–8 см.
 Определите частоту колебаний электрона вблизи
центра шара.
Определите частоту колебаний электрона вблизи
центра шара. -
Предполагая, что электрон в планетарной модели атома водорода вращается по круговой орбите радиусом a = 5,3∙10–11 м, определите:
- напряженность электрического поля ядра на орбите электрона;
- частоту обращения электрона.
-
Какое из приведенных ниже утверждений является серьезным доводом против планетарной модели атомов по Резерфорду?
- Силы электростатического притяжения ядра так велики, что электрон должен упасть на ядро.
- Из-за большой удаленности от ядра силы кулоновского притяжения так малы, что электроны должны легко их преодолевать и покидать атомное ядро.
- Электрон должен терять энергию на электромагнитное излучение и быстро упасть на ядро.
- Из-за большой массы ядра гравитационные силы притяжения должны вызвать падение электрона на ядро.
28 февраля 1913 г. Нильс Бор представил новую модель атома
Модель атома Бора пришла на смену планетарной модели атома Эрнеста Резерфорда.
108 лет назад датский физик-теоретик Нильс Бор предложил свою теорию строения атома, где электроны не подчиняются законам классической физики. В боровской модели атома электроны могут находиться только на разрешенных орбитах и способны мгновенно перескакивать между орбитами при поглощении и испускании фотонов (совершать квантовые скачки).
Ранее, летом 1912 года, ученый прислал своему
наставнику Эрнесту Резерфорду черновик статьи,
посвященной проблеме устойчивости атома. По сути, Нильс Бор
впервые смог объяснить, почему электроны не падают на ядро атома:
когда электроны движутся с ускорением по
строго стационарным орбитам, они не
излучают электромагнитных волн, а значит, не теряют
энергию и не сходят с орбиты. Чтобы найти радиусы
устойчивых орбит, пришлось обращаться к новой на тот момент,
квантовой теории Макса Планка.
Чтобы найти радиусы
устойчивых орбит, пришлось обращаться к новой на тот момент,
квантовой теории Макса Планка.
Справка. Состояние атома, в котором все электроны находятся на стационарных орбитах с наименьшей возможной энергией, называется основным, а все другие состояния — возбужденными. Стационарным состояниям соответствуют определенные стационарные орбиты, по которым движутся электроны.
Бором были сформулированы квантовые постулаты, которые резко расходились с классической механикой и классической электродинамикой, однако успешно позволяли описать простейший атом водорода. Нильс Бор впервые показал, что электрон делает квантовые скачки по орбитам в атоме, и это изменило наше понимание микромира.
Кроме того, Бор ввел понятие об атомном номере, понял, что такое
изотопы, высказал и осмыслил закон радиоактивного смещения. Он
также внес огромный вклад в понимание некоторых процессов,
происходящих внутри тяжелых атомных ядер, что имело решающее
значение для начала исследований, приведших к освобождению
ядерной энергии. (© “Нильс Бор. Жизнь и творчество”, изд-во
“Наука”, 1967 г.).
(© “Нильс Бор. Жизнь и творчество”, изд-во
“Наука”, 1967 г.).
Фото: из презентации физика-теоретика Д.И. Казакова.
Согласно теории Бора, электрон вращается вокруг атома по строго стационарным орбитам. Бор ввел понятие квантового соотношения между радиусом орбиты и скоростью электрона.
“Исходным пунктом атомной теории Бора является признание того факта, что модель атома Резерфорда вместе с классической физикой не могут объяснить той устойчивости, которой, как мы знаем из нашего повседневного опыта, обладают атомы. <…> Исходя из нового положения Бора о существовании атома только в стационарных состояниях, теперь можно было описать эти состояния без какой-либо ссылки на такие классические представления, как электронные орбиты”, — писали о вкладе Бора в развитие физики Х. Меллер и М. Пиль.
Теория датского физика объяснила не только стабильность атомов,
но и линейчатый характер спектров — еще
один важнейший вопрос физики того времени.
Орбитальная модель атома Бора, позже усовершенствованная Арнольдом Зоммерфельдом, стала итогом старой квантовой теории. Рождение новой квантовой теории состоялось в 1925-1926 годах и связано оно было с учеником Нильса Бора — Вернером Гейзенбергом (и его матричной механикой), а также с Эрвином Шредингером и Полем Дираком.
“Решающим моментом в атомной модели Резерфорда было то, что она со всей ясностью показала, что устойчивость атомов нельзя объяснить на основе классической физики и что квантовый постулат — единственно возможный выход из острой дилеммы, и эта острота несоответствия заставила меня абсолютно поверить в правильность квантового постулата”, — говорил сам Нильс Бор.
В июле 1913 года в одном из старейших научных журналов
Великобритании — Philosophical Magazine — вышла
знаменитая статья Бора,
посвященная строению атомов и молекул. Эта публикация имела
фундаментальное значение для развития теоретической физики.
История атома – Теории и модели – Сложный процент
Нажмите для увеличенияВся материя состоит из атомов. Это то, что мы сейчас принимаем как данность, и одна из вещей, которую вы изучаете еще в начале уроков химии в средней или средней школе. Несмотря на это, наши представления о том, что такое атом , на удивление недавние: всего сто лет назад ученые все еще обсуждали, как именно выглядит атом. На этом рисунке показаны ключевые модели, предложенные для атома, и то, как они менялись с течением времени.
Хотя наша графика началась в 1800-х годах, идея атомов появилась задолго до этого. Фактически, мы должны вернуться в Древнюю Грецию, чтобы найти его происхождение. Слово «атом» на самом деле происходит от древнегреческого и примерно переводится как «неделимый». Древнегреческую теорию приписывают нескольким различным ученым, но чаще всего ее приписывают Демокриту (460–370 до н.э.) и его наставнику Левкиппу. Хотя их представления об атомах были рудиментарными по сравнению с нашими сегодняшними представлениями, они изложили идею о том, что все состоит из атомов, невидимых и неделимых сфер материи бесконечного типа и числа.
Эти ученые представляли атомы различной формы в зависимости от типа атома. Они представляли атомы железа как имеющие крючки, скрепляющие их вместе, объясняя, почему железо остается твердым при комнатной температуре. Атомы воды были гладкими и скользкими, что объясняло, почему вода при комнатной температуре была жидкостью и ее можно было переливать. Хотя теперь мы знаем, что это не так, их идеи легли в основу будущих атомных моделей.
Однако пришлось долго ждать, прежде чем эти основы были заложены.Только в 1803 году английский химик Джон Далтон начал разрабатывать более научное определение атома. Он опирался на идеи древних греков, описывая атомы как маленькие твердые сферы, которые неделимы, и что атомы данного элемента идентичны друг другу. Последнее утверждение в значительной степени остается верным, за исключением изотопов различных элементов, которые различаются по количеству нейтронов. Однако, поскольку нейтрон не будет открыт до 1932 года, мы, вероятно, можем простить Далтону эту оплошность. Он также придумал теории о том, как атомы соединяются, чтобы образовать соединения, а также придумал первый набор химических символов для известных элементов.
Он также придумал теории о том, как атомы соединяются, чтобы образовать соединения, а также придумал первый набор химических символов для известных элементов.
Изложение теории атома Дальтоном было началом, но по-прежнему мало что рассказало нам о природе самих атомов. Последовало еще одно, более короткое затишье, когда наши познания в атомах не сильно продвинулись. Были некоторые попытки определить, как могут выглядеть атомы, такие как предположение лорда Кельвина о том, что они могут иметь вихревую структуру, но только на рубеже 20-го века прогресс в выяснении атомной структуры действительно начал поднимать.
Первый прорыв произошел в конце 1800-х годов, когда английский физик Джозеф Джон (Дж. Дж.) Томсон обнаружил, что атом не так неделим, как утверждалось ранее. Он провел эксперименты с использованием катодных лучей, образующихся в разрядной трубке, и обнаружил, что лучи притягиваются положительно заряженными металлическими пластинами, но отталкиваются отрицательно заряженными. Из этого он сделал вывод, что лучи должны быть заряжены отрицательно.
Из этого он сделал вывод, что лучи должны быть заряжены отрицательно.
Измерив заряд частиц в лучах, он смог сделать вывод, что они в две тысячи раз легче водорода, и, изменив металл, из которого сделан катод, он смог сказать, что эти частицы присутствуют во многих типах атомов. .Он открыл электрон (хотя и называл его «корпускулой») и показал, что атомы не неделимы, а имеют более мелкие составные части. Это открытие принесло ему Нобелевскую премию 1906 года.
В 1904 году он выдвинул свою модель атома, основанную на своих открытиях. Названная «моделью сливового пудинга» (хотя и не самим Томсоном), она представляла атом как сферу с положительным зарядом, с электронами, разбросанными повсюду, как сливы в пудинге. Ученые начали вглядываться во внутренности атома, но модель Томсона не продержалась долго – и именно один из его учеников предоставил доказательства, чтобы передать ее в историю.
Эрнест Резерфорд был физиком из Новой Зеландии, учился в Кембриджском университете под руководством Томсона. Это была его более поздняя работа в Манчестерском университете, которая позволила глубже проникнуть в суть атома. Эта работа появилась после того, как он уже получил Нобелевскую премию в 1908 году за свои исследования в области химии радиоактивных веществ.
Это была его более поздняя работа в Манчестерском университете, которая позволила глубже проникнуть в суть атома. Эта работа появилась после того, как он уже получил Нобелевскую премию в 1908 году за свои исследования в области химии радиоактивных веществ.
Резерфорд разработал эксперимент по исследованию атомной структуры, который включал стрельбу положительно заряженными альфа-частицами в тонкий лист золотой фольги.Альфа-частицы были настолько малы, что могли проходить через золотую фольгу, и, согласно модели Томсона, которая показывала, что положительный заряд рассеивается по всему атому, они должны проходить с небольшим отклонением или без него. Проведя этот эксперимент, он надеялся подтвердить модель Томсона, но в итоге сделал прямо противоположное.
Во время эксперимента большая часть альфа-частиц действительно прошла через фольгу с небольшим отклонением или без него. Однако очень небольшое количество частиц отклонялось от своего первоначального пути на очень большие углы.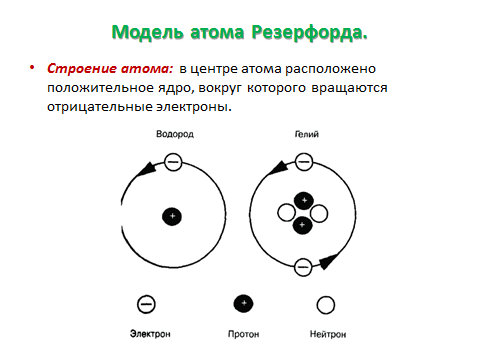 Это было совершенно неожиданно; как заметил сам Резерфорд: «Это было почти так же невероятно, как если бы вы выстрелили 15-дюймовым снарядом по куску папиросной бумаги, а он вернулся и попал в вас». Единственное возможное объяснение заключалось в том, что положительный заряд не распространяется по всему атому, а сосредоточен в небольшом плотном центре: ядре. Большая часть остального атома была просто пустым пространством.
Это было совершенно неожиданно; как заметил сам Резерфорд: «Это было почти так же невероятно, как если бы вы выстрелили 15-дюймовым снарядом по куску папиросной бумаги, а он вернулся и попал в вас». Единственное возможное объяснение заключалось в том, что положительный заряд не распространяется по всему атому, а сосредоточен в небольшом плотном центре: ядре. Большая часть остального атома была просто пустым пространством.
Открытие ядра Резерфордом означало, что модель атома нуждалась в переосмыслении. Он предложил модель, в которой электроны вращаются вокруг положительно заряженного ядра.Хотя это было усовершенствованием модели Томсона, оно не объясняло, что удерживает электроны на орбите, а не просто по спирали в ядре.
Входит Нильс Бор. Бор был датским физиком, который попытался решить проблемы с помощью модели Резерфорда. Он понял, что классическая физика не может должным образом объяснить, что происходит на атомном уровне; вместо этого он обратился к квантовой теории, чтобы попытаться объяснить расположение электронов. Его модель постулировала существование энергетических уровней или оболочек электронов.Электроны можно было найти только на этих определенных энергетических уровнях; Другими словами, их энергия была квантована и не могла иметь никакого значения. Электроны могли перемещаться между этими энергетическими уровнями (называемыми Бором «стационарными состояниями»), но должны были делать это путем поглощения или испускания энергии.
Его модель постулировала существование энергетических уровней или оболочек электронов.Электроны можно было найти только на этих определенных энергетических уровнях; Другими словами, их энергия была квантована и не могла иметь никакого значения. Электроны могли перемещаться между этими энергетическими уровнями (называемыми Бором «стационарными состояниями»), но должны были делать это путем поглощения или испускания энергии.
Предложение Бора о стабильных уровнях энергии решало проблему спиралевидного движения электронов в ядро до некоторой степени, но не полностью. Точные причины немного сложнее, чем мы собираемся здесь обсуждать, потому что мы попадаем в сложный мир квантовой механики; и как сказал сам Бор: «Если квантовая механика вас не сильно шокировала, значит, вы ее еще не поняли».Другими словами, это становится немного странным.
Модель Бора не решает всех проблем с атомной моделью. Он хорошо работал с атомами водорода, но не мог объяснить наблюдения более тяжелых элементов.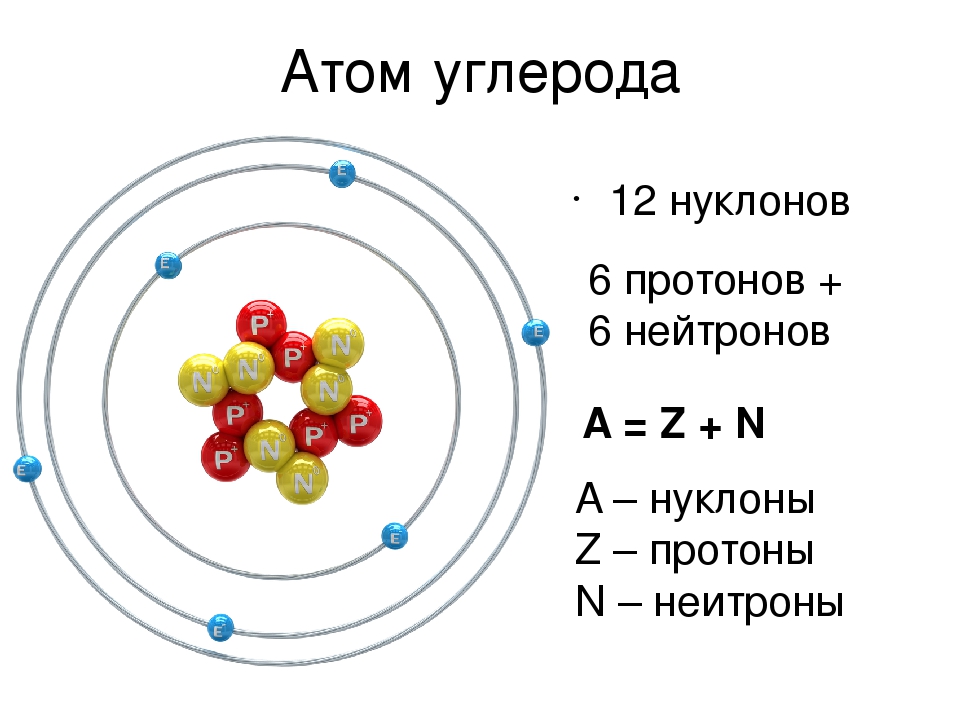 Это также нарушает принцип неопределенности Гейзенберга, один из краеугольных камней квантовой механики, согласно которому мы не можем знать точное положение и импульса электрона. Тем не менее, этот принцип не был постулирован до тех пор, пока Бор не предложил свою модель через несколько лет. Несмотря на все это, модель атома Бора, вероятно, по-прежнему остается той моделью атома, с которой вы наиболее знакомы, поскольку зачастую она впервые используется на курсах химии в средней или средней школе.Он все еще имеет свое применение; это очень удобно для объяснения химической связи и реакционной способности некоторых групп элементов на простом уровне.
Это также нарушает принцип неопределенности Гейзенберга, один из краеугольных камней квантовой механики, согласно которому мы не можем знать точное положение и импульса электрона. Тем не менее, этот принцип не был постулирован до тех пор, пока Бор не предложил свою модель через несколько лет. Несмотря на все это, модель атома Бора, вероятно, по-прежнему остается той моделью атома, с которой вы наиболее знакомы, поскольку зачастую она впервые используется на курсах химии в средней или средней школе.Он все еще имеет свое применение; это очень удобно для объяснения химической связи и реакционной способности некоторых групп элементов на простом уровне.
Во всяком случае, модель все же требовала доработки. В этот момент многие ученые исследовали и пытались разработать квантовую модель атома. Главным из них был австрийский физик Эрвин Шредингер, о котором вы, наверное, слышали раньше (он парень с кошкой и ящиком). В 1926 году Шредингер предположил, что электроны ведут себя как волны, а не электроны, движущиеся по фиксированным орбитам или оболочкам. Это кажется немного странным, но вы, вероятно, уже помните, что свет может вести себя и как волна, и как частица (так называемая дуальность волна-частица), и, оказывается, электроны тоже.
Это кажется немного странным, но вы, вероятно, уже помните, что свет может вести себя и как волна, и как частица (так называемая дуальность волна-частица), и, оказывается, электроны тоже.
Шредингер решил серию математических уравнений, чтобы создать модель распределения электронов в атоме. Его модель показывает ядро, окруженное облаками электронной плотности. Эти облака – облака вероятности; хотя мы не знаем точно, где находятся электроны, мы знаем, что они, вероятно, могут быть обнаружены в данных областях космоса.Эти области пространства называют электронными орбиталями. Возможно, понятно, почему уроки химии в старших классах не соответствуют этой модели, хотя сегодня это общепринятая модель, потому что на то, чтобы разобраться, нужно немного больше времени!
Schrödinger’s не было последним словом об атоме. В 1932 году английский физик Джеймс Чедвик (ученик Эрнеста Резерфорда) открыл существование нейтрона, завершив нашу картину субатомных частиц, составляющих атом.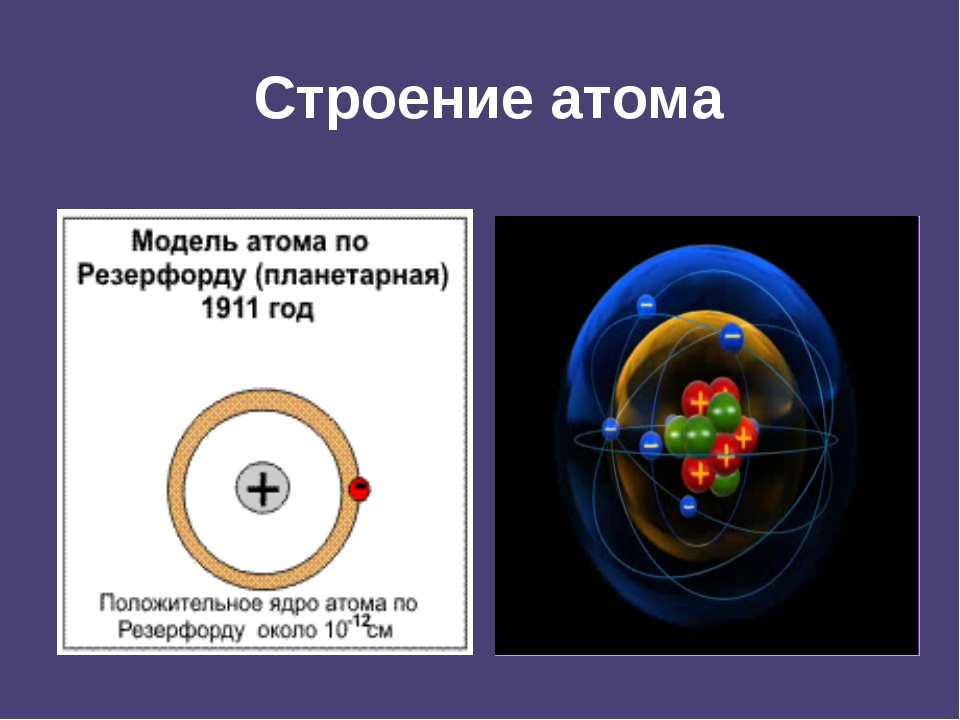 На этом история не заканчивается; С тех пор физики обнаружили, что протоны и нейтроны, составляющие ядро, сами делятся на частицы, называемые кварками, но это выходит за рамки этой статьи! Во всяком случае, атом дает нам отличный пример того, как научные модели могут меняться со временем, и показывает, как новые свидетельства могут привести к новым моделям.
На этом история не заканчивается; С тех пор физики обнаружили, что протоны и нейтроны, составляющие ядро, сами делятся на частицы, называемые кварками, но это выходит за рамки этой статьи! Во всяком случае, атом дает нам отличный пример того, как научные модели могут меняться со временем, и показывает, как новые свидетельства могут привести к новым моделям.
Понравились этот пост и рисунок? Подумайте о поддержке сложного процента на Patreon и получайте предварительные просмотры предстоящих публикаций и многое другое!
Изображение в этой статье находится под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 Международная лицензия. См. Рекомендации по использованию содержания сайта.
Ссылки и дополнительная литература
Развитие модели атома
Если вы выстрелите этими положительными альфа-частицами в этот положительный атом пудинга, они в основном должны отскочить, верно? Что ж, этого не произошло. Резерфорд обнаружил, что большинство из них прошло сквозь фольгу. Некоторые из них пришли в норму. Как такое могло быть, если модель отвеса была правильной? Эксперимент Резерфорда вызвал изменение модели атома.Если положительные альфа-частицы в основном проходят через фольгу, но некоторые отскакивают обратно. И если они уже знали, что электрон маленький и отрицательный, тогда у атома должно быть небольшое положительное ядро с электронами вокруг них.
Резерфорд обнаружил, что большинство из них прошло сквозь фольгу. Некоторые из них пришли в норму. Как такое могло быть, если модель отвеса была правильной? Эксперимент Резерфорда вызвал изменение модели атома.Если положительные альфа-частицы в основном проходят через фольгу, но некоторые отскакивают обратно. И если они уже знали, что электрон маленький и отрицательный, тогда у атома должно быть небольшое положительное ядро с электронами вокруг них.
Модель Бора
Модель, предложенная Нильсом Бором, – это та модель, которую вы увидите во многих вводных научных текстах. В этой модели много хороших идей, но она не согласуется со всеми текущими данными.Модель пытается установить связь между светом и атомами.
Предположим, вы берете немного света и позволяете разным цветам изгибаться в разной степени (представьте себе радугу). Таким образом, вы могли видеть, какие цвета присутствуют для разных источников света. Вот три разных источника света.
Может быть, свет от лампочки – это то, что вы ожидаете. Это цвета радуги. Однако предположим, что вы взяли немного газообразного водорода и возбудили его. Будут производиться только определенные цвета (только определенные длины волн) света.Если вы пропустите свет через газообразный водород, вы увидите темные полосы света того же цвета.
Это цвета радуги. Однако предположим, что вы взяли немного газообразного водорода и возбудили его. Будут производиться только определенные цвета (только определенные длины волн) света.Если вы пропустите свет через газообразный водород, вы увидите темные полосы света того же цвета.
Итак, Бор сказал, что эти цвета света в газообразном водороде соответствуют различным уровням энергии, которые электрон в водороде может иметь. И это ключ к модели Бора – электроны могут находиться ТОЛЬКО на определенных энергетических уровнях в атоме. Это безумие (по крайней мере, для своего времени). Представьте планету, вращающуюся вокруг Солнца. Это может быть на любом уровне энергии. В этом случае существует гравитационная сила, притягивающая планету, которая производит орбитальное движение.Это будет работать в любой точке солнечной системы.
Ранние физики думали, что электрон в атоме очень похож на планету, вращающуюся вокруг Солнца. Ключевое отличие состоит в том, что электрон (в модели Бора) вращается за счет электрического, а не гравитационного взаимодействия.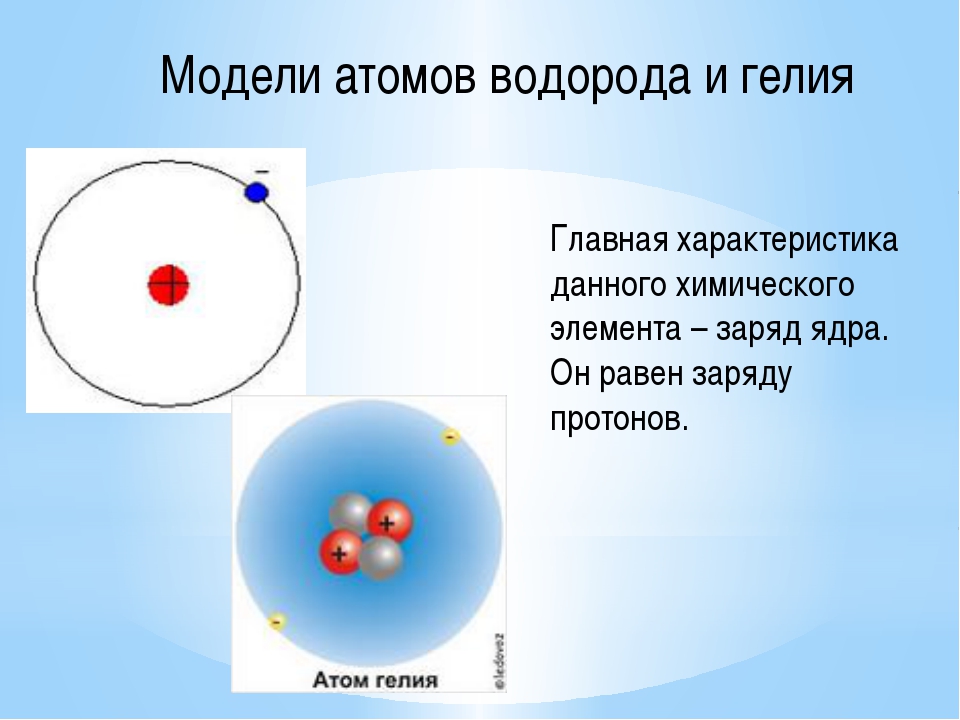 Другое отличие модели Бора состоит в том, что электрон не может вращаться по орбите (если он вращается по орбите, а это не так) на любом расстоянии и при любой энергии. Вот суть модели Бора.
Другое отличие модели Бора состоит в том, что электрон не может вращаться по орбите (если он вращается по орбите, а это не так) на любом расстоянии и при любой энергии. Вот суть модели Бора.
Модель Бора зависит от связи между частотой света и энергией изменения уровня.Если свет с частотой, соответствующей изменению энергии, взаимодействует с атомом, электрон может поглотить свет и подскочить на уровень. Если возбужденный электрон перепрыгивает на уровень, он теряет энергию. Энергия, которую теряет электрон, становится светом с частотой, соответствующей изменению энергии.
Модель Бора может сбивать с толку студентов-новичков, но важно то, что эта модель согласуется со следующими доказательствами.
- Электроны маленькие и заряжены отрицательно
- Протоны в ядре малы по сравнению с размером атома
- Для конкретного элемента только определенные частоты (цвета) света поглощаются или излучаются.
Модель Шредингера и Гейзенберга
В модели Бора есть ключевой момент, который больше не принимается в современных моделях атома.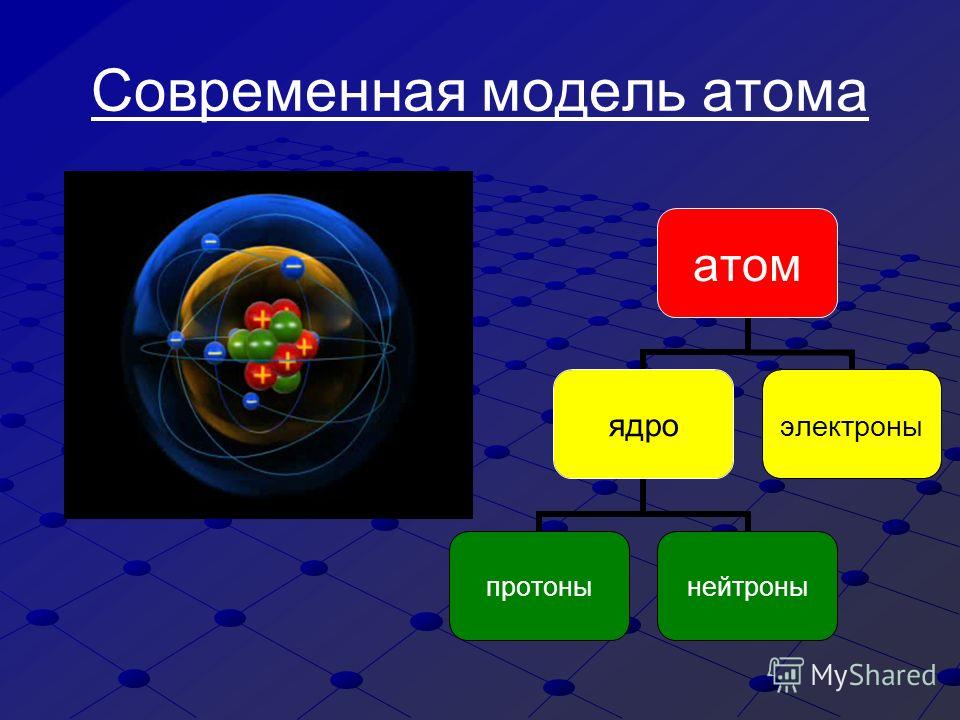 В модели Бора до сих пор считается, что электроны вращаются вокруг ядра так же, как планеты вращаются вокруг Солнца. Собственно, это то, о чем мы не можем сказать правду. Проблема с атомами и электронами в том, что мы, люди, за исключением них, подчиняемся тем же правилам, что и бейсбольные мячи и планеты. На самом деле правила те же, но бейсбольные мячи и планеты следуют правилам квантовой механики, а мы, люди, даже этого не замечаем.
В модели Бора до сих пор считается, что электроны вращаются вокруг ядра так же, как планеты вращаются вокруг Солнца. Собственно, это то, о чем мы не можем сказать правду. Проблема с атомами и электронами в том, что мы, люди, за исключением них, подчиняемся тем же правилам, что и бейсбольные мячи и планеты. На самом деле правила те же, но бейсбольные мячи и планеты следуют правилам квантовой механики, а мы, люди, даже этого не замечаем.
Оказывается, мы ничего не можем сказать о траектории или положении электронов в атоме. Все, что мы можем сказать, – это вероятности. Мы можем сказать, в каких областях может находиться электрон. Вот диаграмма, которая может помочь. Это распределения вероятностей для различных уровней энергии в атоме (из Википедии)
Резюме
Ученые строят модели. Когда собираются новые доказательства, модели меняются.
Ссылки
Обновление:
Я совершенно забыл, что сделал видео-лекцию по тому же самому материалу.Если вам нравится слушать и смотреть, а не читать, посмотрите это.
Материя и атомы от Ретта Аллена на Vimeo.
Еще есть замечательная книга по истории атома. История физики Исаака Азимова. Я очень рекомендую эту книгу, даже если она больше не печатается. Я нашел свою копию в магазине подержанных книг.
Ранний атом | Безграничная физика
Открытие частей атома
В современном научном обиходе атом состоит из составляющих частиц: электрона, протона и нейтрона.
Цели обучения
Обсудить эксперименты, которые привели к открытию электрона и ядра
Основные выводы
Ключевые моменты
- Британский физик Дж. Дж. Томсон провел эксперименты по изучению катодных лучей и обнаружил, что это уникальные частицы, позже названные электронами.
- Резерфорд доказал, что ядро водорода присутствует в других ядрах.
- В 1932 году Джеймс Чедвик показал, что в излучении, которое он использовал, были незаряженные частицы.Эти частицы, позже названные нейтронами, имели массу, аналогичную протонам, но не обладали такими же характеристиками, как протоны.

Ключевые термины
- сцинтилляция : Вспышка света, возникающая в прозрачном материале при прохождении частицы.
- альфа-частица : положительно заряженное ядро атома гелия-4 (состоящее из двух протонов и двух нейтронов), испущенное в результате радиоактивности.
- катод : электрод, через который электрический ток выходит из поляризованного электрического устройства.
Хотя первоначально атом рассматривался как частица, которую нельзя разрезать на более мелкие частицы, современные научные методы обозначают атом как состоящий из различных субатомных частиц. Составные частицы атома (каждая обнаруживается независимо): электрон, протон и нейтрон. (Однако атом водорода-1 не имеет нейтронов, а положительный ион водорода не имеет электронов.)
Классическая модель атома : Модель атома до появления квантовой механики.
Электрон
Немецкий физик Иоганн Вильгельм Хитторф провел исследование электропроводности в разреженных газах. В 1869 году он обнаружил свечение, испускаемое катодом, которое увеличивалось в размерах с уменьшением давления газа. В 1896 году британский физик Дж. Дж. Томсон провел эксперименты, демонстрирующие, что катодные лучи представляют собой уникальные частицы, а не волны, атомы или молекулы, как считалось ранее. Томсон сделал хорошие оценки как заряда [латекс] \ text {e} [/ latex], так и массы [латекс] \ text {m} [/ latex], обнаружив, что частицы катодных лучей (которые он назвал «корпускулами») имели возможно, одна тысячная массы водорода, наименее массивного из известных ионов.Он показал, что их отношение заряда к массе (э / м) не зависит от материала катода. (На рис. 1 показан пучок отклоненных электронов.)
В 1869 году он обнаружил свечение, испускаемое катодом, которое увеличивалось в размерах с уменьшением давления газа. В 1896 году британский физик Дж. Дж. Томсон провел эксперименты, демонстрирующие, что катодные лучи представляют собой уникальные частицы, а не волны, атомы или молекулы, как считалось ранее. Томсон сделал хорошие оценки как заряда [латекс] \ text {e} [/ latex], так и массы [латекс] \ text {m} [/ latex], обнаружив, что частицы катодных лучей (которые он назвал «корпускулами») имели возможно, одна тысячная массы водорода, наименее массивного из известных ионов.Он показал, что их отношение заряда к массе (э / м) не зависит от материала катода. (На рис. 1 показан пучок отклоненных электронов.)
Электронный пучок : пучок электронов, отклоняемых по окружности магнитным полем.
Протон
В 1917 году (в экспериментах, опубликованных в 1919 году) Резерфорд доказал, что ядро водорода присутствует в других ядрах, результат обычно описывается как открытие протона. Ранее Резерфорд научился создавать ядра водорода как тип излучения, возникающего в результате воздействия альфа-частиц на газообразный водород; эти ядра были распознаны по их уникальной сигнатуре проникновения в воздух и их появлению в сцинтилляционных детекторах.Эти эксперименты начались, когда Резерфорд заметил, что когда альфа-частицы запускались в воздух (в основном азот), его сцинтилляционные детекторы отображали сигнатуры типичных ядер водорода в качестве продукта. После экспериментов Резерфорд проследил реакцию на азот в воздухе и обнаружил, что эффект был больше, когда альфа-альфа были произведены в чистый газообразный азот. Резерфорд определил, что единственным возможным источником этого водорода является азот, и поэтому азот должен содержать ядра водорода.Одно ядро водорода было выбито ударом альфа-частицы, в результате чего образовался кислород-17. Это была первая известная ядерная реакция [латекс] 14 \ text {N} + \ alpha \ rightarrow 17 \ text {O} + \ text {p} [/ latex].
Ранее Резерфорд научился создавать ядра водорода как тип излучения, возникающего в результате воздействия альфа-частиц на газообразный водород; эти ядра были распознаны по их уникальной сигнатуре проникновения в воздух и их появлению в сцинтилляционных детекторах.Эти эксперименты начались, когда Резерфорд заметил, что когда альфа-частицы запускались в воздух (в основном азот), его сцинтилляционные детекторы отображали сигнатуры типичных ядер водорода в качестве продукта. После экспериментов Резерфорд проследил реакцию на азот в воздухе и обнаружил, что эффект был больше, когда альфа-альфа были произведены в чистый газообразный азот. Резерфорд определил, что единственным возможным источником этого водорода является азот, и поэтому азот должен содержать ядра водорода.Одно ядро водорода было выбито ударом альфа-частицы, в результате чего образовался кислород-17. Это была первая известная ядерная реакция [латекс] 14 \ text {N} + \ alpha \ rightarrow 17 \ text {O} + \ text {p} [/ latex].
Нейтрон
В 1920 году Эрнест Резерфорд предположил возможное существование нейтрона. В частности, Резерфорд исследовал обнаруженное несоответствие между атомным номером атома и его атомной массой. Он объяснил это существованием нейтрально заряженной частицы внутри атомного ядра.Он считал нейтрон нейтральным двойником, состоящим из электрона, вращающегося вокруг протона. В 1932 году Джеймс Чедвик показал незаряженные частицы в излучении, которое он использовал. Эти частицы имели ту же массу, что и протоны, но не обладали такими же характеристиками, как протоны. Чедвик последовал некоторым предсказаниям Резерфорда, первым, кто работал в этой тогда еще неизвестной области.
В частности, Резерфорд исследовал обнаруженное несоответствие между атомным номером атома и его атомной массой. Он объяснил это существованием нейтрально заряженной частицы внутри атомного ядра.Он считал нейтрон нейтральным двойником, состоящим из электрона, вращающегося вокруг протона. В 1932 году Джеймс Чедвик показал незаряженные частицы в излучении, которое он использовал. Эти частицы имели ту же массу, что и протоны, но не обладали такими же характеристиками, как протоны. Чедвик последовал некоторым предсказаниям Резерфорда, первым, кто работал в этой тогда еще неизвестной области.
Ранние модели атома
Дальтон считал, что материя состоит из дискретных единиц, называемых атомами, – неделимых, элементарных частиц материи.
Цели обучения
Описать постулаты атомной теории Дальтона и атомных теорий древнегреческих философов
Основные выводы
Ключевые моменты
- Атом – это основная единица вещества, состоящая из плотного центрального ядра, окруженного облаком отрицательно заряженных электронов.
- Разрозненные знания, открытые алхимиками в средние века, способствовали открытию атомов.
- Дальтон основал свою атомную теорию, основанную на том факте, что массы реагентов в конкретных химических реакциях всегда имеют определенное соотношение масс.{-1} долларов США
- ядро : массивная положительно заряженная центральная часть атома, состоящая из протонов и нейтронов
Атом – это основная единица материи, состоящая из плотного центрального ядра, окруженного облаком отрицательно заряженных электронов. Ядро атома содержит смесь положительно заряженных протонов и электрически нейтральных нейтронов (за исключением случая водорода-1, который является единственным стабильным нуклидом без нейтронов). Электроны атома связаны с ядром электромагнитной силой.Теперь у нас есть подробная (и точная) модель атома, но на то, чтобы придумать правильный ответ, потребовалось много времени.
Иллюстрация атома гелия : Это иллюстрация атома гелия, изображающая ядро (розовый) и распределение электронного облака (черный). {- 10} [/ латекс] м, или 100 мкм).
{- 10} [/ латекс] м, или 100 мкм).
Люди давно размышляли о структуре материи и существовании атомов. Самые ранние важные идеи, которые выжили, исходят от древних греков пятого века до нашей эры, особенно от философов Левкиппа и Демокрита. (Есть некоторые свидетельства того, что философы и в Индии, и в Китае высказывали аналогичные рассуждения примерно в одно и то же время.) Они рассмотрели вопрос о том, можно ли безгранично делить субстанцию на все более мелкие части. На этот вопрос есть только несколько возможных ответов.Во-первых, возможно бесконечно малое подразделение. Демокрит, в частности, полагал, что существует мельчайшая единица, которую нельзя подразделить дальше. Демокрит назвал это атомом. Теперь мы знаем, что сами атомы можно подразделить, но при этом их идентичность разрушается, так что греки в некотором отношении были правы. Греки также считали, что атомы находятся в постоянном движении – еще одно правильное представление.
Греки и другие исследователи размышляли о свойствах атомов, предполагая, что существует лишь несколько типов атомов и что вся материя образована как различные комбинации этих типов. Известное предположение, что основными элементами были земля, воздух, огонь и вода, было блестящим, но неверным. Греки определили наиболее распространенные примеры четырех состояний материи (твердое тело, газ, плазма и жидкость), а не основные химические элементы. Прошло более 2000 лет, прежде чем можно было проводить наблюдения с помощью оборудования, способного раскрыть истинную природу атомов.
Известное предположение, что основными элементами были земля, воздух, огонь и вода, было блестящим, но неверным. Греки определили наиболее распространенные примеры четырех состояний материи (твердое тело, газ, плазма и жидкость), а не основные химические элементы. Прошло более 2000 лет, прежде чем можно было проводить наблюдения с помощью оборудования, способного раскрыть истинную природу атомов.
На протяжении веков были сделаны открытия, касающиеся свойств веществ и их химических реакций.Были признаны определенные систематические особенности, но сходство между обычными и редкими элементами привело к попыткам превратить их (в частности, свинец в золото) с целью получения финансовой выгоды. Секретность была обычным делом. Алхимики открыли и заново открыли многие факты, но не сделали их общедоступными. Когда средневековье закончилось, практика алхимии постепенно исчезла, и возникла химия. Хранить открытия в секрете уже было невозможно, да и не считалось желательным. Коллективное знание росло, и к началу 19, -го, века, важный факт был хорошо установлен: массы реагентов в конкретных химических реакциях всегда имеют определенное соотношение масс. {23} [/ латекс]).
{23} [/ латекс]).
Дальтон считал, что материя состоит из дискретных единиц, называемых атомами, в отличие от устаревшего представления о том, что материя может быть разделена на любое сколь угодно малое количество. Он также считал, что атомы – это неделимые, первичные частицы материи. Однако это убеждение было опровергнуто в конце 19, -го, -го века Томсоном, когда он открыл электроны.
Введение в историю теории атома – Введение : Резерфорд, Томсон, электроны, ядра и сливы.Я не хочу быть борцом, но считаете ли вы, что пудинг должен сыграть роль в серьезных научных исследованиях?
Модель Thomson
Томсон предположил, что атом состоит из электронов, окруженных супом положительного заряда, чтобы уравновесить отрицательные заряды электронов.
Цели обучения
Опишите модель атома, предложенную Дж. Дж. Томсоном.
Основные выводы
Ключевые моменты
- Дж. Дж. Томсон, открывший электрон в 1897 году, предложил модель атома из сливового пудинга в 1904 году до открытия атомного ядра, чтобы включить электрон в атомную модель.
- В модели Томсона атом состоит из электронов, окруженных супом положительного заряда, чтобы уравновесить отрицательные заряды электронов, как отрицательно заряженные «сливы», окруженные положительно заряженным «пудингом».
- Модель Томсона 1904 года была опровергнута экспериментом Ханса Гейгера и Эрнеста Марсдена с золотой фольгой 1909 года.
Ключевые термины
- ядро : массивная положительно заряженная центральная часть атома, состоящая из протонов и нейтронов
Дж.Дж. Томсон, открывший электрон в 1897 году, предложил модель атома из сливового пудинга в 1904 году до открытия атомного ядра, чтобы включить электрон в атомную модель. В модели Томсона атом состоит из электронов (которые Томсон до сих пор называл «корпускулами», хотя в 1894 г. Г. Дж. Стони предложил называть атомы электричества электронами), окруженных супом положительного заряда, чтобы уравновесить отрицательные заряды электронов, например отрицательно заряженные «сливы» в окружении положительно заряженного «пудинга».Считалось, что электроны (какими мы их знаем сегодня) расположены по всему атому во вращающихся кольцах. В этой модели атом также иногда описывался как «облако» положительного заряда.
В модели Томсона атом состоит из электронов (которые Томсон до сих пор называл «корпускулами», хотя в 1894 г. Г. Дж. Стони предложил называть атомы электричества электронами), окруженных супом положительного заряда, чтобы уравновесить отрицательные заряды электронов, например отрицательно заряженные «сливы» в окружении положительно заряженного «пудинга».Считалось, что электроны (какими мы их знаем сегодня) расположены по всему атому во вращающихся кольцах. В этой модели атом также иногда описывался как «облако» положительного заряда.
Модель атома из сливового пудинга : схематическое изображение модели атома из сливового пудинга; в математической модели Томсона «корпускулы» (на современном языке электроны) располагались неслучайно во вращающихся кольцах.
Используя эту модель, Томсон отказался от своей более ранней гипотезы о «туманном атоме», согласно которой атом состоит из нематериальных вихрей.Теперь, по крайней мере, часть атома должна была состоять из частичных отрицательных корпускул Томсона, хотя остальная часть положительно заряженной части атома оставалась несколько расплывчатой и нечеткой.
Модель Томсона 1904 года была опровергнута экспериментом с золотой фольгой 1909 года, проведенным Гансом Гейгером и Эрнестом Марсденом. Этот эксперимент с золотой фольгой был интерпретирован Эрнестом Резерфордом в 1911 году, чтобы предположить, что существует очень маленькое ядро атома, которое содержит очень высокий положительный заряд (в случае золота, достаточный, чтобы уравновесить коллективный отрицательный заряд около 100 электронов).Его выводы привели его к предложению модели атома Резерфорда.
Введение в историю теории атома – Модель Томсона : Резерфорд, Томсон, электроны, ядра и сливы. Я не хочу быть борцом, но считаете ли вы, что пудинг должен сыграть роль в серьезных научных исследованиях?
Модель Резерфорда
Резерфорд подтвердил, что атом имеет концентрированный центр положительного заряда и относительно большую массу.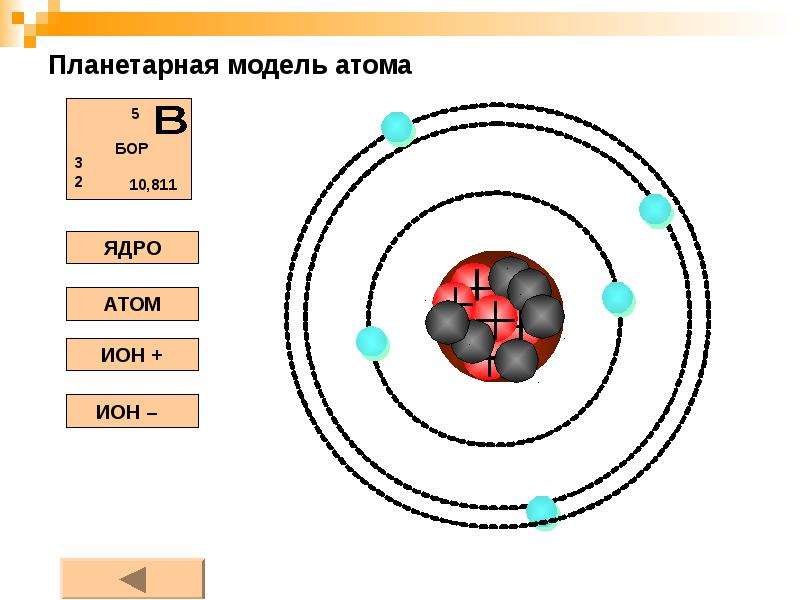
Цели обучения
Опишите эксперимент с золотой фольгой, проведенный Гейгером и Марсденом под руководством Резерфорда, и его значение для модели атома
Основные выводы
Ключевые моменты
- Резерфорд опроверг модель Томсона в 1911 году своим известным экспериментом с золотой фольгой, в котором он продемонстрировал, что атом имеет крошечное ядро большой массы.
- В своем эксперименте Резерфорд заметил, что многие альфа-частицы отклонялись под небольшими углами, в то время как другие отражались обратно к альфа-источнику.
- Эта высококонцентрированная положительно заряженная область называется «ядром» атома.
Ключевые термины
- альфа-частица : положительно заряженное ядро атома гелия-4 (состоящее из двух протонов и двух нейтронов), испущенное в результате радиоактивности; α-частица.
Модель Резерфорда – это модель атома, названная в честь Эрнеста Резерфорда.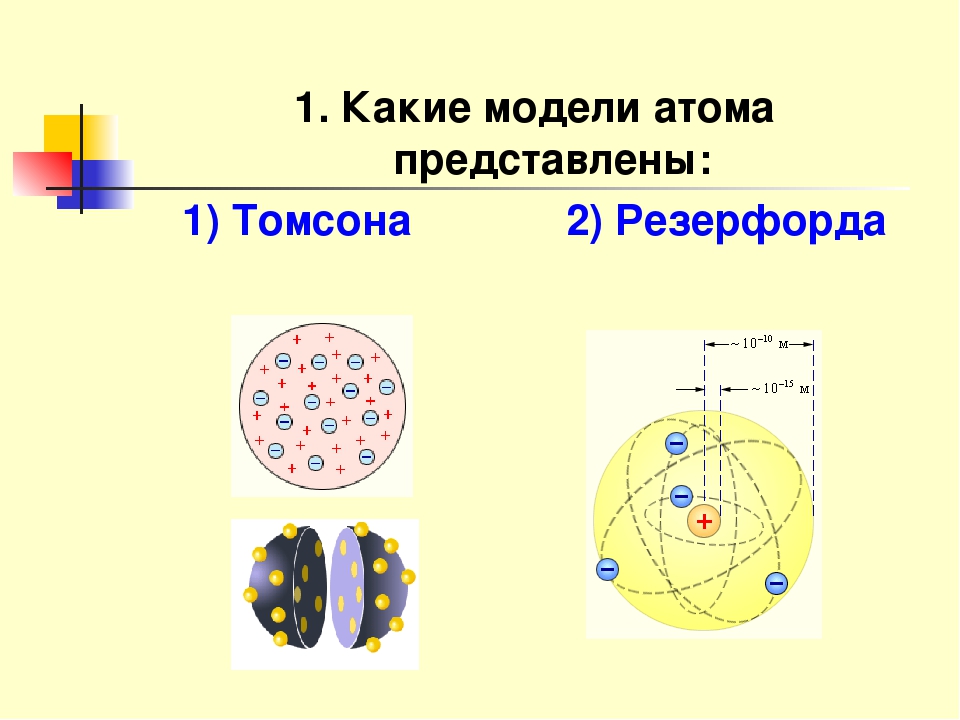 Резерфорд руководил знаменитым экспериментом Гейгера-Марсдена в 1909 году, который, согласно анализу Резерфорда 1911 года, предполагает, что Дж.Так называемая «сливовая пудинговая модель» атома Дж. Томсона была неправильной. Новая модель атома Резерфорда, основанная на экспериментальных результатах, содержала новые особенности относительно высокого центрального заряда, сконцентрированного в очень небольшом объеме по сравнению с остальной частью атома. Этот центральный объем также содержал основную массу атома. Позже эта область будет названа «ядром». ”
Резерфорд руководил знаменитым экспериментом Гейгера-Марсдена в 1909 году, который, согласно анализу Резерфорда 1911 года, предполагает, что Дж.Так называемая «сливовая пудинговая модель» атома Дж. Томсона была неправильной. Новая модель атома Резерфорда, основанная на экспериментальных результатах, содержала новые особенности относительно высокого центрального заряда, сконцентрированного в очень небольшом объеме по сравнению с остальной частью атома. Этот центральный объем также содержал основную массу атома. Позже эта область будет названа «ядром». ”
Модель атомной планеты : Принципиальная схема модели атомной планеты; электроны – зеленым, а ядро - красным
В 1911 году Резерфорд разработал эксперимент по дальнейшему исследованию атомной структуры с использованием альфа-частиц, испускаемых радиоактивным элементом.Следуя его указаниям, Гейгер и Марсден стреляли альфа-частицами с большой кинетической энергией в тонкую золотую фольгу. Ожидалось, что измерение структуры рассеянных частиц предоставит информацию о распределении заряда внутри атома. Согласно преобладающей модели сливового пудинга, все альфа-частицы должны были отклоняться максимум на несколько градусов. Однако реальные результаты удивили Резерфорда. Хотя многие из альфа-частиц действительно прошли, как и ожидалось, многие другие были отклонены под небольшими углами, в то время как другие отражались обратно к альфа-источнику.{-10} [/ latex] метров в радиусе; очень удивительное открытие, поскольку оно подразумевает сильный центральный заряд, меньший, чем [latex] \ frac {1} {3000} [/ latex] th диаметра атома.
Согласно преобладающей модели сливового пудинга, все альфа-частицы должны были отклоняться максимум на несколько градусов. Однако реальные результаты удивили Резерфорда. Хотя многие из альфа-частиц действительно прошли, как и ожидалось, многие другие были отклонены под небольшими углами, в то время как другие отражались обратно к альфа-источнику.{-10} [/ latex] метров в радиусе; очень удивительное открытие, поскольку оно подразумевает сильный центральный заряд, меньший, чем [latex] \ frac {1} {3000} [/ latex] th диаметра атома.
Введение в историю теории атома – Модель Резерфорда : Резерфорд, Томсон, электроны, ядра и сливы. Я не хочу быть борцом, но считаете ли вы, что пудинг должен сыграть роль в серьезных научных исследованиях?
Модель атома Бора
Бор предположил, что электроны в водороде могут иметь определенные классические движения , только если они ограничены квантовым правилом .
Цели обучения
Опишите модель атома, предложенную Нильсом Бором.
Основные выводы
Ключевые моменты
- Согласно Бору: 1) Электроны в атомах вращаются вокруг ядра, 2) Электроны могут вращаться стабильно, не излучая, только на определенных орбитах, и 3) Электроны могут только набирать и терять энергию, прыгая с одной разрешенной орбиты на другую.
- Значение модели Бора состоит в том, что законы классической механики применимы к движению электрона вокруг ядра только тогда, когда они ограничены квантовым правилом.Поэтому его атомная модель называется полуклассической.
- Законы классической механики предсказывают, что электрон должен испускать электромагнитное излучение, вращаясь вокруг ядра, предполагая, что все атомы должны быть нестабильными!
Ключевые термины
- Уравнения Максвелла : Набор уравнений, описывающих, как электрические и магнитные поля генерируются и изменяются друг другом, а также зарядами и токами.

- полуклассический : теория, в которой одна часть системы описывается квантово-механически, а другая рассматривается классически.
Модель атома Бора
Великий датский физик Нильс Бор (1885–1962 гг.) Сразу же использовал планетарную модель атома Резерфорда. Бор убедился в его истинности и провел часть 1912 года в лаборатории Резерфорда. В 1913 году, вернувшись в Копенгаген, он начал публиковать свою теорию простейшего атома, водорода, основанную на планетарной модели атома.
Нильс Бор : Нильс Бор, датский физик, использовал планетарную модель атома, чтобы объяснить атомный спектр и размер атома водорода.Его большой вклад в развитие атомной физики и квантовой механики; его личное влияние на многих студентов и коллег; а его личная неприкосновенность, особенно перед лицом нацистского угнетения, позволила ему занять видное место в истории. (Источник: неизвестный автор, через Wikimedia Commons)
На протяжении десятилетий задавалось много вопросов об атомных характеристиках.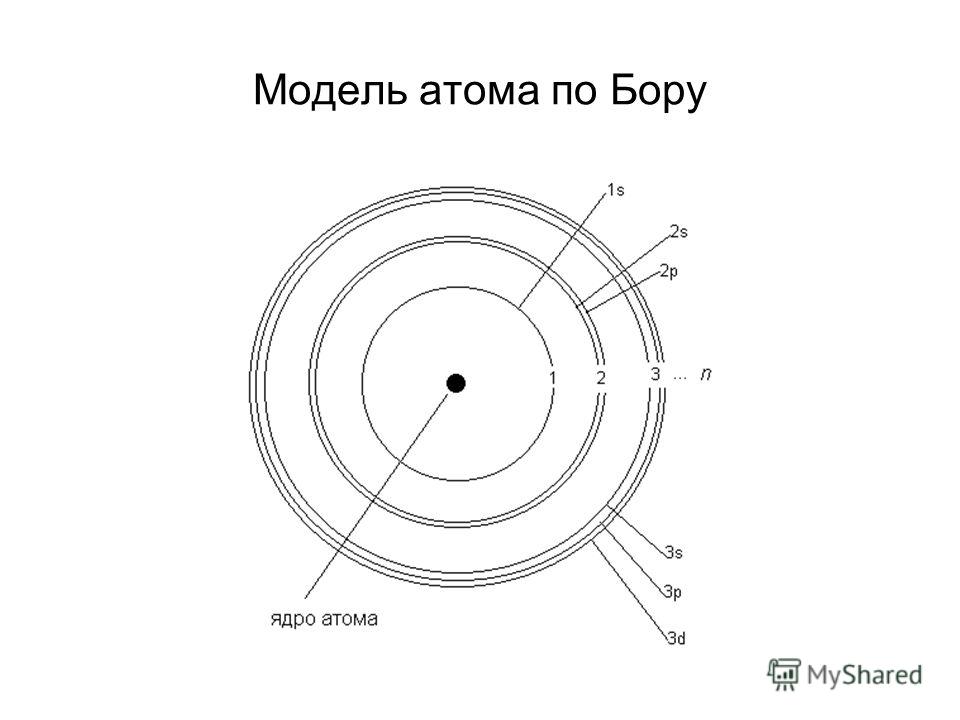 Об атомах было известно многое, от их размеров до спектров, но мало что было объяснено с точки зрения законов физики.Теория Бора объяснила атомный спектр водорода, сразу сделала его знаменитым и установила новые и широко применимые принципы квантовой механики.
Об атомах было известно многое, от их размеров до спектров, но мало что было объяснено с точки зрения законов физики.Теория Бора объяснила атомный спектр водорода, сразу сделала его знаменитым и установила новые и широко применимые принципы квантовой механики.
Одна большая загадка планетарной модели атома заключалась в следующем. Законы классической механики предсказывают, что электрон должен испускать электромагнитное излучение, вращаясь вокруг ядра (согласно уравнениям Максвелла, ускоряющий заряд должен излучать электромагнитное излучение). Поскольку электрон теряет энергию, он постепенно закручивается по спирали внутрь, коллапсируя в ядро.Эта модель атома катастрофична, потому что предсказывает, что все атомы нестабильны. Кроме того, по мере того, как электроны движутся по спирали внутрь, частота излучения будет постепенно увеличиваться по мере того, как орбита становится меньше и быстрее. Это приведет к непрерывному размытию по частоте электромагнитного излучения. Однако эксперименты с электрическими разрядами конца XIX века показали, что атомы излучают свет (то есть электромагнитное излучение) только на определенных дискретных частотах.
Чтобы преодолеть эту трудность, Нильс Бор в 1913 году предложил то, что сейчас называется моделью атома Бора.Он предположил, что электроны могут иметь только определенные классические движения:
- Электроны в атомах вращаются вокруг ядра.
- Электроны могут вращаться стабильно, не излучая, только по определенным орбитам (названным Бором «стационарными орбитами»): на определенном дискретном наборе расстояний от ядра. Эти орбиты связаны с определенными энергиями и также называются энергетическими оболочками или энергетическими уровнями. На этих орбитах ускорение электрона не приводит к излучению и потерям энергии, как того требует классическая электродинамика.
- Электроны могут набирать и терять энергию, только перепрыгивая с одной разрешенной орбиты на другую, поглощая или испуская электромагнитное излучение с частотой [латекс] \ nu [/ латекс], определяемой разностью энергий уровней в соответствии с соотношением Планка:
[латекс] \ Delta {\ text {E}} = \ text {E} _2- \ text {E} _1 = \ text {h} \ nu \, [/ latex]
где [latex] \ text {h} [/ latex] – постоянная Планка, а [latex] \ nu [/ latex] – частота излучения.
Полуклассическая модель
Значение модели Бора состоит в том, что законы классической механики применимы к движению электрона вокруг ядра только тогда, когда они ограничены квантовым правилом .Поэтому его атомная модель называется полуклассической.
Основные предположения модели Бора
Бор успешно объяснил спектр водорода, приняв условие квантования и введя в свою модель постоянную Планка.
Цели обучения
Опишите основные предположения, которые были применены Нильсом Бором к планетарной модели атома.
Основные выводы
Ключевые моменты
- Классическая электродинамика предсказывает, что атом, описываемый (классической) планетарной моделью, будет нестабильным.
- Чтобы объяснить спектр водорода, Бор был вынужден сделать несколько предположений о том, что электроны могут иметь только определенные классические движения.
- После основополагающих работ Планка, Эйнштейна и Бора физики начали понимать, что для объяснения микроскопических миров необходимо ввести понятие «квантование».
Ключевые термины
- черное тело : идеализированное физическое тело, которое поглощает все падающее электромагнитное излучение, независимо от частоты или угла падения.Хотя черное тело является теоретической концепцией, вы можете найти приблизительные реализации черного тела в природе.
- фотоэлектрический эффект : Возникновение электронов, испускаемых веществом (металлами и неметаллическими твердыми телами, жидкостями или газами) в результате поглощения ими энергии электромагнитного излучения.
В предыдущих модулях мы видели загадки классических атомных теорий (например, модель Резерфорда). Что наиболее важно, классическая электродинамика предсказывает, что атом, описываемый (классической) планетарной моделью, будет нестабильным.Чтобы объяснить загадку, Бор в 1913 году предложил то, что сейчас называется моделью атома Бора. Он предположил, что электроны могут иметь только определенные классические движения:
- Электроны в атомах вращаются вокруг ядра.
- Электроны могут вращаться стабильно, не излучая, только по определенным орбитам (названным Бором «стационарными орбитами») на определенном дискретном наборе расстояний от ядра. Эти орбиты связаны с определенными энергиями и также называются энергетическими оболочками или энергетическими уровнями.На этих орбитах ускорение электрона не приводит к излучению и потерям энергии, как того требует классическая электродинамика.
- Электроны могут набирать и терять энергию, только перепрыгивая с одной разрешенной орбиты на другую, поглощая или испуская электромагнитное излучение с частотой [латекс] \ nu [/ латекс], определяемой разностью энергий уровней в соответствии с соотношением Планка: [латекс ] \ Delta {\ text {E}} = \ text {E} _2- \ text {E} _1 = \ text {h} \ nu [/ latex], где [latex] \ text {h} [/ latex] – постоянная Планка.Вдобавок Бор также предположил, что угловой момент [латекс] \ text {L} [/ latex] ограничен целым числом, кратным фиксированной единице: [латекс] \ text {L} = \ text {n} {\ text {h} \ over 2 \ pi} = \ text {n} \ hbar [/ latex], где [latex] \ text {n} = 1, 2, 3, \ dots [/ latex] называется основным квантом число и [латекс] \ hbar = \ frac {\ text {h}} {2 \ pi} [/ latex].
Мы видели, что Планк принял новое условие квантования энергии для объяснения излучения черного тела, где он впервые ввел постоянную Планка [латекс] \ text {h} [/ latex].Вскоре после этого Эйнштейн прибег к этой новой концепции квантования энергии и снова использовал постоянную Планка для объяснения фотоэлектрических эффектов, в которых он предположил, что электромагнитное излучение взаимодействует с материей как частицы (позже названные «фотонами»). Здесь Бор впервые успешно объяснил спектр атомарного водорода, приняв условие квантования и введя постоянную Планка в свою атомную модель. В период радикального развития в начале 20, и веках, физики начали понимать, что для объяснения микроскопических миров необходимо ввести понятие «квантование».
Модель Резерфорда-Бора : Модель Резерфорда-Бора атома водорода ([latex] \ text {Z} = 1 [/ latex]) или водородоподобного иона ([latex] \ text {Z}> 1 [/ latex]), где отрицательно заряженный электрон, заключенный в атомную оболочку, окружает небольшое положительно заряженное атомное ядро, и где скачок электрона между орбитами сопровождается испускаемой или поглощенной электромагнитной энергией ([latex] \ text { h} \ nu [/ latex]). 2 [/ latex], где [latex] \ text {n} [/ latex] – главное квантовое число.Изображенный здесь переход [латекс] 3 \ rightarrow 2 [/ latex] дает первую строку серии Бальмера, а для водорода ([latex] \ text {Z} = 1 [/ latex]) он дает фотон с длиной волны 656 нм (красный свет).
Орбиты Бора
Согласно Бору, электроны могут стабильно вращаться только на определенных орбитах на определенном дискретном наборе расстояний от ядра.
Цели обучения
Объясните взаимосвязь между «орбитами Бора» и эффектом квантования
Основные выводы
Ключевые моменты
- «Орбиты Бора» имеют очень важную особенность квантования: угловой момент L электрона на его орбите квантован, то есть имеет только определенные дискретные значения.Это приводит к уравнению L = mevrn = nℏL = m_e v r_n = n \ hbar.
- Во время предложения Бор сам не знал, зачем нужно квантовать угловой момент, но, используя это предположение, он смог вычислить энергии в спектре водорода.
- Теория атома или любой другой системы должна предсказывать его энергию на основе физики системы, что могла сделать модель Бора.
Ключевые термины
- квантование : процесс объяснения классического понимания физических явлений с точки зрения нового понимания, известного как квантовая механика.
Датский физик Нилс Бор был достаточно умен, чтобы открыть метод расчета орбитальной энергии электронов в водороде. Как мы видели в предыдущем модуле «Модель атома Бора», Бор предположил, что электроны могут двигаться по стабильной орбите без излучения только на определенных орбитах (названных Бором «стационарными орбитами») на определенном дискретном наборе расстояния от ядра. Эти «орбиты Бора» обладают очень важной особенностью квантования, как показано ниже. Это был важный первый шаг, который был улучшен, но его стоит повторить здесь, поскольку он правильно описывает многие характеристики водорода.Предполагая круговые орбиты, Бор предположил, что угловой момент [latex] \ text {L} [/ latex] электрона на его орбите квантован, то есть имеет только определенные дискретные значения. Значение [латекс] \ text {L} [/ latex] дается формулой:
[латекс] \ displaystyle \ text {L} = \ text {m} _ \ text {e} \ text {v} \ text {r} _ \ text {n} = \ text {n} {\ text {h } \ over 2 \ pi} = \ text {n} \ hbar [/ latex]
где [latex] \ text {L} [/ latex] – это угловой момент, [latex] \ text {m} _ \ text {e} [/ latex] – масса электрона, [latex] \ text {r} _ \ text {n} [/ latex] – это радиус [latex] \ text {n} [/ latex] -й орбиты, а [latex] \ text {h} [/ latex] – это постоянная Планка.2) (\ frac {\ text {v}} {\ text {r}}) = \ text {mvr} [/ latex]
Квантование говорит, что это значение [latex] \ text {mvr} [/ latex] может иметь только дискретные значения. В то время Бор сам не знал, зачем нужно квантовать угловой момент, но, используя это предположение, он смог вычислить энергии в спектре водорода, чего в то время еще никто не делал.
Ниже приведена диаграмма уровней энергии, которая является удобным способом отображения энергетических состояний – разрешенных уровней энергии электрона (относительно нашего обсуждения).Энергия отображается вертикально: низшее или основное состояние находится внизу, а возбужденные состояния – вверху. Учитывая энергии линий в атомном спектре, можно (хотя иногда очень сложно) определить энергетические уровни атома. Диаграммы уровней энергии используются для многих систем, включая молекулы и ядра. Теория атома или любой другой системы должна предсказывать его энергию на основе физики системы.
График уровня энергии : Диаграмма уровней энергии отображает энергию по вертикали и полезна для визуализации энергетических состояний системы и переходов между ними.Эта диаграмма предназначена для электронов атома водорода и показывает переход между двумя орбитами, имеющими энергии [латекс] \ text {E} _4 [/ latex] и [latex] \ text {E} _2 [/ latex].
Энергия орбиты Бора
Основываясь на своих предположениях, Бор вывел несколько важных свойств атома водорода из классической физики.
Цели обучения
Примените соответствующее уравнение для расчета уровней энергии и энергии испускаемого фотона для водородоподобного атома
Основные выводы
Ключевые моменты
- Согласно Бору, допустимый радиус орбиты в любом [латексе] \ text {n} [/ latex] равен [latex] \ text {r} _ \ text {n} = {\ text {n} ^ 2 \ hbar ^ 2 \ over \ text {Zk} _ \ text {e} \ text {e} ^ 2 \ text {m} _ \ text {e}} [/ latex].2} \ right) \, [/ latex], которая известна как формула Ридберга.
Ключевые термины
- центростремительный : Направлен или движется к центру.
Исходя из предположений Бора, мы выведем ряд важных свойств атома водорода из классической физики. Начнем с того, что центростремительная сила, заставляющая электрон двигаться по круговой траектории, обеспечивается кулоновской силой. Чтобы быть более общим, отметим, что этот анализ справедлив для любого одноэлектронного атома.2} {2 \ text {r}} [/ latex]
Полная энергия отрицательна и обратно пропорциональна [latex] \ text {r} [/ latex]. Это означает, что требуется энергия, чтобы оттолкнуть вращающийся электрон от протона. Для бесконечных значений [latex] \ text {r} [/ latex] энергия равна нулю, что соответствует неподвижному электрону, бесконечно удаленному от протона.
А вот и квантовое правило: как мы видели в предыдущем модуле, угловой момент [латекс] \ text {L} = \ text {m} _ \ text {e} \ text {r} \ text {v} [/ latex] является целым числом, кратным [latex] \ hbar [/ latex]:
[латекс] \ text {m} _ \ text {e} \ text {v} \ text {r} = \ text {n} \ hbar [/ latex]
Подстановка выражения в уравнение скорости выше дает уравнение для [latex] \ text {r} [/ latex] в терминах [latex] \ text {n} [/ latex]:
[латекс] \ sqrt {\ text {Zk} _ \ text {e} \ text {e} ^ 2 \ text {m} _ \ text {e} \ text {r}} = \ text {n} \ hbar [/ латекс]
Тогда допустимый радиус орбиты при любом n равен:
. 2 \ text {m} _ \ text {e}} [/ latex]Наименьшее возможное значение [latex] \ text {r} [/ latex] в атоме водорода называется радиусом Бора и равно 0.2} \ справа) [/ латекс]
Это формула Ридберга, описывающая весь спектр водорода, а [латекс] \ text {R} [/ latex] – постоянная Ридберга. Модель Бора очень хорошо предсказывала экспериментальный спектр водорода.
Рис. 1 : Схема спектра водорода показывает несколько серий, названных в честь тех, кто внес наибольший вклад в их определение. Часть серии Бальмера находится в видимом спектре, серия Лаймана полностью в УФ, а серия Пашена и другие – в ИК.2}) [/ латекс].
Цели обучения
Объясните разницу между сериями Лаймана, Бальмера и Пашена
Основные выводы
Ключевые моменты
- Атомные и молекулярные спектры излучения и поглощения известны уже более века как дискретные (или квантованные).
- Серии Лаймана, Бальмера и Пашена названы в честь первых исследователей, изучавших их особенно глубоко.
- Бор был первым, кто дал теоретическое объяснение спектрам водорода.
Ключевые термины
- фотон : Квант света и другой электромагнитной энергии, рассматриваемый как дискретная частица, имеющая нулевую массу покоя, отсутствие электрического заряда и неопределенно долгое время жизни.
- спектр : Состояние, которое не ограничивается определенным набором значений, но может бесконечно изменяться в пределах континуума. Это слово впервые было использовано в науке в области оптики для описания радуги цветов в видимом свете при разделении с помощью призмы.
На протяжении десятилетий задавалось много вопросов об атомных характеристиках. Об атомах было известно многое, от их размеров до спектров, но мало что было объяснено с точки зрения законов физики. Спектры атомного и молекулярного излучения и поглощения известны уже более века как дискретные (или квантованные). Максвелл и другие поняли, что должна быть связь между спектром атома и его структурой, что-то вроде резонансных частот музыкальных инструментов.Но, несмотря на годы усилий многих великих умов, ни у кого не было работоспособной теории. (Ходила шутка, что любую теорию атомных и молекулярных спектров можно разрушить, бросив в нее книгу данных, настолько сложны были спектры.) Следуя предложению Эйнштейна о фотонах с квантованной энергией, прямо пропорциональной их длинам волн, она стала даже Более очевидно, что электроны в атомах могут существовать только на дискретных орбитах.
В некоторых случаях удавалось разработать формулы, описывающие спектры излучения.{-1} [/ latex] и [latex] \ text {n} _ \ text {f} [/ latex], [latex] \ text {n} _ \ text {i} [/ latex] являются целыми положительными числами. связаны с определенной серией.
Эти серии названы в честь первых исследователей, изучавших их особенно глубоко. Для серии Lyman [латекс] \ text {n} _ \ text {f} = 1 [/ latex] для серии Balmer [латекс] \ text {n} _ \ text {f} = 2 [/ latex] ; для серии Пашен [латекс] \ text {n} _ \ text {f} = 3 [/ latex]; и так далее. Серия Lyman полностью находится в УФ, в то время как часть серии Бальмера видна с остальной частью УФ.Серия Paschen и все остальное полностью IR. По-видимому, существует неограниченное количество серий, хотя они постепенно уходят в инфракрасный свет и становятся трудными для наблюдения по мере увеличения [latex] \ text {n} _ \ text {f} [/ latex]. Константа [latex] \ text {n} _ \ text {i} [/ latex] является положительным целым числом, но должно быть больше, чем [latex] \ text {n} _ \ text {f} [/ latex]. Таким образом, для серии Balmer [латекс] \ text {n} _ \ text {f} = 2 [/ latex] и [latex] \ text {n} _ \ text {i} = 3,4,5,6 …[/латекс]. Обратите внимание, что [latex] \ text {n} _ \ text {i} [/ latex] может приближаться к бесконечности.
Электронные переходы и их результирующие длины волн для водорода. : Уровни энергии не соответствуют масштабу.
Хотя формула в уравнении длин волн была просто рецептом, разработанным для подбора данных и не основывалась на физических принципах, она имела более глубокий смысл. Балмер сначала разработал формулу только для своей серии, а позже было обнаружено, что она описывает все остальные серии с использованием различных значений [latex] \ text {n} _ \ text {f} [/ latex]. Бор был первым, кто понял более глубокий смысл.Опять же, мы видим взаимодействие между экспериментом и теорией в физике. Экспериментально спектры были хорошо установлены, уравнение соответствовало экспериментальным данным, но теоретическое обоснование отсутствовало.
Модель де Бройля и Бора
Предполагая, что электрон описывается волной и должно соответствовать целое число длин волн, мы выводим предположение о квантовании Бора.
Цели обучения
Опишите новую интерпретацию состояния Бора де Бройлем
Основные выводы
Ключевые моменты
- Условие Бора о том, что угловой момент является целым кратным [латекс] \ hbar [/ латекс], было позже переинтерпретировано в 1924 году де Бройлем как условие стоячей волны.
- Для того, что Бор был вынужден выдвинуть гипотезу как правило для допустимых орбит, концепция волны материи де Бройля объясняет это как условие конструктивной интерференции электрона на круговой орбите.
- Модель Бора применима только к водородоподобным атомам. В 1925 году благодаря Гейзенбергу и Шредингеру появились более общие формы описания (теперь называемые квантовой механикой).
Ключевые термины
- стоячая волна : форма волны, которая возникает в ограниченной фиксированной среде таким образом, что отраженная волна совпадает с создаваемой волной.Типичный пример – вибрация струн на музыкальном струнном инструменте.
- материальная волна : Концепция отражает дуальность материи волна-частица. Теория была предложена Луи де Бройлем.
Условие Бора о том, что угловой момент является целым числом, кратным [латекс] \ hbar [/ латекс], было позже переосмыслено в 1924 году де Бройлем как условие стоячей волны. Впоследствии волнообразные свойства вещества были подтверждены наблюдениями за интерференцией электронов при их рассеянии на кристаллах.Электроны могут существовать только там, где они конструктивно мешают. Как это влияет на электроны на атомных орбитах? Когда электрон связан с атомом, его длина волны должна умещаться в небольшом пространстве, что-то вроде стоячей волны на струне.
Волны на струне : (a) Волны на струне имеют длину волны, связанную с длиной струны, что позволяет им конструктивно интерферировать. (б) Если мы представим струну, изогнутую в замкнутый круг, мы получим приблизительное представление о том, как электроны на круговых орбитах могут конструктивно интерферировать.(c) Если длина волны не соответствует длине окружности, электрон деструктивно вмешивается; он не может существовать на такой орбите.
Допустимые орбиты – это орбиты, на которых электрон конструктивно мешает самому себе. Не все орбиты создают конструктивную интерференцию, и поэтому разрешены только определенные орбиты (то есть орбиты квантуются). Предполагая, что электрон описывается волной, и целое число длин волн должно соответствовать окружности орбиты электрона, мы получаем уравнение:
[латекс] \ text {n} \ lambda = 2 \ pi \ text {r} [/ latex]
Замена длины волны де Бройля [латекс] \ frac {\ text {h}} {\ text {p}} [/ latex] воспроизводит правило Бора.Поскольку [latex] \ lambda = \ text {h} / \ text {m} _ \ text {ev} [/ latex], теперь у нас есть:
[латекс] \ displaystyle \ frac {\ text {nh}} {\ text {m} _ \ text {ev}} = 2 \ pi \ text {r} _ \ text {n} [/ latex]
Переставив термины и отметив, что [latex] \ text {L} = \ text {mvr} [/ latex] для круговой орбиты, мы получаем квантование углового момента как условие для допустимых орбит:
[латекс] \ displaystyle \ text {L} = \ text {m} _ \ text {e} \ text {v} \ text {r} _ \ text {n} = \ text {n} \ frac {\ text {h}} {2 \ pi}, (\ text {n} = 1,2,3…) [/ latex]
Как говорилось ранее, Бор был вынужден выдвинуть гипотезу об этом правиле для разрешенных орбит.Теперь мы понимаем это как условие конструктивной интерференции электрона на круговой орбите.
Соответственно, в 1925 году был предложен новый вид механики, квантовая механика. Модель Бора электронов, движущихся по квантованным орбитам, была расширена до более точной модели движения электронов. Новую теорию предложил Вернер Гейзенберг. По иным соображениям австрийским физиком Эрвином Шредингером независимо была открыта другая форма той же теории – волновая механика.Шредингер использовал волны материи де Бройля, но вместо этого искал волновые решения трехмерного волнового уравнения. Это описывало электроны, которые были вынуждены двигаться вокруг ядра водородоподобного атома, будучи захваченными потенциалом положительного заряда ядра.
Волны материи де Бройля оправдывают магические радиусы орбиты электрона Бора : Я включаю краткое изложение электронной структуры атома водорода и объясняю, как электрон может мешать самому себе на орбите, как это может быть в эксперименте с двумя щелями.
Рентгеновские лучи и эффект Комптона
Комптон объяснил сдвиг частоты рентгеновских лучей во время рассеяния рентгеновских лучей / электронов, приписывая импульс, подобный частицам, «фотонам».
Цели обучения
Описание эффектов Комптона между электронами и рентгеновскими фотонами
Основные выводы
Ключевые моменты
- Комптон вывел математическую зависимость между сдвигом длины волны и углом рассеяния рентгеновских лучей.
- Комптоновские эффекты (с электронами) обычно возникают с рентгеновскими фотонами.
- Если фотон имеет более низкую энергию, в видимом свете в диапазоне мягких рентгеновских лучей наблюдаются фотоэлектрические эффекты. Фотоны с более высокой энергией в диапазоне гамма-лучей могут привести к образованию пар.
Ключевые термины
- гамма-излучение : электромагнитное излучение очень высокой частоты (и, следовательно, очень высокой энергии), излучаемое как следствие радиоактивности.
- фотоэлектрические эффекты : При фотоэлектрических эффектах электроны испускаются из материи (металлов и неметаллических твердых тел, жидкостей или газов) в результате поглощения ими энергии электромагнитного излучения.
- фотон : Квант света и другой электромагнитной энергии, рассматриваемый как дискретная частица, имеющая нулевую массу покоя, отсутствие электрического заряда и неопределенно долгое время жизни.
К началу 20 века исследования взаимодействия рентгеновских лучей с веществом были в полном разгаре. Было замечено, что когда рентгеновские лучи известной длины волны взаимодействуют с атомами, рентгеновские лучи рассеиваются под углом [латекс] \ тета [/ латекс] и выходят на другой длине волны, связанной с [латексом] \ тета [/ латексом. ].Хотя классический электромагнетизм предсказывал, что длина волны рассеянных лучей должна быть равна начальной длине волны, многочисленные эксперименты показали, что длина волны рассеянных лучей была больше (соответствующей меньшей энергии), чем исходная длина волны.
В 1923 году Комптон опубликовал статью в Physical Review, в которой объяснил сдвиг рентгеновских лучей, приписывая импульс, подобный частицам, «фотонам», которые Эйнштейн использовал в своем получившем Нобелевскую премию объяснении фотоэлектрического эффекта.Впервые постулированные Планком, эти «частицы» концептуализировали «квантованные» элементы света как содержащие определенное количество энергии, зависящее только от частоты света. В своей статье Комптон вывел математическую связь между сдвигом длины волны и углом рассеяния рентгеновских лучей, предположив, что каждый рассеянный рентгеновский фотон взаимодействует только с одним электроном. Его статья завершается отчетом об экспериментах, которые подтвердили полученное им соотношение:
[латекс] \ displaystyle \ lambda ‘- \ lambda = \ frac {\ text {h}} {\ text {m} _ \ text {e} \ text {c}} (1- \ cos {\ theta}) [/ латекс]
где λ \ lambda – начальная длина волны, λ ′ \ lambda ‘- длина волны после рассеяния, [latex] \ text {h} [/ latex] – постоянная Планка, mem_e – масса покоя электрона, [latex] \ text {c} [/ latex] – это скорость света, а θ \ theta – угол рассеяния.{-12} [/ латекс] м. Сдвиг длины волны [latex] \ lambda ‘- \ lambda [/ latex] должен быть не менее нуля (для [latex] \ theta = 0 [/ latex] °) и не более чем в два раза больше комптоновской длины волны электрона (для [latex] \ theta = 180 [/ latex] °). (Вывод формулы Комптона немного длинен и здесь не рассматривается.)
Фотон, сталкивающийся с неподвижной целью : фотон с длиной волны [латекс] \ lambda [/ latex] входит слева, сталкивается с неподвижной целью и новый фотон с длиной волны [латекс] \ lambda ‘ [/ latex] выходит под углом [latex] \ theta [/ latex].
Поскольку масса-энергия и импульс системы должны сохраняться, для электрона, как правило, невозможно просто двигаться в направлении падающего фотона. Взаимодействие между электронами и фотонами высокой энергии (сравнимо с энергией покоя электрона, 511 кэВ) приводит к тому, что электрону отдается часть энергии (заставляя его отскочить), а фотон, содержащий оставшуюся энергию, излучается в другом направлении. от оригинала, так что общий импульс системы сохраняется.Если у рассеянного фотона остается достаточно энергии, процесс комптоновского рассеяния может быть повторен. В этом сценарии электрон рассматривается как свободный или слабо связанный. Фотоны с энергией этого порядка величины находятся в рентгеновском диапазоне спектра электромагнитного излучения. Следовательно, можно сказать, что эффекты Комптона (с электронами) возникают с рентгеновскими фотонами.
Если фотон имеет более низкую энергию, но все же имеет достаточную энергию (обычно от нескольких эВ до нескольких кэВ, что соответствует видимому свету через мягкое рентгеновское излучение), он может полностью выбросить электрон из своего основного атома (процесс, известный как фотоэффект), а не подвергаться комптоновскому рассеянию.Фотоны с более высокой энергией (1,022 МэВ и выше в диапазоне гамма-лучей) могут бомбардировать ядро и вызывать образование электрона и позитрона. Этот процесс называется рождением пар.
Рентгеновские спектры: происхождение, дифракция на кристаллах и важность
Рентгеновские лучи показывают свою волновую природу, когда излучаются на атомные / молекулярные структуры, и могут использоваться для их изучения.
Цели обучения
Описать взаимодействие между рентгеновскими лучами и атомами
Основные выводы
Ключевые моменты
- Рентгеновские лучи – это относительно высокочастотное электромагнитное излучение.Они создаются переходами между электронными уровнями внутренней оболочки, которые производят рентгеновские лучи, характерные для атомного элемента, или ускорением электронов.
- Рентгеновская дифракция – это метод, который дает подробную информацию о кристаллографической структуре природных и промышленных материалов.
- Текущие исследования в области материаловедения и физики включают сложные материалы, структура решетки которых имеет решающее значение для получения сверхпроводящего материала, который можно изучать с помощью рентгеновской кристаллографии.
Ключевые термины
- двухспиральная структура : структура, образованная двухцепочечными молекулами нуклеиновых кислот, таких как ДНК и РНК.
- кристаллография : экспериментальная наука об определении расположения атомов в твердых телах.
- дифракция : изгиб волны вокруг краев отверстия или препятствия.
В предыдущем документе «Атом о рентгеновских лучах» мы видели, что есть два процесса, посредством которых рентгеновские лучи производятся в аноде рентгеновской трубки.В одном процессе замедление электронов производит рентгеновские лучи, и эти рентгеновские лучи называются тормозным излучением или тормозным излучением. Второй процесс является атомарным по природе и дает характерные рентгеновские лучи, названные так потому, что они характерны для материала анода. Спектр рентгеновского излучения является типичным для рентгеновской трубки, демонстрируя широкую кривую тормозного излучения с характерными рентгеновскими пиками на ней.
Рентгеновский спектр : Рентгеновский спектр, полученный при ударе энергичных электронов о материал, например анод ЭЛТ.Гладкая часть спектра – это тормозное излучение, а пики характерны для материала анода. Другой материал анода будет иметь характерные рентгеновские пики на разных частотах.
Поскольку рентгеновские фотоны очень энергичны, они имеют относительно короткие длины волн. Например, рентгеновское излучение Kα с энергией 54,4 кэВ, например, имеет длину волны [латекс] \ lambda = \ frac {\ text {hc}} {\ text {E}} = 0,0228 [/ латекс] нм. Таким образом, типичные рентгеновские фотоны действуют как лучи, когда сталкиваются с макроскопическими объектами, такими как зубы, и создают резкие тени.Однако, поскольку атомы и атомные структуры имеют типичный размер порядка 0,1 нм, рентгеновское излучение показывает их волновую природу. Этот процесс называется дифракцией рентгеновских лучей, потому что он включает в себя дифракцию и интерференцию рентгеновских лучей для создания структур, которые можно анализировать для получения информации о структурах, рассеивающих рентгеновские лучи.
Как показано ниже, закон Брэгга дает углы когерентного и некогерентного рассеяния света кристаллической решеткой, которое происходит во время дифракции рентгеновских лучей.Когда рентгеновские лучи падают на атом, они заставляют электронное облако двигаться как электромагнитная волна. Движение этих зарядов повторно излучает волны с той же частотой. Это называется рэлеевским рассеянием, о котором вы должны помнить по предыдущему атому. То же самое происходит, когда нейтронные волны от ядер разлетаются от взаимодействия с неспаренным электроном. Эти повторно излучаемые волновые поля интерферируют друг с другом конструктивно или деструктивно и создают дифракционную картину, которая фиксируется датчиком или пленкой.Это называется дифракцией Брэгга и является основой дифракции рентгеновских лучей.
Дифракция рентгеновских лучей : Закон дифракции Брэгга: иллюстрация того, как рентгеновские лучи взаимодействуют с кристаллической решеткой.
Возможно, самым известным примером дифракции рентгеновских лучей является открытие структуры двойной спирали ДНК в 1953 году. Используя данные дифракции рентгеновских лучей, исследователи смогли различить структуру ДНК, показывающую дифрактограмму, образованную рассеянием рентгеновские лучи от кристалла белка.Этот процесс известен как рентгеновская кристаллография из-за информации, которую он может дать о кристаллической структуре. Рентгеновские лучи не только подтверждают размер и форму атомов, но и дают информацию об их расположении в материалах. Например, текущие исследования высокотемпературных сверхпроводников включают сложные материалы, структура решетки которых имеет решающее значение для получения сверхпроводящего материала. Их можно изучить с помощью рентгеновской кристаллографии.
Дифракция рентгеновских лучей : Дифракция рентгеновских лучей от кристалла белка, лизоцима куриного яйца, дала эту интерференционную картину.Анализ структуры дает информацию о структуре белка.
Эффект Комптона
Эффект Комптона – это явление уменьшения энергии фотона, рассеянного свободной заряженной частицей.
Цели обучения
Объясните, почему комптоновское рассеяние является неупругим.
Основные выводы
Ключевые моменты
- Комптоновское рассеяние является примером неупругого рассеяния, поскольку длина волны рассеянного света отличается от падающего излучения.
- Как и фотоэлектрические эффекты, эффект Комптона важен, потому что он демонстрирует, что свет не может быть объяснен исключительно как волновое явление. Свет должен вести себя так, как будто он состоит из частиц, чтобы объяснить комптоновское рассеяние.
- Эксперимент Комптона убедил физиков в том, что свет может вести себя как поток частиц (квантов), энергия которых пропорциональна частоте.
Ключевые термины
- Доплеровский сдвиг : изменение частоты волны для наблюдателя, движущегося относительно ее источника.
- Томсоновское рассеяние : упругое рассеяние электромагнитного излучения на свободной заряженной частице, описываемое классическим электромагнетизмом. Это просто низкоэнергетический предел комптоновского рассеяния
- неупругое рассеяние : фундаментальный процесс рассеяния, в котором кинетическая энергия падающей частицы не сохраняется
Комптоновское рассеяние – это неупругое рассеяние фотона на свободной заряженной частице (обычно электроне).Это приводит к уменьшению энергии (увеличению длины волны) фотона (который может быть фотоном рентгеновского или гамма-излучения), что называется эффектом Комптона. Часть энергии фотона передается рассеивающему электрону. Обратное комптоновское рассеяние также существует, и происходит, когда заряженная частица передает часть своей энергии фотону.
Рассеяние в эффекте Комптона : Эффект Комптона – это название, данное рассеянию фотона электроном. Энергия и импульс сохраняются, что приводит к уменьшению и для рассеянного фотона.Изучая этот эффект, Комптон подтвердил, что у фотонов есть импульс.
Комптоновское рассеяние является примером неупругого рассеяния, поскольку длина волны рассеянного света отличается от падающего излучения. Тем не менее, происхождение эффекта можно рассматривать как упругое столкновение фотона с электроном. Величина изменения длины волны называется комптоновским сдвигом. Хотя ядерное комптоновское рассеяние существует, комптоновское рассеяние обычно относится к взаимодействию, в котором участвуют только электроны атома.
Эффект Комптона важен, потому что он демонстрирует, что свет не может быть объяснен исключительно как волновое явление. Томсоновское рассеяние, классическая теория электромагнитной волны, рассеянной заряженными частицами, не может объяснить сдвиги длины волны малой интенсивности: классически, свет достаточной интенсивности для того, чтобы электрическое поле ускоряло заряженную частицу до релятивистской скорости, вызывает отдачу радиационного давления и связанный доплеровский сдвиг рассеянного света. Однако эффект станет произвольно малым при достаточно низкой интенсивности света независимо от длины волны.Свет должен вести себя так, как будто он состоит из частиц, чтобы объяснить комптоновское рассеяние малой интенсивности. Эксперимент Комптона убедил физиков в том, что свет может вести себя как поток частиц (квантов), энергия которых пропорциональна частоте.
Структура атома
Обзор атомной структуры
Атомы состоят из частиц, называемых протонами, нейтронами и электронами, которые отвечают за массу и заряд атомов.
Цели обучения
Обсудить электронные и структурные свойства атома
Основные выводы
Ключевые моменты
- Атом состоит из двух областей: ядра, которое находится в центре атома и содержит протоны и нейтроны, и внешней области атома, которая удерживает свои электроны на орбите вокруг ядра.
- Протоны и нейтроны имеют примерно одинаковую массу, около 1,67 × 10-24 грамма, которую ученые определяют как одну атомную единицу массы (а.е.м.) или один Дальтон.
- Каждый электрон имеет отрицательный заряд (-1), равный положительному заряду протона (+1).
- Нейтроны – это незаряженные частицы, находящиеся в ядре.
Ключевые термины
- атом : наименьшее возможное количество вещества, которое все еще сохраняет свою идентичность как химический элемент, состоящее из ядра, окруженного электронами.
- протон : положительно заряженная субатомная частица, составляющая часть ядра атома и определяющая атомный номер элемента.Он весит 1 а.е.м.
- нейтрон : субатомная частица, составляющая часть ядра атома. Это бесплатно. По массе он равен протону или весит 1 а.е.м.
Атом – это наименьшая единица вещества, которая сохраняет все химические свойства элемента. Атомы объединяются в молекулы, которые затем взаимодействуют с образованием твердых тел, газов или жидкостей. Например, вода состоит из атомов водорода и кислорода, которые объединились, чтобы сформировать молекулы воды.Многие биологические процессы посвящены расщеплению молекул на составляющие их атомы, чтобы из них можно было собрать более полезную молекулу.
Атомные частицы
Атомы состоят из трех основных частиц: протонов, электронов и нейтронов. Ядро (центр) атома содержит протоны (положительно заряженные) и нейтроны (без заряда). Внешние области атома называются электронными оболочками и содержат электроны (отрицательно заряженные). Атомы имеют разные свойства в зависимости от расположения и количества их основных частиц.
Атом водорода (H) содержит только один протон, один электрон и не содержит нейтронов. Это можно определить, используя атомный номер и массовое число элемента (см. Понятие атомных номеров и массовых чисел).
Структура атома : Изображенные здесь элементы, такие как гелий, состоят из атомов. Атомы состоят из протонов и нейтронов, расположенных внутри ядра, а электроны находятся на орбиталях, окружающих ядро.
Атомная масса
Протоны и нейтроны имеют примерно одинаковую массу, около 1.67 × 10 -24 грамм. Ученые определяют это количество массы как одну атомную единицу массы (а.е.м.) или один дальтон. Протоны схожи по массе, но заряжены положительно, а нейтроны не имеют заряда. Следовательно, количество нейтронов в атоме существенно влияет на его массу, но не на его заряд.
Электроны намного меньше по массе, чем протоны, всего 9,11 × 10 -28 грамма, или примерно 1/1800 атомной единицы массы. Следовательно, они не вносят большой вклад в общую атомную массу элемента.При рассмотрении атомной массы принято игнорировать массу любых электронов и вычислять массу атома, исходя только из числа протонов и нейтронов.
Электроны вносят большой вклад в заряд атома, поскольку каждый электрон имеет отрицательный заряд, равный положительному заряду протона. Ученые определяют эти обвинения как «+1» и «-1». В незаряженном нейтральном атоме количество электронов, вращающихся вокруг ядра, равно количеству протонов внутри ядра. В этих атомах положительный и отрицательный заряды нейтрализуют друг друга, в результате чего получается атом без чистого заряда.
Протоны, нейтроны и электроны : Протоны и нейтроны имеют массу 1 а.е.м. и находятся в ядре. Однако протоны имеют заряд +1, а нейтроны не заряжены. Электроны имеют массу примерно 0 а.е.м., вращаются вокруг ядра и имеют заряд -1.
Изучение свойств электрона : Сравните поведение электронов с поведением других заряженных частиц, чтобы обнаружить такие свойства электронов, как заряд и масса.
Объем атомов
С учетом размеров протонов, нейтронов и электронов большая часть объема атома – более 99 процентов – фактически является пустым пространством. Несмотря на все это пустое пространство, твердые объекты не проходят сквозь друг друга. Электроны, окружающие все атомы, заряжены отрицательно и заставляют атомы отталкиваться друг от друга, не позволяя атомам занимать одно и то же пространство. Эти межмолекулярные силы не позволяют вам провалиться сквозь такой объект, как стул.
Interactive: создайте атом : создайте атом из протонов, нейтронов и электронов и посмотрите, как изменяются элемент, заряд и масса. Тогда сыграйте в игру, чтобы проверить свои идеи!
Атомный номер и массовое число
Атомный номер – это количество протонов в элементе, а массовое число – это количество протонов плюс количество нейтронов.
Цели обучения
Определите соотношение между массовым числом атома, его атомным номером, его атомной массой и количеством субатомных частиц.
Основные выводы
Ключевые моменты
- Нейтральные атомы каждого элемента содержат равное количество протонов и электронов.
- Число протонов определяет атомный номер элемента и используется, чтобы отличить один элемент от другого.
- Количество нейтронов варьируется, в результате чего образуются изотопы, которые представляют собой разные формы одного и того же атома, которые различаются только количеством нейтронов, которыми они обладают.
- Вместе количество протонов и количество нейтронов определяют массовое число элемента.
- Поскольку изотопы элемента имеют несколько разные массовые числа, атомная масса рассчитывается путем получения среднего массового числа его изотопов.
Ключевые термины
- массовое число : сумма количества протонов и количества нейтронов в атоме.
- атомный номер : количество протонов в атоме.
- атомная масса : Средняя масса атома с учетом всех его естественных изотопов.
Атомный номер
Нейтральные атомы элемента содержат равное количество протонов и электронов. Число протонов определяет атомный номер элемента (Z) и отличает один элемент от другого.Например, атомный номер углерода (Z) равен 6, потому что у него 6 протонов. Количество нейтронов может изменяться для получения изотопов, которые представляют собой атомы одного и того же элемента, имеющие разное количество нейтронов. Число электронов также может быть различным в атомах одного и того же элемента, в результате чего образуются ионы (заряженные атомы). Например, железо Fe может существовать в нейтральном состоянии или в ионных состояниях +2 и +3.
Массовое число
Массовое число элемента (A) – это сумма количества протонов и количества нейтронов.Небольшой вклад массы электронов не учитывается при вычислении массового числа. Это приближение массы можно использовать, чтобы легко вычислить, сколько нейтронов имеет элемент, просто вычтя количество протонов из массового числа. Протоны и нейтроны весят около одной атомной единицы массы или а.е.м. Изотопы одного и того же элемента будут иметь одинаковый атомный номер, но разные массовые числа.
Атомный номер, химический символ и массовое число : Углерод имеет атомный номер шесть и два стабильных изотопа с массовыми числами двенадцать и тринадцать соответственно.Его средняя атомная масса 12,11.
Ученые определяют атомную массу, вычисляя среднее значение массовых чисел естественных изотопов. Часто полученное число содержит десятичную дробь. Например, атомная масса хлора (Cl) составляет 35,45 а.е.м., потому что хлор состоит из нескольких изотопов, некоторые (большинство) с атомной массой 35 а.е.м. (17 протонов и 18 нейтронов), а некоторые с атомной массой 37 а.е.м. (17 протонов и 20 нейтронов).
Зная атомный номер (Z) и массовое число (A), вы можете найти количество протонов, нейтронов и электронов в нейтральном атоме.Например, атом лития (Z = 3, A = 7 а.е.м.) содержит три протона (находится из Z), три электрона (поскольку количество протонов равно количеству электронов в атоме) и четыре нейтрона (7 – 3 = 4).
Изотопы
Изотопы – это различные формы элементов, которые имеют одинаковое количество протонов, но разное количество нейтронов.
Цели обучения
Обсудить свойства изотопов и их использование в радиометрическом датировании
Основные выводы
Ключевые моменты
- Изотопы – это атомы одного и того же элемента, содержащие одинаковое количество протонов, но разное количество нейтронов.
- Несмотря на разное количество нейтронов, изотопы одного и того же элемента имеют очень похожие физические свойства.
- Некоторые изотопы нестабильны и подвергаются радиоактивному распаду, чтобы превратиться в другие элементы.
- Предсказуемый период полураспада различных распадающихся изотопов позволяет ученым датировать материал на основе его изотопного состава, например, с помощью датировки углерода-14.
Ключевые термины
- изотоп : Любая из двух или более форм элемента, в которых атомы имеют одинаковое количество протонов, но разное количество нейтронов в их ядрах.
- период полураспада : время, необходимое половине исходной концентрации изотопа, чтобы вернуться в более стабильную форму.
- радиоактивные изотопы : атом с нестабильным ядром, характеризующийся избыточной доступной энергией, который подвергается радиоактивному распаду и чаще всего создает гамма-лучи, альфа- или бета-частицы.
- радиоуглеродное датирование : Определение возраста объекта путем сравнения отношения обнаруженной в нем концентрации 14C к количеству 14C в атмосфере.
Что такое изотоп?
Изотопы – это различные формы элементов, которые имеют одинаковое количество протонов, но разное количество нейтронов. Некоторые элементы, такие как углерод, калий и уран, содержат несколько изотопов природного происхождения. Изотопы определяются сначала их элементом, а затем суммой присутствующих протонов и нейтронов.
- Углерод-12 (или 12 C) содержит шесть протонов, шесть нейтронов и шесть электронов; следовательно, он имеет массовое число 12 а.е.м. (шесть протонов и шесть нейтронов).
- Углерод-14 (или 14 C) содержит шесть протонов, восемь нейтронов и шесть электронов; его атомная масса 14 а.е.м. (шесть протонов и восемь нейтронов).
Хотя масса отдельных изотопов различна, их физические и химические свойства в основном не меняются.
Изотопы действительно различаются по стабильности. Углерод-12 ( 12 C) – самый распространенный изотоп углерода, составляющий 98,89% углерода на Земле. Углерод-14 ( 14 C) нестабилен и встречается только в следовых количествах.Нестабильные изотопы чаще всего испускают альфа-частицы (He 2+ ) и электроны. Также могут испускаться нейтроны, протоны и позитроны, а электроны могут быть захвачены для достижения более стабильной атомной конфигурации (более низкого уровня потенциальной энергии) посредством процесса, называемого радиоактивным распадом. Созданные новые атомы могут находиться в состоянии высокой энергии и испускать гамма-лучи, которые понижают энергию, но сами по себе не превращают атом в другой изотоп. Эти атомы называются радиоактивными изотопами или радиоизотопами.
Радиоуглеродное датирование
Углерод обычно присутствует в атмосфере в виде газообразных соединений, таких как диоксид углерода и метан. Углерод-14 ( 14 C) представляет собой радиоизотоп природного происхождения, который создается из атмосферного 14 N (азота) в результате добавления нейтрона и потери протона, вызванной космическими лучами. Это непрерывный процесс, поэтому в атмосфере всегда образуется больше 14 ° C. После производства 14 C часто соединяется с кислородом атмосферы с образованием диоксида углерода.Образовавшийся таким образом углекислый газ диффундирует в атмосфере, растворяется в океане и попадает в организм растений посредством фотосинтеза. Животные поедают растения, и в конечном итоге радиоуглерод распространяется по биосфере.
В живых организмах относительное количество 14 C в их теле примерно равно концентрации 14 C в атмосфере. Когда организм умирает, он больше не поглощает 14 ° C, поэтому соотношение между 14 ° C и 12 ° C будет снижаться, поскольку 14 ° C постепенно возвращается к 14 N.Этот медленный процесс, который называется бета-распадом, высвобождает энергию за счет испускания электронов из ядра или позитронов.
Примерно через 5730 лет половина исходной концентрации 14 C будет преобразована обратно в 14 Н. Это называется периодом полураспада или временем, которое требуется для получения половины исходной концентрации вещества. изотоп, чтобы вернуться в более стабильную форму. Поскольку период полураспада 14 C большой, он используется для датирования ранее живых объектов, таких как старые кости или дерево.Сравнивая отношение концентрации 14 C, обнаруженной в объекте, к количеству 14 C в атмосфере, можно определить количество изотопа, который еще не распался. На основе этого количества можно точно рассчитать возраст материала, если предполагается, что возраст материала составляет менее 50 000 лет. Этот метод называется радиоуглеродным датированием, или сокращенно углеродным датированием.
Применение углеродного датирования : Возраст углеродосодержащих останков менее 50 000 лет, таких как этот карликовый мамонт, можно определить с помощью углеродного датирования.
Другие элементы имеют изотопы с разным периодом полураспада. Например, 40 K (калий-40) имеет период полураспада 1,25 миллиарда лет, а 235 U (уран-235) имеет период полураспада около 700 миллионов лет. Ученые часто используют эти другие радиоактивные элементы для датирования объектов, возраст которых превышает 50 000 лет (предел углеродного датирования). Используя радиометрическое датирование, ученые могут изучать возраст окаменелостей или других останков вымерших организмов.
вопросов и ответов – Как сделать модель атома?
Как сделать модель атома?
Вам нужно сделать модель или рисунок атома для урока естествознания? Если да, следуйте этим инструкциям, чтобы узнать, куда идут все части атома.
Шаг 1. Сбор информации
Прежде чем вы сможете построить свою модель, вам необходимо знать, сколько протонов, нейтронов и электронов имеет ваш атом. Если вы еще не знаете, как использовать Периодическую таблицу элементов, чтобы найти эту информацию, прочтите «Сколько протонов, электронов и нейтронов находится в атоме…?» страницу, чтобы узнать, как это сделать.
В качестве примера возьмем азот. Используя информацию из Периодической таблицы элементов, мы можем сказать, что средний атом азота содержит 7 протонов, 7 нейтронов и 7 электронов.
Шаг 2 – Сбор материалов
Теперь, когда вы знаете, сколько протонов, нейтронов и электронов вам понадобится для вашей модели, пора решить, что использовать для их представления. Мячи для пинг-понга, резиновые мячи, шариковые подшипники, мячи для гольфа и мячи из пенополистирола использовались в прошлом. В принципе, подойдет все, что имеет округлую форму и может быть склеено друг с другом. Полезно, если шары имеют цветовую маркировку, чтобы было легче определить, какие шары являются протонами, какие – нейтронами, а какие – электронами.Также полезно, если электроны меньше протонов и нейтронов.
Шаг 3 – Постройте ядро
Ядро, центральная часть атома, состоит из протонов и нейтронов. Все протоны и нейтроны вашего атома переходят в ядро. Для азота ядро будет выглядеть примерно так:
Шаг 4 – Поместите электроны
Электроны находятся вне ядра. То, как вы их разместите, зависит от того, какую модель атомной структуры изучает ваш класс.Это можно сделать несколькими способами:
Планетарная модель
Эта модель изображает более раннее представление о структуре атома вскоре после открытия ядра. Эта модель обычно преподается младшим школьникам как введение в атомную структуру. В нем говорится, что электроны вращаются вокруг ядра так же, как планеты в солнечной системе вращаются вокруг Солнца. В зависимости от вашего учителя фактические орбиты обычно не имеют значения. Обычно достаточно иметь нужное количество электронов.Планетарная модель атома азота может выглядеть примерно так:
В планетарной модели атом азота имеет центральное ядро, состоящее из семи протонов и семи нейтронов, окруженных семью электронами.
Модель Бора
Ученые вскоре поняли, что планетарная модель является неточным описанием атомной структуры. Они узнали, что электроны могут занимать только определенные орбиты (обычно называемые энергетическими уровнями или оболочками) вокруг ядра.Они также обнаружили, что на каждом энергетическом уровне может поместиться только определенное количество электронов.
Чтобы правильно разместить электроны вокруг ядра, вам нужно будет обратиться к таблице электронной конфигурации вашего элемента. Чтобы найти таблицу электронной конфигурации вашего элемента, перейдите в Периодическую таблицу элементов, щелкните свой элемент и прокрутите страницу вниз. Если вы не знаете, как читать таблицу электронной конфигурации, прочтите «Как мне прочитать таблицу электронной конфигурации?» страницу для помощи.
Согласно таблице электронной конфигурации азота, атом азота содержит два электрона на первом уровне энергии и пять электронов на втором уровне энергии. Модель атома азота Бора могла бы выглядеть так:
В модели Бора атом азота имеет центральное ядро, состоящее из семи протонов и семи нейтронов, окруженных семью электронами. Два электрона находятся на первом уровне энергии, а другие пять – на втором уровне энергии.
Уточненная модель Бора
Дальнейшие исследования показали, что модель Бора не так точна, как могла бы быть. Ученые узнали, что каждый энергетический уровень состоит из определенного количества подоболочек. Каждая подоболочка, названная s, p, d и f, может содержать только определенное количество электронов. Подоболочка s может содержать только 2 электрона, подоболочка p может содержать 6, подоболочка d может содержать 10, а подоболочка f может содержать 14. Число доступных подоболочек увеличивается с увеличением уровня энергии. увеличивается.
Чтобы правильно разместить электроны вокруг ядра, вам нужно будет обратиться к таблице электронной конфигурации вашего элемента. Чтобы найти таблицу электронной конфигурации вашего элемента, перейдите в Периодическую таблицу элементов, щелкните свой элемент и прокрутите страницу вниз. Если вы не знаете, как читать таблицу электронной конфигурации, прочтите «Как мне прочитать таблицу электронной конфигурации?» страницу для помощи.
Согласно таблице электронной конфигурации азота, атом азота содержит два электрона на своем первом энергетическом уровне (оба в суб-оболочке s) и пять электронов на своем втором энергетическом уровне (два в суб-оболочке и три в суб-оболочке). p суб-оболочки).Более точная модель атома азота Бора могла бы выглядеть так:
В уточненной модели Бора атом азота имеет центральное ядро, состоящее из семи протонов и семи нейтронов, окруженных семью электронами. Два электрона находятся в подоболочке s первого энергетического уровня, два находятся в подоболочке s второго энергетического уровня и три находятся в подоболочке p второго энергетического уровня.
Шаг 5 – Что следует помнить
Важно помнить, что модель – это упрощенное представление объекта.Некоторые из рассмотренных выше моделей более точны, чем другие, но ни одна из них не является полностью правильной. Вот несколько вещей, которые мы проигнорировали:
Размер ядра
На рисунках выше ядро слишком велико. Или, другими словами, если ядро будет таким большим, электроны окажутся слишком близко. Настоящие атомы – это в основном пустое пространство. Если бы мы хотели, чтобы наши рисунки были точными, нам пришлось бы разместить электроны примерно в миле от них. Понятно, что принести в класс такой большой рисунок будет непросто.
Электроны не вращаются вокруг ядра
На рисунках выше мы нарисовали красивые круги, показывающие, где электроны вращаются вокруг атома. На самом деле ученые не могут точно сказать, где электрон в данный момент или куда он движется. Они могут вычислить вероятность того, что электрон будет найден в данном объеме пространства, но это не то же самое, что знать, где находится этот электрон. Такое поведение описано в квантовой модели атома. Хотя это наиболее точное описание атома, которое есть у ученых в настоящее время, его гораздо труднее понять.
Связанные страницы:
Все об атомах
Видео – Как нарисовать атом!
Что такое атом? Из чего состоят атомы?
Периодическая таблица элементов
Как узнать количество протонов, электронов и нейтронов в атоме элемента?
Сколько электронов умещается в каждой оболочке атома?
Как прочитать таблицу электронной конфигурации?
Боровская модель атома
Модель Бора имеет атом, состоящий из небольшого положительно заряженного ядра, на орбите которого движутся отрицательно заряженные электроны.Вот более подробный взгляд на модель Бора, которую иногда называют моделью Резерфорда-Бора.
Обзор модели Бора
Нильс Бор предложил модель атома Бора в 1915 году. Поскольку модель Бора является модификацией более ранней модели Резерфорда, некоторые люди называют модель Бора моделью Резерфорда-Бора. Современная модель атома основана на квантовой механике. Модель Бора содержит некоторые ошибки, но она важна, потому что она описывает большинство общепринятых черт теории атома без всей математики высокого уровня, как в современной версии.В отличие от более ранних моделей, модель Бора объясняет формулу Ридберга для спектральных эмиссионных линий атомарного водорода.
Модель Бора – это планетарная модель, в которой отрицательно заряженные электроны вращаются вокруг небольшого положительно заряженного ядра, подобного планетам, вращающимся вокруг Солнца (за исключением того, что орбиты не являются плоскими). Гравитационная сила Солнечной системы математически сродни кулоновской (электрической) силе между положительно заряженным ядром и отрицательно заряженными электронами.
Основные положения модели Бора
- Электроны вращаются вокруг ядра по орбитам с заданным размером и энергией.
- Энергия орбиты зависит от ее размера. Самая низкая энергия находится на самой маленькой орбите.
- Излучение поглощается или испускается, когда электрон перемещается с одной орбиты на другую.
Модель водорода Бора
Самый простой пример модели Бора – для атома водорода (Z = 1) или для водородоподобного иона (Z> 1), в котором отрицательно заряженный электрон вращается вокруг небольшого положительно заряженного ядра.Электромагнитная энергия будет поглощаться или испускаться, если электрон перемещается с одной орбиты на другую. Разрешены только определенные электронные орбиты. Радиус возможных орбит увеличивается как n 2 , где n – главное квантовое число. Переход 3 → 2 дает первую строку ряда Бальмера. Для водорода (Z = 1) это дает фотон с длиной волны 656 нм (красный свет).
Модель Бора для более тяжелых атомов
Более тяжелые атомы содержат больше протонов в ядре, чем атом водорода.Чтобы нейтрализовать положительный заряд всех этих протонов, требовалось больше электронов. Бор считал, что каждая электронная орбита может удерживать только определенное количество электронов. Как только уровень будет заполнен, дополнительные электроны будут переведены на следующий уровень. Таким образом, модель Бора для более тяжелых атомов описывает электронные оболочки. Модель объяснила некоторые атомные свойства более тяжелых атомов, которые ранее никогда не воспроизводились. Например, модель оболочек объясняет, почему атомы уменьшаются в размерах, перемещаясь по периоду (строке) периодической таблицы, даже несмотря на то, что у них было больше протонов и электронов.Это также объяснило, почему благородные газы были инертными и почему атомы в левой части таблицы Менделеева притягивают электроны, а атомы в правой части их теряют. Однако модель предполагала, что электроны в оболочках не взаимодействуют друг с другом, и не могла объяснить, почему электроны складываются нерегулярным образом.
Проблемы с моделью Бора
- Он нарушает принцип неопределенности Гейзенберга, поскольку считает, что электроны имеют как известный радиус, так и орбиту.
- Модель Бора дает неверное значение орбитального углового момента основного состояния.
- Он дает плохие предсказания относительно спектров более крупных атомов.
- Не предсказывает относительную интенсивность спектральных линий.
- Модель Бора не объясняет тонкую структуру и сверхтонкую структуру в спектральных линиях.
- Это не объясняет эффект Зеемана.
Уточнения и улучшения модели Бора
Наиболее заметным усовершенствованием модели Бора была модель Зоммерфельда, которую иногда называют моделью Бора-Зоммерфельда.В этой модели электроны движутся по эллиптическим орбитам вокруг ядра, а не по круговым орбитам. Модель Зоммерфельда лучше объясняла атомные спектральные эффекты, такие как эффект Штарка при расщеплении спектральных линий. Однако модель не могла вместить магнитное квантовое число.
В конечном итоге модель Бора и модели, основанные на ней, были заменены моделью Вольфганга Паули, основанной на квантовой механике в 1925 году. Эта модель была улучшена, чтобы создать современную модель, представленную Эрвином Шредингером в 1926 году.Сегодня поведение атома водорода объясняется с помощью волновой механики для описания атомных орбиталей.
Источники
- Лахтакия, Ахлеш; Солпитер, Эдвин Э. (1996). «Модели и моделисты водорода». Американский журнал физики . 65 (9): 933. Bibcode: 1997AmJPh..65..933L. DOI: 10,1119 / 1,18691
- Линус Карл Полинг (1970). «Глава 5-1». Общая химия (3-е изд.). Сан-Франциско: W.H. Freeman & Co. ISBN 0-486-65622-5.
- Нильс Бор (1913). «О строении атомов и молекул, часть I» (PDF). Философский журнал . 26 (151): 1–24. DOI: 10.1080 / 14786441308634955
- Нильс Бор (1914). «Спектры гелия и водорода». Природа . 92 (2295): 231–232. DOI: 10.1038 / 092231d0
Бора
Модель атома БораМодель атома Бора :
В 1913 году Бор предложил свою квантованную оболочечную модель атома, чтобы объяснить, как электроны могут иметь стабильные орбиты вокруг ядра.Движение электронов в модели Резерфорда был нестабильным, потому что, согласно классическая механика и теория электромагнетизма, любая заряженная частица движение по криволинейной траектории излучает электромагнитное излучение; Таким образом электроны потеряют энергию и спиралью попадут в ядро. Чтобы исправить Проблема устойчивости, Бор модифицировал модель Резерфорда, потребовав, чтобы электроны движутся по орбитам с фиксированным размером и энергией. Энергия электрон зависит от размера орбиты и меньше для меньших орбит.Излучение может происходить только тогда, когда электрон перескакивает с одной орбиты на другую. Другая. Атом будет полностью устойчив в состоянии с наименьшим орбите, поскольку нет орбиты с меньшей энергией, на которую электрон может Прыжок.
Отправной точкой Бора было осознание того, что классическая механика сама по себе никогда не мог объяснить стабильность атома. Стабильный атом имеет определенный размер так что любое уравнение, описывающее его, должно содержать некоторую фундаментальную постоянную или комбинация констант с размером длины.Классический фундаментальные константы, а именно заряды и массы электрона а ядро - нельзя объединить в длину. Бор заметил: однако квантовая постоянная, сформулированная немецким физиком Максом Планк имеет размеры, которые в сочетании с массой и зарядом электрон, произведите меру длины. Численно мера близка известному размеру атомов. Это побудило Бора использовать постоянную Планка. в поисках теории атома.
Планк ввел свою постоянную в 1900 году в формулу, объясняющую световое излучение, испускаемое нагретыми телами.Согласно классической теории, сопоставимые количества световой энергии должны производиться на всех частотах. Это не только противоречит наблюдениям, но и подразумевает абсурдную В результате полная энергия, излучаемая нагретым телом, должна быть бесконечной. Планк постулировал, что энергия может излучаться или поглощаться только дискретными суммы, которые он назвал квантами (латинское слово «сколько»). В квант энергии связан с частотой света новым фундаментальная постоянная, ч. Когда тело нагревается, его лучистая энергия в конкретный частотный диапазон, согласно классической теории, пропорционален к температуре тела.Однако согласно гипотезе Планка излучение может происходить только в квантовых количествах энергии. Если сияющий энергия меньше кванта энергии, количество света в этом частотный диапазон будет уменьшен. Формула Планка правильно описывает излучение от нагретых тел. Постоянная Планка имеет размеры действие, которое может быть выражено как единицы энергии, умноженные на время, единицы количества движения, умноженные на длину, или единицы углового момента. Для Например, постоянная Планка может быть записана как h = 6.6×10 -34 джоуль секунд.
Используя постоянную Планка, Бор получил точную формулу для энергии уровни атома водорода.


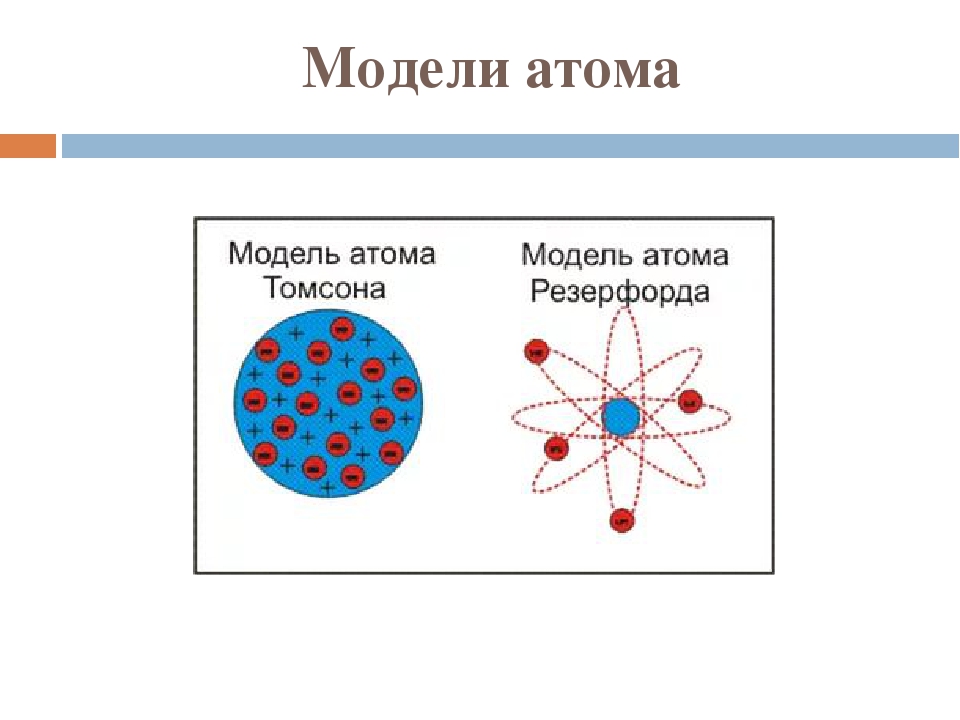 Обратно, освещение атома
электромагнитными волнами этой частоты может привести к процессу поглощения,
переводящее атом из конечного состояния в начальное».
Обратно, освещение атома
электромагнитными волнами этой частоты может привести к процессу поглощения,
переводящее атом из конечного состояния в начальное».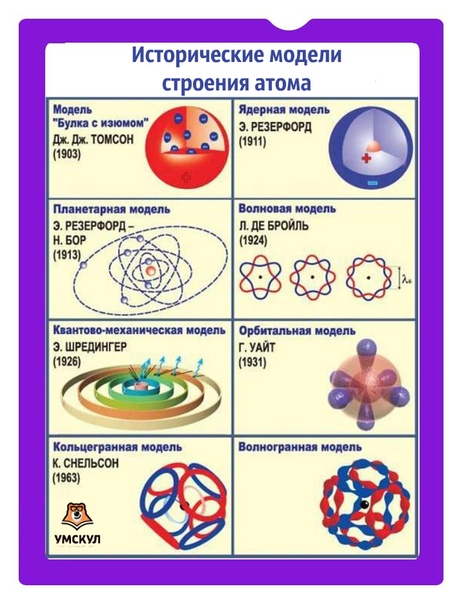 Это приводит к интересному предположению,
которое высказал
Это приводит к интересному предположению,
которое высказал  Э. Резерфорд впервые использовал ядерные реакции под действием
α‑частиц
для изучения свойств атомного ядра. Следующим шагом в познании строения материи
стало открытие в 1919 г. протона Э. Резерфордом и в 1932 г. нейтрона
Дж. Чадвиком. Оказалось, что на уровне 10–12 см вещество состоит из
протонов, нейтронов и электронов. Число
протонов в атомном ядре Z определяет
заряд атомного ядра. Суммарное число протонов Z и
нейтронов N определяет
массовое число A атомного
ядра
Э. Резерфорд впервые использовал ядерные реакции под действием
α‑частиц
для изучения свойств атомного ядра. Следующим шагом в познании строения материи
стало открытие в 1919 г. протона Э. Резерфордом и в 1932 г. нейтрона
Дж. Чадвиком. Оказалось, что на уровне 10–12 см вещество состоит из
протонов, нейтронов и электронов. Число
протонов в атомном ядре Z определяет
заряд атомного ядра. Суммарное число протонов Z и
нейтронов N определяет
массовое число A атомного
ядра 272
272 6·1026 лет
6·1026 лет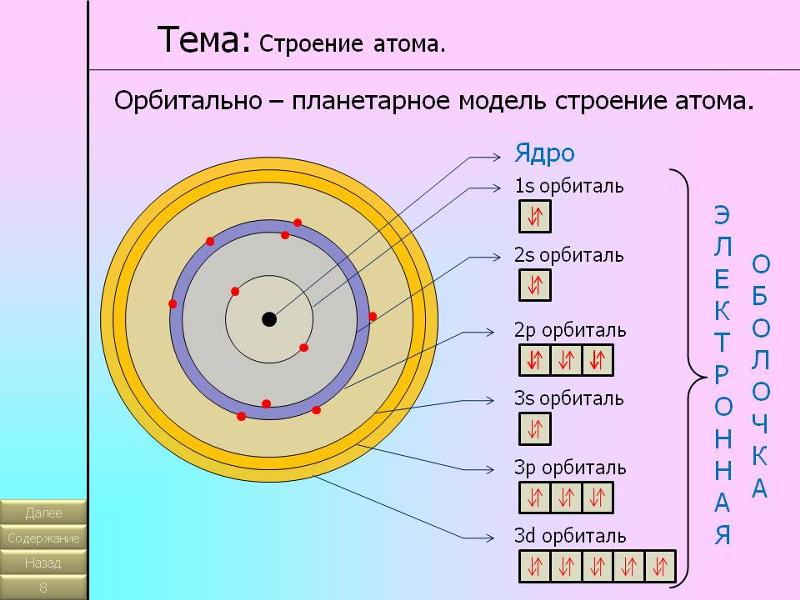 1. Планетарная модель атома Резерфорда. Показаны круговые орбиты четырех электронов
1. Планетарная модель атома Резерфорда. Показаны круговые орбиты четырех электронов Делимость электрического заряда»
Делимость электрического заряда»