Самые интересные факты об атомах и молекулах
Zefirka > Наука и технологии > Самые интересные факты об атомах и молекулах
Все разнообразие нашего мира построено из атомов и молекул. Удивительно, как проявления форм жизни образовались лишь на основе протонов, нейтронов и электронов. Элементарная основа позволяет каждому веществу и организму выполнять свою функцию. Так из семи нот пишется музыка разных направлений, разных стилей. Мы собрали 10 самых интересных фактов об атомах и молекулах.
1.
Самый легкий из атомов – атом водорода
В периодической таблице химических элементов водород стоит на первом месте. Его ядро состоит лишь из одного протона, вокруг которого вращается единственный электрон. Простейшее строение определяет минимальную массу, которую может иметь атом – 1,008 а.е.м. или 1,7х10-24 г.
На Земле водород существует в виде соединений с другими веществами или образует двухатомную молекулу Н2. Если считать в массовом отношении, на его долю приходится 1% земной коры. Если перевести массу в количество атомов, то содержание водорода окажется более внушительным – 17%. Этот показатель ставит элемент на второе место после кислорода (52%).
Если перевести массу в количество атомов, то содержание водорода окажется более внушительным – 17%. Этот показатель ставит элемент на второе место после кислорода (52%).
Во Вселенной водород составляет 88,6% от общей доли атомов, находящихся в космосе в виде звездного вещества и космической пыли.
2.
Главной молекулой живой природы является молекула ДНК
В молекуле ДНК сосредоточена информация о строении каждой клетки живого организма, словно это проектное бюро города, где собраны подробные планы всех зданий. Внешне она напоминает перевитую веревочную лестницу, состоящую из двух нитей и соединенную водородными связями. ДНК вирусов может представлять одну цепочку.
Информация зашифрована в генах, то есть участках молекулы. Ген представляет собой определенную последовательность нуклеотидов, способных передать код для построения белков и РНК (информационных, транспортных, рибосомных, матричных).
Спираль ДНК человека, если ее вытянуть, протянется почти на 2 м. Это тем более удивительно, что она умещается в ядре размером меньше микрометра. Свернуться в компактную хромосому молекуле помогают нуклеосомы. На них ДНК наматывается, как на катушку.
Это тем более удивительно, что она умещается в ядре размером меньше микрометра. Свернуться в компактную хромосому молекуле помогают нуклеосомы. На них ДНК наматывается, как на катушку.
3.
Пыль – это частица, состоящая из квадриллиона атомов
Пылью называют твердые минеральные или органические частицы размером не более 0,05 мм. Природа образования может быть как естественной, так и связанной с деятельностью человека (антропогенной). В воздух поднимаются вулканический пепел, морская соль, сухая почва, продукты горения после пожаров, пыльца растений. Человек способствует загрязнению воздуха продуктами отопления и горных разработок, выхлопами автотранспорта, удобрениями. Вспашка земли и оголение почвы выкосами травы опасны выветриванием и переносом верхнего слоя грунта ветром.
Если сравнивать твердую взвесь с газообразными загрязнителями воздуха, то последние присутствуют в виде отдельных молекул. Пыль же в каждой частице содержит огромное число молекул и еще большее число атомов.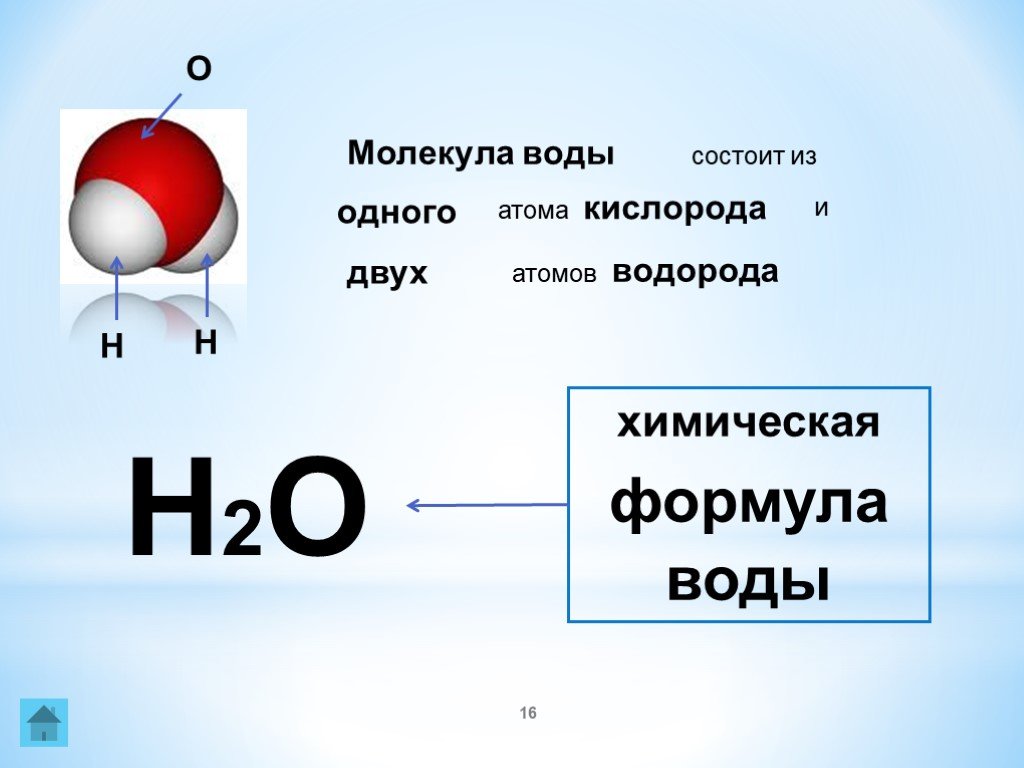
4.
Атом может иметь электрический заряд
В составе атома электроны несут отрицательный заряд, протоны – положительный. Нейтроны не имеют заряда, то есть нейтральны. Когда количество протонов равно количеству электронов, заряд атома равен нулю. В случае, если электронов больше или меньше, чем протонов, у атома появляется заряд. Он становится ионом.
Ядро, состоящее из нейтронов и протонов, обладает ощутимой массой. Нужно определенное количество энергии, чтобы заставить его терять протоны. Электроны, которые вращаются вокруг него, значительно легче могут перемещаться от одного атома к другому. Добавление электронов приводит к образованию отрицательного заряда, потеря частиц – положительного. Атомы с положительным зарядом называют катионами, атомы с избытком электронов становятся анионами.
5.
Самый тяжелый из атомов – атом урана
Из природных элементов атом урана имеет самую большую массу – 238,0289 а.е.м. В природе находится в основном в виде изотопа U-238. Атом с его 92 протонами чрезвычайно перегружен, при любой возможности выбрасывает протоны и нейтроны с огромной скоростью.
Атом с его 92 протонами чрезвычайно перегружен, при любой возможности выбрасывает протоны и нейтроны с огромной скоростью.
Открыл элемент германский химик Мартин Клапрот в 1789 году при анализе отработанной руды после добычи серебра. «Странное вещество», похожее на металл было диоксидом урана, но выяснилось это только через 50 лет. Клапрот назвал находку в честь далекой планеты, открытой к этому времени Гершелем.
В конце 19 века во Франции Анри Беккерель обнаружил радиоактивность урана, то есть способность терять частицы. Распад может иметь 14 циклов. Уран превращается в радий, радон и другие элементы, образуя на последней стадии свинец.
6.
Слово «атом» происходит из древнегреческого языка и означает «неделимый»
Еще в Древней Греции философ и математик Демокрит предположил, что окружающее состоит из мельчайших частичек. Отсюда произошел термин «атом» или «atomos». Однако подтверждение теория получила только в результате работы ученых в последние 150 лет и с помощью изобретенного микроскопа.
Первое исследование провел англичанин Джон Дальтон на рубеже 18-19 веков. Он установил, что химические элементы вступают в реакции в строго определенном соотношении (закон кратных отношений).
Сейчас мы знаем, что атом представляет собой наименьшую частицу химического элемента и не всегда является неделимым. В состав атома входит ядро с протонами и нейтронами или просто нуклонами от латинского слова «nucleus» – ядро. Снаружи вокруг атома расположено электронное облако.
7.
Стекло не является твердым телом
Твердость вещества – характеристика, основанная на прочности химических связей между атомами и молекулами. В жидкости частицы могут перемещаться относительно друг друга. В твердых телах они лишены такой возможности.
При производстве стекла молекулы кремния, обычно принимающие структуру кристаллической решетки, не успевают занят положенное им место. Стекло быстро остывает и частицы остаются перемешанными хаотично. Такое вещество называют аморфным, однако все же оно твердое.
Вязкость стекла сопоставима с вязкостью свинца, но ведь свинец никто не называет жидкостью. Бытует мнение, что со временем оконные стекла «стекают» вниз. В пример ставят витражи в средневековых храмах. Следует уточнить, что утолщения в их основании появились не с течением времени, а были изначально. Причина кроется в несовершенстве технологии производства.
8.
Молекула меньше яблока во столько же раз, во сколько яблоко меньше Земли
Чтобы представить видимые и невидимые параметры окружающего мира, представим все молекулы одного кубического сантиметра воздуха в виде кирпичей. Их количества хватило бы для покрытия поверхности планеты на высоту 40-этажного дома.
Размеры молекул и атомов настолько малы, что в решении задач молекулярной физики используют относительные величины. Установить их удалось лишь с изобретением электронного микроскопа. Средний диаметр атома и простейшей молекулы составляет порядка 10-10 м. Так, размер молекулы белка – 43х10-10 м.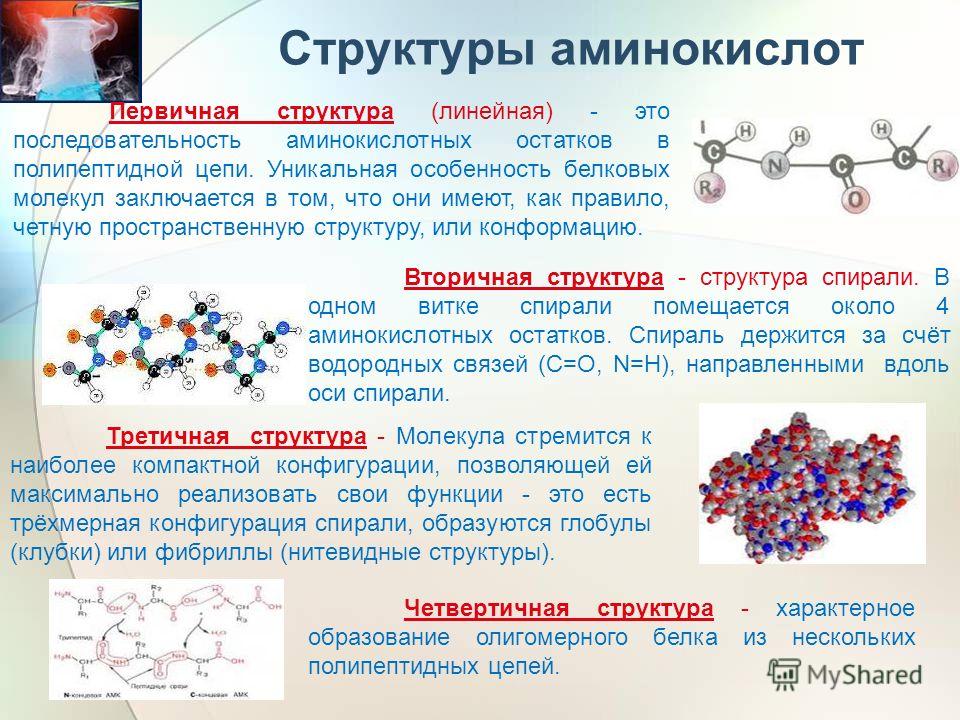 Крупные молекулы достигают 10-7 м.
Крупные молекулы достигают 10-7 м.
В ионный микроскоп можно разглядеть строение кристалла и даже определить межатомные расстояния.
9.
Ученые смогли охладить молекулы монофторида стронция практически до абсолютного нуля
Выбор пал на монофторид стронция (SrF) неслучайно. Принцип охлаждения атомов основан на периодическом повторении поглощения и испускания фотонов под воздействием лазера. Таким образом атом теряет кинетическую энергию. Молекулы не настолько чувствительны. Мешает колебательная и вращательная энергия межатомных связей. У фторида стронция эти явления минимальны.
Группа ученых Йельского университета во главе с Д. Демиллем добилась охлаждения молекулы до 300 мкК (0,0003 К). За счет подобранной длины волны лазер погасил вращательные межатомные движения. В дальнейшем молекулы вели себя аналогично атому.
Практически такое достижение в перспективе можно использовать в квантовых компьютерах.
10.
Скорость движения молекул воды может достигать 650 м/с
Молекулы воды находятся в постоянном тепловом движении. Они колеблются с большой частотой (одно колебание за 10-12 … 10-13 с) возле определенного положения, изредка прыгая на освободившееся соседнее место. Скорость движения при этом может приближаться к 600-650 м/с.
Они колеблются с большой частотой (одно колебание за 10-12 … 10-13 с) возле определенного положения, изредка прыгая на освободившееся соседнее место. Скорость движения при этом может приближаться к 600-650 м/с.
И все же молекулы не разлетаются, остаются жидкостью. Происходит это за счет водородных связей. В молекуле h3O пары электронов смещены в сторону кислорода. Водород, оставшийся практически без электрона, представляет собой положительно заряженное ядро. В результате протон водорода притягивает соседние атомы кислорода, образуя прочную межмолекулярную связь.
Благодаря такому сцеплению вода в условиях Земли принимает в основном жидкое состояние, а не кипит как аналогичные гидриды (серы, селена) при –80°С. Водородные связи определяют физические и химические свойства воды, на которых основана жизнь на нашей планете.
Источник: https://top10a.ru/10-interesnyx-faktov-ob-atomax-i-molekulax.html
Наука и технологии 22 января, 2021 2 236 просмотров
Интересные факты об атомах и молекулах
Все разнообразие нашего мира построено из атомов и молекул.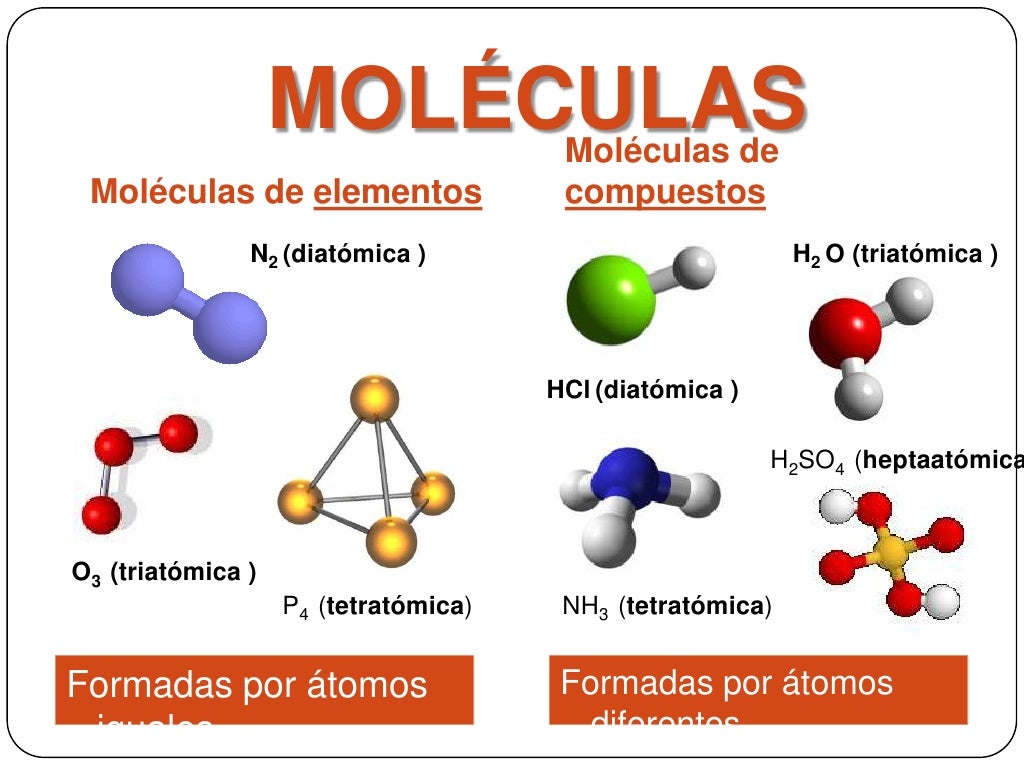 Удивительно, как проявления форм жизни образовались лишь на основе протонов, нейтронов и электронов. Элементарная основа позволяет каждому веществу и организму выполнять свою функцию. Так из семи нот пишется музыка разных направлений, разных стилей. Мы собрали 10 самых интересных фактов об атомах и молекулах.
Удивительно, как проявления форм жизни образовались лишь на основе протонов, нейтронов и электронов. Элементарная основа позволяет каждому веществу и организму выполнять свою функцию. Так из семи нот пишется музыка разных направлений, разных стилей. Мы собрали 10 самых интересных фактов об атомах и молекулах.
Самый легкий из атомов – атом водорода
В периодической таблице химических элементов водород стоит на первом месте. Его ядро состоит лишь из одного протона, вокруг которого вращается единственный электрон. Простейшее строение определяет минимальную массу, которую может иметь атом – 1,008 а.е.м. или 1,7х10-24 г.
На Земле водород существует в виде соединений с другими веществами или образует двухатомную молекулу Н2. Если считать в массовом отношении, на его долю приходится 1% земной коры. Если перевести массу в количество атомов, то содержание водорода окажется более внушительным – 17%. Этот показатель ставит элемент на второе место после кислорода (52%).
Во Вселенной водород составляет 88,6% от общей доли атомов, находящихся в космосе в виде звездного вещества и космической пыли.
Главной молекулой живой природы является молекула ДНК
В молекуле ДНК сосредоточена информация о строении каждой клетки живого организма, словно это проектное бюро города, где собраны подробные планы всех зданий. Внешне она напоминает перевитую веревочную лестницу, состоящую из двух нитей и соединенную водородными связями. ДНК вирусов может представлять одну цепочку.
Информация зашифрована в генах, то есть участках молекулы. Ген представляет собой определенную последовательность нуклеотидов, способных передать код для построения белков и РНК (информационных, транспортных, рибосомных, матричных).
Спираль ДНК человека, если ее вытянуть, протянется почти на 2 м. Это тем более удивительно, что она умещается в ядре размером меньше микрометра. Свернуться в компактную хромосому молекуле помогают нуклеосомы. На них ДНК наматывается, как на катушку.
Пыль – это частица, состоящая из квадриллиона атомов
Пылью называют твердые минеральные или органические частицы размером не более 0,05 мм. Природа образования может быть как естественной, так и связанной с деятельностью человека (антропогенной). В воздух поднимаются вулканический пепел, морская соль, сухая почва, продукты горения после пожаров, пыльца растений. Человек способствует загрязнению воздуха продуктами отопления и горных разработок, выхлопами автотранспорта, удобрениями. Вспашка земли и оголение почвы выкосами травы опасны выветриванием и переносом верхнего слоя грунта ветром.
Если сравнивать твердую взвесь с газообразными загрязнителями воздуха, то последние присутствуют в виде отдельных молекул. Пыль же в каждой частице содержит огромное число молекул и еще большее число атомов.
Атом может иметь электрический заряд
В составе атома электроны несут отрицательный заряд, протоны – положительный. Нейтроны не имеют заряда, то есть нейтральны. Когда количество протонов равно количеству электронов, заряд атома равен нулю. В случае, если электронов больше или меньше, чем протонов, у атома появляется заряд. Он становится ионом.
Когда количество протонов равно количеству электронов, заряд атома равен нулю. В случае, если электронов больше или меньше, чем протонов, у атома появляется заряд. Он становится ионом.
Ядро, состоящее из нейтронов и протонов, обладает ощутимой массой. Нужно определенное количество энергии, чтобы заставить его терять протоны. Электроны, которые вращаются вокруг него, значительно легче могут перемещаться от одного атома к другому. Добавление электронов приводит к образованию отрицательного заряда, потеря частиц – положительного. Атомы с положительным зарядом называют катионами, атомы с избытком электронов становятся анионами.
Самый тяжелый из атомов – атом урана
Из природных элементов атом урана имеет самую большую массу – 238,0289 а.е.м. В природе находится в основном в виде изотопа U-238. Атом с его 92 протонами чрезвычайно перегружен, при любой возможности выбрасывает протоны и нейтроны с огромной скоростью.
Открыл элемент германский химик Мартин Клапрот в 1789 году при анализе отработанной руды после добычи серебра.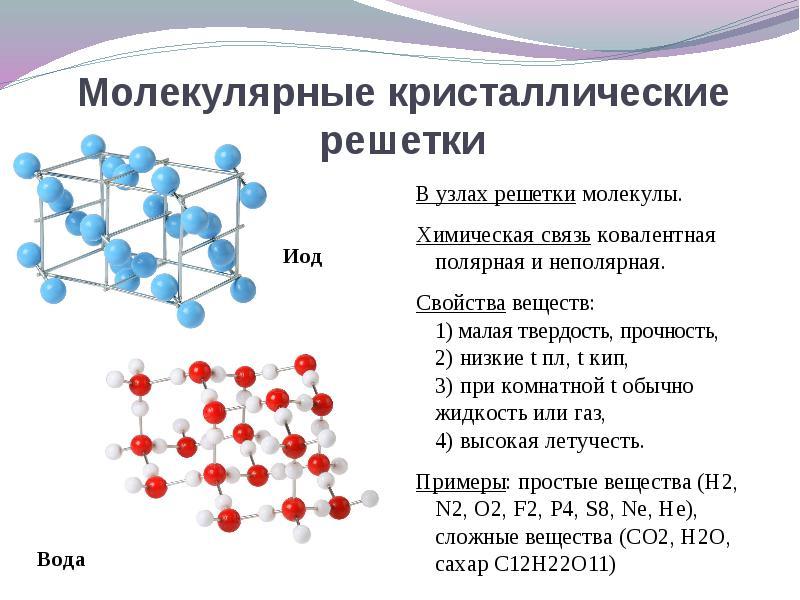 «Странное вещество», похожее на металл было диоксидом урана, но выяснилось это только через 50 лет. Клапрот назвал находку в честь далекой планеты, открытой к этому времени Гершелем.
«Странное вещество», похожее на металл было диоксидом урана, но выяснилось это только через 50 лет. Клапрот назвал находку в честь далекой планеты, открытой к этому времени Гершелем.
В конце 19 века во Франции Анри Беккерель обнаружил радиоактивность урана, то есть способность терять частицы. Распад может иметь 14 циклов. Уран превращается в радий, радон и другие элементы, образуя на последней стадии свинец.
Слово «атом» происходит из древнегреческого языка и означает «неделимый»
Еще в Древней Греции философ и математик Демокрит предположил, что окружающее состоит из мельчайших частичек. Отсюда произошел термин «атом» или «atomos». Однако подтверждение теория получила только в результате работы ученых в последние 150 лет и с помощью изобретенного микроскопа.
Первое исследование провел англичанин Джон Дальтон на рубеже 18-19 веков. Он установил, что химические элементы вступают в реакции в строго определенном соотношении (закон кратных отношений).
Сейчас мы знаем, что атом представляет собой наименьшую частицу химического элемента и не всегда является неделимым.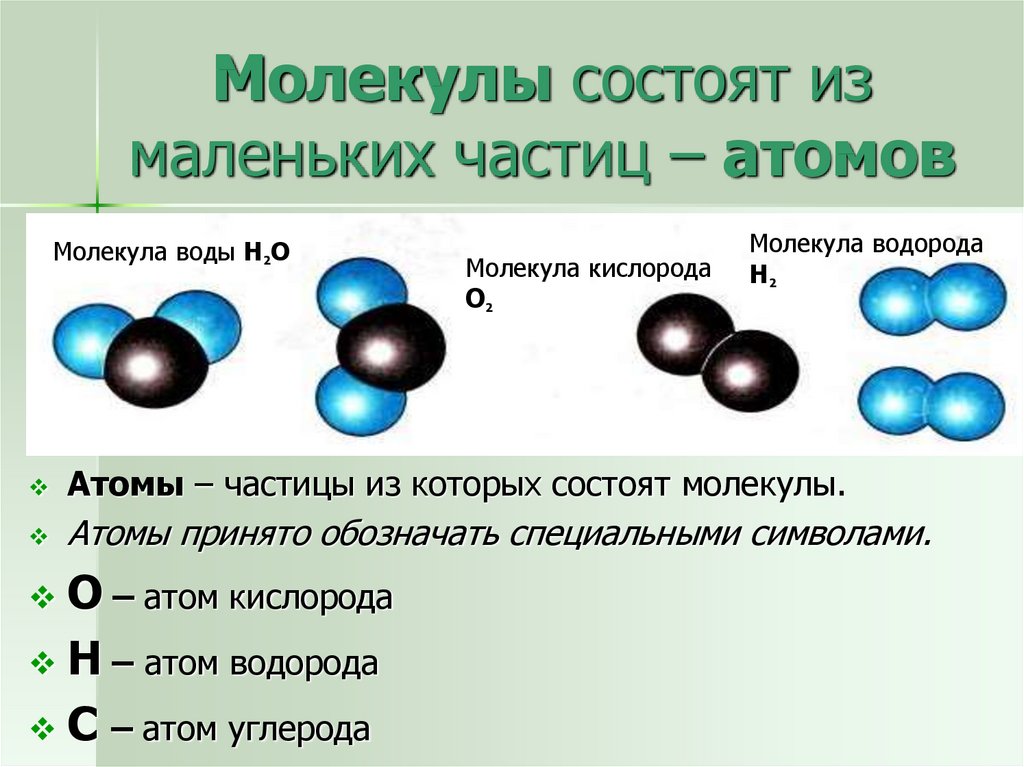 В состав атома входит ядро с протонами и нейтронами или просто нуклонами от латинского слова «nucleus» – ядро. Снаружи вокруг атома расположено электронное облако.
В состав атома входит ядро с протонами и нейтронами или просто нуклонами от латинского слова «nucleus» – ядро. Снаружи вокруг атома расположено электронное облако.
Стекло не является твердым телом
Твердость вещества – характеристика, основанная на прочности химических связей между атомами и молекулами. В жидкости частицы могут перемещаться относительно друг друга. В твердых телах они лишены такой возможности.
При производстве стекла молекулы кремния, обычно принимающие структуру кристаллической решетки, не успевают занят положенное им место. Стекло быстро остывает и частицы остаются перемешанными хаотично. Такое вещество называют аморфным, однако все же оно твердое.
Вязкость стекла сопоставима с вязкостью свинца, но ведь свинец никто не называет жидкостью. Бытует мнение, что со временем оконные стекла «стекают» вниз. В пример ставят витражи в средневековых храмах. Следует уточнить, что утолщения в их основании появились не с течением времени, а были изначально. Причина кроется в несовершенстве технологии производства.
Причина кроется в несовершенстве технологии производства.
Молекула меньше яблока во столько же раз, во сколько яблоко меньше Земли
Чтобы представить видимые и невидимые параметры окружающего мира, представим все молекулы одного кубического сантиметра воздуха в виде кирпичей. Их количества хватило бы для покрытия поверхности планеты на высоту 40-этажного дома.
Размеры молекул и атомов настолько малы, что в решении задач молекулярной физики используют относительные величины. Установить их удалось лишь с изобретением электронного микроскопа. Средний диаметр атома и простейшей молекулы составляет порядка 10-10 м. Так, размер молекулы белка – 43х10-10 м. Крупные молекулы достигают 10-7 м.
В ионный микроскоп можно разглядеть строение кристалла и даже определить межатомные расстояния.
Ученые смогли охладить молекулы монофторида стронция практически до абсолютного нуля
Выбор пал на монофторид стронция (SrF) неслучайно. Принцип охлаждения атомов основан на периодическом повторении поглощения и испускания фотонов под воздействием лазера. Таким образом атом теряет кинетическую энергию. Молекулы не настолько чувствительны. Мешает колебательная и вращательная энергия межатомных связей. У фторида стронция эти явления минимальны.
Таким образом атом теряет кинетическую энергию. Молекулы не настолько чувствительны. Мешает колебательная и вращательная энергия межатомных связей. У фторида стронция эти явления минимальны.
Группа ученых Йельского университета во главе с Д. Демиллем добилась охлаждения молекулы до 300 мкК (0,0003 К). За счет подобранной длины волны лазер погасил вращательные межатомные движения. В дальнейшем молекулы вели себя аналогично атому.
Практически такое достижение в перспективе можно использовать в квантовых компьютерах.
Скорость движения молекул воды может достигать 650 м/с
Молекулы воды находятся в постоянном тепловом движении. Они колеблются с большой частотой (одно колебание за 10-12 … 10-13 с) возле определенного положения, изредка прыгая на освободившееся соседнее место. Скорость движения при этом может приближаться к 600-650 м/с.
И все же молекулы не разлетаются, остаются жидкостью. Происходит это за счет водородных связей. В молекуле h3O пары электронов смещены в сторону кислорода. Водород, оставшийся практически без электрона, представляет собой положительно заряженное ядро. В результате протон водорода притягивает соседние атомы кислорода, образуя прочную межмолекулярную связь.
Водород, оставшийся практически без электрона, представляет собой положительно заряженное ядро. В результате протон водорода притягивает соседние атомы кислорода, образуя прочную межмолекулярную связь.
Благодаря такому сцеплению вода в условиях Земли принимает в основном жидкое состояние, а не кипит как аналогичные гидриды (серы, селена) при –80°С. Водородные связи определяют физические и химические свойства воды, на которых основана жизнь на нашей планете.
©
Tags: Познавательно, Топ-10, Факты
фактов о молекулах | Интересные факты о детях
Пожалуйста, напишите или поделитесь этой статьей!
- Электронная почта
- ФБ
Атомы обычно не встречаются по отдельности. В основном они встречаются вместе, образуя различные виды веществ. Всякий раз, когда два атома соединяются вместе, они образуют молекулу.
Все вокруг вас состоит из разных видов молекул.
Это также включает в себя ваше тело и тела всех, кого вы когда-либо встречали!
Связанный: Попробуйте наш молекулярный тест здесь!
Знаете ли вы, что все мы состоим из триллионов и триллионов различных видов молекул?
Соединения
Если атомы разных элементов соединяются вместе, они образуют молекулу особого типа, называемую соединением.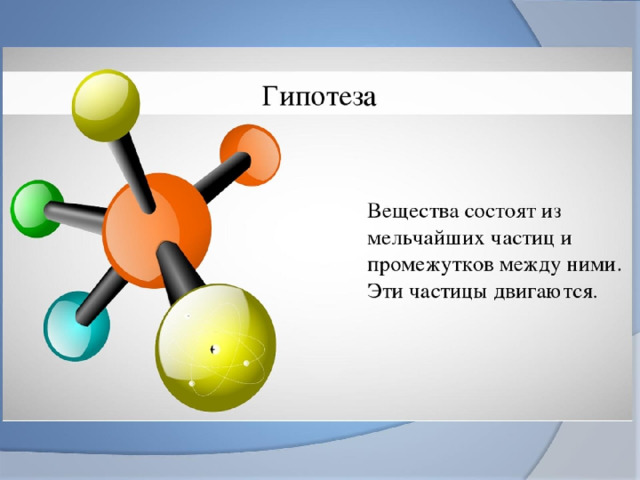
Одно из самых распространенных соединений в мире также является одним из самых простых: вода.
Вода состоит из сложных молекул, представляющих собой комбинацию двух атомов водорода и одного атома кислорода.
Вот почему воду иногда называют H 2 O.
Сколько бы ни было воды, каждая молекула всегда будет состоять из двух атомов водорода и одного атома кислорода.
Молекулярная формула
Всякий раз, когда вы готовите торт или печенье, вы должны использовать правильные ингредиенты или формулу. То же самое происходит, когда создаются разные вещества.
В мире всего около 100 различных видов атомов, но существуют миллионы различных веществ.
Это потому, что у каждого из них есть уникальная формула (рецепт), которая используется для их создания. В зависимости от создаваемого вещества будет различное соотношение элементов, которые объединяются для создания вещества.
В зависимости от того, что исследуется, некоторые из различных формул могут быть либо простыми, например, вода (H 2 O), либо очень сложными, например, кофеин (C8h20N4O2).
Единственный способ создать какое-либо конкретное вещество — это иметь правильные виды атомов в правильном количестве.
Связи
Молекулы внутри соединений удерживаются вместе за счет вещей, называемых химическими связями.
Есть два разных типа связей, которые удерживают молекулы вместе. Эти два разных типа связей известны как ковалентная и ионная связи.
Соединения могут иметь в своем составе один или оба типа связей.
Эти связи образуются, когда электроны сливаются вместе. По сути, электроны вращаются вокруг атомов в чем-то вроде оболочки, и эти оболочки «любят» быть заполненными электронами.
Если оболочки не заполнены, то они соединятся с другим атомом, чтобы получить правильное количество электронов.
Ковалентные связи – Ковалентные связи образуются, когда электроны распределяются между атомами.
Ионные связи – Ионные связи образуются, когда электрон покидает один атом, чтобы присоединиться к другому.
Это делается для того, чтобы каждый атом имел правильное количество электронов, чтобы каждый имел «полную» оболочку.
Молекулярная викторина
А теперь попробуй нашу викторину о молекулах, чтобы проверить, что ты знаешь!
удивительных фактов о молекулах: достаточно ли сильна ваша химия?
Молекулы — это мельчайшие частицы химического соединения, которые могут сохранять химические свойства этого соединения.
Соединения образуются, когда атомы соединяются друг с другом. Молекулы можно увидеть в специализированный микроскоп, но они слишком малы, чтобы увидеть их невооруженным глазом.
Таблица Менделеева, без сомнения, трудно освоить. Самая маленькая молекула — это молекулярный водород (h3), который состоит из двух атомов водорода. Молекула элемента — это просто молекула, состоящая из атомов этого элемента. Например, молекула кислорода (O2) состоит из двух атомов кислорода. Кислород — это молекула, которой мы дышим, чтобы поддерживать жизнь. Атомы кислорода также являются молекулой, из которой состоит большая часть атмосферы Земли. Углекислый газ (CO2) — еще одна важная молекула. Атомы углерода являются парниковым газом, который помогает поддерживать температуру Земли теплой. Углекислый газ образуется при сжигании ископаемого топлива. Молекулы соединений важны для химии, потому что они являются наименьшими единицами, которые могут вступать в химические реакции. Вот почему молекулы находятся в центре внимания многих исследований в области открытия лекарств и науки об окружающей среде. Внешняя оболочка кислорода может содержать около восьми электронов.
Атомы кислорода также являются молекулой, из которой состоит большая часть атмосферы Земли. Углекислый газ (CO2) — еще одна важная молекула. Атомы углерода являются парниковым газом, который помогает поддерживать температуру Земли теплой. Углекислый газ образуется при сжигании ископаемого топлива. Молекулы соединений важны для химии, потому что они являются наименьшими единицами, которые могут вступать в химические реакции. Вот почему молекулы находятся в центре внимания многих исследований в области открытия лекарств и науки об окружающей среде. Внешняя оболочка кислорода может содержать около восьми электронов.
Знаменитый Амадео Авогадро впервые постулировал идею молекул в 1811 году.
Жан Перрен доказал, что молекулы существуют, и был удостоен Нобелевской премии по физике за свою ценную работу. Многие философы и физики решительно выступали против концепции молекул. Одним из них был Эрнст Мах, который утверждал это в соответствии с логическим позитивизмом.
Существует два основных типа молекулярных связей: ионные и ковалентные. Ионные связи образуются, когда атом отдает или принимает электроны для образования ионов.
Ковалентные связи образуются, когда два атома имеют общие электроны. Эти два типа связей по-разному влияют на химические свойства молекулы. Между атомами могут образовываться различные типы связей, которые определяют химические свойства молекулы. Наиболее распространенным типом связи является ковалентная связь, которая образуется, когда два атома имеют общие электроны.
Другим распространенным типом связи является ионная связь. Ионная связь образуется, когда атом отдает или принимает электроны для образования ионов. Молекулы также могут образовываться посредством металлических связей, водородных связей и многих других. Каждый тип связи по-разному влияет на химические свойства молекулы.
Молекула Против. Атом Атомы — это мельчайшие частицы элемента, которые могут сохранять химические свойства этого элемента.
Молекулы состоят из двух или более атомов и обладают отличными от атомов химическими свойствами. Молекулы важны для химии, потому что они являются наименьшими единицами, которые могут вступать в химические реакции. Вот почему молекулы находятся в центре внимания многих исследований в области открытия лекарств и науки об окружающей среде. Например, когда молекула воды расщепляется до низшего уровня, мы получаем два атома водорода и один атом кислорода.
Различные молекулярные структурыМолекулярная структура — это расположение атомов в молекуле. Молекулы могут иметь разную структуру в зависимости от того, как атомы связаны друг с другом.
Некоторые распространенные молекулярные структуры включают линейную структуру, разветвленную структуру, циклическую структуру и треугольную структуру. Каждый тип молекулярной структуры по-разному влияет на химические свойства молекулы. Модели молекулярной структуры делятся на три категории: заполняющие пространство, шарико-стержневые и скелетные. Даже чистое вещество имеет молекулярную структуру. Молекула воды состоит из двух атомов водорода и атома кислорода. Хлорид натрия состоит из натрия и хлорида.
Даже чистое вещество имеет молекулярную структуру. Молекула воды состоит из двух атомов водорода и атома кислорода. Хлорид натрия состоит из натрия и хлорида.
Является ли кислород молекулой?
Да, кислород — это молекула. Он состоит из двух атомов, то есть двух атомов кислорода. Эти атомы связаны между собой ковалентными связями. Кислород — бесцветный газ без запаха, необходимый для жизни человека.
Как еще называют молекулы?Синонимами молекул являются атомы, пылинки, частицы и пылинки; однако они не обязательно означают именно молекулы.
Как образуются молекулы?
Молекулы образуются при соединении атомов. Это может произойти за счет совместного использования электронов (ковалентная связь), через ионы (ионная связь) или за счет атомов металла посередине (металлическая связь). Каждый тип связи по-разному влияет на химические свойства молекулы.
Вы видите молекулу?
Молекулу можно увидеть только с помощью специального микроскопа. Его нельзя увидеть невооруженным глазом.
Какая самая маленькая молекула?
Водород – самая маленькая молекула.
Что такое молекула элемента?
Молекула элемента – это наименьшая частица этого элемента, которая сохраняет свои химические свойства. Например, хлорид натрия (NaCl) не является молекулой, поскольку состоит из двух элементов: натрия (Na) и хлора (Cl).
Заявление об отказе от ответственности
В Kidadl мы гордимся тем, что предлагаем семьям оригинальные идеи, чтобы максимально использовать время, проведенное вместе дома или на улице, где бы вы ни находились. Мы стремимся рекомендовать самые лучшие вещи, предложенные нашим сообществом, и то, что мы сделали бы сами – наша цель – быть надежным другом для родителей.
Мы стараемся изо всех сил, но не можем гарантировать совершенство. Мы всегда будем стремиться предоставить вам точную информацию на дату публикации, однако информация может меняться, поэтому важно, чтобы вы провели собственное исследование, перепроверили и приняли решение, подходящее для вашей семьи.
Мы всегда будем стремиться предоставить вам точную информацию на дату публикации, однако информация может меняться, поэтому важно, чтобы вы провели собственное исследование, перепроверили и приняли решение, подходящее для вашей семьи.
Kidadl вдохновляет детей развлекать и обучать их. Мы понимаем, что не все виды деятельности и идеи подходят и подходят для всех детей и семей или во всех обстоятельствах. Наши рекомендуемые занятия основаны на возрасте, но это ориентир. Мы рекомендуем использовать эти идеи в качестве вдохновения, чтобы идеи воплощались в жизнь под надлежащим наблюдением взрослых, и чтобы каждый взрослый использовал свое собственное усмотрение и знания своих детей для рассмотрения безопасности и пригодности.
Kidadl не может нести ответственность за реализацию этих идей, поэтому рекомендуется постоянно находиться под присмотром родителей, так как безопасность превыше всего. Любой, кто использует информацию, предоставленную Kidadl, делает это на свой страх и риск, и мы не несем ответственности, если что-то пойдет не так.
