Молярная масса некоторых газов значения (Таблица)
Молярная масса газа (или вещества) — это отношение массы газа к количеству молей этого газа, то есть масса одного моля газа (вещества).
В системе СИ молярная масса выражается в кг/моль (или г/моль), обозначают обычно буквой M.
|
Название газа и его химическая формула |
Молярная масса, г/моль |
|
Азот (N2) |
28,016 |
|
Аммиак (NH3) |
17,031 |
|
Аргон (Ar) |
39,944 |
|
Ацетилен (C2H2) |
26,04 |
|
Ацетон (C3H |
58,08 |
|
Н-бутан (C4h20) |
58,12 |
|
Изо-бутан ( C4HJ0) |
58,12 |
|
Н-бутиловый спирт ( C4HJ0O) |
74,12 |
|
Вода (H2O) |
18,016 |
|
Водород (h3) |
2,0156 |
|
Воздух (сухой) |
28,96 |
|
Н-гексан (C |
86,17 |
|
Гелий (He) |
4,003 |
|
Н-гептан (C7HJ6) |
100,19 |
|
Двуокись углерода (CO2) |
44,01 |
|
Н-декан ( C10h32) |
142,30 |
|
Дифенил ( C12h20) |
154,08 |
|
Дифениловый эфир ( CJ2H10O) |
168,8 |
|
Дихлорметан ( CH2Cl2) |
84,94 |
|
Диэтиловый эфир (C4H10O) |
74,12 |
|
Закись азота (N2O) |
44,016 |
|
Йодистый водород (HJ) |
127,93 |
|
Кислород (O2) |
32,00 |
|
Криптон (Kr) |
83,7 |
|
Ксенон (Xe) |
131,3 |
|
Метан (CH4) |
16,04 |
|
Метиламин (CH5N) |
31,06 |
|
Метиловый спирт (CH4O) |
32,04 |
|
Неон (Ne) |
20,183 |
|
Нитрозилхлорид (NOCl) |
65,465 |
|
Озон (O3) |
48,00 |
|
Окись азота (NO) |
30,008 |
|
Окись углерода (CO) |
28,01 |
|
Н-октан ( C8H18) |
114,22 |
|
Н-пентан ( C5H12) |
72,14 |
|
Изо-пентан ( C5H12) |
72,14 |
|
Пропан ( C3H8) |
44,09 |
|
Пропилен ( C |
42,08 |
|
Селеновая кислота (H2Se) |
80,968 |
|
Сернистый газ (SO2) |
64,06 |
|
Сернистый ангидрид (SO3) |
80,06 |
|
Сероводород (H2S) |
34,08 |
|
Фосфористый водород (PH3) |
34,04 |
|
Фреон 11 (CF3CI) |
137,40 |
|
Фреон-12 (CF2CI2) |
120,92 |
|
Фреон-13 (CFCI3) |
114,47 |
|
Фтор (F2) |
38,00 |
|
Фтористый кремний (SiF4) |
104,06 |
|
Фтористый метил (CH3F) |
34,03 |
|
Хлор (Cl2) |
70,914 |
|
Хлористый водород (HCl) |
36,465 |
|
Хлористый метил (CH3Cl) |
50,49 |
|
Хлороформ (CHCl3) |
119,39 |
|
Циан (C2N2) |
52,04 |
|
Цианистая кислота (HCN) |
27,026 |
|
Этан (C2H6) |
30,07 |
|
Этиламин (C2H7N) |
45,08 |
|
Этилен (C2h5) |
28,05 |
|
Этиловый спирт (C2H6O) |
46,07 |
|
Хлористый этил (C2H5Cl) |
64,52 |
Раздел недели: Обезжиривающие водные растворы и органические растворители. Составы для очистки и обезжиривания поверхности. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Поиск на сайте DPVA Поставщики оборудования Полезные ссылки О проекте Обратная связь Ответы на вопросы. Оглавление Таблицы DPVA.ru – Инженерный Справочник | Адрес этой страницы (вложенность) в справочнике dpva.ru: главная страница / / Техническая информация/ / Физический справочник / / Газы. Свойства газов / / Таблица. Молярная масса газов (г/моль = кг/кмоль) от азота до хлористого этила.
Поделиться:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Если Вы не обнаружили себя в списке поставщиков, заметили ошибку, или у Вас есть дополнительные численные данные для коллег по теме, сообщите , пожалуйста. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Коды баннеров проекта DPVA.ru Консультации и техническая | Проект является некоммерческим. Информация, представленная на сайте, не является официальной и предоставлена только в целях ознакомления. Владельцы сайта www.dpva.ru не несут никакой ответственности за риски, связанные с использованием информации, полученной с этого интернет-ресурса. Free xml sitemap generator Free xml sitemap generator | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
6.3: Закон Дальтона — Химия LibreTexts
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 3560
- Стивен Лоуэр
- Университет Саймона Фрейзера
Цели обучения
Убедитесь, что вы полностью поняли следующие основные идеи, представленные ниже.
- Один моль газа занимает объем 22,4 л при STP (стандартная температура и давление, 273K, 1 атм = 103 кПа.)
- Приведенный выше факт позволяет нам связать измеримое свойство плотности газа с его молярной массой .

- Состав смеси газов обычно выражается в виде мольных долей ; убедитесь, что вы знаете, как их вычислить.
- Закон Дальтона о парциальных давлениях гласит, что каждый газ в смеси действует независимо, поэтому общее давление газа на стенки сосуда равно сумме парциальных давлений отдельных компонентов.
Хотя все газы точно следуют закону идеального газа PV = nRT при соответствующих условиях, каждый газ также является уникальным химическим веществом, состоящим из молекулярных единиц, имеющих определенные массы. В этом уроке мы увидим, как эти молекулярные массы влияют на свойства газов, соответствующих закону идеального газа. После этого мы рассмотрим газы, содержащие более одного типа молекул, другими словами, смеси газов. Мы начнем с обзора молярного объема и E.V.E.N. принцип, лежащий в основе нашего понимания газовых смесей.
Молярный объем газа
Вы помните, что молярная масса чистого вещества равна массе 6,02 x 10 23 ( число Авогадро ) частиц или молекулярных единиц этого вещества.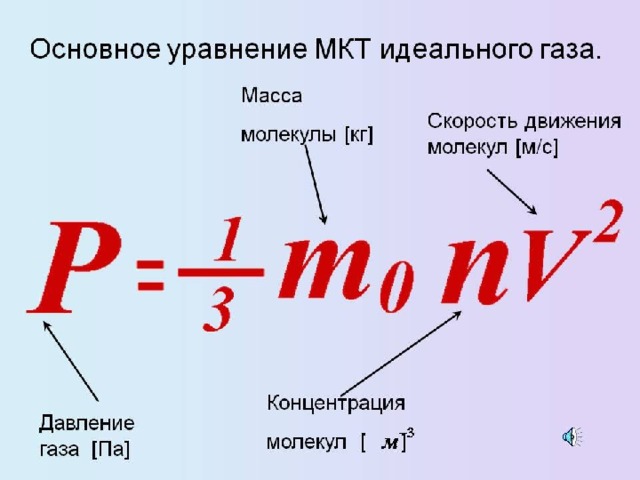 Молярные массы обычно выражаются в граммах на моль (г-моль –1 ) и часто обозначаются как молекулярная масса с. Как было объяснено в предыдущем уроке, равные объемы газов, измеренные при одинаковых температуре и давлении, содержат одинаковое количество молекул (это «четный» принцип , более формально известный как закон Авогадро .) Стандартная температура и давление: 273 К, 1 атм
Молярные массы обычно выражаются в граммах на моль (г-моль –1 ) и часто обозначаются как молекулярная масса с. Как было объяснено в предыдущем уроке, равные объемы газов, измеренные при одинаковых температуре и давлении, содержат одинаковое количество молекул (это «четный» принцип , более формально известный как закон Авогадро .) Стандартная температура и давление: 273 К, 1 атм
Величина этого объема будет, конечно, зависеть от температуры и давления, поэтому для удобства сравнения принято определять набор условий Т = 273 К и Р = 1 атм как стандартная температура и давление , обычно обозначается как STP . Подставляя эти значения в уравнение состояния идеального газа и решая V , мы получаем объем 22,414 литра на 1 моль.
Пример \(\PageIndex{1}\)
Какой будет объем одного моля воздуха при 20°C на вершине Мауна-Кеа, Гавайи (высота 4,2 км), где атмосферное давление составляет примерно 60 кПа ?
Шлаки и шлаковые конусы на вершине Мауна-Кеа зимой. (Общественное достояние; Геологическая служба США)
(Общественное достояние; Геологическая служба США)
Решение
Применить законы Бойля и Шарля в качестве последовательных поправочных коэффициентов к стандартному давлению на уровне моря 101,3 кПа:
помните, что он действителен только при STP. Молярный объем при других температурах и давлениях легко найти простой пропорцией. Молярный объем вещества может кое-что сказать нам о том, сколько места занимает каждая молекула, как показывает следующий пример. 9{–7}\, см = 3,4\, нм \нечисло\]
В условиях, при которых применима модель идеального газа (то есть почти всегда, если вы не инженер-химик, имеющий дело с высокими давлениями), «молекула молекула», поэтому объем числа молекул Авогадро не будет зависеть от состава газа. Причина, конечно, в том, что объем газа в основном состоит из пустого пространства; объемы самих молекул пренебрежимо малы.
Молярная масса и плотность газа
Молекулярная масса (молярная масса) любого газа – это выраженная в граммах масса числа Авогадро его молекул. Это верно независимо от того, состоит ли газ из одного вида молекул или представляет собой смесь. Для смеси газов молярная масса будет зависеть от молярных масс ее компонентов и от фракционного содержания каждого вида молекул в смеси. Термин «средняя молекулярная масса» часто используется для описания молекулярной массы газовой смеси.
Это верно независимо от того, состоит ли газ из одного вида молекул или представляет собой смесь. Для смеси газов молярная масса будет зависеть от молярных масс ее компонентов и от фракционного содержания каждого вида молекул в смеси. Термин «средняя молекулярная масса» часто используется для описания молекулярной массы газовой смеси.
Средняя молярная масса (\(\bar{m}\)) смеси газов равна сумме молярных долей каждого газа, умноженной на молярную массу этого вещества:
\[\bar{m}=\sum_i \chi_im_i\]
Пример \(\PageIndex{3}\)
Найдите среднюю молярную массу сухого воздуха, объемный состав которого равен O 2 (21% ), N 2 (78%) и Ar (1%).
Раствор
Средняя молекулярная масса представляет собой взвешенную по молярным долям сумму молекулярных масс ее компонентов. Мольные доли, конечно, такие же, как и объемные доли (принцип E.V.E.N.)
\[m = (0,21 х 32) + (0,78 х 28) + (0,01 х 20) = 28 \номер \]
Молярные объемы всех газов одинаковы при измерении при одинаковых температуре и давлении.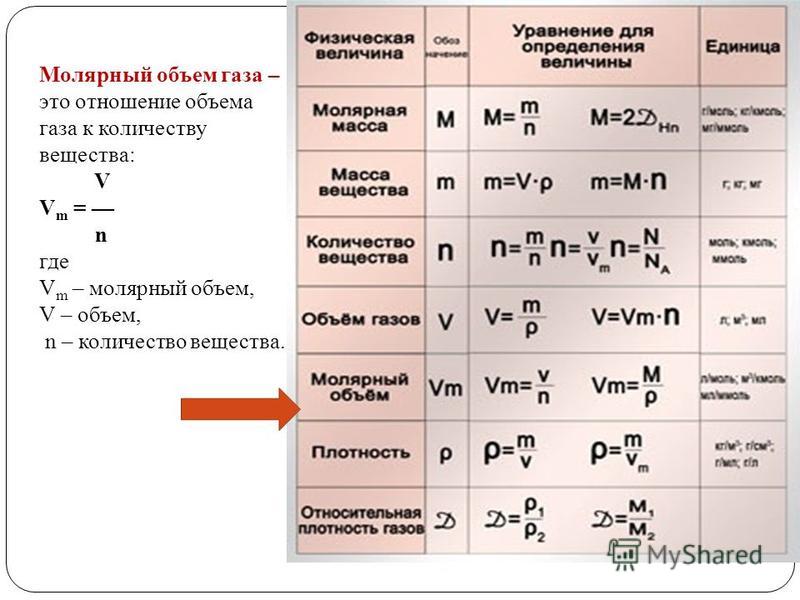 Однако молярные масс различных газов будут различаться. Это означает, что разные газы будут иметь разную плотность (разную массу на единицу объема). Зная молекулярную массу газа, мы можем вычислить его плотность.
Однако молярные масс различных газов будут различаться. Это означает, что разные газы будут иметь разную плотность (разную массу на единицу объема). Зная молекулярную массу газа, мы можем вычислить его плотность.
Пример \(\PageIndex{4}\)
Гексафторид урана UF 6 Газ используется при изотопном обогащении природного урана. Рассчитайте его плотность при СТП. 9{–1} \nonumber\]
Примечание: нет необходимости искать «формулу» для этого вычисления; просто объедините молярную массу и молярный объем таким образом, чтобы получить правильные единицы измерения.
Что еще более важно, если мы можем измерить плотность неизвестного газа, у нас есть удобный способ оценить его молекулярную массу. Это один из многих важных примеров того, как макроскопическое измерение (выполненное на сыпучем веществе) может дать микроскопическую информацию (то есть об объектах молекулярного масштаба) 9.0034
Плотность газа в настоящее время измеряется в промышленности с помощью электромеханических устройств, таких как вибрационные берды, которые могут обеспечивать непрерывную запись в реальном времени в определенных местах, например, внутри трубопроводов. Определение молекулярной массы газа по его плотности известно как метод Дюма , по имени французского химика Жана Дюма (1800-1840), который разработал его. Можно просто измерить вес известного объема газа и преобразовать этот объем в его STP-эквивалент, используя законы Бойля и Чарльза. Вес газа, деленный на его объем STP, дает плотность газа, а плотность умножается на 22,4 моль –1 дает молекулярную массу. Обратите особое внимание на примеры расчета плотности газа, показанные здесь и в вашем учебнике. Ожидается, что вы будете выполнять вычисления такого рода, конвертируя молекулярную массу в плотность газа.
Определение молекулярной массы газа по его плотности известно как метод Дюма , по имени французского химика Жана Дюма (1800-1840), который разработал его. Можно просто измерить вес известного объема газа и преобразовать этот объем в его STP-эквивалент, используя законы Бойля и Чарльза. Вес газа, деленный на его объем STP, дает плотность газа, а плотность умножается на 22,4 моль –1 дает молекулярную массу. Обратите особое внимание на примеры расчета плотности газа, показанные здесь и в вашем учебнике. Ожидается, что вы будете выполнять вычисления такого рода, конвертируя молекулярную массу в плотность газа.
Пример \(\PageIndex{5}\)
Рассчитайте приблизительную молярную массу газа, измеренная плотность которого составляет 3,33 г/л при 30°C и 780 торр.
Решение
Найдите объем, который будет занимать 1 л газа при СТП; обратите внимание, что коррекция до 273 К уменьшит объем, а коррекция до 1 атм (760 торр) увеличит его: 9{–1} \nonumber\]
Плотность газовой смеси
Измерение плотности газа может быть полезным средством оценки состава смеси двух разных газов; это широко используется в операциях промышленной химии, в которых необходимо постоянно контролировать состав газовых потоков.
Пример \(\PageIndex{6}\): Углекислый газ и метан
Найдите состав смеси \(\ce{CO2}\) (44 г/моль) и метана \(\ce{Ch5} \) (16 г/моль), плотность которого составляет 1,214 г/л.
Раствор
Плотность смеси этих двух газов будет прямо пропорциональна ее составу, варьируясь от чистого метана до чистого CO 2 . Начнем с нахождения этих двух плотностей:
Для CO 2 :
(44 г/моль) ÷ (22,4 л/моль) = 1,964 г/л
Для CH 4 :
(16 г/моль) моль) ÷ (22,4 л/моль) = 0,714 г/л
.) представляет собой мольную долю CH 4 , мы можем написать
1,964 x + 0,714 (1–x) = 1,214
(имеет ли это смысл? Обратите внимание, что если x = 0, плотность будет равна плотности чистого CH 4 , а если бы оно было равно 1, то это был бы чистый CO 2 .)
Расширение приведенного выше уравнения и решение относительно x дает мольные доли 0,40 для CO 2 и 0,60 для CH 4 .
Выражение состава газовой смеси
Поскольку большая часть объема, занимаемого газом, состоит из пустого пространства, ничто не препятствует тому, чтобы два или более видов газов занимали один и тот же объем. Гомогенные смеси такого типа обычно известны как растворы , но их принято называть просто газообразными смесями . Мы можем указать состав газовых смесей разными способами, но наиболее распространенными являются объемов и мольных долей .
Объемные доли
Из закона Авогадро мы знаем, что «равные объемы содержат одинаковое количество молекул». Это означает, что объемы газов, в отличие от объемов твердых тел и жидкостей, аддитивны. Итак, если в разделенном сосуде имеется два объема газа А в одном сечении и один моль газа В в другом (оба при одинаковых температуре и давлении), и мы удаляем перегородку, объем остается неизменным.
Мы можем указать состав этой смеси, сказав, что объемная доля А составляет 1/3, а доля В составляет 2/3.
Объемные доли часто называют частичными объемами:
\[V_i = \dfrac{v_i}{\sum v_i}\]
Пусть вас не смущает этот тип записи! Знак суммирования Σ (греч. сигма) просто означает сложение против (объемов) каждого газа. Таким образом, если газ А является « i -м» веществом, как в приведенном выше выражении, суммирование идет от 9от 0058 i =1 до i =2. Обратите внимание, что мы можем использовать частичные объемы для определения состава смеси, даже если она никогда не была получена путем объединения чистых газов.
Когда мы говорим, что воздух, например, состоит из 21 процента кислорода и 78 процентов азота по объему, это то же самое, что сказать, что такое же процентное соотношение молекул в воздухе состоит из O 2 и N 2 . Аналогично, в 1,0 моль воздуха содержится 0,21 моль O 2 и 0,78 моль N 2 (другие 0,1 моля состоят из различных газовых примесей, но в основном это неон). Обратите внимание, что вы никогда не сможете предположить подобную эквивалентность смесям жидкостей или твердых тел, к которым E. V.E.N. принцип не применяется.
V.E.N. принцип не применяется.
Мольные доли
Последние два числа (0,21 и 0,78) также выражают мольные доли кислорода и азота в воздухе. Мольная доля означает именно то, что написано: доля молекул, состоящих из определенного вещества. Это выражается алгебраически как
\[X_i = \dfrac{n_i}{\sum_i n_i}\]
поэтому в случае кислорода в воздухе его молярная доля равна
\[ X_{O_2} = \dfrac{n_{O_2} }{n_{O_2}+n_{N_2}+n_{Ar}}= \dfrac{0,21}{1}=0,21 \nonumber\]
Пример \(\PageIndex{7}\)
Смесь \ (O_2\) и закись азота \(N_2O\) иногда используются в качестве мягкого анестетика в стоматологической хирургии. Некоторая смесь этих газов имеет плотность 1,482 г л –1 при 25 и 0,980 атм. Каков был молярный процент \(N_2O\) в этой смеси? 9{-1}\номер \]
Молярная масса смеси (1,65 г л –1 )(22,4 л моль –1 ) = 37,0 г моль –1 . Молекулярные массы \(O_2\) и \(N_2\) равны 32 и 44 соответственно. 37,0 составляет 5/12 разницы между молярными массами двух чистых газов. Поскольку плотность газовой смеси прямо пропорциональна ее средней молярной массе, мольная доля более тяжелого газа в смеси также равна 5/12:
37,0 составляет 5/12 разницы между молярными массами двух чистых газов. Поскольку плотность газовой смеси прямо пропорциональна ее средней молярной массе, мольная доля более тяжелого газа в смеси также равна 5/12:
\[\dfrac{37-32}{44-32}=\ dfrac{5}{12}=0,42 \номер\]
Пример \(\PageIndex{8}\)
Какова молярная доля углекислого газа в смеси, состоящей из равных масс CO 2 (ММ=44) и неона (ММ=20,2)?
Решение
Примите любую произвольную массу, например 100 г, найдите эквивалентное количество молей каждого газа, а затем подставьте в определение мольной доли:
- n CO2 = (100 г) ÷ (44 г моль –1 ) = 2,3 моль
- п Не = (100 г) ÷ (20,2 г моль –1 ) = 4,9 моль
- X Ne = (2,3 моль) ÷ (2,3 моль + 4,9 моль) = 0,32
Закон Дальтона о парциальных давлениях
Уравнение состояния идеального газа применимо к смесям так же, как и к чистым газам. Именно с газовой смесью, обычным воздухом, Бойль, Гей-Люссак и Шарль проводили свои ранние эксперименты. Единственная новая концепция, которая нам нужна для работы с газовыми смесями, — это парциальное давление , понятие, изобретенное известным английским химиком Джоном Дальтоном (1766-1844). Дальтон рассудил, что низкая плотность и высокая сжимаемость газов указывают на то, что они состоят в основном из пустого пространства; отсюда следует, что когда два или более различных газа занимают один и тот же объем, они ведут себя совершенно независимо.
Именно с газовой смесью, обычным воздухом, Бойль, Гей-Люссак и Шарль проводили свои ранние эксперименты. Единственная новая концепция, которая нам нужна для работы с газовыми смесями, — это парциальное давление , понятие, изобретенное известным английским химиком Джоном Дальтоном (1766-1844). Дальтон рассудил, что низкая плотность и высокая сжимаемость газов указывают на то, что они состоят в основном из пустого пространства; отсюда следует, что когда два или более различных газа занимают один и тот же объем, они ведут себя совершенно независимо.
Вклад каждого компонента газовой смеси в общее давление газа известен как парциальное давление этого газа. Сам Дальтон сформулировал этот закон простым и ярким способом, показанным слева.
Обычный способ формулировки Закон Дальтона о парциальных давлениях равен
Полное давление газа представляет собой сумму парциальных давлений его компонентов
, что алгебраически выражается как
\[P_{total} =P_1+P_2+P_3 . .. = \sum_i P_i\]
.. = \sum_i P_i\]
или, что то же самое,
\[ P_{total} = \dfrac{RT}{V} \sum_i n_i\]
Также существует аналогичная связь на основе объемных долей , известных как закон частичных объемов Амагата . Он в точности аналогичен закону Дальтона в том смысле, что он гласит, что общий объем смеси — это просто сумма частичных объемов ее компонентов. Но есть два важных отличия: закон Амагата справедлив только для идеальных газов, которые должны иметь одинаковые температуру и давление. Закон Дальтона не имеет ни одного из этих ограничений. Хотя закон Амагата кажется интуитивно очевидным, иногда он оказывается полезным в приложениях химической технологии. Мы не будем использовать его в этом курсе.
Пример \(\PageIndex{9}\)
Рассчитайте массу каждого компонента, присутствующего в смеси фтора (MW и ксенона (MW 131,3) в колбе объемом 2,0 л. Парциальное давление Xe составляет 350 торр. а полное давление равно 724 торр при 25°C. chi_{Xe} = \dfrac{350}{724} = 0,48 \nonnumber\]
и
9{–1}) \times (0,48 \times 0,078\, моль) = 4,9\, г \номер\]Пример \(\PageIndex{10}\)
Три колбы разного объема, содержащие разные газы при различных давления соединены запорными кранами, как показано. Когда откроются запорные краны,
Когда откроются запорные краны,
- Какое будет давление в системе?
- Какого газа будет больше всего в смеси?
Предположим, что температура однородна, а объем соединительных трубок незначителен.
Решение
Хитрость здесь заключается в том, чтобы отметить, что общее число молей n T и температура остаются неизменными, поэтому мы можем использовать закон Бойля PV = константа. Мы проработаем детали только для CO 2 , обозначенного нижними индексами a.
Для CO 2 ,
P a V a = (2,13 атм)(1,50 л) = 3,19 л-атм.
Добавление PV продукции на каждую отдельную емкость, получаем
\[\sum P_iV_i = 6,36 л-атм = n_T рт. \nonumber\]
Мы назовем эту сумму P 1 V 1 . После открытия запорных кранов и смешивания газов новые условия обозначаются P 2 V 2 .
Из закона Бойля,
= 6,36 л-атм . В 2 = Σ В i = 4,50 л.
Решение для конечного давления P 2 получаем
(6,36 л-атм)/(4,50 л) = 1,41 атм .
Для CO 2 получается (3,19/ RT )/(6,36/ RT ) = 0,501. Поскольку это значение превышает 0,5, мы знаем, что это самый распространенный газ в конечной смеси.
Применение закона Дальтона: сбор газов над водой
Обычный лабораторный метод сбора газообразного продукта химической реакции состоит в том, чтобы поместить его в перевернутую трубку или бутыль, наполненную водой, отверстие которой погружено в емкость большего размера. воды. Эта схема называется пневматический желоб , который широко использовался на заре химии. Попадая в бутылку, газ вытесняет воду и задерживается в верхней части.
Объем газа можно измерить с помощью калиброванной шкалы на бутылке, а как насчет его давления? Полное давление, удерживающее газ, равно атмосферному, передающему свою силу через воду. (Точный расчет также должен учитывать высоту водяного столба в перевернутой трубке.) Но сама жидкая вода всегда находится в равновесии со своим паром, поэтому пространство в верхней части трубки представляет собой смесь двух газов. : собираемый газ и газообразный H 2 O. Парциальное давление H 2 O известно как давление паров воды и зависит от температуры. Чтобы определить количество собранного газа, мы должны использовать закон Дальтона, чтобы найти парциальное давление этого газа.
(Точный расчет также должен учитывать высоту водяного столба в перевернутой трубке.) Но сама жидкая вода всегда находится в равновесии со своим паром, поэтому пространство в верхней части трубки представляет собой смесь двух газов. : собираемый газ и газообразный H 2 O. Парциальное давление H 2 O известно как давление паров воды и зависит от температуры. Чтобы определить количество собранного газа, мы должны использовать закон Дальтона, чтобы найти парциальное давление этого газа.
Пример \(\PageIndex{11}\)
Газообразный кислород собирали над водой, как показано выше. Атмосферное давление 754 Торр, температура 22°С, объем газа 155 мл. Давление паров воды при 22°С равно 19{-1}\right)(295 \mathrm{K})}=.00619 \mathrm{mol}\nonumber\]
Применение закона Дальтона: подводное плавание с аквалангом
Наша дыхательная система предназначена для поддержания надлежащей концентрации кислорода в крови при парциальном давлении O 2 равном 0,21 атм, что соответствует его нормальному значению на уровне моря. Ниже поверхности воды давление увеличивается на 1 атм на каждые 10,3 м увеличения глубины; таким образом, аквалангист на глубине 10,3 м испытывает давление на тело в общей сложности 2 атм. Чтобы легкие не сжались, воздух, которым дышит дайвер, также должен иметь примерно такое же давление.
Ниже поверхности воды давление увеличивается на 1 атм на каждые 10,3 м увеличения глубины; таким образом, аквалангист на глубине 10,3 м испытывает давление на тело в общей сложности 2 атм. Чтобы легкие не сжались, воздух, которым дышит дайвер, также должен иметь примерно такое же давление.
Но при полном давлении 2 атм парциальное давление \(O_2\) в обычном воздухе будет 0,42 атм; на глубине 100 футов (около 30 м) давление \(O_2\) в 0,8 атм было бы слишком высоким для здоровья. По этой причине воздушная смесь в герметичных баллонах, которые носят аквалангисты, должна содержать меньшую долю \(O_2\). Проще всего этого добиться, увеличив содержание азота, но высокое парциальное давление N 2 также может быть опасным, приводя к состоянию, известному как азотный наркоз. Предпочтительным разбавляющим агентом для длительных глубоких погружений является гелий, который имеет очень небольшую тенденцию растворяться в крови даже при высоком давлении.
Эта страница под названием 6. 3: Закон Дальтона распространяется под лицензией CC BY 3.0 и была создана, изменена и/или курирована Стивеном Лоуэром с использованием исходного контента, который был отредактирован в соответствии со стилем и стандартами платформы LibreTexts; подробная история редактирования доступна по запросу.
3: Закон Дальтона распространяется под лицензией CC BY 3.0 и была создана, изменена и/или курирована Стивеном Лоуэром с использованием исходного контента, который был отредактирован в соответствии со стилем и стандартами платформы LibreTexts; подробная история редактирования доступна по запросу.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или Страница
- Автор
- Стивен Лоуэр
- Лицензия
- СС BY
- Версия лицензии
- 3,0
- Показать страницу TOC
- № на стр.

- Теги
- Закон Дальтона о парциальном давлении
- источник@http://www.chem1.com/acad/webtext/virtualtextbook.html
Как найти молекулярную формулу газа по экспериментальным данным?
General Chemistry Online: FAQ: Газы: Как найти молекулярную формулу газа по экспериментальным данным?| Дом Распространенные соединения Экзаменационное руководство Часто задаваемые вопросы Особенности Глоссарий Конструкторы Сопроводительные заметки Просто спросите Антуана! Моделирование Индекс слайда Инструментальный ящик Индекс учебного пособия FAQ ВВЕДЕНИЕ ИЗМЕНЕНИЕ ИЗМЕНЕНИЯ АТОМ И ИОНА Соединение .  связи связи Твердые вещества Liquids Solutions Acids & bases Redox reactions Reaction rates Organic chemistry Everyday chemistry Inorganic chemistry Environmental chemistry Laboratory History of chemistry Miscellaneous |
| |||||||||||||||
| Общая химия онлайн! Как по экспериментальным данным найти молекулярную формулу газа? Copyright © 1997-2010 Фред Сенезе |

 Молярная масса газов (г/моль = кг/кмоль) от азота до хлористого этила.
Молярная масса газов (г/моль = кг/кмоль) от азота до хлористого этила. Свойства газов
Свойства газов  Введите свой запрос:
Введите свой запрос:
 количество, таким образом, отношения равны 1 для углерода и 14,1 8693 ÷ 7,13 51261 = 1,98 83223 для водорода.
количество, таким образом, отношения равны 1 для углерода и 14,1 8693 ÷ 7,13 51261 = 1,98 83223 для водорода.
