Молярная масса — что это? Как рассчитать? Формулы и примеры
Что такое моль
Прежде чем говорить о том, как найти молярную массу вещества, определимся с понятием «моль». Его ввели как искусственную величину для упрощения расчетов. Это количество вещества, в котором содержится столько же мельчайших частиц, сколько в 12 г одного из изотопов углерода — C12.
Для всех химических веществ это количество одинаково и представляет собой число Авогадро 6,02 · 1023. Постоянная Авогадро обозначается NA, а измеряется в моль-1.
Число Авогадро — это количество молекул, ионов или других мельчайших частиц в 1 моле вещества.
NA = 6,02 · 1023 моль-1.
Историческая справка
В 1811 году химик Амедео Авогадро предположил, что если взять два равных объема газов в равных значимых условиях (при одинаковой температуре и давлении), то количество молекул в этих объемах тоже будет одинаковым. Опираясь на свою гипотезу, он определил атомные и молекулярные массы многих веществ, а также рассчитал количество атомов в молекулах воды, оксидов азота и т. д. Однако в научных кругах гипотеза Авогадро долго не находила понимания. Общепринятой она стала только в 1860 году.
Опираясь на свою гипотезу, он определил атомные и молекулярные массы многих веществ, а также рассчитал количество атомов в молекулах воды, оксидов азота и т. д. Однако в научных кругах гипотеза Авогадро долго не находила понимания. Общепринятой она стала только в 1860 году.
Практикующий детский психолог Екатерина Мурашова
Бесплатный курс для современных мам и пап от Екатерины Мурашовой. Запишитесь и участвуйте в розыгрыше 8 уроков
Что такое молярная масса
Молярная масса — это масса одного моля вещества, она измеряется в граммах деленных на моль (г/моль). Данная величина представляет собой отношение массы вещества к его количеству, которое измеряется в молях.
Как обозначается молярная масса: М.
, где — это масса вещества, а — количество вещества.
Единица измерения молярной массы: г/моль.
Запоминаем!
Правильно говорить именно молярная, а не мольная масса.
Несмотря на то, что в 1 моле любого химического вещества содержится одинаковое количество молекул (и оно равно числу Авогадро), молярные массы разных веществ отличаются. Все потому, что отличаются атомы, которые входят в состав этих молекул. В частности, разница между ними заключается в относительной атомной массе (Ar) — например, Ar(Mg) = 24, а Ar(Hg) = 200. Сейчас станет ясно, какое это имеет значение.
Все потому, что отличаются атомы, которые входят в состав этих молекул. В частности, разница между ними заключается в относительной атомной массе (Ar) — например, Ar(Mg) = 24, а Ar(Hg) = 200. Сейчас станет ясно, какое это имеет значение.
Как определить молярную массу
Данная величина тесно связана с такими понятиями, как относительные атомная и молекулярная массы. Именно относительные, потому что абсолютную массу молекулы или атома вещества в химии не используют для решения задач — это слишком малые величины.
Относительная атомная масса вещества (Ar) показывает, во сколько раз его атом больше 1/12 атома углерода. Это значение для каждого химического элемента можно увидеть в таблице Менделеева.
Относительная молекулярная масса (Mr) складывается из Ar каждого атома в молекуле вещества с учетом индексов. Она показывает, на сколько масса молекулы больше 1/12 атома углерода.
, где — это количество атомов.
Разберемся на примерах.
В молекуле хлорида натрия NaCl есть 1 атом натрия и 1 атом хлора, при этом Ar(Na) = 23, Ar (Cl) = 35,5.
В молекуле NaNO2 есть 1 атом натрия, 1 атом азота и 2 атома кислорода.
Ar(Na) = 23, Ar(N) = 14, Ar(O) = 16.
Mr(NaNO2) = 23 + 14 + 16 · 2 = 69.
Собственно, для вычисления молярной массы больше ничего и не требуется.
Важно
Молярная масса вещества численно равна относительной молекулярной массе. Но путать эти два понятия не стоит — у них разный физический смысл. Молярная масса характеризует 1 моль, а относительная молекулярная — 1 молекулу.
Бесплатные занятия по английскому с носителем
Занимайтесь по 15 минут в день. Осваивайте английскую грамматику и лексику. Сделайте язык частью жизни.
Количество вещества
Из предыдущих формул понятно, что молярная масса и количество вещества тесно связаны. Рассмотрим эту связь подробнее. Начнем с того, что количество вещества может обозначаться как латинской буквой , так и греческой буквой (ню). Международное обозначение — , но не стоит удивляться, встретив в формулах любую из этих букв.
Рассмотрим эту связь подробнее. Начнем с того, что количество вещества может обозначаться как латинской буквой , так и греческой буквой (ню). Международное обозначение — , но не стоит удивляться, встретив в формулах любую из этих букв.
В формуле нахождения молярной массы мы обозначили количество вещества через :
, следовательно .
Пользуясь этим, можно найти количество вещества (в молях), если нам известны его абсолютная и молярная масса.
Пример 1
Как определить, какое количество вещества включают 350 г сульфата бария BaSO4?
Воспользуемся формулой .
Мы помним, что M = Mr (значение молярной массы равно значению относительной молекулярной).
Mr(BaSO4) = Ar(Ba) + Ar(S) + Ar(O) · 4 = 137 + 32 + 16 · 4 = 233.
М(BaSO4) = Mr(BaSO4) = 233 г/моль.
Подставим значение молярной массы в формулу:
моль.
Есть и еще одна формула количества вещества, которая позволяет найти его, если известно число молекул или других структурных единиц.
, где — число структурных единиц, — число Авогадро.
Пример 2
Допустим, некий объем CaCO3 содержит 3,01 · 1023 молекул. Как найти количество вещества, соответствующее данному объему?
Воспользуемся формулой моль.
Молярный объем
Выше мы находили количество вещества через молярную массу, но для газов это можно сделать и через молярный объем. Согласно закону Авогадро количество любого газа, равное 1 моль, будет занимать один и тот же объем, если газы рассматриваются при одинаковой температуре и давлении.
При стандартных физических условиях — температуре 0°С и давлении 1 атм или 760 мм ртутного столба, 1 моль газа занимает объем 22,4 л.
Молярный объем — это объем газа, взятого в количестве 1 моль. Он обозначается Vm.
При нормальных условиях Vm = 22,4 л/моль.
Значения молярного и фактического объема газа помогают найти количество вещества.
, где — фактический объем газа, а — молярный объем.
Пример 1
Сколько молей содержится в 120 литрах газа при нормальных условиях?
Рассчитаем по формуле моль.
Ответ: 120 литров любого газа при стандартных условиях содержат 5,36 моль.
Относительная плотность одного газа по другому
Иногда для решения задачи нужно знать, как найти молярную массу газа, о котором сообщается лишь его плотность по воздуху или по другому газу. Это возможно, если знать формулу относительной плотности, которая обозначается буквой D.
, где и — некие газы.
Пример 1
Как определить, во сколько раз угарный газ плотнее водорода?
Для начала найдем молярную массу CO и H2:
М(CO) = Mr(CO) = Ar(C) + Ar(O) = 12 + 16 = 28.
М(H) = Mr(H2) = 2 · Ar(H) = 2 · 1 = 2.
.
Ответ: угарный газ в 14 раз плотнее водорода.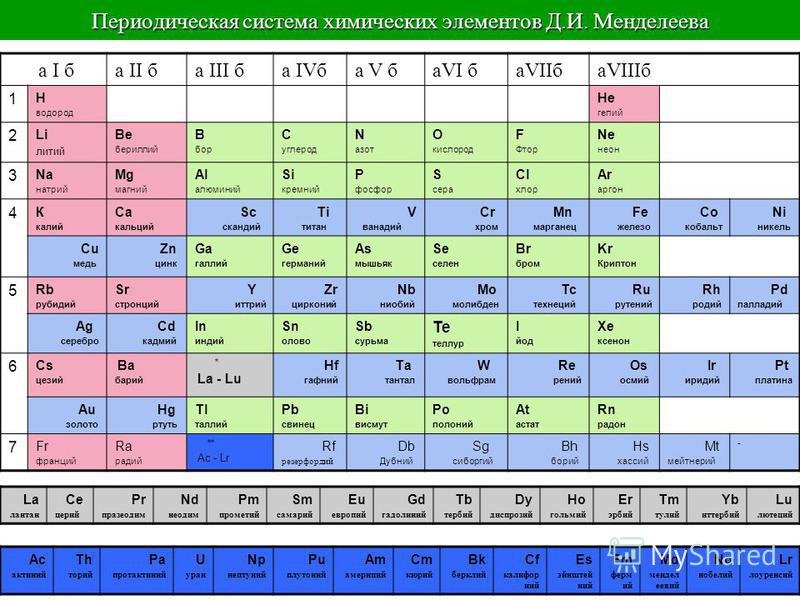
Пример 2
Как посчитать молярную массу газа х, о котором известно, что он в 10 раз плотнее углекислого газа CO2?
Подсчитаем для начала молярную массу углекислого газа:
M(CO2) = Mr(CO2) = 12 + 2 · 16 = 44.
Ориентируясь на формулу относительной плотности, произведем расчет молярной массы искомого газа х.
М(х) = D(х/CO2) · M(CO2) = 10 · 44 = 440 г/моль.
Ответ: у данного газа молярная масса 440 г/моль.
Примеры задач
Итак, мы разобрались, как находить молярную массу жидкости, газа или твердого тела и как это понятие связано с количеством вещества, а также с относительной плотностью одного газа по другому. Чтобы закрепить знания, посмотрите, как эти сведения применяются в решении задач.
Задача 1
Известно, что 300 г неустановленного вещества содержат 12,04 · 1023 молекул. Чему равна молярная масса данного вещества?
Дано:
N(х) = 12,04 · 1023.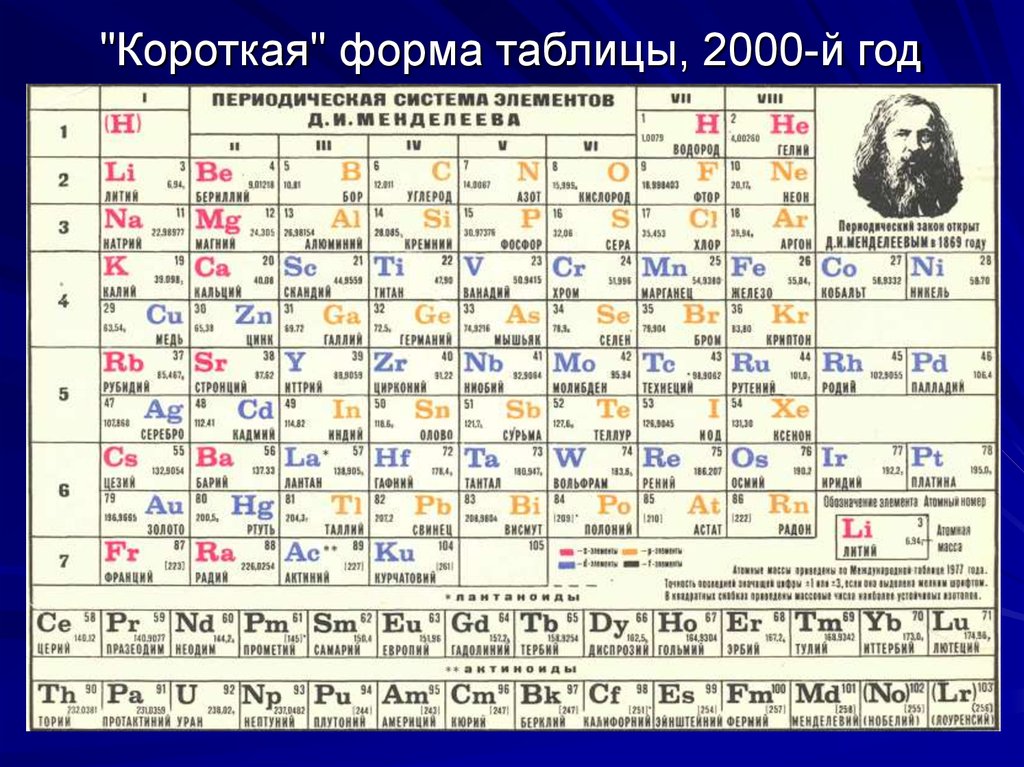
m(х) = 300 г.
M(х) = ?
Решение:
Найдем количество вещества моль.
Подставим количество вещества в формулу :
г/моль.
Ответ: молярная масса данного вещества 150 г/моль.
Задача 2
Какой объем займет водород в количестве 0,7 моль?
Дано:
моль.
Решение:
По формуле мы можем найти объем .
Зная, что молярный объем при обычных условиях составляет 22,4 л/моль, вычислим фактический объем водорода:
л.
Ответ: объем водорода составляет 15,68 литров.
Задача 3
В порции оксида серы SO3 содержится 8,356 · 1023 атомов кислорода. Какова масса этой порции?
Дано:
N(O) = 8,356 · 1023.
m(SO3) = ?
Решение:
Для решения задачи нам подходит формула , т. е. . Но для начала нужно найти количество вещества.
Мы знаем, что в одной молекуле SO3 есть 3 атома кислорода, исходя из этого можно вычислить количество молекул в порции оксида:
, следовательно .
Зная количество молекул, рассчитаем количество вещества:
моль.
Теперь можно узнать молярную массу SO3:
M(SO3) = 32 + 16 · 3 = 80 г/моль.
Рассчитаем фактическую массу через молярную массу:
г.
Ответ: абсолютная масса порции оксида серы 36,8 грамм.
Задача 4
Как рассчитать молярную массу простого вещества, о котором известно, что в порции 100 г содержится 15,05 · 1023 молекул? Назовите это вещество.
Дано:
m(x) = 100 г.
N(x) = 15,05 · 1023.
М(х) = ?
Решение:
В данном случае поможет вычислить молярную массу NA, с помощью которого мы сначала узнаем количество вещества:
моль.
Исходя из этого, рассчитаем молярную массу:
г/моль.
Ответ: согласно таблице Менделеева можно предположить, что это кальций Ca.
Задача 5
Определите, насколько сероводород H2S плотнее водорода H2?
Решение:
Нам требуется вычислить относительную плотность сероводорода по водороду:
.
Для этого вычислим молярные массы H2S и H2:
М(H2S) = 1 · 2 + 32 = 34 г/моль.
М(H2) = 1 · 2 = 2 г/моль.
Подставим значения в формулу:
.
Ответ: сероводород в 17 раз плотнее водорода.
Вопросы для самопроверки
Что такое число Авогадро и чему оно равно?
В чем измеряется молярная масса?
Напишите формулу молярной массы вещества.
Какая формула связывает количество вещества и его объем?
Как узнать количество вещества, если известно число молекул в порции?
Относительная атомная масса и молекулярная масса веществ и элементов в таблице (химия, 8 класс)
Для измерения массы атома используется относительная атомная масса, которая выражается в атомных единицах массы (а. е. м.). Относительная молекулярная масса складывается из относительных атомных масс веществ.
Содержание
- Понятия
- Как рассчитать
- Что мы узнали?
Понятия
Для осознания, что такое относительная атомная масса в химии, следует понимать, что абсолютная масса атома слишком мала, чтобы выражать её в граммах, а тем более в килограммах.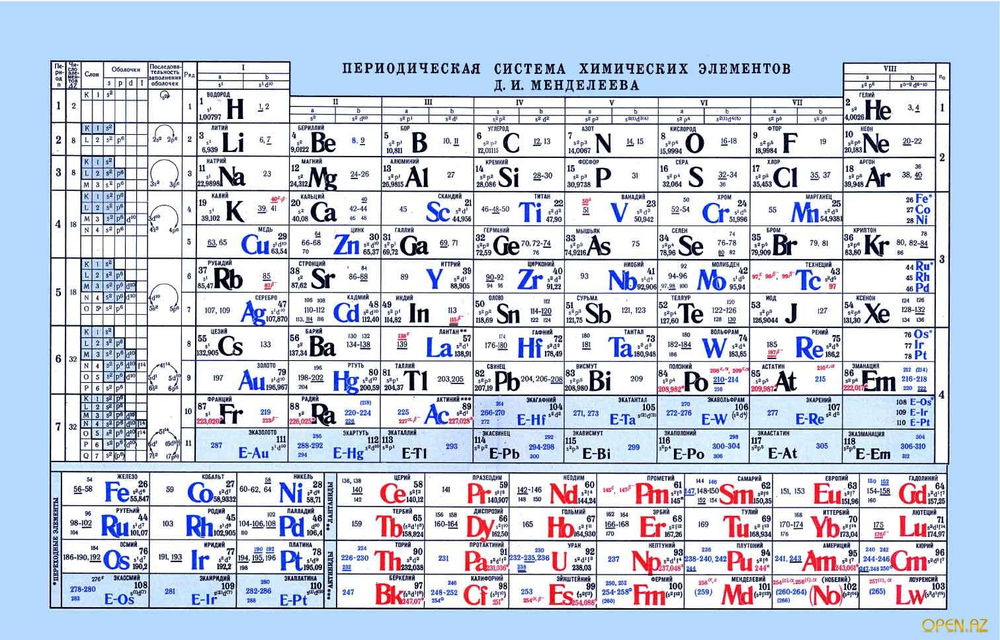 Поэтому в современной химии за атомную единицу массы (а. е. м.) взята 1/12 часть массы углерода. Относительная атомная масса равна отношению абсолютной массы к 1/12 абсолютной массы углерода. Другими словами относительная масса отражает, во сколько раз масса атома конкретного вещества превышает 1/12 массы атома углерода. Например, относительная масса азота – 14, т.е. атом азота содержит 14 а. е. м. или в 14 раз больше, чем 1/12 часть атома углерода.
Поэтому в современной химии за атомную единицу массы (а. е. м.) взята 1/12 часть массы углерода. Относительная атомная масса равна отношению абсолютной массы к 1/12 абсолютной массы углерода. Другими словами относительная масса отражает, во сколько раз масса атома конкретного вещества превышает 1/12 массы атома углерода. Например, относительная масса азота – 14, т.е. атом азота содержит 14 а. е. м. или в 14 раз больше, чем 1/12 часть атома углерода.
Рис. 1. Атомы и молекулы.
Среди всех элементов водород самый лёгкий, его масса равна 1 единице. Самые тяжёлые атомы имеют массу в 300 а. е. м.
Молекулярная масса – значение, показывающее, во сколько раз масса молекулы превышает 1/12 часть массы углерода. Также выражается в а. е. м. Масса молекулы складывается из массы атомов, поэтому для вычисления относительной молекулярной массы необходимо сложить значения масс атомов вещества. Например, относительная молекулярная масса воды равна 18. Это значение складывается из относительных атомных масс двух атомов водорода (2) и одного атома кислорода (16).
Рис. 2. Углерод в периодической таблице.
Как видно, эти два понятия имеют несколько общих характеристик:
- относительная атомная и молекулярная массы вещества – безразмерные величины;
- относительная атомная масса имеет обозначение Ar, молекулярная – Mr;
- единица измерения одинакова в обоих случаях – а. е. м.
Молярная и молекулярная массы совпадают численно, но отличаются по размерности. Молярная масса – это отношение массы вещества к количеству молей. Она отражает массу одного моля, который равен числу Авогадро, т.е. 6,02 ⋅ 1023. Например, 1 моль воды весит 18 г/моль, а Mr(Н2О) = 18 а. е. м. (тяжелее в 18 раз одной атомной единицы массы).
Как рассчитать
Чтобы выразить относительную атомную массу математически, следует определить, что 1/2 часть углерода или одна атомная единица массы равна 1,66⋅10−24 г. Следовательно, формула относительной атомной массы имеет следующий вид:
Ar(X) = ma(X) / 1,66⋅10−24,
где ma – абсолютная атомная масса вещества.
Относительная атомная масса химических элементов указана в периодической таблице Менделеева, поэтому её не нужно рассчитывать самостоятельно при решении задач. Относительные атомные массы принято округлять до целых. Исключение составляет хлор. Масса его атомов равна 35,5.
Следует обратить внимание, что при расчёте относительной атомной массы элементов, имеющих изотопы, учитывается их среднее значение. Атомная масса в этом случае высчитывается следующим образом:
Ar = ΣAr,ini,
где Ar,i – относительная атомная масса изотопов, ni – содержание изотопов в природных смесях.
Например, кислород имеет три изотопа – 16О,17О, 18О. Их относительная масса равна 15,995, 16,999, 17,999, а их содержание в природных смесях – 99,759 %, 0,037 %, 0,204 % соответственно. Поделив проценты на 100 и подставив значения, получим:
Ar = 15,995 ∙ 0,99759 + 16,999 ∙ 0,00037 + 17,999 ∙ 0,00204 = 15,999 а.е.м.
Обратившись к периодической таблице, легко найти это значение в клетке кислорода.
Рис. 3. Таблица Менделеева.
Относительная молекулярная масса – сумма масс атомов вещества:
Mr = ΣAr.
При определении значения относительной молекулярной массы учитываются индексы символов. Например, вычисление массы h3CO3 выглядит следующим образом:
Mr = 1 ∙ 2 + 12 + 16 ∙ 3 = 62 а. е. м.
Зная относительную молекулярную массу, можно вычислить относительную плотность одного газа по второму, т.е. определить, во сколько раз одно газообразное вещество тяжелее второго. Для этого используется уравнение D(y)x = Mr(х) / Mr(y).
Что мы узнали?
Из урока 8 класса узнали об относительной атомной и молекулярной массе. За единицу относительной атомной массы принята 1/12 часть массы углерода, равная 1,66⋅10−24 г. Для вычисления массы необходимо абсолютную атомную массу вещества разделить на атомную единицу массы (а. е. м.). Значение относительной атомной массы указано в периодической системе Менделеева в каждой клетке элемента. Молекулярная масса вещества складывается из суммы относительных атомных масс элементов.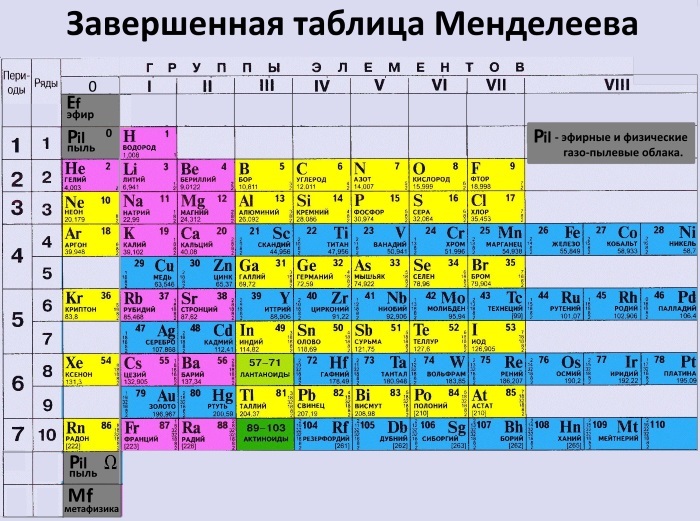
Предыдущая
ХимияНазвания химических элементов – латинское произношение, примеры в таблице
Следующая
ХимияОтносительная молекулярная масса – формула, примеры в таблице (8 класс, химия)
53642-19: MR-96A Фотометры микропланшетные – Производители, поставщики и поверители
Назначение
Фотометры микропланшетные MR-96A (далее – фотометры) предназначены для измерения оптической плотности проб и образцов биологических жидкостей.
Описание
Принцип действия фотометров – фотометрический метод в соответствии с законом Ламберта-Биира, определяющим ослабление параллельного монохроматического пучка света при распространении его в поглощающей среде.
Фотометры состоят из оптико-механического и электронно-вычислительного узлов со встроенным печатающим устройством. В качестве источника света в приборе используется галогенная лампа. Свет галогенной лампы проходит через интерференционный фильтр и попадает на вход гибкого световода. На выходе световода установлена линза, формирующая параллельный пучок, просвечивающий пробу. Выходная линза световода и фотоприемник установлены на кронштейне, в пазу которого расположен планшет с пробами. Пересечения этих пучков света в ячейке и его регистрация на фотодетекторе позволяет рассчитать часть света, поглощенную образцом. Конечный результат появляется на жидкокристаллическом экране. Общий вид фотометров микропланшетных MR-96A представлен на рисунке 1.
На выходе световода установлена линза, формирующая параллельный пучок, просвечивающий пробу. Выходная линза световода и фотоприемник установлены на кронштейне, в пазу которого расположен планшет с пробами. Пересечения этих пучков света в ячейке и его регистрация на фотодетекторе позволяет рассчитать часть света, поглощенную образцом. Конечный результат появляется на жидкокристаллическом экране. Общий вид фотометров микропланшетных MR-96A представлен на рисунке 1.
Схема пломбировки от несанкционированного доступа, представлена на рисунке 2.
Программное обеспечение
■—Г В
Фотометры имеют встроенное программное обеспечение, которое используется для выполнения и просмотра результатов измерений, изменения параметров настройки фотометра, просмотра памяти данных и передачи данных, хранения данных.
Программное обеспечение идентифицируется из главного меню выводом на экран фотометра наименования программного продукта и номера версии.
Уровень защиты программного обеспечения от непреднамеренных и преднамеренных изменений в соответствии с Р 50. 2.077-2014 «средний».
2.077-2014 «средний».
Влияние ПО на метрологические характеристики учтено при нормировании метрологических характеристик.
Идентификационные данные программного обеспечения приведены в таблице 1
Таблица 1 – Идентификационные данные программного обеспечения
|
Идентификационные признаки |
Значение |
|
Идентификационное наименование ПО |
MR-96A_ Operation Software |
|
Идентификационные признаки |
Значение |
|
Номер версии (идентификационный номер) не ниже |
01.09.04.00* |
|
Цифровой идентификатор ПО |
4F 04F 5023AF7ACA5 9FCABAB40BFE9C36 |
|
Алгоритм вычисления контрольной суммы |
MD5 |
|
* Контрольная сумма указана для приведенной версии ПО | |
Технические характеристики
Таблица 2 — Метрологические характеристики
|
Наименование характеристики |
Значение |
|
Спектральный диапазон, нм |
от 400 до 700 |
|
Диапазон показаний оптической плотности, Б |
от 0 до 4,00 |
|
Диапазон измерений оптической плотности, Б |
от 0 до 3,00 |
|
Пределы допускаемой абсолютной погрешности фотометра при измерении оптической плотности*, Б: в диапазоне от 0 до 0,4 Б включ. |
±0,02 |
|
Пределы допускаемой относительной погрешности фотометра при измерении оптической плотности, %: в диапазоне св. 0,4 до 3,0 Б |
±3,0 |
|
* В диапазоне измерений от 0 до 0,02 Б погрешность измерений составляет +0,02 Б | |
Таблица 3 — Основные технические характеристики
|
Наименование характеристики |
Значение |
|
Рабочие длины волн (стандартная поставка), нм |
405; 450; 492; 630 |
|
Г абаритные размеры (ДлинахШиринахВысота), мм, не более |
437x332x174 |
|
Масса, кг, не более |
8,5 |
|
Время измерения, с: – «быстрый» (монохроматика) режим – «нормальный» (бихроматика) режим |
5 12 |
|
Потребляемая мощность, В А, не более |
120 |
|
Напряжение питания частотой (50±1) Гц, В |
220_+£ |
|
Наработка на отказ, ч, не менее |
10 000 |
|
Средний срок службы, лет |
5 |
|
Условия эксплуатации: – диапазон температур окружающего воздуха, °С – диапазон относительной влажности окружающего воздуха, % без конденсации – диапазон атмосферного давления, кПа |
от +15 до +35 от 15 до 85 от 84 до 106,7 |
Знак утверждения типа
наносится на титульных листах Руководств по эксплуатации типографским способом и на корпус фотометров методом сеткографии.
Таблица 4 – Комплектность фотометров
|
Наименование |
Обозначение |
Количество, шт. |
|
Фотометр |
– |
1 |
|
Набор фильтров (405; 450; 492; 630) |
– |
1 |
|
Г алогеновая лампа |
– |
1 |
|
Кабель сетевой, европейский стандарт |
– |
1 |
|
Набор держателей планшетов |
– |
1 |
|
Операционная карта для считывания микропланшетов |
1 | |
|
Руководство по эксплуатации | – |
1 |
|
Методика поверки |
МП 209-0075-2019 |
1 |
Поверка
осуществляется по документу МП 209-0075-2019 «ГСИ. Фотометры микропланшетные MR-96A. Методика поверки», утвержденному ФГУП «ВНИИМ им. Д. И. Менделеева» 22 марта 2019 г.
Фотометры микропланшетные MR-96A. Методика поверки», утвержденному ФГУП «ВНИИМ им. Д. И. Менделеева» 22 марта 2019 г.
Основные средства поверки:
– комплект светофильтров поверочных КСП-02 (регистрационный номер в Федеральном информационном фонде по обеспечению единства измерений 38817-08).
Допускается применение аналогичных средств поверки, обеспечивающих определение метрологических характеристик поверяемых СИ с требуемой точностью.
Знак поверки наносится на корпус в соответствии с рис. 2, или на свидетельство о поверке фотометров.
Сведения о методах измерений
приведены в эксплуатационном документе.
Нормативные документы
Приказ Минздрава РФ от 21.02.2014 № 81н «Об утверждении перечня измерений, относящихся к сфере государственного регулирования обеспечения единства измерений, выполняемых при осуществлении деятельности в области здравоохранения, и обязательных метрологических требований к ним, в том числе показателей точности измерений»
ГОСТ 20790-93 Приборы, аппараты и оборудование медицинские. Общие технические условия
Общие технические условия
ГОСТ 30324.0-95 (МЭК 601-1-88) Изделия медицинские электрические. Часть 1. Общие требования безопасности
Техническая документация фирмы «Shenzhen Mindray Bio-Medical Electronics Co., Ltd.»,
Китай
Chemistry Ch.6 – Elements & The Periodic Table
Chapter 6 – Elements and the Periodic Table PowerPoint’s for this Chapter| 1dchem_-_pp8__atomic_theory_.pdf |
| 1dchem_-_pp9__atoms___elements_.pdf |
| 1dchem__theperiodic.pdf0015 |
| 1dchem_-_pp11__patterns_in_the_periodic_table_.pdf |
6.6 – Theories of the Atom
6. 6_atomic_theory_stations_-_notes1.pdf 6_atomic_theory_stations_-_notes1.pdf |
| 1a._atomic_thoery___history.pptx |
→ |
| ||
2400-летние поиски атома | TED-Ed: https://youtu.be/xazQRcSCRaY
История атомной химии | Ускоренный курс: https://youtu.be/thnDxFdkzZs
Другие примечания:
- Атомная теория Теория Рабочий лист (исследовательские станции)
- Атомная теория Кондиционированная деятельность
.→ |
| ||
| Periodic_table_coloring_solutions.pdf |
Песня периодической таблицы | НАУКА ASAP: https://youtu.be/VgVQKCcfwnU
| the_period_table_of_elements_in_pictures.jpg |
| the_period_table_of_elements_in_pictures_2.jpg |
6.4 – Patterns in the Periodic Table
| colouring_the_periodic_table_families.pptx |
2c. _patterns_in_the_periodic_table_lesson.pdf _patterns_in_the_periodic_table_lesson.pdf |
→ |
| ||
→ |
| ||
→ |
| ||
Решение головоломки таблицы Менделеева | Ted-Ed: https://youtu.be/O-48znAg7VE
Гениальность периодической таблицы Менделеева | TED-Ed: https://youtu.be/fPnwBITSmgU
Группы Периодической таблицы | Класс естествознания: https://youtu. be/REguN296MKI
be/REguN296MKI
→ |
| ||
→ |
| ||
Электронная конфигурация и положение элемента в таблице Менделеева | Designmate: https://youtu.be/CmJOoGq_kJQ
Как создать симуляцию атома | PhET: https://phet.colorado.edu/en/simulation/build-an-atom
Диаграмма Бора-Резерфорда (6.7 – Объяснение периодической таблицы)→ |
| ||
Как рисовать диаграммы Бора-Резерфорда – калий: https://youtu.be/wy83UlGQpWw
Точечные структуры Льюиса (6.7 – Объяснение периодической таблицы)→ |
| ||
→ |
| ||
Как объяснить, почему металлы группы 1 становятся более реакционноспособными по мере продвижения вниз по группе:
| template2018.pdf |
Глава 6 Учебник
| nelson_9_unit_c_c06-04.pdf |
| nelson_9_unit_c_c06-06.pdf |
| nelson_9_unit_c_c06-07.pdf |
Глава 6 Решения для учебников
| 6.1_-_a_table_of_elements_solutions.png |
| 6.4_-_patterns_in_the_periodic_table_solutions.png |
|
| ||||
| 6.7_-_explaining_the_periodic_table_solutions.png |
| chapter_6_review___self_test_solutions.pdf |
Relative Atomic Mass: Definition & Equation, Calculation
Масса атома настолько мала, что ее трудно измерить с помощью прибора. Например, протоны и нейтроны имеют массу порядка . Это миллиардная часть миллиардной миллиардной доли килограмма — слишком мало, чтобы их можно было измерить на практике!
Атомы настолько малы, что их трудно измерить с помощью прибора! Olive [Odagbu], StudySmarter Originals
Ученым нужен был более эффективный способ измерения массы атома.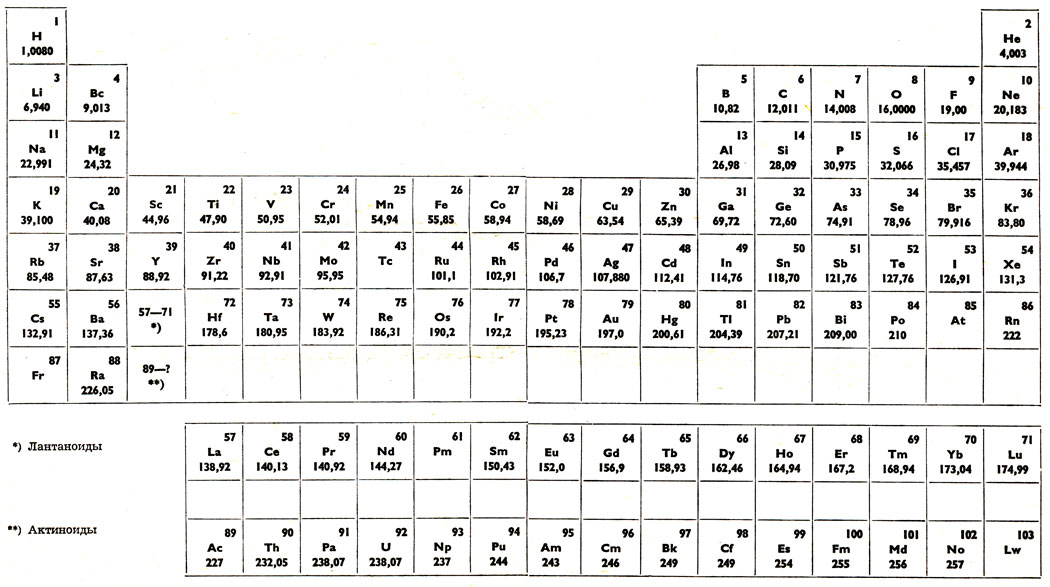 Они решили использовать массу атома углерода-12 в качестве основы для измерения масс всех остальных атомов. Они определяют относительную атомную массу атома углерода-12 как 12 и исходят из этого. Это известно как стандарт углерода-12.
Они решили использовать массу атома углерода-12 в качестве основы для измерения масс всех остальных атомов. Они определяют относительную атомную массу атома углерода-12 как 12 и исходят из этого. Это известно как стандарт углерода-12.
Когда мы говорим относительная масса , мы имеем в виду массу атома или молекулы по сравнению с массой атома углерода-12.
- В этой статье мы узнаем об относительных массах.
- Сначала мы обсудим стандарт углерода-12.
- Затем мы будем использовать его для расчета относительной атомной массы (Ar) и относительной формульной массы (Mr).
- Мы также узнаем, почему мы используем средневзвешенное значение масс.
Что такое относительная изотопная масса?
В природе могут существовать два одинаковых атома, но с разным количеством нейтронов.
Когда атом одного и того же элемента имеет разное количество нейтронов, он называется изотопом .
Масса атома изотопа по сравнению с массой углерода-12 называется относительной изотопной массой s .
Для расчета относительной массы изотопа () ученые используют следующую формулу:
=
Ученые измеряют массу атома изотопа, сравнивая ее с одной унифицированной атомной единицей массы или 1u. 1u равно массе атома углерода-12.
Примечание. Вы не будете использовать эту формулу на экзамене, но это полезно знать!
Что такое относительная атомная масса?
Относительная атомная масса (RAM или ) — это средневзвешенная масса изотопов элемента по сравнению с массой атома углерода-12.
У всех элементов есть изотопы, но одних изотопов больше, чем других. В периодической таблице число, которое мы видим для относительной атомной массы атома, является средним значением масс изотопов элемента. Это среднее значение включает в себя процент того, как часто изотоп встречается в природе. Это называется процентное содержание .
Хлор имеет два изотопа: хлор-35 и хлор-37. Четверть встречающегося в природе хлора — это хлор-37, а три четверти — хлор-35.
Четверть встречающегося в природе хлора — это хлор-37, а три четверти — хлор-35.
Вы можете рассчитать относительную атомную массу, используя эту формулу:
Ar = сумма массы изотопа x содержание изотопа / 100
Таким образом, относительная атомная масса хлора будет:
= (35 × 75) + (37 × 25) ÷ 100
= (2,625 + 925) ÷ 100 = 35,5
В периодической таблице относительный атомный массовый номер представляет собой средневзвешенное значение всех масс изотопов элемента. Оливковое [Odagbu], StudySmarter Originals
Когда мы говорим « средневзвешенное значение » , , мы имеем в виду, что оно учитывает массы всех изотопов этого элемента.
Что такое относительная молекулярная масса?
Средневзвешенное массы молекулы относительно 112 масс атома углерода-12 называется относительной молекулярной массой (Mr или RMM).
Говоря о RMM, мы должны говорить «средневзвешенное значение».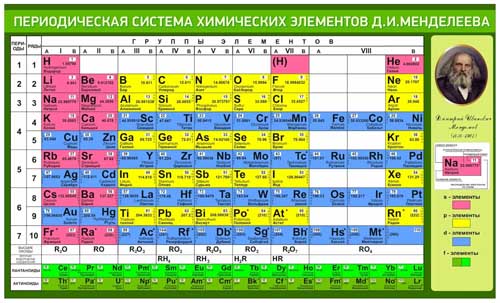 В качестве примера рассмотрим молекулу.
В качестве примера рассмотрим молекулу.
Средняя выборка молекул будет содержать атомы хлора-37 и хлора-35. Это означает, что массы молекул будут изменяться следующим образом:
12 + 1 + (3 х 35) = 118
12 + 1 + (2 х 35) + 37 = 120
12 + 1 + 35 + (2 x 37) = 122
12 + 1 + (3 x 37) = 124
Таким образом, средневзвешенное значение включает в себя количество каждой из этих молекул (или количество) в среднем образце вещества. Рассчитываем содержание изотопа в процентах.
Относительная молекулярная масса относится к молекулам с фиксированным числом атомов, соединенных вместе ковалентной связью, включая благородные газы. Сюда не входят вещества, связанные друг с другом ионными связями, такие как хлорид натрия (NaCl).
Мы можем вычислить Mr как , сложив относительные массы атомов в молекуле. Например, молекула (воды) имеет два атома водорода и один атом кислорода. Вы можете рассчитать его молекулярную массу следующим образом:
Olive [Odagbu], StudySmarter Originals
Атомная масса водорода = 1
Атомная масса атомной атомной массы = 16
MR H3O
= (2×1) + (1×16)
= 2 + 16
= 18
– NO, единица , потому что мы срезим. сравнивая их с массой углерода-12. Значение, которое мы вычисляем, — это не действительная масса атома, а сравнительная мера .
сравнивая их с массой углерода-12. Значение, которое мы вычисляем, — это не действительная масса атома, а сравнительная мера .
Что такое относительная формула массы?
Масса относительной формулы — это еще один способ измерения массы соединения. Он использует тот же символ, что и относительная молекулярная масса — Мистер 9.0019
Относительная формульная масса () представляет собой средневзвешенное значение масс формульной единицы по сравнению с массой атома углерода-12.
Формульная единица – это эмпирическая формула или простейшая формула химического вещества.
При расчете Mr необходимо использовать эмпирическую формулу химического вещества.
Эмпирическая формула Простейшее целочисленное отношение элементов | Molecular Formula |
We can use the relative formula mass to find the mass of both covalently вещества связанные и связанные ионами .
Ученые используют « относительная формула массы » вместо « относительная молекулярная масса », чтобы не предлагать ионные соединения и ионов являются молекулами.
Что такое ион?
Когда в атоме больше электронов на или на электронов меньше, чем протонов, мы называем его ионом . Ионы имеют положительный или отрицательный заряд.
Ион с большим количеством электронов, чем протонов, имеет отрицательный заряд , а ион с меньшим количеством электронов, чем протонов, имеет положительный заряд .
Ионы натрия и хлора Олива [Odagbu], StudySmarter Originals
Как рассчитать относительную формулу массы?
Вы можете найти относительную формульную массу соединения, сложив относительных атомных масс содержащихся в нем атомов.
MR NaCl (хлорид натрия)
Olive Olive [ODAGBU], StudySmarter Originals
= 23 + 35,5
= 58,5
.
 атом или молекула по сравнению с 1/12 атома углерода-12.
атом или молекула по сравнению с 1/12 атома углерода-12.Периодическая таблица и групповые тренды — химия уровня O и химия IP Примечания автора 10-летней серии
Многие студенты не понимают разницы между следующими терминами, обычно используемыми в Mole Concept & Chemical Calculations, а именно:
- Относительная атомная масса
- Относительная молекулярная масса
- Относительная формула масса
- Molar Mass
, чтобы дифференцировать их (а также, как они связаны с другими), мы были подключены к другим), мы были подключены к другим). знать их определения в первую очередь.
знать их определения в первую очередь.
Давайте рассмотрим их по очереди…..
A) Относительная атомная масса, ArОтносительная атомная масса атома – это средняя масса одного атома этого элемента по сравнению с 1/ 12 от массы одного атома углерода-12.
В принципе, для ученых нецелесообразно использовать реальные массы атомов в научных расчетах, поскольку атомы имеют очень маленькую массу.
Таким образом, ученые сравнивают массы различных атомов по отношению к атому углерода-12 (который является изотопом углерода).
Чтобы быть более точным, массы всех элементов (в пересчете на атомы), перечисленных в Периодической таблице, всегда сравниваются с 1/12 массы одного атома углерода-12.
Символ относительной атомной массы Ar.
Относительная атомная масса является отношением и поэтому не имеет единиц измерения.
Если вы обратитесь к периодической таблице, вы заметите, что относительные атомные массы некоторых элементов не являются целыми числами. Эти элементы существуют в виде смеси 90 651 изотопов 90 652 (у которых разные массовые числа ).
Эти элементы существуют в виде смеси 90 651 изотопов 90 652 (у которых разные массовые числа ).
относительных атомных масс , которые вы видите в периодической таблице, рассчитаны на основе относительного процентного содержания изотопов . Итак, относительная атомная масса — это, по сути, среднее значение после рассмотрения всех различных изотопов элемента .
Для студентов GCE O-Level Pure Chemistry (код учебной программы 6092) в Сингапуре периодическая таблица не так точна, как та, которую используют студенты GCE A-Level h3 Chemistry (код учебной программы 9729).
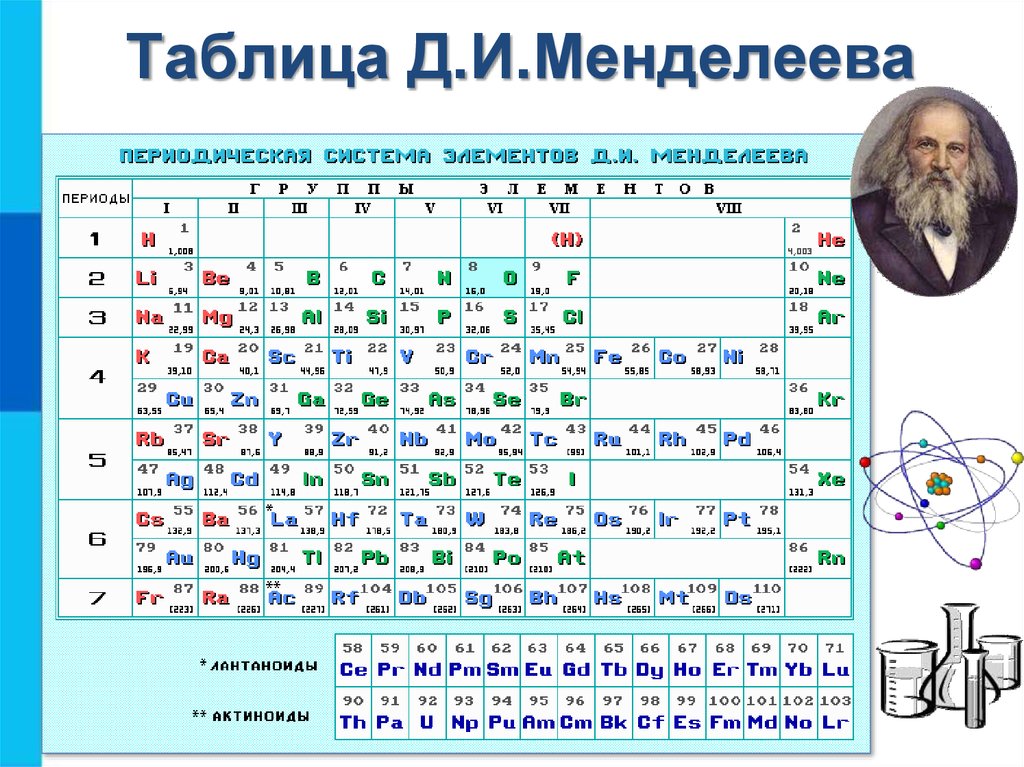
Следующая периодическая таблица используется студентами GCE O-Level Chemistry.
Периодическая таблица, используемая студентами GCE O-Level Pure Chemistry в Сингапуре Обратите внимание, что хлор (атомный номер 17) имеет относительную атомную массу, Ar 35,5, которая не является целым числом. На самом деле, большинство элементов в Периодической таблице существуют в виде изотопов, поэтому их относительная атомная масса не является целым числом.
Если вы посмотрите на Периодическую таблицу, используемую в более продвинутых программах по химии, таких как GCE A-Level h3 Chemistry, то увидите, что большинство элементов не являются целыми числами. Они представлены с 1 десятичным знаком.
Периодическая таблица, используемая студентами-химиками GCE уровня h3 в СингапуреДавайте рассмотрим классический пример расчета относительной атомной массы.
Пример:
Хлор существует в виде хлора-35 (% содержания 75%) и хлора-37 (% содержания 25%).
Следовательно, относительная атомная масса хлора = (75/100 x 35) + (25/100 x 37) = 35,5 (как показано в Периодической таблице)
Резюме определения изотопов:
- Атомы одного и того же элемента
- Одинаковое число протонов и электронов
- Различное число нейтронов
Относительная молекулярная масса молекулы – это средняя масса одной молекулы этого элемента или соединения по сравнению с 1/12 массы одного атома углерода-12.
Многие элементы и соединения существуют в виде ковалентных молекул.
Масса молекулы (элемента или соединения) измеряется относительной молекулярной массой.
Символ относительной молекулярной массы Mr.
Относительная молекулярная масса также является отношением и поэтому не имеет единиц измерения.
Чтобы вычислить относительную молекулярную массу молекулы, вам нужно сложить все относительные атомные массы всех атомов в ее химической формуле.
Из-за изотопных эффектов фактические молекулярные массы могут отличаться, если атомы каждого присутствующего элемента являются изотопами.
Приведу пример.
Известно, что углерод существует в двух изотопах: углерод-12 и углерод-13.
Известно, что кислород существует в трех изотопах: кислород-16, кислород-17 и кислород-18.
Таким образом, мы можем иметь двуокись углерода, молекулы CO 2 с различной молекулярной массой.
Обратите внимание, что для расчета молей мы склонны просто использовать относительные атомные массы (средние значения) элементов (как видно из Периодической таблицы) и вычислять относительные молекулярные массы (средние значения).
Масса относительной формулы ионного соединения представляет собой среднюю массу одной единицы этого ионного соединения по сравнению с 1/12 массы одного атома углерода-12.
Ионные соединения, такие как хлорид натрия и оксид магния, не существуют в виде молекул.
Таким образом, использование термина «относительная молекулярная масса» для ионных соединений сбивает с толку.
Вместо этого мы используем термин относительная формула массы.
Относительная формула массы имеет тот же символ, что и Mr, и не имеет единиц измерения.
Рассчитывается так же, как относительная молекулярная масса молекул, путем рассмотрения химической формулы и сложения относительных атомных масс атомов.
D) Молярная массаМолярная масса относится к массе одного моля вещества (которое может быть элементом или соединением) .
- Молярная масса элемента (в пересчете на атом) равна его относительной атомной массе (Ar) в граммах.
- Молярная масса молекулярного вещества равна его относительной молекулярной массе (Mr) в граммах.
- Молярная масса ионогенного соединения равна его относительной формульной массе (Mr) в граммах.
Пример:
- Относительная атомная масса магния равна 24. Это означает, что один моль атомов магния имеет массу 24 г. Таким образом, молярная масса магния составит 24 г/моль.
- Относительная молекулярная масса двуокиси углерода равна 44. Это означает, что один моль молекул двуокиси углерода имеет массу 44 г. Таким образом, молярная масса диоксида углерода составит 44 г/моль.
Что касается концепций молей и химических расчетов, обратите внимание, что на самом деле «нет никакой разницы» между молярной массой и относительной атомной массой (Ar) или относительной молекулярной/формульной массой (Mr). Когда дело доходит до расчета, вы получите тот же числовой ответ.
И по этой причине я видел, как преподаватели (учителя и профессиональные репетиторы) используют эти два термина взаимозаменяемо и причинно.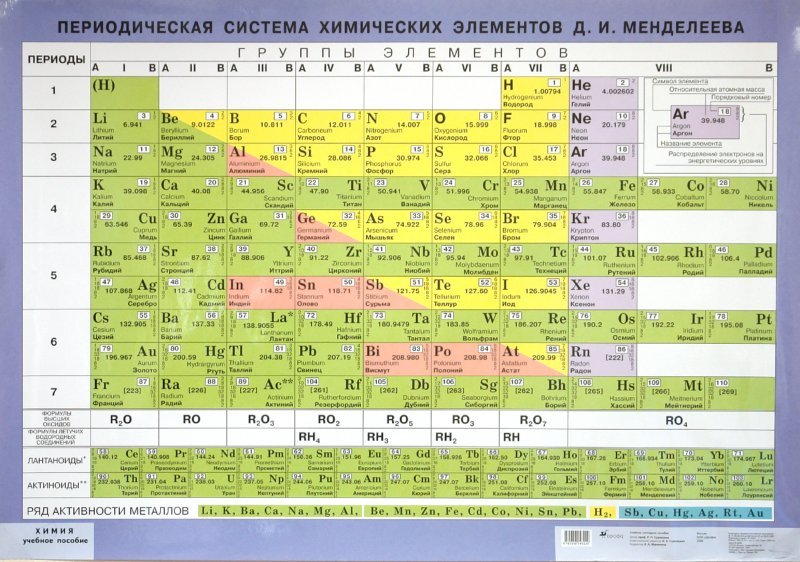
Приведу пример….
Химики подсчитывают частицы, используя единицу измерения, известную как моль (единицей СИ является «моль»), которая используется для определения химических формул веществ при выполнении расчетов.
Один моль любого вещества содержит 6 x 10 23 частиц. Это известно как постоянная Авогадро или число Авогадро.
Вы, вероятно, столкнетесь с двумя похожими формулами, включающими моль и массу, когда будете искать в Интернете.
A) Моль элемента (моль) = масса элемента (г) / относительная атомная масса элемента
Пример: скажем, у нас есть 24 г магнезии
Ответ: моль Mg = (24 г) / (24) = 1 моль
B) Моль элемента (моль) = масса элемента (г) / молярная масса элемента (г/моль)
Пример: Допустим, у нас есть 24 г магнезии
Ответ: Моль Mg = (24 г) / (24 г/моль) = 1 моль
Как видите, формула B, основанная на единицах СИ, является более точной, поскольку единицы измерения сокращаются.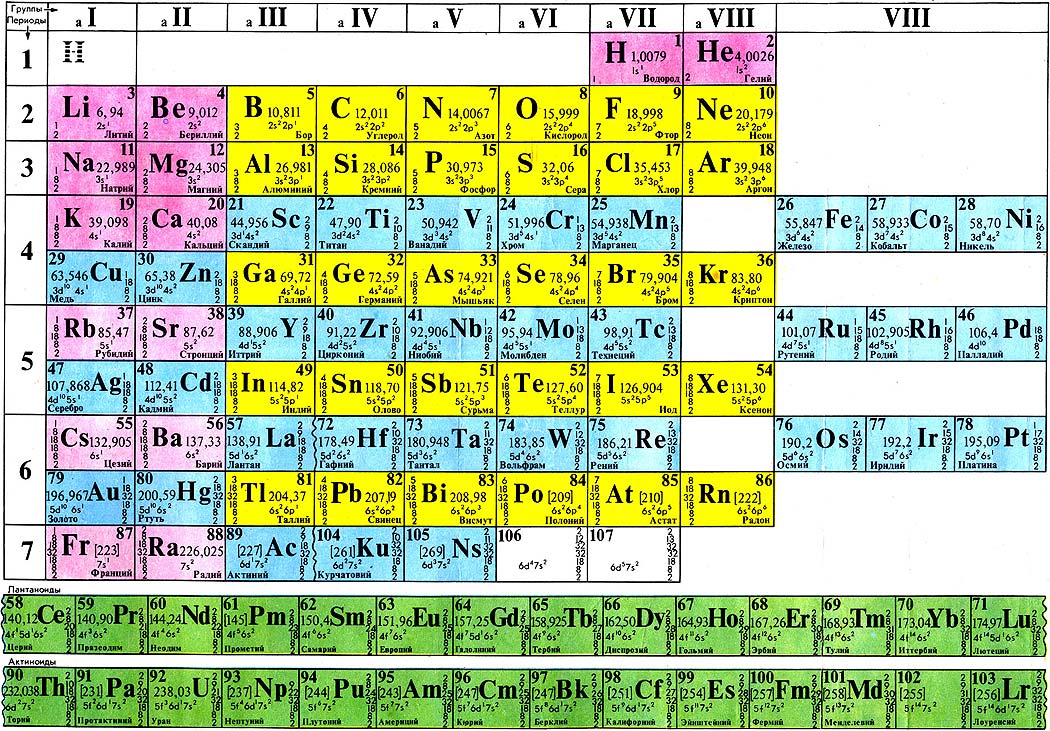 приятно дать вам «моль».
приятно дать вам «моль».
Однако вы также можете видеть, что обе формулы дадут вам одинаковые ответы «1 моль».
Это также иногда зависит от содержания учебного плана, предоставленного Министерством образования их страны. Школьные учителя, как правило, очень внимательно следят за ними. Как профессиональный репетитор по химии в Сингапуре, я также внимательно слежу за ней, чтобы мне не приходилось спорить со студентами, которые посещают мои еженедельные занятия GCE O-Level и IP Pure Chemistry Weekly Tuition, когда они говорят, что формула, которую они видели, в их школе немного по-другому.
Позвольте мне показать вам, что я имею в виду.
Учебник «Chemistry Matters» издательства Marshall Cavendish Education является одним из двух учебников по чистой химии, одобренных Министерством образования Сингапура (MOE), которые все студенты, изучающие 3 и 4 курсы химии, должны получить в качестве справочного пособия.
Формула для расчета количества молей вещества немного отличается в 1-м издании (до 2013 г. ) и во 2-м/3-м издании (начиная с 2013 г.).
) и во 2-м/3-м издании (начиная с 2013 г.).
Формула А напечатана в 1-м издании (для использования до 2013 года).
Формула B напечатана во 2-м издании (для использования с 2013 по 2017 год). Новейшее 3-е издание (начиная с 2014 г.) также следует этой версии.
Итак, для всех моих индивидуальных заметок по химии, видео на YouTube и блогов по химии до 2013 года я использовал Формулу А. Я начал использовать Формулу Б с 2013 года.
Вы можете видеть, что я использовал формулу A (использование относительной молекулярной массы, Mr вместо Molar Mass) в одном из моих видеороликов по химии на YouTube, выпущенных в апреле 2009 года.и имеет около 15 000 просмотров. Вау, время летит незаметно, этому видео уже 11 лет!
Надеемся, что вышеизложенное понятно, и вы знаете различия, а также связь между четырьмя общими терминами, используемыми в Mole Concept и Chemical Calculations.



 _bohr-rutherford_diagram_solutions.pdf
_bohr-rutherford_diagram_solutions.pdf  6_-_theories_of_the_atom_solutions_part_1.png
6_-_theories_of_the_atom_solutions_part_1.png