Таблица Менделеева online – Na
Na
11
1
8
2
22.98977±1
3s1
Натрий
| Относительная электроотрицательность (по Полингу): | 1,01 |
| Температура плавления: | 97,81°C |
| Температура кипения: | 882,9°C |
| Теплопроводность: | 150 |
| Плотность: | 0,971 г/см3 |
| Открыт: | Гемфри Дэви |
| Цвет в твёрдом состоянии: | Серебристо-белый (в очень чистом виде – розовый) |
| Тип: | Щелочной металл |
| Орбитали: | 1s22s22p63s1 |
| Электронная формула: |
Na – 1s2 2s2 2p6 3s1 Na – [Ne] 3s |
| Валентность: | +1 |
| Степени окисления: | 0, +I |
| Сверхпроводящее состояние при температуре: | 0 К |
| Потенциалы ионизации: | 5,139 В 47,286 В 71,641 В |
Электропроводность в тв. фазе: фазе: |
21,1*106 при 273K |
| Ковалентный радиус: | 1,54 Å |
| Атомный объем: | 23,7 см3/моль |
| Атомный радиус: | 2,32 Å |
| Теплота распада: | 2,598 Кдж/моль |
| Теплота парообразования: | 96,96 Кдж/моль |
| Кристаллическая структура: | Объемоцентрированный куб. Высота, ширина, длина равны. Все углы прямые. По атому имеется в каждой вершине, а также атом в центре куба |
Реклама
Изотопы
| Символ нуклида |
Z(p) | N(n) | Масса изотопа (а. е. м.) |
Период полураспада (T1/2 |
Спин и чётность ядра |
|---|---|---|---|---|---|
| Энергия возбуждения | |||||
| 18Na | 11 | 7 | 18,02597 | 1,3·10−21 с | 1- |
| 19Na | 11 | 8 | 19,013877 | 40 нс | 5/2+ |
| 20Na | 11 | 9 | 20,007351 | 447,9 мс | 2+ |
| 21Na | 11 | 10 | 20,9976552 | 22,49 с | 3/2+ |
| 22Na | 11 | 11 | 21,9944364 | 2,6027 года | 3+ |
| 22mNa | 583,03 кэВ | 244 нс | 1+ | ||
| 23Na | 11 | 12 | 22,9897692809 | стабилен | 3/2+ |
| 24Na | 11 | 13 | 23,99096278 | 14,9590 ч | 4+ |
| 24mNa | 472,207 кэВ | 20,20 мс | 1+ | ||
| 25Na | 11 | 24,9899540 | 59,1 с | 5/2+ | |
| 26Na | 11 | 15 | 25,992633 | 1,077 с | 3+ |
| 27Na | 11 | 16 | 26,994077 | 301 мс | 5/2+ |
| 28Na | 11 | 17 | 27,998938 | 30,5 мс | 1+ |
| 29Na | 11 | 18 | 29,002861 | 44,9 мс | 3/2+ |
| 30Na | 11 | 19 | 30,008976 | 48,4 мс | 2+ |
| 31Na | 11 | 20 | 31,01359 | 17,0 мс | 3/2+ |
| 32Na | 11 | 21 | 32,02047 | 12,9 мс | 3- |
| 33Na | 11 | 22 | 33,02672 | 8,2 мс | 3/2+ |
| 34Na | 11 | 23 | 34,03517 | 5,5 мс | 1+ |
| 35Na | 11 | 24 | 35,04249 | 1,5 мс | 3/2+ |
| 36Na | 25 | 36,05148 | 260 нс | ||
| 37Na | 11 | 26 | 37,05934 | 1 мс | 3/2+ |
XuMuK.
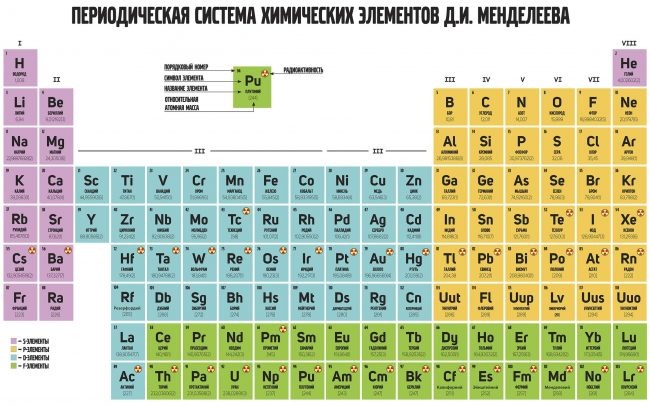 ru — Таблица Менделеева — периодическая система химических элементов
ru — Таблица Менделеева — периодическая система химических элементовПредисловие
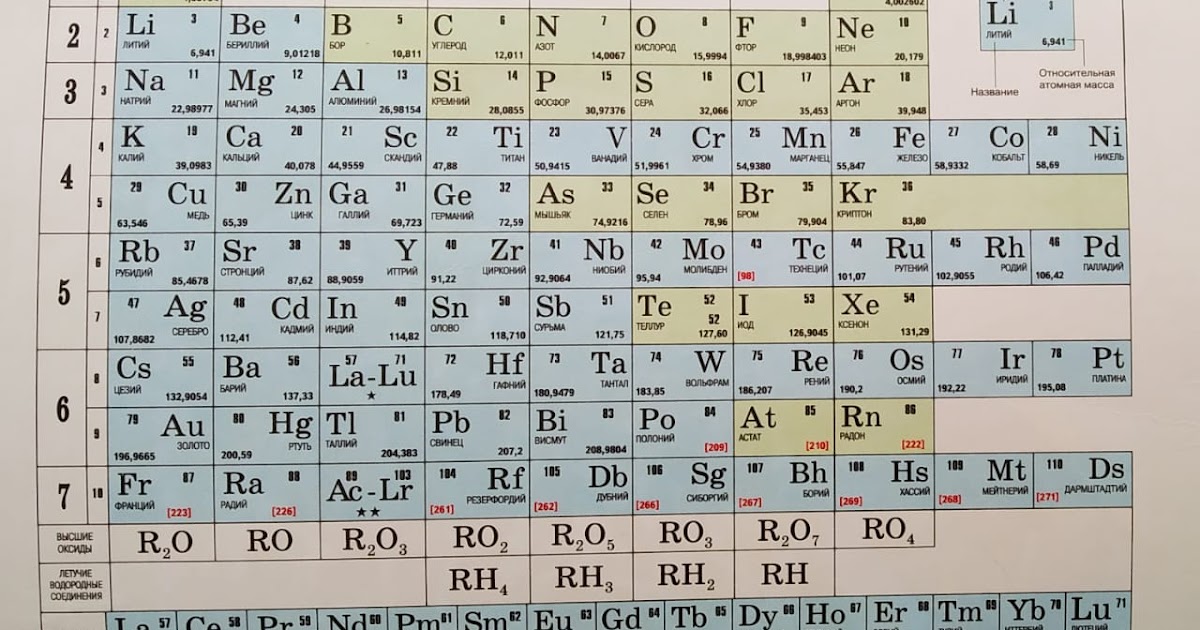
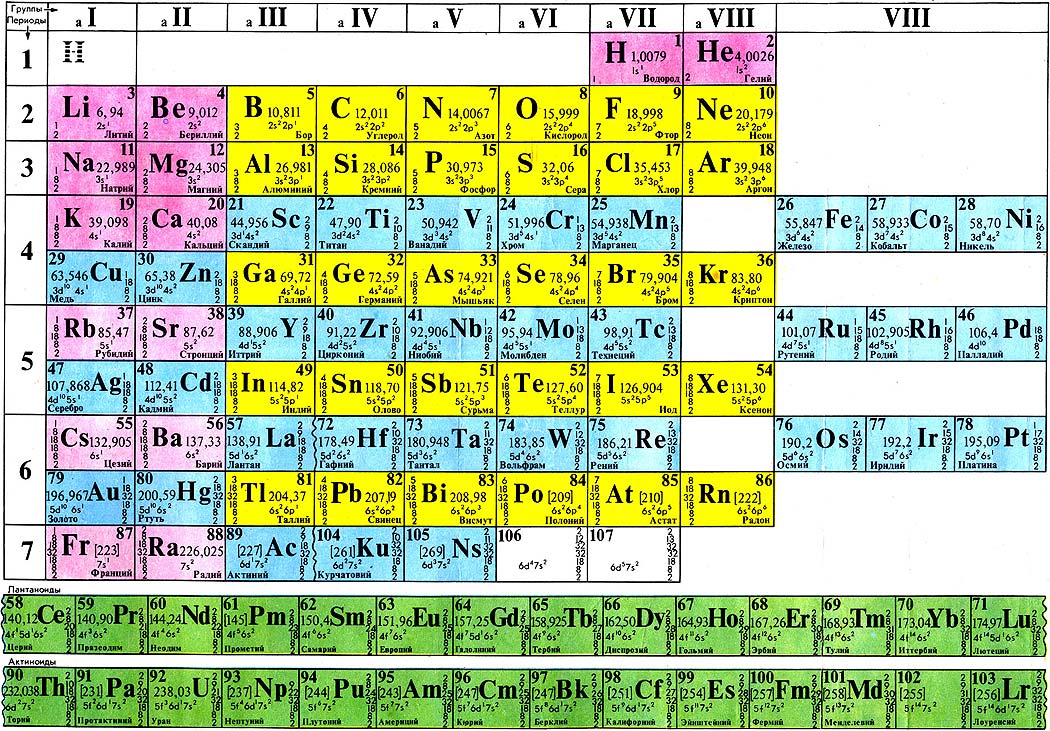
Таблица Менделеева или периодическая таблица химических элементов – это
представленный в виде таблицы свод химических элементов, которые расположены по возрастанию атомного
номера. В каждой ячейке таблицы Менделеева так же есть обозначение элемента, его атомная масса, принадлежность к
определенной группе обозначенная цветом, а так же иногда указывается электронная конфигурация. Структура
таблицы показывает периодических характер химических свойств элементов.
Она имеет 7 строк, которые называются периодами, и столбцы, которые называются группами. Именно столбцы
объединяют элементы со схожими химическими свойствами.
Например, щелочные металлы, щелочно-земельные металлы, галогениды, благородные газы и т.д. Так же
имеется четыре прямоугольные области, которые объединяют элементы со схожим электронным строением их
атомов.
На данный момент открыто 118 химических элементов, которые завершили заполнение семи строк таблицы. Первые 94 элемента были найдены в природе, хотя некоторые в очень маленьких количествах, а вот остальные синтезированы искусственно в физических лабораториях или вообще при ядерных взрывах. В настоящее время ученые-физики продолжают попытки синтезировать 119 элемент и более тяжелые, теоретически возможность этих элементов была доказана ранее – они начнут восьмой ряд периодической таблицы Менделеева. Кроме того, все элементы имеют так называемые изотопы, которые так же в большом количестве были синтезированы в лабораториях и обнаружены в природе. Наиболее известный пример – тяжелая вода, где водород с атомным весом 1 заменяет его изотоп дейтерий (вес 2) или тритий (вес 3).
Структура периодической таблицы используется для нахождения взаимосвязи между свойствами различных
элементов и их соединений, а так же для прогноза этих свойств в том числе еще не открытых соединений.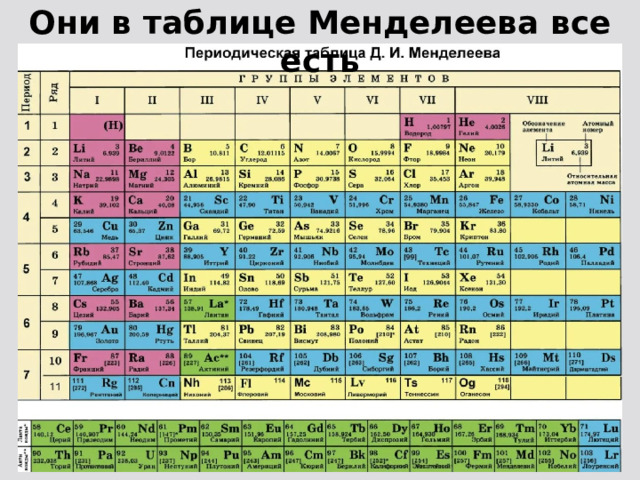
Первую известную таблицу Менделеев опубликовал в 1869 году, которая демонстрировала периодический характер свойств известных на тот момент элементов. Так же Менделеев дал предсказания по свойствам не открытых на тот момент элементов и большинство его предсказания оказались близки к верным. В последующем с открытием других элементов расширялись и теоретические знания, стали появляться всё более точные теоретические математические модели для объяснения и предсказания свойств элементов.
Современная таблица Менделеева теперь широко используется для анализа химических реакций и вообще широко
используется как в химии так и физике. Однако, много споров ведется относительно того на сколько
оптимален тот или иной вид таблицы (их несколько десятков), а так же размещения некоторых элементов.
Введение
Каждый химический элемент в таблице Менделеева имеет свой уникальный атомный номер (Z), который равен числу
протонов в его атомном ядре. У каждого атома в ядре может быть разное число нейтронов и поэтому атом
одного элемента может иметь разную массу – такие «варианты» одного атома отличающиеся по
массе называют изотопами. Например, самые распространенные изотопы урана U
В общепринятой периодической таблице (см. выше) химические элементы указываются в порядке возрастания
атомного номера Z. Новая строка (период) начинается тогда, когда начинает заполняться новая электронная
оболочка атома.
Новая строка (период) начинается тогда, когда начинает заполняться новая электронная
оболочка атома.
Столбцы (группы) определяются электронной конфигурацией атома. Элементы с одинаковым чистом электронов на валентном электронном уровне попадают в одни и те же группы. Элементы находящиеся в одной группе как правило имеют схожие химические свойства.
Первые 94 элемента встречаются в природе в свободном и связанном виде либо только в виде составе соединений, остальные же синтезированы в лабораториях. Некоторые элементы, например, франций (Fr) был зафиксирован только в виде излучения (получено всего 300 тыс. атомов). Другие элементы выше 94 получены так же в очень малых количествах.
Металлы, металлоиды и неметаллы
По своим физико-химическим свойствам все элементы можно разделить на три основные категории – металлы,
металлоиды и неметаллы.
Металлы – это как правило блестящие высоко теплопроводные твёрдые вещества способные плавиться при нагревании и образовывать друг с другом сплавы, а так же образовывать ионные и ковалентные соединения с неметаллами.
Неметаллы – это как правило бесцветные либо цветные твёрдые, жидкие или газообразные вещества. Неметаллые образуют соединения друг с другом при помощи ковалентных связей.
Металлоиды – это вещества, которые могут проявлять в определенных условиях как металлические свойства, так и неметаллические.
Металлы и неметаллы могут быть дополнительно классифицированы на подкатегории, которые видны в таблице в
строках слева направо. Так металлы подразделяются на химически очень активные щелочные металлы, чуть
менее активные щелочно-земельные, характерные переходные металлы и химически достаточно инертные
постпереходные металлы.
Неметаллы подразделяются на многоатомные неметаллы, при этом они ближе к металлоидам т.к. иногда проявляют металлические свойства, на галогениды и инертные газы. Доля неметаллов среди всех элементов небольшая – их 19 из 118 известных элементов.
На самом же деле такое подразделение даже внутри каждой категории весьма условно и на этих условных
границах есть большое «перекрытие». Например, бериллий относится к щелочно-земельным
элементам, но его амфотерность и склонность образовывать ковалентные соединения позволяют относить его к
постпереходным металлам. Радон относится к благородным газам, но образует ряд ионных соединений характерных
для металлов. Поэтому
существуют и другие типы разделения элементов на группы, например, по минералогическим признакам или
кристаллическим структурам соединений.
Щелочные и щелочно-земельные металлы
Эти две категории очень похожи друг на друга, но щелочно-земельные металлы менее химически активны. Все они образуют основные оксиды. Для них характерна низкая механическая прочность, все щелочные металлы легко режутся ножом, очень высокая химическая активность (например, калий, и тем более рубидий могут воспламеняться прямо на воздухе, а с водой реагировать со «взрывом» – реакиция идет настолько быстро, что раздаётся хлопок). Магний и бериллий более твёрдые и гораздо менее реакционно способные, поэтому они используются иногда в чистом виде или в виде сплавов (магний-алюминиевый сплав очень важен в авиационной отрасли, например).
Переходные металлы
У этой группы очень широкий спектр физических и химических свойств. Например, температура плавления у
ртути -38,8 ºC, а у иттрия 1795 ºC. Так же в очень широком диапазоне находится твёрдость,
плотность, химическая активность (например, благородный металл золото очень химически инертен, а цинк
наоборот весьма реакционно способен и по этому показателю ближе к щелочно-земельным элементам). Металлы
этой группы – основа всех промышленных производств и сфер жизни. Они применяются во всех отраслях
промышленности – от конструкционных материалов до микроэлектронной промышленности.
Так же в очень широком диапазоне находится твёрдость,
плотность, химическая активность (например, благородный металл золото очень химически инертен, а цинк
наоборот весьма реакционно способен и по этому показателю ближе к щелочно-земельным элементам). Металлы
этой группы – основа всех промышленных производств и сфер жизни. Они применяются во всех отраслях
промышленности – от конструкционных материалов до микроэлектронной промышленности.
Лантаноиды
По своим свойствам они похожи так же на щелочно-земельные металлы, но менее активны. Лантаноиды и их соединения очень похожи друг на друга, поэтому трудно поддаются разделению. В природе они очень рассеяны и их добыча весьма сложна. Однако благодаря свойствам их соединений они крайне важны в современной промышленности.
Актиноиды
Почти все актиноиды мягкие, плотные и достаточно реакционно способные металлы. Металлы от актиния до
плутона встречаются в природе, остальные получают только в лабораториях.
Металлы от актиния до
плутона встречаются в природе, остальные получают только в лабораториях.
Постпереходные металлы
Мягкие или хрупкие металлы с низкой механической прочностью и температурой плавления ниже температур плавления переходных металлов (например, ртуть -38,8 ºC, индий 156,6 ºC, олово 231,9 ºC, алюминий 660 ºC). С неметаллами образуют как правило ковалентные соединения, кислотно-основные соли, для их оксидов характерна амфотерность.
Металлоиды
Это промежуточный тип элементов между металлами и неметаллами. Кремний, например, внешне выглядит как металл (серый блестящий), но при этом совершенно непластичный (хрупкий) и является полупроводником. Химически они в основном ведут себя как неметаллы. Образуют кислотные или амфотерные оксиды.
Неметаллы (реакционные)
При нормальных условиях бор, углерод, фосфор, сера, селен – твёрдые вещества различных цветов.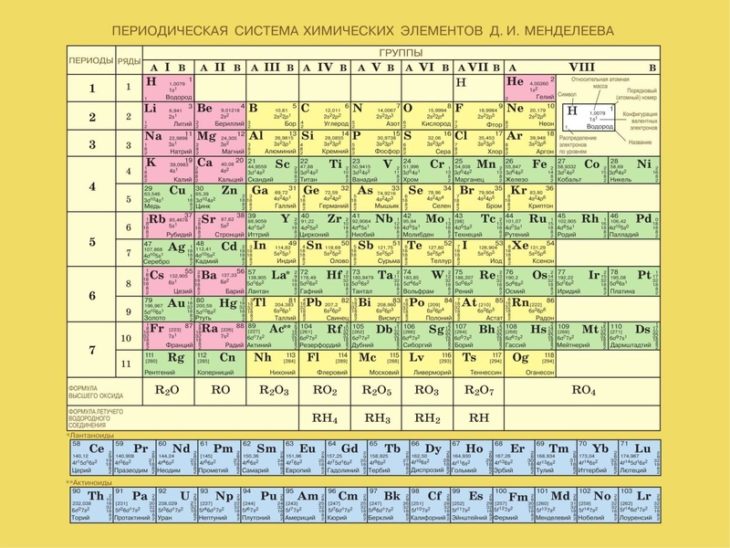 Каждое их
них имеет различные формы кристаллической решетки (аллотропные модификации), например красный, желтый,
черный, белый фосфор, которая очень сильно влияет на их химическую активность (например, графит гораздо
менее активен обычного угля) и физические свойства (алмаз самое твердое вещество в природе и это
прозрачный материал, а графит хрупкий, мягкий, непрозрачный).
Каждое их
них имеет различные формы кристаллической решетки (аллотропные модификации), например красный, желтый,
черный, белый фосфор, которая очень сильно влияет на их химическую активность (например, графит гораздо
менее активен обычного угля) и физические свойства (алмаз самое твердое вещество в природе и это
прозрачный материал, а графит хрупкий, мягкий, непрозрачный).
Азот и кислород – газы. При этом азот достаточно химически инертен, кислород напротив является очень активным окислителем.
Галогениды имеют разные физические свойства (фтор, хлор – газы, бром – жидкость, иод – твердое
вещество). Астат получен только в крайне малых количествах как и теннессин, их свойства изучены плохо.
Химически галогениды – очень сильные окислители (фтор самый сильный в Таблице Менделеева). С металлами
образуют как правило соли с ионной решеткой, а с водородом очень сильные кислоты. С неметаллами так же
образуют множество многоатомных соединений как правило с ковалентными связями.
С металлами
образуют как правило соли с ионной решеткой, а с водородом очень сильные кислоты. С неметаллами так же
образуют множество многоатомных соединений как правило с ковалентными связями.
Неметаллы (инертные газы)
Крайне химически пассивные вещества. Первое соединение ксенона XePtF6 было синтезировано в 1962 году, а соединения неона и гелия до сих пор неизвестны. Тем не менее инертные газы играют огромную роль в различных отраслях промышленности, медицине, при подводных погружениях и т.д.
P.S.: Интересно, что название “Таблица Менделеева” известна в основном только в России, а в остальном мире она называется чаще всего просто “Периодическая таблица”.
P.P.S.: Статья будет дополняться и корректироваться.
Третий период 3 период, периоды — периодическая система химических элементов
- Главная
- Статьи
- Периодическая система элементов — Периодическая система химических элементов, периодическая система элементов Менделеева
- Третий период 3 период, периоды — периодическая система химических элементов
+++++
Третий период периодической системы элементов
Третий период (Na — Ar) также содержит 8 элементов, характер изменения свойств которых во многом аналогичен наблюдающемуся во втором периоде. Однако Mg, в отличие от Be, более металличен, равно как и Al по сравнению с В, хотя Al присуща амфотерность. Si, Р, S, Cl, Ar — типичные неметаллы, но все они (кроме Ar) проявляют высшие степени окисления, равные номеру группы. Таким образом, в обоих периодах по мере увеличения Z наблюдается ослабление металлического и усиление неметаллического характера элементов.
Однако Mg, в отличие от Be, более металличен, равно как и Al по сравнению с В, хотя Al присуща амфотерность. Si, Р, S, Cl, Ar — типичные неметаллы, но все они (кроме Ar) проявляют высшие степени окисления, равные номеру группы. Таким образом, в обоих периодах по мере увеличения Z наблюдается ослабление металлического и усиление неметаллического характера элементов.
Менделеев называл элементы второго и третьего периодов (малых, по его терминологии) типическими. Существенно, что они принадлежат к числу наиболее распространённых в природе, а С, N и O являются наряду с H основными элементами органической материи (органогенами). Все элементы первых трёх периодов входят в подгруппы а.
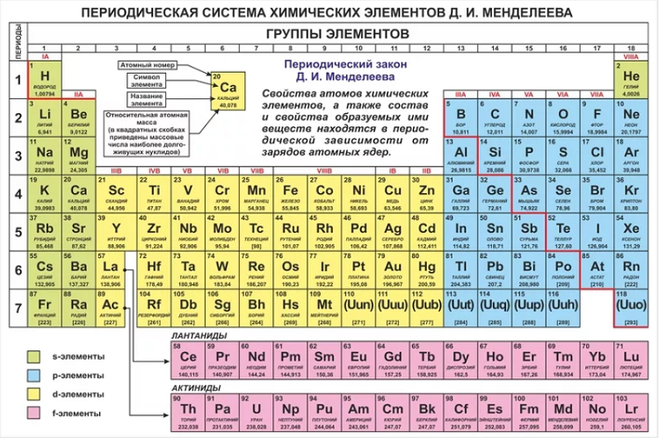
Современная терминология – элементы этих периодов относятся к s-элементам (щелочные и щёлочноземельные металлы), составляющим Ia- и IIa-подгруппы (выделены на цветной таблице красным цветом), и р-элементам (В — Ne, At — Ar), входящим в IIIa — VIIIa-подгруппы (их символы выделены оранжевым цветом). Для элементов малых периодов с возрастанием порядковых номеров сначала наблюдается уменьшение атомных радиусов, а затем, когда число электронов в наружной оболочке атома уже значительно возрастает, их взаимное отталкивание приводит к увеличению атомных радиусов. Очередной максимум достигается в начале следующего периода на щелочном элементе. Примерно такая же закономерность характерна для ионных радиусов.
Для элементов малых периодов с возрастанием порядковых номеров сначала наблюдается уменьшение атомных радиусов, а затем, когда число электронов в наружной оболочке атома уже значительно возрастает, их взаимное отталкивание приводит к увеличению атомных радиусов. Очередной максимум достигается в начале следующего периода на щелочном элементе. Примерно такая же закономерность характерна для ионных радиусов.
Третий период периодической системы химических элементов
|
IA |
IIA |
IIIB |
IVB |
VB |
VIB |
VIIB |
—- |
VIIIB |
—- |
IB |
IIB |
IIIA |
IVA |
VA |
VIA |
VIIA |
VIIIA |
|
| Период | ||||||||||||||||||
| 3 |
11
Na |
12
Mg |
13
Al |
14
Si |
15
P |
16
S |
17
Cl |
18
Ar |
| Щелочные металлы | Щёлочноземельные металлы | Лантаноиды | Актиноиды | Переходные металлы |
| Лёгкие металлы | Полуметаллы | Неметаллы | Галогены | Инертные газы |
Периодическая система химических элементов Менделеева
Классификация хим. элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра. Система является графическим выражением периодического закона/
элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра. Система является графическим выражением периодического закона/
| IA | IIA | IIIB | IVB | VB | VIB | VIIB | —- | VIIIB | —- | IB | IIB | IIIA | IVA | VA | VIA | VIIA | VIIIA | |
| Период | ||||||||||||||||||
| 1 |
1 H Водород |
2 He Гелий |
||||||||||||||||
| 2 |
3 Li Литий |
4 Be Бериллий |
5 B Бор |
6 C Углерод |
7 N Азот |
8 O Кислород |
9 F Фтор |
10 Ne Неон |
||||||||||
| 3 |
11 Na Натрий |
12 Mg Магний |
13 Al Алюминий |
14 Si Кремний |
15 P Фосфор |
16 S Сера |
17 Cl Хлор |
18 Ar Аргон |
||||||||||
| 4 |
19 K Калий |
20 Ca Кальций |
21 Sc Скандий |
22 Ti Титан |
23 V Ванадий |
24 Cr Хром |
25 Mn Марганец |
26 Fe Железо |
27 Co Кобальт |
28 Ni Никель |
29 Cu Медь |
30 Zn Цинк |
31 Ga Галлий |
32 Ge Германий |
33 As Мышьяк |
34 Se Селен |
35 Br Бром |
36 Kr Криптон |
| 5 |
37 Rb Рубидий |
38 Sr Стронций |
39 Y Иттрий |
40 Zr Цирконий |
41 Nb Ниобий |
42 Mo Молибден |
(43) Tc Технеций |
44 Ru Рутений |
45 Rh Родий |
46 Pd Палладий |
47 Ag Серебро |
48 Cd Кадмий |
49 In Индий |
50 Sn Олово |
51 Sb Сурьма |
52 Te Теллур |
53 I Иод |
54 Xe Ксенон |
| 6 |
55 Cs Цезий |
56 Ba Барий |
* |
72 Hf Гафний |
73 Ta Тантал |
74 W Вольфрам |
75 Re Рений |
76 Os Осмий |
77 Ir Иридий |
78 Pt Платина |
79 Au Золото |
80 Hg Ртуть |
81 Tl Таллий |
82 Pb Свинец |
83 Bi Висмут |
(84) Po Полоний |
(85) At Астат |
86 Rn Радон |
| 7 |
87 Fr Франций |
88 Ra Радий |
** |
(104) Rf Резерфордий |
(105) Db Дубний |
(106) Sg Сиборгий |
(107) Bh Борий |
(108) Hs Хассий |
(109) Mt Мейтнерий |
(110) Ds Дармштадтий |
(111) Rg Рентгений |
(112) Cp Коперниций |
(113) Uut Унунтрий |
(114) Uuq Унунквадий |
(115) Uup Унунпентий |
(116) Uuh Унунгексий |
(117) Uus Унунсептий |
(118) Uuo Унуноктий |
| 8 |
(119) Uue Унуненний |
(120) Ubn Унбинилий |
||||||||||||||||
| Лантаноиды * |
57 La Лантан |
58 Ce Церий |
59 Pr Празеодим |
60 Nd Неодим |
(61) Pm Прометий |
62 Sm Самарий |
63 Eu Европий |
64 Gd Гадолиний |
65 Tb Тербий |
66 Dy Диспрозий |
67 Ho Гольмй |
68 Er Эрбий |
69 Tm Тулий |
70 Yb Иттербий |
71 Lu Лютеций |
|||
| Актиноиды ** |
89 Ac Актиний |
90 Th Торий |
91 Pa Протактиний |
92 U Уран |
(93) Np Нептуний |
(94) Pu Плутоний |
(95) Am Америций |
(96) Cm Кюрий |
(97) Bk Берклий |
(98) Cf Калифорний |
(99) Es Эйнштейний |
(100) Fm Фермий |
(101) Md Менделевий |
(102) No Нобелей |
(103) Lr Лоуренсий |
|||
| Щелочные металлы | Щёлочноземельные металлы | Лантаноиды | Актиноиды | Переходные металлы |
| Лёгкие металлы | Полуметаллы | Неметаллы | Галогены | Инертные газы |
Натрий – информация об элементе, свойства и использование
Перейти к основному содержанию
У вас не включен JavaScript. Пожалуйста, включите JavaScript, чтобы получить доступ ко всем функциям сайта.
Пожалуйста, включите JavaScript, чтобы получить доступ ко всем функциям сайта.
Перейти к магнию >
| Группа | 1 | Температура плавления | 97,794 ° С, 208,029 ° F, 370,944 К |
| Период | 3 | Точка кипения | 882,940°С, 1621,292°F, 1156,090 К |
| Блок | с | Плотность (г см −3 ) | 0,97 |
| Атомный номер | 11 | Относительная атомная масса | 22. 990 990 |
| Состояние при 20°C | Твердый | Ключевые изотопы | 23 Нет |
| Электронная конфигурация | [Ne] 3s 1 | Номер КАС | 7440-23-5 |
| ChemSpider ID | 4514534 | ChemSpider — бесплатная база данных химической структуры. | |
Две линии в круге представляют натрий и являются одним из символов элемента, разработанным Джоном Дальтоном в XIX веке.век. Оранжевое свечение похоже на цвет уличного освещения натрия, а символ «вспышка» с шипами отражает высокую реакционную способность элемента.
Натрий — мягкий металл, который тускнеет в течение нескольких секунд после контакта с воздухом. Он также бурно реагирует с водой.
Натрий используется в качестве теплообменника в некоторых ядерных реакторах и в качестве реагента в химической промышленности. Но соли натрия имеют больше применений, чем сам металл.
Наиболее распространенным соединением натрия является хлорид натрия (поваренная соль). Его добавляют в пищу и используют для размораживания дорог зимой. Он также используется в качестве сырья для химической промышленности.
Карбонат натрия (стиральная сода) также является полезной натриевой солью.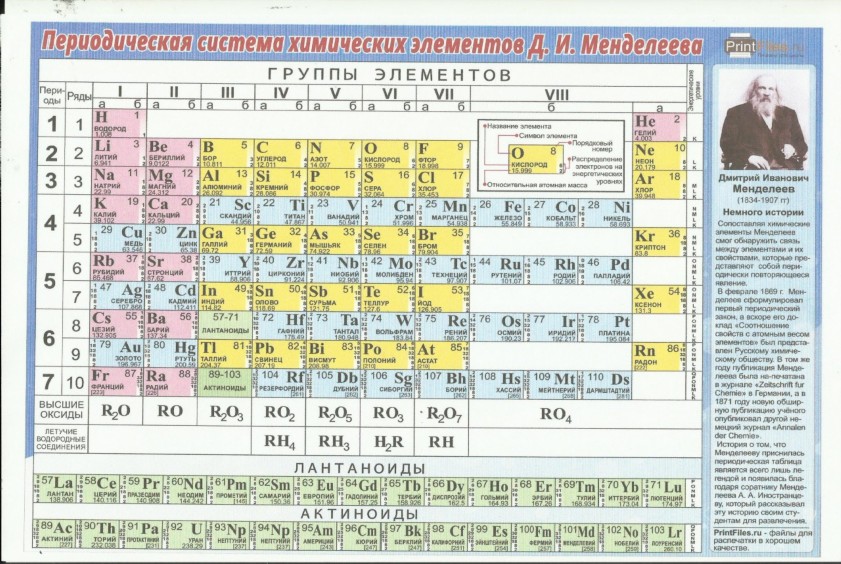 Используется как смягчитель воды.
Используется как смягчитель воды.
Натрий необходим всем живым существам, и люди знали об этом с доисторических времен. В нашем организме содержится около 100 граммов, но мы постоянно теряем натрий разными путями, поэтому нам необходимо восполнить его. Мы можем получить весь необходимый нам натрий из пищи, не добавляя ничего лишнего. В среднем человек съедает около 10 граммов соли в день, но на самом деле нам нужно всего около 3 граммов. Любой дополнительный натрий может способствовать повышению кровяного давления. Натрий важен для многих различных функций человеческого организма. Например, он помогает клеткам передавать нервные сигналы и регулировать уровень воды в тканях и крови.
Натрий является шестым наиболее распространенным элементом на Земле и составляет 2,6% земной коры. Наиболее распространенным соединением является хлорид натрия. Эта хорошо растворимая соль выщелачивалась в океаны на протяжении всей жизни планеты, но многие соляные залежи или «озера» находятся там, где испарились древние моря. Он также содержится во многих минералах, включая криолит, цеолит и содалит.
Он также содержится во многих минералах, включая криолит, цеолит и содалит.
Поскольку натрий настолько реактивен, он никогда не встречается в природе как металл. Металлический натрий получают электролизом сухого расплавленного хлорида натрия.
Элементы и история периодической таблицы
Соль (хлорид натрия, NaCl) и сода (карбонат натрия, Na 2 CO 3 ) были известны с доисторических времен, первая использовалась в качестве ароматизатора и консерванта, а вторая для производства стекла. Соль получали из морской воды, а соду — из долины Натрон в Египте или из пепла некоторых растений. Их состав обсуждался ранними химиками, и решение, наконец, пришло из Королевского института в Лондоне в октябре 1807 года, где Хамфри Дэви подверг едкий натр (гидроксид натрия, NaOH) электрическому току и получил глобулы металлического натрия, как он это сделал ранее. для калия, хотя ему нужно было использовать более сильный ток.
В следующем году Луи-Жозеф Гей-Люссак и Луи-Жак Тенар получили натрий, нагрев до красного каления смесь едкого натра и железных опилок.
| Атомный радиус, несвязанный (Å) | 2,27 | Ковалентный радиус (Å) | 1,60 |
| Сродство к электрону (кДж моль −1 ) | 52,867 | Электроотрицательность (шкала Полинга) | 0,93 |
| Энергии ионизации (кДж моль −1 ) | 1 ст 495. 2 -й 4562.444 3 рд 6910,28 4 -й 9543,36 5 -й 13353,6 6 -й 16612,85 7 -й 20117. 8 -й 25496,25 | ||
| Общие степени окисления | 1 | ||||
| Изотопы | Изотоп | Атомная масса | Естественное изобилие (%) | Период полураспада | Режим распада |
| 23 Нет | 22.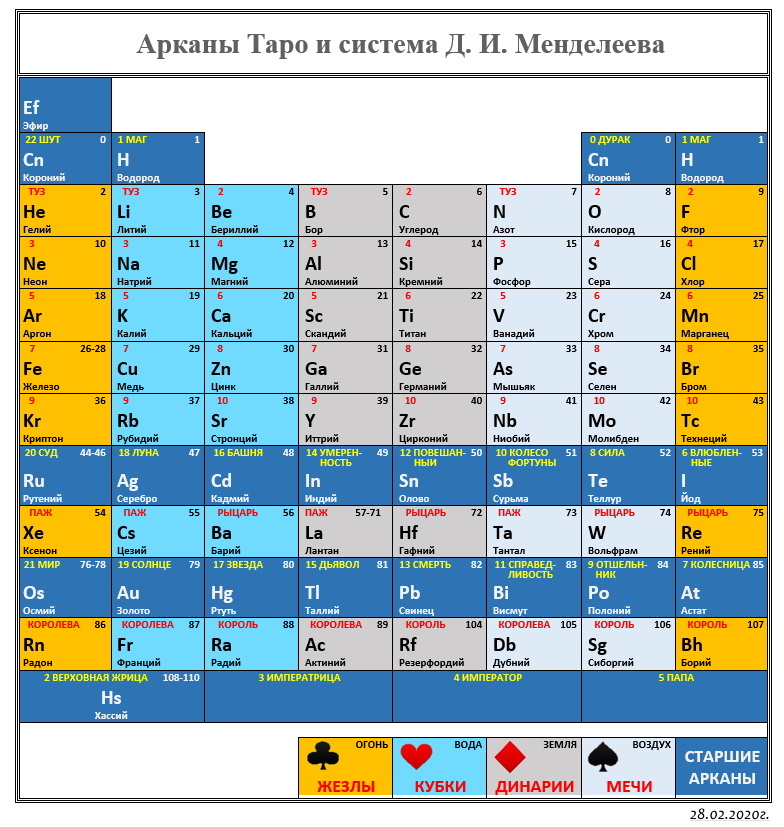 990 990 | 100 | – | – | |
|
|
| Удельная теплоемкость (Дж кг -1 К -1 ) | 1228 | Модуль Юнга (ГПа) | Неизвестный | |||||||||||
| Модуль сдвига (ГПа) | Неизвестный | Объемный модуль (ГПа) | 6.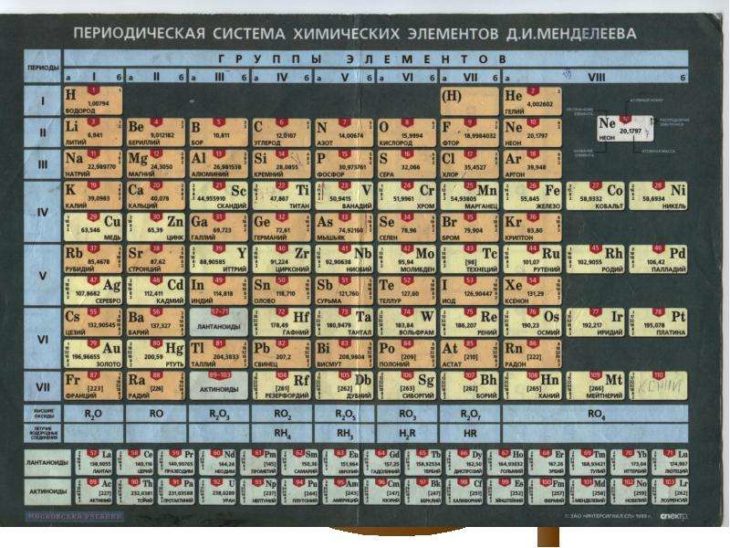 3 3 | |||||||||||
| Давление пара | ||||||||||||||
| Температура (К) |
| |||||||||||||
| Давление (Па) |
| |||||||||||||
| Слушайте подкаст натрия |
Стенограмма: (Promo) Вы слушаете Химию в ее стихии, представленную вам Chemistry World , журнал Королевского химического общества. (Конец промо) Мира Сентилингам На этой неделе важный элемент с раздвоением личности. Вот Дэвид Рид. Дэвид Рид Можно сказать, что натрий, как и большинство элементов в периодической таблице, обладает раздвоением личности. С одной стороны, это необходимое питательное вещество для большинства живых существ, и все же, благодаря своей реактивной природе, оно также способно нанести ущерб, если вы соедините его с чем-то, чего не следует делать. Как таковой натрий встречается в природе только в виде соединений и никогда в виде свободного элемента. Несмотря на это, он очень распространен, составляя около 2,6% земной коры по весу. Его наиболее распространенные соединения включают растворенный хлорид натрия (или поваренную соль), его твердую форму, галит и катион, уравновешивающий заряд в цеолитах. Помимо того, что это важное питательное вещество, история человека и натрия, как говорят, началась еще во времена фараонов в Древнем Египте, с первого письменного упоминания о соединении натрия в виде иероглифов. Однако в средневековой Европе карбонат натрия также использовался как лекарство от головной боли, поэтому он получил название sodanum от арабского suda, что означает головная боль. Именно эта терминология вдохновила сэра Хамфри Дэви назвать элемент натрием, когда он впервые выделил его, пропуская электрический ток через едкий натр или гидроксид натрия в 1807 году. Этот процесс известен как электролиз, и, используя его, Дэви продолжил выделение элементарного калий, кальций, магний и барий очень похожим методом. Учителя химии часто путают детей, рассказывая им о химических символах. В то время как H, N, C и O кажутся совершенно логичными, сокращение натрия до Na поначалу кажется нелогичным. Однако если мы рассмотрим слово натрон, то увидим, откуда взялась сокращенная форма. При выделении в металлической форме серебристо-белый натрий является агрессивным элементом, немедленно окисляющимся при контакте с воздухом и бурно выделяющим газообразный водород, который может воспламениться при контакте с водой. Это один из высокореакционноспособных элементов первой группы, которые называют щелочными металлами. Как и другие щелочные металлы, он имеет очень характерный тест на пламя – ярко-оранжевый цвет в D-линии излучения. Это то, что вы видели во всех застроенных районах в виде уличных фонарей, в которых используется натрий для получения неестественного желтого света, омывающего наши улицы. Этот эффект был впервые отмечен в 1860 году Кирхгофом и Бунзеном, известными как Bunsen Burner. Почти все молодые химики в какой-то момент проводят испытание пламенем, и хлорид натрия является популярным выбором. К сожалению, интенсивность цвета такова, что если какое-либо соединение прольется в горелку Бунзена, оно обречено гореть синим и оранжевым пятнистым пламенем, казалось бы, вечно. Реакция натрия с водой — любимая демонстрация, и в Интернете полно роликов с ней. Применение натрия и его соединений настолько разнообразно, что здесь невозможно перечислить их все. Пара примеров включает в себя тот факт, что натрий используется для охлаждения ядерных реакторов, поскольку он не кипит, как вода, при высоких температурах. достигнуты. Гидроксид натрия можно использовать для удаления серы из бензина и дизельного топлива, хотя образующийся токсичный бульон из побочных продуктов привел к тому, что этот процесс объявлен вне закона в большинстве стран. Гидроксид натрия также используется в производстве биодизельного топлива и в качестве ключевого компонента продуктов, удаляющих засоры из канализации. Пищевая сода на самом деле содержит натрий (это указано в названии!), и ее химическое название — бикарбонат натрия, и я уверен, что вы сталкивались с ним при выпечке или приготовлении пищи, где он подвергается термическому разложению при температуре выше 70°C с выделением углерода. диоксид – который затем заставляет ваше тесто подниматься. Однако именно в виде иона натрий становится действительно важным. Среднестатистическому человеку необходимо потреблять около двух граммов натрия в день, и практически все это будет поступать в виде соли с пищей. Ионы натрия используются для создания электрических градиентов при возбуждении нейронов в головном мозге. При этом натрий (и его старший брат калий) диффундирует через клеточные мембраны. Натрий диффундирует внутрь и откачивается обратно, в то время как калий совершает обратное путешествие. На это может уйти огромное количество энергии тела — иногда до 40 процентов. Я хотел бы закончить короткой историей, в которой подчеркивается двойственность натрия. Мира Сентилингам Это был Дэвид Рид из Саутгемптонского университета с двуличной химией натрия. На следующей неделе химический эквивалент обнаружения поезда. Брайан Клегг Легко обвинить ученых, производящих новые, очень тяжелые элементы, в том, что они следят за движением поездов в химии. Мира Сентилингам А чтобы узнать, почему элемент 114 стоит затраченных усилий, присоединяйтесь к Брайану Клеггу на следующей неделе в программе «Химия в своей стихии». (Promo) Химия в ее стихии представлена вам Королевским химическим обществом и произведена thenakedscientists.com. Дополнительную информацию и другие эпизоды химии в ее стихии можно найти на нашем веб-сайте chemistryworld.org/elements. (Конец акции) |
Нажмите здесь, чтобы посмотреть видео о натрии
Learn Chemistry: ваш единственный путь к сотням бесплатных учебных ресурсов по химии.
Изображения и видео Visual Elements
© Murray Robertson 1998-2017.
W. M. Haynes, ed., CRC Handbook of Chemistry and Physics , CRC Press/Taylor and Francis, Boca Raton, FL, 95th Edition, Internet Version 2015, по состоянию на декабрь 2014 г. 1 905 & Chemical Constants, Kaye & Laby Online, 16-е издание, 1995 г. Версия 1.0 (2005 г.), по состоянию на декабрь 2014 г.
Дж. С. Курси, Д. Дж. Шваб, Дж. Дж. Цай и Р. А. Драгосет, Атомные веса и изотопные композиции (версия 4.1) , 2015 г., Национальный институт стандартов и технологий, Гейтерсбург, Мэриленд, по состоянию на ноябрь 2016 г.
TL Cottrell, The Strengths of Chemical Bonds , Butterworth, London, 1954.
John Emsley, Nature’s Building Blocks: An AZ Guide to the Elements , Oxford University Press, New York, 2nd, New York, 2nd.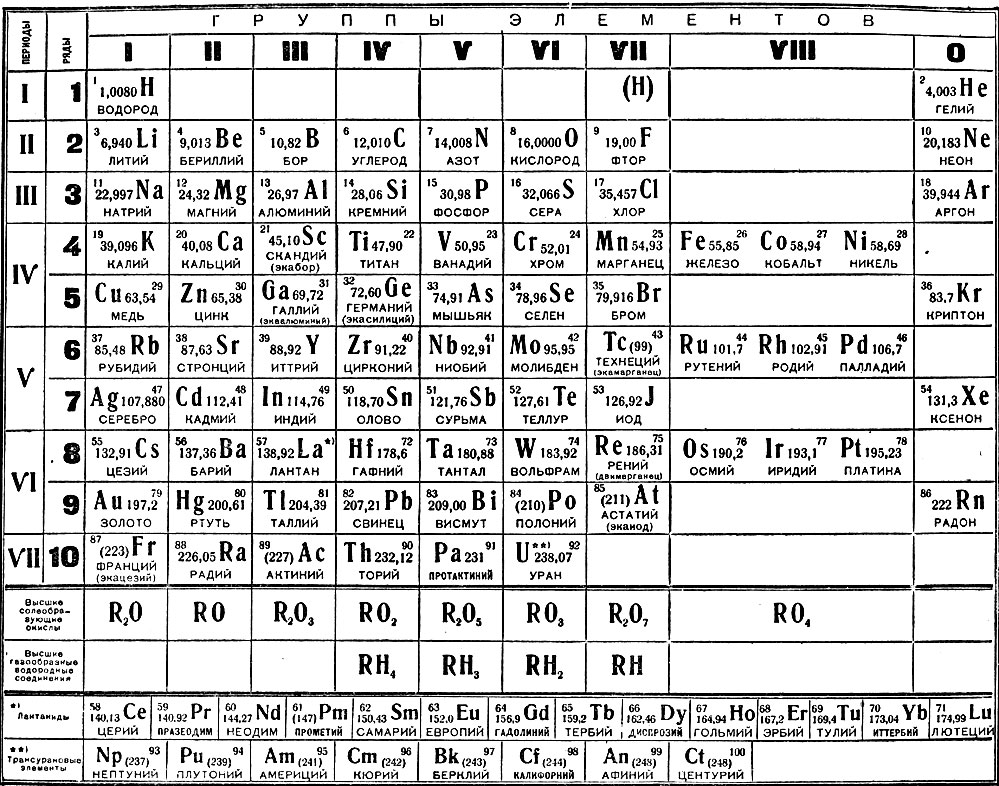 Издание 2011 г.
Издание 2011 г.
Национальный ускорительный центр Томаса Джефферсона — Управление научного образования, It’s Elemental — The Periodic Table of Elements, по состоянию на декабрь 2014 г.
Периодическая таблица видео, по состоянию на декабрь 2014 г.
Частично получены из материалов, предоставленных Британской геологической службой © NERC.
Исторический текст
Элементы 1-112, 114, 116 и 117 © Джон Эмсли 2012. Элементы 113, 115, 117 и 118 © Королевское общество химии 2017.
Podcasts
, созданные The Nake Scients Scientists. .
Создано видеожурналистом Брэди Хараном, работающим с химиками Ноттингемского университета.
Загрузите наше бесплатное приложение Периодической таблицы для мобильных телефонов и планшетов.
Исследуйте все элементы
натрий | Факты, использование и свойства
натрий
Посмотреть все СМИ
- Ключевые люди:
- сэр Хамфри Дэви Жозеф-Луи Гей-Люссак Рудольф Фиттиг
- Похожие темы:
- химический элемент щелочной металл дефицит натрия натрий-24 натрий-22
Просмотреть весь связанный контент →
Резюме
Прочтите краткий обзор этой темы
натрий (Na) , химический элемент группы щелочных металлов (группа 1 [Ia]) периодической таблицы. Натрий — очень мягкий серебристо-белый металл. Натрий является наиболее распространенным щелочным металлом и шестым по распространенности элементом на Земле, составляющим 2,8 процента земной коры. Он широко встречается в природе в соединениях, особенно в поваренной соли — хлориде натрия (NaCl), который образует минерал галит и составляет около 80% растворенных компонентов морской воды.
| atomic number | 11 |
|---|---|
| atomic weight | 22.9898 |
| melting point | 97.81 °C (208 °F) |
| boiling point | 882.9 °C ( 1,621 °F) |
| specific gravity | 0.971 (20 °C) |
| oxidation states | +1, −1 (rare) |
| electron configuration | 2-8-1 or 1 S 2 2 S 2 2 P 6 3 S 1 |
3. состояние в земной коре. В 1807 году сэр Хамфри Дэви первым получил натрий в его элементарной форме, применив электролиз к расплавленному гидроксиду натрия (NaOH). Натрий является важным компонентом ряда силикатных материалов, таких как полевые шпаты и слюды.
 В разных частях света имеются огромные залежи каменной соли, а в Чили и Перу — месторождения нитрата натрия. Содержание натрия в море составляет примерно 1,05%, что соответствует концентрации примерно 3% галогенидов натрия. Натрий идентифицирован как в атомарной, так и в ионной формах в спектрах звезд, в том числе Солнца, и в межзвездной среде. Анализ метеоритов показывает, что присутствующий силикатный материал имеет среднее содержание примерно 4,6 атома натрия на каждые 100 атомов кремния.
В разных частях света имеются огромные залежи каменной соли, а в Чили и Перу — месторождения нитрата натрия. Содержание натрия в море составляет примерно 1,05%, что соответствует концентрации примерно 3% галогенидов натрия. Натрий идентифицирован как в атомарной, так и в ионной формах в спектрах звезд, в том числе Солнца, и в межзвездной среде. Анализ метеоритов показывает, что присутствующий силикатный материал имеет среднее содержание примерно 4,6 атома натрия на каждые 100 атомов кремния.Легче воды, натрий можно резать ножом при комнатной температуре, но он становится хрупким при низких температурах. Он легко проводит тепло и электричество и проявляет фотоэлектрический эффект (испускание электронов при воздействии света) в заметной степени.
Натрий является наиболее коммерчески важным щелочным металлом. Большинство процессов производства натрия включают электролиз расплавленного хлорида натрия. Недорогой и доступный в автоцистернах элемент используется для производства присадок к бензину, полимеров, таких как нейлон и синтетический каучук, фармацевтических препаратов и ряда металлов, таких как тантал, титан и кремний.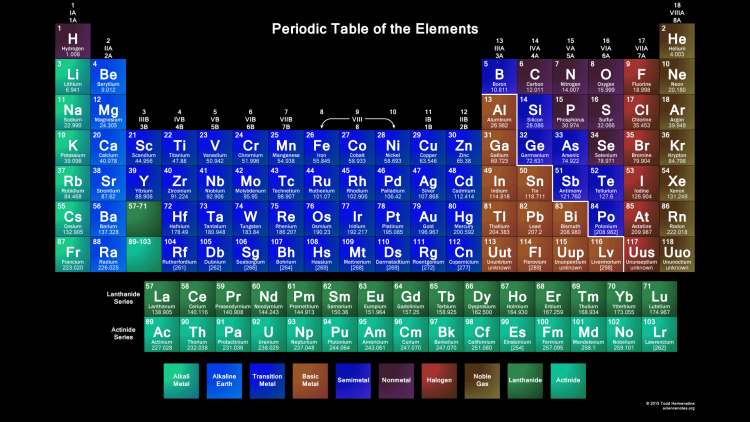 Он также широко используется в качестве теплообменника и в натриевых лампах. Желтый цвет натриевой лампы и натриевого пламени (основа аналитического теста для натрия) определяется двумя заметными линиями в желтой части светового спектра.
Он также широко используется в качестве теплообменника и в натриевых лампах. Желтый цвет натриевой лампы и натриевого пламени (основа аналитического теста для натрия) определяется двумя заметными линиями в желтой части светового спектра.
Викторина “Британника”
Так много химии, так мало времени Викторина
Какой французский химик первым выделил кодеин? Кому приписывают открытие урана? Проверьте свои знания. Пройди тест.
Существенные области применения
Два из первых применений металлического натрия были в производстве цианида натрия и пероксида натрия. Значительные количества тетраэтилсвинца использовались в качестве присадки к бензину, но этот рынок исчез с появлением неэтилированного бензина. Значительные количества натрия используются в производстве алкилсульфатов натрия в качестве основного ингредиента синтетических моющих средств.
Натрий также используется в качестве исходного материала при производстве гидрида натрия (NaH) и боргидрида натрия (NaBH 4 ). Кроме того, натрий используется в производстве красителей и их промежуточных продуктов, в синтезе отдушек и в различных органических восстановителях. Он используется при очистке углеводородов и при полимеризации ненасыщенных углеводородов. Во многих органических применениях натрий используется в виде дисперсий в жидких углеводородных средах.
Кроме того, натрий используется в производстве красителей и их промежуточных продуктов, в синтезе отдушек и в различных органических восстановителях. Он используется при очистке углеводородов и при полимеризации ненасыщенных углеводородов. Во многих органических применениях натрий используется в виде дисперсий в жидких углеводородных средах.
Оформите подписку Britannica Premium и получите доступ к эксклюзивному контенту. Подпишитесь сейчас
Расплавленный натрий является отличным теплоносителем, и благодаря этому свойству он нашел применение в качестве теплоносителя в жидкометаллических реакторах-размножителях на быстрых нейтронах. Натрий широко используется в металлургии в качестве раскислителя и восстановителя для получения кальция, циркония, титана и других переходных металлов. Промышленное производство титана включает восстановление тетрахлорида титана (TiCl 4 ) с натрием. Продукты представляют собой металлический Ti и NaCl.
Основные соединения
Натрий обладает высокой реакционной способностью, образуя широкий спектр соединений почти со всеми неорганическими и органическими анионами (отрицательно заряженными ионами). Обычно он имеет степень окисления +1, и его единственный валентный электрон легко теряется, образуя бесцветный катион натрия (Na + ). Также были синтезированы соединения, содержащие анион натрия Na – . Основными коммерческими соединениями натрия являются хлорид, карбонат и сульфат.
Обычно он имеет степень окисления +1, и его единственный валентный электрон легко теряется, образуя бесцветный катион натрия (Na + ). Также были синтезированы соединения, содержащие анион натрия Na – . Основными коммерческими соединениями натрия являются хлорид, карбонат и сульфат.
Наиболее важным и известным соединением натрия является хлорид натрия, или поваренная соль, NaCl. Большинство других соединений натрия получают прямо или косвенно из хлорида натрия, который содержится в морской воде, в природных рассолах и в виде каменной соли. Большие количества хлорида натрия используются в производстве других тяжелых (промышленных) химикатов, а также используются непосредственно для удаления льда и снега, для кондиционирования воды и в продуктах питания.
Другие основные коммерческие применения хлорида натрия включают его использование в производстве хлора и гидроксида натрия путем электролитического разложения и в производстве карбоната натрия (Na 2 CO 3 ) по методу Solvay.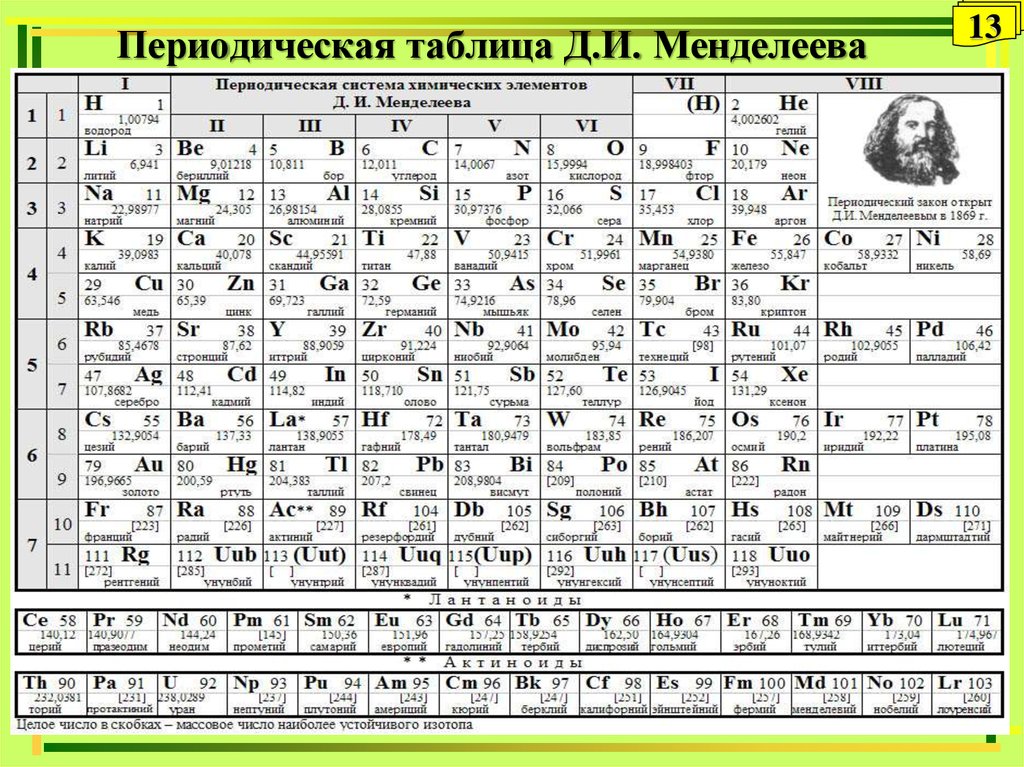 Электролиз водного хлорида натрия дает гипохлорит натрия, NaOCl, соединение натрия, кислорода и хлора, используемое в больших количествах в бытовых хлорных отбеливателях. Гипохлорит натрия также используется в качестве промышленного отбеливателя для бумажной массы и текстиля, для хлорирования воды и в некоторых лекарственных препаратах в качестве антисептика и фунгицида. Это нестабильное соединение известно только в водном растворе.
Электролиз водного хлорида натрия дает гипохлорит натрия, NaOCl, соединение натрия, кислорода и хлора, используемое в больших количествах в бытовых хлорных отбеливателях. Гипохлорит натрия также используется в качестве промышленного отбеливателя для бумажной массы и текстиля, для хлорирования воды и в некоторых лекарственных препаратах в качестве антисептика и фунгицида. Это нестабильное соединение известно только в водном растворе.
Карбонаты содержат карбонат-ион (CO 3 2– ). Бикарбонат натрия, также называемый гидрокарбонатом натрия или бикарбонатом соды, NaHCO 3 , является источником двуокиси углерода и поэтому используется в качестве ингредиента разрыхлителей, шипучих солей и напитков, а также в качестве основного компонента сухих напитков. химические огнетушители. Его легкая щелочность делает его полезным при лечении повышенной кислотности желудка или мочевыводящих путей и ацидоза. Он также используется в некоторых промышленных процессах, таких как дубление и подготовка шерсти. Карбонат натрия, или кальцинированная сода, Na 2 CO 3 , широко распространен в природе, встречается в составе минеральных вод и в виде твердых минералов натрона, трона и термонатрита. Большие количества этой щелочной соли используются в производстве стекла, моющих и чистящих средств. Карбонат натрия обрабатывают двуокисью углерода с получением бикарбоната натрия. Моногидрат карбоната натрия Na 2 CO 3 · H 2 O широко используется в фотографии в качестве компонента проявителей.
Карбонат натрия, или кальцинированная сода, Na 2 CO 3 , широко распространен в природе, встречается в составе минеральных вод и в виде твердых минералов натрона, трона и термонатрита. Большие количества этой щелочной соли используются в производстве стекла, моющих и чистящих средств. Карбонат натрия обрабатывают двуокисью углерода с получением бикарбоната натрия. Моногидрат карбоната натрия Na 2 CO 3 · H 2 O широко используется в фотографии в качестве компонента проявителей.
Сульфат натрия, Na 2 SO 4 , представляет собой белое кристаллическое твердое вещество или порошок, используемый в производстве крафт-бумаги, картона, стекла и моющих средств, а также в качестве сырья для производства различных химикатов. Его получают либо из месторождений сульфатно-натриевых минералов мирабилита и тенардита, либо синтетически путем обработки хлорида натрия серной кислотой. Кристаллизованный продукт представляет собой гидрат Na 2 SO 4 · 10H 2 O, широко известный как глауберова соль.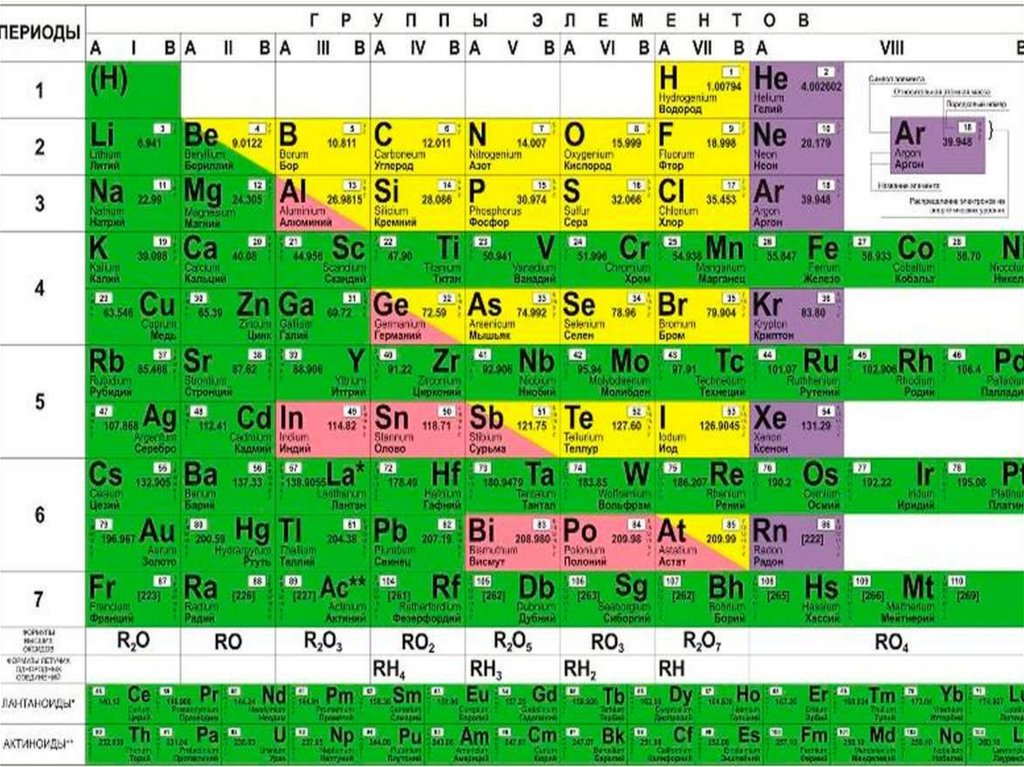 Тиосульфат натрия (гипосульфит натрия), Na 2 S 2 O 3 , используется фотографами для фиксации проявленных негативов и отпечатков; он действует, растворяя часть солей серебра, нанесенных на пленку, которые остаются неизменными под воздействием света.
Тиосульфат натрия (гипосульфит натрия), Na 2 S 2 O 3 , используется фотографами для фиксации проявленных негативов и отпечатков; он действует, растворяя часть солей серебра, нанесенных на пленку, которые остаются неизменными под воздействием света.
Гидроксид натрия (NaOH) представляет собой едкое белое кристаллическое твердое вещество, которое легко поглощает влагу до тех пор, пока не растворится. Гидроксид натрия, обычно называемый едким натром или щелочью, является наиболее широко используемой промышленной щелочью. Он сильно разъедает ткани животных и растений. Щелочные растворы, которые он образует при растворении в воде, нейтрализуют кислоты в различных промышленных процессах: при переработке нефти он удаляет серную и органические кислоты; в мыловарении реагирует с жирными кислотами. Растворы NaOH используются при обработке целлюлозы и в производстве многих химических веществ.
Натриевая селитра, или натриевая селитра, NaNO 3 , обычно называемая чилийской селитрой, в честь месторождений полезных ископаемых в северной части Чили, основного источника. Нитрат натрия используется как азотное удобрение и как компонент динамита.
Нитрат натрия используется как азотное удобрение и как компонент динамита.
Соленый элемент Натрий | Периодическая таблица
Введение в натрий
Элемент натрий представляет собой мягкий легковоспламеняющийся металл серебристо-белого цвета. Натрий, названный в честь английского слова «soda», имеет соединения, которые обычно используются в нашей повседневной жизни. Возможно, вы знакомы с поваренной солью, которая представляет собой NaCl (хлорид натрия), соединение натрия. Это один из самых активных металлов в периодической таблице.
Десять интересных и забавных фактов о натрии
- Ежемесячное довольствие римских солдат называлось « salarium », где « sal » на латыни означает соль. То есть римским солдатам часто платили солью, которая в то время считалась весьма ценной.
- Натрий — шестой по распространенности элемент на Земле.
- Интересно, что 0,15% вашего тела составляет натрий.
- Плотность натрия ниже, чем у воды.

- Элемент натрия составляет 2,6% земной коры.
- Нож может легко разрезать металл натрия.
- Натрий имеет только один стабильный изотоп.
- Латинское название карбоната натрия: « natrium ». Таким образом, символ элемента натрия « Na » происходит от этого слова.
- Исследователи пытаются узнать о разном содержании натрия в разных звездах, чтобы предсказать их эволюцию.
- Большое количество натрия было сброшено в озеро взрывным способом после Второй мировой войны (https://www.youtube.com/watch?v=HY7mTCMvpEM).
Натрий в периодической таблице
Натрий, атомный символ Na, имеет атомный номер одиннадцать и находится в группе 1 в периодической таблице, ниже лития и слева от магния. Этот элемент относится к семейству щелочных металлов и имеет только один валентный электрон. Следовательно, это очень активный элемент. Кроме того, натрий легко связывается с любым элементом, которому нужен один электрон.
Натрий имеет электроотрицательность 0,93 (шкала Полинга). Натрий электронная конфигурация равна 1s 2 2s 2 2p 6 3s 1 . К другим элементам семейства щелочных металлов относятся: калий, литий, цезий и рубидий. Кроме того, говоря о калии, натрий и химические калия и физические свойства очень похожи.
Натрий электронная конфигурация равна 1s 2 2s 2 2p 6 3s 1 . К другим элементам семейства щелочных металлов относятся: калий, литий, цезий и рубидий. Кроме того, говоря о калии, натрий и химические калия и физические свойства очень похожи.
Элемент натрия в нашем организме
Элемент натрия чрезвычайно важен для нашего организма. Он действует как электролит и минерал, который регулирует жидкость в наших клетках. Натрий также поддерживает наши нервные функции, движение мышц и электролитный баланс. Более того, этот натрий поступает в наш организм при употреблении пищевых продуктов, а выходит в виде пота/мочеиспускания. Во время этого «цикла» наша кровь/лимфа хранит натрий. Кроме того, если этот натрий достигает нездорового уровня, то наш организм реагирует на это изменение – иногда в виде диареи, недоедания или гипонатриемии/гипернатриемии. Следовательно, очень важно, чтобы мы следили за уровнем натрия в нашем организме, регулируя свой рацион.
Сплавы элемента натрия
Натрий образует сплавы с несколькими элементами, включая калий, кальций и свинец. Давайте обсудим несколько сплавов и их использование/свойства. Начнем с того, что сплав натрия и калия (NaK) используется в различных процессах (например, NaK действует как теплоноситель, восстановитель и катализатор). Этот сплав, называемый NaK , обычно жидкий при комнатной температуре, опасно вступает в реакцию с водой и воздухом. В дальнейшем натрий также присутствует в тройном сплаве, содержащем калий и цезий (NaKCs), и в амальгаме натрия, сплаве натрия и ртути. Амальгама натрия действует как восстановитель в водных суспензиях.
Применение натрия в современном мире
Для чего используется натрий?
Натрий как теплообменник
Теплообменники — это устройства, передающие тепло из одного места в другое. Натрий является часто встречающимся теплообменником на атомных электростанциях. Кроме того, задача натрия состоит в том, чтобы отводить тепло от реакторов этих заводов и передавать его в систему водоснабжения, которая использует это тепло для производства пара и выработки электроэнергии.
Использование натрия для производства других материалов
Соединения натрия используются для производства различных материалов. Во-первых, они используются для производства бумаги. В процессе изготовления бумаги гидроксид натрия обрабатывает/разделяет волокна на этапе вытягивания. Во-вторых, они используются для производства прозрачного стекла. В этом процессе мы нагреваем карбонат натрия с оксидом кальция. В-третьих, соединения натрия используются при создании различных металлов. Например, натрий в сочетании с тетрахлоридом титана дает металлический титан. В другой реакции натрий является катализатором для создания искусственного каучука. Точно так же существуют другие материалы (например, продукты питания и удобрения), в производстве/использовании которых используется натрий.
Элемент натрия в натриевых лампах
Натриевые лампы излучают желтое монохроматическое свечение, которое освещает уличные фонари. Эти лампы содержат электроды, металлический натрий и формы неона и аргона. Когда ток проходит через ионизированный неон и аргон, металлический натрий испаряется, а натрий ионизируется, создавая блестящее желтое свечение.
Когда ток проходит через ионизированный неон и аргон, металлический натрий испаряется, а натрий ионизируется, создавая блестящее желтое свечение.
Когда и как был открыт натрий?
История натрия
Удивительно, но элемент натрия использовался в доисторические времена по ряду причин. Его соединения используются в ароматизаторах, для облегчения головной боли и в производстве стекла. Эти соединения натрия были получены из различных источников. Например, карбонат натрия получали из пепла особых растений, а хлорид натрия — из морской воды. Излишне говорить, что универсальность натрия привлекла нескольких ученых и химиков к изучению его состава.
Кто открыл натрий?
Одним из таких химиков был сэр Хамфри Дэви , который в 1807 году провел электролиз едкого натра для получения чистого натрия. Эта реакция, питаемая тремя большими батареями, была похожа на реакцию выделения калия.
Где во Вселенной присутствует натрий?
Натрий в больших количествах присутствует на солнце и в звездах. D-линии натрия (спектральные линии) являются одними из самых заметных в солнечном спектре. Они известны как линии Фраунгофера. Натрий является седьмым по распространенности элементом на земле, составляющим около 2,27% земной коры.
D-линии натрия (спектральные линии) являются одними из самых заметных в солнечном спектре. Они известны как линии Фраунгофера. Натрий является седьмым по распространенности элементом на земле, составляющим около 2,27% земной коры.
Электролиз абсолютно сухого расплавленного хлорида натрия является коммерчески предпочтительным методом получения чистого натрия. Этот метод стоит значительно меньше, чем метод, использовавшийся несколько лет назад; в результате в наши дни он более популярен. Старый метод, процесс Кастнера, электролиз гидроксида натрия. Кроме того, минерал галит, содержащий хлорид натрия, присутствует по всей планете.
Химия натрия – соединения, реакции, степени окисления, выделение
Химические свойства натрия Элемент
Натрий очень активен и вступает в реакцию с большинством неметаллов. Следовательно, чтобы избежать этих реакций, мы храним/храним натрий в инертных жидкостях (например, керосине) или в азотной атмосфере. Вот список нескольких реакций, происходящих с натрием:
- Натрий и воздух: при воздействии на натрий вступает в реакцию с кислородом и образует оксид натрия.
 Однако этот оксид натрия быстро прореагирует с водородом, и в результате получится гидроксид натрия. В другом аспекте при сжигании натрия на воздухе образуется пероксид натрия.
Однако этот оксид натрия быстро прореагирует с водородом, и в результате получится гидроксид натрия. В другом аспекте при сжигании натрия на воздухе образуется пероксид натрия. - Натрий реагирует со всеми галогенами с образованием галогенидов натрия. Эти реакции будут производить хлорид натрия, йодид натрия и бромид натрия среди других соединений.
- Натрий будет реагировать с плавиковой и соляной кислотами в очень экзотермических реакциях.
Как натрий реагирует с водой?
Натрий, имеющий один валентный электрон, делает его очень реакционноспособным. При смешивании металлического натрия и воды реакция натрия с водой может быть бурной. Начнем с того, что натрий плавает, если его поместить в воду. Это связано с тем, что плотность натрия ниже плотности воды. Впоследствии произойдет экзотермическая реакция, и образуется раствор гидроксида натрия и газообразного водорода. Эта реакция выделяет столько тепла, что натрий плавится и выделяет водород из добавленной воды. Кроме того, этот выделившийся газообразный водород может загореться.
Кроме того, этот выделившийся газообразный водород может загореться.
Соединения натрия
Элемент натрия легко образует соединения практически с любым анионом. Большинство соединений натрия растворимы в воде. Вот несколько распространенных соединений натрия, их свойства и применение:
Ацетат натрия
- Ацетат натрия, натриевая соль уксусной кислоты, хорошо растворима в воде. Он является источником ионов натрия, приправой к ароматным продуктам и содержится в грелках для рук.
Бензоат натрия
- Это соединение белого цвета без запаха; сочетание гидроксида натрия и бензойной кислоты дает его. Бензоат натрия «распадается» на ионы натрия и бензойной кислоты, если его поместить в воду.
 Это соединение широко присутствует в пищевых консервантах.
Это соединение широко присутствует в пищевых консервантах.
Бикарбонат натрия
- Бикарбонат натрия представляет собой белый кристаллический порошок, твердый при комнатной температуре. Обычно называемая пищевой содой, она имеет несколько применений в качестве антацида. Например, он нейтрализует избыток желудочной кислоты, снимает изжогу и другие болезненные ощущения. Кроме того, щелочная природа бикарбоната натрия позволяет ему реагировать с кислотами, что делает его широко используемым ингредиентом для выпечки и в сухих химических огнетушителях.
Бромид натрия
- Бромид натрия представляет собой белое твердое вещество, которое легко растворяется в воде и имеет различные применения. Он действует как катализатор, реагент, дезинфицирующее средство и источник ионов брома. Кроме того, это соединение образуется в результате реакции между гидроксидом натрия и бромистым водородом. Его нет в природе.
Карбонат натрия
- Карбонат натрия, также называемый «кальцинированной содой», представляет собой белое кристаллическое твердое вещество, растворимое в воде.
 Эта щелочная соль получается из соли и известняка и используется, помимо прочего, в качестве пищевой добавки и чистящего средства. Он также продается как стиральная сода, которая отличается от пищевой соды.
Эта щелочная соль получается из соли и известняка и используется, помимо прочего, в качестве пищевой добавки и чистящего средства. Он также продается как стиральная сода, которая отличается от пищевой соды.
Хлорид натрия
- Хлорид натрия представляет собой белое кристаллическое твердое вещество, легко растворимое в воде. NaCl известен своей функцией на кухне в качестве поваренной соли, придающей вкус пище. Тем не менее, хлорид натрия получают путем очистки морской воды, и его также можно использовать для создания других химических соединений (например, бикарбоната натрия). Узнайте несколько интересных фактов о соли.
Цитрат натрия
- Это соединение представляет собой белый кристаллический порошок. Это подщелачивающее средство.
Фторид натрия
- Это соединение получают путем нейтрализации плавиковой кислоты основаниями (например, гидроксидом натрия). Это белое/зеленое кристаллическое твердое вещество, растворимое в воде.
 Кроме того, это соединение обычно действует как консервант древесины, химический реагент, инсектицид и источник ионов фтора.
Кроме того, это соединение обычно действует как консервант древесины, химический реагент, инсектицид и источник ионов фтора.
Гидроксид натрия
- Это соединение, также называемое «едким натром», является обычным неорганическим основанием. Белое кристаллическое твердое вещество производится электролитическим хлорно-щелочным процессом и имеет множество применений. Например, он может быть консервантом для защиты пищевых продуктов и важным компонентом различных лекарственных средств (например, аспирина), а также мыла/моющих средств.
Гипохлорит натрия
- Гипохлорит натрия представляет собой прозрачный раствор с желтоватым оттенком. Его получают реакцией хлора с раствором гидроксида натрия. Этот распространенный отбеливатель притупляет любые запахи при добавлении в сточные воды.
Йодид натрия
- Йодид натрия представляет собой белый порошок без запаха. Для его получения карбонат натрия реагирует с раствором йодистоводородной кислоты.
 Кроме того, йодид натрия часто действует как реагент в органическом синтезе. И он используется для предотвращения дефицита йода, поскольку он является источником йода.
Кроме того, йодид натрия часто действует как реагент в органическом синтезе. И он используется для предотвращения дефицита йода, поскольку он является источником йода.
Нитрат натрия
- Нитрат натрия (и нитрит натрия) присутствует во многих пищевых консервантах. В частности, они сохраняют определенные виды мяса и сыров.
Фосфаты натрия
- Фосфаты натрия представляют собой группу химических веществ, состоящих из атомов натрия, фосфора и кислорода. Монофосфат натрия создается путем нейтрализации фосфорной кислоты и используется в качестве эмульгатора. Двунатрийфосфат используется для смягчения воды и производится аналогично мононатрийфосфату. Тринатрийфосфат производится, когда гидроксид натрия нейтрализует фосфорную кислоту, и используется для производства химикатов, обезжиривающих материал.
Сульфат натрия
- Сульфат натрия представляет собой белое кристаллическое твердое вещество. Его использование лежит преимущественно в обрабатывающей промышленности.
 Хлорид натрия и серная кислота объединяются, чтобы произвести его. Кроме того, он используется для производства других химикатов, бумаги и стекла.
Хлорид натрия и серная кислота объединяются, чтобы произвести его. Кроме того, он используется для производства других химикатов, бумаги и стекла.
Сульфид натрия
- Сульфид натрия представляет собой бесцветное твердое вещество. В промышленности его производят карботермической реакцией восстановления. Кроме того, это твердое вещество окисляется при нагревании. Кроме того, это соединение используется для растворения лигнина древесных волокон в процессе изготовления бумаги, в производстве резиновых химикатов и в производстве отбеливателей.
Выделение натрия
Натрий обычно получают векторным способом. Однако производство элементарного натрия в небольшой лаборатории чрезвычайно сложно. Однако сделать это с трудом можно, проводя электролиз расплавленного NaCl, но это опасно и трудно восстановить натрий.
Степени окисления натрия
Натрий существует почти исключительно в степени окисления +1. Бесцветный ион натрия – это Na+.
Физические свойства натрия
Натрий настолько мягкий, что его можно резать ножом. Если вы когда-нибудь держите натрий, вы должны надеяться, что он покрыт маслом.
- Symbol: Na
- Melting point: 97.794°C
- Boiling point: 882.940°C
- Density (g cm −3 ): 0.97
- Atomic mass: 22.990
- Atomic number: 11
- Electronegativity (Шкала Полинга): 0,93
- Классификация: Щелочной металл, металл группы I
- Содержание в земной коре (млн): 23600
- Электронная конфигурация: [Ne] 3s1
- Ключевые изотопы: 23 Na
- Содержится в природных минералах: амфибол, цеолит, галит и криолит
- Токсичность: ион натрия, Na + 9005, как правило, нетоксичен3 . Токсичность определяется анионом, присутствующим с натрием.
Где я могу купить элементарный натрий?
Вы можете купить натрий на Amazon, Ebay или в интернет-магазинах, таких как Luciteria.

 845
845 2
2 1
1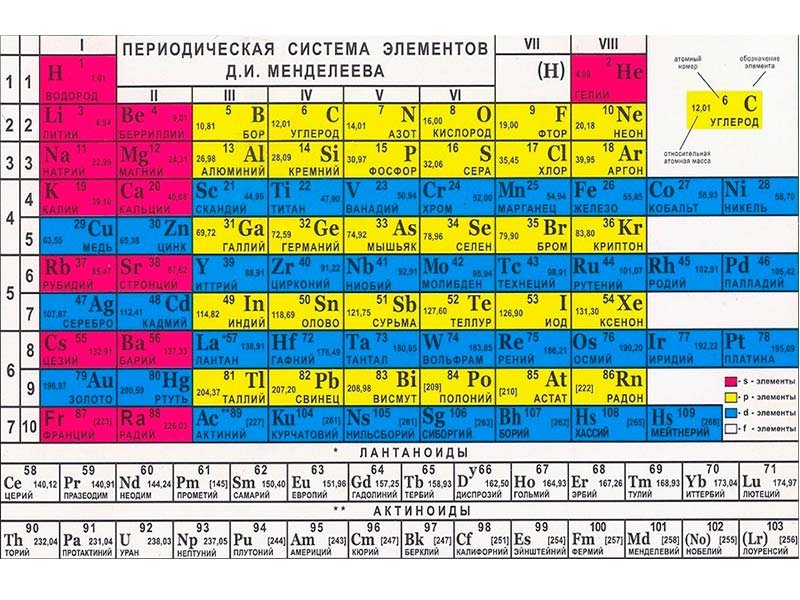
 6
6
 Трудно описать пиктограмму словами, но представьте себе волнистую линию поверх полого глаза, поверх полукруга, а рядом с ними — изображение стервятника, обращенного влево. Эта пиктограмма означала божественный или чистый, и ее название является корнем слова натрон, которое использовалось для обозначения стиральной соды или декагидрата карбоната натрия, как мы знаем его сегодня. Карбонат натрия использовался в мыле, а также в процессе мумификации благодаря его водопоглощающим и убивающим бактерии свойствам регулирования pH.
Трудно описать пиктограмму словами, но представьте себе волнистую линию поверх полого глаза, поверх полукруга, а рядом с ними — изображение стервятника, обращенного влево. Эта пиктограмма означала божественный или чистый, и ее название является корнем слова натрон, которое использовалось для обозначения стиральной соды или декагидрата карбоната натрия, как мы знаем его сегодня. Карбонат натрия использовался в мыле, а также в процессе мумификации благодаря его водопоглощающим и убивающим бактерии свойствам регулирования pH.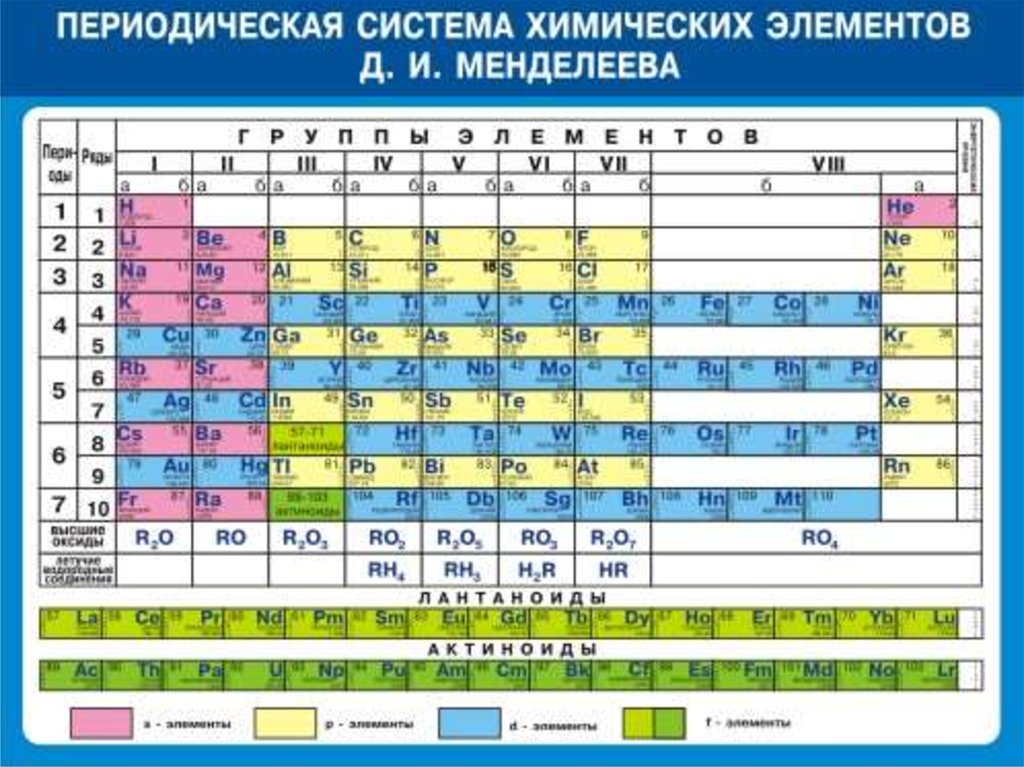

 Один человек купил в Интернете три с половиной фунта металлического натрия и провел вечер, реагируя с водой различных форм и размеров, пока он и его друзья наблюдали за происходящим с безопасного расстояния. Вечеринка явно удалась, но он не предлагает устраивать собственную. На следующий день, когда хозяин вышел на улицу, чтобы проверить чистоту места, где он взорвал натрий, он заметил, что оно было покрыто роями желтых бабочек. Проведя небольшое исследование, он обнаружил, что у этих бабочек есть интересная привычка. Самцы ищут натрий и постепенно собирают его, а позже преподносят своим самкам в качестве ритуала. Итак, это суммирует две стороны натрия. Его агрессивный реактивный характер контрастирует с его использованием влюбчивыми бабочками.
Один человек купил в Интернете три с половиной фунта металлического натрия и провел вечер, реагируя с водой различных форм и размеров, пока он и его друзья наблюдали за происходящим с безопасного расстояния. Вечеринка явно удалась, но он не предлагает устраивать собственную. На следующий день, когда хозяин вышел на улицу, чтобы проверить чистоту места, где он взорвал натрий, он заметил, что оно было покрыто роями желтых бабочек. Проведя небольшое исследование, он обнаружил, что у этих бабочек есть интересная привычка. Самцы ищут натрий и постепенно собирают его, а позже преподносят своим самкам в качестве ритуала. Итак, это суммирует две стороны натрия. Его агрессивный реактивный характер контрастирует с его использованием влюбчивыми бабочками. Подобно тому, как наблюдатели поездов часами высматривают определенный локомотив, чтобы подчеркнуть его в своей книге, может показаться, что эти химики кропотливо производят атом или два сверхтяжелого элемента в качестве упражнения, чтобы поставить галочку. Но элемент 114 преподнес не один сюрприз, показав, почему такие элементы стоит исследовать.
Подобно тому, как наблюдатели поездов часами высматривают определенный локомотив, чтобы подчеркнуть его в своей книге, может показаться, что эти химики кропотливо производят атом или два сверхтяжелого элемента в качестве упражнения, чтобы поставить галочку. Но элемент 114 преподнес не один сюрприз, показав, почему такие элементы стоит исследовать.