Символы химических элементов и принципы их обозначения
Химия, как и любая наука, требует точности. Система представления данных в этой области знаний вырабатывалась столетиями, и актуальный на сегодняшний день стандарт представляет собой оптимизированную структуру, содержащую всю необходимую информацию для дальнейшей теоретической работы с каждым конкретным элементом.
При записи формул и уравнений крайне неудобно использовать целые названия веществ, и сегодня для этой цели используются одна или две буквы – химические символы элементов.
История
В Древнем мире, а также в Средние века ученые применяли символические изображения для обозначения различных элементов, однако эти знаки не были стандартизованы. Лишь к XIII веку предпринимаются попытки систематизации символов веществ и элементов, а с XV века новооткрытые металлы начали обозначаться первыми буквами своих названий. Подобная стратегия наименования применяется в химии до сегодняшнего дня.
Современное состояние системы наименования
На сегодняшний день известно более ста двадцати химических элементов, часть из которых найти в природе крайне проблематично. Неудивительно, что ещё в середине XIX века наука знала о существовании лишь 63 из них, и не существовало ни единой системы наименования, ни цельной системы представления химических данных.
Неудивительно, что ещё в середине XIX века наука знала о существовании лишь 63 из них, и не существовало ни единой системы наименования, ни цельной системы представления химических данных.
Последнюю задачу решил во второй половине того же века русский ученый Д. И. Менделеев, опираясь на неудачные попытки предшественников. Процесс наименования продолжается и сегодня – существует несколько элементов с номерами от 119 и выше, условно обозначенных в таблице латинским сокращением своего порядкового номера. Произношение символов химических элементов этой категории осуществляется по латинским правилам чтения числительных: 119 – унуненний (букв. «сто девятнадцатый»), 120 – унбинилий («сто двадцатый») и так далее.
Большая же часть элементов имеет собственные названия, происходящие от латинских, греческих, арабских, немецких корней, в одних случаях отражающих объективные характеристики веществ, а в других выступающих в качестве ничем не мотивированных символов.
Этимология некоторых элементов
Как было сказано выше, некоторые названия и символы химических элементов базируются на объективно наблюдаемых признаках.
Название фосфора, светящегося в темноте, происходит от греческого словосочетания «нести свет». При переводе на русский язык обнаруживается достаточно много «говорящих» названий: хлор – «зеленоватый», бром – «дурно пахнущий», рубидий – «темно-красный», индий – «цвета индиго». Поскольку химические символы элементов даны латинскими буквами, прямая связь названия с веществом для носителя русского языка обычно остается незамеченной.
Существуют и более тонкие ассоциации при наименовании. Так, название селена происходит от греческого слова, означающего «Луна». Произошло это потому, что в природе данный элемент является спутником теллура, название которого в том же греческом означает «Земля».
Сходным образом назван и ниобий. Согласно древнегреческой мифологии, Ниоба – дочь Тантала. Химический элемент тантал был открыт раньше и по своим свойствам схож с ниобием – таким образом, логическая связь «отец-дочь» была спроецирована на “взаимоотношения” химических элементов.
Более того, своё название тантал получил в честь известного мифологического персонажа не случайно. Дело в том, что получение этого элемента в чистом виде было сопряжено с большими трудностями, благодаря чему ученые и обратились к фразеологизму «Танталовы муки».
Дело в том, что получение этого элемента в чистом виде было сопряжено с большими трудностями, благодаря чему ученые и обратились к фразеологизму «Танталовы муки».
Ещё один любопытый историческиЙ факт заключается в том, что название платины буквально переводится как «серебришко», т. е. нечто похожее, но не такое ценное, как серебро. Причина заключается в том, что данный металл плавится гораздо труднее серебра, а потому долгое время не находил применения и не представлял особой ценности.
Общий принцип наименования элементов
При взгляде на периодическую таблицу первое, что бросается в глаза, – названия и символы химических элементов. Это всегда одна или две латинские буквы, первая из которых – заглавная. Выбор букв обусловлен латинским названием элемента. Несмотря на то что корни слов происходят и из древнегреческого, и из латинского, и из других языков, по стандарту наименования к ним добавляются латинские окончания.
Интересно, что большинство символов носителю русского языка будут интуитивно понятны: алюминий, цинк, кальций или магний школьник легко запоминает с первого раза. Сложнее обстоит дело с теми названиями, которые различаются в русском и латинском варианте. Ученик может далеко не сразу запомнить, что кремний – это силициум, а ртуть – гидраргирум. Тем не менее запомнить это придется – графическое изображение каждого элемента ориентировано на латинское название вещества, которое и будет фигурировать в химических формулах и реакциях как Si и Hg соответственно.
Сложнее обстоит дело с теми названиями, которые различаются в русском и латинском варианте. Ученик может далеко не сразу запомнить, что кремний – это силициум, а ртуть – гидраргирум. Тем не менее запомнить это придется – графическое изображение каждого элемента ориентировано на латинское название вещества, которое и будет фигурировать в химических формулах и реакциях как Si и Hg соответственно.
Чтобы запомнить такие названия, ученикам полезно выполнять упражнения типа: «Установите соответствие между символом химического элемента и его названием».
Иные способы наименования
Наименования некоторых элементов произошли из арабского языка и были «стилизованы» под латынь. Например, натрий получил название от корневой основы, означающей «бурлящее вещество». Арабские корни прослеживаются также у названий калия и циркония.
Своё влияние оказал и немецкий язык. Из него происходят наименования таких элементов, как марганец, кобальт, никель, цинк, вольфрам. Логическая связь при этом не всегда очевидна: например, никель – это сокращение от слова, означающего «медный дьявол».
В редких случаях названия были переведены на русский язык в виде кальки: гидрогениум (буквально «рождающий воду») превратился в водород, а карбонеум – в углерод.
Имена и топонимы
Более десятка элементов названы именами различных ученых, среди которых Альберт Эйнштейн, Дмитрий Менделеев, Энрико Ферми, Альфред Нобель, Эрнест Резерфорд, Нильс Бор, Мария Кюри и другие.
Некоторые наименования произошли от других имён собственных: названий городов, штатов, стран. Например: московий, дубний, европий, тенессин. Не все топонимы покажутся знакомыми носителю русского языка: вряд ли человек без культурной подготовки узнает в слове нихоний самоназвание Японии – Нихон (букв.: Страна восходящего солнца), а в гафнии – латинский вариант Копенгагена. Узнать даже название родной страны в слове рутений – не самая простая задача. Тем не менее Россия на латинском языке именуется Рутенией, и именно в честь неё назван 44-й химический элемент.
Фигурируют в периодической таблице и названия космических тел: планет Урана, Нептуна, Плутона, Цереры, астероида Паллады. Помимо имен персонажей древнегреческой мифологии (Тантал, Ниобий), встречаются и скандинавские: торий, ванадий.
Помимо имен персонажей древнегреческой мифологии (Тантал, Ниобий), встречаются и скандинавские: торий, ванадий.
Периодическая таблица
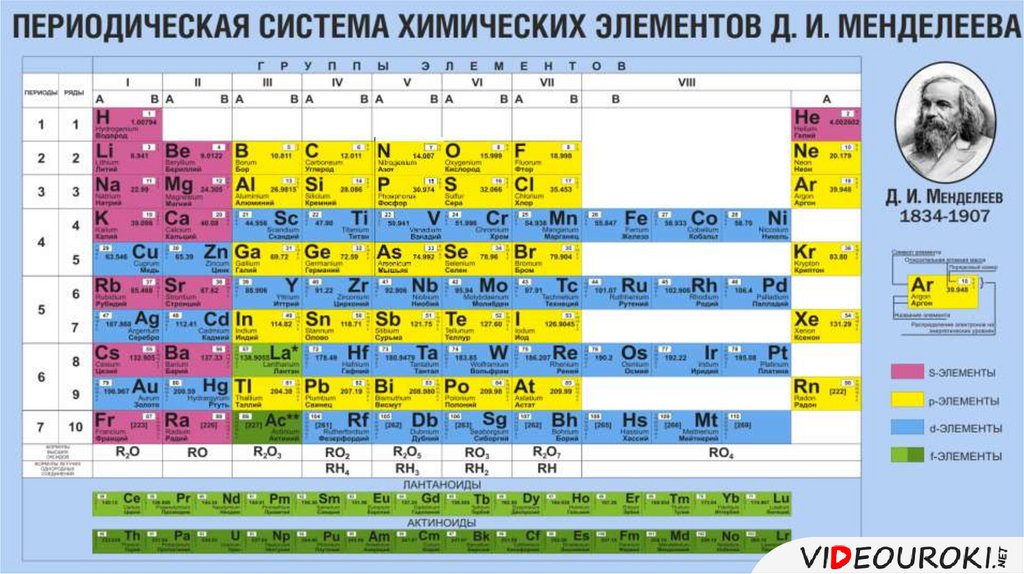
В привычной нам сегодня периодической таблице, носящей имя Дмитрия Ивановича Менделеева, элементы представлены по рядам и периодам. В каждой ячейке химический элемент обозначается химическим символом, рядом с которым представлены другие данные: его полное название, порядковый номер, распределение электронов по слоям, относительная атомная масса. Каждая ячейка имеет свой цвет, который зависит от того, выделяется s-, p-, d- или f- элемент.
Принципы записи
При записи изотопов и изобаров слева сверху относительно символа элемента ставится массовое число – общее количество протонов и нейтронов в ядре. При этом слева снизу ставится атомный номер, представляющий собой количество протонов.
Заряд иона записывается справа сверху, и с той же стороны снизу указывается число атомов. Символы химических элементов всегда начинаются с заглавной буквы.
Национальные варианты записи
В азиатско-тихоокеанском регионе существуют свои варианты написания символов химических элементов, основанные на местных способах письма. В китайской системе обозначения используются знаки радикалов, за которыми следуют иероглифы в их фонетическом значении. Символы металлов предваряются знаком «металл» или «золото», газы – радикалом «пар», неметаллы – иероглифом «камень».
В европейских странах также существуют ситуации, когда знаки элементов при записи отличаются от зафиксированных в международных таблицах. Например, во Франции азот, вольфрам и бериллий имеют собственные названия на национальном языке и обозначаются соответствующими символами.
В заключение
Обучаясь в школе или даже высшем учебном заведении, запоминать наизусть содержание всей периодической таблицы вовсе не требуется. В памяти следует держать химические символы элементов, которые чаще всего встречаются в формулах и уравнениях, а малоупотребительные время от времени смотреть в Интернете или учебнике.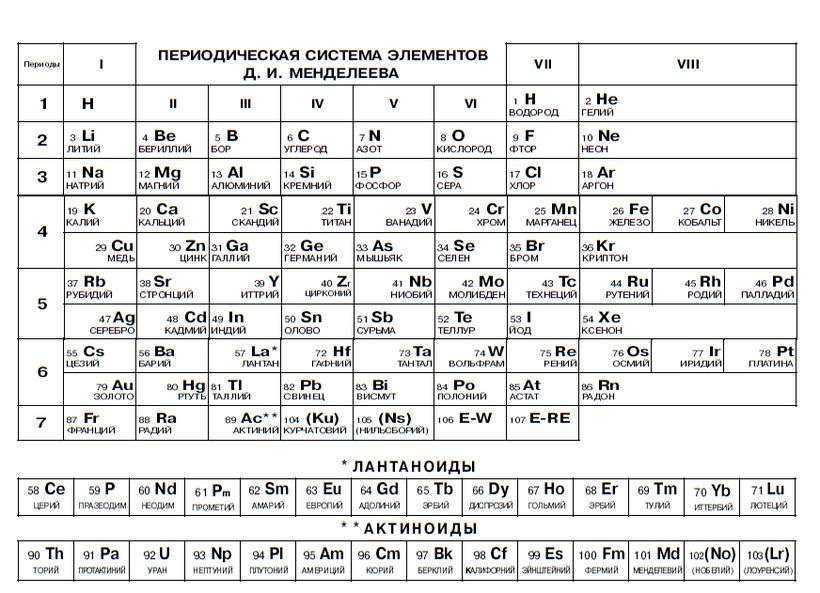
Однако во избежание ошибок и путаницы необходимо знать, каким образом осуществляется структурирование данных в таблице, в каком именно источнике найти требуемые данные, чётко помнить, какие названия элементов различаются в русском и латинском варианте. В противном случае можно случайно принять Mg за марганец, а N – за натрий.
Чтобы получить практику на начальном этапе, выполняйте упражнения. Например, укажите символы химических элементов для случайно взятой последовательности названий из периодической таблицы. По мере получения опыта всё встанет на свои места и вопрос запоминания этой базовой информации отпадет сам собой.
Символы химических элементов. Структура Периодической системы Д.И. Менделеева
Цель: познакомить учащихся с символами химических элементов, их названиями и произношениями; познакомить с этимологическими началами их названий, познакомить со структурой Периодической системы Д.И.Менделеева.
Задачи:
Обучающие.
 Ввести понятие о знаках
химических элементов и познакомить с
этимологическими началами их названий,
познакомить учащихся со структурой
Периодической таблицы.
Ввести понятие о знаках
химических элементов и познакомить с
этимологическими началами их названий,
познакомить учащихся со структурой
Периодической таблицы.
Планируемые результаты обучения. Знать
структуру периодической системы Д.И.Менделеева,
уметь описывать положение элемента в
периодической системе, знать символы химических
элементов, их произношения и понимать их
происхождение.
Оборудование: компьютер, видеопроектор, электронное мультимедийное приложение к УМК “Химия. 8 класс” изд “Дрофа”; шаро–стержневые модели атомов и молекул, рабочие и информационные листы,
Подготовка к уроку: на столы выдаются для каждого ученика рабочие и информационные листы. Заранее на обратной стороне доски записывается тема и план урока, на другой доске с обратной стороны делается запись: “Две молекулы воды, под действием электрического ток разлагаются с образованием одной молекулы кислорода и двух молекул водорода”.
Приложение 1
Ход урока
1. Организационный момент
Проверка готовности к уроку.
2. Проверка домашнего задания. Актуализация знаний
Ученикам сообщают, что проверка домашнего
задания проходит в виде “Аукциона знаний”, за
правильные ответы учащиеся получают “жетоны
знаний”, по количеству которых учитель
оценивает активность учащихся на уроке.
Учитель: Вы начали изучать тему “Свойства веществ. Химические знаки и формулы” Я предлагаю вам вспомнить основные понятия прошлого урока. Что называется химическим элементом?
Ученик: химический элемент – это определённый вид атомов.
Учитель: – Что называется веществом?
Ученик: Вещество – это то, из чего состоят тела.
Учитель: Давайте подумаем, чем отличаются эти два понятия: “химический элемент” и “вещество”?
Ученики: химический элемент входит в состав простых и сложных веществ, у него нет физических и химических свойств; а вещество обладает физическими и химическими свойствами. Например: простое вещество кислород – газ, поддерживает горение, входит в состав воздуха и необходим нам для дыхания. Молекула простого вещества кислорода образована
Учитель: – Из чего состоят вещества?
Ученик: вещества состоят из молекул, а молекулы состоят из атомов.
Учитель: На какие две группы делятся все вещества?
Ученик: вещества бывают простыми и сложными.
Учитель: – Какие вещества мы называем простыми веществами? (Демонстрирует шаро-стержневые модели молекул простых веществ – кислорода, озона, водорода, азота)
Ученик: простые вещества – это вещества, образованные атомами одного и того же химического элемента.
Учитель: – какие вещества мы называем сложными? (Демонстрирует шаро-стержневые модели молекул сложных веществ – воды, углекислого газа и серной кислоты)
Ученик: сложные вещества – это вещества, образованные атомами разных химических элементов.
Учитель: Итак, все вещества образованы атомами либо разными, либо одинаковыми!
– Сколько примерно этих видов атомов может быть? (Демонстрация во время вопроса– учитель разбирает несколько молекул веществ и выкладывает по одному шарику – “атому” разного цвета (вида) на демонстрационном столе)
Ученик: столько, сколько разных химических
элементов в периодической системе, примерно 110.
Учитель: Молекула воды – сложное вещество (демонстрация шаростержневой модели молекулы воды). – Как можно доказать, что это сложное вещество?
Предположения ученика: из сложных веществ можно получить простые вещества -кислород и водород.
Учитель: Верно. Давайте с вами проведём пример реакции разложения на примере шаростержневых молекул. Я приглашаю к доске двух желающих, которые смогут провести это превращение: из двух молекул воды получить молекулы простых веществ.
Каждому из двух учащихся выдаётся по две
шаростержневые модели молекул воды, перестроив
которые получают две молекулы водорода и одну
молекулу кислорода.
Каждому из учащихся, выполняющих работу с
моделями задаются по два вопроса:
– Молекулы каких веществ вы получили? (Ответ: получили молекулы кислорода и водорода)
– Сколько получилось молекул каждого
вещества из двух молекул воды?
– Почему для реакции мы взяли две молекулы
воды? (Ответ: т.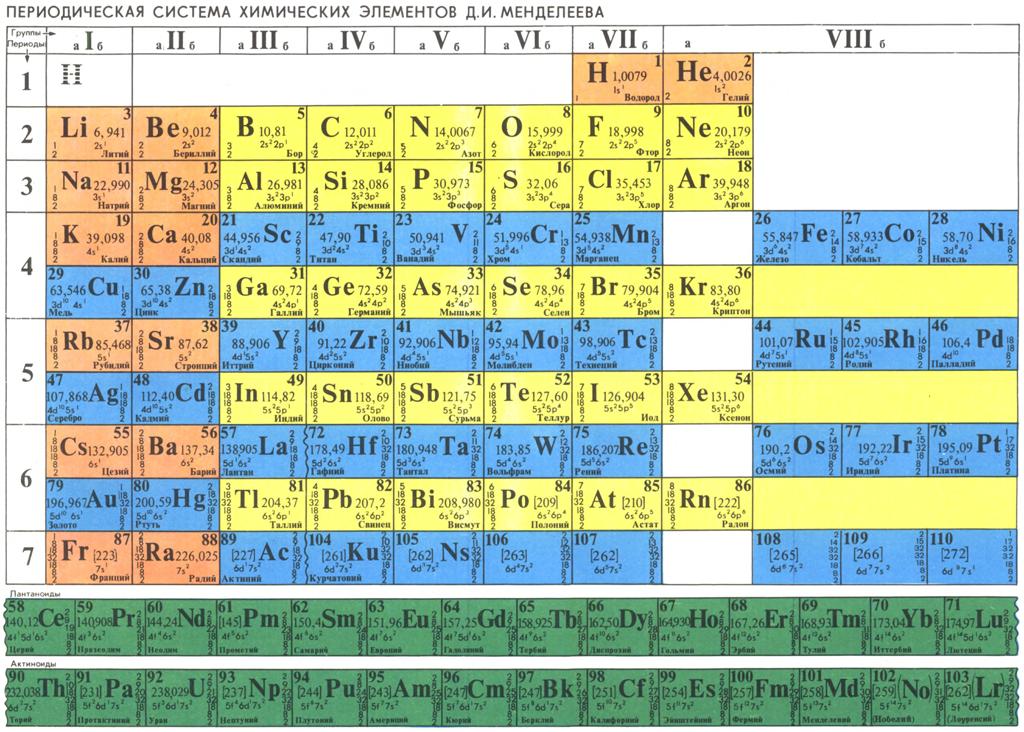 к. молекула кислорода
состоит из двух атомов, а в состав молекулы воды
входит один атом кислорода).
к. молекула кислорода
состоит из двух атомов, а в состав молекулы воды
входит один атом кислорода).
– Как вы думаете – реакция разложения воды –
это химическое явление или физическое? – Что
доказывает правильность вашего ответа?
Далее учитель обращает внимание, что при химической реакции, все связи, которые были между атомами в двух молекулах воды все израсходовались для образования молекул новых веществ.
Объяснение новой темы:
Учитель: Мы с вами грамотные люди и умеем писать. Я записала на доске реакцию разложения воды.
Демонстрация записи сделанной до урока на обратной стороне доски: “Две молекулы воды под действием электрического тока разлагаются на две молекулы водорода и одну молекулу кислорода”
– А кто является авторами славянской письменности – алфавита?
Ученик: болгарские просветитель Кирилл и
Мефодий.
Учитель: мы знаем буквы алфавита, из них мы складываем слова, а из слов – пишем предложения.
Подобно русской письменности в химии есть тоже буквы – химические символы.
На доске напротив записи сделанной заранее учитель пишет в ряд символы некоторых химических элементов и демонстрирует на примере шаростержневых молекул отдельные атомы.
Учитель: Атом кислорода обозначается
символом “О”, атом водорода обозначается
символом “Н”. С помощью химических символов мы
будем учиться писать слова –  Сравните одна и та
же фраза записанная с помощью русского алфавита
и с помощью химического языка.
Сравните одна и та
же фраза записанная с помощью русского алфавита
и с помощью химического языка.
Полное оформление демонстрационной записи на доске выглядит так:
|
Учитель: Итак, сегодня на уроке мы знакомимся
с “буквами” химического алфавита – символами
химических элементов.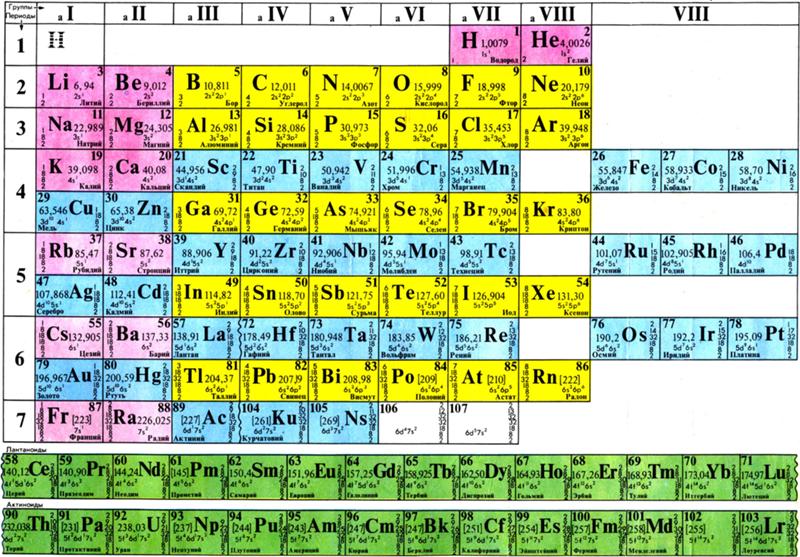
Запишите тему сегодняшнего урока в своих тетрадях:
“СИМВОЛЫ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ”.
При изучении темы урока мы будем придерживаться следующего плана:
- Автор химической письменности.
- Принцип обозначения химических элементов.
- Периодическая система химических элементов Д.И.Менделеева.
- Этимологические начала названий химических элементов.
(Тема урока и план урока пишутся заранее, перед уроком, на обратной стороне доски.)
На протяжении всего урока во время беседы с учителем ученики, правильно отвечая на вопросы, получают такие жетоны:
Учитель: на первый и второй вопрос нашего плана я знаю, что уже некоторые учащиеся смогут ответить.
– Кто является автором химического алфавита? Как вы это узнали?
Учащийся: автором химического алфавита
является Йенс Якоб Берцелиус. Я эту информацию
нашёл в жетоне знаний.
Я эту информацию
нашёл в жетоне знаний.
Учитель: – Как Й.Я.Берцелиус предложил обозначать химические элементы?
Учитель: Шведский учёный Й.Я.Берцелиус предложил в качестве символов химических элементов использовать первую или первую и одну из последующих букв латинского названия элемента. Сейчас откройте учебник на странице 92, посмотрите на 4ю и 2ю колонки таблицы. В 4й колонке даны латинские названия некоторых химических элементов, а во второй – их химические символы
Пример:
Hidrogenium – Н – водород
Ferrum – Fe – железо
Magnium – Mg – магний
Mangants – Mn – марганец
Для чтения химических формул будем
использовать произношения химических
элементов. Возьмите информационный
лист №1 Там у вас есть такая же таблица, но
дополненная и с большим числом химических
элементов. Она вам пригодится в дальнейшем.
Рассмотрим её. В 3ей колонке, обратите
внимание, на произношения химических элементов:
некоторые из них произносятся произношением
букв латинского алфавита, некоторые имеют такое
же произношение как и их русское название, а
некоторые произносятся латинским названием
элемента. В этом информационном листе 4я
и 5я колонки для вас интересная
информация об этимологии названия химических
элементов и названы учёные, открывшие данные
химические элементы.
Она вам пригодится в дальнейшем.
Рассмотрим её. В 3ей колонке, обратите
внимание, на произношения химических элементов:
некоторые из них произносятся произношением
букв латинского алфавита, некоторые имеют такое
же произношение как и их русское название, а
некоторые произносятся латинским названием
элемента. В этом информационном листе 4я
и 5я колонки для вас интересная
информация об этимологии названия химических
элементов и названы учёные, открывшие данные
химические элементы.
Таблицу, которая у вас в учебнике надо выучить
наизусть первые три колонки. К следующему уроку
выучите названия, символы и произношения первых
10 химических элементов (половина таблицы). Она
начинается на странице 83, вы учите элементы до
меди включительно, отметьте карандашом в
таблице. И сразу отметьте карандашом на странице
86 до слов “Обозначение состава вещества….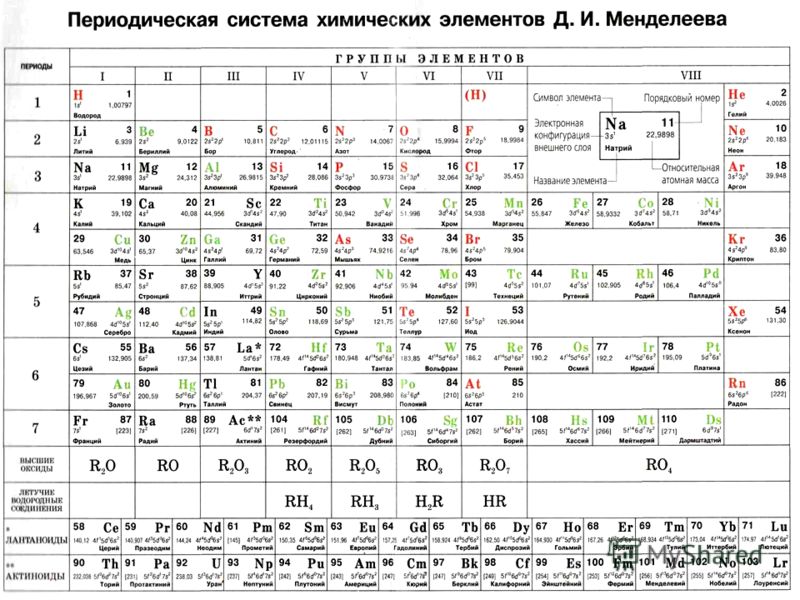 ”
второй абзац снизу – вы дома учите параграф 13 до
этих слов.
”
второй абзац снизу – вы дома учите параграф 13 до
этих слов.
Учитель: В таблице учебника вместилось всего 20 химических элементов.
– Сколько всего химических элементов? Откуда мы возьмём эти сведения?
Ученик: все известные химические элементы расположены в периодической таблице Д.И.Менделеева, их известно около 110 элементов.
Учитель: Правильно. Все известные химические
элементы расположены в периодической таблице
химических элементов Д.И.Менделеева.
Д.И.Менделеев – великий химик, русский учёный,
создатель периодической системы. На тот момент,
когда он составил таблицу было известно 63
химических элемента. Дмитрий Иванович хорошо
знал свойства каждого химического элемента и
расположил их так, что выделил группы элементов
сходных по химическим свойствам, и даже оставил
места в таблице ещё не изученным химическим
элементам. Дмитрий Иванович предугадал свойства
некоторых ещё не открытых элементов и указал
пути открытия этих элементов. О гениальности
этого учёного и его открытиях можно много
говорить, и для этого мы посвятим не один, а
несколько уроков. Сегодня мы должны
познакомиться со структурой периодической
системы химических элементов Д.И.Менделеева.
Дмитрий Иванович предугадал свойства
некоторых ещё не открытых элементов и указал
пути открытия этих элементов. О гениальности
этого учёного и его открытиях можно много
говорить, и для этого мы посвятим не один, а
несколько уроков. Сегодня мы должны
познакомиться со структурой периодической
системы химических элементов Д.И.Менделеева.
Учитель демонстрирует несколько вариантов периодической системы с разными цветовыми изображениями (демонстрационную, на форзаце учебника, на обложке дневников, …) и отмечает:
В любой периодической таблице изображены одни
и те же химические элементы, в одинаковой
последовательности. Гениальность этого творения
заключается в том, что она таит в себе очень много
информации о химических элементах, о
закономерностях их расположения, о строении
атомов химических элементов,… Поэтому изображая
периодические системы стараются выделить цветом
разные смысловые категории элементов.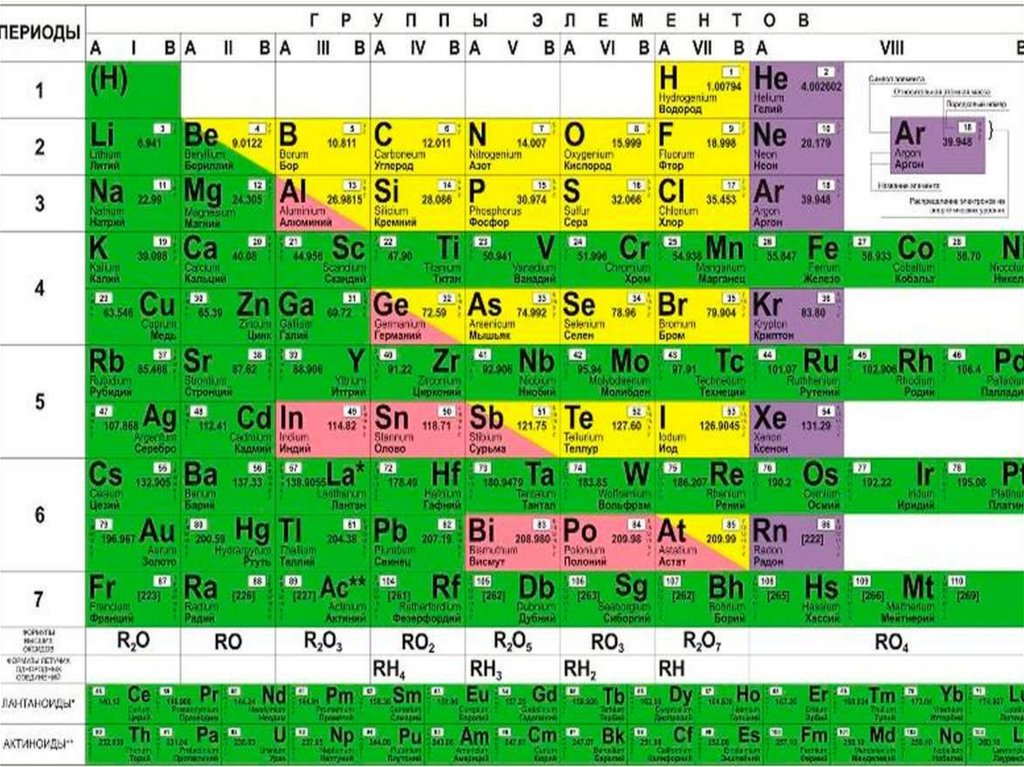 Каждая из
них удобна на разных этапах изучения химии.
Каждая из них находит в своё время удобное
применение.
Каждая из
них удобна на разных этапах изучения химии.
Каждая из них находит в своё время удобное
применение.
В нашей таблице (на форзаце учебника) цветом выделены красным цветом выделения элементы–неметаллы, а черным и зелёным – элементы-металлы.
– Приведите примеры элементов-неметаллов.
– Приведите примеры элементов-металлов.
По горизонтали эта таблица состоит из периодов.
Периоды – это горизонтальные ряды в периодической таблице химических элементов.
Периоды делятся на малые и большие, малые периоды имеют только 1 ряд элементов, а большие периоды – по 2 ряда элементов.
Сейчас внимательно посмотрите один видеосюжет, и после него вам надо будет ответить на вопросы.
Демонстрация видеосюжета мультимедийного
приложения к УМК “Химия. 8 класс” издание второе.
Изд “Дрофа” , 2006г Раздел “Введение. Предмет
химии”, урок 4 “Символы химических элементов.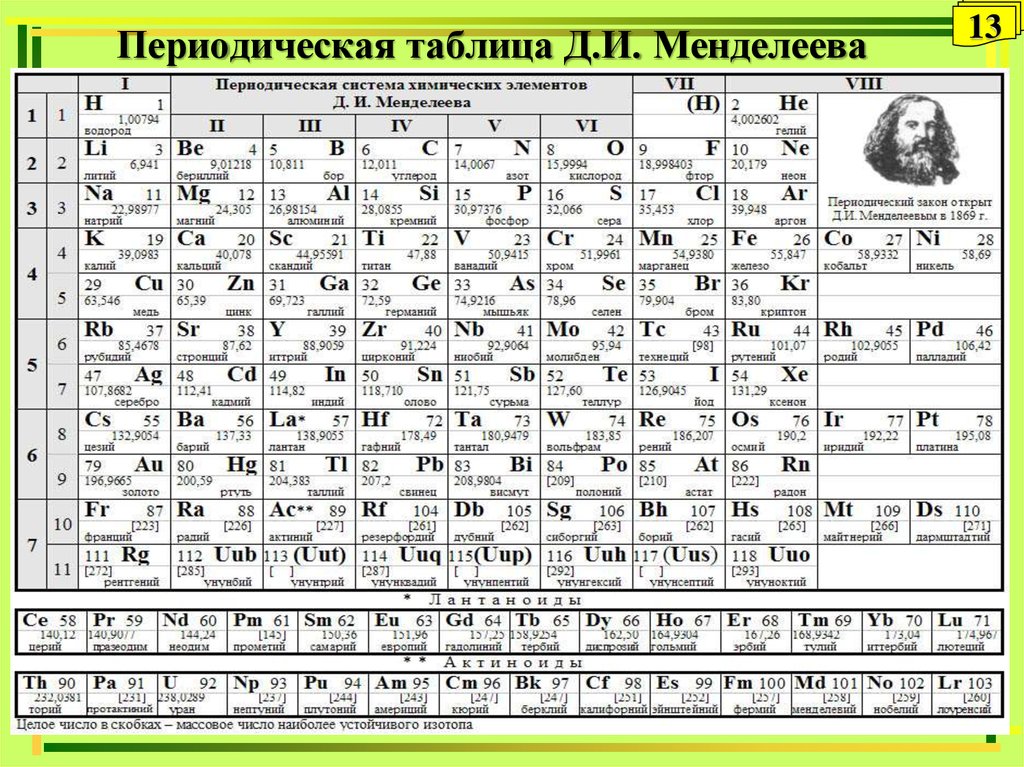 Периодическая система химических элементов
Д.И,Менделеева”, видеосюжет №12 “структурные
части Периодической системы Д.И.Менделева:
период”
Периодическая система химических элементов
Д.И,Менделеева”, видеосюжет №12 “структурные
части Периодической системы Д.И.Менделева:
период”
Учитель: Сейчас закрепим изученное понятие. В рабочих листах №1 самостоятельно допишите предложения 2,3,4. Через 2-3 минуты мы проверим ваши ответы.
Учитель спрашивает одного человека, проверяя правильность самостоятельного ответа, а учащиеся проверяют правильность своих записей.
Учитель: По вертикали периодическая система состоит из 8 групп. Группа – это вертикальный ряд элементов в Периодической системе Д. И. Менделеева.
Каждая группа, в свою очередь, подразделяется на две подгруппы: главную и побочную. Элементы главной подгруппы располагаются в малых и больших периодах, а элементы побочной подгруппы находятся только в больших периодах.
Сейчас внимательно посмотрите ещё один
видеосюжет, и после него опять выполним
следующие задания в рабочем листе №1.
Демонстрация видеосюжета мультимедийного приложения к УМК “Химия. 8 класс” издание второе. Изд “Дрофа” , 2006г Раздел “Введение. Предмет химии”, урок 4 “Символы химических элементов. Периодическая система химических элементов Д.И,Менделеева”, видеосюжет №13 “структурные части Периодической системы Д.И.Менделева: группы и подгруппы”
Учитель: допишите предложения 1,5,6,7 в рабочих листа №1. Через три минуты мы проверим правильность ваших ответов.
Учитель спрашивает одного человека, проверяя правильность самостоятельного ответа, а учащиеся проверяют правильность своих записей.
Учитель: А теперь, поучимся работать с периодической таблицей, ведь она не только великое творение Д.И.Менделеева, но и самая законная шпаргалка на любой контрольной, экзамене и даже ЕГЭ. Поэтому стоит научиться ей пользоваться!
– Выполните задание №1 в рабочем листе №1.
Учитель вместе с классом выполняет задание 1а, а следующие задания 1б и 1в учащиеся выполняют сами, затем учитель и класс проверяют.
– Выполните самостоятельно задание №2а и №2б. Это задания противоположные первому.
Учитель через 2 мин проверяет правильность выполнения задания.
Учитель: Мы научились называть адрес химических элементов в Периодической системе. Переходим к последнему вопросу нашего урока. Открытие каждого химического элемента воспринималось в науке как событие огромной важности. Названия, которые давались при открытии химическому элементу, никогда не были случайными.
– Каким правилам придерживались учёные, давая названия химическим элементам.
Я предлагаю вам вместе узнать этимологические
начала названий химических элементов. Поэтому
предлагаю работу в группах. Каждые две парты
учащихся работают вместе изучая свой рабочий
материал и выбирают одного отвечающего с
сообщением.. На работу выделяю 4-5 минут.
Поэтому
предлагаю работу в группах. Каждые две парты
учащихся работают вместе изучая свой рабочий
материал и выбирают одного отвечающего с
сообщением.. На работу выделяю 4-5 минут.
Учащимся выдаётся один на парту рабочий лист с заданием. Каждые две парты учащихся выполняет свои варианты заданий: Информационный лист №2, информационный лист №3, информационный лист №4, информационный лист №5 и информационный лист №6.
Приложение_2, Приложение_3, Приложение_4
Затем учащиеся выступают со своим сообщением.
Закрепление. Обобщение. Обратная связь.
Учитель: задаёт ряд вопросов по изучаемой теме.
– Какую тему мы изучали сегодня на уроке.
– Какие понятия вы запомнили на этом уроке.
– Что вам особенно запомнилось сегодня на уроке.
– Выполните задания № 2в , № 2г
и задание №3 в рабочем листе №1.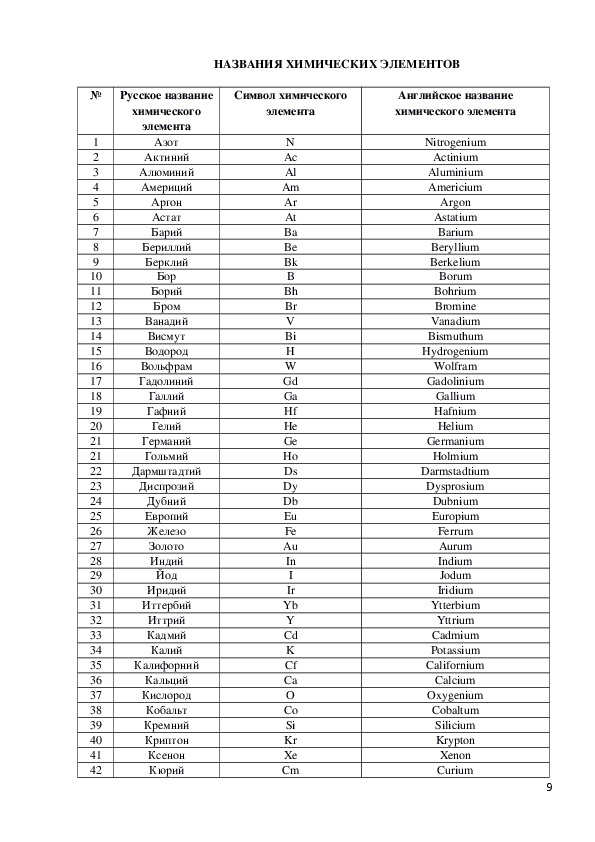
– Как вы считаете, по данной теме возникнут в дальнейшем у вас какие-нибудь сложности в изучении химии.
Я тоже думаю, что вы прекрасно справились с изучением данной темы урока. И выучив, домашний параграф и таблицу с химическими элементами, вы будете прекрасно пользоваться этими понятиями при дальнейшем изучении химии.
Домашнее задание
В дневник записываем §13 до слов “Обозначение состава вещества…” и задания на рабочем листе №2.
XuMuK.ru — Таблица Менделеева — периодическая система химических элементов
Еще в школе, сидя на уроках химии, все мы помним таблицу на стене класса или химической лаборатории. Эта таблица содержала классификацию всех известных человечеству химических элементов, тех фундаментальных компонентов, из которых состоит Земля и вся Вселенная. Тогда мы и подумать не могли, что таблица Менделеева бесспорно является одним из величайших научных открытий, который является фундаментом нашего современного знания о химии.
Периодическая система химических элементов Д. И. Менделеева
На первый взгляд, ее идея выглядит обманчиво просто: организовать химические элементы в порядке возрастания веса их атомов. Причем в большинстве случаев оказывается, что химические и физические свойства каждого элемента сходны с предыдущим ему в таблице элементом. Эта закономерность проявляется для всех элементов, кроме нескольких самых первых, просто потому что они не имеют перед собой элементов, сходных с ними по атомному весу. Именно благодаря открытию такого свойства мы можем поместить линейную последовательность элементов в таблицу, очень напоминающую настенный календарь, и таким образом объединить огромное количество видов химических элементов в четкой и связной форме. Разумеется, сегодня мы пользуемся понятием атомного числа (количества протонов) для того, чтобы упорядочить систему элементов. Это помогло решить так называемую техническую проблему «пары перестановок», однако не привело к кардинальному изменению вида периодической таблицы.
В периодической таблице Менделеева все элементы упорядочены с учетом их атомного числа, электронной конфигурации и повторяющихся химических свойств. Ряды в таблице называются периодами, а столбцы группами. В первой таблице, датируемой 1869 годом, содержалось всего 60 элементов, теперь же таблицу пришлось увеличить, чтобы поместить 118 элементов, известных нам сегодня.
Периодическая система Менделеева систематизирует не только элементы, но и самые разнообразные их свойства. Химику часто бывает достаточно иметь перед глазами Периодическую таблицу для того, чтобы правильно ответить на множество вопросов (не только экзаменационных, но и научных).
The YouTube ID of 1M7iKKVnPJE is invalid.
Предисловие
Таблица Менделеева или периодическая таблица химических элементов — это представленный в виде таблицы свод химических элементов, которые расположены по возрастанию атомного номера. В каждой ячейке таблицы Менделеева так же есть обозначение элемента, его атомная масса, принадлежность к определенной группе обозначенная цветом, а так же иногда указывается электронная конфигурация. Структура таблицы показывает периодических характер химических свойств элементов. Она имеет 7 строк, которые называются периодами, и столбцы, которые называются группами. Именно столбцы объединяют элементы со схожими химическими свойствами. Например, щелочные металлы, щелочно-земельные металлы, галогениды, благородные газы и т.д. Так же имеется четыре прямоугольные области, которые объединяют элементы со схожим электронным строением их атомов.
Структура таблицы показывает периодических характер химических свойств элементов. Она имеет 7 строк, которые называются периодами, и столбцы, которые называются группами. Именно столбцы объединяют элементы со схожими химическими свойствами. Например, щелочные металлы, щелочно-земельные металлы, галогениды, благородные газы и т.д. Так же имеется четыре прямоугольные области, которые объединяют элементы со схожим электронным строением их атомов.
На данный момент открыто 118 химических элементов, которые завершили заполнение семи строк таблицы. Первые 94 элемента были найдены в природе, хотя некоторые в очень маленьких количествах, а вот остальные синтезированы искусственно в физических лабораториях или вообще при ядерных взрывах. В настоящее время ученые-физики продолжают попытки синтезировать 119 элемент и более тяжелые, теоретически возможность этих элементов была доказана ранее — они начнут восьмой ряд периодической таблицы Менделеева. Кроме того, все элементы имеют так называемые изотопы, которые так же в большом количестве были синтезированы в лабораториях и обнаружены в природе. Наиболее известный пример — тяжелая вода, где водород с атомным весом 1 заменяет его изотоп дейтерий (вес 2) или тритий (вес 3).
Наиболее известный пример — тяжелая вода, где водород с атомным весом 1 заменяет его изотоп дейтерий (вес 2) или тритий (вес 3).
Структура периодической таблицы используется для нахождения взаимосвязи между свойствами различных элементов и их соединений, а так же для прогноза этих свойств в том числе еще не открытых соединений.
Первую известную таблицу Менделеев опубликовал в 1869 году, которая демонстрировала периодический характер свойств известных на тот момент элементов. Так же Менделеев дал предсказания по свойствам не открытых на тот момент элементов и большинство его предсказания оказались близки к верным. В последующем с открытием других элементов расширялись и теоретические знания, стали появляться всё более точные теоретические математические модели для объяснения и предсказания свойств элементов.
Современная таблица Менделеева теперь широко используется для анализа химических реакций и вообще широко используется как в химии так и физике. Однако, много споров ведется относительно того на сколько оптимален тот или иной вид таблицы (их несколько десятков), а так же размещения некоторых элементов.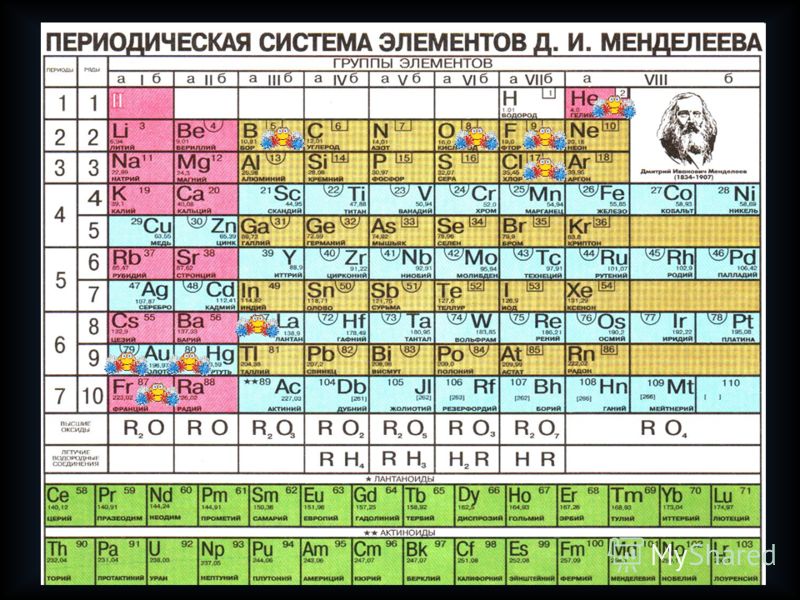
Как была открыта медь
Такие металлы как медь, золото, серебро и олово были известны людям очень давно. Так как с медью легко работать, она использовалась древнейшими известными культурами уже 10000 лет назад. Пик популярности использования меди приходится начиная с 5 и заканчивая 3 тысячелетием до Нашей Эры. Это время в некоторых регионах принято называть «медным веком». Из этого металла изготавливались как орудия труда, так и украшения. На территории современного Ирана был найден медный кулон возраст которого приблизительно оценивается в 8700 год до Нашей Эры. Так же медь является первым металлом, который научились легировать с помощью олова и мышьяка до бронзы. В связи с этим открытием, которое произошло вероятно около 3 тысячелетия до Нашей Эры, началась так называемая эпоха «Бронзового века». Эта эпоха продлилась ориентировочно до первого тысячелетия до Нашей эры.
Затем производство меди и его обработка набирала уже значительные обороты. К началу новой эпохи мировое производство меди ориентировочно варьировалось в пределах 15 тонн в год. В первом тысячелетии Нашей Эры уже производились массивные сооружения из меди и его сплавов. В пример можно поставить бронзовую статую Будды храма Нара в Японии. По историческим сведениям ее отлили в 749 году. Для сооружения 16-ти метровой конструкции понадобилось 400 тонн сырья. Научное открытие самого металла можно присудить немецкому ученому Готфриду Осанну. Он изобрел порошковую металлургию, которую использовал на меди в 1830 году. В ходе своих испытаний он описал и определил атомный вес этого химического элемента.
В первом тысячелетии Нашей Эры уже производились массивные сооружения из меди и его сплавов. В пример можно поставить бронзовую статую Будды храма Нара в Японии. По историческим сведениям ее отлили в 749 году. Для сооружения 16-ти метровой конструкции понадобилось 400 тонн сырья. Научное открытие самого металла можно присудить немецкому ученому Готфриду Осанну. Он изобрел порошковую металлургию, которую использовал на меди в 1830 году. В ходе своих испытаний он описал и определил атомный вес этого химического элемента.
Читайте: Никель как химический элемент таблицы Менделеева
Введение
Каждый химический элемент в таблице Менделеева имеет свой уникальный атомный номер (Z), который равен числу протонов в его атомном ядре. У каждого атома в ядре может быть разное число нейтронов и поэтому атом одного элемента может иметь разную массу — такие «варианты» одного атома отличающиеся по массе называют изотопами. Например, самые распространенные изотопы урана U235 и U238, но на самом деле изотопов известно восемь на данный момент с атомными массам от 233 до 240.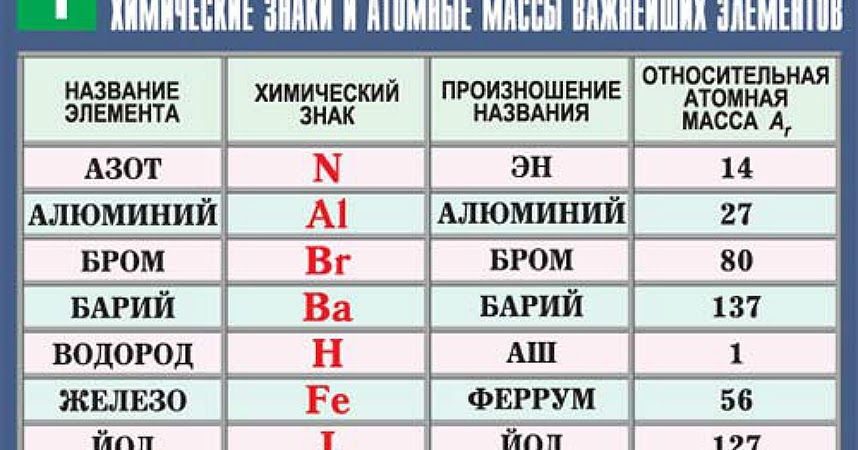 Изотопы в таблице не разделяются, в ней указывается самый распространенный природный изотоп или для атомов, которые стабильных изотопов не имеют, указывается наиболее стабильный (долгоживущий).
Изотопы в таблице не разделяются, в ней указывается самый распространенный природный изотоп или для атомов, которые стабильных изотопов не имеют, указывается наиболее стабильный (долгоживущий).
В общепринятой периодической таблице (см. выше) химические элементы указываются в порядке возрастания атомного номера Z. Новая строка (период) начинается тогда, когда начинает заполняться новая электронная оболочка атома.
Столбцы (группы) определяются электронной конфигурацией атома. Элементы с одинаковым чистом электронов на валентном электронном уровне попадают в одни и те же группы. Элементы находящиеся в одной группе как правило имеют схожие химические свойства.
Первые 94 элемента встречаются в природе в свободном и связанном виде либо только в виде составе соединений, остальные же синтезированы в лабораториях. Некоторые элементы, например, франций (Fr) был зафиксирован только в виде излучения (получено всего 300 тыс. атомов). Другие элементы выше 94 получены так же в очень малых количествах.
Расшифровка хим элементов состава стали
Займемся расшифровкой свойств химических элементов для того, чтобы понять, какое влияние оказывают химические элементы на свойства стали.
- С – углерод. Углерод в составе стали необходим для увеличения прочности и твердости. Чем углерода больше, тем прочнее и тверже сталь. Если в составе углеродистой металлопродукции присутствует более 0,4 % углерода, то при отрицательной температуре, от нуля градусов и ниже, сталь становится, менее надежна, и более хрупка.
- Si – кремний. Если кремний присутствует в металле в диапазоне 0,3%-0,4%, то он повышает прочность металла, а так же предел текучести, но уменьшается пластичность (уменьшается способность металла к вытяжке). Если его содержание в стали более 0,4%, то уменьшается свариваемость и стойкость к коррозии. Если кремния менее 0,3 %, пластичность металла не снижается. Кремний особенно упрочняет сталь в нержавеющем прокате — он придает ему повышение коррозионной стойкости, износостойкость и повышение упругости.
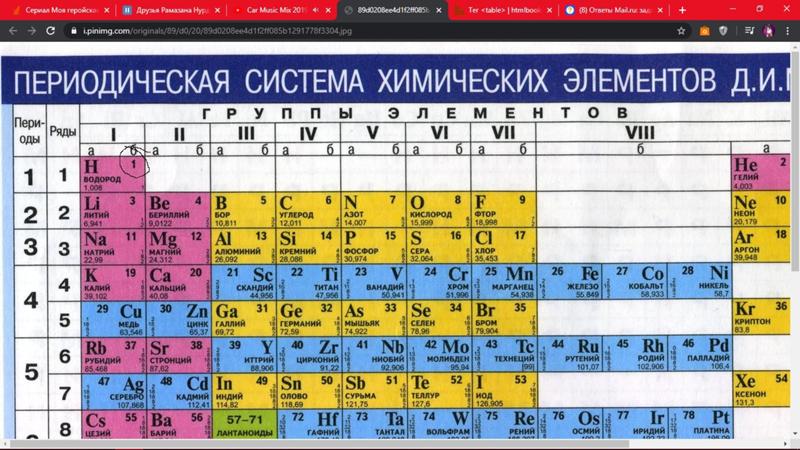
- Mn – марганец. Если его в металле более 0,8 %, то он увеличивает прочность, упругость и износостойкость, но уменьшает теплопроводность, пластичность и свариваемость. Если его менее 0,8 %, то он не оказывает никакого существенного влияния на сталь. Так же если марганца в составе много, то можно увидеть в металлопродукции красноватый цвет (цвет марганцовки), поэтому невооруженным взглядом можно понять много ли марганца в металле или нет.
- P – фосфор. Это вредная примесь. Если в составе более 1% Si, то фосфор вытесняется и уменьшается. Если фосфора не более 0,04%, то понижается порог хладноломкости и увеличивается риск появления трещин. Если фосфора более 0,04%, то зерна феррита становятся крупнее и склонность металла к перегреву увеличивается. Чем больше в составе Si (кремния) и Al (алюминия), тем меньше отрицательного воздействия (в особенности, уменьшается степень нагрева).
- S – сера. Является постоянной примесью.
 Она негативно влияет на ударную вязкость, свариваемость и качество поверхности металлопродукции. В горячем состоянии сера приводит к снижению пластичности. Марганец уменьшает влияние вредных свойств серы.
Она негативно влияет на ударную вязкость, свариваемость и качество поверхности металлопродукции. В горячем состоянии сера приводит к снижению пластичности. Марганец уменьшает влияние вредных свойств серы. - Cr – хром. Повышает термическую прочность стали, увеличивает стойкость к коррозии и окислению.
- Ni – никель. Улучшает вязкость стали и усталой прочности. В комбинации с хромом и молибденом он улучшает термическую прочность. Защищает от коррозии. Облагораживает поверхность.
- Cu – медь. Увеличивает коррозионную сопротивляемость стали. Она повышает прочностные характеристики и уменьшает ударную вязкость и пластичность стали.
- As – мышьяк. В количестве от 0,1-0,16% увеличивает коррозионную стойкость. В составе стали он аналогичен фосфора, но негативное воздействие его меньше. В качественных сталях допускается присутствие мышьяка не более 0,08%.
- N – азот. Является присадкой, которая позволяет снизить содержание в стали никеля, хрома и марганца.
 Повышает предел текучести. Способен измельчать зерно феррита (ем меньше зерно, тем меньше способность к перегреву).
Повышает предел текучести. Способен измельчать зерно феррита (ем меньше зерно, тем меньше способность к перегреву). - Al – алюминий. Изолирует металл от окисления воздухом, оказывает антикоррозионные свойства. Улучшает прочность, пластичность и упругость.
- Mo – молибден. Придает стали большую твердость. Уменьшает отпускную хрупкость. Повышает вязкость при низкой температуре. Увеличивает стойкость к высокой температуре.
- Ti – титан. Повышает твердость, пластичность и устойчивость к коррозии. По прочности превосходит все химические элементы в составе стали.
Выбрать лист стальной Вы можете на нашем сайте!
Так же Вы можете отправить заявку на почту: Этот адрес электронной почты защищен от спам-ботов. У вас должен быть включен JavaScript для просмотра.
Или позвонив нам на по телефону: +
Источник статьи: https://artmetallural.ru/stati/23-vliyanie-himicheskih-ehlementov-v-markah-stali-na-ih-svojstva
Металлы, металлоиды и неметаллы
По своим физико-химическим свойствам все элементы можно разделить на три основные категории — металлы, металлоиды и неметаллы.
Металлы — это как правило блестящие высоко теплопроводные твёрдые вещества способные плавиться при нагревании и образовывать друг с другом сплавы, а так же образовывать ионные и ковалентные соединения с неметаллами.
Неметаллы — это как правило бесцветные либо цветные твёрдые, жидкие или газообразные вещества. Неметаллые образуют соединения друг с другом при помощи ковалентных связей.
Металлоиды — это вещества, которые могут проявлять в определенных условиях как металлические свойства, так и неметаллические.
Металлы и неметаллы могут быть дополнительно классифицированы на подкатегории, которые видны в таблице в строках слева направо. Так металлы подразделяются на химически очень активные щелочные металлы, чуть менее активные щелочно-земельные, характерные переходные металлы и химически достаточно инертные постпереходные металлы.
Неметаллы подразделяются на многоатомные неметаллы, при этом они ближе к металлоидам т.к. иногда проявляют металлические свойства, на галогениды и инертные газы. Доля неметаллов среди всех элементов небольшая — их 19 из 118 известных элементов.
Доля неметаллов среди всех элементов небольшая — их 19 из 118 известных элементов.
На самом же деле такое подразделение даже внутри каждой категории весьма условно и на этих условных границах есть большое «перекрытие». Например, бериллий относится к щелочно-земельным элементам, но его амфотерность и склонность образовывать ковалентные соединения позволяют относить его к постпереходным металлам. Радон относится к благородным газам, но образует ряд ионных соединений характерных для металлов. Поэтому существуют и другие типы разделения элементов на группы, например, по минералогическим признакам или кристаллическим структурам соединений.
Маркировка нержавеющей стали: тонкости обозначения нержавейки
Маркировка, с помощью которой обозначаются различные типы нержавеющих сталей, позволяет получить информацию не только о химическом составе сплава, но и об основных свойствах, которыми он обладает. Правила формирования обозначения, состоящего из буквенных и цифровых символов, регламентируются положениями как отечественных, так и международных нормативных документов.
Труба нержавеющая тонкостенная марки 12Х18Н10Т
Щелочные и щелочно-земельные металлы
Эти две категории очень похожи друг на друга, но щелочно-земельные металлы менее химически активны. Все они образуют основные оксиды. Для них характерна низкая механическая прочность, все щелочные металлы легко режутся ножом, очень высокая химическая активность (например, калий, и тем более рубидий могут воспламеняться прямо на воздухе, а с водой реагировать со «взрывом» — реакиция идет настолько быстро, что раздаётся хлопок). Магний и бериллий более твёрдые и гораздо менее реакционно способные, поэтому они используются иногда в чистом виде или в виде сплавов (магний-алюминиевый сплав очень важен в авиационной отрасли, например).
Переходные металлы
У этой группы очень широкий спектр физических и химических свойств. Например, температура плавления у ртути -38,8 ºC, а у иттрия 1795 ºC. Так же в очень широком диапазоне находится твёрдость, плотность, химическая активность (например, благородный металл золото очень химически инертен, а цинк наоборот весьма реакционно способен и по этому показателю ближе к щелочно-земельным элементам). Металлы этой группы — основа всех промышленных производств и сфер жизни. Они применяются во всех отраслях промышленности — от конструкционных материалов до микроэлектронной промышленности.
Металлы этой группы — основа всех промышленных производств и сфер жизни. Они применяются во всех отраслях промышленности — от конструкционных материалов до микроэлектронной промышленности.
Неметаллы (реакционные)
При нормальных условиях бор, углерод, фосфор, сера, селен — твёрдые вещества различных цветов. Каждое их них имеет различные формы кристаллической решетки (аллотропные модификации), например красный, желтый, черный, белый фосфор, которая очень сильно влияет на их химическую активность (например, графит гораздо менее активен обычного угля) и физические свойства (алмаз самое твердое вещество в природе и это прозрачный материал, а графит хрупкий, мягкий, непрозрачный).
Азот и кислород — газы. При этом азот достаточно химически инертен, кислород напротив является очень активным окислителем.
Галогениды имеют разные физические свойства (фтор, хлор — газы, бром — жидкость, иод — твердое вещество). Астат получен только в крайне малых количествах как и теннессин, их свойства изучены плохо. Химически галогениды — очень сильные окислители (фтор самый сильный в Таблице Менделеева). С металлами образуют как правило соли с ионной решеткой, а с водородом очень сильные кислоты. С неметаллами так же образуют множество многоатомных соединений как правило с ковалентными связями.
Химически галогениды — очень сильные окислители (фтор самый сильный в Таблице Менделеева). С металлами образуют как правило соли с ионной решеткой, а с водородом очень сильные кислоты. С неметаллами так же образуют множество многоатомных соединений как правило с ковалентными связями.
Периодический закон
Существуют две формулировки периодического закона химических элементов: классическая и современная.
Классическая, в изложении его первооткрывателя Д.И. Менделеева: свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величин атомных весов элементов.
Современная: свойства простых веществ, а также свойства и формы соединений элементов находятся в периодической зависимости от заряда ядра атомов элементов (порядкового номера).
Графическим изображением периодического закона является периодическая система элементов, которая представляет собой естественную классификацию химических элементов, основанную на закономерных изменениях свойств элементов от зарядов их атомов. Наиболее распространёнными изображениями периодической системы элементов Д.И. Менделеева являются короткая и длинная формы.
Наиболее распространёнными изображениями периодической системы элементов Д.И. Менделеева являются короткая и длинная формы.
Неметаллы (инертные газы)
Крайне химически пассивные вещества. Первое соединение ксенона XePtF6 было синтезировано в 1962 году, а соединения неона и гелия до сих пор неизвестны. Тем не менее инертные газы играют огромную роль в различных отраслях промышленности, медицине, при подводных погружениях и т.д.
P.S.: Интересно, что название «Таблица Менделеева» известна в основном только в России, а в остальном мире она называется чаще всего просто «Периодическая таблица».
P.P.S.: Статья будет дополняться и корректироваться.
Интересные факты
Так как применение меди очень широкое, соответственно и интересных фактов связанных с медью достаточно. Стоит начать с того, что цена на чистую медь на мировом рынке не такая уж и маленькая. В 2014 году 1 тонна меди на мировом рынке оценивалась в 7000 американских долларов. В связи с такой высокой ценой увеличилось количество краж медных предметов. Например в Германии железнодорожная кампания Deutsche Bahn AG понесла убытков на 14 миллионов евро из-за воровства медных заземляющих железнодорожных кабелей.
Например в Германии железнодорожная кампания Deutsche Bahn AG понесла убытков на 14 миллионов евро из-за воровства медных заземляющих железнодорожных кабелей.
Еще одним интересным моментом является то, что первые изобретенные человеком зеркала изготавливались именно из меди. Медь натиралась(полировалась) до такой степени, пока не было видно отбражение на поверхности меди. Так же в области применения стоит отметить, что большая часть монет произведенных по всему миру содержит в своем составе медь. Еще одним интересным фактом является то, что медь как железо и алюминий могут подвергаться вторичной переработке без потери своих свойств.
Так же можно отметить и биологическую составляющую меди. В больших количествах она является токсичной, а в малых — неотъемлемая часть существования организма человека. В различных состояниях в человеческом организме содержится около 150 мг меди. Суточная доза потребления меди является нормальной для человека весом 75 кг равной 2 мг.
Химическая номенклатура | Химия для специальностей
Результаты обучения
- Получение названий распространенных типов неорганических соединений с использованием систематического подхода
Номенклатура , набор правил для наименования вещей, важна в науке и во многих других ситуациях. В этом модуле описывается подход, который используется для обозначения простых ионных и молекулярных соединений, таких как NaCl, CaCO 3 и N 2 O 4 . Самые простые из них бинарные соединения , содержащие только два элемента, но мы также рассмотрим, как называть ионные соединения, содержащие многоатомные ионы, и один особый, очень важный класс соединений, известных как кислоты (последующее обсуждение в этом тексте будет сосредоточено на этих соединениях в большом количестве). деталь). Мы ограничим наше внимание здесь неорганическими соединениями, соединениями, которые состоят в основном из элементов, отличных от углерода, и будем следовать рекомендациям по номенклатуре, предложенным IUPAC. Правила для органических соединений, в которых углерод является основным элементом, будут рассмотрены в модуле по органической химии.
В этом модуле описывается подход, который используется для обозначения простых ионных и молекулярных соединений, таких как NaCl, CaCO 3 и N 2 O 4 . Самые простые из них бинарные соединения , содержащие только два элемента, но мы также рассмотрим, как называть ионные соединения, содержащие многоатомные ионы, и один особый, очень важный класс соединений, известных как кислоты (последующее обсуждение в этом тексте будет сосредоточено на этих соединениях в большом количестве). деталь). Мы ограничим наше внимание здесь неорганическими соединениями, соединениями, которые состоят в основном из элементов, отличных от углерода, и будем следовать рекомендациям по номенклатуре, предложенным IUPAC. Правила для органических соединений, в которых углерод является основным элементом, будут рассмотрены в модуле по органической химии.
Ионные соединения
Чтобы назвать неорганическое соединение, нам нужно рассмотреть ответы на несколько вопросов.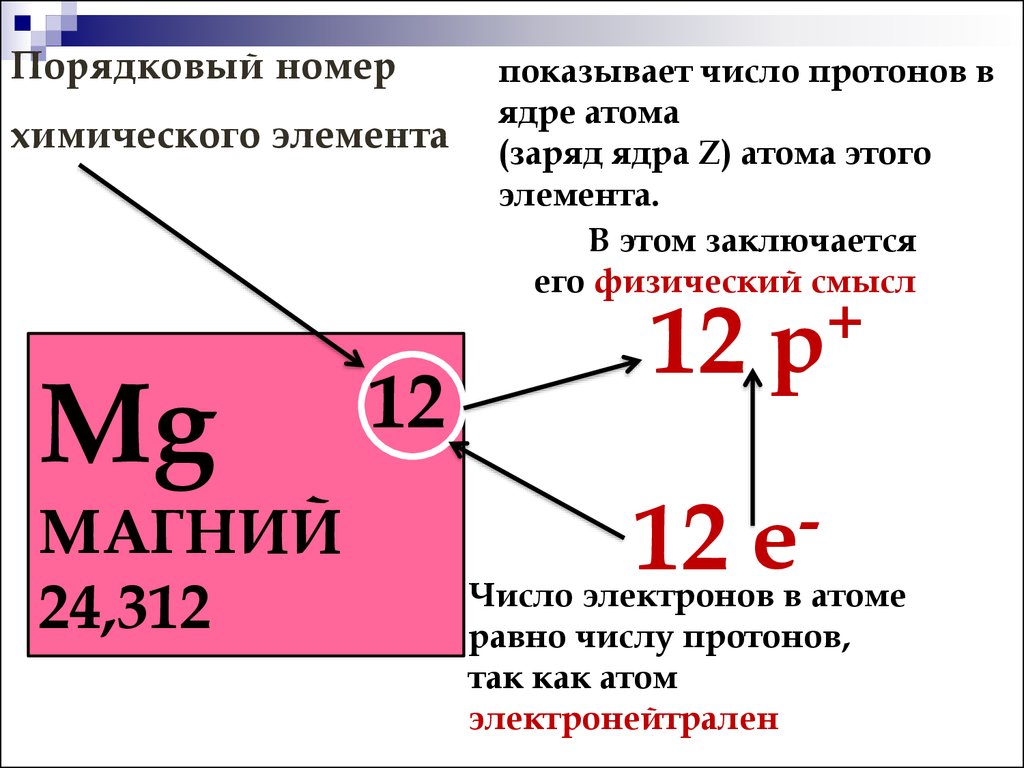 Во-первых, является ли соединение ионным или молекулярным? Если соединение является ионным, образует ли металл ионы только одного типа (фиксированный заряд) или более одного типа (переменный заряд)? Ионы одноатомные или многоатомные? Если соединение молекулярное, содержит ли оно водород? Если да, то содержит ли он также кислород? На основе ответов, которые мы получаем, мы помещаем соединение в соответствующую категорию, а затем называем его соответствующим образом.
Во-первых, является ли соединение ионным или молекулярным? Если соединение является ионным, образует ли металл ионы только одного типа (фиксированный заряд) или более одного типа (переменный заряд)? Ионы одноатомные или многоатомные? Если соединение молекулярное, содержит ли оно водород? Если да, то содержит ли он также кислород? На основе ответов, которые мы получаем, мы помещаем соединение в соответствующую категорию, а затем называем его соответствующим образом.
Соединения, содержащие только одноатомные ионы
Название бинарного соединения, содержащего одноатомные ионы, состоит из названия катиона (название металла), за которым следует название аниона (название неметаллического элемента с заменой окончания по суффиксу – ide ). Некоторые примеры приведены в таблице 1.
| Таблица 1. Названия некоторых ионных соединений | |
|---|---|
| NaCl, хлорид натрия | На 2 О, оксид натрия |
| KBr, калия бромид | CdS, сульфид кадмия |
| CaI 2 , кальция йодид | Mg 3 N 2 , нитрид магния |
| CsF, фторид цезия | Ca 3 P 2 , фосфид кальция |
| LiCl, хлорид лития | Ал 4 К 3 , карбид алюминия |
Соединения, содержащие многоатомные ионы
Соединения, содержащие многоатомные ионы, называются так же, как и соединения, содержащие только одноатомные ионы, за исключением того, что нет необходимости менять окончание на – или , поскольку суффикс уже присутствует в названии аниона. Примеры приведены в Таблице 2.
| Таблица 2. Названия некоторых многоатомных ионных соединений | ||
|---|---|---|
| KC 2 H 3 O 2 , ацетат калия | (NH 4 )Cl, хлорид аммония | |
| NaHCO 3 , бикарбонат натрия | CaSO 4 , сульфат кальция | |
| Al 2 (CO 3 ) 3 , карбонат алюминия | Mg 3 (PO 4 ) 2 , фосфат магния | |
Ионные соединения в ваших шкафах
Каждый день вы сталкиваетесь с большим количеством ионных соединений и используете их. Некоторые из этих соединений, где они находятся и для чего используются, перечислены в таблице 3. Посмотрите на этикетку или список ингредиентов на различных продуктах, которые вы будете использовать в течение следующих нескольких дней, и посмотрите, не столкнетесь ли вы с каким-либо из те, что в этой таблице, или найдите другие ионные соединения, которые вы теперь можете назвать или записать в виде формулы.
| Таблица 3. Ежедневные ионные соединения | |
|---|---|
| Ионное соединение | Использовать |
| NaCl, хлорид натрия | соль поваренная обыкновенная |
| KI, калия йодид | добавлен в «йодированную» соль для здоровья щитовидной железы |
| NaF, фторид натрия | ингредиент зубной пасты |
| NaHCO 3 , бикарбонат натрия | пищевая сода; используется в кулинарии (и как антацид) |
| Na 2 CO 3 , карбонат натрия | стиральная сода; используется в чистящих средствах |
| NaOCl, гипохлорит натрия | активный ингредиент бытового отбеливателя |
| CaCO 3 карбонат кальция | ингредиент антацидов |
| Mg(OH) 2 , гидроксид магния | ингредиент антацидов |
| Al(OH) 3 , гидроксид алюминия | ингредиент антацидов |
| NaOH, гидроксид натрия | щелочь; используется в качестве очистителя канализации |
| K 3 PO 4 , фосфат калия | пищевая добавка (многоцелевая) |
| MgSO 4 , сульфат магния | добавляется в очищенную воду |
| Na 2 HPO 4 , гидрофосфат натрия | средство против слеживания; используется в порошкообразных продуктах |
| Na 2 SO 3 , сульфит натрия | консервант |
Соединения, содержащие ион металла с переменным зарядом
Большинство переходных металлов могут образовывать два или более катиона с разными зарядами. Соединения этих металлов с неметаллами обозначаются тем же способом, что и соединения первой категории, за исключением того, что заряд иона металла указывается римской цифрой в скобках после названия металла. Заряд иона металла определяется из формулы соединения и заряда аниона. Например, рассмотрим бинарные ионные соединения железа и хлора. Железо обычно имеет заряд 2+ или 3+ (см. Молекулярные и ионные соединения), а формулы двух соответствующих соединений: FeCl 2 и FeCl 3 . Самое простое название «хлорид железа» в этом случае будет двусмысленным, так как не делает различий между этими двумя соединениями. В подобных случаях заряд иона металла указывается римской цифрой в круглых скобках сразу после названия металла. Эти два соединения затем однозначно называются хлоридом железа (II) и хлоридом железа (III) соответственно. Другие примеры приведены в Таблице 4.
Соединения этих металлов с неметаллами обозначаются тем же способом, что и соединения первой категории, за исключением того, что заряд иона металла указывается римской цифрой в скобках после названия металла. Заряд иона металла определяется из формулы соединения и заряда аниона. Например, рассмотрим бинарные ионные соединения железа и хлора. Железо обычно имеет заряд 2+ или 3+ (см. Молекулярные и ионные соединения), а формулы двух соответствующих соединений: FeCl 2 и FeCl 3 . Самое простое название «хлорид железа» в этом случае будет двусмысленным, так как не делает различий между этими двумя соединениями. В подобных случаях заряд иона металла указывается римской цифрой в круглых скобках сразу после названия металла. Эти два соединения затем однозначно называются хлоридом железа (II) и хлоридом железа (III) соответственно. Другие примеры приведены в Таблице 4.
| Таблица 4. Названия некоторых ионных соединений переходных металлов | |
|---|---|
| Ионное соединение переходного металла | Имя |
| FeCl 2 | железа(II) хлорид |
| FeCl 3 | железа(III) хлорид |
| Рт. 2 О | оксид ртути(I) |
| HgO | оксид ртути(II) |
| СНФ 2 | фторид олова(II) |
| СНФ 4 | фторид олова(IV) |
Устаревшая номенклатура использовала суффиксы – ic и – ous для обозначения металлов с более высоким и более низким зарядом соответственно: Хлорид железа(III), FeCl 3 , ранее назывался хлоридом железа, и хлорид железа (II), FeCl 2 , был известен как хлорид железа. Хотя научное сообщество в значительной степени отказалось от этого соглашения об именах, оно по-прежнему используется в некоторых сегментах промышленности. Например, вы можете увидеть слова фторид олова на тюбике зубной пасты. Это представляет собой формулу SnF 2 , которая более правильно называется фторидом олова (II). Другим фторидом олова является SnF 4 , который ранее назывался фторидом олова, но теперь называется фторидом олова (IV).
Например, вы можете увидеть слова фторид олова на тюбике зубной пасты. Это представляет собой формулу SnF 2 , которая более правильно называется фторидом олова (II). Другим фторидом олова является SnF 4 , который ранее назывался фторидом олова, но теперь называется фторидом олова (IV).
Ионные гидраты
Ионные соединения, которые содержат молекулы воды в качестве неотъемлемых компонентов своих кристаллов, называются гидратами. Название ионного гидрата получено путем добавления термина к названию безводного (что означает «не гидратированный») соединения, которое указывает количество молекул воды, связанных с каждой формульной единицей соединения. Добавленное слово начинается с греческого префикса, обозначающего количество молекул воды (см. табл. 5), и заканчивается словом «гидрат». Например, безводное соединение сульфат меди (II) также существует в виде гидрата, содержащего пять молекул воды, и называется пентагидратом сульфата меди (II). Стиральная сода — это общее название гидрата карбоната натрия, содержащего 10 молекул воды; систематическое название – декагидрат карбоната натрия.
Стиральная сода — это общее название гидрата карбоната натрия, содержащего 10 молекул воды; систематическое название – декагидрат карбоната натрия.
Формулы для ионных гидратов записываются путем добавления вертикально расположенной точки, коэффициента, представляющего количество молекул воды, и формулы воды. Два примера, упомянутые в предыдущем абзаце, представлены формулами
[латекс]\text{пентагидрат сульфата меди(II}}\text{ CuSO}_{4}\cdot{5}\text{H}_ {2}\text{O}[/latex]
[латекс]\text{декагидрат карбоната натрия}\text{ Na}_{2}\text{CO}_{3}\cdot{10}\text{ Н}_{2}\текст{О}[/латекс]
| Таблица 5. Префиксы номенклатуры | ||||
|---|---|---|---|---|
| Номер | Префикс | Номер | Префикс | |
| 1 (иногда опускается) | моно- | 6 | шестигранник | |
| 2 | ди- | 7 | гепта- | |
| 3 | три- | 8 | окта- | |
| 4 | тетра- | 9 | нон- | |
| 5 | пента- | 10 | дека- | |
Пример 1:
Ионные ионные соединенияНазовите следующие ионные соединения, которые содержат металл, который может иметь более одного ионного заряда:
- Fe 2 S 3 8
- Fe 2 S 3 69
- Fe 2 S 3 669
- FE 2 S 3 669
- CuSe
- GaN
- MgSO 4 ·7H 2 О
- Ти 2 (СО 4 ) 3
Показать решение
Check Your LearningНапишите формулы следующих ионных соединений:
- фосфид хрома(III)
- ртути(II) сульфид
- фосфат марганца(II)
- оксид меди(I)
- железа(III) хлорид дигидрат
Показать решение
Эрин Брокович и Загрязнение хромом
В начале 1990-х клерк юридического дела Эрин Брокович (рис. 1) обнаружила высокий уровень серьезных заболеваний в маленьком городке Хинкли, штат Калифорния. Ее расследование в конечном итоге связало болезни с грунтовыми водами, загрязненными Cr (VI), которые Pacific Gas & Electric (PG&E) использовала для борьбы с коррозией в близлежащем газопроводе. Как показано в фильме «Эрин Брокович » (за который Джулия Робертс получила «Оскар»), Эрин и адвокат Эдвард Масри подали в суд на PG&E за загрязнение воды возле Хинкли в 1919 году.93. Урегулирование, которое они выиграли в 1996 году — 333 миллиона долларов — было самой крупной суммой, когда-либо присужденной по иску прямого действия в США на тот момент.
1) обнаружила высокий уровень серьезных заболеваний в маленьком городке Хинкли, штат Калифорния. Ее расследование в конечном итоге связало болезни с грунтовыми водами, загрязненными Cr (VI), которые Pacific Gas & Electric (PG&E) использовала для борьбы с коррозией в близлежащем газопроводе. Как показано в фильме «Эрин Брокович » (за который Джулия Робертс получила «Оскар»), Эрин и адвокат Эдвард Масри подали в суд на PG&E за загрязнение воды возле Хинкли в 1919 году.93. Урегулирование, которое они выиграли в 1996 году — 333 миллиона долларов — было самой крупной суммой, когда-либо присужденной по иску прямого действия в США на тот момент.
Рисунок 1. (a) Эрин Брокович обнаружила, что Cr(IV), используемый PG&E, загрязнил систему водоснабжения Хинкли, Калифорния. (б) Ион Cr(VI) часто присутствует в воде в виде многоатомных ионов хромата CrO 4 2– (слева) и дихромата Cr 2 O 7 2– (справа) .
Соединения хрома широко используются в промышленности, например, для хромирования, производства красителей, в качестве консервантов и для предотвращения коррозии в воде градирни, как это произошло недалеко от Хинкли. В окружающей среде хром существует преимущественно в форме Cr(III) или Cr(VI). Cr(III), входящий в состав многих витаминных и пищевых добавок, образует соединения, плохо растворимые в воде, малотоксичен. Но Cr(VI) гораздо более токсичен и образует соединения, достаточно растворимые в воде. Воздействие небольших количеств Cr(VI) может привести к повреждению дыхательной, желудочно-кишечной и иммунной систем, а также почек, печени, крови и кожи.
В окружающей среде хром существует преимущественно в форме Cr(III) или Cr(VI). Cr(III), входящий в состав многих витаминных и пищевых добавок, образует соединения, плохо растворимые в воде, малотоксичен. Но Cr(VI) гораздо более токсичен и образует соединения, достаточно растворимые в воде. Воздействие небольших количеств Cr(VI) может привести к повреждению дыхательной, желудочно-кишечной и иммунной систем, а также почек, печени, крови и кожи.
Несмотря на усилия по очистке, загрязнение грунтовых вод Cr(VI) остается проблемой в Хинкли и других местах по всему миру. Исследование, проведенное в 2010 году Рабочей группой по окружающей среде, показало, что из 35 протестированных городов США в 31 уровень Cr(VI) в водопроводной воде был выше, чем цель общественного здравоохранения, составляющая 0,02 части на миллиард, установленная Калифорнийским агентством по охране окружающей среды.
Молекулярные (ковалентные) соединения
Характеристики связывания неорганических молекулярных соединений отличаются от характеристик ионных соединений, и они также называются с использованием другой системы. Заряды катионов и анионов определяют их соотношение в ионных соединениях, поэтому указание названий ионов дает достаточно информации для определения химических формул. Однако, поскольку ковалентная связь допускает значительные вариации соотношений комбинаций атомов в молекуле, названия молекулярных соединений должны явно идентифицировать эти соотношения.
Заряды катионов и анионов определяют их соотношение в ионных соединениях, поэтому указание названий ионов дает достаточно информации для определения химических формул. Однако, поскольку ковалентная связь допускает значительные вариации соотношений комбинаций атомов в молекуле, названия молекулярных соединений должны явно идентифицировать эти соотношения.
Соединения, состоящие из двух элементов
Когда два неметаллических элемента образуют молекулярное соединение, часто возможны несколько соотношений комбинаций. Например, углерод и кислород могут образовывать соединения CO и CO 2 . Поскольку это разные вещества с разными свойствами, они не могут оба иметь одинаковое название (нельзя оба называться оксидом углерода). Чтобы справиться с этой ситуацией, мы используем метод именования, который чем-то похож на тот, который используется для ионных соединений, но с добавлением префиксов для указания количества атомов каждого элемента. Название более металлического элемента (тот, что дальше слева и/или внизу таблицы Менделеева) стоит первым, за ним следует название более неметаллического элемента (тот, что дальше справа и/или вверху) с окончанием изменен на суффикс – иде . Номера атомов каждого элемента обозначаются греческими префиксами, показанными выше в таблице 5.
Номера атомов каждого элемента обозначаются греческими префиксами, показанными выше в таблице 5.
Когда присутствует только один атом первого элемента, префикс моно – обычно удаляется из этой части. Таким образом, CO называется окисью углерода, а CO 2 — двуокисью углерода. Когда две гласные стоят рядом, a в греческом префиксе обычно опускается. Некоторые другие примеры показаны в таблице 6.
| Таблица 6. Названия некоторых молекулярных соединений, состоящих из двух элементов | ||||
|---|---|---|---|---|
| Соединение | Имя | Соединение | Имя | |
| СО 2 | диоксид серы | БКл 3 | трихлорид бора | |
| СО 3 | триоксид серы | СФ 6 | гексафторид серы | |
| НЕТ 2 | азота диоксид | ПФ 5 | пятифтористый фосфор | |
| Н 2 О 4 | тетраоксид диазота | П 4 О 10 | декаоксид тетрафосфора | |
| Н 2 О 5 | пятиокись азота | ЕСЛИ 7 | йод гептафторид | |
Есть несколько общих имен, с которыми вы столкнетесь, продолжая изучать химию. Например, хотя NO часто называют оксидом азота, его собственное название — монооксид азота. Аналогично N 2 O известен как закись азота, даже несмотря на то, что в наших правилах указано название закись азота. (И H 2 O обычно называют водой, а не монооксидом дигидрогена.) Вам следует запоминать общие названия соединений, когда вы с ними сталкиваетесь.
Например, хотя NO часто называют оксидом азота, его собственное название — монооксид азота. Аналогично N 2 O известен как закись азота, даже несмотря на то, что в наших правилах указано название закись азота. (И H 2 O обычно называют водой, а не монооксидом дигидрогена.) Вам следует запоминать общие названия соединений, когда вы с ними сталкиваетесь.
Пример 2:
Наименование ковалентных соединенийНазовите следующие ковалентные соединения:
- SF 6
- Н 2 О 3
- Класс 2 О 7
- П 4 О 6
Показать решение
Check Your LearningНапишите формулы следующих соединений:
- пентахлорид фосфора
- монооксид диазота
- гептафторид йода
- четыреххлористый углерод
Показать решение
Бинарные кислоты
Некоторые соединения, содержащие водород, относятся к важному классу веществ, известных как кислоты. Химия этих соединений будет рассмотрена более подробно позже, а сейчас достаточно отметить, что многие кислоты выделяют ионы водорода, H + при растворении в воде. Чтобы обозначить это особое химическое свойство, смеси воды с кислотой дается название, производное от названия соединения. Если соединение представляет собой бинарную кислоту (состоящую из водорода и одного другого неметаллического элемента):
Химия этих соединений будет рассмотрена более подробно позже, а сейчас достаточно отметить, что многие кислоты выделяют ионы водорода, H + при растворении в воде. Чтобы обозначить это особое химическое свойство, смеси воды с кислотой дается название, производное от названия соединения. Если соединение представляет собой бинарную кислоту (состоящую из водорода и одного другого неметаллического элемента):
- Слово «водород» заменяется префиксом гидро-
- Название другого неметаллического элемента изменяется путем добавления суффикса – ic
- Слово «кислота» добавлено вторым словом
Например, когда газ HCl (хлороводород) растворяется в воде, раствор называется соляной кислотой . Несколько других примеров этой номенклатуры показаны в таблице 7.
| Таблица 7. Названия некоторых простых кислот | |
|---|---|
| Наименование газа | Наименование кислоты |
| HF ( г ), фтористый водород | HF( aq ), плавиковая кислота |
| HCl ( г ), хлористый водород | HCl ( водный ), соляная кислота |
| HBr( г ), бромистый водород | HBr( водный ), бромистоводородная кислота |
| HI( г ), йодистый водород | HI( водный ), йодистоводородная кислота |
| H 2 S( г ), сероводород | H 2 S( aq ), сероводородная кислота |
Оксикислоты
Многие соединения, содержащие три или более элементов (например, органические соединения или координационные соединения), подчиняются специальным правилам номенклатуры, которые вы узнаете позже. Однако мы кратко обсудим важные соединения, известные как оксикислоты , соединения, которые содержат водород, кислород и по крайней мере еще один элемент и связаны таким образом, что придают кислотные свойства соединению (подробности вы узнаете об этом позже). Типичные оксикислоты состоят из водорода в сочетании с многоатомным кислородсодержащим ионом. Назвать оксикислоты:
Однако мы кратко обсудим важные соединения, известные как оксикислоты , соединения, которые содержат водород, кислород и по крайней мере еще один элемент и связаны таким образом, что придают кислотные свойства соединению (подробности вы узнаете об этом позже). Типичные оксикислоты состоят из водорода в сочетании с многоатомным кислородсодержащим ионом. Назвать оксикислоты:
- Пропустить “водород”
- Начните с корневого имени аниона
- Заменить – ate на – ic , или – ite на – ous
- Добавить «кислота»
Например, рассмотрите H 2 CO 3 (который у вас может возникнуть соблазн назвать «гидрокарбонатом»). Чтобы назвать это правильно, «водород» опущен; – ate карбоната заменить на – ic ; и прибавляется кислота — поэтому ее имя — угольная кислота. Другие примеры приведены в Таблице 8. Существуют некоторые исключения из общего метода именования (например, H 2 SO 4 называется серной кислотой, а не серной кислотой, а H 2 SO 3 — сернистой, а не сернистой кислотой).
| Таблица 8. Названия распространенных оксикислот | ||
|---|---|---|
| Формула | Название аниона | Название кислоты |
| HC 2 H 3 O 2 | ацетат | уксусная кислота |
| HNO 3 | нитрат | азотная кислота |
| HNO 2 | нитрит | азотистая кислота |
| HClO 4 | перхлорат | хлорная кислота |
| H 2 CO 3 | карбонат | угольная кислота |
| Н 2 SO 4 | сульфат | серная кислота |
| H 2 SO 3 | сульфит | сернистая кислота |
| Н 3 Заказ на покупку 4 | фосфат | фосфорная кислота |
Видеообзор: Язык химии
Научиться говорить о химии может быть похоже на изучение иностранного языка, но Хэнк здесь, чтобы помочь вам с некоторыми простыми правилами, которые помогут вам научиться говорить на химическом, как носитель языка.
Вы можете просмотреть стенограмму «Как говорить на химическом языке: Ускоренный курс химии № 11» здесь (откроется в новом окне).
Основные понятия и резюме
Химики используют правила номенклатуры для четкого обозначения соединений. Ионные и молекулярные соединения называются несколько по-разному. Бинарные ионные соединения обычно состоят из металла и неметалла. Сначала пишется название металла, затем название неметалла с измененным окончанием на – ide . Например, K 2 O называется оксидом калия. Если металл может образовывать ионы с разными зарядами, после названия металла в скобках следует римская цифра, указывающая его заряд. Таким образом, FeCl 2 представляет собой хлорид железа (II), а FeCl 3 представляет собой хлорид железа (III).
Некоторые соединения содержат многоатомные ионы; следует запомнить названия обычных многоатомных ионов. Молекулярные соединения могут образовывать соединения с различным соотношением их элементов, поэтому префиксы используются для указания количества атомов каждого элемента в молекуле соединения. Примеры включают SF 6 , гексафторид серы, и N 2 O 4 , четырехокись азота. Кислоты представляют собой важный класс соединений, содержащих водород и имеющих особые правила номенклатуры. Бинарные кислоты называются с использованием префикса 9.0027 hydro-, заменив суффикс –ide на –ic и добавив слово «кислота»; HCl – соляная кислота. Оксикислоты названы путем изменения окончания аниона на – ic и добавления «кислоты»; H 2 CO 3 – угольная кислота.
Попробуйте
- Назовите следующие соединения:
- CsCl
- БаО
- К 2 С
- BeCl 2
- ХБр
- Альф 3
- Назовите следующие соединения:
- НаФ
- Руб 2 О
- БКл 3
- Н 2 Се
- П 4 О 6
- ICl 3
- Напишите формулы следующих соединений:
- рубидий бромид
- селенид магния
- оксид натрия
- хлорид кальция
- фтористый водород
- фосфид галлия
- бромид алюминия
- сульфат аммония
- Напишите формулы следующих соединений:
- карбонат лития
- перхлорат натрия
- бария гидроксид
- карбонат аммония
- серная кислота
- ацетат кальция
- фосфат магния
- сульфит натрия
- Напишите формулы следующих соединений:
- диоксид хлора
- тетраоксид диазота
- фосфид калия
- сульфид серебра(I)
- нитрид алюминия
- диоксид кремния
- Напишите формулы следующих соединений:
- хлорид бария
- нитрид магния
- диоксид серы
- трихлорид азота
- триоксид диазота
- олово(IV) хлорид
- Каждое из следующих соединений содержит металл, который может иметь более одного ионного заряда.
 Назовите эти соединения:
Назовите эти соединения:- Cr 2 O 3
- FeCl 2
- CrO 3
- TiCl 4
- СоО
- MoS 2
- Каждое из следующих соединений содержит металл, который может иметь более одного ионного заряда. Назовите эти соединения:
- NiCO 3
- МоО 3
- Co(NO 3 ) 2
- В 2 О 5
- MnO 2
- Fe 2 O 3
- Следующие ионные соединения содержатся в обычных бытовых товарах. Напишите формулы каждого соединения:
- фосфат калия
- сульфат меди(II)
- хлорид кальция
- титана диоксид
- нитрат аммония
- бисульфат натрия (общепринятое название гидросульфата натрия)
- Следующие ионные соединения содержатся в обычных бытовых товарах.
 Назовите каждое из соединений:
Назовите каждое из соединений:- Ca(H 2 PO 4 ) 2
- FeSO 4
- CaCO 3
- MgO
- NaNO 2
- КИ
- Каковы названия IUPAC следующих соединений?
- диоксид марганца
- хлорид ртути (Hg 2 Cl 2 )
- нитрат железа [Fe(NO 3 ) 3 ]
- тетрахлорид титана
- бромид меди (CuBr 2 )
Показать выбранные решения
Глоссарий
бинарная кислота: соединение, содержащее водород и еще один элемент, связанные таким образом, что придает соединению кислотные свойства (способность выделять ионы H + при растворении в воде)
бинарное соединение: Соединение , содержащее два разных элемента.
номенклатура: система правил наименования объектов интереса
оксикислота: соединение, содержащее водород, кислород и еще один элемент, связанное таким образом, что придает соединению кислотные свойства (способность выделять ионы H + при растворении в воде)
В алфавитном порядке:Актиний (89)Алюминий (13, Великобритания) Алюминий (13, США) Америций (95) Сурьма (51) Аргон (18) Мышьяк (33) Астатин (85) Барий (56) Берклиум (97) Берилий (4) Висмут (83) Борий (107) Бор (5) Бром (35) Кадмий (48) Цезий (55, Великобритания) Кальций (20) Калифорния (98) Углерод (6) Церий (58) Цезий (55, США) Хлор (17) Хром (24) Кобальт (27) Коперниций (112) Медь (29) Куриум (96) Дармстатиум (110) Дубниум (105) Диспрозий (66) Эйнштейний (99) Эрбий (68) Европий (63) Фермий (100) Флеровий (114) Фтор (9) Франций (87) Гадолиний (64) Галлий (31) Германий (32) Золото (79) Гафний (72) Хассиум (108) Гелий (2) Гольмий (67) Водород (1) Индий (49) Йод (53) Иридиум (77) Железо (26) Криптон (36) Лантан (57) Лоуренсиум (103) Свинец (82) Литий (3) Ливерморий (116) Лютеций (71) Магний (12) Марганец (25) Мейтнериум (109) Менделевий (101) Меркурий (80) Молибден (42) Московиум (115) Неодим (60) Неон (10) Нептуний (93) Никель (28) Нихоний (113) Ниобий (41) Азот (7) Нобелий (102) Оганесон (118) Осмий (76) Кислород (8) Палладий (46) Фосфор (15) Платина (78) Плутоний (94) Полоний (84) Калий (19) Празеодим (59) Прометий (61) Протактиний (91) Радий (88) Радон (86) Рений (75) Родий (45) Рентгений (111) Рубидий (37) Рутений (44) Резерфордиум (104) Самарий (62) Скандий (21) Сиборгиум (106) Селен (34) Кремний (14) Серебро (47) Натрий (11) Стронций (38) Сера (16) Сера (16) Тантал (73) Технеций (43) Теллур (52) Теннессин (117) Тербий (65) Таллий (81) Торий (90) Тулий (69) Олово (50) Титан (22) Вольфрам (74) Уран (92) Ванадий (23) Ксенон (54) Иттербий (70) Иттрий (39) Цинк (30) Цирконий (40) | Химический элемент однозначно характеризуется своими атомными номерами (Z). Впервые было продемонстрировано, что атомный номер является однозначной измеримой физической величиной. Анри Мозли (1887–1915), 1913 г. (Закон Мозли в рентгеновских спектрах). Мозли был убит в Битва при Галлиполи 10 августа 1915. Ему было 27 лет, и большинство экспертов сходятся во мнении, что в 1916 году он должен был получить Нобелевскую премию. (в том году премий не присуждалось, кроме литературы). Британские власти изменили правила прохождения боевой службы после его смерти. До этого химикам приходилось полагаться на массовые числа (молярные массы).
в конечном итоге на основе весовых соотношений газов низкого давления с использованием
Закон Авогадро (1811 г.).
Менделеев (1834-1907)
сделал истинную схему нумерации ясной с ранней версией (1869 г.)
вышеприведенной таблицы, где он присвоил возрастание атомных номеров в основном в соответствии с наблюдаемыми периодическими вариациями
химических свойств. История периодической таблицы |
Ранние периодические таблицы (24:45) Питер Уотерс (Периодическая таблица видео, 14 июня 2019 г. Чтобы точно присвоить атомные номера известным химическим элементам, эти пионеры должны были предположить, что были исключения из обычного увеличения массы с атомным номером. Например, кобальт (Co, Z = 27, 58,9 г) на самом деле немного тяжелее, чем следующий элемент, никель (Ni, Z=28, 58,7 г). Что еще более важно, Менделеев догадался, что некоторые пробелы возникли из-за к отсутствующим атомным номерам еще не открытых элементов… Массовые числа часто близки к целым числам, но не всегда.
Например, Шееле
(1742-1786) открыл в 1774 г.
эта соляная кислота
состоял из водорода и чего-то еще, о чем он догадался
быть оксидом какого-то нового элемента с массовым числом 19,45,
условное название «muriaticum» (предубеждение той эпохи,
сформулирован Лавуазье в 1777 г.
заключалась в том, что все кислоты должны содержать кислород).
Опровержение предубеждений Лавуазье и догадок Шееле, Хамфри Дэви
(1778-1829 гг.) показал в 1810 году, что muriaticum не существует. Причина, по которой массовые числа для многих важных элементов близки к целым числам но не для некоторых других, в том числе хлора, не было понято, пока не появилось понятие изотоп появился, в 1913 г. Великая неразбериха ушедшей эпохи полностью разрешается периодическая таблица элементов , структуру которой стоит запомнить:
О лантаноидах (элементы 57–71) см. Более простая американская мнемоника для лантаноидов (элементы 57-71): Основная классификация :
Приведенная выше группировка по столбцам дополняется важными отличиями, перечисленными ниже. Ранние учебники (до 1950-х годов) исключали группы 11 и 12 из списка.
переходные металлы.
Элементы 11-й группы в настоящее время повсеместно признаны переходными металлами. Актиниды обычно классифицируются как редкоземельных элементов из-за их очевидного химического состава. сходство с лантаноидами, без одобрения IUPAC (этот вопрос относительно не важен из-за отсутствия химического применения актинидов за пределами ядерная техника).
Как видно из приведенной выше таблицы,
лихорадочные поиски элементов 85 и 87 (до Второй мировой войны)
когда-то осталось несколько номенклатурных обломков.
Он также оставил по крайней мере один пример из учебника патологических наук (воспринимаемые наблюдения на пороге обнаруживаемости, которые превращаются в псевдонаука ). Так называемый (воображаемый) Эффект Эллиссона пропагандировался
Фред С. Эллисон
(1882-1974) далеко за пределами призвания
научный долг, даже после того, как его метод был опровергнут
Г. Текущие официальные процедуры для введения в действие названия новых элементов были приняты уже после заселения (1997) крупного спора об именах (Трансфермиумная война) про элементы 104, 105 и 106. В 1997 году элемент 109 (мейтнерий, Mt) был назван в честь Лиз Мейтнер (1878-1968). Редкая честь получила широкое признание. имеет какое-то посмертное извинение за то, что не поделился Нобелевская премия (Химия 1944) награжден Otto Hahn за совместную работу. Это также был способ почтить память команды Hahn/Meitner под названием Hahnium . (для элемента 105) пришлось навсегда исключить, чтобы избежать путаницы после война имен . 19
Февраль 2010 года (537 года 90 516 летия
рождения Коперника) элемент 112 был
официально дано название, которое находилось на рассмотрении с
июль 2009 г.: Copernicium (Cn). 31 В мае 2012 года были официально названы элементы 114 и 116. Флеровиум и Ливермориум соответственно. Эти имена находились на рассмотрении с декабрь 2011 г. 12 августа 2012 года японская команда RIKEN
(Rikagaku Kenkyujo = Институт физико-химических исследований)
опубликовали свое наблюдение за
цепочка распада атома Уут-278,
включая хорошо известный альфа-распад Db-262 в Lr-258, который четко идентифицирует
элемент 113 как источник этой цепочки распада.
Это интерпретируется как определенное открытие 113, для которого были получены более неоднозначные результаты. 2015-12-30,
IUPAC объявил о завершении окончательного рассмотрения заявлений об обнаружении
для элементов 113, 115, 117 и 118 и признал их удовлетворительными.
IUPAC теперь приглашает соответствующие группы исследователей предложить имена и символы. 08.06.2016 предпоследний шаг принял форму пресс-релиз IUPAC объявляя четыре предложенных имени и открытие общественного обсуждения о них, который должен закончиться в ноябре 2016 года.
Электронные конфигурации:Квантовое состояние движения электрона вокруг ядра полностью описывается в терминах из следующих четырех квантовых чисел : Принцип исключения Паули утверждает, что два электрона
не могут находиться в одном и том же квантовом состоянии.
Минимальная энергия электронного облака, окружающего одинокое ядро, равна
достигается, когда электроны занимают доступное пространство подоболочки в
порядок слева, начиная с подоболочки 1s.
Это упрощенная версия принципа Aufbau .
объясняет структуру периодической таблицы элементов,
где элементы со схожими химическими свойствами перечислены в
тот же столбец: химические свойства элемента
в основном зависит от валентность электроны, расположенные в самых внешних подоболочках, которые обычно
энергетически наименее выгодный
(с оговорками, указанными ниже, в случае подоболочек “f”). Электронную конфигурацию вокруг ядра можно обобщить, перечислив все непустые подоболочек в указанном выше порядке возрастания энергий (1s, 2s, 2p, 3s и т. д.) с верхний индекс, указывающий количество электронов в каждом. Перераспределением электронов на орбитали одной и той же подоболочки обычно пренебрегают. Дополнительный символ термина иногда добавляется для лучшего описания наземной конфигурации. Его можно получить с помощью правило Хунда, набор эмпирических рецептов Фридриха Хунда (1896-1997). Электроны избегают спаривания на одной и той же орбитали, если только все орбитали подоболочки не заняты. Для краткости конфигурация благородного газа может быть обозначена его символом в квадратных скобках.
[в качестве префикса] в электронной конфигурации последующих элементов.
Обратите внимание, что все подоболочки благородных газов заполнены.
Химическая инертность обусловлена внешней оболочкой, содержащей в общей сложности 8 электронов.
В периодической таблице последовательные «переходные металлы»
соответствуют «заполнению» подоболочки «d» (от 1 до 10 электронов). Для полноты следует отметить, что энергетические уровни некоторых подоболочек настолько близко, что спаривание электронов может привести к нескольким исключениям (в частности, для Cr и Cu) при применении упрощенного Принцип Ауфбау представлен выше.
Теоретически химия даже высокорадиоактивных тяжелых элементов может быть
точно вычислены из хорошо известных законов квантовой
электродинамика ( как если бы радиоактивности не существовало). Происхождение элементов: Нуклеосинтез (Википедия) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Отец периодической таблицы
Вспомните дни, когда вы занимались химией. Какие инструменты были для вас наиболее полезными? Твои очки? Лабораторный халат? Может быть, это была тетрадь, в которой вы яростно строчили, чтобы ничего не забыть? Возможно, вы забыли еще один инструмент, который оказался чрезвычайно полезным для поколений студентов и ученых: периодическая таблица элементов.
Одно из самых значительных достижений в науке, периодическую таблицу, можно найти повсюду: от квестов до занавесок для душа, кружек, нашего блога о стекле и учебных аудиторий по всему миру. Периодическая таблица представляет собой общий язык, который могут расшифровать химики, а также люди с различным научным или ненаучным образованием. Он состоит из аккуратно расположенной таблицы с согласованными по цвету строками и столбцами элементов (вещество, атомы которого имеют одинаковое количество протонов), все с одно- или двухбуквенными обозначениями, а также несколько чисел, представляющих химические свойства, нацарапанные в каждом квадрате. В этом году исполняется 150 9 лет.0515-й -й годовщины таблицы Менделеева, и это во многом приписывается одному гениальному уму Дмитрию Менделееву.
Молодость
Дмитрий Менделеев в 1897 году Выросший на окраине маленького городка Тобольскин в Сибири (род. пожар на рабочем месте на стекольном заводе семьи его матери. Переехав в Петербург с братом и матерью, Менделеев был принят в Петербургский университет, где в 1856 г. успешно защитил магистерскую диссертацию о соотношениях между объемами веществ и их кристаллографическими и химическими свойствами. Менделеев получил двухлетнее государственное финансирование для обучения за границей и таким образом оказался в Гейдельбергском университете в Германии. Там он проводил исследования по самым разным темам, от испарения и поверхностного натяжения до межмолекулярных сил, которые опосредуют взаимодействие между молекулами. Вернувшись в Санкт-Петербург, он возобновил свои преподавательские обязанности и сделал плодотворную карьеру, опубликовав научно-исследовательские статьи и учебник по органической химии. Только когда университет назначил его профессором общей химии (и когда он начал писать учебник по неорганической химии), его внимание переключилось на идею упорядоченного расположения химических элементов в соответствии с их свойствами.
Переехав в Петербург с братом и матерью, Менделеев был принят в Петербургский университет, где в 1856 г. успешно защитил магистерскую диссертацию о соотношениях между объемами веществ и их кристаллографическими и химическими свойствами. Менделеев получил двухлетнее государственное финансирование для обучения за границей и таким образом оказался в Гейдельбергском университете в Германии. Там он проводил исследования по самым разным темам, от испарения и поверхностного натяжения до межмолекулярных сил, которые опосредуют взаимодействие между молекулами. Вернувшись в Санкт-Петербург, он возобновил свои преподавательские обязанности и сделал плодотворную карьеру, опубликовав научно-исследовательские статьи и учебник по органической химии. Только когда университет назначил его профессором общей химии (и когда он начал писать учебник по неорганической химии), его внимание переключилось на идею упорядоченного расположения химических элементов в соответствии с их свойствами.
Рождение периодического закона
Рукописный набросок периодической таблицы Менделеева с элементами, упорядоченными по атомному весу. Фото кредит.
Фото кредит. Недовольный текущим российским учебником по неорганической химии, Менделеев задался целью написать свой вариант. Результатом его решимости стала книга «Основы химии » или «Принципы химии» (любознательные читатели могут найти ее в Библиотеке редких книг и специальных коллекций Иллинойского университета в Урбана-Шампейн). Пока он писал одну из глав, он определил закономерность, в которой « Элементы, расположенные в соответствии с их атомным весом, обнаруживают кажущуюся периодичность свойств. » После дальнейших параллельных сравнений Менделеев понял, что элементы могут быть организованы по их атомным весам. Каждый элемент имеет свой атомный вес, отличный от всех других элементов. Эти веса состоят из субатомных частиц, которые охватывают этот конкретный элемент. Менделеев заметил, что некоторые элементы с почти одинаковым атомным весом имеют общие свойства друг с другом. Используя атомные веса, чтобы записать все 63 известных элемента на отдельных карточках для заметок и расположив их, как в пасьянсе, Менделеев пришел к своей таблице элементов. Его открытие стало известно как Периодический закон, который гласит, что сходные свойства периодически повторяются, когда элементы располагаются в порядке возрастания атомного веса. Как показано в оригинальной рукописной периодической таблице Менделеева, элементы были организованы по сходным характеристикам (горизонтальные строки) и возрастанию атомного веса (вертикальные столбцы). Менделеев пришел к выводу, что «размер атомного веса определяет природу элементов». Взволнованный своим открытием, Менделеев спешно отправил свою таблицу в типографию для своего учебника и для представления Русскому химическому обществу. Однако, к его большому огорчению, другие химики не проявили особого интереса к сформулированному им закону, когда его коллега профессор Николай Меншуткин представил свою периодическую таблицу (Менделеев был болен) Русскому физико-химическому обществу в марте 1869 года.. Несмотря на то, что его первое выступление не было хорошо встречено, Менделеев не отказался от своего открытия.
Его открытие стало известно как Периодический закон, который гласит, что сходные свойства периодически повторяются, когда элементы располагаются в порядке возрастания атомного веса. Как показано в оригинальной рукописной периодической таблице Менделеева, элементы были организованы по сходным характеристикам (горизонтальные строки) и возрастанию атомного веса (вертикальные столбцы). Менделеев пришел к выводу, что «размер атомного веса определяет природу элементов». Взволнованный своим открытием, Менделеев спешно отправил свою таблицу в типографию для своего учебника и для представления Русскому химическому обществу. Однако, к его большому огорчению, другие химики не проявили особого интереса к сформулированному им закону, когда его коллега профессор Николай Меншуткин представил свою периодическую таблицу (Менделеев был болен) Русскому физико-химическому обществу в марте 1869 года.. Несмотря на то, что его первое выступление не было хорошо встречено, Менделеев не отказался от своего открытия.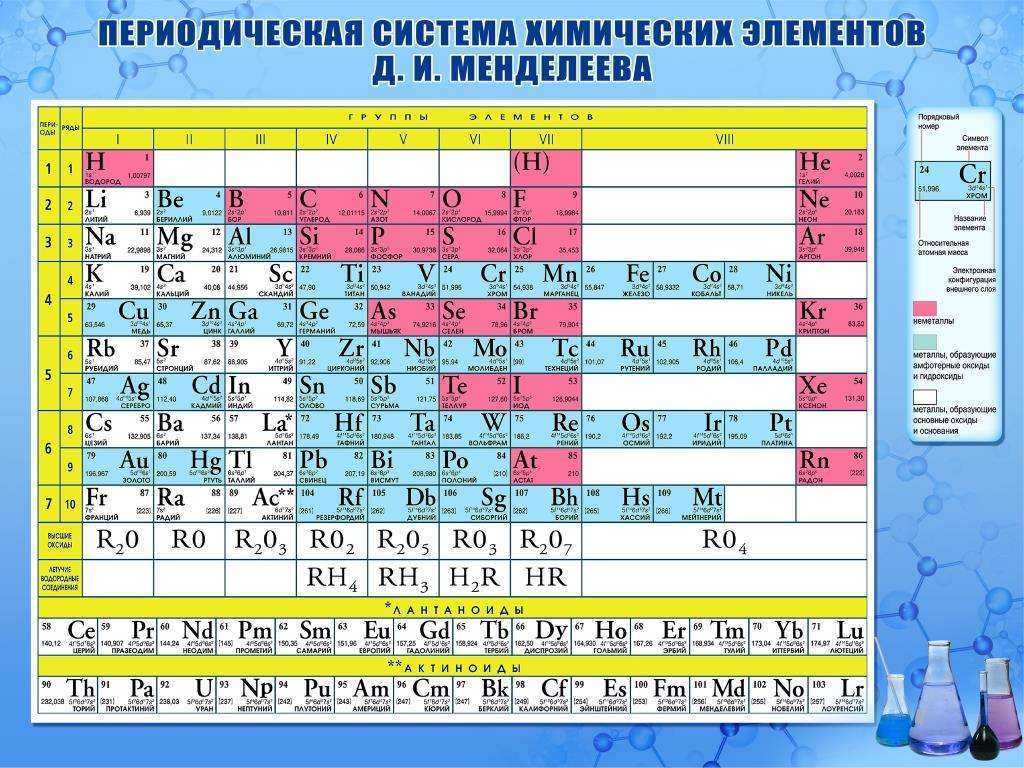

 который теперь определяется как количество протонов в каждом ядре этого элемента.
который теперь определяется как количество протонов в каждом ядре этого элемента. Та же идея независимо пришла в голову нескольким другим химикам той же эпохи, которые публиковали меньше
заметно, чем Менделеев, и не использовал схему достаточно смело, чтобы предсказать химический
свойства неоткрытых элементов, как это сделал Менделеев в 1871 году. Это включает,
в хронологическом порядке рождения:
Иоганн Вольфганг Доберейнер
(1780-1849 гг.) , впервые обнаружившие релевантные корреляции в 1829 году,
Александр-Эмиль
Бегуйе де Шанкуртуа (1820-1886) в 1862 г.,
Уильям Одлинг (1829-1921) в 1864 г.,
Юлиус Лотар Мейер (1830-1895) в 1864-1870 гг.,
Густав Хинрихс (1836-1923) в 1855-1867 гг.
и Джон Ньюлендс (1837–1898) в 1863–1865 гг.
В частности, Лотар Майер был награжден (2020-08-19) за свой ранний вклад дудлом слева,
который показывает периодическое изменение электроотрицательности во всем диапазоне химических элементов, которые он знал.
Та же идея независимо пришла в голову нескольким другим химикам той же эпохи, которые публиковали меньше
заметно, чем Менделеев, и не использовал схему достаточно смело, чтобы предсказать химический
свойства неоткрытых элементов, как это сделал Менделеев в 1871 году. Это включает,
в хронологическом порядке рождения:
Иоганн Вольфганг Доберейнер
(1780-1849 гг.) , впервые обнаружившие релевантные корреляции в 1829 году,
Александр-Эмиль
Бегуйе де Шанкуртуа (1820-1886) в 1862 г.,
Уильям Одлинг (1829-1921) в 1864 г.,
Юлиус Лотар Мейер (1830-1895) в 1864-1870 гг.,
Густав Хинрихс (1836-1923) в 1855-1867 гг.
и Джон Ньюлендс (1837–1898) в 1863–1865 гг.
В частности, Лотар Майер был награжден (2020-08-19) за свой ранний вклад дудлом слева,
который показывает периодическое изменение электроотрицательности во всем диапазоне химических элементов, которые он знал. )
)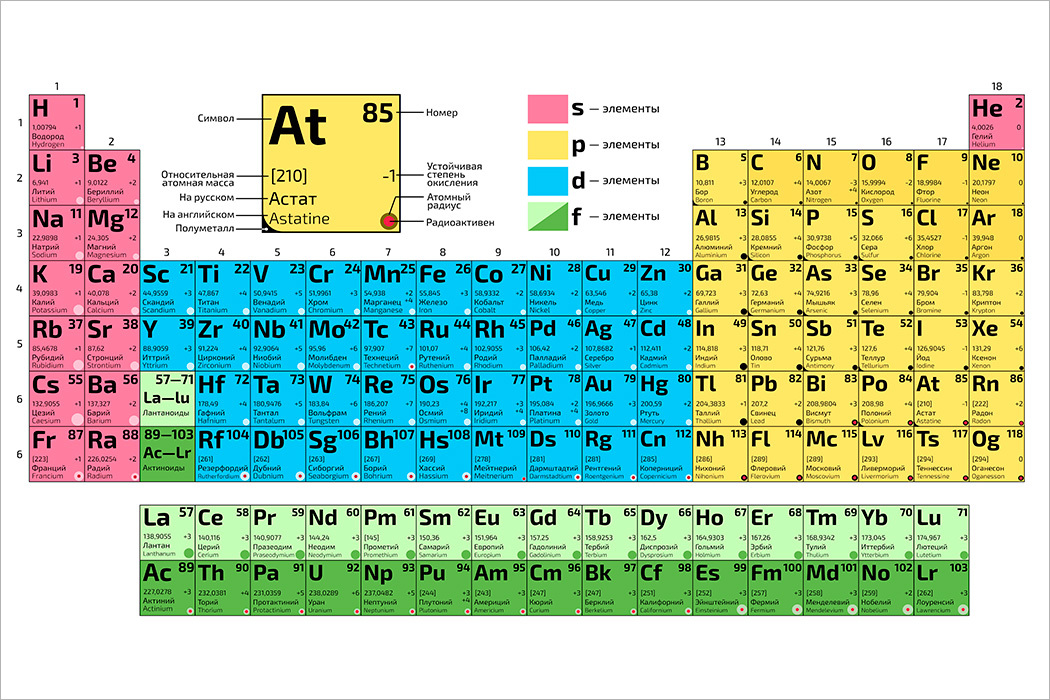 «Окись muriaticum», открытая Шееле, на самом деле была
новый элемент (Cl = хлор, массой 35,45).
«Окись muriaticum», открытая Шееле, на самом деле была
новый элемент (Cl = хлор, массой 35,45).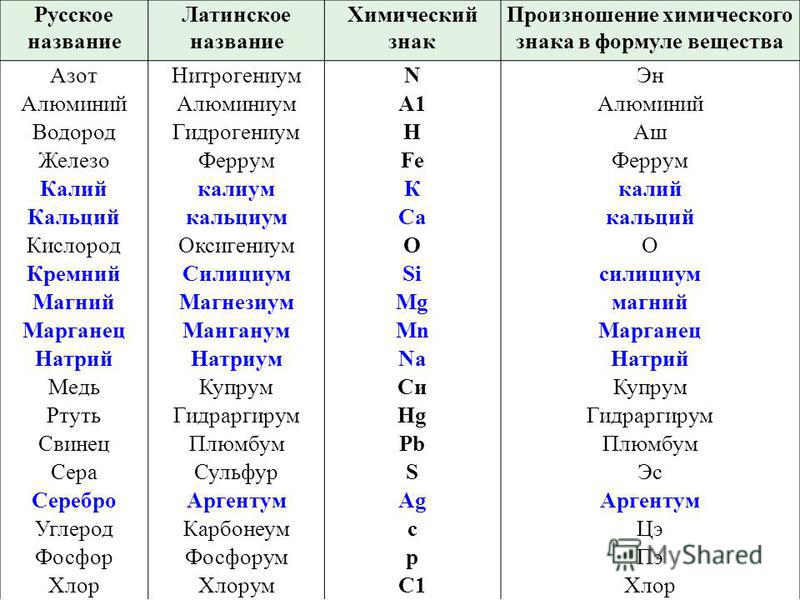
 Видео Мартина Полякова
на лантане:
Видео Мартина Полякова
на лантане:  Валентность +1.
Валентность +1.  элементы группы 12 по принятому здесь простому соглашению, следуя многим современным
авторы, которые просматривают d-блок и переход
металлы строго синонимичны.
Текущее определение IUPAC противоречиво;
он классифицировал бы цинк и кадмий
как постпереходные металлы, в то время как Меркурий (и Коперниций) должен быть
считаются переходными металлами из-за недавнего (2007 г.) синтеза
тетрафторид ртути
(введение новой степени окисления ртути, которая была
дал релятивистское объяснение
что не относится к цинку или кадмию).
элементы группы 12 по принятому здесь простому соглашению, следуя многим современным
авторы, которые просматривают d-блок и переход
металлы строго синонимичны.
Текущее определение IUPAC противоречиво;
он классифицировал бы цинк и кадмий
как постпереходные металлы, в то время как Меркурий (и Коперниций) должен быть
считаются переходными металлами из-за недавнего (2007 г.) синтеза
тетрафторид ртути
(введение новой степени окисления ртути, которая была
дал релятивистское объяснение
что не относится к цинку или кадмию).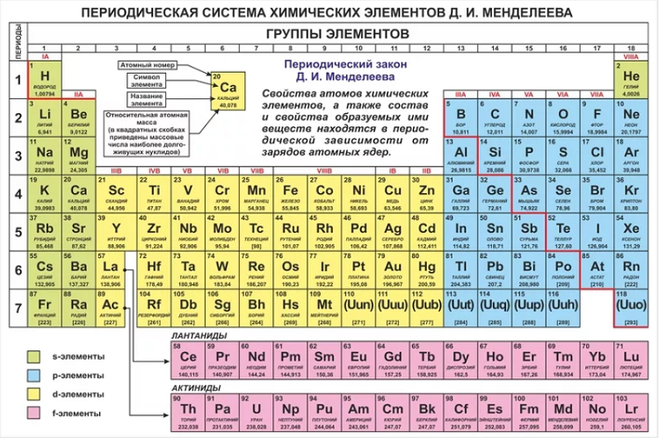
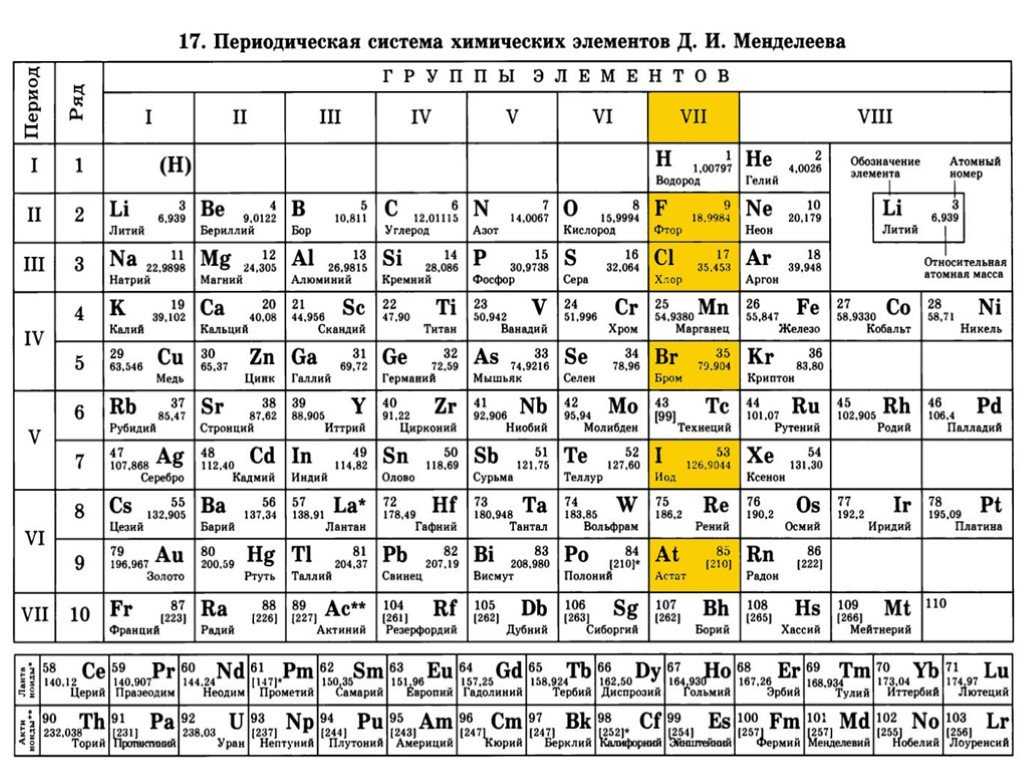 (Некоторые авторы включают Zn и Cd).
(Некоторые авторы включают Zn и Cd). ..
.. ) технеция (Tc) Ноддаком и др.
) технеция (Tc) Ноддаком и др.

 Г. Макферсон (из Калифорнийского университета в Беркли) в 1934 году…
Случай, который стоит изучить.
Г. Макферсон (из Калифорнийского университета в Беркли) в 1934 году…
Случай, который стоит изучить. Его временное название в системе IUPAC было
Унунбиум
(Ууб). С другой стороны, его можно идентифицировать как эка-ртуть.
(или eka-hydrargyrum, eka-Hg) так же, как элемент 111
(Рентгений, Rg) раньше назывался эка-золото.
Сам Менделеев ввел приставку «эка-» для обозначения любого неоткрытого элемента в его честь.
появляется выше в периодической таблице (такие элементы химически схожи).
Его временное название в системе IUPAC было
Унунбиум
(Ууб). С другой стороны, его можно идентифицировать как эка-ртуть.
(или eka-hydrargyrum, eka-Hg) так же, как элемент 111
(Рентгений, Rg) раньше назывался эка-золото.
Сам Менделеев ввел приставку «эка-» для обозначения любого неоткрытого элемента в его честь.
появляется выше в периодической таблице (такие элементы химически схожи).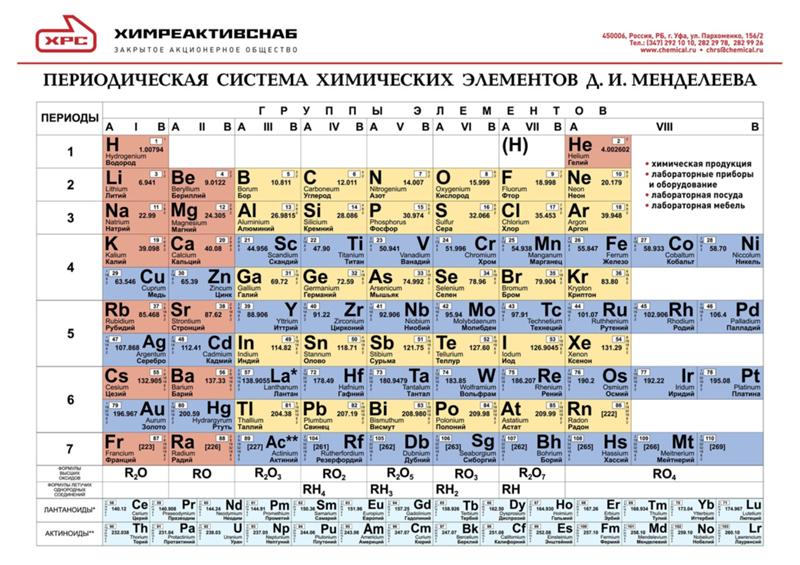 полученные в РИКЕН в 2004 и 2005 годах (а также в Ливерморе и Дубне в период с 2003 по 2005 год).
Результаты 2012 г. предоставили права на наименование японцам, которые впервые упомянули четыре возможных названия для элемента 113:
Япониум, Рикениум
Нишинариум или Ниппониум .
Большинство ставок было на последний из них, но символ Np не подходил (он уже означает Neptunium).
К счастью, есть две транскрипции
для местного названия Страны восходящего солнца .
Всего после часа размышлений в феврале 2016 года команда Riken остановилась на альтернативном Nihon .
в качестве основы как для названия, так и для символа нового элемента, поэтому он официально называется
Нигоний (обозначение Nh) с марта 2017 года.
полученные в РИКЕН в 2004 и 2005 годах (а также в Ливерморе и Дубне в период с 2003 по 2005 год).
Результаты 2012 г. предоставили права на наименование японцам, которые впервые упомянули четыре возможных названия для элемента 113:
Япониум, Рикениум
Нишинариум или Ниппониум .
Большинство ставок было на последний из них, но символ Np не подходил (он уже означает Neptunium).
К счастью, есть две транскрипции
для местного названия Страны восходящего солнца .
Всего после часа размышлений в феврале 2016 года команда Riken остановилась на альтернативном Nihon .
в качестве основы как для названия, так и для символа нового элемента, поэтому он официально называется
Нигоний (обозначение Nh) с марта 2017 года.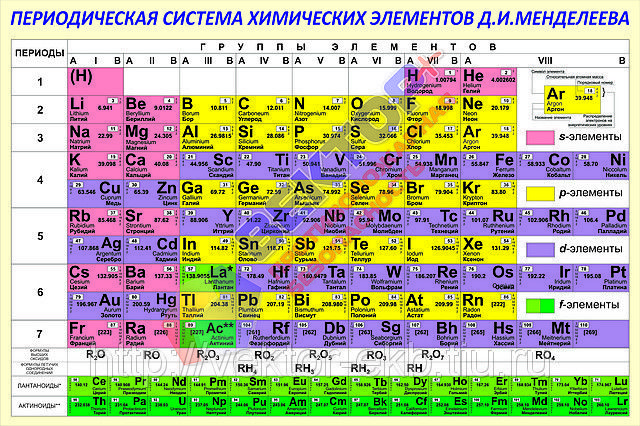 для новых элементов. После этого научному сообществу в целом будет предоставлена возможность
предлагать комментарии до того, как имена будут определены до конца 2016 года.
Эта веха отмечается в 9 1419 завершение периодической таблицы
(или, по крайней мере, его первые семь строк , включая
элемент 118, которому скоро будет присвоено правильное название).
По крайней мере, это важно по типографским и эстетическим причинам!
для новых элементов. После этого научному сообществу в целом будет предоставлена возможность
предлагать комментарии до того, как имена будут определены до конца 2016 года.
Эта веха отмечается в 9 1419 завершение периодической таблицы
(или, по крайней мере, его первые семь строк , включая
элемент 118, которому скоро будет присвоено правильное название).
По крайней мере, это важно по типографским и эстетическим причинам! Они должны отличаться хотя бы одним из значений четырех указанных выше квантовых чисел.
Отсюда следует, что подоболочка (n,l) может содержать не более 2(2l+1) электронов,
как указано выше
(общее количество внутри всей оболочки
не превышает 2n 2 ).
Они должны отличаться хотя бы одним из значений четырех указанных выше квантовых чисел.
Отсюда следует, что подоболочка (n,l) может содержать не более 2(2l+1) электронов,
как указано выше
(общее количество внутри всей оболочки
не превышает 2n 2 ).
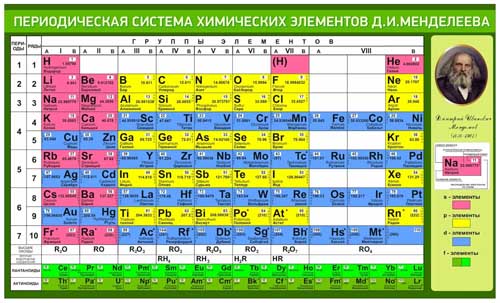 (кроме гелия).
(кроме гелия).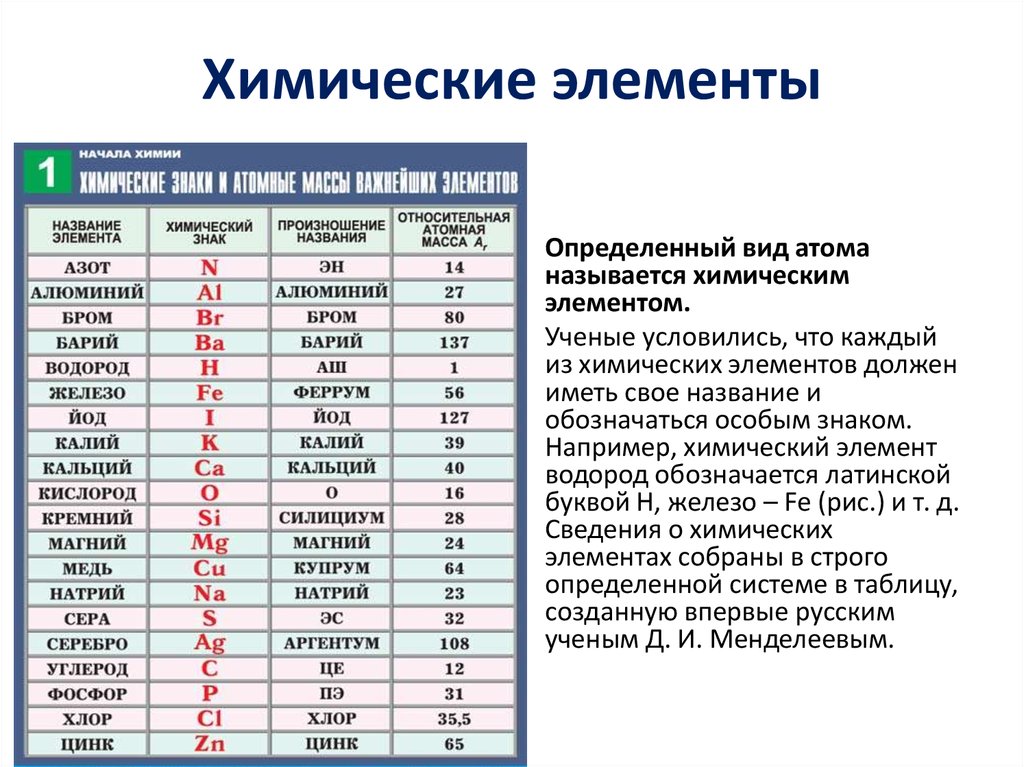 Добавление от 1 до 14 электронов к пустой подоболочке «f» лантана.
дает другие элементы ряда лантанидов (Z = от 58 до 71)
чье химическое сходство с лантаном можно объяснить, заявив, что подоболочка «f»
соответствует орбиталям, которые «ближе» к ядру, чем орбитали
предыдущая подоболочка «s», поэтому электроны «f» с меньшей вероятностью будут валентными электронами
(такая же ситуация повторяется с Actinium и серией Actinides,
от Z = 89до 103).
Это геометрическое объяснение не следует воспринимать слишком буквально…
В совокупности элементы в f-блоке (лантаниды и актиниды)
известны как внутренние переходные металлы (ITM).
Они химически похожи на два более легких редкоземельных элемента.
(скандий и иттрий), которые лучше всего расположены в последних редкоземельных столбцах.
(над Лу и Лр) когда таблица Менделеева представлена строго в порядке возрастания атомных номеров,
не прибегая к двум неуместным нижним рядам,
по типографским причинам (поскольку ширина экрана обычно ограничена).
Добавление от 1 до 14 электронов к пустой подоболочке «f» лантана.
дает другие элементы ряда лантанидов (Z = от 58 до 71)
чье химическое сходство с лантаном можно объяснить, заявив, что подоболочка «f»
соответствует орбиталям, которые «ближе» к ядру, чем орбитали
предыдущая подоболочка «s», поэтому электроны «f» с меньшей вероятностью будут валентными электронами
(такая же ситуация повторяется с Actinium и серией Actinides,
от Z = 89до 103).
Это геометрическое объяснение не следует воспринимать слишком буквально…
В совокупности элементы в f-блоке (лантаниды и актиниды)
известны как внутренние переходные металлы (ITM).
Они химически похожи на два более легких редкоземельных элемента.
(скандий и иттрий), которые лучше всего расположены в последних редкоземельных столбцах.
(над Лу и Лр) когда таблица Менделеева представлена строго в порядке возрастания атомных номеров,
не прибегая к двум неуместным нижним рядам,
по типографским причинам (поскольку ширина экрана обычно ограничена).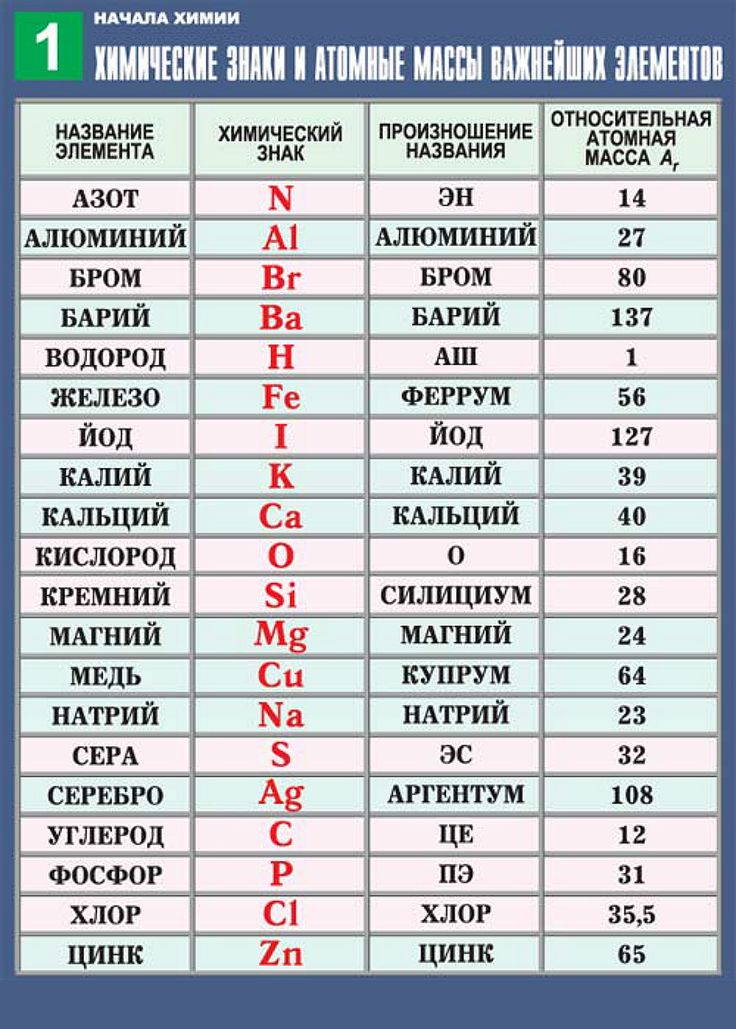 Просмотреть актуальное предупреждение
на 9 1419 Мартин Поляков …
Просмотреть актуальное предупреждение
на 9 1419 Мартин Поляков …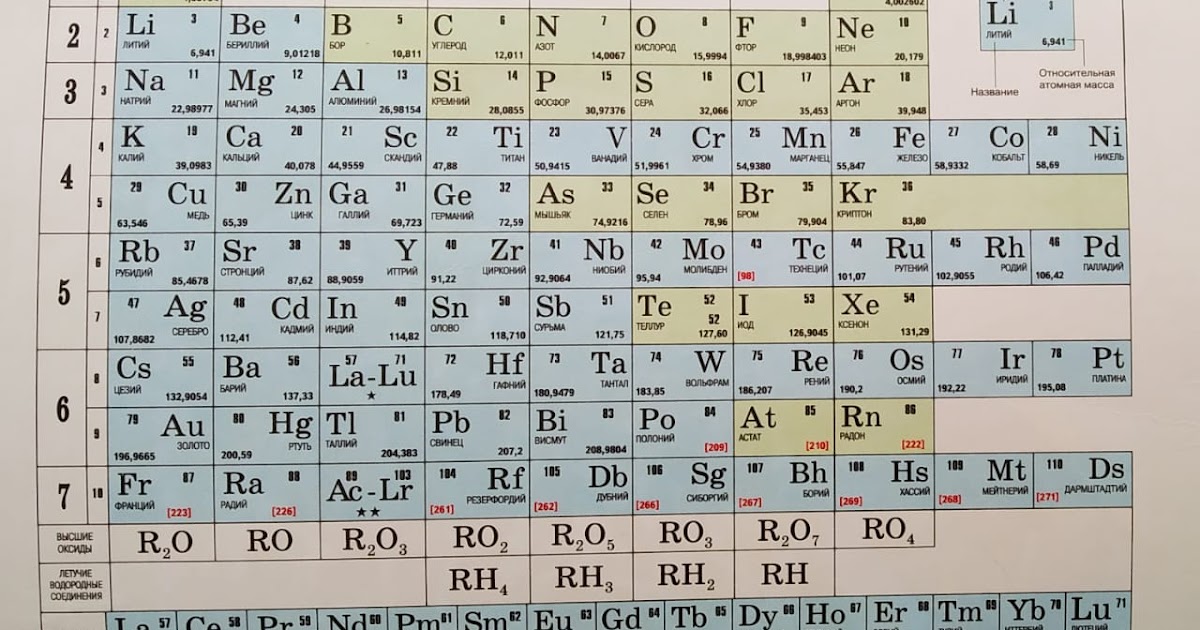 г
г  На практике такое вычисление выходит далеко за рамки наших нынешних возможностей.
а химия остается экспериментальной наукой…
Тем не менее, изобретательность экспериментаторов значительна.
и некоторые химические факты были получены для такого элемента, как
Хассий (Z = 108), хотя только около 40 атомов
это когда-либо наблюдалось.
Это стало возможным благодаря тому, что Hassium встречается с
имеют удивительно стабильный изотоп
(Hs-277) с периодом полураспада более
10 минут, как объясняется в прекрасном
видеоинтервью
из Мартын Поляков (часть
Периодический
Таблица видео, созданная
Брэди Харан).
На практике такое вычисление выходит далеко за рамки наших нынешних возможностей.
а химия остается экспериментальной наукой…
Тем не менее, изобретательность экспериментаторов значительна.
и некоторые химические факты были получены для такого элемента, как
Хассий (Z = 108), хотя только около 40 атомов
это когда-либо наблюдалось.
Это стало возможным благодаря тому, что Hassium встречается с
имеют удивительно стабильный изотоп
(Hs-277) с периодом полураспада более
10 минут, как объясняется в прекрасном
видеоинтервью
из Мартын Поляков (часть
Периодический
Таблица видео, созданная
Брэди Харан).