ХиМиК.ru – НЕОРГАНИЧЕСКАЯ ХИМИЯ – Химическая энциклопедия
А Б В Г Д Е Ж З И К Л М Н О П Р С Т У Ф Х Ц Ч Ш Щ Э Ю Я
НЕОРГАНИЧЕСКАЯ ХИМИЯ,
наука о хим. элементах и образуемых ими простых и сложных в-вах, за исключением
орг. соединений.
Понятие “неорганическая химия”
(минер. химия) появилось первоначально для обозначения в-в минер. происхождения.
Осн. задачи соврем. неорганической химии: изучение строения, св-в и хим. р-ций простых в-в и соед., взаимосвязи строения
со св-вами и реакц. способностью в-в, разработка методов синтеза и глубокой
очистки в-в, общих методов получения неорганических материалов.
Важнейшие разделы неорганической химии-теоретич.,
синтетич. и прикладная неорганическая химия. По изучаемым объектам ее подразделяют на химию отдельных
элементов, химию групп элементов в составе периодич. системы (химия щелочных
металлов, щелочноземельных элементов, галогенов, халькогенов и др.), химию
определенных соед. тех или иных элементов (химия силикатов, пероксидных соед.
и др.), химию элементов, объединенных в группы по исторически сложившимся признакам
(напр., химия редких элементов), химию близких по св-вам
и применению в-в (химия тугоплавких в-в, интер-металлидов, полупроводников,
энергонасыщенных соед., благородных металлов, неорг. полимеров и др.). Самостоят.
раздел неорганической химии-координац. химия, или химия координационных соединений. Нередко
обособляют химию переходных элементов.
По изучаемым объектам ее подразделяют на химию отдельных
элементов, химию групп элементов в составе периодич. системы (химия щелочных
металлов, щелочноземельных элементов, галогенов, халькогенов и др.), химию
определенных соед. тех или иных элементов (химия силикатов, пероксидных соед.
и др.), химию элементов, объединенных в группы по исторически сложившимся признакам
(напр., химия редких элементов), химию близких по св-вам
и применению в-в (химия тугоплавких в-в, интер-металлидов, полупроводников,
энергонасыщенных соед., благородных металлов, неорг. полимеров и др.). Самостоят.
раздел неорганической химии-координац. химия, или химия координационных соединений. Нередко
обособляют химию переходных элементов.
Границы между неорганической химией и др.
хим. науками часто условны или неопределенны. Одни и те же в-ва или р-ции м.
б. объектами исследования разл. хим. дисциплин.
Как и мн. др. хим. науки,
неорганическая химия неразрывно связана с физ. химией, к-рая может считаться теоретич. и методологич.
основой совр. химии, с аналит. химией-одним из главных инструментов химии.
науки,
неорганическая химия неразрывно связана с физ. химией, к-рая может считаться теоретич. и методологич.
основой совр. химии, с аналит. химией-одним из главных инструментов химии.
Неорганическая химия отчасти пересекается
с орг. химией, особенно с химией металлоорг. соед., бионеорг. химией и др.
Теоретич. представления
неорганической химии используют в геохимии, космохимии, химии твердого тела, химии высоких энергий,
радиохимии, ядерной химии, в нек-рых разделах биохимии и агрохимии.
Прикладная часть неорганической химии связана
с хим. технологией, металлургией, галургией, электроникой, с добычей полезных
ископаемых, произ-вом керамики, строительных, конструкционных, а также оптич.
и др. неорг. материалов, с обеспечением работы энергетич. установок (напр.,
АЭС), с с. х-вом, с обезвреживанием пром. отходов, охраной природы и др.
История развития. История
неорганической химии тесно связана с общей историей химии, а вместе с ней-с историей естествознания
и историей человеческой цивилизации.
Все осн. периоды развития
общей химии (древнейший, алхимии, ятрохимии, возникновения техн. химии,
классич. химии, современный) – это и периоды развития неорганической химии в ее совр. понимании.
В течение древнейшего периода
(до нач. 13 в.) стали известны углерод, сера, железо, олово, свинец, медь, ртуть,
серебро и золото. С 7 в. в Китае производился фарфор. В алхим. период (до нач.
16 в.) были охарактеризованы мн. минералы, открыты мышьяк, сурьма, висмут, цинк,
изучены нек-рые сплавы (в частности, отдельные амальгамы), соли, неск. к-т и
щелочей. Возник пробирный анализ. В Европе с сер. 13 в. стала применяться, а
в 15 в. и производиться селитра.
В нач. 16 в. возникло направление
в алхимии и медицине – ятрохимия (от греч. iatros-врач и химия; химиатрия, иатрохимия),
отводившее осн. роль в возникновении болезней нарушениям хим. процессов в организме
человека и ставившее задачу отыскания и приготовления хим. ср-в их лечения.
Основатель ятрохимии-Парацельс-ввел в мед. практику препараты ртути, серебра,
золота и др. металлов. Ятрохимия утратила свое значение в нач. 18 в.
iatros-врач и химия; химиатрия, иатрохимия),
отводившее осн. роль в возникновении болезней нарушениям хим. процессов в организме
человека и ставившее задачу отыскания и приготовления хим. ср-в их лечения.
Основатель ятрохимии-Парацельс-ввел в мед. практику препараты ртути, серебра,
золота и др. металлов. Ятрохимия утратила свое значение в нач. 18 в.
В период возникновения
техн. химии (17 в.- 1-я пол. 18 в.) установлено существование фосфора, кобальта,
платины и никеля. Были созданы произ-ва азотной, соляной и серной к-т, разл.
солей (поваренная соль, квасцы, бура, нашатырь, сульфат цинка), минер. красителей,
керамики.
Нач. 18 в. связано с распространением
теории флогистона-некоего в-ва, якобы выделяемого при горении. Эта ошибочная
теория оказала положит. влияние на развитие химии, впервые позволив рассматривать
разл. хим. процессы с одной общей точки зрения.
Во 2-й пол. 18 в. хим.-аналит.
методами были открыты барий, марганец, молибден и др. металлы, теллур, с помощью
электричества была разложена вода, обнаружены первые газообразные простые в-ва
– водород, азот, хлор и кислород.
хим.-аналит.
методами были открыты барий, марганец, молибден и др. металлы, теллур, с помощью
электричества была разложена вода, обнаружены первые газообразные простые в-ва
– водород, азот, хлор и кислород.
М. В. Ломоносов и А. Лавуазье
сформулировали закон сохранения массы при хим. р-циях. Лавуазье показал несостоятельность
теории флогистона, дал определение хим. элемента (в-во, к-рое не м. б. разложено
хим. способами), предложил впервые перечень известных тогда хим. элементов.
Принципы хим. номенклатуры этого периода в осн. сохранились до нашего времени.
На основе работ Л. Гальвани
и А. Вольта был открыт электрохим. ряд напряжений металлов.
В нач. 19 в. зародилась
классич. химия. В 1-й пол. 19 в. были найдены осн. количеств. законы химии.
Ж. Пруст открыл закон постоянства состава в-ва (к-рый стал общепринятым после
длит. спора с К. Бертолле). Дж. Дальтон в 1802 суммировал идеи др.
Этапными для развития неорганической химии
явились работы И. Берцелиуса, к-рый в 1814 опубликовал таблицу атомных масс.
А. Авогадро и Ж. Гей-Люссак открыли газовые законы, П. Дюлонг и А. Пти нашли
правило, связывающее теплоемкость с числом атомов в соединении, Г. И. Гесс-закон
постоянства кол-ва теплоты (см. Гесса закон). Возникла атомно-мол. теория.
В 1807 Г. Дэви электрохимически
разложил гидроксиды натрия и калия и ввел в практику новый метод выделения простых
в-в; в 1834 М. Фарадей опубликовал осн. законы электрохимии (см. Фарадея
законы).
2-я половина – конец 19
в. ознаменовались обособлением физ. химии. К. Гульдберг и П. Вааге сформулировали
действующих масс закон. Работы С. Аррениуса, Я. Вант-Гоффа, В. Оствальда
положили начало теории р-ров.
Оствальда
положили начало теории р-ров.
В этот же период зародилось
учение о валентности (Ф. Кекуле, Ш. Вюрц и др.), стали известными новые
хим. элементы (бор, литий, кадмий, селен, кремний, бром, алюминий, иод, торий,
ванадий, лантан, эрбий, тербий, диспрозий, рутений, ниобий), с помощью введенного
в практику спектр. анализа было доказано существование цезия, рубидия, таллия
и индия. Было проведено определение и уточнение атомных масс мн. хим. элементов.
К кон. 1860-х гг. стало
известно 63 хим. элемента и большое число разнообразных хим. соед., однако научная
классификация элементов отсутствовала. Основой для систематики явился периодич.
закон Менделеева, с помощью к-рого были исправлены атомные массы мн. элементов
и предсказаны св-ва неизвестных в то время в-в. Послед. открытия галлия (П.
Э. Лекок де Буабодран, 1875), скандия (Л. Нильсон, 1879), германия (К. А. Винклер,
1886), ланта-ноидов, благородных газов (У.
Теория строения атома (Э.
Резерфорд, 1911; Н. Бор, 1913), введение понятия атомного номера (Г. Мозли,
1914) позволили дать периодич. закону физ. обоснование.
В 1893 А. Вернер высказал
идею пространств. строения комплексных соед. металлов, создал основы классификации
координац. соединений.
Позднее в неорганической химии стали использоваться
такие понятия, как введенная Л. Полингом электроотрииательность, ионные
и ковалентные радиусы (см. Атомные радиусы), степень окисления, к-ты
и основания по Брёнстеду и по Льюису (см. Кислоты и основания). В 1927
И. И. Черняев открыл явление трансвлияния в комплексных соединениях. Достижения
рус. и сов. школы химии комплексных соединений (Н. С. Курнаков, Л. А. Чугаев,
И. И. Черняев, О. Е. Звягинцев, А. А. Гринберг) были положены в основу методов
аффинажа благородных металлов. Совр. период неорганической химии отличается расширением ее
теоретич. базы, резким увеличением кол-ва изучаемых объектов, применением физ.,
особенно спектроскопич., методов исследования и анализа, увеличением числа используемых
сложных методов синтеза.
Кислоты и основания). В 1927
И. И. Черняев открыл явление трансвлияния в комплексных соединениях. Достижения
рус. и сов. школы химии комплексных соединений (Н. С. Курнаков, Л. А. Чугаев,
И. И. Черняев, О. Е. Звягинцев, А. А. Гринберг) были положены в основу методов
аффинажа благородных металлов. Совр. период неорганической химии отличается расширением ее
теоретич. базы, резким увеличением кол-ва изучаемых объектов, применением физ.,
особенно спектроскопич., методов исследования и анализа, увеличением числа используемых
сложных методов синтеза.
Химия большинства элементов
в 20 в. интенсивно развивалась, однако нек-рые области неорганической химии прогрессировали
особенно быстро. Появились и новые быстро растущие направления. Х и м и я р
е д к и х м е т а л л о в начала выделяться в
самостоят. раздел неорганической химии в 30-х гг. благодаря зарождению произ-ва редких металлов
и росту их потребления, комплексному характеру мн. видов прир. сырья и общности
технол. операций переработки сырья (см. Гидрометаллургия). Появление
атомной энергетики, авиационно-космич. пром-сти и электроники повысили роль
этой области неорганической химии.
видов прир. сырья и общности
технол. операций переработки сырья (см. Гидрометаллургия). Появление
атомной энергетики, авиационно-космич. пром-сти и электроники повысили роль
этой области неорганической химии.
Х и м и я г а л о г е н
о в, особенно фтора, получила мощный импульс развития во 2-й пол. 20 в. в связи
с развитием металлургии, атомной и ракетной техники, произ-в орг. в-в, полупроводниковых
и др. материалов. Заметному увеличению числа исследований неорг. фторидов способствовало
открытие в 1962 фторидов благородных газов. В 70-80-х гг. расширилось применение
атомарных и ионизированных галогенов, каталитич. р-ций галогенирования. Многообразие
соед. галогенов и широкий диапазон их св-в сделали эти соед. удобными объектами
для изучения осн. задач неорганической химии.
Несмотря на то что уран
известен с кон. 18 в., х и м и я а к т и н о и д о в приобрела самостоят. значение
только в 40-х гг. 20 в., когда стали проводиться работы по созданию ядерного
оружия. Начиная с 60-х гг. первенство в прикладных исследованиях принадлежит
проблемам ядерного топлива. Большая часть актиноидов получена искусств.
путем (Г. Сиборг, Г. Н. Флеров и др.). Особенность химии актиноидов заключается
в трудности выделения многих из них в больших кол-вах из-за их радиоактивности.
Для получения актиноидов разработаны спец. методы синтеза и очистки, созданы
микрометоды неорганической химии и методы дистанц. управления процессами. Появилось понятие
“ядерной чистоты” материалов, способы контроля чистоты продуктов.
20 в., когда стали проводиться работы по созданию ядерного
оружия. Начиная с 60-х гг. первенство в прикладных исследованиях принадлежит
проблемам ядерного топлива. Большая часть актиноидов получена искусств.
путем (Г. Сиборг, Г. Н. Флеров и др.). Особенность химии актиноидов заключается
в трудности выделения многих из них в больших кол-вах из-за их радиоактивности.
Для получения актиноидов разработаны спец. методы синтеза и очистки, созданы
микрометоды неорганической химии и методы дистанц. управления процессами. Появилось понятие
“ядерной чистоты” материалов, способы контроля чистоты продуктов.
Начало 2-й пол. 20 в. связано
с возникновением х и м и и п о л у п р о в о д н и к о в (см. Полупроводники,
Полупроводниковые материалы), а несколько более позднее время-с развитием
планарной технологии интегральных схем. Перед неорганической химией возникли задачи получения
особо чистых в-в, что потребовало резкого улучшения методов очистки и анализа. Инструмент. методы анализа в этой области неорганической химии полностью вытеснили традиционные.
Инструмент. методы анализа в этой области неорганической химии полностью вытеснили традиционные.
В связи с развитием ракетно-космич.
техники, а, также химических источников тока во 2-й пол. 20 в. самостоят.
значение стала приобретать х и м и я э н е р г о н а с ы щ е н н
ы х с о е д и н е н и й-сильнейших окислителей и восстановителей.
Позже все большее внимание стало уделяться твердым источникам (аккумуляторам)
разл. газов – кислорода (см. Пиротехнические источники газов), водорода
(см. Водородная энергетика), фтора и др.-для топливных элементов, газовых
лазеров, систем жизнеобеспечения космич. станций и кораблей.
Х и м и я РЗЭ (см. Редкоземельные
элементы) близка к химии нек-рых редких металлов и химии актиноидов,
что связано с определенными аналогиями в электронном строении и хим. св-вах
всех этих элементов и определяет их совместное присутствие в нек-рых прир. источниках.
Уникальные св-ва РЗЭ были изучены и реализованы лишь начиная с 60-70-х гг. Особенностью
этих элементов является близость их хим. и многих физ. св-в, что привело к необходимости
преодоления трудностей при выделении, глубокой очистке и определении индивидуальных
элементов. Интерес к этой области неорганической химии возрастает в связи с открытием высокотемпературных
оксидных сверхпроводников.
Особенностью
этих элементов является близость их хим. и многих физ. св-в, что привело к необходимости
преодоления трудностей при выделении, глубокой очистке и определении индивидуальных
элементов. Интерес к этой области неорганической химии возрастает в связи с открытием высокотемпературных
оксидных сверхпроводников.
Х и м и я б л а г о р о
д н ы х г а з о в зародилась в 1962, когда Н. Бартлетт получил первое хим. соед.
ксенона-XePtF6. Ныне известны криптона дифторид, ксенона фториды,
а также фториды радона, оксиды и хлориды ксенона, ксенаты и перксенаты,
многочисл. комплексные соед., содержащие ксенон и криптон. Мн. соед. благородных
газов м. б. получены только в условиях физ. активирования реагентов; являются
термодинамически неустойчивыми в-вами и сильнейшими окислителями,
поэтому развитие этого раздела неорганической химии потребовало разработки специфич. методов
синтеза и исследований. Открытие соед. благородных газов имело принципиальное
значение и привело к видоизменению периодич. таблицы хим. элементов – исключению
“нулевой” группы и размещению благородных газов в VIII группе.
Открытие соед. благородных газов имело принципиальное
значение и привело к видоизменению периодич. таблицы хим. элементов – исключению
“нулевой” группы и размещению благородных газов в VIII группе.
В 70-х гг. новый импульс
развития получила х и м и я г и д р и д о в, особенно гидридов металлов и интерметаллич.
соед. (см. Гидриды), в связи с перспективой их использования как источников
топлива для автономных энергосистем.
Х и м и я т в е р д о г
о т е л а, переживающая с 60-70-х гг. период бурного развития, способствовала
ускорению разработки мн. ключевых для неорганической химии вопросов. Среди этих вопросов – природа
нестехиометрич. (см. Нестехиометрия)и аморфных (см. Аморфное состояние)в-в, влияние не-значит. изменений состава кристаллов на их св-ва и др. В
неорганической химии большое внимание уделяется неорг. материалам -сформировались такие области
неорганической химии, как химия материалов для электроники, формируется направление, связанное
с сенсорами химическими.
Открытие, сделанное в 1986
И. Беднорцем и К. Мюллером, положило начало еще одной области неорганической химии и химии твердого
тела-х и м и и в ы с о к о т е м п е р а т у р н ы х с
в е р х п р о в о д н и к о в (см. Сверхпроводники).
Теоретическая неорганическая химия. Этот
раздел неорганической химии рассматривает вопросы хим. связи в неорг. в-вах, структуры в-в,
их св-ва и реакц. способность. Основными в неорганической химии являются периодич. закон, закон
постоянства состава в-в и др. Однако ключевой проблемой сейчас является природа
хим. связи. В неорг. в-вах встречаются все виды хим. связи – ковалентная, ионная
и металлическая. Теория хим. связи, в частности, рассматривает вопросы природы
связи, ее энергии, длины, полярности. Наиб. распространение получили молекулярных
орбиталей методы, наряду с к-рыми используют валентных связей метод,
кристаллического поля теорию и др. Для неорганической химии особенно актуально приложение
методов мол. орбиталей к твердым телам.
орбиталей к твердым телам.
Большое значение придается
спектрам в электромагн. диапазоне (для определения структуры в-в) и магн. св-вам
в-в (в целях создания магн. материалов). Теоретич. неорганическая химия активно использует методы
хим. термодинамики и хим. кинетики.
Теоретич. неорганическая химия изучает
также закономерности образования дефектов кристаллич. решетки, влияние дефектов
на св-ва в-в, исследует кинетику твердофазных процессов.
Нек-рые вопросы, разрабатываемые
теоретич. неорганической химией, являются одновременно и проблемами физики и физ. химии. Напр.,
квантово-хим. описание электронной конфигурации атомов и ионов, проблемы происхождения
хим. элементов и их превращений в космосе, создание теории высокотемпературной
сверхпроводимости и др.
Методы синтеза неорганических
соединений. Физ. и хим. св-ва, а также реакц. способность простых в-в и
неорг. соед. изменяются в очень широких пределах. Поэтому для синтеза неорг.
в-в используют широкий набор разл. методов (см. Неорганический синтез). В
общем виде простейший синтез включает смешение реагентов, активацию смеси, собственно
хим. р-цию, выделение из нее целевого продукта и очистку последнего.
соед. изменяются в очень широких пределах. Поэтому для синтеза неорг.
в-в используют широкий набор разл. методов (см. Неорганический синтез). В
общем виде простейший синтез включает смешение реагентов, активацию смеси, собственно
хим. р-цию, выделение из нее целевого продукта и очистку последнего.
Мн. методы синтеза специфичны.
При получении тугоплавких соед. и материалов применяют методы порошковой технологии
(см. Порошковая металлургия), реакц. спекания и химического осаждения
из газовой фазы. Сферич. однородные частицы порошков получают плазменной
обработкой или с помощью золь-гель процессов. Разработаны спец. методы
выделения в-в в виде монокристаллов (см. Монокристаллов выращивание), монокристаллич.
пленок, в т.ч. эпитаксиальных (см. Эпитаксия), и нитевидных кристаллов,
волокон, а также в аморфном состоянии. Нек-рые р-ции проводят в условиях
горения, напр. синтез тугоплавких соед. из смеси порошков простых в-в (см. Горение,
Самораспространяющийся высокотемпературный синтез). Все более широкое
применение в неорг. синтезе находит криогенная техника (см. Криохимия).
Горение,
Самораспространяющийся высокотемпературный синтез). Все более широкое
применение в неорг. синтезе находит криогенная техника (см. Криохимия).
Прикладная химия. Еще
в 18 в. установилась тесная связь между неорганической химией и ремеслами – основой зарождавшейся
пром-сти. Позднее неорганическая химия стала научной базой мн. произ-в, определяющих уровень
пром. развития отдельных стран и всего человечества.
Прикладной частью неорганической химии
традиционно считается технология неорг. в-в. Она связана с крупномасштабными
про-из-вами серной, соляной, фосфорной, азотной к-т, соды, аммиака, хлора, фтора,
фосфора, а также солей натрия, калия, магния и др. (см. Галургия), диоксида
углерода, водорода, разл. минер. удобрений и мн. др. в-в. Большая часть этих
продуктов потребляется др. хим. произ-вами, металлургией и при получении конструкц.
материалов.
Прикладная неорганическая химия играет
существ.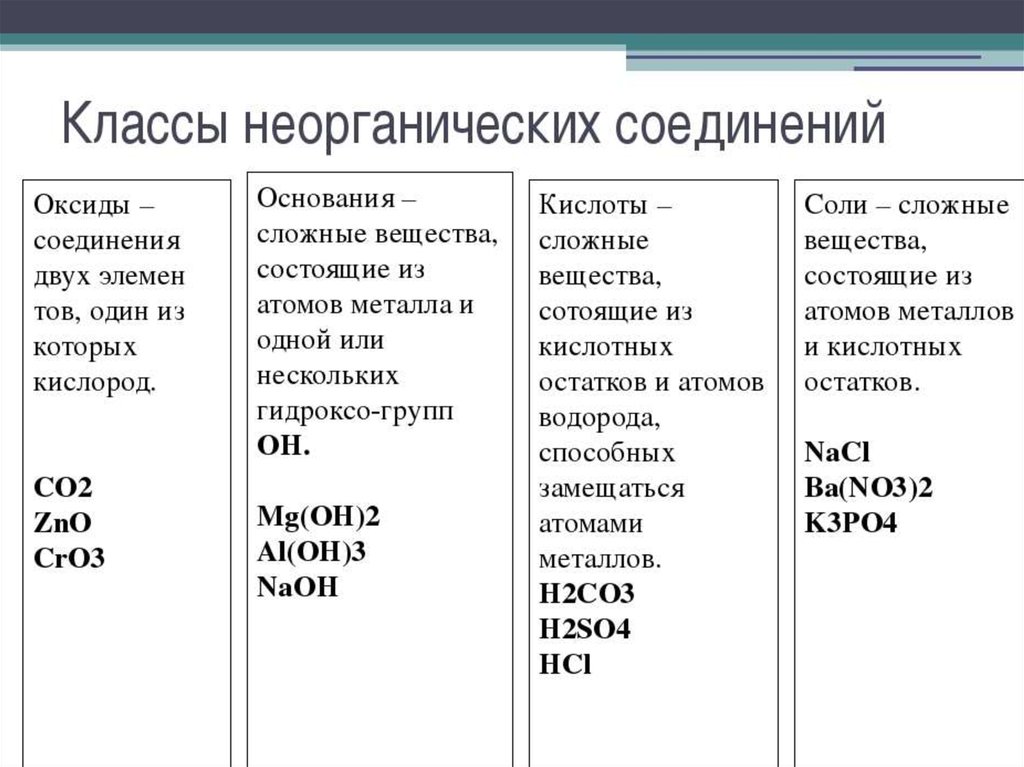 роль в развитии важнейших отраслей народного хозяйства. Так, в машиностроении
и стр-ве широко используют материалы, получаемые из минер. сырья хим. методами.
Это, напр., металлы и сплавы, минер. красители, твердые сплавы для режущего
инструмента.
роль в развитии важнейших отраслей народного хозяйства. Так, в машиностроении
и стр-ве широко используют материалы, получаемые из минер. сырья хим. методами.
Это, напр., металлы и сплавы, минер. красители, твердые сплавы для режущего
инструмента.
В таких отраслях пром-сти,
как электроника, электротехника, приборостроение, применение новых неорг. материалов
позволяет повысить техн. уровень произ-ва и выпускаемых товаров. Примерами являются
в-ва и материалы для интегральных схем, телевизионных экранов, люминесцентных
ламп, лазеров на кристаллах, волоконных световодов, сверхпроводниковых и магн.
устройств.
В энергетике, помимо применения
тугоплавких, жаростойких и жаропрочных конструкц. материалов, достижения неорганической химии
используются также для произ-ва активных в-в и электролитов в хим. источниках
тока, высокотемпературных электролитов, в ядерном реактостроении, ядерной энергетике
и произ-ве материалов для них (ядерного топлива, замедлителей нейтронов, конструкц. материалов). Развивается произ-во материалов для прямого преобразования солнечной
и тепловой энергии в электрическую, материалов для МГД-генераторов, для преобразования,
хранения и транспортирования энергии, в перспективе-для термоядерных реакторов.
Создаются также термохим. циклы разложения воды, к-рые м. б. использованы в
водородной энергетике.
материалов). Развивается произ-во материалов для прямого преобразования солнечной
и тепловой энергии в электрическую, материалов для МГД-генераторов, для преобразования,
хранения и транспортирования энергии, в перспективе-для термоядерных реакторов.
Создаются также термохим. циклы разложения воды, к-рые м. б. использованы в
водородной энергетике.
Для с. х-ва ведется произ-во
минер. удобрений и кормовых добавок, нек-рых видов пестицидов и консервантов
кормов.
Возрастает роль неорганической химии в
решении проблем охраны окружающей среды и рационального природопользования.
Все более глубоко и полно исследуется поведение разл. в-в в природе, прир. круговороты
в-в, влияние хозяйств. деятельности человека на эти процессы. Разрабатываются
новые технол. процессы, позволяющие снизить уровень нарушения экологич. равновесия
в природе, сохранить прир. ландшафты при добыче и переработке полезных ископаемых
(напр. , в результате применения подземного выщелачивания). Решаются задачи
резкого уменьшения потребления воды в пром-сти, снижения кол-ва отходов (см.
Безотходные производства), повышения комплексности использования минер.
сырья, более полного использования вторичных ресурсов. См. также Охрана природы.
, в результате применения подземного выщелачивания). Решаются задачи
резкого уменьшения потребления воды в пром-сти, снижения кол-ва отходов (см.
Безотходные производства), повышения комплексности использования минер.
сырья, более полного использования вторичных ресурсов. См. также Охрана природы.
Методы неорганической химии и хим. технологии
применяют для ликвидации вредных выбросов в разл. отраслях произ-ва (напр.,
в энергетике при сжигании угля), для превращения отходов др. отраслей в полезные
продукты. Примерами являются изготовление строит. материалов из металлургич.
шлаков, пром. переработка отработанного ядерного топлива.
Лит.: Менделеев
Д. И., Основы химии, 13 изд., т. 1-2, М.-Л., 1947; Некрасов Б. В., Основы общей
химии, 3 изд., т. 1-2, М., 1973; Реми Г., Курс неорганической химии, т. 1-2,
М., 1972-74; Джуа М., История химии, пер. с итал., М., 1975; Дей М.К., Селбин
Дж., Теоретическая неорганическая химия, пер. с англ., М., 1976; Полинг Л.,
Полинг П., Химия, пер. с англ., М., 1978; Коттон Ф., Уилкинсон Дж., Основы неорганической
химии, пер. с англ., М., 1979; Карапетьянц М. X., Дракин С. И., Общая и неорганическая
химия, М., 1981; Штрубе В., Пути развития химии, т. 1-2, пер. с нем., М., 1984;
Хьюи Дж., Неорганическая химия. Строение вещества и реакционная способность,
пер. с англ., М., 1987; Williams A. F., A theoretical approach to inorganic
chemistry, В., 1979; Anorganische Chemie, Bd 1-2, В., 1980; Holle-man A. F.,
Wiberg E., Lehrbuch der anorganischen Chemie, B.-N.Y., 1985.
с англ., М., 1976; Полинг Л.,
Полинг П., Химия, пер. с англ., М., 1978; Коттон Ф., Уилкинсон Дж., Основы неорганической
химии, пер. с англ., М., 1979; Карапетьянц М. X., Дракин С. И., Общая и неорганическая
химия, М., 1981; Штрубе В., Пути развития химии, т. 1-2, пер. с нем., М., 1984;
Хьюи Дж., Неорганическая химия. Строение вещества и реакционная способность,
пер. с англ., М., 1987; Williams A. F., A theoretical approach to inorganic
chemistry, В., 1979; Anorganische Chemie, Bd 1-2, В., 1980; Holle-man A. F.,
Wiberg E., Lehrbuch der anorganischen Chemie, B.-N.Y., 1985.
Г.А. Ягодин, Э.Г. Раков.
А Б В Г Д Е Ж З И К Л М Н О П Р С Т У Ф Х Ц Ч Ш Щ Э Ю Я
общая и неорганическая химия – Аптекарский остров
|
Вопросы и задачи по общей и неорганической химии в Тобольске: 500-товаров: бесплатная доставка, скидка-46% [перейти]
Партнерская программаПомощь
Тобольск
Каталог
Каталог Товаров
Одежда и обувь
Одежда и обувь
Стройматериалы
Стройматериалы
Текстиль и кожа
Текстиль и кожа
Здоровье и красота
Здоровье и красота
Детские товары
Детские товары
Электротехника
Электротехника
Продукты и напитки
Продукты и напитки
Промышленность
Промышленность
Мебель и интерьер
Мебель и интерьер
Вода, газ и тепло
Вода, газ и тепло
Сельское хозяйство
Сельское хозяйство
Все категории
ВходИзбранное
Вопросы и задачи по общей и неорганической химии
Общая и Неорганическая Химия. Вопросы Задач 2-е Изд. Испр. Доп.. Учебное посо…
Вопросы Задач 2-е Изд. Испр. Доп.. Учебное посо…
В МАГАЗИНЕще цены и похожие товары
Книга Общая и неорганическая химия. Вопросы задачи
В МАГАЗИНЕще цены и похожие товары
Задачи, упражнения и вопросы по общей химии.
ПОДРОБНЕЕЕще цены и похожие товары
Вопросы и задачи по общей химии. К учебнику «Общая химия».
ПОДРОБНЕЕЕще цены и похожие товары
Книга Задачи и упражнения по общей химии
В МАГАЗИНЕще цены и похожие товары
Задачи по общей химии с элементами биоорганической
В МАГАЗИНЕще цены и похожие товары
Книга Задачи по общему курсу органической химии с решениями для бакалавров. Учебное пос…
Учебное пос…
В МАГАЗИНЕще цены и похожие товары
Жмурко Г. П., Кузнецов В. Н., Кабанова Е. Г., Филиппова С. Е., Казакова Е. Ф., Яценко А. В. “Вопросы и задачи по общей и неорганической химии“
ПОДРОБНЕЕЕще цены и похожие товары
Неорганическая Химия. Вопросы и Задач 2-е Изд. Испр. Доп.. Учебное пособие для СПО
В МАГАЗИНЕще цены и похожие товары
Неорганическая Химия. Вопросы и Задач 2-е Изд. Испр. Доп.. Учебное пособие для п…
В МАГАЗИНЕще цены и похожие товары
Задачи по общему курсу органической химии с решениями для бакалавров.
ПОДРОБНЕЕЕще цены и похожие товары
И. И. Новошинский, Н. С. Новошинская “Химия. Готовимся к ОГЭ и ЕГЭ. Экспериментальная химия. Решение экспериментальных задач по неорганической химии. Курс по выбору. 8-11 классы | Новошинская Нина Степановна, Новошинский Иван Иванович”
Готовимся к ОГЭ и ЕГЭ. Экспериментальная химия. Решение экспериментальных задач по неорганической химии. Курс по выбору. 8-11 классы | Новошинская Нина Степановна, Новошинский Иван Иванович”
ПОДРОБНЕЕЕще цены и похожие товары
Общая и неорганическая химия: экспериментальные задачи упражнения.
ПОДРОБНЕЕЕще цены и похожие товары
786
1405
Лаборатория знаний / Задачи по общему курсу органической химии с решениями для бакалавров: учебное пособие, Лаборатория знаний
ПОДРОБНЕЕЕще цены и похожие товары
Задачи по общей химии с элементами биоорганической химии.
ПОДРОБНЕЕЕще цены и похожие товары
190
272
Гольцман Г. Н., Казанцева Алла Борисовна, Соина Н. В. “Сборник вопросов и задач по общей физике. Раздел 5. Молекулярная физика”
Раздел 5. Молекулярная физика”
ПОДРОБНЕЕЕще цены и похожие товары
Готовимся к ОГЭ и ЕГЭ. Экспериментальная химия. Решение экспериментальных задач по неорганической химии: курс по выбору.8-11 класс.
ПОДРОБНЕЕЕще цены и похожие товары
Рябов Михаил Алексеевич “Сборник задач, упражнений и тестов по химии. 10-11 класс. К учебнику Г. Е. Рудзитиса, Ф. Г. Фельдмана “Химия. 10 класс”, “Химия. 11 класс”. ФГОС”
ПОДРОБНЕЕЕще цены и похожие товары
Органическая химия. Задачи по общему курсу. В 2 томах
ПОДРОБНЕЕЕще цены и похожие товары
Сборник заданий, упражнений и тестов по химии: 11 классс.: к учебнику Рудзитиса и др
ПОДРОБНЕЕЕще цены и похожие товары
Блинов Л. Н. “Сборник задач и упражнений по общей химии. Уч. пособие” Издательство: Лань,
Н. “Сборник задач и упражнений по общей химии. Уч. пособие” Издательство: Лань,
ПОДРОБНЕЕЕще цены и похожие товары
Козлов В.Ф., Маношкин Ю.В., Миллер А.Б. и др. “Задачи по общей и прикладной физике” Издательство:
ПОДРОБНЕЕЕще цены и похожие товары
Доронькин Владимир Николаевич, Бережная александра Григорьевна, Сажнева Татьяна Владимировна, Февралева Валентина Александровна “Химия ЕГЭ Раздел Общая химия 10-11 классы Задания и решения Тренировочная тетрадь”
ПОДРОБНЕЕЕще цены и похожие товары
Карлов С.С, Нуриев В.Н., Теренин В.И.,Зайцева Г.С “Задачи по общему курсу органической химии с решениями для бакалавров.”
ПОДРОБНЕЕЕще цены и похожие товары
Врублевский Александр Иванович “Учимся решать задачи по химии.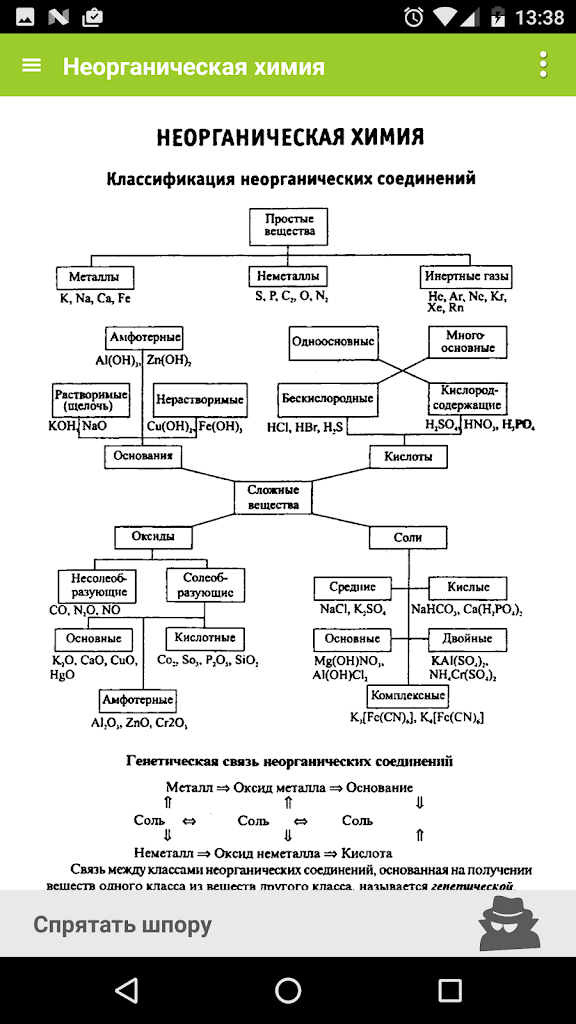 Общий подход” Предмет: химия, Класс:
Общий подход” Предмет: химия, Класс:
ПОДРОБНЕЕЕще цены и похожие товары
689
1299
Дерябина Н.Е. “Мини справочник-шпаргалка по химии 5 штук: Неорганическая химия в реакциях, Органическая химия в реакциях, Для решения качественных задач, Формулы для решения задач по химии, Связи между классами веществ | Дерябина”
ПОДРОБНЕЕЕще цены и похожие товары
А. Б. Казанцева “Сборник вопросов и задач по общей физике. Раздел 3. Оптика. Раздел 4. Квантовая физика”
ПОДРОБНЕЕЕще цены и похожие товары
Е. М. Мясоедов “Помощник по химии с ответами и решениями ко многим вопросам и задачам“
ПОДРОБНЕЕЕще цены и похожие товары
Хомченко Иван Гавриилович “Общая химия. Сборник задач и упражнений. Учебное пособие” Издательство:
Сборник задач и упражнений. Учебное пособие” Издательство:
ПОДРОБНЕЕЕще цены и похожие товары
2 страница из 18
Основы неорганической химии – Курс
Этот курс в основном посвящен основам неорганической химии. Это включает в себя периодические свойства элементов, источник и извлечение металлов. Изучение переходных металлов составляет большую часть неорганической химии. Поэтому мы обсудим некоторые общие свойства, такие как энергия стабилизации кристаллического поля, магнитные свойства, спектроскопические свойства и использование этих свойств в различных областях, в том числе в биологических системах.
ПРЕДНАЗНАЧЕННАЯ АУДИТОРИЯ: Студенты бакалавриата, изучающие науку и технику
ПРЕДВАРИТЕЛЬНЫЕ ТРЕБОВАНИЯ: Базовые курсы химии, базовая математика из школьного стандарта 10+2
ПОДДЕРЖКА ПРОМЫШЛЕННОСТИ: Пока не обращались, в процессе.
Резюме
| Статус курса: | Завершено |
| Тип курса: | Ядро |
| Продолжительность : | 4 недели |
| Дата начала: | 24 января 2022 г. |
| Дата окончания: | 18 фев 2022 |
| Дата экзамена: | 27 марта 2022 г. IST |
| Окончание регистрации: | 07 фев 2022 |
| Категория: |
|
| Кредитные очки: | 1 |
| Уровень: | Бакалавриат |
Посещения страниц
Схема курса
Неделя 1: Основы неорганической химии
Неделя 2: Очистка элементов; координационная химия; правило 18 электронов; теория валентных связей; Теория кристаллического поля
Неделя 3: Термины; спектроскопия комплексов; искажение Ян-Теллера; шпинели; Магнетизм
Неделя 4: Био-неорганическая химия, Ферменты; гемоглобин и миоглобин; Токсичность; Лекарственные неорганические соединения
Книги и ссылки
1. Дж. Д. Ли, Краткая неорганическая химия, 4-е издание, ELBS, 1991.
Дж. Д. Ли, Краткая неорганическая химия, 4-е издание, ELBS, 1991.
Хьюи. Дж. Э. Кейтер. А. Э. и Кейтер. Р. Л. Неорганическая химия, 1993.
5. Джеймс. E. House Inorganic Chemistry, 2008.
4. Shriver and Atkins’ Inorganic Chemistry, Fifth Edition, 2010.
Биография инструктора
Профессор Д. Маити
ИИТ Бомбея
Я доктор Дебабрата Маити, доцент ИИТ Бомбея. У меня есть получил докторскую степень в Университете Джона Хопкинса с профессором Кеннетом Д. Карлин в бионеорганической химии. Затем я перешел в Массачусетский технологический институт, где я сделал свой Постдокторское исследование с профессором Стивеном Бухвальдом. я начал независимый перевозчик в IIT Bombay в 2011 году и с тех пор участвует активно преподает бионеорганическую химию и металлоорганические химия. Наша группа также активно занимается исследованиями в области бионеорганических химия и активация CH.
Сертификат о прохождении курса
Зарегистрироваться на этот курс и пройти обучение можно бесплатно. Но если вам нужен сертификат, вы должны зарегистрироваться и сдать экзамен под наблюдением, который мы проводим лично в любом из назначенных экзаменационных центров.
Но если вам нужен сертификат, вы должны зарегистрироваться и сдать экзамен под наблюдением, который мы проводим лично в любом из назначенных экзаменационных центров.
Экзамен является необязательным, его стоимость составляет 1000 рупий (только одна тысяча рупий).
Дата и время экзаменов: 27 марта 2022 г. Утренняя сессия с 9:00 до 12:00; Дневная сессия с 14:00 до 17:00.
URL-адрес регистрации: Объявления будут сделаны, когда регистрационная форма будет открыта для регистрации.
Необходимо заполнить регистрационную онлайн-форму и оплатить сертификационный экзамен. Более подробная информация будет доступна после публикации формы регистрации на экзамен. Если будут какие-то изменения, тогда об этом будет сказано.
Пожалуйста, ознакомьтесь с формой для получения более подробной информации о городах, где будут проводиться экзамены, условиях, на которые вы соглашаетесь при заполнении формы и т. д.
КРИТЕРИИ ДЛЯ ПОЛУЧЕНИЯ СЕРТИФИКАТА 3 лучших задания из 4-х заданий курса.
Экзаменационный балл = 75% от контролируемого сертификационного экзамена из 100
Окончательный балл = средний балл за задание + экзаменационный балл = 30/75. Если один из двух критериев не выполнен, вы не получите сертификат, даже если окончательный балл >= 40/100.
В сертификате будет указано ваше имя, фотография и оценка на итоговом экзамене после разрыва.
Будет доступен только электронный сертификат. Печатные копии не будут отправлены.
Еще раз спасибо за интерес к нашим онлайн-курсам и сертификации. Приятного обучения.
– Команда NPTEL
Политика конфиденциальности | Условия использования | Кодекс чести |
Общие сведения об органических и неорганических соединениях
В относительной терминологии слово «органический» относится ко всему, что происходит из живой материи или относится к ней. И наоборот, его антоним неорганический относится ко всему, что не происходит из живой материи и не состоит из нее. Это определение верно в рамках научной области биологии, но современная химия представляет собой разнообразный предмет. Существенная основа химии вращается вокруг динамического дуэта, а именно, органических и неорганических соединений. С научной точки зрения из-за этих расходящихся аспектов химии, изучающей материю, существуют две отдельные дисциплины – органическая химия и неорганическая химия.
Существенная основа химии вращается вокруг динамического дуэта, а именно, органических и неорганических соединений. С научной точки зрения из-за этих расходящихся аспектов химии, изучающей материю, существуют две отдельные дисциплины – органическая химия и неорганическая химия.
Основное различие между этими противоположными дисциплинами заключается в области их изучения. Обобщая разницу, органическая химия включает изучение живых соединений, содержащих атомы углерода, тогда как неорганическая химия включает изучение в основном неуглеродных соединений, полученных из неживых существ. Ученые в основном рассматривают вещества, которые не подпадают непосредственно под определение органических, как неорганические.
В этой структурной структуре химических соединений химики-органики изучают органические молекулы и их врожденные реакции. Напротив, химики-неорганики изучают минеральные или антропогенные реакции. Такая схематическая категоризация может показаться простой, но историческая подоплека четкого разграничения гораздо сложнее. На ваше рассмотрение, давайте рассмотрим характеристики соединений поближе, чтобы лучше понять органические и неорганические соединения. Эта осведомленность обеспечивает дальнейшее понимание современных химических применений в ядерной медицине и общем здравоохранении.
На ваше рассмотрение, давайте рассмотрим характеристики соединений поближе, чтобы лучше понять органические и неорганические соединения. Эта осведомленность обеспечивает дальнейшее понимание современных химических применений в ядерной медицине и общем здравоохранении.
История органической химии
В начале 19 го века как естествоиспытатели, так и ученые наблюдали широкий спектр химических соединений. Эти исследователи отметили критические различия, существующие между соединениями, полученными из живых веществ, и теми, которые не произошли. Химики в этот период времени осознали фундаментальное, но необъяснимое различие, существующее между типами различных соединений. Из этих опытных наблюдений теория жизненной силы 1809 г.стала общепринятой гипотезой.
Йонс Берцелиус предложил эту теорию витализма. Он также был первым, кто использовал термин органическая химия, имея в виду изучение соединений, происходящих из биологических источников. Теория жизненной силы предполагала, что жизненная сила — или жизненная сила — существует исключительно в присутствии органических материалов, таких как тела живых животных и растений. Согласно этому убеждению, органические соединения образовывались исключительно в живых клетках. Поэтому приготовить такие соединения в лаборатории было невозможно.
Согласно этому убеждению, органические соединения образовывались исключительно в живых клетках. Поэтому приготовить такие соединения в лаборатории было невозможно.
Ученый Фридрих Велер несколько десятилетий спустя отказался от этой теории с помощью своего новаторского метода синтеза. В контролируемых условиях Велер продемонстрировал, как получать органические соединения в лаборатории. Этот синтез органического вещества «in-vitro» оказался ключевым открытием в биохимии для дальнейших исследований, концептуализирующих современную область органической химии.
Примеры и производные органических соединений
Хотя органическая химия изначально определялась как химия биологических существующих молекул, с тех пор область ее применения определяется как относящаяся к характеристикам соединений углерода и их производных. По сути, органические соединения состоят из углерода в качестве основного компонента.
Соединения углерода небиологического происхождения, тем не менее, относятся к области органической химии. Тем не менее, имейте в виду, что простое присутствие элемента автоматически указывает на то, что само соединение является органическим. Органические соединения также неизменно связаны с водородом, поскольку известно, что они образуют ковалентные связи. Атомы углерода сливаются с атомами водорода, образуя углеводороды.
Тем не менее, имейте в виду, что простое присутствие элемента автоматически указывает на то, что само соединение является органическим. Органические соединения также неизменно связаны с водородом, поскольку известно, что они образуют ковалентные связи. Атомы углерода сливаются с атомами водорода, образуя углеводороды.
Неорганические соединения, напротив, не обладают указанными выше идиосинкразическими характеристиками. Опять же, любые молекулы, относительно связанные с живыми существами, считаются органическими. Обычно они являются результатом врожденной активности организма и процессов, происходящих в организме. Общие примеры включают жиры, сахара, белки, ферменты, нуклеиновые кислоты, липиды и углеводородное топливо. Органические соединения существуют в виде твердых веществ, газов и жидкостей. Конкретные категории включают ДНК, столовый сахар, научно известный как сахароза (C 12 H 22 O 11 ), метан (CH 4 ), этанол (C 2 H 6 O) и бензол (C 7 6 H 90).
История неорганической химии
В общем и целом область химии вращается вокруг существования металлов. Древние техники алхимиков Азии и Европы в конечном итоге привели к развитию этой отрасли науки. Хотя алхимикам не удалось успешно превратить свинец в ценное золото, их открытие кислот и оснований, разработка методов химических реакций и систематический исследовательский подход заложили основу для периодической таблицы.
Химическая природа таких веществ не была широко известна до 19 века, когда ученые начали лучше понимать органические соединения. С тех пор химики-неорганики изучают поведение неорганических элементов, образующихся в результате неживых процессов, и работают над разработкой прикладной методологии или проводят исследования того, как эти соединения можно эффективно модифицировать и использовать в промышленности.
Примеры неорганических соединений
Понять органические и неорганические соединения несложно, если вспомнить, что в неорганических соединениях отсутствуют связи углерод-водород. Неорганические молекулы состоят из металлов, солей, минералов, отдельных элементов и любых соединений углерода, не связанных с водородом. Хорошо известные примеры включают серебро, серу, алмаз (также известный как чистый углерод), двуокись углерода (CO 2 ) и поваренная соль, известная в науке как хлорид натрия (NaCl). Поскольку эти соединения имеют более высокие температуры плавления и точную проводимость, их часто используют в качестве катализаторов, пигментов, покрытий, топлива или лекарств.
Неорганические молекулы состоят из металлов, солей, минералов, отдельных элементов и любых соединений углерода, не связанных с водородом. Хорошо известные примеры включают серебро, серу, алмаз (также известный как чистый углерод), двуокись углерода (CO 2 ) и поваренная соль, известная в науке как хлорид натрия (NaCl). Поскольку эти соединения имеют более высокие температуры плавления и точную проводимость, их часто используют в качестве катализаторов, пигментов, покрытий, топлива или лекарств.
Применение в фармацевтической промышленности
Каждая из этих областей химии в последнее время актуальна в нашем мире и продолжит играть важную роль в будущем. Одним из наиболее активных направлений химии сегодня является органическая химия. Результаты прошлых экспериментов позволили нам узнать о последовательности изменений, происходящих в ходе реакций и синтеза. Благодаря актуальности и полезности этой биохимии ценные молекулярные приложения появляются как в промышленности, так и в технологии.
Кроме того, производство радиоизотопных соединений неорганических элементов имеет решающее значение для ядерной медицины и секторов здравоохранения. Эта область химии остается актуальной для разработки радиофармпрепаратов для терапевтических и диагностических целей. Производство соединений с радиоактивной меткой для исследования лекарств, разработки в клинических испытаниях и, в конечном итоге, производства является столь же сложным процессом. Радиохимики должны использовать надлежащие знания, методы и опыт для производства высококачественных продуктов в соответствии с установленными стандартами.
Moravek — сертифицированный GMP производитель для фармацевтической промышленности. Мы являемся надежной контрактной производственной организацией, которая предлагает квалифицированный индивидуальный синтез соединений углерода-14 с радиоактивной меткой. Как предприятие с большим опытом в радиосинтезе, очистке и анализе соединений, наши услуги легко доступны для поддержки любого этапа процесса разработки лекарств. Наша команда химиков имеет обширный опыт работы в различных областях, производя продукты с радиоактивной меткой и предоставляя услуги в области химии органического синтеза. Moravek разрабатывает эффективные кампании для клиентов, чтобы соответствовать нормативным требованиям FDA и достигать целей проектов химических исследований.
Наша команда химиков имеет обширный опыт работы в различных областях, производя продукты с радиоактивной меткой и предоставляя услуги в области химии органического синтеза. Moravek разрабатывает эффективные кампании для клиентов, чтобы соответствовать нормативным требованиям FDA и достигать целей проектов химических исследований.
Неорганическая химия – определение, объяснение, классификация и часто задаваемые вопросы
Термин «органические» относится к соединениям, содержащим атомы углерода. Так, раздел химии, занимающийся изучением соединений, не содержащих в себе атомов углерода и водорода, известен как «неорганическая химия». Проще говоря, это полная противоположность органической химии. Вещества, не имеющие связи углерод-водород, называются солями, металлами или химическими веществами и т. д.
Об основах неорганической химии
Известно, что на всей планете существует около 1 лакха неорганических соединений. Кроме того, неорганическая химия изучает поведение этих соединений, включая их свойства, их физические свойства и химические характеристики. Элементы периодической таблицы, за исключением водорода и углерода, входят в список неорганических соединений.
Элементы периодической таблицы, за исключением водорода и углерода, входят в список неорганических соединений.
Технологически большинство элементов необходимы. Например, железо, титан, медь и никель можно использовать в электрическом и конструктивном отношении. Во-вторых, переходные металлы образуют множество полезных сплавов друг с другом, включая другие металлические элементы.
Химия Определение
Химия – это изучение веществ, из которых состоит материя. Химия экспериментально тяжела, потому что мы можем изучать только восстановление, если полностью смешаем вещества. К счастью, нам не нужно рисковать своей безопасностью и здоровьем, чтобы лучше понять тему химии, потому что смелые ученые уже это сделали. Существует более 100 элементов, составляющих материю нашей вселенной и мира. Вместе они образуют тысячи и тысячи соединений.
Химическое соединение образуется из атомов различных элементов, соединенных химической связью. Эти связи настолько прочны, что соединение действует как единое вещество. Молекулы и соединенные атомы образуют молекулы, которые соединяются, образуя соединение.
Эти связи настолько прочны, что соединение действует как единое вещество. Молекулы и соединенные атомы образуют молекулы, которые соединяются, образуя соединение.
Металлоорганическая химия
Металлоорганическая химия описывается как междисциплинарная наука части неорганической химии, которая развивалась феноменальными темпами в течение последних 3-4 десятилетий. Попытки прояснить природу связей в академическом плане в постоянно растущем списке захватывающих металлоорганических соединений привели к краткому пониманию разнообразия химических связей и их природы.
В первую очередь металлоорганические соединения могут быть использованы в качестве гомогенных катализаторов в промышленности.
Переходные элементы
Переходный элемент можно определить как имеющий частично заполненные d-орбитали в предпоследней оболочке. Кроме того, это концептуальное определение может быть полезным, поскольку оно позволяет нам легко распознать переходный элемент, взглянув на его электронную конфигурацию. Кроме того, это определение исключает кадмий, ртуть и цинк из переходных элементов, поскольку они не имеют частично заполненной d-орбитали. Но они также считаются переходными элементами, поскольку их свойства являются расширением свойств переходных элементов в неорганической химии. Группа цинка, по сути, служит мостом между переходом и его репрезентативными элементами.
Кроме того, это определение исключает кадмий, ртуть и цинк из переходных элементов, поскольку они не имеют частично заполненной d-орбитали. Но они также считаются переходными элементами, поскольку их свойства являются расширением свойств переходных элементов в неорганической химии. Группа цинка, по сути, служит мостом между переходом и его репрезентативными элементами.
Наиболее заметные характеристики, общие для 24 элементов, касаются того, что все они являются металлами, и большинство из них твердые, блестящие, твердые и имеют высокие температуры плавления и кипения. Они также являются хорошими проводниками электричества и тепла. Диапазон этих свойств значителен; таким образом, операторы эквивалентны общим свойствам всех других элементов.
Координационная химия
Координационные соединения нашли свое применение задолго до возникновения неорганической химии. Систематическое исследование связи и структуры в координационной химии началось с любознательности Тассарта и продолжалось выдающимися химиками Йоргенсеном, Альфредом Вернером и Вильгельмом Бломстрандом до 19 века. конец го века. Но со временем координационная теория Вернера стала основой современной координационной химии.
конец го века. Но со временем координационная теория Вернера стала основой современной координационной химии.
Элементы P-блока
Элементы, расположенные в группах с 13 по 18 периодической таблицы, составляют p-блок. На свойства p-блочных элементов неорганической химии, как и на свойства других блочных элементов, сильно влияют их энтальпия ионизации, размер атома, электроотрицательность и энтальпия поглощения электронов. Отсутствие d-орбиталей во 2-м периоде и наличие либо d-, либо f-орбиталей у более тяжелых элементов оказывает существенное влияние на свойства элементов. Таким образом, более тяжелые элементы p-блока отличаются от своих более легких собратьев.
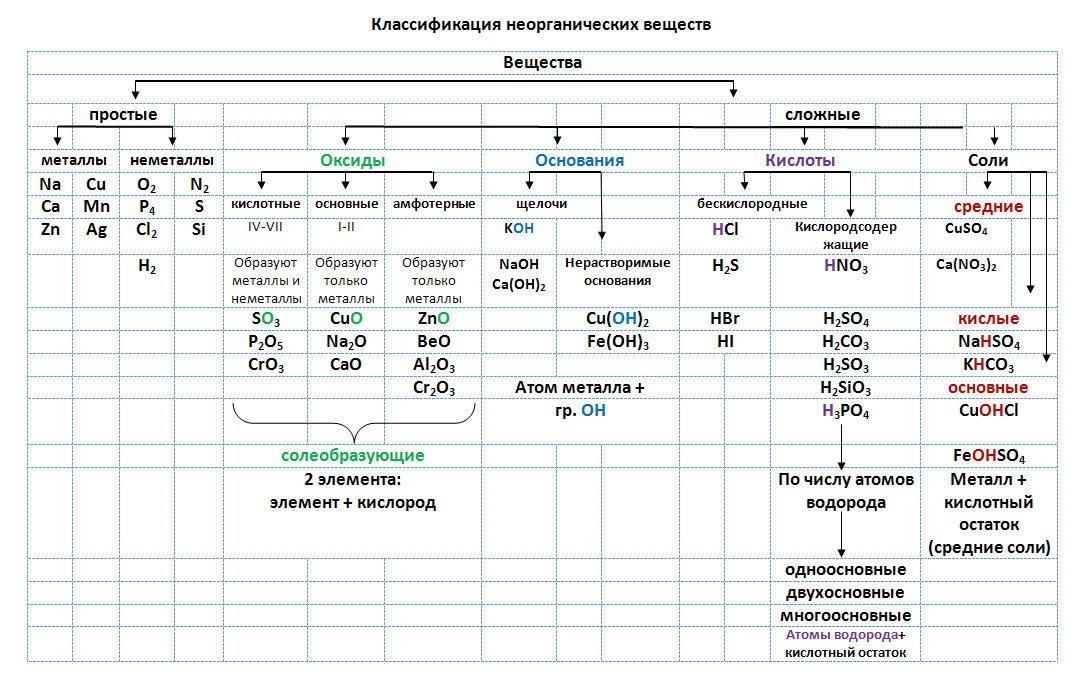
Классификация неорганических соединений
Органические соединения, отнесенные к категории неорганической химии, перечислены ниже.
Кислоты: Кислоты представляют собой соединения, которые растворяются в воде и образуют водород или ионы H + .


 Представлены основы химии координационных соединений и окислительно-восстановительного равновесия в водной среде.
Представлены основы химии координационных соединений и окислительно-восстановительного равновесия в водной среде. Сформулированы контрольные вопросы, упражнения. Приведены также методические указания к лабораторной работе, посвященной .методам получения и свойствам координационных соединений. Пособие предназначено для студентов 1 курса фармацевтического факультета и ФПТЛ, а также может быть использовано студентами заочного отделения фармацевтического факультета.Цена:27,50 руб
Сформулированы контрольные вопросы, упражнения. Приведены также методические указания к лабораторной работе, посвященной .методам получения и свойствам координационных соединений. Пособие предназначено для студентов 1 курса фармацевтического факультета и ФПТЛ, а также может быть использовано студентами заочного отделения фармацевтического факультета.Цена:27,50 руб Новое издание пособия дополнено разделом, связанным с расчетом тепловых эффектов химических процессов (глава 3).
Новое издание пособия дополнено разделом, связанным с расчетом тепловых эффектов химических процессов (глава 3). / под ред. проф. А. В. Москвина. — СПб.: Изд-во СПХФА, 2010. — 44 с.
/ под ред. проф. А. В. Москвина. — СПб.: Изд-во СПХФА, 2010. — 44 с. Беляев Н. Н. — СПб.: Изд-во СПХФА, 2010, — 100с.
Беляев Н. Н. — СПб.: Изд-во СПХФА, 2010, — 100с.