Особенности строения атомов металлов
Таблица химических элементов содержит наименования и характеристики ста пяти различных веществ. Основная масса из них является металлами. Эти химические элементы имеют достаточно широкое распространение на нашей планете. Металлы можно встретить в различных соединениях в атмосфере и в недрах земли, в составе живых организмов и растений, а также водах океанов, морей озер и рек. Свойства данных химических элементов весьма специфичны. Их характеристики имеют ярко выраженные отличия от веществ других групп. Так, если элемент относится к разряду металла, то у него в обязательном порядке должен наблюдаться определенный перечень свойств:
– наличие плотной кристаллической структуры;
– выраженный блеск;
– способность к электрической проводимости;
– высокая степень теплопроводности;
– снижение способности проводить электричество с увеличением теплового режима;
– легкая отдача электронов;
– тягучесть, а также ковкость;
– способность образовывать различные сплавы.
Строение металлов, которое определено современным научным мировоззрением, представляет собой кристаллическую решетку. В ее основе находятся свободные электроны и ионы, обладающие положительным зарядом. Сам кристалл изображается в форме решетки, имеющей пространственную структуру. Узлы данной системы заняты ионами, а между ними находятся электроны, обладающие высокой способностью к движению. Строение атомов металлов позволяет активным частицам постоянно перемещаться. Электроны совершают переходы между атомами, а также вращаются вокруг их ядер. Зная особенности строения атомов металлов, можно легко объяснить возникновение в них электрического тока. Он появляется под воздействием разности потенциалов, когда электроны, не имеющие связей с ионами, начинают упорядоченное движение в одном направлении.
Особенности строения атомов металлов обуславливают и высокую тепловую проводимость данных элементов. Электроны, которые совершают непрерывное движение, обмениваются энергией с ионами в момент столкновения с последними. Элементы, находящиеся в узлах кристаллической решетки, передают колебания соседним частицам, те следующим и так далее. Вследствие этого процесса тепловой режим металла уравновешивается. В результате температура всей массы становится одинаковой.
Особенности строения атомов металлов заключаются в существовании между ними связей ковалентного характера. В кристаллической решетке присутствует также сила кулона, которая притягивает электроны и ионы. Это и есть металлическая связь, которая существует между частицами элемента. Данный тип соединения присутствует даже при наличии жидкого состояния вещества. Исходя из этого, можно сделать вывод, что металлической связью обладают не отдельные частицы. Ею владеют их агрегаты.
С точки зрения химии, особенности строения атомов металлов заключаются в беспрепятственной отдаче электронов валентности и переходе при этом в ионы. Вследствие этого, само вещество служит энергетическим восстановителем. Способность отдавать свои электроны у различных металлов находит свое проявление в различной степени. Чем легче происходит данный процесс, тем более активным считается элемент. При этом его взаимодействие с другими веществами происходит максимально энергично. Существует ряд напряжений, который опытным путем был составлен Бекетовым – русским ученым-химиком. Металлы в этом перечне находятся в определенной последовательности, которая характеризует убывание их химической способности к активности. Исходя из ряда напряжений, можно определить свойства элемента:
– при снижении электродного потенциала металла увеличивается его восстановительная функция;
– металлы способны вытеснять из солевых растворов те элементы, которые расположены после них в ряду напряжений;
– металлы, располагаемые в перечне активности слева от водорода, могут вытеснять его из кислотных растворов.
fb.ru
Основные сведения о строении атома: характеристики, особенности и формула
Атом – это мельчайшая частица химического вещества, которая способна сохранять его свойства. Слово «атом» происходит от древнегреческого «atomos», что означает «неделимый». В зависимости о того, сколько и каких частиц находится в атоме, можно определить химический элемент.
Кратко о строении атома
Как можно вкратце перечислить основные сведения о строении атома? Атом является частицей с одним ядром, которое заряжено положительно. Вокруг этого ядра расположено отрицательно заряженное облако из электронов. Каждый атом в своем обычном состоянии является нейтральным. Размер этой частицы полностью может быть определен размером электронного облака, которое окружает ядро.
Само ядро, в свою очередь, тоже состоит из более мелких частиц – протонов и нейтронов. Протоны являются положительно заряженными. Нейтроны не несут в себе никакого заряда. Однако протоны вместе с нейтронами объединяются в одну категорию и носят название нуклонов. Если необходимы основные сведения о строении атома кратко, то эта информация может быть ограничена перечисленными данными.

Первые сведения об атоме
О том же, что материя может состоять из мелких частиц, подозревали еще древние греки. Они полагали, что все существующее и состоит из атомов. Однако такое воззрение носило чисто философский характер и не может быть трактовано научно.
Первым основные сведения о строении атома получил английский ученый Джон Дальтон. Именно этот исследователь сумел обнаружить, что два химических элемента могут вступать в различные соотношения, и при этом каждая такая комбинация будет представлять собой новое вещество. Например, восемь частей элемента кислорода порождают собой углекислый газ. Четыре части кислорода – угарный газ.
В 1803 году Дальтон открыл так называемый закон кратных отношений в химии. При помощи косвенных измерений (так как ни один атом тогда не мог быть рассмотрен под тогдашними микроскопами) Дальтон сделал вывод об относительном весе атомов.

Исследования Резерфорда
Почти столетие спустя основные сведения о строении атомов были подтверждены еще одним английским химиком – Эрнестом Резерфордом. Ученый предложил модель электронной оболочки мельчайших частиц.
На тот момент названная Резерфордом «Планетарная модель атома» была одним из важнейших шагов, которые могла сделать химия. Основные сведения о строении атома свидетельствовали о том, что он похож на Солнечную систему: вокруг ядра по строго определенным орбитам вращаются частицы-электроны, подобно тому, как это делают планеты.
Электронная оболочка атомов и формулы атомов химических элементов
Электронная оболочка каждого из атомов содержит ровно столько электронов, сколько находится в его ядре протонов. Именно поэтому атом является нейтральным. В 1913 году еще один ученый получил основные сведения о строении атома. Формула Нильса Бора была похожа на ту, что получил Резерфорд. Согласно его концепции, электроны также вращаются вокруг ядра, расположенного в центре. Бор доработал теорию Резерфорда, внес стройность в ее факты.
Уже тогда были составлены формулы некоторых химических веществ. Например, схематически строение атома азота обозначается как 1s22s22p3, строение атома натрия выражается формулой 1s22s22p63s1. Через эти формулы можно увидеть, какое количество электронов движется по каждой из орбиталей того или иного химического вещества.

Модель Шредингера
Однако затем и эта атомная модель устарела. Основные сведения о строении атома, известные науке сегодня, во многом стали доступны благодаря исследованиям австрийского физика Э. Шредингера.
Он предложил новую модель его строения – волновую. К этому времени ученые уже доказали, что электрон наделен не только природой частицы, но обладает свойствами волны.
Однако у модели Шредингера и Резерфорда имеются и общие положения. Их теории сходны в том, что электроны существуют на определенных уровнях.
Такие уровни также называются электронными слоями. При помощи номера уровня может быть охарактеризована энергия электрона. Чем выше слой, тем большей энергией он обладает. Все уровни считаются снизу вверх, таким образом, номер уровня соответствует его энергии. Каждый из слоев в электронной оболочке атома имеет свои подуровни. При этом у первого уровня может быть один подуровень, у второго – два, у третьего – три и так далее (см. приведенные выше электронные формулы азота и натрия).

Еще более мелкие частицы
На данный момент, конечно, открыты еще более мелкие частицы, нежели электрон, протон и нейтрон. Известно, что протон состоит из кварков. Существуют и еще более мелкие частицы мироздания – например, нейтрино, который по своим размерам в сто раз меньше кварка и в миллиард раз меньше протона.
Нейтрино – это настолько мелкая частица, что она в 10 септиллионов раз меньше, чем, к примеру, тираннозавр. Сам тираннозавр во столько же раз меньших размеров, чем вся обозримая Вселенная.
Основные сведения о строении атома: радиоактивность
Всегда было известно, что ни одна химическая реакция не может превратить один элемент в другой. Но в процессе радиоактивного излучения это происходит самопроизвольно.
Радиоактивностью называют способность ядер атомов превращаться в другие ядра – более устойчивые. Когда люди получили основные сведения о строении атомов, изотопы в определенной мере могли служить воплощением мечтаний средневековых алхимиков.
В процессе распада изотопов испускается радиоактивное излучение. Впервые такое явление было обнаружено Беккерелем. Главный вид радиоактивного излучения – это альфа-распад. При нем происходит выброс альфа-частицы. Также существует бета-распад, при котором из ядра атома выбрасывается, соответственно, бета-частица.
Природные и искусственные изотопы
В настоящее время известно порядка 40 природных изотопов. Их большая часть расположена в трех категориях: урана-радия, тория и актиния. Все эти изотопы можно встретить в природе – в горных породах, почве, воздухе. Но помимо них, известно также порядка тысячи искусственно выведенных изотопов, которые получают в ядерных реакторах. Многие их таких изотопов используются в медицине, особенно в диагностике.

Пропорции внутри атома
Если представить себе атом, размеры которого будут сопоставимы с размерами международного спортивного стадиона, тогда можно визуально получить следующие пропорции. Электроны атома на таком «стадионе» будут располагаться на самом верху трибун. Каждый из них будет иметь размеры меньше, чем булавочная головка. Тогда ядро будет расположено в центре этого поля, а его размер будет не больше, чем размер горошины.
Иногда люди задают вопрос, как в действительности выглядит атом. На самом деле он в буквальном смысле слова не выглядит никак – не по той причине, что в науке используются недостаточно хорошие микроскопы. Размеры атома находятся в тех областях, где понятие «видимости» просто не существует.
Атомы обладают очень малыми размерами. Но насколько малы в действительности эти размеры? Факт состоит в том, что самая маленькая, едва различимая человеческим глазом крупица соли содержит в себе порядка одного квинтиллиона атомов.
Если же представить себе атом такого размера, который мог бы уместиться в человеческую руку, то тогда рядом с ним находились бы вирусы 300-метровой длины. Бактерии имели бы длину 3 км, а толщина человеческого волоса стала бы равна 150 км. В лежачем положении он смог бы выходить за границы земной атмосферы. А если бы такие пропорции были действительны, то человеческий волос в длину смог бы достигать Луны. Вот такой он непростой и интересный атом, изучением которого ученые продолжают заниматься и по сей день.
fb.ru
Особенности строения атома водорода :: SYL.ru
Самый распространенный элемент в космосе, состоящий из самых легких атомов, – это водород. Он открыт еще в 14 столетии великим алхимиком Парацельсом. Ученого по праву считают основоположником не только медицины, но и химии. Строение атома водорода было в дальнейшем детально рассмотрено Нильсом Бором. Элемент был затем обнаружен астрономами в составе Солнца и других планет, а также в газовых звездных туманностях. В них происходит процесс превращения атомов водорода в атомы гелия, иными словами, наблюдается ядерная реакция. В нашей статье мы изучим не только строение атома водорода, но и рассмотрим характерные особенности свойств этого химического элемента.
Место элемента в периодической системе Менделеева
Водород – единственный химический элемент, находящийся сразу в двух группах периодической системы: 1 и 7. Объяснить следующий факт можно так: он проявляет двойственные химические свойства. Особое строение атома водорода позволяет ему отдавать свой единственный электрон атомам, например, активных элементов – неметаллов. Это прежде всего галогены: агрессивные по своим свойствам фтор, хлор, бром и йод. Легко взаимодействует H2 и с халькогенами: серой, кислородом, селеном. В этом случае атомы водорода превращаются в катионы – положительно заряженные частицы.
Благодаря этой особенности элемент занимает место в первой группе периодической системы. Иначе выглядит механизм реакции между металлами и водородом. Согласно теории строения атома водорода по Н. Бору, элемент имеет один неспаренный электрон. Атом H принимает электроны от атомов активных щелочных или щелочноземельных металлов. Таким образом, его электронная конфигурация становится похожей на частицу инертного газа гелия. Единственный энергетический слой теперь полностью завершен. В данных процессах строение атома водорода изменяется и он переходит в форму аниона. Именно по этой причине элемент одновременно располагается в периодической системе еще и в ее 7 группе.

Все в сравнении
Продолжая изучать особенности строения водородных частиц, давайте посмотрим, насколько их внутренняя структура влияет на поведение элемента в реакциях. Для этого обратим внимание на его ближайших соседей по периодической системе и определим, каково строение атомов водорода, гелия и лития. С частицами инертного газа водород объединяет одинаковое количество энергетических уровней, с литием – похожее строение внешнего энергетического слоя, на котором расположен один электрон. Однако свойства водорода сильно отличаются как от инертного газа, так и от щелочного металла. Этот факт доказывает, что все характеристики химического элемента полостью определяются строением атома и молекулы водорода, то есть количеством энергетических уровней и распределением электронов на них.
Рождающий воду
Название элемента говорит о том, что соединение его атомов с частицами кислорода приводит к появлению такого уникального и важного для Земли вещества, как вода. В обычных условиях эта реакция не происходит, температура горения газовой смеси достигает 2800 °C. В лаборатории взаимодействие между H2 и O2 в соотношении 2:1 приводит к взрыву. Сама смесь получила название гремучего газа, а процесс, протекающий в ней, идет по свободно-радикальному механизму. Если его не контролировать, то реакция заканчивается серьезной проблемой – мощным взрывом. По этой причине, несмотря на его исключительную легкость, от водорода отказались как от наполнителя для воздушных летательных аппаратов. Печальным поводом послужило крушение в 1937 году дирижабля “Гинденбург”, направлявшегося в Америку. Посмотрим теперь, как строение атома водорода влияет на физические признаки газа.

Водород, дейтерий, тритий
Пусть вас не удивляет приведенный выше перечень терминов. Речь идет все об одном и том же химическом элементе водороде, заряд ядра атома которого равен +1. Второе и третье названия – это имена изотопов. Причина их различий заключается в количестве нейтронов в ядре, тогда как протонное число всех трех видов частиц одинаково. У дейтерия два нейтрона, у трития – 3, сам же водород имеет 1 нейтрон в составе своего ядра. Вода, содержащая в составе своих молекул дейтерий, называется тяжелой. Ее можно обнаружить в прудах-охладителях атомных станций, а также в составе цитоплазмы клеток, имеющих нарушения нормального метаболизма.
Электронное строение атома водорода
Схема, приведенная ниже, поможет нам понять специфику поведения простого вещества H2 в различных химических взаимодействиях.

Наличие единственного электрона, занявшего s-орбиталь первого энергетического уровня, обеспечивает постоянную валентность водорода, равную 1. В большинстве случаев этот электрон покидает пространство атома и переходит во владение более электроотрицательных элементов. Лишь реакции с металлами позволяют водороду притянуть в сферу влияния собственного ядра электрон от атомов активных щелочных или щелочноземельных элементов, образуя белые кристаллические соединения – их гидриды.
Активный и агрессивный
Атомарный водород, так сказать, легок на подъем. Его быстроте в восстановлении металлов из их оксидов могут позавидовать другие восстановители вроде углерода или его окислов. Так же активно атомы H соединяются с частицами серы, кислорода, фосфора. А пламя горелки с атомарным водородом дает разогрев выше 4000 °C. По этой причине такими приборами легко обрабатывать поверхности металлов: резать или сваривать их.

Атомарный водород хорошо зарекомендовал себя в качестве восстановителя чистых металлов – вольфрама, молибдена – из их руд, представленных в основном оксидами. Встречаясь с такими же атомами, как и он сам, водород образует устойчивую и пассивную структуру – молекулу. Оба атома H держатся друг за друга с помощью общей электронной пары, являясь образцом стабильной ковалентной неполярной связи. Она прочная и обеспечивает устойчивость молекул H2 как в условиях земного существования, так и на просторах космоса. Не обошлась без водорода и пищевая промышленность, в которой его применяют для гидрогенизации масел и получения модных в современной диетологии низкокалорийных спредов.

В нашей статье мы рассмотрели, каково строение атома водорода, и выяснили, как оно влияет на свойства простого вещества
www.syl.ru
Особенности строения атома углерода
1. Четыре валентных орбитали. Четыре свободных электрона. Максимальная ковалентность (IV). Самый малый радиус. Самые прочные связи.
2. Атом углерода способен к ковалентному связыванию как с электроположительными, так и с электроотрицательными элементами.
3. Атом углерода образует химические связи с высокими значениями энергии.
| С-С 348 кДж/моль | N-N 250кДж/моль | Si-Si 226кДж/моль |
| С-Н 415кДж/моль | S-S 225кДж/моль | |
| С-O 360кДж/моль | O-O 146кДж/моль |
На углеродном остове могут прочно «крепиться» самые разнообразные функциональные группировки.
Атом углерода способен к катенации (формирование циклов, цепей любой длины и разветвлённости).
4. Атом углерода обладает сопоставимой величиной энергий s- и p- орбиталей. (Переход атома в возбужденное состояние, три валентных состояния –sp3-,sp2– иsp- гибридизация).
Сравнительная характеристика неорганический и органических соединений представлена в таблице
1.2 Теории строения органических веществ. Изомеризация ,виды изомеризации.
Теория строения органических соединений. 1861 г. А.М. Бутлеров
«Химическая натура сложной частицы определяется натурой элементарных составных частей, количеством их и химическим строением».
Таблица 1- Сравнительная характеристикаорганических и неорганических соединений и реакций с их участием
| Неорганические соединения | Органические соединения |
| Высокополярны. Часто солеобразны. Хорошо растворимы в воде. Их растворы и расплавы электропроводны. Имеют высокие Тпл, Ткип. В реакции вступают легко, реагируют очень быстро. Для успешного осуществления реакций не требуются особые условия (температура, катализатор и др.). Выходы в реакциях высокие. | Малополярны. Не растворимы в воде. Неэлектролиты. Имеют низкие Тпл, Ткип. В реакции вступают плохо, реагируют очень медленно. Для успешного осуществления реакций требуются особые условия (температура, катализатор, облучение и др.) – дополнительная энергия для разрыва и образования ковалентных связей. Выходы в реакциях низкие. Часто образуется смесь изомеров, т.к. одновременно протекают несколько конкурирующих реакций по разным реакционным центрам субстрата. |
| Основная причина отличий в свойствах – природа связи в молекулах | |
| Ионная | Ковалентная |
Положения теории:
1. Атомы в молекулах соединяются друг с другом в определённой последовательности, согласно их валентности. Эта последовательность атомов называется химическим строением.
Структурная формула – изображение химических связей в молекуле с учетом их валентности.
2. Свойства органических веществ зависят не только от их качественного и количественного состава, но и от того, в каком порядке соединены атомы в молекулах, т.е. от химического строения.
3. Атомы в молекулах взаимно влияют друг на друга.
4. Свойства органических веществ определяются их строением, и, наоборот, зная свойства, можно прогнозировать строение веществ.
Физические и химические свойства органических соединений определяются составом их молекул, а также химическим, пространственным и электронным строением.
Изомерия органических соединений
Изомерия– явление существования веществ с одинаковым качественным и количественным составом, но различными свойствами(1830 г. Берцелиус).
Причина изомерии стала понятной лишь после появления теории химического строения А.М. Бутлерова (1861 г.) – различное строение молекул, обусловленное способностью атома углерода к образованию
4-хковалентных связей, в том числе и с др. атомами углерода.
| Виды изомерии | |
| Структурная: – обусловлена разным порядком соединения атомов в молекуле. | Пространственная (стереоизомерия): – обусловлена различным расположением заместителей относительно друг друга в пространстве. |
| 1. С-скелета; | 1. Геометрическая; |
| 2. Положения: | 2. Оптическая; |
| а) кратных связей; | 3. Конформационная; |
| б) заместителей; | 4. Конфигурационная. |
| в) функциональных групп; | |
| 3. Межклассовая; | |
| 4. Таутомерия. |
Структурная изомерия
Количество изомеров С-скелета очень быстро возрастает с увеличением числа С-атомов:
| Гексан (6) | 5 изомеров |
| Гептан (7) | 9 изомеров |
| Октан (8) | 18 изомеров |
| Нонан (9) | 35 изомеров |
| Декан (10) | 75 возможных изомеров |
| Эйкосан (20) | 366315 возможных изомеров |
| В случае циклоалканов изомерия скелета может быть обусловлена различным числом атомов углерода в кольце: |
Изомерия положения

infopedia.su
Особенности строения атомов металлов
Таблица химических элементов содержит наименования и характеристики ста пяти различных веществ. Основная масса из них является металлами. Эти химические элементы имеют достаточно широкое распространение на нашей планете. Металлы можно встретить в различных соединениях в атмосфере и в недрах земли, в составе живых организмов и растений, а также водах океанов, морей озер и рек. Свойства данных химических элементов весьма специфичны. Их характеристики имеют ярко выраженные отличия от веществ других групп. Так, если элемент относится к разряду металла, то у него в обязательном порядке должен наблюдаться определенный перечень свойств:
– наличие плотной кристаллической структуры;
– выраженный блеск;
– способность к электрической проводимости;
– высокая степень теплопроводности;
– снижение способности проводить электричество с увеличением теплового режима;
– легкая отдача электронов;
– тягучесть, а также ковкость;
– способность образовывать различные сплавы.
Строение металлов, которое определено современным научным мировоззрением, представляет собой кристаллическую решетку. В ее основе находятся свободные электроны и ионы, обладающие положительным зарядом. Сам кристалл изображается в форме решетки, имеющей пространственную структуру. Узлы данной системы заняты ионами, а между ними находятся электроны, обладающие высокой способностью к движению. Строение атомов металлов позволяет активным частицам постоянно перемещаться. Электроны совершают переходы между атомами, а также вращаются вокруг их ядер. Зная особенности строения атомов металлов, можно легко объяснить возникновение в них электрического тока. Он появляется под воздействием разности потенциалов, когда электроны, не имеющие связей с ионами, начинают упорядоченное движение в одном направлении.
Особенности строения атомов металлов обуславливают и высокую тепловую проводимость данных элементов. Электроны, которые совершают непрерывное движение, обмениваются энергией с ионами в момент столкновения с последними. Элементы, находящиеся в узлах кристаллической решетки, передают колебания соседним частицам, те следующим и так далее. Вследствие этого процесса тепловой режим металла уравновешивается. В результате температура всей массы становится одинаковой.
Особенности строения атомов металлов заключаются в существовании между ними связей ковалентного характера. В кристаллической решетке присутствует также сила кулона, которая притягивает электроны и ионы. Это и есть металлическая связь, которая существует между частицами элемента. Данный тип соединения присутствует даже при наличии жидкого состояния вещества. Исходя из этого, можно сделать вывод, что металлической связью обладают не отдельные частицы. Ею владеют их агрегаты.
С точки зрения химии, особенности строения атомов металлов заключаются в беспрепятственной отдаче электронов валентности и переходе при этом в ионы. Вследствие этого, само вещество служит энергетическим восстановителем. Способность отдавать свои электроны у различных металлов находит свое проявление в различной степени. Чем легче происходит данный процесс, тем более активным считается элемент. При этом его взаимодействие с другими веществами происходит максимально энергично. Существует ряд напряжений, который опытным путем был составлен Бекетовым – русским ученым-химиком. Металлы в этом перечне находятся в определенной последовательности, которая характеризует убывание их химической способности к активности. Исходя из ряда напряжений, можно определить свойства элемента:
– при снижении электродного потенциала металла увеличивается его восстановительная функция;
– металлы способны вытеснять из солевых растворов те элементы, которые расположены после них в ряду напряжений;
– металлы, располагаемые в перечне активности слева от водорода, могут вытеснять его из кислотных растворов.
autogear.ru
Особенность – электронное строение – атом
Особенность – электронное строение – атом
Cтраница 1
Особенности электронного строения атомов определяют закономерности в изменении свойств элементов в периодической системе. [1]
Особенности электронного строения атома бора и его большой размер ( радиус атома бора 0 088 нм) по сравнению с атомами азота ( 0 070 нм) и углерода ( 0 077 нм) делают характерным для боридов в отличие от нитридов и карбидов наличие в структуре непосредственных связей между атомами бора. Это отличает их от типичных фаз внедрения, причем различные комбинации sp3 – и 5р2 – гидридных орбиталей атома бора обусловливают большое многообразие структур, образуемых боридами. [2]
Таким образом, прочность химической связи в газообразных и твердых моносульфидах определяется главным образом особенностями электронного строения атомов лантаноидов, что и находит выражение в характеристиках испарения этих соединений. [3]
Это возрастание монотонно, если не считать резкого отклонения для карбида хрома Сг3С2, которое может быть объяснено с учетом
Разделение металлов на простые ( sp) и переходные ( с дефектными d – и / – оболочками), обусловленное особенностями электронного строения атомов
Систематическое, целенаправленное и осознанное изучение огромного фактического материала современной неорганической химии невозможно без руководящего принципа, роль которого играют Периодический закон и Периодическая система элементов как его графическое выражение. Физическая сущность этого явления заключается в
Основным продуктом, гидрирования является фур иловый спирт. Rum) бертоллидного каталитического комплекса, который является результатом особенностей электронного строения атомов компонентов и их положения в периодической системе. [7]
Определим сродство к электрону как энергию, выделяемую или поглощаемую при присоединении электрона к нейтральному атому в газообразном состоянии. Знак и численное значение этой величины зависят от тех же
Таким образом, каждый период, хотя и похож на другие, отличается определенным своеобразием. На фоне закономерного изменения свойств элементов в группах наблюдается вторичная периодичность – немонотонное изменение свойств элементов, сопряженное с особенностями электронного строения атомов в отдельных периодах. Вкратце эти особенности сводятся к следующему. [10]
Алюминий образует соединения почти со всеми элементами Периодической системы. Физико-химические свойства алюминидов обусловлены особенностями электронного строения атомов алюминия. [11]
Систематическое, целенаправленное и осознанное изучение огромного фактического материала современной неорганической химии невозможно без руководящего принципа, роль которого играют периодический закон и периодическая система элементов как его графическое выражение. Без преувеличения можно сказать, что уровень квалификации химика определяется тем, насколько он способен творчески и свободно использовать те общие закономерности в изменении природы химической связи, химического и кри-сталлохимического строения, свойств веществ, которые диктуются явлением периодичности. Физическая сущность этого явления заключается в особенностях электронного строения атомов. [12]
Систематическое, целенаправленное и осознанное изучение огромного фактического материала современной неорганической химии невозможно без руководящего принципа, роль которого играют Периодический закон и Периодическая система элементов как его графическое выражение. Без преувеличения можно сказать, что уровень квалификации химика определяется тем, насколько он способен творчески и свободно использовать те общие закономерности в изменении характера химической связи, химического и кристаллохимического строения, свойств веществ, которые диктуются явлением периодичности. Физическая сущность этого явления заключается в особенностях электронного строения атомов. [13]
Так как вокруг атомов растворенного элемента в объеме кристалла решетка всегда искажена, то, следовательно, всегда существует упругое взаимодействие этих атомов с межзеренной границей. Получается, что все растворенные элементы в той или иной степени должны быть горофильны. Однако имеются экспериментальные данные о том, что некоторые элементы горофобны – их концентрация на границе зерен меньше, чем в объеме. Это значит что, кроме упругого, существует еще и химическое взаимодействие атомов растворенного элемента с межзеренной границей, которое ( в зависимости от особенностей электронного строения атомов) может способствовать равновесной сегрегации на границе, а может, перекрывая упругое притяжение, вызывать очищение приграничной зоны от атомов растворенного элемента. [14]
Страницы: 1 2
www.ngpedia.ru
Периодическая система элементов и ее связь со строением атома. Особенности электронного строения атомов в главных и побочных подгруппах: s-, p-, d-, f-элементы.
Итак, главной характеристикой атома является не атомная масса, а величина положительного заряда ядра. Это более общая точная характеристика атома, а значит, и элемента. От величины положительного заряда ядра атома зависят все свойства Элемента и его положение в периодической системе. Таким образом, порядковый номер химического элемента численно совпадает с зарядом ядра его атома. Периодическая система элементов является графическим изображением периодического закона и отражает строение атомов элементов.
В каждом периоде с возрастанием порядкового номера элементов металлические свойства постепенно ослабевают и возрастают неметаллические, заканчивается период инертным газом.
В зависимости от того, какой подуровень заполняется электронами, все элементы делят на четыре типа.
1. s-элементы. Заполняется s-подуровень внешнего уровня (s1 — s2). Сюда относятся первые два элемента каждого периода.
2. р-элементы. Заполняется р-подуровень внешнего уровня (р1 — p6)- Сюда относятся последние шесть элементов каждого периода, начиная со второго.
3. d-элементы. Заполняется d-подуровень последнего уровня (d1 — d10), а на последнем (внешнем) уровне остается 1 или 2 электрона. К ним относятся элементы вставных декад (10) больших периодов, начиная с 4-го, расположенные между s- и p-элементами (их также называют переходными элементами).
4. f-элементы. Заполняется f-подуровень глубинного (треть его снаружи) уровня (f1 —f14), а строение внешнего электронного уровня остается неизменным. Это лантаноиды и актиноиды, находящиеся в шестом и седьмом периодах.
Итак, строение атомов обуславливает две закономерности:
а) изменение свойств элементов по горизонтали — в периоде слева направо ослабляются металлические и усиливаются неметаллические свойства;
б) изменение свойств элементов по вертикали — в группе с ростом порядкового номера усиливаются металлические свойства и ослабевают неметаллические.
Таким образом: по мере возрастания заряда ядра атомов химических элементов периодически изменяется строение их электронных оболочек, что является причиной периодического изменения их свойств.
Радиусы атомов (орбитальные и эффективные) и их изменение по периодической системе. Атомные и ионные радиусы, и зависимость от электронного строения и степени окисления. Энергия ионизации атомов и ионов. Сродство к электрону. Электроотрицательность.
Орбитальные радиусы (rорб) – это расстояния от ядра до главного максимума функции радиального распределения электронной плотности. Эти величины рассчитаны квантово-механическими методами для всех элементов периодической системы.
Эффективные радиусы (rэфф), в отличие от орбитальных, определяют экспериментально из значений межъядерных расстояний в молекулах или в кристаллах.
На атомные радиусы элементов оказывают влияние следующие факторы:
1. Эффективный заряд ядра. Увеличение Zэфф при прочих равных условиях усиливает притяжение валентных электронов к ядру и, следовательно, уменьшает радиус.
2. Число энергетических уровней, заполненных электронами. Увеличение числа электронных слоев атома способствует увеличению его радиуса.
3. Электронная конфигурация атома.
Проанализируем закономерности изменения атомных радиусов в периодической системе элементов. В периодах число электронных слоев не изменяется, а эффективный заряд ядер растет. Можно ожидать, что в периодах слева направо будет наблюдаться тенденция к уменьшению атомных радиусов.
Несколько сложнее изменение атомных радиусов в больших периодах. Так, в IV периоде атомные радиусы монотонно уменьшаются по рядам s-элементов (К – Са) и d-элементов (Sc – Zn)
Для VI периода наблюдается резкое уменьшение радиуса при переходе от элемента IIIB-подгруппы к элементу IVB-подгруппы.
Энергия ионизации – это количество энергии, необходимое для отрыва электрона от атома или иона данного элемента. Различают первую, вторую, третью и т.д. энергии ионизации, соответствующие удалению первого, второго, третьего и т.д. электрона атомной частицы.
Сродство к электрону (Еэл) – это энергетический эффект присоединения электрона к атомной частице.
Электроотрицательность элемента – это характеристика, определяющая способность его атома притягивать к себе электроны, участвующие в образовании химических связей.
9. Ковалентная связь. Метод валентных связей. Механизм образования ковалентной связи (обменный, донорно-акцепторный, дативный). Свойства ковалентной связи: направленность, насыщаемость. Характеристики химической связи: длина, энергия. σ-, и π-связи, их особенности.
Ковалентная связь – это связь между атомами, при которой образуются одна или несколько общих электронных пар.
Для описания ковалентной связи используют преимущественно два метода, основанных на разных приближениях при решении уравнения Шредингера: метод молекулярных орбиталей и метод валентных связей.
Метод валентных связей основывается на положении, что каждая пара атомов в химической частице удерживается вместе при помощи одной или нескольких электронных пар.
Различают несколько механизмов образования ковалентной связи: обменный (равноценный), донорно-акцепторный, дативный.
При использовании обменного механизма образование связи рассматривается как результат спаривания спинов свободных электронов атомов. При этом осуществляется перекрывание двух атомных орбиталей соседних атомов, каждая из которых занята одним электроном. Таким образом, каждый из связываемых атомов выделяет для обобществления пары по электрону, как бы обмениваясь ими.
По донорно-акцепторному механизму перекрывается орбиталь с парой электронов одного атома и свободная орбиталь другого атома. В этом случае в области перекрывания также оказывается пара электронов.
Атомы, у которых внешняя электронная оболочка включает d-орбитали, могут выступать в роли и донора, и акцептора пар электронов. В этом случае рассматривается дативный механизм образования связи.
Одно из существенных свойств ковалентной связи – ее насыщаемость. При ограниченном числе внешних электронов в областях между ядрами образуется ограниченное число электронных пар вблизи каждого атома (и, следовательно, число химических связей). Именно это число тесно связано с понятием валентности атома в молекуле (валентностью называют общее число ковалентных связей, образуемых атомом). Другое важное свойство ковалентной связи – ее направленность в пространстве.
Энергия E0, необходимая для того, чтобы разъединить атомы и удалить их друг от друга на расстояние, на котором они не взаимодействуют, называется энергией связи.
Межъядерное расстояние между химически связанными атомами называется длинойхимической связи.
Перекрывание атомных орбиталей вдоль линии, связывающей ядра атомов, приводит к образованию σ-связей. Между двумя атомами в химической частице возможна только одна σ-связь. Все σ-связи обладают осевой симметрией относительно межъядерной оси.
При дополнительном перекрывании атомных орбиталей, перпендикулярных линии связи, образуются π-связи.
С появлением π-связи, не имеющей осевой симметрии, свободное вращение фрагментов химической частицы вокруг σ-связи становится невозможным, так как оно должно привести к разрыву π-связи.
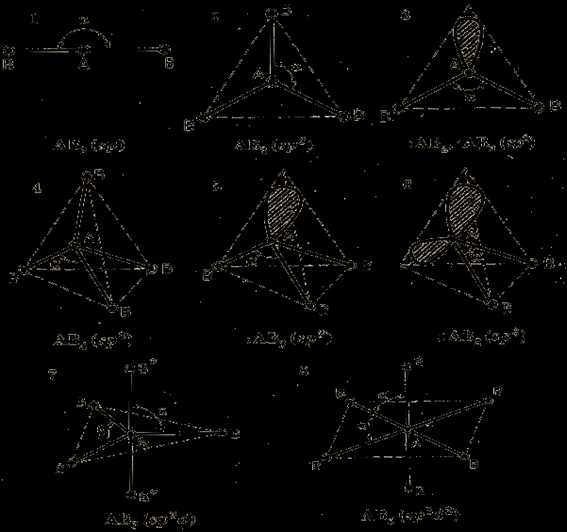
10. Гибридизация волновых функций, примеры sp-, sp2-, sp3-, sp3d-, sp3d2 – гибридизаций. Делокализация π-связи. Длина одинарных и кратных связей, их энергия.
Гибридизация – это изменение формы некоторых орбиталей при образовании ковалентной связи для достижения более эффективного перекрывания орбиталей.
Делокализованная связь – это ковалентная связь, молекулярная орбиталь которой охватывает более двух атомов.
infopedia.su
