Элементы переходные – Справочник химика 21
Кроме бериллия, электролизом расплавленных солей можно получать и другие тугоплавкие металлы (скандий, иттрий, титан, цирконий, гафний, торий, ванадий, ниобий, тантал, хром, молибден, вольфрам и рений). Все они являются элементами переходных групп периодической системы, для которых характерно образование катионов нескольких валентностей. [c.530] Нецелесообразно сравнивать рассмотренные выше ионы металлов с ионами переходных элементов, у которых важную роль при комплексообразовании играют незаполненные -орбитали. Более того, даже довольно трудно сравнивать эти ионы между собой. Устойчивость комплексов, образуемых ионами элементов переходных рядов, зависит не только от ионного потенциала, но и от таких переменных, как энергия стабилизации кристаллическим полем, наличие пустых -орбиталей для принятия л-электронов лиганда, наличие пар -электронов для обратной дативной я-связи. Все эти факторы можно объединить, сказав, что устойчивость комплекса в значительной мере зависит от числа -электронов в ионе или атоме переходного металла.
Органические соединения остальных переходных элементов. Переходные элементы остальных (кроме ПБ) побочных подгрупп периодической системы в проявляемых их атомами степенях окисления имеют незавершенные электронные -подоболочки предвнешнего уровня. Поэтому, наряду с образованием ординарной полярной ковалентной связи с углеродом за счет вклада внешних з- и р-орбиталей, они способны образовывать совершенно иные по строению и свойствам соединения за счет участия ( -орбиталей. В таких соединениях металл можно так же, как и соединения магния, бора, алюминия (см. выше), считать координационно ненасыщенным. Данная ненасыщенность металла теперь определяется наличием вакантных орбиталей не только на внешнем, но и на втором снаружи энергетических уровнях его атома.

Чем отличаются элементы, принадлежащие к трем важнейшим категориям,-типические элементы, переходные металлы и внутренние переходные металлы [c.324]
Утверждены некоторые групповые названия элементов. Так, элементы Не, Ые, Аг, Кг, Хе, Кп принято называть благородные газы элементы Р, С1, Вг, I, А1 — галогены элементы О, 5, Зе,, Те, Ро — халькогены элементы Ыа, К, РЬ, Сз, Рг — щелочные элементы элементы Са, 5г, Ва, Ка — щелочноземельные элементы элементы с порядковыми номерами 57—71 (от Ьа до-Ьи включительно) — лантаноиды (до 1965 г.
В последнее время в промышленности при проведении этерификации используют амфотерные катализаторы — соединения элементов переходной валентности, из которых наибольший интерес представляют производные алюминия, титана и олова, в частности тетрабутоксититан, С тетрабутоксититаном этерификация карбоновых кислот спиртами осуществляется при 170—200 °С до достижении кислотного числа ие более 0,35. Применение этого катализатора позволяет упростить стадии обработки эфира-сырца,, повысить степень конверсии, т. е. снизить расходные нормы на сырье и улучшить качество пластификаторов. [c.338]
Рассмотренный случайный процесс будет полностью определен, когда задано правило расчета элементов переходной матрицы Рц и элементов матрицы оценок гп ,.
 Структура матрицы 5 во многом зависит от гидродинамической обстановки в аппарате [109]. [c.135]
Структура матрицы 5 во многом зависит от гидродинамической обстановки в аппарате [109]. [c.135]Расчет толщины стенки конического элемента переходной части производится с помощью отношения (31 — с)/(хг — по условию (7.22). [c.140]
До открытия трансурановых элементов (нептуния и др.) положение урана, так же как тория и протактиния (атомные номера 92, 91 и 90), в периодической системе Менделеева не вызывало сомнения их помещали под переходными элементами шестого периода — гафнием, танталом и вольфрамом. В соответствии с тем, что у атомов Nb, Та и W идет достройка электронного уровня 5 d, принималось, что у Th, Ра и и происходит заполнение электронного уровня 6 d. Химические свойства тория, протактиния и урана в значительной степени напоминают свойства элементов переходных групп IVa (Ti, Zr, Hf), Va (V, Nb, Та) и Via ( r, Mo, W) [171 ]. По этой причине в большинстве довоенных учебников, а также статьях уран считали аналогом Сг, Мо и W и помещали в VI подгруппу периодической системы.
XVI. ЭЛЕМЕНТЫ ПЕРЕХОДНЫХ РЯДОВ [c.181]
Элементы, относящиеся к этому классу, выделены из элементов переходных рядов. Это обусловлено особенностью в строении электронных оболочек их атомов. В их атомах незаполненными оказываются три слоя, в том числе п — 2)/-подуровни. В общем электронная конфигурация атомов элементов этого класса [п — [c.105]
Одновременно был уточнен и чрезвычайно важный вопрос о числе еще не открытых элементов. Принятая в то время форма периодической системы, с одной стороны, оставляла возможность предполагать существование элементов, переходных между водородом (который ставился в I группу) и гелием, с другой — создавала существенную неясность, касающуюся как числа, так и расположения элементов в промежутке между Ва и Та. Работы Мозли со всей определенностью установили, что между водородом и гелием новых элементов быть не может и что общее их число между Ва и Та равно шестнадцати.  219]
219]
Заполнение s-орбиталей происходит в главных подгруппах I и И групп системы Менделеева, почему соответствующие элементы и называют иногда 5-элементами. У элементов главных подгрупп П1—Vn групп заполняются р-орбитали. Элементы этих подгрупп, а также благородные газы —это р-элементы. Переходные металлы в побочных подгруппах образуют совокупность -элементов в их атомах заполняются d-орбитали.
По характеру химической связи элементов с углеродом и другими элементами в их составе элементоорганические соединения делят на две большие группы. В первую группу включают соединения в- и р-элементов непереходных элементов), а во вторую — органические производные й- и /-элементов (переходных элементов). Для соединений первой группы характерно образование ковалентных полярных органических производных второй группы типичны комплексные соединения с участием -электронов предвнешней электронной оболочки атомов элемента. Существуют и другие способы классификации, однако свойства элементоорганических соедршений столь разнообразны, что проще рассмотреть наиболее типичные из них в порядке изменения строения электронной оболочки атома элемента, как это делалось при рассмотрении свойств неорганических соединений.
В последовательности элементов углерод идет сразу же за бором и кремний за алюминием, но затем элементы IV группы периодической системы — германий, олово и свинец — значительно отдалены от соответствующих элементов III группы — скандия, иттрия и лантана. Германий от скандия отделен десятью элементами переходного ряда железа, олово от иттрия отделено десятью элементами переходного ряда палладия и свинец от лантана—десятью элементами переходного ряда платины и четырнадцатью лантаноидами.
Первая реакция идет значительно быстрее, чем вторая. Необходимым условием протекания обеих реакций является легкое отщепление и присоединение электрона катионом. Это свойство присуще элементам переходной валентности, занимающим [c.182]
Из приведенных данных о влиянии металлов на скорость окислительной деструкции ясно, насколько важна эффективная дезактивация остатков катализаторов полимеризации. Важно также, чтобы в полимер не попали железо и медь.
Непереходные элементы Переходные элементы [c.36]
Расчет толщины стенки конического элемента переходной части производят с помощью условия (3.75). [c.58]
Теоретическая форма линии имеет симметричный вид относительно максимума интенсивности. Однако для ряда элементов форма линии несимметрична. Особенно сильна асимметрия у элементов переходной группы железа. Такая асимметрия линии объясняется спин-спино-вым взаимодействием 2р-электронов с электронами незаполненной Зй-оболочки [3]. Это взаимодействие приводит к расщеплению 2р-уровня, несимметричному относительно начального положения 2р-уровня. Так как расщепление меньше полной ширины каждого из подуровней, то форма результирующей линии становится асимметричной. Аналогичная картина асимметрии линий рентгеновского излучения наблюдается в некоторых химических соединениях и сплавах и связана с характером химических связей [3]. [c.806]
Аналогичная картина асимметрии линий рентгеновского излучения наблюдается в некоторых химических соединениях и сплавах и связана с характером химических связей [3]. [c.806]
Современные формы периодической таблицы. Периоды и группы. Типические (непереходные) элементы, переходные металлы и внутренние переходные. металлы (лантаноиды и актиноиды). Семейства элементов семи.металлы, щелочные. металлы, щсло июзсмглькыс . сталли и галогены. [c.302]
Реакции замещения в водных растворах — наиболее простой способ получения комплексов. Этот способ основан на взаимодействии гидратирО Ванного ио,на металла с координируемым лигандом. Если металл относится к элементам переходных рядов, реакция обычно сопровождается изменением цвета раствора. [c.190]
Исходя из электронной конфигурации, можно различать четыре класса элементов инертные газы, типичные элементы, переходные элементы и внутрирядные переходные элементы. Эта классификация основывается на том, в какой степени заполнены подуровни 3, р, (1 и /, т. е. на том, заполнены или нет те или иные орбитали. При заполненном подуровне следует обратить внимание на числа электронов в различных уровнях (слоях) у данного атома и числа электронов в соответствующих уровнях у атома предыдущего по порядковому номеру или ближайшего следующего инертного газа. [c.103]
Эта классификация основывается на том, в какой степени заполнены подуровни 3, р, (1 и /, т. е. на том, заполнены или нет те или иные орбитали. При заполненном подуровне следует обратить внимание на числа электронов в различных уровнях (слоях) у данного атома и числа электронов в соответствующих уровнях у атома предыдущего по порядковому номеру или ближайшего следующего инертного газа. [c.103]
Важнейшим проявлением специфики электронного строения и вытекающих отсюда химических свойств платиновых элементов является их склонность к образованию комплексных соединений. Элементы-металлы других групп периодической системы, особенно поливалентные элементы переходных рядов, также дают комплексные соединения той или иной устойчивости практически со всеми известными лигандами. Спецификой комплексных соединений платиновых элементов и прежде всего наиболее изученных комплексов платины и палладия является высокая прочность ковалентной связи, обусловливающая кинетическую инертность этих соединений. Последнее даже делает невозможным определение обычными методами такой важной характеристики комплекса, как его /Сует- Обмен лигандами внутри комплекса и с лигандами из окружающей среды также затруднен. Это позволяет конструировать, например, октаэдрические комплексы платины (IV), в которых все шесть лигандов различны. Такие системы могут существовать без изменения во времени состава как в растворах, так и в твердом состоянии. Мы уже отмечали, что, напротив, осуществить синтез столь раз-нолигандмых комплексов для элементов-металлов, образующих пре- [c.152]
Последнее даже делает невозможным определение обычными методами такой важной характеристики комплекса, как его /Сует- Обмен лигандами внутри комплекса и с лигандами из окружающей среды также затруднен. Это позволяет конструировать, например, октаэдрические комплексы платины (IV), в которых все шесть лигандов различны. Такие системы могут существовать без изменения во времени состава как в растворах, так и в твердом состоянии. Мы уже отмечали, что, напротив, осуществить синтез столь раз-нолигандмых комплексов для элементов-металлов, образующих пре- [c.152]
Классификация анионов, как и катионов, связана с положением соответствующих элементов в периодической системе Д. И. Менделеева. Наиболее типичные и часто встречающиеся анноны образуются элементами II, III, IV и V периодов. В таблице на форзаце отмечены элементы, образующие амфотерные, кислотно-амфотерные, щелочноам-фотерные соединения в IV и V периодах — элементы, образующие анионы, находятся в 4-м и б-м рядах, а также составляющие семейства элементов переходных, побочных подгрупп. [c.42]
[c.42]
Э. X. принято подразделять на металлы п неметаллы. К неметаллам относят 22 элемента — Н, В, С, Si, N, Р, As, О, S, Se, Те, га югены и инертные газы, к металлам — все остальные. В зависимости от того, какой электронный уровень — S, р, d или f содержит электроны в атомах данного Э. X. самой высокой знергии, различают s-, p-, d- и -элементы. К s-элементам относят Н, Не, а также металлы главных подгрупп I и П групп периодич. системы, к р-эле-ментам — элементы главных подгрупп III—VIII групп, к ( -элементам — металлы побочных подгрупп III—VIII групп (кроме лантаноидов и актиноидов, к-рые принадлежат к f-элементам). s- и р-Элементы наз. непереходными, d- и -элементы — переходными. Э. х., все изотопы к-рых радиоактивны, наз. редиоактивными к ним относятся Тс, Рт, Ро и все элементы с более высокими, чем у Ро, ат. номерами. [c.707]
Н, Не, а также металлы главных подфупп I и П фупп периодич. системы, к / -элементам – алементы главных под-фупп Ш-УШ Фупп, к -элементам – металлы побочных подфупп 1-УШ фупп (кроме лантаноидов и акпиноидов, принадлежащих к/-элементам) и / -элементы наз. непереходными, и /-элементы – переходны ш. Э. х., все изотопы к-рых радиоактивны, наз. радиоактивными. [c.472]
непереходными, и /-элементы – переходны ш. Э. х., все изотопы к-рых радиоактивны, наз. радиоактивными. [c.472]
Как известно, название актиниды патучило сейчас широкое распространение, и в настоящее время бачьшинство ученых считают, что элементы, начиная с актиния, следует располагать в периодической системе Менделеева как семейство, аналогичное семейству лантанидов [2, 7, 50, 51, 148, 170, 221, 294]. Но все-таки электронную структуру и место этих элементов в периодической системе нельзя рассматривать как твердо установленные [227]. Сходство химических свойств актинидов, в частности Ра, Th и U, с лантани-дами, с одной стороны, и элементами переходных подгрупп IVa, Va и Via, с другой стороны, говорит о двойственности химической природы актинидных элементов [147, 148]. Поскольку разность энергетических уровней таких удаленных подгрупп, как 5/ и 6d [c.6]
В образовании МО участвуют только валентные электроны, т. е. электроны последней, валентной оболочки атомов.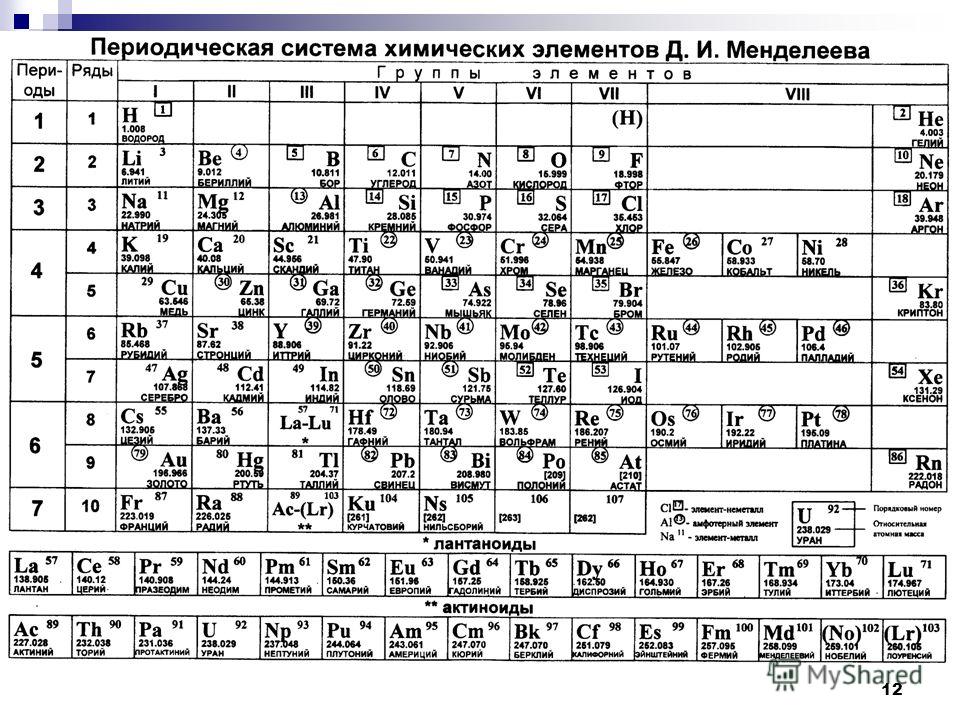 При этом в образовании МО могут участвовать не только атомные, но и молекулярные орбитали (Д-А-связь). Так, в атоме С1 с электронной оболочкой в 2 2р Ъз Ър не могут участвовать в образовании МО электронные уровни с главным квантовым числом и = 1 и и = 2. У многих элементов переходных рядов больших периодов периодической системы Д. И. Менделеева наблюдается заполнение электронами как пу- и и пoдypoвнeй, так и предыдущего n- )d- или n-iy-уровня. В соединениях этих элементов связывающими могут оказаться кроме л-уровня, Е также (и – )d- и реже (и – 2)/ уровни. [c.63]
При этом в образовании МО могут участвовать не только атомные, но и молекулярные орбитали (Д-А-связь). Так, в атоме С1 с электронной оболочкой в 2 2р Ъз Ър не могут участвовать в образовании МО электронные уровни с главным квантовым числом и = 1 и и = 2. У многих элементов переходных рядов больших периодов периодической системы Д. И. Менделеева наблюдается заполнение электронами как пу- и и пoдypoвнeй, так и предыдущего n- )d- или n-iy-уровня. В соединениях этих элементов связывающими могут оказаться кроме л-уровня, Е также (и – )d- и реже (и – 2)/ уровни. [c.63]
Октаэдрическая координация наблюдается в основном у элементов переходных групп и в особенности в координационных комплексах Вернера этого и следовало ожидать, так как для гибридизации необходимо наличие неполностью занятых -орбиталей центрального атома. Даже если для образования этих гибридных АО необходима затрата энергии, их появление объясняется способностью образовывать сильные связи (согласно определению Полинга, упомянутому в разделе 8.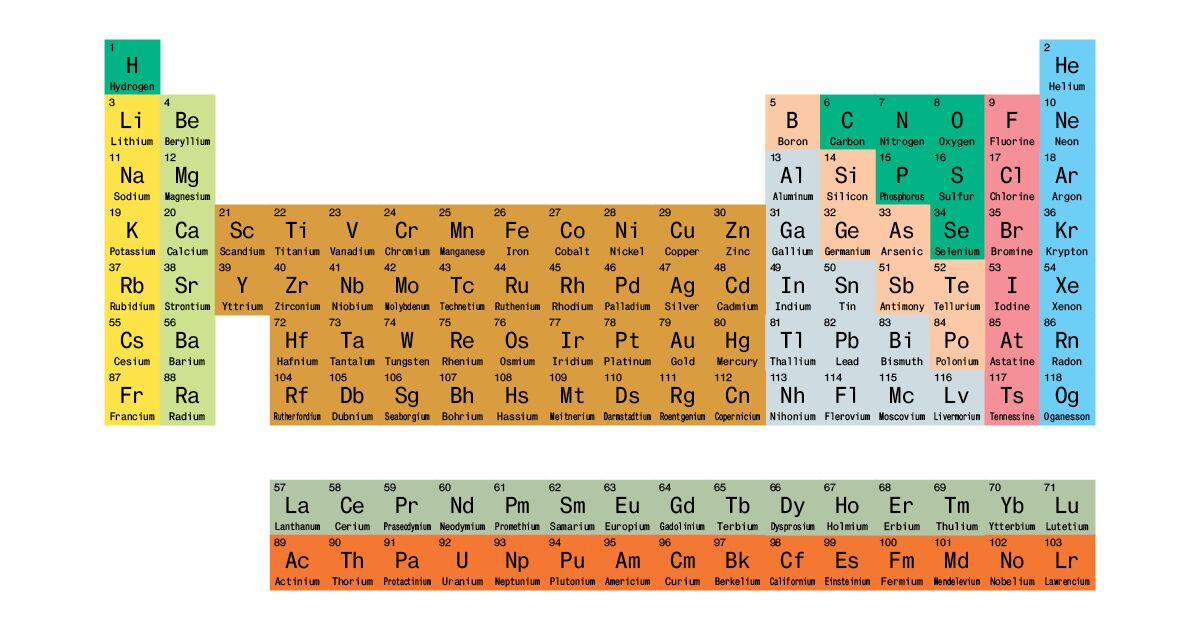 5, сила октаэдрической орбитали равна 2,923, в то время как силы 5-, р-, -ор-биталей равны соответственно 1, 1,732, 2,236). Так, образование [c.243]
5, сила октаэдрической орбитали равна 2,923, в то время как силы 5-, р-, -ор-биталей равны соответственно 1, 1,732, 2,236). Так, образование [c.243]
Теплоты образования в газовой фазе АЯгаз для комплексных ионов элементов переходных периодов могут быть рассмотрены с точки зрения [c.37]
Химия (1978) — [ c.472 , c.484 , c.486 ]
Общая химия (1979) — [ c.343 ]
Общая химия (1964) — [ c.93 , c.100 , c.417 ]
Курс неорганической химии (1963) — [ c.23 , c.41 ]
Современная неорганическая химия Часть 3 (1969) — [
c. 0
,
c.3
,
c.9
]
0
,
c.3
,
c.9
]
Аналитическая химия (1975) — [ c.26 ]
Общая химия (1974) — [ c.124 , c.509 , c.511 , c.595 , c.649 ]
Ионообменные смолы (1952) — [ c.63 ]
Общая химия (1968) — [ c.82 , c.629 ]
Курс неорганической химии (1972) — [ c.23 , c.39 ]
Переходные металлы | Transition Metal Complexes in Organic Synthesis
Периодическая система всегда под руками
В органической химии элементов немного, и можно не сомневаться, что любой человек, осмелившийся назвать себя химиком, помнит, где находится углерод, кислород, азот и галогены, и уж тем более водород.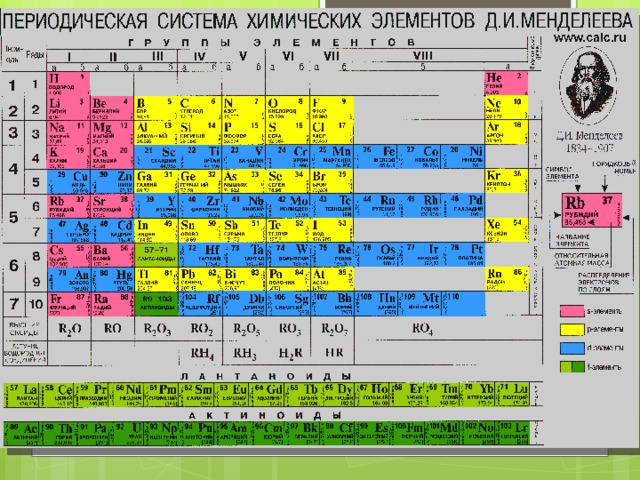 В химии переходных металлов элементов намного больше, и упомнить их все не всем по силам, и человек, даже отдавший химии всю жизнь, имеет полное право замешкаться, вспоминая, где, например, находится какой-нибудь иридий, и элемент ли это вообще, а может быть цветок какой аленький или синенький.
В химии переходных металлов элементов намного больше, и упомнить их все не всем по силам, и человек, даже отдавший химии всю жизнь, имеет полное право замешкаться, вспоминая, где, например, находится какой-нибудь иридий, и элемент ли это вообще, а может быть цветок какой аленький или синенький.
Но здесь это совершенно необходимо – мы все время будем считать электроны, оценивать положение элементов в группах и рядах, и не попадаться на глупые вопросы, например, про катализ кросс-сочетания фосфиновыми комплексами свинца. Фосфиновые комплексы у свинца вполне могут быть, но металл это непереходный, а следовательно нам в этом курсе малоинтересный. Вторая буква в символе просто предательская – перевернем ее и все встанет на свои места.
Поэтому сразу обзаведемся Периодической таблицей элементов. Для наших целей больше подходит не привычная с детства (раннего или позднего, кому как повезло) уютная и компактная короткопериодная таблица, восходящая еще к Д.И.Менделееву, а так называемая длиннопериодная. Историческая короткопериодная таблица была основана на ранжировании элементов по единственно доступному в глубокой древности параметру, атомным весам. Ни о каких электронах, а тем более атомных орбиталях, валентных оболочках и пр. тогда не было известно совершенно ничего. Короткопериодная форма поэтому мешает в группах элементы различных типов, разделяя их только по неочевидным на близорукий взгляд главным и побочным подгруппам. Но самая неудачная особенность исторической формы – запихивание 15 элементов в одну восьмую группу, что делает непростым понимание того, чем все эти восхитительные элементы различаются, и почему только им, благородным газам и металлам, и тройке более банальных металлов досталась такая свалка. Воздадим поэтому должное восхищение величию исторической Таблицы, и перейдем к более современной форме, которая построена по заполнению валентных уровней электронами, и четко разделяет разные блоки элементов.
Историческая короткопериодная таблица была основана на ранжировании элементов по единственно доступному в глубокой древности параметру, атомным весам. Ни о каких электронах, а тем более атомных орбиталях, валентных оболочках и пр. тогда не было известно совершенно ничего. Короткопериодная форма поэтому мешает в группах элементы различных типов, разделяя их только по неочевидным на близорукий взгляд главным и побочным подгруппам. Но самая неудачная особенность исторической формы – запихивание 15 элементов в одну восьмую группу, что делает непростым понимание того, чем все эти восхитительные элементы различаются, и почему только им, благородным газам и металлам, и тройке более банальных металлов досталась такая свалка. Воздадим поэтому должное восхищение величию исторической Таблицы, и перейдем к более современной форме, которая построена по заполнению валентных уровней электронами, и четко разделяет разные блоки элементов.
Вот она, в некрасивом, но максимально авторитетном виде, рекомендованным Международным союзом по чистой и прикладной химии (IUPAC), в Номенклатуре неорганических и координационных соединений 2005 года. Многим она как-то интуитивно не нравится, она слишком длинная и плохо вписывается на задние страницы тетрадей и учебников, не умещается целиком в поле зрения, и вообще какая-то странно ступенчатая, на нормальную таблицу никак не похожа. Читать ее приходится, мотая головой слева направо и обратно, почти как болельщику на теннисном матче. Но структура у нее совершенно гениальная – элементы расположены строго по мере заполнения валентных оболочек, поэтому все элементы естественным путем образуют блоки s-, p-, d- и f-элементов (последние приходится вынести наружу, но место их в таблице хорошо понятно. Вместо восьми групп имеем 18, а это очень важное число в счете электронов, соответствующее полностью заполненной валентной spd-оболочке. Да, при этом оказались обижены первые три периода, которым эти 18 электронов могут только присниться, и которые обречены блюсти более скромный 2-х и 8-электронный счет (правило октета Льюиса), но это мелочи.
Многим она как-то интуитивно не нравится, она слишком длинная и плохо вписывается на задние страницы тетрадей и учебников, не умещается целиком в поле зрения, и вообще какая-то странно ступенчатая, на нормальную таблицу никак не похожа. Читать ее приходится, мотая головой слева направо и обратно, почти как болельщику на теннисном матче. Но структура у нее совершенно гениальная – элементы расположены строго по мере заполнения валентных оболочек, поэтому все элементы естественным путем образуют блоки s-, p-, d- и f-элементов (последние приходится вынести наружу, но место их в таблице хорошо понятно. Вместо восьми групп имеем 18, а это очень важное число в счете электронов, соответствующее полностью заполненной валентной spd-оболочке. Да, при этом оказались обижены первые три периода, которым эти 18 электронов могут только присниться, и которые обречены блюсти более скромный 2-х и 8-электронный счет (правило октета Льюиса), но это мелочи.
Кто-то может спросить, а какая разница, какой Таблицей пользоваться, все равно все понимают, как они устроены, и что там где. Безусловно это так, но здесь имеются в виду конкретные и простые вещи, в первую очередь система нумерации групп и рядов. Если мы будем, например, упоминать металлы 8-й группы, то это однозначно и только железо-рутений-осмий, а не вообще все 9 или даже 15 элементов, как в исторической таблице. И мы не будем падать в обморок от ссылок на элементы 10-й или 12-й групп. И не будем путать второй ряд переходных металлов с вторым периодом, и не будем возмущенно вопрошать, откуда там взялись переходные металлы, когда каждый знает, что во втором периоде из металлов только литий и бериллий.
Безусловно это так, но здесь имеются в виду конкретные и простые вещи, в первую очередь система нумерации групп и рядов. Если мы будем, например, упоминать металлы 8-й группы, то это однозначно и только железо-рутений-осмий, а не вообще все 9 или даже 15 элементов, как в исторической таблице. И мы не будем падать в обморок от ссылок на элементы 10-й или 12-й групп. И не будем путать второй ряд переходных металлов с вторым периодом, и не будем возмущенно вопрошать, откуда там взялись переходные металлы, когда каждый знает, что во втором периоде из металлов только литий и бериллий.
Разработана модель для предсказания новых металлоорганических структур
В работе исследуются металлоорганические структуры, формирующиеся на поверхности твердого тела в процессе поглощения органических молекул и атомов металлов. По данным Большой российской энциклопедии, в природе металлорганические структуры встречаются редко, в качестве примера можно привести формы витамина B12, связанного с активностью различных ферментов клетки. Эти вещества используются человеком в качестве лекарственных препаратов и регуляторов процессов горения.
Эти вещества используются человеком в качестве лекарственных препаратов и регуляторов процессов горения.
Авторы статьи заинтересовались этой темой, когда узнали о работе американских исследователей, которые в 2011 году наблюдали в микроскоп металлоорганические структуры. Они показались знакомыми российским ученым: подобные образуются в однокомпонентном слое тримезиновой кислоты на поверхности золота. Сотрудники Омского государственного технического университета задумались: возможно ли это и в двухкомпонентной металлоорганической системе и как на это влияет тип координирующего атома металла. Для ответа они использовали разрабатываемую ими программу SuSMoST для моделирования адсорбционных монослоев – слоев молекул из газовой смеси на поверхности вещества. Была создана модель специально для класса молекул с треугольной симметрией расположения функциональных пиридиновых групп. Именно они способны соединяться друг с другом через атом переходного металла (элементы между s- и р-элементами в таблице Менделеева).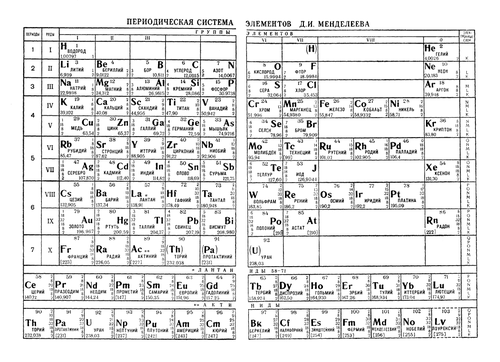 Модель описывает самосборку сотовой структуры, ряда цветочных фаз и треугольной структуры.
Модель описывает самосборку сотовой структуры, ряда цветочных фаз и треугольной структуры.
В исследованиях в качестве поверхности применяли золото Au(111) из-за его относительной химической пассивности, а также переходные металлы (Fe, Ni, Co, Cu) и органическое вещество — 1,3,5-трис (4-пиридил) бензол. В качестве параметра для модели использовалась разница между энергиями двойной и тройной координации — единовременная связь атома металла с двумя или тремя молекулами соответственно. Исследователи изучали такие взаимодействия в адсорбционном слое, контактирующем с поверхностью золота. Для этого применялись методы DFT, Монте-Карло и TRG. Так, с помощью метода расчета электронной структуры заданной системы DFT вычислили энергию координационных связей между молекулой и атомом металла.
«Монте-Карло и TRG — это наиболее мощные методы современной статистической физики. Они дополняют друг друга: Монте-Карло подходит для любых систем, но он приблизительный, а TRG точный, но имеет ограничения по применимости.
С помощью этих методов мы рассчитали основные термодинамические характеристики модельных металлоорганических слоев», — поясняет Виталий Горбунов, доцент, старший научный сотрудник кафедры «Химия и химическая технология» Омского государственного технического университета.
С помощью этих методов определялось влияние типа металлического центра на фазовое поведение адсорбционного слоя: от него зависит предпочтительный вид координации молекул. Учитывая значение параметров каждого из переходных металлов, провели статистическое моделирование в той же программе SuSMoST. Так, выяснилось, что атомы меди и серебра имеют тенденцию образовывать двойную координацию, а железо, кобальт и никель — тройную.
Для проведения эксперимента была важна устойчивость к температурам: ученые выяснили, что некоторые из наблюдаемых структур разрушаются с течением времени. Также оказалось, что структуры устойчивых фаз (сотовой, цветочной и треугольной) двухкомпонентного слоя аналогичны структурам фаз в однокомпонентном адсорбционном слое тримезиновой кислоты на поверхности золота.
«Металлоорганические адсорбционные слои потенциально применимы в молекулярной электронике, поскольку обладают уникальными электромагнитными свойствами, также могут служить модельными системами для ферментативного катализа. Наша модель предсказывает образование новых металлоорганических структур в таких системах и может послужить фундаментом для дальнейшего исследования их функциональных свойств. Мы надеемся, что результаты, полученные в нашей работе, стимулируют экспериментальный поиск предсказанных нами структур», — говорит Виталий Горбунов.
9 класс. Урок химии “Переходные металлы” (“Амфотерность”) – МКОУ средняя общеобразовательная школа д.Васькино
Разработка урока химии в 9 классе по теме “Переходные металлы” (“Амфотерность”) по программе О.С. Габриеляна.
Задачи урока:
- создать условия для развития умений учащихся давать характеристику химических элементов на основании положения в ПСХЭ.

- организовать деятельность учащихся по изучению и первичному закреплению понятия «амфотерность».
- содействовать развитию у учащихся исследовательских умений в процессе выполнения и наблюдения эксперимента.
Требования к уровню подготовки учащихся:
объяснять:
- физический смысл атомного (порядкового) номера химического элемента, номеров группы и периода, к которым элемент принадлежит в периодической системе Д.И. Менделеева;
- закономерности изменения свойств элементов в пределах малых периодов и главных подгрупп
характеризовать:
- химические элементы на основе их положения в периодической системе Д.И.Менделеева и особенностей строения их атомов;
- химические свойства основных классов неорганических веществ;
составлять:
- формулы неорганических соединений изученных классов;
- схемы строения атомов первых 20 элементов периодической системы Д.
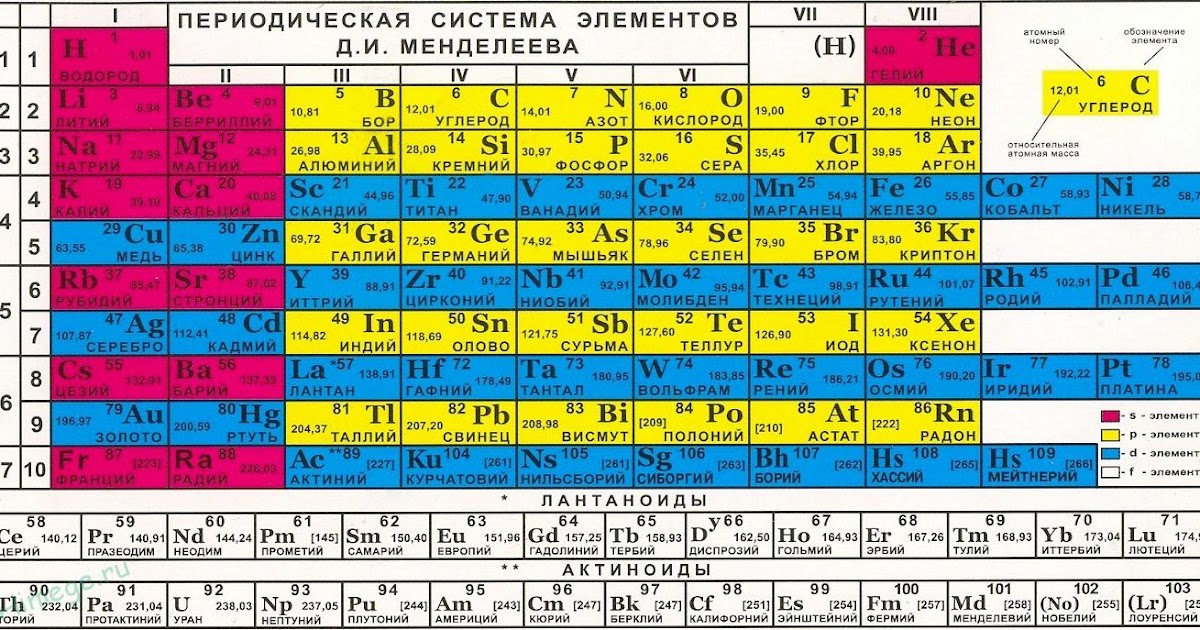 И.Менделеева;
И.Менделеева; - уравнения химических реакций;
обращаться с химической посудой и лабораторным оборудованием.
Оборудование: ПСХЭ, таблица «Зависимость диссоциации гидроксидов от заряда ядра и радиуса центрального атома», штатив с пробирками, универсальный индикатор, оксид хрома(VI), растворы: хлорида хрома(III), сульфата цинка, гидроксида натрия, соляной кислоты.
На столах учащихся: штатив для пробирок, 2 пробирки, растворы: сульфата цинка, гидроксида натрия, соляная кислота.
Ход урока:
1. Организационный момент.
2. Проверка домашнего задания.
3. Актуализация знаний учащихся – фронтальная беседа.
1) На какие группы делят химические элементы по проявляемым свойствам?
2) На какие группы делят химические элементы по электронному строению?
3) Как изменяются металлические свойства атомов химических элементов, расположенных в одной главной группе?
4) Объясните причину усиления металлических свойств атомов химических элементов, расположенных в одной главной группе.
5) Какие окислительно-восстановительные свойства характерны для атомов металлов?
6) Как изменяются металлические свойства атомов химических элементов, расположенных в одном малом периоде?
7) Объясните причину ослабления металлических свойств атомов химических элементов, расположенных в одном малом периоде.
8) Какие окислительно-восстановительные свойства характерны для атомов неметаллов?
4. Постановка целей и задач урока.
Познакомиться с особенностями строения атомов переходных химических элементов, свойствами их оксидов и гидроксидов.
5. Переходные элементы расположены в побочных подгруппах больших периодов периодической системы. Они являются d- и f-элементами. Название «переходные» связано с тем, что в периодах переходные элементы вклиниваются между s- и р-элементами.
IV, V и VI периоды содержат по 10 d-элементов, VI период включает также 14 f-элементов (лантаноиды). В незавершенном VII периоде известно 7 d-элементов, начиная с Ac, и 14 f-элементов (актиноиды). В отличие от s- и p-элементов, у которых заполняется внешний энергетический уровень (соответственно ns- и np-оболочки), у атомов переходных элементов заполняются внутренние (n – 1) d-оболочки (d-элементы) или (n – 2) f-оболочки (f-элементы).
В отличие от s- и p-элементов, у которых заполняется внешний энергетический уровень (соответственно ns- и np-оболочки), у атомов переходных элементов заполняются внутренние (n – 1) d-оболочки (d-элементы) или (n – 2) f-оболочки (f-элементы).
Задание. Дать характеристику цинка на основании его положения в Периодической системе химических элементов.
Для выяснения характера гидроксида цинка и его оксида выполним лабораторную работу. Ознакомьтесь с инструкцией. Какие вещества необходимы для выполнения работы? Ответьте на вопросы, перечисленные в начале инструкции.
ЛАБОРАТОРНАЯ РАБОТА
Получение гидроксида цинка и исследование его свойств.
Рассмотрите схему опытов получения и исследования свойств гидроксида цинка.
Какие действия вам нужно выполнить по ходу лабораторной работы? Какова их цель?
Целесообразно ли выполнять все предложенные опыты?
Выполните все предложенные опыты.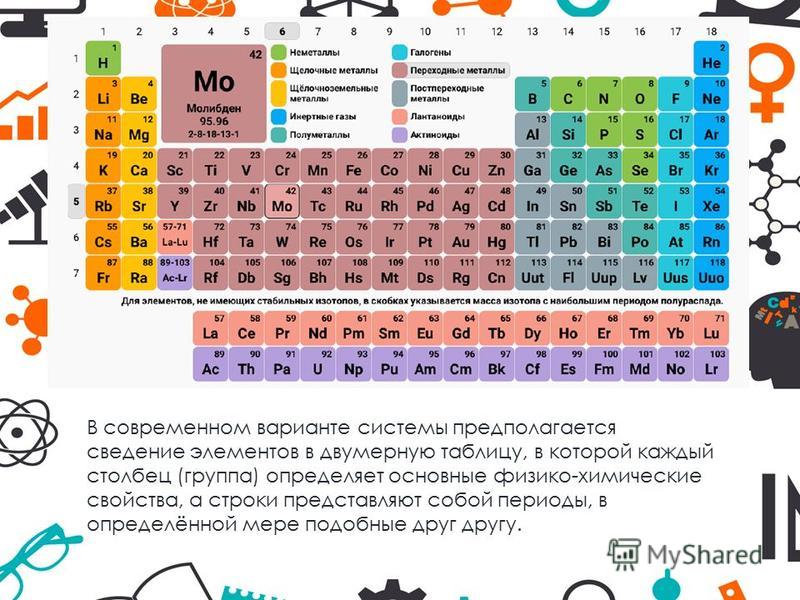 Запишите сделанные наблюдения, составьте уравнения проведенных реакций в молекулярной и ионной форме.
Запишите сделанные наблюдения, составьте уравнения проведенных реакций в молекулярной и ионной форме.
Сделайте вывод, какими свойствами обладает гидроксид цинка.
Обсуждение результата лабораторной работы.
Гидроксид цинка взаимодействует как с раствором кислоты, так и с раствором щелочи. В чем причина такого необычного поведения гидроксида цинка как нерастворимого основания? Чтобы ответить на этот вопрос вспомним, что взаимодействовать могут гидроксиды, проявляющие противоположные свойства:
основание + кислота = соль + вода.
В реакции с кислотой гидроксид цинка выступает в роли основания:
Zn(OH)2 + 2HCl = ZnCl2 + 2H2O.
В реакции с основанием гидроксид цинка проявляет свойства кислоты:
2NaOH + Zn(OH)2 = Na2ZnO2 + 2H2O.
Формулу гидроксида цинка можно записать как основной форме Zn(OH)2, так и в кислотной – H2ZnO2.
Более правильно данную реакцию записать в следующем виде:
2NaOH + Zn(OH)2 = Na2[Zn(OH)4] .
Аналогичными свойствами обладает не только гидроксид цинка, но его оксид:
ZnO + 2HCl = ZnCl2 + H2O.
2NaOH + ZnO + Н2О = Na2[Zn(OH)4] .
Амфотерные соединения – вещества, которые в зависимости от условий проявляют кислотные или основные свойства.
Элементы, образующие амфотерные оксиды и гидроксиды, в Периодической системе химических элементов обозначены зеленым цветом. Как видно из Периодической системы, к этим элементам относят большинство переходных металлов, а также бериллий и алюминий.
Большинство d-металлов не имеют постоянной степени окисления и образуют соответственно несколько оксидов и гидроксидов. Например, хром в соединениях проявляет степени окисления +2, +3, +6.
Задание. Составьте формулы всех оксидов и гидроксидов хрома, заполните таблицу.
| Cr+2 | Cr+3 | Cr+6 |
| Формула оксида | CrO | Cr2O3 | CrO3 |
| Формула гидроксида | Cr(OH)2 | Cr(OH)3 | H2CrO4 |
| Характер оксида и гидроксида | основный | амфотерный | кислотный |
Демонстрация. Получение гидроксида хрома(III) и изучение его кислотно-основных свойств.
Получение гидроксида хрома(III) и изучение его кислотно-основных свойств.
CrCl3 + 3NaOH = Cr(OH)3 + 3NaCl.
Cr(OH)3 + 3HCl = CrCl3 + 3H2O.
Cr(OH)3 + 3NaOH = Na3[Cr(OH)6] + H2O.
Вывод – гидроксид хрома(III) – амфотерный гидроксид.
Демонстрация. Получение хромовой кислоты и изучение ее кислотно-основных свойств.
CrО3 + Н2O = Н2CrO4.
Испытание раствора хромовой кислоты универсальным индикатором.
Вывод – гидроксид хрома(VI) – кислотный гидроксид.
Оксид и гидроксид хрома в низшей степени окисления имеют основные свойства, в вышей – кислотные, а в промежуточной – амфотерные. Эта закономерность справедлива не только для соединений хрома, но и для соединений всех переходных металлов, имеющих разные степени окисления.
Обобщим изменение кислотно-основных свойств атомов химических элементов на примере элементов III периода.
Алюминий стоит на границе между элементами, проявляющими металлические и неметаллические свойства. Он отличается от остальных химических элементов III периода. У него произошло совмещение двух противоположных свойств – металлических и неметаллических. Этот факт отражается на свойствах соединений алюминия, его оксида и гидроксида. Они проявляют амфотерный характер.
Таким образом, изменение кислотно-основных свойств оксидов и гидроксидов химических элементов, расположенных в одном периоде происходит постепенно: от элементов–металлов, через элементы, образующие амфотерные оксиды и гидроксиды к элементам–неметаллам.
10. Закрепление.
Дайте определение понятий:
Переходный элемент
Амфотерные соединения.
Ответьте на вопрос:
От чего зависит химическая роль амфотерного соединения в химической реакции?
. pdf (1 161КБ)
pdf (1 161КБ)
Переходные металлы (разработка урока)
Тема: Металлы
Урок: Переходные металлы
1. Общие свойства переходных металловПереходные элементы располагаются в побочных подгруппах Периодической системы Д.И. Менделеева. Их подразделяют на d-элементы и f-элементы. f-элементы – это лантаноиды и актиноиды.
При образовании соединений атомы металлов могут использовать не только валентные s- и p-электроны , но и d-электроны. Поэтому для d-элементов гораздо более характерна переменная валентность, чем для элементов главных подгрупп. Благодаря этому свойству переходные металлы часто образуют комплексные соединения.
Переходные элементы – это металлы. Поэтому в своих соединениях они проявляют положительные степени окисления.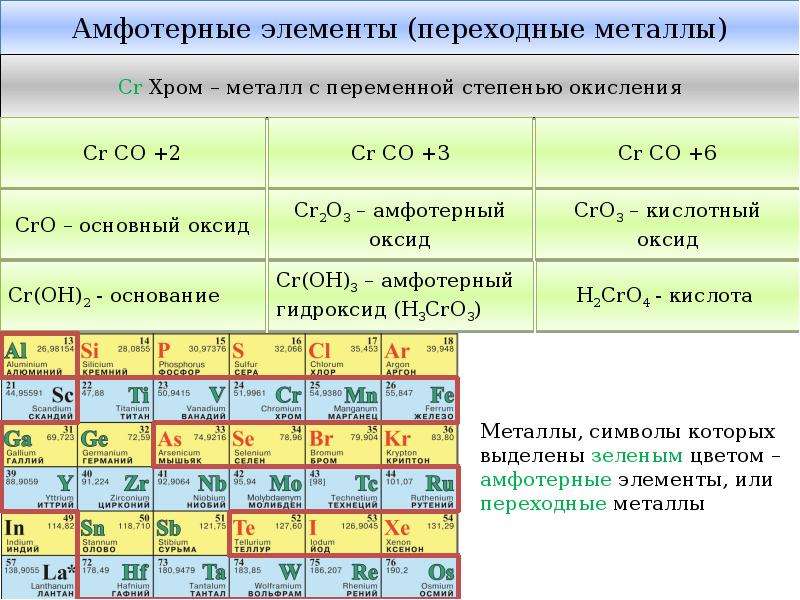 Очень сильно видно различие в свойствах у элементов IV–VIII подгрупп периодической системы. Элементы побочных подгрупп – это металлы, а главных подгрупп – неметаллы. Однако, когда элементы главных и побочных подгрупп находятся в высших степенях окисления, их соединения проявляют заметное сходство.
Очень сильно видно различие в свойствах у элементов IV–VIII подгрупп периодической системы. Элементы побочных подгрупп – это металлы, а главных подгрупп – неметаллы. Однако, когда элементы главных и побочных подгрупп находятся в высших степенях окисления, их соединения проявляют заметное сходство.
Например, оксид CrO3 близок по свойствам SO3. Оба эти вещества в обычных условиях находятся в твердом состоянии и образуют при взаимодействии с водой кислоты состава H2ЭO4. Точно также – оксиды марганца и хлора. Соответствующие им высшие оксиды – Mn2O7 и Cl2O7. Им соответствуют кислоты состава HЭО4. Подобная близость свойств объясняется тем, что часто элементы главных и побочных подгрупп в высших степенях окисления приобретают сходное электронное строение. Что касается химических свойств d-элементов, то обращает на себя внимание тот факт, что в пределах одной декады переходных элементов число стабильных степеней окисления сначала увеличивается, а потом уменьшается. См. Табл. 1. Химические свойства переходных элементов довольно сложны.
См. Табл. 1. Химические свойства переходных элементов довольно сложны.
Табл. 1
Значение переходных металлов для организма и жизнедеятельности
Без переходных металлов наш организм существовать не может. Железо – это действующее начало гемоглобина. Цинк участвует в выработке инсулина. Кобальт – центр витамина
В-12. Медь, марганец и молибден, а также некоторые другие металлы входят в состав ферментов.
Многие переходные металлы и их соединения используются в качестве катализаторов. Например, реакция гидрирования алкенов на платиновом или палладиевом катализаторе. Полимеризация этилена проводится с помощью титансодержащих катализаторов.
Рис. 1
Большое использование сплавов переходных металлов: сталь, чугун, бронза, латунь, победит. Рис. 1. При исследовании сплавов прослеживается уникальное значение железа для человека. Сплавы даже разделяют на черные и цветные по содержанию в них железа.
Сплавы даже разделяют на черные и цветные по содержанию в них железа.
Химические свойства железа и его соединений
Железо – это химический элемент №26, который находится в побочной подгруппе VIII группы, в четвертом периоде. Электронная конфигурация атома железа – 1s22s22p63s23p63d64s2.
Рис. 2
Распределение валентных электронов на орбиталях представлено на Рис. 2.
Степени окисления железа: 0, +2, +3. Соединения железа (III) проявляют слабые окислительные свойства, образуемые оксиды и гидроксиды Fe2O3 и Fe(OH)3 проявляют амфотерные свойства, хотя основные свойства у этих соединений значительно преобладают.
1. Взаимодействие с неметаллами
При нагревании железо, особенно порошкообразное, способно взаимодействовать практически со всеми неметаллами. Хлор и фтор окисляют железо до Fe+3. Бром может окислить и до Fe+2, и до Fe+3 в зависимости от количества, а йод окисляет только до степени окисления +2 Fe+2. При реакции с серой сначала образуется сульфид железа, а затем дисульфид железа.
Хлор и фтор окисляют железо до Fe+3. Бром может окислить и до Fe+2, и до Fe+3 в зависимости от количества, а йод окисляет только до степени окисления +2 Fe+2. При реакции с серой сначала образуется сульфид железа, а затем дисульфид железа.
Fe + S FeS
FeS + S FeS2 природный минерал такого состава называется пирит. Рис. 3.
Он используется для получения серной кислоты, а также железа и соединений железа.
Рис. 3
2. Взаимодействие железа с кислородом
При взаимодействии железа с кислородом, в зависимости от его количества, могут образовываться разные оксиды. В том числе и смешанный оксид Fe3O4.
2Fe + О2 2FeО
4Fe + 3О2 2Fe2О3
3Fe + 2О2 Fe3О4
3. Взаимодействие железа с водой
Взаимодействие железа с водой
При сильном нагревании металлическое железо взаимодействует с водой.
3Fe + 4Н2О Fe3О4 + 4Н2↑
Во влажном воздухе при обычных условиях железо реагирует с парами воды и кислородом, с образованием ржавчины. Она состоит из смешенных оксидов, гидроксидов и соединений кислорода. Это не индивидуальное вещество.
Примерная схема ржавления железа:
4Fe + 6Н2О + 3О2 → 4Fe(ОН)3
4. Взаимодействие железа с кислотами
Как и другие типичные металлы, железо взаимодействует с кислотами-неокислителями с выделением водорода.
Fe + 2НCl → FeCl2 + Н2↑
С кислотами-окислителями железо не реагирует из-за пассивации. Но с разбавленными кислотами реакция происходит.
Fe + 4НNO3 → Fe(NO3)3 +NO↑ + 2Н2O
5. С растворами солей
Металлическое железо вытесняет менее активные металлы из растворов их солей.
Fe + CuSO4 → Cu + FeSO4
Амфотерные свойства железа
Железо и некоторые его соединения способны проявлять амфотерные свойства.
Fe + 2NaOH + 2H2O → Na2[Fe(OH)4] + H2↑ В горячем концентрированном растворе щелочи образуется комплексное соединение, и выделяется водород.
3. Соединения железа (II) и железа (III)Соединения железа (II)
Соли железа (II) можно получить при взаимодействии металлического железа с кислотами-неокислителями или восстановлением железа (III).
2FeCl3 + Fe→ 3FeCl2
Соединения железа (II) обладают восстановительными свойствами.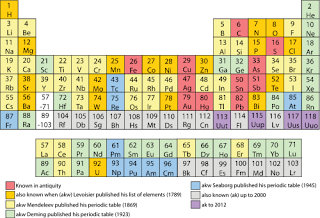
FeCl2 + 2NaOH → Fe(OH)2 ↓+ 2NaCl. На воздухе Fe(OH)2 ↓окисляется кислородом.
4Fe(OH)2 ↓+2H2O + O2 → 4Fe(OH)3↓
Соединения железа (III)
Соли железа (III) получают либо окислением железа галогенами, либо при его взаимодействии с разбавленными кислотами-окислителями. Соли железа (III) могут проявлять слабые окислительные свойства.
2FeCl3 +2 KI → 2FeCl2 + I2↓ + 2KCl. На этой реакции основан йодометрический способ определения солей железа.
Качественная реакция на соли железа (III)
FeCl3 + 6NaSCN →Na3[Fe(SCN)6] + 3NaCl. При взаимодействии с роданидами образуются ярко-красные, похожие на кровь комплексы различного состава.
Взаимодействие со щелочью.
FeCl3 + 3NaOH → Fe(OH)3 ↓+ 3NaCl
Fe(OH)3 ↓как и Fe(OH)2 ↓ амфотерен, с преобладанием основных свойств.
Fe(OH)3 ↓+3HCl → FeCl3 + 3H2O
Fe(OH)3 + NaOH → NaFeO2+ 2H2O
4. Железная кислотаЖелезная кислота и её соли
При окислении Fe(OH)3 ↓ или при электролизе раствора щелочи на железном аноде образуются соли, содержащие железо в составе аниона:
2Fe(OH)3 + 3Cl2 + 10NaOH →2Na2FeO4 + 6NaCl + 8H2O
Fe + 2KOH + 2H2O K2FeO4 + 3H2↑
Железо имеет степень окисления +6. Такие соли называются ферраты: Na2FeO4, K2FeO4. Это соли не существующей в свободном виде железной кислоты Н2FeO4. Они относятся к наиболее сильным органическим окислителям и способны медленно окислять даже воду.
Подведение итога урока
В ходе урока вы изучили тему «Переходные металлы». Вы узнали о некоторых общих свойствах переходных металлов, о химических свойствах железа как наиболее важного переходного металла. Мы подчеркнули важность и необходимость для организма человека наличия именно переходных металлов. Рассмотрели некоторые примеры сплавов переходных металлов, исследовали амфотерные свойства железа и его соединений с различными степенями окисления. Немного узнали о железной кислоте и ее солях – ферратах.
Вы узнали о некоторых общих свойствах переходных металлов, о химических свойствах железа как наиболее важного переходного металла. Мы подчеркнули важность и необходимость для организма человека наличия именно переходных металлов. Рассмотрели некоторые примеры сплавов переходных металлов, исследовали амфотерные свойства железа и его соединений с различными степенями окисления. Немного узнали о железной кислоте и ее солях – ферратах.
Список литературы
1. Рудзитис Г.Е. Химия. Основы общей химии. 11 класс: учебник для общеобразовательных учреждений: базовый уровень / Г.Е. Рудзитис, Ф.Г. Фельдман. – 14-е изд. – М.: Просвещение, 2012.
2. Попель П.П. Химия: 8 кл.: учебник для общеобразовательных учебных заведений / П.П. Попель, Л.С.Кривля. – К.: ИЦ «Академия», 2008. – 240 с.: ил.
3. Габриелян О.С. Химия. 11 класс. Базовый уровень. 2-е изд., стер. – М.: Дрофа, 2007. – 220 с.
11 класс. Базовый уровень. 2-е изд., стер. – М.: Дрофа, 2007. – 220 с.
Домашнее задание
1. №№1, 5-б, в (с. 173) Габриелян О.С. Химия. 11 класс. Базовый уровень. 2-е изд., стер. – М.: Дрофа, 2007. – 220 с.
2. Что такое металлотермия? Приведите примеры.
3. Какие свойства характерны для соединений железа (III)?
переходные элементы
- переходные элементы
- pereinamieji elementai statusas T sritis chemija apibrėžtis d ir f elementai. atitikmenys: angl. transition elements rus. переходные элементы
Chemijos terminų aiškinamasis žodynas – 2-asis patais. ir papild. leid. – Vilnius: Mokslo ir enciklopedijų leidybos institutas.
Kazys Daukšas, Jurgis Barkauskas, Vitas Daukšas.
2003.
– Vilnius: Mokslo ir enciklopedijų leidybos institutas.
Kazys Daukšas, Jurgis Barkauskas, Vitas Daukšas.
2003.
- transition elements
- pereinamoji būsena
Look at other dictionaries:
ПЕРЕХОДНЫЕ ЭЛЕМЕНТЫ — (переходные металлы) химические элементы подгрупп б периодической системы Менделеева. Атомы переходных элементов имеют незавершенные внутренние электронные оболочки. Различают d элементы, у которых происходит заполнение внутренних 3d , 4d , 5d и… … Большой Энциклопедический словарь
Переходные элементы — Переходные металлы (переходные элементы) химические элементы побочных подгрупп I VIII групп Периодической системы элементов Д.И. Менделеева (3 12 групп в длиннопериодном варианте таблицы). Переходные металлы выделяют на основании незавершённости… … Википедия
ПЕРЕХОДНЫЕ ЭЛЕМЕНТЫ — ПЕРЕХОДНЫЕ ЭЛЕМЕНТЫ, химические элементы, расположенные в побочных подгруппах больших периодов периодической системы; металлы.
 Из 109 элементов 65 переходные. Переходные элементы, кроме железа, мало распространены в природе … Современная энциклопедия
Из 109 элементов 65 переходные. Переходные элементы, кроме железа, мало распространены в природе … Современная энциклопедияПереходные элементы — ПЕРЕХОДНЫЕ ЭЛЕМЕНТЫ, химические элементы, расположенные в побочных подгруппах больших периодов периодической системы; металлы. Из 109 элементов 65 переходные. Переходные элементы, кроме железа, мало распространены в природе. … Иллюстрированный энциклопедический словарь
ПЕРЕХОДНЫЕ ЭЛЕМЕНТЫ — ПЕРЕХОДНЫЕ ЭЛЕМЕНТЫ, металлические элементы, имеющие незаполненные внутренние электронные оболочки. Переходные элементы характеризуются переменной ВАЛЕНТНОСТЬЮ и образованием окрашенных ионов. Сюда входят элементы с атомным номером от 21 до 112.… … Научно-технический энциклопедический словарь
ПЕРЕХОДНЫЕ ЭЛЕМЕНТЫ — хим. элементыпобочных подгрупп (b подгрупп) периодической системы элементов. К ним относятся d и f элементы, т. е. элементы, у к рыхпроисходит заполнение 3d ,4d , 5d оболочки (переходныеметаллы) или 4f и 5f оболочки (лантаноиды и актиноиды… … Физическая энциклопедия
переходные элементы — (переходные металлы), химические элементы подгрупп «б» периодической системы.
 Атомы переходных элементов имеют незавершённые внутренние электронные оболочки. Различают d элементы, у которых происходит заполнение внутренних 3d , 4d , 5d и 6d… … Энциклопедический словарь
Атомы переходных элементов имеют незавершённые внутренние электронные оболочки. Различают d элементы, у которых происходит заполнение внутренних 3d , 4d , 5d и 6d… … Энциклопедический словарьПЕРЕХОДНЫЕ ЭЛЕМЕНТЫ — В соответствии с периодической классификацией элементов существует 44 элемента, образующих подгруппы А. В каждой из этих подгрупп (или семейств) на внешней (валентной) электронной оболочке число электронов равно номеру группы. При переходе от… … Энциклопедия Кольера
ПЕРЕХОДНЫЕ ЭЛЕМЕНТЫ — (переходные металлы; хим. элементы, расположенные в побочных подгруппах больших периодов периодической системы; являются d и f элементами. Назв. переходные связано с тем, что в периодах П. э. вклиниваются между s и р элементами. Всего известно 65 … Химическая энциклопедия
ПЕРЕХОДНЫЕ ЭЛЕМЕНТЫ — (переходные металлы), хим. элементы подгрупп б периодич. системы. Атомы П. э. имеют незавершённые внутр.
 электронные оболочки. Различают rf элементы, у к рых происходит заполнение внутр. 3d , 4d , 5d и 6d подоболочек, и f элементы, у к рых… … Естествознание. Энциклопедический словарь
электронные оболочки. Различают rf элементы, у к рых происходит заполнение внутр. 3d , 4d , 5d и 6d подоболочек, и f элементы, у к рых… … Естествознание. Энциклопедический словарь
РАЗНИЦА МЕЖДУ ПЕРЕХОДНЫМИ МЕТАЛЛАМИ И ВНУТРЕННИМИ ПЕРЕХОДНЫМИ МЕТАЛЛАМИ | СРАВНИТЕ РАЗНИЦУ МЕЖДУ ПОХОЖИМИ ТЕРМИНАМИ – НАУКА
Переходные металлы против внутренних переходных металлов В элементы таблицы Менделеева расположены по возрастанию в зависимости от того, как электроны заполнены атомными энергетическими уровнями и их
Переходные металлы против внутренних переходных металлов
В элементы таблицы Менделеева расположены по возрастанию в зависимости от того, как электроны заполнены атомными энергетическими уровнями и их подоболочками. Характеристики этих элементов прямо коррелируют с электронной конфигурацией. Следовательно, для удобства можно идентифицировать и блокировать области элементов с похожими свойствами. Первые два столбца в периодической таблице содержат элементы, в которых последний электрон заполняется в подоболочку «s», поэтому называется «s-блоком». Последние шесть столбцов расширенной периодической таблицы содержат элементы, в которых последний электрон заполняется в подоболочку «p», поэтому называется «p-блоком». Точно так же столбцы с 3 по 12 содержат элементы, в которых последний электрон заполняется в подоболочку «d», таким образом называемую «d-блоком». Наконец, дополнительный набор элементов, который часто записывается в виде двух отдельных строк в нижней части периодической таблицы или иногда записывается между столбцами 2 и 3 в качестве расширения, называется “ f-блоком ”, поскольку их последний электрон заполняется в подоболочка ‘f’. Элементы «d-блока» также называются «переходными металлами», а элементы «f-блок» также называются «внутренними переходными металлами».
Первые два столбца в периодической таблице содержат элементы, в которых последний электрон заполняется в подоболочку «s», поэтому называется «s-блоком». Последние шесть столбцов расширенной периодической таблицы содержат элементы, в которых последний электрон заполняется в подоболочку «p», поэтому называется «p-блоком». Точно так же столбцы с 3 по 12 содержат элементы, в которых последний электрон заполняется в подоболочку «d», таким образом называемую «d-блоком». Наконец, дополнительный набор элементов, который часто записывается в виде двух отдельных строк в нижней части периодической таблицы или иногда записывается между столбцами 2 и 3 в качестве расширения, называется “ f-блоком ”, поскольку их последний электрон заполняется в подоболочка ‘f’. Элементы «d-блока» также называются «переходными металлами», а элементы «f-блок» также называются «внутренними переходными металлами».
Переходные металлы
Эти элементы появляются на картинке, начиная с 4-го ряда, и термин «переход» был использован потому, что он расширил внутренние электронные оболочки, создав стабильную конфигурацию «8 электронов» до конфигурации «18 электронов». Как упоминалось выше, элементы в d-блоке относятся к этой категории, которая охватывает группы 3-12 периодической таблицы, и все элементы являются металлами, отсюда и название ‘переходные металлы’. Элементы в 4th строки, группы 3-12, вместе называются первой серией переходов, 5th ряд как второй ряд переходов и так далее. Элементы в первой переходной серии включают; Sc, Ti, V, Cr, Mn, Fe, Co, Ni, Cu, Zn. Обычно считается, что переходные металлы имеют незаполненные d-подоболочки, следовательно, такие элементы, как Zn, Cd и Hg, которые находятся в 12th столбец, как правило, исключаются из переходного ряда.
Как упоминалось выше, элементы в d-блоке относятся к этой категории, которая охватывает группы 3-12 периодической таблицы, и все элементы являются металлами, отсюда и название ‘переходные металлы’. Элементы в 4th строки, группы 3-12, вместе называются первой серией переходов, 5th ряд как второй ряд переходов и так далее. Элементы в первой переходной серии включают; Sc, Ti, V, Cr, Mn, Fe, Co, Ni, Cu, Zn. Обычно считается, что переходные металлы имеют незаполненные d-подоболочки, следовательно, такие элементы, как Zn, Cd и Hg, которые находятся в 12th столбец, как правило, исключаются из переходного ряда.
Помимо того, что элементы d-блока состоят из всех металлов, они обладают рядом других характерных свойств, которые определяют их идентичность. Большинство соединений металлов переходного ряда окрашены. Это связано с электронными d-d переходами; то есть KMnO4 (фиолетовый), [Fe (CN)6]4- (кроваво красный), CuSO4 (синий), K2CrO4 (желтый) и т. д. Еще одно свойство – выставка многих степени окисления. В отличие от элементов s-блока и p-блока, большинство элементов d-блока имеют различные степени окисления; то есть Mn (от 0 до +7). Благодаря этому качеству переходные металлы работают хорошо. катализаторы в реакциях. Кроме того, они проявляют магнитные свойства и, по сути, действуют как парамагнетики при наличии неспаренных электронов.
д. Еще одно свойство – выставка многих степени окисления. В отличие от элементов s-блока и p-блока, большинство элементов d-блока имеют различные степени окисления; то есть Mn (от 0 до +7). Благодаря этому качеству переходные металлы работают хорошо. катализаторы в реакциях. Кроме того, они проявляют магнитные свойства и, по сути, действуют как парамагнетики при наличии неспаренных электронов.
Внутренние переходные металлы
Как сказано во введении, элементы f-блока подпадают под эту категорию. Эти элементы еще называют ‘редкоземельные металлы. Эта серия включена после 2nd столбец как две нижние строки, соединяющиеся с d-блоком в расширенной периодической таблице или как две отдельные строки в нижней части периодической таблицы. 1ул строка называется “Лантаноиды’, А 2nd строка называется “Актинидов. И лантаноиды, и актиниды имеют схожий химический состав, и их свойства отличаются от всех других элементов из-за природы f-орбиталей. (Прочтите Разница между актинидами и лантаноидами.) Электроны на этих орбиталях погребены внутри атома и защищены внешними электронами, и, в результате, химический состав этих соединений в значительной степени зависит от размера. Пример: La / Ce / Tb (лантаноиды), Ac / U / Am (актиниды).
В чем разница между переходными металлами и внутренними переходными металлами?
• Переходные металлы состоят из элементов d-блока, тогда как внутренние переходные металлы состоят из элементов f-блока.
• Внутренние переходные металлы менее доступны, чем переходные металлы, и поэтому называются «редкоземельными металлами».
• Химический состав переходных металлов в основном обусловлен различными числа окисления, в то время как химия внутренних переходных металлов в основном зависит от размера атомов.
• Переходные металлы обычно используются в окислительно-восстановительные реакции, но использование внутренних переходных металлов для этой цели редко.
Также прочтитеРазница между переходными металлами и металлами
Переходный металл — Энциклопедия Нового Света
В общепринятой терминологии переходных металла (или переходных элемента ) — это химические элементы, которые лежат в группах с 3 по 12 периодической таблицы в стандартном представлении таблицы. Название перехода происходит от их положения в таблице — они образуют переход между элементами основной группы, которые встречаются в группах 1 и 2 слева, и в группах 13–18 справа.
Некоторые переходные элементы встречаются в природе в металлическом состоянии и известны с древних времен.Три из них — золото, серебро и медь — широко использовались в чеканке монет и ювелирных изделий. Использование меди в инструментах было одним из первых исторических технологических достижений.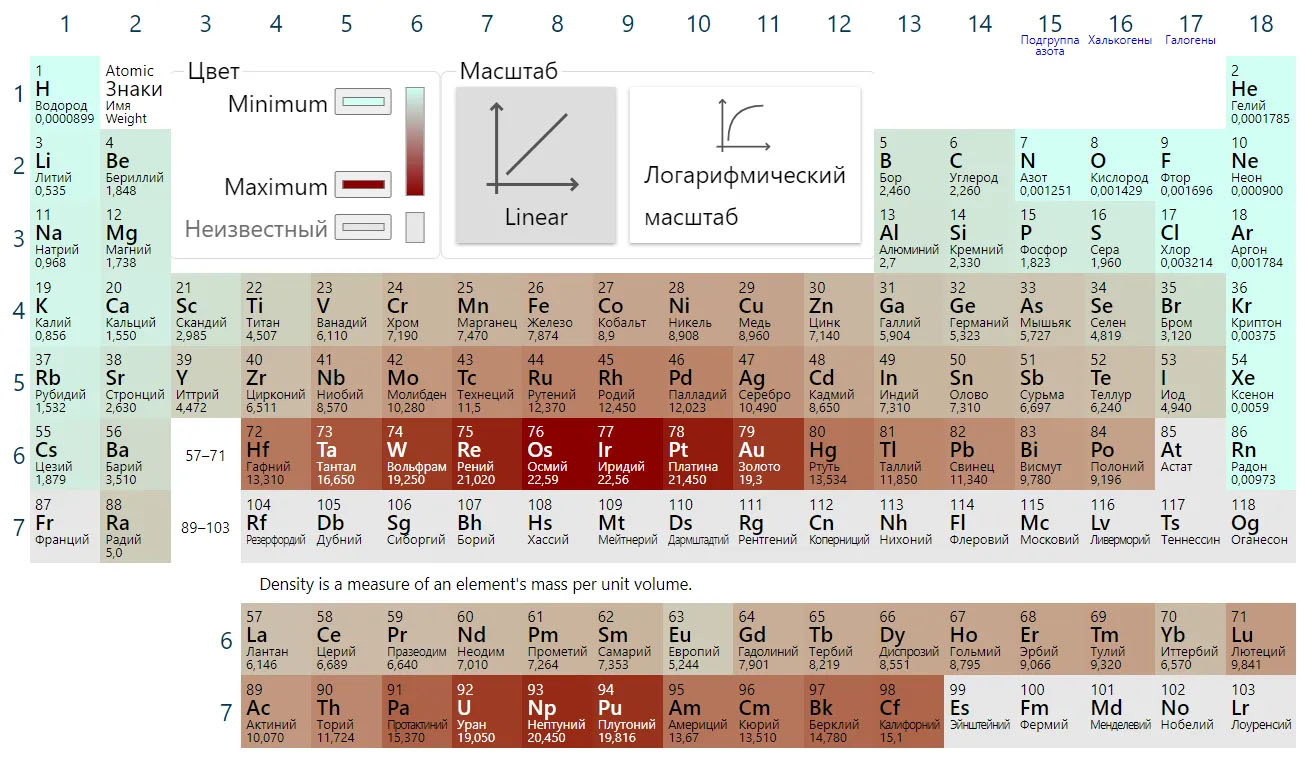 Кроме того, железо в виде стали используется во многих конструкциях, от автомобилей до мостов. Многие переходные металлы используются в качестве катализаторов в промышленных и лабораторных условиях, и многие из этих элементов образуют ярко окрашенные соединения.
Кроме того, железо в виде стали используется во многих конструкциях, от автомобилей до мостов. Многие переходные металлы используются в качестве катализаторов в промышленных и лабораторных условиях, и многие из этих элементов образуют ярко окрашенные соединения.
Периодическая таблица
Расположение группы переходных элементов в периодической таблице можно проследить, изучив приведенную ниже таблицу с цветовой кодировкой.
Состояние при стандартной температуре и давлении
- Элементы, пронумерованные красным цветом, являются газами.
- Элементы, пронумерованные зеленым цветом, являются жидкостями.
- Элементы, пронумерованные черным цветом, являются твердыми телами.
Естественное явление
Элементы без границ еще не открыты/не синтезированы.
Элементы с пунктирными границами не встречаются в природе (синтетические элементы).
Элементы с пунктирными границами естественным образом возникают в результате распада других химических элементов.

- Элементы со сплошными границами старше Земли (изначальные элементы).
- Примечание: Хотя калифорний (Cf, 98) не является первичным для Земли, он (и продукты его распада) встречается в природе: его электромагнитное излучение регулярно наблюдается в спектрах сверхновых.
Определения
Общее определение переходных металлов как тех, которые находятся в группах с 3 по 12 периодической таблицы, упомянутое выше, является простым и традиционно используется.Хотя это определение до сих пор широко используется, характерные свойства переходных металлов возникают из-за электронной конфигурации их атомов, которые частично заполнили « d орбиталей». Исходя из этой точки зрения, термин переходный элемент определен более строго. Международный союз теоретической и прикладной химии (IUPAC) определяет переходный элемент как «элемент, атом которого имеет неполную d-подоболочку или который может давать катионы с неполной d-подоболочкой. [1]
[1]
По этому определению цинк, кадмий и ртуть (элементы 12 группы) не считаются переходными металлами. Это связано с тем, что атомы этих элементов и их стабильные ионы содержат электроны, полностью заполняющие d Когда эти элементы образуют ионы, они обычно теряют электроны только из самой внешней подоболочки s , оставляя нетронутой подоболочку d . Всего в нескольких исключительных случаях они образовали нестабильные ионы, в которых подоболочка d частично заполнены. [2] Элемент 112 (в группе 12) также может быть исключен, поскольку его электронная конфигурация, вероятно, аналогична электронной конфигурации других членов группы 12, а его окислительные свойства вряд ли будут наблюдаться из-за его радиоактивной природы. Таким образом, это более строгое определение переходных металлов ограничивает термин элементами в группах с 3 по 11.
Свойства
Существует несколько общих характерных свойств переходных элементов:
- Почти все они представляют собой твердые вещества при комнатной температуре, с высокой прочностью на растяжение (способностью выдерживать нагрузки), плотностью, температурами плавления и кипения.
Единственным исключением является ртуть, которая представляет собой жидкость.
- Большинство из них серебристо-голубые при комнатной температуре. Исключение составляют медь и золото.
- Они образуют одноатомные ионы с зарядом 2+, но могут образовывать другие ионы с другим зарядом. Например, железо может образовывать ионы Fe 2+ и Fe 3+ . Кроме того, они часто имеют более высокие степени окисления в соединениях.
- Они образуют комплексы, известные как «координационные соединения», многие из которых ярко окрашены.
- Они часто являются хорошими катализаторами. Например, железо является катализатором процесса Габера, включающего реакцию азота и водорода с образованием аммиака. Никель, палладий или платину можно использовать при гидрировании (присоединении атомов водорода к) алкенов и алкинов. Платина является катализатором в каталитических нейтрализаторах автомобильных выхлопных систем.
В дополнение к этим общим характеристикам существуют некоторые тенденции в свойствах по мере того, как мы проходим через определенный период, очень похожие на тенденции в элементах основной группы, но с менее резкими изменениями. При переходе через переходные металлы периода атомный радиус обычно имеет тенденцию к уменьшению, а первая энергия ионизации (энергия, необходимая для отрыва электрона от нейтрального атома) увеличивается. Кроме того, по мере прохождения периода металлы становятся мягче, а ртуть при комнатной температуре представляет собой жидкость. Элементы группы 11 (медь, серебро и золото) особенно неактивны. Эти «благородные» металлы могут встречаться в природе в их элементарном металлическом состоянии, и их иногда называют металлами для чеканки монет, поскольку они использовались для чеканки монет.
При переходе через переходные металлы периода атомный радиус обычно имеет тенденцию к уменьшению, а первая энергия ионизации (энергия, необходимая для отрыва электрона от нейтрального атома) увеличивается. Кроме того, по мере прохождения периода металлы становятся мягче, а ртуть при комнатной температуре представляет собой жидкость. Элементы группы 11 (медь, серебро и золото) особенно неактивны. Эти «благородные» металлы могут встречаться в природе в их элементарном металлическом состоянии, и их иногда называют металлами для чеканки монет, поскольку они использовались для чеканки монет.
Электронная конфигурация
- Основная статья: электронная конфигурация
Свойства переходных металлов возникают из-за их определяющей характеристики частично заполненных d орбиталей. Они являются металлами, потому что d орбитальных электронов делокализованы внутри металлической решетки, образуя металлические связи.
Большинство переходных металлов имеют два электрона в самой внешней, s подоболочке.Когда мы рассматриваем эти элементы в течение периода, число d электронов увеличивается на один. Так, в четвертом периоде скандий (Sc, группа 3) имеет конфигурацию [Ar]4 s 2 3 d 1 , а следующий за ним элемент титан (Ti, группа 4) имеет конфигурацию Ar]4 s 2 3 d 2 и так далее. Однако есть некоторые исключения из этой прогрессии. Например, в четвертом периоде медь имеет конфигурацию ([Ar]4 s 1 3 d 10 ), а хром – ([Ar]4 s 1 3
9d 5
).Эти исключения возникают из-за того, что атомы приобретают дополнительную устойчивость, когда их подоболочки заполнены наполовину или полностью. Медь имеет полностью заполненную подоболочку d , а хром имеет наполовину заполненную подоболочку d . Подобные исключения более распространены в пятом, шестом и седьмом периодах.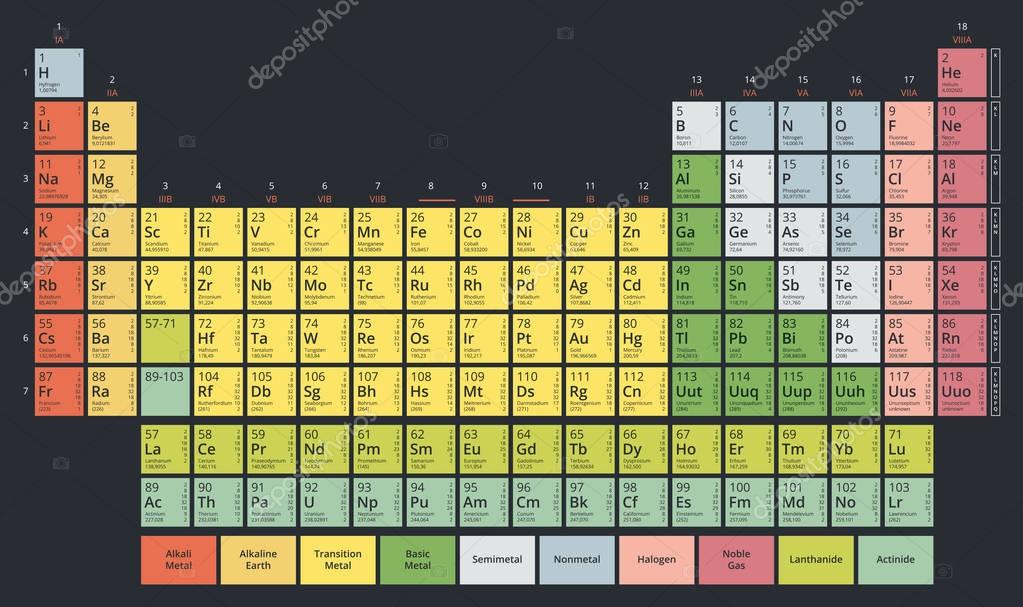
Когда эти металлы теряют электроны с образованием одноатомных ионов, они обычно первыми теряют свои s электронов. Таким образом, большинство переходных металлов образуют ионы с зарядом 2+.Более высокие степени окисления также включают d электронов. Одноатомные ионы с зарядом более 3+ встречаются редко, а более высокие степени окисления переходных металлов встречаются в соединениях с сильно электроотрицательными элементами, такими как кислород.
Различные степени окисления
В отличие от ионов большинства металлов основной группы одноатомные ионы переходных металлов могут иметь более одного стабильного заряда, а в соединениях могут иметь несколько высших степеней окисления. (Степень окисления — это мера степени окисления атома в соединении; это электрический заряд, который атом имел бы, по крайней мере гипотетически, если бы его связи со всеми другими атомами в соединении были полностью ионными.)
Эта изменчивость степени окисления связана с тем, что атомы переходных элементов могут потерять или разделить d электронов без больших энергетических потерь. Атом марганца, например, имеет два 4 s электронов и пять 3 d электронов, которые могут быть удалены или разделены с другими атомами. Потеря или совместное использование всех этих электронов приводит к степени окисления 7+. Соединения осмия и рутения обычно выделяют в стабильных степенях окисления 8+, что является одним из самых высоких для выделяемых соединений.
Атом марганца, например, имеет два 4 s электронов и пять 3 d электронов, которые могут быть удалены или разделены с другими атомами. Потеря или совместное использование всех этих электронов приводит к степени окисления 7+. Соединения осмия и рутения обычно выделяют в стабильных степенях окисления 8+, что является одним из самых высоких для выделяемых соединений.
В этой таблице показаны некоторые степени окисления соединений переходных металлов.
Сплошной кружок представляет распространенную степень окисления, а кольцо представляет менее распространенную (энергетически менее благоприятную) степень окисления.
Перемещаясь по периоду переходных элементов, появляются определенные закономерности в их состояниях окисления:
- Число степеней окисления каждого элемента увеличивается до марганца (группа 7), после чего уменьшается. Более поздние переходные металлы имеют более сильное притяжение между протонами и электронами (поскольку их больше), и для удаления электронов требуется больше энергии.
- Когда эти элементы находятся в более низких степенях окисления, их можно найти в виде простых ионов. В своих более высоких степенях окисления эти элементы обычно ковалентно связаны с электроотрицательными элементами, такими как кислород или фтор, образуя многоатомные ионы, такие как хромат, ванадат или перманганат.
Другими свойствами, связанными со стабильностью степеней окисления, являются следующие:
- Ионы в более высоких степенях окисления, как правило, являются хорошими окислителями, тогда как элементы в низких степенях окисления становятся восстановителями.
- Проходя период, ионы 2+ становятся сильными восстановителями и становятся более стабильными.
- И наоборот, ионы 3+ начинают с более высокой стабильности и со временем становятся более окисляющими.
Цветные составы
Как отмечалось выше, химия переходных металлов характеризуется частично заполненными орбиталями d , допускающими несколько степеней окисления.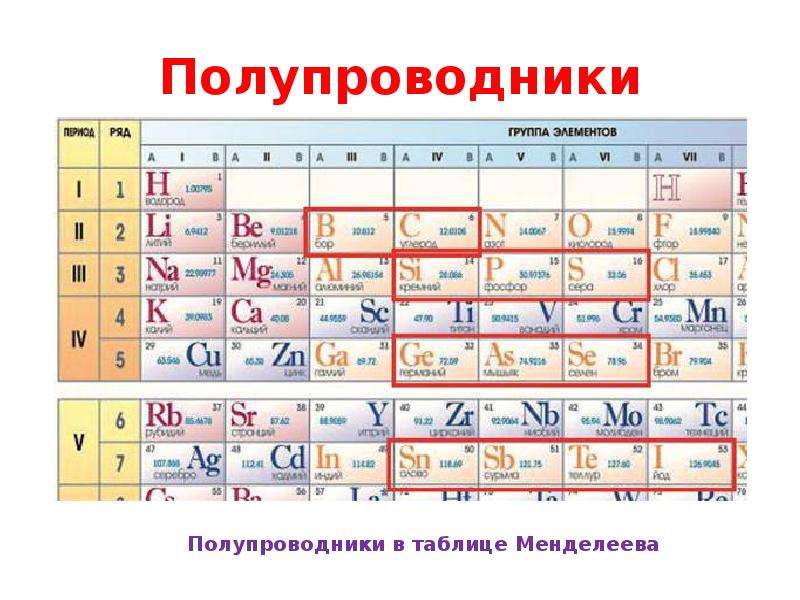 Еще одним следствием их электронной конфигурации является то, что эти элементы могут образовывать устойчивые комплексы или координационные соединения.В таком комплексе атом или ион переходного металла образует слабые ковалентные связи с другими небольшими молекулами или ионами, известными как «лиганды». В некоторых случаях степень окисления переходного металла может быть нулевой или отрицательной.
Еще одним следствием их электронной конфигурации является то, что эти элементы могут образовывать устойчивые комплексы или координационные соединения.В таком комплексе атом или ион переходного металла образует слабые ковалентные связи с другими небольшими молекулами или ионами, известными как «лиганды». В некоторых случаях степень окисления переходного металла может быть нулевой или отрицательной.
Соединения переходных металлов часто сильно окрашены, и координация лигандами играет большую роль в определении цвета соединения. В отсутствие лигандов все d орбиталей атома имеют одинаковую энергию, но в окружении лигандов энергии d орбиталей изменяются и уже не равны.Это явление описывается теорией цистального поля. Для многих соединений этого типа результирующая разница в энергии орбиталей d находится в диапазоне энергий видимого света. В результате они сильно поглощают определенные длины волн видимого света и выглядят ярко окрашенными. Можно наблюдать много разных цветов, и цвет может различаться даже между разными ионами одного и того же элемента. Ярким примером могут служить различные ионы ванадия (V): VO 2 + – в растворе желтый цвет, VO 2+ – синий, V 3+ (водн.) – зеленый и V 2+ ( aq) фиолетовый.
Цвет комплекса зависит от:
- природа иона металла, особенно количество электронов на d орбиталях;
- расположение лигандов вокруг иона металла; и
- природа лигандов, окружающих ион металла. (Чем сильнее лиганд, тем больше разница в энергии между различными d орбиталями.)
Интересно, что хотя цинк может образовывать комплексы, они бесцветны, потому что 3d-орбитали цинка полностью заполнены.Полные орбитали d предотвращают поглощение комплексом видимого света, когда энергии орбиталей d изменяются лигандами. Поскольку цинк находится в группе 12, он не считается переходным металлом по новому определению ИЮПАК.
См. также
Примечания
- ↑ переходной элемент.
 Золотая книга ИЮПАК. Проверено 9 января 2009 г.
Золотая книга ИЮПАК. Проверено 9 января 2009 г. - ↑ Коттон, Ф. Альберт, Г. Уилкинсон, К.А. Мурильо и М. Бохманн. 1999. Передовая неорганическая химия , 6-е изд.Нью-Йорк: Уайли. ISBN 0471199575.
Ссылки
Ссылки ISBN поддерживают NWE за счет реферальных сборов
- Коттон, Ф. Альберт, Г. Уилкинсон, К.А. Мурильо и М. Бохманн. 1999. Передовая неорганическая химия , 6-е изд. Нью-Йорк: Уайли. ISBN 0471199575
- Крэбтри, Роберт Х. 2005. Металлоорганическая химия переходных металлов. Хобокен, Нью-Джерси: Wiley. ISBN 978-0471662563
- Гринвуд, Н.Н. и А. Эрншоу. 1997. Химия элементов , 2-е изд. Оксфорд: Баттерворт-Хайнеманн. ISBN 0750633654
Кредиты
Энциклопедия Нового Света писатели и редакторы переписали и дополнили статью Википедии в соответствии со стандартами New World Encyclopedia . Эта статья соответствует условиям лицензии Creative Commons CC-by-sa 3. 0 (CC-by-sa), которая может использоваться и распространяться с надлежащим указанием авторства.Упоминание должно быть выполнено в соответствии с условиями этой лицензии, которая может ссылаться как на авторов New World Encyclopedia , так и на самоотверженных добровольных участников Фонда Викимедиа. Чтобы процитировать эту статью, щелкните здесь, чтобы просмотреть список допустимых форматов цитирования. История более ранних вкладов википедистов доступна исследователям здесь:
0 (CC-by-sa), которая может использоваться и распространяться с надлежащим указанием авторства.Упоминание должно быть выполнено в соответствии с условиями этой лицензии, которая может ссылаться как на авторов New World Encyclopedia , так и на самоотверженных добровольных участников Фонда Викимедиа. Чтобы процитировать эту статью, щелкните здесь, чтобы просмотреть список допустимых форматов цитирования. История более ранних вкладов википедистов доступна исследователям здесь:
История этой статьи с момента ее импорта в New World Encyclopedia :
Примечание. На использование отдельных изображений, лицензированных отдельно, могут распространяться некоторые ограничения.
Переходной элемент – Oxford Reference
Набор элементов периодической таблицы, в котором происходит заполнение электронами внутреннего уровня d или f . С увеличением номера протона, электроны наполнить атомные уровни до аргона, который имеет электронную конфигурацию 1 S 2 2 S 2 2 P 6 3 S 2 3 P 6 .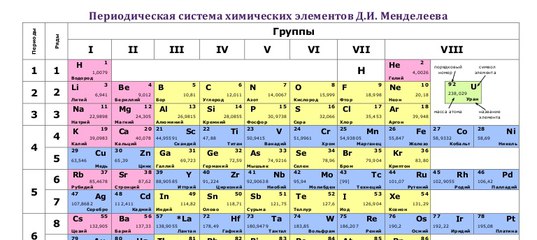 В этой оболочке 5 d -орбиталей, каждая из которых может содержать по 2 электрона.Однако в этой точке подоболочка с наименьшей энергией — это не 3 d , а 4 s . Следующие два элемента, калий и кальций, имеют конфигурации [Ar]4 s 1 и [Ar]4 s 2 соответственно. Для следующего элемента, скандия, уровень 3 d имеет более низкую энергию, чем уровень 4 p , и скандий имеет конфигурацию [Ar]3 d 1 4 s 2 . Это заполнение внутреннего d -уровня продолжается до цинка [Ar]3 d 10 4 s 2 , давая первый переходный ряд.В следующем периоде таблицы имеется еще ряд такого типа: между иттрием ([Kr]4 d 5 s 2 ) и кадмием ([Kr]4 d 10 5 s 2 ). Это вторая переходная серия. В следующем периоде таблицы ситуация несколько сложнее. Лантан имеет конфигурацию [Xe]5 d 1 6 s 2 .
В этой оболочке 5 d -орбиталей, каждая из которых может содержать по 2 электрона.Однако в этой точке подоболочка с наименьшей энергией — это не 3 d , а 4 s . Следующие два элемента, калий и кальций, имеют конфигурации [Ar]4 s 1 и [Ar]4 s 2 соответственно. Для следующего элемента, скандия, уровень 3 d имеет более низкую энергию, чем уровень 4 p , и скандий имеет конфигурацию [Ar]3 d 1 4 s 2 . Это заполнение внутреннего d -уровня продолжается до цинка [Ar]3 d 10 4 s 2 , давая первый переходный ряд.В следующем периоде таблицы имеется еще ряд такого типа: между иттрием ([Kr]4 d 5 s 2 ) и кадмием ([Kr]4 d 10 5 s 2 ). Это вторая переходная серия. В следующем периоде таблицы ситуация несколько сложнее. Лантан имеет конфигурацию [Xe]5 d 1 6 s 2 . Тогда уровень наименьшей энергии становится уровнем 4 f , а следующий элемент, церий, имеет конфигурацию [Xe]4 f 1 5 d 1 6 s 4 3.Таких f -орбиталей 7, каждая из которых может содержать 2 электрона, и заполнение f -уровней продолжается до лютеция ([Xe]4 f 14 5 d 1 6 с 2 ). Затем продолжается заполнение уровней 5 d от гафния к ртути. Ряд из 14 элементов от церия до лютеция представляет собой «ряд внутри ряда», называемый внутренним переходным рядом. Это серия лантаноидов. В следующем периоде имеется аналогичная внутренняя переходная серия, актиноидная серия, от тория к лоуренсию.Затем заполнение уровня d продолжается с элемента 104 и далее.
На самом деле классификация химических элементов ценна только в той мере, в какой она иллюстрирует химическое поведение, и принято использовать термин «переходные элементы» в более узком смысле. Элементы внутреннего переходного ряда от церия (58) к лютецию (71) называются лантаноидами; в ряду от тория (90) до лоуренсия (103) — актиноиды. Эти две серии вместе составляют блок f в периодической таблице.Также обычно к лантаноидам относят скандий, иттрий и лантан (из-за химического сходства), а актиний к актиноидам. Из остальных переходных элементов принято говорить о трех основных переходных рядах: от титана к меди; от циркония до серебра; и от гафния к золоту. Все эти элементы имеют сходные химические свойства, обусловленные наличием незаполненных d -орбиталей в элементе или (в случае меди, серебра и золота) в ионах.Элементы со 104 по 109 и неоткрытые элементы 110 и 111 составляют четвертую серию переходов. Элементы цинк, кадмий и ртуть заполнили d -орбиталей как в элементах, так и в соединениях и обычно рассматриваются как непереходные элементы, образующие 12-ю группу периодической таблицы.
Элементы внутреннего переходного ряда от церия (58) к лютецию (71) называются лантаноидами; в ряду от тория (90) до лоуренсия (103) — актиноиды. Эти две серии вместе составляют блок f в периодической таблице.Также обычно к лантаноидам относят скандий, иттрий и лантан (из-за химического сходства), а актиний к актиноидам. Из остальных переходных элементов принято говорить о трех основных переходных рядах: от титана к меди; от циркония до серебра; и от гафния к золоту. Все эти элементы имеют сходные химические свойства, обусловленные наличием незаполненных d -орбиталей в элементе или (в случае меди, серебра и золота) в ионах.Элементы со 104 по 109 и неоткрытые элементы 110 и 111 составляют четвертую серию переходов. Элементы цинк, кадмий и ртуть заполнили d -орбиталей как в элементах, так и в соединениях и обычно рассматриваются как непереходные элементы, образующие 12-ю группу периодической таблицы.
Все элементы трех основных переходных рядов являются типичными металлами (в нехимическом смысле), т. е. большинство из них представляют собой прочные твердые материалы, которые являются хорошими проводниками тепла и электричества и имеют высокие температуры плавления и кипения.Химически их поведение зависит от наличия незаполненных d -орбиталей. Они обладают переменной валентностью, имеют окрашенные соединения и образуют координационные соединения. Многие из их соединений являются парамагнитными из-за наличия неспаренных электронов. Многие из них являются хорошими катализаторами. Они менее реакционноспособны, чем s – и p -блочные металлы.
[…]
Переходные металлы – Периодическая таблица элементов –
Периодическая таблица элементов Группы. [ Щелочные металлы ] [ Щелочноземельные металлы ] [ Блоки ] [ Газы ] [ Галогены ] [ Лантаниды/Актиниды ] [ Жидкости (станц.) ] [ Основная группа ] [ Металлоиды ] [ Металлы ] [ Благородные газы ] [Неметаллы] [ Твердые вещества (станц.) ] [ Переходные металлы ] [ Периодические ]Переходные металлы
Внутренние переходные металлы Переходные металлы или переходные элементы традиционно занимают весь блок d периодической таблицы.
 Название переходного металла относится к положению в периодической таблице элементов.Переходные элементы представляют собой последовательное добавление электронов к d-атомным орбиталям атомов. Таким образом, переходные металлы представляют собой переход между элементами группы 2 (2А) и элементами группы 13 (3А).
Название переходного металла относится к положению в периодической таблице элементов.Переходные элементы представляют собой последовательное добавление электронов к d-атомным орбиталям атомов. Таким образом, переходные металлы представляют собой переход между элементами группы 2 (2А) и элементами группы 13 (3А).Переходные металлы можно более строго определить как элемент, атом или катион которого имеет неполную d-подоболочку. Это определение исключает цинк (Zn), кадмий (Cd), ртуть (Hg) и, вероятно, Uub из переходных элементов, поскольку они имеют полные конфигурации d 10 .
Внутренние переходные металлы занимают f-блок периодической таблицы и снова действуют как переход между элементами группы 2 и переходными металлами.
Наведите указатель мыши на элемент или щелкните его, чтобы получить дополнительную информацию:
| Группа *** Период | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 | 2 IIA | 3 IIIB 3B | 4 IVB 4B | 5 В.  Б. Б. 5B | 6 VIB 6B | 7 VIIB 7В | 8 VIII, 8 | 9 VIII 8 | 10 VIII 8 | 11 И.Б. 1B | 12 МИБ 2B | 13 IIIA 3A | 14 IVA 4A | 15 9045 8 ВА 5A | 16 VIA 6A | 17 VIIA 7A | 18 VIIIA 8A | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 | 1 Н 1.  008 008 | 2 Он 4,003 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2 | 3 Li 6,941 | 4 Be 9,012 | 5 B 10.  81 81 | 6 С 12,01 | 7 Н 14,01 | 8 О 16,00 | 9 F 19,00 | 10 Н 20,18 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3 | 11 Na 22.99 | 12 Мг 24,31 | 13 Аль 26,98 | 14 SI 28. | 15 P P 30.97 | 16 S 32.07 | 17 Cl 35,45 | 18 Ар 39,95 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4 | 19 К 39.10 | 20 Ca CA 40.  08 08 | 21 SC 44.96 | 22 Ti 47,88 | 23 V 50,94 | 24 | 25 | 26 Fe 55,85 | 27 Co 58.47 | 28 Ni 58,69 | 29 | + 30 Zn 65,39 | 31 GA 69. 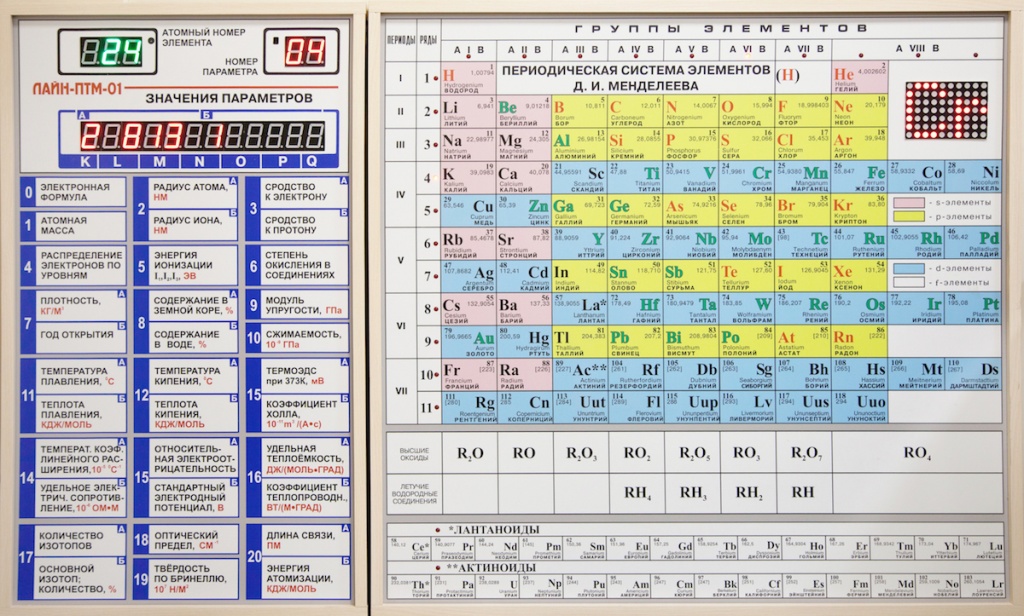 72 72 | 39 GE Ge 72.59 7259 | 33 Ar 9000 74.92 | 34 Se 78,96 | 35 Br 79,90 | 36 Кр 83,80 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 5 | 39 RB RB 85.47 | 38 SR SR 87.  62 62 | 39 Y 88.91 | 40 Zr 91.22 | 41 Nb 92.91 | 42 Mo 95.94 | 43 Tc (98) | 44 Ru 101.1 | 45 резус 102,9 | 46 Pd 106,4 | 47 Ag 107,9 | 48 CD 112.  0457 0457 | 49 в в 114.8 | 50 Sn 118.7 | 51 Sb 121,8 | 52 Те 127,6 | 53 Я 126,9 | 54 XE 131.3 131.3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 6 | 55 55 CS 132.  9 9 | 56 Ба 137,3 | * | 72 гафний 178,5 | 73 TA 180458 180457 | 74 74 W W 183.9 | 75 Re 186.2 | 76 Ос 190,2 | 77 Ir 190,2 | 78 Pt 195,1 | 79 AU 1970 | HG HG 200,5 | 81 TL 204.  4 4 | 82 Pb 207,2 | 83 Би 209,0 | 84 По (209) | 85 В (210) | 86 Rn (222) | 90 460|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 7 | 87 ПТ (223) | 88 Ра (226) | ** | 104 Rf ( 261) | 105 Дб (262) | 106 Sg (266) | 107 Bh (264) | 108 Hs (269) | 109 Мт (268) | 110 Ds (281) | 111 Rg (272) | 112 Сп (285) | 113 Nh (284) | 114 Fl (289) | 115 MC (288) | 116 LV (292) 904 59 | 117 Ц.  (294) | 118 Ога (294) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lanthanide Series * (Lanthanoid) | 57 La 138.9 | 58 Се 140,1 | 59 Пр 140,9 | 60 Nd 144,2 | 61 PM (145) | 62 1504 | 63 EU 152.  0 0 | 64 Б 157,3 | 65 Тб 158,9 | 66 Dy 162,5 | 67 Ho 164.9 | 68 Er Er Er 1673 | 69 TM 168.9 | 70 Yb 173,0 | 71 Lu 175,0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| актинидов ** (актиноидов) | 89 Ас (227) | 90 ЧТ 232,0 | 91 Па (231) | 92 U (238) | 93 Np (237) | 94 Pu (244) | 95 Ам (243) | 96 См 9045 8 (247) | + 97 Бк (247) | + 98 Cf (251) | + 99 Эс- (252) | 100 Fm (257) | 101 Md (258) | 102 Нет (259) | 103 Lr (262) 1628 8 628 906 *** Группы представлены по трем условным обозначениям.  Электронная почта: [email protected] Внесение Природу термических распылительных покрытий поверхностные машины в двух словах поверхностный инженерный форум термический распылительный пистолет Ремонт Плазма Расходные материалы Термический распылительный порошок поставки Применения: Термальные распылительные покрытия На углеродно-стеклянном волокне армированные полимеры HVOF Покрытие бумаги, изготовление бумаги Roll Мягкие покрытия Photomicroggraphts Процессы термического распыления: Провод сгорания Тепловой распылитель Процесс Порошок сгорания Тепловой распылительный процесс Дуговая провод Процесс термического напыления Процесс плазменного термического напыления Процесс термического напыления HVOF Процесс термического напыления HVAF Процесс детонационного термического напыления Теория плазменного пламени Процесс холодного напыления Износ и использование rmal Spray Coatings Коррозия и использование термических покрытий Глоссарий терминов термического напыления и обработки поверхности Каталог изображений для термических покрытий Информация о расходе плазменного газа Калькулятор коррекции расхода плазменного газа Форма 2 Ссылки Контактная информация на другие интересные сайты, связанные с термическим напылением и обработкой поверхностиВзаимные ссылки Периодическая таблица элементов Единицы СИ Калькуляторы для преобразования единиц измерения Измерение твердости Обработка поверхности0 Доска объявлений Архив обработки поверхностей0 Фотогалерея2 Фотогалерея3 © Copyright Gordon England Переходные металлы — элементы, определение, список, свойстваЧто такое переходные металлы? Переходные металлы или Переходные элементы в периодической таблице представляют собой химические элементы d-блока, лежащие между элементами p- и s-блока. Переходные металлы в периодической таблице Согласно определению переходного металла, медь, серебро и золото должны быть исключены из элементов d-блока периодической таблицы. Поскольку эти элементы не имеют частично заполненных d-орбиталей в их атомной или обычной степени окисления. Точно так же цинк, кадмий, ртуть и палладий не содержат частично заполненных d-орбиталей в их атомной или обычной степени окисления +2. Из-за сходных свойств и для сохранения рациональной классификации эти элементы обычно изучаются с d-блоками или переходными металлами. Электронная конфигурация переходных элементовВсе переходные элементы или элементы d-блока подразделяются на четыре серии, такие как 3d, 4d, 5d и 6d. Каждая серия 3d, 4d, 5d и 6d состоит из десяти химических элементов. Общая электронная конфигурация валентной оболочки переходных элементов: от (n-1)d 1 до 10 ns 0, 1, 2 .
Свойства переходных элементов Свойства переходных элементов данного периода не так уж сильно отличаются друг от друга. Металлический характер переходных элементовВсе переходные элементы являются металлами из-за небольшого числа электронов на самой внешней квантовой оболочке. Они твердые, податливые и пластичные.Они образовали все четыре типа кристаллических тел, такие как гранецентрированная кубическая, гексагональная закрытая упаковка, объемно-центрированная кубическая и гранецентрированная кубическая кристаллическая решетка. Металлическая и ковалентная связь существуют в атомах переходных металлов. Из-за наличия неполной d-орбитали большинство переходных металлов соединяются с другими элементами ковалентной химической связью. Эти металлы являются хорошими проводниками тепла и электричества. Тенденции изменения температуры плавления переходных металлов Переходные элементы имеют очень высокие температуры плавления и кипения по сравнению с элементами s- и p-блока. Атомные и ионные радиусы переходных элементовАтомный и ионный радиусы обычно уменьшаются при движении слева направо по периоду. Это связано с тем, что увеличение заряда ядра имеет тенденцию притягивать электронные облака к ядру атома.Атомные радиусы хрома к меди очень близки друг к другу. За счет одновременного добавления экранирующего электрона к 3d-уровню происходит обратное воздействие на внешние 4s-электроны. Ионные радиусы ионов М +2 и М +3 следуют тем же трендам атомных радиусов. Энергия ионизации переходных металлов Первая энергия ионизации переходных металлов лежит между значениями элементов s- и p-блока. Первые значения энергии ионизации лежат в пределах от 5 до 10 электрон-вольт.
Степень окисления переходных металлов Одним из наиболее важных свойств, отличающих переходные металлы от непереходных элементов, является переменная степень окисления или степень окисления. Каталитическая активность переходных металловБольшинство переходных металлов и их соединений используются в качестве хороших химических катализаторов в различных типах реакций. Некоторые примеры:
Переходные элементы | Encyclopedia. com comПереходные элементы — это элементы, составляющие группы с 3 по 12 периодической таблицы.Эти элементы, все из которых являются металлами, включают в себя некоторые из самых известных названий в периодической таблице — среди них железо, золото, серебро, медь, ртуть, цинк, никель, хром и платина. Ряд других переходных элементов, вероятно, несколько менее известен, хотя они имеют важное промышленное применение. Эти элементы включают титан, ванадий, марганец, цирконий, молибден, палладий и вольфрам. Особого упоминания заслуживает один член переходной семьи. Технеций (элемент № 43) — один из двух «легких» элементов, не встречающихся в природе.Первоначально он был получен синтетическим путем в 1937 году среди продуктов циклотронной реакции. Первооткрывателями технеция были итальянские физики Карло Перрье и Эмилио Сегре (1905–1989). Переходные элементы имеют много общих физических свойств. За заметным исключением ртути, единственного жидкого металла, все они имеют относительно высокие температуры плавления и кипения. Кроме того, переходные металлы имеют некоторые общие химические свойства.Например, они имеют тенденцию образовывать комплексы, соединения, в которых группа атомов группируется вокруг одного атома металла. Обычный сульфат меди, например, обычно встречается в конфигурации, включающей четыре молекулы воды, окружающие один ион меди. Комплексы переходных элементов имеют множество применений в медицине и промышленности. Еще одним общим свойством переходных элементов является их склонность к образованию окрашенных соединений. Некоторые из самых ярких и красивых известных химических соединений включают в себя переходные металлы.Соединения меди имеют тенденцию быть синими или зелеными; соединения хрома имеют желтый, оранжевый или зеленый цвет; соединения никеля имеют синий, зеленый или желтый цвет; а соединения марганца имеют пурпурный, черный или зеленый цвет. Полезные словаАмальгама: Сплав, содержащий ртуть. Основной кислородный процесс (BOP): Метод производства стали, при котором смесь чугуна, железного лома и стального лома плавится в большом стальном контейнере, и через контейнер продувается струя чистого кислорода. Преобразователь Бессемера: Устройство для преобразования чугуна в сталь, в котором поток горячего воздуха продувается через расплавленный чугун. Доменная печь: Сооружение, в котором металлическая руда (часто железная руда) восстанавливается до элементарного состояния. Чугун: Термин, используемый для описания различных форм железа, которые также содержат от 0,5 до 4,2 процента углерода и от 0,2 до 3,5 процента кремния. Комплекс: Химическое соединение, в котором один атом металла окружен двумя или более группами атомов. Ковкий: Способен вытягиваться или растягиваться в тонкую проволоку. Электролитическая ячейка: Система, в которой электрическая энергия используется для осуществления химических превращений. Электролитическая медь: Очень чистая форма меди. Ковкий: Можно раскатывать или штамповать в тонкие листы. Мартеновский процесс: Способ производства стали, при котором поток горячего воздуха или кислорода обдувают поверхность расплавленной смеси чугуна, гематита, железного лома и известняка в большом кирпичном контейнере. Патина: Антикоррозийная пленка, часто образующаяся на медных поверхностях. Чугун: Форма железа, состоящая приблизительно из 90 процентов чистого железа и оставшихся 10 процентов различных примесей. Шлак: Побочный продукт реакций производства железа, состоящий в основном из силиката кальция. Последующее обсуждение сосредоточено только на трех переходных элементах: железе, меди и ртути.Эти три элемента являются одними из самых известных и наиболее широко используемых из всех химических элементов. Железо Железо является четвертым по распространенности элементом в земной коре после кислорода, кремния и алюминия. Недвижимость. Железо — серебристо-белый или серый металл с температурой плавления 2795°F (1535°C) и точкой кипения 4982°F (2750°C). Его химический символ Fe происходит от латинского названия железа ferrum. Он податлив и пластичен. Ковкость — это свойство, присущее большинству металлов, означающее, что из вещества можно выбить тонкие листы. Многие металлы также пластичны, а это означает, что их можно вытянуть в тонкую проволоку. В чистом виде железо относительно мягкое и слабо магнитное.При затвердевании он становится намного более магнитным. Железо является наиболее широко используемым из всех металлов. Одной из наиболее распространенных форм чугуна является передельный чугун, получаемый путем плавки железной руды с коксом (почти чистым углеродом) и известняком в доменной печи. (Плавка — это процесс получения чистого металла из руды.) Чугун примерно на 90 процентов состоит из чистого железа и используется в основном для производства чугуна и стали. Чугун — это термин, используемый для описания различных форм железа, которые также содержат углерод и кремний в диапазоне концентраций от 0,5 до 4,2 процента первого и от 0,2 до 3,5 процента второго. Чугун имеет широкий спектр применения в различных изделиях, от тонких колец до массивных корпусов турбин. Кованое железо содержит небольшое количество ряда других элементов, включая углерод, кремний, фосфор, серу, хром, никель, кобальт, медь и молибден. Как получают железо. Железо — один из немногих элементов, известных древним цивилизациям. Первоначально его готовили путем нагревания встречающейся в природе железной руды с древесным углем в очень горячем пламени. Древесный уголь получали путем нагревания дров без доступа воздуха. Есть некоторые свидетельства того, что этот метод приготовления был известен еще в 3000 г. до н.э.Но секрет выплавки руды тщательно охранялся хеттской цивилизацией Ближнего Востока почти 2000 лет. Затем, когда эта цивилизация пала примерно в 1200 г. до н.э., процесс выплавки железной руды распространился по всей восточной и южной Европе. Вскоре кузнецы стали изготавливать из железа декоративные предметы, простые инструменты и оружие. Влияние этой новой технологии на человеческое общество было настолько драматичным, что в период после 1200 г. до н.э. обычно называют железным веком. Крупное изменение в технологии производства железа из руды произошло примерно в 1709 году.Поскольку деревьев (и, следовательно, древесного угля, получаемого из них) в Великобритании становилось все меньше, английский изобретатель Абрахам Дарби (ок. 1678–1717) открыл метод производства кокса из мягкого угля. Поскольку на Британских островах было много угля, метод Дарби обеспечил последовательный и надежный метод преобразования железных руд в чистый металл. Современное производство чугуна включает нагревание железной руды с коксом и известняком в доменной печи, где температура колеблется от 400°F (200°C) в верхней части печи до 3600°F (2000°C) в нижней части печи. .Некоторые доменные печи имеют высоту 15-этажного дома и могут производить 2400 тонн (2180 метрических тонн) железа в день. Внутри доменной печи происходит ряд химических реакций. Один из них включает реакцию кокса (почти чистого углерода) с кислородом с образованием монооксида углерода. Этот монооксид углерода затем реагирует с железной рудой с образованием чистого железа и диоксида углерода. Ранние попытки использовать чугун в коммерческих и промышленных целях не увенчались успехом. Материал оказался довольно хрупким, и предметы, сделанные из него, легко ломались. Например, пушки, сделанные из чугуна, могли разорваться на части при выстреле снаряда.К 1760 году изобретатели начали искать способы упрочнения чугуна. Эти методы включали переплавку чугуна и последующее сжигание углерода, оставшегося в смеси с продуктом. Самым успешным ранним устройством для выполнения этого шага был преобразователь Бессемера, названный в честь его английского изобретателя Генри Бессемера (1813–1898). Более поздние изобретения улучшили производство стали в конвертере Бессемера. Например, в мартеновском процессе смесь расплавленного чугуна, гематита, железного лома и известняка помещают в большой кирпичный контейнер. Затем на поверхность расплавленной смеси обдувают струю горячего воздуха или кислорода. Химические реакции в расплавленной смеси приводят к образованию либо чистого железа, либо, с добавлением легирующих металлов, таких как марганец или хром, высококачественной стали. Еще более поздней вариацией концепции бессемеровского конвертера является основной кислородный процесс (BOP). В противовыбросовом превенторе смесь чугуна, железного и стального лома плавится в большом стальном контейнере, и через контейнер продувается поток чистого кислорода. Использование железа. В сплаве с другими металлами железо является наиболее широко используемым из всех металлических элементов.Способ его сплавления определяет применение конечного продукта. Например, сталь — это общий термин, используемый для описания сплава железа с углеродом и, в некоторых случаях, с другими элементами. Американский институт чугуна и стали признает 27 стандартных типов стали. Три из них обозначены как углеродистые стали, которые могут содержать, помимо углерода, небольшое количество фосфора и/или серы. Еще 20 видов стали изготавливаются из железа, легированного одним или несколькими из следующих элементов: хромом, марганцем, молибденом, никелем, кремнием и ванадием.Наконец, четыре типа нержавеющих и жаропрочных сталей содержат некоторое сочетание хрома, никеля и марганца, легированного железом. Сталь широко используется во многих типах строительства. Металлурги (специалисты в области науки и технологии металлов) изобрели специальные сплавы железа для удовлетворения очень специфических потребностей. Сплавы кобальта и железа (оба магнитных материала сами по себе) можно использовать в производстве очень мощных постоянных магнитов.Стали, содержащие элемент ниобий (первоначально называвшийся колумбием), обладают необычайно высокой прочностью и использовались, в частности, в строительстве ядерных реакторов. Металлическое железо имеет и другие применения.Его естественные магнитные свойства делают его пригодным как для постоянных магнитов, так и для электромагнитов. Он также используется в производстве различных типов красителей, включая чертежную бумагу и некоторые чернила, а также в производстве абразивов. Биохимические применения. Железо необходимо для выживания всех позвоночных. Гемоглобин, молекула в крови, которая переносит кислород от легких к клеткам организма, содержит единственный атом железа, спрятанный глубоко внутри его сложной структуры.Когда люди не получают достаточного количества железа в своем ежедневном рационе, у них может развиться расстройство, известное как анемия. Железо также важно для здоровья растений. Он содержится в группе соединений, известных как порфирины (произносится как POUR-fuhrinz), которые играют важную роль в росте и развитии клеток растений. Растения, которым не хватает железа, имеют тенденцию терять свой цвет, становиться слабыми и погибать. МедьМедь — один из двух металлов с характерным цветом (второй — золото). Медь часто описывается как имеющая красновато-коричневый оттенок. Он имеет температуру плавления 1985°F (1085°C) и температуру кипения 4645°F (2563°C). Его химический символ Cu происходит от латинского названия элемента cuprum. Медь является одним из элементов, необходимых для жизни в небольших количествах (часто называемых микроэлементами), хотя большие количества могут быть токсичными.Около 0,0004 процента веса человеческого тела составляет медь. Медь также входит в состав важного биохимического соединения, известного как гемоцианин. Гемоцианин химически похож на красный гемоглобин, обнаруженный в крови человека, который имеет атом железа в центре своей молекулы. Напротив, гемоцианин содержит в своем ядре атом меди, а не железа. Омары и другие крупные ракообразные имеют голубую кровь, цвет которой обусловлен наличием гемоцианина. История меди. Медь была одним из первых металлов, известных человеку. Одна из причин этого факта заключается в том, что медь встречается не только в виде руд (соединений, которые необходимо превратить в металл), но иногда и в виде самородной меди, чистой формы элемента, обнаруженного в земле. В доисторические времена первобытный человек мог найти в земле кусок чистой меди и вбить его в инструмент камнем. Самородная медь добывалась и использовалась в долине Тигра и Евфрата (современный Ирак) еще 7000 лет назад. Изготовление чистой меди. Чрезвычайно чистая медь (чистота более 99,95 процентов) обычно называется электролитической медью, поскольку она производится с помощью процесса, известного как электролиз. Электролиз — это реакция, при которой электрическая энергия используется для осуществления каких-либо химических изменений.Высокая чистота необходима, потому что большая часть меди используется для изготовления электрического оборудования. Небольшие количества примесей, присутствующих в меди, могут серьезно снизить ее способность проводить электричество. Например, даже 0,05 процента мышьяка в качестве примеси снизит проводимость меди на 15 процентов. Электрические провода должны быть сделаны из очень чистой меди, особенно если электричество должно передаваться на многие мили по высоковольтным линиям электропередач. Использование меди. Безусловно, наиболее важным применением меди является электропроводка.Это отличный проводник электричества (уступает только серебру), его можно сделать очень чистым, он очень медленно подвергается коррозии, и из него можно легко сделать тонкие провода. Медь также является важным компонентом многих полезных сплавов. (Сплав — это смесь одного металла с другим для улучшения свойств исходного металла.) Латунь — это сплав меди и цинка. Если латунь содержит в основном медь, она имеет золотисто-желтый цвет; если он содержит в основном цинк, он бледно-желтый или серебристый.Латунь — один из самых полезных сплавов. Из него можно отлить или выточить что угодно, от подсвечников до дешевых украшений, имитирующих золото (но этот тип украшений часто окрашивает кожу человека в зеленый цвет — медь вступает в реакцию с солями и кислотами в коже, образуя зеленый хлорид меди и другие соединения). Некоторые другие медные сплавы включают: бронзу, состоящую в основном из меди и олова; Нейзильбер и стерлинговое серебро, состоящие из серебра и меди; и серебряные зубные пломбы, которые содержат около 12 процентов меди. Вероятно, первым сплавом, который когда-либо был изготовлен и использован людьми, была бронза. Археологи широко делят историю человечества на три периода. Бронзовый век (ок. 4–3 тыс. до н. э.) — второй из этих периодов, наступивший после каменного века и до железного века. В эпоху бронзы как бронза, так и чистая медь использовались для изготовления инструментов и оружия. Поскольку медь устойчива к коррозии и хорошо проводит тепло, она широко используется в сантехнике и отоплении. Медные трубы и трубки используются для распределения горячей и холодной воды по домам и другим зданиям.Превосходная способность меди проводить тепло также делает ее полезной в производстве кухонной утвари, такой как кастрюли и сковородки. Равномерная температура по всему дну кастрюли важна для приготовления пищи, чтобы пища не пригорала и не прилипала к горячим точкам. Однако внутренняя часть кастрюль должна быть покрыта оловом, чтобы чрезмерное количество меди не просачивалось в пищу. Медь медленно подвергается коррозии во влажном воздухе — гораздо медленнее, чем ржавеет железо. РтутьРтуть, единственный жидкий металл, имеет красивый серебристый цвет. Его химический символ Hg происходит от латинского названия элемента, Hydrargyrum, для «жидкого серебра». Ртуть имеет температуру плавления -38°F (-70°C) и температуру кипения 673°F (352.5°С). Его присутствие в земной коре относительно невелико по сравнению с другими элементами и составляет около 0,08 частей на миллион. Однако ртуть не считается редкостью, потому что она находится в крупных высококонцентрированных месторождениях. Почти вся ртуть существует в виде красной руды, называемой киноварью, или сульфида ртути (II). Иногда среди выходов киновари появляются блестящие шарики ртути, что, вероятно, является причиной того, что ртуть была открыта так давно. Ртуть не вступает в реакцию с воздухом, водой, кислотами, щелочами или большинством других химических веществ. Его поверхностное натяжение в шесть раз больше, чем у воды.Поверхностное натяжение относится к тенденции жидкости образовывать прочную «пленку» на своей поверхности. Высокое поверхностное натяжение ртути объясняет ее склонность не «смачивать» поверхности, с которыми она соприкасается. Никто точно не знает, когда была открыта ртуть, но многие древние цивилизации были знакомы с этим элементом. Еще во времена Римской империи люди научились извлекать ртуть из руды и использовать ее для очистки золота и серебра. Токсичность. Ртуть и все ее соединения чрезвычайно ядовиты. Этот элемент также не имеет известной естественной функции в организме человека. Классифицируемая как тяжелый металл, ртуть с трудом выводится из организма. Это означает, что даже небольшое количество металла может действовать как кумулятивный яд, накапливаясь в течение длительного периода времени, пока не достигнет опасного уровня. Человек может всасывать ртуть через любую слизистую оболочку и через кожу.Его пары можно вдыхать, а ртуть может попасть в организм с такими продуктами, как рыба, яйца, мясо и зерно. В организме ртуть поражает нервную систему, печень и почки. Симптомы отравления ртутью включают тремор, туннельное зрение, потерю равновесия, невнятную речь и непредсказуемые эмоции. периферическое зрение — внешняя часть поля зрения, охватывающая крайнюю правую и крайнюю левую стороны — полностью исчезает.) Фраза «безумный, как шляпник» обязана этому. происхождения к симптомам отравления ртутью, которые поражали шляпников в 1800-х годах, когда соединение ртути использовалось для изготовления бобрового меха и войлочных материалов. До недавнего времени ученые считали неорганическую ртуть относительно безвредной. В результате промышленные отходы, содержащие ртуть, регулярно сбрасывались в большие водоемы. Затем, в 1950-х годах, более 100 человек в Японии отравились рыбой, содержащей ртуть. Сорок три человека погибли, еще десятки были ужасно искалечены, а дети, родившиеся после вспышки, получили необратимые повреждения. Было обнаружено, что неорганическая ртуть в промышленных отходах превратилась в гораздо более вредную органическую форму, известную как метилртуть.По мере того, как это вещество продвигается вверх по пищевой цепочке, его количество накапливается до опасного уровня в более крупной рыбе. Использование. Ртуть широко используется в различных измерительных приборах и устройствах, таких как термометры, барометры, ареометры и пирометры. Он также используется в электрических переключателях и реле, в ртутных дуговых лампах и для извлечения золота и серебра из амальгам.Небольшое количество все еще используется при приготовлении амальгам для ремонта зубов. Однако в настоящее время ртуть чаще всего используется в электролитических элементах, в которых хлорид натрия преобразуется в металлический натрий и газообразный хлор. Ртуть используется для образования амальгамы с натрием в клетках. [ См. также Сплав ] Периодические тенденции переходных металлов Периодические тренды играют огромную роль в органической химии.Регулярные изменения электроотрицательности, размера атома, энергии ионизации и других переменных в периодической таблице позволяют нам делать систематические прогнозы поведения подобных соединений. Прежде чем начать, необходимо сделать пару предостережений. Во-первых, многие тенденции переходного ряда не совсем регулярны. Хартвиг мудро советует рассматривать ряды переходов блоками, а не в целом при рассмотрении периодических трендов. Например, общее увеличение количества может прерываться внезапным уменьшением; в таком случае мы можем сказать, что количество в целом увеличивается, но определенные выводы возможны только тогда, когда сравниваемые металлы находятся близко друг к другу в периодической таблице (и мы должны быть осторожны с неожиданными скачками). Атомный размерТенденции в размерах атомов, вероятно, являются наиболее прямыми из переходных серий.На рисунке ниже показаны ковалентные радиусы металлов в группах 4-10. Ковалентный радиус — удобный показатель размера атома, особенно потому, что нас интересует размер металлов в комплексах ОМ. Обратите внимание, что приведенные ниже номера строк относятся только к серии переходов, а не к периодической таблице в целом. Ковалентный радиус как функция номера группы и строки. Даже этот график таит в себе некоторую загадку, но давайте начнем с того, что бросается в глаза:
Тенденция вниз по группе имеет смысл по той простой причине, что главное квантовое число увеличивается по мере продвижения вниз по группе. Предыдущее предложение кажется вам бредом? (Возможно, вы химик-органик, если…) Просто запомните: орбиталей увеличиваются по мере того, как мы движемся вниз по группе . Это так же верно для переходных металлов, как и для остальной части таблицы Менделеева. Что касается тренда слева направо, то он тоже имеет простое объяснение.По мере того, как мы движемся вправо по таблице Менделеева, к ядру добавляются протоны, но добавленные электроны не уравновешивают заряд протона в точности (из-за экранирования). Есть еще кое-что неладное: металлы третьего ряда примерно того же размера, что и металлы второго ряда, особенно когда мы приближаемся к поздним металлам. Что дает?! Вы не можете объяснить это… это определенно кажется несовместимым с нашим предыдущим обсуждением больших орбиталей по мере того, как мы движемся вниз по группе. На самом деле, мистер О’Рейли, мы можем это объяснить, и для этого нам не нужно прибегать к чему-то новому. лантаноидов , зажатых между 2 и 3 рядами переходного ряда, являются ключевыми.От строки 2 к строке 3 орбитали действительно увеличиваются из-за увеличения главного квантового числа, но этот эффект уравновешивается большим горизонтальным блужданием по лантаноидам до — мы достигаем третьей строки ряда переходов. Переходные металлы третьего ряда обладают относительно небольшими ковалентными радиусами из-за «лантаноидного сжатия». Значительная разница в размерах между металлами первого и второго ряда использовалась в ряде случаев, и мы еще увидим ее.Известным примером является асимметричное катализируемое никелем альфа-арилирование, которое демонстрирует более высокую энантиоселективность, чем методы, катализируемые палладием. Более высокая стереоселективность никелевого катализатора объясняется меньшим размером никелевого центра. Или, если хотите звучать как профессионалы, «более интимная хиральная среда» никелевых катализаторов. Энергия ионизации Энергия ионизации переходного металла связана с энергиями его орбиталей d , легкостью его окисления и его основностью.Проще говоря, чем больше энергия ионизации металла, тем труднее вырвать из него электрон. Какой порядок мы можем извлечь из этого хаоса энергий ионизации? Первое, что мы можем заметить, это то, что в целом энергия ионизации увеличивается, когда мы движемся слева направо по ряду.Заметные провалы наблюдаются в ряду 1, группе 10 (Ni) и ряду 3, группе 7 (Re). Однако общая тенденция согласуется с нашим предыдущим представлением о том, что электроотрицательность увеличивается, когда мы двигаемся слева направо по строке . Что касается трендов вниз по группе, то на графике выше трудно разглядеть что-то полезное. Что мы можем сказать (учитывая второй и более высокие потенциалы ионизации, не показанные), так это то, что высших степеней окисления более доступны для металлов третьего ряда . Мы снова коснемся трендов кислотности/основности в более позднем посте о гидридных лигандах, но они, как правило, следуют трендам прочности связи, описанным ниже: основность увеличивается (а кислотность снижается) по мере продвижения вниз по группе, как правило. Сила связи Прочность связей металл-основная группа в металлоорганических комплексах варьируется в некоторой степени предсказуемым образом. В общем, сила связи увеличивается при движении вниз по группе . Хотите верьте, хотите нет, но эта тенденция не так уж удивительна в свете тенденций изменения энергии ионизации, которые мы уже обсуждали.Большая энергия ионизации предполагает низкоэнергетические орбитали d , а более низкоэнергетические орбитали d лучше подходят для перекрытия с орбиталями органических элементов. РезюмеВот удобный маркированный список общих тенденций, обсуждаемых в этом посте. ИСПОЛЬЗУЙТЕ С ОСТОРОЖНОСТЬЮ!
Нравится:Нравится Загрузка… РодственныеМеталлы после перехода – Химия для учащихсяПостпереходные элементы в периодической таблице представляют собой группу элементов, расположенных между переходными металлами (справа) и металлоидами (слева).Из-за своих свойств их также называют «другими» или «бедными» металлами [1] . Место постпереходных металлов в периодической таблицеХотя существуют некоторые противоречивые теории, обычно постпереходные металлы включают элементы из групп 13-15 [1,2] . Постпереходные металлы в периодической таблице Элементы 113-116 в периодической таблице, т. е. нихоний (Nh), флеровий (Fl), московий (Mc) и ливерморий (Lv), считаются, возможно, принадлежащими к семейству постпереходных металлов, хотя он еще должно быть подтверждено из-за некоторых неизвестных свойств элементов [6] . Полоний иногда также включается в список постпереходных металлов. То же самое можно сделать для цинка, кадмия и ртути (иначе считающихся переходными металлами), а также для германия и сурьмы (иначе считающихся металлоидами) [1] . Свойства и характеристики металлов после переходаПример металла после перехода Висмут Физические свойства
Химические свойства
Как правило, атомные радиусы уменьшаются, энергия ионизации увеличивается, в результате меньше электронов доступно для металлической связи, поэтому ионы становятся меньше, более поляризованы и склонны к образованию ковалентных связей. Использование металлов после переходаРазличные элементы этого семейства имеют различное применение. Алюминий и олово соответственно используются для изготовления посуды, в электронике, а также для пайки и покрытия стали [5] . Висмут используется для производства пепто-бисмола, лекарства, используемого для успокоения расстройства желудка [1,5] . Индий используется в электронике, например, при изготовлении сенсорных экранов и плоских дисплеев, а галлий применяется в полупроводниках и топливных элементах [1, 2] .Среди прочего свинец используется для изготовления аккумуляторов. Интересные факты
Каталожные номера:
 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 Эти элементы либо в их атомарном состоянии, либо в любой их общей степени окисления или состоянии имеют частично заполненную (n-1)d-орбиталь. Электронная конфигурация валентной оболочки элементов d-блока или переходных металлов: (n-1)d 1 до 10 ns 0, 1, 2 . Элементы f-блока (лантаниды или редкоземельные элементы и актиноиды) в периодической таблице называются внутренними переходными металлами. Их называют внутренними переходными металлами, потому что дополнительный электрон входит в (n-2)f-орбитали.
Эти элементы либо в их атомарном состоянии, либо в любой их общей степени окисления или состоянии имеют частично заполненную (n-1)d-орбиталь. Электронная конфигурация валентной оболочки элементов d-блока или переходных металлов: (n-1)d 1 до 10 ns 0, 1, 2 . Элементы f-блока (лантаниды или редкоземельные элементы и актиноиды) в периодической таблице называются внутренними переходными металлами. Их называют внутренними переходными металлами, потому что дополнительный электрон входит в (n-2)f-орбитали.
 Причина этого факта кроется в электронной конфигурации переходных элементов. Общая электронная конфигурация переходных металлов отличается друг от друга только числом электронов на d-орбитали. Количество электронов на самой внешней оболочке неизменно равно 0, 1, 2.
Причина этого факта кроется в электронной конфигурации переходных элементов. Общая электронная конфигурация переходных металлов отличается друг от друга только числом электронов на d-орбитали. Количество электронов на самой внешней оболочке неизменно равно 0, 1, 2.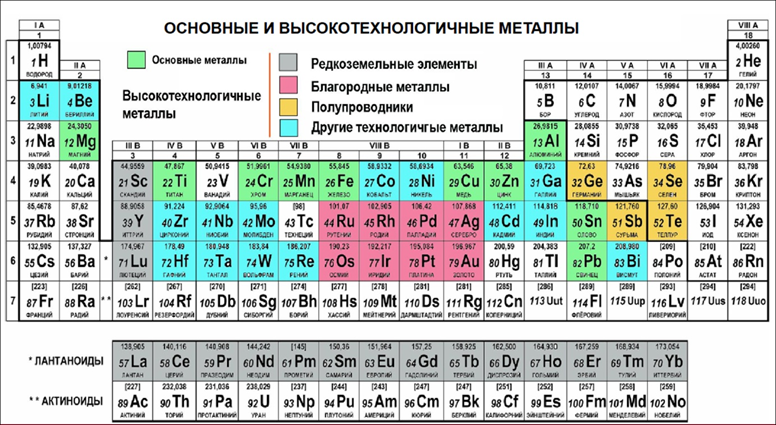 Металлы цинк, кадмий и ртуть имеют относительно низкие значения из-за полностью заполненных d-орбиталей. Для ковалентной связи между атомами цинка, кадмия и ртути отсутствуют неспаренные электроны. Другой переходный металл содержит не полностью заполненную d-орбиталь для ковалентной связи.
Металлы цинк, кадмий и ртуть имеют относительно низкие значения из-за полностью заполненных d-орбиталей. Для ковалентной связи между атомами цинка, кадмия и ртути отсутствуют неспаренные электроны. Другой переходный металл содержит не полностью заполненную d-орбиталь для ковалентной связи..jpg) В случае переходных металлов добавление дополнительных экранирующих электронов экранирует или уменьшает внутреннее притяжение положительного ядра и ns-электронов. Поэтому эффекты увеличения заряда ядра и эффекты экранирования противодействуют друг другу. За счет этих встречных эффектов потенциалы ионизации медленно возрастают при движении в периоде первой переходной серии.
В случае переходных металлов добавление дополнительных экранирующих электронов экранирует или уменьшает внутреннее притяжение положительного ядра и ns-электронов. Поэтому эффекты увеличения заряда ядра и эффекты экранирования противодействуют друг другу. За счет этих встречных эффектов потенциалы ионизации медленно возрастают при движении в периоде первой переходной серии.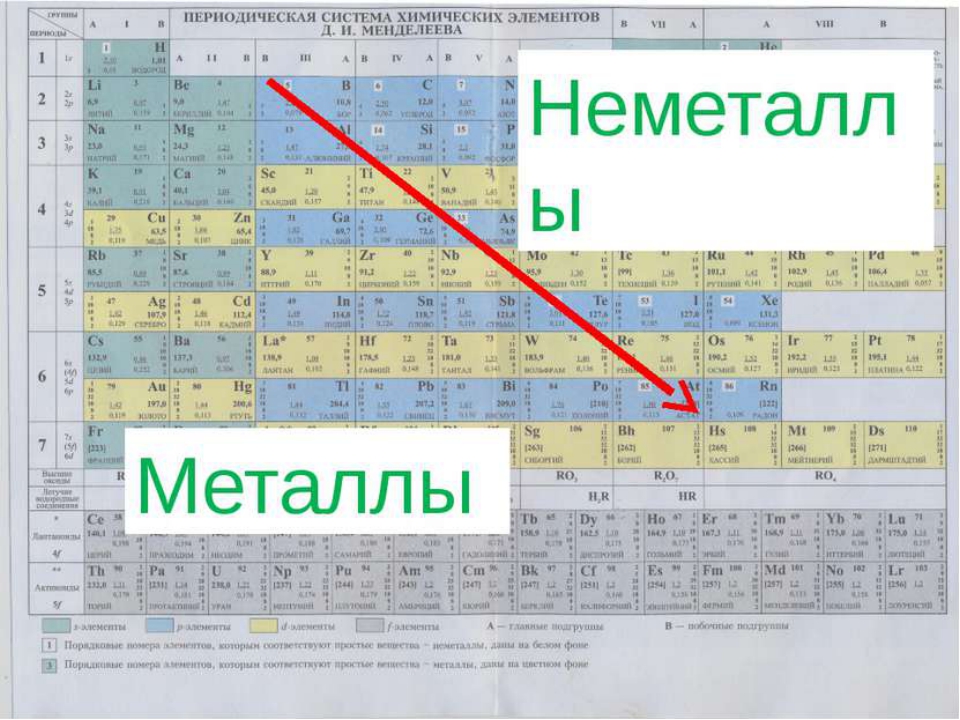 Это уникальное свойство связано с тем, что энергетические уровни 3d-, 4d- и 5d-орбиталей близки к 4s-, 5s- и 6s-орбиталям соответственно. Следовательно, помимо ns-электронов, различное количество (n-1)d-электронов также теряется из-за различных степеней окисления.
Это уникальное свойство связано с тем, что энергетические уровни 3d-, 4d- и 5d-орбиталей близки к 4s-, 5s- и 6s-орбиталям соответственно. Следовательно, помимо ns-электронов, различное количество (n-1)d-электронов также теряется из-за различных степеней окисления. Они также имеют блестящий, блестящий металлический вид, который может варьироваться от серебристого до золотого, от белого до серого.
Они также имеют блестящий, блестящий металлический вид, который может варьироваться от серебристого до золотого, от белого до серого.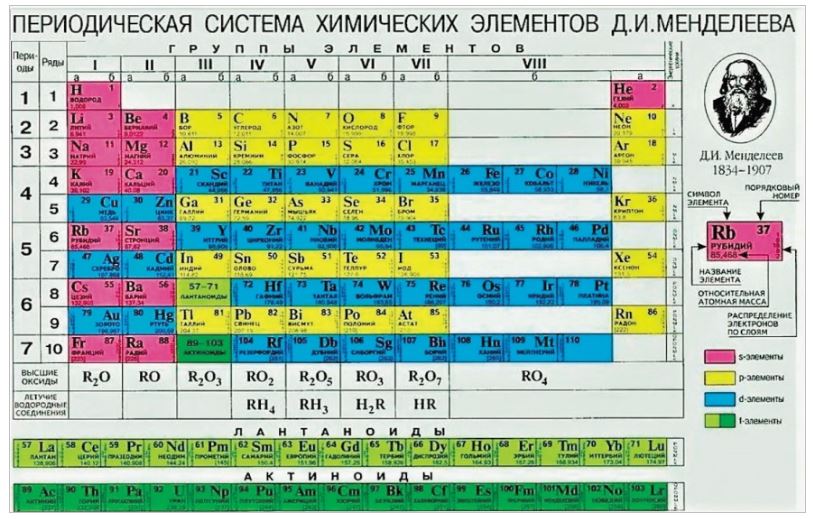

 Кроме того, считается, что ядро Земли состоит в основном из железа. Этот элемент редко встречается в несвязанной форме, но обычно встречается в виде минерала, такого как гематит (оксид железа [III]), магнетит (магнитный магнит, смесь оксидов железа [II] и железа [III]), лимонит (гидратированное железо [III]). III]), пирит (сульфид железа) и сидерит (железо[II] карбонат).
Кроме того, считается, что ядро Земли состоит в основном из железа. Этот элемент редко встречается в несвязанной форме, но обычно встречается в виде минерала, такого как гематит (оксид железа [III]), магнетит (магнитный магнит, смесь оксидов железа [II] и железа [III]), лимонит (гидратированное железо [III]). III]), пирит (сульфид железа) и сидерит (железо[II] карбонат). Однако перед использованием его необходимо каким-то образом обработать для улучшения свойств или соединить с одним или несколькими другими элементами (в данном случае с другим металлом) для образования сплава. На сегодняшний день самым популярным сплавом железа является сталь.
Однако перед использованием его необходимо каким-то образом обработать для улучшения свойств или соединить с одним или несколькими другими элементами (в данном случае с другим металлом) для образования сплава. На сегодняшний день самым популярным сплавом железа является сталь.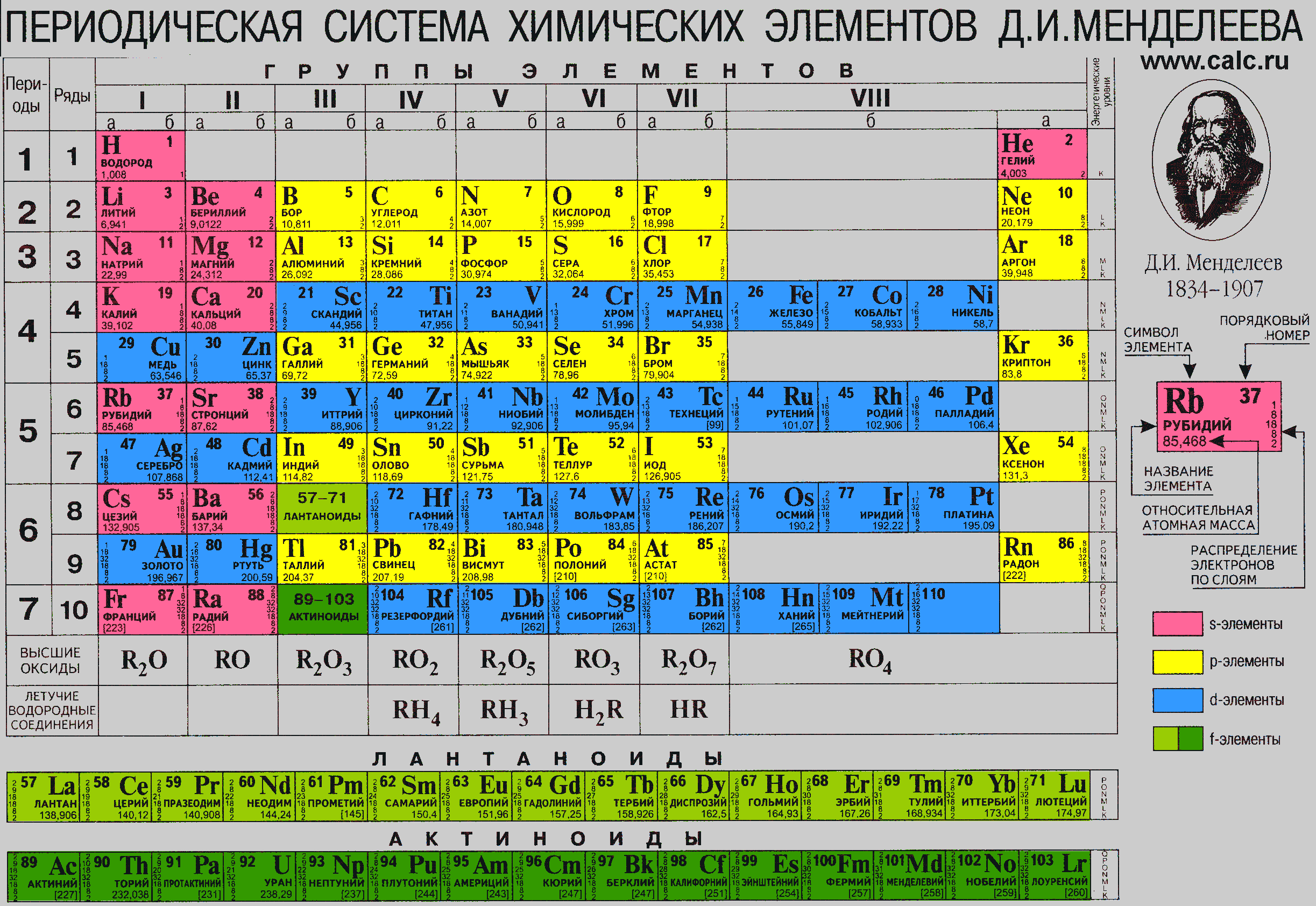 Кованое железо может быть изготовлено в различных формах и широко используется из-за его устойчивости к коррозии.
Кованое железо может быть изготовлено в различных формах и широко используется из-за его устойчивости к коррозии.
 Введение легирующих металлов делает возможным производство различных марок стали с самыми разными свойствами.
Введение легирующих металлов делает возможным производство различных марок стали с самыми разными свойствами. Он как минимум в шесть раз прочнее бетона, другого традиционного строительного материала, и примерно в три раза прочнее специальных форм высокопрочного бетона. Комбинация этих двух материалов, называемая железобетоном, является одним из самых прочных строительных материалов, доступных архитекторам.Прочность стали сделала возможными некоторые замечательные строительные подвиги, в том числе очень высокие здания (небоскребы) и мосты с очень широкими пролетами. Он также используется в производстве автомобильных кузовов, корпусов кораблей, тяжелой техники и деталей машин.
Он как минимум в шесть раз прочнее бетона, другого традиционного строительного материала, и примерно в три раза прочнее специальных форм высокопрочного бетона. Комбинация этих двух материалов, называемая железобетоном, является одним из самых прочных строительных материалов, доступных архитекторам.Прочность стали сделала возможными некоторые замечательные строительные подвиги, в том числе очень высокие здания (небоскребы) и мосты с очень широкими пролетами. Он также используется в производстве автомобильных кузовов, корпусов кораблей, тяжелой техники и деталей машин. Вольфрамовые стали также очень прочны и используются в производстве высокоскоростных металлорежущих инструментов и сверл. Легирование алюминия железом дает материал, который можно использовать в магнитных цепях переменного тока (переменного тока), поскольку он может очень быстро приобретать и терять магнетизм.
Вольфрамовые стали также очень прочны и используются в производстве высокоскоростных металлорежущих инструментов и сверл. Легирование алюминия железом дает материал, который можно использовать в магнитных цепях переменного тока (переменного тока), поскольку он может очень быстро приобретать и терять магнетизм. Анемия характеризуется потерей цвета кожи, слабостью и тенденцией к обморокам, учащенным сердцебиением и общим чувством истощения.
Анемия характеризуется потерей цвета кожи, слабостью и тенденцией к обморокам, учащенным сердцебиением и общим чувством истощения. Его можно найти в таких продуктах, как печень, моллюски, орехи, изюм и сушеные бобы.
Его можно найти в таких продуктах, как печень, моллюски, орехи, изюм и сушеные бобы. Медные руды добывались по крайней мере 5000 лет, потому что извлечь медь из руды довольно легко. Например, если руда оксида меди нагревается в дровяном огне, углерод в древесном угле вступает в реакцию с кислородом в оксиде и превращает его в чистую металлическую медь.
Медные руды добывались по крайней мере 5000 лет, потому что извлечь медь из руды довольно легко. Например, если руда оксида меди нагревается в дровяном огне, углерод в древесном угле вступает в реакцию с кислородом в оксиде и превращает его в чистую металлическую медь.
 Во-первых, он темнеет по цвету из-за образования тонкого слоя черного оксида меди.Затем, с течением времени, оксид меди превращается в голубовато-зеленую патину (поверхностный вид, который приходит с возрастом) основного карбоната меди. Так образовался зеленый цвет Статуи Свободы, например.
Во-первых, он темнеет по цвету из-за образования тонкого слоя черного оксида меди.Затем, с течением времени, оксид меди превращается в голубовато-зеленую патину (поверхностный вид, который приходит с возрастом) основного карбоната меди. Так образовался зеленый цвет Статуи Свободы, например. Металл относительно легко извлечь из руды.Фактически современный метод извлечения ртути в принципе почти идентичен методу, использовавшемуся много веков назад. Киноварь нагревают на открытом воздухе. Кислород в воздухе вступает в реакцию с серой в киновари, образуя чистую металлическую ртуть. Металлическая ртуть испаряется и конденсируется на прохладной поверхности, с которой ее можно собрать.
Металл относительно легко извлечь из руды.Фактически современный метод извлечения ртути в принципе почти идентичен методу, использовавшемуся много веков назад. Киноварь нагревают на открытом воздухе. Кислород в воздухе вступает в реакцию с серой в киновари, образуя чистую металлическую ртуть. Металлическая ртуть испаряется и конденсируется на прохладной поверхности, с которой ее можно собрать. Руда, содержащая золото или серебро, будет измельчена и обработана ртутью, которая удаляет примеси, с образованием ртутного сплава, называемого амальгамой.Когда амальгама нагревается, ртуть испаряется, оставляя чистое золото или серебро.
Руда, содержащая золото или серебро, будет измельчена и обработана ртутью, которая удаляет примеси, с образованием ртутного сплава, называемого амальгамой.Когда амальгама нагревается, ртуть испаряется, оставляя чистое золото или серебро. (Туннельное зрение — это сужение поля зрения, поэтому
(Туннельное зрение — это сужение поля зрения, поэтому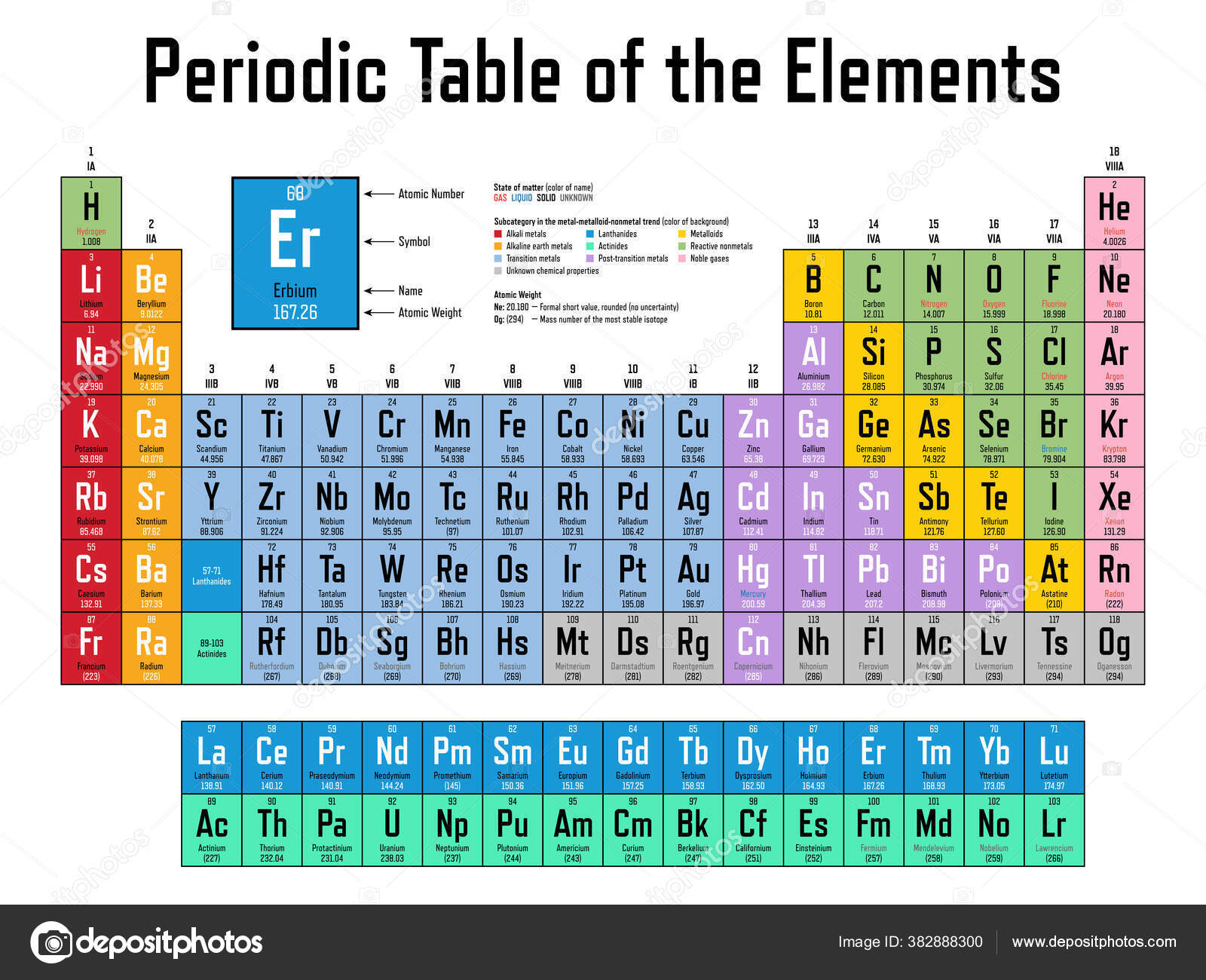 Сегодня захоронение содержащих ртуть отходов в значительной степени запрещено, и многие виды ее промышленного использования прекращены.
Сегодня захоронение содержащих ртуть отходов в значительной степени запрещено, и многие виды ее промышленного использования прекращены.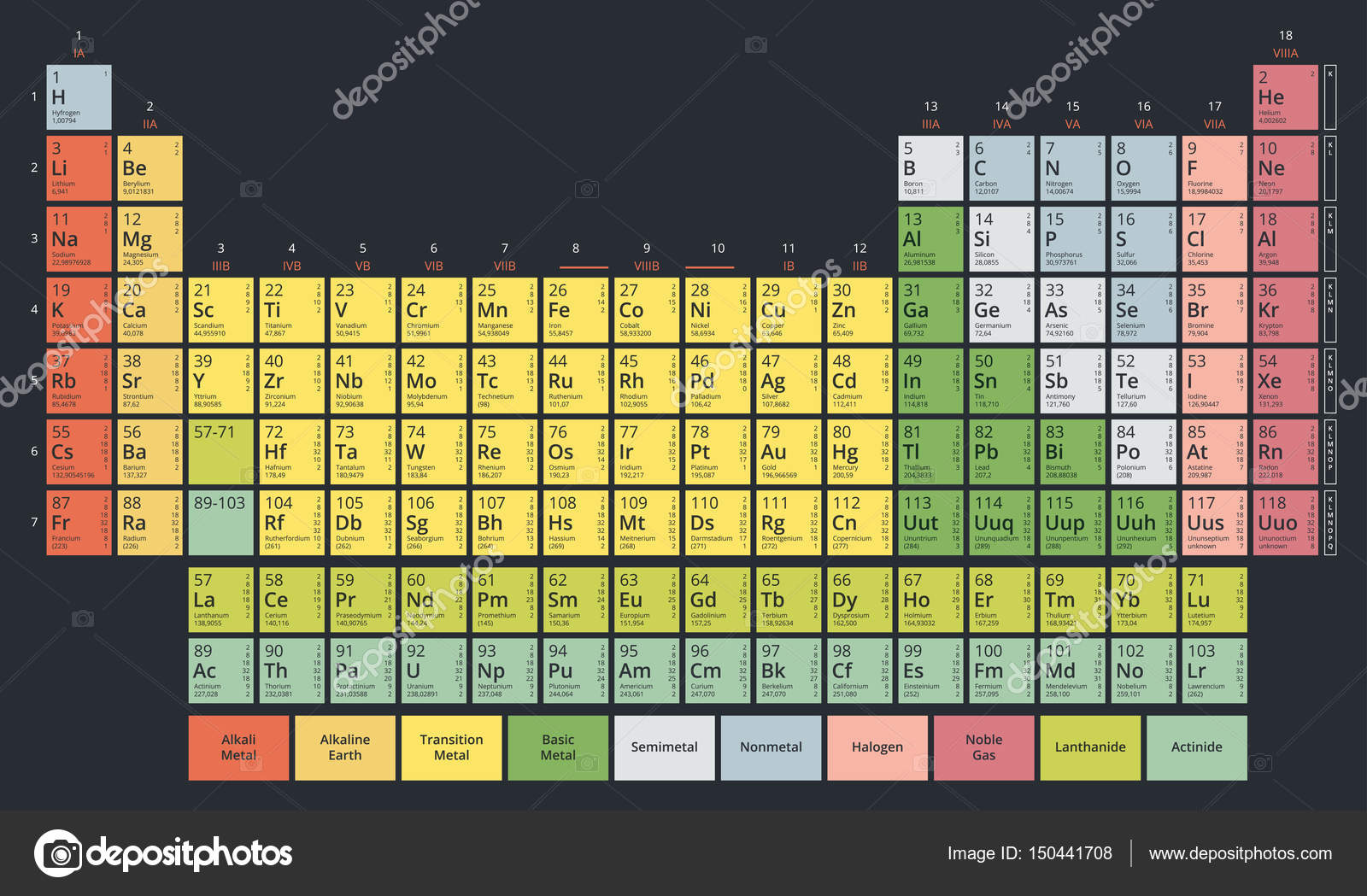 Конечно, то же самое верно и для металлоорганических комплексов! Твердо ухватившись за периодические тенденции переходных металлов, мы можем начать сравнивать комплексы, с которыми мы знакомы, и те, которые мы никогда раньше не видели. Периодические тренды по существу обеспечивают экспоненциальное увеличение прогностической способности.В этом посте мы рассмотрим основные периодические тренды переходных металлов и обсудим несколько примеров, для которых эти тренды могут быть полезны.
Конечно, то же самое верно и для металлоорганических комплексов! Твердо ухватившись за периодические тенденции переходных металлов, мы можем начать сравнивать комплексы, с которыми мы знакомы, и те, которые мы никогда раньше не видели. Периодические тренды по существу обеспечивают экспоненциальное увеличение прогностической способности.В этом посте мы рассмотрим основные периодические тренды переходных металлов и обсудим несколько примеров, для которых эти тренды могут быть полезны. Во-вторых, на периодические тенденции в значительной степени влияет идентичность лигандов и степень окисления металлического центра, поэтому сравнения необходимо соответствующим образом контролировать. Использование периодических трендов для сравнения комплекса Pd(II) и комплекса Ru(III) в значительной степени бесполезно, но разумно сравнивать комплексы Pt(II) и Pd(II) с аналогичными наборами лигандов. Помните об этих идеях, чтобы не крутить колеса без необходимости! Хорошо, давайте погрузимся…
Во-вторых, на периодические тенденции в значительной степени влияет идентичность лигандов и степень окисления металлического центра, поэтому сравнения необходимо соответствующим образом контролировать. Использование периодических трендов для сравнения комплекса Pd(II) и комплекса Ru(III) в значительной степени бесполезно, но разумно сравнивать комплексы Pt(II) и Pd(II) с аналогичными наборами лигандов. Помните об этих идеях, чтобы не крутить колеса без необходимости! Хорошо, давайте погрузимся… Обратите внимание на странный переход от строки 2 к строке 3!
Обратите внимание на странный переход от строки 2 к строке 3! Конечным результатом является то, что эффективный заряд ядра увеличивается по мере того, как мы двигаемся слева направо по периодической таблице. Есть два важных следствия этого явления: электроотрицательность увеличивается , а размер уменьшается по мере движения слева направо. Такая же тенденция наблюдается для углерода, азота, кислорода и фтора.
Конечным результатом является то, что эффективный заряд ядра увеличивается по мере того, как мы двигаемся слева направо по периодической таблице. Есть два важных следствия этого явления: электроотрицательность увеличивается , а размер уменьшается по мере движения слева направо. Такая же тенденция наблюдается для углерода, азота, кислорода и фтора.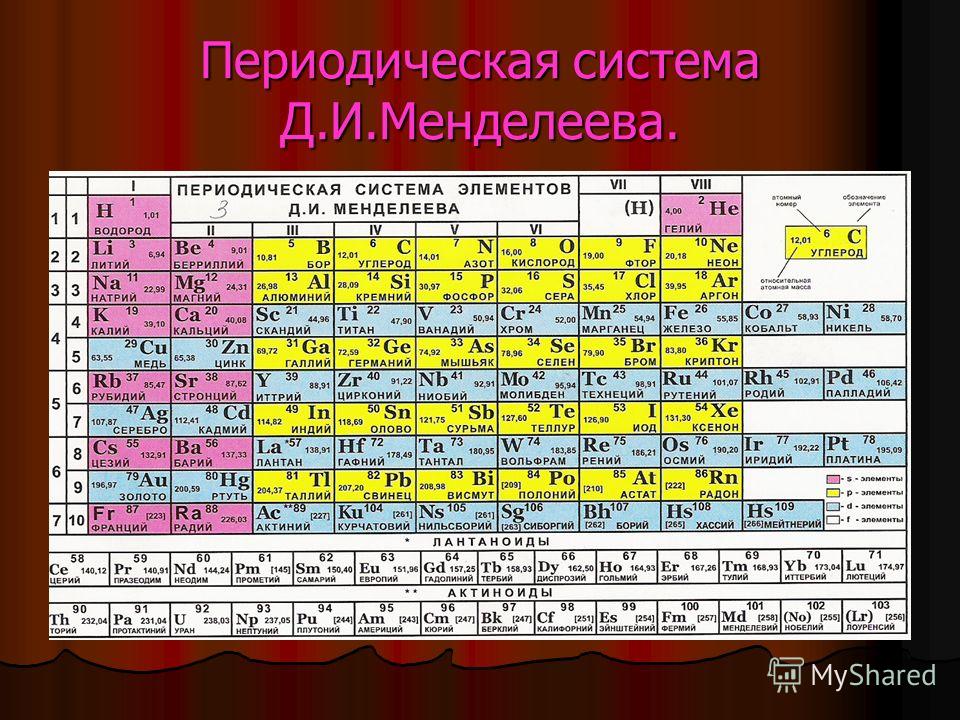 Конечным результатом является то, что переходные металлы третьего ряда имеют примерно тот же размер, что и их аналоги из второго ряда.
Конечным результатом является то, что переходные металлы третьего ряда имеют примерно тот же размер, что и их аналоги из второго ряда. Таким образом, металлические центры с высокими энергиями ионизации обладают низкой основностью (или нуклеофильностью) и устойчивы к окислению. Тенденции в энергии ионизации более сложны, чем тенденции в размерах атомов, как наглядно демонстрирует приведенный ниже график.
Таким образом, металлические центры с высокими энергиями ионизации обладают низкой основностью (или нуклеофильностью) и устойчивы к окислению. Тенденции в энергии ионизации более сложны, чем тенденции в размерах атомов, как наглядно демонстрирует приведенный ниже график. Простой способ запомнить это: OsO 4 — стабильный реагент, реагирующий только с алкенами; RuO 4 готовится на месте и разрушает алкены и спирты; FeO 4 никогда не наблюдалось.
Простой способ запомнить это: OsO 4 — стабильный реагент, реагирующий только с алкенами; RuO 4 готовится на месте и разрушает алкены и спирты; FeO 4 никогда не наблюдалось. Таким образом, мы должны ожидать, что более прочные связи будут связаны с более высокими энергиями ионизации… и это то, что в целом наблюдается! Это в значительной степени ковалентный аргумент, поскольку он основан на идеях орбитального перекрытия; ионные эффекты, связанные с частичными зарядами, также важны, но мы не будем открывать эту банку с червями здесь.
Таким образом, мы должны ожидать, что более прочные связи будут связаны с более высокими энергиями ионизации… и это то, что в целом наблюдается! Это в значительной степени ковалентный аргумент, поскольку он основан на идеях орбитального перекрытия; ионные эффекты, связанные с частичными зарядами, также важны, но мы не будем открывать эту банку с червями здесь.
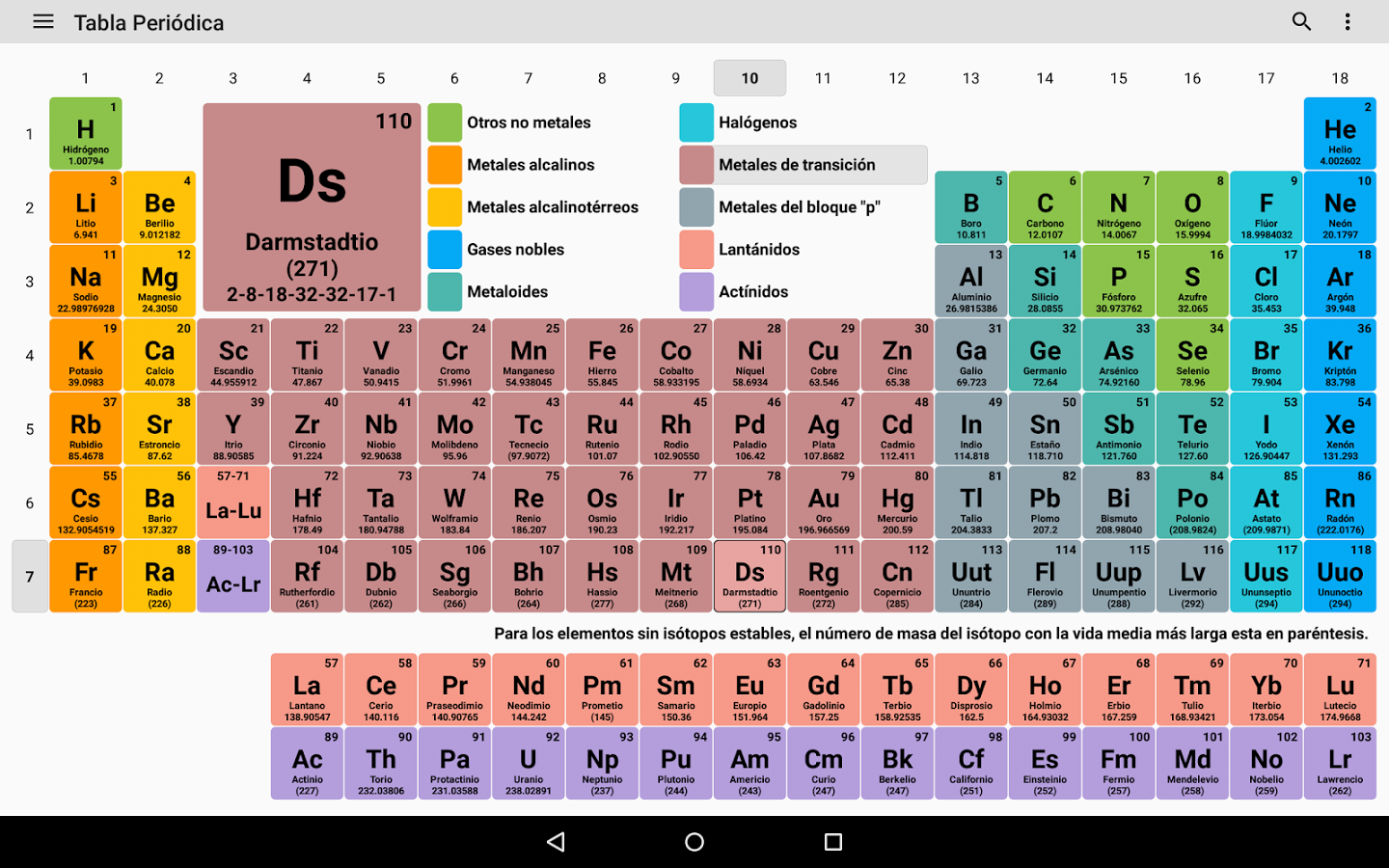 Следовательно, они демонстрируют меньшую металлическую природу [3] .
Следовательно, они демонстрируют меньшую металлическую природу [3] .