Доклад На Тему Периодическая Система Менделеева
Значение периодической системы Дмитрия Менделеева сложно переоценить, так как благодаря ей. Изучение таблицы легче всего дается тем людям, которые постоянно поддерживают мозг в тонусе, проходя тренинги на BrainApps. Выбор реферата. Рефераты по химии. Реферат: Периодическая система элементов Менделеева.. Готовясь к лекциям, собирая материал для своего учебника ‘Основы химии’, Д. Менделеев раздумывал над тем, как.
• • • Реферат: Периодическая система элементов. Периоды, группы, подгруппы. Периодический закон и его обоснование: Сочинский Государственный Университет туризма и курортного дела в г. Нижний Новгород Реферат Дисциплина: «Общая химия» Тема: «Периодическая система элементов. Периоды, группы, подгруппы. Периодический закон и его обоснование» Выполнил: студент гр. А 33 – 09 Филиппова А.С.
Проверил: ______________ Нижний Новгород 2009 План 1. Основная часть: 2.1 История открытия периодического закона и периодической системы элементов; 2. 2 Периодический закон и периодическая система элементов; 2.3 Структура периодической системы: периоды, группы, подгруппы; 2.4 Периодический закон и его обоснование; 3. Список используемой литературы. «Будут появляться и умирать новые теории, блестящие обобщения. Новые представления будут сменять наши уже устаревшие понятия об атоме и электроне. Величайшие открытия и эксперименты будут сводить на нет прошлое и открывать на сегодня невероятные по новизне и широте горизонты – всё это будет приходить и уходить, но Периодический закон Менделеева будет всегда жить и руководить исканиями».
2 Периодический закон и периодическая система элементов; 2.3 Структура периодической системы: периоды, группы, подгруппы; 2.4 Периодический закон и его обоснование; 3. Список используемой литературы. «Будут появляться и умирать новые теории, блестящие обобщения. Новые представления будут сменять наши уже устаревшие понятия об атоме и электроне. Величайшие открытия и эксперименты будут сводить на нет прошлое и открывать на сегодня невероятные по новизне и широте горизонты – всё это будет приходить и уходить, но Периодический закон Менделеева будет всегда жить и руководить исканиями».
Академик А.Е. Введение Мне захотелось попробовать раскрыть эту тему и посмотреть на неё со стороны дилетанта в вопросах химии, так как меня заинтересовал сам процесс создания Дмитрием Ивановичем Менделеевым периодической системы химических элементов. Меня постоянно удивляет внутренний потенциал человеческого организма, в частности, мозга. Замечательно то, что Дмитрий Иванович не только предсказал существование новых элементов, но и описал их свойства. Я считаю, что Периодический закон и Периодическая система химических элементов Д.И. Менделеева является основой современной химии.
Я считаю, что Периодический закон и Периодическая система химических элементов Д.И. Менделеева является основой современной химии.
Они относятся к таким научным закономерностям, которые отражают явления, реально существующие в природе, и поэтому никогда не потеряют своего значения. Открытие периодического закона и периодической системы химических элементов было подготовлено всем ходом истории развития химии, однако потребовалась гениальность Дмитрия Ивановича, его дар научного предвидения, чтобы эти закономерности были сформулированы и графически представлены в виде таблицы.
Основная часть 2.1 История открытия периодического закона и периодической системы химических элементов Утверждение атомно-молекулярной теории на рубеже XIIX – XIXвеков сопровождалось бурным ростом числа известных химических элементов. Только за первое десятилетие 19 века было открыто 14 новых элементов. Рекордсменом среди первооткрывателей оказался английский химик Гемфри Деви, который за один год с помощью электролиза получил 6 новых простых веществ (натрий, калий, магний, кальций, барий, стронций). А к 1830 году число известных элементов достигло 55. Существование такого количества элементов, разнородных по своим свойствам, озадачивало химиков и требовало упорядочения и систематизации элементов.
А к 1830 году число известных элементов достигло 55. Существование такого количества элементов, разнородных по своим свойствам, озадачивало химиков и требовало упорядочения и систематизации элементов.Многие учёные занимались поисками закономерностей в списке элементов и добивались определённого прогресса. Можно выделить три наиболее значительные работы, которые оспаривали приоритет открытия периодического закона у Д.И. В 1860 году состоялся первый Международный химический конгресс, после которого стало ясно, что основной характеристикой химического элемента является его атомный вес.
Французский учёный Б. Де Шанкуртуа в 1862 году впервые расположил элементы в порядке возрастания атомных весов и разместил их по спирали вокруг цилиндра.
Каждый виток спирали содержал 16 элементов, сходные элементы, как правило, попадали в вертикальные столбцы, хотя были отмечены и значительные расхождения. Работа де Шанкуртуа осталась незамеченной, но выдвинутая им идея сортировки элементов в порядке возрастания атомных весов оказалась плодотворной.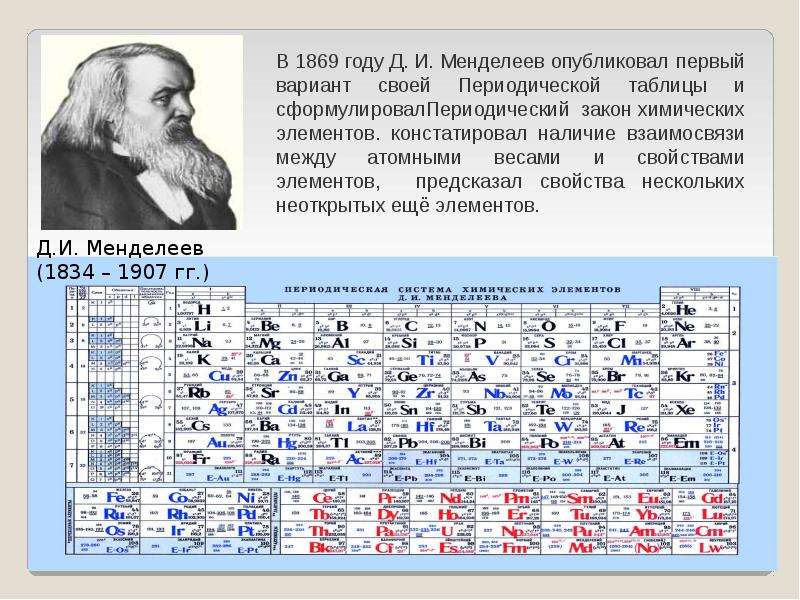 И двумя годами позже, руководствуясь этой идеей, английский химик Джон Ньюлендс разместил элементы в виде таблицы и заметил, что свойства элементов периодически повторяются через каждые семь номеров. Например, хлор по свойствам похож на фтор, калий – на натрий, селен – на серу и т.д. Данную закономерность Ньюлендс назвал «законом октав», практически опередив понятие периода.
И двумя годами позже, руководствуясь этой идеей, английский химик Джон Ньюлендс разместил элементы в виде таблицы и заметил, что свойства элементов периодически повторяются через каждые семь номеров. Например, хлор по свойствам похож на фтор, калий – на натрий, селен – на серу и т.д. Данную закономерность Ньюлендс назвал «законом октав», практически опередив понятие периода.
Но Ньюлендс настаивал на том, что длина периода (равная семи) является неизменной, поэтому его таблица содержит не только правильные закономерности, но и случайные пары (кобальт – хлор, железо – сера и углерод – ртуть). А вот немецкий учёный Лотар Мейер в 1870 году построил график зависимости атомного объёма элементов от их атомного веса и обнаружил отчётливую периодическую зависимость, причём длина периода не совпадала с законом октав и была переменной величиной. Во всех этих работах много общего.
Де Шанкуртуа, Ньюлендс и Мейер открыли проявление периодичности изменения свойств элементов в зависимости от их атомного веса. Но они не смогли создать единую периодическую систему всех элементов, поскольку в открытых ими закономерностях многие элементы не находили своего места. Никаких серьёзных выводов из своих наблюдений этим учёным так же сделать не удалось, хотя они чувствовали, что многочисленные соотношения между атомными весами элементов являются проявлением какого-то общего закона. Этот общий закон был открыт великим русским химиком Дмитрием Ивановичем Менделеевым в 1869 году.
Но они не смогли создать единую периодическую систему всех элементов, поскольку в открытых ими закономерностях многие элементы не находили своего места. Никаких серьёзных выводов из своих наблюдений этим учёным так же сделать не удалось, хотя они чувствовали, что многочисленные соотношения между атомными весами элементов являются проявлением какого-то общего закона. Этот общий закон был открыт великим русским химиком Дмитрием Ивановичем Менделеевым в 1869 году.
Менделеев сформулировал периодический закон в виде следующих основных положений: 1. Элементы, расположенные по величине атомного веса, представляют явственную периодичность свойств. Должно ожидать открытия ещё многих неизвестных простых тел, например, сходных с Al и Si элементов с атомным весом 65 – 75. Величина атомного веса элемента иногда может быть исправлена, зная его аналогии. Некоторые аналогии открываются по величине веса их атома.
Первое положение было известно ещё до Менделеева, но именно он придал ему характер всеобщего закона, предсказав на его основе существование ещё не открытых элементов, изменив атомные веса ряда элементов и расположив некоторые элементы в таблице вопреки их атомным весам, но в полном соответствии с их свойствами (главным образом, валентностью).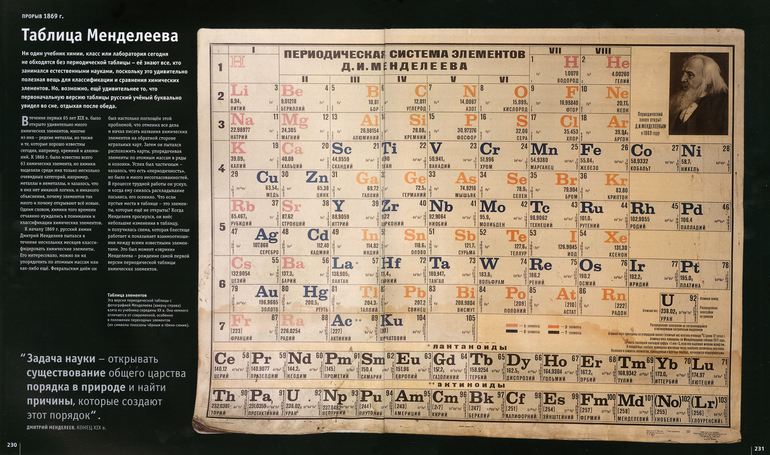 Остальные положения открыты только Менделеевым и являются логическими следствиями из периодического закона. Правильность этих следствий подтверждалась многими опытами в течение последующих двух десятилетий и позволила говорить о периодическом законе как о строгом законе природы. Используя эти положения, Менделеев составил свой вариант периодической системы элементов. Первый черновой набросок таблицы элементов появился 17 февраля (1 марта по новому стилю) 1869 года. А 6 марта 1869 года официальное сообщение об открытии Менделеева сделал профессор Меншуткин на заседании Русского химического общества. В уста учёного вложили такую исповедь: Вижу во сне таблицу, где все элементы расставлены, как нужно.
Остальные положения открыты только Менделеевым и являются логическими следствиями из периодического закона. Правильность этих следствий подтверждалась многими опытами в течение последующих двух десятилетий и позволила говорить о периодическом законе как о строгом законе природы. Используя эти положения, Менделеев составил свой вариант периодической системы элементов. Первый черновой набросок таблицы элементов появился 17 февраля (1 марта по новому стилю) 1869 года. А 6 марта 1869 года официальное сообщение об открытии Менделеева сделал профессор Меншуткин на заседании Русского химического общества. В уста учёного вложили такую исповедь: Вижу во сне таблицу, где все элементы расставлены, как нужно.
Проснулся, тотчас записал на клочке бумаги – только в одном месте впоследствии оказалась нужной поправка». Как всё просто в легендах! На разработку и поправку ушло более 30 лет жизни учёного. Процесс открытия периодического закона поучителен и сам Менделеев рассказывал об этом так: «Невольно зародилась мысль о том, что между массой и химическими свойствами необходимо должна быть связь. А так как масса вещества, хотя и не абсолютная, а лишь относительная, выражается окончательно в виде весов атомов, то надо искать функциональное соответствие между индивидуальными свойствами элементов и их атомными весами. Искать же что – либо, хотя бы грибы или какую-нибудь зависимость, нельзя иначе, как смотря и пробуя. Вот я и стал подбирать, написав на отдельных карточках элементы с их атомными весами и коренными свойствами, сходные элементы и близкие атомные веса, что быстро и привело к тому заключению, что свойства элементов стоят в периодической зависимости от их атомного веса, причём, сомневаясь во многих неясностях, я ни минуты не сомневался в общности сделанного вывода, так как случайность допустить не возможно».
А так как масса вещества, хотя и не абсолютная, а лишь относительная, выражается окончательно в виде весов атомов, то надо искать функциональное соответствие между индивидуальными свойствами элементов и их атомными весами. Искать же что – либо, хотя бы грибы или какую-нибудь зависимость, нельзя иначе, как смотря и пробуя. Вот я и стал подбирать, написав на отдельных карточках элементы с их атомными весами и коренными свойствами, сходные элементы и близкие атомные веса, что быстро и привело к тому заключению, что свойства элементов стоят в периодической зависимости от их атомного веса, причём, сомневаясь во многих неясностях, я ни минуты не сомневался в общности сделанного вывода, так как случайность допустить не возможно».
В самой первой таблицы Менделеева все элементы до кальция включительно – такие же, как и в современной таблице, за исключением благородных газов. Это можно увидеть по фрагменту страницы из статьи Д.И.
Менделеева, содержащей периодическую систему элементов. Если исходить из принципа увеличения атомных весов, то следующими элементами после кальция должны были быть ванадий (А = 51), хром (А = 52) и титан (А = 52). Но Менделеев поставил после кальция знак вопроса, а следом поместил титан, изменив его атомный вес с 52 до 50. Неизвестному элементу, обозначенному знаком вопроса, был приписан атомный вес А = 45, являющийся средним арифметическим между атомными весами кальция и титана. Затем, между цинком и мышьяком Менделеев оставил место сразу для двух ещё не открытых элементов.
Если исходить из принципа увеличения атомных весов, то следующими элементами после кальция должны были быть ванадий (А = 51), хром (А = 52) и титан (А = 52). Но Менделеев поставил после кальция знак вопроса, а следом поместил титан, изменив его атомный вес с 52 до 50. Неизвестному элементу, обозначенному знаком вопроса, был приписан атомный вес А = 45, являющийся средним арифметическим между атомными весами кальция и титана. Затем, между цинком и мышьяком Менделеев оставил место сразу для двух ещё не открытых элементов.
Кроме того, он поместил теллур перед йодом, хотя последний имеет меньший атомный вес. При таком расположении элементов все горизонтальные ряды в таблице содержали только сходные элементы, и отчётливо проявлялась периодичность изменения свойств элементов. В последующие два года Менделеев значительно усовершенствовал систему элементов. В 1871 году вышло первое издание учебника Дмитрия Ивановича «Основы химии», в котором приведена периодическая система в почти современном виде.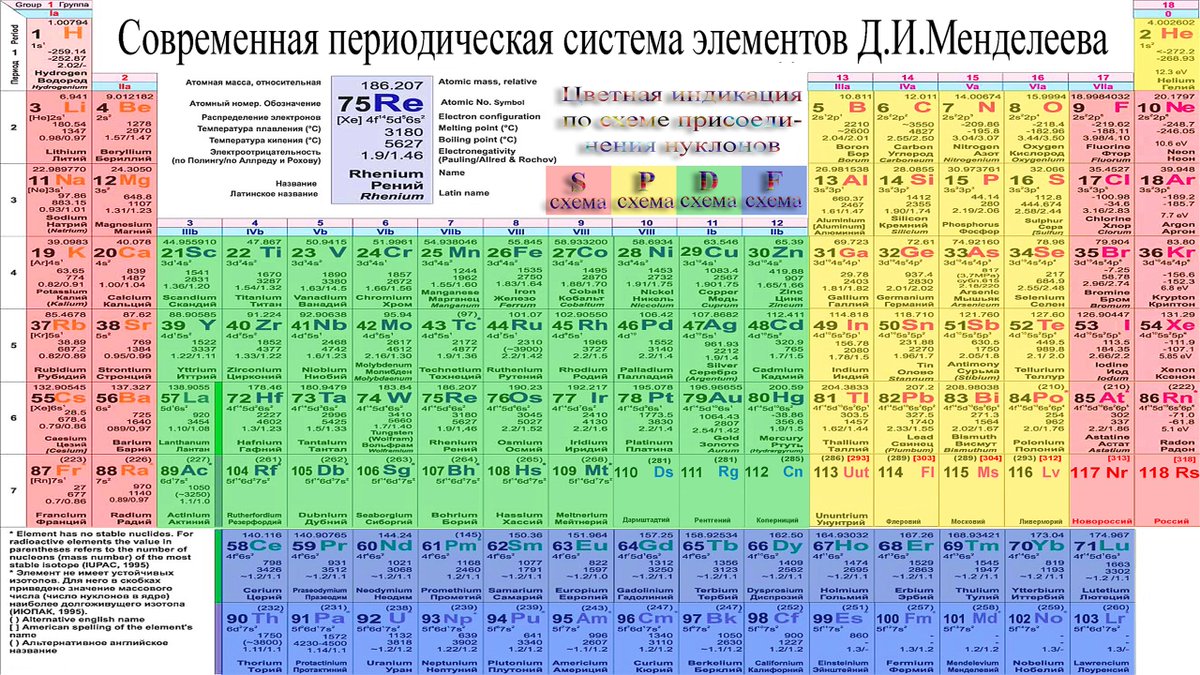 В таблице образовалось 8 групп элементов, номера групп указывают на высшую валентность элементов тех рядов, которые включены в эти группы, и периоды становятся более близкими к современным, разбитые на 12 рядов. Теперь каждый период начинается активным щелочным металлом и заканчивается типичным неметаллом галогеном. Второй вариант системы дал возможность Менделееву предсказать существование не 4, а 12 элементов и, бросая вызов учёному миру, с изумительной точностью описал свойства трёх неизвестных элементов, которые он назвал экабор (эка на санскрите означает «одно и то же»), экаалюминий и экасилиций.
В таблице образовалось 8 групп элементов, номера групп указывают на высшую валентность элементов тех рядов, которые включены в эти группы, и периоды становятся более близкими к современным, разбитые на 12 рядов. Теперь каждый период начинается активным щелочным металлом и заканчивается типичным неметаллом галогеном. Второй вариант системы дал возможность Менделееву предсказать существование не 4, а 12 элементов и, бросая вызов учёному миру, с изумительной точностью описал свойства трёх неизвестных элементов, которые он назвал экабор (эка на санскрите означает «одно и то же»), экаалюминий и экасилиций.
Современные названия их Se, Ga, Ge. Учёный мир Запада в начале отнёсся к Менделеевской системе и его предсказаниям скептически, но всё изменилось, когда в 1875 году французский химик П. Лекок де Буабодран, исследуя спектры цинковой руды, обнаружил следы нового элемента, который он назвал галлием в честь своей родины (Галлия – древнеримское название Франции). Учёному удалось выделить этот элемент в чистом виде и изучить его свойства. А Менделеев увидел, что свойства галлия совпадают со свойствами предсказанного им экаалюминия, и сообщил Лекок де Буабодрану, что тот неверно измерил плотность галлия, которая должна быть равна 5,9-6,0 г/см 3вместо 4,7 г/см 3. И действительно, более аккуратные измерения привели к правильному значению 5,904 г/см 3. В 1879 году шведский химик Л.
А Менделеев увидел, что свойства галлия совпадают со свойствами предсказанного им экаалюминия, и сообщил Лекок де Буабодрану, что тот неверно измерил плотность галлия, которая должна быть равна 5,9-6,0 г/см 3вместо 4,7 г/см 3. И действительно, более аккуратные измерения привели к правильному значению 5,904 г/см 3. В 1879 году шведский химик Л.
Нильсон при разделении редкоземельных элементов, полученных из минерала гадолинита, выделил новый элемент и назвал его скандием. Это оказывается предсказанный Менделеевым экабор. Окончательного признания периодический закон Д.И. Менделеева добился после 1886 года, когда немецкий химик К. Винклер, анализируя серебряную руду, получил элемент, который он назвал германием. Это оказывается экасицилий.
2.2 Периодический закон и периодическая система химических элементов Периодический закон – один из важнейших законов химии. Менделеев считал, что главной характеристикой элемента является его атомная масса. Поэтому он расположил все элементы в один ряд в порядке увеличения их атомной массы.
Если рассмотреть ряд элементов от Li до F, то можно увидеть, что металлические свойства элементов ослабляются, а неметаллические свойства усиливаются. Аналогично изменяются и свойства элементов в ряду от Na до Cl. Следующий знак К, как Li и Na, является типичным металлом. Высшая валентность элементов увеличивается от IyLi до VyN (кислород и фтор имеют постоянную валентность, соответственно II и I) и от IyNa до VIIyCl. Следующий элемент К, как Li и Na, имеет валентность I. В ряду оксидов от Li 2O до N 2O 5и гидроксидов от LiОН до HNO 3основные свойства ослабляются, а кислотные свойства усиливаются.
Аналогично изменяются свойства оксидов в ряду от Na 2O и NaOH до Cl 2O 7и HClO 4. Оксид калия К 2О, как и оксиды лития и натрия Li 2O и Na 2O, является основным оксидом, а гидроксид калия КОН, как и гидроксиды лития и натрия LiOH и NaOH, является типичным основанием.
Аналогично изменяются формы и свойства неметаллов от CH 4до HF и от SiH 4до HCl. Такой характер свойств элементов и их соединений, какой наблюдается при увеличении атомной массы элементов, называется периодическим изменением. Свойства всех химических элементов при увеличении атомной массы изменяются периодически. Это периодическое изменение называется периодической зависимостьюсвойств элементов и их соединений от величины атомной массы. Менделеев сформулировал открытый им закон так: Свойства элементов, а так же формы и свойства соединений элементов находятся в периодической зависимости от величины атомной массы элементов. Менделеев расположил периоды элементовдруг под другом и в результате составил периодическую систему элементов. Он говорил, что таблица элементов – плод не только его собственного труда, но и усилий многих химиков, среди которых он особо отмечал «укрепителей периодического закона», открывших предсказанные им элементы. Для создания современной таблицы потребовалась напряженная многолетняя работа тысяч и тысяч химиков и физиков.
Свойства всех химических элементов при увеличении атомной массы изменяются периодически. Это периодическое изменение называется периодической зависимостьюсвойств элементов и их соединений от величины атомной массы. Менделеев сформулировал открытый им закон так: Свойства элементов, а так же формы и свойства соединений элементов находятся в периодической зависимости от величины атомной массы элементов. Менделеев расположил периоды элементовдруг под другом и в результате составил периодическую систему элементов. Он говорил, что таблица элементов – плод не только его собственного труда, но и усилий многих химиков, среди которых он особо отмечал «укрепителей периодического закона», открывших предсказанные им элементы. Для создания современной таблицы потребовалась напряженная многолетняя работа тысяч и тысяч химиков и физиков.
Если бы Менделеев был сейчас жив, он, глядя на современную таблицу элементов, вполне мог бы повторить слова английского химика Дж.У.Меллора, автора классической 16-томной энциклопедии по неорганической и теоретической химии.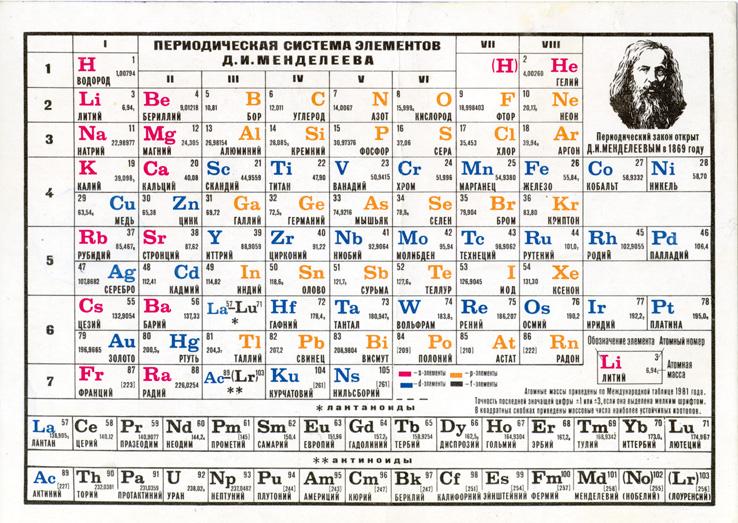 Закончив в 1937, после 15-летней работы, свой труд, он написал с признательностью на титульном листе: «Посвящается рядовым огромной армии химиков. Их имена забыты, их работы остались».
Закончив в 1937, после 15-летней работы, свой труд, он написал с признательностью на титульном листе: «Посвящается рядовым огромной армии химиков. Их имена забыты, их работы остались».
Периодическая система –это классификация химических элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра. Система является графическим выражением периодического закона.
На октябрь 2009 года известно 117 химических элементов (с порядковыми номерами с 1 по 116 и 118), из них 94 обнаружены в природе (некоторые — лишь в следовых количествах). Остальные23 получены искусственно в результате ядерных реакций – это процесс превращения атомных ядер, происходящий при их взаимодействии с элементарными частицами, гамма-квантами и друг с другом, обычно приводящий к выделению колоссального количества энергии. Первые 112 элементов имеют постоянные названия, остальные — временные. Открытие 112-го элемента (самый тяжелый из официальных) признано Международным союзом теоретической и прикладной химии. Самый стабильный из известных изотопов данного элемента имеет период полураспада 34 секунды.
Самый стабильный из известных изотопов данного элемента имеет период полураспада 34 секунды.На начало июня 2009 года носит неофициальное имя унунбий, был впервые синтезирован в феврале 1996 года на ускорителе тяжелых ионов в Институте тяжелых ионов в Дармштадте, Германия (в результате бомбардировки свинцовой мишени ядрами цинка). Первооткрыватели имеют полгода, чтобы предложить новое официальное название для добавления в таблицу (ими уже предлагались Виксхаузий, Гельмгольций, Венусий, Фриший, Штрассманий и Гейзенбергий). В настоящее время известны трансурановые элементы с номерами 113-116 и 118, полученные в Объединенном институте ядерных исследований в Дубне, однако они официально пока не признаны. Распространённее других являются 3 формы таблицы Менделеева: «короткая» (короткопериодная), «длинная» (длиннопериодная) и «сверхдлинная». В «сверхдлинном» варианте каждый период занимает ровно одну строчку. В «длинном» варианте лантаноиды (семейство из 14 химических элементов с порядковыми номерами 58—71, расположенных в VI периоде системы) и актиноиды (семейство радиоактивных химических элементов, состоящее из актиния и 14 подобных ему по своим химическим свойствам) вынесены из общей таблицы, делая её более компактной.
В «короткой» форме записи, в дополнение к этому, четвёртый и последующие периоды занимают по 2 строчки; символы элементов главных и побочных подгрупп выравниваются относительно разных краёв клеток. Короткая форма таблицы, содержащая восемь групп элементов, была официально отменена ИЮПАК в 1989 году. Несмотря на рекомендацию использовать длинную форму, короткая форма продолжила приводиться в большом числе российских справочников и пособий и после этого времени. Из современной иностранной литературы короткая форма исключена полностью, вместо неё используется длинная форма. Такую ситуацию некоторые исследователи связывают, в том числе с кажущейся рациональной компактностью короткой формы таблицы, а также со стереотипностью мышления и невосприятием современной (международной) информации. В 1969 году Теодор Сиборг предложил расширенную периодическую таблицу элементов. Нильсом Бором разрабатывалась лестничная (пирамидальная) форма периодической системы.
Существует и множество других, редко или вовсе не используемых, но весьма оригинальных, способов графического отображения Периодического закона. Сегодня существуют несколько сот вариантов таблицы, при этом учёные предлагают всё новые варианты. 2.3 Структура периодической системы: периоды, группы, подгруппы Итак, мы выяснили, что периодическая система – это графическое выражение периодического закона. Каждый элемент занимает определённое место (клетку) в периодической системе и имеет свой порядковый (атомный) номер. Например: Символ элемента Порядковый (атомный) номер (Z) Относительная атомная Русское название масса (А 1) элемента Горизонтальные ряды элементов, в пределах которых свойства элементов изменяются последовательно, Менделеев назвал периодами(начинаются щелочным металлом (Li, Na, K, Rb, Cs, Fr) и заканчиваются благородным газом (He, Ne, Ar, Kr, Xe, Rn)). Исключения: первый период, который начинается водородом и седьмой период, который является незавершённым. Периоды разделяются на малыеи большие.
Сегодня существуют несколько сот вариантов таблицы, при этом учёные предлагают всё новые варианты. 2.3 Структура периодической системы: периоды, группы, подгруппы Итак, мы выяснили, что периодическая система – это графическое выражение периодического закона. Каждый элемент занимает определённое место (клетку) в периодической системе и имеет свой порядковый (атомный) номер. Например: Символ элемента Порядковый (атомный) номер (Z) Относительная атомная Русское название масса (А 1) элемента Горизонтальные ряды элементов, в пределах которых свойства элементов изменяются последовательно, Менделеев назвал периодами(начинаются щелочным металлом (Li, Na, K, Rb, Cs, Fr) и заканчиваются благородным газом (He, Ne, Ar, Kr, Xe, Rn)). Исключения: первый период, который начинается водородом и седьмой период, который является незавершённым. Периоды разделяются на малыеи большие.
Малые периоды состоят из одногогоризонтального ряда. Первый, второй и третий периоды являются малыми, в них находится 2 элемента (1-й период) или 8 элементов (2-й, 3-й периоды). Большие периоды состоят из двух горизонтальных рядов.
Большие периоды состоят из двух горизонтальных рядов.
Четвёртый, пятый и шестой периоды являются большими, в них находятся 18 элементов (4-й, 5-й периоды) или 32 элемента (6-й, 7-й период). Верхние рядыбольших периодов называются чётными, нижние ряды – нечётными. В шестом периоде лантаноиды и в седьмом периоде актиноиды располагаются в нижней части периодической системы. В каждом периоде слева направо металлические свойства элементов ослабевают, а неметаллические свойства усиливаются. В чётных рядах больших периодов находятся только металлы. В результате в таблице имеется 7 периодов, 10 рядов и 8 вертикальных столбцов, названных группами –это совокупность элементов, которые имеют одинаковую высшую валентность в оксидах и в других соединениях. Эта валентность равна номеру группы.
Исключения: Номер группы Элемент Высшая валентность I Cu Ag Au II III III VI O II VII H F I I В VIII группе только Ru и Os имеют высшую валентность VIII. Группы – вертикальные последовательности элементов, они нумеруется римской цифрой от I до VIII и русскими буквами А и Б.
Каждая группа состоит из двух подгрупп: главной и побочной. Главная подгруппа – А, содержит элементы малых и больших периодов. Побочная подгруппа – В, содержит элементы только больших периодов. В них входят элементы периодов, начиная с четвёртого. В главных подгруппах сверху вниз металлические свойства усиливаются, а не металлические свойства ослабляются. Все элементы побочных подгрупп являются металлами. 2.4 Периодический закон и его обоснование Периодический закон позволил привести в систему и обобщить огромный объем научной информации в химии.
Эту функцию закона принято называть интегративной.Особо четко она проявляется в структурировании научного и учебного материала химии. Ферсман говорил, что система объединила всю химию в рамки единой пространственной, хронологической, генетической, энергетической связи. Интегративная роль Периодического закона проявилась и в том, что некоторые данные об элементах, якобы выпадавшие из общих закономерностей, были проверены и уточнены как самим автором, так и его последователями. Так случилось с характеристиками бериллия. До работы Менделеева его считали трехвалентным аналогом алюминия из-за их так называемого диагонального сходства. Таким образом, во втором периоде оказывалось два трехвалентных элемента и ни одного двухвалентного. Именно на этой стадии Менделеев заподозрил ошибку в исследованиях свойств бериллия, он нашел работу российского химика Авдеева, утверждавшего, что бериллий двухвалентен и имеет атомный вес 9.
Так случилось с характеристиками бериллия. До работы Менделеева его считали трехвалентным аналогом алюминия из-за их так называемого диагонального сходства. Таким образом, во втором периоде оказывалось два трехвалентных элемента и ни одного двухвалентного. Именно на этой стадии Менделеев заподозрил ошибку в исследованиях свойств бериллия, он нашел работу российского химика Авдеева, утверждавшего, что бериллий двухвалентен и имеет атомный вес 9.
Работа Авдеева оставалась не замеченной ученым миром, автор рано скончался, по-видимому, получив отравление чрезвычайно ядовитыми бериллиевыми соединениями. Результаты исследования Авдеева утвердились в науке благодаря Периодическому закону. Такие изменения и уточнения значений и атомных весов, и валентностей были сделаны Менделеевым еще для девяти элементов (In, V, Th, U, La, Ce и трех других лантаноидов). Еще у десяти элементов были исправлены только атомные веса.
И все эти уточнения впоследствии были подтверждены экспериментально. Прогностическая(предсказательная) функция Периодического закона получила самое яркое подтверждение в открытии неизвестных элементов с порядковыми номерами 21, 31 и 32. Их существование сначала было предсказано на интуитивном уровне, но с формированием системы Менделеев с высокой степенью точности смог рассчитать их свойства. Хорошо известная история открытия скандия, галлия и германия явилась триумфом менделеевского открытия. Он все предсказания делал на основе им же самим открытого всеобщего закона природы. Всего же Менделеевым были предсказаны двенадцать элементов. С самого начала Менделеев указал, что закон описывает свойства не только самих химических элементов, но и множества их соединений.
Прогностическая(предсказательная) функция Периодического закона получила самое яркое подтверждение в открытии неизвестных элементов с порядковыми номерами 21, 31 и 32. Их существование сначала было предсказано на интуитивном уровне, но с формированием системы Менделеев с высокой степенью точности смог рассчитать их свойства. Хорошо известная история открытия скандия, галлия и германия явилась триумфом менделеевского открытия. Он все предсказания делал на основе им же самим открытого всеобщего закона природы. Всего же Менделеевым были предсказаны двенадцать элементов. С самого начала Менделеев указал, что закон описывает свойства не только самих химических элементов, но и множества их соединений.
Для подтверждения этого достаточно привести такой пример. С 1929 г., когда академик П.
Капица впервые обнаружил неметаллическую проводимость германия, во всех странах мира началось развитие учения о полупроводниках. Сразу стало ясно, что элементы с такими свойствами занимают главную подгруппу IV группы. Со временем пришло понимание, что полупроводниковыми свойствами должны в большей или меньшей мере обладать соединения элементов, расположенных в периодах равно удаленной от этой группы (например, с общей формулой типа АзВ).
Со временем пришло понимание, что полупроводниковыми свойствами должны в большей или меньшей мере обладать соединения элементов, расположенных в периодах равно удаленной от этой группы (например, с общей формулой типа АзВ).
Это сразу сделало поиск новых практически важных полупроводников целенаправленным и предсказуемым. На таких соединениях основывается практически вся современная электроника.
Важно отметить, что предсказания в рамках Периодической системы делались и после ее всеобщего признания. Мозли обнаружил, что длина волн рентгеновских лучей, которые получены от антикатодов, сделанных из разных элементов, изменяется закономерно в зависимости от порядкового номера, условно присвоенного элементам в Периодической системе. Эксперимент подтвердил, что порядковый номер элемента имеет прямой физический смысл. Лишь позднее порядковые номера были связаны со значением положительного заряда ядра. Зато закон Мозли позволил сразу экспериментально подтвердить число элементов в периодах и вместе с тем предсказать места еще не открытых к тому времени гафния (№ 72) и рения (№ 75).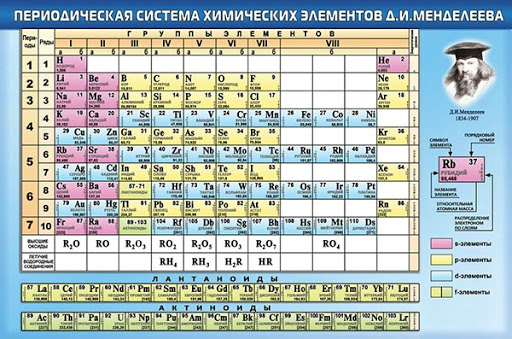 , а за ним и другие соединения газов, которые теперь правильнее называть благородными, а не инертными. Свою предсказательную функцию периодический закон сохраняет и до наших дней. Нужно отметить, что предсказания неизвестных членов любого множества могут быть двух видов. Если предсказываются свойства элемента, находящегося внутри известного ряда себе подобных, то такое предсказание носит название интерполяции.Можно предположить, что эти свойства будут подчинены тем же закономерностям, что и свойства соседних элементов.
, а за ним и другие соединения газов, которые теперь правильнее называть благородными, а не инертными. Свою предсказательную функцию периодический закон сохраняет и до наших дней. Нужно отметить, что предсказания неизвестных членов любого множества могут быть двух видов. Если предсказываются свойства элемента, находящегося внутри известного ряда себе подобных, то такое предсказание носит название интерполяции.Можно предположить, что эти свойства будут подчинены тем же закономерностям, что и свойства соседних элементов.
Так были предсказаны свойства недостающих элементов внутри периодической таблицы. Гораздо труднее предвидеть характеристики новых членов множеств, если они находятся за пределами описанной части. Экстраполяция —предсказание значений функции, находящихся за пределами ряда известных закономерностей, — всегда носит менее определенный характер. Искусственно синтезированный Еиенном Теодором Сиборгом и его сотрудниками элемент № 101 получил название «менделевий».
Сам Сиборг об этом сказал так: «Особенно существенно отметить, что элемент 101 назван в честь великого русского химика Д. Менделеева американскими учеными, которые всегда считали его пионером в химии».
Менделеева американскими учеными, которые всегда считали его пионером в химии».
Выводы Открытие периодического закона и разработка периодической системы химических элементов Д.И. Менделеевым явились вершиной развития химии ХIX века, стала важнейшей вехой в развитии атомно-молекулярного учения. Благодаря ей сложилось современное понятие о химическом элементе, были уточнены представления о простых веществах и соединениях. Обширная сумма знаний о свойствах 63 элементов, известных к тому времени, была приведена в стройный порядок. Так же можно сказать, что периодический закон является началом эпохи современной химии. Изучение строения атомов вскрывает физический смысл периодического закона и объясняет закономерности изменения свойств элементов в периодах и в группах периодической системы. Знание строения атомов явилось необходимым для понимания причин образования химической связи, а природа химической связи в молекулах определила свойства веществ.
Периодическую систему по праву называют «компасом для исследователя, путеводной нитью в области химии, физики, минералогии, технике, таблицей истории и мироздания». Академик Ферсман неоднократно подчёркивал, что периодический закон помогает поискам и разведке полезных ископаемых, так как место химического элемента в периодической системе тесно связано с местом того же элемента в самой природе, его реальным местом нахождением. Возможность предсказания свойств элементов и их соединений по положению элемента в периодической системе широко использовалась и используется в различных областях промышленности техники для решения разнообразных проблем, связанных с созданием новых материалов с определёнными, заранее заданными свойствами. Таким образом: появление периодической системы открыло новую, подлинно научную эру в истории химии и ряде смежных наук — взамен разрозненных сведений об элементах и соединениях появилась стройная система, на основе которой стало возможным обобщать, делать выводы, предвидеть. Периодический закон и сделанные на его основе открытия в различных областях естествознания и техники являются величайшим триумфом человеческого разума, свидетельством всё более глубокого проникновения в самые сокровенные тайны природы, успешного преобразования природы на благо человека.
Академик Ферсман неоднократно подчёркивал, что периодический закон помогает поискам и разведке полезных ископаемых, так как место химического элемента в периодической системе тесно связано с местом того же элемента в самой природе, его реальным местом нахождением. Возможность предсказания свойств элементов и их соединений по положению элемента в периодической системе широко использовалась и используется в различных областях промышленности техники для решения разнообразных проблем, связанных с созданием новых материалов с определёнными, заранее заданными свойствами. Таким образом: появление периодической системы открыло новую, подлинно научную эру в истории химии и ряде смежных наук — взамен разрозненных сведений об элементах и соединениях появилась стройная система, на основе которой стало возможным обобщать, делать выводы, предвидеть. Периодический закон и сделанные на его основе открытия в различных областях естествознания и техники являются величайшим триумфом человеческого разума, свидетельством всё более глубокого проникновения в самые сокровенные тайны природы, успешного преобразования природы на благо человека.
«Общая химия», Москва, изд. «Интеграл – пресс», 2002 г. «Актуальные вопросы курса неорганической химии», Москва, изд. «Просвещение», 1991 г.
Макареня А.А., Рысев Ю.В, «Д.И. Менделеев», Москва, изд. «Просвещение», 1988 г. «Репетитор по химии», Ростов-на-Дону, изд.
«Феникс», 2006 г. Кузьменко Н.Е., Ерёмин В.В., Попков В.А. «Начала химии», Москва, изд.
«Экзамен», 2004 г. «Большая школьная энциклопедия. 2., Москва, изд. «ОЛМА – Пресс», 1999 г. Я познаю мир: Детская энциклопедия: Химия, Москва, изд.
«АСТ – ЛТД», 1988 г. 9 класс: Учеб. Для общеобразоват.
– 3-е изд., стереотип. – Москва, изд. «Дрофа», 2000 г.
Первый вариант Периодической таблицы элементов был опубликован Д. Менделеевым в 1869 году – задолго до того, как было изучено строение атома. В это время Менделеев преподавал химию в Петербургском университете. Готовясь к лекциям, собирая материал для своего учебника ‘Основы химии’, Д. Менделеев раздумывал над тем, как систематизировать материал таким образом, чтобы сведения о химических свойствах элементов не выглядели набором разрозненных фактов.
Менделеевым в 1869 году – задолго до того, как было изучено строение атома. В это время Менделеев преподавал химию в Петербургском университете. Готовясь к лекциям, собирая материал для своего учебника ‘Основы химии’, Д. Менделеев раздумывал над тем, как систематизировать материал таким образом, чтобы сведения о химических свойствах элементов не выглядели набором разрозненных фактов.
Ориентиром в этой работе Д. Менделееву послужили атомные массы (атомные веса) элементов. После Всемирного конгресса химиков в 1860 году, в работе которого участвовал и Д. Менделеев, проблема правильного определения атомных весов была постоянно в центре внимания многих ведущих химиков мира, в том числе и Д. Располагая элементы в порядке возрастания их атомных весов, Д. Менделеев обнаружил фундаментальный закон природы, который теперь известен как Периодический закон: Свойства элементов периодически изменяются в соответствии с их атомным весом. Приведенная формулировка нисколько не противоречит современной, в которой понятие ‘атомный вес’ заменено понятием ‘заряд ядра’.
Ядро состоит из протонов и нейтронов. Число протонов и нейтронов в ядрах большинства элементов примерно одинаково, поэтому атомный вес увеличивается примерно так же, как увеличивается число протонов в ядре (заряд ядра Z). Принципиальная новизна Периодического закона заключалась в следующем: 1.
Устанавливалась связь между НЕСХОДНЫМИ по своим свойствам элементами. Эта связь заключается в том, что свойства элементов плавно и примерно одинаково изменяются с возрастанием их атомного веса, а затем эти изменения ПЕРИОДИЧЕСКИ ПОВТОРЯЮТСЯ.
В тех случаях, когда создавалось впечатление, что в последовательности изменения свойств элементов не хватает какого-нибудь звена, в Периодической таблице предусматривались ПРОБЕЛЫ, которые надо было заполнить еще не открытыми элементами. Во всех предыдущих попытках определить взаимосвязь между элементами другие исследователи стремились создать законченную картину, в которой не было места еще не открытым элементам. Менделеев считал важнейшей частью своей Периодической таблицы те ее клеточки, которые оставались пока пустыми. Это давало возможность предсказать существование еще неизвестных элементов. Достойно восхищения, что свое открытие Д.
Это давало возможность предсказать существование еще неизвестных элементов. Достойно восхищения, что свое открытие Д.
Менделеев сделал в то время, когда атомные веса многих элементов были определены весьма приблизительно, а самих элементов было известно всего 63 – то есть чуть больше половины известных нам сегодня. В свою Периодическую таблицу, опубликованную в марте 1869 года, Д. Менделеев поместил элементов больше, чем было открыто к тому времени! Глубокое знание химических свойств различных элементов позволило Менделееву не только указать на еще не открытые элементы, но и точно предсказать их свойства! Менделеев точно предсказал свойства элемента, названного им ‘эка-силицием’. Спустя 16 лет этот элемент действительно был открыт немецким химиком Винклером и назван германием.
Сопоставление свойств, предсказанных Д. Менделеевым для еще не открытого элемента ‘эка-силиция’ со свойствами элемента германия (Ge). В современной Периодической таблице германий занимает место ‘эка-силиция’. Бесплатно скачать реферат ‘Периодическая система элементов Менделеева’ в полном объеме.
Бесплатно скачать реферат ‘Периодическая система элементов Менделеева’ в полном объеме.
• • • • • • • • • • • • • • • • • • • • • • • • • • • • • 1. Переміщенням акорду називається його повторення в зміненому вигляді; переміщення міняє мелодичне положення або розташування акорду – або і то і інше одночасно. Зміна мелодичного. Как ранее было отмечено, к полимерам относятся многочисленные природные соединения: белки, нуклеиновые кислоты, целлюлоза, крахмал, каучук и другие органические вещества. Твердые топлива, используемые как источник энергии и сырье для химического производства, подразделяются на топлива естественного происхождения – природные – и топлива искусственные. Крім виглядів і розрізів на робочих кресленнях досить часто застосовують перерізи.
За їх допомогою у тому чи іншому місці виявляють поперечну форму деталі. Суть цього способу наочн. Поверхность – это геометрическое место линии, движущейся в пространстве по определённому закону.
Эту линию называют образующей.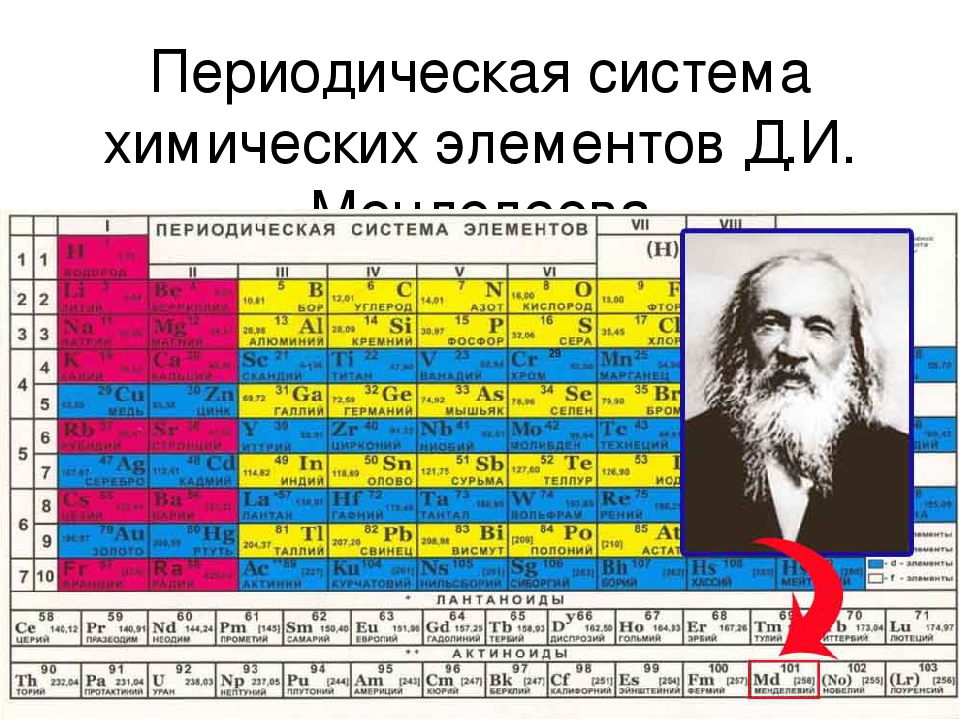 Она может быть прямой, тогда образованную ей поверхн.
Она может быть прямой, тогда образованную ей поверхн.
Промисловий потенціал України формувався диспропорційно: посилювалися і розширювалися традиційно індустріальні райони — Донбас і Придніпров’я, а промисловість досить густо заселено. Перикл, настраивая свою речь, как музыкальный инструмент, в тон этому укладу жизни и высокому образу мыслей, во многих случаях пользовался Анаксагором, примешивая понемногу как бы. В целях проведения анализа экономического положения стран мира эксперты, как правило, используют ряд важных индикаторов, характеризующих динамику и состояние мировой экономики. Заполнение атомных орбиталей электронами определяется правилом минимума энергии, принципом Паули и правилом Хунда.
Электроны заполняют атомные орбитали, начиная с подуровня с мень. Первые попытки классификации элементов относятся к концу 18-началу 19 вв. Особенно же богат работами в этой области 19 век, что связано с открытием и исследованием многих новых эле.
Реферат: Периодическая система элементов Менделеева Первый вариант Периодической таблицы элементов был опубликован Д.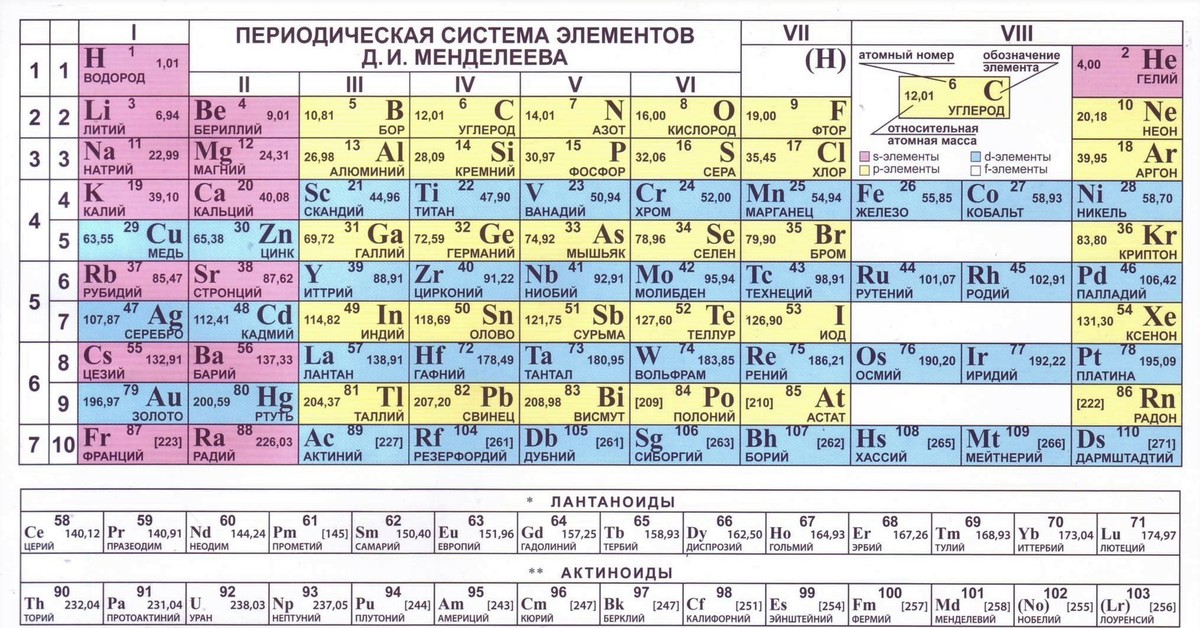 Менделеевым в 1869 году – задолго до того, как было изучено строение атома. В это время Менделеев преподавал хи. Открытие периодического закона и разработка периодической системы химических элементов Д.
Менделеевым в 1869 году – задолго до того, как было изучено строение атома. В это время Менделеев преподавал хи. Открытие периодического закона и разработка периодической системы химических элементов Д.
Античність увійшла в історію етичної науки як початок її становлення. Тут уперше була зроблена спроба вирішення моральних проблем, а також обгрунтування власне проблеми моральності. Перша частина Новітньої історії – період з 1914 по 1939 рік – один з найскладніших у всесвітній історії. Це час і нечуваного технічного прогресу в розвинутих країнах світу, і морал. Возможны три случая проецирования прямого угла: 1. Если обе стороны прямого угла прямые общего положения, то прямой угол проецируется искаженно на все три плоскости проекций. Кроме прямых линий общего положения, в плоскости отмечают три главные линии: горизонтальную (горизонталь), фронтальную (фронталь) и линию наибольшего наклона.
Кроме прямых линий общего положения, в плоскости отмечают три главные линии: горизонтальную (горизонталь), фронтальную (фронталь) и линию наибольшего наклона.
Эти линии применяют. Найбільш важливим елементом продуктивних сил і головним джерелом розвитку економіки є люди; їх майстерність, освіта, підготовка, мотивація діяльності. Існує непересічна залежність. До основних форм активізації навчального процесу належать: проведення семінарів, «круглих столів», тестування, ділових ігор, тренінгів, застосування опорних сигналів тощо [1, 2]. Легка промисловість є однією з найважливіших серед галузей виробництва непродовольчих товарів.
Продукція легкої промисловості йде на задоволення потреб населення, забезпечуючи його. Несмотря на сложную финансовую ситуацию, на многих предприятиях ведут реконструкцию и техническое переоснащение производства, внедряют новые виды высококачественной продукции в сов.
Тест с ответами на тему: Периодическая система элементов Д.И. Менделеева
1. Сколько химических элементов было известно к моменту открытия Периодического закона?
а) 18 б)32 в) 63 г)98
2. Кто впервые разделил все элементы на металлы и неметаллы?
а) Менделеев б) Берцелиус в) Аристотель г) Томсон
3. На чем основана классификация элементов в Периодической системе?
а) относительные атомные массы элементов б) количество электронов в)название элемента
г) количество нейтронов
3. У каких элементов наиболее ярко выражены металлические свойства?
а) галогены б) металлы побочных подгрупп в) щелочные металлы г) инертные газы
4. Кислотные свойства в периоде увеличиваются
а) не увеличиваются б) изменяются периодически в) справа налево г) слева направо
5. Как изменяются основные свойства в группе сверху вниз?
а) увеличиваются б) уменьшаются в) не изменяются г) изменяются периодически
6. В каком ряду элементов усиляются неметаллические свойства?
7. Чем отличаются друг от друга изотопы одного и того же элемента?
а) массовым числом б) зарядом ядра в) номером в таблице г) числом электронов
8.
 Порядковый номер химического элемента не показывает
Порядковый номер химического элемента не показываета) заряд ядра атома б) количество нейтронов в) количество протонов г) количество электронов
9. Радиус атома увеличивается
а) в группе снизу вверх б) в периоде слева направо в) диагонально г) в периоде справа налево
10. Что означает слово «атом» в переводе с греческого?
а) неделимый б) единственный в) нейтральный г) маленький
11. Какая структура атома была предложена Томсоном?
12. Кто предложил планетарную модель атома?
а) Эйнштейн б) Томсон в) Резерфорд г) Бор
13. В каком году Бор внес квантовые представления в строение атома?
а) 1913 б) 1911 в) 1915 г) 1905
14. Какая орбиталь имеет сферическую форму?
а) s б) p в) d г) f
15. Какую форму имеет р-обиталь?
а) сферическую б) объемного цветка в) шара г) гантели
16. Какое максимальное число электронов может находиться на 3-м энергетическом уровне?
а) 9 б) 32 в) 8 г) 18
17.
 Чему равно значение главного квантового числа?
Чему равно значение главного квантового числа?18. Какое квантовое число может принимать отрицательные целые значения?
а) магнитное б) орбитальное в) спиновое г) главное
19. Какое квантовое число может принимать только 2 значения?
а) побочное б) главное в) орбитальное г) спиновое
20. В каком атоме полностью завершен второй электронный слой?
а) O б) P в) F г) C
21. Какой элемент не является p-элементом?
а) As б) Ca в) I г) Al
22. Чем определяется валентность атома?
а) зарядом ядра б) числом электронов на внешнем уровне в) числом неспаренных электронов г) числом энергетических уровней
23. Какая валентность не может быть у атома S?
24. Какова максимальная валентность у атома С?
а) 3 б) 2 в) 6 г)4
25. В каком соединении N имеет наименьшую степень окисления?
а) KNO2 б) N2O в) HNO3 г) Nh4
26. В каком соединении металл имеет степень окисления +3?
а) K[AL(OH)4] б) Mg3N2 в) B2O3 г) Na2ZnO2
27.
 Какое вещество является жидкостью?
Какое вещество является жидкостью?а) Cl2 б) I2 в) O2 г) Br2
28. Какое вещество не имеет металлического блеска?
а) I2 б) Hg в) Be г) S
29. В каком периоде меньше всего металлов?
а) 1 б) 2 в) 3 г) 4
30. В какой группе нет неметаллов?
а) 1 б) 2 в) 3 г) 8
1.в 16.г
2.б 17.б
3.а 18.а
4.г 19.г
5.а 20.б
6.г 21.б
7.а 22.в
8.б 23.б
9.г 24.г
10.а 25.г
11.б 26.а
12.в 27.г
13.а 28.г
14.а 29.а
15.г 30.б
система химэлементов вскоре будет носить имя Менделеева во всем мире
Источник: tass.ru2019 год провозглашен Генеральной ассамблеей ООН Международным годом Периодической таблицы химических элементов в честь 150-летия открытия Периодического закона химэлементов Дмитрием Менделеевым
САНКТ-ПЕТЕРБУРГ /ТАСС/. Периодическая таблица химических элементов вскоре получит имя Менделеева и на международном уровне, сообщил в четверг глава Минобрнауки России Михаил Котюков на Петербургском международном экономическом форуме.
“Было открытие международного года периодической таблицы химических элементов. Мы все ее знаем как таблицу Менделеева. В мире таблица пока имени собственного, к сожалению, не имеет, но мы считаем, что этот пробел точно может быть заполнен в самое ближайшее время”, – сказал Котюков.
Год Периодической таблицы
2019 год провозглашен Генеральной ассамблеей ООН Международным годом Периодической таблицы химических элементов в честь 150-летия открытия Периодического закона химических элементов Дмитрием Менделеевым. С инициативой о проведении Международного года выступили Российская академия наук, Российское химическое общество имени Д. И. Менделеева, Министерство науки и высшего образования РФ, российские и зарубежные ученые. Инициативу России поддержали зарубежные страны, международные научные организации, а также более 80 национальных академий наук и научных обществ.
 Официальное закрытие планируется провести в декабре в Японии.
Официальное закрытие планируется провести в декабре в Японии.
Международный год Периодической таблицы химических элементов проходит под эгидой ЮНЕСКО в нескольких странах мира. Намечено проведение научных конференций, тематических выставок, конкурсов молодых ученых. В России планируется проведение более 500 научно-популярных и образовательных мероприятий, направленных на привлечение внимания школьников, студентов и молодежи в целом к науке и ее достижениям.
Одним из ключевых событий Международного года станет XXI Менделеевский съезд по общей и прикладной химии, который состоится с 9 по 13 сентября 2019 в Санкт-Петербурге. Также в России планируется проведение нескольких международных конференций и симпозиумов, среди которых, например, Всероссийский съезд учителей и преподавателей химии в Москве, Международная Менделеевская олимпиада школьников в Санкт-Петербурге.
Международный год Периодической таблицы
Знаете ли вы, что 2019 год объявлен Генеральной Ассамблеей ООН Международным годом Периодической таблицы? А еще столу исполняется 150 лет.
Вот несколько способов, которыми NIST помогает праздновать.
Периодическая таблица, разработанная NIST
Кредит: Н. Ханачек/NIST
Кредит: Н.Ханачек/NIST
Загрузите версию периодической таблицы NIST для печати (в формате PDF).
Видео
Химик NIST Мелисса Филлипс об углероде
Физик NIST Джун Йе о стронции
Физик NIST Эндрю Ладлоу об иттербии
Физик NIST Олли Слэттери о цезии
Инженер NIST Стив Фельдман о Iron
Директор NIST Уолтер Копан об азоте
сообщений в блоге
Кредит:
Добро пожаловать/Shutterstock.
Бена П. Штейна
Это Международный год Периодической таблицы, и хотя меня (точно) обвиняли в том, что я фанат физики, я здесь, чтобы сказать вам, что эта знаменитая таблица касается не только физики, химии и других наук. Это также касается математики, инженерии и даже ненаучных областей знаний, включая историю, географию и происхождение слов. Опубликовано 28 мая 2019 г.
С.В. Кларк
Из всего множества полезных и интересных периодических таблиц в Интернете — периодических таблиц животных, овощей и минералов — и президентов США, приправ для хот-догов в венском чикагском стиле, объектов динамического управления сервером SQL и палео-продуктов — оригинальная Периодическая таблица элементов остается моей любимой.
Художественное исполнение элемента 117, теннессин.
Кредит: Квей-Ю Чу / Ливерморская национальная лаборатория Лоуренса
Майкл Э.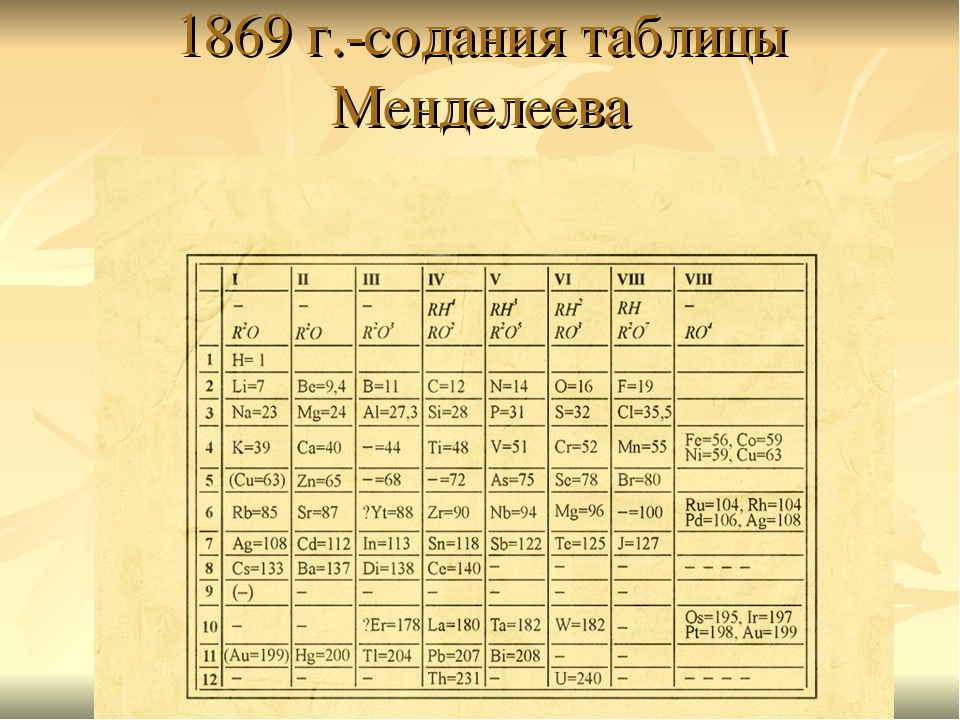 Ньюман
Ньюман
В случае, если вы еще не слышали, если вы хотели сделать своему любимому человеку этот особенный, единственный в жизни подарок, назвав один из элементов в строке 7 Периодической таблицы в его честь, уже слишком поздно ( и, вероятно, все равно против правил, но об этом позже). С недавно объявленными официальными названиями элементов с атомными номерами 113 (нихоний), 115 (московий), 117 (теннессин) и 118 (оганесон) полностью радиоактивный ряд 7 Периодической таблицы теперь завершен.Включены два (торий и уран), встречающиеся в природе, пять, которые возникают в результате радиоактивного распада других элементов, таких как всеми любимое топливо для кинематографической машины времени, плутоний, и 25, которые могут быть синтезированы только в лаборатории.
@NIST Твиттер-вечеринка
12 ноября мы устроили викторину в Твиттере в честь Международного года Периодической таблицы!
Ознакомьтесь с нашими вопросами, забавными подсказками и ответами, выполнив поиск в Твиттере по запросу #NISTrivia.
150 лет периодической таблицы
‘) var buybox = document.querySelector(“[data-id=id_”+ метка времени +”]”).parentNode ;[].slice.call(buybox.querySelectorAll(“.вариант-покупки”)).forEach(initCollapsibles) функция initCollapsibles(подписка, индекс) { var toggle = subscribe.querySelector(“.цена опциона на покупку”) подписка.classList.remove(“расширенный”) var form = подписка.querySelector(“.форма-варианта-покупки”) если (форма) { вар formAction = form.getAttribute(“действие”) form.setAttribute(“действие”, formAction.replace(“/checkout”, “/cart”)) document.querySelector(“#ecommerce-scripts”).addEventListener(“load”, bindModal(form, formAction, timestamp, index), false) } var priceInfo = подписка. селектор запросов(“.Информация о цене”)
var PurchaseOption = toggle.parentElement если (переключить && форма && priceInfo) {
toggle.setAttribute(“роль”, “кнопка”)
toggle.setAttribute(“tabindex”, “0”) toggle.addEventListener («щелчок», функция (событие) {
var expand = toggle.getAttribute(“aria-expanded”) === “true” || ложный
переключать.setAttribute(“расширенная ария”, !расширенная)
form.hidden = расширенный
если (! расширено) {
покупкаOption.classList.add(“расширенный”)
} еще {
покупкаOption.classList.remove(“расширенный”)
}
priceInfo.hidden = расширенный
}, ложный)
}
} функция bindModal (форма, formAction, метка времени, индекс) {
var weHasBrowserSupport = окно.
селектор запросов(“.Информация о цене”)
var PurchaseOption = toggle.parentElement если (переключить && форма && priceInfo) {
toggle.setAttribute(“роль”, “кнопка”)
toggle.setAttribute(“tabindex”, “0”) toggle.addEventListener («щелчок», функция (событие) {
var expand = toggle.getAttribute(“aria-expanded”) === “true” || ложный
переключать.setAttribute(“расширенная ария”, !расширенная)
form.hidden = расширенный
если (! расширено) {
покупкаOption.classList.add(“расширенный”)
} еще {
покупкаOption.classList.remove(“расширенный”)
}
priceInfo.hidden = расширенный
}, ложный)
}
} функция bindModal (форма, formAction, метка времени, индекс) {
var weHasBrowserSupport = окно. выборка && Array.from функция возврата () {
var Buybox = EcommScripts ? EcommScripts.Buybox : ноль
var Modal = EcommScripts ? EcommScripts.Modal : ноль
if (weHasBrowserSupport && Buybox && Modal) {
var modalID = “ecomm-modal_” + метка времени + “_” + индекс
var modal = новый модальный (modalID)
модальный.domEl.addEventListener(“закрыть”, закрыть)
функция закрыть () {
form.querySelector(“кнопка[тип=отправить]”).фокус()
} форма.setAttribute(
“действие”,
formAction.replace(“/checkout”, “/cart?messageOnly=1”)
)
форма.
выборка && Array.from функция возврата () {
var Buybox = EcommScripts ? EcommScripts.Buybox : ноль
var Modal = EcommScripts ? EcommScripts.Modal : ноль
if (weHasBrowserSupport && Buybox && Modal) {
var modalID = “ecomm-modal_” + метка времени + “_” + индекс
var modal = новый модальный (modalID)
модальный.domEl.addEventListener(“закрыть”, закрыть)
функция закрыть () {
form.querySelector(“кнопка[тип=отправить]”).фокус()
} форма.setAttribute(
“действие”,
formAction.replace(“/checkout”, “/cart?messageOnly=1”)
)
форма. добавить прослушиватель событий (
“представить”,
Buybox.interceptFormSubmit(
Buybox.fetchFormAction(окно.fetch),
Buybox.triggerModalAfterAddToCartSuccess(модальный),
консоль.лог,
),
ложный
)
документ.body.appendChild(modal.domEl)
}
}
} функция initKeyControls() {
document.addEventListener (“нажатие клавиши”, функция (событие) {
if (document.activeElement.classList.contains(“цена-варианта-покупки”) && (event.code === “Пробел” || event.code === “Enter”)) {
если (document.
добавить прослушиватель событий (
“представить”,
Buybox.interceptFormSubmit(
Buybox.fetchFormAction(окно.fetch),
Buybox.triggerModalAfterAddToCartSuccess(модальный),
консоль.лог,
),
ложный
)
документ.body.appendChild(modal.domEl)
}
}
} функция initKeyControls() {
document.addEventListener (“нажатие клавиши”, функция (событие) {
if (document.activeElement.classList.contains(“цена-варианта-покупки”) && (event.code === “Пробел” || event.code === “Enter”)) {
если (document. activeElement) {
мероприятие.предотвратить по умолчанию ()
документ.activeElement.click()
}
}
}, ложный)
} функция InitialStateOpen() {
var узкаяBuyboxArea = buybox.offsetWidth -1
;[].slice.call(buybox.querySelectorAll(“.опция покупки”)).forEach(функция (опция, индекс) {
var toggle = option.querySelector(“.цена опциона на покупку”)
var form = option.querySelector(“.форма-варианта-покупки”)
var priceInfo = option.querySelector(“.Информация о цене”)
если (allOptionsInitiallyCollapsed || узкаяBuyboxArea && индекс > 0) {
toggle.setAttribute («ария-расширенная», «ложь»)
form.hidden = “скрытый”
priceInfo.
activeElement) {
мероприятие.предотвратить по умолчанию ()
документ.activeElement.click()
}
}
}, ложный)
} функция InitialStateOpen() {
var узкаяBuyboxArea = buybox.offsetWidth -1
;[].slice.call(buybox.querySelectorAll(“.опция покупки”)).forEach(функция (опция, индекс) {
var toggle = option.querySelector(“.цена опциона на покупку”)
var form = option.querySelector(“.форма-варианта-покупки”)
var priceInfo = option.querySelector(“.Информация о цене”)
если (allOptionsInitiallyCollapsed || узкаяBuyboxArea && индекс > 0) {
toggle.setAttribute («ария-расширенная», «ложь»)
form.hidden = “скрытый”
priceInfo. hidden = “скрытый”
} еще {
переключать.щелчок()
}
})
} начальное состояниеОткрыть() если (window.buyboxInitialized) вернуть
window.buyboxInitialized = истина initKeyControls()
})()
hidden = “скрытый”
} еще {
переключать.щелчок()
}
})
} начальное состояниеОткрыть() если (window.buyboxInitialized) вернуть
window.buyboxInitialized = истина initKeyControls()
})()Год Периодической таблицы
02.11.2019
МЦТФ присоединился к празднованию Международного года Периодической таблицы химических элементов.Год был официально открыт в штаб-квартире ЮНЕСКО в Париже 29 января программой конференций и дискуссий, подчеркивающих актуальность Периодической таблицы для решения актуальных задач устойчивого развития общества в таких различных областях, как здравоохранение, продовольственная безопасность и энергетика.
Празднование включало в себя лекцию Бена Феринги, лауреата Нобелевской премии по химии 2016 года, а также презентацию последних синтезированных элементов Юрием Оганесяном, сыгравшим важную роль в синтезе и изучении самых тяжелых и новейших элементов из 104 до 118. Другие темы включали приложения для устойчивого развития, образовательную деятельность и происхождение элементов.
Другие темы включали приложения для устойчивого развития, образовательную деятельность и происхождение элементов.
Сандро Скандоло из секции конденсированных сред и статистической физики ICTP представлял ICTP на групповом заседании по периодической таблице и целям устойчивого развития. Его презентация продемонстрировала, как некоторые химические элементы играют центральную роль в исследованиях ICTP, и представила два новых воображаемых элемента Периодической таблицы: Educatium — «Ed» («нулевой элемент, основа всех наших знаний») и Researchium — «Rs». («элемент 119, будущее, неизвестность, что нас ждет впереди»).Подчеркнув важность этих двух элементов для основной миссии МЦТФ, он заявил: «Гарантировать надлежащий доступ к передовому образованию и исследованиям — это не роскошь, это необходимость, чтобы дать странам возможность сосредоточиться на своих собственных приоритетах».
В 2019 году исполняется 150 лет со дня открытия Дмитрием Менделеевым Периодической системы. В 1869 году Менделеев понял, что при упорядочении известных элементов по атомному весу определенные типы элементов встречаются регулярно. Эта система указывала на наличие связи между структурой элемента и его свойствами и показывала пробелы между известными элементами, что позволило Менделееву предсказать существование еще неизвестных элементов, что вскоре было подтверждено открытием галлия (1875 г.) , скандий (1879 г.) и германий (1887 г.).Периодическая таблица химических элементов остается одним из самых значительных достижений в науке, фиксируя суть не только химии, но и физики и биологии. Это уникальный инструмент, позволяющий ученым предсказывать появление и свойства материи на Земле и в остальной части Вселенной.
Эта система указывала на наличие связи между структурой элемента и его свойствами и показывала пробелы между известными элементами, что позволило Менделееву предсказать существование еще неизвестных элементов, что вскоре было подтверждено открытием галлия (1875 г.) , скандий (1879 г.) и германий (1887 г.).Периодическая таблица химических элементов остается одним из самых значительных достижений в науке, фиксируя суть не только химии, но и физики и биологии. Это уникальный инструмент, позволяющий ученым предсказывать появление и свойства материи на Земле и в остальной части Вселенной.
Международный год Периодической таблицы химических элементов проводится ЮНЕСКО совместно с Международным союзом теоретической и прикладной химии (IUPAC), Европейской ассоциацией химических и молекулярных наук (EuCheMS), Международным научным советом (ISC), Международный астрономический союз (IAU), Международный союз теоретической и прикладной физики (IUPAP) и Международный союз истории и философии науки и техники (IUHPST).
Редакционная статья: Празднование Международного года Периодической таблицы: после Менделеева 150
Периодическая таблица всех химических элементов впервые была разработана и графически отображена как всеобъемлющий закон природы русским ученым Дмитрием Менделеевым в марте 1869 г., за которым сразу последовал большой скачок в чистой и прикладной химии, физике и других естественных науках, а также в образовании. Периодическая таблица элементов охватывает большую часть предыдущих усилий других исследований по тому же предмету; это было убедительно подтверждено знаменитыми количественными графиками различных свойств элементов Юлиуса Лотара Мейера.За последние полтора века Периодическая таблица, несомненно, стала настоящей иконой химии, вдохновив многих ученых различных специальностей, философов, беллетристов и ученых-кормителей. Таким образом, он открыл новые захватывающие горизонты для инновационного устойчивого развития и улучшенных достижений человечества. Периодические таблицы стали неотъемлемой частью фундаментальных естественных наук, всех химических классов и даже популярной культуры и искусства во всем мире (Ball, 2019; Chapman, 2019; Düllmann, 2019; Goodilin et al. , 2019; Горбунова и др., 2019; Лиддл, 2019; Полякофф и др., 2019; Рэдфорд, 2019 г.; Рам и др., 2019; Рэмплинг, 2019; Шерри, 2019; Шайк и др., 2019).
, 2019; Горбунова и др., 2019; Лиддл, 2019; Полякофф и др., 2019; Рэдфорд, 2019 г.; Рам и др., 2019; Рэмплинг, 2019; Шерри, 2019; Шайк и др., 2019).
На этом фоне Генеральная Ассамблея Организации Объединенных Наций провозгласила Международный год Периодической таблицы химических элементов (МГПТ 2019) в ознаменование 150-летия открытия Природной системы химических элементов как одного из самых важных и влиятельных достижений. в современных науках. Это предоставило беспрецедентную возможность подчеркнуть непрерывный характер научных открытий в мирном и просвещенном мире.Успехи в исследованиях во многих различных контекстах были вызваны открытием Природной системы, что дало хорошую почву для признания важности химии в сотрудничестве с другими базовыми дисциплинами в мире, которому угрожают изменение климата и неограниченный рост населения.
Настоящий сборник тем исследований посвящен естественной системе элементов и ее различным представлениям в форме периодических таблиц, ее научным химическим и физическим основам, ее инновационным применениям в лабораторных исследованиях, ее передовым открытиям в области химической периодичности и группы элементов в передовых химических исследованиях, физике, химической технологии, материаловедении, катализе, науке об окружающей среде, фотогальванике и мемристорах.
Цао и др. рассматривают химические элементы в своем обзоре как «ядро», которое сохраняется при изменении веществ. Графические отображения химических свойств элементов в виде периодических таблиц были разработаны либо с целью классификации реальных химических веществ, либо с акцентом на формальные и эстетические концепции. Первые таблицы обычно включают типичные конфигурации валентных электронов связанных атомов в химических соединениях вместо обычных, но химически нетипичных основных состояний свободных атомов в физическом вакууме; основные химические свойства, такие как числа валентностей, размер и энергия валентных оболочек с их совместным изменением по элементам, проявляющим главную и вторичную периодичность; своеобразные элементы вверху и внизу периодической таблицы.Хотя очень важно, чтобы Периодические таблицы отображали важные тенденции в химии элементов, мы можем ожидать необычного химического поведения в окружающей среде, вблизи окружающей среды или в необычных условиях. Сочетание экспериментальных данных и теоретических знаний способствует более тонкому пониманию сложных периодических тенденций и непериодических явлений.
Сочетание экспериментальных данных и теоретических знаний способствует более тонкому пониманию сложных периодических тенденций и непериодических явлений.
В качестве примера богатого химического состава элементов и его ярко выраженного влияния на фундаментальные свойства и структурные корреляции современных материалов Белич и др.сравнить несколько революционных материалов на основе перовскитного типа кристаллических решеток, включая легендарные семейства высокотемпературных сверхпроводящих купратов, колоссальных магниторезистивных манганитов и гибридных галогенидов свинца для нового поколения солнечных элементов. Авторы демонстрируют, что широко распространенные кристаллические решетки перовскитов представляют собой естественную гибкую платформу для химического дизайна различных перспективных функциональных материалов с уникальными свойствами. Взаимодействие между химической связью, дефектами и особенностями кристаллохимии делает структуру перовскита «конструктором лего», использующим естественные свойства химических элементов.
Несколько авторов представили свои идеи, продвигающие важные классы материалов и наноматериалов из семейства C, Si, Ti, Sn, Pb элементов IV группы классической формы Периодической таблицы. Навроцкая и др. описывает глубоко модифицированные одномерные углеродные наноматериалы, уделяя особое внимание гибридным наноматериалам с уникальными механическими, электрическими, тепловыми и оптическими характеристиками. Среди них особое внимание привлекают гибриды на основе нитевидных форм углерода, таких как углеродные нанотрубки и углеродные нановолокна, в сочетании с неорганическими наночастицами.Из-за структуры и морфологии процессы передачи заряда и энергии приводят к синергетическим эффектам, которые позволяют использовать меньше материалов с более высокой производительностью, включая их экологические применения.
Морозова и др. обсудить важный класс кремниевых наноматериалов — квантовые точки. Авторы отмечают, что широко известные кремниевые квантовые точки (SiQD), полупроводниковые наночастицы Si размером от 1 до 10 нм, по-прежнему имеют большой прикладной потенциал для оптоэлектронных устройств и флуоресцентных биомаркирующих агентов. Их гораздо более высокая биосовместимость по сравнению с обычными токсичными квантовыми точками на основе металлов групп II-VI и III-V делает их практическое применение еще более привлекательным для предотвращения загрязнения окружающей среды и предотвращения повреждения живых организмов.
Их гораздо более высокая биосовместимость по сравнению с обычными токсичными квантовыми точками на основе металлов групп II-VI и III-V делает их практическое применение еще более привлекательным для предотвращения загрязнения окружающей среды и предотвращения повреждения живых организмов.
Оксидные производные кремния составляют особый класс стеклянных материалов. В частности, Шахгильдян и соавт. поделился точкой зрения о том, что стекло является единственным материалом, который может представлять внутри себя почти все элементы Периодической таблицы, демонстрируя влияние Периодического закона на свойства конечного материала.Авторы впервые воспроизвели периодическую таблицу в двулучепреломляющих цветах в объеме кварцевого стекла, используя технику прямой лазерной записи.
Очень важные и технологически значимые олигосилоксаны обсуждаются Rabanzo-Castillo et al. В частности, полезность (C 6 F 5 ) 3 B(OH 2 ) в качестве катализатора для простых обсуждается экологически безопасный синтез олигосилоксанов непосредственно из гидросиланов. Авторы отмечают, что этот протокол предлагает несколько преимуществ по сравнению с другими методами синтеза силоксанов, таких как мягкие условия реакции, низкая загрузка катализатора и короткое время реакции с высокими выходами и чистотой, хотя такие реакции имеют довольно сложный механизм.С гидросиланом (R 3 SiH) в качестве единственного исходного материала судьба реакции в значительной степени зависит от образования силанола (R 3 SiOH) из R 3 SiH, поскольку эти два вещества подвергаются дегидросочетанию с образованием дисилоксана. товар. Получение силанола основано на модифицированной реакции Пирса-Рубинштайна. После получения силанола механизм включает ряд конкурирующих реакций с несколькими каталитически значимыми частицами, включающими воду, силан и силанол, взаимодействующими с кислотой Льюиса, и предпочтительный цикл реакции зависит от концентрации различных частиц в растворе.
Авторы отмечают, что этот протокол предлагает несколько преимуществ по сравнению с другими методами синтеза силоксанов, таких как мягкие условия реакции, низкая загрузка катализатора и короткое время реакции с высокими выходами и чистотой, хотя такие реакции имеют довольно сложный механизм.С гидросиланом (R 3 SiH) в качестве единственного исходного материала судьба реакции в значительной степени зависит от образования силанола (R 3 SiOH) из R 3 SiH, поскольку эти два вещества подвергаются дегидросочетанию с образованием дисилоксана. товар. Получение силанола основано на модифицированной реакции Пирса-Рубинштайна. После получения силанола механизм включает ряд конкурирующих реакций с несколькими каталитически значимыми частицами, включающими воду, силан и силанол, взаимодействующими с кислотой Льюиса, и предпочтительный цикл реакции зависит от концентрации различных частиц в растворе.
Родионов и др. описать улучшенный доступ к ожидаемым применениям диоксида титана и его производных для фотокаталитических систем. Представлены новые способы получения, конечные структурно-функциональные свойства слоистых гибридных производных диоксида титана как эффективного фотокатализатора получения водорода из водно-спиртового раствора. Гибридный фотокатализатор H 2 Nd 2 Ti 3 O 10 × BuNH 2 синтезирован твердофазным керамическим методом с последующим протонированием, интеркалированием метиламином и последующим замещением н-бутиламином.В то время как неинтеркалированные Pt-содержащие H 2 Nd 2 Ti 3 O 10 показали максимальную квантовую эффективность всего 2% в диапазоне 220–340 нм, эффективность для гибридных образцов достигала 23–52 %. Этот эффект может быть связан со значительным расширением межслоевого пространства, которое рассматривается как отдельная реакционная зона.
Представлены новые способы получения, конечные структурно-функциональные свойства слоистых гибридных производных диоксида титана как эффективного фотокатализатора получения водорода из водно-спиртового раствора. Гибридный фотокатализатор H 2 Nd 2 Ti 3 O 10 × BuNH 2 синтезирован твердофазным керамическим методом с последующим протонированием, интеркалированием метиламином и последующим замещением н-бутиламином.В то время как неинтеркалированные Pt-содержащие H 2 Nd 2 Ti 3 O 10 показали максимальную квантовую эффективность всего 2% в диапазоне 220–340 нм, эффективность для гибридных образцов достигала 23–52 %. Этот эффект может быть связан со значительным расширением межслоевого пространства, которое рассматривается как отдельная реакционная зона.
Кроме того, Voytovich et al. сравнить титанаты и их роль как фотокаталитических расщепляющих систем с аналогичным рядом гибридных ниобатов HCa 2 Nb 3 O 10 × RNH 2 , содержащих интеркалированные н-алкиламины (R = Me, Et, Pr, Bu, Нх, Ос). Особое внимание также уделялось возможному повышению фотокаталитической активности образцов за счет их модификации наночастицами Pt в качестве сокатализатора. Таким образом, модификация слоистых перовскитоподобных оксидов органическими веществами представляется эффективной стратегией управления их фотокаталитической активностью, которую можно применить к другим родственным фотокаталитическим материалам.
Особое внимание также уделялось возможному повышению фотокаталитической активности образцов за счет их модификации наночастицами Pt в качестве сокатализатора. Таким образом, модификация слоистых перовскитоподобных оксидов органическими веществами представляется эффективной стратегией управления их фотокаталитической активностью, которую можно применить к другим родственным фотокаталитическим материалам.
Илларионов и др. обзор современного мемристивного диоксида титана как одного из наиболее широко используемых материалов в приложениях резистивного переключения, включая память с произвольным доступом, нейроморфные вычисления, биогибридные интерфейсы и датчики.Функциональные мемристивные свойства тонких пленок диоксида титана сильно зависят от методов их обработки, включая синтез, изготовление и обработку после изготовления, поэтому авторы представляют обзор основных областей применения мемристивных устройств на основе TiO 2 .
В своем мини-обзоре Петров и Тарасов обобщают имеющиеся данные об уникальных свойствах реакционных полииодидных расплавов (РПМ), используемых для разработки нового типа технологий масштабируемого производства солнечных элементов нового поколения на основе гибридного галлоплюмбата перовскиты.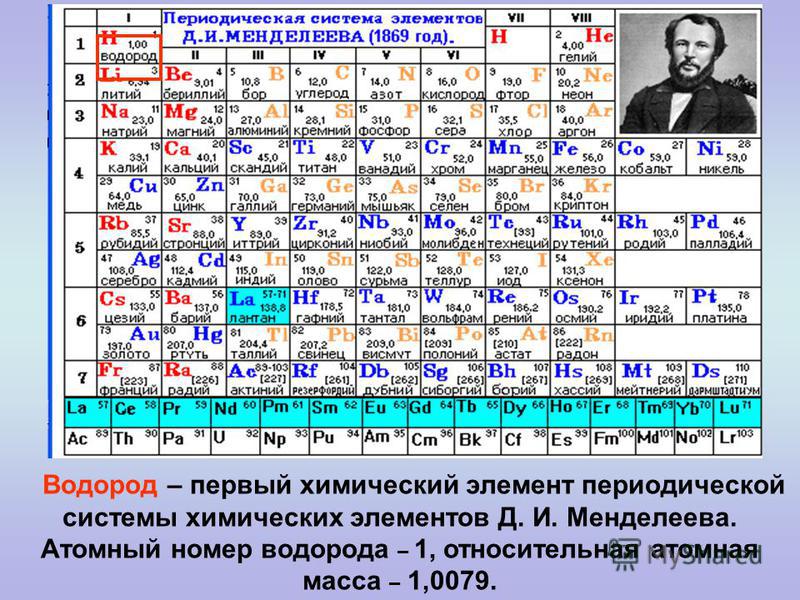 Авторы обсуждают потенциал RPM для изготовления гибридных перовскитных пленок и описывают роль полигалогенидов в деградации перовскитных солнечных элементов.
Авторы обсуждают потенциал RPM для изготовления гибридных перовскитных пленок и описывают роль полигалогенидов в деградации перовскитных солнечных элементов.
Еще один потенциальный кандидат для фотовольтаики на основе галостаннатов представлен в статье Умедова и др. Структура и свойства неорганического перовскита Cs 2 SnI 6 демонстрируют его потенциал в качестве материала для сбора света или переноса электронов и дырок. Авторы сообщают о способе легкой настройки абсорбционных и транспортных свойств йодостанната(IV) цезия Cs 2 SnI 6 путем частичного гетеровалентного замещения индия оловом.Поглощение света и оптическая ширина запрещенной зоны таких материалов были исследованы с помощью спектроскопии поглощения в УФ-видимой области спектра и фотолюминесцентной спектроскопии. Спектроскопия низкотемпературного электронного парамагнитного резонанса использовалась для изучения типа парамагнитных центров в этих материалах.
Еще одна область статей в этом сборнике тесно связана с f-элементами. Довольно оригинальный мини-обзор специалистов-радиохимиков Романчука и соавт. раскрыть некоторые важнейшие основные проблемы радиоэкологии.В обзоре кратко, но всесторонне анализируется очень сложная химия актинидов, их применение и использование. Среди них уран и плутоний являются наиболее важными, так как они используются в ядерном топливном цикле и производстве ядерного оружия, и поэтому обзор сосредоточен на последних экспериментальных, модельных и тематических достижениях в исследовании миграции плутония и урана в окружающей среде, включая видообразование этих элементов и химические реакции, контролирующие пути их миграции.
Довольно оригинальный мини-обзор специалистов-радиохимиков Романчука и соавт. раскрыть некоторые важнейшие основные проблемы радиоэкологии.В обзоре кратко, но всесторонне анализируется очень сложная химия актинидов, их применение и использование. Среди них уран и плутоний являются наиболее важными, так как они используются в ядерном топливном цикле и производстве ядерного оружия, и поэтому обзор сосредоточен на последних экспериментальных, модельных и тематических достижениях в исследовании миграции плутония и урана в окружающей среде, включая видообразование этих элементов и химические реакции, контролирующие пути их миграции.
Висентин и др. представил текущее состояние исследований газового переноса однозарядных ионов лантанидов и актинидов в свете потенциальных приложений к сверхтяжелым ионам. Корреляция потенциала ион-нейтрального взаимодействия и вариаций подвижности с пространственными параметрами распределения электронов в голых ионах исследуется в рамках концепции ионных радиусов. В то время как качественные тенденции, обнаруженные для потенциалов взаимодействия и подвижностей, делают их привлекательными для исследования сверхтяжелых ионов, недостаток экспериментальных данных и ограничения используемых скалярно-релятивистских подходов ab initio требуют дальнейших усилий, чтобы включить измерения переноса в список методов, работающих в режим «по одному атому за раз».
В то время как качественные тенденции, обнаруженные для потенциалов взаимодействия и подвижностей, делают их привлекательными для исследования сверхтяжелых ионов, недостаток экспериментальных данных и ограничения используемых скалярно-релятивистских подходов ab initio требуют дальнейших усилий, чтобы включить измерения переноса в список методов, работающих в режим «по одному атому за раз».
Наконец, Элькина и Курушкин написали исчерпывающий мини-обзор истории, различных синтезов и, возможно, всех известных применений искусственного элемента прометия. Ожидается, что мини-обзор станет окончательной отправной точкой для всех, кто интересуется изучением единственного химического элемента в ряду лантанидов, не имеющего стабильных изотопов.
В целом, Сборник обобщает различные новые достижения и тенденции в химии элементов периодической системы и, безусловно, полезен для химиков и практических исследователей в области материаловедения, а также устойчивой химии.
150 лет назад периодическая таблица навела порядок в химической вселенной
Почти незамеченным в углах бесчисленных классов по всему миру висит уникальное достижение ученого сибирского происхождения и основополагающий документ современной химии.
И в этом году ему нужно впихнуть много свечей в свой праздничный торт.
Да, периодической таблице элементов в этом году исполняется 150 лет. Полувековой юбилей вездесущего стола ознаменовался глобальными праздниками.Его хвалили в Париже и лебезили в журналах.
К чему вся эта суета?
Поскольку до того, как Дмитрий Менделеев изложил периодический закон, лежащий в основе его знаменитой таблицы, не было хорошего способа разобраться в быстро растущем списке элементов, из которых состоит вся нормальная материя во Вселенной.
Мэтт Боуман ведет курс органической химии для студентов бакалавриата в Ингрэм-холле. «Можно сказать, что мы воспринимаем периодическую таблицу как должное, — говорит Боумен. «Но я не мог представить себе химию без него.Фото: Лорен Джастис
При написании своего учебника «Основы химии» Менделеев искал логический способ организовать 64 элемента, известных науке того времени. Как и многие до него, Менделеев заметил, что некоторые элементы по своим химическим свойствам похожи друг на друга.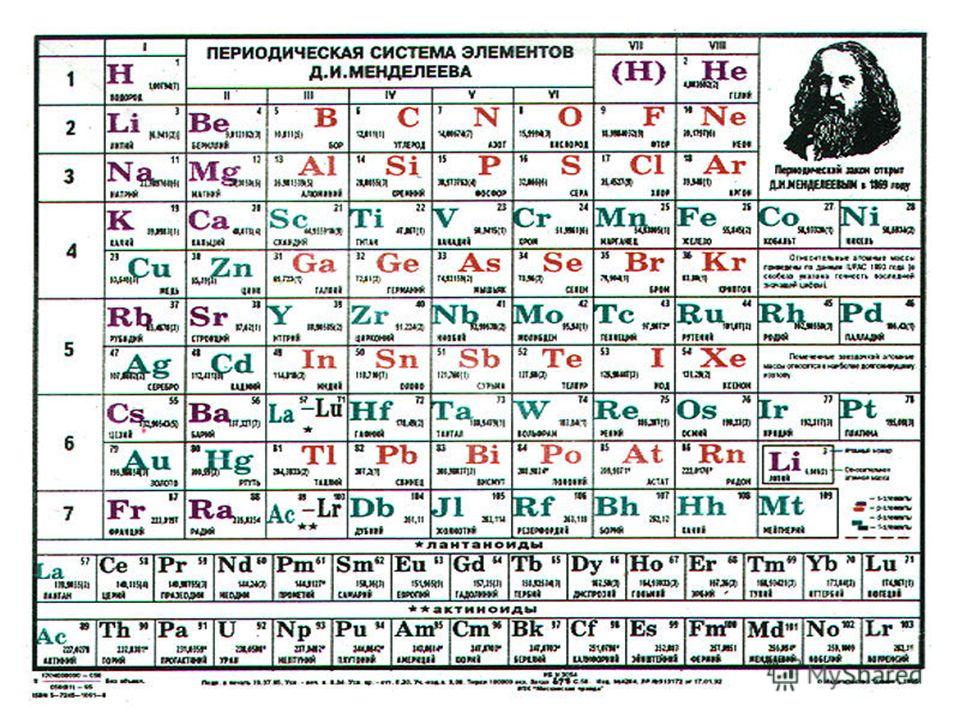 Упорядочив элементы по возрастанию атомного веса, он заметил периодическое повторение этих общих свойств. Он опубликовал свой периодический закон и табличный список элементов в 1869 году.
Упорядочив элементы по возрастанию атомного веса, он заметил периодическое повторение этих общих свойств. Он опубликовал свой периодический закон и табличный список элементов в 1869 году.
«Таблица Менделеева — великое интеллектуальное достижение, потому что она объединяет так много важных компонентов поведения элементов», — говорит Бассам Шахашири, профессор химии Университета Вашингтона в Мэдисоне и Университет Уильяма Т.Evjue Distinguished Chair for Wisconsin Idea. «Пришло время задуматься об этих открытиях».
Периодический закон позволил Менделееву предсказать существование и свойства неоткрытых элементов, которые в конечном итоге заполнили пробелы в его таблице. Открытие галлия и германия всего несколько лет спустя подтвердило его правоту и закрепило за ним место в истории химии.
Дмитрий Менделеев искал логический способ организовать 64 элемента, известных науке в то время.
«Как только эти элементы были открыты и их свойства оказались практически идентичными тому, что предсказывал Менделеев, это действительно побудило химиков постепенно превратить периодическую таблицу в икону, какой она является сегодня», — говорит Билл Дженсен, почетный профессор химия и историк химии в Университете Цинциннати, получивший степень бакалавра, магистра и доктора в Университете Вашингтона в Мэдисоне.
Но потребовалось еще несколько десятков лет, чтобы таблица Менделеева получила всемирное признание. В конце концов, это стало стандартом для организации элементов. Теперь таблица считается настолько логичным и фундаментальным устройством химической вселенной, что ее предложили в качестве способа общения с инопланетянами.
«Стол похож на носки, — говорит преподаватель химии Университета Вашингтона в Мэдисоне Мэтт Боуман. «Я носки использую каждый день, но не думаю о них сознательно. Таким образом, можно сказать, что мы принимаем периодическую таблицу как должное.Но я не мог представить себе химию без него».
В конце концов, открытие протонов и электронов изменило таблицу неуловимым, но важным образом. Менделеев первоначально упорядочил свою таблицу по атомному весу, но теперь таблица Менделеева упорядочена по атомному номеру, который относится к числу протонов в ядре атома. Протоны определяют количество электронов, находящихся вне ядра, которые, в свою очередь, контролируют свойства, которые так регулярно повторяются в каждом столбце таблицы.
Бассам Шахашири проводит ежегодную демонстрацию «Однажды на Рождество в лаборатории Шахашири» в 2009 году. Периодическая таблица видна в правом верхнем углу. Фото: Брайс Рихтер
За последние 150 лет стихия обрела множество приверженцев. В 2003 году Шахашири способствовал празднованию периодической таблицы, написав о свинце. В эссе он вспомнил дни, когда выкапывал свинцовые монеты давно умерших империй в своей родной стране Ливане. И, как писал Шахашири, древний металл породил талисман UW-Madison, потому что первые европейско-американские поселенцы территории Висконсин, как говорили, напоминали барсуков, когда они спали в вырытых вручную свинцовых шахтах.
Свинец также был особенным для автора и нейробиолога Оливера Сакса, который написал о своей глубокой связи с элементами, когда столкнулся с неизлечимой формой рака в 2015 году. Он собрал столько элементов, сколько смог, по одному на каждый год своей жизни. Мешки дожили до 82 лет, атомный номер свинца. Если бы он дожил до 83 лет, он бы достиг того, что он называл милым, непонятым висмутом, который стоял в его кабинете рядом со свинцом.
В этом году у Шахашири тоже юбилей. Он представит свою 50-ю ежегодную рождественскую лекцию «Однажды рождественское веселье в лаборатории Шахашири» в воскресенье, 12 декабря.1, в Центре исполнительских искусств Миддлтона.
Тема? Жесть, конечно. Атомный номер: 50.
Сатирик Том Лерер исполняет «Элементы» в Копенгагене, Дания, в 1967 году. Это его музыкальное исполнение таблицы Менделеева на мелодию Гилберта и Салливана «Я — образец современного генерал-майора».
Международный год периодической таблицы
Уроки периодической таблицы
Поскольку периодической таблице исполняется 150 лет, мы размышляем об историческом поиске новых элементов и рассматриваем тенденции использования элементов в некоторых ключевых областях исследований.
Внутриатомный заряд
В 1913 году были нарисованы лишь самые наброски строения атома.Фредерик Содди, хотя и пытался понять, как электрон мог вылететь из ядра при бета-распаде, поддержал выводы А. ван де Брока о том, что атомный номер элемента, а не его атомный вес, является фундаментальным параметром, определяющим химические свойства. Содди ввел слово «изотоп» для элементов, занимающих одно и то же место в периодической таблице и, следовательно, обладающих одинаковыми свойствами, но разной массой. Он также оспаривал «предварительную теорию Резерфорда» о том, что ядро имеет только положительный заряд.Неделей позже довольно возмущенный Эрнест Резерфорд ответил: ядро имеет «результирующий» положительный заряд, сказал он, и по мере того, как он уточнял, Резерфорд был мучительно близок к постулированию протона.
Конституция стихий
В 1919 году Фрэнсис Астон построил первый масс-спектрограф, способный измерять массы элементов с полезной точностью.К декабрю того же года он получил достаточно данных, чтобы предложить «правило целых чисел»: элементы представляют собой смеси изотопов, каждый из которых имеет массу, кратную одной двенадцатой массы углерода, или одна шестнадцатая массы кислорода. Провидческий вывод Астона: «Если это целочисленное отношение окажется общим, оно должно многое сделать для выяснения окончательной структуры материи».Блестящая история фотоокислительно-восстановительного катализа
За 10 лет фотоокислительно-восстановительный катализ превратился из лабораторной диковинки в промышленную основу. Внутренняя история о том, как это произошло и что будет дальше.
Внутренняя история о том, как это произошло и что будет дальше.Реклама |
За пределами периодической таблицы
Спустя 150 лет после того, как Менделеев упорядочил элементы по их характеристикам, в специальном выпуске исследуется непреходящее влияние этого научного шедевра.
Особенность новостей | | Природа
Новый период в охоте за сверхтяжелыми элементами
Периодическая таблица в том виде, в каком мы ее знаем, теперь кажется завершенной, ее нынешние 118 элементов хорошо укладываются в семь знакомых строк.Пределы ядерной массы и заряда
Добавление нихония, московия, теннессина и оганесона в периодическую таблицу напоминает о достижениях ядерной физики и химии.Витольд Назаревич обрисовывает в общих чертах будущие задачи в этой области.
Матрица Менделеева
Периодическая таблица Дмитрия Менделеева позволила ему систематизировать важнейшие химические данные.Но ее настоящий триумф состоялся как упражнение в теоретическом моделировании, позволившее предсказать открытие ранее неизвестных элементов.Наука и имидж | | Природа
Познакомьтесь с Дмитрием
Биография Менделеева выходит далеко за рамки его самого известного творения.Новое измерение для Менделеева
Спустя более века, что нового можно сказать о Периодической таблице? Простой вопрос такой обезоруживающей простоты, конечно, сигнализирует о том, что кто-то действительно хочет сказать что-то новое.
Комментарий | | Природа
Правила поведения за столом
Существует множество различных версий периодической таблицы, но одна из них доминирует. Мишель Франкл размышляет о том, почему химики помещают элементы в коробки.
Мишель Франкл размышляет о том, почему химики помещают элементы в коробки.Концы элементов
Когда элементы 117 и 118 будут наконец названы, должны ли эти новые члены семейств галогенов и инертных газов получить имена, оканчивающиеся на – или , как предложил ИЮПАК? Бретт Ф.Thornton и Shawn C. Burdette изучают историю суффиксов элементов и обосновывают несоблюдение этой рекомендации.- org/Person”> Бретт Ф. Торнтон и
- Шон С. Бёрдетт
Прямой допинг на изотопах
Столетие назад в этом месяце Фредерик Содди описал и назвал изотопы на страницах Nature . Brett F. Thornton и Shawn C. Burdette обсуждают, как химики рассматривали и использовали изотопы с тех пор — либо как химически идентичные, либо как химически отличные виды, в зависимости от потребности и технологий.
- Бретт Ф. Торнтон и
- Шон С. Бёрдетт
Элементы науки и фантастики
И ученые, и неученые давно мечтают об элементах с могучими свойствами. Возможно, придуманные ими вымышленные материалы не так далеки от реальности, как может показаться на первый взгляд.
Возможно, придуманные ими вымышленные материалы не так далеки от реальности, как может показаться на первый взгляд.Нейтронная звездная пыль и элементы Земли
С самого начала периодическая таблица сортировала элементы по весу, поэтому может показаться удивительным, что самый тяжелый природный элемент на Земле остается спорным или, в лучшем случае, туманным.В странных, возможно, незавершенных поисках этого самого тяжелого ядра единственный окончательный вывод заключается в том, что оно находится где-то за пределами урана.
- Бретт Ф. Торнтон и
- Шон С. Бёрдетт
Еще четыре кирпича в стене
Из всех вещей, которым люди могут дать имена, новые химические элементы — едва ли не самые редкие. Наша группа экспертов по периодической таблице пытается прочитать чайные листья и предсказать названия элементов 113, 115, 117 и 118.
Наша группа экспертов по периодической таблице пытается прочитать чайные листья и предсказать названия элементов 113, 115, 117 и 118.- Шон С. Бердетт,
- Филип Болл ⋯
- Бретт Ф. Торнтон
Что такое периодическая система инвентаризации и как она работает?
3 мин.Читать
- Ступица
- Бухгалтерский учет
- Что такое периодическая система инвентаризации и как она работает?
Система периодической инвентаризации — это форма оценки запасов, при которой учет запасов обновляется в конце отчетного периода, а не после каждой продажи и покупки.
Этот метод позволяет предприятию отслеживать начальные и конечные запасы в течение отчетного периода.
О чем рассказывается в этой статье:
ПРИМЕЧАНИЕ. Члены группы поддержки FreshBooks не являются сертифицированными специалистами по подоходному налогу или бухгалтерскому учету и не могут давать советы в этих областях, за исключением вопросов поддержки о FreshBooks.Если вам нужна консультация по подоходному налогу, свяжитесь с бухгалтером в вашем районе .
Как работает система периодической инвентаризации?
В системе периодической инвентаризации не ведется непрерывный учет изменений. Годовые закупки запасов регистрируются в счете покупок, который представляет собой бухгалтерскую книгу, в которой перечислены все закупки запасов и их затраты.
Дебет | Кредит | |
Покупки | ххх | |
Кредиторская задолженность | ххх |
В конце года проводится инвентаризация для определения конечного остатка запасов и себестоимости проданных товаров.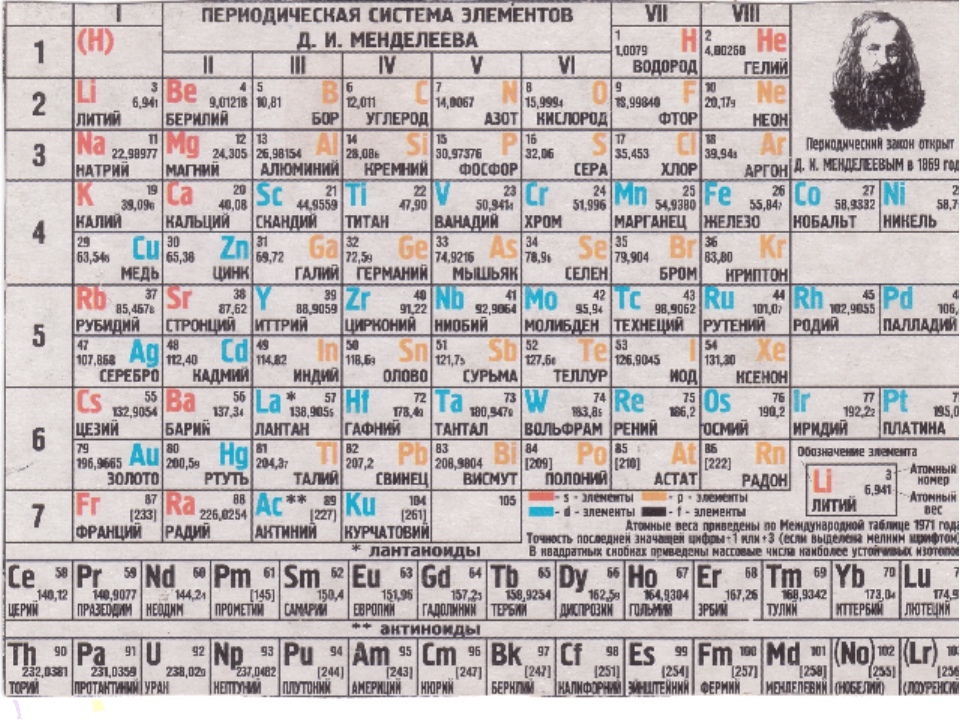
| Дебет | Кредит |
Инвентарь | ххх | |
Покупки | ххх |
Как рассчитать себестоимость товаров, проданных с использованием системы периодической инвентаризации?
Общая сумма покупок добавляется к начальному балансу запасов для расчета стоимости товаров, имеющихся в наличии для продажи.
Конечный запас определяется в конце периода путем физического подсчета каждого предмета, а его себестоимость рассчитывается с использованием таких методов расчета запасов, как ФИФИ, ЛИФО и средневзвешенных значений.
Эта сумма вычитается из стоимости товаров, имеющихся в наличии для продажи (или стоимости произведенных товаров), для расчета стоимости проданных товаров.
Общая формула для расчета себестоимости товаров, проданных в рамках системы периодической инвентаризации, приведена ниже:
Себестоимость проданных товаров (COGS) = Начальный запас + Покупки – Заключительный запас
Например, XYZ Corporation имеет начальные запасы в размере 100 000 долларов США, имеет расходы на закупки в размере 120 000 долларов США, а ее инвентаризация показывает конечную стоимость запасов в размере 80 000 долларов США.
Расчет себестоимости проданных товаров:
Стоимость имеющихся товаров = Начальные запасы + Покупки
220 000 долл. США = 100 000 долл. США + 120 000 долл. США
Стоимость проданных товаров = Стоимость имеющихся товаров – Закрытие запасов
140 000 долл. США = 220 000 долл. США – 80 000 долл. США
Преимущества системы периодической инвентаризации
Легче реализовать
Поскольку периодическая система включает меньше записей и более простые вычисления, чем непрерывная система, ее проще реализовать.Простота также позволяет использовать ручное ведение записей для небольших запасов.
Идеально подходит для малого бизнеса
Система периодической инвентаризации идеально подходит для небольших предприятий, которые поддерживают минимальный объем запасов. Инвентаризацию легко выполнить, малые предприятия могут оценить стоимость проданных товаров за временные периоды.
Хотя система может работать для небольших предприятий, она может оказаться весьма проблематичной для крупных предприятий из-за высокого уровня неточности.
