Периодическая таблица
Открытие Дмитрием Менделеевым периодической таблицы химических элементов в марте 1869 года стало настоящим прорывом в химии
Российскому ученому удалось систематизировать знания о химических элементах и представить их в виде таблицы, которую и сейчас обязательно изучают школьники на уроках химии. Периодическая таблица стала фундаментом для бурного развития этой сложной и интересной науки, а история ее открытия окутана легендами и мифами.
Периодическая система химических элементов (табли́ца Менделе́ева) — классификация химических элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра. Система является графическим выражением периодического закона, установленного русским химиком Д. И. Менделеевым в 1869 году. Её первоначальный вариант был разработан Д. И. Менделеевым в 1869—1871 годах и устанавливал зависимость свойств элементов от их атомного веса (по-современному, от атомной массы). В современном варианте системы предполагается сведение элементов в двумерную таблицу, в которой каждый столбец (группа) определяет основные физико-химические свойства, а строки представляют собой периоды, в определённой мере подобные друг другу.
В современном варианте системы предполагается сведение элементов в двумерную таблицу, в которой каждый столбец (группа) определяет основные физико-химические свойства, а строки представляют собой периоды, в определённой мере подобные друг другу.
Периодическая система Менделеева систематизирует не только элементы, но и самые разнообразные их свойства. Химику часто бывает достаточно иметь перед глазами Периодическую таблицу для того, чтобы правильно ответить на множество вопросов (не только экзаменационных, но и научных).
Попытки классифицировать и систематизировать известные химические элементы предпринимались задолго до Дмитрия Менделеева. Свои системы элементов предлагали такие известные ученые, как Деберейнер, Ньюлендс, Мейер и другие. Однако из-за нехватки данных о химических элементах и их правильных атомных массах предложенные системы были не совсем достоверными.
История открытия
История открытия таблицы Менделеева начинается в 1869 году, когда российский ученый на заседании Русского химического общества рассказал своим коллегам о сделанном им открытии. В предложенной ученым таблице химические элементы располагались в зависимости от их свойств, обеспечивающихся величиной их молекулярной массы.
В предложенной ученым таблице химические элементы располагались в зависимости от их свойств, обеспечивающихся величиной их молекулярной массы.
Интересной особенностью
таблицы Менделеева было также наличие пустых клеток, которые в будущем были заполнены открытыми химическими элементами, предсказанными ученым (германий, галлий, скандий). После открытия периодической таблицы в нее много раз вносились добавления и поправки. Совместно с шотландским химиком Уильямом Рамзаем Менделеев добавил в таблицу группу инертных газов (нулевую группу).
В дальнейшем история периодической таблицы Менделеева была напрямую связана с открытиями в другой науке – физике. Работа над таблицей периодических элементов продолжается до сих пор, и современные ученые добавляют новые химические элементы по мере их открыти
Значение
периодической системы Дмитрия Менделеева сложно переоценить, так как благодаря ей
Систематизировались знания о свойствах уже открытых химических элементов
Появилась возможность прогнозирования открытия новых химических элементов
Начали развиваться такие разделы физики, как физика атома и физика ядра;
Существует множество вариантов изображения химических элементов согласно периодическому закону, однако наиболее известный и распространенный вариант – это привычная для каждого таблица Менделеева.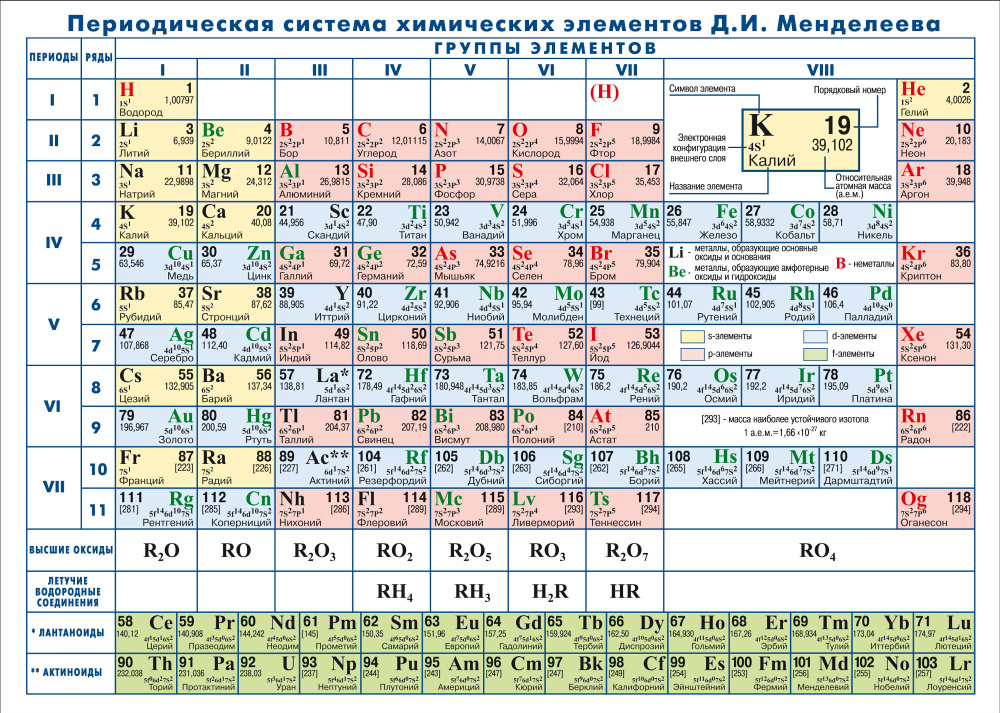
2019 год – Международный год Периодической таблицы химических элементов
2019 год провозглашен Генеральной ассамблеей ООН Международным годом Периодической таблицы химических элементов. Это масштабное событие посвящено 150-летию открытия Периодического закона химических элементов великим русским ученым Д.И. Менделеевым.
С инициативой о проведении Международного года Периодической таблицы химических элементов выступили Российская академия наук, Российское химическое общество имени Д.И. Менделеева, Министерство науки и высшего образования РФ, российские и зарубежные ученые.
Инициативу России поддержали зарубежные страны, международные научные организации, а также более 80 национальных академий наук и научных обществ. Среди них – Международный Союз по теоретической и прикладной химии (IUPAC), Международный союз теоретической и прикладной физики (IUPAP), Европейская Ассоциация химических и молекулярных наук (EuCheMS), Международный астрономический союз (IAU) и другие.
Международный год Периодической таблицы химических элементов пройдет под эгидой ЮНЕСКО в нескольких странах мира. В рамках этого события планируется проведение большого количества мероприятий: научных конференций, тематических выставок, конкурсов молодых ученых и т.д.
29 декабря 2018 года Председатель Правительства РФ Дмитрий Медведев подписал распоряжение «О проведении в 2019 году Международного года Периодической таблицы химических элементов» и возглавил Оргкомитет. В состав Оргкомитета вошли руководители федеральных органов исполнительной власти, ведомств и ведущих научных организаций.
Торжественная церемония открытия Международного года Периодической таблицы химических элементов состоялась 29 января 2019 года во Франции, в Париже, в штаб-квартире ЮНЕСКО.
В России церемония открытия Международного года пройдет 6 февраля 2019 года в Москве, в Президиуме РАН, и будет приурочена ко Дню российской науки и одновременно Дню рождения Дмитрия Ивановича Менделеева.
Официальным оператором церемоний открытия Международного года Периодической таблицы химических элементов в Париже и Москве выступит Всероссийский фестиваль науки NAUKA 0+. Главной темой Фестиваля науки в 2019 году станет Таблица Менделеева. Генеральный партнер Международного года Периодической таблицы химических элементов в России – Благотворительный Фонд «Искусство, наука и спорт».
В рамках Международного года во всех регионах России планируется проведение более 500 научно-популярных и образовательных мероприятий, посвященных 150-летию выдающегося открытия Д.И. Менделеева и направленных на привлечение внимания школьников, студентов и молодежи в целом к науке и ее достижениям.
Проведение в 2019 году Международного года Периодической таблицы химических элементов имеет особое значение для России. Это событие будет способствовать международному признанию заслуг великого русского ученого Д.И. Менделеева, а также укреплению престижа и популяризации отечественной науки.
Как периодическая таблица пережила войну, чтобы обеспечить будущее химии
- ОТ РЕДАКЦИИ
Столетие назад открытие гафния подтвердило справедливость периодической таблицы — но только благодаря ученым, которые отстаивали доказательства во времена глобальных потрясений.
Гафний — это переходный металл, названный в честь латинского названия Копенгагена (Hafnia), где этот элемент был открыт. Фото: Клаудия Килман/Alamy
Гафний не особенно примечательный элемент. Это не ваш взрывоопасный натрий, мерцающая ртуть или вонючая сера. Это сероватый металл, который обычно используется в качестве поглотителя нейтронов в управляющих стержнях атомных электростанций и атомных подводных лодок, а также в качестве изолятора в компьютерных микросхемах. Но открытие гафния, о котором сообщалось в журнале

Периодическая таблица элементов Дмитрия Менделеева, созданная в 1869 году, возникла в результате осознания того, что химические элементы, такие как кислород и водород, находятся в определенных отношениях. Вклад Менделеева и немецкого химика Юлиуса Лотара Мейера, работавших независимо друг от друга, обеспечили порядок элементов, а также критерии их классификации в четкие группы. Примечательно, что схемы Менделеева и Лотара Мейера основывались на субатомной структуре элементов — за несколько десятилетий до открытия электронов и протонов.
Когда Менделеев разработал приблизительную форму таблицы Менделеева, он начал с 63 известных элементов. Чтобы таблица работала, ему пришлось оставить пробелы, в которые могли бы быть помещены еще не обнаруженные элементы. Эти элементы вскоре начали появляться. Например, предсказанный «элемент 68», галлий, был идентифицирован несколькими годами позже, в 1875 году. К 1914 году осталось всего семь пробелов.
Прорыв произошел в 1913 году, когда Генри Мозли, британский физик, показал, что элементы можно расположить по их атомному номеру или количеству протонов.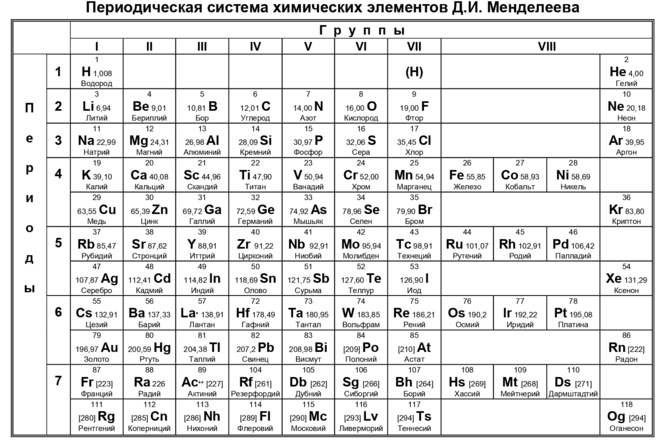 Работа Мозли предоставила как более точную «карту пробелов», так и метод идентификации элементов по спектрам, полученным путем воздействия на элементы-кандидаты рентгеновскими лучами.
Работа Мозли предоставила как более точную «карту пробелов», так и метод идентификации элементов по спектрам, полученным путем воздействия на элементы-кандидаты рентгеновскими лучами.
Битва за последние дополнения к периодической таблице
Но открытие (и название) элемента 72, гафния, было далеко не простым. Французский химик Жорж Урбен первоначально предположил в 1911 году, что 72-й элемент относится к редкоземельным элементам периодической таблицы, и назвал его кельтием. Но примерно десятилетие спустя датский физик Нильс Бор, который использовал квантовую теорию для разработки модели атома, в котором электроны вращаются вокруг ядра, предсказал, что элемент 72 будет среди переходных металлов и ближе к цирконию (элемент 40). В конце концов это подтвердили Костер и фон Хевеси, работавшие в лаборатории Бора в Копенгагене, которые искали в минералах циркония элемент 9.0017 2

Дебаты продолжались, ученые из Нидерландов, Германии и Скандинавии поддержали команду Копенгагена, в то время как ученые из Франции и Великобритании (которые поддержали бойкот немецкой науки после Первой мировой войны) выступили против встречная позиция. Гафний был принят Международным союзом теоретической и прикладной химии только в 1930, через несколько лет после официального прекращения бойкота. Во Франции кельтий продолжал занимать место 72-го элемента среди редкоземельных элементов до начала 1940-х годов
Гафний был принят Международным союзом теоретической и прикладной химии только в 1930, через несколько лет после официального прекращения бойкота. Во Франции кельтий продолжал занимать место 72-го элемента среди редкоземельных элементов до начала 1940-х годов
Спустя сто лет после открытия гафния периодическая таблица остается надежной и актуальной, даже в то время, когда к множеству данных об элементе можно получить доступ одним щелчком мыши. Таблица дает краткий обзор того, как элемент может вести себя в химической реакции, и указывает на его сходство с другими элементами в группе.
На данный момент подтверждено 118 элементов с добавлением четырех сверхтяжелых синтетических элементов в 2015 году. Но обязательно придет время, когда новых элементов не будет и периодическая таблица достигнет своего предела. Пока нет единого мнения о том, когда это может произойти или насколько большим будет последний элемент, но химики говорят, что его атомный номер может превысить 170.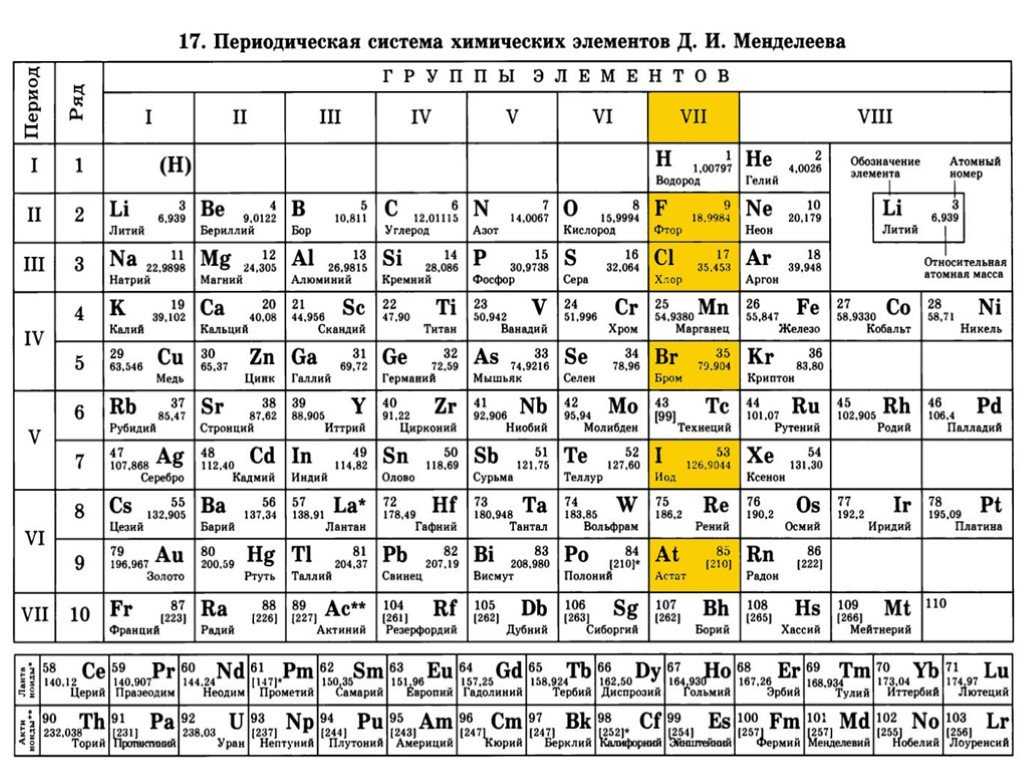
Костер Д. и Хевеси Г. Nature 111 , 79 (1923).
Артикул Google ученый
Kragh, H. Centaurus 23 , 275–301 (1980).
Артикул Google ученый
Frederick-Frost, K.M. Chem. Междунар. 41 (2), 23–27 (2019).
Артикул Google ученый
Резерфорд, Э. Природа 109 , 781 (1922).
Артикул Google ученый
Урбен Г. и Довилье А. Природа 111 , 218 (1923).
Артикул Google ученый
Костер, Д. и Хевеси, Г. Природа 111 , 462–463 (1923).
Артикул Google ученый
Ссылки для скачивания
Празднование Периодической таблицы | Элементы
Периодическая таблица химических элементов является одним из самых значительных достижений в науке, поскольку она упорядочивает 118 известных элементов в обманчиво простой схеме, раскрывающей их свойства. Так как же возник этот «Розеттский камень природы»? Скорее всего, вы ответите Дмитрию Менделееву, русскому химику, опубликовавшему в 1869 году версию таблицы Менделеева, которую мы знаем сегодня.
Среди важных событий, которые привели к открытию периодической таблицы, было появление теории атома, первоначально предложенной в 1808 году Джоном Дальтоном, британским наставником и школьным учителем. Ключевым достижением стало назначение Далтона относительных весов к атомам элементов. Но как получить абсолютный вес атома? В 1811 году итальянский физик и математик Амедео Авогадро предложил идею вычисления атомных весов по газам, но его гипотеза не получила широкого распространения.
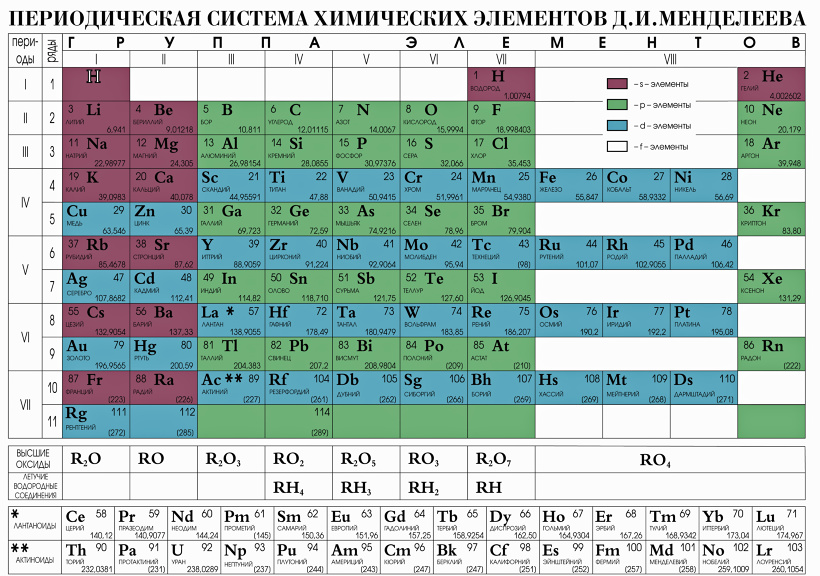
Французский геолог и минералог Александр-Эмиль Бегуйе де Шанкуртуа первым расположил химические элементы в порядке их атомного веса. Он разработал трехмерный спиральный график и нанес атомные веса на поверхность цилиндра, которые помещали аналогичные элементы в соответствующие точки цилиндра выше или ниже друг друга (рис. 1). Он представил свои идеи Французской академии наук и опубликовал свою работу в 1862 году. К сожалению, оригинальная диаграмма не была включена в публикацию, что затрудняло понимание статьи. Хотя де Шанкуртуа позже переиздал свою работу с диаграммой, химики в значительной степени проигнорировали ее. После этого он, похоже, потерял интерес к своей идее и вернулся к другим научным занятиям.
Вскоре последовали новые открытия периодической системы элементов. Джон Ньюлендс, британский химик-сахарист и частный репетитор по химии, заметил закономерности между элементами и их массами и опубликовал свой «закон октав» в 1865 году. Подобно де Шанкуртуа, работа Ньюлендса привлекла мало внимания, а его модель не выдержала большой критики. хорошо. Через четыре года после Карлсруэ британский химик Уильям Одлинг опубликовал таблицу, в которую вошли 57 элементов. Однако система Одлинга также не оказала большого влияния, и он не стал развивать ее дальше. Густавус Хинрихс, датчанин, иммигрировавший в Соединенные Штаты, опубликовал уникальную периодическую систему с элементами в форме «велосипедного колеса», где группы элементов отображаются в виде спиц. Лотар Мейер, влиятельный немецкий химик, создал несколько версий периодической таблицы, начиная с 1864 года. К сожалению, работа Мейера не была опубликована до 1870 г., через год после работы Менделеева в 1869 г.периодической таблицы, поэтому его вклады затмеваются Менделеевым.
хорошо. Через четыре года после Карлсруэ британский химик Уильям Одлинг опубликовал таблицу, в которую вошли 57 элементов. Однако система Одлинга также не оказала большого влияния, и он не стал развивать ее дальше. Густавус Хинрихс, датчанин, иммигрировавший в Соединенные Штаты, опубликовал уникальную периодическую систему с элементами в форме «велосипедного колеса», где группы элементов отображаются в виде спиц. Лотар Мейер, влиятельный немецкий химик, создал несколько версий периодической таблицы, начиная с 1864 года. К сожалению, работа Мейера не была опубликована до 1870 г., через год после работы Менделеева в 1869 г.периодической таблицы, поэтому его вклады затмеваются Менделеевым.
История периодической таблицы — замечательная история, включающая открытия, сделанные шестью разными людьми за семилетний период. Были ключевые открытия и события, такие как конгресс 1860 года, которые ускорили его развитие. Менделеев, возможно, не был первым, кто разработал периодическую систему элементов, но он был мастером ее использования. Открытие периодической таблицы в том виде, в каком мы ее знаем в настоящее время, в 1869 г.был преобразовательным, потому что освободил химическую науку от ассоциаций со средневековой мистикой алхимии. Периодическая таблица даже намекала на существование субатомной структуры, которая будет открыта в следующем столетии.
Открытие периодической таблицы в том виде, в каком мы ее знаем в настоящее время, в 1869 г.был преобразовательным, потому что освободил химическую науку от ассоциаций со средневековой мистикой алхимии. Периодическая таблица даже намекала на существование субатомной структуры, которая будет открыта в следующем столетии.
Из истории периодической таблицы можно извлечь много уроков. Открытия четырех из шести первооткрывателей таблицы не были признаны до тех пор, пока они не были опубликованы спустя много лет. Мейер и Менделеев оба активно продвигали свои версии периодической таблицы, но имя Менделеева мы узнаем, потому что его более полная версия была опубликована до версии Мейера. И есть уроки, которые следует усвоить сегодняшним ученым, молодым и старым: широко читайте литературу в областях, выходящих за рамки вашей непосредственной специальности; публиковать широко и мудро; и будьте активны в продвижении своих идей, как только они будут подтверждены научными данными.
Какой будет периодическая таблица в ближайшие 150 лет? Сколько новых элементов будет открыто? Будут ли эти элементы вести себя так, как предсказывает периодическая таблица? Можно ли получить сверхтяжелые ядра в космосе? Оставайтесь с нами… увлекательная история таблицы Менделеева продолжается.
