Открытия
Русский химик, открывший периодический закон химических элементов, разносторонний учёный, педагог и общественный деятель, физик и натуралист в широком смысле этого слова.
Родители Менделеева – чисто русского происхождения. В гимназии Менделеев учился неважно. Благоприятную почву для развития своих способностей Менделеев нашел только в Главном Педагогическом институте. В Санкт-Петербурге, где защитил диссертацию на степень магистра химии: “Об удельных объемах” 23 лет от роду он становится доцентом Петербургского университета, где читает сначала теоретическую, потом органическую химию. В 1864 г. Менделеев был избран профессором Петербургского технологического института.
Менделеев создал современную гидратную теорию растворов, уравнение состояния идеального газа, разработал технологию получения бездымного пороха, открыл Периодический закон и предложил Периодическую систему химических элементов, написал лучший для своего времени учебник химии.
 И. Менделеев раздумывал над тем, как систематизировать материал таким образом, чтобы сведения о химических свойствах элементов не выглядели набором разрозненных фактов.
Ориентиром в этой работе Д. И. Менделееву послужили атомные массы элементов. После Всемирного конгресса химиков в 1860 году, в работе которого участвовал и Д. И. Менделеев, проблема правильного определения атомных весов была постоянно в центре внимания многих ведущих химиков мира, в том числе и Д. И. Менделеева.
И. Менделеев раздумывал над тем, как систематизировать материал таким образом, чтобы сведения о химических свойствах элементов не выглядели набором разрозненных фактов.
Ориентиром в этой работе Д. И. Менделееву послужили атомные массы элементов. После Всемирного конгресса химиков в 1860 году, в работе которого участвовал и Д. И. Менделеев, проблема правильного определения атомных весов была постоянно в центре внимания многих ведущих химиков мира, в том числе и Д. И. Менделеева.Работая над трудом «Основы химии», Д. И. Менделеев открыл в феврале 1869 года один из фундаментальных законов природы — периодический закон химических элементов. Периодическая система элементов Менделеева
 Среди наиболее известных открытий — периодический закон химических элементов, один из фундаментальных законов мироздания, неотъемлемый для всего естествознания. Одно из важных открытий Менделеева – определение «температуры абсолютного кипения жидкостей», известной ныне под названием критической температуры. Внёс в первоначальный вариант периодической системы ряд исправлений и уточнений, и в 1871 г. опубликовал две классические статьи –
Среди наиболее известных открытий — периодический закон химических элементов, один из фундаментальных законов мироздания, неотъемлемый для всего естествознания. Одно из важных открытий Менделеева – определение «температуры абсолютного кипения жидкостей», известной ныне под названием критической температуры. Внёс в первоначальный вариант периодической системы ряд исправлений и уточнений, и в 1871 г. опубликовал две классические статьи – 6 марта 1869 года знаменитый доклад Д. И. Менделеева «Соотношение свойств с атомным весом элементов» был прочтён Н. А. Меншуткиным на заседании Русского химического общества. В том же году это сообщение на немецком языке появилось в журнале
 И. Менделеева, посвящённая его открытию — «Die periodische Gesetzmässigkeit der Elemente» (Периодическая закономерность химических элементов).
И. Менделеева, посвящённая его открытию — «Die periodische Gesetzmässigkeit der Elemente» (Периодическая закономерность химических элементов).Предсказал в 1870 году существование, вычислил атомные массы и описал свойства трёх ещё не открытых тогда элементов — «экаалюминия», «экабора» и «экасилиция». Затем предсказал существование ещё восьми элементов, в том числе
Дизайн: школа №548 Санкт-Петербург || Содержание: школа №548 Санкт-Петербург, Willy-Brandt-Schule Norderstedt
Периодический закон и периодическая система химических элементов д.И.Менделеева на основе представлений о строении атомов. Значение периодического закона для развития науки.
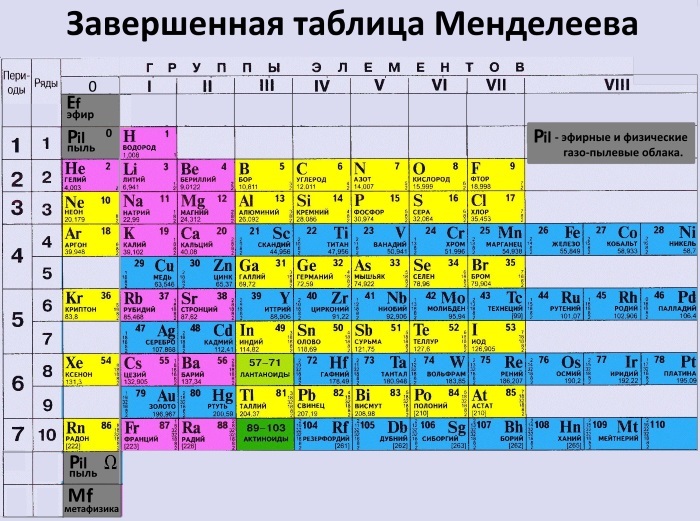
Основной закон химии – был открыт Д.И. Менделеевым в то время когда в науке господствовало атомно-молекулярное учение, согласно которому атомы химических элементов отличаются друг от друга размерами, свойствами, массой. Именно это последнее постоянное свойство атомов Д.И. Менделеев взял за основу сравнения химических элементов. До него при попытках классифицировать химические элементы их делили по какому-либо одному признаку: либо по химическим свойствам, либо по валентности, либо по относительной атомной массе. В отличие от предшественников Д.И. Менделеев для классификации элементов использовал два основных признака – значение атомных масс и химические свойства элементов. Расположив 63 известных в то время элемента в порядке возрастания их атомных масс, Д.И. Менделеев получил ряд химических элементов, где он обнаружил периодическую повторяемость химических свойств, которая легла в основу периодического закона химических элементов.
На
основе периодического закона Д.
Важно указать, что периоды – это горизонтальные ряды таблицы, они подразделяются на малые и большие. В малых периодах находиться 2 элемента (1-й период) или 8 элементов (2-й, 3-й периоды), в больших – 18 элементов (2-й, 3- периоды) или 32 (6-й период), 7-й период еще не закончен. Каждый период начинается с типичного щелочного металла, а заканчивается типичным неметаллом (галогеном) и благородным газом.
Вертикальные
столбцы называются группами элементов.
Каждая группа делиться на две подгруппы:
главную и побочную. Главные подгруппы
включают
элементы маллых и польших периодов;
химические свойства их изменяются от
неметаллических к металлическим
(например, в главной подгруппе V
группы азот – неметалл, а висмут –
металл). Все элементы побочных подгрупп
– переходные металлы, они образуют
высшие оксиды и гидроксиды, обладающие
амфотерными или даже кислотными
свойствами.
Высшая валентность элементов в соединениях с кислородом, как правило, численно равна номеру группы, в которую они входят. Например, элементам подгрупп бериллия и цикла (главная и побочная подгруппы II группы) отвечает высшая валентность (II), а элементам подгруппы углерода и титана (IV группа) – высшая валентность (IV).
В конце XIX – начале XX века физики доказали, что атом является сложной частицей и чтов атоме каждого элемента присутствуют протоны, нейтроны и электроны. Протоны и нейтроны сосредоточены в ядре атома, а электроны движуться вокруг него. Атом – частица электронейтральная, т. е. не имееющая заряда. Ядро же заряжено положительно, но его заряд нейтрализуется суммарным отрицательным зарядом всех электронов. Например, если ядро атома имеет заряд +8, то вокруг него движуться 8 электронов, каждый из которых имеет заряд, равный -1.
Теория
строения атома дала физическое обоснование
переодическому закону, позволила
объяснить его основные положения и
выводы.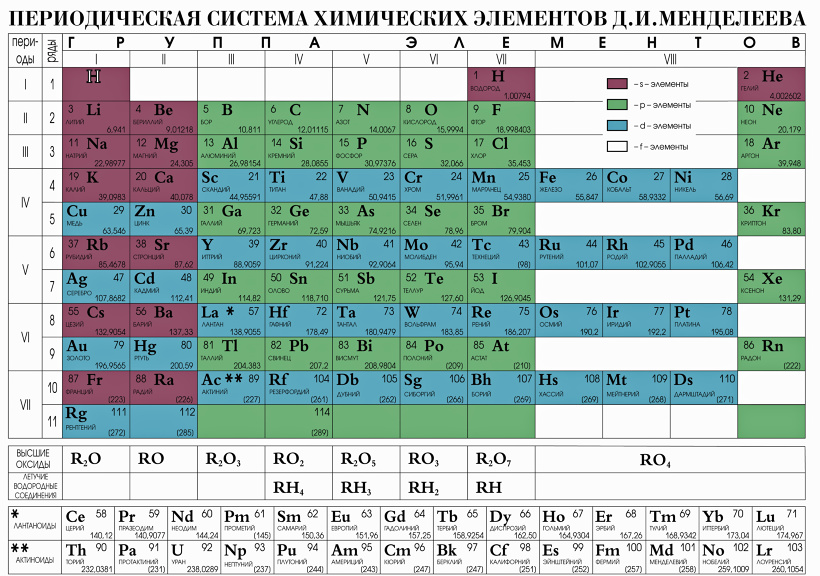
Эксперементально было установленн, что порядковые номера в переодической системе Д.И. Менделеева совпадают со значением зарядов ядер их атомов. Порядковый (атомный) номер химического элемента численно равен заряду ядра его атома.
С тех пор как ученные выявили смысл порядкового номера элемента, периодических закон формулируется так:
Далее
на основе знаний об изотопах
можно объяснять, почему значения зарядов
ядер атомов химических элементов
периодической системы возрастают, а
правильная последовательность увеличения
относительной атомной массы нарушается.
Для этого достаточно вспомнить, что в
ядрах атомов одного и того же элемента
число нейтронов может быть разным. Так,
природный калий, образовывая в основном
атомами его легких изотопов, а аргон –
тяжелых.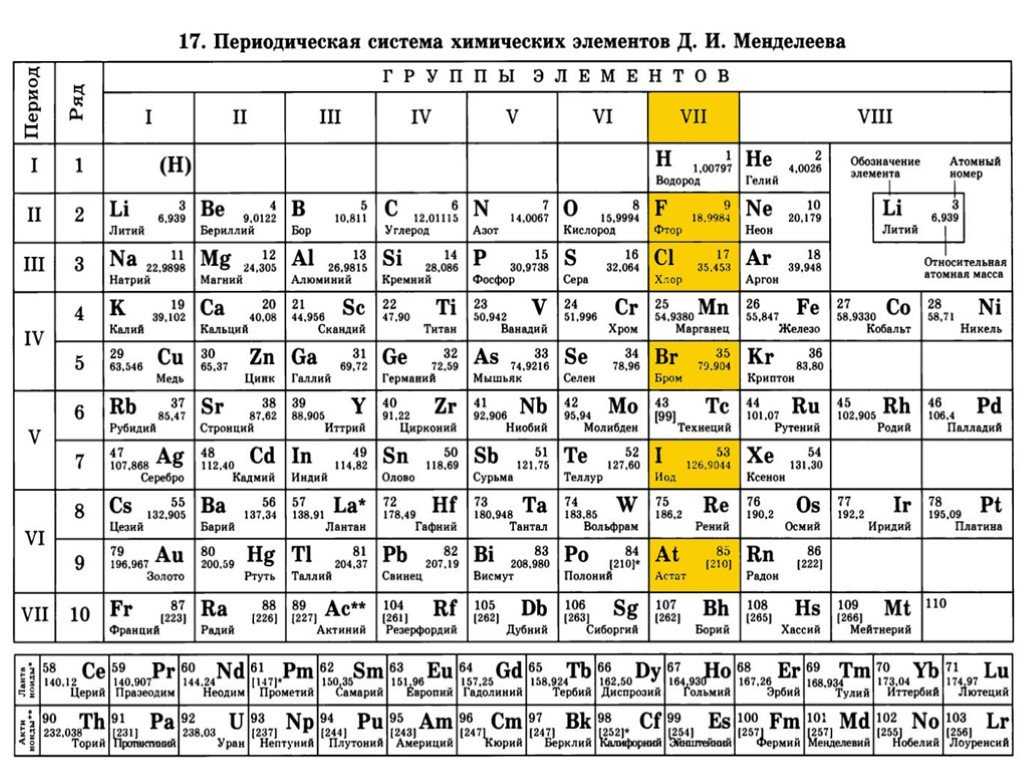
Важно подчеркнуть, что число электронов в электронной оболочке атома равно заряду его ядра. Электроны располагаются на разном удалении от ядра, образуя электронные слои.
Число электронных слоев в атоме совпадает с номером периода, в котором находиться химический элемент.
Электронная оболочка атома каждого следующего элемента в периодической системе повторяет строение электронной оболочки предыдущего элемента, но отличается от нее на один электрон.
Переходя к объяснению периодической повторяемости свойств химических элементов, расположенных в порядке возрастания заряда ядра, можно выписать, например, элементы 2-го и 3-го периодов, схемы строения их атомов, свойства простого вещества, формулы соединений:
2-й период | ||||||||
3Li | 4Be | 5B | 6C | 7N | 8O | 9F | 10Ne | |
Распределение электронов по слоям | 2,1 | 2,2 | 2,3 | 2,4 | 2,5 | 2,6 | 2,7 | 2,8 |
Электронная формула | 1s22s1 | 1s22s2 | 1s22s22p1 | 1s22s22p2 | 1s22s22p3 | 1s22s22p4 | 1s22s22p5 | 1s22s22p6 |
Свойства простого вещества | Металл (щелочной) | Переходный металл | неметалл | неметалл | неметалл | неметалл | Неметалл (галоген) | Инертный газ |
Формула высшего оксида и характер его свойств | Li2O
(осн. Na2O | BeO(амф.) MgO(осн.) | B2O3(кисл.) Al2O3 (амф.) | CO2 (кисл.) SiO2 (кисл.) | N5O5 (кисл.) P2O5 (кисл.) | – | OF2 | – |
Формула высшего гидроксида и характер его свойств | Li(OH) (осн.) NaOH (осн.) | Be(OH)2 (амф.) Mg(OH)2 (осн. | H3BO3 (кисл.) Al(OH)3 (амф.) | H2CO3 (кисл.) H2SiO3 (кисл.) | HNO3 (кисл.) H3PO4 (кисл.) | – H2SO4 (кисл.) | – HClO4 (кисл.) | – – |
3-й период | ||||||||
11Na | 12Mg | 13Al | 14Si | 15P | 16S | 17Cl | 18Ar | |
Распределение элементов по слоям | 2, 8, 1 | 2, 8, 2 | 2, 8, 3 | 2, 8, 4 | 2, 8, 5 | 2, 8, 6 | 2, 8, 7 | 2, 8, 8 |
Электронная формула | 1s22s22p63s1 | 1s22s22p63s2 | 1s2…3s23p1 | 1s2…3s23p2 | 1s2…3s23p3 | 1s2…3s23p4 | 1s2…3s23p5 | 1s2…3s23p6 |
На
примере элементов 2-го и 3-го периодов
записано строение атомов этих элементов
(ученик по желанию может использовать
схему распределения электронов по слоям
или электронную формулу) и зависимость
свойств простых веществ и соединений
этих элементов от строения атомов. это
позволит сделать важнейший вывод о том,
что свойства
химических элементов, расположенных в
порядке возрастания заряда ядра,
изменяются периодически повторяется
сходное строение внешнего электронного
слоя атомов электронов.
это
позволит сделать важнейший вывод о том,
что свойства
химических элементов, расположенных в
порядке возрастания заряда ядра,
изменяются периодически повторяется
сходное строение внешнего электронного
слоя атомов электронов.
Изменение свойств элементов в пределах одного периода можно объяснить постепенным увеличением числа электронов на внешнем слое атомов, а в группах – одинаковым числом электронов внешнего слоя. Появление нового внешнего электронного слоя – причина резкого скачка в свойствах при переходе от инертного элемента к щелочному металлу.
В
заключение важно подчеркнуть значение
периодического закона – гениального
открытия Д.И. Менделеева уже хотя бы по
тому, что в то время представления о
молекулах и атомов начинали только
формироваться. Периодический закон
положил начало современному этапу
развития химии. С его открытием появились
возможности предсказывать новые элементы
и описывать их свойства, а три из них –
галлий, скандий и германий – Д. И. Менделеев
не только предсказал, но и дал точное
описание их свойств. В настоящее время
в периодической системе уже 116 элементов,
как найденных в природе, так и полученных
искусственно.
И. Менделеев
не только предсказал, но и дал точное
описание их свойств. В настоящее время
в периодической системе уже 116 элементов,
как найденных в природе, так и полученных
искусственно.
С помощью периодического закона были исправлены атомные массы и уточнены валентности некоторых элементов; закон отражает взаимность элементов и взаимообусловленность их свойств.
Периодический закон подтвердил наиболее общие законы развития природы, открыл путь к познанию строения атома.
Краткая история периодической таблицы
В визуальном представлении научных концепций периодическую таблицу трудно превзойти. Он легко узнаваем, относительно прост для понимания и в течение последних 150 лет служил надежной дорожной картой, помогающей химикам открывать новые элементы и расширять совокупность человеческих знаний. Американское химическое общество (ACS) охарактеризовало это как «возможно, такое же фундаментальное для химии, как открытие ДНК для биологии».
Но элементарная электронная таблица Excel Дмитрия Менделеева также стала своего рода пробным камнем культуры. Столы любого размера и формы легко доступны. Хотите цветное представление ключевых элементарных групп? Без проблем. Нужна периодическая таблица EleMUTTS в собачьей тематике? Конечно! Хотите выучить периодическую таблицу с помощью песни на мотив «Адского галопа» Жака Оффенбаха? Конечно, вы делаете.
Поэтому неудивительно, что Организация Объединенных Наций решила, что полувековой юбилей таблицы заслуживает признания: согласно официальному веб-сайту ЮНЕСКО, 2019 год является Международным годом Периодической таблицы. Итак, давайте углубимся — как Менделеев разработал свою таблицу? Насколько хорошо он выдерживает давление? А что происходит, когда стола недостаточно для всех элементов на вечеринке?
Давайте обсудим это обсуждение Как отмечает Королевское химическое общество, Дмитрий Менделеев был не первым ученым, который попытался сгруппировать элементы в какую-то легко узнаваемую структуру. В 1789 г.Антуан Лавуазье классифицировал элементы по их свойствам (газы, металлы, неметаллы и земли). В 1865 году Джон Ньюлендс заметил сходство элементов с атомным весом, отличающимся на семь. Он назвал это «законом октав», позже известным как «периодический закон».
В 1789 г.Антуан Лавуазье классифицировал элементы по их свойствам (газы, металлы, неметаллы и земли). В 1865 году Джон Ньюлендс заметил сходство элементов с атомным весом, отличающимся на семь. Он назвал это «законом октав», позже известным как «периодический закон».
Менделеев заметил, что определенные типы элементов регулярно повторяются, когда элементы располагаются в соответствии с атомным весом — за реактивными неметаллами сразу следуют легкие химически активные металлы и менее реакционноспособные легкие металлы. По словам Королевского химического общества, он не боялся перемещать элементы по столу в зависимости от их поведения.
Это противоречило представлению о том, что элементы следует упорядочивать по атомному весу, но дало лучшие результаты. Например, никель легче кобальта, но лучше сочетается с палладием, расположенным в следующем ряду ниже, чем с родием. Выбор действия вместо атомного веса сделал таблицу Менделеева намного более точной, особенно после открытия протонов; По данным Королевского химического общества, при классификации по количеству протонов в ядре таблица Менделеева была точной.
Самым большим преимуществом таблицы была предсказуемость. Элементы непосредственно друг над другом или под ним в столбцах — или «группах» — имеют схожие характеристики. Например, щелочные металлы из первой колонки «обычно несут в реакциях заряд +1, энергично реагируют с водой и легко соединяются с неметаллами», как отмечает ThoughtCo. Те, что находятся в одном ряду — или «периоде», — имеют самый высокий энергетический уровень невозбужденных электронов. Таблица помогла лучше понять работу химических реакций, предсказать результаты при объединении элементов разных групп или периодов, а также помогла открыть путь к открытию новых элементов.
Заполнение пробеловНаряду со своим законом октав Джон Ньюлендс также создал версию таблицы Менделеева. Проблема? Сохранение шаблона означало втиснуть несколько элементов в одно и то же пространство и надеяться на лучшее. Излишне говорить, что Химическое общество не было впечатлено.
Между тем Менделеев знал, что у него нет ответов на все вопросы. Поэтому всякий раз, когда он сталкивался с потенциальным пробелом в своей таблице, он не трогал его. Более того, он предсказал, что будут найдены новые элементы, которые закроют эти пробелы — и действительно, они были найдены. Он знал, что после алюминия должен быть элемент (который он назвал «эка-алюминием»), но, поскольку ни один из известных элементов не обладал нужными свойствами, он оставил место пустым. Он также предсказал свойства эка-алюминия, в том числе атомный вес около 68, плотность твердого вещества 6,0 грамм на кубический сантиметр и валентность три. В 1875 году Поль-Эмиль Лекок де Буабодран открыл галлий с атомным весом 69.0,72, плотность 5,9 грамма на кубический сантиметр и валентность три — как и предсказывал Менделеев, сообщает Королевское химическое общество.
Поэтому всякий раз, когда он сталкивался с потенциальным пробелом в своей таблице, он не трогал его. Более того, он предсказал, что будут найдены новые элементы, которые закроют эти пробелы — и действительно, они были найдены. Он знал, что после алюминия должен быть элемент (который он назвал «эка-алюминием»), но, поскольку ни один из известных элементов не обладал нужными свойствами, он оставил место пустым. Он также предсказал свойства эка-алюминия, в том числе атомный вес около 68, плотность твердого вещества 6,0 грамм на кубический сантиметр и валентность три. В 1875 году Поль-Эмиль Лекок де Буабодран открыл галлий с атомным весом 69.0,72, плотность 5,9 грамма на кубический сантиметр и валентность три — как и предсказывал Менделеев, сообщает Королевское химическое общество.
Также следует отметить открытие благородных газов Уильямом Рамзи. В то время как некоторые считали их противоречащими работе Менделеева, дальнейшие исследования нашли свое естественное место в последней группе периодической таблицы.
Химики регулярно добавляли в таблицу новые элементы. Как отмечает JSTOR Daily, таблица в настоящее время ограничивается элементом 118 — оганесоном — благородным газом, период полураспада которого составляет всего 0,89.миллисекунды. Работа по поиску элементов 119 и 120 уже ведется, но, как ясно из недолговечного существования оганесона, это непростая задача.
Начиная с элемента 105, резерфордия, требуется искусственная подготовка, и у исследователей очень мало времени, чтобы наблюдать какие-либо врожденные свойства до того, как произойдет распад. Есть предсказания, что будет найден «остров стабильности» — группа элементов с исключительно стабильными ядрами, потому что их ядерные оболочки заполнены «магическим числом» протонов или нейтронов. Согласно части JSTOR, 184 нейтрона — это следующее предсказанное магическое число.
Новые элементы также могут быть обнаружены с использованием технологий из других дисциплин, таких как телескоп Джеймса Уэбба, который скоро будет запущен, который будет наблюдать и анализировать далекие газовые облака. Тот факт, что мы не можем производить сверхтяжелые и сверхстабильные элементы здесь, на Земле, не означает, что какое-то древнее газовое облако не делает великой работы.
Тот факт, что мы не можем производить сверхтяжелые и сверхстабильные элементы здесь, на Земле, не означает, что какое-то древнее газовое облако не делает великой работы.
И пока мы на этом, давайте зайдем очень далеко в сторону науки: согласно Phys.org, новая статья предполагает, что как только элементы превысят атомный вес 300, правила нормальной материи могут нарушиться. вниз. Вот идея: обычная, или барионная, материя состоит из протонов и нейтронов, содержащих связанные триплеты кварков. Существует предположение, что после 300 элементов элементы могут состоять из «свободно текущих «верхних» и «нижних» кварков», что не являются связанными тройками. Эта кварковая материя (udQM) была бы стабильной для сверхтяжелых элементов за пределами конца периодической таблицы и могла бы существовать на «континенте», а не только на острове! — стабильности.
Не Менделеев Меня Здесь Работа Менделеева стала важной отправной точкой для развития химии, технологии и научных рассуждений. Однако, как показывает наша краткая история периодической таблицы, это не ситуация «найди и забудь»: всегда есть больше места для элементов, опущенных в первом наброске (и даже для тех, которые могут оказаться слишком большими для нашей текущей таблицы).
Однако, как показывает наша краткая история периодической таблицы, это не ситуация «найди и забудь»: всегда есть больше места для элементов, опущенных в первом наброске (и даже для тех, которые могут оказаться слишком большими для нашей текущей таблицы).
Наряду с признанием в 2019 году Международным годом Периодической таблицы Менделеев был увековечен в элементе 101: металлическом радиоактивном трансурановом элементе из ряда актинидов, который был открыт в 1955 году и назван менделевием в честь его работы.
Развитие и история периодической таблицы — краткий обзор
Автор Адил Аббас
Важность периодической таблицыСодержание
Когда мы смотрим на химию, мы видим, что более значимые химические науки достижения заключаются в разработке периодической таблицы элементов, которые могут помочь нам систематизировать свойства элемента. Это показывает важность периодической таблицы, поскольку она обеспечивает хорошо организованный список химических элементов.
Посмотрите видеолекцию, чтобы лучше понять историю и развитие периодической таблицы
Видеолекция об истории и развитии периодической таблицы информация из периодической таблицыПериодическая таблица дает нам базовую основу для понять химию элементов, это также дает нам информацию о периодических свойствах соединений. тем более периодичность хорошо понятна из таблицы Менделеева
История периодической таблицы Развитие и история периодической таблицыБольшой вклад в разработку модели периодической таблицы внесли следующие ученые.
- Al Razi
- Dobereiner
- Newland
- Mendeleev
- Moseley
HE Classerte Elements на основе физических работ.
Этот немецкий химик дал триады смеха в 1829 году. В нем он заявил, что они состоят из трех элементов. атомная масса среднего элемента является средним значением двух других элементов, все элементы триадной системы обладают одинаковыми свойствами классифицировал 62 элемента, которые были известны в то время. Он расположил их в порядке возрастания атомных масс, заметив, что каждый земной элемент имеет те же общие свойства, что и первый.
Международная таблица МенделееваПосмотреть видеоурок о периодической таблице Менделеева
Видеолекция по периодической таблице Менделеева Менделеев был русским химиком. В 1871 году Он дал более полезную и точную понятную схему классификации элементов. Он открыл роль классификации элементов, известную как периодический закон.
В 1871 году Он дал более полезную и точную понятную схему классификации элементов. Он открыл роль классификации элементов, известную как периодический закон.
Согласно периодическому закону Менделеева свойства элементов являются периодической функцией их атомных масс.
Основные черты периодического закона Менделеева- Вертикальные столбцы были названы группами
- Горизонтальные ряды в периодической таблице были названы периодами
- Расположение было сделано в порядке возрастания атомных масс
- элементы с похожим химическим поведением и свойствами появлялись через равные промежутки времени
- В этой таблице остались пробелы, которые еще не были открыты
- Предсказал свойства элементов, которые еще не были открыты
Менделеев оставил несколько вакантных мест для тех элементов, которые еще предстояло открыть позже, когда эти элементы были открыты, они были помещены на те места
2 Коррекция атомных массМенделееву удалось исправить сомнительные атомные массы.

Например, на основании сходства химических свойств оставить бериллий и поместить его во вторую группу наряду с магнием, кальцием, стронцием и барием. Считалось, что его атомная масса составляет 13,5 а.е.м. Это было не правильно. его правильная атомная масса была предложена равной 9,0 а.е.м.
Дефекты в периодической таблице Менделеева 1 Положение водородаСвойства водорода напоминают щелочные металлы и галоген, его положение не могло быть определено Менделеевым.
2 представление о строении атомаЕго таблица не давала представления о строении атома. Собственно, он образовался на основе атомной массы
3 Положение лантаноидов и актинидовЕсть группа из 14 элементов с атомным номером Ce 57 –Lu 71 . Их называют лантаноидами, эти элементы не находят должного места в периодической таблице Менделеева.
Аналогично и другая группа блочных элементов F с атомным номером Th 90 –Lr 103 называется актинидом
Они также не нашли правильного положения в листьях монетного двора в периодической таблице
4 неправильное положение некоторых элементовСледующие четыре пары элементов очень интересны своим атомным строением массы имеют иной тренд, чем атомные номера Менделеев расположил их в порядке возрастания атомных масс, они должны были быть расположены в порядке возрастания атомного номера.
Таблица с неправильным расположением некоторых элементов 5 Положение изотопов
В периодической таблице Менделеева не указано положение изотопов
6 Разнородные элементы помещаются вместеСвойства монетного металла, такого как медь, серебро и оранжевый, отличаются от щелочных металлов. он поместил их вместе
7 Причина периодичностиНесомненно, периодичность свойств может быть до некоторой степени оправдана, но причина периодичности не ясна из его таблицы.
Улучшения в периодической таблице Менделеева Автор Мозли периодический закон МозлиМозли был британским физиком, который сформулировал свой закон в 1913 году. Он подготовил периодическую таблицу, дав свой закон, который называется законом Мозли.
Определение закона МозлиФизические и химические свойства элементов являются периодической функцией их атомного номера.
Преимущества закона Мозли
Неровности, имевшиеся в таблице Менделеева, были устранены в основном
1 Правильное расположение некоторых элементовПринимая во внимание самый периодический закон. Кобальт должен быть помещен перед никелем
- Te должен быть помещен перед йодом
Положение редкоземельного элемента лантанида и актинида было скорректировано
3 Положение изотоповИзотопы одного и того же элемента имеют одинаковый атомный номер, все они должны занимать одно и то же место в таблице Менделеева
4 Положение благородных газовДополнительная группа благородных газов была разработана и количество групп для них VIIIA или нулевая группа.
5 Позиция металлов для чеканки Такие металлы, как цинк, кадмий и ртуть, и металл для чеканки, такой как медь, серебро и золото, были помещены отдельно от Be, Mg, Ca, Sr и Ba.

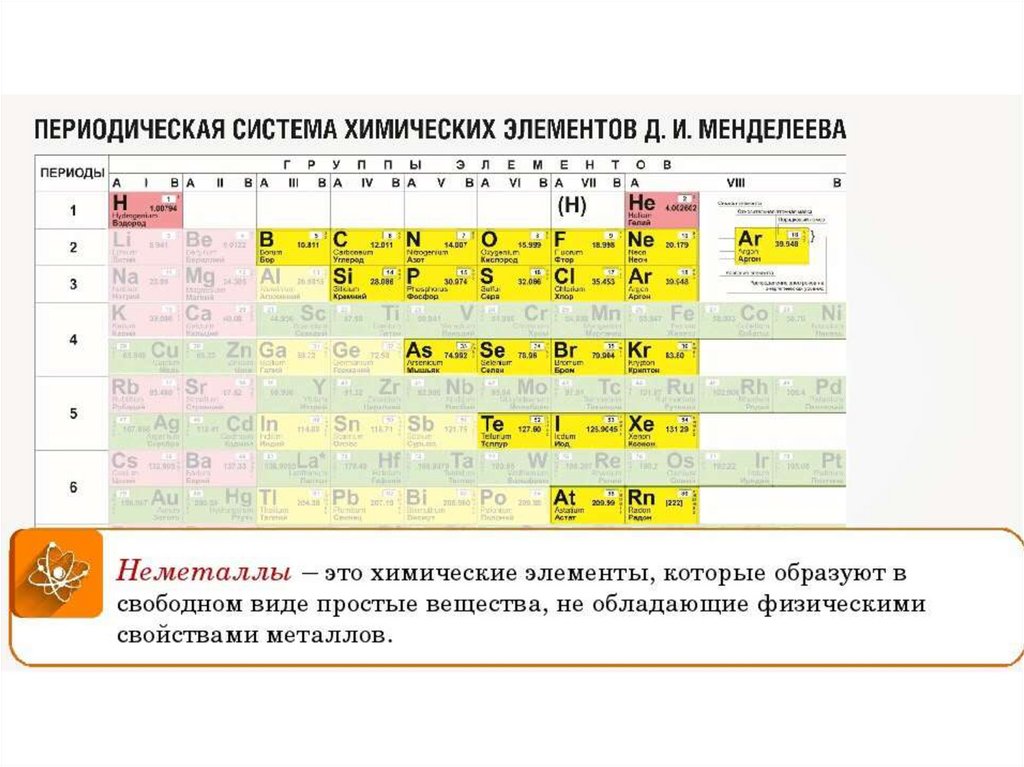 )
) )
)