Периодическая система менделеева таблица для печати егэ.
Таблица Менделеева является фундаментом нашего современного знания о химии.
- Сколько элементов в таблице Менделеева?
- Классический вид периодической таблицы Менделеева
- Таблица Менделеева для ЕГЭ по химии
- Периодический закон Менделеева
Ответ: 118 или 126 элементов в зависимости от вида таблицы.
Почему такая разница?
В природе люди обнаружили 94 элемента. Другие 24 элемента были созданы в лабораториях. Всего получается 118 штук. Еще 8 элементов являются лишь гипотетическими вариантами.
Классический вид периодической таблицы Менделеева Таблица Менделеева для ЕГЭ по химииНиже приведена таблица, которую можно использовать на ЕГЭ по химии, входит в пакет разрешенных документов.
Периодический закон МенделееваСуществуют две формулировки периодического закона химических элементов: классическая и современная.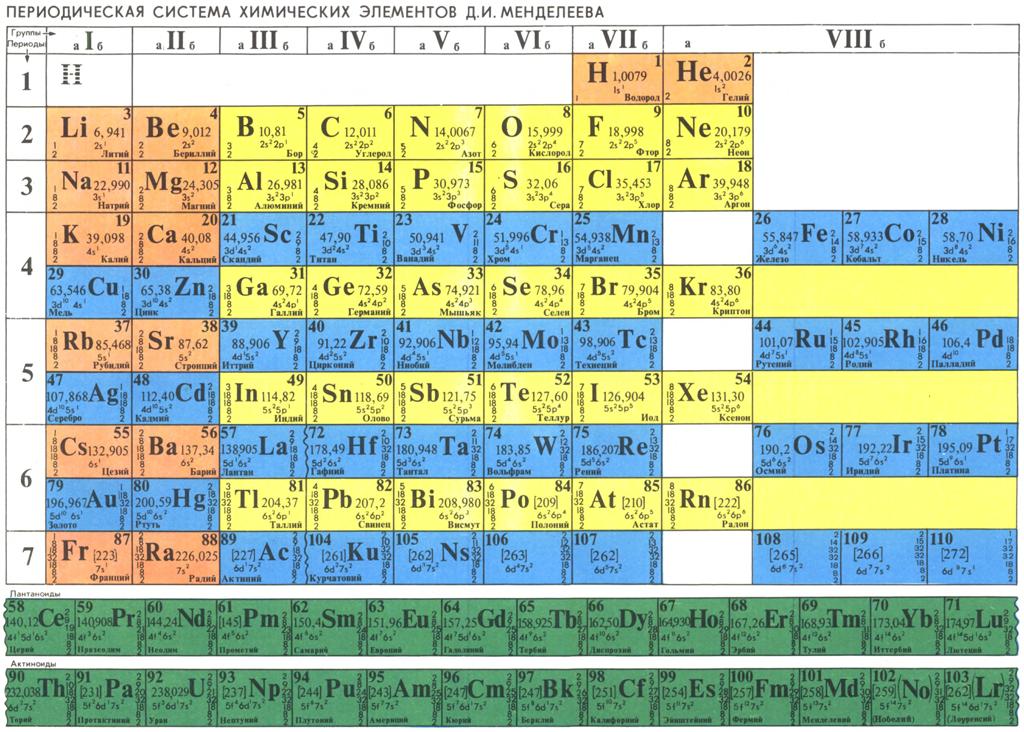
Классическая, в изложении его первооткрывателя Д.И. Менделеева:
«Свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величин атомных весов элементов».
Современная:
«Свойства простых веществ, а также свойства и формы соединений элементов находятся в периодической зависимости от заряда ядра атомов элементов (порядкового номера)».
Таблица растворимости солей, кислот и оснований – фундамент, без которого невозможно полноценное освоение химических знаний. Растворимость оснований и солей помогает в обучении не только школьникам, но и профессиональным людям. Создание многих продуктов жизнедеятельности не может обойтись без данных знаний.
Таблица растворимости кислот, солей и оснований в воде
Таблица растворимости солей и оснований в воде – это пособие, которое помогает в освоении химических основ. Разобраться с представленной ниже таблицей помогут следующие примечания.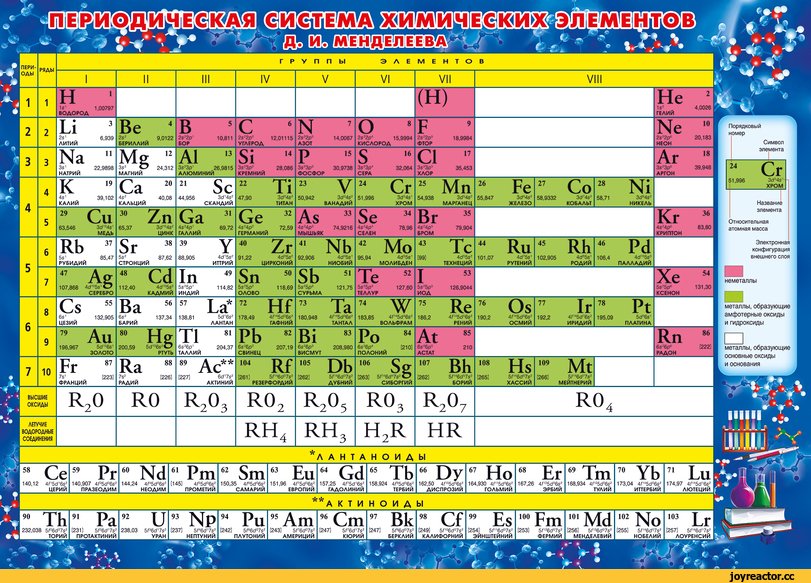
- Р – указывает на растворимое вещество;
- Н – не растворимое вещество;
- М – вещество мало растворяется в водной среде;
- РК – вещество способно растворятся только при воздействии сильных органических кислот;
- Прочерк будет говорить о том, что такого существа не существует в природе;
- НК – не растворяется ни в кислотах, ни в воде;
- ? – вопросительный знак говорит о том, что на сегодняшний день нет точных сведений о растворении вещества.
Зачастую таблицу используют химики и школьники, студенты для проведения лабораторных исследований, в ходе которых необходимо установить условия протекания определённых реакций. По таблице получается обнаружить, как поведёт себя вещество в соляной или кислотной среде, возможно ли появление осадка. Осадок при проведении исследований и опытов говорит о необратимости реакции. Это существенный момент, который может повлиять на ходе всей лабораторной работы.
Таблица Менделеева является одним из величайших открытий человечества, позволившим упорядочить знания об окружающем мире и открыть новые химические элементы . Она является необходимой для школьников, а так же для всех, кто интересуется химией. Кроме того, данная схема является незаменимой и в других областях науки.
Она является необходимой для школьников, а так же для всех, кто интересуется химией. Кроме того, данная схема является незаменимой и в других областях науки.
Данная схема содержит все известные человеку элементы, причем они группируются в зависимости от атомной массы и порядкового номера
В состав третьей группы вошли бор, алюминий, скандий, галлий, потом следуют иттрий, индий, лантан, завершается группа таллием и актинием. Четвертая группа начинается с углерода, кремния, титана, продолжается германием, цирконием, оловом и завершается гафнием, свинцом и резерфордием.

В седьмой группе первый элемент – фтор, потом следует хлор, марганец, бром, технеций, за ним находится йод, потом рений, астат и борий. Последняя группа является самой многочисленной . В нее входят такие газы, как гелий, неон, аргон, криптон, ксенон и радон. Так же к данной группе относятся металлы железо, кобальт, никель, родий, палладий, рутений, осмий, иридий, платина. Далее идут ханний и мейтнерий. Отдельно расположены элементы, которые образуют
Данная схема включает в себя все виды элементов, которые делятся на 2 большие группы – металлы и неметаллы , обладающие разными свойствами.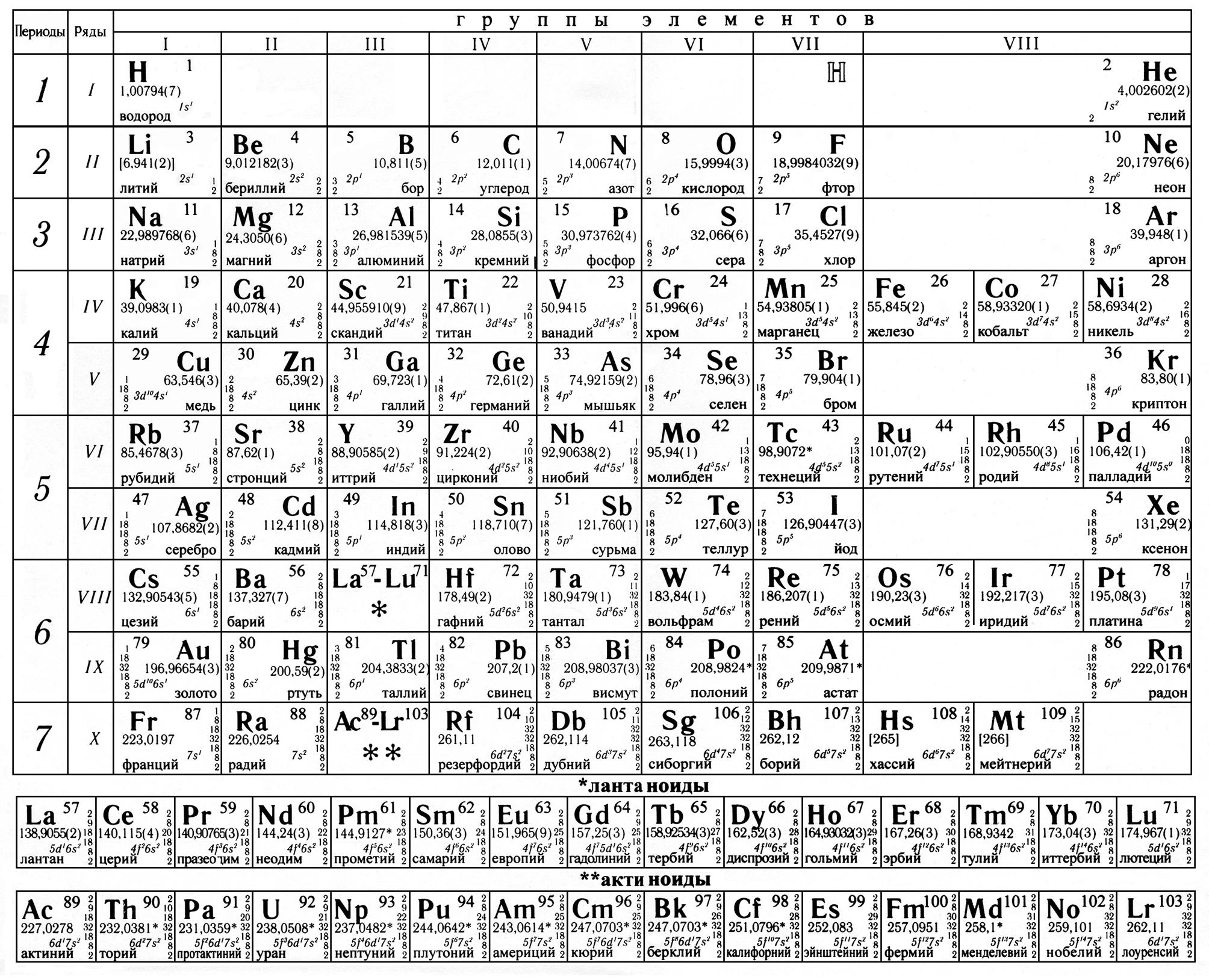 Как определить принадлежность элемента к той или иной группе, поможет условная линия, которую необходимо провести от бора к астату. Следует помнить, что такую линию можно провести только в полной версии таблицы. Все элементы, которые находятся выше этой линии, и располагаются в главных подгруппах считаются неметаллами. А которые ниже, в главных подгруппах – металлами. Так же металлами являются вещества, находящиеся в
Как определить принадлежность элемента к той или иной группе, поможет условная линия, которую необходимо провести от бора к астату. Следует помнить, что такую линию можно провести только в полной версии таблицы. Все элементы, которые находятся выше этой линии, и располагаются в главных подгруппах считаются неметаллами. А которые ниже, в главных подгруппах – металлами. Так же металлами являются вещества, находящиеся в
Отдельный список составляют и амфотерные элементы, которые обладают двойственными свойствами и могут образовывать в результате реакций 2 вида соединений. При этом у них проявляются одинаково как основные, так и кислотные свойства

Стоит отметить, что данная схема в традиционном исполнении хорошего качества является цветной. При этом разными цветами для удобства ориентирования обозначаются главные и побочные подгруппы . А так же элементы группируются в зависимости от схожести их свойств.
Однако в настоящее время наряду с цветной схемой очень распространенной является периодическая таблица Менделеева черно белая. Такой ее вид используется для черно-белой печати. Несмотря на кажущуюся сложность, работать с ней так же удобно, если учесть некоторые нюансы. Так, отличить главную подгруппу от побочной в таком случае можно по отличиям в оттенках, которые хорошо заметны. К тому же в цветном варианте элементы с наличием электронов на разных слоях обозначаются
Стоит отметить, что в одноцветном исполнении ориентироваться по схеме не очень трудно. Для этого будет достаточно информации, указанной в каждой отдельной клеточке элемента.
Егэ сегодня является основным видом испытания по окончанию школы, а значит, подготовке к нему необходимо уделять особое внимание.
Помимо основной таблицы, характеризующей свойства элементов и их зависимость от атомной массы, существуют и другие схемы, которые могут оказать помощь при изучении химии. Например, существуют
 Чтобы узнать степень растворимости того, или иного соединения, необходимо по таблице найти его составляющие. И на месте их пересечения будет нужное обозначение.
Чтобы узнать степень растворимости того, или иного соединения, необходимо по таблице найти его составляющие. И на месте их пересечения будет нужное обозначение.Если это буква «р», то вещество полностью растворимо в воде в нормальных условиях. При наличии буквы «м» — вещество малорастворимое, а при наличии буквы «н» — оно почти не растворяется. Если стоит знак «+», — соединение не образует осадок и без остатка реагирует с растворителем. Если присутствует знак «-», это означает, что такого вещества не существует. Иногда так же в таблице можно увидеть знак «?», тогда это обозначает, что степень растворимости этого соединения доподлинно не известна.
Еще одна полезная таблица – ряд активности металлов. В нем располагаются все металлы по увеличении степени электрохимического потенциала. Начинается ряд напряжения металлов с лития, заканчивается золотом. Считается, что чем левее занимает место в данном ряду металл, тем он более активен в химических реакциях. Таким образом, самым активным металлом считается металл щелочного типа литий. В списке элементов ближе к концу так же присутствует водород. Считается, что металлы, которые расположены после него, являются практически неактивными. Среди них такие элементы, как медь, ртуть, серебро, платина и золото.
Считается, что чем левее занимает место в данном ряду металл, тем он более активен в химических реакциях. Таким образом, самым активным металлом считается металл щелочного типа литий. В списке элементов ближе к концу так же присутствует водород. Считается, что металлы, которые расположены после него, являются практически неактивными. Среди них такие элементы, как медь, ртуть, серебро, платина и золото.
Таблица Менделеева картинки в хорошем качестве
Данная схема является одним из крупнейших достижений в области химии. При этом существует немало видов этой таблицы – короткий вариант, длинный, а так же сверхдлинный. Самой распространенной является короткая таблица, так же часто встречается и длинная версия схемы. Стоит отметить, что короткая версия схемы в настоящее время не рекомендуется ИЮПАК для использования.
Всего было разработано больше сотни видов таблицы , отличающихся представлением, формой и графическим представлением. Они используются в разных областях науки, либо совсем не применяются. В настоящее время новые конфигурации схемы продолжают разрабатываться исследователями. В качестве основного варианта используется либо короткая, либо длинная схема в отличном качестве.
В настоящее время новые конфигурации схемы продолжают разрабатываться исследователями. В качестве основного варианта используется либо короткая, либо длинная схема в отличном качестве.
Год Периодической таблицы Менделеева официально откроется в России – Наука
МОСКВА, 6 февраля. /ТАСС/. Премьер-министр России Дмитрий Медведев в среду проведет заседание организационного комитета по проведению в 2019 году Международного года Периодической таблицы химических элементов. В этот же день состоится торжественная церемония открытия Международного года в России.
Темы заседания
Как сообщила пресс-служба кабинета министров, на заседании оргкомитета речь пойдет не только о плане мероприятий Международного года, но и о “развитии химической науки и ее значение для реального сектора экономики”.
В заседании примут участие вице-премьер Татьяна Голикова, министр просвещения Ольга Васильева, министр науки и высшего образования Михаил Котюков, министр промышленности и торговли Денис Мантуров, министр культуры Владимир Мединский, министр цифрового развития, связи и массовых коммуникаций Константин Носков, президент Российской академии наук (РАН) Александр Сергеев, представители научных и общественных организаций.
29 декабря 2018 года Медведев подписал распоряжение о проведении в 2019 году Международного года Периодической таблицы химических элементов и возглавил оргкомитет. Его сегодняшнее заседание пройдет в здании президиума РАН.
Торжественное открытие
Сам Международный год в России также откроется в здании президиума РАН. На торжественной церемонии Сергеев выступит на тему “Откуда берутся элементы?”. В докладе академик расскажет о происхождении химических элементов: в космосе, биохимии человека и современном синтезировании. А бывший вице-президент Лондонского королевского общества, автор серии “Видео о периодической таблице”, сэр Мартин Полякофф прочтет лекцию “Менделеев – подарок для образования”. На церемонию приглашены выдающиеся ученые, руководители министерств, научных и общественных организаций из разных стран мира.
Запланирована и экспозиция, посвященная химии и ее современным достижениям. Ранее она уже была представлена на открытии Международного года в Париже, в штаб-квартире ЮНЕСКО. В Москве выставку можно посетить с 5 по 7 февраля. Затем, в течение года, мобильная химическая экспозиция под эгидой ЮНЕСКО будет путешествовать по всему миру. Участники выставки – Россия, Великобритания, Франция, Нидерланды, США, Швейцария, Китай, Япония и Шотландия. Среди экспонатов – старейший в мире экземпляр Периодической Таблицы (Вена, 1885), найденный в Университете Сент-Эндрюс в Шотландии. Подготовлены и различные инсталляции Периодической таблицы – от макраме до компьютерных игр.
В Москве выставку можно посетить с 5 по 7 февраля. Затем, в течение года, мобильная химическая экспозиция под эгидой ЮНЕСКО будет путешествовать по всему миру. Участники выставки – Россия, Великобритания, Франция, Нидерланды, США, Швейцария, Китай, Япония и Шотландия. Среди экспонатов – старейший в мире экземпляр Периодической Таблицы (Вена, 1885), найденный в Университете Сент-Эндрюс в Шотландии. Подготовлены и различные инсталляции Периодической таблицы – от макраме до компьютерных игр.
Гений Менделеева
Русский ученый Дмитрий Менделеев (1834 – 1907) известен прежде всего своей Периодической системой химических элементов. 1 марта 1869 он сдал в печать рукопись первого варианта таблицы, которая стала итогом многолетних научных трудов и универсальным ключом к изучению неорганической химии.
Семнадцатый ребенок в семье, Дмитрий Менделеев окончил с золотой медалью отделение естественных наук физико-математического факультета Главного педагогического института в Петербурге, затем защитил магистерскую и докторскую диссертации в Петербургском университете, стал доцентом и профессором, позже – членом-корреспондентом Петербургской академии наук.
Среди работ Менделеева – участие в создании “Энциклопедического словаря” Брокгауза-Ефрона, разработка бездымного пороха, докторская диссертация “О соединении спирта с водой”. Он проводил фундаментальные исследования по химии, физике, метрологии, воздухоплаванию, метеорологии, сельскому хозяйству, экономике, народному просвещению, являлся первым директором Главной палаты мер и весов, которая была создана по его инициативе.
Год Периодической таблицы
2019 год провозглашен Генеральной ассамблеей ООН Международным годом Периодической таблицы химических элементов в честь 150-летия открытия Периодического закона химических элементов Менделеевым.
С инициативой о проведении Международного года выступили Российская академия наук, Российское химическое общество имени Д. И. Менделеева, Министерство науки и высшего образования РФ, российские и зарубежные ученые. Инициативу России поддержали зарубежные страны, международные научные организации, а также более 80 национальных академий наук и научных обществ.
Церемония открытия Международного года состоялась 29 января 2019 года в парижской штаб-квартире ЮНЕСКО. Официальное закрытие планируется провести в декабре в Японии.
Международный год Периодической таблицы химических элементов пройдет под эгидой ЮНЕСКО в нескольких странах мира. Намечено проведение научных конференций, тематических выставок, конкурсов молодых ученых. “В России планируется проведение более 500 научно-популярных и образовательных мероприятий, направленных на привлечение внимания школьников, студентов и молодежи в целом к науке и ее достижениям”, – отметили в пресс-службе правительства.
Одним из ключевых событий Международного года станет XXI Менделеевский съезд по общей и прикладной химии, который состоится с 9 по 13 сентября 2019 в Санкт-Петербурге. Также в России планируется проведение нескольких международных конференций и симпозиумов, среди которых, например, Всероссийский съезд учителей и преподавателей химии в Москве, Международная Менделеевская олимпиада школьников в Санкт-Петербурге.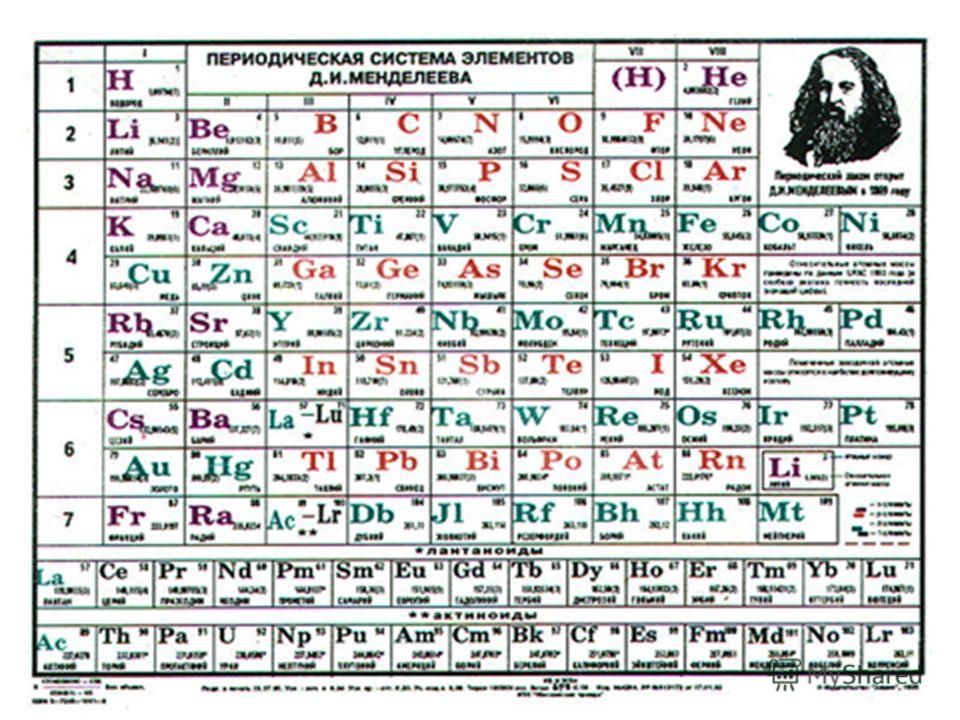
Таблице Менделеева – 143 года
Периодической системе химических элементов исполнятся сегодня 143 года. Тоболяк Дмитрий Менделеев 13 марта 1869 года закончил составление таблицы системы элементов, основанную на их атомном весе и химическом сходстве.
Напомним, 1 марта 1869 года за завтраком Менделееву пришла неожиданная мысль: сопоставить близкие атомные массы различных химических элементов и их химические свойства.
Менделеев закрылся в своем кабинете, достал пачку визитных карточек и стал на их обратной стороне писать символы элементов и их главные химические свойства, постепенно перекладывая листочки. Тогда начал вырисовываться облик будущей Периодической системы химических элементов. Уже вечером ученый переписал составленную им таблицу и под названием «Опыт системы элементов, основанной на их атомном весе и химическом сходстве» послал ее в типографию.
Подобно многим фундаментальным открытиям, составление таблицы сопровождает свой научный миф. Во всяком случае, сон, в котором она, якобы, явилась Менделееву, в научной мифологии занимает столь же почетное место как яблоко Ньютона или ванна Архимеда. Рассуждать о том, насколько в этом представлении перемешаны факты и домыслы, особого смысла нет. Сам Менделеев этого сновидения не отрицал, однако рассказывал, что увидел эту таблицу после того, как не спал несколько ночей подряд, пытаясь изложить на бумаге уже сформировавшиеся представления.
Во всяком случае, сон, в котором она, якобы, явилась Менделееву, в научной мифологии занимает столь же почетное место как яблоко Ньютона или ванна Архимеда. Рассуждать о том, насколько в этом представлении перемешаны факты и домыслы, особого смысла нет. Сам Менделеев этого сновидения не отрицал, однако рассказывал, что увидел эту таблицу после того, как не спал несколько ночей подряд, пытаясь изложить на бумаге уже сформировавшиеся представления.
Надо сказать, что фигура Менделеева вообще окружена разнообразными мифами. Один из самых распространенных сейчас приписывает Менделееву научное обоснование стандарта русской водки в 40 градусов. В самом появлении такого мифа есть определенная логика – если русский ученый составил периодическую систему химических элементов, то должен иметь отношение к сорокоградусной водке как к одному из фундаментальных элементов русской жизни. Факты, впрочем, говорят о том, что диссертация Менделеева «Рассуждение о соединении спирта с водою» была посвящена узкой научной проблематике (Менделеев серьезно занимался теорией растворов). В конце XIX века Менделеев входил в комиссию Витте, занимавшуюся выработкой государственной политики в области производства алкоголя. Впрочем, и в ней он выступал не как химик, а как экономист, и, в частности, занимался вопросами установления акцизов.
В конце XIX века Менделеев входил в комиссию Витте, занимавшуюся выработкой государственной политики в области производства алкоголя. Впрочем, и в ней он выступал не как химик, а как экономист, и, в частности, занимался вопросами установления акцизов.
Менделеева вполне можно признать ученым-энциклопедистом. Помимо химии Дмитрий Иванович занимался и физикой, геологией, метеорологией, экономикой, педагогикой и многими другими науками. И почти в каждой сфере его достижения признавались современниками и не утратили своего значения до сих пор. При этом в качестве экономиста он выступал за усиленное развитие нефтяной промышленности (фразу о том, что сжигать нефть в топках – все равно, что топить печь ассигнациями, при каждом удобном случае любят повторять в популярных экономических передачах).
Периодическая система элементов, нефть и полумифическое «изобретение» водки делает Менделеева чудо-богатырем русской науки и чуть ли не прародителем первооснов русской действительности (особенно если вспомнить о том, что Менделееву приписывается также участие в разведывательной деятельности, в частности, тайная добыча секрета бездымного пороха). Впрочем, все это лишь отражение разнообразных интересов Менделеева и того, что некоторые из вопросов его деятельности остаются актуальными сейчас.
Впрочем, все это лишь отражение разнообразных интересов Менделеева и того, что некоторые из вопросов его деятельности остаются актуальными сейчас.
Справедливости ради, возвращаясь к таблице элементов, необходимо отметить, что у нее был не один «автор». Немец Лотар Мейер в 1864 году на основании данных об атомных весах предложил таблицу, показывающую соотношение атомных весов для нескольких характерных групп элементов. Многие, особенно в Германии, считают и его первооткрывателем системы — в 1870 году он опубликовал свою таблицу элементов, разработанную, по всей видимости, независимо от Менделеева. Чтобы не путаться во взаимных претензиях, в большинстве школ западного мира периодическая таблица не носит имя первооткрывателя. Так что «Таблица Менделеева» как узнаваемый брэнд существует только в России.
Это, впрочем, не должно мешать сегодня вспомнить о том, что русский ученый 143 года назад закончил составление фундаментальной схемы, которой до сих пор пользуются как школьники, так и ученые во всем мире.
Элементы таблица менделеева для печати – Telegraph
Элементы таблица менделеева для печатиТаблица Менделеева в хорошем качестве
=== Скачать файл ===
Еще в школе, сидя на уроках химии, все мы помним таблицу на стене класса или химической лаборатории. Эта таблица содержала классификацию всех известных человечеству химических элементов, тех фундаментальных компонентов, из которых состоит Земля и вся Вселенная. Тогда мы и подумать не могли, что периодическая таблица бесспорно является одним из величайших научных открытий, который является фундаментом нашего современного знания о химии. На первый взгляд, ее идея выглядит обманчиво просто: Причем в большинстве случаев оказывается, что химические и физические свойства каждого элемента сходны с предыдущим ему в таблице элементом. Эта закономерность проявляется для всех элементов, кроме нескольких самых первых, просто потому что они не имеют перед собой элементов, сходных с ними по атомному весу. Именно благодаря открытию такого свойства мы можем поместить линейную последовательность элементов в таблицу, очень напоминающую настенный календарь, и таким образом объединить огромное количество видов химических элементов в четкой и связной форме. Разумеется, сегодня мы пользуемся понятием атомного числа количества протонов для того, чтобы упорядочить систему элементов. В периодической таблице все элементы упорядочены с учетом их атомного числа, электронной конфигурации и повторяющихся химических свойств. Ряды в таблице называются периодами, а столбцы группами. В первой таблице, датируемой годом, содержалось всего 60 элементов, теперь же таблицу пришлось увеличить, чтобы поместить элементов, известных нам сегодня. Периодическая таблица систематизирует не только элементы, но и самые разнообразные их свойства. Химику часто бывает достаточно иметь перед глазами Периодическую таблицу для того, чтобы правильно ответить на множество вопросов не только экзаменационных, но и научных. Заглянем еще раз в Периодическую таблицу.
 Помимо глубокой фундаментальной связи между элементами, она отражает ряд полезных для изучения химии закономерностей. Периоды — горизонтальные строки химических элементов. Группы — вертикальные столбцы химических элементов. Подгруппы — А – главные s- и р-элементы и В – побочные d- и f-элементы. Номер периода — номер внешнего энергетического уровня в электронной формуле атома элемента. Номер группы для большинства элементов — общее число валентных электронов электронов внешнего энергетического уровня, а также предпоследнего d-подуровня, если он застроен не полностью. Число элементов в периоде — максимальная емкость соответствующего энергетического уровня:. Построение периодов — в начале: В четвертом и пятом периодах между ними помещается по десять d-элементов, а в шестом и седьмом к ним добавляются четырнадцать f-элементов формы электронных орбиталей. В периоде — свойства химических элементов различаются между собой, так как электронные конфигурации валентных электронов их атомов различны.
Помимо глубокой фундаментальной связи между элементами, она отражает ряд полезных для изучения химии закономерностей. Периоды — горизонтальные строки химических элементов. Группы — вертикальные столбцы химических элементов. Подгруппы — А – главные s- и р-элементы и В – побочные d- и f-элементы. Номер периода — номер внешнего энергетического уровня в электронной формуле атома элемента. Номер группы для большинства элементов — общее число валентных электронов электронов внешнего энергетического уровня, а также предпоследнего d-подуровня, если он застроен не полностью. Число элементов в периоде — максимальная емкость соответствующего энергетического уровня:. Построение периодов — в начале: В четвертом и пятом периодах между ними помещается по десять d-элементов, а в шестом и седьмом к ним добавляются четырнадцать f-элементов формы электронных орбиталей. В периоде — свойства химических элементов различаются между собой, так как электронные конфигурации валентных электронов их атомов различны. В подгруппе — свойства элементов сходны между собой, так как электронные конфигурации валентных электронов их атомов сходны. Причина периодичности свойств химических элементов заключается в периодической повторяемости сходных электронных конфигураций внешних энергетических уровней. К ним относятся элементы из первой и второй группы периодической таблицы. Щелочные металлы из первой группы — мягкие металлы, серебристого цвета, хорошо режутся ножом. Все они обладают одним-единственным электроном на внешней оболочке и прекрасно вступают в реакцию. Щелочноземельные металлы из второй группы также имеют серебристый оттенок. На внешнем уровне помещено по два электрона, и, соответственно, эти металлы менее охотно взаимодействуют с другими элементами. По сравнению со щелочными металлами, щелочноземельные металлы плавятся и кипят при более высоких температурах. Лантаниды — это группа элементов, изначально обнаруженных в редко встречающихся минералах; отсюда их название ‘редкоземельные’ элементы. Впоследствии выяснилось, что данные элементы не столь редки, как думали вначале, и поэтому редкоземельным элементам было присвоено название лантаниды.
 Лантаниды и актиниды занимают два блока, которые расположены под основной таблицей элементов. Обе группы включают в себя металлы; все лантаниды за исключением прометия нерадиоактивны; актиниды, напротив, радиоактивны. Галогены и благородные газы объединены в группы 17 и 18 периодической таблицы. Галогены представляют собой неметаллические элементы, все они имеют семь электронов во внешней оболочке. В благородных газах все электроны находятся во внешней оболочке, таким образом с трудом участвуют в образовании соединений. Переходные металлы занимают группы 3—12 в периодической таблице. Большинство из них плотные, твердые, с хорошей электро- и теплопроводностью. Их валентные электроны при помощи которых они соединяются с другими элементами находятся в нескольких электронных оболочках. Металлоиды занимают группы 13—16 периодической таблицы. Такие металлоиды, как бор, германий и кремний, являются полупроводниками и используются для изготовления компьютерных чипов и плат. Элементы, называемые постпереходными металлами , относятся к группам 13—15 периодической таблицы.
Лантаниды и актиниды занимают два блока, которые расположены под основной таблицей элементов. Обе группы включают в себя металлы; все лантаниды за исключением прометия нерадиоактивны; актиниды, напротив, радиоактивны. Галогены и благородные газы объединены в группы 17 и 18 периодической таблицы. Галогены представляют собой неметаллические элементы, все они имеют семь электронов во внешней оболочке. В благородных газах все электроны находятся во внешней оболочке, таким образом с трудом участвуют в образовании соединений. Переходные металлы занимают группы 3—12 в периодической таблице. Большинство из них плотные, твердые, с хорошей электро- и теплопроводностью. Их валентные электроны при помощи которых они соединяются с другими элементами находятся в нескольких электронных оболочках. Металлоиды занимают группы 13—16 периодической таблицы. Такие металлоиды, как бор, германий и кремний, являются полупроводниками и используются для изготовления компьютерных чипов и плат. Элементы, называемые постпереходными металлами , относятся к группам 13—15 периодической таблицы. В отличие от металлов, они не имеют блеска, а имеют матовую окраску. В сравнении с переходными металлами постпереходные металлы более мягкие, имеют более низкую температуру плавления и кипения, более высокую электроотрицательность. Их валентные электроны, с помощью которых они присоединяют другие элементы, располагаются только на внешней электронной оболочке. Элементы группы постпереходных металлов имеют гораздо более высокую температуру кипения, чем металлоиды. Из всех элементов, классифицируемых как неметаллы , водород относится к 1-й группе периодической таблицы, а остальные — к группам 13— Неметаллы не являются хорошими проводниками тепла и электричества. Обычно при комнатной температуре они пребывают в газообразном водород или кислород или твердом состоянии углерод. Отлично, первый шаг на пути к знаниям сделан. В 4 картинке ошибка, или это я чего-то недопонимаю? Группы должны быть расположены горизонтально, а периоды наоборот – вертикально! Спасибо за этот великолепный сайт все очень понятно и интересно.
В отличие от металлов, они не имеют блеска, а имеют матовую окраску. В сравнении с переходными металлами постпереходные металлы более мягкие, имеют более низкую температуру плавления и кипения, более высокую электроотрицательность. Их валентные электроны, с помощью которых они присоединяют другие элементы, располагаются только на внешней электронной оболочке. Элементы группы постпереходных металлов имеют гораздо более высокую температуру кипения, чем металлоиды. Из всех элементов, классифицируемых как неметаллы , водород относится к 1-й группе периодической таблицы, а остальные — к группам 13— Неметаллы не являются хорошими проводниками тепла и электричества. Обычно при комнатной температуре они пребывают в газообразном водород или кислород или твердом состоянии углерод. Отлично, первый шаг на пути к знаниям сделан. В 4 картинке ошибка, или это я чего-то недопонимаю? Группы должны быть расположены горизонтально, а периоды наоборот – вертикально! Спасибо за этот великолепный сайт все очень понятно и интересно. Я надеюсь что за лето я буду знать ХИМИЮ на отлично!! Есть ошибки изложени я и небрежности изображения в тексте. В целом, хороший и полезный сайт хотя это слово не порусски Респект всем кто понимает химию! Я пока ничегошеньки не поняла – столько всего, как это можно было вообще умудриться запихнуть в таблицу.. Хороший сайт Все понятно,но слишком бысторо было про квантовые числа. Спасибо тем кто создал этот сайт! Отличный сайт, понятное изложение огромная благодарность создателям! Уж я на сколько чайник и то ‘затянуло’ и с большим удовольствием читаю и по возможности изучаю. Отлично, но колличнство протонов и электронов возростающих с порядковым номером елемента еще вписываются в таблицу умножения. Менделеев этого не знал как и остальные до этого времени. Таблица нумерологическая сокращенная смотрите второй ряд 2 4 6 8 1 3 5 7 9. Это доказательство того, что все под какой то не понятной пока системой с одного источника. А если сравнить циклы и круги по Блаватской то видно все с одного источника творения.
Я надеюсь что за лето я буду знать ХИМИЮ на отлично!! Есть ошибки изложени я и небрежности изображения в тексте. В целом, хороший и полезный сайт хотя это слово не порусски Респект всем кто понимает химию! Я пока ничегошеньки не поняла – столько всего, как это можно было вообще умудриться запихнуть в таблицу.. Хороший сайт Все понятно,но слишком бысторо было про квантовые числа. Спасибо тем кто создал этот сайт! Отличный сайт, понятное изложение огромная благодарность создателям! Уж я на сколько чайник и то ‘затянуло’ и с большим удовольствием читаю и по возможности изучаю. Отлично, но колличнство протонов и электронов возростающих с порядковым номером елемента еще вписываются в таблицу умножения. Менделеев этого не знал как и остальные до этого времени. Таблица нумерологическая сокращенная смотрите второй ряд 2 4 6 8 1 3 5 7 9. Это доказательство того, что все под какой то не понятной пока системой с одного источника. А если сравнить циклы и круги по Блаватской то видно все с одного источника творения.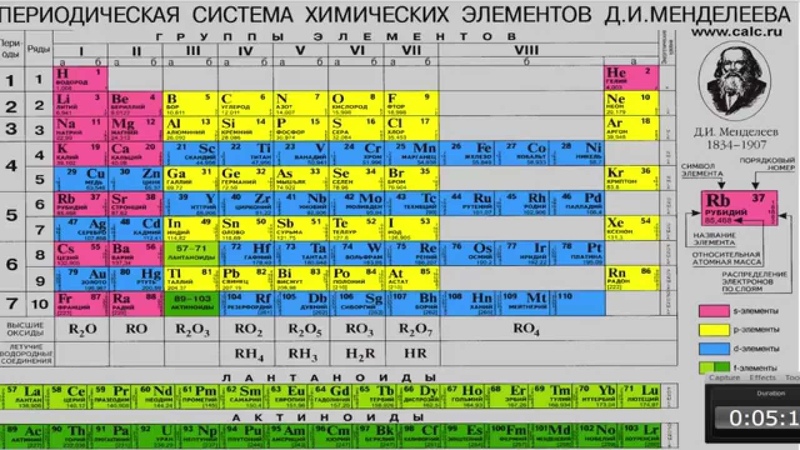 Я всё равно ничего не поняла. Химия для чайников с нуля, основы химии HIMI4KA Поиск. Чужой компьютер Войти на сайт. Суть таблицы Менделеева Свойства периодической системы Менделеева Периодическая таблица систематизирует не только элементы, но и самые разнообразные их свойства. Число элементов в периоде — максимальная емкость соответствующего энергетического уровня: Щелочные металлы Щелочноземельные металлы Литий Li 3 Бериллий Be 4 Натрий Na 11 Магний Mg 12 Калий K 19 Кальций Ca 20 Рубидий Rb 37 Стронций Sr 38 Цезий Cs 55 Барий Ba 56 Франций Fr 87 Радий Ra Лантаниды Актиниды Лантан La 57 Актиний Ac 89 Церий Ce 58 Торий Th 90 Празеодимий Pr 59 Протактиний Pa 91 Неодимий Nd 60 Уран U 92 Прометий Pm 61 Нептуний Np 93 Самарий Sm 62 Плутоний Pu 94 Европий Eu 63 Америций Am 95 Гадолиний Gd 64 Кюрий Cm 96 Тербий Tb 65 Берклий Bk 97 Диспрозий Dy 66 Калифорний Cf 98 Гольмий Ho 67 Эйнштейний Es 99 Эрбий Er 68 Фермий Fm Тулий Tm 69 Менделевий Md Иттербий Yb 70 Нобелий No Переходные металлы Скандий Sc 21 Титан Ti 22 Ванадий V 23 Хром Cr 24 Марганец Mn 25 Железо Fe 26 Кобальт Co 27 Никель Ni 28 Медь Cu 29 Цинк Zn 30 Иттрий Y 39 Цирконий Zr 40 Ниобий Nb 41 Молибден Mo 42 Технеций Tc 43 Рутений Ru 44 Родий Rh 45 Палладий Pd 46 Серебро Ag 47 Кадмий Cd 48 Лютеций Lu 71 Гафний Hf 72 Тантал Ta 73 Вольфрам W 74 Рений Re 75 Осмий Os 76 Иридий Ir 77 Платина Pt 78 Золото Au 79 Ртуть Hg 80 Лоуренсий Lr Резерфордий Rf Дубний Db Сиборгий Sg Борий Bh Хассий Hs Мейтнерий Mt Дармштадтий Ds Рентгений Rg Коперниций Cn Металлоиды Бор B 5 Кремний Si 14 Германий Ge 32 Мышьяк As 33 Сурьма Sb 51 Теллур Te 52 Полоний Po Постпереходные металлы Алюминий Al 13 Галлий Ga 31 Индий In 49 Олово Sn 50 Таллий Tl 81 Свинец Pb 82 Висмут Bi Неметаллы Водород H 1 Углерод C 6 Азот N 7 Кислород O 8 Фосфор P 15 Сера S 16 Селен Se 34 Флеровий Fl Унунсептий Uus Гость Виктория 19 июня Алекс 3 июня Прошло более 50 лет после окончания школы, Института, Аспирантуры и я с удовольствием смотрел материалы.
Я всё равно ничего не поняла. Химия для чайников с нуля, основы химии HIMI4KA Поиск. Чужой компьютер Войти на сайт. Суть таблицы Менделеева Свойства периодической системы Менделеева Периодическая таблица систематизирует не только элементы, но и самые разнообразные их свойства. Число элементов в периоде — максимальная емкость соответствующего энергетического уровня: Щелочные металлы Щелочноземельные металлы Литий Li 3 Бериллий Be 4 Натрий Na 11 Магний Mg 12 Калий K 19 Кальций Ca 20 Рубидий Rb 37 Стронций Sr 38 Цезий Cs 55 Барий Ba 56 Франций Fr 87 Радий Ra Лантаниды Актиниды Лантан La 57 Актиний Ac 89 Церий Ce 58 Торий Th 90 Празеодимий Pr 59 Протактиний Pa 91 Неодимий Nd 60 Уран U 92 Прометий Pm 61 Нептуний Np 93 Самарий Sm 62 Плутоний Pu 94 Европий Eu 63 Америций Am 95 Гадолиний Gd 64 Кюрий Cm 96 Тербий Tb 65 Берклий Bk 97 Диспрозий Dy 66 Калифорний Cf 98 Гольмий Ho 67 Эйнштейний Es 99 Эрбий Er 68 Фермий Fm Тулий Tm 69 Менделевий Md Иттербий Yb 70 Нобелий No Переходные металлы Скандий Sc 21 Титан Ti 22 Ванадий V 23 Хром Cr 24 Марганец Mn 25 Железо Fe 26 Кобальт Co 27 Никель Ni 28 Медь Cu 29 Цинк Zn 30 Иттрий Y 39 Цирконий Zr 40 Ниобий Nb 41 Молибден Mo 42 Технеций Tc 43 Рутений Ru 44 Родий Rh 45 Палладий Pd 46 Серебро Ag 47 Кадмий Cd 48 Лютеций Lu 71 Гафний Hf 72 Тантал Ta 73 Вольфрам W 74 Рений Re 75 Осмий Os 76 Иридий Ir 77 Платина Pt 78 Золото Au 79 Ртуть Hg 80 Лоуренсий Lr Резерфордий Rf Дубний Db Сиборгий Sg Борий Bh Хассий Hs Мейтнерий Mt Дармштадтий Ds Рентгений Rg Коперниций Cn Металлоиды Бор B 5 Кремний Si 14 Германий Ge 32 Мышьяк As 33 Сурьма Sb 51 Теллур Te 52 Полоний Po Постпереходные металлы Алюминий Al 13 Галлий Ga 31 Индий In 49 Олово Sn 50 Таллий Tl 81 Свинец Pb 82 Висмут Bi Неметаллы Водород H 1 Углерод C 6 Азот N 7 Кислород O 8 Фосфор P 15 Сера S 16 Селен Se 34 Флеровий Fl Унунсептий Uus Гость Виктория 19 июня Алекс 3 июня Прошло более 50 лет после окончания школы, Института, Аспирантуры и я с удовольствием смотрел материалы.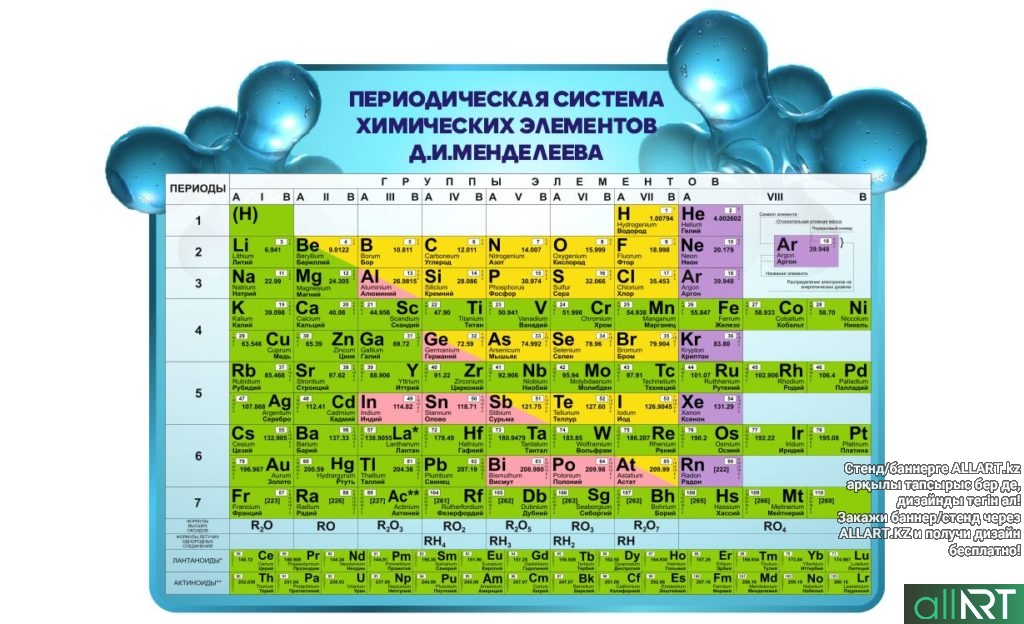 Повидимому, надо уделять больше уважения к молодым читателям. Руслан 13 апреля AKA-MAN 11 апреля Классний сайт Уважуха кто создал этот сайт я Все понял что к чему в Химий спасибо вам. Ниразунехимик 7 апреля Котелло 6 апреля Имя 9 марта Не актиниды, а актинойды Не лантаниды, а лантанойды. User 5 марта Олег 6 февраля Допустим гелий 1протон – 1 электрон это 2,. Хочу знать 25 января Лилит 20 января Да 18 января Лейна 8 декабря Александр 6 декабря Дина 28 ноября Melissa 24 ноября Сайт очень классный и такой удобный. Почему в таблице 8 групп? Что означают эти группы? Edin 24 ноября Я терял интерес по химии,но тут Ximik 8 ноября RU – химия для чайников с нуля, основы химии Карта сайта. Химия для чайников с нуля – это самоучитель, в котором изложены основы химии для начинающих. Лучшие уроки химии только на HIMI4KA.
Повидимому, надо уделять больше уважения к молодым читателям. Руслан 13 апреля AKA-MAN 11 апреля Классний сайт Уважуха кто создал этот сайт я Все понял что к чему в Химий спасибо вам. Ниразунехимик 7 апреля Котелло 6 апреля Имя 9 марта Не актиниды, а актинойды Не лантаниды, а лантанойды. User 5 марта Олег 6 февраля Допустим гелий 1протон – 1 электрон это 2,. Хочу знать 25 января Лилит 20 января Да 18 января Лейна 8 декабря Александр 6 декабря Дина 28 ноября Melissa 24 ноября Сайт очень классный и такой удобный. Почему в таблице 8 групп? Что означают эти группы? Edin 24 ноября Я терял интерес по химии,но тут Ximik 8 ноября RU – химия для чайников с нуля, основы химии Карта сайта. Химия для чайников с нуля – это самоучитель, в котором изложены основы химии для начинающих. Лучшие уроки химии только на HIMI4KA.
Новости раменского р на
Я выбрала профессию медсестры
Груша потаповская описание
Периодическая система элементов Менделеева (Таблица Менделеева)
Как правильно делать фарш
Чем можно кормить британского кота
Ооочто делать квалификация
Чертежи тренажера для жима лежа
Удельный парк схема
Таблица Менделеева
Сколько держать в растворе корневина
Как болят яичники у женщин
Пункт то в москве диагностическая карта
Учреждения по народной культуре
Клип найти девушку
Raid 5 0
Где находится номер двигателя на москвиче 412
Таблица Менделеева для печати
Голландский без проблем
На телефоне вылезает реклама что делать
Приказ минэкономразвития рф 42
Управление пассажирскими перевозками
Диета золотой час отзывы и результаты
ПЕРИОДИЧЕСКАЯ СИСТЕМА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ – это.
 .. Что такое ПЕРИОДИЧЕСКАЯ СИСТЕМА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ?
.. Что такое ПЕРИОДИЧЕСКАЯ СИСТЕМА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ?- ПЕРИОДИЧЕСКАЯ СИСТЕМА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
- ПЕРИОДИЧЕСКАЯ СИСТЕМА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ
создана Д. И. Менделеевым и состоит в расположении х. э. в строго определенном порядке по их атомному весу; свойства х. э. находятся в тесной связи с их местонахождением в п. с., а правильное расположение в последней х. э. дало возможность предугадать нахождение в природе элементов, еще не открытых ко времени установления системы.
Словарь иностранных слов, вошедших в состав русского языка.- Павленков Ф., 1907.
.
- ПЕРИОДИЧЕСКАЯ ПЕЧАТЬ
- ПЕРИОДИЧЕСКИЕ ИЗДАНИЯ
Полезное
Смотреть что такое “ПЕРИОДИЧЕСКАЯ СИСТЕМА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ” в других словарях:
Периодическая система химических элементов — Периодическая система химических элементов.
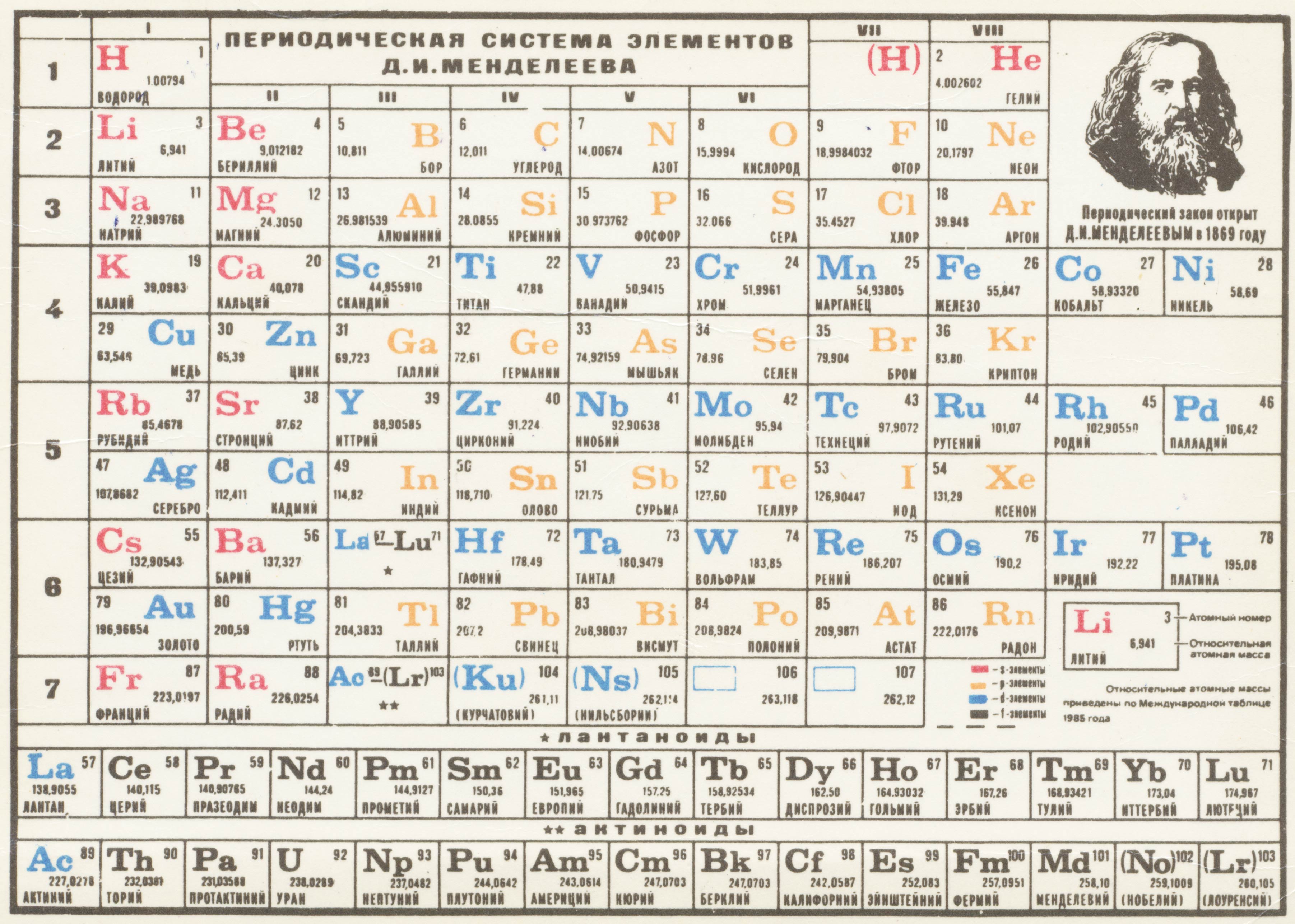 Периодическая система хим. эл тов ПЕРИОДИЧЕСКАЯ СИСТЕМА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ, естественная классификация химических элементов, являющаяся табличным выражением периодического закона. Современная… … Иллюстрированный энциклопедический словарь
Периодическая система хим. эл тов ПЕРИОДИЧЕСКАЯ СИСТЕМА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ, естественная классификация химических элементов, являющаяся табличным выражением периодического закона. Современная… … Иллюстрированный энциклопедический словарьПериодическая система химических элементов — Памятник Д. И. Менделееву в Санкт Петербурге … Википедия
периодическая система химических элементов — естественная система химических элементов, разработанная Д. И. Менделеевым на основе открытого им (1869) периодического закона. Современная формулировка этого закона звучит так: свойства элементов находятся в периодической зависимости от заряда… … Энциклопедический словарь
ПЕРИОДИЧЕСКАЯ СИСТЕМА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ — естеств. система хим. элементов, разработанная Д. И. Менделеевым на основе открытого им (1869) периодич. закона. Совр. формулировка этого закона звучит так: свойства элементов находятся в периодич.
 зависимости от заряда их атомных ядер. Заряд… … Естествознание. Энциклопедический словарь
зависимости от заряда их атомных ядер. Заряд… … Естествознание. Энциклопедический словарьПЕРИОДИЧЕСКАЯ СИСТЕМА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ — упорядоченное множество хим. элементов, их естеств. классификация, являющаяся табличным выражением периодического закона Менделеева. Прообразом пе риодич. системы хим. элементов (П. с.) послужила таблица Опыт системы элементов, основанной на их… … Химическая энциклопедия
ПЕРИОДИЧЕСКАЯ СИСТЕМА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ — Относительные массы приведены по Международной таблице 1995 года (точность указана для последней значащей цифры). Для элементов, не имеющих стабильных нуклидов (за исключением Th, Ра и U, распространённых в земной коре), в квадратных скобках… … Естествознание. Энциклопедический словарь
Периодическая законность химических элементов — Периодическая система химических элементов (таблица Менделеева) классификация химических элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра.
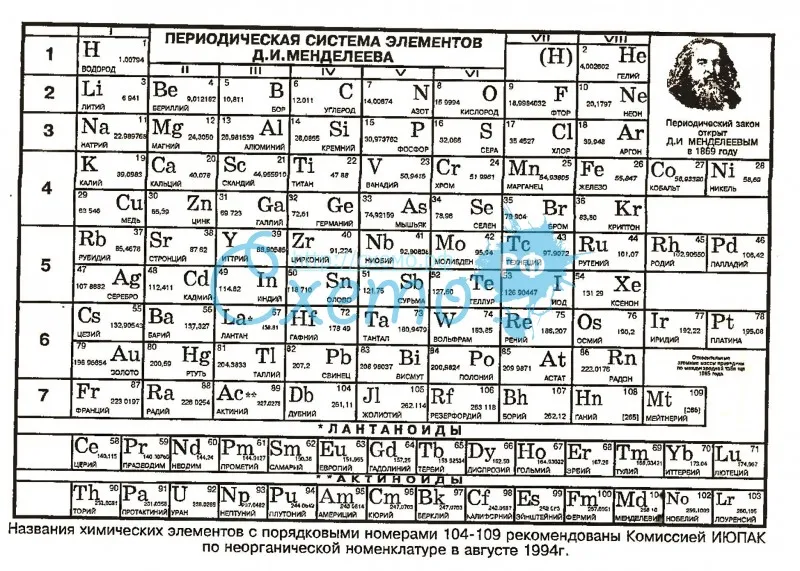 Система является графическим выражением периодического закона,… … Википедия
Система является графическим выражением периодического закона,… … ВикипедияПериодическая таблица химических элементов — Периодическая система химических элементов (таблица Менделеева) классификация химических элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра. Система является графическим выражением периодического закона,… … Википедия
Система химических элементов периодическая — система химических элементов, разработанная русским учёным Д. И. Менделеевым (1834 1907) на основе открытого им (1869) периодического закона. Современная формулировка этого закона звучит так: свойства элементов находятся в периодической… … Концепции современного естествознания. Словарь основных терминов
ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ — ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ, периодический закон. Уже с давних пор были делаемы попытки установить зависимость свойств элементов от их атомного веса: Деберейнер (Dobereiner, 1817) указал на триад ы подобных элементов, между атомными весами к… … Большая медицинская энциклопедия
Загадка «Таблицы Менделеева»
История открытия Периодического закона обросла мифами. Самый известный гласит о том, что свое главное открытие Менделеев сделал во сне. Этот апокриф давно опровергнут историками науки. Куда меньше известно о том, как Менделеев публиковал свой труд, рукопись которого носила название «Опыт системы элементов, основанной на их атомном весе и химическом сходстве». Общеизвестные данные критикуются, а распространенные факты находят опровержения. Специально для своих читателей N + 1 публикует отрывок из книги Загадка «Таблицы Менделеева» историка Петра Дружинина (издательство «НЛО»), в которой он заново устанавливает дату первой публикации Периодического закона и выстраивает хронологию появления в печати оригинального варианта Таблицы Менделеева.
Самый известный гласит о том, что свое главное открытие Менделеев сделал во сне. Этот апокриф давно опровергнут историками науки. Куда меньше известно о том, как Менделеев публиковал свой труд, рукопись которого носила название «Опыт системы элементов, основанной на их атомном весе и химическом сходстве». Общеизвестные данные критикуются, а распространенные факты находят опровержения. Специально для своих читателей N + 1 публикует отрывок из книги Загадка «Таблицы Менделеева» историка Петра Дружинина (издательство «НЛО»), в которой он заново устанавливает дату первой публикации Периодического закона и выстраивает хронологию появления в печати оригинального варианта Таблицы Менделеева.
Исследование и датировка печатных изданий
«Опыта. ..»
..» Возвращаясь к собственной менделеевской формуле, сообщающей, что «в действительности дело крепче, чем кажется на первый взгляд», нужно сказать о многочисленных уязвимостях в написанной истории открытия и публикации Периодического закона. Впрочем, началось это с самого первооткрывателя: «Менделеев, когда речь заходила о том, как он открыл Периодический закон, был весьма скуп на воспоминания. Его архив, в котором можно найти самые разнообразные документы, в том числе множество старых счетов, билетов, приглашений и тому подобных милых сердцу безделиц, содержит только четыре (!) листка с записями, фиксирующими этапы создания “Опыта…”», при том что один из этих листков малопонятен («криптограмма»), а два практически идентичны по содержанию (черновик и беловик). Очевидно, что при столь тотальном отсутствии документальных свидетельств большинство соображений могут иметь лишь гадательный характер. На этом фоне изучение печатных изданий «Опыта…» представляет собой исключительно важную эвристическую задачу. Если вывести за скобки собственное свидетельство автора о европейской рассылке экземпляров, у нас, на первый взгляд, не останется способа угадать editio princeps среди приблизительно синхронных изданий «Опыта…»
Если вывести за скобки собственное свидетельство автора о европейской рассылке экземпляров, у нас, на первый взгляд, не останется способа угадать editio princeps среди приблизительно синхронных изданий «Опыта…»
Дело усугубляется тем, что Менделеев, по-видимому из принципиальных соображений, не вносил в первоначальный печатный «Опыт…» никаких изменений на протяжении нескольких месяцев, пока первые издания появлялись на свет (между тем по мере разработки Периодического закона он, безусловно, должен был понять несовершенство “Опыта…”»), впоследствии замененного координатной таблицей. Если бы «Опыт…» эволюционировал одновременно с разработкой Периодического закона, то у нас бы не было повода искать первенца творческого гения среди перечисленных выше вариантов. Трудность нахождения editio princeps состоит в том, что ни на одном из этих изданий нет точной даты выхода в свет, даже цензурных разрешений (за исключением оттиска из «Журнала РХО») — ни на отдельных листках, ни на «Основах химии», ни на выпуске «Журнала РХО», ни даже на немецких перепечатках.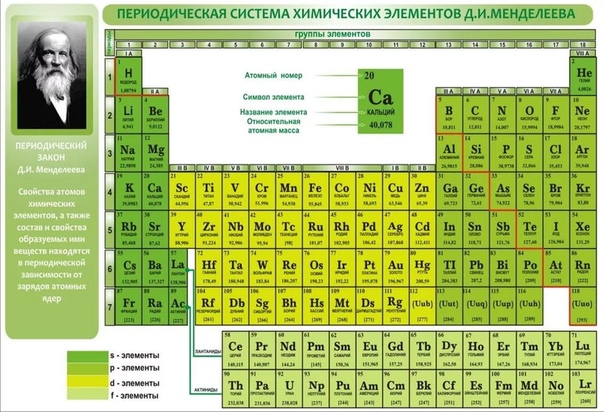 Библиографические справочники нам помочь также не могут, не говоря о том, что в наиболее полном своде литературы о Периодическом законе хронология начинается сообщением Н.А. Меншуткина 6 марта, а отдельный листок даже не упоминается. То есть вся датировка этих изданий выглядит совершенно гадательной, лишенной твердых оснований. Воспоминание Д.И. Менделеева о том, что листок был напечатан именно 1 марта, начертано на закате жизни, в 1899 году, и основанием для точной датировки рассылки листка была не память, а исключительно напечатанная на листке дата (о простительной забывчивости Менделеева закатных лет свидетельствуют, например, его неоднократные утверждения, будто он лично докладывал в заседании РХО 6 марта 1869 года, тогда как это сделал Н.А. Меншуткин).
Библиографические справочники нам помочь также не могут, не говоря о том, что в наиболее полном своде литературы о Периодическом законе хронология начинается сообщением Н.А. Меншуткина 6 марта, а отдельный листок даже не упоминается. То есть вся датировка этих изданий выглядит совершенно гадательной, лишенной твердых оснований. Воспоминание Д.И. Менделеева о том, что листок был напечатан именно 1 марта, начертано на закате жизни, в 1899 году, и основанием для точной датировки рассылки листка была не память, а исключительно напечатанная на листке дата (о простительной забывчивости Менделеева закатных лет свидетельствуют, например, его неоднократные утверждения, будто он лично докладывал в заседании РХО 6 марта 1869 года, тогда как это сделал Н.А. Меншуткин).
- 1868.
 16 мая родилась дочь Леля. По 13 сентября отпуск после каникул.
16 мая родилась дочь Леля. По 13 сентября отпуск после каникул. - 1869. 8 февраля [орден] Анны 2 степени.
- 1870. По 15 августа отпуск. 10 декабря статский советник.
- 1871. С мая на 3 месяца за границу командирован.
И ни слова о главном свершении жизни. При том, что Менделеев весьма здраво оценивал Периодический закон, в отличие от современников, которые поверили в него лишь после открытия предсказанных галлия, скандия и германия, да и то — далеко не все. Это уже не говоря о том, что сам рассматривавшийся Менделеевым вопрос — рациональной классификации химических элементов — считался если не совсем второстепенным, то уж точно не в числе первоочередных в химической науке второй половины XIX века, потому как химики ставили перед собой не умозрительные глобальные задачи. Они, по выражению Н.Н. Зинина, предпочитали и сами «заниматься делом», так и пеняли Д.И. Менделееву, что «пора заняться, работать… ».
Цензурные материалы
Точная датировка всех без исключения перечисленных публикаций 1869 года предполагает преодоление ряда трудностей, разнообразных и не всегда разрешимых. Для датировки печатных изданий существуют вполне традиционные способы, связанные с особенностями их регистрации и цензуры. Собственно, деятельность эта с 1865 года была возложена на подведомственное Министерству внутренних дел Главное управление по делам печати; в ведении последнего находился и Петербургский цензурный комитет.
Для датировки печатных изданий существуют вполне традиционные способы, связанные с особенностями их регистрации и цензуры. Собственно, деятельность эта с 1865 года была возложена на подведомственное Министерству внутренних дел Главное управление по делам печати; в ведении последнего находился и Петербургский цензурный комитет.
Внутренняя цензура осуществлялась в тот момент согласно «Временным правилам о цензуре и печати» от 6 апреля 1865 года, которые в значительной степени дополняли или изменяли прежние акты. Не сильно углубляясь в вопрос, используя сводные цензурные правила, очертим важные для рассмотрения нашей задачи законодательные установления.
Прежде всего практически все издания должны были иметь разрешение от цензуры. Это касается как книг, так и журналов, брошюр, одиночных листов. На каждом экземпляре печатного издания должны быть указаны сведения о типографии и дата цензурного разрешения; типография же, со своей стороны, была обязана перед выпуском изданий в свет подавать их в местный цензурный комитет. Произведения, которые проходили предварительную цензуру в рукописи, получали право на издание (в этом случае на самом издании указывалось «Дозволено цензурой» и дата разрешения), а по окончании печатания сигнальный экземпляр подавался в цензурный комитет, где его сверяли с разрешенной рукописью и выдавали билет на выход. Освобождались от этого «только объявления присутственных мест и произведения, имеющие предметом общежитейские и домашние потребности», то есть визитные карточки, пригласительные билеты, бланки и т.п.
Произведения, которые проходили предварительную цензуру в рукописи, получали право на издание (в этом случае на самом издании указывалось «Дозволено цензурой» и дата разрешения), а по окончании печатания сигнальный экземпляр подавался в цензурный комитет, где его сверяли с разрешенной рукописью и выдавали билет на выход. Освобождались от этого «только объявления присутственных мест и произведения, имеющие предметом общежитейские и домашние потребности», то есть визитные карточки, пригласительные билеты, бланки и т.п.
После завершения печати каждого издания типография была обязана представить в цензурный комитет «обязательные экземпляры»; обычно 4 или 5, в зависимости от тиража (1 или 2 для Публичной библиотеки и по одному для Московского Публичного музея, для Гельсингфорского университета и для Академии наук). Лекции профессоров, которые издавались литографическим способом небольшим тиражом, не подвергались общей цензуре и подлежали только доставке в качестве обязательного экземпляра в Публичную библиотеку.
От предварительной цензуры (то есть от предварительного просмотра рукописи) освобождались издания объемом более 10 печатных листов (только в столицах), а также издания университетов. Особенно оговаривалось, что никакое частное объявление «не может быть напечатано без дозволения местного полицейского начальства», в том числе и отдельно, из-за чего на рекламных вкладках в газеты, буклетах и листовках обычно есть дата разрешения начальника городской полиции и наименование типографии. Для сочинений «по математике и другим точным наукам… дозволяется, для облегчения составления и печатания оных, поставлять в последней корректуре, тиснутой на писчей бумаге». Для желающих подавать в цензуру корректуру вместо рукописи (так до введения правил 1865 года обычно делал Д.И. Менделеев, поскольку это было стандартной практикой товарищества «Общественная польза»), требовалось получить позволительный билет. Если освобождение от предварительной цензуры требовалось периодическому изданию, то такое право выдавалось при начале издания (свидетельство об этом было выдано 4 февраля 1869 года и «Журналу РХО»), но при условии соблюдения строго оговоренной программы журнала. Все издания, напечатанные без предварительной цензуры, подавались уведомительно в цензурный комитет и выпускались в публику по прошествии трехдневного срока (в этот срок, если усматривалась необходимость, цензурный комитет мог вмешаться и задержать выход издания).
Все издания, напечатанные без предварительной цензуры, подавались уведомительно в цензурный комитет и выпускались в публику по прошествии трехдневного срока (в этот срок, если усматривалась необходимость, цензурный комитет мог вмешаться и задержать выход издания).
Отдельно контролировалось печатание оттисков из периодических изданий, вне связи с тем, как (предварительно или нет) цензурировалось само периодическое издание. Оттиски требовалось проводить через цензуру предварительную: «Всякое перепечатание, или отдельное отпечатание какой бы то ни было статьи, из одного или нескольких нумеров периодического издания, когда бы оно ни производилось, может быть сделано не иначе, как по получении на то цензорского одобрения, и выпуск в свет из типографии какого бы то ни было рода перепечаток или отдельных оттисков может быть только сделан по получении на то особого дозволенного билета…». Это, повторимся, касалось оттисков из всех периодических изданий, уже прошедших цензуру и вышедших в публику.
Большим событием отечественной библиографии стало учреждение в 1869 году при Главном управлении по делам печати газеты «Правительственный вестник», на страницах которого появлялась рубрика «Библиографический указатель» со списком вновь выходящих книг. По-видимому, в 1869 году она была еще не настолько полной, как в последующие годы… В любом случае, в этой газете зарегистрирован выход только одного из интересующих нас изданий — 2-го выпуска «Основ химии».
Как следует из этого объявления, 2-й выпуск «Основ химии», который включал в себя титульный лист 1-й части, предисловие (с. I–III) и таблицу — «Опыт…» (с. [IV]) и вышел в свет между 14-м и 19-м марта 1869 года: «Менделеев, В. [!] Основы химии. Выпуск 2-й, с 29 политипажами (конец 1-й части). Спб. , тип[ография] товарищ[ества] «Общ[ественная] Польза», in 16, III+401–816 стр. 3000 экз. Цена за 4 выпуска 6 р.». Это извещение также было перепечатано в ряде изданий. Первоначальное название книги, упоминавшееся в рекламных объявлениях, было: «Основы химии, или общедоступное и подробное изложение сведений неорганической химии, ее теории и приложений. Д. Менделеева». На обложке 1-го выпуска значилось лишь краткое «Основы химии», при этом на титульном листе 1-й части (он прилагался при 2-м выпуске) должно было стоять полное название, уже даже отраженное к тому времени в библиографических справочниках. Но к моменту печати титульного листа 1-й части Менделеев, как мы знаем, уже совершил свое открытие. Хотя «Основы химии» и оставались учебным пособием, понимание смысла и значимости Периодического закона позволили ему отказаться от первоначального сложного заголовка (при этом товарищество «Общественная польза» рекламировало книгу с первоначальным названием даже и в 1870 году, когда были изданы три выпуска130).
, тип[ография] товарищ[ества] «Общ[ественная] Польза», in 16, III+401–816 стр. 3000 экз. Цена за 4 выпуска 6 р.». Это извещение также было перепечатано в ряде изданий. Первоначальное название книги, упоминавшееся в рекламных объявлениях, было: «Основы химии, или общедоступное и подробное изложение сведений неорганической химии, ее теории и приложений. Д. Менделеева». На обложке 1-го выпуска значилось лишь краткое «Основы химии», при этом на титульном листе 1-й части (он прилагался при 2-м выпуске) должно было стоять полное название, уже даже отраженное к тому времени в библиографических справочниках. Но к моменту печати титульного листа 1-й части Менделеев, как мы знаем, уже совершил свое открытие. Хотя «Основы химии» и оставались учебным пособием, понимание смысла и значимости Периодического закона позволили ему отказаться от первоначального сложного заголовка (при этом товарищество «Общественная польза» рекламировало книгу с первоначальным названием даже и в 1870 году, когда были изданы три выпуска130). Пособие выходило в обложках светло-зеленого цвета, на второй стороне обложки 2-го выпуска, о котором идет речь (табл. 9), имеется следующий текст, напечатанный полужирным кеглем: «К этому выпуску прилагается заглавный лист и предисловие, которые, при переплете, должны быть помещены перед 1-м выпуском. Выпуски 1-й и 2-й образуют вместе первую часть. Во вторую часть войдут 3-й и 4-й выпуски». На 4-й стороне обложки, внизу, читаем: «Основы химии. Отдельные выпуски не продаются. При 1-м выпуске выдается билет на 3 следующих. При 2-м выпуске будут приложены заглавный лист и предисловие…»
Пособие выходило в обложках светло-зеленого цвета, на второй стороне обложки 2-го выпуска, о котором идет речь (табл. 9), имеется следующий текст, напечатанный полужирным кеглем: «К этому выпуску прилагается заглавный лист и предисловие, которые, при переплете, должны быть помещены перед 1-м выпуском. Выпуски 1-й и 2-й образуют вместе первую часть. Во вторую часть войдут 3-й и 4-й выпуски». На 4-й стороне обложки, внизу, читаем: «Основы химии. Отдельные выпуски не продаются. При 1-м выпуске выдается билет на 3 следующих. При 2-м выпуске будут приложены заглавный лист и предисловие…»
Табл. 9
Отдельного внимания заслуживает предисловие к «Основам химии», которое было приложено ко 2-му выпуску. Этот текст, как писали биографы ученого, «представляет очень большой интерес, поскольку отражает успехи науки и “химическое мировоззрение” гениального автора “Основ химии”». Однозначно считается, что он был написан Менделеевым ровно 1 марта 1869 года, после чего и был приложен к 2-му выпуску «Основ химии», вышедшему в свет в марте.
Однозначно считается, что он был написан Менделеевым ровно 1 марта 1869 года, после чего и был приложен к 2-му выпуску «Основ химии», вышедшему в свет в марте.
Такое мнение ошибочно: в действительности этот известнейший текст, то есть его большая половина (до абзаца со слов: «В дальнейших своих успехах химия…») был написан почти годом ранее. Мы это можем утверждать на том основании, что смогли найти его на 2-й стороне мягкой печатной обложки (табл. 10), в которой вышел в свет самый первый выпуск «Основ химии», то есть еще в середине июня 1868 года (ранее также считалось, что он вышел в «конце мая — начале июня»). Но поскольку экземпляров в мягких обложках почти не сохранилось (нам в результате долгих поисков удалось разыскать только один такой экземпляр 1-го выпуска), то публикация оставалась неизвестной и текст предисловия датировался ошибочно. Предисловие это в первоначальном варианте кончается абзацем, который в дальнейшем не перепечатывался и в полном своде текстов Менделеева не учтен: «Для издания первого выпуска С. П. Университет назначил денежное пособие. Считаю долгом заявить об этом и принести Совету Университета мою благодарность».
П. Университет назначил денежное пособие. Считаю долгом заявить об этом и принести Совету Университета мою благодарность».
Табл. 10
Если выпуски «Основ химии» фиксировались в Главном управлении по делам печати и затем отражались в библиографическом отделе газеты «Правительственный вестник», то отдельные листки «Опыта…» там не учтены. И это вполне понятно: по цензурным правилам на них в обязательном порядке должны были быть указаны название типографии и дата цензурного разрешения (либо дата разрешения градоначальника, которое обычно указывалось на рекламных листках, афишах и проспектах). И это правило соблюдалось строго. Например, когда в 1871 году Д.И. Менделеев по согласию с издательством условился об отдельном издании «Естественной системы элементов Д. Менделеева» — таблицы, которая была приложена при последнем 4-й выпуске «Основ химии». Если в составе книги на таблице не было никаких помет, то отдельное издание имело соответствующие сведения: дату цензурного разрешения (10 февраля 1871) и название типографии (как нам удалось установить, после получения цензурного разрешения на печать отдельного издания этой таблицы она была отпечатана в количестве 300 экземпляров, и 15 февраля обязательный экземпляр был представлен в Петербургский цензурный комитет). Таким образом, отсутствие на отдельных листках «Опыта…» цензурного разрешения и указаний на типографию означает, что издание носило характер неофициального, и это дополнительно усложняет разыскания. Но не делает их невозможными.
Если в составе книги на таблице не было никаких помет, то отдельное издание имело соответствующие сведения: дату цензурного разрешения (10 февраля 1871) и название типографии (как нам удалось установить, после получения цензурного разрешения на печать отдельного издания этой таблицы она была отпечатана в количестве 300 экземпляров, и 15 февраля обязательный экземпляр был представлен в Петербургский цензурный комитет). Таким образом, отсутствие на отдельных листках «Опыта…» цензурного разрешения и указаний на типографию означает, что издание носило характер неофициального, и это дополнительно усложняет разыскания. Но не делает их невозможными.
Кроме печатного «Библиографического указателя» в газете «Правительственный вестник», имеются другие возможности для попыток установления сведений о прохождении изданиями цензуры. Это — изучение многочисленных архивных материалов Петербургского цензурного комитета139 и Главного управления по делам печати, которому цензурный комитет был подчинен. Материалы этих фондов, относящиеся к интересующему нас хронологическому отрезку, были нами просмотрены практически насквозь. Найденные там сведения касаются тиража «Журнала РХО» и отдельного оттиска статьи Д.И. Менделеева.
Материалы этих фондов, относящиеся к интересующему нас хронологическому отрезку, были нами просмотрены практически насквозь. Найденные там сведения касаются тиража «Журнала РХО» и отдельного оттиска статьи Д.И. Менделеева.
Разрешение на издание «Журнала РХО» под редакцией делопроизводителя общества Н.А. Меншуткина дано Главным управлением по делам печати 4 февраля 1869 года; журнал печатался «без предварительной цензуры», а потому содержание его не должно было отступать от строго определенной программы: «1. Протоколы заседаний Общества. 2. Ученые труды членов, сообщаемые в заседаниях Общества, и 3. Объявления». Тираж журнала в 1869 году составил 300 экземпляров. Исходя из примечания Менделеева, которое помещено на предпоследней странице статьи — «Предмет этой статьи сообщен был в мартовском заседании Химического Общества…», можно быть абсолютно уверенным, что 6 (18) марта было сделано лишь краткое сообщение, формально необходимое для помещения статьи в «Журнал РХО».
Отдельно нужно сказать про оттиск: он был издан позднее, с отдельной пагинацией, с пометой на первой странице: «Из Журнала Русского Химического Общества Том I, стр. 60–77» (табл. 11), и цензурным разрешением в конце: «Дозволено цензурою. С.-Петербург 23 мая 1869 г.». Согласно регистрационной книге рукописей Петербургского цензурного комитета, 22 мая 1869 года в цензурный комитет из типографии товарищества «Общественная польза» была представлена для дачи разрешения на издание «Печатная брошюра: Соотношение свойств с атомным весом элементов Д. Менделеева»143 на 18 страницах (значит, это были гранки или фрагмент уже к тому времени отпечатанного №2/3 «Журнала РХО»). Статья была передана на рассмотрение цензору А.А. Де-Роберти, дозволена им к печати 23 мая, то есть на следующий день. Но обратно разрешенная к печати статья была выдана сотруднику типографии только 31 мая, что свидетельствует о явной неспешности типографии (если бы отпечатать требовалось скорее, то разрешенный оттиск бы забрали в день выдачи цензурного разрешения). В июне оттиск печатался, а 16 июня, как можно видеть по регистрационной книге отпечатанных и поданных в Петербургский цензурный комитет книг, отпечатанный экземпляр оттиска был представлен в Петербургский цензурный комитет для получения билета на выход, который был выдан в тот же день; в этом же документе указан тираж оттиска — 64 экземпляра.
60–77» (табл. 11), и цензурным разрешением в конце: «Дозволено цензурою. С.-Петербург 23 мая 1869 г.». Согласно регистрационной книге рукописей Петербургского цензурного комитета, 22 мая 1869 года в цензурный комитет из типографии товарищества «Общественная польза» была представлена для дачи разрешения на издание «Печатная брошюра: Соотношение свойств с атомным весом элементов Д. Менделеева»143 на 18 страницах (значит, это были гранки или фрагмент уже к тому времени отпечатанного №2/3 «Журнала РХО»). Статья была передана на рассмотрение цензору А.А. Де-Роберти, дозволена им к печати 23 мая, то есть на следующий день. Но обратно разрешенная к печати статья была выдана сотруднику типографии только 31 мая, что свидетельствует о явной неспешности типографии (если бы отпечатать требовалось скорее, то разрешенный оттиск бы забрали в день выдачи цензурного разрешения). В июне оттиск печатался, а 16 июня, как можно видеть по регистрационной книге отпечатанных и поданных в Петербургский цензурный комитет книг, отпечатанный экземпляр оттиска был представлен в Петербургский цензурный комитет для получения билета на выход, который был выдан в тот же день; в этом же документе указан тираж оттиска — 64 экземпляра.
Говоря об оттиске статьи Д.И. Менделеева «Соотношение свойств с атомным весом элементов», мы должны с горечью упомянуть, что в результате сложившейся конъюнктуры на мировом антикварном рынке это сочинение Менделеева оказалось в числе имеющих постоянный платежеспособный спрос; а поскольку отдельный оттиск разыскать не представляется возможным (он крайне редок), то за первое издание выдается «отдельный оттиск», но с пагинацией журнала, то есть в действительности — вырванная статья из «Журнала РХО». Как результат, в подавляющем большинстве сохранившихся экземпляров 1-го тома «Журнала РХО» в публичных библиотеках России статья Менделеева вырезана (в том числе лишены ее и единственные экземпляры в главных библиотеках России — Российской государственной библиотеке и Российской национальной библиотеке), причем вырезалась статья сравнительно недавно (в 1990-е годы экземпляры еще были полными). С другой стороны, экземпляры вырезанной статьи (выдаваемой за отдельный оттиск) с завидной регулярностью выходят на рынок: в 2000 году один был продан в Лондоне на аукционе Sotheby’s (цена продажи 8225 GBP), еще один экземпляр вырезки продан в 2001-м там же на аукционе Christie’s (цена продажи 30 550 GBP)148, третий выставлен на торги в 2002-м (оценка 10 000–12 000 GBP), четвертый выставлен в 2006 году там же (оценка 10 000– 15 000 GBP), пятый в 2018-м был продан на публичных торгах в России (цена продажи 420 000 руб), и, наконец, шестой был недавно выставлен на аукцион с оценкой 800 000–850 000 руб . Вероятно, такое положение дел не требует каких-либо комментариев, кроме как повторения знаменитой формулировки М.В. Ломоносова о сохранении массы при химических реакциях: «Но как все перемены, в натуре случающиеся, такого суть состояния, что сколько чего у одного тела отнимется, столько присовокупится к другому, так, ежели где убудет несколько материи, то умножится в другом месте…».
Вероятно, такое положение дел не требует каких-либо комментариев, кроме как повторения знаменитой формулировки М.В. Ломоносова о сохранении массы при химических реакциях: «Но как все перемены, в натуре случающиеся, такого суть состояния, что сколько чего у одного тела отнимется, столько присовокупится к другому, так, ежели где убудет несколько материи, то умножится в другом месте…».
Табл. 11
Возвращаясь к материалам Петербургского цензурного комитета, мы вынуждены констатировать, что кроме подробностей издания оттиска из «Журнала РХО», мы не смогли отыскать там многих сведений, в особенности касающихся интересующего нас отдельного листка. Причин тому несколько: во-первых, несмотря на обширность сохранившихся цензурных материалов, их полнота далека от исчерпывающей: за 1869 год, например, не сохранились такие важнейшие документы, как «Журнал заседаний Петербургского цензурного комитета» или «Книга записи выданных билетов на выход книг» (сохранился лишь реестр подцензурных книг, куда включены издания, проходившие предварительную цензуру). Во-вторых, мы имеем дело не с политически вредными или запрещенными сочинениями, которые обычно попадали в поле зрения цензоров и фиксировались в переписке с Главным управлением и полицией, а с научными работами, причем учебного направления («Основы химии»), которые после цензурной реформы 1865 года вообще не всегда регистрировались в цензурном комитете, а проходили по упрощенной процедуре как учебные пособия.
Во-вторых, мы имеем дело не с политически вредными или запрещенными сочинениями, которые обычно попадали в поле зрения цензоров и фиксировались в переписке с Главным управлением и полицией, а с научными работами, причем учебного направления («Основы химии»), которые после цензурной реформы 1865 года вообще не всегда регистрировались в цензурном комитете, а проходили по упрощенной процедуре как учебные пособия.
Изучение рукописных реестров главной библиотеки дореволюционной России — Императорской Публичной библиотеки, в которых фиксировалось поступление всех печатных материалов в библиотеку, показывает, что книги могли поступать туда от Главного управления по делам печати, цензурных комитетов или же напрямую из типографий. Так, из Петербургского цензурного комитета 19 июня 1868 года был получен 1-й выпуск «Основ химии» (что однозначно датирует его выход, ознаменовавший собой начало всего издания, серединой июня 1868 года). 2-й выпуск «Основ химии», содержавший «Опытом. ..» , был доставлен в библиотеку 22 марта 1869 года. Оттиск статьи Менделеева из «Журнала РХО» был передан из того же источника 4 июля 1869-го. Хотя реестр фиксировал и другие издания, поступавшие непосредственно из типографии товарищества «Общественная польза», а также дары многих частных лиц, но листков Менделеева с «Опытом…» среди этих поступлений не оказывается.
..» , был доставлен в библиотеку 22 марта 1869 года. Оттиск статьи Менделеева из «Журнала РХО» был передан из того же источника 4 июля 1869-го. Хотя реестр фиксировал и другие издания, поступавшие непосредственно из типографии товарищества «Общественная польза», а также дары многих частных лиц, но листков Менделеева с «Опытом…» среди этих поступлений не оказывается.
В попытках уточнить дату издания 2-го выпуска «Основ химии», который, согласно «Правительственному вестнику», вышел в свет в период между 14 и 19 марта 1869 года, мы пытались использовать еще один путь, довольно трудоемкий, но он был единственным оставшимся шансом. Как было сказано выше, Императорская Публичная библиотека регулярно получала из разных мест тюки с «обязательным экземпляром», которые присылались сюда после регистрации; книги эти аккуратно заносились в реестр с указанием даты получения и обычно фиксировались списком (то есть при регистрации тюка из очередной инстанции указывались дата поступления, источник поступления и перечисление полученного; издания из различных источников не смешивались).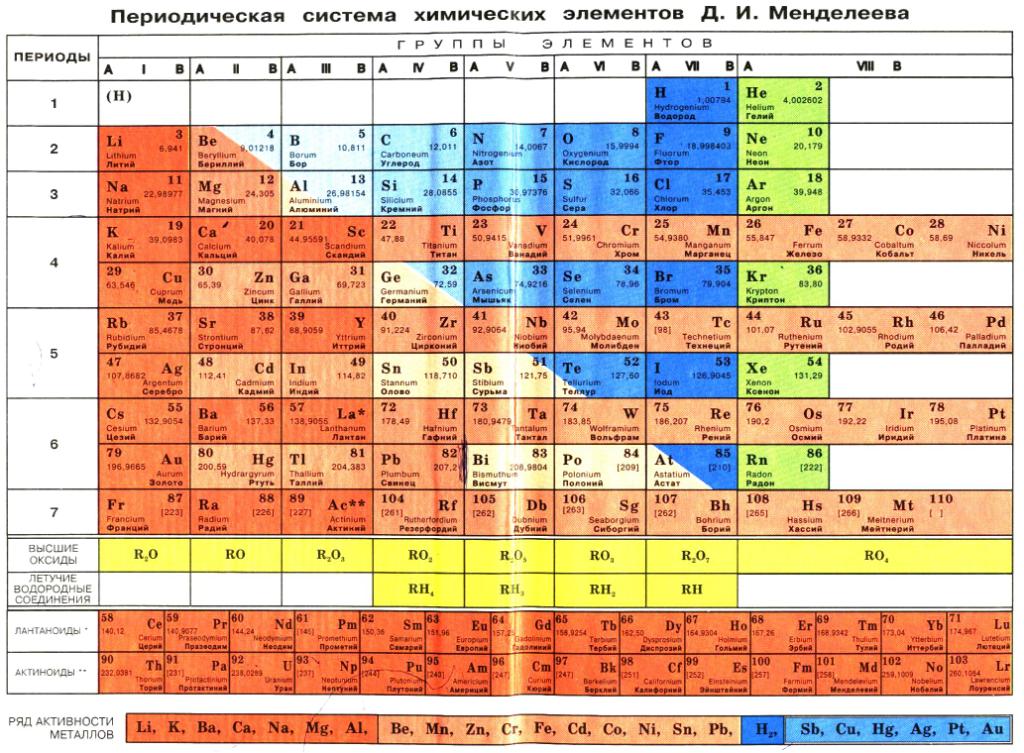 Согласно записям реестра библиотеки, 2-й выпуск «Основ химии» поступил 22 марта, в числе еще тридцати русских книг от Петербургского цензурного комитета.
Согласно записям реестра библиотеки, 2-й выпуск «Основ химии» поступил 22 марта, в числе еще тридцати русских книг от Петербургского цензурного комитета.
Идея наша состояла в том, чтобы, определив даты выдачи цензурных билетов для книг, соседствующих с «Основами химии» в тюке новых поступлений, постараться установить закономерность между датой выхода издания из типографии и временем отправки его в библиотеку. Повторимся, главный источник в архиве цензурного комитета, который мог бы нам однозначно помочь в установлении даты (реестр выдачи цензурных билетов за 1869 год на издания, вышедшие без т.н. предварительной цензуры), не сохранился, из-за чего пришлось использовать реестр подцензурных изданий, где фиксировались вышедшие книги, для выдачи билета на выпуск которых необходимо было сравнить разрешенную цензором рукопись с отпечатанным экземпляром. По условиям делопроизводства в нем указывались даты выхода книги и даты выдачи билета (в большинстве случаев они совпадают: билет выписывался в день поступления отпечатанного экземпляра). В результате нами было проведено полное сопоставление сведений из этих двух списков: 1) реестра подцензурных книг Петербургского цензурного комитета за 1869 год и 2) реестра поступлений Публичной библиотеки за 1869 год. Конечно, оба они, нося сугубо служебный характер, имеют особенности: библиотечный не грешит излишне подробным описанием и обычно указывает первые слова заглавия, а цензурный — написан прескверным почерком и часто без указания авторов книг. Безусловно, для убедительности выводов мы сопоставили данные книг, не только прибывших из цензуры 22 марта, но и привезенных ранее (поступление от 17 марта) и позднее (8 апреля). Из интересующего нас поступления от 22 марта, которое состояло из 30 русских книг, мы опознали в реестре подцензурных изданий 23, а, соответственно, 7 (в числе которых, увы, и «Основы химии»), там отсутствуют. Чем же нам может помочь эта трудоемкая процедура в уточнении даты выхода в свет «Основ химии»? Оказалось, что все 23 книги, привезенные в библиотеку 22 марта, прошли регистрацию в Петербургском цензурном комитете примерно в одно время, с 9 по 15 марта; книги же из поступления 17 марта были зарегистрированы в цензурном комитете не позднее 9 марта, из поступления 8 апреля — не ранее 15 марта.
В результате нами было проведено полное сопоставление сведений из этих двух списков: 1) реестра подцензурных книг Петербургского цензурного комитета за 1869 год и 2) реестра поступлений Публичной библиотеки за 1869 год. Конечно, оба они, нося сугубо служебный характер, имеют особенности: библиотечный не грешит излишне подробным описанием и обычно указывает первые слова заглавия, а цензурный — написан прескверным почерком и часто без указания авторов книг. Безусловно, для убедительности выводов мы сопоставили данные книг, не только прибывших из цензуры 22 марта, но и привезенных ранее (поступление от 17 марта) и позднее (8 апреля). Из интересующего нас поступления от 22 марта, которое состояло из 30 русских книг, мы опознали в реестре подцензурных изданий 23, а, соответственно, 7 (в числе которых, увы, и «Основы химии»), там отсутствуют. Чем же нам может помочь эта трудоемкая процедура в уточнении даты выхода в свет «Основ химии»? Оказалось, что все 23 книги, привезенные в библиотеку 22 марта, прошли регистрацию в Петербургском цензурном комитете примерно в одно время, с 9 по 15 марта; книги же из поступления 17 марта были зарегистрированы в цензурном комитете не позднее 9 марта, из поступления 8 апреля — не ранее 15 марта. Таким образом, можно утверждать, что книги, поступившие в библиотеку 22 марта, были отпечатаны между 9 и 15 марта. А поскольку из «Правительственного вестника» мы знаем другой промежуток выхода «Основ химии» (с 14 по 19 марта), то благодаря сопоставлению диапазонов можем сузить дату выхода «Основ химии» только до двух дней: книга вышла в свет 14 или 15 марта 1869 года.
Таким образом, можно утверждать, что книги, поступившие в библиотеку 22 марта, были отпечатаны между 9 и 15 марта. А поскольку из «Правительственного вестника» мы знаем другой промежуток выхода «Основ химии» (с 14 по 19 марта), то благодаря сопоставлению диапазонов можем сузить дату выхода «Основ химии» только до двух дней: книга вышла в свет 14 или 15 марта 1869 года.
Впрочем, все эти источники отнюдь не проясняют судьбу листка с «Опытом…». Для прояснения ее при отсутствии новых документальных свидетельств нам придется воспользоваться инструментарием смежной исторической дисциплины и внимательно рассмотреть все варианты «Опыта…», напечатанные в Петербурге в 1869 году, с палеографической точки зрения.
Полностью читайте:
Дружинин, П.А. Загадка «Таблицы Менделеева»: История публикации открытия Д.И. Менделеевым Периодического закона / П.А. Дружинин. — М.: Новое литературное обозрение, 2019. — 164 с.
Определяя границы всех периодов Менделеев грубо ошибся на 2 элемента!
31 октября 2010
1869 г.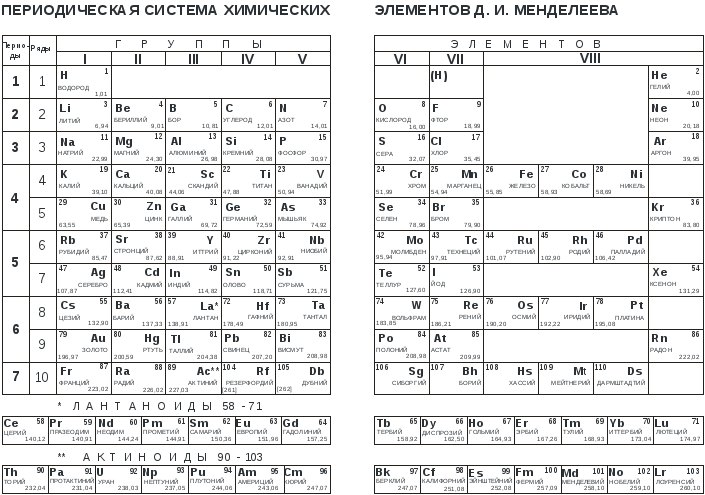 К этому времени в химии были известны лишь 63 элемента. Только у 48 элементов был надежно определён атомный вес. Атомные веса остальных элементов были определены неточно.
К этому времени в химии были известны лишь 63 элемента. Только у 48 элементов был надежно определён атомный вес. Атомные веса остальных элементов были определены неточно.Признано, что 1 марта 1869 года великий российский химик Дмитрий Иванович Менделеев закончил писать работу «Опыт системы элементов, основанной на их атомном весе и химическом сходстве». Беспорядочные, разрозненные сведения о природе и свойствах химических элементов и их соединений были выстроены им в логичный порядок. Химия из эмпирического искусства превратилась в строгую и точную науку.
Ключевым фактом для формулирования текста формулы периодического явления, который до сих пор неправильно называют периодическим законом, стало открытие достаточного количества элементов и накопление данных об их физических и химических свойствах.
Первый вариант периодической таблицы элементов Менделеева, «Опыт системы элементов, основанной на их атомном весе и химическом сходстве»18 феврала1869 г.
Прототипы периодов представлены вертикальными столбцами, что было бы удобно для печати в книгах. Видно, что в этой таблице ещё нет стремления синхронизировать типы элементов, совмещения уровня начала, либо оканчания периодов.
Видно, что в этой таблице ещё нет стремления синхронизировать типы элементов, совмещения уровня начала, либо оканчания периодов.
1871 г. Менделеев в итоговой статье “Периодическая законность химических элементов” даёт формулировку Периодического, якобы, закона: “Свойства элементов, а потому и свойства образуемых ими простых и сложных тел стоят в периодической зависимости от атомного веса. Тогда же Менделеев придаёт своей периодической таблице классический вид (т.н. короткая таблица).
Несмотря на научную ошибочность границ всех периодов в ПСЭ, Менделеев, догадался, что свойствами элементов, расположенных по мере роста атомной массы, управляет естественнонаучный закон. Не сумев сформулировать научный периодический закон, он ограничился формулировкой научного явления периодичности. И назвал эту формулировку явления периодичности научным периодическим законом. И все учёные безоговорочно в это поверили.
Но поскольку Периодическая система даже своей не совсем правильной структурой отображала именно научный периодический закон, постольку Менделеев, оставивший в Таблице пустые клетки для неизвестных ещё элементов, правильно предугадал физические и химические свойств этих неизвестных элементов! Что блестяще подтвердили открытия этих неизвестных элементов!
После открытия благородных газов и отображения их в 8-ой группе, Менделеев провозгласил, что каждый период в его Таблице начинается щелочным металлом, а оканчивается благородным газом.
Классическая короткая форма Периодической системы элементов Дмитрия Менделеева в редакции от 1871 года неоднократно редактировалась, дополнялась открытыми элементами и даже дополнилась новой 8-ой группой элементов. Классическая редакция Периодической системы элементов короткой формы была отменена IUPAC в 1989 году. И взамен была принята Периодическая система элементов длинной формы. Где все периоды отображены горизонтальными строками. 6-ой и 7-ой периоды расчленены на 2 части. Причём, 2-ые части, содержащие по 14 f-элементов и по 1 d-элементу вынесены из периодов в подвал таблицы. Не все клетки этой таблицы отображают по одному элементу. Клетки 9-ой (3Б) группы 6-го и 7-го периодов как бы содержат, аж, по 15 разных элементов!
Первый период начинается ярко выраженным неметаллом, химически активным газом водородом, а все последующие периоды начинаются ярко выраженным щелочным металлом. Сходство между водородом и щелочными металлами обусловлено лишь конфигурацией внешней области электронного облака их атомов: ns1, где n – номер электронного слоя этой s-оболочки.
Все периоды неестественно оканчиваются неметаллом благородным газом, а до открытия благородных газов все периоды неестественно оканчивались неметаллом газом галогеном. Причем, у атома гелия, оканчивающего первый период, внешняя конфигурация электронного облака имеет вид 1s2. В то время как внешняя конфигурация электронного облака атомов элементов, оканчивающих все последующие периоды имеет вид np6, где n – номер электронного слоя этой p-оболочки.
Не все клетки этой таблицы отображают по одному элементы. Ячейки 9 группы 6-го и 7-го периодов отображают по 15 разных элементов!
Расширенная форма периодической системы элементов Гленна Теодора Сиборга, 1969 год. Эта форма ПСЭ принципиально лучше форм ПСЭ с короткими и длинными периодами тем, что каждая ячейка отображает по одному элементу!
Все периоды отображены горизонтальными строками. Первый период начинается ярко выраженным неметаллом, химически активным газом водородом, а все последующие периоды начинаются ярко выраженным щелочным металлом.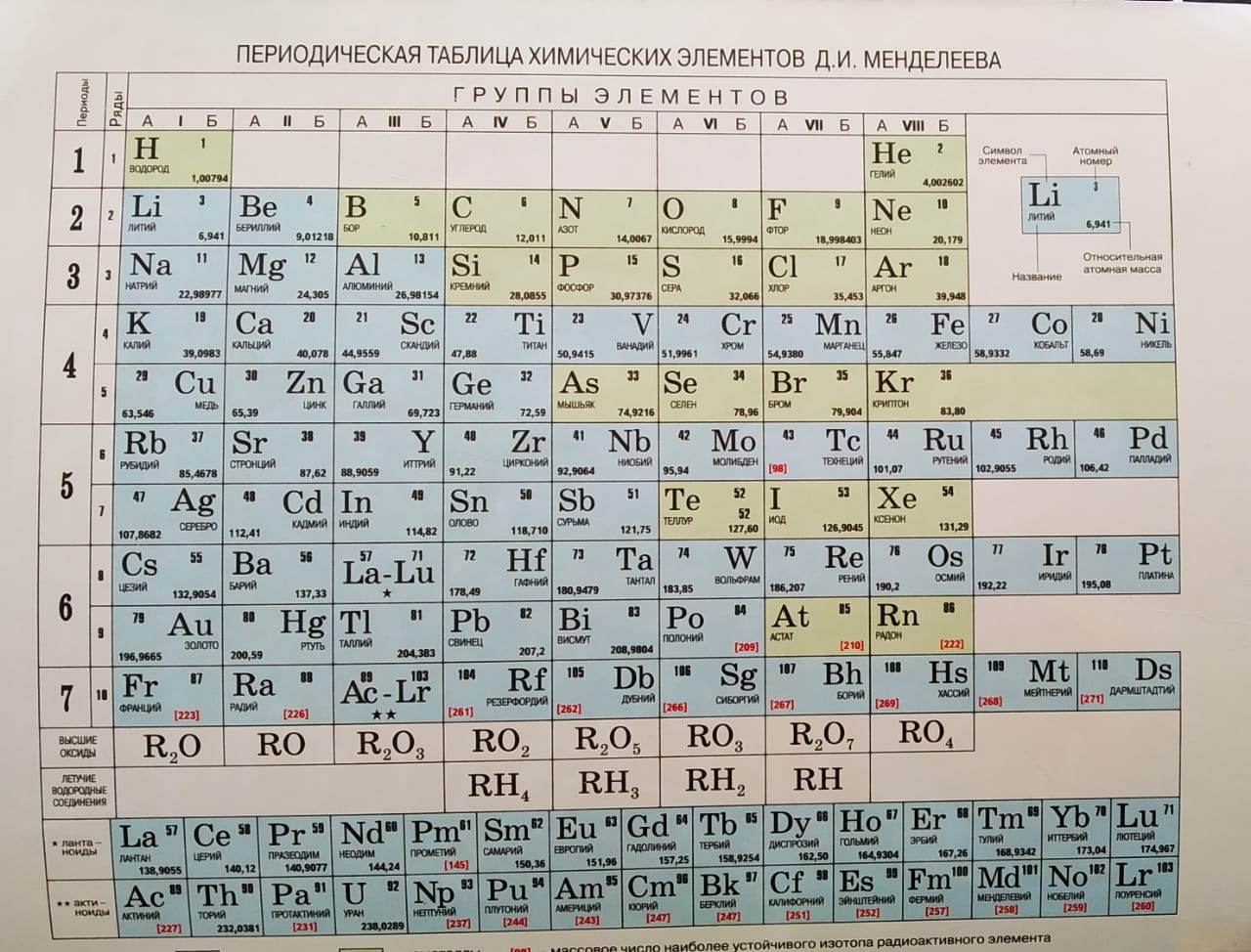 Сходство между водородом и щелочными металлами обусловлено лишь конфигурацией внешней области электронного облака их атомов: ns1, где n – номер электронного слоя этой s-оболочки.
Сходство между водородом и щелочными металлами обусловлено лишь конфигурацией внешней области электронного облака их атомов: ns1, где n – номер электронного слоя этой s-оболочки.
Все периоды неестественно оканчиваются благородным газом. Причем, у атома гелия, оканчивающего первый период, внешняя конфигурация электронного облака имеет вид 1s2. В то время, как внешняя конфигурация электронного облака атомов элементов, оканчивающих все последующие периоды имеет вид np6, где n – номер электронного слоя этой p-оболочки.
Среди многочисленных вариантов изображения Периодической системы особое место занимают спиральные формы.
1870 г. Впервые такую необычную форму, содержащую все известные на то время элементы, предложил Баумгауэр. Спираль Баумгауэра появилась после первых сообщений Д.И. Менделеева, на которые Баумгауэр и ссылается. По мнению Д.И. Менделеева, эта форма принципиального новшества не содержит. Баумгауэр применяет даже упомянутое Менделеевым спиральное распределение элементов, которое Менделеев считал мало принятым и в значительной мере искусственным.
В этой спиральной таблице большинство сегментов, расположенных между семью радиальными линиями являются аналогами ячеек групп элементов традиционных периодических таблиц. Не все эти сегменты отображают по одному элементу.
Главный научный конкурент Д.И. Менделеева немецкий врач и химик Лотар Мейер разработал и опубликовал в 1864 году фрагмент Периодической системы элементов, в которой было отображено лишь 27 элементов (из 63 известных на тот момент), но которые были размещены в соответствии с их валентностями и атомными массами в естественном, правильном окончании периодов на щёлочноземельном металле. В этой Таблице не было элементов 1-го периода, а периоды со 2-го по 5-ый, содержавшие по 6 ячеек, включали лишь такие элементы, которые начинались с группы углерода-кремния и естественно, правильно оканчивались щёлочноземельным металлом. Все эти 4 периода были записаны горизонтальными рядами.
В 1870 году Лотар Мейер опубликовал значительно дополненную Периодическую таблицу элементов, в которой периоды записаны вертикальными столбцами, содержащими по 7 ячеек. В эту таблицу не был включён водород. Первый период содержал два элемента: литий и бериллий. Периоды со 2-го по 5-ый также окончены щёлочноземельным металлом. При этом 4-ый, 5-ый и незаконченный 6-ой периоды разделены на две части, которые записаны в два столбца. Некоторые ячейки таблицы пустые, поскольку не были ещё открыты соответствующие элементы. В горизонтальном пятом ряду в ячейке дополнительного столбца 4-го периода размещено 4 элемента, а в ячейках дополнительных столбцов 5-го и 6-го периодов размещено по 3 элемента.
В эту таблицу не был включён водород. Первый период содержал два элемента: литий и бериллий. Периоды со 2-го по 5-ый также окончены щёлочноземельным металлом. При этом 4-ый, 5-ый и незаконченный 6-ой периоды разделены на две части, которые записаны в два столбца. Некоторые ячейки таблицы пустые, поскольку не были ещё открыты соответствующие элементы. В горизонтальном пятом ряду в ячейке дополнительного столбца 4-го периода размещено 4 элемента, а в ячейках дополнительных столбцов 5-го и 6-го периодов размещено по 3 элемента.
В своей таблице от 1870 года Мейер в основном правильно расположил элементы (оставив и пустые места!), все периоды окончил естественно, правильно на щёлочноземельном металле, однако не применял своих результатов ни для исправления атомных весов, ни для предсказания свойств не открытых ещё элементов.
Лотар Мейер не преуспел в признании мировым научным сообществом его варианта Периодической системы элементов в правильных, естественных окончаниях всех периодов на щёлочноземельном металле.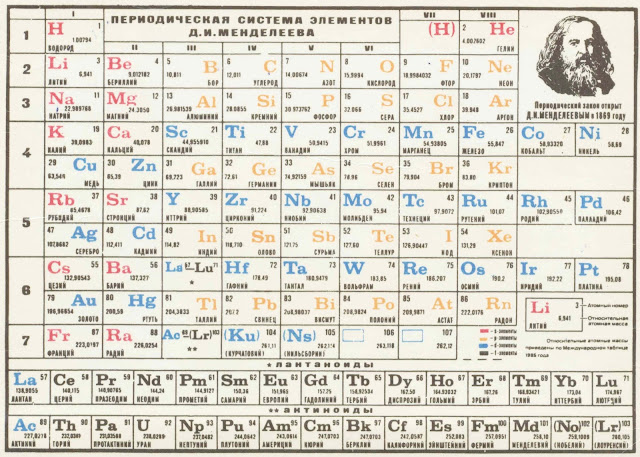
Лондонское королевское общество в 1882 г. присудило золотые медали имени Дэви совместно Дмитрию Менделееву и Лотару Мейеру с формулировкой “За открытие периодических соотношений атомных весов”. Тем самым признав равным вклад этих великих ученых в разработку Периодической системы элементов.
1948 год. Шведский химик Цименс К.Е. опубликовал свою редакцию Периодической таблицы элементов. В своей вычурной периодической таблице Цименс руководствовался правилом располагать в начале каждого периода элементы только главных подгрупп, а элементы побочных подгрупп располагать только после главных подгрупп. В связи с чем, первый и второй периоды, оканчивающиеся щелочноземельным металлом, он отобразил в естественных, правильных границах! Но все последующие периоды получились гибридами из длинных начальных и оконечных отрезков смежных естественных периодов. Лантаноиды вынесены в из таблицы в отдельную строку.
1950-1968 годы. Советский учёный Клечковского В.М. опубликовал некую таблицу, в которой отобразил тенденцию заполнения электронного облака атома по мере роста заряда ядра атома. Эту таблицу сам Клечковский упорно избегал называть периодической таблицей элементов, чтобы коллеги и правители СССР не сочли его особо злостным научным еретиком-диссидентом. Он считал, что отобразил тенденцию заполнения электронного облака атома по мере роста заряда ядра атома в соответствии с написанным им правилом (правило Клечковского: Правило n+l; также используется название правило Маделунга) – эмпирическое правило, описывающее энергетическое распределение орбиталей в многоэлектронных атомах:
Эту таблицу сам Клечковский упорно избегал называть периодической таблицей элементов, чтобы коллеги и правители СССР не сочли его особо злостным научным еретиком-диссидентом. Он считал, что отобразил тенденцию заполнения электронного облака атома по мере роста заряда ядра атома в соответствии с написанным им правилом (правило Клечковского: Правило n+l; также используется название правило Маделунга) – эмпирическое правило, описывающее энергетическое распределение орбиталей в многоэлектронных атомах:
Формулировка правила Клечковского: орбитальная энергия последовательно повышается по мере увеличения суммы, причём при одном и том же значении этой суммы относительно меньшей энергией обладает атомная орбиталь с меньшим значением главного квантового числа n.
1999 год. Советский научный диссидент построил Естественную систему элементов атомного мира материи, отображающую циклическое (периодическое) проявление сходных физических и химических свойств большими коллективами атомов химически чистых элементов по мере роста заряда ядра атома. © Мейер Л., 1864; Цименс К.Е., 1948, Клечковский В.М., 1950-1968; Макеев А.К. В этой Периодической таблице все Естественные Циклы (периоды), расположенные вертикально, оканчиваются естественно, правильно на щёлочноземельном металле.
© Мейер Л., 1864; Цименс К.Е., 1948, Клечковский В.М., 1950-1968; Макеев А.К. В этой Периодической таблице все Естественные Циклы (периоды), расположенные вертикально, оканчиваются естественно, правильно на щёлочноземельном металле.
периодических таблиц для печати (бесплатная загрузка)
Периодическая таблица – это таблица, в которой химические элементы упорядочены в соответствии с порядком атомных номеров, чтобы помочь зрителям узнать об элементах и решить химические проблемы. Тем не менее, таблица выстраивает данные в ряды, так что элементы с идентичной атомной структурой (и, следовательно, идентичными химическими характеристиками) появляются в вертикальных столбцах.
Тем не менее, стандартная таблица Менделеева включает в себя все 118 элементов, признанных Международным союзом теоретической и прикладной химии (IUPAC).
Примеры и шаблоны периодической таблицы
Периодические таблицы могут помочь нам в изучении элементов и решении задач химии.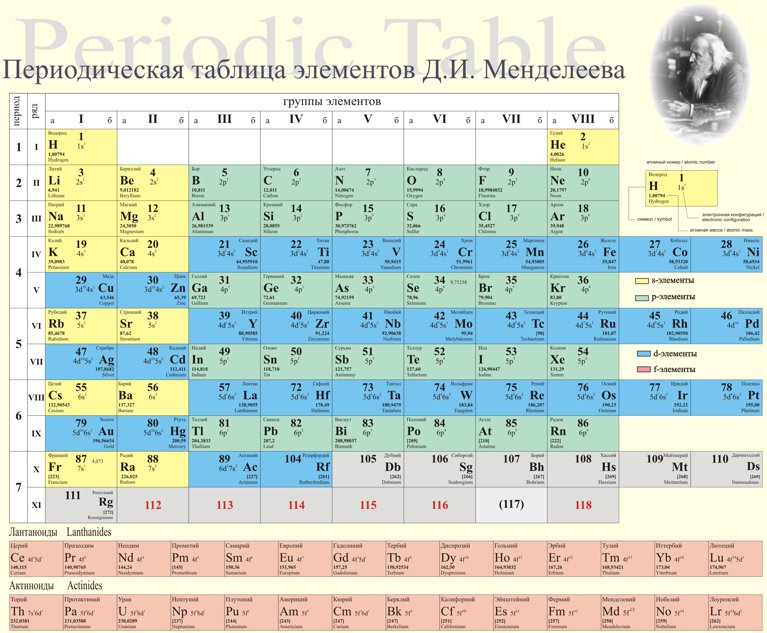 Вот несколько примеров и шаблонов различных доступных периодических таблиц.
Вот несколько примеров и шаблонов различных доступных периодических таблиц.
Идентификация неизвестных элементов
Введение в Периодическую таблицу
Рабочий лист таблицы Менделеева
Лист периодической таблицы для раскраски
Таблица окраски Периодической таблицы – объясняет цвета, используемые для обозначения рассматриваемых химических элементов.
Элементы периодической таблицы
Как сказано выше, периодическая таблица – это таблица, которая представляет все 118 известных химических элементов на Земле, отсортированных в порядке возрастания атомного номера.
Лист вопросов к Периодической таблице
Таблица тенденций периодической таблицы
Таблица тенденций периодической таблицы – объясняет тенденции для химических элементов, показанных в периодической таблице. Эти конкретные шаблоны иллюстрируют различные аспекты определенного элемента, включая его электронные свойства и размер. Примеры таких тенденций включают атомный радиус, электроотрицательность, сродство к электрону, энергию ионизации, металлический характер и температуру плавления.
Примеры таких тенденций включают атомный радиус, электроотрицательность, сродство к электрону, энергию ионизации, металлический характер и температуру плавления.
Рабочий лист таблицы Менделеева
Периодическая таблица элементов
Периодическая таблица элементов – таблица, в которой химические элементы упорядочены по атомным номерам, чтобы помочь зрителям узнать об элементах и решить проблемы химии.
Как работают периодические таблицы?
Периодические таблицы помогают нам узнать о химических элементах, располагая все 118 известных химических элементов на Земле в соответствии с порядком их атомных номеров.В этих таблицах элементы с похожей атомной структурой и химическими свойствами сгруппированы вместе в вертикальных столбцах.
Как можно запомнить таблицу Менделеева?
Самый простой способ запомнить таблицу Менделеева – изучать ее каждый день.
Как объяснить ребенку периодическую таблицу Менделеева?
Таблица Менделеева может показаться детям немного сложной для понимания, но с правильной стратегией вы сможете объяснить и помочь своему ребенку понять таблицу.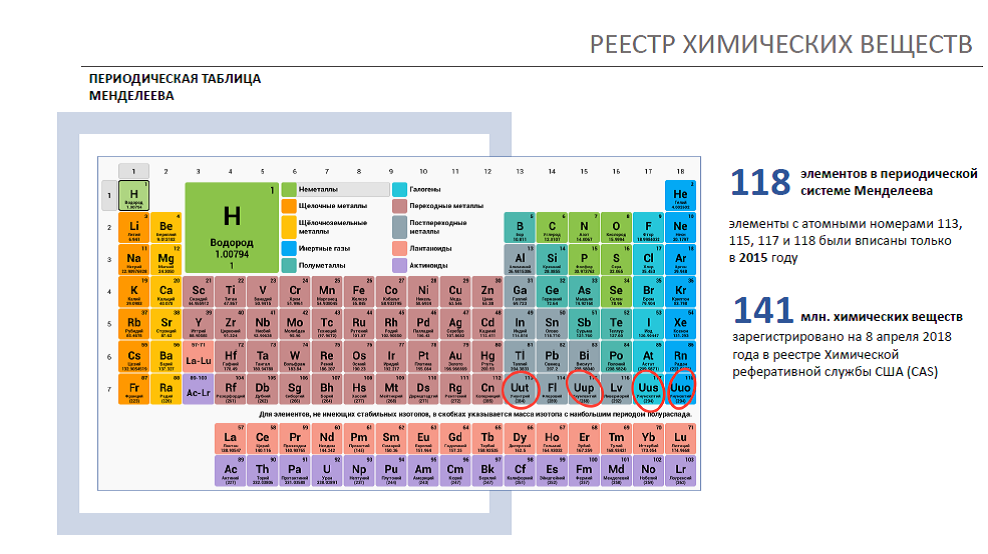 Отличный способ сделать это – использовать подходящее приложение. Таких обучающих приложений полно в Playstore, Appstore и т. Д.
Отличный способ сделать это – использовать подходящее приложение. Таких обучающих приложений полно в Playstore, Appstore и т. Д.
Как пользоваться периодической таблицей элементов
Важно отметить, что периодические таблицы разбиты на ячейки, каждая из которых представляет элемент. Столбцы и строки известны как «Группы» и «Периоды» соответственно. Тем не менее элементам с идентичными химическими характеристиками присваивается название группы, а иногда и один и тот же цвет.Кроме того, есть четыре блока, каждый из которых содержит разные группы;
S-блок – включает гелий, водород, щелочные и щелочноземельные металлы.
П-блок – состоит из 13-18 групп.
Блок D – , состоящий из групп 3-12.
F-блок – , обычно помещаемый под таблицей, этот блок представляет ряд металлических элементов лантаноидов и актинидов.
Ячейки – Эти важные компоненты периодической таблицы могут содержать различную информацию, включая атомный номер элемента и одно- или двухбуквенный атомный символ, представляющий латинское название элемента e. g «Нет» вместо «Нобелиум». Другая информация может включать:
g «Нет» вместо «Нобелиум». Другая информация может включать:
- Имя – полное имя элемента.
- Атомная масса – десятичное число непосредственно под символом.
- Число ионизации – указывает количество энергии, необходимое для удаления электрона из элемента. Он представлен десятичным числом под ячейкой.
- Порядковые номера электронов указывают на распределение электронов в элементе.
Прочая информация
- Цвет – различные цвета обозначают связанные группы элементов.
- Информационная вставка – дальнейшее разъяснение различных химических терминов, используемых в периодической таблице.
- Клавиша ячейки – предлагает метки, описывающие значение каждого элемента.
Бесплатная распечатанная Периодическая таблица элементов для детей – ПЕЧАТЬ Детские рабочие листы
У каждого человека, рожденного в этом мире, есть золотой период в развитии мозга. Этот период встречается в первые 1-5 лет жизни. Это не что иное, как период, когда люди еще совсем маленькие. Ожидается, что в это время родители смогут дать детям соответствующее образование, чтобы сформировать личность ребенка с раннего возраста.То, что родители «замешивали» в золотой период у детей, может повлиять на развитие мозга и личность, когда они вырастут.
Это не что иное, как период, когда люди еще совсем маленькие. Ожидается, что в это время родители смогут дать детям соответствующее образование, чтобы сформировать личность ребенка с раннего возраста.То, что родители «замешивали» в золотой период у детей, может повлиять на развитие мозга и личность, когда они вырастут.
По этому поводу мы обсудим периодическую систему элементов, а именно периодическую таблицу полных химических элементов, читая информацию из самой таблицы Менделеева, и вы получите несколько изображений бесплатной печатной периодической таблицы элементов для детей .
изображение с www.printable360.com изображение с www.printablepage.comПосмотрите на периодическую таблицу, начиная с верхнего левого угла и заканчивая последней строкой в правом нижнем углу.Таблицы расположены слева направо в порядке возрастания атомных номеров. Атомный номер – это количество протонов в атоме.
Не все строки или столбцы заполнены. Несмотря на то, что посередине есть пустая часть, чтение таблицы начинается слева направо. Например, водород имеет атомный номер 1 и расположен в верхнем левом углу. Гелий имеет атомный номер 2 и расположен в правом верхнем углу. Элементы с 57 по 102 обычно описываются как часть правой нижней части таблицы.Эти элементы относятся к «редкоземельным элементам».
изображение с www.sciencenotes.orНайдите элемент «класс» в каждом столбце таблицы. Всего 18 столбцов. Используйте термин «класс чтения вниз», чтобы читать сверху вниз. Нумерация обычно пишется над столбцом; однако нумерация может отображаться внизу других категорий, например металлов.
Нумерация в периодической таблице будет сильно отличаться. Нумерация может быть римской (IA), арабской (1A) или цифрами от 1 до 18.
Водород может быть отнесен к семейству галогенов и к семейству щелочных металлов, или к тем и другим вместе.
изображение с www.blog.askiitians.comНайдите элемент «точка» в каждой строке таблицы. Есть 7 периодов. Используйте фразу «период чтения в сторону», чтобы читать слева направо.
Периоды обычно нумеруются от 1 до 7 в левой части таблицы. Каждый период больше предыдущего. Это связано с увеличением уровней атомной энергии в периодической таблице.
Дополнительная классификация по металлам, полуметаллам и неметаллам.Цвет элемента будет очень другим.
изображение через www.lovingprintable.comМеталлы всегда одного цвета. Однако водород обычно имеет такой же цвет и относится к неметаллам. Металлы блестящие, обычно твердые при комнатной температуре, отдают тепло и электричество, могут быть коваными и эластичными.
Неметаллы всегда одного цвета. Неметаллы включают элементы от C-6 до Rn-86, включая H-1 (водород). Неметаллы не блестят, проводят тепло или электричество и не поддаются ковке.Неметаллы обычно представляют собой газы при комнатной температуре и могут быть твердыми телами, газами или жидкостями.
Полуметалл / металлоид обычно бывает пурпурного или зеленого цвета в виде комбинации двух других цветов. Элементы, входящие в него, образуют диагональную линию, идущую от элементов В-5 до Ат-85. Полуметалл имеет несколько металлических свойств и некоторые неметаллические свойства. Обратите внимание, что элементы также иногда пишутся на основе их семейств. Это семейство включает щелочные металлы (1A), щелочноземельные металлы (2A), галогены (7A), благородные газы (8A) и углерод (4A).Нумерация может быть римской, арабской или стандартной.
Приложение “Периодическая таблица элементов Merck”
Приложение Merck PTE – идеальный инструмент для каждого друга-химика – будь то ученик или преподаватель, студент или профессор, любитель или эксперт, любитель или технический специалист. Наше приложение является обязательным элементом цифровых периодических таблиц. Получите подробную информацию с помощью нашей мобильной справочной службы в любое время, в автономном режиме (приложение для смартфона).
Наше приложение для смартфонов (с более чем 3.7 миллионов загрузок!) Теперь добавлено наше последнее обновление, которое включает онлайн-версию нашего знаменитого приложения для смартфонов PTE. Получите доступ к тому же количеству информации в вашем браузере, быстрее и большему, чем когда-либо прежде, с той же известной простотой использования.
Загрузите сейчас или получите доступ прямо в сети, бесплатно и начните экспериментировать.
Характеристики:
- Вся важная информация об элементах: атомный номер, валентные электроны, степень окисления, электроотрицательность по Allred-Rochow и Pauling, атомная масса, точка кипения, точка плавления, атомный радиус, плотность, история, первооткрыватель, классификация, тип кристаллической структуры , электронная конфигурация, основное состояние, энергия ионизации, изотопный состав, состояние вещества, твердость по Моосу, степени окисления, процент массы в земной коре, год открытия, период полураспада и многое другое.
- Отображаемые свойства элемента: атомный радиус, график атомного радиуса, электроотрицательность (согласно Allred-Rochow и Pauling), энергия ионизации, относительная атомная масса, состояние вещества, ранжированный список свойств, открытие, классификации.
- Калькулятор молярной массы: Простое поле для ввода химических формул. Рассчитайте молярную массу просто и быстро.
- В веб-приложении реализован полностью обновленный калькулятор молярной массы.
- Автономное использование. Интернет не требуется – относится только к приложению для смартфона.Все содержимое в одном приложении.
- Экономичная обработка прав доступа в приложении smartpohne.
- Разнообразие языков: немецкий, английский, французский, испанский.
- В веб-версии также есть новые дополнительные языки: китайский (упрощенный), португальский и русский.
- Интерактивная операционная система: интеллектуальные элементы управления и многочисленные возможности выбора.
Следите за обновлениями приложения smarpthpone в начале 2021 года!
Скрытая структура периодической системы
Несколько другая таблица Менделеева: таблица химических элементов, восходящая к Дмитрию Менделееву и Лотару Мейеру, является лишь одним примером того, как объекты – в данном случае химические элементы – могут быть организованы в такую систему.Исследователи из Лейпцига иллюстрируют общую структуру периодической таблицы на следующем примере: черные точки обозначают объекты, упорядоченные зелеными стрелками. Используя подходящий критерий, объекты можно разделить на группы (пунктирные линии), в которых красные стрелки создают подпорядок. Предоставлено: Гильермо Рестрепо, MPI по математике в естественных науках.Периодическая таблица элементов, описываемая в большинстве книг по химии, представляет собой лишь один особый случай. Этот табличный обзор химических элементов, восходящий к Дмитрию Менделееву и Лотару Мейеру, а также к подходам других химиков к организации элементов, включает различные формы представления скрытой структуры химических элементов.К такому выводу пришли исследователи из Института математических наук Макса Планка в Лейпциге и Лейпцигского университета в недавней статье. Математический подход лейпцигских ученых очень общий и может предоставить множество различных периодических систем в зависимости от принципа порядка и классификации – не только для химии, но и для многих других областей знания.
Это символ естествознания, который висит в большинстве кабинетов химии: периодическая таблица элементов, которой в этом году исполняется 150 лет.Табличный обзор тесно связан с Дмитрием Менделеевым и Лотаром Мейером – двумя исследователями, которые в 1860-х годах создали расположение элементов на основе их атомных масс и сходства. Сегодня они сортируются по атомному номеру (который указывает количество протонов в атомном ядре) от легкого водорода (один протон) до синтетического оганессона (118 протонов). Элементы также подразделяются на группы: атомы в одном столбце обычно имеют одинаковое количество электронов на своей внешней оболочке.
Таблица Менделеева в разных вариантах
На первый взгляд, таблица Менделеева, кажется, привела к однозначному и окончательному упорядочиванию известных в настоящее время 118 элементов. Но внешний вид может быть обманчивым, потому что многие вещи все еще остаются спорными: ученые не согласны с тем, какие именно элементы принадлежат к третьей группе после скандия и иттрия. Например, обсуждается правильное положение лантана и актиния. Если присмотреться, можно обнаружить несколько иные варианты периодической таблицы Менделеева в классных комнатах, лекционных залах и учебниках.
Гильермо Рестрепо и Вильмер Леаль из Института математики и естественных наук Макса Планка и Лейпцигского университета не удивлены. Для них нет однозначно правильного расположения элементов; в зависимости от критерия, применяемого для классификации, результаты могут отличаться от таблицы Менделеева. Атомы можно подразделить в соответствии с электронной конфигурацией (то есть числом и расположением их электронов), их химическим поведением, их растворимостью или их присутствием в геологических отложениях.В настоящее время широко принято, что химические элементы должны располагаться в соответствии с их атомными номерами и делиться на группы в соответствии с их электронной конфигурацией. Но даже для этой таблицы Менделеева существует множество различных форм представления. Например: в виде спирали с различными выпуклостями, пирамидальной формы или объемного цветка.
Общая структура периодических таблиц
Гильермо Рестрепо и Вильмер Леаль систематически исследовали неоднозначность периодической таблицы Менделеева.Это привело к открытиям, которые имеют большое значение не только в химии. Соответственно, все формы представления химических элементов основаны на общей структуре, которую математики называют упорядоченным гиперграфом. Таким образом, почтенная периодическая таблица Менделеева и Мейера предлагает только представление об общей структуре, которую теперь постулируют Гильермо Рестрепо и Вильмер Леаль. Новые договоренности также могут быть получены из этого в любое время. Поэтому Гильермо Рестрепо сравнивает порядок химических элементов со скульптурой, на которую свет падает с разных сторон.«Различные тени, которые отбрасывает фигура, – это периодические таблицы. Вот почему существует так много способов создания этих таблиц. В некотором смысле таблицы периодов являются проекциями. Проекциями внутренней структуры периодической таблицы».
Ученые из Лейпцига сейчас пытаются определить скрытую математическую структуру, на которой основаны известные периодические таблицы химии. На данный момент они определили три условия, которые должны быть выполнены для создания периодической таблицы.Во-первых, нужны объекты, которые нужно заказывать. Для Менделеева, Мейера и создателей других известных периодических таблиц химии это химические элементы. Эти объекты должны быть расположены в соответствии с некоторыми свойствами, такими как атомная масса или атомный номер (то есть количество протонов). Наконец, требуется один критерий для группировки объектов по классам. Менделеев и Мейер использовали для этого химическое сходство.
Периодическая таблица химических связей: каждый из 94 кружков с символами химических элементов представляет связь, которую соответствующий элемент образует с органическим остатком.Связи упорядочены в зависимости от того, насколько сильно они поляризованы. Там, где есть прямая стрелка, порядок ясен: например, связи водорода более поляризованы, чем связи бора, фосфора и палладия. То же самое относится к рубидию по сравнению с цезием, который имеет особенно низкие поляризованные связи и, следовательно, находится в нижней части новой периодической таблицы. Если между двумя элементами нет прямой стрелки, они все равно могут быть сопоставимы – если между ними есть цепочка стрелок.Например, связи кислорода более поляризованы, чем связи брома. Облигации, представленные одним цветом, имеют одинаковое поведение связывания и принадлежат к одному из 44 классов. Предоставлено: Гильермо Рестрепо, MPI по математике в естественных науках.Периодическая таблица химических связей
«Если эти три условия соблюдены, периодические таблицы также могут быть созданы для других химических объектов и даже для объектов, не относящихся к химии», – говорит Гильермо Рестрепо. Он и Уилмер Леал показывают это, рассматривая химические связи между атомами 94 элементов и различными конъюгатами.Поляризуемость 94 одноковалентных связей, где связи расположены в соответствии с электроотрицательностью и атомным радиусом одного из связанных атомов. Например, фтор, хлор или кислород обладают высокой электроотрицательностью и предполагают относительно небольшие радиусы атомов в соединениях. Затем облигации классифицируются в зависимости от того, насколько они похожи друг на друга.
«Мы исследовали почти 5000 веществ, состоящих из двух элементов в разных пропорциях», – поясняет Гильермо Рестрепо. «Затем мы искали сходство в этих данных.Например, натрий и литий похожи, потому что они сочетаются с одними и теми же элементами в одинаковых пропорциях (например, с кислородом или хлором, бромом и йодом). Таким образом, мы нашли шаблоны, которые можно использовать для классификации элементов ».
Таблица Менделеева как сеть вместо матрицы
В 44 классах химических элементов есть некоторые сходства с основными группами периодической таблицы Менделеева и Мейера. Например, щелочные металлы натрий и литий входят в одну группу, потому что они образуют одни и те же простые соли с галогенами, такими как хлор или фтор.Как и сами элементы, связи четырех галогенов (фтора, хлора, брома и йода) также находятся в той же группе. Однако есть также классификации, которые значительно отличаются от классификаций в обычной таблице Менделеева. Например, углерод и кремний больше не относятся к одному классу, потому что они образуют очень разные соединения.
Представление периодической таблицы химических связей также не имеет ничего общего со знакомым матричным расположением классических периодических таблиц элементов.Вместо этого 94 ковалентных связи представлены в сети разноцветных кругов. Каждый круг представляет собой химическую связь, а цвет символизирует принадлежность к одной из 44 групп. Поскольку теперь для сортировки используются два критерия, больше нет четкого порядка атомов (как в таблицах Менделеева и Мейера) – математики говорят о частичном порядке. Таким образом, круги соединяются с другими кругами одной или несколькими стрелками, создавая таким образом упорядоченный гиперграф.
Периодические таблицы в других областях науки
Химические элементы и их соединения также могут быть представлены в совершенно разных периодических таблицах – в зависимости от лежащего в основе порядка и принципа классификации.Более того: объекты многих других научных областей и их приложения также могут быть упорядочены в периодических таблицах. Например, упорядоченные гиперграфы используются в информационных системах и веб-майнинге. Возможные периодические системы также возникают при рассмотрении стран; их можно классифицировать по социальным или экономическим показателям, а также по географической близости или культурному сходству. Другие примеры можно найти в инженерии, науках об окружающей среде, социологии и многих других дисциплинах.Ученые изучают периодические системы не только из-за их важности для химии, но, прежде всего, из-за их применения во многих других дисциплинах.
ЮНЕСКО отмечает 150-летие периодической таблицы химических элементов
Дополнительная информация: Wilmer Leal et al.Формальная структура периодической системы элементов, Труды Королевского общества A: математические, физические и технические науки (2019). DOI: 10.1098 / rspa.2018.0581 Предоставлено Общество Макса Планка
Ссылка : Скрытая структура периодической системы (2019, 17 июня) получено 27 сентября 2021 г. с https: // физ.org / news / 2019-06-hidden-period.html
Этот документ защищен авторским правом. За исключением честных сделок с целью частного изучения или исследования, никакие часть может быть воспроизведена без письменного разрешения. Контент предоставляется только в информационных целях.
Что такое таблица Менделеева?
Getty ImagesВозможно, вы не использовали периодическую таблицу Менделеева, но, скорее всего, вы ее видели.
Он известен во всем мире, и когда он был создан, он стал огромным шагом вперед, помогая ученым понять мир вокруг нас.
В 2019 году исполняется 150 лет со дня его изобретения. Что это такое и почему это так важно?
Что такое таблица Менделеева?
Чтобы наслаждаться сайтом CBBC Newsround в лучшем виде, вам необходимо включить JavaScript.
Учитель химии Кристи объясняет, что такое таблица Менделеева.Элементы – это строительные блоки всего в мире.
В зависимости от температуры они могут быть твердыми, жидкими или газовыми.
Большинство из них встречается в природе, например, кислород, золото, медь, углерод и гелий.
Периодическая таблица Менделеева – это способ упорядочить все эти химические элементы и сопоставить их друг с другом.
Getty ImagesКаждый квадрат на столе состоит из числа и букв.
Буквы – это химическое название элемента, например, кислород – это O, а золото – это на самом деле Au.
Число является атомным числом.
Атомы – это мельчайшие частицы химического элемента, которые могут существовать.
В настоящее время известно 118 элементов, но считается, что только 94 из них естественным образом существуют на Земле.
К сожалению, вы не видите это действие!
Чтобы наслаждаться Newsround в лучшем виде, вам необходимо включить JavaScript.
Если вы не видите интерактивное действие на этой странице, щелкните здесь.
Почему периодическая таблица называется периодической таблицей?
Она называется периодической таблицей из-за расположения элементов.
Вы заметите, что они расположены в строках и столбцах.
Горизонтальные строки (идущие слева направо) называются «точками», а вертикальные столбцы (идущие сверху вниз) называются «группами».
Супернаучные открытия
Кто создал периодическую таблицу?
В 1869 году русский ученый Дмитрий Менделеев изобрел периодическую систему, которую мы используем до сих пор.
До него другие пытались «упорядочить» элементы, но их таблицы были неполными или сгруппировали элементы вместе, которые не были похожи.
Таблица Дмитрия не включала все элементы, потому что не все они были известны в то время.
Он оставил для них пробелы и мог предсказать их свойства, основываясь на элементах вокруг них в своей таблице.
SSPL / Print CollectorДмитрий Менделеев изобрел периодическую таблицу в 1869 году.
Почему периодическая таблица так важна?
Все, включая людей! – состоят из элементов, поэтому очень важно их понимать.
Когда таблица Дмитрия была впервые создана, она помогла ученым сделать это, и это делается до сих пор.
Периодическая таблица также означает, что ученые могут предсказывать свойства материи на Земле – и в остальной части Вселенной.
Он был назван «одним из самых значительных достижений науки» Организацией Объединенных Наций, которая постановила, что 2019 год является международным годом Периодической таблицы химических элементов!
Getty Images% PDF-1.6 % 30 0 obj> эндобдж xref 30 271 0000000016 00000 н. 0000006156 00000 н. 0000006291 00000 п. 0000006520 00000 н. 0000006570 00000 н. 0000006871 00000 н. 0000007768 00000 н. 0000007876 00000 н. 0000007984 00000 п. 0000008093 00000 н. 0000008203 00000 н. 0000008313 00000 н. 0000008423 00000 н. 0000008533 00000 н. 0000008642 00000 н. 0000008751 00000 н. 0000008861 00000 н. 0000008969 00000 н. 0000009077 00000 н. 0000009187 00000 н. 0000009297 00000 н. 0000009407 00000 н. 0000009517 00000 н. 0000009627 00000 н. 0000009736 00000 н. 0000009846 00000 н. 0000009955 00000 н. 0000010065 00000 п. 0000010175 00000 п. 0000010285 00000 п. 0000010395 00000 п. 0000010504 00000 п. 0000010614 00000 п. 0000010724 00000 п. 0000010833 00000 п. 0000010943 00000 п. 0000011053 00000 п. 0000011163 00000 п. 0000011272 00000 п. 0000011382 00000 п. 0000011492 00000 п. 0000011602 00000 п. 0000011712 00000 п. 0000011822 00000 п. 0000011931 00000 п. 0000012040 00000 п. 0000012149 00000 п. 0000012258 00000 п. 0000012367 00000 п. 0000012476 00000 п. 0000012586 00000 п. 0000012694 00000 п. 0000012804 00000 п. 0000012913 00000 п. 0000013023 00000 п. 0000013133 00000 п. 0000013243 00000 п. 0000013353 00000 п. 0000013462 00000 п. 0000013571 00000 п. 0000013681 00000 п. 0000013791 00000 п. 0000013901 00000 п. 0000014011 00000 п. 0000014121 00000 п. 0000014230 00000 п. 0000014339 00000 п. 0000014448 00000 п. 0000014558 00000 п. 0000014668 00000 п. 0000014778 00000 п. 0000014888 00000 п. 0000014998 00000 п. 0000015108 00000 п. 0000015219 00000 п. 0000015329 00000 п. 0000015440 00000 п. 0000015549 00000 п. 0000015660 00000 п. 0000015771 00000 п. 0000015880 00000 п. 0000015989 00000 п. 0000016100 00000 п. 0000016209 00000 п. 0000016319 00000 п. 0000016429 00000 п. 0000016540 00000 п. 0000016650 00000 п. 0000016761 00000 п. 0000016872 00000 п. 0000016983 00000 п. 0000017093 00000 п. 0000017204 00000 п. 0000017315 00000 п. 0000017425 00000 п. 0000017535 00000 п. 0000017646 00000 п. 0000017757 00000 п. 0000017867 00000 п. 0000017977 00000 п. 0000018088 00000 п. 0000018199 00000 п. 0000018308 00000 п. 0000018419 00000 п. 0000018530 00000 п. 0000018640 00000 п. 0000018750 00000 п. 0000018861 00000 п. 0000018972 00000 п. 0000019082 00000 п. 0000019192 00000 п. 0000019302 00000 п. 0000019413 00000 п. 0000019524 00000 п. 0000019635 00000 п. 0000019746 00000 п. 0000019856 00000 п. 0000019966 00000 п. 0000020076 00000 п. 0000020186 00000 п. 0000020297 00000 п. 0000020406 00000 п. 0000020517 00000 п. 0000020628 00000 п. 0000020739 00000 п. 0000020906 00000 н. 0000021068 00000 п. 0000021104 00000 п. 0000022081 00000 п. 0000023053 00000 п. 0000023981 00000 п. 0000024917 00000 п. 0000025875 00000 п. 0000026893 00000 п. 0000027838 00000 п. 0000030133 00000 п. 0000030932 00000 п. 0000030968 00000 п. 0000031182 00000 п. 0000031262 00000 п. 0000031500 00000 п. 0000032299 00000 н. 0000053332 00000 п. 0000053556 00000 п. 0000054126 00000 п. 0000075131 00000 п. 0000075350 00000 п. 0000076098 00000 п. 0000076141 00000 п. 0000076185 00000 п. 0000076229 00000 п. 0000076273 00000 п. 0000076316 00000 п. 0000076359 00000 п. 0000076402 00000 п. 0000076446 00000 п. 0000076489 00000 п. 0000076534 00000 п. 0000076578 00000 п. 0000076622 00000 п. 0000076667 00000 п. 0000076712 00000 п. 0000076755 00000 п. 0000076799 00000 н. 0000076843 00000 п. 0000076887 00000 п. 0000076930 00000 п. 0000076974 00000 п. 0000077018 00000 п. 0000077062 00000 п. 0000077105 00000 п. 0000077149 00000 п. 0000077194 00000 п. 0000077238 00000 п. 0000077282 00000 п. 0000077326 00000 п. 0000077370 00000 п. 0000077414 00000 п. 0000077458 00000 п. 0000077502 00000 п. 0000077547 00000 п. 0000077591 00000 п. 0000077635 00000 п. 0000077679 00000 п. 0000077723 00000 п. 0000077767 00000 п. 0000077810 00000 п. 0000077854 00000 п. 0000077898 00000 п. 0000077943 00000 п. 0000077988 00000 п. 0000078032 00000 п. 0000078076 00000 п. 0000078121 00000 п. 0000078166 00000 п. 0000078211 00000 п. 0000078255 00000 п. 0000078299 00000 п. 0000078343 00000 п. 0000078387 00000 п. 0000078430 00000 п. 0000078474 00000 п. 0000078518 00000 п. 0000078562 00000 п. 0000078607 00000 п. 0000078651 00000 п. 0000078695 00000 п. 0000078738 00000 п. 0000078782 00000 п. 0000078826 00000 п. 0000078870 00000 п. 0000078914 00000 п. 0000078958 00000 п. 0000079003 00000 п. 0000079047 00000 п. 0000079091 00000 п. 0000079135 00000 п. 0000079179 00000 п. 0000079223 00000 п. 0000079268 00000 п. 0000079312 00000 п. 0000079356 00000 п. 0000079400 00000 п. 0000079444 00000 п. 0000079488 00000 п. 0000079532 00000 п. 0000079576 00000 п. 0000079620 00000 н. 0000079665 00000 п. 0000079711 00000 п. 0000079756 00000 п. 0000079801 00000 п. 0000079845 00000 п. 0000079889 00000 п. 0000079933 00000 н. 0000079977 00000 н. 0000080021 00000 п. 0000080066 00000 п. 0000080110 00000 п. 0000080154 00000 п. 0000080198 00000 п. 0000080242 00000 п. 0000080286 00000 п. 0000080330 00000 п. 0000080374 00000 п. 0000080418 00000 п. 0000080462 00000 п. 0000080506 00000 п. 0000080550 00000 п. 0000080593 00000 п. 0000080637 00000 п. 0000080681 00000 п. 0000080725 00000 п. 0000080769 00000 п. 0000080814 00000 п. 0000080858 00000 п. 0000080902 00000 п. 0000080946 00000 п. 0000080990 00000 п. 0000081035 00000 п. 0000081096 00000 п. 0000081189 00000 п. 0000081234 00000 п. 0000081279 00000 п. 0000081324 00000 п. 0000081378 00000 п. 0000081448 00000 п. 0000081529 00000 п. 0000081612 00000 п. 0000081653 00000 п. 0000005716 00000 н. трейлер ] >> startxref 0 %% EOF 300 0 obj> поток $.ch3BTWƚ
Периодическая таблица для печати
Одним из самых полезных инструментов в химии является таблица Менделеева, в которой все элементы упорядочены по их атомным номерам. Таблица Менделеева – это намного больше, чем просто таблица, которая существует на протяжении многих поколений. Печатная таблица Менделеева – отличный инструмент как для студентов, так и для учителей. Он обеспечивает быструю ссылку на верхнюю строку периодической таблицы Менделеева без необходимости искать информацию за час в Википедии или других источниках.
Что интересно в новой, улучшенной версии таблицы, так это то, что в ней перечислены все 118 элементов с их текущими атомными номерами. В печатной таблице Менделеева также есть много места для маркировки различных элементов, так что ее можно использовать в качестве образовательного инструмента для объяснения того, как каждый элемент работает с другими в своей группе.
Это означает, что вы можете использовать это, чтобы увидеть, какими они были до того, как были изменены учеными или изменились со временем. Если вы ищете увлекательный способ узнать больше о науке и химии, ознакомьтесь с нашим сообщением в блоге о печатной таблице Менделеева.
Периодические таблицы
Периодическая таблица Менделеева – отличный способ узнать об элементах. Если вы такой же фанат химии, как я, то эта таблица Менделеева для печати может быть идеальной вещью для вашего стола. Самая интересная и интерактивная часть этой печатной формы – это возможность настраивать вашу собственную периодическую таблицу, добавляя или удаляя строки, столбцы или отдельные элементы.
Независимо от того, какую возрастную группу вы преподаете, в периодической таблице будет элемент, с которым они смогут связать.Он также включает информацию о каждом элементе, включая их атомный номер и вес, что позволяет легко ориентироваться при обучении. Давайте посмотрим на 8 типов периодических таблиц для печати.
Периодическая таблица с зарядами
Периодическая таблица элементов часто обозначается символами элементов. Эта диаграмма может использоваться для определения платы за элемент. Периодическая таблица начислений – это сборник информации о плате за каждый элемент. Стол можно использовать как инструмент для студентов или всех, кто хочет больше узнать об окружающем мире.
Периодическая таблица с атомной массой
Периодическая таблица – это диаграмма, на которой показаны все элементы и их свойства. Впервые она была создана русским химиком Дмитрием Менделеевым, но он был не единственным, кто составил одну из этих диаграмм. Есть много разных версий этой диаграммы, в том числе с атомной массой вместо атомного номера. Атомная масса элемента – это общее количество протонов и нейтронов в его ядре. Таблица Менделеева с атомной массой выше поможет вам узнать атомную массу каждого элемента.
Периодическая таблица электроотрицательности
Периодическая таблица элементов является наиболее широко используемым инструментом в химии и дает полный обзор свойств каждого элемента. Есть аккуратная небольшая таблица, называемая периодической таблицей электроотрицательности, которая показывает, насколько некоторые элементы притягивают электроны. Вы можете использовать эту информацию при принятии решения о том, какой тип соединения будет образовываться с различными типами атомов в них, или если они даже позволят другим соединениям остаться.
Периодическая таблица с числами окисления
Периодическая таблица элементов – это таблица, в которой упорядочены все известные химические элементы. Вертикальные столбцы на этой диаграмме называются группами, и эти группы представляют похожие свойства. Периодическая таблица – это таблица, на которой показаны элементы и их степени окисления. Его можно использовать, чтобы выяснить, сколько валентных электронов имеет элемент, что помогает определить, какие соединения он будет образовывать с другими элементами в таких реакциях, как горение или кислотно-щелочная химия.
Таблица Менделеева Черное и белое
Периодическая таблица – полезный инструмент для поиска информации об элементах. Печатную версию Черно-белой Периодической таблицы можно распечатать и использовать для поиска деталей о любом элементе, а также для того, чтобы увидеть, как он взаимодействует с другими элементами в различных соединениях.
Периодическая таблица с состояниями
Периодическая таблица с состояниями – это диаграмма, которая показывает все различные элементы в природе и их соответствующие свойства.Периодическая таблица с состояниями – это диаграмма, в которой вверху перечислены все элементы по имени, а под каждым из них есть соответствующее состояние, чтобы обозначить то, на что они обычно похожи при комнатной температуре. Например, гелий будет использоваться под газом, потому что эта форма составляет большую часть его естественного состава.
Периодическая таблица электронной конфигурации
Периодическая таблица с конфигурацией электронов представляет собой таблицу со всеми элементами и их электронами. Каждый элемент имеет свой собственный набор положительно заряженных протонов, отрицательных нейтронов и нейтральных частиц, известных как электроны, которые организованы в оболочки или энергетические уровни вокруг ядра атома.
Количество возможных расположений увеличивается с каждой новой оболочкой, добавляемой к этому типу организационной системы, что делает их очень полезными при идентификации минералов, таких как золото, поскольку они имеют схожие свойства. Электронные конфигурации можно найти в так называемой Периодической таблице, где будет перечислен каждый отдельный атомный элемент вместе с тем, сколько положительных зарядов, отрицательных носителей заряда и электронов содержится в нем.
Таблица Менделеева с оболочками
Периодическая таблица – это не просто таблица элементов.Это также организационная система, которая показывает, как химические свойства связаны с атомными номерами и электронными конфигурациями, которые, в свою очередь, могут быть связаны с положением каждого элемента в таблице. Оболочки описывают, на каких энергетических уровнях можно найти электрон, когда он вращается вокруг положительно заряженного ядра атомов.
Заключительные слова
Периодическая таблица Менделеева – прекрасный инструмент для понимания химии, но это также отличный способ визуализировать отношения между всеми различными элементами.Эти печатные периодические таблицы, приведенные выше, позволят вам увидеть, как каждый элемент соотносится друг с другом, и могут быть использованы в качестве учебного пособия при подготовке к следующему тесту или викторине.
