Читать книгу «Загадка «Таблицы Менделеева»» онлайн полностью📖 — Петра Дружинина — MyBook.
© П.А. Дружинин, 2019
© ООО «Новое литературное обозрение», 2019
* * *
Памяти историка Арсения Борисовича Рогинского (30.III.1946–17.XII.2017)
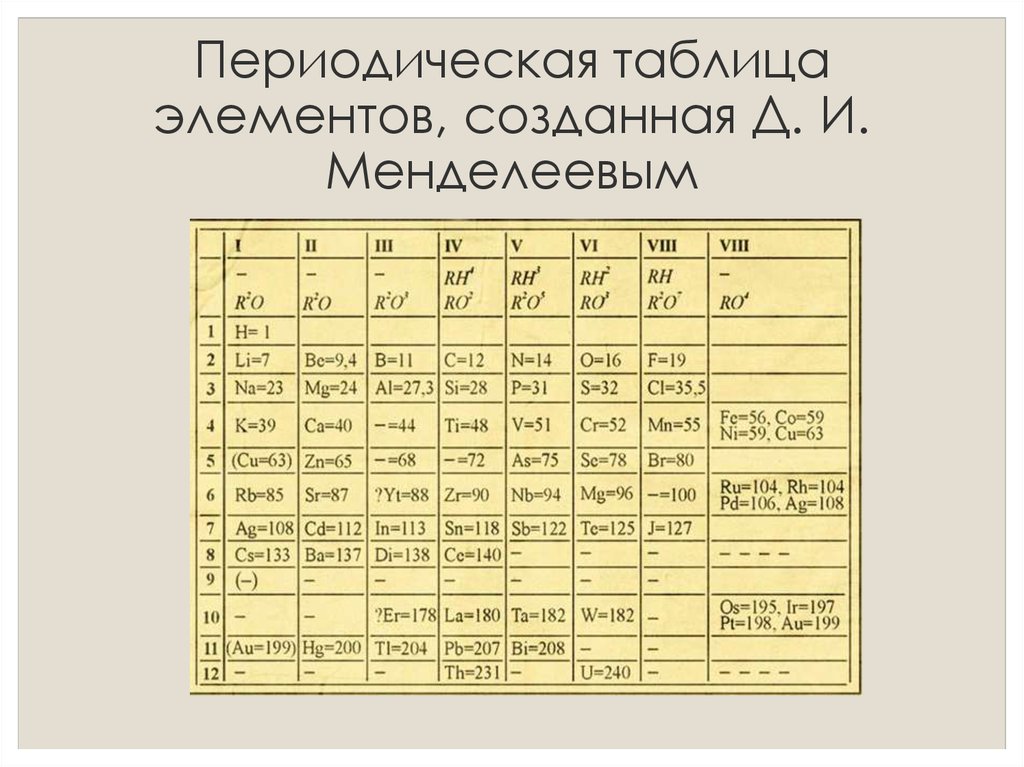
17 февраля (1 марта) 1869 года Д.И. Менделеевым был завершен «Опыт системы элементов, основанной на их атомном весе и химическом сходстве» – бескоординатная таблица, прообраз Периодической системы химических элементов, включавшая 63 известных элемента и 4 предсказанных. Это событие знаменовало открытие Периодического закона. Вскоре закон получил формулировку: «Свойства элементов, а потому и свойства образуемых ими простых и сложных тел находятся в периодической зависимости от их атомного веса», система элементов в ноябре 1870 года была Менделеевым названа «естественной», а в марте 1871 и «периодической», обретя знакомые нам графические очертания.
То есть именно составление и затем публикация «Опыта системы элементов…» знаменовали собой начало открытия Д. И. Менделеевым Периодического закона – одного из фундаментальных законов естествознания.
И. Менделеевым Периодического закона – одного из фундаментальных законов естествознания.
Точная дата открытия – редкое явление в истории науки, но она была указана самим Д.И. Менделеевым на сохранившейся рукописи «Опыта системы элементов…» (далее – «Опыт…»), служившей образцом для типографского набора[1]. Этот лист уцелел и ныне хранится в Музее-архиве Д.И. Менделеева[2].
Хотя «правдивое изложение великих открытий, сделанных даже не в очень давние времена, затруднено тем, что мы вынуждены довольствоваться свидетельствами современников и отдельными трудами и записками самих ученых, не имея возможности расспросить их лично о подробностях работы»[3], но день 17 февраля (1 марта) 1869 года оказался реконструирован со многими подробностями. Особенно прочно в научную и научно-популярную литературу вошли две версии открытия: каждая из них представляет собою род фантазии, но привлекательной.
Первая проистекает из воспоминаний друга Менделеева, профессора по кафедре геологии Петербургского университета А.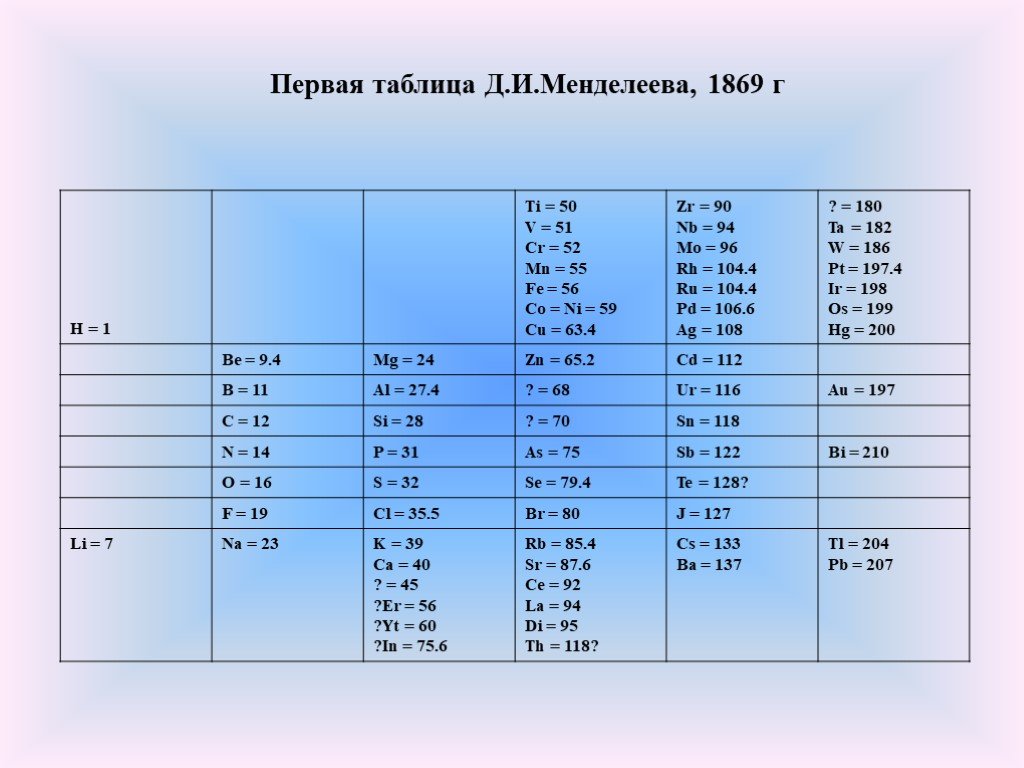 А. Иностранцева: «Перед самым открытием закона Дмитрий Иванович провозился над искомою таблицею целую ночь до утра, но и все же ничего не вышло; он с досады бросил работу и, томимый желанием выспаться, тут же, в рабочем кабинете, не раздеваясь, повалился на диван и крепко заснул. Во сне он увидел вполне ясно ту таблицу, которая позднее была напечатана. Даже во сне радость его была настолько сильна, что он сейчас же проснулся и быстро набросал эту таблицу на первом клочке бумаги, валявшемся у него на конторке»[4]. Этот запоминающийся рассказ оказался крайне популярным у потомков.
А. Иностранцева: «Перед самым открытием закона Дмитрий Иванович провозился над искомою таблицею целую ночь до утра, но и все же ничего не вышло; он с досады бросил работу и, томимый желанием выспаться, тут же, в рабочем кабинете, не раздеваясь, повалился на диван и крепко заснул. Во сне он увидел вполне ясно ту таблицу, которая позднее была напечатана. Даже во сне радость его была настолько сильна, что он сейчас же проснулся и быстро набросал эту таблицу на первом клочке бумаги, валявшемся у него на конторке»[4]. Этот запоминающийся рассказ оказался крайне популярным у потомков.
Вторая возникает позднее, уже в середине ХХ века, на волне борьбы за приоритет русской науки (возникшей антитезой к «низкопоклонству перед Западом»), когда после обнаружения в январе 1949 года в архиве Д.И. Менделеева важных черновых материалов[5], вопросом открытия Периодического закона занялся будущий академик, химик по образованию, философ по призванию Б.М. Кедров. К тому времени он был известным научным и партийным деятелем: ранее сотрудник аппарата ЦК, в 1948 году, будучи креатурой Г. Ф. Александрова, возглавил журнал «Вопросы философии», в том же году вышла его книга «Развитие понятия элемента от Менделеева до наших дней», но опала патрона положила конец восхождению на партийный олимп. Работы Кедрова были печатно названы «антимарксистскими и космополитическими»[6], а по поводу книги Кедрова «Энгельс и естествознание» (1947) И.В. Сталин высказался следующим образом: «У некоторых наших ученых нет чувства национальной гордости, патриотизма… У нас разглагольствуют об “интернационализации науки”. Даже в книгу Кедрова эта идея проникла. Идея об интернационализации науки – это шпионская идея»[7]. В марте 1949 года, как «не справившийся с работой», он лишается поста редактора журнала, но остается зав. редакцией естествознания и техники БСЭ.
Ф. Александрова, возглавил журнал «Вопросы философии», в том же году вышла его книга «Развитие понятия элемента от Менделеева до наших дней», но опала патрона положила конец восхождению на партийный олимп. Работы Кедрова были печатно названы «антимарксистскими и космополитическими»[6], а по поводу книги Кедрова «Энгельс и естествознание» (1947) И.В. Сталин высказался следующим образом: «У некоторых наших ученых нет чувства национальной гордости, патриотизма… У нас разглагольствуют об “интернационализации науки”. Даже в книгу Кедрова эта идея проникла. Идея об интернационализации науки – это шпионская идея»[7]. В марте 1949 года, как «не справившийся с работой», он лишается поста редактора журнала, но остается зав. редакцией естествознания и техники БСЭ.
Будучи составной частью номенклатуры, Б.М. Кедров быстро оправился от удара и вскоре вновь оказался среди бойцов идеологического фронта. Возвратившись к химии, Кедров вступает в развернутую к тому времени т. н. антирезонансную кампанию[8][9][10], где занимает место одного из наиболее неумолимых критиков. В роли трибуна он громит «порочную» теорию резонанса Л. Полинга, мезомерный эффект К. Ингольда; критикует «с точки зрения химии» работы Э. Шредингера, выступает против «некритического перенесения на химию некоторых представлений, проповедуемых “физическими” идеалистами в квантовой механике», подвергает остракизму принцип суперпозиции П. Дирака и принцип дополнительности В. Гейзенберга, предостерегает химиков от развития таких положений, поскольку это может «завести химию в дебри, значительно худшие, чем теория резонанса»[11] и т. д.
антирезонансную кампанию[8][9][10], где занимает место одного из наиболее неумолимых критиков. В роли трибуна он громит «порочную» теорию резонанса Л. Полинга, мезомерный эффект К. Ингольда; критикует «с точки зрения химии» работы Э. Шредингера, выступает против «некритического перенесения на химию некоторых представлений, проповедуемых “физическими” идеалистами в квантовой механике», подвергает остракизму принцип суперпозиции П. Дирака и принцип дополнительности В. Гейзенберга, предостерегает химиков от развития таких положений, поскольку это может «завести химию в дебри, значительно худшие, чем теория резонанса»[11] и т. д.
Почти одновременно с лишением Б.М. Кедрова номенклатурных благ, в Ленинграде в музее-архиве Д.И. Менделеева М.Д. Менделеева-Кузьмина (приходившаяся фондообразователю дочерью) и Т.С. Кудрявцева обнаруживают неизвестные материалы. Б.М. Кедров быстро заинтересовался ими и вскоре превратился в крупнейшего исследователя Периодического закона[12][13], параллельно критикуя 25-томное издание «Сочинений» Д.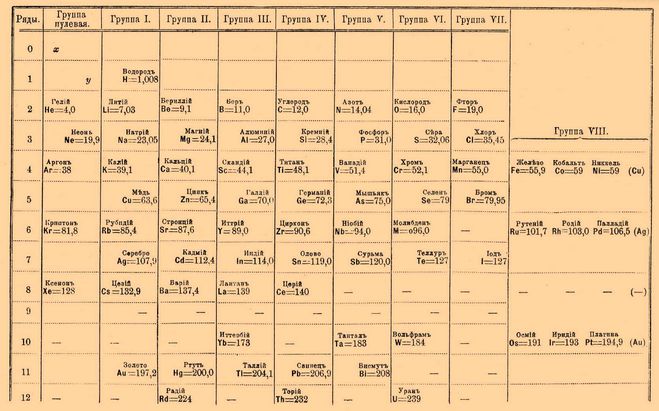 И. Менделеева (1937–1952)[14] за «принципиальные ошибки философского характера», за «грубое извращение» и явные ошибки в истории открытия Периодического закона, «в корне извращающие историю научного подвига»[15], освобождая таким образом себе поле научной деятельности.
И. Менделеева (1937–1952)[14] за «принципиальные ошибки философского характера», за «грубое извращение» и явные ошибки в истории открытия Периодического закона, «в корне извращающие историю научного подвига»[15], освобождая таким образом себе поле научной деятельности.
Учитывая требования эпохи и собственные воззрения, Б.М. Кедров, с одной стороны, старался в своих трудах еще более убедительно утвердить приоритет Менделеева в открытии Периодического закона, с другой же, проводил собственную оригинальную теорию, что открытие совершилось Менделеевым хотя и не во сне, но в один -единственный день, после раскладки «химического пасьянса». Теория «дня одного великого открытия» потребовала от Б.М. Кедрова хронометрировать или, как он выразился, «микроанатомировать» день 17 февраля (1 марта) 1869 года практически по минутам, чему был посвящен ряд его работ[16][17][18][19][20]. И факты, и предположения, и совпадения, и несовпадения… Все оказалось сдавлено Б. М. Кедровым под прессом «однодневной» теории.
М. Кедровым под прессом «однодневной» теории.
Научный авторитет (а еще более – административный вес) Б.М. Кедрова был во второй половине ХХ века столь высок, что на долгие десятилетия миф о «дне одного великого открытия» оказался канонизирован в истории науки, став непреложной исторической истиной. Причем не только в России, но и, благодаря переводам его работ[21][22], за рубежом. Распространению этой версии в отечественной литературе способствовало навязываемое единомыслие; в зарубежной – ограниченность источников и невозможность без знания русского языка критически рассмотреть сохранившиеся материалы, которыми оперировал Б.М. Кедров.
Категоричность его версии если и становилась в ХХ столетии предметом научной критики, то крайне редко и всегда одинаково робко. Например, в книге А.А. Макарени[23], где автор постарался избегать всякой критики, но отстраненно излагал свой взгляд на проблему. (Ранее, в написанной совместно с С.А. Щукарёвым рецензии на подготовленный Б.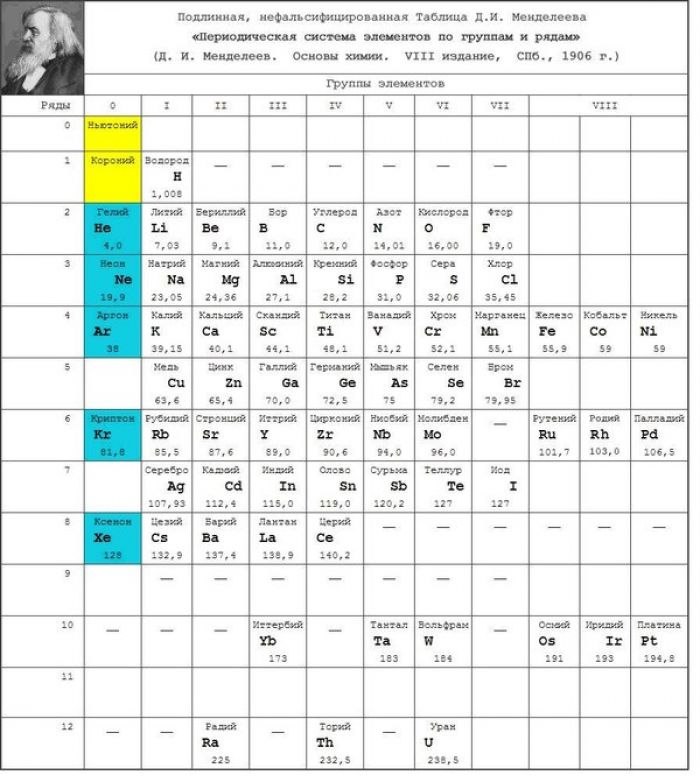 М. Кедровым том «Периодический закон» в серии «Классики науки»[24], критика касалась слабости собственно научной, химической составляющей трактовок Б.М. Кедрова, в особенности же его смелого заявления, что «система элементов в принципе может быть выражена также и аналитически, алгебраически, в виде определенного математического уравнения».) Исключением же является, по-видимому, лишь примечание в книге В.И. Семишина относительно формулировки заголовка книги Кедрова: «Это название малоудачное: речь идет о завершающем дне открытия, над которым Д.И. Менделеев работал около 15 лет»[25]. Уже после смерти Б.М. Кедрова историк химии Д.Н. Трифонов, который был единомышленником и соавтором академика[26], предложил «Версию-2» открытия Периодического закона[27], в которой шел по стопам Б.М. Кедрова, но все-таки отверг теорию, что беловая рукопись «Опыта…» была создана в течение одного дня, указывая на уязвимость такой теории именно в соединении всех событий в одном дне и рассматривая эту дату как «день завершения одного великого открытия»[28].
М. Кедровым том «Периодический закон» в серии «Классики науки»[24], критика касалась слабости собственно научной, химической составляющей трактовок Б.М. Кедрова, в особенности же его смелого заявления, что «система элементов в принципе может быть выражена также и аналитически, алгебраически, в виде определенного математического уравнения».) Исключением же является, по-видимому, лишь примечание в книге В.И. Семишина относительно формулировки заголовка книги Кедрова: «Это название малоудачное: речь идет о завершающем дне открытия, над которым Д.И. Менделеев работал около 15 лет»[25]. Уже после смерти Б.М. Кедрова историк химии Д.Н. Трифонов, который был единомышленником и соавтором академика[26], предложил «Версию-2» открытия Периодического закона[27], в которой шел по стопам Б.М. Кедрова, но все-таки отверг теорию, что беловая рукопись «Опыта…» была создана в течение одного дня, указывая на уязвимость такой теории именно в соединении всех событий в одном дне и рассматривая эту дату как «день завершения одного великого открытия»[28]. Несмотря на в целом скептическое отношение к «Версии-2» Д.Н. Трифонова у позднейших исследователей[29][30], в ней есть важный, хотя и скрытый рациональный смысл: показывая сомнительность многих утверждений, которые преподносились Б.М. Кедровым в качестве безусловной истины, тем самым Д.Н. Трифонов в значительной степени (может быть, и неосознанно) дезавуирует выводы Б.М. Кедрова. В любом случае из работ Д.Н. Трифонова становится очевидной совершенная гадательность многих «истин» в истории открытии Периодического закона, чем открывается возможность для будущих исследователей к новым интерпретациям событий.
Несмотря на в целом скептическое отношение к «Версии-2» Д.Н. Трифонова у позднейших исследователей[29][30], в ней есть важный, хотя и скрытый рациональный смысл: показывая сомнительность многих утверждений, которые преподносились Б.М. Кедровым в качестве безусловной истины, тем самым Д.Н. Трифонов в значительной степени (может быть, и неосознанно) дезавуирует выводы Б.М. Кедрова. В любом случае из работ Д.Н. Трифонова становится очевидной совершенная гадательность многих «истин» в истории открытии Периодического закона, чем открывается возможность для будущих исследователей к новым интерпретациям событий.
Европейские историки науки, которым внешние обстоятельства не мешали проявлять свободомыслие, также пытались рассмотреть «день одного великого открытия» не в качестве даты божественного откровения или молниеносного озарения. В первую очередь в данной связи нужно сказать о работе 1969 года шведского историка химии Яна-Вильгельма ван Спронсена[31] и 1986 года французского историка химии Бернадетт Бенсод-Вансанн[32].
Началом XXI века можно датировать окончательное освобождение от оков теории «дня одного великого открытия», зафиксированное прежде всего в работах И.С. Дмитриева[33][34][35][36][37], показавшего, что «история открытия Периодического закона сложна и драматична, гораздо более сложна и драматична, нежели она представлена в версии Кедрова». Процитируем фрагмент вывода, который делает И.С. Дмитриев: «В любом случае, 17 февраля 1869 г. не может считаться днем “одного великого открытия” и даже днем его завершения. Создание “Опыта” означало вступление работы по систематике элементов в ту фазу, когда Менделеев, убедившись, что “способ распределения элементов по их атомному весу не противоречит естественному сходству, существующему между элементами, а напротив того, прямо на него указывает”, и что в подмеченных им закономерностях “случайности допустить было невозможно”, уже мог сформулировать первые фундаментальные выводы, составившие ядро учения о периодичности и дать, пусть не вполне совершенное, графическое представление почти полной системы элементов, “основанной на их атомном весе и химическом сходстве”. Но самая трудная часть работы была впереди, и на нее у Менделеева ушел год и девять месяцев»[38].
Но самая трудная часть работы была впереди, и на нее у Менделеева ушел год и девять месяцев»[38].
Основные версии были отреферированы в работе А.М. Смолеговского «История открытия Периодического закона»[39], где автор не отдает предпочтения ни одной из них, лишь допуская легкую иронию по поводу некоторых из рассмотренных фактов. Обобщенная история версий, без всякой иронии, но уже с собственными ошибками компиляторов, вошла в учебные пособия[40].
Из публикаций же зарубежных ученых, внесших вклад в изучение вопроса, особенно нужно отметить работы Масанори Кайдзи[41][42] и Майкла Гордина[43][44].
Все наличествующие версии сходятся прежде всего в одном бесспорном факте: совершенное Д.И. Менделеевым открытие Периодического закона было обнародовано посредством публикации первой таблицы – «Опыта…». Традиционно считается, что он отпечатан 1 марта 1869 года[45][46].
Кроме того, в истории открытия Периодического закона зафиксирована еще одна точная дата – день 6 (18) марта 1869 года, когда об открытии было объявлено в заседании Русского химического общества при Императорском Санкт-Петербургском университете (далее – РХО): «Н. Меншуткин сообщает от имени Д. Менделеева опыт системы элементов, основанной на их атомном весе и химическом сходстве. За отсутствием Д. Менделеева обсуждение этого сообщения отложено до следующего заседания»[47][48]. Как известно, на следующем заседании 3 (15) апреля 1869 года никакого обсуждения уже не последовало, зато в № 2/3 «Журнала РХО» за 1869 год была напечатана статья Д.И. Менделеева «Соотношение свойств элементов с атомным весом элементов», также с первоначальной таблицей – то есть «Опытом…». Не вполне очевидно, почему Д.И. Менделеев не стал лично докладывать об открытии в заседании РХО: формальным основанием был указан его отъезд (хотя вопрос о том, в действительности ли Менделеев уезжал или остался дома из-за недомогания, как ошибочно в свое время указал Б.Н. Меншуткин[49] и потом повторил А.Е. Ферсман[50] и другие, неожиданно вылился в отдельный диспут историков химии[51][52][53][54]), но в чем была первопричина – неясно.
Меншуткин сообщает от имени Д. Менделеева опыт системы элементов, основанной на их атомном весе и химическом сходстве. За отсутствием Д. Менделеева обсуждение этого сообщения отложено до следующего заседания»[47][48]. Как известно, на следующем заседании 3 (15) апреля 1869 года никакого обсуждения уже не последовало, зато в № 2/3 «Журнала РХО» за 1869 год была напечатана статья Д.И. Менделеева «Соотношение свойств элементов с атомным весом элементов», также с первоначальной таблицей – то есть «Опытом…». Не вполне очевидно, почему Д.И. Менделеев не стал лично докладывать об открытии в заседании РХО: формальным основанием был указан его отъезд (хотя вопрос о том, в действительности ли Менделеев уезжал или остался дома из-за недомогания, как ошибочно в свое время указал Б.Н. Меншуткин[49] и потом повторил А.Е. Ферсман[50] и другие, неожиданно вылился в отдельный диспут историков химии[51][52][53][54]), но в чем была первопричина – неясно. То ли потому, что «Опыт…», как пишет И.С. Дмитриев, был пока еще «компромиссным вариантом системы элементов»[55], то ли Менделееву непременно нужно было посетить свое имение; в любом случае неприсутствие Менделеева 6 (18) марта на заседании РХО вполне справедливо трактуется Д.Н. Трифоновым как «психологическая загадка»[56]. Но при всей дискуссионности этих двух важных вопросов сама дата открытия Периодического закона 17 февраля (1 марта) 1869 года, начертанная на рукописи «Опыта…», остается незыблемой.
То ли потому, что «Опыт…», как пишет И.С. Дмитриев, был пока еще «компромиссным вариантом системы элементов»[55], то ли Менделееву непременно нужно было посетить свое имение; в любом случае неприсутствие Менделеева 6 (18) марта на заседании РХО вполне справедливо трактуется Д.Н. Трифоновым как «психологическая загадка»[56]. Но при всей дискуссионности этих двух важных вопросов сама дата открытия Периодического закона 17 февраля (1 марта) 1869 года, начертанная на рукописи «Опыта…», остается незыблемой.
И здесь мы подступаем к формулировке основной задачи настоящей работы: попытаться установить, когда и где было впервые опубликовано первое свидетельство о выдающемся открытии, то есть подвергнуть ревизии разрозненные сведения о подготовке и печатании «Опыта…» – типографского первенца Периодической системы химических элементов.
Этот принципиальный вопрос истории науки давно считается решенным если не в тонкостях, то in toto. Как сообщается в «Летописи жизни и деятельности Д.М. Менделеева» (далее – «Летопись»), 17 февраля (1 марта) Менделеев «вечером послал набело переписанную таблицу “Опыт…” в типографию, сделав пометки для наборщиков и поставив дату “17 февраля 1869 г. ”»; 20 февраля «держал корректуру “Опыта…”»; 1 (12) марта «разослал отпечатанные листки с “Опытом…” многим отечественным и зарубежным химикам»[57]. Точная дата рассылки «Опыта…» была указана самим Менделеевым в 1899 году в рукописном «Списке моих сочинений», где, упоминая французский листок с «Опытом…» (№ 43), он пишет: «Первые мысли о периодичности вложены в листок № 43, который 1 марта 1869 г. был послан многим ученым»[58]
Как сообщается в «Летописи жизни и деятельности Д.М. Менделеева» (далее – «Летопись»), 17 февраля (1 марта) Менделеев «вечером послал набело переписанную таблицу “Опыт…” в типографию, сделав пометки для наборщиков и поставив дату “17 февраля 1869 г. ”»; 20 февраля «держал корректуру “Опыта…”»; 1 (12) марта «разослал отпечатанные листки с “Опытом…” многим отечественным и зарубежным химикам»[57]. Точная дата рассылки «Опыта…» была указана самим Менделеевым в 1899 году в рукописном «Списке моих сочинений», где, упоминая французский листок с «Опытом…» (№ 43), он пишет: «Первые мысли о периодичности вложены в листок № 43, который 1 марта 1869 г. был послан многим ученым»[58]
Введение в периодическую таблицу элементов
AB 11 Наука 20 (2007 г., обновлено в 2014 г.) Блок A: химические изменения
AB 12 Химия 30 (2007 г., обновление 2014 г.) Модуль B: Электрохимические изменения
MB 12 Химия 12 класс (2013) Тема 6: Электрохимия
NL 12 Химия 3202 (2005) Блок 4: Электрохимия
НС 12 Химия 12 (2009, 2019) Электрохимия
НУ
11
Science 20 (Альберта, 2007 г. , обновлено в 2014 г.)
Блок А: Химические изменения
, обновлено в 2014 г.)
Блок А: Химические изменения
НУ 12 Химия 30 (Альберта, 2007 г., обновлено в 2014 г.) Модуль B: Электрохимические изменения
ON 12 Химия, 12 класс, Колледж (СЧ5С) Нить D: Электрохимия
ON 12 Химия, 12 класс, университет (СЧ5У) Нить F: Электрохимия
ПЭ 12 Химия 621А (проект 2021 г.) Знание контента: CK 4.3
YT 12 Химия 12 (Британская Колумбия, июнь 2018 г.) Большая идея: Окисление и восстановление — это взаимодополняющие процессы, включающие приобретение или потерю электронов.
СК 12 Химия 30 (2016) Электрохимия
НТ 11 Science 20 (Альберта, 2007 г., обновлено в 2014 г.) Блок A: Химические изменения
NT 12 Химия 30 (Альберта, 2007 г., обновлено в 2014 г.) Раздел B: Электрохимические изменения
AB 11 Наука о знаниях и трудоустройстве 20–4 (2006 г.) Модуль A: Применение вещества и химических изменений
AB 10 Наука о знаниях и трудоустройстве 10-4 (2006) Модуль A: Исследование свойств материи
AB
9
Наука о знаниях и трудоустройстве 8, 9(пересмотрено в 2009 г.
AB 10 Наука 14 (2003 г., обновлено в 2014 г.) Модуль A: Исследование свойств материи
AB 9 Наука 7-8-9 (2003 г., обновлено в 2014 г.) Блок B: Материя и химические изменения
до н.э. 7 Естествознание, 7 класс (июнь 2016 г.) Большая идея: Элементы состоят из атомов одного типа, а соединения состоят из атомов разных элементов, химически объединенных.
до н.э. 9 Естествознание 9 класс (июнь 2016 г.) Большая идея: электронное расположение атомов влияет на их химическую природу.
МБ 9 Старший 1 Наука (2000) Кластер 2: Атомы и элементы
NL 9 9 класс Наука Блок 2: Атомы, элементы и соединения (пересмотрено в 2011 г.)
NL 12 Наука 3200 (2005) Модуль 1: Химические реакции
NS 9 Наука 9 (2021) Атомы и элементы
НУ 9 Наука о знаниях и трудоустройстве 9 (Альберта, редакция 2009 г.) Блок B: Материя и химические изменения
NU 9 Наука 9 (Альберта, 2003 г., обновлено в 2014 г.) Блок B: Материя и химические изменения
NU
11
Наука о знаниях и трудоустройстве 20–4 (Альберта, 2006 г. )
Раздел A: Применение материи и химических изменений
)
Раздел A: Применение материи и химических изменений
НУ 10 Наука о знаниях и трудоустройстве 10-4 (2006) Модуль A: Исследование свойств материи
NU 10 Наука 14 (2003 г., обновлено в 2014 г.) Модуль A: Исследование свойств материи
PE 9 Естествознание, 9 класс (пересмотрено в 2018 г.) Знание содержания: CK 2.1
YT 7 Science Grade 7 (Британская Колумбия, июнь 2016 г.) Большая идея: электромагнитная сила производит как электричество, так и магнетизм.
ЮТ 9 Science Grade 9 (Британская Колумбия, июнь 2016 г.) Большая идея: электронное расположение атомов влияет на их химическую природу.
СК 9 Наука 9 (2009) Физические науки – атомы и элементы (AE)
NT 9 Наука о знаниях и трудоустройстве 9 (Альберта, редакция 2009 г.) Модуль B: Материя и химические изменения
NT 9 Наука 9 (Альберта, 2003 г., обновлено в 2014 г.) Модуль B: Материя и химические изменения
NT 11 Наука о знаниях и трудоустройстве 20–4 (Альберта, 2006 г.) Модуль A: Применение материи и химических изменений
NT
10
Наука о знаниях и трудоустройстве 10-4 (Альберта, 2006 г. )
Модуль A: Исследование свойств материи
)
Модуль A: Исследование свойств материи
НТ 10 Наука 14 (Альберта, 2003 г., обновлено в 2014 г.) Модуль A: Исследование свойств материи
ON 9 9 класс естественных наук (SNC1W) (2022) Strand C: Природа материи
до н.э. 8 Наука 8 класс (июнь 2016 г.) Большая идея: поведение материи можно объяснить кинетической молекулярной теорией и атомной теорией.
КК Раздел III Наука и технология Материальный мир
КК Раздел III Прикладная наука и технологии Материальный мир
YT 8 Science Grade 8 (Британская Колумбия, июнь 2016 г.) Большая идея: поведение материи можно объяснить кинетической молекулярной теорией и атомной теорией.
до н.э. 11 Химия 11 (июнь 2018 г.) Большая идея: Атомы и молекулы являются строительными блоками материи.
КК Раздел I Наука и технология Материальный мир: Организация
QC Раздел II Наука и технология Материальный мир: Организация
YT
11
Химия 11 (Британская Колумбия, июнь 2018 г.)
Большая идея: Атомы и молекулы являются строительными блоками материи.
Поздравляем с 150-летием Периодической таблицы
Этот пост был написан специалистом по научным справочникам Нейтом Смитом .
В этом году исполняется 150 лет одному из важнейших открытий в области химии: Периодической таблице элементов. Хотя было сделано более 700 различных итераций таблицы (Scerri, 20), первые таблицы, явно показывающие периодичность, были созданы в 1860-х годах.
Первый пришел в 1862 году от французского геолога Александра Эмиля Бегуйе де Шанкуртуа в форме его теллурического винта. Согласно Королевскому химическому обществу, его система «отображала атомный вес элементов на внешней стороне цилиндра, так что один полный оборот соответствовал увеличению атомного веса на 16» (например, калий при 39и Марганец на 55). Общая форма напоминает леденец или парикмахерскую.
В 1863 году английский химик Джон Ньюлендс опубликовал другую таблицу, показывающую периодичность. С 1863 по 1890 год Ньюлендс опубликовал шестнадцать статей, объясняющих различные классификации элементов, хотя сегодня он наиболее известен своим законом октав. Эта классификация поместила шестьдесят пять элементов в группы на основе сходных химических свойств, что совпало с повторением свойств с интервалом в восемь. Ньюлендс также был первым, кто поместил теллур и йод в таблицу только на основании химических свойств вместо типичного метода увеличения атомного веса. (Шерри, 76)
Эта классификация поместила шестьдесят пять элементов в группы на основе сходных химических свойств, что совпало с повторением свойств с интервалом в восемь. Ньюлендс также был первым, кто поместил теллур и йод в таблицу только на основании химических свойств вместо типичного метода увеличения атомного веса. (Шерри, 76)
В 1864 году, в том же году, когда Ньюлендс опубликовал одну из этих таблиц, другой английский химик по имени Уильям Одлинг опубликовал свою таблицу, показывающую периодичность элементов. Он также был основан на химических свойствах и разделил сорок девять элементов на тринадцать отдельных групп. К его чести, Одлинг составил свою таблицу исключительно по химическим свойствам, «не принимая во внимание атомный вес». (Моррис, 155) Кроме того, он смог «правильно сгруппировать свинец, ртуть и платину, чего не заметили его современники». (по-прежнему, 11)
Густав Хинрихс, Программа атомной механики, 1867. стр. 9.
//lccn.loc.gov/11023427
Густавус Хинрихс, известный по целому ряду причин, включая введение термина «дерехо», также создал уникальную периодическую таблицу, основанную на взаимосвязи того, что он назвал «пантогенами, с их атомов, называемых панатомами, что объясняет числовые соотношения атомных весов и дает простую классификацию элементов». Эта система классификации завершилась в 1867 году его спиральной периодической таблицей, которая лучше прояснила группировку элементов. Классификация Хинрихса, хотя и заметно отличается от других периодических таблиц этого периода, «похоже, охватывает многие первичные отношения периодичности, наблюдаемые в современной периодической таблице… она не загромождена попытками показать вторичные отношения родства». (Шерри, 92)
Эта система классификации завершилась в 1867 году его спиральной периодической таблицей, которая лучше прояснила группировку элементов. Классификация Хинрихса, хотя и заметно отличается от других периодических таблиц этого периода, «похоже, охватывает многие первичные отношения периодичности, наблюдаемые в современной периодической таблице… она не загромождена попытками показать вторичные отношения родства». (Шерри, 92)
Еще одним химиком, которому приписывают самостоятельное создание периодической таблицы элементов, является Юлиус Лотар Мейер. В 1864 году Лотар Мейер опубликовал книгу, в которой содержалась таблица из двадцати восьми элементов, сгруппированных в «шесть семейств в порядке их валентности». (Тем не менее, 14) Эта таблица ясно показала периодическую связь между элементами, хотя она не предсказывала химические свойства неоткрытых элементов.
Первая периодическая таблица химических элементов, демонстрирующая периодический закон, 1869 г.. //www.loc.gov/item/92517587/
Это подводит нас к таблице Менделеева этой эпохи, которая наиболее широко известна и принята как первая (и положена в основу юбилея этого года): таблица Дмитрия Ивановича Менделеева 1869 г. При написании нового учебника по химии он искал способ упорядочить элементы. Он начал с того, что записал каждый элемент на карточке вместе с его атомным весом и химическими свойствами. Затем Менделеев распределил их по семи группам, внося поправки на основе свойств, а не атомного веса или того, что в то время считалось атомным весом. Например, считалось, что атомный вес урана равен 120, но для того, чтобы его можно было отнести к группе с аналогичными свойствами, его вес должен быть равен 240. Невозмутимый Менделеев присвоил урану этот атомный вес, который, как оказалось, не слишком велик. от современной цифры 238. (Моррис, 166) Главный скачок вперед, вызванный этой таблицей, заключался в том, что она «не только имела возможность предсказывать существование новых элементов, но и то, как они могут быть обнаружены. Образцы предсказывали, как элементы реагируют с другими химическими веществами, что стало ключом к их открытию». (по-прежнему, 13-14)
При написании нового учебника по химии он искал способ упорядочить элементы. Он начал с того, что записал каждый элемент на карточке вместе с его атомным весом и химическими свойствами. Затем Менделеев распределил их по семи группам, внося поправки на основе свойств, а не атомного веса или того, что в то время считалось атомным весом. Например, считалось, что атомный вес урана равен 120, но для того, чтобы его можно было отнести к группе с аналогичными свойствами, его вес должен быть равен 240. Невозмутимый Менделеев присвоил урану этот атомный вес, который, как оказалось, не слишком велик. от современной цифры 238. (Моррис, 166) Главный скачок вперед, вызванный этой таблицей, заключался в том, что она «не только имела возможность предсказывать существование новых элементов, но и то, как они могут быть обнаружены. Образцы предсказывали, как элементы реагируют с другими химическими веществами, что стало ключом к их открытию». (по-прежнему, 13-14)
У людей есть врожденная способность обнаруживать закономерности в окружающем нас мире.