11 лучших примеров химических изменений в повседневной жизни
Химическое изменение – это процесс, в котором одно или несколько веществ превращаются в одно или несколько новых и разных веществ. Эти вещества могут быть как химическими элементами, так и соединениями.
Химические изменения происходят в результате химических реакций. В ходе химической реакции происходит перегруппировка атомов, и реакция сопровождается изменением энергии, поскольку образуются новые вещества.
Другими словами, химические изменения – это фундаментальные изменения, которые порождают новые комбинации материи. Эти изменения обычно необратимы или обратимы только при дополнительном химическом изменении.
Хотя существуют сотни тысяч различных химических реакций, большинство из них имеют схожие свойства. Эти сходства позволяют нам разделить химические изменения на три широкие категории.
- Органические изменения включают химические реакции сложных углеродных соединений, в которых один или несколько атомов углерода ковалентно связаны с атомами других элементов, чаще всего водорода, азота или кислорода.

- Неорганические изменения – это химические реакции веществ, в которых, как правило, не участвуют атомы углерода. Эти изменения обычно происходят в лабораториях и тяжелой промышленности.
- Биохимические изменения происходят в живых организмах. Они контролируются или регулируются гормонами и ферментами.
Чтобы объяснить этот процесс более подробно, мы перечислили несколько наиболее распространенных примеров химических изменений, которые вы видите в повседневной жизни.
11. Выпечка торта
Тип: неорганическое изменение
Когда вы печете пирог, его ингредиенты (мука, яйцо, сахар, пекарский порошок и т.д.) претерпевают химические изменения. Это происходит в процессе выпечки:
- Тепло позволяет пекарскому порошку образовывать крошечные пузырьки газа, что делает пирог пушистым.
- Под воздействием тепла яичный белок изменяется и делает пирог твердым.
- Масло не дает теплу высушить пирог.

Поскольку этот процесс выпечки требует тепла, это эндотермическая реакция. Она не может быть обращена вспять, поскольку сахар и дрожжи создали новые вещества. Это означает, что после выпечки пирога вы не сможете разделить его на исходные компоненты (муку, яйца, сахар).
10. Сжигание природного газа
Тип: Органическое изменение
Природный газ – это углеводородная смесь, состоящая из множества различных соединений. Его основной компонент – метан (Ch5), соединение с одним атомом углерода и четырьмя атомами водорода. При сгорании метана в присутствии воздуха (кислорода) образуется вода, углекислый газ и тепло (в виде голубого пламени).
9. Взрыв фейерверка
Тип: Неорганические изменения
Фейерверки – это великолепное сочетание науки и инноваций. Они состоят из высокоэнергетических соединений, которые создают взрывы. При выделении достаточного количества тепла (энергии активации) в них происходит несколько химических реакций в быстрой последовательности.
Точнее, высокоэнергетические соединения, плотно упакованные внутри фейерверка, сгорают с кислородом воздуха и превращаются в другие соединения, выделяя при этом звук, тепло и газы (такие, как угарный газ, углекислый газ и азот).
Различные соединения дают разные цвета и оттенки, которые мы видим в темном ночном небе. Например, барий дает зеленый цвет, медь – синий, натрий – желтовато-оранжевый, а стронций – красный.
8. Созревание плодов
Тип: Органическое изменение
Созревание связано с изменениями в составе (например, превращение крахмала в сахар). Это процесс, в результате которого плоды приобретают желаемый вкус, цвет, качество и другие характеристики. По характеру созревания фрукты можно разделить на две группы:
- Климактерические плоды могут созревать после снятия с растения. Например, бананы, манго и яблоки продолжают созревать и не выдерживают жестких условий транспортировки и многократного перемещения.

- Неклимактеричные плоды не могут созревать после сбора урожая. Они производят небольшое количество этилена (гораздо меньше, чем климактерические плоды) и не реагируют на обработку этиленом. В качестве примера можно привести апельсин, виноград, ежевику, гранат и арбуз.
Поскольку созревание включает образование новых углеродсодержащих химикатов, которые приводят к изменению цвета и вкуса, можно смело назвать процесс созревания органическим химическим изменением.
7. Переваривание пищи
Тип: Органическое
В отличие от механического пищеварения, которое начинается во рту с жевания, химическое пищеварение – это сложный процесс, который разбивает пищу на составляющие. Эти строительные блоки в конечном итоге всасываются в плазму крови для питания клеток организма.
Более конкретно, большие молекулы пищи редуцируются до субъединиц, которые достаточно малы для поглощения слизистой оболочкой пищеварительного тракта.
- Белки распадаются на аминокислоты.
- Нуклеиновые кислоты распадаются на нуклеотиды.
- Углеводные сахара распадаются на моносахариды.
- Жиры расщепляются на жирные кислоты и моноглицериды.
Это достигается с помощью различных ферментов (таких, как ферменты слюны, желудка, щеточной каймы и ферменты поджелудочной железы) посредством гидролиза.
6. Гальваническое покрытие металла
Тип: неорганическое изменение
Гальваника – это процесс осаждения материала на твердую подложку с помощью электрического тока. Он используется для улучшения химических, физических и механических свойств подложки.
В этом процессе раствор, содержащий ионы металлов, помещается в резервуар, а подложка, на которую наносится покрытие, подключается к электрической сети, чтобы сделать ее катодом. Ионы металла в растворе движутся к катоду, где они приобретают электроны и образуют металлическое покрытие.
Распространенная форма гальванического покрытия используется для производства монет. Например, американский пенни сделан из цинка, покрытого слоем гальванической меди.
Например, американский пенни сделан из цинка, покрытого слоем гальванической меди.
5. Прокисание молока
Тип: Органическое изменение
Испорченное молоко кислое, с неприятным запахом и вкусом. Со временем оно становится комковатым и свертывается. В процессе скисания образуются новые молекулы, и этот процесс нельзя обратить вспять.
Сырое молоко содержит сахар лактозу. Если оставить молоко на несколько часов при комнатной температуре, содержащиеся в нем бактерии лактобактерии начинают превращать лактозу в молочную кислоту, которая имеет кислый вкус. Бактерии Lactobacillus часто встречаются в молоке, и они не причиняют никакого вреда.
Кислое молоко также получают путем добавления кислоты (с добавлением или без добавления микробных организмов). Такое молоко называется подкисленным. По вкусу оно отличается от молока, полученного путем бактериальной ферментации, поскольку кислоты, добавляемые в процессе промышленного производства, имеют другой вкус, чем молочная кислота.
4. Смешивание кислоты с основанием
Тип: Неорганическое изменение
Смешивание кислоты с основанием – одна из самых распространенных химических реакций, проводимых в химических лабораториях. При смешивании в равных пропорциях они уравновешивают друг друга и образуют соль и воду. Это называется реакцией нейтрализации.
Например, в результате реакции между соляной кислотой (сильная кислота) и гидроксидом натрия (сильное основание) образуется хлорид натрия (поваренная соль).
HCl + NaOH → NaCl + h3O + тепло
В таких реакциях катион H(+) кислоты соединяется с анионом OH(-) основания, образуя соль и воду.
В некоторых реакциях образуются газы. Например, если смешать уксус (слабую кислоту) с пищевой содой (слабым основанием), то вместе с ацетатом натрия (солью) образуется углекислый газ.
3. Ржавое железо
Тип: Неорганическое изменение
Когда железные предметы остаются в воде или влажной атмосфере в течение длительного времени, они покрываются красновато-коричневой чешуйчатой массой, называемой ржавчиной.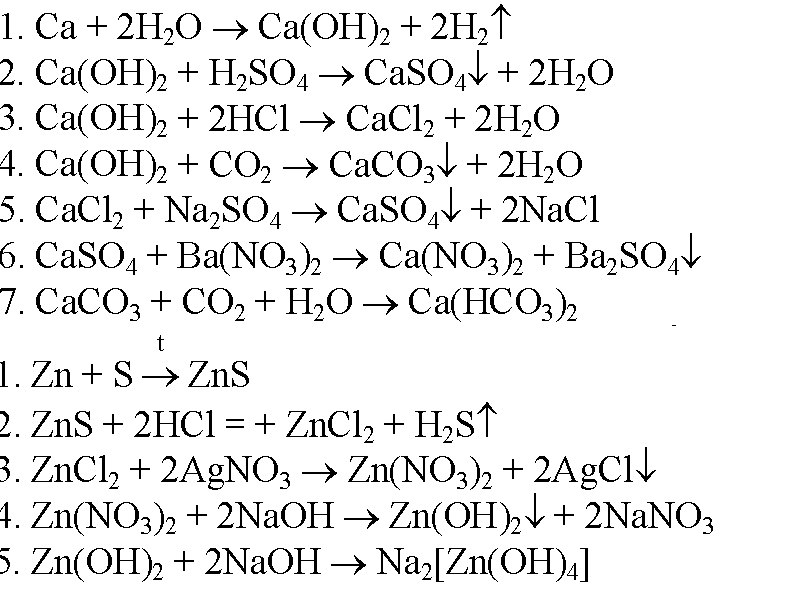 Ржавление – это непрерывный процесс, который постепенно разрушает предметы и делает их бесполезными. Различные факторы, такие как кислотная среда и соленая вода, могут ускорить процесс ржавления железа.
Ржавление – это непрерывный процесс, который постепенно разрушает предметы и делает их бесполезными. Различные факторы, такие как кислотная среда и соленая вода, могут ускорить процесс ржавления железа.
Ржавчина – это не что иное, как оксид железа, соединение, образующееся при реакции железа с кислородом и водой. Хотя это сложный процесс, его химическое уравнение можно записать как:
4Fe + 3O2 + 6H2O → 4Fe(OH)3
Этот процесс также является хорошим примером коррозии, когда металлические поверхности разлагаются на более химически устойчивые оксиды.
2. Варка яйца
Тип: Неорганические изменения
Сырые яйца содержат сложные сети белка и воды. На каждую молекулу белка приходится почти тысяча молекул воды.
Молекулы белка относительно велики и содержат сотни аминокислот, связанных между собой в длинные цепочки. Цепочки складываются в компактные шарики, которые удерживаются вместе слабыми химическими связями (нековалентными).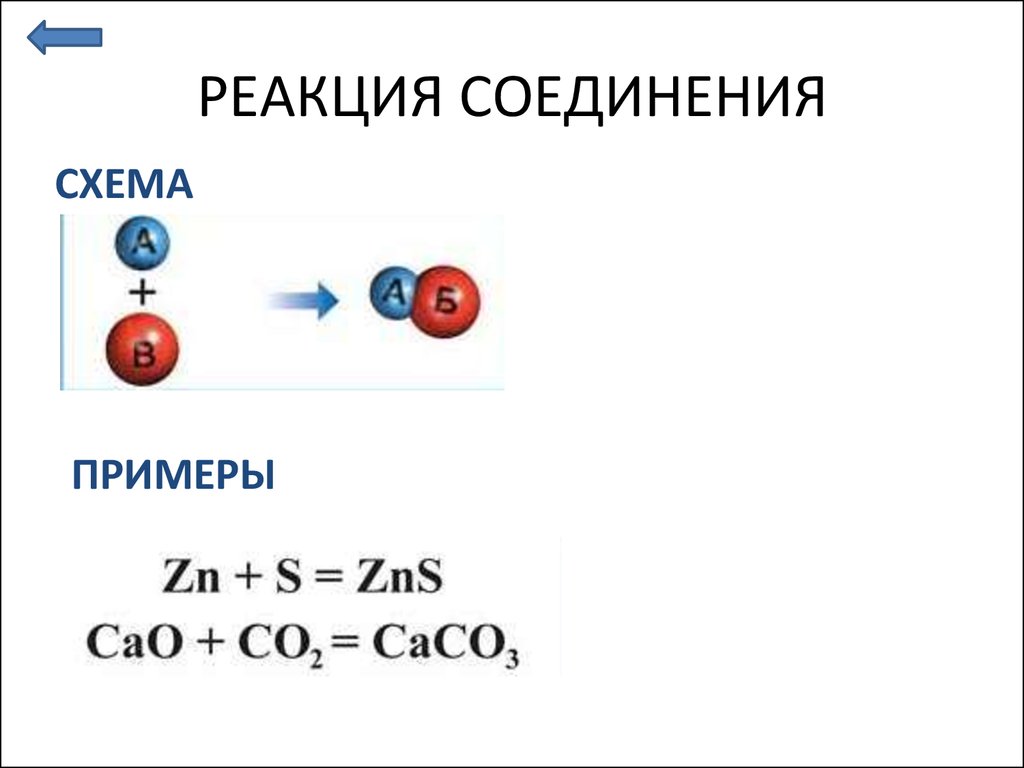
Когда вы нагреваете яйца, их молекулы движутся быстрее и сталкиваются. При повышении температуры скорость столкновения увеличивается. Слабые связи (которые удерживают цепочки аминокислот) начинают разрываться, и белки яйца разворачиваются. В конце концов, белковые нити запутываются в трехмерную паутину.
В вареном яйце теперь содержится вода, которая диспергируется в белковой паутине, так что она больше не может сливаться воедино. В результате жидкое яйцо превращается в полутвердое.
По сути, вы изменили химические вещества, из которых состоит яйцо, применив тепло. Это необратимое изменение, а значит, вареное яйцо нельзя превратить обратно в сырое.
1. Фотосинтез
Тип: Биохимическое изменение
Фотосинтез – это процесс, используемый растениями и другими организмами для производства пищи. В этом естественном процессе световая энергия (солнечный свет) преобразуется в химическую энергию.
Растения являются основными продуцентами, которые составляют основу нашей экосистемы и подпитывают следующие трофические уровни. Они используют фотосинтез для преобразования солнечного света, воды, углекислого газа в кислород и простой сахар.
Они используют фотосинтез для преобразования солнечного света, воды, углекислого газа в кислород и простой сахар.
6CO2 + 6H2O + Световая энергия → C6H12O6 (сахар) + 6O2
Поскольку для фотосинтеза требуется внешняя энергия (солнечный свет), чтобы привести в движение химические изменения, это эндотермическая реакция. Этот процесс не только используется растениями для получения пищи и роста, но и оказывает огромное влияние на нашу атмосферу и океаны, поскольку поглощает углекислый газ и производит кислород.
Без фотосинтеза на Земле было бы слишком мало кислорода – его не хватало бы для выживания людей.
Часто задаваемые вопросы
В чем разница между химическим изменением и физическим изменением?
Физическое изменение влияет на форму вещества. Он включает в себя изменения таких свойств, как прочность, долговечность, температура плавления, форма кристаллов, объем, плотность, форма, размер, цвет и текстура. Хорошим примером может служить закалка стали для изготовления лезвия ножа.
Хорошим примером может служить закалка стали для изготовления лезвия ножа.
Химическое изменение, с другой стороны, включает в себя изменения в составе вещества. Оно происходит, когда различные вещества соединяются, образуя новые вещества с новыми свойствами. Эти химические реакции необратимы и сопровождаются изменением энергии.
Как определить химическое изменение?
Не всегда легко определить, произошло ли химическое изменение (в отличие от физического). Однако можно обратить внимание на такие признаки, как:
- Изменение цвета или порядка.
- Разложение органических веществ, таких как продукты питания и овощи.
- изменение энергии или температуры, например, потеря (эндотермическая) или выделение (экзотермическая) тепла.
- Образование газов или осадков.
- Изменение состава, например, при сжигании дерева оно превращается в пепел.
- Изменения невозможно обратить вспять.
- Некоторые химические реакции производят свет.
Какое вещество не может быть изменено обычными химическими реакциями?
Элемент – это чистое вещество, которое никогда не может быть уменьшено до более простой формы в результате какой-либо химической реакции. Это означает, что вы не можете превратить элемент в другой элемент или разложить его обычными химическими средствами, такими как электролиз, нагревание или реакция. Кислород, азот, золото и серебро являются примерами чистых веществ.
Это означает, что вы не можете превратить элемент в другой элемент или разложить его обычными химическими средствами, такими как электролиз, нагревание или реакция. Кислород, азот, золото и серебро являются примерами чистых веществ.
Химические реакции: типы, классификация, скорость, признаки
Часто мы даже не подозреваем, что на наших глазах идет химическая реакция, а нередко и сами являемся ее участниками. Разбираемся, что же такое химические реакции, каковы их типы, классификация, скорость и признаки
Игорь Геращенко
Автор КП
Анастасия Чистякова
Старший методист по естественно-научному направлению Домашней школы «ИнтернетУрок»
Без химических реакций была бы невозможна эволюция в природе. В открытом космосе встречаются в основном только атомы водорода (H) и гелия (He). Это объясняется отсутствием необходимых условий для прохождения химических реакций.
А вот на Земле ситуация в корне иная. Здесь химические элементы поражают своим разнообразием и могут вступать в различные взаимодействия. Богатство природного мира напрямую зависит от количества и качества химических реакций. Переход от неорганического вещества к живому стал возможен только благодаря химическим процессам. Да и сам человек представляет собой мини-фабрику, где идут не только простые, но и сложнейшие химические реакции по синтезу и расщеплению веществ. Эффективность этой живой «фабрики» поражает воображение.
Что такое химическая реакция
Химическая реакция – это процесс превращения одного или нескольких веществ в другие вещества, в результате чего происходит перераспределение электронов и ядер. Сами ядра атомов при этом не меняются:
H₂ + Cl₂ = 2HCl
Химические реакции нельзя путать с физическими процессами. В физических процессах вещества сохраняют свой состав, хотя могут образовывать смеси, изменять внешнюю форму либо агрегатное состояние. Так, превращение воды в пар или лед является физическим процессом, а не химической реакцией. Химическое взаимодействие, в результате которого образуется вода, описывается формулой:
Так, превращение воды в пар или лед является физическим процессом, а не химической реакцией. Химическое взаимодействие, в результате которого образуется вода, описывается формулой:
2H₂ + O₂ = 2H₂O
Отличаются химические реакции и от ядерных реакций, в которых происходят изменения в ядрах атомов и образуются атомы новых элементов. В ходе химических процессов новые вещества получаются в результате изменений, происходящих в электронной оболочке атомов.
Типы химических реакций
Выделяют следующие типы химических реакций: реакции соединения, разложения, замещения и обмена.
Реакция соединения представляет собой образование одного сложного вещества в результате соединения двух или более веществ. Например:
Fe + S = FeS
В результате реакции разложения происходит распад одного сложного вещества на несколько простых.
CaCO3 = CaO + CO₂
Реакция замещения протекает между простыми и сложными веществами, при этом атомы простого вещества замещают атомы одного из элементов в сложном веществе.
Zn + 2HCL = ZnCl₂ + H₂
Реакция обмена возможна между двумя сложными веществами, в результате чего они обмениваются своими составными частями и образуются два новых сложных вещества.
MgO + h3SO₄ = MgSO₄ + H₂O
Коррозия представляет собой реакцию замещения. Фото: pixabay.com
Классификация химических реакций
Существует целый ряд признаков, по которым можно классифицировать химические реакции: по агрегатному состоянию, по изменению степеней окисления реагентов, по тепловому эффекту реакции, по направлению протекания, по наличию катализаторов.
По агрегатному состоянию (газообразному, жидкому, твердому) реагирующих веществ химические реакции подразделяются на гомогенные и гетерогенные. Гомогенные реакции протекают в одной фазе, например, в виде раствора:
HCl + NaOH = NaCl + H₂O
Гетерогенные реакции осуществляются на границе раздела двух фаз. Например, твердое вещество и газ:
C + O₂ = CO₂
По изменению степеней окисления реагентов выделяют окислительно- восстановительные реакции. Окисление – это процесс отдачи электронов, что приводит к увеличению степени окисления. Восстановление – это присоединение электронов и уменьшение степени окисления. Элемент, отдающий электроны, называется восстановителем, а элемент, принимающий электроны, – окислителем. Например, в реакции Fe + CuSO₄ = FeSO₄ + Cu железо отдает два электрона и является восстановителем, а медь принимает два электрона и выступает в качестве окислителя.
Окисление – это процесс отдачи электронов, что приводит к увеличению степени окисления. Восстановление – это присоединение электронов и уменьшение степени окисления. Элемент, отдающий электроны, называется восстановителем, а элемент, принимающий электроны, – окислителем. Например, в реакции Fe + CuSO₄ = FeSO₄ + Cu железо отдает два электрона и является восстановителем, а медь принимает два электрона и выступает в качестве окислителя.
По тепловому эффекту химические реакции делятся на экзотермические (сопровождающиеся выделением тепла +Q) и эндотермические (идущие с поглощением тепла -Q).
Яркий пример экзотермических реакций – процесс горения:
CH₄ + 2O₂ = CO₂ + 2H₂O +Q
К эндотермическим реакциям относятся реакции разложения:
CaCO₃ = CaO + CO₂ –Q
По направлению протекания химические реакции бывают обратимыми и необратимыми. Обратимые реакции одновременно протекают в двух противоположных направлениях: H₂ + I₂ = 2HI
Необратимые реакции идут только в одном направлении: 2Mg + O₂ = 2MgO
По наличию катализаторов (веществ, участвующих в реакции, изменяющих ее скорость, но остающихся неизменными после завершения реакции) химические реакции подразделяются на каталитические (протекающие в присутствии катализаторов) и некаталитические (идущие без катализаторов). В уравнениях каталитических реакций химическая формула катализатора записывается над знаком равенства или обратимости.
В уравнениях каталитических реакций химическая формула катализатора записывается над знаком равенства или обратимости.
Скорость химических реакций
Скорость химической реакции показывает, как изменяется концентрация реагирующих веществ в единицу времени. Скорость реакции тем выше, чем больше количество реагирующих веществ и чем меньше время самой реакции. Данные процессы изучаются специальным разделом химии – химической кинетикой.
Скорость химических реакций зависит от следующих условий: наличие катализатора, степень измельченности реагирующих веществ, давление и температура, природа веществ, вступающих в реакцию, концентрация реагентов.
В соответствие с правилом Вант-Гофа в случае возрастания температуры на каждые 10 градусов по Цельсию скорость химической реакции увеличивается в 2-4 раза.
Признаки химических реакций
В результате химических реакций происходит превращение одних веществ в другие. При этом изменяются не только сами вещества, но и их свойства. Такие изменения и являются признаками химических реакций. К ним относятся:
При этом изменяются не только сами вещества, но и их свойства. Такие изменения и являются признаками химических реакций. К ним относятся:
- Яркое свечение и выделение или поглощение тепла
При горении магния выделяется много теплоты и излучается яркий свет.
- Выделение газа
При нагревании порошка малахита в пробирке образуется углекислый газ, вода и оксид меди CuO.
- Образование или растворение осадка
При сливании известковой воды и раствора соды образуется белый осадок, который может легко раствориться в уксусе.
- Изменение цвета и запаха
В процессе горения спички образуется специфический запах, кроме того, изменяется цвет пламени и выделяется тепло.
Реакция, протекающая при сгорании головки спички, – это один из наиболее бурных химических процессов.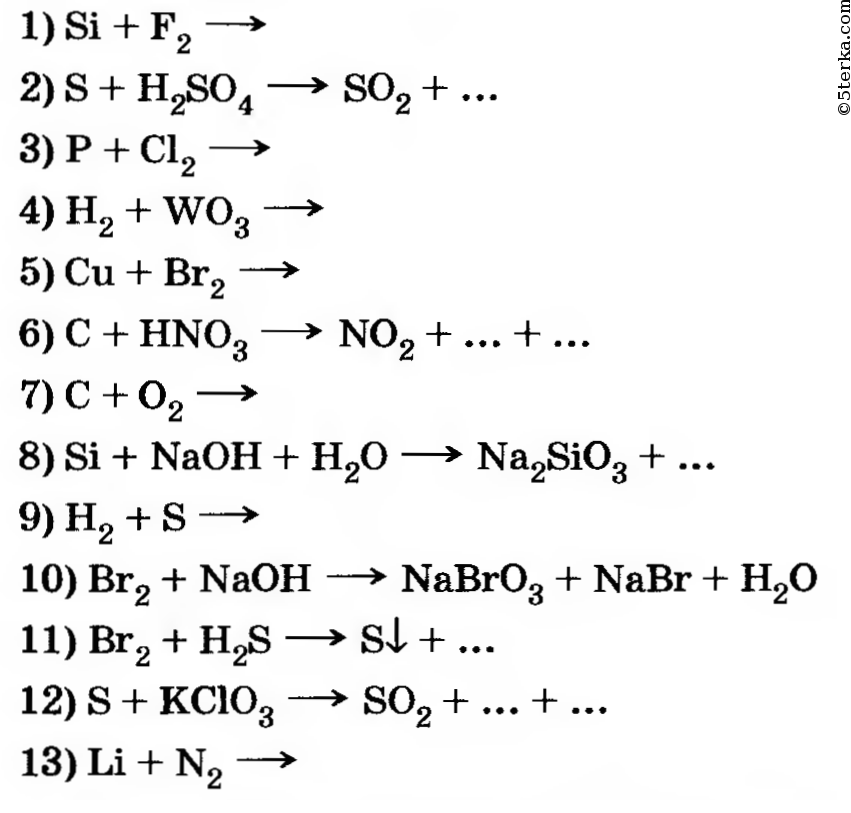 Фото: pixabay.com
Фото: pixabay.com
Популярные вопросы и ответы
Отвечает Анастасия Чистякова, старший методист по естественно-научному направлению Домашней школы «ИнтернетУрок»
Какие факторы влияют на скорость химической реакции?
Скорость химической реакции зависит от целого ряда факторов.
1. Природа веществ, вступающих в химическую реакцию. Так, чем активнее металл, тем он быстрее окисляется и более бурно взаимодействует с водой. Знание природы реагирующих веществ позволяет предсказать скорость протекания химической реакции.
2. Концентрация реагентов. Чем выше их концентрация, тем больше скорость реакции, поскольку с увеличением концентрации возрастает количество столкновений молекул реагирующих веществ. Например, горение в чистом кислороде идет гораздо активнее, чем на воздухе, так как концентрация кислорода в воздушной среде в пять раз ниже.
3. Площадь поверхности реагирующих веществ. Чем эта площадь больше, тем выше скорость реакции. Твердые вещества поэтому измельчают, а жидкости – распыляют. К примеру, если кусок мрамора превратить в порошок, то его реакция с соляной кислотой намного ускорится.
Площадь поверхности реагирующих веществ. Чем эта площадь больше, тем выше скорость реакции. Твердые вещества поэтому измельчают, а жидкости – распыляют. К примеру, если кусок мрамора превратить в порошок, то его реакция с соляной кислотой намного ускорится.
4. Температура. Повышение температуры на каждый градус ведет к возрастанию скорости реакции. Это связано с увеличение числа активных молекул, имеющих повышенную энергию, способствующую вступлению веществ в химическую реакцию.
5. Давление. Оно оказывает существенное воздействие на скорость реакции в газообразном состоянии. При увеличении давления скорость реакции возрастает, что объясняется повышением концентрации молекул реагирующих веществ.
6. Катализатор. Скорость реакции увеличивается в присутствии специальных веществ – катализаторов. Они образуют промежуточные вещества, которые более активно реагируют между собой. При этом сам катализатор в процессе реакции не расходуется. Существуют также вещества, замедляющие процесс реакции (ингибиторы).
Какие химические реакции протекают в организме человека?
В организме человека постоянно идут различные химические реакции, которые по своей эффективности намного превосходят аналогичные процессы в лабораторных условиях. Этому способствуют особые вещества – ферменты, являющиеся биологическими катализаторами. В настоящее время известно несколько тысяч белков-ферментов, каждый из которых участвует в строго определенной химической реакции.
В организме человека происходит расщепление пищи, когда жиры и сахара превращаются в воду и углекислый газ. При этом высвобождается энергия, идущая на жизнеобеспечение организма. В процессе дыхания кислород превращается в углекислый газ. В ходе деления ДНК из одной молекулы образуются две.
Человеческий организм нуждается в минеральных веществах и витаминах, которые он не может получить непосредственно из пищи. В данном случае также необходимы химические реакции, которые способствуют образованию и усвоению этих веществ.
Какие химические реакции встречаются в природе?
В природе химические реакции происходят постоянно, однако их нельзя путать с физическими процессами. Если вода испаряется, она просто меняет свое агрегатное состояние, а молекулы воды остаются без изменения. А вот в процессе фотосинтеза в зеленом растении на свету осуществляется взаимодействие молекул воды с углекислым газом, в результате чего образуется глюкоза и выделяется кислород. Во время грозы идет химическая реакция образования озона из кислорода. Химические процессы связаны также с гниением органических веществ, прокисанием молока, брожением сахара. Появление ржавчины на металле – это еще одна химическая реакция. Когда в чайнике оседает накипь, мы и не подозреваем, что это то же самое химическое взаимодействие, которое приводит к возникновению сталактитов в пещере. И в том, и в другом случае образуется карбонат кальция.
Химические реакции
Познавательный и несложный тест позволит проверить ваши знания о химических реакциях.
| Пройти тест |
Изменяется агрегатное состояние вещества
Меняется форма вещества
Происходит перераспределение электронов и ядер
| Дальше |
| Проверить |
| Узнать результат |
Реакция возгорания
Реакция соединения
Реакция разложения
| Дальше |
| Проверить |
| Узнать результат |
Гомогенными
Агрегатными
Гетерогенными
| Дальше |
| Проверить |
| Узнать результат |
Изменяется степень окисления реагентов
Выделяется кислород
Образуется вода
| Дальше |
| Проверить |
| Узнать результат |
Реакция разложения
Реакция обмена
Реакция замещения
| Дальше |
| Проверить |
| Узнать результат |
Реакция соединения
Реакция обмена
Реакция замещения
| Дальше |
| Проверить |
| Узнать результат |
Изменение агрегатного состояния
Выделение газа
Изменение цвета и запаха
| Дальше |
| Проверить |
| Узнать результат |
Возможно, вам стоит перечитать статью, чтобы лучше разбираться в теме.
| Пройти еще раз |
Возможно, вам стоит перечитать статью, чтобы лучше разбираться в теме.
| Пройти еще раз |
Возможно, вам стоит перечитать статью, чтобы лучше разбираться в теме.
| Пройти еще раз |
Вы неплохо справились с заданиями. Но нет предела совершенству! Потренируйтесь еще!
| Пройти еще раз |
Вы неплохо справились с заданиями. Но нет предела совершенству! Потренируйтесь еще!
| Пройти еще раз |
Прекрасный результат! Вы с легкостью справились с тестом, несмотря на сложную тему.
| Пройти еще раз |
Фото на обложке: pexels.com
Философия химии… и что она может рассказать нам о жизни, Вселенной и обо всем на свете
Философия задает себе несколько фундаментальных и наводящих вопросов. Что это такое? Почему мы делаем это? Чего он может достичь? В качестве отправной точки слово «философия» происходит от греческих слов, означающих любовь к мудрости. И каждый, кто это делает, пытается осмыслить окружающий мир. В этом смысле философы немного похожи на ученых.
Что это такое? Почему мы делаем это? Чего он может достичь? В качестве отправной точки слово «философия» происходит от греческих слов, означающих любовь к мудрости. И каждый, кто это делает, пытается осмыслить окружающий мир. В этом смысле философы немного похожи на ученых.
Но наука сама по себе является достаточно большим предметом, поэтому требует отдельной ветви философии. И если мы можем разбить научное исследование на различные предметы, почему бы не сделать то же самое с его философией? Именно это произошло с развитием философии химии, относительно молодой и нишевой области философских исследований. Он ставит уникальные и интересные вопросы, касающиеся как знания, приобретаемого в науке, так и понимания самой природы.
Некоторые дискуссии в рамках философии химии касаются вопросов, тесно связанных с философией науки. Идеи объяснения, законы природы и реализм исследуются с использованием конкретных теорий, концепций, методов и экспериментальных инструментов химии.
И эти философские вопросы интересны не только философам науки, но и самим ученым. Ответы имеют прямое отношение к автономии наук и единству природы. Например, можно было бы утверждать, что сам предмет химии отличен и независим от предмета физики и что он включает понятия, влияющие на реальность.
Подобно тому, как индивидуумы, состоящие из миллионов клеток, в целом обладают уникальными чертами и свойствами, молекулы и химические связи являются реальными объектами, заслуживающими отдельного исследования, нежели электроны и ядра, из которых они состоят.
Химия также уникальна методами и моделями, которые она использует. Как предмет она считается научной дисциплиной, совершенно отличной от физики, поскольку она гораздо сильнее основана на использовании эмпирических методов для объяснения и предсказания.
В отличие от физики, которая в основном обсуждается на языке математики, химия разработала особый язык, который организован и классифицирован в терминах периодической таблицы. Химия также использует уникальные визуальные представления структуры молекул, чтобы понять и объяснить сложные структурные различия и химические свойства веществ. Эта уникальность химической практики и теоретизирования означает, что она заслуживает отдельного философского исследования.
Философы химии также изучают определяющие признаки, которые химики используют для дифференциации и классификации материи на вещества, элементы, соединения и смеси. Важным аспектом этого является исследование роли периодической таблицы, которая классифицирует и группирует элементы с точки зрения их сходства в конкретных химических свойствах. Историческое исследование того, как такие классификации менялись с течением времени и какие открытия способствовали этим изменениям, играет важную роль в этих дискуссиях.
Важным аспектом этого является исследование роли периодической таблицы, которая классифицирует и группирует элементы с точки зрения их сходства в конкретных химических свойствах. Историческое исследование того, как такие классификации менялись с течением времени и какие открытия способствовали этим изменениям, играет важную роль в этих дискуссиях.
На самом деле было бы неправильно игнорировать важность истории химии для современных философских исследований в этой области. Восприятие химических понятий, таких как атом, значительно изменилось со времен античности с прогрессом как в химических экспериментах, так и в физике.
Философия химии — это область философских исследований, которая за последние 20 лет превратилась в отдельную и отдельную область. Пока химия существует как отдельная научная дисциплина, исследующая вопросы и использующая уникальные инструменты, философия химии будет продолжать исследовать философские последствия такой деятельности.
Вы будете поражены этими примерами химии в повседневной жизни
Химия, хотя и является загадкой для многих, тесно связана со всеми аспектами нашей повседневной жизни. От этого зависит само наше существование. Вокруг лежит множество примеров — больших и маленьких, которые могут помочь нам понять, насколько важна химия в повседневной жизни. Давайте взглянем!
Человеческое тело содержит достаточно углерода, чтобы обеспечить «свинец» (который на самом деле является графитом) для примерно 9000 карандашей!
Химия — это отрасль науки, которая занимается изучением состава, строения, свойств, реакций и поведения веществ. Следовательно, химия называется центральной наукой. Это сущность нашей повседневной жизни, и она проявляется в пище, которую мы едим, в воздухе, которым мы дышим, в воде, которую мы пьем, все является результатом химических процессов.
На самом деле такие эмоции, как любовь и ненависть, также обусловлены химией. Чтобы лучше понять химию, которая окружает нас практически повсюду, мы предоставили примеры из повседневной жизни в двух разделах. Во-первых, примеры химии внутри нашего тела и, во-вторых, примеры химии, которые существуют вне нашего тела или происходят вокруг нас.
Химия внутри нас
Химия играет жизненно важную роль в нашем выживании, а жизнь без химических веществ невозможно даже представить. Они участвуют в основных функциях организма, контролируют наши эмоции, наблюдают за метаболическими процессами и предотвращают болезни. Кислород, которым мы дышим, необходимые нам питательные вещества, генетическая структура нашего тела — ДНК и РНК — состоят из различных элементов и соединений. Давайте взглянем на несколько таких случаев, связанных с химией и являющихся неотъемлемой частью нашего существования.
Состав человеческого тела
Примерно 96% массы нашего тела состоит всего из 4 элементов: кислорода, углерода, водорода и азота.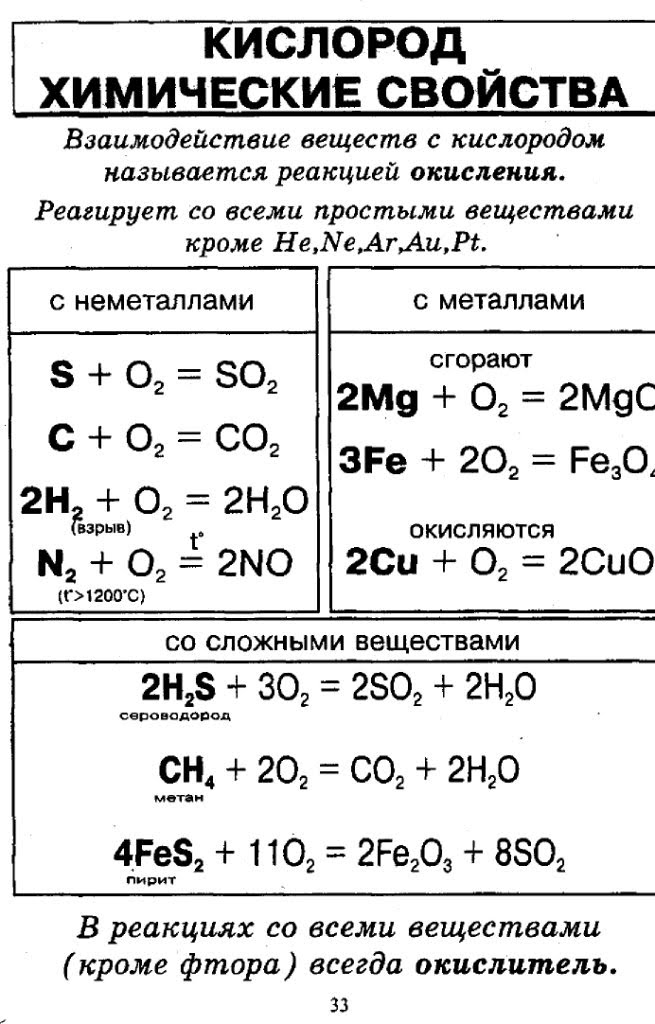 Остальные 4% состоят примерно из 60 элементов, включая натрий, калий, кальций, цинк, и этот список можно продолжить.
Остальные 4% состоят примерно из 60 элементов, включая натрий, калий, кальций, цинк, и этот список можно продолжить.
Элементы, которые требуются в больших количествах, называются макроэлементами, а другие элементы, которые необходимы в незначительных количествах, обычно в частях на миллион или меньше, называются микроэлементами. Химически человеческий организм состоит из воды и органических соединений – углеводов, белков, липидов и нуклеиновых кислот.
Метаболизм
Органические процессы, протекающие в организме человека, называются метаболизмом, который включает в себя огромное количество химических реакций. Ферменты, секретируемые различными органами, действуют как биокатализаторы, ускоряя скорость этих реакций, а гормоны регулируют их протекание, время и скорость.
Наше благополучие, нормальное функционирование и нормальное здоровье зависят от этих метаболических процессов. Координация и одновременное протекание этих жизненных процессов в упорядоченном порядке является причиной того, что мы в хорошей форме, здоровы и живы.
Дыхание
Дыхание — это газообмен между организмом и окружающей средой. Дыхание — это химический процесс, представляющий собой реакцию между глюкозой или сахарами и кислородом, в результате которой выделяется энергия. Это процесс, при котором вдыхание кислорода из воздуха вызывает раздувание легких, а затем происходит сдувание путем выдыхания углекислого газа в окружающую среду.
Реакция, происходящая при дыхании:-
C 6 H 12 O 6 + 6O 2 ➜ 6CO 2 + 6H 2 O + Энергия
Состав воды
Вода — эликсир жизни на Земле. Водород — легковоспламеняющийся газ и Кислород — газ, без которого горение невозможно, образуют ковалентную связь друг с другом для создания наиболее эффективного огнетушителя, которым является вода. Химическая формула воды H 2 O.
Да! Мы пьем химию каждый день. Вода важна для всех обменных процессов, происходящих внутри нашего организма. Как сказал Леонардо да Винчи: «Вода — движущая сила всей природы».
Как сказал Леонардо да Винчи: «Вода — движущая сила всей природы».
Чувство голода
Когда вы чувствуете голод, желудок вырабатывает гормон грелин, который вызывает чувство голода. Он стимулирует выброс гормона роста. Он играет роль в высвобождении инсулина и защите сердечно-сосудистых органов. Итак, в следующий раз, когда ваш желудок урчит, съешьте кусочек, потому что, если вы голодаете или пропускаете приемы пищи, вырабатывается больше грелина, что увеличивает вашу тягу к еде.
Пищеварение
Желудочная кислота состоит из соляной кислоты (HCl) и больших количеств хлорида калия (KCl) и хлорида натрия (NaCl), которые секретируются париетальными клетками, выстилающими желудок.
Эта желудочная кислота помогает превращать пепсиноген в пепсин, который отвечает за денатурацию белков в желудке. Он также убивает микроорганизмы в пище, прежде чем они могут вызвать у вас заболевание. HCl нейтрализует кислоту, присутствующую в продуктах, которые вы едите, тем самым поддерживая кислотный или щелочной уровень вашего тела, чтобы поддерживать ваше здоровье.
Слезы и плач
Иногда плач является естественным рефлексом. Исследования показали, что эмоциональные слезы содержат больше марганца 9.0029 , элемент, влияющий на темперамент и большее количество пролактина. Пролактин – это гормон, который регулирует выработку молока. Считается, что это устранение марганца и пролактина ослабляет напряжение, накапливающееся в организме, и вы чувствуете себя энергичным и омоложенным. Итак, в следующий раз, когда вы почувствуете себя подавленным и вам нужно будет выплеснуть свои эмоции, не сдерживайтесь. Просто плачь! Это поможет вам чувствовать себя лучше.
Химия ЛЮБВИ
Мы влюбляемся или испытываем влечение к кому-то и испытываем чувство принадлежности из-за увеличения секреции -Фенилэтиламин (ФЭА, или «химическое вещество любви») и гормоны тестостерон и эстроген , которые способствуют спариванию.
Когда мы влюбляемся, наш мозг последовательно выделяет дофамин, норадреналин и феромоны , которые активируют центр удовольствия в мозге, что приводит к побочным эффектам, таким как учащение пульса, бессонница, сильное чувство возбуждения, приподнятости и сосредоточенности. внимание.
внимание.
Кофе и сон
Кофе не дает вам уснуть благодаря наличию кофеин в нем. Этот кофеин повышает уровень дофамина в нашем организме, который стимулирует « областей удовольствия » в нашем мозгу, заставляя нас чувствовать себя хорошо. Он увеличивает секрецию адреналина в организме и ускоряет активность мозга, которая не дает нам уснуть.
Запах тела
Потоотделение — это способ охлаждения тела. Запах тела в основном исходит от апокринных желез, которые находятся в подмышечных впадинах, ушах, груди, половых органах и волосяных фолликулах, которые становятся активными в начале полового созревания. Пот, выделяемый этими железами, имеет светло-желтый цвет из-за присутствия в нем жирных кислот и белков. Бактерии, живущие на нашей коже, расщепляют секреты апокриновых желез и создают неприятные запахи.
Вот некоторые примеры химии внутри нашего тела. Давайте посмотрим на некоторые примеры химии в повседневной жизни, которая происходит вокруг нас.
Химия вокруг нас
Химические реакции влияют на то, что нас окружает, и во многих случаях химические вещества и химия помогают нам жить лучше. Приготовление пищи, одежда, которую мы носим, удобрения, которые мы используем для выращивания сельскохозяйственных культур, цемент, используемый для строительства наших домов, электростанции, вырабатывающие электричество, и многие другие процессы зависят от химии. Зависимость человека от этой естественной науки возрастает, и чтобы понять это, вот несколько примеров, которые подчеркивают важность химии вокруг нас.
Фотосинтез
Фотосинтез включает преобразование энергии и представляет собой химический процесс, при котором растения, водоросли и некоторые бактерии производят себе пищу. Это синтез глюкозы с использованием углекислого газа и воды в присутствии солнечного света, захваченного хлорофиллом, присутствующим в листьях. Происходящая реакция изображается как:
6 CO 2 + 6 H 2 O + Световая Энергия ➜ C 6 H 12 O 6 + 6 O 2
Фотосинтез — процесс, обратный дыханию. Они оба взаимозависимы. Мы получаем бесперебойное снабжение кислородом, а растения – необходимым им углекислым газом. Таким образом, фотосинтез играет важную роль в нашей повседневной жизни.
Они оба взаимозависимы. Мы получаем бесперебойное снабжение кислородом, а растения – необходимым им углекислым газом. Таким образом, фотосинтез играет важную роль в нашей повседневной жизни.
Цвет мяса
Есть два вида мяса: красное и белое. Красное мясо содержит сильно пигментированный белок под названием миоглобин , который запасает кислород в мышечных клетках. Чем больше миоглобина в клетках, тем краснее мясо. Однако по мере нагревания мяса белки разрушаются и уменьшаются в размерах.
Когда температура внутри мяса достигает 170°F, уровень гемихрома (соединение желтовато-коричневого цвета) повышается, и миоглобин становится метмиоглобином , который придает хорошо прожаренному мясу коричнево-серый оттенок. Белое мясо содержит гликогена, из которых имеют полупрозрачное «стекловидное» качество, когда оно сырое. Когда его готовят, белки рекомбинируют или коагулируют, и мясо становится непрозрачным и беловатым.
Яблоки, приобретающие коричневый цвет
Яблоки содержат фермент под названием полифенолоксидаза (ПФО), также известный как тирозиназа.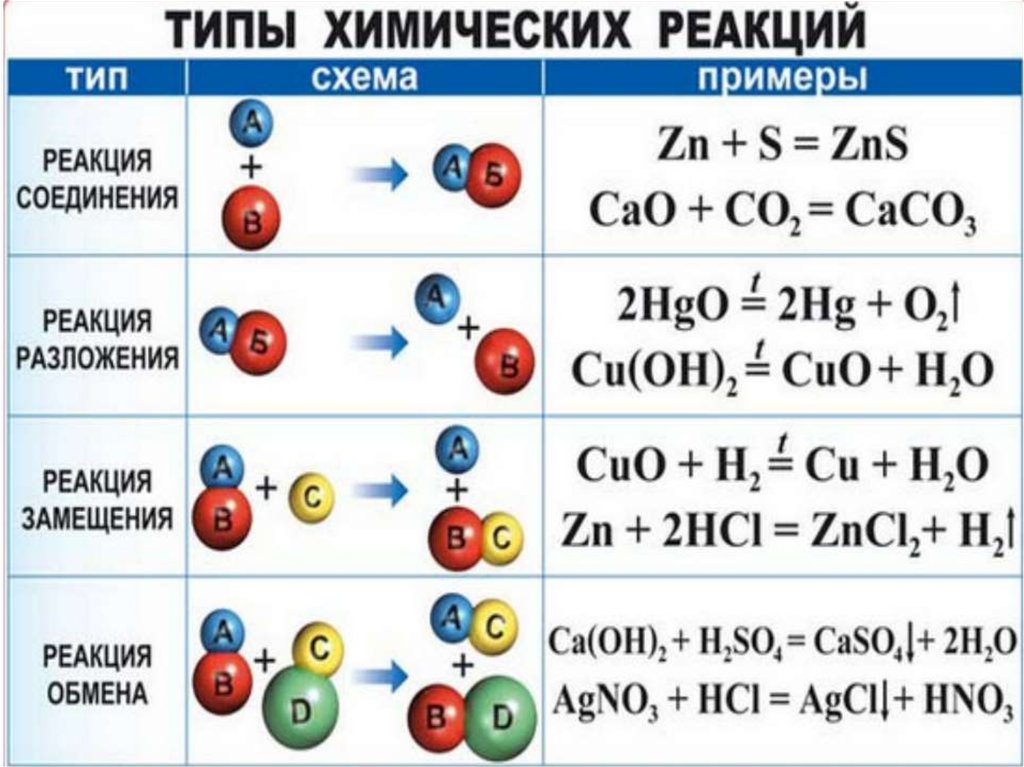 Разрезание яблока подвергает его клетки воздействию атмосферного кислорода и окисляет фенольные соединения, присутствующие в яблоках. Это называется ферментативным подрумяниванием, при котором нарезанное яблоко становится коричневым. Помимо яблок, ферментативное потемнение проявляется также в бананах, грушах, авокадо и даже картофеле.
Разрезание яблока подвергает его клетки воздействию атмосферного кислорода и окисляет фенольные соединения, присутствующие в яблоках. Это называется ферментативным подрумяниванием, при котором нарезанное яблоко становится коричневым. Помимо яблок, ферментативное потемнение проявляется также в бананах, грушах, авокадо и даже картофеле.
Crying and Onions
Когда вы режете лук, вы разрушаете клетки, образующие слои в луковице, высвобождая таким образом фермент Alliinase, который реагирует с серосодержащим соединением, известным как «presco», , который также высвобождается при резке. Эта реакция приводит к образованию 1-пропенилсульфеновой кислоты.
1-пропенилсульфеновая кислота далее превращается в пропантиол S-оксид , летучее соединение серы, под действием фермента LF-синтазы (имеется в виду фермент, синтезирующий слезоточивый фактор). Этот газ, известный как слезоточивый фактор (фактор плача), реагирует с водой в наших глазах с образованием серной кислоты , вызывая жжение в ваших глазах и указывая слезной железе на выделение слез.
Пятновыводители
Мыло образуется в результате реакции между щелочью и жирной кислотой. В результате получается молекула с одним гидрофильным (водолюбивым) и одним липофильным (жиролюбивым) концами. Липофильные концы прилипают к маслу, жиру или грязи. Они поглощаются мылом и смываются свежей струей воды, оставляя после себя чистую поверхность.
Это просто физическая реакция. Мыло и пятновыводители действуют как эмульгаторы, которые позволяют маслу и воде смешиваться, поэтому маслянистые смеси и сложные пятна на теле и одежде можно удалить после применения мыла, пятновыводителей и воды.
Созревание фруктов
Простой углеводородный газ этилен включает необходимые гены, которые стимулируют секрецию ферментов созревания, которые катализируют реакции по изменению свойств фруктов. Этилен направляет действие нескольких других химических веществ, называемых гидролазой , амилазой, киназой и пектиназой. Эти ферменты превращают крахмал в сахар, изменяют стенки клеток, делая их более мягкими, нейтрализуют кислоты и заставляют фрукты издавать аромат.
Ферментация
Ферментация – это превращение сложных веществ в более простые в анаэробных условиях. Конкретный продукт ферментации зависит от типа микроорганизмов, воздействующих на вещество, в котором происходит ферментация. Продуктами брожения являются спирты или кислоты и выделение углекислого газа.
Например, вино, полученное из фруктового сока, представляет собой спирт в результате дрожжевого брожения, тогда как пиво является результатом дрожжевого брожения зерна. Антибиотики получают путем ферментации плесенью и некоторыми бактериями. Йогурт, сыр и уксус являются продуктами бактериального брожения. Хлеб на дрожжах получают путем дрожжевого брожения.
Солнцезащитные средства
Солнцезащитные средства представляют собой комбинацию органических и неорганических соединений. Неорганические химические вещества, такие как диоксид титана или оксид цинка, образуют физический барьер, который отражает или рассеивает УФ-волны. Органические компоненты, такие как октилметоксициннамат (OMC) или оксибензон , поглощают ультрафиолетовые лучи и выделяют свою энергию в виде тепла. Это защищает нашу кожу от солнечных ожогов и вредных воздействий, таких как рак.
Это защищает нашу кожу от солнечных ожогов и вредных воздействий, таких как рак.
Средства для снятия краски с ногтей
Краска для ногтей состоит из трех типов ингредиентов: органических растворителей и осушителей, загустителей и отвердителей и красителей. Ремувер на самом деле представляет собой органический растворитель, который используется в качестве ингредиента в краске для ногтей, которая может быть 9.0028 ацетон или этилацетат .
Таким образом, когда вы применяете средство для удаления, вы просто возвращаете его в исходное состояние. Молекулы растворителя проникают между цепочками полимеров и разделяют их, что позволяет легко стереть их ватным тампоном.
Статические удары
Все материалы состоят из электрических зарядов в атомах материала. Существует равное количество электронов (отрицательно заряженных) и протонов (положительно заряженных), которые пытаются сбалансировать друг друга во Вселенной. Трение между двумя материалами вызывает перераспределение этих зарядов.

