Концентрация растворов. Правило креста
В данном разделе рассмотрены задачи на пересчет концентрации растворов, применение правила креста для нахождения концентрации при смешении и разбавлении растворов. Больше задач на расчет массовой доли растворенного вещества представлены в разделе подготовки к ОГЭ по химии.
Концентрация растворов и способы ее выражения
Задача 1. К 150 г 20% раствора сахарозы добавили 45 г глюкозы. Рассчитайте массовые доли углеводов в новом растворе.
Показать решение »
Решение.
Вначале сахарозы было 30 г:
20 г сахарозы содержится в 100 г раствора
х г — в 150 г
х =30 г
После прибавления глюкозы:
mобщ = m (сахарозы) + m (глюкозы) = 150 + 45 = 195 г
m раствора стала 195 г
Найдем полученные массовые доли сахарозы и глюкозы:
30 г сахарозы содержится в 195 г раствора
х г — в 100 г
х =15,4
ω2 (сахарозы) = 15,4%:
45 г глюкозы содержится в 195 г раствора
х г — в 100 г
х = = 23,1
ω2 (глюкозы) = 23,1%
Задача 2. Для нейтрализации 20 мл 0,1 н раствора кислоты потребовалось 6 мл раствора едкого натра. Определить нормальную концентрацию раствора едкого натра.
Для нейтрализации 20 мл 0,1 н раствора кислоты потребовалось 6 мл раствора едкого натра. Определить нормальную концентрацию раствора едкого натра.
Задача 3. Нормальная концентрация раствора KNO3 равна 0,2 моль/л. Найти процентную концентрацию раствора KNO3 и молярную концентрацию раствора KNO3. Плотность раствора принять раной 1 г/мл.
Показать решение »
Решение:
Найдем молярную массу и молярную массу эквивалента KNO3.
В данном случае, они совпадают.
М (KNO3) = 39+14+(16×3) = 101 г/моль
Найдем массу KNO3, содержащуюся в его 0,2 н. растворе:
1 н раствор KNO3 содержит – МЭ KNO3 в 1000 мл
Т.е. 1 н – 101 г
0,2 н. – х г
– х г
х = 20,2 г
Теперь вычислим молярную концентрацию
1М раствор KNO3 содержит – М KNO3 в 1000 мл
Т.е. 1 М – 101 г
х – 20,2 г
х = 0,2 моль/л
Таким образом, Сн = См = 0,2 моль/л
Далее находим процентную концентрацию.
Сначала необходимо рассчитать массу раствора объемом 1000 мл.
m = ρ×V = 1×1000 = 1000 г
тогда, решая пропорцию, находим:
20,2 г KNO3 содержится – в 1000 г раствора
х г – в 100 г раствора
х = 2,02 г
ω = 2,02%
Задача 4. Вычислите молярную и молярную концентрацию эквивалента (нормальность) 20 % раствора хлорида кальция плотностью 1,178 г/мл.
Показать решение »
Решение.
Найдем массу раствора
mр-ра = V·ρ = 1000 · 1,178 = 1178 г.
Найдем массу CaCl2, содержащуюся в 1178 г. 20 % раствора
20 г CaCl2 содержится в 100 г раствора
х г — в 1178 г раствора
х = 235,6 г.
Молярность определим с помощью соотношения:
См = n/V
n = m/M = 235,6/111 = 2,1 моль
M(CaCl2) = 40+35,5·2 = 111 г/моль
См = 2,1/1 = 2,1 М
Молярная концентрация эквивалента определяется с помощью соотношения:
Сн = nэ/V
Мэ = fэкв· М(CaCl2) = 1/2·111 = 55,5 г/моль
nэ = m/ Мэ = 235,6/55,5 = 4,2 моль
Сн = 4,2/1 = 4,2 н
Задача 5. Чему равна нормальность 30% раствора NaOH плотностью 1,328 г/мл? К 1 л этого раствора прибавили 5 л воды. Вычислите массовую долю полученного раствора.
Вычислите массовую долю полученного раствора.
Показать решение »
Решение.
Найдем массу NaOH, содержащуюся в 1328 г. 30 % раствора используя формулу:
ω(NaOH) = m (NaOH)/m
mр-ра = V·ρ = 1000 · 1,328 = 1328 г.
m(NaOH) = ω(NaOH) · m = 0,3 · 1328 = 398,4 г.
Найдем Молярную концентрацию эквивалента или нормальность:
M(NaOH) = 23+16+1 = 40 г/моль
Сн = nэ/V
Мэ = fэкв· М(NaOH) = 1·40 = 40 г/моль
nэ = m/ Мэ = 398,4/40 = 9,96 моль
Сн = 9,96/1 = 9,96 н
Найдем массу раствора после прибавления 5 л воды:
m2 = 1328 + 5000 = 6328 г
Далее находим процентную концентрацию или массовую долю вещества.
ω2(NaOH) = m (NaOH)/m2 = 398,4/6328 = 0,063 или 6,3 %
Задача 6. К 3 л 10 % раствора HNO3 плотностью 1,054 г/мл прибавили 5 л 2 % раствора той же кислоты плотностью 1,009 г/мл. Вычислите массовую долю в процентах и молярную концентрацию полученного раствора, объем которого равен 8 л.
К 3 л 10 % раствора HNO3 плотностью 1,054 г/мл прибавили 5 л 2 % раствора той же кислоты плотностью 1,009 г/мл. Вычислите массовую долю в процентах и молярную концентрацию полученного раствора, объем которого равен 8 л.
Показать решение »
Решение.
Найдем массу растворов объемом 3 л и 5 л
m1= V1·ρ = 3000·1,054 = 3162 г
m2= V2·ρ = 5000·1,009 = 5045 г
Найдем массу HNO3, содержащуюся в 3162 г. 10 % раствора
10 г HNO3 содержится в 100 г ее раствора
х1 г — в 3162 г раствора
х1 = 316,2 г
Найдем массу HNO3, содержащуюся в 5045 г. 2 % раствора
2 г HNO3 содержится в 100 г ее раствора
х2 г — в 5045 г раствора
х2 = 100,9 г
При смешивании:
m (HNO3) = 316,2+100,9 = 417,1 г
mр-ра (HNO3) = 3162+5045 = 8207 г
Найдем Молярность
См = n/V
n = m/M = 417,1/63 = 6,62 моль
M(HNO3) = 1+14+16·3 = 63 г/моль
См= 6,62/1 = 6,62 М
ω(HNO3) = m (HNO3)/mр-ра = 417,1/8207 = 0,05 или 5 %
Задача 7. Определить молярность, нормальность, моляльность и титр 4 % раствора FeSO4 объем которого равен 1,5 л, плотность 1037 кг/м3
Определить молярность, нормальность, моляльность и титр 4 % раствора FeSO4 объем которого равен 1,5 л, плотность 1037 кг/м3
Показать решение »
Решение.
M (FeSO4) = 56+32+16·4 = 152 г/моль
Мэ = fэкв· М(FeSO4) = 1/2·152 = 76 г/моль
Найдем m раствора объемом 1,5 л
m = V·ρ = 1,5·10-3 ·1037 = 1,56 кг
Найдем m 4 % раствора
m(FeSO4) = ω(FeSO4) · mр-ра = 0,04·1,56 = 0,0624 кг = 62,4 г
Найдем молярность, которая определяется как количество молей растворенного вещества в одном литре раствора
n = m/М = 62,4/152 = 0,41 моль
См = n/V = 0,41/1,5 = 0,274 М
Найдем нормальность:
nэ = m/Мэ = 62,4/76 = 0,82 моль
Сн = nэ/V = 0,82/1,5 = 0,547 н
Моляльная концентрация равна:
b (x) = n(x)/m
Масса растворителя равна: mH2O = 1560-62,4 = 1497,6 г = 1,5 кг
b (FeSO4) = n(FeSO4)/m = 0,41/1,5 = 0,27 моль/кг
Титр определим следующим образом:
Т (х) = m (х)/V
Т (FeSO4) = m (FeSO4)/V = 62,4/1500 = 0,0416 г/мл
Задачи на смешение и разбавление растворов
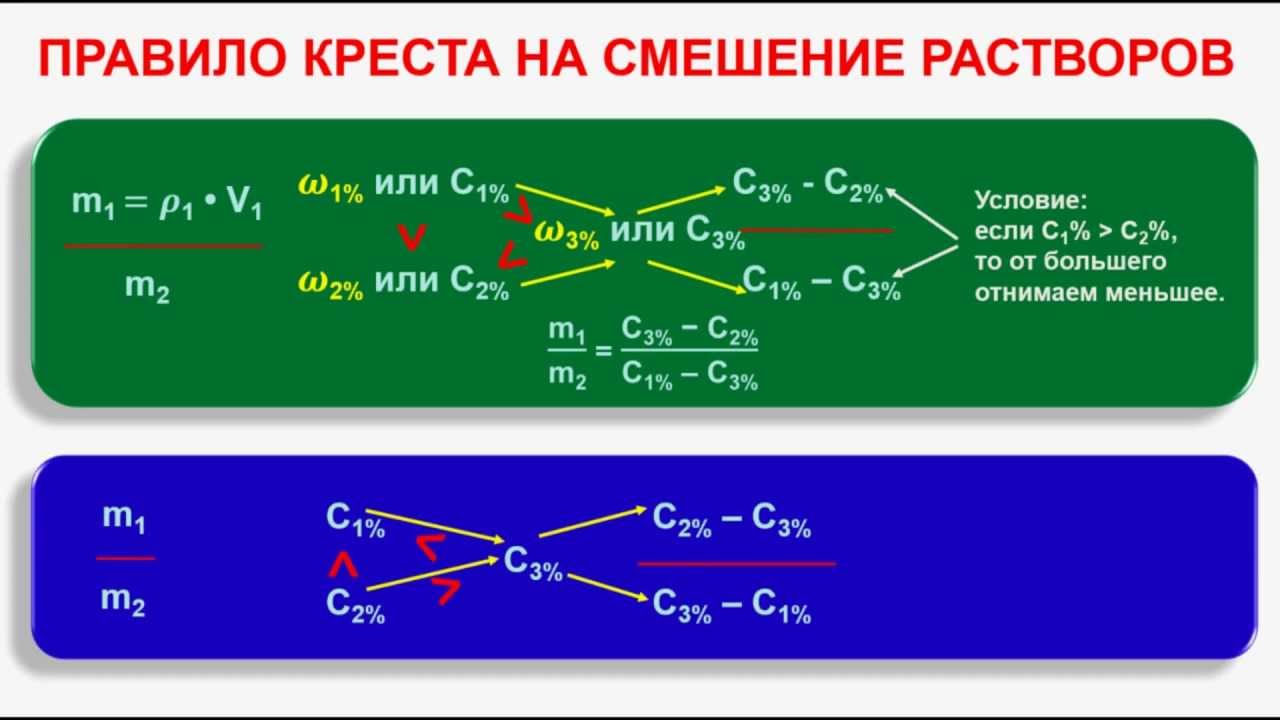
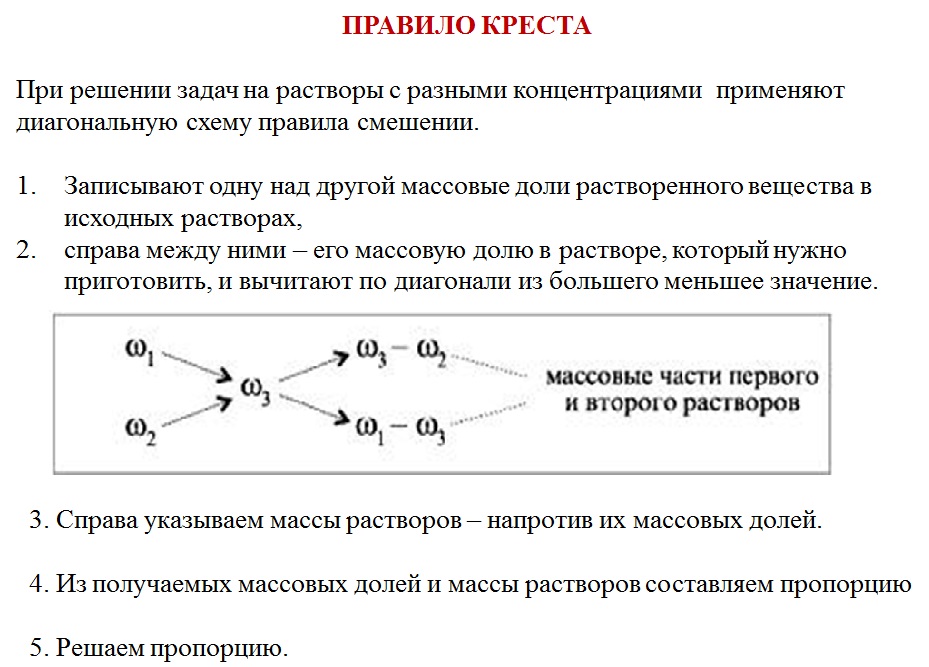
Такие задачи можно решить с помощью правила креста или правила смешения. Суть его заключается в составлении «креста», в виде которого располагают две прямые линии. В центре пишут ту концентрацию, которую надо получить, у концов линий креста слева – концентрации исходных растворов (большую – сверху, меньшую — снизу), у концов линий креста справа – искомые концентрации (или массы) растворов, которые получают вычитанием по направлению линий из большей величины меньшей. В общем виде схема решения задач по правилу креста имеет вид:
Суть его заключается в составлении «креста», в виде которого располагают две прямые линии. В центре пишут ту концентрацию, которую надо получить, у концов линий креста слева – концентрации исходных растворов (большую – сверху, меньшую — снизу), у концов линий креста справа – искомые концентрации (или массы) растворов, которые получают вычитанием по направлению линий из большей величины меньшей. В общем виде схема решения задач по правилу креста имеет вид:
Таким образом, следует взять mА грамм раствора с массовой долей а% и прибавить к нему mB грамм раствора с массовой долей b%. Если надо узнать, какие массы растворов данной концентрации следует взять, чтобы получить заданную массу раствора новой концентрации, то сначала определяют отношение mА и mB . Затем пропорционально этому отношению делят заданную массу.
Задача 8. Сколько граммов раствора с массовой долей серной кислоты 96% необходимо влить в 1 л воды, чтобы получить раствор с массовой долей 10%
Показать решение »
Решение.
Для решения данной задачи используем правило креста.
Чистый растворитель (воду) можно представить как раствор с массовой долей растворенного вещества 0%
Определим m раствора с ω (H2SO4) = 96%, который надо влить в 1 л воды:
10 г H2SO4 надо влить в 86 г воды
х г — 1000 г
х = 116,28 г
m (р-ра H2SO4) = 116,28 г
Задача 9. Сколько мл 0,5 М и 0,1 М растворов азотной кислоты следует взять для приготовления 1000 мл 0,2 М раствора.
Показать решение »
Решение.
По правилу креста, определяем в каких соотношениях следует взять 0,5 М и 0,1 М растворы азотной кислоты, чтобы получить раствор заданной концентрации:
V0.5/V0.1 = 0,1/0,3 = 1/3
Взяв 0,1 л и 0,3 л исходных растворов, получим 0,4 л 0,2 М раствора HNO3, но по условию задачи нужно получить 1 л. Для этого разделим 1 л на две части в соотношении 1:3, составив пропорции:
Для этого разделим 1 л на две части в соотношении 1:3, составив пропорции:
Для 0,5 М раствора HNO3
из 0,1 л 0,5 М раствора получим 0,4 л 0,2 М р-ра HNO3
х1 л — 1 л
х1 = 0,25 л
Для 0,1 М раствора HNO3
из 0,3 л 0,5 М раствора получим 0,4 л 0,2 М р-ра HNO3
х2 л — 1 л
х2 = 0,75 л
Формула концентрации раствора в химии
Определение и формула концентрации раствора
Наиболее распространены следующие способы выражения концентрации раствора.
Массовая доля – отношение (обычно – процентное) массы растворенного вещества к массе раствора:
w = msolute / msolution× 100%.
Например, 15: (масс.) водный раствор хлорида натрия – это такой раствор, в 100 единицах массы которого содержится 15 единиц массы NaCl и 85 единиц массы воды.
Молярная доля – это отношение количества растворенного вещества (или растворителя) к сумме количеств всех веществ, составляющих раствор. В случае раствора одного вещества в другом молярная доля растворенного вещества (N2) равна:
N2 = n2 / (n1 + n2),
а молярная доля растворителя (N1):
N1
где n1иn2 – соответственно количество вещества растворителя и растворенного вещества.
Молярная концентрация, или молярность – отношение количества растворенного вещества к объему раствора:
СМ = n / V.
Обычно молярность обозначается СМили (после численного значения молярности) М. Так, 2М H2SO4 означает раствор, в каждом литре которого содержится 2 моля серной кислоты, т.е. СМ = 2 моль/л.
Моляльная концентрация, или моляльность – это отношение количества растворенного вещества к массе растворителя:
m = nsolute / msolvent.
Обычно моляльность обозначается буквой m. Так, для раствора серной кислоты запись m = 2 моль/кг (воды) означает, что в этом растворе на каждый килограмм растворителя (воды) приходится 2 моля серной кислоты. Моляльность раствора в отличие от его молярности не изменяется при изменении температуры.
Нормальность раствора (нормальная концентрация, молярная концентрация эквивалента) СН(Х) – это отношение количества вещества эквивалента, содержащегося в растворе, к объему этого раствора [моль / м3]. На практике нормальность раствора по аналогии с молярной концентрацией выражают в моль/л. Так, например, с(H д. Приняты и такие обозначения: 1 н. раствор H2SO4; 0,01 н. раствор KOH.
д. Приняты и такие обозначения: 1 н. раствор H2SO4; 0,01 н. раствор KOH.
Эквивалентом называется реальная или условная частица вещества, которая может замещать, присоединять, высвобождать или быть каким-либо другим способом эквивалентна одному иону водорода в кислотно-основных или ионообменных реакциях или одному электрону в окислительно-восстановительных реакциях. Моль вещества эквивалента содержит 6,02×10
Титр раствора – это масса вещества, содержащаяся в одном кубическом сантиметре (одном миллилитре) раствора [г/мл]. Обычно обозначается буквой Т. Например, T(HCl) = 0,02 г/мл означает, что в 1 мл раствора содержится 0,02 г соляной кислоты.
Примеры решения задач
Решение задач на вычисление массовой доли вещества в растворе
ПОДГОТОВКА К ЭКЗАМЕНУ
«Вычисление массы растворенного вещества, содержащегося в определенной массе раствора с известной массовой долей»
Алгоритмы решения задач:
Пример 1. Вычисление массовой доли растворенного вещества
Вычисление массовой доли растворенного вещества
Определите массовую долю нитрата калия в растворе, полученном растворением 50 г нитрата калия в 200 г воды.
Дано: m(KNO3 ) = 50 г, m(Н2О) = 200 г. | Решение ω(в-ва) = m(в-ва) / m(р-ра)*100 (%). m(р-ра) = m(в-ва) + m(Н2 О) = = 50 (г) + 200 (г) = 250 г. ω(KNO3 ) = = 50 (г) / 250 (г) * 100 (%) = 20 %. Ответ. ω(KNO3) = 20 %. |
ω(KNO3 ) – ? |
Пример 2. Вычисление массы растворенного вещества
Вычислите массу гидроксида калия в растворе объемом 600 мл и плотностью 1,082 г/мл, если массовая доля гидроксида калия составляет 10 %.
Дано: V(р-ра) = 600 мл, ρ = 1,082 г/мл, ω(KОН) = 10 %, или 0,1. | Решение m(в-ва) = ω(в-ва)*m(р-ра). m(р-ра) = ρ*V(р-ра) = = 1,082 (г/мл)*600 (мл) = 649,2 г. m(KОН) = 649,2 (г)*0,1 = 64,92 г. Ответ. m(KОН) = 64,92 г. |
m(KОН) – ? |
Пример 3. Смешивание растворов с разными концентрациями одного вещества Смешали 300 г раствора с массовой долей хлорида натрия 20 % и 500 г раствора того же вещества с массовой долей 40 %. Вычислите массовую долю хлорида натрия в полученном растворе.
Дано: m1 = 300 г, ω1 = 20 %, или 0,2, m2 = 500 г, ω2 = 40 %, или 0,4. | Решение m1 *ω1 + m2 *ω2 = m3 *ω3 , где m1 , m2 , m3 – массы растворов. 300 (г)*0,2 + 500 (г)*0,4 = = 800 (г)*ω3 , 60 (г) + 200 (г) = 800 (г)*ω3 , 260 (г) = 800 (г)*ω3 , ω3 = 260 (г) / 800 (г) = 0,325, или 32,5 %. Ответ. ω3 (NaCl) = 32,5 %. |
ω3 – ? |
Пример 4. Разбавление водой
ω2 = 0, т.к. в воде не содержится вещество, находящееся в первом растворе.
Какую массу воды надо добавить к раствору гидроксида натрия массой 150 г с массовой долей 10 %, чтобы получить раствор с массовой долей 2 %?
Дано: m1 = 150 г, ω1 = 10 %, или 0,1, ω2 = 0, ω3 = 2 %, или 0,02. | Решение m1 *ω1 + m2 *ω2 = m3 *ω3 . 150 (г)*0,1 + m2 *0 = = (150 (г) + m2 )*0,02, 15 (г) + 0 = 3 (г) + 0,02m2 , 0,02m2 = 12 г, m2 = 12 (г) / 0,02 = 600 г. Ответ. m(Н2О) = 600 г. |
m2 – ? |
Пример 5. Концентрирование (добавление твердого вещества)
ω2 = 100 %, или 1, т.к. добавляемое вещество чистое.
Какую массу хлорида бария надо добавить к раствору хлорида бария массой 150 г с массовой долей 10 %, чтобы получить раствор с массовой долей 25 %?
Дано: m1 = 150 г, ω1 = 10 %, или 0,1, ω2 = 100 %, или 1, ω3 = 25 %, или 0,25. | Решение m1 *ω1 + m2 *ω2 = m3 *ω3 . 150 (г)*0,1 + m2 *1 = = (150 (г) + m2 )*0,25, 15 (г) + 1*m2 = 37,5 (г) + 0,25m2 , 0,75m2 = 22,5 г, m2 = 22,5 (г) / 0,75 = 30 г. Ответ. m(BaCl2 ) = 30 г. |
m2 – ? |
Пример 6. Упаривание раствора (частичное выпаривание воды)
Вычислите массовую долю хлорида натрия в растворе, если из 200 г 30 %-го раствора испарилось 50 г воды.
Дано: m1 = 200 г, ω1 = 30 %, или 0,3, m2 = 50 г, ω2 = 0. | Решение m1 *ω1 + m2 *ω2 = m3 *ω3 . 200 (г)*0,3 + 50 (г)*0 = = 150 (г)*ω3 , 60 (г) = 150 (г)*ω3 , ω3 = 60 (г) / 150 (г) = 0,4, или 40 %. Ответ. ω3 (NaCl) = 40 % |
ω3 – ? |
ПРИМЕРЫ ЗАДАЧ
1. Какая масса карбоната натрия (в граммах) потребуется для приготовления 0,5 л 13%-го раствора плотностью 1,13 г/мл?
а) 73,45; б) 50; в) 72; г) 75.
2. Из раствора хлорида бария массой 100 г с массовой долей соли 3 % выпарили 25 г воды и до- бавили в него 15 г соли. Массовая доля соли (в %) в полученном растворе равна:
а) 12; б) 15; в) 18; г) 20.
3. Смешали 120 г раствора серной кислоты с массовой до лей 20 % и 40 г 50%-го раствора того же вещества. Определите массовую долю кислоты (в %) в полученном растворе.
а) 25; б) 27,5; в) 27; г) 29,5.
4. Какая масса азотной кислоты (в граммах) содержится в 1 л ее 20%-го раствора с плотностью 1,05 г/мл?
а) 105; б) 63; в) 210; г) 176.
5. Какая масса соли (в граммах) вводится в организм человека при вливании 353 г 0,85%-го физиологического раствора?
а) 3; б) 6; в) 4; г) 2 г.
6. К 180 г 8%-го раствора хлорида натрия добавили 20 г NaCl. Найдите массовую долю (в %) хлорида натрия в образовавшемся растворе.
а) 17,2; б) 17,4; в) 18; г) 12,7.
7. К раствору хлорида кальция массой 140 г с массовой долей соли 5 % добавили 10 г этой же соли. Определите массовую долю (в %) хлорида кальция в полученном растворе.
а) 13,1; б) 14; в) 11,3; г) 25.
8. Какую массу соли (в граммах) надо добавить к 60 г раствора с массовой долей этой соли 10 %, чтобы получить раствор с массовой долей 40 %?
а) 15; б) 22; в) 17; г) 30.
9. Смешали 200 г 15%-го раствора нитрата хрома(III) и 300 г 20%-го раствора той же соли. Вычислите массовую долю (в %) ни- трата хрома(III) в полученном растворе.
а) 24; б) 18; в) 17,9; г) 18,1.
10. Из 150 г раствора хлорида натрия с массовой долей 5 % выпарили 10 г воды и добавили 5 г той же соли. Вычислите массовую долю (в %) соли в полученном растворе.
а) 8,4; б) 8,6; в) 9; г) 11,2.
11. Смешали 200 г 5%-го и 400 г 12,5%-го растворов серной кислоты. Найдите массу кислоты в полученном растворе (в граммах).
а) 60; б) 98; в) 49; г) 58.
12. При растворении 16 г гидроксида натрия получили 10%- й раствор. Определите массу (в граммах) взятой для этого воды.
а) 126; б) 144; в) 151; г) 164.
13. К 200 г 10%-го раствора ни- трата калия добавили некоторую порцию нитрата калия и получи- ли 20%-й раствор. Найдите массу (в граммах) добавленной порции твердого вещества. а) 2,5; б) 5; в) 25; г) 15.
14. Найдите массу воды (в граммах), которую нужно добавить к 300 г 8%-го раствора сульфата натрия для получения 5%-го раствора.
а) 90; б) 45; в) 18; г) 180.
15. Какая масса раствора (в граммах) получится при упаривании 200 г 5%-го раствора гидроксида калия до 20%-го раствора?
а) 10; б) 45; в) 100; г) 50.
16. 92 мл 10%-го раствора серной кислоты (плотность 1,066 г/мл) полностью нейтрализовали 40%-м раствором гидроксида натрия. Найдите массу затраченного на нейтрализацию раствора гидроксида натрия (в граммах).
а) 10; б) 55; в) 20; г) 30.
17. Определите, какую массу гидроксида калия (в граммах) нужно добавить к 150 г 20%-го раствора гидроксида калия для получения 40%-го раствора.
а) 5; б) 50; в) 56; г) 78.
18. К 200 г 8%-го раствора хлорида натрия добавили 50 г воды. Вычислите массовую долю (в %) соли в образовавшемся растворе.
а) 6,4; б) 6,5; в) 6,1; г) 6,2.
19. Определите массу воды (в граммах), которую надо добавить к 20 г 70%-го раствора уксусной кислоты для получения 5%-го раствора уксуса.
а) 260; б) 130; в) 26; г) 258.
20. Определите массу сахара (в граммах), необходимую для приготовления 0,5 кг 45%-го раствора.
а) 245; б) 225; в) 345; г) 500.
21. Вычислите массовую долю соляной кислоты (в %) в растворе, полученном при растворении 11,2 л (н.у.) хлороводорода в 1 л воды.
а) 1,3; б) 1,6; в) 1,8; г) 3,6.
22. Вычислите массу 40%-го раствора уксусной кислоты (в граммах), которую необходимо добавить к 500 г воды для получения 15%-го раствора.
Вычислите массу 40%-го раствора уксусной кислоты (в граммах), которую необходимо добавить к 500 г воды для получения 15%-го раствора.
а) 29; б) 32; в) 48; г) 300.
23. Массовая доля соли в морской воде составляет 3,5 %. Найдите массу соли (в граммах), которая останется после выпаривания 5 кг морской воды.
а) 175; б) 170; в) 167; г) 163.
24. Смешали 250 г раствора гидроксида натрия с массовой долей 16 % и 300 мл раствора (ρ = 1,2 г/мл) с массовой долей того же вещества 20 %. Рассчитайте массу гидроксида натрия (в граммах) в полученном растворе:
а) 120; б) 112; в) 11; г) 115.
25. Какова масса поваренной соли (в граммах), которую следует растворить в 250 г раствора этой соли с массовой долей 10 % для получения раствора с массовой долей 18 %?
а) 22; б) 42,4; в) 24,4; г) 44.
26. К 50 г раствора хлорида кальция с массовой долей 3,5 % добавили 5 г этой же соли и 20 г воды. Определите массовую долю (в %) соли в полученном растворе.
Определите массовую долю (в %) соли в полученном растворе.
а) 6; б) 7; в) 8; г) 9.
27. Какая масса серной кисло ты (в граммах) содержится в 0,6 л ее 40%-го раствора с плотностью 1,3 г/мл?
а) 63; б) 26; в) 60; г) 312.
28. Найдите массу хлорида натрия (в граммах), который необходимо растворить в 50 г воды для приготовления раствора с массовой долей соли 20 %.
а) 20; б) 12,5; в) 5; г) 24.
29. К 350 г водного раствора этанола с массовой долей 20 % добавили 120 мл спирта (плотность 0,8 г/мл). Рассчитайте массу спирта (в граммах) в полученном растворе.
а) 167; б) 156; в) 166; г) 170.
30. Из 50 г раствора хлорида натрия с массовой долей 2 % выпарили 10 г воды и добавили 5 г этой же соли. Определите массовую долю соли (в %) в полученном растворе.
а) 6,3; б) 13,3; в) 8,9; г) 9,4
Ответы. 1–а, 2–г, 3–б, 4–в, 5–а, 6–а, 7–в, 8–г, 9–б, 10–б, 11–а, 12–б, 13–в, 14–г, 15–г, 16–в, 17–б, 18–а, 19–а, 20–б, 21–в, 22–г, 23–а, 24–б, 25–в, 26–г, 27–г, 28–б, 29–в, 30–б.
Решение задач на смеси, сплавы и растворы для ЕГЭ по математике
Хочу продолжить тему, начатую одним из моих коллег – решение задач на смеси, сплавы и растворы.
Подобные задачи довольно часто встречаются в реальных и демонстрационных вариантах ОГЭ и ЕГЭ. В обычных школах таким задачам не уделяется должного внимания и даже у учеников 11 классов возникают сложности при их решении.
Рассмотрим решение на примере не сложной задачи.
Имеется два сплава. Первый содержит 10% никеля, второй – 25% никеля. Из этих двух сплавов получили третий сплав массой 105 кг, содержащий 20% никеля. На сколько килограммов масса первого сплава была меньше массы второго?
Решение.
Обозначим: m1 – масса первого сплава. Если третий сплав, получившийся из двух, равен 105 кг, то масса второго сплава (105-m1)кг.
Главная идея решения – равенство масс чистого вещества в начале и после соединения сплавов.
Найдём количество чистого никеля в первом сплаве – 0,1 m1
Количество чистого никеля во втором сплаве – 0,25(105-m1).
Тогда общая масса чистого никеля в обоих сплавах – (0,1 m1+0,25(105-m1))кг. (1)
После соединения сплавов общая масса 105кг, а содержание никеля 20%, тогда в новом славе чистого никеля будет – 0,20*105кг. (2).
Чистый никель никуда не исчез и нового чистого никеля не добавлено, значит величины (1) и (2) равны.
Запишем уравнение ( 0,1 m1+0,25(105-m1))= 0,20*105, решая его находим m1=35,
масса второго сплава 105 -35 = 70кг. И в итоге 70 – 35=35кг – масса первого сплава больше массы второго на 35кг. Ответ: 35
Решим ещё задачу.
Имеется два сосуда. Первый содержит 100кг., а второй -20кг. раствора кислоты различной концентрации. Если эти растворы смешать, то получится раствор, содержащий 72% кислоты. Если же смешать равные массы этих растворов, то получится раствор, содержащий 78% кислоты. Сколько килограммов кислоты содержится в первом растворе?
Решение.
Пусть к – концентрация первого раствора, р – концентрация второго раствора. Чистой кислоты в первом растворе – 100к кг., во втором – 20р кг. и всего в двух растворах – (100к +20р) кг.
Чистой кислоты в первом растворе – 100к кг., во втором – 20р кг. и всего в двух растворах – (100к +20р) кг.
Если смешать растворы, то вес нового раствора -120кг. и концентрация 72%., при том же количестве, что и в начале, чистой кислоты, т.е (100к +20р) = 0,72*120 (1).
Возьмём теперь равные массы растворов, для простоты возьмём по 10кг.
Определим начальное количество чистой кислоты в обоих растворах. В первом растворе 10к чистой кислоты, во втором 10р чистой кислоты. Тогда всего вначале чистой кислоты было (10к +10р) кг. Масса нового раствора 10+10 =20 кг и по условию его концентрация 0,78. Чистой кислоты в новом растворе – 0,78*20. По условию равенства чистого вещества (10к +10р)= 0,78*20 (2).
Решая совместно (1) и (2) получаем к = 0,69, тогда чистой кислоты в первом растворе – 69кг. Отв.: 69
Теперь посмотрим как легко решается известная задача про изюм и виноград.
Изюм получается в процессе сушки винограда. Сколько килограммов винограда потребуется для получения 14 килограммов изюма, если виноград содержит 90% воды, а изюм содержит 5% воды?
Решение.
Если в винограде 90% воды, значит 10% чистого изюма (название образное).
В изюме (магазинном) должно быть 95% чистого изюма. В 14кг. магазинного изюма чистого изюма будет чуть меньше – 14*0,95= 13,3кг. Это количество необходимо набрать из винограда, где только 10% чистого изюма. Значит 13,3 кг в винограде, должны составлять десятую часть, тогда необходимо взять 133 кг. винограда. В 133кг. винограда будет 13,3 чистого изюма, что позволит иметь 14 кг магазинного изюма. Ответ: 133
При решении всех простых задачах на сплавы, смеси, и растворы применяют условие равенства чистых масс вещества в начале и после соединения. В более сложных, это условие помогает найти ходы решения.
В завершении приведу решение сложной задачи, решение которой опирается на понятие «концентрация». Такая задача может быть в задании 11 профильного ЕГЭ. Обычно такого рода задачи прорешивают заранее, чтобы на экзамене не возникла тревога при виде сложного и на первый взгляд, запутанного условия.
В сосуде было 20 литров соляной кислоты. Часть кислоты отлили, и сосуд дополнили водой. Затем отлили в два раза большую (чем в первый раз) часть полученной смеси и снова дополнили сосуд водой. В результате получился 28% раствор кислоты. Сколько литров кислоты отлили в первый раз?
Редакция не несет ответственности за наполнение блогов, они есть персональным мнением автора
Как правильно пересчитать концентрации растворов из одних единц в другие – 27 Ноября 2012 – Примеры решений задач
Пересчет концентраций растворов из одних единиц в другие
При пересчете процентной концентрации в молярную и наоборот, необходимо помнить, что процентная концентрация рассчитывается на определенную массу раствора, а молярная и нормальная – на объем, поэтому для пересчета необходимо знать плотность раствора. Если мы обозначим: с – процентная концентрация; M – молярная концентрация; N – нормальная концентрация; э – эквивалентная масса, p – плотность раствора; m – мольная масса, то формулы для пересчета из процентной концентрации будут следующими:
M = (c · p · 10) / m
N = (c · p · 10) / э
Этими же формулами можно воспользоваться, если нужно пересчитать нормальную или молярную концентрацию на процентную.
Пример
Какова молярная и нормальная концентрация 12%-ного
раствора серной кислоты, плотность которого р = 1,08 г/см3?
Решение
Мольная масса серной кислоты равна 98. Следовательно,
m(H2SO4) = 98 и э(H2SO4) = 98 : 2 = 49.
Подставляя необходимые значения в формулы, получим:
а) Молярная концентрация 12% раствора серной кислоты равна
M = (12 · 1,08 · 10) / 98 = 1,32 M
б) Нормальная концентрация 12% раствора серной кислоты равна
N = (12 ·1,08 ·10) / 49 = 2,64 H.
Иногда в лабораторной практике приходится
пересчитывать молярную концентрацию в нормальную и наоборот. Если
эквивалентная масса вещества равна мольной массе (Например, для HCl,
KCl, KOH), то нормальная концентрация равна молярной концентрации. Так,
1 н. раствор соляной кислоты будет одновременно 1 M раствором. Однако
для большинства соединений эквивалентная масса не равна мольной и,
следовательно, нормальная концентрация растворов этих веществ не равна
молярной концентрации.
Для пересчета из одной концентрации в другую можно использовать формулы:
M = (N · Э) / m
N = (M · m) / Э
Пример
Нормальная концентрация 1 М раствора серной кислоты
N = (1 · 98) / 49 = 2 H.
Пример
Молярная концентрация 0,5 н. Na2CO3
Упаривание, разбавление, концентрирование, смешивание растворов
Имеется mг исходного раствора с массовой долей растворенного вещества w1 и плотностью ρ1.
Упаривание раствора
В результате упаривания исходного раствора его масса уменьшилась на Dm г. Определить массовую долю раствора после упаривания w2
Решение
Исходя из определения массовой доли, получим выражения для w1 и w2 (w2 > w1):
w1
(где m1 – масса растворенного вещества в исходном растворе)
m1 = w1·m
w1 = m1 / (m – Dm) = (w1· m) / (m – Dm)
Пример
Упарили 60 г 5%-ного раствора сульфата меди до 50 г. Определите массовую долю соли в полученном растворе.
Определите массовую долю соли в полученном растворе.
m = 60 г; Dm = 60 – 50 = 10 г; w1 = 5% (или 0,05)
w2 = (0,05 · 60) / (60 – 10) = 3 / 50 = 0,06 (или 6%-ный)
Концентрирование раствора
Какую массу вещества (X г) надо дополнительно растворить в исходном растворе, чтобы приготовить раствор с массовой долей растворенного вещества w2?
Решение
Исходя из определения массовой доли, составим выражение для w1 и w2:
w1 = m1 / m2,
(где m1 – масса вещества в исходном растворе).
m1 = w1 · m
w2 = (m1+x) / (m + x) = (w1 · m + x) / (m+x)
Решая полученное уравнение относительно х получаем:
w2 · m + w2 · x = w1 · m + x
w2 · m – w1 · m = x – w
(w2– w1 ) · m = (1 – w2 ) · x
x = ((w2 – w1) · m) / (1 – w2 )
Пример
Сколько граммов хлористого калия надо растворить в
90 г 8%-ного раствора этой соли, чтобы полученный раствор стал
10%-ным?
m = 90 г
w1 = 8% (или 0,08), w2 = 10% (или 0,1)
x = ((0,1 – 0,08) ·90) / (1 – 0,1) = (0,02 · 90) / 0,9 = 2 г
Онлайн сервис решения задач по химии
Решение задач на процентную концентрацию растворов
Решение задач
на процентную концентрацию
растворов
МЕТОДИЧЕСКАЯ РАЗРАБОТКА
ИНТЕГРИРОВАННОГО ОТКРЫТОГО УРОКА
ПО МАТЕМАТИКЕ И ХИМИИ
Технологическая карта занятия
Тема урока. Решение задач на процентную концентрацию, сплавы и растворы.
Решение задач на процентную концентрацию, сплавы и растворы.
Тип урока: систематизация и обобщение знаний.
Вид урока: интерактивная групповая работа.
Цель: отработать умения рассчитывать процентную концентрацию растворов и приготовление растворов с заданной концентрацией.
Задачи урока:
образовательные – применение знаний полученных на уроках химии и математики для решения задач;
развивающие – развивать логическое мышление, приемы умственной деятельности, познавательную активность, внимание, умение сопоставлять, анализировать, делать выводы;
воспитательные – развитие дисциплинированности, ответственности, наблюдательности, внимательности и аккуратности при работе с опасными веществами.
Общие компетенции:
ОК 2. Организовывать собственную деятельность, выбирать типовые способы выполнения задач.
Организовывать собственную деятельность, выбирать типовые способы выполнения задач.
ОК 3. Принимать решения в стандартных и нестандартных ситуациях и нести за них ответственность.
ОК 5. Использование коммуникационных технологий.
ОК 6. Работать в коллективе и команде, эффективно общаться с коллегами.
ОК 7. Брать на себя ответственность за работу членов команды, за результат выполнения задания.
Обеспечение урока:
Методическое обеспечение – организация упражнений по углублению практических умений и навыков, практический, контроль и взаимоконтроль.
Дидактическое обеспечение
а) раздаточный материал на тему Концентрация растворов: тест, задачи, практикум;
б) лабораторное оборудование – штатив для пробирок – 1 шт., пробирки – 2 шт., мерные цилиндры – 5 шт. , весы аптечные с набором гирь, ареометры – 3 шт., термометр водный, шпатель, стеклянные палочки – 5 шт;
, весы аптечные с набором гирь, ареометры – 3 шт., термометр водный, шпатель, стеклянные палочки – 5 шт;
в) реактивы – вода, гидроксид натрия (кристаллический), нитрат аммония (кристаллический), перманганат калия (кристаллический), 96%-ный раствор этилового спирта, 70%-ный раствор уксусной кислоты.
3. Информационно-компьютерное обеспечение
а) мультимедийный проектор, презентация;
б) основные источники информации:
Химия
1. Габриелян О.С. Химия: Учебник для студ. сред. проф. учеб. заведений / О.С. Габриелян, И.Г. Остроумов. – М.: Издательский центр «Академия», 2005.
2. Габриелян О.С. Практикум по общей, неорганической и органической химии: учеб. пособие для студ. сред. проф. учеб. заведений / О.С. Габриелян, И.Г. Остроумов, Н.М. Дорофеева. – 2-е изд., стер. – М.: Издательский центр «Академия», 2009.
3 Ерохин Ю. М. Химия: Учеб. для средних спец. учебных заведений. – М.: Издательский центр «Академия»: Высшая школа, 2001.
М. Химия: Учеб. для средних спец. учебных заведений. – М.: Издательский центр «Академия»: Высшая школа, 2001.
Математика
Колягин Ю.М Математика: В 2 кн. Кн.1: Учеб. Пособие для студентов образовательных учреждений среднего профессионального образования/ Ю.М. Колягин, Г.Л. Луканин, Г.Н. Яковлев; Под ред. Г.Н. Яковлева.- 5-е изд.- М.: ООО «Издательство Оникс»: ООО «Издательство «Мир и Образование», 2008.
Математика «Типовые тестовые задания», под редакцией А.Л. Семенова, И.В. Ященко, издательство «Экзамен» Москва 2012г.
в) дополнительные источники информации:
Химия
1. Евстифеева А.Г. Пособие для подготовки к централизованному тестированию по химии. – Ростов-на-Дону: Феникс, 2002.
2. Задачи и упражнения по общей химии: Учеб. пособие / Б.И. Адамсон, О.Н. Гончарук, В.Н. Камышова и др., Под ред. Н.В. Коровина. – 2-е изд., испр. – М.: Высш. шк., 2004.
– 2-е изд., испр. – М.: Высш. шк., 2004.
3. Шипуло Е.В. Решение задач по химии / Е.В. Шипуло. – М.: Филол. о-во «СЛОВО», Изд-во Эксмо, 2005.
Математика
Будлянская Н.Л, Сумина Г.Н Решение текстовых задач: Пособие для учащихся. – Комсомольск-на-Амуре: Издательство Комсомольского –на-Амуре государственного педагогического университета, 2004.
№ | Этапы урока | Содержание | Деятельность преподавателя | Деятельность обучающихся | Реализация целей |
1 | Организационный этап | Приветствие, психологический настрой на совместную деятельность, определение мотивации и постановка целей урока | – приветствие студентов -объявление студентам целей урока; – стимулирование положительной мотивации к обучению; – напоминание студентам о межпредметных связях; | Слуховое восприятие | Воспитание дисциплинированности, ответственности, внимательности . |
2 | Подготовка обучающихся к активному усвоению знаний | Перекрестный фронтальный опрос; Демонстрация опыта; Письменное тестирование | – целевая установка на работу; – постановка вопросов и заданий; – подведение итогов | – продумывание ответов на вопросы и задания; – анализ демонстрационного опыта. | – Применение знаний полученных на уроках химии и математики; – развитие внимания, познавательной активности; – развитие умений анализировать и делать выводы. |
3 | Обобщение и систематизация ранее изученного материала | Решение расчетных задач ; Практическая работа по приготовлению растворов заданной концентрации | – целевая установка на работу; – указание на алгоритм решения задач; – повторение правил техники безопасности на уроке; – контроль за деятельностью обучающихся | – слуховое воспириятие и осмысление полученного задания; – запись алгоритма решения задач; – соблюдение правил ТБ; – выполнение под контролем преподавателя практического задания. | -Применение ранее полученных знаний; – развитие логического мышления; – активизация умственной деятельности; – развитие навыков внимания и аккуратности при работе с опасными веществами. |
4 | Подведение итогов занятия и рефлексия | – анализ деятельности обучающихся на уроке; – выставление оценок за работу на уроке; – использование методов рефлексии для определения эмоционального фона урока. | – Подведение итогов урока; – выставление и комментирование оценок за работу на уроке; | – слуховое восприятие; – участие в рефлексии; | Развитие позитивной мотивации к изучению дисциплин химии и математики. |
5 | Домашнее задание | Постановка дифференцированного домашнего задания | – целевая установка на выполнение домашнего задания; – определение сроков выполнения д/з | – слуховое восприятия д/з; – осмысление содержания д/з | Развитие ответственности за выполнение полученного задания. |
ХОД ЗАНЯТИЯ
I.Организационный этап:
1. Приветствие, психологический настрой на совместную деятельность преподавателей и студентов;
2. Определение мотивации и постановка целей урока.
II. Подготовка обучающихся к активному усвоению знаний:
Содержание | Методы контроля ЗУН |
1.Что такое растворы? 2.Что называют процентом? 3. Что называют растворителем, а что растворенным веществом? 4.Из чего складывается масса раствора? 5. Какие типы растворов различают по типу растворителя? 6. 48% раствор. Что это значит? 7. 8. 1,5 г соли растворили в 10 г жидкости. Определите процентную концентрацию раствора. | Перекрестный фронтальный опрос вопросов теории по химии и математике. |
Демонстрация опыта «Изменение температуры при растворении веществ». | Анализ наблюдаемых явлений. |
Тест на тему «Концентрация растворов». | Индивидуальная письменная работа с взаимоконтролем. |
III. Обобщение и систематизация ранее изученного материала.
План | Методы обучения |
1.Решение задач. | Расчет по химическим и математическим формулам. |
2. Приготовление растворов заданной концентрации. | Групповая практическая работа |
3. Значение растворов в природе и жизни человека. | Просмотр видеофильма с анализом видеоматериала. |
IV. Подведение итогов занятия и рефлексия.
Выставление оценок студентам за работу на уроке, рефлексия.
V. Домашнее задание.
1 уровень – на оценку «3».
2 уровень – на оценку «4».
Смешали 4 литра 15%-ного водного раствора некоторого вещества с 6 литрами 25%-ного водного раствора этого же вещества. Сколько процентов составляет концентрация получившегося раствора?
3 уровень – на оценку «5».
Смешали 30%-ный и 60%-ный растворы кислоты и добавили 10 кг воды, получили 36%-ный раствор кислоты. Если бы вместо 10 кг воды добавили 10 кг 50%-ного раствора той же кислоты, то получили бы 41%-ный раствор кислоты. Сколько кг 30%-ного раствора использовали для получения смеси?
Ход урока
I. Организационный этап.
1. Приветствие, психологический настрой на совместную деятельность преподавателей и студентов.
Сегодня на уроке вам предстоит не только вспомнить и закрепить пройденный материал, но и научиться организовывать собственную деятельность, выбирать типовые способы выполнения задач, работать в коллективе и команде, эффективно общаться с одногруппниками.
2.Определение мотивации и постановка целей урока.
В жизни человек постоянно сталкивается с различными веществами. Чаще всего эти вещества находятся в каком-нибудь соотношении между собой, т. е. с чистыми веществами имеем дело очень редко. Обычно это какие-либо растворы веществ. В жизни нам приходится растворы смешивать, разбавлять или наоборот делать более концентрированными, нам необходимо порой вычислить концентрацию используемых растворов или даже самим их готовить. Для этого недостаточно знаний только химии поможет нам и наука математика.
е. с чистыми веществами имеем дело очень редко. Обычно это какие-либо растворы веществ. В жизни нам приходится растворы смешивать, разбавлять или наоборот делать более концентрированными, нам необходимо порой вычислить концентрацию используемых растворов или даже самим их готовить. Для этого недостаточно знаний только химии поможет нам и наука математика.
Сегодня на уроке мы будем применять знания двух наук – химии и математики для решения задач на процентную концентрацию растворов. Запишите тему урока «Решение задач на процентную концентрацию растворов».
Эпиграфом нашего урока может послужить фраза сказанная Антуаном де Сент-Экзюпери: «Только из союза двоих работающих вместе и при помощи друг друга, рождаются великие вещи».
Познакомьтесь с планом работы на уроке.
План урока:
1. Повторение понятий о растворимости веществ и процентах.
2. Решение задач на процентную концентрацию растворов химическим и математическими способами.
3. Практическая часть – приготовление растворов.
4. Просмотр видеофильма.
5. Подведение итогов урока.
Цель нашего урока: применение знаний полученных на уроках химии и математики для решения задач.
II. Подготовка обучающихся к активному усвоению знаний:
1. Перекрестный фронтальный вопрос:
1.1.Что такое растворы?
1.2. Что называют процентом?
1.3. Что называют растворителем, а что растворенным веществом?
1.4. Из чего складывается масса раствора?
1.5. Какие типы растворов различают по типу растворителя?
1.6. 48% раствор. Что это значит?
1.7. Что называют процентной концентрацией раствора и чем ее можно выразить?
1.8. 1,5 г соли растворили в 10 г жидкости. Определите процентную концентрацию раствора.
Определите процентную концентрацию раствора.
2. Демонстрация опыта «Изменение температуры при растворении веществ». Опыт представлен в форме видеоклипа.
Растворы – это физико-химические системы. Физический процесс растворения вещества заключается в разрушении кристаллической решетки растворяемого вещества и диффузии его частиц в частицах растворителя.
Химический процесс растворения вещества – гидратация частиц растворенного вещества, т.е. окружение их частицами растворителя, например, воды. Часто растворение сопровождается термическими явлениями.
В две пробирки налить (до 1/3) воды и измерить ее температуру. В первую пробирку всыпать 2-3 г нитрата аммония, осторожно перемешать и измерить температуру раствора. Во вторую пробирку внести несколько кусочков гидроксида натрия и после перемешивания измерить температуру раствора.
При растворении какого из веществ теплота выделяется, а какого поглощается, как называются такие процессы?
Следующий этап нашего урока – проверочная тестовая работа со взаимоконтролем.
Тест на тему «Концентрация растворов»
Вариант 1
1. В 200 г воды растворили 50 г сахара. Массовая доля сахара в растворе составляет:
а) 25%; б) 4%; в) 8%; г) 20%.
2. Масса растворенного вещества, содержащегося в 200 г раствора с массовой долей 10%, равна:
а) 10 г; б) 20 г; в) 30 г; г) 40 г.
3. Объем азота, содержащегося в 200 л воздуха с объемной долей азота 78% равен:
а) 256 л; б) 156 л; в) 15,6 л; г) 25,6 л.
Вариант 2
1. В 180 г воды растворили 20 г соли. Массовая доля соли в растворе составляет:
а) 11%; б) 10%; в) 9%; г) 8%.
2. Масса растворенного вещества, содержащегося в 30 г раствора с массовой долей 20% равна:
а) 0,6 г; б) 3 г; в) 6 г; г) 30 г.
3. Объем кислорода содержащегося в 500 л воздуха с объемной долей кислорода 21% равен:
а) 105 л; б) 23,8 л; в) 10,5 л; г) 21,0 л.
Критерии оценки: «5» – три правильных ответа;
«4» – два правильных ответа;
«3» – один правильный ответ;
«2» – нет правильных ответов.
III. Обобщение и систематизация ранее изученного материала.
1. Решение задач с помощью химических формул и математических методов.
1. Ржавчину – рыхлую корку гидроксида железа (III) Fe(OH)3 на поверхности металлических изделий – проще всего снять обработкой разбавленным раствором соляной кислоты, содержащей ингибитор (замедлитель реакции окисления железа) – уротропин C6H12N4. Мелкие детали погружают в 5%-ный раствор соляной кислоты добавкой 0,5 г уротропина на литр, а на крупные вещи такой раствор наносят кистью.
Рассчитайте объем воды и объем 35%-ной соляной кислоты (плотность 1,175 г/мл) который потребуются для приготовления 3 литров 5%-ного раствора (плотность 1,023 г/мл).
2. Определите, сколько нужно взять растворов соли 60%-ной и 10% -ной концентрации для приготовления 300 г раствора 25% -ной концентрации?
Однообразная работа утомляет человека. Поэтому необходимо менять виды деятельности для достижения положительного результата. Предлагаем Вам при смене деятельности немного привести свое зрение в норму, сделав зрительную гимнастику. Это поможет вам восстановить кровообращение в органах зрения и активизировать работу мозга, что будет способствовать повышению качества работы на уроке.
ГИМНАСТИКА ДЛЯ ГЛАЗ
2. Приготовление растворов заданной концентрации.
Группа студентов делится на 3 подгруппы, каждая подгруппа получает задачу. Каждая подгруппа делится еще на две группы: группа теоретиков и группа практиков. Теоретики должны рассчитать, сколько необходимо взять веществ для приготовления раствора и полученные данные передать практикам. Практики должны, используя данные теоретиков, приготовить раствор и проверить его правильность с помощью ареометра.
Теоретики должны рассчитать, сколько необходимо взять веществ для приготовления раствора и полученные данные передать практикам. Практики должны, используя данные теоретиков, приготовить раствор и проверить его правильность с помощью ареометра.
Преподаватель математики проверяет теоретиков, а преподаватель химии – практиков.
Перед выполнением практической части проводится повторный инструктаж по технике безопасности (в стихах).
Чай и вкусный бутерброд
Очень просятся в твой рот.
Не обманывай себя –
Есть и пить у нас нельзя!
Это, друг, химкабинет,
Для еды условий нет.
Пусть в пробирке пахнет воблой,
В колбе – будто мармелад,
Вещества на вкус не пробуй!
Сладко пахнет даже яд.
Вдруг попал тебе на кожу
Ядовитый химикат:
Срочно смой его водою,
Не то будешь сам не рад!
Нюхать нужно осторожно,
И при том, махнув рукой,
И тогда не будет плохо
У ребенка с головой.
Прежде чем начать работать,
Парту надо расчищать,
А не то учебник будет
Под рукой тебе мешать!
Рукой не трогай реактивы –
Начнутся страшные нарывы.
А коль коснешься кислоты,
О, скоро пожалеешь ты!
Группа 1. Для засолки огурцов используют 3,5%-ный раствор уксусной кислоты (уксусная эссенция) для подавления образования гнилостных бактерий.
Приготовьте 200 мл столового уксуса (массовая доля 3,5 % плотностью 1,004 г/мл) разбавлением уксусной кислоты (массовая доля 70% и плотность 1,07 г/мл). Рассчитайте, сколько потребуется мл воды и уксусной эссенции?
Группа 2. Для приготовления различных спиртовых компрессов, растираний, лосьонов часто необходимо использование 40%-ного раствора этилового спирта (водка).
Приготовьте 100 мл водки (массовая доля 40%) из этилового спирта, если плотность этилового спирта 0,8 г/мл. Рассчитайте, сколько потребуется мл воды и этилового спирта?
Группа 3. «Препарат номер один» в домашней аптечке – перманганат калия KMnO4 (марганцовка). В медицине применяют водные растворы перманганата калия разной концентрации при лечении ангины, змеиных укусов, промывании желудка, обработки ран. Для обработки ожогов используют 2 – 5%-ные растворы KMnO4.
«Препарат номер один» в домашней аптечке – перманганат калия KMnO4 (марганцовка). В медицине применяют водные растворы перманганата калия разной концентрации при лечении ангины, змеиных укусов, промывании желудка, обработки ран. Для обработки ожогов используют 2 – 5%-ные растворы KMnO4.
Рассчитайте массу перманганата калия и объем мл воды, которые требуются для приготовления 100 г 3%-ного раствора KMnO4.
Пока работает группа теоретиков, практики выполняют задание по рефлексии, и наоборот, когда работает группа практиков, теоретики выполняют задание по рефлексии.
IV. Подведение итогов занятия и рефлексия.
Итак, в ходе урока мы убедились, что науки химия и математика находятся в тесном взаимодействии. Это относится и к другим дисциплинам естественнонаучного цикла.
Выставление оценок.
Каждой подгруппе (теоретикам и практикам) предлагается продолжить фразу «Химия и математика – это . ..»
..»
Вашего внимания в изучении заслуживают все дисциплины, изучаемые на 1 курсе для успешного продолжения учебы в дальнейшем и успешной сдачи предстоящей весенней сессии, чтоб не произошла с вами забавная история одного студента (звучит песня студента о сессии).
V. Домашнее задание.
1 уровень – на оценку «3»
На 3,9 г калия подействовали 41,1 мл воды. Определите массовую долю полученной щелочи.
2 уровень – на оценку «4».
Смешали 4 литра 15%-ного водного раствора некоторого вещества с 6 литрами 25%-ного водного раствора этого же вещества. Сколько процентов составляет концентрация получившегося раствора?
3 уровень – на оценку «5».
Смешали 30%-ный и 60%-ный растворы кислоты и добавили 10 кг воды, получили 36%-ный раствор кислоты. Если бы вместо 10 кг воды добавили 10 кг 50%-ного раствора той же кислоты, то получили бы 41%-ный раствор кислоты.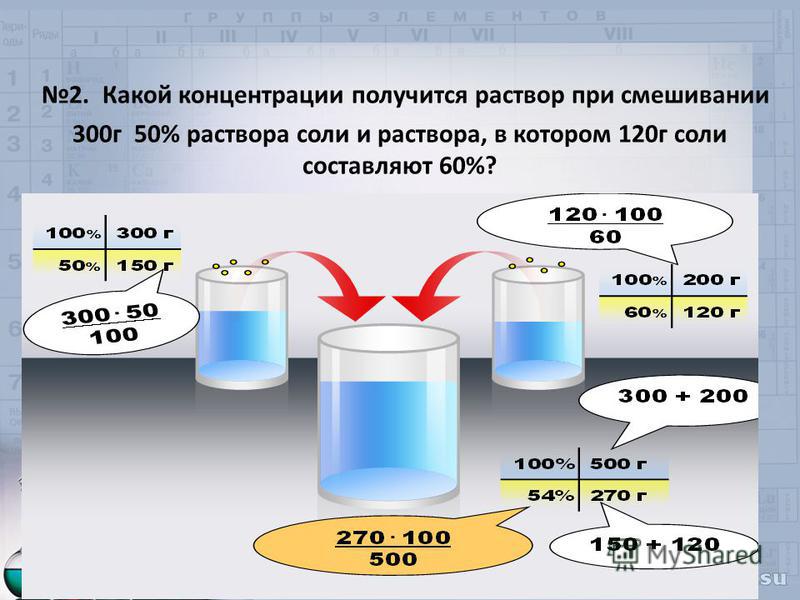 Сколько кг 30%-ного раствора использовали для получения смеси?
Сколько кг 30%-ного раствора использовали для получения смеси?
4.5: Концентрация растворов – Химия LibreTexts
Многие люди имеют качественное представление о том, что подразумевается под концентрацией . Любой, кто варил растворимый кофе или лимонад, знает, что слишком много порошка дает сильно ароматизированный и высококонцентрированный напиток, тогда как слишком мало приводит к разбавленному раствору, который может быть трудно отличить от воды. В химии концентрация раствора – это количество растворенного вещества , которое содержится в определенном количестве растворителя или раствора.Знание концентрации растворенных веществ важно для контроля стехиометрии реагентов для реакций в растворе. Химики используют множество различных методов для определения концентраций, некоторые из которых описаны в этом разделе.
Молярность
Наиболее распространенной единицей концентрации является молярность , что также является наиболее полезным для расчетов, включающих стехиометрию реакций в растворе.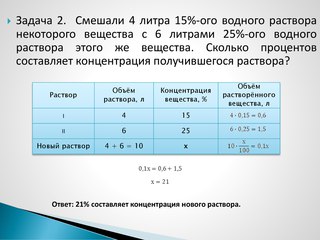 Молярность (M) определяется как количество молей растворенного вещества, присутствующего ровно в 1 л раствора.Это эквивалентно количеству миллимолей растворенного вещества, присутствующего точно в 1 мл раствора:
Молярность (M) определяется как количество молей растворенного вещества, присутствующего ровно в 1 л раствора.Это эквивалентно количеству миллимолей растворенного вещества, присутствующего точно в 1 мл раствора:
\ [молярность = \ dfrac {моль \: of \: solute} {литры \: of \: solution} = \ dfrac {ммоль \: of \: solute} {миллилитры \: of \: solution} \ label {4.5 .1} \]
Таким образом, единицами молярности являются моль на литр раствора (моль / л), сокращенно \ (М \). Водный раствор, содержащий 1 моль (342 г) сахарозы в достаточном количестве воды, чтобы получить конечный объем 1,00 л, имеет концентрацию сахарозы 1.00 моль / л или 1,00 М. В химической записи квадратные скобки вокруг названия или формулы растворенного вещества представляют молярную концентрацию растворенного вещества. Следовательно,
\ [[\ rm {сахароза}] = 1,00 \: M \]
читается как «концентрация сахарозы 1,00 молярная». Отношения между объемом, молярностью и молями могут быть выражены как
\ [V_L M_ {mol / L} = \ cancel {L} \ left (\ dfrac {mol} {\ cancel {L}} \ right) = моль \ label {4. 5.2} \]
5.2} \]
или
\ [V_ {mL} M_ {ммоль / мл} = \ cancel {mL} \ left (\ dfrac {mmol} {\ cancel {mL}} \ right) = ммоль \ label {4.5.3} \]
На рисунке \ (\ PageIndex {1} \) показано использование формул \ (\ ref {4.5.2} \) и \ (\ ref {4.5.3} \).
Рисунок \ (\ PageIndex {1} \): Приготовление раствора известной концентрации с использованием твердого раствораПример \ (\ PageIndex {1} \): расчет молей по концентрации NaOH
Рассчитайте количество молей гидроксида натрия (NaOH) в 2,50 л 0,100 M NaOH.
Дано: идентичность растворенного вещества, а также объем и молярность раствора
Запрошено: количество растворенного вещества в молях
Стратегия:
Используйте уравнение \ ref {4.5.2} или Equation \ ref {4.5.3}, в зависимости от единиц, указанных в задаче.
Решение:
Поскольку нам задают объем раствора в литрах и спрашивают количество молей вещества, уравнение \ ref {4. 5.2} более полезно:
5.2} более полезно:
\ (моль \: NaOH = V_L M_ {моль / л} = (2,50 \: \ cancel {L}) \ left (\ dfrac {0.100 \: mol} {\ cancel {L}} \ right) = 0,250 \: моль \: NaOH \)
Упражнение \ (\ PageIndex {1} \): вычисление молей по концентрации аланина
Вычислите количество миллимолей аланина, биологически важной молекулы, в 27.2 мл 1,53 М аланина.
- Ответ
41,6 ммоль
Расчеты с учетом молярности (M): https://youtu.be/TVTCvKoSR-Q
Концентрации также часто указываются в зависимости от массы к массе (м / м) или по отношению к массе к объему (м / об), особенно в клинических лабораториях и инженерных приложениях. Концентрация, выраженная на основе м / м, равна количеству граммов растворенного вещества на грамм раствора; Концентрация на основе м / об – это количество граммов растворенного вещества на миллилитр раствора.Каждое измерение можно выразить в процентах, умножив соотношение на 100; результат выражается в процентах по массе или в процентах по массе. Концентрации очень разбавленных растворов часто выражаются в частей на миллион ( частей на миллион ), что составляет граммы растворенного вещества на 10 6 г раствора, или в частях на миллиард ( частей на миллиард ), что составляет граммов растворенного вещества на 10 9 г раствора. Для водных растворов при 20 ° C 1 ppm соответствует 1 мкг на миллилитр, а 1 ppb соответствует 1 нг на миллилитр.Эти концентрации и их единицы приведены в Таблице \ (\ PageIndex {1} \).
Концентрации очень разбавленных растворов часто выражаются в частей на миллион ( частей на миллион ), что составляет граммы растворенного вещества на 10 6 г раствора, или в частях на миллиард ( частей на миллиард ), что составляет граммов растворенного вещества на 10 9 г раствора. Для водных растворов при 20 ° C 1 ppm соответствует 1 мкг на миллилитр, а 1 ppb соответствует 1 нг на миллилитр.Эти концентрации и их единицы приведены в Таблице \ (\ PageIndex {1} \).
| Концентрация | Шт. |
|---|---|
| м / м | г растворенного вещества / г раствора |
| м / об | г растворенного вещества / мл раствора |
| частей на миллион | г растворенного вещества / 10 6 г раствора |
| мкг / мл | |
| частей на миллиард | г растворенного вещества / 10 9 г раствора |
| нг / мл |
Приготовление растворов
Чтобы приготовить раствор, содержащий определенную концентрацию вещества, необходимо растворить желаемое количество молей растворенного вещества в достаточном количестве растворителя, чтобы получить желаемый конечный объем раствора. Рисунок \ (\ PageIndex {1} \) иллюстрирует эту процедуру для раствора дигидрата хлорида кобальта (II) в этаноле. Обратите внимание, что объем растворителя не указан. Поскольку растворенное вещество занимает место в растворе, необходимый объем растворителя почти всегда на меньше , чем желаемый объем раствора. Например, если желаемый объем был 1,00 л, было бы неправильно добавлять 1,00 л воды к 342 г сахарозы, потому что это привело бы к получению более 1,00 л раствора.Как показано на рисунке \ (\ PageIndex {2} \), для некоторых веществ этот эффект может быть значительным, особенно для концентрированных растворов.
Рисунок \ (\ PageIndex {1} \) иллюстрирует эту процедуру для раствора дигидрата хлорида кобальта (II) в этаноле. Обратите внимание, что объем растворителя не указан. Поскольку растворенное вещество занимает место в растворе, необходимый объем растворителя почти всегда на меньше , чем желаемый объем раствора. Например, если желаемый объем был 1,00 л, было бы неправильно добавлять 1,00 л воды к 342 г сахарозы, потому что это привело бы к получению более 1,00 л раствора.Как показано на рисунке \ (\ PageIndex {2} \), для некоторых веществ этот эффект может быть значительным, особенно для концентрированных растворов.
Пример \ (\ PageIndex {2} \)
Раствор содержит 10,0 г дигидрата хлорида кобальта (II), CoCl 2 • 2H 2 O, в этаноле, достаточном для приготовления ровно 500 мл раствора. Какова молярная концентрация \ (\ ce {CoCl2 • 2h3O} \)?
Какова молярная концентрация \ (\ ce {CoCl2 • 2h3O} \)?
Дано: масса растворенного вещества и объем раствора
Запрошено: концентрация (M)
Стратегия:
Чтобы найти количество молей \ (\ ce {CoCl2 • 2h3O} \), разделите массу соединения на его молярную массу. Рассчитайте молярность раствора, разделив количество молей растворенного вещества на объем раствора в литрах.
Решение:
Молярная масса CoCl 2 • 2H 2 O составляет 165.87 г / моль. Следовательно,
\ [молей \: CoCl_2 \ cdot 2H_2O = \ left (\ dfrac {10.0 \: \ cancel {g}} {165 .87 \: \ cancel {g} / mol} \ right) = 0 .0603 \: mol \ nonumber \]
Объем раствора в литрах
\ [volume = 500 \: \ cancel {mL} \ left (\ dfrac {1 \: L} {1000 \: \ cancel {mL}} \ right) = 0 .500 \: L \ nonumber \]
Молярность – это количество молей растворенного вещества на литр раствора, поэтому молярность раствора равна
.
\ [молярность = \ dfrac {0,0603 \: моль} {0.500 \: L} = 0,121 \: M = CoCl_2 \ cdot H_2O \ nonumber \]
Упражнение \ (\ PageIndex {2} \)
Раствор, показанный на рисунке \ (\ PageIndex {2} \), содержит 90,0 г (NH 4 ) 2 Cr 2 O 7 в достаточном количестве воды, чтобы получить конечный объем ровно 250 мл. Какова молярная концентрация дихромата аммония?
- Ответ
\ [(NH_4) _2Cr_2O_7 = 1,43 \: M \ nonumber \]
Чтобы приготовить конкретный объем раствора, который содержит указанную концентрацию растворенного вещества, нам сначала нужно вычислить количество молей растворенного вещества в желаемом объеме раствора, используя соотношение, показанное в уравнении \ (\ ref {4.5.2} \). Затем мы переводим количество молей растворенного вещества в соответствующую массу необходимого растворенного вещества. Эта процедура проиллюстрирована в примере \ (\ PageIndex {3} \).
Пример \ (\ PageIndex {3} \): D5W Решение
Так называемый раствор D5W, используемый для внутривенного замещения биологических жидкостей, содержит 0,310 М глюкозы. (D5W представляет собой примерно 5% раствор декстрозы [медицинское название глюкозы] в воде.) Рассчитайте массу глюкозы, необходимую для приготовления пакета D5W объемом 500 мл. Глюкоза имеет молярную массу 180.16 г / моль.
Дано: молярность, объем и молярная масса растворенного вещества
Запрошено: Масса растворенного вещества
Стратегия:
- Рассчитайте количество молей глюкозы в указанном объеме раствора, умножив объем раствора на его молярность.
- Получите необходимую массу глюкозы, умножив количество молей соединения на его молярную массу.
Решение:
A Сначала мы должны вычислить количество молей глюкозы, содержащихся в 500 мл 0. 310 M раствор:
310 M раствор:
\ (V_L M_ {моль / л} = моль \)
\ (500 \: \ cancel {mL} \ left (\ dfrac {1 \: \ cancel {L}} {1000 \: \ cancel {mL}} \ right) \ left (\ dfrac {0 .310 \: моль \: глюкоза} {1 \: \ cancel {L}} \ right) = 0,155 \: моль \: глюкоза \)
B Затем мы переводим количество молей глюкозы в требуемую массу глюкозы:
\ (масса \: of \: глюкоза = 0,155 \: \ cancel {моль \: глюкоза} \ left (\ dfrac {180.16 \: g \: глюкоза} {1 \: \ cancel {моль \: глюкоза}} \ справа) = 27.9 \: г \: глюкоза \)
Упражнение \ (\ PageIndex {3} \)
Другой раствор, обычно используемый для внутривенных инъекций, – это физиологический раствор, 0,16 М раствор хлорида натрия в воде. Рассчитайте массу хлорида натрия, необходимую для приготовления 250 мл физиологического раствора.
- Ответ
2,3 г NaCl
Раствор желаемой концентрации можно также приготовить путем разбавления небольшого объема более концентрированного раствора дополнительным растворителем. Базовый раствор – это коммерчески приготовленный раствор известной концентрации, который часто используется для этой цели. Разбавление основного раствора является предпочтительным, поскольку альтернативный метод взвешивания крошечных количеств растворенного вещества трудно осуществить с высокой степенью точности. Разбавление также используется для приготовления растворов из веществ, которые продаются в виде концентрированных водных растворов, таких как сильные кислоты.
Базовый раствор – это коммерчески приготовленный раствор известной концентрации, который часто используется для этой цели. Разбавление основного раствора является предпочтительным, поскольку альтернативный метод взвешивания крошечных количеств растворенного вещества трудно осуществить с высокой степенью точности. Разбавление также используется для приготовления растворов из веществ, которые продаются в виде концентрированных водных растворов, таких как сильные кислоты.
Процедура приготовления раствора известной концентрации из исходного раствора показана на рисунке \ (\ PageIndex {3} \).Это требует расчета желаемого количества молей растворенного вещества в конечном объеме более разбавленного раствора, а затем расчета объема исходного раствора, который содержит это количество растворенного вещества. Помните, что разбавление данного количества исходного раствора растворителем не приводит к изменению , а не количества молей присутствующего растворенного вещества. Таким образом, соотношение между объемом и концентрацией основного раствора и объемом и концентрацией желаемого разбавленного раствора составляет
.
\ [(V_s) (M_s) = моль \: of \: solute = (V_d) (M_d) \ label {4.5.4} \]
, где индексы s и d указывают на исходный и разбавленный растворы, соответственно. Пример \ (\ PageIndex {4} \) демонстрирует вычисления, связанные с разбавлением концентрированного исходного раствора.
Рисунок \ (\ PageIndex {3} \): Приготовление раствора известной концентрации путем разбавления исходного раствора. (a) Объем ( V s ), содержащий желаемые моли растворенного вещества (M s ), измеряют для исходного раствора известной концентрации.(b) Отмеренный объем исходного раствора переносят во вторую мерную колбу. (c) Измеренный объем во второй колбе затем разбавляется растворителем до объемной отметки [( V s ) (M s ) = ( V d ) (M d ). ].Пример \ (\ PageIndex {4} \)
Какой объем 3,00 М исходного раствора глюкозы необходим для приготовления 2500 мл раствора D5W в Примере \ (\ PageIndex {3} \)?
Дано: Объем и молярность разбавленного раствора
Запрошено: объем основного раствора
Стратегия:
- Рассчитайте количество молей глюкозы, содержащихся в указанном объеме разбавленного раствора, умножив объем раствора на его молярность.

- Чтобы определить необходимый объем исходного раствора, разделите количество молей глюкозы на молярность исходного раствора.
Решение:
A Раствор D5W в Примере 4.5.3 содержал 0,310 М глюкозы. Начнем с использования уравнения 4.5.4 для расчета количества молей глюкозы, содержащихся в 2500 мл раствора:
\ [моль \: глюкоза = 2500 \: \ cancel {mL} \ left (\ dfrac {1 \: \ cancel {L}} {1000 \: \ cancel {mL}} \ right) \ left (\ dfrac { 0.310 \: моль \: глюкоза} {1 \: \ cancel {L}} \ right) = 0,775 \: моль \: глюкоза \]
B Теперь мы должны определить объем исходного раствора 3,00 M, который содержит это количество глюкозы:
\ [объем \: of \: stock \: soln = 0,775 \: \ cancel {mol \: gluosis} \ left (\ dfrac {1 \: L} {3 .00 \: \ cancel {mol \: глюкоза}} \ right) = 0,258 \: L \: или \: 258 \: mL \]
При определении необходимого объема исходного раствора мы должны были разделить желаемое количество молей глюкозы на концентрацию исходного раствора, чтобы получить соответствующие единицы.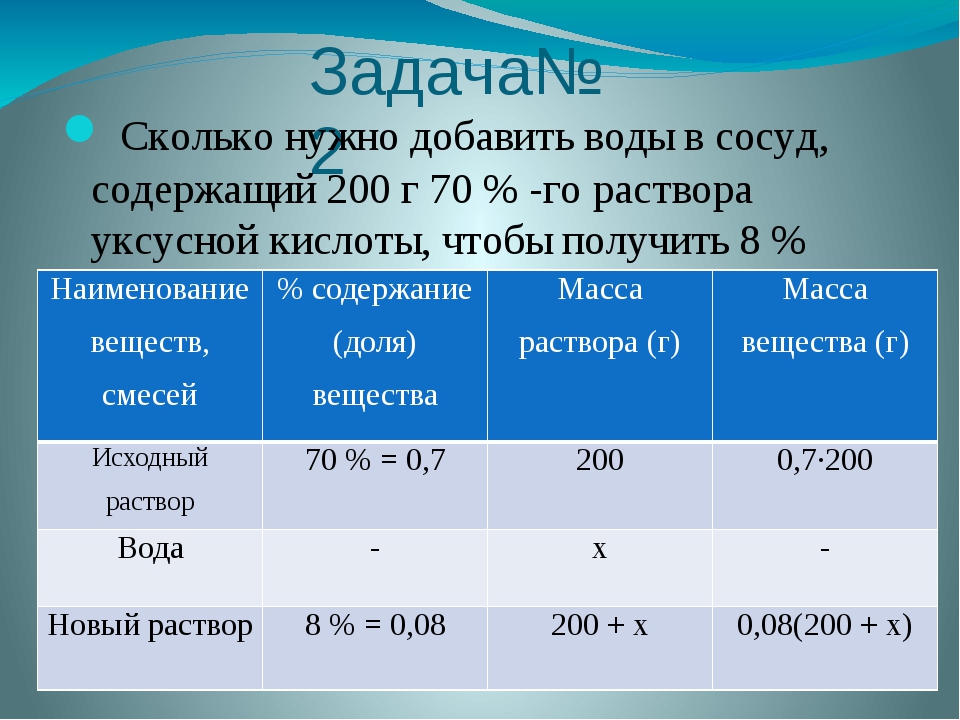 Кроме того, количество молей растворенного вещества в 258 мл исходного раствора такое же, как количество молей в 2500 мл более разбавленного раствора; изменилось только количество растворителя . Полученный нами ответ имеет смысл: разбавление основного раствора примерно в 10 раз увеличивает его объем примерно в 10 раз (258 мл → 2500 мл). Следовательно, концентрация растворенного вещества должна уменьшиться примерно в 10 раз, как это происходит (3,00 M → 0,310 M).
Кроме того, количество молей растворенного вещества в 258 мл исходного раствора такое же, как количество молей в 2500 мл более разбавленного раствора; изменилось только количество растворителя . Полученный нами ответ имеет смысл: разбавление основного раствора примерно в 10 раз увеличивает его объем примерно в 10 раз (258 мл → 2500 мл). Следовательно, концентрация растворенного вещества должна уменьшиться примерно в 10 раз, как это происходит (3,00 M → 0,310 M).
Мы также могли решить эту проблему за один шаг, решив уравнение 4.5.4 для В с и подставив соответствующие значения:
\ [V_s = \ dfrac {(V_d) (M_d)} {M_s} = \ dfrac {(2 .500 \: L) (0,310 \: \ cancel {M})} {3 .00 \: \ отменить {M}} = 0 .258 \: L \]
Как мы уже отмечали, часто существует несколько правильных способов решения проблемы.
Упражнение \ (\ PageIndex {4} \)
Какой объем 5,0 М маточного раствора NaCl необходим для приготовления 500 мл физиологического раствора (0,16 М NaCl)?
- Ответ
16 мл
Концентрации ионов в растворе
В примере \ (\ PageIndex {2} \) – концентрация раствора, содержащего 90. {2-} (водн.) \ Label {4.5.5} \]
{2-} (водн.) \ Label {4.5.5} \]
Таким образом, 1 моль единиц формулы дихромата аммония растворяется в воде с образованием 1 моля анионов Cr 2 O 7 2 – и 2 моль катионов NH 4 + (см. Рисунок \ (\ PageIndex {4} \)).
Рисунок \ (\ PageIndex {4} \): Растворение 1 моля ионного соединения. В этом случае растворение 1 моля (NH 4 ) 2 Cr 2 O 7 дает раствор, содержащий 1 моль Cr 2 O 7 2 – ионов и 2 моль NH 4 + ионов.(Молекулы воды для ясности не показаны с точки зрения молекул.) При проведении химической реакции с использованием раствора соли, например дихромата аммония, важно знать концентрацию каждого иона, присутствующего в растворе. Если раствор содержит 1,43 M (NH 4 ) 2 Cr 2 O 7 , то концентрация Cr 2 O 7 2 – также должна быть 1,43 M, поскольку один Cr 2 O 7 2 – иона на формульную единицу. Однако на формульную единицу приходится два иона NH 4 + , поэтому концентрация ионов NH 4 + составляет 2 × 1,43 М = 2,86 М. Поскольку каждая формульная единица (NH 4 ) 2 Cr 2 O 7 при растворении в воде образует трех ионов (2NH 4 + + 1Cr 2 O 7 2 – ), общая концентрация ионов в растворе составляет 3 × 1,43 M = 4.29 м.
Однако на формульную единицу приходится два иона NH 4 + , поэтому концентрация ионов NH 4 + составляет 2 × 1,43 М = 2,86 М. Поскольку каждая формульная единица (NH 4 ) 2 Cr 2 O 7 при растворении в воде образует трех ионов (2NH 4 + + 1Cr 2 O 7 2 – ), общая концентрация ионов в растворе составляет 3 × 1,43 M = 4.29 м.
Концентрация ионов в растворе из растворимой соли: https://youtu.be/qsekSJBLemc
Пример \ (\ PageIndex {5} \)
Каковы концентрации всех веществ, полученных из растворенных веществ, в этих водных растворах?
- 0,21 М NaOH
- 3,7 M (CH 3 ) 2 CHOH
- 0,032 M дюйм (NO 3 ) 3
Дано: Молярность
Запрошено: концентраций
Стратегия:
A Классифицируйте каждое соединение как сильный электролит или как неэлектролит. – (aq ) \)
– (aq ) \)
B Поскольку каждая формульная единица NaOH производит один ион Na + и один ион OH –, концентрация каждого иона такая же, как концентрация NaOH: [Na + ] = 0.21 M и [OH – ] = 0,21 M.
B Таким образом, единственным растворенным веществом в растворе является (CH 3 ) 2 молекулы CHOH, поэтому [(CH 3 ) 2 CHOH] = 3.- (водн.) \)
B Одна формульная единица In (NO 3 ) 3 производит один ион In 3 + ион и три иона NO 3 – , поэтому 0,032 M In (NO 3 ) 3 Раствор содержит 0,032 M In 3 + и 3 × 0,032 M = 0,096 M NO 3 – , то есть [In 3 + ] = 0,032 M и [NO 3 –] = 0,096 М.
Упражнение \ (\ PageIndex {5} \)
Каковы концентрации всех веществ, полученных из растворенных веществ, в этих водных растворах?
- 0.{2-}] = 0,17 \: M \)
- Ответ c
\ ([(CH_3) _2CO] = 0,50 \: M \)
Определение концентрации раствора
Определение концентрации раствора
Есть много способов измерить количество растворенного вещества, присутствующего в растворе. Каждый метод полезен для разных целей в химии, поэтому, к сожалению, мы застряли перед задачей изучить их все. Без лишних слов, вот они:
Качественные концентрации
Количество растворенного вещества, присутствующего в растворе, можно описать без цифр одним из следующих терминов:
- Ненасыщенный: «Ненасыщенный» относится к любому раствору, который все еще способен растворения большего количества растворенного вещества.
 Например, стакан холодного чая не насыщен сахаром, если вы добавили в него одну столовую ложку сахара, потому что он все еще способен растворять больше сахара. Этот термин не очень подходит для определения точного количества присутствующего растворенного вещества – например, и стакан воды, и наполненный бассейн можно было бы назвать ненасыщенными солевыми растворами, если бы в каждом из них был растворен один грамм соли.
Например, стакан холодного чая не насыщен сахаром, если вы добавили в него одну столовую ложку сахара, потому что он все еще способен растворять больше сахара. Этот термин не очень подходит для определения точного количества присутствующего растворенного вещества – например, и стакан воды, и наполненный бассейн можно было бы назвать ненасыщенными солевыми растворами, если бы в каждом из них был растворен один грамм соли. - Насыщенный: эти растворы растворили максимально возможное количество растворенного вещества. Например, если вы продолжаете добавлять сахар в стакан с Kool-Aid, он в конечном итоге перестанет растворяться и осядет на дно (маленькие дети, однако, отказываются этому верить).Этот раствор называется насыщенным.
- Перенасыщенные: это те растворы, в которых растворено больше, чем обычно максимально возможное количество растворенного вещества. Эти решения необычны и не очень стабильны. Например, добавление небольшой частицы пыли к такому раствору вызывает достаточно возмущения, что кристаллы спонтанно образуются, пока раствор не достигнет состояния насыщения.

Легко определить, является ли раствор ненасыщенным, насыщенным или перенасыщенным, добавив очень небольшое количество растворенного вещества.Если раствор ненасыщенный, растворенное вещество растворится. Если раствор будет насыщенным, этого не произойдет. Если раствор перенасыщен, вокруг добавленного вами растворенного вещества очень быстро образуются кристаллы.
Молярность (M)
Плохие реакции
При чтении определений следующих методов определения концентрации обратите особое внимание на то, запрашивает ли объемный компонент вес или объем «раствора» или вес или объем »растворителя. ” Если указан вес или объем раствора, это означает, что вас интересует количество раствора, присутствующего после добавления растворенного вещества.Если указан вес или объем растворителя, это означает, что вас интересует количество растворителя до того, как будет добавлено растворенное вещество.

Молярность, вероятно, является наиболее часто используемым способом измерения концентрации и определяется как количество молей растворенного вещества на литр раствора.
У вас проблемы
Задача 1: Какова молярность раствора объемом 3,0 литра, содержащего 120 граммов уксусной кислоты (C 2 H 3 O 2 H)?
Допустим, мы приготовили раствор, добавив воды до 40 граммов (1.0 моль) гидроксида натрия до тех пор, пока конечный объем раствора не достигнет одного литра (чтобы просмотреть расчеты молей, вернитесь к The Mole). Поскольку у нас один моль растворенного вещества в одном литре раствора, молярность равна (1 моль) / (1 литр) = 1 М. Мы называем раствор с молярностью один «одномолярным» раствором.
Моляльность (м)
Моляльность определяется как количество молей растворенного вещества на килограмм растворителя. Например, если бы мы добавили два килограмма воды к 4 молям сахара, молярность была бы равна 4 молям / 2 килограмма = 2 м («два моляля»).
 При проведении расчетов с моляльностью учтите, что, поскольку плотность воды составляет 1,0 г / мл при стандартных условиях, количество килограммов воды равно количеству литров воды.
При проведении расчетов с моляльностью учтите, что, поскольку плотность воды составляет 1,0 г / мл при стандартных условиях, количество килограммов воды равно количеству литров воды.Нормальность (N)
Нормальность раствора определяется как количество молей реакционноспособных частиц, обычно называемых «эквивалентами» на литр раствора. Использование «эквивалентов» будет зависеть от выполняемой реакции, поэтому перед вычислением нормальности необходимо некоторое знание конкретного химического процесса в реакции.По крайней мере, это «нормальный» способ решения этой проблемы. (Я не мог устоять.)
Молярная доля (?)
У вас проблемы
Задача 2: Какова мольная доля воды в растворе, полученном путем смешивания 4,5 моль изопропанола с 15,0 моль воды?
Мольная доля определяется как количество молей одного компонента в растворе, деленное на общее количество молей всех компонентов в смеси.
 В форме уравнения мы можем выразить мольную долю одного компонента в растворе как:
В форме уравнения мы можем выразить мольную долю одного компонента в растворе как:- ? A = моль A ? моль A + моль B + моль C +?
где A относится к первому компоненту, B относится ко второму компоненту, а C относится к третьему компоненту.Как знак “?” указывает, что этот расчет может быть расширен, чтобы включить любое количество компонентов в смеси.
частей на миллион (ppm) и частей на миллиард (ppb)
Как части на миллион, так и части на миллиард являются единицами концентрации, наиболее часто используемыми в анализе окружающей среды. Поскольку в качестве растворителя чаще всего используется вода, концентрацию раствора в миллионных долях можно определить, разделив количество мг (0,001 г) растворенного вещества на количество литров воды. Частей на миллиард можно определить, разделив количество мкг (10 -6 г) растворенного вещества на количество литров воды.
Краткое описание единиц концентрации
Следующая таблица включает все единицы концентрации, упомянутые в этом разделе, а также способы их определения.

Единица Символ Как это измеряется молярность M моль растворенного вещества / литры раствора моляльность м моль растворенного вещества / кг раствора 9094 нормальность N «эквиваленты», которые варьируются в зависимости от проводимой реакции мольная доля ? моль А ? моль A + моль B +? частей на миллион частей на миллион мг растворенного вещества / л воды частей на миллиард частей на миллиард мкг растворенного вещества / л воды Выдержка из The Complete Guide to Idi Chemistry 2003 Ян Гуч.Все права защищены, включая право на полное или частичное воспроизведение в любой форме. Используется по договоренности с Alpha Books , членом Penguin Group (USA) Inc.

Чтобы заказать эту книгу непосредственно у издателя, посетите веб-сайт Penguin USA или позвоните по телефону 1-800-253-6476. Вы также можете приобрести эту книгу на Amazon.com и Barnes & Noble.
Разведений и концентраций – Вводная химия – 1-е канадское издание
Цель обучения
1.Узнайте, как разбавлять и концентрировать растворы.
Часто рабочему необходимо изменить концентрацию раствора, изменив количество растворителя. Разбавление – это добавление растворителя, которое снижает концентрацию растворенного вещества в растворе. Концентрация – это удаление растворителя, которое увеличивает концентрацию растворенного вещества в растворе. (Не путайте здесь два значения слова , концентрация !)
И при разбавлении, и при концентрации количество растворенного вещества остается неизменным.Это дает нам возможность рассчитать, каким должен быть новый объем раствора для желаемой концентрации растворенного вещества. Из определения молярности,
молярность = моль растворенного вещества / литр раствора
мы можем найти количество молей растворенного вещества:
моль растворенного вещества = (молярность) (литры раствора)
Более простой способ записать это – использовать M для представления молярности и V для представления объема.
 Таким образом, уравнение становится
Таким образом, уравнение становитсямоль растворенного вещества = MV
Поскольку это количество не меняется до и после изменения концентрации, продукт MV должен быть одинаковым до и после изменения концентрации.Используя числа для представления начальных и конечных условий, мы получаем
M 1 V 1 = M 2 V 2
как уравнение разбавления. Объемы должны быть выражены в одинаковых единицах. Обратите внимание, что это уравнение дает только начальные и конечные условия, а не величину изменения. Сумма изменения определяется вычитанием.
Пример 9
Если 25,0 мл 2.19 М раствор разбавляют до 72,8 мл, какова конечная концентрация?
Решение
Не имеет значения, какой набор условий помечен как 1 или 2, если условия правильно спарены вместе. Используя уравнение разбавления, получаем
(2,19 M) (25,0 мл) = M 2 (72,8 мл)
Решение для второй концентрации (с учетом того, что единицы миллилитры отменяют),
M 2 = 0,752 M
Концентрация раствора уменьшилась.
 При переходе от 25,0 мл до 72,8 мл необходимо добавить 72,8–25,0 = 47,8 мл растворителя.
При переходе от 25,0 мл до 72,8 мл необходимо добавить 72,8–25,0 = 47,8 мл растворителя.Проверьте себя
В 0,885 М раствор KBr, начальный объем которого составляет 76,5 мл, добавляют еще воды до тех пор, пока его концентрация не станет 0,500 М. Каков новый объем раствора?
Ответ
135,4 мл
Концентрирование растворов включает удаление растворителя. Обычно это делается путем испарения или кипячения, предполагая, что теплота кипения не влияет на растворенное вещество.Уравнение разбавления также используется в этих случаях.
Химия везде: подготовка растворов для внутривенного введения
В отделении неотложной помощи больницы врач назначает внутривенное введение 100 мл 0,5% KCl пациенту, страдающему гипокалиемией (низким уровнем калия). Бежит ли помощник к шкафу с припасами и вынимает ли ему пакет для внутривенного вливания с такой концентрацией KCl?
Вряд ли. Более вероятно, что помощник должен приготовить подходящий раствор из пакета для внутривенного вливания стерильного раствора и более концентрированного стерильного раствора, называемого маточным раствором , KCl.
Медицинский персонал обычно должен выполнять разведения для внутривенных растворов. Источник: «Infuuszakjes» Хармида находится в открытом доступе.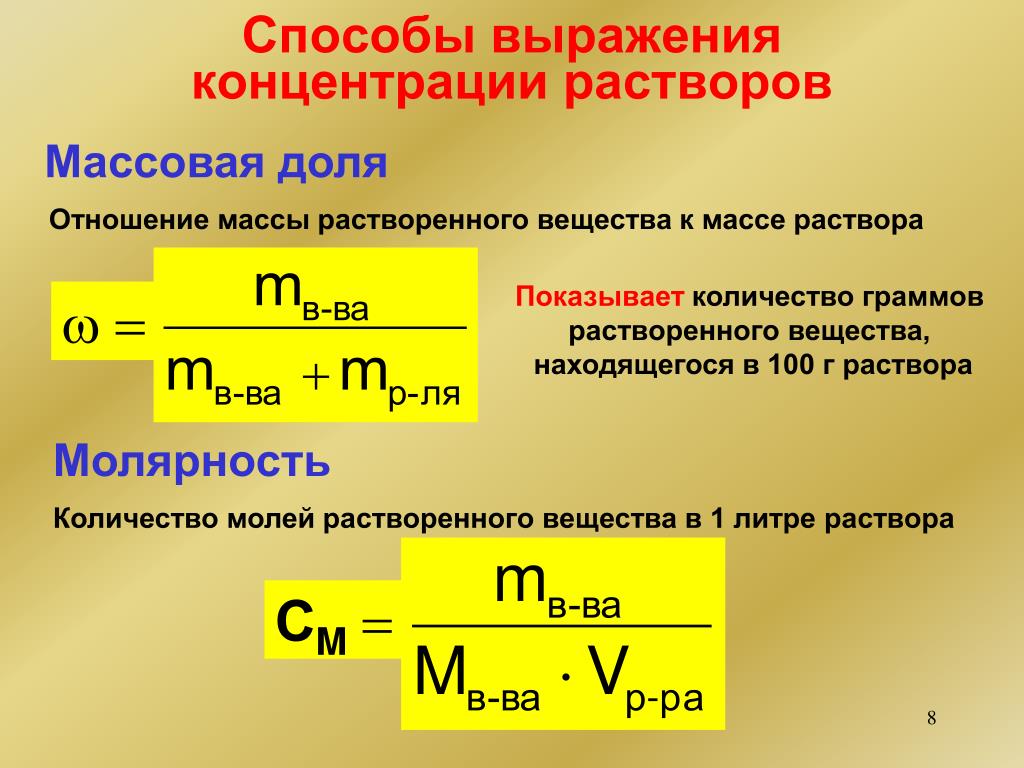 Ожидается, что помощник с помощью шприца наберет немного исходного раствора, введет его в ожидающий пакет для внутривенных вливаний и разбавит до нужной концентрации. Таким образом, помощник должен выполнить расчет разбавления.
Ожидается, что помощник с помощью шприца наберет немного исходного раствора, введет его в ожидающий пакет для внутривенных вливаний и разбавит до нужной концентрации. Таким образом, помощник должен выполнить расчет разбавления.Если исходный раствор содержит 10,0% KCl, а конечный объем и концентрация должны составлять 100 мл и 0,50%, соответственно, то определить количество используемого основного раствора несложно:
(10%) В 1 = (0.50%) (100 мл)
V 1 = 5 млКонечно, добавление основного раствора влияет на общий объем разбавленного раствора, но конечная концентрация, вероятно, достаточно близка даже для медицинских целей.
Медицинский и фармацевтический персонал постоянно работает с дозировками, требующими измерения концентрации и разведения. Это важная ответственность: неправильный расчет дозы может быть бесполезным, вредным или даже фатальным!
Основные выводы
- Рассчитайте новую концентрацию или объем для разведения или концентрации раствора.

Упражнения
В чем разница между разбавлением и концентрацией?
Какое количество остается постоянным при разбавлении раствора?
1,88 М раствор NaCl имеет начальный объем 34,5 мл. Какова конечная концентрация раствора, если его развести до 134 мл?
0,664 М раствор NaCl имеет начальный объем 2,55 л. Какова конечная концентрация раствора, если его разбавить до 3?88 л?
Если необходимо разбавить 1,00 мл 2,25 M раствора H 2 SO 4 до 1,00 M, каков будет его конечный объем?
Если 12,00 л 6,00 М раствора HNO 3 необходимо разбавить до 0,750 М, каков будет его окончательный объем?
Если 665 мл 0,875 M раствора KBr осторожно кипятить для концентрирования растворенного вещества до 1,45 M, каков будет его конечный объем?
Если 1.00 л раствора LiOH доводится до 164 мл, и его начальная концентрация составляет 0,00555 М, какова его конечная концентрация?
Сколько воды необходимо добавить к 75,0 мл 0,332 М FeCl 3 (водн.
 ), Чтобы снизить его концентрацию до 0,250 М?
), Чтобы снизить его концентрацию до 0,250 М?Сколько воды необходимо добавить к 1,55 л 1,65 M Sc (NO 3 ) 3 (водный), чтобы снизить его концентрацию до 1,00 M?
ответы
1.
Разбавление – это уменьшение концентрации раствора, тогда как концентрация – это увеличение концентрации раствора.
3.
0,484 M
5.
2,25 мл
7.
401 мл
9.
24,6 мл
Концентрация и единицы – AP Chemistry
Если вы считаете, что контент, доступный через Веб-сайт (как определено в наших Условиях обслуживания), нарушает или другие ваши авторские права, сообщите нам, отправив письменное уведомление («Уведомление о нарушении»), содержащее в информацию, описанную ниже, назначенному ниже агенту.
 Если репетиторы университета предпримут действия в ответ на
ан
Уведомление о нарушении, оно предпримет добросовестную попытку связаться со стороной, которая предоставила такой контент
средствами самого последнего адреса электронной почты, если таковой имеется, предоставленного такой стороной Varsity Tutors.
Если репетиторы университета предпримут действия в ответ на
ан
Уведомление о нарушении, оно предпримет добросовестную попытку связаться со стороной, которая предоставила такой контент
средствами самого последнего адреса электронной почты, если таковой имеется, предоставленного такой стороной Varsity Tutors.Ваше Уведомление о нарушении прав может быть отправлено стороне, предоставившей доступ к контенту, или третьим лицам, таким как в качестве ChillingEffects.org.
Обратите внимание, что вы будете нести ответственность за ущерб (включая расходы и гонорары адвокатам), если вы существенно искажать информацию о том, что продукт или действие нарушает ваши авторские права.Таким образом, если вы не уверены, что контент находится на Веб-сайте или по ссылке с него нарушает ваши авторские права, вам следует сначала обратиться к юристу.
Чтобы отправить уведомление, выполните следующие действия:
Вы должны включить следующее:
Физическая или электронная подпись правообладателя или лица, уполномоченного действовать от их имени; Идентификация авторских прав, которые, как утверждается, были нарушены; Описание характера и точного местонахождения контента, который, по вашему мнению, нарушает ваши авторские права, в \ достаточно подробностей, чтобы позволить репетиторам университетских школ найти и точно идентифицировать этот контент; например нам требуется а ссылка на конкретный вопрос (а не только на название вопроса), который содержит содержание и описание к какой конкретной части вопроса – изображению, ссылке, тексту и т.
 д. – относится ваша жалоба;
Ваше имя, адрес, номер телефона и адрес электронной почты; а также
Ваше заявление: (а) вы добросовестно считаете, что использование контента, который, по вашему мнению, нарушает
ваши авторские права не разрешены законом, владельцем авторских прав или его агентом; (б) что все
информация, содержащаяся в вашем Уведомлении о нарушении, является точной, и (c) под страхом наказания за лжесвидетельство, что вы
либо владелец авторских прав, либо лицо, уполномоченное действовать от их имени.
д. – относится ваша жалоба;
Ваше имя, адрес, номер телефона и адрес электронной почты; а также
Ваше заявление: (а) вы добросовестно считаете, что использование контента, который, по вашему мнению, нарушает
ваши авторские права не разрешены законом, владельцем авторских прав или его агентом; (б) что все
информация, содержащаяся в вашем Уведомлении о нарушении, является точной, и (c) под страхом наказания за лжесвидетельство, что вы
либо владелец авторских прав, либо лицо, уполномоченное действовать от их имени.Отправьте жалобу нашему уполномоченному агенту по адресу:
Чарльз Кон Varsity Tutors LLC
101 S. Hanley Rd, Suite 300
St. Louis, MO 63105Или заполните форму ниже:
Концентрация раствора – определение, методы, формулы и расчет
Все говорят о концентрации растворов. Также они могут говорить о концентрации кофе или чая.
 У каждого свое мнение о том, что подразумевается под концентрацией раствора. Вы, должно быть, заметили, что всякий раз, когда вы делаете кофе, если вы добавляете много порошка, вы получаете концентрированный напиток, тогда как если вы добавляете мало, получается разбавленный раствор. Поэтому важно понимать, какова концентрация раствора. В этой главе мы узнаем, что подразумевается под концентрацией раствора; мы также увидим, как найти концентрацию раствора и различные методы выражения концентрации раствора.
У каждого свое мнение о том, что подразумевается под концентрацией раствора. Вы, должно быть, заметили, что всякий раз, когда вы делаете кофе, если вы добавляете много порошка, вы получаете концентрированный напиток, тогда как если вы добавляете мало, получается разбавленный раствор. Поэтому важно понимать, какова концентрация раствора. В этой главе мы узнаем, что подразумевается под концентрацией раствора; мы также увидим, как найти концентрацию раствора и различные методы выражения концентрации раствора.Что означает концентрация раствора
В водном растворе существуют две части, а именно растворенное вещество и растворитель. Это два основных термина концентрации раствора, которые вам необходимо знать. Нам всегда нужно учитывать количество растворенного вещества в растворе. Количество растворенного вещества в растворителе – это то, что называется концентрацией раствора. В химии мы определяем концентрацию раствора как количество растворенного вещества в растворителе.
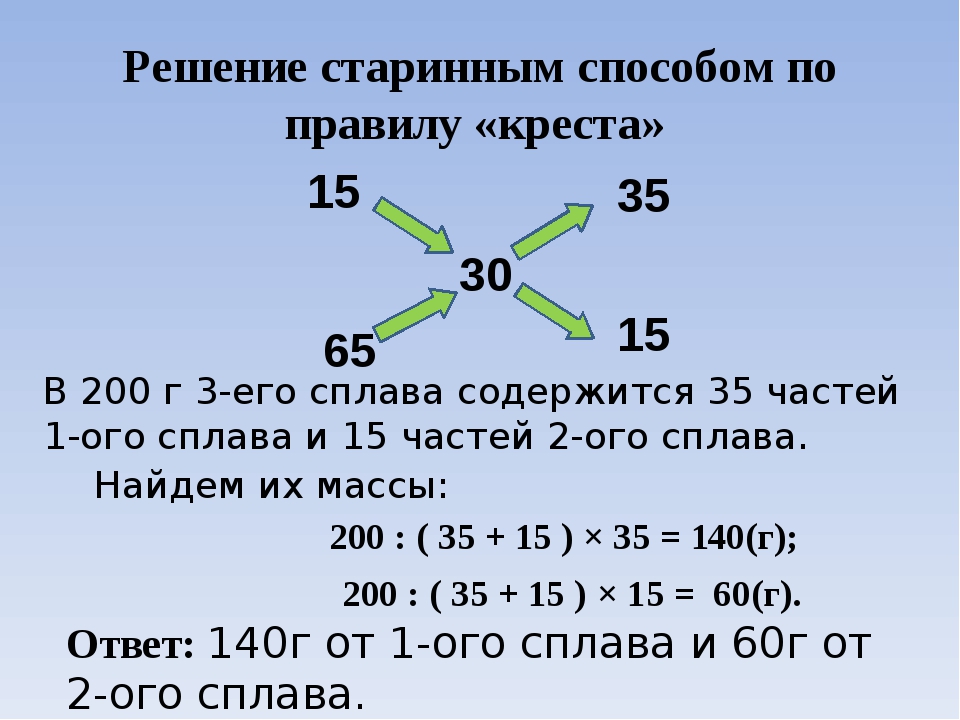 Когда в растворе содержится больше растворенного вещества, мы называем его концентрированным раствором.Если в растворе больше растворителя, мы называем его разбавленным. Теперь, когда вы понимаете, что такое концентрация раствора, давайте перейдем к различным методам выражения концентрации.
Когда в растворе содержится больше растворенного вещества, мы называем его концентрированным раствором.Если в растворе больше растворителя, мы называем его разбавленным. Теперь, когда вы понимаете, что такое концентрация раствора, давайте перейдем к различным методам выражения концентрации.(изображение будет загружено в ближайшее время)
На изображении показан раствор от наиболее разбавленного до наиболее концентрированного.
Как определить концентрацию раствора различными методами
Существуют различные методы выражения концентрации раствора.Обычно вы видите, как химики работают с количеством родинок. Фармацевты будут использовать процентные концентрации вместо количества молей. Следовательно, важно понимать все методы выражения концентрации растворов.
Формула концентрации раствора имеет следующий вид.
Cor S = \ [\ frac {\ text {Вес растворенного вещества в граммах}} {\ text {Объем в литрах}} \]
Мы также увидим другие методы расчета концентрации раствора на основе различные методы выражения концентраций.
 {6} \]
{6} \]Массовый процент (мас. / Мас.)
Выражается в виде массового процента растворенного вещества в растворе. Формула для массового процента дается следующим образом.
Массовый процент A = \ [\ frac {\ text {Масса компонента A}} {\ text {Общая масса раствора}} \ times 100 \]
например Ch4COOH 33% по массе и H 2 SO 4 98,0% по массе.
Объемный процент (об. / Об.)
Выражается в объемных процентах растворенного вещества по отношению к растворителю. Формула для процентного объема приведена ниже.
Объемный процент A = \ [\ frac {\ text {Объем компонента A}} {\ text {Общий объем раствора}} \ times 100 \]
Массовый объем в процентах (мас. / Об.)
Процент Вес в объеме выражает количество граммов растворенного вещества в 100 мл продукта.
например Раствор BaCl2 10% мас. / Об. И раствор h3O2 5-7% мас.
 / Об.
/ Об.Молярность (M)
Это количество молей растворенного вещества, содержащегося в 1000 мл раствора. Это широко используемый метод выражения концентраций.
Моляльность (м)
Моляльность выражается как количество молей растворенного вещества, содержащегося в 1000 г растворителя. Формула моляльности дается следующим образом.
Моляльность (м) = \ [\ frac {\ text {Масса растворенного вещества}} {\ text {Масса растворителя в кг}} \]
Нормальность (N)
Мы можем определить это как количество эквивалентов растворенного вещества, присутствующего в растворе, и это также называется эквивалентной концентрацией. Формула нормальности дается следующим образом.
Нормальность (N) = \ [\ frac {\ text {Вес растворенного вещества в граммах}} {\ text {Эквивалентная масса \ раз Объем в литрах}} \]
Теперь, когда вы знаете, как найти концентрацию раствора с использованием различных концентраций рецептур раствора, мы постараемся решить некоторые вопросы концентрации раствора.

Решенные проблемы
Вопрос 1) 2 мл воды добавляют к 4 г порошкообразного лекарства. Окончательный объем – 3 мл. Найти массовую долю раствора в процентах по объему?
Ответ 1) Дано, Масса растворенного вещества = 4 г
Объем раствора = 3 мл
Масса в процентах от объема = \ [\ frac {\ text {Масса растворенного вещества}} {\ text {Объем раствора}} \ раз 100% \]
= \ [\ frac {4g} {3ml} \ times 100% \]
= 133%
Следовательно, массовая доля в процентах составляет 133%.
Вопрос 2) Многие люди используют раствор Na3PO4 для очистки стен перед оклейкой обоев. Рекомендуемая концентрация 1,7% (м / об). Найти массу Na3PO4, необходимую для приготовления 2,0 л раствора?
Ответ 2) Дано, масса / объем в процентах = 1,7%
Объем раствора = 2000 мл
Масса в процентах по объему = \ [\ frac {\ text {Масса растворенного вещества}} {\ text {Объем раствора}} \ times 100% \]
1,7% = \ [\ frac {\ text {Масса растворенного вещества}} {2000 мл} \ times 100% \]
Масса растворенного вещества = 34 г
Следовательно, требуемая масса равна 34г.

Разведений и концентраций – Вводная химия – 1-е канадское издание
- Узнайте, как разбавлять и концентрировать растворы.
Часто рабочему необходимо изменить концентрацию раствора, изменив количество растворителя. Разбавление – это добавка растворителя, которая снижает концентрацию растворенного вещества в растворе. Концентрация – это удаление растворителя, которое увеличивает концентрацию растворенного вещества в растворе.(Не путайте здесь два значения слова , концентрация !)
И при разбавлении, и при концентрации количество растворенного вещества остается неизменным. Это дает нам возможность рассчитать, каким должен быть новый объем раствора для желаемой концентрации растворенного вещества. Из определения молярности:
мы можем найти количество молей растворенного вещества:
Более простой способ записать это – использовать M для представления молярности и V для представления объема.
 Таким образом, уравнение принимает следующий вид:
Таким образом, уравнение принимает следующий вид:Поскольку это количество не меняется до и после изменения концентрации, продукт MV должен быть одинаковым до и после изменения концентрации. Используя числа для представления начальных и конечных условий, мы имеем:
как уравнение разбавления . Объемы должны быть выражены в одинаковых единицах. Обратите внимание, что это уравнение дает только начальные и конечные условия, а не величину изменения.Сумма изменения определяется вычитанием.
Если 25,0 мл 2,19 М раствора разбавить до 72,8 мл, какова конечная концентрация?
Решение
Не имеет значения, какой набор условий помечен как 1 или 2, если условия правильно спарены вместе. Используя уравнение разбавления, мы имеем:Решение для второй концентрации (с учетом отмены миллилитров):
Концентрация раствора уменьшилась.При переходе от 25,0 мл до 72,8 мл необходимо добавить 72,8–25,0 = 47,8 мл растворителя.

Проверьте себя
В 0,885 М раствор KBr, начальный объем которого составляет 76,5 мл, добавляют еще воды до тех пор, пока его концентрация не станет 0,500 М. Каков новый объем раствора?Ответ
135,4 млКонцентрирование растворов включает удаление растворителя. Обычно это делается путем испарения или кипячения, предполагая, что теплота кипения не влияет на растворенное вещество.Уравнение разбавления также используется в этих случаях.
В отделении неотложной помощи больницы врач назначает внутривенное введение 100 мл 0,5% KCl пациенту, страдающему гипокалиемией (низким уровнем калия). Бежит ли помощник к шкафу с припасами и вынимает ли ему пакет для внутривенного вливания с такой концентрацией KCl?
Вряд ли. Более вероятно, что помощник должен приготовить подходящий раствор из пакета для внутривенного вливания стерильного раствора и более концентрированного стерильного раствора, называемого маточным раствором , KCl.
Медицинский персонал обычно должен выполнять разведения для внутривенных растворов. Ожидается, что помощник с помощью шприца наберет немного исходного раствора, введет его в ожидающий пакет для внутривенных вливаний и разбавит до нужной концентрации. Таким образом, помощник должен выполнить расчет разбавления.
Ожидается, что помощник с помощью шприца наберет немного исходного раствора, введет его в ожидающий пакет для внутривенных вливаний и разбавит до нужной концентрации. Таким образом, помощник должен выполнить расчет разбавления.Если исходный раствор содержит 10,0% KCl, а конечный объем и концентрация должны составлять 100 мл и 0,50%, соответственно, то определить количество используемого основного раствора несложно:
Конечно, добавление основного раствора влияет на общий объем разбавленного раствора, но конечная концентрация, вероятно, достаточно близка даже для медицинских целей.
Медицинский и фармацевтический персонал постоянно работает с дозировками, требующими измерения концентрации и разведения. Это важная ответственность: неправильный расчет дозы может быть бесполезным, вредным или даже фатальным!
- Рассчитайте новую концентрацию или объем для разведения или концентрации раствора.

- В чем разница между разбавлением и концентрацией?
- Какое количество остается постоянным при разбавлении раствора?
- А 1.88 М раствор NaCl имеет начальный объем 34,5 мл. Какова конечная концентрация раствора, если его развести до 134 мл?
- 0,664 М раствор NaCl имеет начальный объем 2,55 л. Какова конечная концентрация раствора, если его разбавить до 3,88 л?
- Если необходимо разбавить 1,00 мл 2,25 M раствора H 2 SO 4 до 1,00 M, каков будет его конечный объем?
- Если необходимо развести 12,00 л 6,00 М раствора HNO 3 до 0.750 M, каков будет его окончательный объем?
- Если 665 мл 0,875 M раствора KBr осторожно кипятить для концентрирования растворенного вещества до 1,45 M, каков будет его конечный объем?
- Если 1,00 л раствора LiOH довести до 164 мл и его начальная концентрация составляет 0,00555 М, какова его конечная концентрация?
- Сколько воды необходимо добавить к 75,0 мл 0,332 М FeCl 3 (водн.
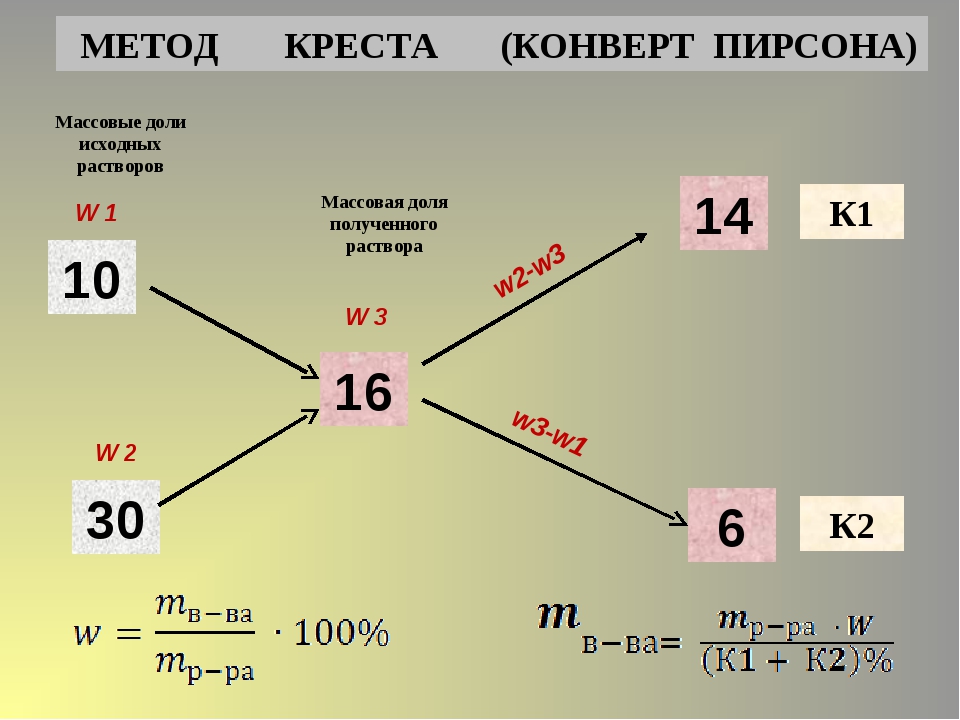 ), Чтобы снизить его концентрацию до 0,250 М?
), Чтобы снизить его концентрацию до 0,250 М? - Сколько воды нужно добавить в 1,55 л 1.65 M Sc (NO 3 ) 3 (водн.), Чтобы снизить его концентрацию до 1,00 M?
- Разбавление – это уменьшение концентрации раствора, тогда как концентрация – это увеличение концентрации раствора.
- 0,484 M
- 2,25 мл
- 401 мл
- 24,6 мл
Авторство в СМИ
Практическое применение: расчет концентраций раствора
Пример задачи №1: Молярность
Рассчитайте молярность раствора двух литров воды, смешанного с 30 граммами хлорида натрия (NaCl).
Чтобы рассчитать молярность, мы сначала должны вспомнить, что молярность равна молям растворенного вещества на литр раствора.
Шаг 1. Рассчитайте литры
Во-первых, убедитесь, что у вас есть объем раствора в литрах. Эта задача дает вам количество в литрах, но если вам даны миллилитры или галлоны, вы должны сначала преобразовать.

Шаг 2: Расчет молей
Затем рассчитайте количество молей в растворе. Для этого вы должны найти молярную массу вашего соединения.Найдите ближайшую к вам периодическую таблицу, а затем определите молярную массу каждого элемента в составе. Для хлорида натрия мы складываем молярную массу натрия (22 г / моль) с молярной массой хлорида (35 г / моль), чтобы получить общую молярную массу 57 г / моль.
Затем настройте преобразование, чтобы узнать, сколько молей содержится в общей массе растворенного вещества. Переверните вашу молярную массу вверх дном, чтобы у вас была доля в 1 моль над массой в граммах. Затем умножьте это на общее количество граммов.
Для нашего примера получаем:
30 г NaCl x (1 моль / 57 г) = 0.52 моль NaCl
Шаг 3: Расчет молярности
Теперь вы можете просто разделить количество молей на литры раствора и получить молярность.
0,52 моль NaCl / 2 л воды = 0,26 M
Примеры Задача № 2: мольная доля
Рассчитайте мольную долю раствора двух литров воды, смешанного с 30 г хлорида натрия.
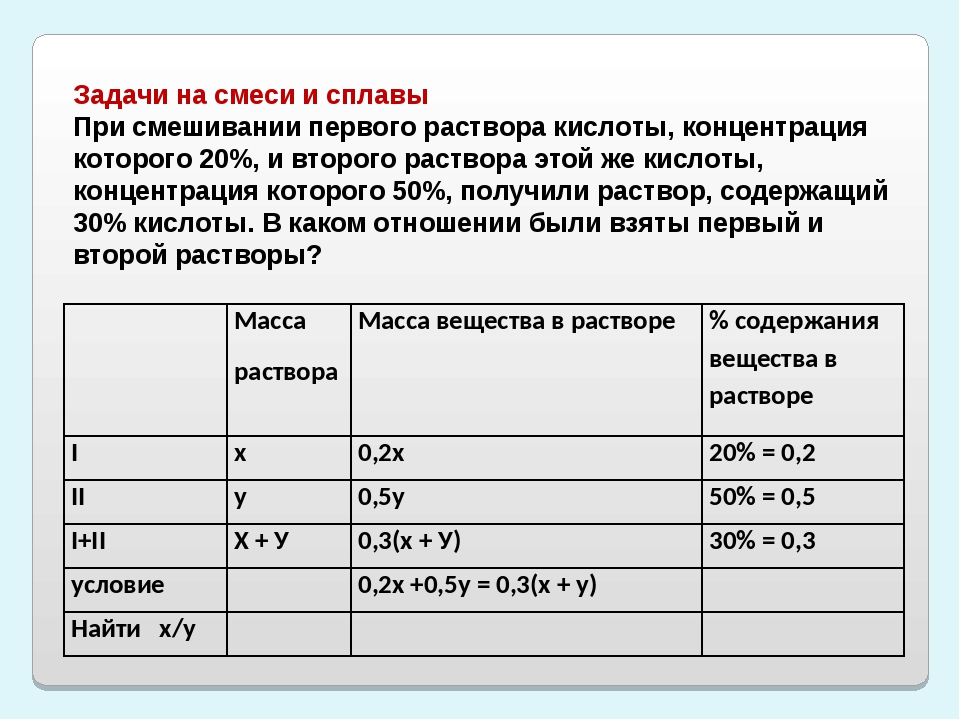
Другой способ расчета концентрации – мольная доля. Здесь мы вычисляем отношение молей растворенного вещества к молям всего раствора.
Шаг 1. Рассчитайте количество молей каждого вещества
Сначала рассчитайте количество молей каждого вещества в растворе. Здесь мы сделаем это так же, как и при вычислении молярности, используя молярные массы натрия и хлорида. Молярная масса 30 г хлорида натрия составляет 57 г / моль, что дает 0,52 моль хлорида натрия.
Аналогично, для воды можно использовать таблицу Менделеева, чтобы найти молярную массу (18 г / моль). Затем мы можем использовать плотность воды, чтобы найти массу из заданного объема, которая составляет 1 г / мл.Итак, у нас есть 2000 г воды. Используя нашу формулу для расчета молей, мы получаем:
2,000 г воды / (1 моль / 18 г) = 111,1 моль воды
Шаг 2: сложите моли
Затем сложите все моли, чтобы получить общее количество молей. В нашем примере 0,52 моль NaCl + 111,1 моль воды = 111,62 моль всего.

Шаг 3: Разделите
Теперь разделите моли растворенного вещества на общее количество молей в растворе, чтобы получить мольную долю.
0,52 моль NaCl / 111,62 моль всего = 0.004
Пример проблемы № 3: Молярность
Моляльность может звучать очень похоже на молярность, но на самом деле это другое. Моляльность – это количество молей растворенного вещества, деленное на массу растворителя в килограммах. Рассчитаем моляльность для этого примера.
Шаг 1: Рассчитайте моль растворенного вещества
Снова используйте молярную массу, а затем преобразуйте массу, указанную в задаче, в моль. В нашем примере у нас есть 0,52 моль хлорида натрия.
Шаг 2: Рассчитайте килограммы растворителя
Опять же, мы можем преобразовать объем воды в массу, используя плотность воды 1 г / мл.Поскольку у нас есть 2000 мл воды, это равно 2000 г воды или 2 кг.
Шаг 3. Разделите
Теперь разделите количество молей растворенного вещества на килограммы растворителя.
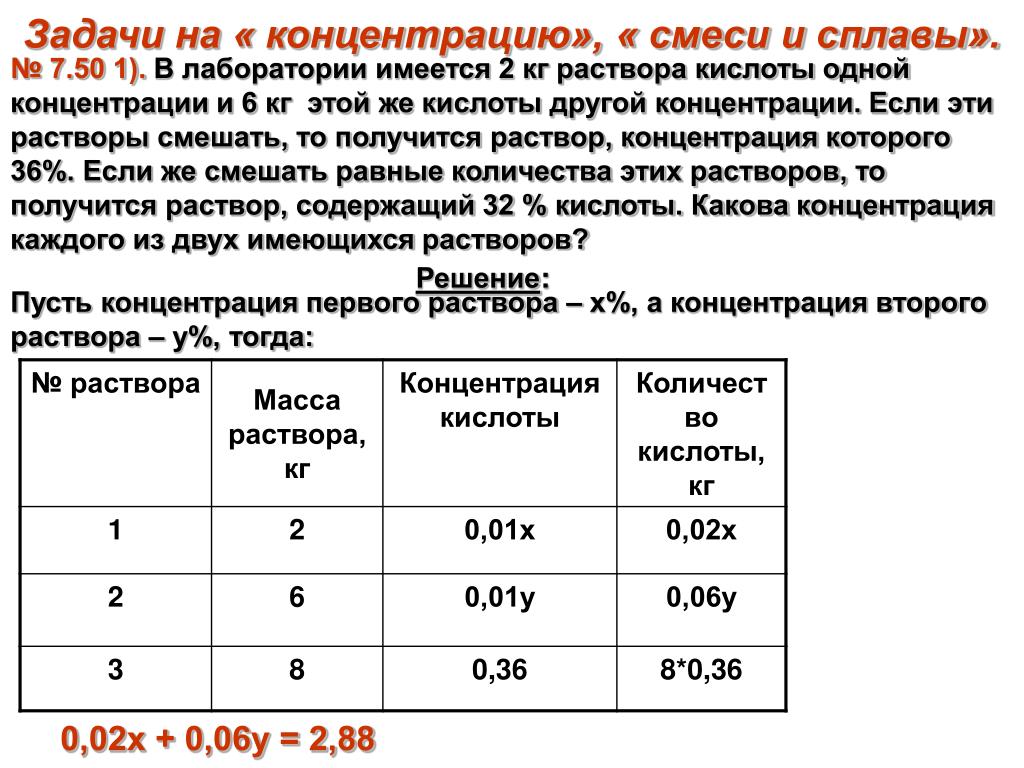 В нашем примере мы получаем:
В нашем примере мы получаем:0,52 моль NaCl / 2 кг воды = 0,26 м
Пример задачи № 4: массовый процент
Теперь давайте рассчитаем массовый процент 30 г NaCl в 2 л воды. Массовый процент – это масса растворенного вещества, деленная на массу раствора.
Шаг 1: Рассчитайте массу растворенного вещества
Поскольку эта задача уже сообщает вам массу NaCl, вам не нужно выполнять вычисления.Но если проблема дала вам родинки, вы можете работать в обратном направлении, используя молярную массу, как объяснено в первом примере задачи.
Шаг 2: Рассчитайте массу раствора
Теперь мы будем использовать плотность воды для вычисления ее массы, как мы делали в предыдущих задачах. Плотность воды составляет 1 г / мл, поэтому для 2 л воды или 2000 мл воды плотность составляет 2000 г. Чтобы получить массу раствора, сложите массу растворителя и растворенного вещества. В нашем примере это 2000 г воды + 30 г NaCl = всего 2030 г.
Шаг 3. Разделите
Теперь разделите массу растворенного вещества на массу раствора. Здесь мы получаем 30 г NaCl / 2030 г всего = 0,014 или 1,4%.
Пример задачи № 5: Объемный процент
Объемный процент используется, когда и растворенное вещество, и растворитель являются жидкостями. Допустим, вы хотите растворить 35 мл этанола в 1000 мл воды. Чтобы решить эту проблему, просто разделите объем растворенного вещества (этанола) на объем раствора.
В нашем примере мы объединили 35 мл этанола с 1000 мл воды, поэтому общий объем раствора составляет 1035 мл.
Итак, 35 мл / 1035 мл = 0,034 или 3,4% этанола по объему.
Краткое содержание урока
Растворы представляют собой гомогенные смеси, состоящие из растворенных веществ , растворенных в растворителях . Отношение растворенного вещества к растворителю составляет , концентрация и может быть рассчитана несколькими способами. Молярность – моль на литр растворителя.







 Что называют процентной концентрацией раствора и чем ее можно выразить?
Что называют процентной концентрацией раствора и чем ее можно выразить?