Строение атома, 11 класс – презентация онлайн
Похожие презентации:
Сложные эфиры. Жиры
Физические, химические свойства предельных и непредельных карбоновых кислот, получение
Газовая хроматография
Хроматографические методы анализа
Искусственные алмазы
Титриметрические методы анализа
Биохимия гормонов
Антисептики и дезинфицирующие средства. (Лекция 6)
Клиническая фармакология антибактериальных препаратов
Биохимия соединительной ткани
Строение атома
Химия, 11 класс
Домашнее задание: профильный
учебник, параграфы 1 и 2, вспомнить,
как записывать схему строения атома,
электронную и графическую формулу.
Атом –
Химический элемент –
Доказательства сложности строения атома:
– Открытие рентгеновских лучей
– Открытие радиоактивности
– Открытие «катодных лучей» (электронов)
– Изучение явления радиоактивности
Модели строения атома
• Пудинг с изюмом (1902-04 гг) Кельвин,
Томсон)
• Модель Бора-Зоммерфельда (1913 г)
• Квантово-механическая модель,
опирающаяся на протонно-нейтронную
теорию ядра (совр.
 ) Шредингер,
) Шредингер,Гейзенберг, Бор и др.
Модель Резерфорда
Схема строения атома
Современные представления о делимости нуклонов
Основные
характеристики протонов, нейтронов и электронов
Среднее значение относительной атомной
массы с учетом распространенности изотопов
Обратите внимание! При решении задач ЕГЭ среднее значение
относительной атомной массы всех атомов, кроме хлора, округляется до
целого по правилам математики. Среднее значение относительной
атомной массы атома хлора в ЕГЭ принято считать равным 35,5.
Периодической таблице –
Массовое число –
Номер периода –
Номер группы для элементов главных и побочных
подгрупп Для чего можно использовать эти данные?
Составим схему строения атома одного из элементов малых
периодов, например, серы.
Чего следует ожидать при изменении
числа элементарных частиц в атоме?
Изменение числа протонов- появление нового элемента.
Изменение числа нейтронов – появление изотопов одного и того
же элемента.
Изменение числа электронов – образование положительных или
Нуклиды
Массовое число
одинаковое, заряд и
число нейтронов
различны
изобары
заряд одинаков,
массовое число и
число нейтронов
различны
изотопы
число нейтронов
одинаковое, заряд и
массовое число
различны
изотоны
Изотопы водорода
Попробуйте ответить на вопросы:
1. У изотопов одного элемента массовое число одинаковое
или разное?
2. У изотопов одного элемента число протонов одинаковое
или разное?
1. У изотопов одного химического элемента массовое
число всегда разное, т.к. массовое число складывается
из числа протонов и нейтронов. А у изотопов
2. У изотопов одного элемента число протонов всегда
одинаковое, т.к. число протонов характеризует
химический элемент.
3. Определите количество нейтронов, протонов и
электронов в изотопе брома-81.
4. Определите число нейтронов в изотопе хлора-37.
3. Массовое число изотопа брома-81 равно 81.
Атомный номер = заряд ядра брома = число протонов в
ядре = 35. Вычитаем из массового числа число
протонов, получаем 81-35=46 нейтронов.
4. Массовое число изотопа хлора равно 37. Атомный
номер, заряд ядра и число протонов в ядре равно 17.
Электронное облако –
Электронная орбиталь –
Формы электронных орбиталей –
Варианты расположения орбиталей в пространстве
Сводная таблица
Принцип минимума энергии. Электроны заполняют сначала
орбитали с наименьшей энергией. Энергия атомной орбитали
эквивалентна сумме главного и орбитального квантовых
чисел: n + l. Если сумма одинаковая, то заполняется первой та
орбиталь, у которой меньше главное квантовое число n.
Энергетическая диаграмма атома углерода
Электронная формула
С +6
1s22s22p2
Электронные формулы элементов первых четырех
периодов
H +1
1s1
1s
He +2
1s2
1s
1s22s1
1s
2s
Be +4
1s22s2
1s
2s
B +5
1s22s22p1 1s
2s
C +6
1s22s22p2 1s
2s
2p
2p
Ne +10
1s22s22p6
1s
2s
Na+11 1s22s22p63s1 1s
2p
2s
2p
3s
У неона завершено заполнение второго
энергетического уровня.
У натрия начинается заполнение третьего
энергетического уровня.
От натрия до аргона заполнение 3-го уровня
происходит в том же порядке, что и заполнение
2-го энергетического уровня.
А вот начиная с 19-го элемента, калия,
заполняется не 3d-орбиталь, а 4s. Заполнение
энергетических
и
подуровней
электронами происходит по энергетическому
ряду орбиталей, а не по порядку.
Таким образом, формула калия:
K +19 1s22s22p63s23p64s1
1s
2s
2p
3s
3p
4s
У кальция 4s-подуровень заполнен:
Ca +20 1s22s22p63s23p64s2
1s
2s
2p
3s
3p
4s
У элемента 21, скандия, согласно энергетическому ряду
орбиталей, начинается заполнение 3d-подуровня:
Sc +21 1s22s22p63s23p63d14s2
3d
4s
Дальнейшее заполнение 3d-подуровня происходит согласно
квантовым правилам, от титана до ванадия.
Однако, у хрома порядок заполнения орбиталей нарушается.
Электронная конфигурация хрома такая:
Cr +24 [Ar]3d54s1
4s
Этот эффект так и называется —провал или проскок
электрона.
 И наблюдается он, когда d-орбиталь
И наблюдается он, когда d-орбитальнедозаполнена на 1 электрон (по одному электрону в ячейке
или по два).
Основное и возбужденное состояние атома бора
B +5 1s22s22p1
1s
2s
2p
B* +5 1s22s12p2
1s
2s
2p
Электронные формулы ионов
Если атом отдаёт электроны, то общий заряд образовавшейся
частицы будет положительный (вспомним, что число протонов в
атоме равно числу электронов, а при отдаче электронов число
заряженные ионы — это катионы. Например: катион натрия
образуется так:
Na +11 1s22s22p63s1 -1е = Na+ +11 1s22s22p63s0
Если атом принимает электроны, то
приобретает отрицательный заряд. Отрицательно заряженные
частицы — это анионы. Например, анион хлора образуется так:
Cl +17 1s22s22p63s23p5 +1e = Cl— +17 1s22s22p63s23p6
Таким образом, электронные формулы ионов можно
получить добавив или отняв электроны у атома. Обратите
внимание, при образовании катионов электроны уходят
с внешнего энергетического уровня.

электроны приходят на внешний энергетический уровень.
В некоторых случаях совершенно разные атомы
образуют ионы с одинаковой электронной
конфигурацией. Частицы с одинаковой электронной
конфигурацией и одинаковым числом электронов
называют изоэлектронными частицами.
Например, ионы Na+ и F—.
Электронная формула катиона натрия:
Na+ 1s22s22p6, всего 10 электронов.
Электронная формула аниона фтора:
F— 1s22s22p6, всего 10 электронов.
Таким образом, ионы Na+ и F— — изоэлектронные.
Также они изоэлектронны атому аргона.
English Русский Правила
Строение атома | CHEMEGE.RU
Темы кодификатора ЕГЭ: Строение электронных оболочек атомов элементов первых четырех периодов: s-, p- и d-элементы. Электронная конфигурация атомов и ионов. Основное и возбужденное состояние атомов.
Тренировочные тесты в формате ЕГЭ по теме «Строение атома» (задание 1 ЕГЭ по химии) ( с ответами)
Одну из первых моделей строения атома — «пудинговую модель» — разработал Д. Д. Томсон в 1904 году. Томсон открыл существование электронов, за что и получил Нобелевскую премию. Однако наука на тот момент не могла объяснить существование этих самых электронов в пространстве. Томсон предположил, что атом состоит из отрицательных электронов, помещенных в равномерно заряженный положительно «суп», который компенсирует заряд электронов (еще одна аналогия — изюм в пудинге). Модель, конечно, оригинальная, но неверная. Зато модель Томсона стала отличным стартом для дальнейших работ в этой области.
Д. Томсон в 1904 году. Томсон открыл существование электронов, за что и получил Нобелевскую премию. Однако наука на тот момент не могла объяснить существование этих самых электронов в пространстве. Томсон предположил, что атом состоит из отрицательных электронов, помещенных в равномерно заряженный положительно «суп», который компенсирует заряд электронов (еще одна аналогия — изюм в пудинге). Модель, конечно, оригинальная, но неверная. Зато модель Томсона стала отличным стартом для дальнейших работ в этой области.
И дальнейшая работа оказалась эффективной. Ученик Томсона, Эрнест Резерфорд, на основании опытов по рассеянию альфа-частиц на золотой фольге предложил новую, планетарную модель строения атома.
Согласно модели Резерфорда, атом состоит из массивного, положительно заряженного ядра и частиц с небольшой массой — электронов, которые, как планеты вокруг Солнца, летают вокруг ядра, и на него не падают.
Модель Резерфорда оказалась следующим шагом в изучении строения атома. Однако современная наука использует более совершенную модель, предложенную Нильсом Бором в 1913 году. На ней мы и остановимся подробнее.
Однако современная наука использует более совершенную модель, предложенную Нильсом Бором в 1913 году. На ней мы и остановимся подробнее.
Атом — это мельчайшая, электронейтральная, химически неделимая частица вещества, состоящая из положительно заряженного ядра и отрицательно заряженной электронной оболочки.
При этом электроны двигаются не по определенной орбите, как предполагал Резерфорд, а довольно хаотично. Совокупность электронов, которые двигаются вокруг ядра, называется электронной оболочкой.
Атомное ядро, как доказал Резерфорд — массивное и положительно заряженное, расположено в центральной части атома. Структура ядра довольно сложна, и изучается в ядерной физике. Основные частицы, из которых оно состоит — протоны и нейтроны. Они связаны ядерными силами (сильное взаимодействие).
Рассмотрим основные характеристики протонов, нейтронов и электронов:
| Протон | Нейтрон | Электрон | |
| Масса | 1,00728 а. е.м. е.м. | 1,00867 а.е.м. | 1/1960 а.е.м. |
| Заряд | + 1 элементарный заряд | 0 | — 1 элементарный заряд |
1 а.е.м. (атомная единица массы) = 1,66054·10-27 кг
1 элементарный заряд = 1,60219·10-19 Кл
И — самое главное. Периодическая система химических элементов, структурированная Дмитрием Ивановичем Менделеевым, подчиняется простой и понятной логике: номер атома — это число протонов в ядре этого атома. Причем ни о каких протонах Дмитрий Иванович в XIX веке не слышал. Тем гениальнее его открытие и способности, и научное чутье, которое позволило перешагнуть на полтора столетия вперёд в науке.
Следовательно, заряд ядра Z равен числу протонов, т.е. номеру атома в Периодической системе химических элементов.
Атом — это электронейтральная частица, следовательно, число протонов равно числу электронов: Ne = Np = Z.
Масса атома (массовое число A) примерно равна суммарной массе крупных частиц, которые входят в состав атома — протонов и нейтронов. Поскольку масса протона и нейтрона примерно равна 1 атомной единице массы, можно использовать формулу:
M = Np + Nn
Массовое число указано в Периодической системе химических элементов в ячейке каждого элемента.
Обратите внимание! При решении задач ЕГЭ массовое число всех атомов, кроме хлора, округляется до целого по правилам математики. Массовое число атома хлора в ЕГЭ принято считать равным 35,5.
Таким образом, рассчитать число нейтронов в атоме можно, вычтя из массового числа номер атома: Nn = M – Z.
В Периодической системе собраны химические элементы — атомы с одинаковым зарядом ядра. Однако, может ли меняться у этих атомов число остальных частиц? Вполне. Например, атомы с разным числом нейтронов называют изотопами данного химического элемента. У одного и того же элемента может быть несколько изотопов.
Например, атомы с разным числом нейтронов называют изотопами данного химического элемента. У одного и того же элемента может быть несколько изотопов.
Попробуйте ответить на вопросы. Ответы на них — в конце статьи:
- У изотопов одного элемента массовое число одинаковое или разное?
- У изотопов одно элемента число протонов одинаковое или разное?
Химические свойства атомов определяются строением электронной оболочки и зарядом ядра. Таким образом, химические свойства изотопов одного элемента практически не отличаются.
Поскольку атомы одного элемента могут существовать в форме разных изотопов, в названии часто указывается массовое число, например, хлор-35, и принята такая форма записи атомов:
Еще немного вопросов:
3. Определите количество нейтронов, протонов и электронов в изотопе брома-81.
4. Определите число нейтронов в изотопе хлора-37.
Строение электронной оболочки
Согласно квантовой модели строение атома Нильса Бора, электроны в атоме могут двигаться только по определенным (стационарным) орбитам, удаленным от ядра на определенное расстояние и характеризующиеся определенной энергией.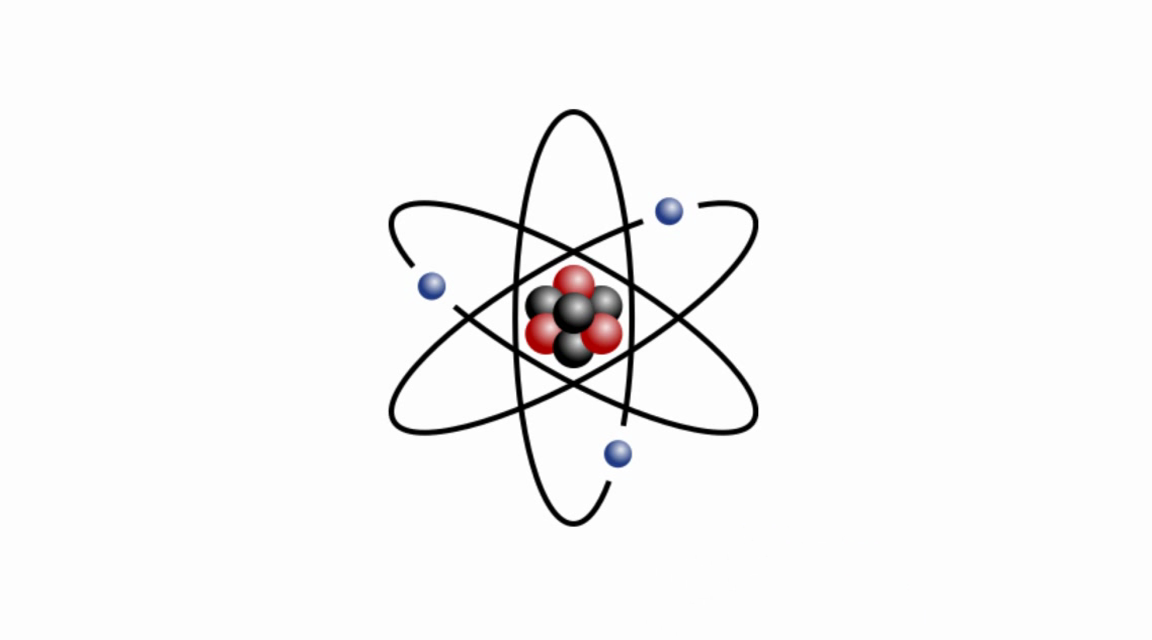 Другое название стационарны орбит — электронные слои или энергетические уровни.
Другое название стационарны орбит — электронные слои или энергетические уровни.
Электронные уровни можно обозначать цифрами — 1, 2, 3, …, n. Номер слоя увеличивается мере удаления его от ядра. Номер уровня соответствует главному квантовому числу n.
В одном слое электроны могут двигаться по разным траекториям. Траекторию орбиты характеризует электронный подуровень. Тип подуровня характеризует орбитальное квантовое число l = 0,1, 2, 3 …, либо соответствующие буквы — s, p, d, g и др.
В рамках одного подуровня (электронных орбиталей одного типа) возможны варианты расположения орбиталей в пространстве. Чем сложнее геометрия орбиталей данного подуровня, тем больше вариантов их расположения в пространстве. Общее число орбиталей подуровня данного типа l можно определить по формуле: 2l+1. На каждой орбитали может находиться не более двух электронов.
На каждой орбитали может находиться не более двух электронов.
| Тип орбитали | s | p | d | f | g |
| Значение орбитального квантового числа l | 0 | 1 | 2 | 3 | 4 |
| Число атомных орбиталей данного типа 2l+1 | 1 | 3 | 5 | 7 | 9 |
| Максимальное количество электронов на орбиталях данного типа | 2 | 6 | 10 | 14 | 18 |
Получаем сводную таблицу:
Номер уровня, n | Подуровень | Число АО | Максимальное количество электронов |
| 1 | 1s | 1 | 2 |
| 2 | 2s | 1 | 2 |
| 2p | 3 | 6 | |
3 | 3s | 1 | 2 |
| 3p | 3 | 6 | |
| 3d | 5 | 10 | |
4 | 4s | 1 | 2 |
| 4p | 3 | 6 | |
| 4d | 5 | 10 | |
| 4f | 7 | 14 |
Заполнение электронами энергетических орбиталей происходит согласно некоторым основным правилам. Давайте остановимся на них подробно.
Давайте остановимся на них подробно.
Принцип Паули (запрет Паули): на одной атомной орбитали могут находиться не более двух электронов с противоположными спинами (спин — это квантовомеханическая характеристика движения электрона).
Правило Хунда. На атомных орбиталях с одинаковой энергией электроны располагаются по одному с параллельными спинами. Т.е. орбитали одного подуровня заполняются так: сначала на каждую орбиталь распределяется по одному электрону. Только когда во всех орбиталях данного подуровня распределено по одному электрону, занимаем орбитали вторыми электронами, с противоположными спинами.
Таким образом, сумма спиновых квантовых чисел таких электронов на одном энергетическом подуровне (оболочке) будет максимальной.
Например, заполнение 2р-орбитали тремя электронами будет происходить так: , а не так:
Принцип минимума энергии. Электроны заполняют сначала орбитали с наименьшей энергией. Энергия атомной орбитали эквивалентна сумме главного и орбитального квантовых чисел: n + l. Если сумма одинаковая, то заполняется первой та орбиталь, у которой меньше главное квантовое число n.
Энергия атомной орбитали эквивалентна сумме главного и орбитального квантовых чисел: n + l. Если сумма одинаковая, то заполняется первой та орбиталь, у которой меньше главное квантовое число n.
| АО | 1s | 2s | 2p | 3s | 3p | 3d | 4s | 4p | 4d | 4f | 5s | 5p | 5d | 5f | 5g |
| n | 1 | 2 | 2 | 3 | 3 | 3 | 4 | 4 | 4 | 4 | 5 | 5 | 5 | 5 | 5 |
| l | 0 | 0 | 1 | 0 | 1 | 2 | 0 | 1 | 2 | 3 | 0 | 1 | 2 | 3 | 4 |
| n + l | 1 | 2 | 3 | 3 | 4 | 5 | 4 | 5 | 6 | 7 | 5 | 6 | 7 | 8 | 9 |
Таким образом, энергетический ряд орбиталей выглядит так:
1s < 2s < 2 p < 3s < 3p < 4s < 3d < 4p < 5s < 4d < 5p < 6s < 4f~5d < 6p < 7s <5f~6d …
Электронную структуру атома можно представлять в разных формах — энергетическая диаграмма, электронная формула и др. Разберем основные.
Разберем основные.
Энергетическая диаграмма атома — это схематическое изображение орбиталей с учетом их энергии. Диаграмма показывает расположение электронов на энергетических уровнях и подуровнях. Заполнение орбиталей происходит согласно квантовым принципам.
Например, энергетическая диаграмма для атома углерода:
Электронная формула — это запись распределения электронов по орбиталям атома или иона. Сначала указывается номер уровня, затем тип орбитали. Верхний индекс справа от буквы показывает число электронов на орбитали. Орбитали указываются в порядке заполнения. Запись 1s2 означает, что на 1 уровне s-подуровне расположено 2 электрона.
Например, электронная формула углерода выглядит так: 1s22s22p2.
Для краткости записи, вместо энергетических орбиталей, полностью заполненных электронами, иногда используют символ ближайшего благородного газа (элемента VIIIА группы), имеющего соответствующую электронную конфигурацию.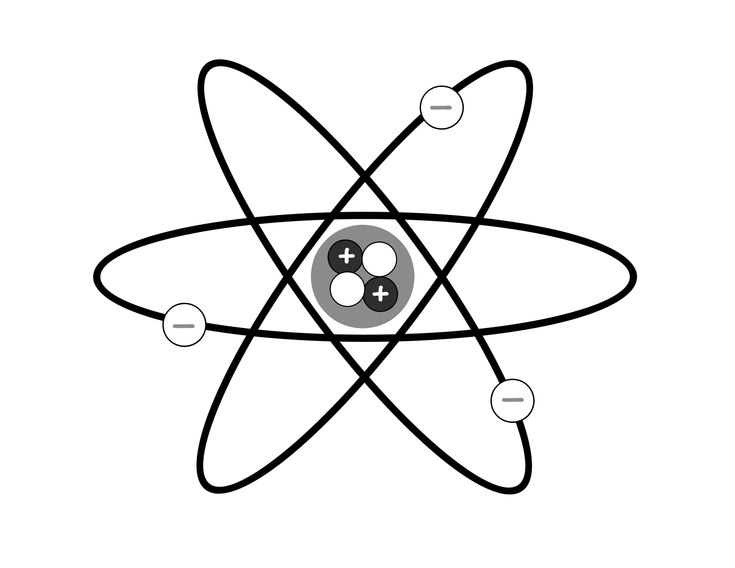
Например, электронную формулу азота можно записать так: 1s22s22p3 или так: [He]2s22p3.
1s2 = [He]
1s22s22p6 = [Ne]
1s22s22p63s23p6 = [Ar] и так далее.
Электронные формулы элементов первых четырех периодов
Рассмотрим заполнение электронами оболочки элементов первых четырех периодов. У водорода заполняется самый первый энергетический уровень, s-подуровень, на нем расположен 1 электрон:
+1H 1s1 1s
У гелия 1s-орбиталь полностью заполнена:
+2He 1s2 1s
Поскольку первый энергетический уровень вмещает максимально 2 электрона, у лития начинается заполнение второго энергетического уровня, начиная с орбитали с минимальной энергией — 2s.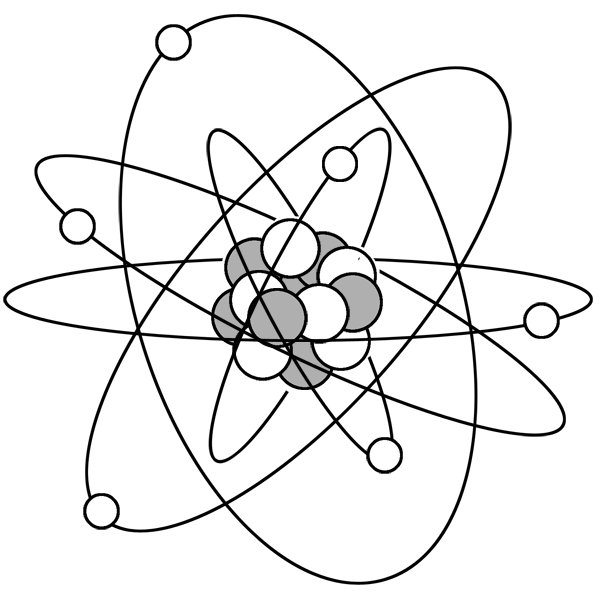 При этом сначала заполняется первый энергетический уровень:
При этом сначала заполняется первый энергетический уровень:
+3Li 1s22s1 1s 2s
У бериллия 2s-подуровень заполнен:
+4Be 1s22s2 1s 2s
Далее, у бора заполняется p-подуровень второго уровня:
+5B 1s22s22p1 1s 2s 2p
У следующего элемента, углерода, очередной электрон, согласно правилу Хунда, заполняет вакантную орбиталь, а не заполняет частично занятую:
+6C 1s22s22p2 1s 2s 2p
Попробуйте составить электронную и электронно-графическую формулы для следующих элементов, а затем можете проверить себя по ответам конце статьи:
5. Азот
Азот
6. Кислород
7. Фтор
У неона завершено заполнение второго энергетического уровня:
+10Ne 1s22s22p6 1s 2s 2p
У натрия начинается заполнение третьего энергетического уровня:
+11Na 1s22s22p63s1 1s 2s 2p 3s
От натрия до аргона заполнение 3-го уровня происходит в том же порядке, что и заполнение 2-го энергетического уровня. Предлагаю составить электронные формулы элементов от магния до аргона самостоятельно, проверить по ответам.
8. Магний
9. Алюминий
10. Кремний
11. Фосфор
12. Сера
13. Хлор
Хлор
14. Аргон
А вот начиная с 19-го элемента, калия, иногда начинается путаница — заполняется не 3d-орбиталь, а 4s. Ранее мы упоминали в этой статье, что заполнение энергетических уровней и подуровней электронами происходит по энергетическому ряду орбиталей, а не по порядку. Рекомендую повторить его еще раз. Таким образом, формула калия:
+19K 1s22s22p63s23p64s11s 2s 2p3s 3p4s
Для записи дальнейших электронных формул в статье будем использовать сокращенную форму:
+19K [Ar]4s1 [Ar] 4s
У кальция 4s-подуровень заполнен:
+20Ca [Ar]4s2 [Ar] 4s
У элемента 21, скандия, согласно энергетическому ряду орбиталей, начинается заполнение 3d-подуровня:
+21Sc [Ar]3d14s2 [Ar] 4s 3d
Дальнейшее заполнение 3d-подуровня происходит согласно квантовым правилам, от титана до ванадия:
+22Ti [Ar]3d24s2 [Ar] 4s 3d
+23V [Ar]3d34s2 [Ar] 4s 3d
Однако, у следующего элемента порядок заполнения орбиталей нарушается. Электронная конфигурация хрома такая:
Электронная конфигурация хрома такая:
+24Cr [Ar]3d54s1 [Ar] 4s 3d
В чём же дело? А дело в том, что при «традиционном» порядке заполнения орбиталей (соответственно, неверном в данном случае — 3d44s2) ровно одна ячейка в d-подуровне оставалась бы незаполненной. Оказалось, что такое заполнение энергетически менее выгодно. А более выгодно, когда d-орбиталь заполнена полностью, хотя бы единичными электронами. Этот лишний электрон переходит с 4s-подуровня. И небольшие затраты энергии на перескок электрона с 4s-подуровня с лихвой покрывает энергетический эффект от заполнения всех 3d-орбиталей. Этот эффект так и называется — «провал» или «проскок» электрона. И наблюдается он, когда d-орбиталь недозаполнена на 1 электрон (по одному электрону в ячейке или по два).
И наблюдается он, когда d-орбиталь недозаполнена на 1 электрон (по одному электрону в ячейке или по два).
У следующих элементов «традиционный» порядок заполнения орбиталей снова возвращается. Конфигурация марганца:
+25Mn [Ar]3d54s2
Аналогично у кобальта и никеля. А вот у меди мы снова наблюдаем провал (проскок) электрона — электрон опять проскакивает с 4s-подуровня на 3d-подуровень:
+29Cu [Ar]3d104s1
На цинке завершается заполнение 3d-подуровня:
+30Zn [Ar]3d104s2
У следующих элементов, от галлия до криптона, происходит заполнение 4p-подуровня по квантовым правилам. Например, электронная формула галлия:
Например, электронная формула галлия:
+31Ga [Ar]3d104s24p1
Формулы остальных элементов мы приводить не будем, можете составить их самостоятельно.
Некоторые важные понятия:
Внешний энергетический уровень — это энергетический уровень в атоме с максимальным номером, на котором есть электроны.
Например, у меди ([Ar]3d104s1) внешний энергетический уровень — четвёртый.
Валентные электроны — электроны в атоме, которые могут участвовать в образовании химической связи. Например, у хрома (+24Cr [Ar]3d54s1) валентными являются не только электроны внешнего энергетического уровня (4s1), но и неспаренные электроны на 3d-подуровне, т.к. они могут образовывать химические связи.
Основное и возбужденное состояние атома
Электронные формулы, которые мы составляли до этого, соответствуют основному энергетическому состоянию атома. Это наиболее выгодное энергетически состояние атома.
Однако, чтобы образовывать химические связи, атому в большинстве ситуаций необходимо наличие неспаренных (одиночных) электронов. А химические связи энергетически очень для атома выгодны. Следовательно, чем больше в атоме неспаренных электронов — тем больше связей он может образовать, и, как следствие, перейдёт в более выгодное энергетическое состояние.
Поэтому при наличии свободных энергетических орбиталей на данном уровне спаренные пары электронов могут распариваться, и один из электронов спаренной пары может переходить на вакантную орбиталь. Таким образом число неспаренных электронов увеличивается, и атом может образовать больше химических связей, что очень выгодно с точки зрения энергии. Такое состояние атома называют возбуждённым и обозначают звёздочкой.
Такое состояние атома называют возбуждённым и обозначают звёздочкой.
Например, в основном состоянии бор имеет следующую конфигурацию энергетического уровня:
+5B 1s22s22p1 1s 2s 2p
На втором уровне (внешнем) одна спаренная электронная пара, один одиночный электрон и пара свободных (вакантных) орбиталей. Следовательно, есть возможность для перехода электрона из пары на вакантную орбиталь, получаем возбуждённое состояние атома бора (обозначается звёздочкой):
+5B* 1s22s12p2 1s 2s 2p
Попробуйте самостоятельно составить электронную формулу, соответствующую возбуждённому состоянию атомов. Не забываем проверять себя по ответам!
15. Углерода
16. Бериллия
17. Кислорода
Кислорода
Электронные формулы ионов
Атомы могут отдавать и принимать электроны. Отдавая или принимая электроны, они превращаются в ионы.
Ионы — это заряженные частицы. Избыточный заряд обозначается индексом в правом верхнем углу.
Если атом отдаёт электроны, то общий заряд образовавшейся частицы будет положительный (вспомним, что число протонов в атоме равно числу электронов, а при отдаче электронов число протонов будет больше числа электронов). Положительно заряженные ионы — это катионы. Например: катион натрия образуется так:
+11Na 1s22s22p63s1 -1е = +11Na+ 1s22s22p63s0
Если атом принимает электроны, то приобретает отрицательный заряд. Отрицательно заряженные частицы — это анионы. Например, анион хлора образуется так:
Отрицательно заряженные частицы — это анионы. Например, анион хлора образуется так:
+17Cl 1s22s22p63s23p5 +1e = +17Cl— 1s22s22p63s23p6
Таким образом, электронные формулы ионов можно получить добавив или отняв электроны у атома. Обратите внимание, при образовании катионов электроны уходят с внешнего энергетического уровня. При образовании анионов электроны приходят на внешний энергетический уровень.
Попробуйте составить самостоятельно электронный формулы ионов. Не забывайте проверять себя по ключам!
18. Ион Са2+
19. Ион S2-
20. Ион Ni2+
Ион Ni2+
В некоторых случаях совершенно разные атомы образуют ионы с одинаковой электронной конфигурацией. Частицы с одинаковой электронной конфигурацией и одинаковым числом электронов называют изоэлектронными частицами.
Например, ионы Na+ и F—.
Электронная формула катиона натрия: Na+ 1s22s22p6, всего 10 электронов.
Электронная формула аниона фтора: F— 1s22s22p6, всего 10 электронов.
Таким образом, ионы Na+ и F— — изоэлектронные. Также они изоэлектронны атому неона.
Тренажер по теме «Строение атома» — 10 вопросов, при каждом прохождении новые.
1152
Создан на По Admin
Тренировочный тест “Строение атома”
Тренировочный тест по теме “Строение атома”
1 / 10
1) V 2) B 3) Li 4) C 5) He
Определите элементы, атомы которых в основном состоянии имеют электронную формулу внешнего энергетического уровня ns2.
2 / 10
1) Cr 2) Na 3) P 4) As 5) N
Определите, атомы каких из указанных в ряду элементов в основном состоянии имеют электронную конфигурацию внешнего энергетического уровня ns1.
3 / 10
1) Cu 2) Cl 3) Zn 4) Si 5) P
Определите, атомы каких из указанных в ряду элементов в основном состоянии содержат один неспаренный электрон.
4 / 10
1) Cl 2) Sn 3) Ge 4) Mg 5) Na
Определите, атомы каких из указанных в ряду элементов в основном состоянии содержат два неспаренных электрона.
5 / 10
1) Sn 2) Fe 3) C 4) Pb 5) Cr
Определите, атомы каких из указанных в ряду элементов в основном состоянии имеют валентные электроны как на s-, так и на d-подуровнях.
6 / 10
1) S 2) Ti 3) Sc 4) Se 5) Cu
Определите, атомы каких из указанных в ряду элементов в основном энергетическом состоянии не содержат неспаренные электроны на внешнем энергетическом уровне.
7 / 10
1) O 2) H 3) Be 4) Cu 5) N
Определите, атомы каких из указанных в ряду элементов в основном состоянии содержат одинаковое число неспаренных электронов.
8 / 10
1) S 2) P 3) Ar 4) Si 5) Mg
Определите элементы, атомы которых в основном состоянии не содержат неспаренных электронов.
9 / 10
1) V 2) Br 3) S 4) As 5) I
Определите элементы, атомы которых имеют по пять валентных электронов.
10 / 10
1) Cr 2) P 3) Na 4) Si 5) N
Определите элементы, атомы которых в основном состоянии содержат на внешнем уровне один неспаренный электрон.
Ваша оценка
Средний балл 40%
Ответы на вопросы:
1. У изотопов одного химического элемента массовое число всегда разное, т.к. массовое число складывается из числа протонов и нейтронов. А у изотопов различается число нейтронов.
2. У изотопов одного элемента число протонов всегда одинаковое, т.к. число протонов характеризует химический элемент.
3. Массовое число изотопа брома-81 равно 81. Атомный номер = заряд ядра брома = число протонов в ядре = 35. Вычитаем из массового числа число протонов, получаем 81-35=46 нейтронов.
Вычитаем из массового числа число протонов, получаем 81-35=46 нейтронов.
4. Массовое число изотопа хлора равно 37. Атомный номер, заряд ядра и число протонов в ядре равно 17. Получаем число нейтронов = 37-17 =20.
5. Электронная формула азота:
+7N 1s22s22p3 1s 2s 2p
6. Электронная формула кислорода:
+8О 1s22s22p4 1s 2s 2p
7. Электронная формула фтора:
8. Электронная формула магния:
+12Mg 1s22s22p63s2 1s 2s 2p 3s
9. Электронная формула алюминия:
Электронная формула алюминия:
+13Al 1s22s22p63s23p1 1s 2s 2p 3s 3p
10. Электронная формула кремния:
+14Si 1s22s22p63s23p2 1s 2s 2p 3s 3p
11. Электронная формула фосфора:
+15P 1s22s22p63s23p3 1s 2s 2p 3s 3p
12. Электронная формула серы:
+16S 1s22s22p63s23p4 1s 2s 2p 3s 3p
13. Электронная формула хлора:
Электронная формула хлора:
14. Электронная формула аргона:
+18Ar 1s22s22p63s23p6 1s 2s 2p 3s 3p
15. Электронная формула углерода в возбуждённом состоянии:
+6C* 1s22s12p3 1s 2s 2p
16. Электронная формула бериллия в возбуждённом состоянии:
+4Be 1s22s12p1 1s 2s 2p
17. Электронная формула кислорода в возбуждённом энергетическом состоянии соответствует формуле кислорода в основном энергетическом состоянии, т. к. нет условий для перехода электрона — отсутствуют вакантные энергетические орбитали.
к. нет условий для перехода электрона — отсутствуют вакантные энергетические орбитали.
18. Электронная формула иона кальция Са2+: +20Ca2+ 1s22s22p63s23p6
19. Электронная формула аниона серы S2-: +16S2- 1s22s22p63s23p6
20. Электронная формула катиона никеля Ni2+: +28Ni2+ 1s22s22p63s23p63d84s0. Обратите внимание! Атомы отдают электроны всегда сначала с внешнего энергетического уровня. Поэтому никель отдаёт электроны сначала с внешнего 4s-подуровня.
Тренировочные тесты в формате ЕГЭ по теме «Строение атома» (задание 1 ЕГЭ по химии) ( с ответами)
Понравилось это:
Нравится Загрузка. ..
..
Разработка урока химии “Строение атома”
Тип урока: изучения и первичного закрепления нового материала.
Цели урока: Развивать пространственное воображение как элемента творческой деятельности, развивать мировоззрение как систему взаимодействия макро- и микромира.
Задачи урока:
- Познакомить учащихся с историей установления сложного строения атома, с частицами, составляющими атом и их характеристиками.
- Отработать умение записывать массовое число, порядковый номер элемента рядом с его символом, определять число протонов, нейтронов и электронов атомов любых химических элементов.
- Показать, что этимологическое начало
понятия “атом” (“неделимый”) не соответствует
действительности – атом делим. Дать понятие о
составе атома и атомного ядра. Раскрыть
взаимосвязь понятий: протон, нейтрон, электрон,
массовое число.

- Воспитывать в учениках уверенность в своих силах.
Оборудование:
- Самодельные ЛСМ “Строение атома”. На доске построен каркас логико-смысловой модели “Строение атома”, на которой показаны точками узлы этой модели без подписей.
- Фрагменты фильма “Строение атома” (Можно заменить презентацией).
- На столах у групп раздаточный материал
- Словари, в которых представлено понятие “атом”
- Так как предусмотрена работа в группах, то ученики разделены на 3 группы.
- В каждой группе на столах лежит раздаточный материал, содержание которого представлено отдельно.
Содержание урока.
Здравствуйте, ребята.
Сегодня мы с вами должны познакомиться с одним
из основных понятий химии – “атом” и выстроить
весь материал урока в виде логико-смысловой
модели, каркас которой размещен на доске, а мы его
должны заполнить.
Начнем мы с вами с истории. Римский поэт и философ, Тит Лукреций Кар (Iв до н.э.) рассказал в бессмертной поэме “О природе вещей” об атоме.
(Если через окно в класс проникают солнечные лучи, то можно во время чтения стихотворения акцентировать внимание учащихся на этом моменте)
Вот посмотри: всякий раз, когда солнечный свет
проникает
В наши жилища и мрак прорезает своими лучами,
Множество маленьких тел в пустоте ты увидишь;
мелькая,
Мечутся взад и вперед, в лучистом сиянии света;
Будто бы в вечной борьбе они бьются в сраженьях и битвах,
В схватки бросаются вдруг по отрядам, не зная покоя,
Или сходясь или врозь постоянно опять разлетаясь.
Вопрос: Как вы думаете, суть каких явлений, с точки зрения современных представлений, описал поэт в данном стихотворении?
Ответы:
– явление диффузии;
– броуновское движение: пылинки в солнечном
свете – хаотичное движение молекул и их
столкновение.
Вывод: Учение об атомах по своей сути материалистично. Самые различные явления природы находят себе простое объяснение. Движения атомов и их соударения подчиняются простым и строгим законам. Однако, по мнению Демокрита, атом неизменен и вечен: У вас на столах лежат словари. Используя их дайте определение понятию “атом”. Итак, согласно всем словарям атом характеризуется неделимой частицей. Действительно ли это так?
Я предлагаю вам самостоятельно познакомиться с основными этапами развития учения об атомах. У вас на столах в каждой группе (это блок №1) лежит лист с описанием опытов, проведенных физиками в XIX в. Изучите, пожалуйста, материал в течение 3 мин. Затем один человек от группы должен кратко изложить суть открытия.
Каркас ЛСМ представлен на доске. Первый луч, направленный к координате “История открытия” заполняем вместе с выходящими учащимися. Должно получиться 4 узла на луче:
– Ирландский физик Стони открыл электроны
– Англичанин Дж. Томсон и француз Жан Перрен
дали характеристику электрона и получили поток
электронов
Томсон и француз Жан Перрен
дали характеристику электрона и получили поток
электронов
– Физик Анри Беккерель открыл явление радиоактивности.
– Англичанин Эрнест Резерфорд изучал рассеивание a-частиц.
Атом любого химического элемента – как бы крохотная Солнечная система, в центре которой ядро, а вокруг вращаются электроны. Поэтому такую модель атома, предложенную Резерфордом, называют планетарной. (Заполняем луч каркаса ЛСМ от атома к ядру: узел 1 – планетарная модель атома)
Но и это не все. Оказывается, и крошечное атомное ядро, в котором сосредоточена вся масса атома, состоит из частиц двух видов.
Посмотрите, пожалуйста, на экран.
Просматриваем пять страниц электронного урока “Как устроен атом”.
На 1 странице фильма мы с вами можем увидеть как
раз планетарную модель атома углерода. Обратите
внимание на выводы, которые мы с вами только что
сделали. Итак, атом состоит из трех видов частиц: протонов
и нейтронов, которые образуют ядро и электронов.
Итак, атом состоит из трех видов частиц: протонов
и нейтронов, которые образуют ядро и электронов.
На 2 странице электронного урока показано, что ядра имеют положительный заряд. Самое простое ядро – это ядро атома водорода. (Заполняем луч каркаса ЛСМ от атома к ядру: узел 2 – ядро имеет положительный заряд)
Также, здесь дана характеристика каждого вида частиц, составляющих атом. Повторите их, пожалуйста.
Ответ: Протоны, имеют массу равную 1, положительный заряд равный +1, обозначаются р+. Нейтроны имеют массу равную 1, заряда не имеют, обозначаются n0. Электроны имеют отрицательный заряд равный -1, массу, равную1/1840 массы протона, обозначаются е–.
Задание группам: (Блок №2) У вас на столах
лежит одинаковый набор карточек со всеми
характеристиками частиц, составляющих атомы. 1
группа должна выбрать характеристики протона, 2
группа должна выбрать характеристики нейтрона, а
третья группа должна выбрать характеристики
электрона.
Через 30 секунд представители от каждой группы должны прикрепить выбранные карточки на лучах ЛСМ для вашей координаты.
(Во время ответа ребята прикрепляют таблички характеристик частиц с помощью магнитов на каркас ЛСМ, заполняя лучи: протоны, нейтроны, электроны, на каждом луче по 3 узла – заряд, масса, обозначение частицы)
На 3 странице рассмотрено правило о том, что порядковый номер элемента равен числу протонов.
На 4 странице показана модель ядра атома углерода и рассмотрена закономерность:
р+ + n0 = массовому числу А
Показано правило записи символа химического элемента, его порядкового номера и массового числа.
Задание группам: (Блок №3) 1 группа напишет символы, массовое число и порядковый номер для кремния и лития, 2 группа для азота и натрия, 3 группа для гелия и фосфора. Прикрепите полученные записи на доску.
На 5 странице урока показаны правила определения нейтронов
n0 = А – z.
Атомы электронейтральны, следовательно, электронов в атоме должно быть столько же, сколько протонов
р+= е–
Задание группам: (Блок №4) С помощью цветных кружочков и листов с прорезями соберите модели ядер тех атомов, символы которых ваши группы записывали.
Прикрепите их рядом с символами. Защитите вашу модель (почему столько протонов и нейтронов в ядре ваших атомов? Сколько электронов должно быть в атомах этих элементов?)
Молодцы, вы очень хорошо справились с заданием.
Вопрос: А как вы думаете, так ли уж необходимо
нам с вами изучать строение атомов? Для чего нам
необходимы эти знания? (Во время ответа
заполняется ЛСМ) (А ведь энергетические ресурсы
атома неисчерпаемы, в отличие, например, от
запасов природных ископаемых, таких как уголь,
нефть, газ. Мирный атом и атомная энергия,
используемая в военных целях. Тяжелые
последствия применения атомной бомбы известны
всему миру, когда в 1945 г Хиросима была
уничтожена).
Тяжелые
последствия применения атомной бомбы известны
всему миру, когда в 1945 г Хиросима была
уничтожена).
Греки говорили, что атом неделим. Так ли это? Используя материал этого урока, как вы можете ответить на этот вопрос? Как это ни странно, но правы и вы и Демокрит. Атом – это химически неделимая частица, так как в химических реакциях атомы не изменяются, но знать строение атома необходимо каждому химику для объяснения многих химических процессов.
В дальнейшем вы можете дополнить нашу ЛСМ. Ведь если к атому добавить еще один протон, то меняется заряд ядра, а следовательно и порядковый номер элемента, т.е. происходит ядерная реакция. Если к атому добавить нейтрон, то заряд ядра не меняется, а меняется только масса атома. Возникает разновидность атомов химического элемента, которые называют изотопами. С этими понятиями вы познакомитесь на следующих уроках.
У нас осталось немного времени. Загадайте,
пожалуйста, химический элемент. Его порядковый
номер умножьте на 2, прибавьте к этому
произведению 5. Теперь всю сумму умножьте на пять.
По очереди говорите мне ответ, а я скажу вам
порядковый номер вашего загаданного элемента.
Загадайте,
пожалуйста, химический элемент. Его порядковый
номер умножьте на 2, прибавьте к этому
произведению 5. Теперь всю сумму умножьте на пять.
По очереди говорите мне ответ, а я скажу вам
порядковый номер вашего загаданного элемента.
(Разгадка: От предложенного ответа необходимо отбросить последнюю цифру и вычесть от оставшегося числа 2. Получится порядковый номер задуманного элемента в таблице Д.И.Менделеева).
Рисунок. Логико-смысловая модель “Строение атома”
Приложение.
Строение атома | Физика
В 1897 г. было сделано открытие, позволившее объяснить большинство электрических явлений: английский ученый Дж. Дж. Томсон открыл частицу, являющуюся носителем элементарного заряда. Эту частицу назвали электроном.
Масса электрона оказалась почти в 2000 раз меньше массы самого легкого атома в природе — атома водорода. Заряд электрона отрицательный:
qэл = –e = –1,6·10–19 Кл.
Этот заряд является неотъемлемой характеристикой электрона. В отличие от обычных тел, которые можно зарядить или, наоборот, разрядить, «избавить» электрон от его заряда невозможно. Более того, заряд электрона нельзя ни увеличить, ни уменьшить. Он всегда имеет одно и то же значение.
Из курса химии вы знаете, что электроны входят в состав атомов. Электроны внутри атома обращаются вокруг положительно заряженного атомного ядра.
Строение атома было открыто в 1911 г. в результате экспериментов, которыми руководил английский ученый Э. Резерфорд. Идея опытов состояла в том, чтобы выяснить, что происходит с быстролетящими частицами, когда на их пути оказываются атомы вещества.
Нужно сказать, что за несколько лет до этого было открыто явление радиоактивности: были обнаружены невидимые лучи, которые испускались некоторыми (теперь их называют радиоактивными) веществами (ураном, радием и др.). Изучение этих лучей показало, что в общем случае они состоят из трех компонентов, отличающихся друг от друга электрическим зарядом. Для обозначения отдельных видов радиоактивных излучений было предложено использовать первые три буквы греческого алфавита: α (альфа), β (бета) и γ (гамма).
Для обозначения отдельных видов радиоактивных излучений было предложено использовать первые три буквы греческого алфавита: α (альфа), β (бета) и γ (гамма).
Альфа-лучи состоят из положительно заряженных частиц (альфа-частиц), бета-лучи — из отрицательно заряженных частиц (электронов), гамма-лучи — никаким зарядом не обладают. Эти лучи опасны для человека. Поэтому, работая с радиоактивными препаратами, следует соблюдать особые меры предосторожности: использовать специальные защитные экраны и, конечно, никогда не брать эти препараты руками.
Резерфорд предложил использовать альфа-частицы в качестве тех «снарядов», которыми можно было бы «бомбардировать» атомы вещества. Направив узкий пучок этих частиц на тонкую пластинку (фольгу) исследуемого вещества, он обнаружил, что большинство альфа-частиц пролетало через фольгу почти беспрепятственно и лишь очень небольшая их часть, столкнувшись с чем-то внутри атома, отскакивала от фольги назад. Более подробно об опытах Резерфорда будет рассказано в старших классах. Здесь же мы ограничимся тем выводом, к которому он пришел на основе анализа полученных данных.
Здесь же мы ограничимся тем выводом, к которому он пришел на основе анализа полученных данных.
Согласно Резерфорду, атом по своему строению напоминает Солнечную систему. Подобно тому как планеты, притягиваясь к Солнцу, движутся вокруг него, так и электроны в атоме движутся вокруг ядра, удерживаемые силами притяжения к нему. Из-за этого сходства модель строения атома (рис. 11), предложенную Резерфордом, назвали планетарной моделью.
Расстояния между ядром и электронами очень велики по сравнению с размерами этих частиц. Если бы весь атом увеличился так, что ядро приняло бы размеры десятикопеечной монеты, то расстояние между ядром и электронами стало бы равным примерно километру!
Подсчитано, что если бы все электроны примкнули вплотную к атомным ядрам, то объем тела взрослого человека стал бы равным одной миллионной доле кубического миллиметра! Это означает, что более 99% внутри тела человека (как и любого другого тела) занимает пустота! Именно через пустоту внутри атомов и пролетали те альфа-частицы в опыте Резерфорда, которые не отклонялись фольгой назад.
Совокупность атомов одного вида называют химическим элементом. Атомы разных химических элементов отличаются друг от друга зарядом своих ядер и числом электронов, обращающихся вокруг них. Так, например, в атоме водорода движется всего лишь один электрон, в атоме кислорода — восемь электронов, в атоме урана — девяносто два.
Число электронов в атоме совпадает с порядковым номером элемента в таблице Д. И. Менделеева. Через этот же номер выражается и заряд атомного ядра. Введем обозначение:
Z — порядковый номер элемента = число электронов в атоме.
Тогда для заряда атомного ядра и общего заряда всех электронов в атоме можно записать:
qядра = +Ze,
qэл-нов = –Ze.
Сложив общий заряд электронов в атоме с зарядом атомного ядра, мы получим нуль. Это означает, что в целом атом нейтрален. Нейтральными являются и молекулы вещества, так как они состоят из нейтральных атомов.
В некоторых случаях (например, при столкновениях) атомы могут потерять один или несколько своих электронов. Вместе с электронами атомы теряют часть своего отрицательного заряда и перестают быть нейтральными. Образующийся в результате этого положительно заряженный атом называют положительным ионом.
Вместе с электронами атомы теряют часть своего отрицательного заряда и перестают быть нейтральными. Образующийся в результате этого положительно заряженный атом называют положительным ионом.
Бывают и обратные случаи: нейтральный атом присоединяет к себе лишний электрон и становится отрицательно заряженным. Такой атом называют отрицательным ионом.
??? 1. Кто и когда открыл электрон? 2. Как заряжен электрон? 3. Вокруг чего обращаются электроны внутри атома? 4. Как заряжено атомное ядро? 5. Докажите, что атом в целом нейтрален. 6. Кто и когда открыл строение атома? 7. Чем отличаются альфа-, бета- и гамма-лучи друг от друга? 8. Приведите примеры радиоактивных веществ. 9. Почему большинство альфа-частиц в опыте Резерфорда практически беспрепятственно пролетало сквозь фольгу? 10. На что наталкивались внутри атома альфа-частицы, которые в опыте Резерфорда отскакивали от фольги назад? 11. Чем отличаются друг от друга атомы разных химических элементов? 12. Что представляют собой положительные и отрицательные ионы? Как они образуются?
Что представляют собой положительные и отрицательные ионы? Как они образуются?
Строение электронных оболочек атома
Урок 8. Химия 8 класс
Данный видеофрагмент поможет учащимся вспомнить строение атома, познакомит с электронными оболочками атомов, раскрывает физический смысл номера группы и номера периода, на конкретных примерах показан принцип составления электронной и графической схемы атома, урок наглядный и станет понятным для любого учащегося.
Конспект урока “Строение электронных оболочек атома”
Быть может, эти электроны –
Миры, где пять материков,
Искусство, знания, войны, троны
И память сорока веков.
Вспомним,
из чего состоит атом. Помните планетарную модель строения атома,
согласно которой, в центре атома расположено положительно заряженное ядро,
вокруг которого вращаются отрицательно заряженные электроны, подобно тому,
как вращаются планеты вокруг Солнца.
Строение атома
Электроны, двигаясь вокруг ядра, в совокупности образуют электронную оболочку атома. Число электронов в атоме равно числу протонов в ядре и соответствует порядковому номеру элемента.
Электроны двигаются в определённом порядке и различаются своей энергией. Электроны с маленьким запасом энергии расположены ближе к ядру, они связаны крепко с ядром и их тяжелее вырвать из электронной оболочки. А вот электроны с большим запасом энергии, напротив, находятся дальше от ядра, слабо с ним связаны, поэтому их легче оторвать.
Несмотря на это, в атоме находятся электроны, которые имеют близкие значения энергии. Эти электроны образуют электронные слои, или энергетические уровни.
Чтобы
определить число энергетических уровней, достаточно знать номер периода, в
котором находится данный элемент. Например, у азота семь
электронов в атоме, и два энергетических уровня. Теперь распределим эти семь
электронов по уровням. Получается на первом их 2, а на втором – оставшиеся 5.
Теперь распределим эти семь
электронов по уровням. Получается на первом их 2, а на втором – оставшиеся 5.
Максимальное число электронов на энергетическом уровне определяется по формуле: 2n2, где n – номер периода.
Если подставить значения первых трех периодов, то получится, что максимально на первом энергетическом уровне возможно только 2 электрона, на втором – 8, на третьем – 18.
Число электронов на внешнем энергетическом уровне для элементов главных подгрупп равно номеру группы.
Рассмотрим это на примере атома натрия.
Ядро
атома натрия имеет заряд +11, т.е. и электронов в атоме тоже 11.
Натрий находится в третьем периоде, значит, у него три энергетических
уровня, которые мы будем изображать в виде скобки «)». Это записывают с
помощью электронной формулы следующим образом: 11Na
2ē, 8ē, 1ē.
И так, на первом уровне 2 электрона (это максимально), на втором – 8 (больше быть не может), а на третий остается один электрон. Вот этот электрон и будет электроном внешнего энергетического уровня. Натрий – элемент главной подгруппы I группы, поэтому число электронов на внешнем уровне равно номеру группы, т.е. единице.
Двигаясь, электроны образуют своеобразный рисунок, так называемое электронное облако, которое можно ещё назвать орбиталью. Электронное облако, или орбиталь, – пространство вокруг ядра, где наиболее вероятно нахождение данного электрона.
На
всех энергетических уровнях есть s-орбитали,
они сферической формы, и она только одна, на втором уровне уже появляются p-орбитали,
которые имеют форму гантели, их всего три. На каждой орбитали максимально может
находится не более двух электронов, следовательно, на s-орбитали
– их два, на р-орбитали – шесть.
Для того, чтобы записать электронную формулу атома, для обозначения уровня используют арабские цифры, орбитали соответственно буквами s и р, а число электронов данной орбитали – арабской цифрой сверху справа над буквой орбитали.
Например, азот будет иметь электронную формулу 1s22s22p3.
Если элементы имеют одинаковое число электронов на внешнем уровне, значит, у них будут схожие свойства. Вспомните, благородные газы – инертны, не вступают в химические реакции, ведь у них, кроме гелия, восемь электронов на внешнем уровне, который считается завершенным. Вот почему они все инертны.
Предыдущий урок 7 Структура периодической таблицы элементов
Следующий урок 9 Ионная связь
Получите полный комплект видеоуроков, тестов и презентаций Химия 8 класс
Чтобы добавить комментарий зарегистрируйтесь или войдите на сайт
Строение атома – электронная конфигурация, структура и модели
Любые материальные объекты во Вселенной состоят из вещества. А оно представляет собой упорядоченные и сложные структуры, построенные из мельчайших частиц. К таким частицам относятся молекулы, атомы, электроны и кварки. Именно атом долгое время считался основной и неделимой единицей материи, о чем и говорит его название, которое с древнегреческого переводится как «неделимый». Но, как оказалось впоследствии, строение атома очень далеко от полностью неделимого.
А оно представляет собой упорядоченные и сложные структуры, построенные из мельчайших частиц. К таким частицам относятся молекулы, атомы, электроны и кварки. Именно атом долгое время считался основной и неделимой единицей материи, о чем и говорит его название, которое с древнегреческого переводится как «неделимый». Но, как оказалось впоследствии, строение атома очень далеко от полностью неделимого.
Содержание
- Как устроен атом
- Ядро: протоны и нейтроны
- Процесс ионизации
- Что такое электрон
- Немного истории
- Природа частицы
- Электронная конфигурация
- Наглядная запись
- Различные атомные модели
Как устроен атом
Со временем учёные выяснили, что они крупно заблуждались: структура атома оказалась вовсе не монолитной. С постепенным увеличением точности приборов стало ясно, что она включает в себя 3 типа микрочастиц: положительно, отрицательно и нейтрально заряженные. Называются они следующим образом:
Называются они следующим образом:
Частицы, несущие положительный заряд, назвали протонами, нейтральный — нейтронами, отрицательный — электронами.
Основа любого атома — это его ядро. Оно состоит из положительных и нейтральных микрочастиц, то есть из протонов и нейтронов. Их количество может быть одинаковым, а может и разниться. В результате получается, что ядро — это всегда положительно заряженная часть атома. Однако сам он заряжен нейтрально, и причина тому — электроны, летающие вокруг ядра по орбитальным спиралям. Такова общая схема строения атома.
Свойства вещества, которое может образовывать атом, напрямую зависят от количества микрочастиц в его составе. Каждая из них абсолютно идентична другой аналогичной микрочастице, поэтому они полностью взаимозаменяемы. Все электроны являются химическими «клонами» друг друга, то же самое правило касается протонов и нейронов. Именно поэтому ко всему веществу, имеющемуся в природе, можно применять общие законы химии, на основании которых оно будет работать.
Именно поэтому ко всему веществу, имеющемуся в природе, можно применять общие законы химии, на основании которых оно будет работать.
Любые атомы состоят всего лишь из трёх простых микрочастиц, представленных в разных количествах. А более сложные структуры, молекулы, являются сочетаниями различных атомов, взятых в определённых пропорциях, то есть все без исключения объекты в природе — как живые, так и неживые, как очень сложные по своей структуре, так и простейшие — построены всего из трёх типов мелких «кирпичиков». Если в этот факт как следует вдуматься, он действительно способен поразить воображение.
Ядро: протоны и нейтроны
Общее название для составных частиц ядра, коими являются протоны и нейроны — нуклоны. Вместе они и составляют почти всю массу атома, а значит, и почти всю материю во Вселенной. Теория гласит, что каждый протон или нейтрон включает в себя ровно 3 составные частицы, именуемые кварками, между которыми имеется связующее глюонов облако. Кварки, согласно модели, являются такими же неделимыми частицами, как электроны. Глюоны же обеспечивают их взаимную связь друг с другом.
Кварки, согласно модели, являются такими же неделимыми частицами, как электроны. Глюоны же обеспечивают их взаимную связь друг с другом.
В то же время сами атомные ядра чрезвычайно малы. Размеры каждого ядра в десятки тысяч раз меньше размеров всего атома. Но несмотря на это, почти вся атомная масса заключается в его положительно заряженном ядре, тогда как электрон представляет собой чисто энергетическую, нематериальную частицу. Получается, что материального вокруг нас вовсе не так много, как кажется на первый взгляд. Куда больше места занимают энергетические потоки, связывающие физическое вещество.
Число протонов, содержащихся в том или ином атоме, указывает на его порядковый номер в Периодической системе химических элементов. Например, у кислорода порядковый номер 8, а значит, и число протонов у него точно такое же. Формула, по которой вычисляется количество нейтронов: округлённая атомная масса минус число протонов. Атомная масса элемента указана под его порядковым номером в графической таблице Менделеева. Например, для атома хлора (Cl) это будет 35 — 17 = 18, для брома (Br) 80 — 35 = 45, а для серы (S) 32 — 16 = 16. С числом нейтронов связано понятие изотопа.
Например, для атома хлора (Cl) это будет 35 — 17 = 18, для брома (Br) 80 — 35 = 45, а для серы (S) 32 — 16 = 16. С числом нейтронов связано понятие изотопа.
Процесс ионизации
Количество электронов в «чистом» атоме должно уравновешивать число протонов. Если же оно несколько больше или меньше, чем нужно, атом перестаёт быть нейтральным и обретает положительный или отрицательный заряд. Если электроны отсоединяются, общий заряд увеличивается, а в случае их присоединения — наоборот, уменьшается. Преобразованный таким образом атом называется ионом.
Возьмём для примера медь (Cu), относящуюся к классу простых веществ. В обычном состоянии у неё имеется 29 электронов. Но если она отдаст 2 электрона, у неё их останется всего 27. А сам атом меди превратится в положительный ион меди или, иначе, в катион меди. В их роли часто выступают всевозможные металлы (магний, алюминий, литий, натрий, хром), которые могут легко терять до трёх электронов.
Отрицательно заряженные ионы, в свою очередь, называются анионами.
Как правило, они являются неметаллами, так как обладают высокой электроотрицательностью — способностью притягивать к себе электроны. Например, им может стать атом кремния, присоединив к себе хотя бы один электрон.
Что такое электрон
Электроны, двигающиеся вокруг ядра по сферической траектории, образуют так называемое электронное облако. А оно уже создаёт вокруг каждого атома его личное электромагнитное поле, оказывающее влияние на другие атомы.
Немного истории
В 1891 году в результате проведённых экспериментов ирландский физик Стони сумел вывести, что электричество переносится мельчайшими частицами, которые имеются в составе любого атома. Тогда же он и предложил назвать их электронами.
Спустя несколько лет, физики Перрен и Томсон нашли доказательства, что электрон имеет сугубо отрицательный заряд. Кроме того, они смогли рассчитать массу и скорость электрона.
Кроме того, они смогли рассчитать массу и скорость электрона.
Природа частицы
Отрицательная частица электрон имеет крайне маленькие размеры. Отдельные электроны не поможет разглядеть даже самый мощный микроскоп. Визуально их можно наблюдать только в виде размытого электронного облака вокруг ядра. Электрон — это устойчивая частица энергии, которая постоянно находится в движении. Вне движения он просто не существует. И не похоже, чтобы у этой энергетической единицы была какая-то структура. Но масса у него всё-таки есть, хотя, как и его габариты, она очень маленькая.
В теории электрон включает в себя 3 нематериальные квазичастицы, несущие о нём различную информацию. Всего их 3:
Но это всего лишь условности, и они никак не указывают, что электрон и правда можно поделить на отдельные частицы.
На текущем уровне развития науки эта частица пока считается неделимой. И нет оснований полагать, что в будущем это может измениться.
Электроны обладают способностью поглощать энергию. В случаях, когда это происходит, атом, который в себе их содержит, переходит с одного энергетического уровня на другой. Если поглощенной энергии слишком много, электрон может выйти из атомной структуры и стать независимой частицей. При этом он будет проявлять волновые свойства.
Электронная конфигурация
Электронная конфигурация атома — схематическое отображение отрицательных частиц, расположенных на атомных орбиталях. Умея делать такую запись, можно очень быстро определять количество орбиталей у того или иного атома. Перед тем как приступать к определению самой конфигурации, необходимо найти порядковый номер и заряд нужного элемента.
Любой атом состоит из нескольких электронных оболочек. Их максимальное количество достигает семи. Каждая из них имеет подуровни, заполняемые электронами последовательно, в строго установленном порядке. Число подуровней, содержащееся в той или иной оболочке, равняется её номеру. Внешние слои с большим количеством подуровней, находящиеся дальше от ядра, имеют большую энергию по сравнению с внутренними, чьё расположение близко к ядру.
Число подуровней, содержащееся в той или иной оболочке, равняется её номеру. Внешние слои с большим количеством подуровней, находящиеся дальше от ядра, имеют большую энергию по сравнению с внутренними, чьё расположение близко к ядру.
Всего есть 6 типов подуровней, каждый из которых может содержать определённое число орбиталей. Электроны на каждом из них, когда они заполнены полностью, располагаются в чётном количестве. Эти подуровни обозначаются следующими буквами:
Орбитали заполняются в следующем порядке:
1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, 5d, 6p, 7s, 5f, 6d, 7p.
Цифра справа обозначает номер оболочки, буква слева — подуровень этой оболочки.
Наглядная запись
Теперь возьмём для примера какой-нибудь химический элемент. Например, калий. В таблице Менделеева он имеет запись K и его можно найти под номером 19. Значит, у него имеется 19 электронов, которые нужно расфасовать по орбиталям в указанном порядке. Делаем это.
Сначала идёт уровень 1s. Подуровень s может содержать только 2 электрона. Число электронов записывается в виде маленького индекса над буквой. В данном случае это будет 1s2.
Следом по порядку идёт 2s. Тоже s и тоже только 2 электрона. 2s2 .
Дальше 2p. Смотрим, сколько электронов может содержать уровень p. 2p6.
Теперь снова возвращаемся на подуровень s, который опять-таки включает в себя всего лишь 2 электрона. 3s2 .
12 уже упорядочено. Осталось 7. И следующий уровень — 3p6.
Остался всего один электрон, который нужно разместить на следующем s-подуровне. В результате на нём остаётся одно свободное место — всего частиц может быть 2, но мы располагаем только одну оставшуюся. А записывается это как 4s1.
В одну строчку это всё записывается следующим образом: 1s2 2s2 2p6 3s2 3p6 4s1.
Важно учитывать, что это электронная конфигурация для основного состояния атома. В Периодической системе элементов у атомов тоже указаны исключительно те их свойства, которыми они обладают в своём основном состоянии. Но также они могут пребывать и в возбуждённом состоянии. Это происходит при сообщении им дополнительной энергии. Тогда электроны с положенных им орбиталей будут перескакивать на другие и запись будет несколько иной.
Различные атомные модели
Ещё философы Древней Греции — колыбели науки, пытались постичь природу этой необыкновенной частицы. Особенно среди прочих выделился Демокрит. И пусть с вершины нынешней науки его идеи кажутся немного наивными и примитивными, на тот момент это всё же был большой прорыв.
Особенно среди прочих выделился Демокрит. И пусть с вершины нынешней науки его идеи кажутся немного наивными и примитивными, на тот момент это всё же был большой прорыв.
По мнению философа, из атомов состоит даже такая неосязаемая субстанция, как человеческая душа. Ещё он считал, что каждый отдельный атом имеет примерно те же физические свойства, что и вещество, которое он образует. Например, огонь, как он думал, должен иметь острые атомы, а вода — наоборот, гладкие.
Английский физик Дж. Томсон тоже внёс значительный вклад в развитие представлений об атомном устройстве. Но несмотря на это, и его идеи были несколько ошибочными. В 1904 году он выдвинул модель, рассматривающую атом в качестве физического тела, имеющего положительный заряд, внутри которого располагались отрицательно заряженные частицы.
В том же году, что и Томсон, Х. Нагаока предложил планетарную модель атома, которая была уже ближе к истине, но все равно не дотягивала до неё. В его модели строения атома электроны подобны кольцам Сатурна, и по тому же принципу крутятся вокруг ядра с положительным зарядом.
Последняя предложенная модель была разработана совместно Бором и Резерфордом. Она же и является устоявшейся в современном учёном мире. Практически все последующие научные наработки берут за основу именно их теорию строения атома, лишь с некоторыми незначительными изменениями. Её так и назвали — модель Резерфорда-Бора.
Предыдущая
ХимияИонная химическая связь – свойства, механизм образования и примеры веществ
Следующая
ХимияЗадачи по органической химии – примеры с решениями
Рисунок атома – Как нарисовать атом шаг за шагом
Возможно, мы не сможем увидеть атомы невооруженным глазом, но технически вы видите их везде, куда бы вы ни посмотрели!
Атомы составляют всю окружающую нас материю, и удивительно думать, что на микроскопическом уровне эти крошечные клетки составляют все, что мы видим и с чем взаимодействуем. Атомы очень важны, но также может быть интересно научиться рисовать атом!
Атомы очень важны, но также может быть интересно научиться рисовать атом!
С помощью этого руководства вы будете точно знать, как это сделать.
Мы надеемся, что вам понравится это пошаговое руководство о том, как нарисовать атом за 6 шагов!
О чем эта запись в блоге
- Как нарисовать атом — приступим!
- Шаг 1
- Шаг 2 – Нарисуйте следующий овал для вашего атома
- Шаг 3 – Затем нарисуйте еще один овал для вашего атома
- Шаг 4 – Теперь начните рисовать некоторые детали вашего атома Добавьте ядро атома
- Шаг 6. Завершите рисунок атома цветом
- 3 Еще несколько советов, которые облегчат рисование атомов!
- Ваш атомный рисунок готов!
Шаг 1
В этом первом шаге нашего руководства по рисованию атома мы начнем с очень простой формы. На самом деле мы будем строить атом, используя несколько экземпляров одной и той же формы.
Эта форма будет длинным овалом, а первая будет вертикальной. В идеале вы хотели бы, чтобы все последующие овалы, которые вы будете рисовать, были одного размера.
В идеале вы хотели бы, чтобы все последующие овалы, которые вы будете рисовать, были одного размера.
Вы можете убедиться в этом, используя трафарет или обведя что-то плоское и овальное.
В противном случае вы можете измерить длину и ширину этого овала и попытаться воспроизвести его в следующих шагах. Как только вы нарисуете этот овал, вы будете готовы к следующему шагу!
Шаг 2 – Нарисуйте следующий овал для вашего атомаВы сделали первый овал вашего атомного рисунка, и теперь вы можете добавить еще один на этом шаге. Как мы упоминали в предыдущем шаге, вы должны изо всех сил стараться, чтобы этот овал был идентичен по размеру и форме первому.
Вот почему использование чего-то вроде трафарета для обводки было бы идеальным для такого рода рисунков! Как бы вы ни нарисовали его, этот овал будет проходить по диагонали над другим овалом.
Шаг 3 – Затем нарисуйте еще один овал для вашего атома Теперь вы действительно освоились! Прежде чем мы добавим некоторые детали частиц к атому, у нас есть еще один овал, который нужно добавить на этом этапе нашего руководства по рисованию атома.
Этот также будет проходить по диагонали над первым овалом, за исключением того, что этот будет идти в направлении, противоположном тому, что на предыдущем шаге.
Нарисовав все овалы, мы перейдем к окончательным деталям частиц в следующих нескольких шагах, так что давайте двигаться дальше!
Шаг 4 – Теперь начните рисовать некоторые детали вашего атомаНа этом этапе рисования вашего атома мы добавим некоторые мелкие детали частиц на атом. Они будут маленькими и простыми, но с их помощью ваш атом будет выглядеть как настоящий!
Для этого просто нарисуйте несколько маленьких кругов на линиях атома, которые вы рисовали до сих пор.
Для этого руководства мы нарисовали три, но вы можете нарисовать больше или меньше, если хотите, а также изменить их положение на атоме.
Тогда нам нужно добавить еще один важный элемент, прежде чем вы начнете раскрашивать свой атомный рисунок!
Шаг 5 – Добавьте ядро атома Центр атома называется ядром, и это самая важная часть атома! К счастью, хотя это может быть очень важно, на этом этапе нашего руководства по рисованию атома будет очень легко рисовать.
Все, что вам нужно сделать, это нарисовать круг в центре атома. Если вы хотите нарисовать идеальный круг для центра, вы можете использовать чертежный циркуль или обвести что-то круглое и плоское, чтобы сделать это.
Прежде чем двигаться дальше, вы также можете добавить некоторые детали и элементы самостоятельно! Мы упоминали о том, чтобы добавить больше частиц к атому или изменить их положение, но вы также можете придумать еще больше творческих идей.
Возможно, вы могли бы нарисовать еще несколько атомов, плавающих на заднем плане! Что вы можете придумать, чтобы закончить этот рисунок атома, прежде чем перейти к последнему шагу?
Шаг 6 – Завершите рисунок атома цветомЭто подводит вас к последнему этапу рисования атома, и это шаг, на котором вы получите массу удовольствия, добавляя цвет к своему рисунку!
Мы сделали его простым и чистым для нашего изображения, и мы использовали красный, синий и желтый цвета для различных частиц атома. Однако это всего лишь предложение, и у вас есть много вариантов того, как вы можете раскрасить это изображение!
Однако это всего лишь предложение, и у вас есть много вариантов того, как вы можете раскрасить это изображение!
Вам также не нужно ограничиваться раскрашиванием только частиц атома, вы также можете раскрасить промежутки между овалами, которые вы нарисовали.
У вас также есть безграничные варианты цветов, которые вы можете использовать, так что это прекрасная возможность использовать все ваши любимые цвета!
Вы можете весело провести время, выбирая цвета, но вы также можете отлично провести время, играя с вашими любимыми художественными средствами, чтобы воплотить их в жизнь.
Независимо от того, хотите ли вы сохранить цвета яркими и яркими или более холодными и приглушенными, мы знаем, что вы сделаете этот атомный рисунок еще лучше!
3 Еще несколько советов, которые облегчат рисование атомов!Создайте этот рисунок, пока мы покажем вам, как сделать легко рисуемый атом еще проще!
Один из самых простых способов облегчить восприятие этого рисунка атома — нарисовать его как можно больше.
Структура атома может быть довольно сложной и запутанной, поэтому чем меньше вы сделаете ее, тем сложнее она будет.
Если вы сделаете его красивым и большим, вы также можете начать использовать инструменты для рисования, такие как циркуль, чтобы упростить рисование кругов.
Вы также можете использовать более толстые инструменты для рисования, такие как маркеры или ручки, чтобы сделать линии более гладкими.
Увеличение размера рисунка сделает его более впечатляющим!
Подготовка является ключом к облегчению любого рисунка, и это относится к этому рисунку атома. В предыдущем шаге мы упомянули, что может помочь рисование большого изображения, но вы также можете использовать карандаш для подготовки.
Работать карандашом очень удобно, так как вы можете стереть любые ошибки. Таким образом, вы можете сосредоточиться на самом рисунке, не отвлекаясь.
Затем, когда вы довольны тем, как выглядят линии карандаша, вы можете переключиться на более стойкие средства, чтобы тщательно пройтись по линиям. Как только вы стерли карандаш, никто никогда не узнает, что вы его использовали!
Как только вы стерли карандаш, никто никогда не узнает, что вы его использовали!
Иногда хороший способ преодолеть трудности в рисовании — отвлечь внимание от проблемных областей. Допустим, вы сделали одну часть своего наброска атома слишком длинной, и уже слишком поздно ее исправлять.
Как художник, легко зациклиться на такой ошибке, но большинство людей даже не заметят ее! Один из способов убедиться, что это так, — добавить несколько меток.
Вы можете сделать это, посмотрев на схему атома, чтобы увидеть, как называются различные части. Затем нарисуйте несколько линий, отходящих от вашего атома с этими метками.
Таким образом, люди будут обращать внимание на это, а не на мелкие ошибки!
Ваш атомный рисунок готов!
Это подводит вас к концу этого руководства как нарисовать атом . Мы надеемся, что это руководство показало вам, что рисование атома не обязательно должно быть сложной задачей!
Кроме того, мы надеемся, что это руководство показало вам, что рисование атома может быть увлекательным и увлекательным занятием.
Завершение этого руководства — лишь часть веселья! Вы также можете продолжить этот рисунок, добавляя свои собственные детали и элементы.
Мы упомянули несколько идей, таких как рисование большего количества атомов на заднем плане или изменение дизайна, но что еще вы можете придумать?
Если вы готовы к большему, на нашем сайте есть еще много замечательных руководств по рисованию. Они охватывают огромное разнообразие тем, так что каждый найдет что-то для себя! Обязательно заходите почаще, так как мы часто загружаем новые.
Как только ваш рисунок атома будет готов, мы надеемся, что вы поделитесь им, чтобы мы могли его увидеть на наших страницах в Facebook и Pinterest. Нам не терпится увидеть ваши работы!
Как нарисовать атом
254 акции
Узнайте, как нарисовать красивый атом с шаг за шагом, видео и инструкции 90 Атом Теперь вы можете легко создать красивый рисунок атома.
Перейти к пошаговым инструкциям.
Атом — это «мельчайшая единица, на которую можно разделить материю без высвобождения электрически заряженных частиц». Атомы считаются строительными блоками химии.
Знаете ли вы? Атомы в основном пустое пространство. Подобно тому, как планеты вращаются вокруг Солнца на большом расстоянии друг от друга, крошечные протоны и нейтроны ядра далеки от крошечных электронов.
Электроны одного атома могут взаимодействовать с электронами другого, образуя химические связи и строя молекулы.
Каждый тип атома может быть идентифицирован как определенный элемент в периодической таблице. В нашем руководстве по рисованию изображен литий, третий элемент, потому что у него три электрона.
Прокрутите вниз, чтобы загрузить PDF-файл этого руководства.
Атом в нашем руководстве по рисованию — это упрощенная версия атома. Такие диаграммы часто используются на уроках естествознания, в мультфильмах и на вывесках, указывающих на радиацию.
Это диаграмма в старом стиле; теперь известно, что точное местоположение электронов обнаружить невозможно. Поэтому электроны теперь изображаются как «облако», а не как единый объект с фиксированным вращением.
У многих мультипликационных персонажей атом является эмблемой. К ним относятся Atom Ant, Atom и Captain Atom.
Хотите нарисовать мультяшный атом? Это простое пошаговое руководство по рисованию мультфильмов поможет вам научиться этому.
Все, что вам нужно, это карандаш, ластик и лист бумаги.
Если вам понравился этот урок, см. Также следующие руководства по рисованию: Cartoon Scientist, Microscope и Rick из Rick and Morty.
Пошаговые инструкции по рисованию атома
Как нарисовать красивый атом для детей, начинающих и взрослых. Шаг 1
1. Начните с рисования круга. Это сформирует ядро атома.
Easy Atom Drawing – Шаг 2
2. Нарисуйте круг меньшего размера на некотором расстоянии от первого круга. Это формирует первый электрон.
Easy Atom Drawing – Step 3
3. Нарисуйте неполный овал вокруг ядра. Электрон должен находиться в центре, как если бы линия проходила через него. Этот овал указывает путь вращения электрона вокруг ядра.
Easy Atom Drawing — Шаг 4
4. Нарисуйте еще одну изогнутую линию примерно параллельно первой. Начните с электрона и подведите линию к открытому концу незавершенного овала в острой точке.
Easy Atom Drawing – Step 5
5. Нарисуйте еще один маленький кружок за пределами овала, образуя еще один электрон.
Easy Atom Drawing – Шаг 6
6. Нарисуйте еще один путь вращения, как если бы он проходил позади первого. Нарисуйте пару изогнутых линий между электроном и предыдущим путем. На другой стороне пути нарисуйте еще один набор изогнутых линий, стирая при необходимости. Наконец, нарисуйте две короткие линии, которые встречаются в одной точке.
Easy Atom Drawing — Шаг 7
7. Нарисуйте третий электрон в виде маленького кружка сразу за пределами рисунка.
Добавьте больше деталей к вашему изображению атома – Шаг 8
8. Нарисуйте траекторию вращения этого электрона, проходящую позади двух других. Сначала нарисуйте пару изогнутых линий между электроном и почти горизонтальным вращением. Затем нарисуйте изогнутые линии между вертикальным и горизонтальным поворотами, стирая при необходимости. Нарисуйте две линии в форме буквы «С», выгибающиеся наружу от этого пути вращения и возвращающиеся к нему. Нарисуйте еще одну пару изогнутых линий между двумя поворотами и последнюю пару, которая встречается в острой точке.
Завершите набросок вашего рисунка атома – шаг 9
9. Нарисуйте одинарные или двойные кривые линии сразу за крайними точками траекторий вращения. Это помогает создать ощущение движения, когда электроны вращаются вокруг ядра.
Раскрась свой рисунок атома
Раскрась свой мультяшный атом. На схемах атомов протоны, нейтроны и электроны часто окрашиваются в разные цвета. Вы можете создать знак «Осторожно: радиация», покрасив свой атом в черный цвет и придав ему желтый фон.
Дополнительные уроки по рисованию вещей см. в посте «100 простых вещей для рисования художественных проектов для детей».
Простое пошаговое руководство по рисованию атомаНажмите ЗДЕСЬ, чтобы сохранить урок в Pinterest!
Учебное пособие по рисованию атома — легко и весело Страницы для печати
УСТРАНЕНИЕ НЕИСПРАВНОСТЕЙ ДЛЯ УЧАСТНИКОВ
Все еще видите рекламу или не можете загрузить PDF-файл?
Во-первых, убедитесь, что вы вошли в систему. Вы можете войти на странице входа участника.
Если вы по-прежнему не можете загрузить PDF-файл, вероятное решение — перезагрузить страницу.
Это можно сделать, нажав кнопку перезагрузки браузера.
Это значок в виде круглой стрелки в верхней части окна браузера, обычно расположенный в верхней левой части (вы также можете использовать сочетания клавиш: Ctrl+R на ПК и Command+R на Mac).
Учебник по основам химии 2, Рисование атомов – изучение биологии
Атомы (Учебник по основам химии 1) посвящен общей структуре атомов. Здесь вы узнаете, как определить конкретную структуру атома, что подготовит нас к изучению химических связей в следующих уроках.
Здесь вы узнаете, как определить конкретную структуру атома, что подготовит нас к изучению химических связей в следующих уроках.
Если вы уже смотрели видео, нажмите здесь или прокрутите вниз под видео, чтобы начать взаимодействие.
1. Простейшие атомы: водород и гелий
Наиболее распространенным элементом во Вселенной является водород , газ, составляющий около 99% известной массы Вселенной 1 . Водород является основным компонентом звезд, а звезда, безусловно, является самым массивным объектом в любой солнечной системе.
1 Это не считая «темной материи», которая выходит за рамки этого курса.Атомы водорода имеют один протон и один электрон. Таким образом, мы можем представить водород следующим образом:
Водород: один протон и один электрон. Стрелка указывает на первый энергетический уровень. Водород имеет один-единственный протон, который входит в ядро. Вне ядра вращается один электрон, который находится на первом энергетическом уровне.
Вне ядра вращается один электрон, который находится на первом энергетическом уровне.
[стиль qwiz = «ширина: 528 пикселей; минимальная высота: 0px; граница: 3 пикселя, сплошной черный цвет; qrecord_id=”sciencemusicvideosMeister1961-Рисование атомов, предсказание гелия”]
[ч]Предсказать!
[q] Гелий — второй по распространенности элемент во Вселенной. Атомы гелия имеют два протона, два нейтрона и два электрона. Посмотрите, сможете ли вы расширить то, что мы уже узнали, и нарисовать диаграмму гелия. После того, как вы нарисовали его, нажмите «показать ответ», чтобы увидеть, правильно ли вы его нарисовали.
[c]wqBzaG93IHRo ZSBhbnN3ZXI=[Qq]
[f]IEFOU1dFUg==
Cg==
[Qq]Гелий: 2 протона, 2 нейтрона и 2 электрона . Стрелка указывает на первый энергетический уровень. В ядре гелия два протона и два нейтрона. Два электрона вращаются вокруг ядра на первом энергетическом уровне (также называемом «оболочкой» или «орбитой»). Обратите внимание, что термин «орбитальный», используемый в сопроводительном видео, имеет немного более техническое значение, и мы будем его здесь избегать.
Обратите внимание, что термин «орбитальный», используемый в сопроводительном видео, имеет немного более техническое значение, и мы будем его здесь избегать.
[x]
[/qwiz]
Прежде чем продолжить, убедитесь, что вы нажали «показать ответ» и изучили диаграмму выше.
2. Правило октета
Для атомов с более чем двумя протонами и двумя электронами необходимо ввести несколько правил, чтобы изобразить их таким образом, чтобы они представляли их химические свойства. 1
1 Когда вы изучаете атомы на уроках химии, вы изучаете гораздо более сложную и точную модель расположения электронов. Но для биологии, которую вы будете изучать на вводном курсе средней школы (или даже колледжа), следующие правила будут работать.Первое правило называется правилом октетов. «Октет» относится к восьми электронам, как вы увидите ниже. Ключевыми частями правила являются:
- Каждый из энергетических уровней, на которых находятся электроны, имеет фиксированную способность удерживать электроны.

- На первом энергетическом уровне может находиться до двух электронов.
- Второй и третий энергетические уровни могут содержать до восьми электронов (отсюда «октет»).
- Когда один энергетический уровень заполнен, вы начинаете заполнять следующий.
Давайте воспользуемся правилом октетов, чтобы нарисовать атом лития.
[стиль qwiz = «ширина: 528 пикселей; минимальная высота: 0px; граница: 3 пикселя, сплошной черный цвет; qrecord_id=”sciencemusicvideosMeister1961-Drawing Atoms, Predict Lithium”]
[h]Предсказать!
[q]Литий — это металлический элемент, который имеет 3 протона, 4 нейтрона и 3 электрона. Первые два электрона переходят на первый энергетический уровень. При заполнении первого энергетического уровня следующий электрон переходит на второй энергетический уровень. Используйте описание правила октета, чтобы нарисовать диаграмму лития. После того, как вы нарисовали его, нажмите «показать ответ», чтобы увидеть, правильно ли вы его нарисовали.
[c]wqBzaG93IHRo ZSBhbnN3ZXI=[Qq]
[f]IEFOU1dFUg==
Cg==
[Qq] Литий: 3 протона, 4 нейтрона и 3 электронаВ литии в ядре находятся три протона и четыре нейтрона. Два электрона вращаются вокруг ядра на первом энергетическом уровне (также называемом «оболочкой»). Третий электрон переходит на второй энергетический уровень.
[x]
[/qwiz]
Прежде чем продолжить, убедитесь, что вы нажали «показать ответ» и изучили диаграмму выше.
С этого момента мы будем упрощать наши схемы, рисуя ядро по-другому.
- Вместо отдельных протонов и нейтронов нарисуйте кружок, чтобы обозначить ядро.
- Напишите количество протонов и нейтронов внутри круга.
Ниже слева вы можете увидеть это новое представление лития, рядом с тем, которое мы использовали ранее.
Литий: 3 протона, 4 нейтрона, 3 электрона | Литий: 3 протона, 4 нейтрона, 3 электрона |
| Новое представление лития (обратите внимание, как протоны и нейтроны обозначены в ядре) | Предыдущее изображение лития, показывающее отдельные протоны и нейтроны |
Чтобы представить атомы следующих нескольких элементов, нам нужно еще одно правило: размещайте электроны на энергетическом уровне по одному, пока у вас не будет четыре, а затем соединяйте их в пары, пока вы не заполните энергетический уровень 8 электронами. Как мы увидим, это правило поможет вам понять, что происходит, когда мы узнаем о химических связях, когда электроны обмениваются или делятся электронами. Следуя этому правилу, мы можем нарисовать следующие атомы через весь неон.
Как мы увидим, это правило поможет вам понять, что происходит, когда мы узнаем о химических связях, когда электроны обмениваются или делятся электронами. Следуя этому правилу, мы можем нарисовать следующие атомы через весь неон.
[стиль qwiz = «ширина: 528 пикселей; минимальная высота: 0px; граница: 3 пикселя, сплошной черный цвет; qrecord_id=»наукамузыкавидеоMeister1961-Drawing Atoms, Predict B, C, и N”]
[h]Предсказать!
[q]Используя то, что вы знаете о правиле октета, нарисуйте еще три атома
- Бор: 5 протонов, 6 нейтронов, 5 электронов
- Углерод: 6 протонов, 6 нейтронов, 6 электронов
- Азот: 7 протонов, 7 нейтронов, 7 электронов
После того, как вы их нарисовали, нажмите «показать ответ», чтобы проверить, правильно ли вы их нарисовали.
[c]wqBzaG93IHRo ZSBhbnN3ZXI=[Qq]
[f]IEFOU1dFUg==
Cg==
| [Qq] Бор | Углерод | Азот |
Два электрона идут на первом энергетическом уровне. Следующие три переходят на второй энергетический уровень. Каждый внешний электрон неспарен. Следующие три переходят на второй энергетический уровень. Каждый внешний электрон неспарен. | Два электрона переходят на первый энергетический уровень. Следующие четыре переходят на второй энергетический уровень. Каждый внешний электрон неспарен. | Два электрона переходят на первый энергетический уровень. Следующие пять переходят на второй энергетический уровень. Один из внешних электронов должен быть спарен. |
[x]
[/qwiz]
Прежде чем продолжить, убедитесь, что вы изучили ответ на указанный выше вопрос.
2а. Элементы с 3 по 10 (от лития до неона)
В приведенной ниже таблице показаны все атомы во второй строке периодической таблицы элементов. Изучите его и убедитесь, что расположение электронов имеет для вас смысл, прежде чем продолжить.
2б. Элементы с 11 по 20
Если число электронов в атоме превышает 10 (предел первых двух энергетических уровней), то следующие электроны переходят на третий энергетический уровень. Правила заполнения третьего энергетического уровня такие же, как описано выше.
Правила заполнения третьего энергетического уровня такие же, как описано выше.
[qwiz style = «ширина: 528 пикселей; минимальная высота: 0px; граница: 3 пикселя, сплошной черный цвет; qrecord_id=”sciencemusicvideosMeister1961-Drawing Atoms, Predict Aluminium”]
[ч] Predict!
[q]Алюминий имеет 13 протонов, 14 нейтронов и 13 электронов. Используйте описание правила октета, чтобы нарисовать диаграмму алюминия. После того, как вы нарисовали его, нажмите «показать ответ», чтобы увидеть, правильно ли вы его нарисовали.
[c]wqBzaG93IHRo ZSBhbnN3ZXI=[Qq]
[f]IEFOU1dFUg==
Cg==
[Qq]АлюминийЧтобы нарисовать алюминий, поместите два электрона на первый энергетический уровень. Следующие восемь переходят на второй энергетический уровень. Остальные 3 электрона переходят на третий энергетический уровень.
[x]
[/qwiz]
Вот элементы с 10 по 18, которые находятся в третьей строке Периодической таблицы. Прежде чем читать дальше, убедитесь, что их расположение электронов имеет смысл.
Прежде чем читать дальше, убедитесь, что их расположение электронов имеет смысл.
И поскольку они довольно распространены среди живых существ, мы также добавим следующие два элемента. В этих элементах электроны начинают заполнять четвертый энергетический уровень.
Структура калия и кальция. Обратите внимание на электроны на четвертом энергетическом уровне.3. Обзор: четыре вещи, которые нужно знать о рисовании атомов
В этом уроке мы сосредоточились на понимании структуры атомов. Мы специально узнали, что
- Электроны находятся на энергетических уровнях вне ядра
- Первый энергетический уровень имеет емкость двух электронов
- Следующие два энергетических уровня имеют емкость по 8 электронов каждый.
- Эти правила об электронной емкости известны как правило октета.
Используя эти правила, если вам известно количество протонов в атоме, вы сможете вычислить расположение его электронов.
4. Проверка понимания (карточки: строение атома)
Чтобы проверить ваше понимание, мы начнем с нескольких карточек, а затем перейдем к интерактивной викторине.
[qdeck style=”border: 2px сплошной черный; qrecord_id=»наукамузыкавидеоMeister1961-Атомная структура/Рисование атомов. Карточки (M3)»]
[h] Карточки: «Атомная структура»
[i] Инструкции
- Нажмите «Проверить ответ», чтобы увидеть ответ на каждую карточку.
- Если вы это знаете, нажмите «Понятно».
- Если вы не знаете ее так хорошо, как хотели бы, нажмите «Нужно больше практики», и эта карта уйдет в конец колоды, чтобы вы могли попрактиковаться еще раз.
- «Перемешать» позволяет перетасовать колоду.
[!]КАРТА 1 ++++++++++++++++++++++++++++++++++++++++++++++ ++[/!]
[q] У углерода 6 протонов, 6 нейтронов, 6 электронов. На листе бумаги нарисуйте атом углерода, затем переверните карточку, чтобы проверить, правильно ли вы его нарисовали.
[a]
Протоны и нейтроны углерода входят в ядро. Первые два электрона переходят на первый энергетический уровень. Следующие четыре электрона переходят на второй энергетический уровень. Чтобы представить, как углерод образует химические связи, лучше всего изобразить все четыре электрона непарными.
[!]КАРТА 2 ++++++++++++++++++++++++++++++++++++++++++++++ ++++++++++++++++++++++++++++++++++++++++++++[/!]
[q] Натрий имеет 11 протонов, 11 нейтронов, 11 электронов. На листе бумаги нарисуйте атом натрия, затем переверните карточку, чтобы проверить, правильно ли вы его нарисовали.
[a]
Протоны и нейтроны натрия входят в ядро. Первые два электрона переходят на первый энергетический уровень. Следующие восемь электронов переходят на второй энергетический уровень и лучше всего изображаются четырьмя парами. Последний электрон переходит на третий энергетический уровень.
[!]КАРТА 3 ++++++++++++++++++++++++++++++++++++++++++++++ ++++++++++++++++++++++++++++++++++++++++++++++++++[/ !]
[q] Кислород имеет 8 протонов, 8 нейтронов и 8 электронов. На листе бумаги нарисуйте атом кислорода, затем переверните карточку, чтобы проверить, правильно ли вы его нарисовали.
На листе бумаги нарисуйте атом кислорода, затем переверните карточку, чтобы проверить, правильно ли вы его нарисовали.
[a]
Протоны и нейтроны кислорода проникают в ядро. Первые два электрона переходят на первый энергетический уровень. Следующие шесть электронов переходят на второй энергетический уровень. Лучший способ представить электроны — изобразить их в виде двух пар и еще двух одиночных электронов.
[!]КАРТА 4 ++++++++++++++++++++++++++++++++++++++++++++++ ++++++++++++++++++++++++++++++++++++++++++++++++++[/ !]
[q] Фосфор имеет 15 протонов, 15 нейтронов и 15 электронов. На листе бумаги нарисуйте атом фосфора, затем переверните карточку, чтобы проверить, правильно ли вы его нарисовали.
[a]
Протоны и нейтроны фосфора входят в ядро. Первые два электрона переходят на первый энергетический уровень. Следующие восемь электронов переходят на второй энергетический уровень. Следующие пять электронов переходят в третий.
[!]КАРТА 5 ++++++++++++++++++++++++++++++++++++++++++++++ ++++++++++++++++++++++++++++++++++++++++++++++++++[/ !]
[q] Калий имеет 19 протонов, 19 нейтронов, 19 электронов. На листе бумаги нарисуйте атом калия, затем переверните карточку, чтобы проверить, правильно ли вы его нарисовали.
[a]
Протоны и нейтроны калия входят в ядро. Первые два электрона переходят на первый энергетический уровень. Следующие восемь электронов переходят на второй энергетический уровень. Следующие восемь электронов переходят на третий энергетический уровень. Последний электрон переходит на четвертый энергетический уровень.
[!]КАРТА 6 ++++++++++++++++++++++++++++++++++++++++++++++++ ++++++++++++++++++++++++++++++++++++++++++++++++[/!]
[q] Азот имеет 7 протонов, 7 нейтронов и 7 электронов. На листе бумаги нарисуйте атом азота, затем переверните карточку, чтобы проверить, правильно ли вы его нарисовали.
[a]
Протоны и нейтроны азота входят в ядро. Первые два электрона переходят на первый энергетический уровень. Следующие пять электронов переходят на второй энергетический уровень. Лучший способ представить электроны — нарисовать их как одну пару и три одиночных электрона.
Первые два электрона переходят на первый энергетический уровень. Следующие пять электронов переходят на второй энергетический уровень. Лучший способ представить электроны — нарисовать их как одну пару и три одиночных электрона.
[x]
Если вы хотите попрактиковаться в этих терминах или понятиях, нажмите кнопку перезапуска ниже. В противном случае перейдите к финальной викторине.
[перезагрузка]
[/qdeck]
5. Тест: Структура атомов
Этот тест проверяет вас на все термины, которые вы уже изучили. Он также проверяет вашу способность правильно определять структуру атома.
[qwiz style = «граница: 3 пикселя, сплошной черный цвет; ” qrecord_id=”sciencemusicvideosMeister1961-Атомная структура/Викторина по рисованию атомов (M3)”]
[h] ВИКТОРИНА: Структура атомов
[i] В этой викторине рассматриваются ключевые понятия и термины, связанные со структурой атомов.
Вот как это работает.
- Викторина состоит из серии вопросов с несколькими вариантами ответов, но ведет себя как стопка карточек.

- Если вы правильно ответили на вопрос, вы переходите к следующему вопросу.
- Если вы ответите на вопрос неправильно, вы получите объяснение, после чего этот вопрос окажется в самом низу стека.
- Чтобы выйти из викторины, вы должны правильно ответить на каждый вопрос.
[q] Строительным блоком материи является
[c]IG51Y2xldXM=[Qq]
[c]IGF0 b20=[Qq]
[0Qv2g=9[0Q0g3R] [c]IGVsZWN0cm9uIA==[Qq]
[f]IE5vLiBUaGUgbnVjbGV1cyBpcyB0aGUgY2VudHJhbCBwYXJ0IG9mIHRoZSBidWlsZGluZyBibG9jayBvZiBtYXR0ZXIuIFdoYXQgd291bGQgeW91IGNhbGwgdGhlIHVuaXQgdGhhdCBtYWtlcyB1cCB0aGUgbnVjbGV1cyBwbHVzIHRoZSBlbGVjdHJvbnM/[Qq]
[f]IENvcnJlY3QuIEF0b21zIGFyZSB0aGUgYnVpbGRpbmcgYmxvY2tzIG9mIG1hdHRlci4=[Qq]
[f]IE5vLiBQcm90b25zIGFyZSBmb3VuZCBpbiB0aGUgbnVjbGV1cy4gV2hhdCB3b3VsZCB5b3UgY2FsbCB0aGUgdW5pdCB0aGF0IG1ha2VzIHVwIHRoZSBudWNsZXVzIHBsdXMgdGhlIGVsZWN0cm9ucz8=[Qq]
[f]IE5vLiBFbGVjdHJvbnMgb3JiaXQgb3V0c2lkZSB0aGUgbnVjbGV1cy4gV2hhdCB3b3VsZCB5b3UgY2FsbCB0aGUgdW5pdCB0aGF0IG1ha2VzIHVwIHRoZSBudWNsZXVzIHBsdXMgdGhlIGVsZWN0cm9ucz8=
Cg==
[Qq]
[q] Almost all of an atom’s mass is in the
[c]IHByb3RvbnM=[Qq]
[c]IG5ldXRyb25z[Qq]
[c]IG51Y2 xldXM=[Qq]
[c]IGVsZWN0cm9uIGVuZXJneSBsZXZlbHM=[Qq]
[f]IE5vLiBQcm90b25zIGRvIG1ha2UgdXAgYSBzaWduaWZpY2FudCBwYXJ0IG9mIGFuIGF0b20mIzgyMTc7cyBtYXNzLCBidXQgYSBiZXR0ZXIgYW5zd2VyIHdvdWxkIGJlIHRoZSBwYXJ0IHRoYXQgaW5jbHVkZXMgYm90aCBwcm90b25zIGFuZCBuZXV0cm9ucy4gV2hhdCBwYXJ0IG9mIHRoZSBhdG9tIGlzIHRoYXQ/[Qq]
[f]IE5vLiBOZXV0cm9ucyBkbyBtYWtlIHVwIGEgc2lnbmlmaWNhbnQgcGFydCBvZiBhbiBhdG9tJiM4MjE3O3MgbWFzcywgYnV0IGEgYmV0dGVyIGFuc3dlciB3b3VsZCBiZSB0aGUgcGFydCB0aGF0IGluY2x1ZGVzIGJvdGggcHJvdG9ucyBhbmQgbmV1dHJvbnMuIFdoYXQgcGFydCBvZiB0aGUgYXRvbSBpcyB0aGF0Pw==[Qq]
[f]IFllcy4gQWxtb3N0IGFsbCBvZiBhbiBhdG9tJiM4MjE3O3MgbWFzcyBpcyBmb3VuZCBpbiB0aGUgbnVjbGV1cywgd2hpY2ggY29uc2lzdHMgb2YgcHJvdG9ucyBhbmQgbmV1dHJvbnMu[Qq]
[f]IE5vLiBBbiBlbmVyZ3kgbGV2ZWwgaXMgYSByZWdpb24gb3V0c2lkZSBvZiB0aGUgbnVjbGV1cyB3aGVyZSBlbGVjdHJvbnMgYXJlIGZvdW5kLiBXaGVyZSBkbyB5b3UgZmluZCB0aGUgcHJvdG9ucyBhbmQgbmV1dHJvbnMsIHRoZSBtb3N0IG1hc3NpdmUgcGFydGljbGVzIGluIGFuIGF0b20/
Cg==
WQA = [QQ]
[Q] Две частицы, обнаруженные в ядре атома, – это
[C] IG5LDXRYB24GYW 5KIHBIB3RVBG == [QQ]
[C] IG5LDXRIB24GYW5KIGVSSRSWN0SBM. HBM.HBM.IHBM99.HIBSBM.HSBM.HBM99.HIBSBM.HEN0BM9.HEN0SBM.HEN0BM9.HEN0SBM.HSBM.HSBM.HSBM.HSBM.HSBM99. [Qq]
HBM.HBM.IHBM99.HIBSBM.HSBM.HBM99.HIBSBM.HEN0BM9.HEN0SBM.HEN0BM9.HEN0SBM.HSBM.HSBM.HSBM.HSBM.HSBM99. [Qq]
[f]IENvcnJlY3QuIE5ldXRyb25zIGFuZCBwcm90b25zIG1ha2UgdXAgdGhlIGF0b20mIzgyMTc7cyBudWNsZXVzLg==[Qq]
[f]IE5vLiBOZXV0cm9ucyBhcmUgZm91bmQgaW4gdGhlIG51Y2xldXMsIGJ1dCBub3QgZWxlY3Ryb25zLiBUaGUgc2Vjb25kIHBhcnRpY2xlIGlzIG9uZSB3aXRoIGEgcG9zaXRpdmUgY2hhcmdlLg==[Qq]
[f]IE5vLiBQcm90b25zIGFyZSBmb3VuZCBpbiB0aGUgbnVjbGV1cywgYnV0IG5vdCBlbGVjdHJvbnMuIFRoZSBzZWNvbmQgcGFydGljbGUgaXMgdGhlIG9uZSB3aXRoIGEgbmV1dHJhbCBjaGFyZ2UuwqA=
Cg==
wqA= [Qq]
[q] The positively charged particle in an atom is the
[c]IGVsZWN0cm9u[Qq]
[c]IHByb3 Rvbg==[Qq]
[c]IG5ldXRyb24=[Qq]
[f]IE5vLiBFbGVjdHJvbnMgaGF2ZSBhIG5lZ2F0aXZlIGNoYXJnZS4gVGhlIHBvc2l0aXZlbHkgY2hhcmdlZCBwYXJ0aWNsZSBpcyBmb3VuZCBpbiB0aGUgbnVjbGV1cy4=[Qq]
[f]IENvcnJlY3QuIFRoZSBwb3NpdGl2ZWx5IGNoYXJnZWQgcGFydGljbGUgaW4gdGhlIGF0b20gaXMgdGhlIHByb3Rvbi4=[Qq]
[f]IE5vLiBOZXV0cm9ucyBoYXZlIG5vIGNoYXJnZSAobWFraW5nIHRoZW0gbmV1dHJhbCkuIFRoZSBwb3NpdGl2ZWx5IGNoYXJnZWQgcGFydGljbGUgaXMgdGhlIG90aGVyIHBhcnRpY2xlIChiZXNpZGVzIHRoZSBuZXV0cm9uKSBpbiB0aGUgbnVjbGV1cy4=
Cg==
wqA= [Qq]
[q] The negatively charged particle in an atom is the
[c] IGVsZW N0cm9u[Qq]
[c]IHByb3Rvbg==[Qq]
[c]IG5ldXRyb24=[Qq]
[f]IFllcy4gRWxlY3Ryb25zIGhhdmUgYSBuZWdhdGl2ZSBjaGFyZ2UuIA==[Qq]
[f]IE5vLiBQcm90b25zIGhhdmUgYSBwb3NpdGl2ZSBjaGFyZ2UuIFRoZSBuZWdhdGl2ZWx5IGNoYXJnZWQgcGFydGljbGUgaW4gdGhlIGF0b20gaXMgdGhlIG9uZSBvdXRzaWRlIHRoZSBudWNsZXVzLg==[Qq]
[f]IE5vLiBOZXV0cm9ucyBoYXZlIG5vIGNoYXJnZSAobWFraW5nIHRoZW0gbmV1dHJhbCkuIFRoZSBuZWdhdGl2ZWx5IGNoYXJnZWQgcGFydGljbGUgaW4gdGhlIGF0b20gaXMgdGhlIG9uZSBvdXRzaWRlIHRoZSBudWNsZXVzLg==
Cg==
wqA= [Qq]
[q] Частица в атоме, не имеющая заряда, называется =[Qq]
[f]wqAgTm8uIEVsZWN0cm9ucyBoYXZlIGEgbmVnYXRpdmUgY2hhcmdlLiA=[Qq]
[f]IE5vLiBQcm90b25zIGhhdmUgYSBwb3NpdGl2ZSBjaGFyZ2UuIFRoZSBwYXJ0aWNsZSB3aXRob3V0IGFueSBjaGFyZ2UgaXMgdGhlIG90aGVyIHBhcnRpY2xlIChiZXNpZGVzIHRoZSBwcm90b24pIGluIHRoZSBudWNsZXVzLiA=[Qq]
[f]IEV4YWN0bHkuIE5ldXRyb25zIGhhdmUgbm8gY2hhcmdlIChtYWtpbmcgdGhlbSBuZXV0cmFsKS4=
Cg==
[Qq]
[q] Electrons are found in
[c]IHRoZSBudWNsZXVz[Qq]
[c]IGVuZXJneSBsZXZl bHMgb3Igc2hlbGxz[Qq]
[f]IE5vLiBUaGUgbnVjbGV1cyBpcyB0aGUgY2VudHJhbCBwYXJ0IG9mIHRoZSBhdG9tLCB3aGVyZSBwcm90b25zIGFuZCBuZXV0cm9ucyBhcmUgZm91bmQu[Qq]
[f] ienvcnjly3quievswn0cm9ucybhcmugzm91bmqgaw4gzw5lcmd5igxldmvscyoywxzbybjywxszwtcoa == C2Hlbgxz KQ ==
44444444444444. CGLBGXZ kq ==
CGLBGXZ kq ==
44444444444444444444444444444444444444444444444444444444444444444444444444444444444444444444444444444444..0002 [q] Of the terms below, the one most similar to “orbit” is
[c]IGVuZXJneS BsZXZlbA==[Qq]
[c]IG51Y2xldXM=[Qq]
[f]IFllcy4gVGhlIHRlcm1zICYjODIxNjtlbmVyZ3kgbGV2ZWwmIzgyMTc7IGFuZCAmIzgyMTY7b3JiaXQmIzgyMTc7IGJvdGggcmVmZXIgdG8gdGhlIHJlZ2lvbiBvdXRzaWRlIG9mIHRoZSBudWNsZXVzIHdoZXJlIGVsZWN0cm9ucyBhcmUgZm91bmQuIA==[Qq ]
[F] IE5Vlibuagugbnvjbgv1cybpcyb0agugy2vudhjhbcbyzwdpb24gb2ygdghligf0b20sihdozxjlihb3rvbnmgyw5kig5ldxryb25zigfyzbmb3vbnmgyw5k5ldxryb25zigfyb3vbnmgyw5k5ldxryb25zigfmb3vbnmgyw5kg5ldxryb25zigmb3 -grvbnmgyw5 -wighligf25zigm -grvbnmgyw5 -wighligf0b25zigmb3vbnmgyw5 -wighligf0b25zigfmb3rvbnmgyw5 -yIGEgdGVybSB0aGF0IHJlZmVycyB0byB3aGVyZSBlbGVjdHJvbnMgYXJlIGZvdW5kLg==
Cg==
wqA= [Qq]
[q] In an uncharged atom, the number of protons is equal to the number of
[c]IGVuZXJneSBsZXZlbHM=[Qq]
[ c]IHNoZWxscw==[Qq]
[c]IG5ldXRyb25z[Qq]
[c]IGVsZWN0 cm9ucw==[Qq]
[f]IE5vLiBXaGlsZSB0aGUgbnVtYmVyIG9mIHByb3RvbnMgY2FuIGVxdWFsIHRoZSBudW1iZXIgb2YgZW5lcmd5IGxldmVscywgaXQmIzgyMTc7cyBub3QgYSBuZWNlc3NhcnkgcmVsYXRpb25zaGlwLiBUaGluayBhYm91dCBhIHBhcnRpY2xlIHdob3NlIGNoYXJnZSBpcyB0aGUgb3Bwb3NpdGUgb2YgdGhlIHByb3RvbiYjODIxNztzIGNoYXJnZS4=[Qq]
[f]IE5vLiBXaGlsZSB0aGUgbnVtYmVyIG9mIHByb3RvbnMgY2FuIGVxdWFsIHRoZSBudW1iZXIgb2YgZWxlY3Ryb24gc2hlbGxzLCBpdCYjODIxNztzIG5vdCBhIG5lY2Vzc2FyeSByZWxhdGlvbnNoaXAuIFRoaW5rIGFib3V0IGEgcGFydGljbGUgd2hvc2UgY2hhcmdlIGlzIHRoZSBvcHBvc2l0ZSBvZiB0aGUgcHJvdG9uJiM4MjE3O3MgY2hhcmdlLg==[Qq]
[f]IE5vLiBXaGlsZSBpdCYjODIxNztzIG5vdCB1bmNvbW1vbiBmb3IgdGhlIG51bWJlciBvZiBwcm90b25zIHRvIGVxdWFsIHRoZSBudW1iZXIgb2YgbmV1dHJvbnMsIHRoZSBudW1iZXIgY2FuIGFsc28gYmUgZGlmZmVyZW50LiBUaGluayBhYm91dCBhIHBhcnRpY2xlIHdob3NlIGNoYXJnZSBpcyB0aGUgb3Bwb3NpdGUgb2YgdGhlIHByb3RvbiYjODIxNztzIGNoYXJnZS8=[Qq]
[f]IEV4Y2VsbGVudCEgSW4gYW4gdW5jaGFyZ2VkIGF0b20sIHRoZSBudW1iZXIgb2YgcHJvdG9ucyBpcyBlcXVhbCB0byB0aGUgbnVtYmVyIG9mIGVsZWN0cm9ucy4g
Cg==
wqA= [Qq]
[q] An element is composed of
[c]IE9ubHkgb25lIHR5 cGUgb2YgYXRvbQ==[Qq]
[ c]IEF0IGxlYXN0IHR3byB0eXBlcyBvZiBhdG9tcw==[Qq]
[c]IE9ubHkgYXRvbXMgdGhhdCBoYXZlIGxvc3QgdGhlaXIgZWxlY3Ryb25z[Qq]
[f]IFllcy4gQW4gZWxlbWVudCBpcyBhIHN1YnN0YW5jZSB0aGF0IGlzIGNvbXBvc2VkIG9mIG9ubHkgb25lIHR5cGUgb2YgYXRvbS4=[Qq]
[f]IE5vLiBTdWJzdGFuY2VzIGNvbXBvc2VkIG9mIHR3byBvciBtb3JlIHR5cGVzIG9mIGF0b21zIGFyZSBjb21wb3VuZHMgKGFuZCB3ZSYjODIxNztsbCBsZWFybiBtb3JlIGFib3V0IHRoZW0gbGF0ZXIu[Qq]
[f]IE5vLiBXaGlsZSBhbiBhdG9tIG1pZ2h0IHRlbXBvcmFyaWx5IGxvc2UgaXRzIGVsZWN0cm9ucyAobW9yZSBhYm91dCB0aGF0IGxhdGVyKSwgdGhlcmUgYXJlIG5vIHN1YnN0YW5jZXMgdGhhdCBhcmUgY29tcG9zZWQgb2YgYXRvbXMgdGhhdCBoYXZlIGxvc3QgdGhlaXIgZWxlY3Ryb25zLg==
Cg==
wqA= [Qq]
[q] Что из следующего НЕ может быть химическим символом элемента
[c]IEZl[Qq]
[c]IEhl Zw== [Qq]
[c]IEk=[Qq]
[c]IE1u[Qq]
[f]IE5vLiBDaGVtaWNhbCBzeW1ib2xzIGNvbnNpc3Qgb2Ygb25lIG9yIHR3byBsZXR0ZXJzLiBUaGUgZmlyc3QgKG9yIG9ubHkpIGxldHRlciBpcyBjYXBpdGFsaXplZC4gVGhlIHNlY29uZCBsZXR0ZXIgaXMgbG93ZXJjYXNlLiAmIzgyMjA7RmUmIzgyMjE7IGlzIGEgbGVnaXRpbWF0ZSBzeW1ib2wmIzgyMzA7dGhlIHN5bWJvbCBmb3IgdGhlIGxldHRlciBJcm9uLiA=[Qq]
[f]IFllczogJiM4MjIwO0hlZyYjODIyMTsgY291bGQgTk9UIGJlIGEgY2hlbWljYWwgc3ltYm9sIGZvciBhbiBlbGVtZW50LiBDaGVtaWNhbCBzeW1ib2xzIGNvbnNpc3Qgb2Ygb25lIG9yIHR3byBsZXR0ZXJzLiBUaGUgZmlyc3QgKG9yIG9ubHkpIGxldHRlciBpcyBjYXBpdGFsaXplZC4gVGhlIHNlY29uZCBsZXR0ZXIgaXMgbG93ZXJjYXNlLiBXaXRoIHRocmVlIGxldHRlcnMsICYjODIyMDtIZWcmIzgyMjE7IGlzIG5vdCBhIGxlZ2l0aW1hdGUgY2hlbWljYWwgc3ltYm9sLsKg[Qq]
[f]IE5vLiBDaGVtaWNhbCBzeW1ib2xzIGNvbnNpc3Qgb2Ygb25lIG9yIHR3byBsZXR0ZXJzLiBUaGUgZmlyc3QgKG9yIG9ubHkpIGxldHRlciBpcyBjYXBpdGFsaXplZC4gVGhlIHNlY29uZCBsZXR0ZXIgaXMgbG93ZXJjYXNlLiAmIzgyMjA7SSYjODIyMTsgaXMgYSBsZWdpdGltYXRlIHN5bWJvbCYjODIzMDt0aGUgc3ltYm9sIGZvciB0aGUgZWxlbWVudCBJb2RpbmUu[Qq]
[f]IE5vLiBDaGVtaWNhbCBzeW1ib2xzIGNvbnNpc3Qgb2Ygb25lIG9yIHR3byBsZXR0ZXJzLiBUaGUgZmlyc3QgKG9yIG9ubHkpIGxldHRlciBpcyBjYXBpdGFsaXplZC4gVGhlIHNlY29uZCBsZXR0ZXIgaXMgbG93ZXJjYXNlLiAmIzgyMjA7TW4mIzgyMjE7IGlzIGEgbGVnaXRpbWF0ZSBzeW1ib2wmIzgyMzA7dGhlIHN5bWJvbCBmb3IgdGhlIGVsZW1lbnQgTWFuZ2FuZXNl
Cg==
wqA= [Qq]
[q] Азот имеет 7 протонов, 7 нейтронов и 7 электронов. Следуя правилу октета для размещения электронов на энергетических уровнях, какое из следующих расположений является правильным?
Следуя правилу октета для размещения электронов на энергетических уровнях, какое из следующих расположений является правильным?
[c]wqBBbGwgc2V2ZW4gZWxlY3Ryb25zIGluIHRoZSBmaXJzdMKgZW5lcmd5IGxldmVsLsKg[Qq]
[c]IFRocmVlIGVsZWN0cm9ucyBpbiB0aGUgZmlyc3QgZW5lcmd5IGxldmVsIGFuZCBmb3VyIGVsZWN0cm9ucyBpbiB0aGUgc2Vjb25kIGVuZXJneSBsZXZlbC7CoA==[Qq]
[c]wqBUd28gZWxlY3Ryb25zIGluIHRoZSBmaXJzdMKgZW5lcmd5IGxldm VsLCBmaXZlIGluIHRoZSBzZWNvbmTCoGVuZXJneSBsZXZlbC7CoA==[Qq]
[f]IE5vLiBUbyByZXByZXNlbnQgdGhlIHN0cnVjdHVyZSBvZiB0aGUgZWxlY3Ryb25zIGluIGFuIGF0b20sIGtlZXAgaW4gbWluZCB0aGUgY2FwYWNpdHkgb2YgZWFjaCBlbmVyZ3kgbGV2ZWwgKHR3byBlbGVjdHJvbnMgaW4gdGhlIGZpcnN0LCBlaWdodCBpbiB0aGUgc2Vjb25kLCBhbmQgZWlnaHQgaW4gdGhlIHRoaXJkLiBJbiBOaXRyb2dlbiwgd2l0aCBzZXZlbiBlbGVjdHJvbnMsIHRoZSBmaXJzdCB0d28gZWxlY3Ryb25zIG5lZWQgdG8gZ28gaW50byB0aGUgZmlyc3QgZW5lcmd5IGxldmVsLiBUaGF0IGxlYXZlcyBmaXZlIGVsZWN0cm9ucyBmb3IgdGhlIHNlY29uZCBlbmVyZ3kgbGV2ZWwu[Qq]
[f]IE5vLiBUbyByZXByZXNlbnQgdGhlIHN0cnVjdHVyZSBvZiB0aGUgZWxlY3Ryb25zIGluIGFuIGF0b20sIGtlZXAgaW4gbWluZCB0aGUgY2FwYWNpdHkgb2YgZWFjaCBlbmVyZ3kgbGV2ZWwgKHR3byBlbGVjdHJvbnMgaW4gdGhlIGZpcnN0LCBlaWdodCBpbiB0aGUgc2Vjb25kLCBhbmQgZWlnaHQgaW4gdGhlIHRoaXJkLiBJbiBOaXRyb2dlbiwgd2l0aCBzZXZlbiBlbGVjdHJvbnMsIHRoZSBmaXJzdCB0d28gZWxlY3Ryb25zIG5lZWQgdG8gZ28gaW50byB0aGUgZmlyc3QgZW5lcmd5IGxldmVsLiBUaGF0IGxlYXZlcyBmaXZlIGVsZWN0cm9ucyBmb3IgdGhlIHNlY29uZCBlbmVyZ3kgbGV2ZWwu[Qq]
[f]IENvcnJlY3QuIEluIE5pdHJvZ2VuLCB3aXRoIHNldmVuIGVsZWN0cm9ucywgdGhlIGZpcnN0IHR3byBlbGVjdHJvbnMgbmVlZCB0byBnbyBpbnRvIHRoZSBmaXJzdMKgZW5lcmd5IGxldmVsLiBUaGF0IGxlYXZlcyBmaXZlIGVsZWN0cm9ucyBmb3IgdGhlIHNlY29uZMKgZW5lcmd5IGxldmVsLg==
Cg==
[Qq]
[q] Sulfur has 16 protons, 16 neutrons, and 16 electrons. Следуя правилу октета для размещения электронов на энергетическом уровне, какое из следующих расположений является правильным?
Следуя правилу октета для размещения электронов на энергетическом уровне, какое из следующих расположений является правильным?
[c]IFR3byBlbGVjdHJvbnMgaW4gdGhlIGZpcnN0IGVuZXJneSBsZXZlbCwgZWlnaHQgZWxlY3Ryb25zIGluIH RoZSBzZWNvbmTCoGVuZXJneSBsZXZlbCwgYW5kIHNpeCBpbiB0aGUgdGhpcmTCoGVuZXJneSBsZXZlbC4=[Qq]
[c]wqBFaWdodCBlbGVjdHJvbnMgaW4gdGhlIGZpcnN0wqBlbmVyZ3kgbGV2ZWwsIGVpZ2h0IGVsZWN0cm9ucyBpbiB0aGUgc2Vjb25kwqBlbmVyZ3kgbGV2ZWwuwqA=[Qq]
[c]wqBTaXggZWxlY3Ryb25zIGluIHRoZSBmaXJzdMKgZW5lcmd5IGxldmVsLCBzaXggaW4gdGhlIHNlY29uZMKgZW5lcmd5IGxldmVsLCBhbmQgZm91ciBpbiB0aGUgdGhpcmQuwqA=[Qq]
[f]IEV4Y2VsbGVudC4gSW4gU3VsZnVyLCB3aXRoIDE2IGVsZWN0cm9ucywgdGhlIGZpcnN0IHR3byBlbGVjdHJvbnMgZ28gaW4gdGhlIGZpcnN0wqBlbmVyZ3kgbGV2ZWwsIHRoZSBuZXh0IDggaW4gdGhlIHNlY29uZMKgZW5lcmd5IGxldmVsLCBhbmQgdGhlIGxhc3Qgc2l4IGluIHRoZSB0aGlyZMKgZW5lcmd5IGxldmVsLg==
Cg==
[Qq]
[f]IE5vLiBUbyByZXByZXNlbnQgdGhlIHN0cnVjdHVyZSBvZiBlbGVjdHJvbnMgaW4gYXRvbXMsIGtlZXAgaW4gbWluZCB0aGUgY2FwYWNpdHkgb2YgZWFjaCBlbmVyZ3kgbGV2ZWwgKHR3byBlbGVjdHJvbnMgaW4gdGhlIGZpcnN0LCBlaWdodCBpbiB0aGUgc2Vjb25kLCBhbmQgZWlnaHQgaW4gdGhlIHRoaXJkKS4gSW4gc3VsZnVyLCB3aXRoIDE2IGVsZWN0cm9ucywgdGhlIGZpcnN0IHR3byBlbGVjdHJvbnMgbmVlZCB0byBnbyBpbnRvIHRoZSBmaXJzdCBlbmVyZ3kgbGV2ZWwuIFRoZSBuZXh0IGVpZ2h0IHdvdWxkIGdvIGludG8gdGhlIHNlY29uZCBlbmVyZ3kgbGV2ZWwsIHdoaWNoIGxlYXZlcyBzaXggZWxlY3Ryb25zIGZvciB0aGUgdGhpcmQgZW5lcmd5IGxldmVsLg==[Qq]
[f]IE5vLiBUbyByZXByZXNlbnQgdGhlIHN0cnVjdHVyZSBvZiBlbGVjdHJvbnMgaW4gYXRvbXMsIGtlZXAgaW4gbWluZCB0aGUgY2FwYWNpdHkgb2YgZWFjaCBlbmVyZ3kgbGV2ZWwgKHR3byBlbGVjdHJvbnMgaW4gdGhlIGZpcnN0LCBlaWdodCBpbiB0aGUgc2Vjb25kLCBhbmQgZWlnaHQgaW4gdGhlIHRoaXJkKS4gSW4gc3VsZnVyLCB3aXRoIDE2IGVsZWN0cm9ucywgdGhlIGZpcnN0IHR3byBlbGVjdHJvbnMgbmVlZCB0byBnbyBpbnRvIHRoZSBmaXJzdCBlbmVyZ3kgbGV2ZWwuIFRoZSBuZXh0IGVpZ2h0IHdvdWxkIGdvIGludG8gdGhlIHNlY29uZCBlbmVyZ3kgbGV2ZWwsIHdoaWNoIGxlYXZlcyBzaXggZWxlY3Ryb25zIGZvciB0aGUgdGhpcmQgZW5lcmd5IGxldmVsLg==
Cg==
wqA= [Qq]
[q] Carbon has 6 protons, 6 neutrons, and 6 electrons. Следуя правилу октета для размещения электронов на энергетическом уровне, какое из следующих расположений является правильным?
Следуя правилу октета для размещения электронов на энергетическом уровне, какое из следующих расположений является правильным?
[c]wqBUaHJlZSBlbGVjdHJvbnMgaW4gdGhlIGZpcnN0wqBlbmVyZ3kgbGV2ZWwsIGFuZCB0aHJlZSBpbiB0aGUgc2Vjb25kLg==[Qq]
[c]wqBPbmUgZWxlY3Ryb24gaW4gdGhlIGZpcnN0wqBlbmVyZ3kgbGV2ZWwsIGFuZCBmaXZlIGluIHRoZSBzZWNvbmQuwqA=[Qq]
[c]wqBUd28gZWxlY3Ryb25zIGluIHRoZSBmaXJzdMKgZW5lcm d5IGxldmVsLCBhbmQgZm91ciBpbiB0aGUgc2Vjb25kLsKg[Qq]
[f]IE5vLiBUbyByZXByZXNlbnQgdGhlIHN0cnVjdHVyZSBvZiBlbGVjdHJvbnMgaW4gYXRvbXMsIGtlZXAgaW4gbWluZCB0aGUgY2FwYWNpdHkgb2YgZWFjaCBlbmVyZ3kgbGV2ZWwgKHR3byBlbGVjdHJvbnMgaW4gdGhlIGZpcnN0LCBlaWdodCBpbiB0aGUgc2Vjb25kLCBhbmQgZWlnaHQgaW4gdGhlIHRoaXJkKS4gSW4gQ2FyYm9uLCB3aXRoIDYgZWxlY3Ryb25zLCB0aGUgZmlyc3QgdHdvIGVsZWN0cm9ucyBuZWVkIHRvIGdvIGludG8gdGhlIGZpcnN0IGVuZXJneSBsZXZlbC4gVGhlIG5leHQgZm91ciBnbyBpbnRvIHRoZSBzZWNvbmQgZW5lcmd5IGxldmVsLg==[Qq]
[f]IE5vLiBUbyByZXByZXNlbnQgdGhlIHN0cnVjdHVyZSBvZiBlbGVjdHJvbnMgaW4gYXRvbXMsIGtlZXAgaW4gbWluZCB0aGUgY2FwYWNpdHkgb2YgZWFjaCBlbmVyZ3kgbGV2ZWwgKHR3byBlbGVjdHJvbnMgaW4gdGhlIGZpcnN0LCBlaWdodCBpbiB0aGUgc2Vjb25kLCBhbmQgZWlnaHQgaW4gdGhlIHRoaXJkKS4gSW4gQ2FyYm9uLCB3aXRoIDYgZWxlY3Ryb25zLCB0aGUgZmlyc3QgdHdvIGVsZWN0cm9ucyBuZWVkIHRvIGdvIGludG8gdGhlIGZpcnN0IGVuZXJneSBsZXZlbC4gVGhlIG5leHQgZm91ciBnbyBpbnRvIHRoZSBzZWNvbmQgZW5lcmd5IGxldmVsLg==[Qq]
[f]IEV4Y2VsbGVudC4gSW4gQ2FyYm9uLCB3aXRoIDYgZWxlY3Ryb25zLCB0aGUgZmlyc3QgdHdvIGVsZWN0cm9ucyBnbyBpbnRvIHRoZSBmaXJzdCBlbmVyZ3kgbGV2ZWwsIGFuZCB0aGUgbmV4dCA0IGdvIGludG8gdGhlIHNlY29uZCBlbmVyZ3kgbGV2ZWwu
Cg==
[Qq]
[q] Potassium has 19 protons, 19 neutrons, and 19 electrons. Следуя правилу октета для размещения электронов на энергетическом уровне, какое из следующих расположений является правильным?
Следуя правилу октета для размещения электронов на энергетическом уровне, какое из следующих расположений является правильным?
[c]wqBUZW4gZWxlY3Ryb25zIGluIHRoZSBmaXJzdMKgZW5lcmd5IGxldmVsLCBuaW5lIGluIHRoZSBzZWNvbmQu[Qq]
[c]IFR3byBlbGVjdHJvbnMgaW4gdGhlIGZpcnN0wqBlbmVyZ3kgbGV2ZWwsIGVpZ2h0IGluIHRo ZSBzZWNvbmQsIGVpZ2h0IGluIHRoZSB0aGlyZCwgYW5kIG9uZSBpbiB0aGUgZm91cnRoLg==[Qq]
[c]wqBUd28gZWxlY3Ryb25zIGluIHRoZSBmaXJzdMKgZW5lcmd5IGxldmVsLCB0ZW7CoGluIHRoZSBzZWNvbmQsIGFuZCBzZXZlbiBpbiB0aGUgdGhpcmQu[Qq]
[f]IE5vLiBUbyByZXByZXNlbnQgdGhlIHN0cnVjdHVyZSBvZiBlbGVjdHJvbnMgaW4gYXRvbXMsIGtlZXAgaW4gbWluZCB0aGUgY2FwYWNpdHkgb2YgZWFjaCBlbmVyZ3kgbGV2ZWwgKHR3byBlbGVjdHJvbnMgaW4gdGhlIGZpcnN0LCBlaWdodCBpbiB0aGUgc2Vjb25kLCBhbmQgZWlnaHQgaW4gdGhlIHRoaXJkKS4gSW4gUG90YXNzaXVtLCB3aXRoIDE5IGVsZWN0cm9ucywgdGhlIGZpcnN0IHR3byBlbGVjdHJvbnMgZ28gaW50byB0aGUgZmlyc3QgZW5lcmd5IGxldmVsLiBUaGUgbmV4dCA4IGdvIGludG8gdGhlIHNlY29uZCBlbmVyZ3kgbGV2ZWwuIFRoZSBuZXh0IDggZ28gaW50byB0aGUgdGhpcmQgZW5lcmd5IGxldmVsLiBUaGF0IGxlYXZlcyBvbmUgZWxlY3Ryb24gZm9yIHRoZSBmb3VydGggZW5lcmd5IGxldmVsLiA=[Qq]
[f]IE5pY2Ugam9iISBJbiBQb3Rhc3NpdW0sIHdpdGggMTkgZWxlY3Ryb25zLCB0aGUgZmlyc3QgdHdvIGVsZWN0cm9ucyBnbyBpbnRvIHRoZSBmaXJzdMKgZW5lcmd5IGxldmVsLiBUaGUgbmV4dCA4IGdvIGludG8gdGhlIHNlY29uZMKgZW5lcmd5IGxldmVsLiBUaGUgbmV4dCA4IGdvIGludG8gdGhlIHRoaXJkwqBlbmVyZ3kgbGV2ZWwuIFRoYXQgbGVhdmVzIG9uZSBlbGVjdHJvbiBmb3IgdGhlIGZvdXJ0aMKgZW5lcmd5IGxldmVsLg==
Cg==
[Qq]
[f]IE5vLiBUbyByZXByZXNlbnQgdGhlIHN0cnVjdHVyZSBvZiBlbGVjdHJvbnMgaW4gYXRvbXMsIGtlZXAgaW4gbWluZCB0aGUgY2FwYWNpdHkgb2YgZWFjaCBlbmVyZ3kgbGV2ZWwgKHR3byBlbGVjdHJvbnMgaW4gdGhlIGZpcnN0LCBlaWdodCBpbiB0aGUgc2Vjb25kLCBhbmQgZWlnaHQgaW4gdGhlIHRoaXJkKS4gSW4gUG90YXNzaXVtLCB3aXRoIDE5IGVsZWN0cm9ucywgdGhlIGZpcnN0IHR3byBlbGVjdHJvbnMgZ28gaW50byB0aGUgZmlyc3QgZW5lcmd5IGxldmVsLiBUaGUgbmV4dCA4IGdvIGludG8gdGhlIHNlY29uZCBlbmVyZ3kgbGV2ZWwuIFRoZSBuZXh0IDggZ28gaW50byB0aGUgdGhpcmQgZW5lcmd5IGxldmVsLiBUaGF0IGxlYXZlcyBvbmUgZWxlY3Ryb24gZm9yIHRoZSBmb3VydGggZW5lcmd5IGxldmVsLsKg[Qq]
[x]
If you want to take this quiz again, click the button below
[restart]
[/qwiz]
6.
 Next steps
Next stepsIf you need more practice, please scroll до самого верха и снова пройдите этот урок. В противном случае перейдите к следующему руководству: Элементы, соединения и молекулы.
Atom Drawing Stock-Fotos und Bilder
- CREATIVE
- EDITORIAL
- VIDEOS
- Beste Übereinstimmung
- Neuestes
- Ältestes
- Am beliebtesten
Alle Zeiträume24 Stunden48 Stunden72 Stunden7 Tage30 Tage12 MonateAngepasster Zeitraum
- Lizenzfrei
- Lizenzpflichtig
- RF und RM
Lizenzfreie Kollektionen auswählen >Editorial-Kollektionen auswählen >
Bilder zum Einbetten
Durchstöbern Sie 1.
 064 атомный рисунок Stock-Photografie und Bilder. Oder starten Sie eine neuesuche, um noch mehr Stock-Photografie und Bilder zu entdecken. ядерный гекрицель – рисунок атома сток-график, -клипарт, -мультфильмы и -символикосаэдр – рисунок атома сток-график, -клипарт, -мультфильмы и -символекрафтверк-чертеж – рисунок атома сток-график, -клипарт, -мультфильмы и -символы kernkraftwerk – рисунок атома стоковая графика, -клипарт, -мультфильмы и -symbolewissenschaft zeichnungen – рисунок атома стоковая графика, -клипарт, -мультфильмы и -символ Stock-fotos und bilderzeichnung bleistift skizzen wissenschaftlicher konzepte – атомный рисунок стоковая графика, -клипарт, -мультфильмы и -symbolenahtlose Meetingfläche und kritzeleien set – атомный рисунок стоковая графика, -клипарт, -мультфильмы и -символофизика – атомный рисунок стоковая графика , -clipart, -cartoons und -symbolewissenschaft icons – серия skizzierte – атомный рисунок стоковая графика, -клипарт, -мультфильмы и -symboleforschungsutensilien – атом рисунок стоковая графика, -клипа rt, -cartoons und -symboleminimal122 – стоковая графика для рисования атома, -clipart, -cartoons und -symboleabstrakte technologie-hintergrund – атомная графика для рисования, -clipart, -cartoons und -symboleabstrakte technologie-hintergrund – атомная графика для рисования, -клипарт, -мультфильмы и -символикосаэдр – атомный рисунок стоковой графики, -клипарт, -мультфильмы и -символыцветные круги, связанные вместе на фоне белой бумаги – стоковые фотографии атома и изображения, сгенерированные компьютером, абстрактные фракталы -клипарт, -мультфильмы и -символика, связанные с мультяшным стилем, каракули векторные иллюстрации – рисунок атома musterhintergrund-ring-technologie – рисунок стоковой графики атома, -клипарт, -мультфильмы и -symbolesatz von schulsymbolen auf gefüttertem papier mit einem zurück zur schule nachricht – рисунок стоковой графики атома, -clipart, -cartoons und -symboleatomic forschung, zeichnung auf dem board – стоковая графика атома, -клипарт, -мультфильмы и -symboleretro-sci-fi und kritzeleien – атомный рисунок стоковой графики, -клипарт, -мультфильмы и -symbowissenschaftliche набор каракулей – атом рисунок стоковая графика, -клипарт , -cartoons und -symboleenergie und strom symbole skizzierte serie – атом рисунок сток-графика, -клипарт, -мультфильмы и -symbole1950 er und kritzeleien – рисунок атома стоковая графика, -клипарт, -мультфильмы и -символволокно оптика расширяющийся рисунок земной шар – рисунок атома стоковые фотографии и бильдератом нарисованные durch wissenschaftler oder студент – рисунок атома стоковые фотографии и бильдерорганическая химия на доске – рисунок атома стоковые фото и бильярдные линии частиц – рисунок атома стоковые фото и бильярдные идеи, химия, инновации, астрономия, атом, эксперимент дизайн иконок – рисунок атома стоковые графики, -клипарты, -мультфильмы и -символыкреативитет процесс для понимания идеи – атомный рисунок Stock-grafiken, -clipart, -cartoons und -symboleatomic kern zeichnung auf dem papier – атомный рисунок Stock-grafiken, -clipart, -cartoons und -symbolechemisches work ausrüstung doodles – атомный рисунок Stock-grafiken, -clipart, -cartoons und -symboleversand und herstellung skizze icons 10 – атомный рисунок стоковая графика, -клипарт, -мультфильмы и -символический взрыв – абстрактная иллюстрация – атомный рисунок стоковые фото и бильярд Strakte netzwerkhintergrund – рисунок атома сток-графика, -клипарт, -мультфильмы и -symbowissenschaftliche sechsecke – рисунок атома сток-графика, -клипарт, -мультфильмы и -symbolemolekulare vorlage – рисунок атома сток-графика, -клипарт, -мультфильмы и -символика -symbol mit bearbeitbarem strich – атом рисунок сток-графика, -клипарт, -мультфильмы и -symbolemolekulare ecke – атом рисунок сток-графика, -клипарт, -мультфильмы и -symbolefireworks – абстрактная цифровая иллюстрация – атом рисунок сток-фотографии и изображения科技線條粒子素材背景 – атомный рисунок стоковых фотографий и изображений и объектов энергии и элементов.
064 атомный рисунок Stock-Photografie und Bilder. Oder starten Sie eine neuesuche, um noch mehr Stock-Photografie und Bilder zu entdecken. ядерный гекрицель – рисунок атома сток-график, -клипарт, -мультфильмы и -символикосаэдр – рисунок атома сток-график, -клипарт, -мультфильмы и -символекрафтверк-чертеж – рисунок атома сток-график, -клипарт, -мультфильмы и -символы kernkraftwerk – рисунок атома стоковая графика, -клипарт, -мультфильмы и -symbolewissenschaft zeichnungen – рисунок атома стоковая графика, -клипарт, -мультфильмы и -символ Stock-fotos und bilderzeichnung bleistift skizzen wissenschaftlicher konzepte – атомный рисунок стоковая графика, -клипарт, -мультфильмы и -symbolenahtlose Meetingfläche und kritzeleien set – атомный рисунок стоковая графика, -клипарт, -мультфильмы и -символофизика – атомный рисунок стоковая графика , -clipart, -cartoons und -symbolewissenschaft icons – серия skizzierte – атомный рисунок стоковая графика, -клипарт, -мультфильмы и -symboleforschungsutensilien – атом рисунок стоковая графика, -клипа rt, -cartoons und -symboleminimal122 – стоковая графика для рисования атома, -clipart, -cartoons und -symboleabstrakte technologie-hintergrund – атомная графика для рисования, -clipart, -cartoons und -symboleabstrakte technologie-hintergrund – атомная графика для рисования, -клипарт, -мультфильмы и -символикосаэдр – атомный рисунок стоковой графики, -клипарт, -мультфильмы и -символыцветные круги, связанные вместе на фоне белой бумаги – стоковые фотографии атома и изображения, сгенерированные компьютером, абстрактные фракталы -клипарт, -мультфильмы и -символика, связанные с мультяшным стилем, каракули векторные иллюстрации – рисунок атома musterhintergrund-ring-technologie – рисунок стоковой графики атома, -клипарт, -мультфильмы и -symbolesatz von schulsymbolen auf gefüttertem papier mit einem zurück zur schule nachricht – рисунок стоковой графики атома, -clipart, -cartoons und -symboleatomic forschung, zeichnung auf dem board – стоковая графика атома, -клипарт, -мультфильмы и -symboleretro-sci-fi und kritzeleien – атомный рисунок стоковой графики, -клипарт, -мультфильмы и -symbowissenschaftliche набор каракулей – атом рисунок стоковая графика, -клипарт , -cartoons und -symboleenergie und strom symbole skizzierte serie – атом рисунок сток-графика, -клипарт, -мультфильмы и -symbole1950 er und kritzeleien – рисунок атома стоковая графика, -клипарт, -мультфильмы и -символволокно оптика расширяющийся рисунок земной шар – рисунок атома стоковые фотографии и бильдератом нарисованные durch wissenschaftler oder студент – рисунок атома стоковые фотографии и бильдерорганическая химия на доске – рисунок атома стоковые фото и бильярдные линии частиц – рисунок атома стоковые фото и бильярдные идеи, химия, инновации, астрономия, атом, эксперимент дизайн иконок – рисунок атома стоковые графики, -клипарты, -мультфильмы и -символыкреативитет процесс для понимания идеи – атомный рисунок Stock-grafiken, -clipart, -cartoons und -symboleatomic kern zeichnung auf dem papier – атомный рисунок Stock-grafiken, -clipart, -cartoons und -symbolechemisches work ausrüstung doodles – атомный рисунок Stock-grafiken, -clipart, -cartoons und -symboleversand und herstellung skizze icons 10 – атомный рисунок стоковая графика, -клипарт, -мультфильмы и -символический взрыв – абстрактная иллюстрация – атомный рисунок стоковые фото и бильярд Strakte netzwerkhintergrund – рисунок атома сток-графика, -клипарт, -мультфильмы и -symbowissenschaftliche sechsecke – рисунок атома сток-графика, -клипарт, -мультфильмы и -symbolemolekulare vorlage – рисунок атома сток-графика, -клипарт, -мультфильмы и -символика -symbol mit bearbeitbarem strich – атом рисунок сток-графика, -клипарт, -мультфильмы и -symbolemolekulare ecke – атом рисунок сток-графика, -клипарт, -мультфильмы и -symbolefireworks – абстрактная цифровая иллюстрация – атом рисунок сток-фотографии и изображения科技線條粒子素材背景 – атомный рисунок стоковых фотографий и изображений и объектов энергии и элементов. набор векторных иллюстраций. handgezeichnetes icon-set oder banner-template – атом рисунок сток-графика, -клипарт, -мультфильмы и -symbolelichtmuster – атом рисунок сток-фотографии и бильдерабстракция курвенлиния фрактале структурные технологии musterhintergrund – атом рисунок сток-графика, -клипарт, -мультфильмы и -symboleatom молекулярная наука рисунок символа – рисунок атома стоковые фотографии и бильярдная линия символ акварели хинтергрунд – рисунок атома стоковая графика, -клипарт, -мультфильмы и -symbolehandgezeichnete karikatur ядерный взрыв – атомный рисунок стоковая графика, -клипарт, -мультфильмы и -символядерный стихийное бедствие. дерево за побегом радиоактивных частиц – рисунок атома стоковые фотографии и абстракционистские технологии красочных светящихся линий – рисунок атома стоковые фотографии и билдерсила и плоский значок масла – атом – рисунок атома сток-график, -клипарт, -мультфильмы и -символикатом-символ с медвежьей полосой – рисунок атома сток-график, -клипарт, -мультфильмы und -symbolezurück to school – атомный рисунок стоковые графики, -клипарты, -мультфильмы и -символы из 18
набор векторных иллюстраций. handgezeichnetes icon-set oder banner-template – атом рисунок сток-графика, -клипарт, -мультфильмы и -symbolelichtmuster – атом рисунок сток-фотографии и бильдерабстракция курвенлиния фрактале структурные технологии musterhintergrund – атом рисунок сток-графика, -клипарт, -мультфильмы и -symboleatom молекулярная наука рисунок символа – рисунок атома стоковые фотографии и бильярдная линия символ акварели хинтергрунд – рисунок атома стоковая графика, -клипарт, -мультфильмы и -symbolehandgezeichnete karikatur ядерный взрыв – атомный рисунок стоковая графика, -клипарт, -мультфильмы и -символядерный стихийное бедствие. дерево за побегом радиоактивных частиц – рисунок атома стоковые фотографии и абстракционистские технологии красочных светящихся линий – рисунок атома стоковые фотографии и билдерсила и плоский значок масла – атом – рисунок атома сток-график, -клипарт, -мультфильмы и -символикатом-символ с медвежьей полосой – рисунок атома сток-график, -клипарт, -мультфильмы und -symbolezurück to school – атомный рисунок стоковые графики, -клипарты, -мультфильмы и -символы из 18Нарисуйте модели атомов — выберите МЕСТО
По предыдущей ссылке вы узнали, что такое атом. Теперь пришло время нарисовать несколько моделей.
Помните, атом состоит из протонов, нейтронов и электронов. Протоны и нейтроны имеют массу 1 а.е.м. Они слипаются в ядре. Электроны в тысячу раз меньше протонов, и они кружатся вокруг ядра в электронном облаке.
Вспомните также, как мы находим количество протонов, нейтронов и электронов. Это обобщено в таблице ниже.
| Количество протонов | То же, что и атомное число |
| Номер электронов | То же, что и от атомного числа | 77777777777777777777 гг. ответ до ближайшего целого числа) |
Протоны положительны, поэтому нарисуйте их в виде кругов со знаком плюс. Нейтроны нейтральны, поэтому нарисуйте их в виде пустых кругов. Электроны маленькие и отрицательные, поэтому нарисуйте их как «е-», потому что точку размером в 1/1000 размера протона будет трудно увидеть на бумаге. Используя это, если вы хотите нарисовать атомы с ядром и электронным облаком, это будет выглядеть примерно так:
Электроны маленькие и отрицательные, поэтому нарисуйте их как «е-», потому что точку размером в 1/1000 размера протона будет трудно увидеть на бумаге. Используя это, если вы хотите нарисовать атомы с ядром и электронным облаком, это будет выглядеть примерно так:
2 HE Гелий 4.002 |
3
LI
Lithium
6.94
Протоны = 3
Электроны = 3
NetueRon4, which rounds to 4
4 Be Beryllium 9.01 |
Protons = 4
Electrons = 4
Neutrons = 9. 01 – 4 = 5.01 , что округляется до 5
01 – 4 = 5.01 , что округляется до 5
Проблема с этими моделями в том, что они плохо показывают, что делают электроны. Электроны жужжат вокруг ядра в облаке, но они не все одинаковы. Электроны имеют разные энергетические уровни. Мы называем эти уровни «оболочками». Представьте, что электроны образуют слои вокруг атома. Первый слой может содержать только два электрона. Второй слой может содержать 8 электронов. Самый большой слой может содержать более 30 электронов. Вот периодическая таблица, в которой показаны электроны в их оболочках.
Я никогда не попрошу вас нарисовать модель атома крупнее аргона, поэтому вам достаточно знать, как работают первые три электронных оболочки. Это очень просто, потому что таблица Менделеева построена так же, как электронные оболочки. В первой строке периодической таблицы есть два элемента, и первая оболочка может содержать два электрона. Второй ряд может содержать восемь элементов, а вторая оболочка — восемь электронов. Третий ряд содержит восемь элементов, а третья оболочка аргона содержит восемь электронов.
Атомы крупнее аргона начинают усложняться: электроны начинают заполнять четвертую оболочку, а затем возвращаются и начинают увеличивать третью оболочку (третья оболочка может содержать 18 электронов), затем добавляют еще немного к четвертой оболочке, затем запустите пятую оболочку, затем добавьте еще несколько электронов в четвертую оболочку, чтобы закончить ее… Это беспорядок . В продвинутой химии вам придется узнать, как это работает. На данный момент все, что вам нужно знать, это то, как электроны движутся к первым 18 элементам.
Если вы посмотрите на периодическую таблицу, на которую я только что дал ссылку, вы увидите закономерность в электронах. Водород является первым элементом в первом ряду, поэтому у него есть один электрон на первой оболочке. Гелий — второй элемент в первом ряду, поэтому у него два электрона на первой оболочке. Литий находится во втором ряду, поэтому у лития две оболочки: два электрона на первой оболочке и один электрон на второй оболочке. Углерод является 4-м атомом во втором ряду, поэтому у него 2 электрона на первой оболочке и 4 электрона на второй оболочке. Аргон является 8-м атомом в третьем ряду, поэтому у него 2 электрона на первой оболочке, 8 электронов на второй оболочке и 8 электронов на третьей оболочке. Посмотрите на периодическую таблицу и УБЕДИТЕСЬ, ЧТО ВЫ ПОНИМАЕТЕ ЭТОТ ШАБЛОН!
Углерод является 4-м атомом во втором ряду, поэтому у него 2 электрона на первой оболочке и 4 электрона на второй оболочке. Аргон является 8-м атомом в третьем ряду, поэтому у него 2 электрона на первой оболочке, 8 электронов на второй оболочке и 8 электронов на третьей оболочке. Посмотрите на периодическую таблицу и УБЕДИТЕСЬ, ЧТО ВЫ ПОНИМАЕТЕ ЭТОТ ШАБЛОН!
Теперь пришло время рисовать модели атомов, включающие электронные оболочки. Гелий, бериллий и литий (которые мы смоделировали выше) теперь выглядят так:
Атом гелия с двумя протонами, двумя нейтронами и двумя электронами в первой оболочке.
Обратите внимание, что этот атом лития имеет полную первую оболочку и один электрон на второй оболочке.
Бериллий — второй атом во втором ряду, и у него два электрона на второй оболочке.
Используйте это слайд-шоу Google, чтобы попрактиковаться в рисовании моделей атомов.
Практика рисования атома
Открытые Практика рисования атома
Atomic Design и Sketch -Porplecting Offerlow
9 . для создания систем проектирования, обеспечивающих стандартизацию и более эффективный рабочий процесс.Дизайн-система — это набор повторно используемых компонентов и руководств, которые помогают командам объединяться вокруг общего языка во время создания и жизненного цикла продукта.
В большинстве случаев дизайн-системы состоят из руководства по стилю и библиотеки компонентов. Они также могут включать такие элементы, как голос и тон, а также ценности бренда. Смысл системы дизайна в том, чтобы создать набор стандартов, которые действуют как единый источник правды для продукта или бренда.
Google Material Design — это система структурированного дизайна, предоставляющая набор повторно используемых шаблонов и руководств пользовательского интерфейса.
Material Design от Google является примером структурированной системы дизайна пользовательского интерфейса. Материальный дизайн был представлен еще в 2014 году как способ проектирования и разработки целостных приложений для Android.
Другой пример — Voice and Tone Mailchimp. Он описывает, как голос всегда один и тот же, но тон меняется в зависимости от контекста. Понимание этого помогает расширить возможности контента и придать бренду индивидуальность.
Хотя существует множество различных методов, которые можно использовать для создания дизайн-системы, рекомендуется выбрать структуру, которая позволит команде объединиться вокруг общего языка и набора стандартов. Atomic Design — отличный пример фреймворка, который достигает этих двух целей.
Атомарный дизайн, методология, представленная Брэдом Фростом в 2013 году, основана на идее, что каждую систему дизайна можно определить как серию строительных блоков, которые сосуществуют.
Вот краткий обзор компонентов Atomic Design:
- атомов . Представление основных строительных блоков дизайн-системы. Примером может служить кнопка или стиль текста.
- Молекулы . Группа атомов, работающих вместе как единое целое. Молекулы — это материальные элементы пользовательского интерфейса. Например, кнопка и текстовое поле могут быть сгруппированы для создания формы поиска.
- Организмы . Атомы и молекулы работают вместе в сложной структуре. Поле поиска, сгруппированное с панелью навигации, формирует организм заголовка на веб-сайте.
- Шаблоны. Объекты уровня страницы, помещающие компоненты в макет, определяющий структуру содержимого. Например, взять организм заголовка и поместить его в шаблон домашней страницы.
- страниц. Экземпляры шаблонов, представляющие конечный продукт.
Отличным фреймворком и методологией для дизайн-системы является атомарный дизайн, который включает повторно используемые компоненты дизайна и элементы пользовательского интерфейса.
«Нам поручено создавать интерфейсы для большего числа пользователей в большем количестве контекстов с использованием большего количества браузеров на большем количестве устройств с большим размером экрана и большими возможностями, чем когда-либо прежде. Это действительно непростая задача. К счастью, дизайн-системы здесь, чтобы помочь». — Брэд Фрост, введение в атомарный дизайн и дизайн-системы.
Использование Atomic Design для создания и поддержки системы дизайна поможет дизайнерам работать более эффективно и лучше общаться в своих командах. Существует множество инструментов и методов для создания и обслуживания дизайн-систем, но зачастую лучшими инструментами являются те, с которыми мы лучше всего знакомы.
Для разработки системы дизайна с помощью Atomic Design отличным (и уже знакомым) инструментом является Sketch. Он предоставляет нам холст для создания атомов, молекул и организмов: элементов, необходимых для определения ядра дизайн-системы.
Создание атомов
Мы начинаем с создания трех типов атомов в Sketch: символы, стили слоя и стили текста.
Символы. Символы — это не что иное, как повторно используемые компоненты. Они определяются один раз, потому что их можно создавать во всем продукте. Например, стрелка символ (атом) может быть определен с такими свойствами, как цвет границы, размер и т. д. Затем мы можем повторно использовать этот символ без необходимости его повторного создания каждый раз.
Стили слоя . Стили слоя — это повторно используемые элементы визуального стиля, которые остаются едиными для каждого слоя. Например, цвет заливки стрелки, определенный ранее.
Стили текста. Стили текста, как и стили слоев, представляют собой элементы многократного использования, обеспечивающие единообразие похожих текстовых объектов. Например, определение размера шрифта и цвета элемента h2. Он работает аналогично стилям текста в Google Docs или Microsoft Word.
Когда мы определяем символы, стили слоя и стили текста, Sketch может разделить их на иерархические категории в своих меню символов и стилей текста с помощью «/» (косая черта). Соблюдение соглашений об именах и наличие четко определенного набора основных категорий придаст файлам организованную структуру, уменьшая путаницу и несоответствия.
Соблюдение соглашений об именах и наличие четко определенного набора основных категорий придаст файлам организованную структуру, уменьшая путаницу и несоответствия.
В Sketch мы можем использовать меню панели вставки для перетаскивания повторно используемых компонентов, которые были созданы.
Вот несколько способов создания иерархических категорий для символов, текста и стилей слоя в Sketch.
Мы можем представить символы, используя следующее предлагаемое соглашение об именах в разделе Atoms/ :
- Assets
- Кнопки
- Элементы управления вводом
- Изображения
- Навигация
- Информация
Мы можем быстро и легко создавать атомы символов в Sketch, которые станут основой для системы дизайна с использованием атомарного дизайна.
Мы не будем преобразовывать стили слоев в символы, поэтому достаточно идентифицировать их по семантической группе. Опять же, используя Атомы /:
- Заполняет
- Границы
- Тени
- Градиенты
Атомы стиля слоя могут быть определены в Sketch, который будет использоваться во всей системе дизайна.
Подобно стилям слоя, вот как мы можем создать стили текста под Atoms /:
- Заголовки
- Корпус
- Заголовок
- Этикетки
- Ссылки
Атомы текстового стиля в Sketch помогают создать основу системы дизайна с использованием методологии атомарного дизайна.
Единый язык дизайна не должен быть просто набором статических правил и отдельных атомов; это должна быть развивающаяся экосистема. — Airbnb о создании визуального языка.
Создание молекул
Атомы определяют основную часть рекомендаций по дизайну продукта, но сами по себе они не совсем полезны. Чтобы получить некоторую функциональность, мы соединяем атомы вместе и создаем молекулы.
Соединение метки (атома) с кнопкой ввода (атома) для создания функции поиска — хороший пример часто используемого элемента молекулы.
Объединение атомов в Sketch для формирования функциональных молекул.
Предостережение: здесь может быть некоторая серая зона. Кнопка на уровне кода считается атомом, но кнопка на уровне дизайна считается молекулой, поскольку мы группируем стиль слоя и атом стиля текста. Чтобы избежать путаницы, рекомендуется думать только об элементах уровня кода.
Основные категории, подпадающие под Молекулы/:
- Информация
- Навигация
- Элементы управления вводом
Поскольку молекулы будут формировать нашу продукцию интерактивным образом, было бы неплохо уточнить вышеуказанные категории. В этом случае мы определим набор подкатегорий, представляющих библиотеку шаблонов:
- Раскрывающиеся списки
- Переключатели
- Слайдеры
- Вкладки
- Пагинация
- Индикаторы выполнения
- Поля даты
- Текстовые поля
- Флажки
- Радиокнопки
- Модули
Объединение атомов в Sketch для создания функциональных молекул.
Создание организмов
Организмы представляют собой группы атомов и молекул. Они также могут быть частью других организмов.
В отличие от атомов и молекул, организмы не имеют абстрактного включения в продукты, которые мы разрабатываем; это конкретные повторно используемые компоненты, которые можно легко идентифицировать с конкретными действиями. Их структура сложнее, чем у атома или молекулы.
Если предварительно определенное поле поиска сгруппировано с другими компонентами, такими как панель навигации (молекула) и логотип (атом), создается организм. Примером может служить панель навигации или календарь.
Организмы, как и молекулы, могут относиться к одним и тем же категориям и подкатегориям:
Вот основные категории, которые мы создадим для Организмов/:
- Информация
- Навигация
- Элементы управления вводом
В Sketch, Atomic Design организмы можно создавать, комбинируя атомы и молекулы. Слева направо у нас есть организм чата, организм заголовка и два примера мобильных навигационных организмов.
Слева направо у нас есть организм чата, организм заголовка и два примера мобильных навигационных организмов.
Как и в случае с молекулами, мы также создадим подкатегории для организмов:
- Выпадающие списки
- Переключатели
- Слайдеры
- Вкладки
- Пагинация
- Индикаторы выполнения
- Поля даты
До этого момента большая часть пользовательского интерфейса уже была разработана, так что теперь это так же просто, как вызывать экземпляры наших компонентов, когда они необходимы для дизайна.
Каждый из этих компонентов легко найти по их семантическим группам, либо выполнив поиск непосредственно с помощью панели вставки на панели инструментов «Эскиз», где мы найдем хорошо организованный набор из 3 основных категорий, либо с помощью плагин, такой как Runner для Sketch.
Компоненты Atomic Design в Sketch можно найти с помощью панели вставки на панели инструментов Sketch. Это позволяет дизайнерам быстро и легко использовать компоненты во всем дизайне.
Runner for Sketch оптимизирует рабочий процесс дизайнера, предоставляя набор клавиатурных команд, которые они могут использовать вместо поиска вещей в бесконечных меню. Например, они могут ввести слово , вставить , нажать клавишу вкладки и найти нужные компоненты.
При вводе атомов раскрывающийся список покажет нам все элементы, подпадающие под эту категорию. Если атомы и молекулы имеют общие категории, будут видны только атомы, а все молекулы будут проигнорированы.
Плагины, такие как Runner for Sketch , позволяют использовать сочетания клавиш для поиска компонентов вместо просмотра бесконечных меню.
Подведение итогов
Sketch и Atomic Design — это мощный набор инструментов, которые можно использовать вместе для улучшения рабочих процессов проектирования и создания эффективной структуры системы проектирования.
Используя концепцию атомов , молекул и организмов в качестве основы компонентов, Atomic Design помогает дизайнерам объединяться вокруг общего языка во время создания и жизни продукта.
