Валентность мышьяка (As), формулы и примеры
Общие сведения о валентности мышьяка
Мышьяк существует в виде нескольких аллотропных модификаций. Наиболее устойчив при обычных условиях металлический (серый) мышьяк. Он образует серо-стальную хрупкую кристаллическую массу с металлическим блеском на свежем изломе. Плотность 5,72 г/см3. При нагревании под нормальным давлением серый мышьяк сублимируется. Обладает металлической электрической проводимостью.
При быстром охлаждении пара, состоящего из молекул As4, образуется неметаллическая модификация желтый мышьяк. Плотность 2,0 г/см3. При действии света или слабом нагревании переходит в серый мышьяк.
Валентность мышьяка в соединениях
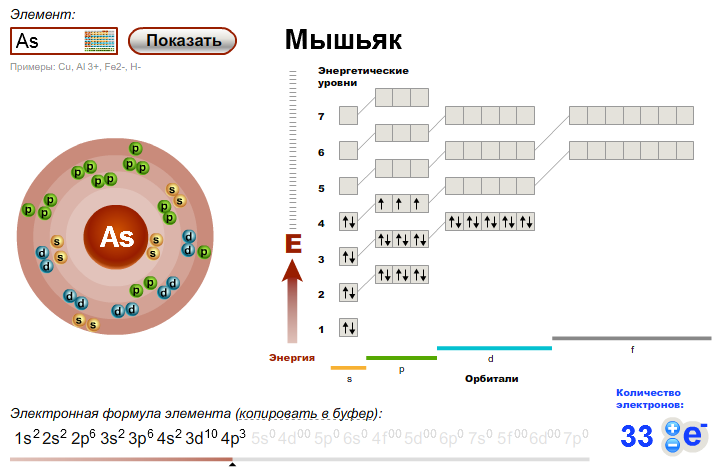
Мышьяк – тридцать третий по счету элемент Периодической таблицы Д.И. Менделеева. Он находится в четвертом периоде в VA группе. В ядре атома мышьяка содержится 33 протона и 42 нейтрона (массовое число равно 75). В атоме мышьяка есть четыре энергетических уровня, на которых находятся 33 электрона (рис.
Рис. 1. Строение атома мышьяка.
Электронная формула атома мышьяка в основном состоянии имеет следующий вид:
1s22s22p63s23p63d104s24p3.
А энергетическая диаграмма (строится только для электронов внешнего энергетического уровня, которые по-другому называют валентными):
Наличие трех неспаренных электронов свидетельствует о том, что мышьяк способен проявлять валентность III (низшая валентность) в своих соединениях (As2O3, AsH3
Для атома мышьяка характерно наличие возбужденного состояния из-за того, что орбитали 4d-подуровня являются вакантными (на четвертом энергетическом слое помимо 4s- и 4p-подуровней есть еще и 4d-подуровень). Электроны 4s-подуровня распариваются и занимают свободную орбиталь 4p -подуровня:
Наличие пяти неспаренных электронов в возбужденном состоянии свидетельствует о том, что мышьяк также проявляет в своих соединениях валентность V (H3AsO4, As2O5) (высшая валентность).
Примеры решения задач
Электронная конфигурация атома элемента (мышьяк)
Решение задачи
4-й период, VA-группа.
Определим, атом какого элемента расположен в 4 периоде, VA-группе Периодической системы Д.И. Менделеева (смотри таблицу Менделеева) – мышьяк (As).
Число электронов в атоме равно заряду его ядра, следовательно, электронная оболочка As содержит 33 электрона. Номер периода равен числу энергетических уровней в атоме, а номер группы – числу электронов на внешнем уровне (валентных электронов). Координаты As: (4, VА) то есть атом имеет четыре энергетических уровня; имеет пять электрон на внешнем уровне; р – элемент.
Запишем электронную конфигурацию атома элемента As:
Используя электронную конфигурацию атома элемента, изобразим электронную схему строения внешнего уровня, которая характеризует распределение электронов по энергетическим уровням, подуровням и атомным орбиталям, руководствуясь принципом Паули и правилом Гунда:
Электронная конфигурация атома элемента.
Химические свойства атома определяются строением внешнего энергетического уровня. Вступая в химическое взаимодействие, любой атом стремится завершить внешний уровень. Атом As имеет 5 валентных электронов, поэтому завершение внешнего уровня возможно за счет присоединения трех электронов. Принимая их, атом мышьяка проявляет окислительные свойства:
As0 + 3 e—= As -3
As0 (4s2 4p3)
As -3 (4s2 4p6)
Атом мышьяка может проявлять восстановительные свойства, отдавая электроны внешнего уровня — три или все пять:
As0 — 3 e—
As0 — 5 e—= As +5
As0 (4s2 4p3)
As +3 (4s2)
As +5 (3s2 3p6 3d10)
Мышьяк электронное строение – Справочник химика 21
Фосфор, мышьяк или сурьма (имеющие электронное строение внешнего энергетического уровня s pЗ и проявляющие валентность 5), будучи введенными в кристаллические решетки германия или олова (электронное строение внешнего уровня 5 р валентность 4) ведут себя как донорные примеси, т. е. отдают электроны и создают проводимость п-типа. Если же в германий или кремний ввести бор, алюминий, галлий или индий (электронное строение внешнего уровня 5 р, валентность 3), то атомы примеси захватывают четвертый электрон и полупроводник обнаруживает проводимость р-типа.
е. отдают электроны и создают проводимость п-типа. Если же в германий или кремний ввести бор, алюминий, галлий или индий (электронное строение внешнего уровня 5 р, валентность 3), то атомы примеси захватывают четвертый электрон и полупроводник обнаруживает проводимость р-типа. Научные работы посвящены физикохимии флотационных процессов и исследованию комплексооб-)азования парамагнитных ионов. Исследовал продукты взаимодействия реагентов с минералами с применением методов радиоспектроскопии. Установил влияние электронно-дырочных центров минералов на изменение их флотационных свойств. Разработал синтез спин-меченых флотореагентов и нашел пути их широкого использования для изучения механизма взаимодействия реагентов с поверхностью минералов. Разработал технологию комплексной переработки руд ряда месторождений. Изучал комнлексообразование парамагнитных ионов с лигандами, содержащими атомы серы, кислорода, азота, селена, фосфора и мышьяка.
Электронное строение атомов фосфора, мышьяка, сурьмы и висмута [c.275]
На основании электронного строения атомов р-элементов IV и V групп, изменения их атомных радиусов, их металлических и неметаллических свойств решите вопрос об изменении наиболее устойчивой степени окисления этих элементов по группам. Ответ мотивируйте составлением уравнений реакций растворения в азотной кислоте а) углерода, кремния, олова, свинца б) мышьяка, сурьмы, висмута.
Строение внешней электронной оболочки атома Азот Фосфор Мышьяк Сурьма Висмут [c.427]
Рассмотренное строение двойного слоя характерно для собственных полупроводников, в которых нет ни объемных примесей (добавок), ни так называемых поверхностных состояний, обусловленных чаще всего адсорбцией чужеродных атомов. Часто полупроводник в качестве примеси содержит атомы такого вещества, благодаря которому резко увеличивается число свободных электронов п.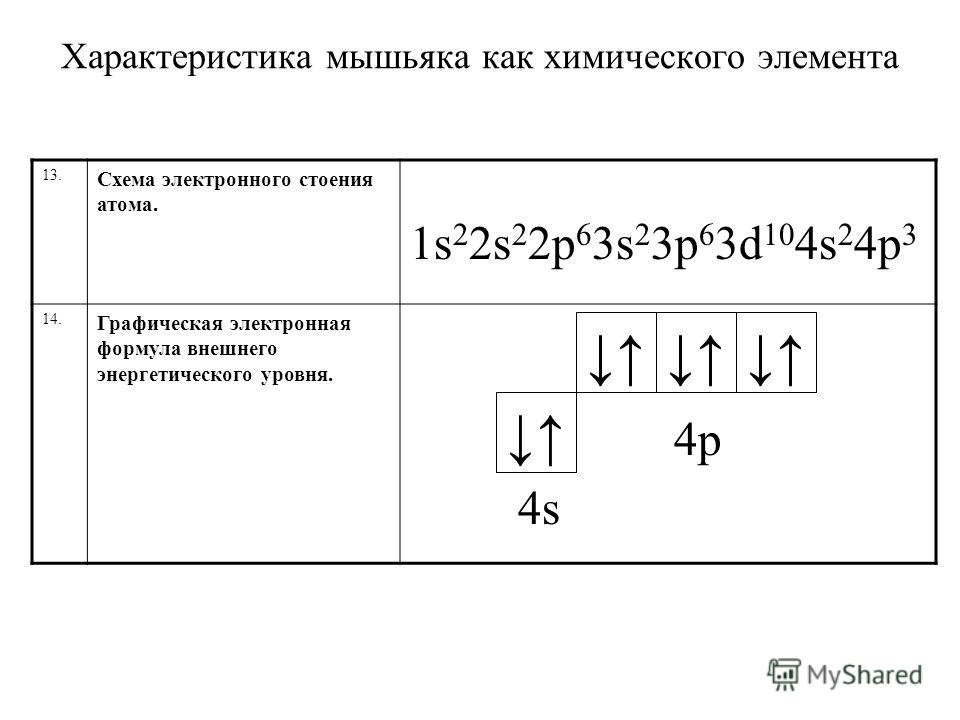
Рассмотренное строение двойного слоя характерно для собственных полупроводников, в которых нет ни объемных примесей (добавок), ни так называемых поверхностных состояний, обусловленных чаще всего адсорбцией чужеродных атомов. Часто полупроводник в качестве примеси содержит атомы такого вещества, благодаря которому резко увеличивается число свободных электронов п. Такие добавки называются донорами электронов. Для германия такой добавкой служит мышьяк. Поскольку произведение пр в присутствии доноров электронов остается постоянным [уравнение (28.3)1, то увеличение п приводит к соответствующему уменьшению числа дырок р = Поэтому
Часто полупроводник в качестве примеси содержит атомы такого вещества, благодаря которому резко увеличивается число свободных электронов п. Такие добавки называются донорами электронов. Для германия такой добавкой служит мышьяк. Поскольку произведение пр в присутствии доноров электронов остается постоянным [уравнение (28.3)1, то увеличение п приводит к соответствующему уменьшению числа дырок р = Поэтому
Больщинство известных химических элементов, находясь в виде простых веществ, представляют собой металлы. Некоторые элементы (германий, мышьяк, сурьма, алюминий) в одних условиях ведут себя как металлы, в других условиях — как неметаллы. Все металлы имеют на внешнем энергетическом уровне небольшое число валентных электронов — электронные конфигурации металлов представлены в табл. I. Повторение химических свойств металлов обусловлено периодическим повторением строения электронных конфигураций внешних электронных уровней.
Сурьма принадлежит к пятой группе периодической системы химических элементов Д.
 И. Менделеева и входит в подгруппу мышьяка. Атомная масса сурьмы равна 121,75 [213, 992], атомный номер 51. Строение электронной оболочки 1 , 2 , 2/) , З , Зр 45 , 4р , 4 1 , 5s 5р [c.7]
И. Менделеева и входит в подгруппу мышьяка. Атомная масса сурьмы равна 121,75 [213, 992], атомный номер 51. Строение электронной оболочки 1 , 2 , 2/) , З , Зр 45 , 4р , 4 1 , 5s 5р [c.7]Процессы старения и связанные с ними изменения формы и строения коллоидных частиц в золях сернистого мышьяка протекают очень медленно. Так, золи полуторагодичной давности дают такую же электронографическую картину, как и свежеприготовленные золи. Электронно-микроско-пическая картина отличается лишь тем, что в старых золях можно наблюдать большее количество агрегатов. [c.171]
Внутреннее строение атома В1 роднит его не только с мышьяком и сурьмой, что естественно, но и со многими другими металлами. В атоме висмута есть предпоследний 18-электронный слой (слой типа купро ), который характерен для свинца, а также меди и ее аналогов (Ап, Ag). Интересно, что с этими же элементами висмут нередко бывает связан в рудных месторождениях. [c.240]
Мышьяк Аз (5-10 %), сурьма 8Ь (110″ %) и висмут В1 (2-10″ %). Строение электронных оболочек атомов этих элементов отличается от такового для азота и фосфора. Второй снаружи энергетический уровень в атомах мышьяка, сурьмы и висмута содержит 18 электронов (п—1)5 (тг—1)р (/г—1) 1 . В связи со значительным ростом радиусов атомов и уменьшением энергии ионизации атомы этих элементов могут превращаться в положительно заряженные ионы Однако восстановительные свойства их [c.364]
Строение электронных оболочек атомов этих элементов отличается от такового для азота и фосфора. Второй снаружи энергетический уровень в атомах мышьяка, сурьмы и висмута содержит 18 электронов (п—1)5 (тг—1)р (/г—1) 1 . В связи со значительным ростом радиусов атомов и уменьшением энергии ионизации атомы этих элементов могут превращаться в положительно заряженные ионы Однако восстановительные свойства их [c.364]
Соединения бора с другими элементами. Существует много других типов соединений, в которых атом бора связан с азотом, фосфором, мышьяком, серой и углеродом. Борорганические соединения уже упоминались в разд. 12.5. Здесь мы отметим лишь некоторые соединения бора с азотом. Фрагмент —ЫН — ВК — идентичен структурному элементу—СН = СН—и может замещать его во многих соединениях. Мы уже отмечали графитоподобное строение нитрида бора ВЫ (разд, 12.2). Эту аналогию можно сделать более понятной, если принять, что истинное электронное распределение в связи В — N может быть описано резонансным гибридом, [c. 291]
291]
Таким образом, теория Льюиса объясняет кислотно- и основные свойства веществ с позиции их строения. Это является одним из существенных недостатков рассматриваемой теории. Не только строение, но и состав и многие другие, неучитываемые Льюисом факторы, определяют проявление веществом кислотно-основного характера. Теория Льюиса не объясняет кислотные свойства многих кислот (в том числе как содержащих, таки не содержащих в своем составе водород), ограничиваясь узкими рамками кислотноосновных реакций, которые протекают по донорно-акцепторному механизму. Например, сопоставляя электронные формулы молекул аммиака и хлорида мышьяка(П1) [c.136]
Строение внешних электронных слоев ионов подгруппы мышьяка такое же, как и катионов подгруппы меди. К подгруппе мышьяка относятся ионы, имеющие а) внешний 18- или (18 + 2)-электронный слой б) незаконченный, т. е. переходный, от 8-к 18-электронному внешнему слою, при условии, если имеются 18- или 32-электронные глубинные слои, наличие которых усиливает и поляризующее действие и собственную поляризуемость ионов. [c.397]
[c.397]
Подгруппа мышьяка. Мышьяк. Элементы подгруппы мышьяка — мышьяк, сурьма и висмут — имеют во внешнем квантовом слое атомов такое же число электронов, как азот и фосфор. Однако они отличаются строением предпоследнего квантового слоя, который содержит 18 электронов . Этим объясняется зна- [c.274]
Свойства атомов. Сопоставление внутренних электронных остовов, валентных и вакантных подуровней показывает, что различия в физических и химических свойствах элементов обусловлены в основном особенностями строения электронных оболочек атомов (табл. 19.2). Атомы элементов этой подгруппы имеют совпадающие по строению валентные подуровни (пз пр ), различные электронные остовы и вакантные подуровни. Два электрона валентных з-подуровней спарены, три электрона р-подуровней заселяют орбитали этих подуровней по одному. Электронная структура азота выделяется отсутствием вакантных подуровней, энергетически близких к наполовину заполненному 2р-подуровню. У фосфора есть один вакантный с -подуровень, а мышьяк, сурьма и висмут имеют несколько вакантных подуровней, близко расположенных к валентным подуровням. [c.383]
У фосфора есть один вакантный с -подуровень, а мышьяк, сурьма и висмут имеют несколько вакантных подуровней, близко расположенных к валентным подуровням. [c.383]
Используя представления о кайносимметрии, можно выделить более тонкий вид электронной аналогии, так называемую слоевую аналогию (в дополнение к групповой и типовой аналогии). Слоевыми аналогами называют элементы, которые являются типовыми аналогами, но не имеют внешних или предвнешних кайносимметричных электронов. К таким аналогам относятся, например, в IA-группе К, Rb, s и Fr, а Li и Na не являются слоевыми аналогами с остальными щелочными металлами, поскольку у Li присутствует внешняя кайносимметричная 2р-оболочка (вакантная), а у Na кайносимметрнчная заполненная 2р-оболочка является предвнеш-ней. В ПА-группе слоевыми аналогами являются щелочно-земельные металлы (подгруппа кальция), а в П1А-группе — элементы подгруппы галлия и т. д. С точки зрения электронного строения слоевые аналоги являются между собой полными электронными аналогами. Поэтому рассматривать химические свойства элементов группы мы будет в такой последовательности первый типический элемент, второй типический элемент, остальные элементы главной подгруппы, элементы побочной подгруппы. Например, в И1 группе отдельно рассматриваются бор, алюминий, подгруппа галлия, подгруппа скандия в V группе — азот, фосфор, подгруппа мышьяка, подгруппа ванадия п т. п. [c.15]
Поэтому рассматривать химические свойства элементов группы мы будет в такой последовательности первый типический элемент, второй типический элемент, остальные элементы главной подгруппы, элементы побочной подгруппы. Например, в И1 группе отдельно рассматриваются бор, алюминий, подгруппа галлия, подгруппа скандия в V группе — азот, фосфор, подгруппа мышьяка, подгруппа ванадия п т. п. [c.15]
Валентная электронная конфигурация всех элементов VA-группы— ns np , т. е. на внешнем энергетическом (валентном) уровне они содержат 2 спаренных s-электрона и 3 неспаренных (в соответствии с правилом Гунда) электрона на трехкратно вырожденном р-уровне. Однако между элементами этой группы существуют и различия в электронном строении. Так, у фосфора в отличие от азота впервые появляется вакантный внешний М-уровепь, что обусловливает возможность промотирования одного 35-электрона с образованием пятиковалентного состояния, которое, как известно, отсутствует у азота. У мышьяка, сурьмы и висмута к вакантному -уровню добавляется еще в отличие от фосфора полностью завершенный внутренний (п—1) -уровень, а у висмута, следующего за лентаноидами, кроме того, и 4/ -уровень.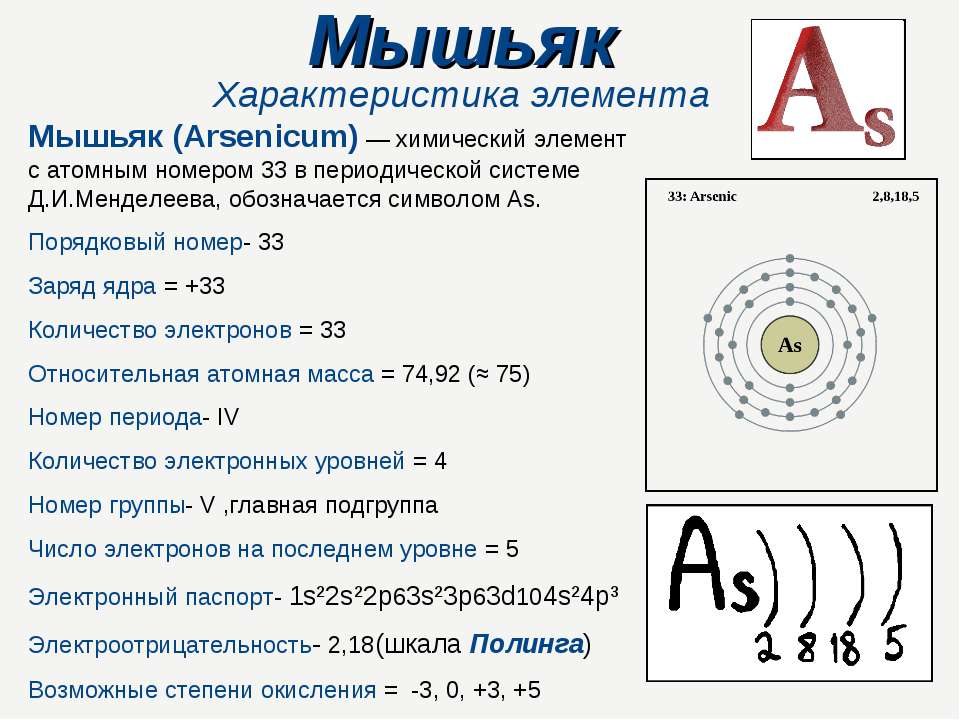 [c.282]
[c.282]
Наличие заполненных предвнешних (п—l)d- и (п—2)/-уровней сверх оболочки предыдущего благородного газа накладывает отпечаток на свойства элементов подгруппы мышьяка. Отметим, что между собой мышьяк, сурьма и висмут являются полными электронными аналогами и отличаются с точки зрения электронного строения от типических элементов VA-группы — азота и фосфора, т. е. по отношению к ним являются неполными электронными аналогами. [c.282]
Подгруппа иьппьяка. Характеристика элементов УА-группы. Валентная электронная конфигурация всех элементов УА-Г1зуппы — пз пр , т.е. на внешнем энергетическом (валентном) уровне они содержат два спаренных -электрона и три неспаренных электрона на трехкратно вырожденном пр-уровне. Однако между элементами этой группы существуют и р личия в электронном строении. У мышьяка, сурьмы и висмута к вакантному пс(-уровню добавляется еще в отличие от фосфора полностью завершенный внутренний (п — 1) -уровень, а у висмута, следующего за лантаноидами, кроме того, и 4/ -уровень.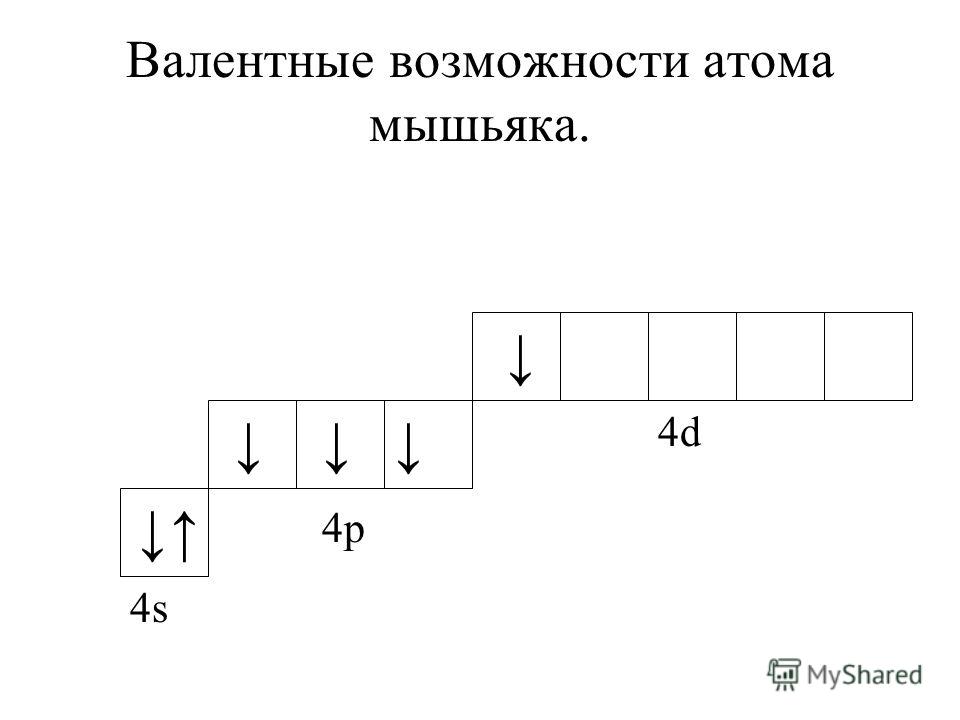 В силу наличия внутренних и /оболочек, экранирующих внешние электроны, в ряду Аз — 8Ь — В1 проявляется вторичная периодичность. В результате этого для среднего элемента ряда — сурьмы — степень окисления +5 оказывается более стабильной, чем для мышьяка и висмута. [c.417]
В силу наличия внутренних и /оболочек, экранирующих внешние электроны, в ряду Аз — 8Ь — В1 проявляется вторичная периодичность. В результате этого для среднего элемента ряда — сурьмы — степень окисления +5 оказывается более стабильной, чем для мышьяка и висмута. [c.417]
В результате оба атома образуют ковалентные а-связи с тремя заместителями, например КзАз или Кз5Ь, причем орбитали центрального атома оказываются средними между Зр-орби-талями, требующими угла 90° между связями, и хр -гибридизо-ванными орбиталями, требующими углов около 109,5° [1]. Как и следовало ожидать из электронного строения и по аналогии с такими же соединениями фосфора, соединения трехвалентного мышьяка и сурьмы являются основаниями Льюиса и образуют четвертичные соли. [c.302]
Хотя химия органических соединений фосфора и мышьяка широко изучается многими авторами с использованием разнообразных физических и химических методов /1-15/,проблема механизма электронных взаимодействий в них еще далека от своего решения. С целью получения дополнительной информации по этому вопросу в настоящей работе исследовано влияние факторов электронного строения на скорость основного дейтерообмена метильной группы и некоторые спектроскопические характеристики третичных метил-фенилфосфинов и арсинов,соответствующих им окисей,сульфидов и “ониевых” соединений. [c.443]
С целью получения дополнительной информации по этому вопросу в настоящей работе исследовано влияние факторов электронного строения на скорость основного дейтерообмена метильной группы и некоторые спектроскопические характеристики третичных метил-фенилфосфинов и арсинов,соответствующих им окисей,сульфидов и “ониевых” соединений. [c.443]
Свойства элементов и простых веществ закономерно изменяются в подгруппе с ростом радиуса атомов и уменьшением энергии ионизации, как это можно видеть из табл. 27. Азот и фосфор — типичные неметаллы, т. е. кислотообразователи. Различия в строении предвнеш-него электронного уровня у атомов фосфора и мышьяка меньше сказываются на изменении свойств элементов, чем при переходе от кремния к германию в IVA-подгруппе. У мышьяка сильнее выражены неметаллические свойства. У сурьмы неметаллические и металлические свойства проявляются приблизительно в одинаковой степени. Для висмута характерно преобладание металлических (основных) свойств. [c.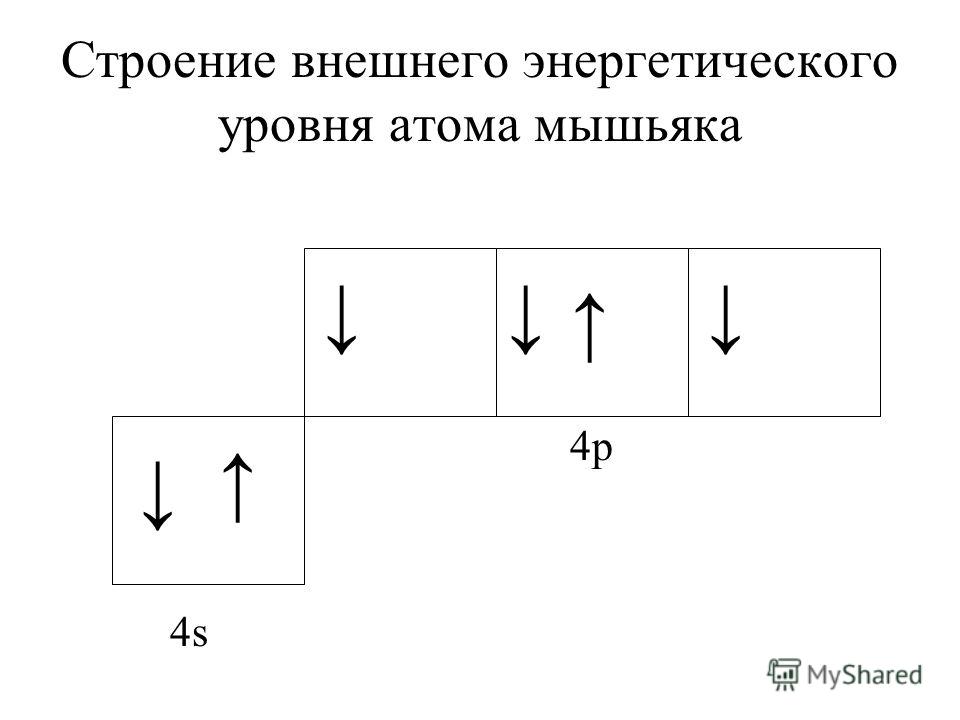 339]
339]
Бинарные соединения, оба компонента которых расположены справа от границы Цинтля, как отмечено выше, характеризуются преимущественно ковалентным типом взаимодействия в силу незначительной разности ОЭО. Правило октета здесь соблюдается, поскольку число валентных электронов у обоих компонентов достаточно для реализации ковалентного взаимодействия. Для соединений, подчиняющихся правилу формальной валентности, у катионообразователя необходимо учитывать лишь число электронов, участвующих в образовании связи. Так, в оксидах мышьяка АзгОз и АззОз у кислорода в обоих случаях учитывается шесть электронов, а у мышьяка в первом случае три, а втором — пять электронов. Тогда для АзгОз получим (3-2 + 6-3)/3 = 8, а для АзгОб — (5-2 + 6-5)/5 = 8. Если соединения не подчиняются правилу формальной валентности, то применимо правило Музера — Пирсона. Особенности кристаллохимического строения бинарных соединений с компонентами, расположенными справа от границы Цинтля, состоят в том, что в их структуре присутствуют группировки атомов в виде цепочек, сеток и молекул.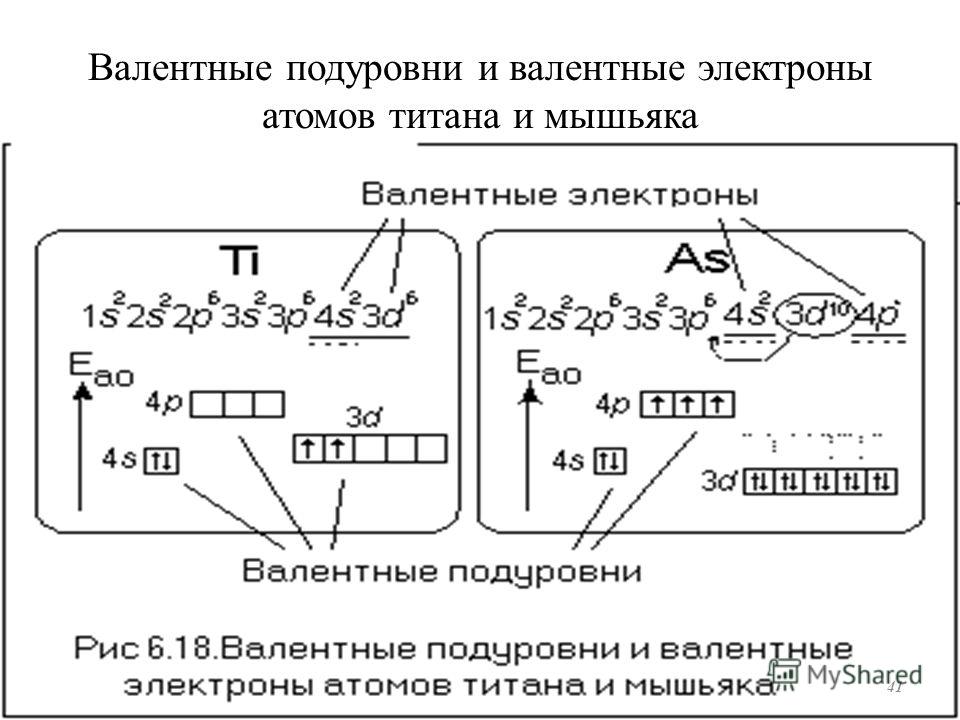 Следовательно, кроме ковалентной связи здесь реализуется и межмолекулярное взаимодействие. [c.261]
Следовательно, кроме ковалентной связи здесь реализуется и межмолекулярное взаимодействие. [c.261]
В настоящей работе было предпринято электронно-микроскопическое исследование структуры некоторых аморфных полимеров, обладающих различным строением молекулярных цепей. В качестве объектов были изучены полимеры мышьяка (сальварсан), полиакриламид и сополимер па основе метилметакрилата и метакриловой кислоты. Таким образом, были исследованы полимеры, содержащие различные полярные группы в цепи и, следовательно, обладающие различными внутри- и межмолекулярными силами взаимодействия. [c.121]
Проведены некоторые определения сравнительной легкости, с которой фосфины, арсины и стибины аналогичного строения способны расширять свою валентную оболочку. Обширная информация получена при использовании этих соединений в качестве лигандов в комплексах с металлами. Чатт и Харт [11] исследовали монозамещенные карбонилы никеля Ы1(С0)зЦ где Ь=(СбН5)зР или (СбН5)зАз.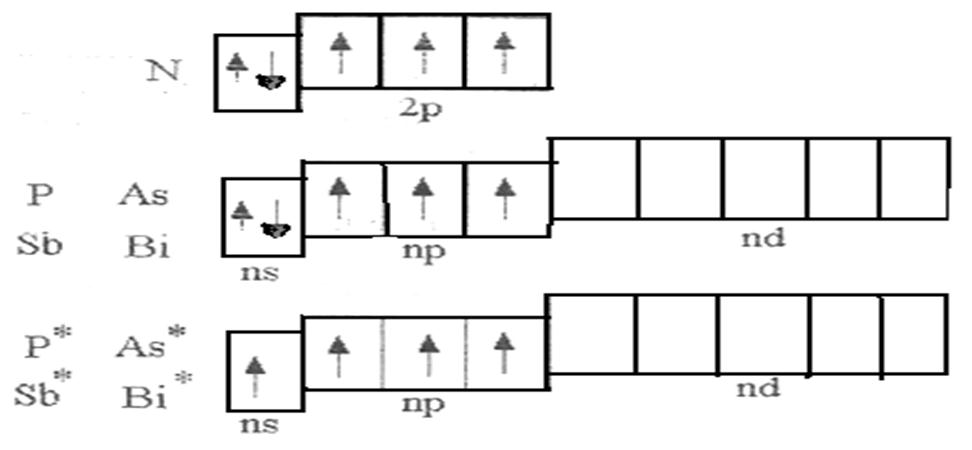 Эти соединения были приготовлены вытеснением окиси углерода из тетракарбонила никеля, причем эта реакция шла много быстрее в случае фосфина. Однако частота колебаний карбонильной группы фосфина составляла 2063 см тогда как для арсина 2072 см К На основании этих данных было принято, что обратная подача электронов с заполненных -орбиталей никеля в направлении СО-групп больше в случае фосфинового комплекса по сравнению с тем же эффектом в арсиновом комплексе. Другими словами, арсин (фактически в виде арсониевой группы, поскольку мышьяк поделил электроны с никелем) вновь принимает электроны на свои вакантные -орбитали в большей мере, чем фосфор в фосфине (т. е. вклад структуры Па больше, чем вклад 1а в истинное р ас-пределение электронной плотности в соответствующем комплексе). [c.304]
Эти соединения были приготовлены вытеснением окиси углерода из тетракарбонила никеля, причем эта реакция шла много быстрее в случае фосфина. Однако частота колебаний карбонильной группы фосфина составляла 2063 см тогда как для арсина 2072 см К На основании этих данных было принято, что обратная подача электронов с заполненных -орбиталей никеля в направлении СО-групп больше в случае фосфинового комплекса по сравнению с тем же эффектом в арсиновом комплексе. Другими словами, арсин (фактически в виде арсониевой группы, поскольку мышьяк поделил электроны с никелем) вновь принимает электроны на свои вакантные -орбитали в большей мере, чем фосфор в фосфине (т. е. вклад структуры Па больше, чем вклад 1а в истинное р ас-пределение электронной плотности в соответствующем комплексе). [c.304]
Как видно из приведенных в табл. III. 4 данных, по химическому строению диазиды делятся на четыре группы к первой группе (соединения 1—6) относятся вещества, в которых азидсодержащие арильные ядра не сопряжены, ко второй (7—20)—соединения, в которых электронное взаимодействие между такими ядрами осуществляется через карбонил, к третьей (21—27)—диазиды, в молекулах которых имеется единая сопряженная система, к четвертой (28—31)—формально сопряженные и несопряженные диазиды, содержащие гетероатом фосфора, мышьяка и другие в цепи, связывающей два ароматических ядра. [c.122]
[c.122]
С)т формы частиц дисперсной фазы зависят некоторые свойства коллоидных растворов. Так, коллоидные системы асимметрического строения способны образовать внутреннюю сетчатую структуру. На рис. 174 и 175 приведены полученные на электронном микроскопе снимки коллоидных частиц свежеприготовленного золя сульфида мышьяка и пятнокиси ванадия. Как видно из этих рисунков, частицы пятиолиси [c.407]
На основании приведенных данных можно считать твердо установленным экстремум значений проводимости, магнитной восприимчивости, плотности и микротвердости у стекол системы мышьяк—селен, содержащих 9 ат. % мышьяка. Наличие экстремальных значений характеристических величин свидетельствует о существенном изменении структуры стеклообразных сплавов в этой области составов. Л инимальное значение магнитной восприимчивости у стекол, содержащих -9ат. % мышьяка, связано с изменением степени деформации валентных электронных облаков в химических связях As—Se и Se—Se.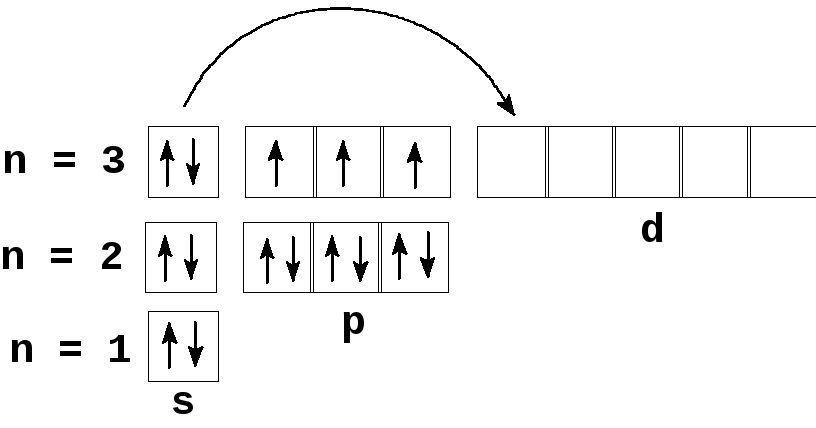 Это изменение обусловлено статистическим распределением трехмерных пространственных структурных единиц образующегося AsaSes в структуре стеклообразного селена. В таких стеклообразных сплавах с максимально неупорядоченным строением затрудняется сквозной перенос носителей заряда, для них получены заниженные значения плотности и микро-твердости. Перенос носителей заряда с конца оборванной цепи на соседнюю цепь в таких стеклообразных сплавах требует преодоления значительного активационного барьера. Такой перенос может осуществляться в результате перекрытия электронных орбит в процессе низкочастотных термических колеба- [c.44]
Это изменение обусловлено статистическим распределением трехмерных пространственных структурных единиц образующегося AsaSes в структуре стеклообразного селена. В таких стеклообразных сплавах с максимально неупорядоченным строением затрудняется сквозной перенос носителей заряда, для них получены заниженные значения плотности и микро-твердости. Перенос носителей заряда с конца оборванной цепи на соседнюю цепь в таких стеклообразных сплавах требует преодоления значительного активационного барьера. Такой перенос может осуществляться в результате перекрытия электронных орбит в процессе низкочастотных термических колеба- [c.44]
Общим для трех исследованных систем является наличие области максимальных значений парамагнетизма Ван-Флека. Для составов с максимальными значениями парамагнитной составляющей получены также экстремальные значения парамет-)0Б электропроводности и других физико-химических величин. 4з анализа полученных экстремальных значений следует, что стекла указанных составов характеризуются статистическим распределением структурных единиц АзЗез/г, АзЗз/г и ОеЗе4/г в полимерных цепях и циклах стеклообразных селена и серы. Такое распределение приводит к нарушению правильности чередования структурных единиц, нарушению исходного ближнего порядка и вносит тем самым дополнительную асимметрию в строение электронных оболочек атомов. Стекла в системе Аз—Зе с содержанием 9 ат. % мышьяка, в системе Аз—3 с содержанием мышьяка 12 ат. % и в системе Се—Зе с содержанием 6—7 ат, % германия имеют наименьшую степень [c.73]
Одним из последних экспериментальных подтверждений уменьшения тенденции к образованию я-связей у тяжелых элементов V группы является работа Бигли и др. [23], изучавших молекулу А5(5 Нз)з. Эта молекула имеет пирамидальное строение, все углы SiAsS равны 93°. Очевидно, для образования связей АзЗ мышьяк использует только р-орбитали неподеленная пара электронов располагается в основном на х-орбитали. Электроны неподеленной пары не могут переходить на вакантные З -орбитали кремния и вносить вклад в образование двойных связей. [c.175]
Мышьяк
| Мышьяк | |
|---|---|
| Атомный номер | 33 |
| Внешний вид простого вещества | |
| Свойства атома | |
|
Атомная масса (молярная масса) |
74,92159 а.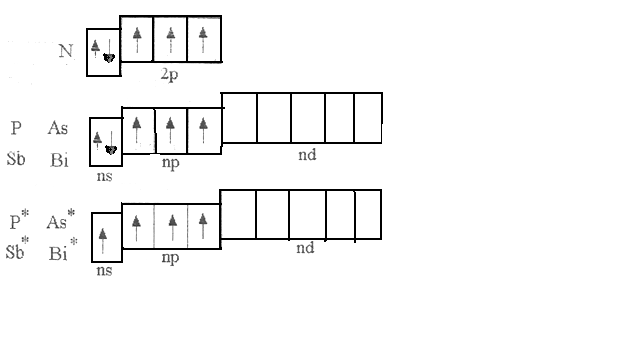 е. м. (г/моль) е. м. (г/моль) |
| Радиус атома | 139 пм |
|
Энергия ионизации (первый электрон) |
946,2(9,81) кДж/моль (эВ) |
| Электронная конфигурация | [Ar] 3d10 4s2 4p3 |
| Химические свойства | |
| Ковалентный радиус | 120 пм |
| Радиус иона | (+5e)46 (-3e)222 пм |
|
Электроотрицательность (по Полингу) |
2,18 |
| Электродный потенциал | 0 |
| Степени окисления | 5, 3, −3 |
| Термодинамические свойства простого вещества | |
| Плотность | 5,73 (grey arsenic) г/см³ |
| Молярная теплоёмкость | 25,05 Дж/(K·моль) |
| Теплопроводность | (50,2) Вт/(м·K) |
| Температура плавления | 1090 K |
| Теплота плавления | n/a кДж/моль |
| Температура кипения | 876 K |
| Теплота испарения | 32,4 кДж/моль |
| Молярный объём | 13,1 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | ромбоэдрическая |
| Параметры решётки | a=4,132 α=54,13 Å |
| Отношение c/a | 2,805 |
| Температура Дебая | 285 K |
| As | 33 |
| 74,9216 | |
| 4s24p3 | |
| Мышьяк | |
Мышьяк — химический элемент с атомным номером 33 в периодической системе, обозначается символом As. Представляет собой хрупкий полуметалл стального цвета.
Представляет собой хрупкий полуметалл стального цвета.
Название мышьяка в русском языке связывают с употреблением его соединений для истребления мышей и крыс. Греческое название arsenikon происходит от персидского زرنيخ (zarnik) — «жёлтый аурипигмент». Иногда его производят от греческого «арсен» — сильный, мощный.
Нахождение в природе
Мышьяк — рассеянный элемент. Содержание в земной коре 1,7·10-4% по массе. Это вещество может встречаться в самородном состоянии, имеет вид металлически блестящих серых скорлупок или плотных масс, состоящих из маленьких зернышек. Известно около 200 мышьяксодержащих минералов. В небольших концентрациях часто содержится в свинцовых, медных и серебряных рудах. Довольно часто встречаются два природных соединения мышьяка с серой: оранжево-красный прозрачный реальгар AsS и лимонно-желтый аурипигмент As2S3. Минерал, имеющий промышленное значение — арсенопирит (мышьяковый колчедан) FeAsS или FeS2•FeAs2, также добывают мышьяковистый колчедан — лёллингит (FeAs2).
Получение
Открытие способа получения так называемого металлического мышьяка (серого мышьяка) приписывают знаменитому средневековому алхимику Альберту Великому, жившему в XIII в. Однако гораздо ранее греческие и арабские алхимики умели получать мышьяк в свободном виде, нагревая «белый мышьяк» (то, что это триоксид мышьяка, а не простое вещество, было выявлено лишь в 1789 г. А. Л. Лавуазье, который и присвоил элементу название «арсеникум») с различными органическими веществами. Существует множество способов получения мышьяка: сублимацией природного мышьяка, способом термического разложения мышьякового колчедана, восстановлением мышьяковистого ангидрида и др.
Нагрев арсенопирит в муфельных печах
Для получения металлического мышьяка чаще всего нагревают арсенопирит в муфельных печах без доступа воздуха. При этом освобождается мышьяк, пары которого конденсируются и превращаются в твердый мышьяк в железных трубках, идущих от печей, и в особых керамиковых приемниках. Остаток в печах потом нагревают при доступе воздуха, и тогда мышьяк превращается в As2O3. Металлический мышьяк получается в довольно незначительных количествах, и главная часть мышьякосодержащих руд перерабатывается в белый мышьяк, то есть в триоксид мышьяка — мышьяковистый ангидрид As2О3.
Остаток в печах потом нагревают при доступе воздуха, и тогда мышьяк превращается в As2O3. Металлический мышьяк получается в довольно незначительных количествах, и главная часть мышьякосодержащих руд перерабатывается в белый мышьяк, то есть в триоксид мышьяка — мышьяковистый ангидрид As2О3.
Применение
Мышьяк используется для легирования сплавов свинца, идущих на приготовление дроби, так как при отливке дроби башенным способом капли сплава мышьяка со свинцом приобретают строго сферическую форму, и кроме того, прочность и твёрдость свинца возрастают. Мышьяк особой чистоты (99,9999 %) используется для синтеза ряда практически очень ценных и важных полупроводниковых материалов — арсенидов и сложных алмазоподобных полупроводников. Сульфидные соединения мышьяка — аурипигмент и реальгар — используются в живописи в качестве красок и в кожевенной отрасли промышленности в качестве средств для удаления волос с кожи.
В пиротехнике реальгар употребляется для получения «греческого», или «индийского», огня, возникающего при горении смеси реальгара с серой и селитрой (ярко-белое пламя). Многие из мышьяковых соединений в очень малых дозах применяются в качестве лекарств для борьбы с малокровием и рядом тяжелых заболеваний, так как оказывают клинически значимое стимулирующее влияние на ряд функций организма, в частности, на кроветворение.
Многие из мышьяковых соединений в очень малых дозах применяются в качестве лекарств для борьбы с малокровием и рядом тяжелых заболеваний, так как оказывают клинически значимое стимулирующее влияние на ряд функций организма, в частности, на кроветворение.
Из неорганических соединений мышьяка мышьяковистый ангидрид может применяться в медицине для приготовления пилюль и в зубоврачебной практике в виде пасты как некротизирующее лекарственное средство (тот самый «мышьяк», который закладывают в канал зуба перед удалением нерва и пломбированием). В настоящее время препараты мышьяка применяются в зубоврачебной практике редко из-за токсичности и возможности проведения безболезненной денервации зуба под местной анестезией.
Биологическая роль и физиологическое действие
Мышьяк и все его соединения ядовиты. При остром отравлении мышьяком наблюдаются рвота, боли в животе, понос, угнетение центральной нервной системы. Сходство симптомов отравления мышьяком с симптомами холеры длительное время позволяло успешно использовать соединения мышьяка (чаще всего, триоксид мышьяка) в качестве смертельного яда. Во Франции порошок триоксида мышьяка за высокую «эффективность» получил обиходное название «наследственный порошок» (фр. poudre de succession). В 1832 появилась надёжная качественная реакция на мышьяк — проба Марша, значительно повысившая эффективность раскрытия отравлений.
Во Франции порошок триоксида мышьяка за высокую «эффективность» получил обиходное название «наследственный порошок» (фр. poudre de succession). В 1832 появилась надёжная качественная реакция на мышьяк — проба Марша, значительно повысившая эффективность раскрытия отравлений.
Помощь и противоядия при отравлении мышьяком: приём водных растворов тиосульфата натрия Na2S2O3, промывание желудка, приём молока и творога; специфическое противоядие — унитиол. ПДК в воздухе для мышьяка 0,5мг/м³. Работают с мышьяком в герметичных боксах, используя защитную спецодежду. Из-за высокой токсичности соединения мышьяка использовались Германией как отравляющие вещества в Первую мировую войну. Существует предположение, что соединениями мышьяка был отравлен Наполеон на острове Святой Елены.
На территориях, где в почве и воде избыток мышьяка, он накапливается в щитовидной железе у людей и вызывает эндемический зоб.
Мышьяк в малых дозах канцерогенен, его использование в качестве лекарства, «улучшающего кровь» (так называемый «белый мышьяк», например «Таблетки Бло с мышьяком», и др. ) продолжалось до середины 1950-х гг., и внесло свой весомый вклад в развитие онкологических заболеваний.
) продолжалось до середины 1950-х гг., и внесло свой весомый вклад в развитие онкологических заболеваний.
Недавно широкую огласку получила техногенная экологическая катастрофа на юге Индии — из-за чрезмерного отбора воды из водоносных горизонтов мышьяк стал поступать в питьевую воду. Это вызвало токсическое и онкологическое поражение у десятков тысяч людей.
Считалось, что «микродозы мышьяка, вводимые с осторожностью в растущий организм, способствуют росту костей человека и животных в длину и толщину, в отдельных случаях рост костей может быть вызван микродозами мышьяка в период окончания роста».
Считалось также, что «При длительном потреблении небольших доз мышьяка у организма вырабатывается иммунитет: Этот факт установлен как для людей, так и для животных. Известны случаи, когда привычные потребители мышьяка принимали сразу дозы, в несколько раз превышающие смертельную, и оставались здоровыми. Опыты на животных показали своеобразие этой привычки. Оказалось, что животное, привыкшее к мышьяку при его употреблении, быстро погибает, если значительно меньшая доза вводится в кровь или под кожу.» Однако такое «привыкание» носит очень ограниченный характер, в отношении т. н. «острой токсичности», и не защищает от новообразований. Тем не менее, в настоящее время исследуется влияние микродоз мышьяксодержащих препаратов в качестве противоракового средства.
Загрязнения мышьяком
На территорииРоссийской Федерации в г. Скопин Рязанской области вследствие многолетней работы местного металлургического комбината СМК «Металлург» в могильниках предприятия было захоронено около полутора тысяч тонн пылеобразных отходов с 80 % содержанием мышьяка. С учётом того, что пяти миллиграммов мышьяка достаточно, чтобы отравить человека, в могильниках находится более 200 миллиардов смертельных доз мышьяка.
Соединения мышьяка
Электронные конфигурации атомов | Задачи 183
Задача 183.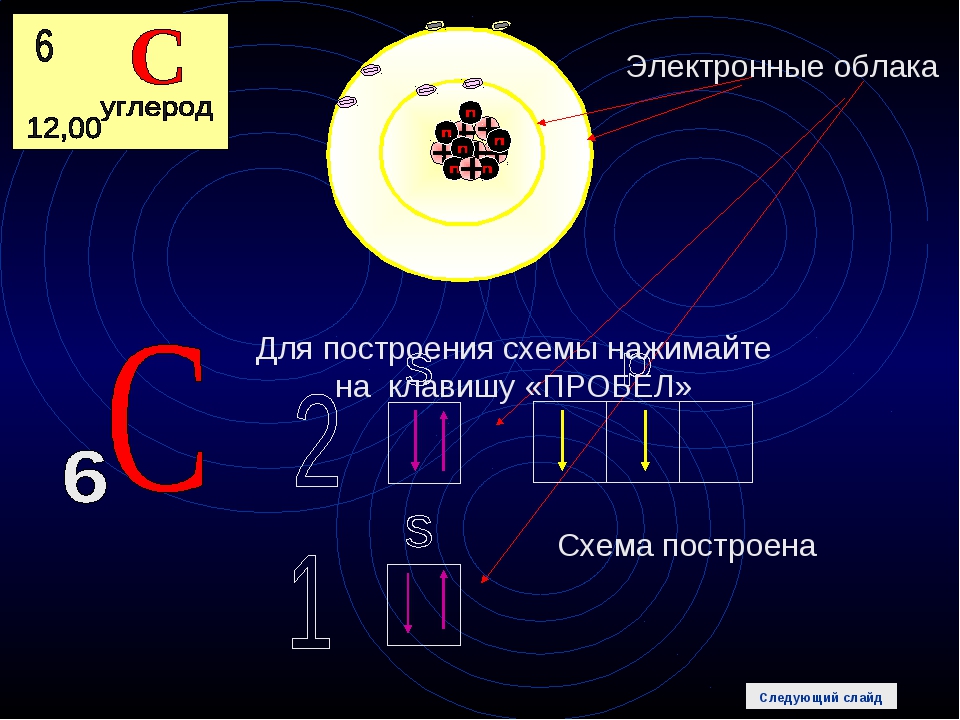
Среди приведенных ниже электронных конфигураций указать невозможные и объяснить причину невозможности их реализации: а) 1р3 б) 3p6 в) 3s2; г) 2s2; д) 2d5; е) 5d2; ж) 3f12; з) 2р4 и) 3p7.
Решение:
а) Электронная конфигурация 1p3 не реализуется, потому что первый энергетический уровень (n = 1 ) содержит только s-подуровень. Максимальное число электронов на каждом энергетическом уровне равно 2n2, где n – главное квантовое число. Так на первом энергетическом уровне (n = 1) может находиться максимальное число электронов 2(2 .12 = 2). Следовательно, не только неправильно указан подуровень, но общее число электронов.
б) 3p6 – электронная конфигурация возможна, потому что на третьем энергетическом уровне содержатся s-, p- и d-подуровни. На p-подуровне содержится три атомные орбитали, а в каждой орбитали, согласно правилу Хунда, может находиться максимальное число электронов равное двум.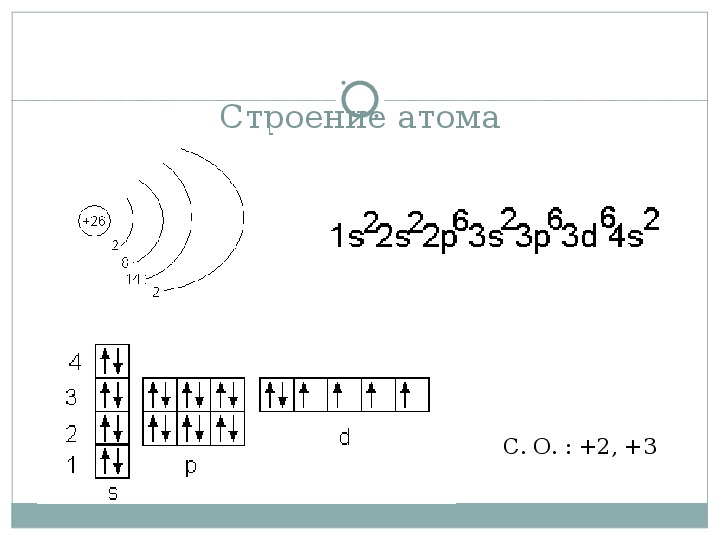 Поэтому на 3p-подуровне может максимально находиться шесть электронов (3 . 2 = 6).
Поэтому на 3p-подуровне может максимально находиться шесть электронов (3 . 2 = 6).
в) Электронная конфигурация 3s2 верна, потому что на третьем энергетическом уровне (n = 3) находятся s-, p- и d-подуровни. Согласно правилу Хунда, на s-подуровне, состоящем из одной атомной орбитали, может находиться максимальное число электронов равное двум.
г) Электронная конфигурация 2s2 реализуется, потому что на втором энергетическом уровне (n = 2) содержатся s- и p-подуровни, и на s-подуровне, в его единственной атомной орбитали, может содержаться максимальное число электронов равное двум.
д) Электронная конфигурация 2d5 не реализуется, потому что во втором энергетическом уровне (n = 2) d-подуровень не содержится, в этом слое расположены только s- и p-подуровни.
е) Электронная конфигурация 5d2 реализуется, потому что на пятом энергетическом уровне (n = 5) содержатся s-, p- d- и f-подуровни. Подуровень d содержит пять атомных орбиталей, в которых может находиться максимальное число электронов равное десяти (5 . 2 = 10). Запись 5d2 означает, что на 5d-подуровне содержится два неспаренных электрона.
2 = 10). Запись 5d2 означает, что на 5d-подуровне содержится два неспаренных электрона.
ж) Электронная конфигурация 3f12 не реализуется, потому что на третьем энергетическом уровне (n = 3) могут находиться только s-, p- и d-подуровни.
з) Электронная конфигурация 2p4 реализуется, потому что на втором энергетическом уровне (n = 2) могут находиться только s- и p-подуровни. Подуровень p состоит из трёх атомных орбиталей, на которых, согласно правилу Хунда, может находиться до шести электронов.
и) Электронная конфигурация 3p7 не реализуется, потому что на p-подуровне, состоящем из трёх атомных орбиталей, согласно правилу Хунда, максимальное число электронов равно 6.
Задача 184.
Сколько вакантных Зd-орбиталей имеют возбужденные атомы: а) С1; б) V; в) Мn?
Решение:
а) электронная конфигурация атома хлора имеет вид: …3s23p53d0. Графическое заполнение валентного энергетического слоя атома хлора можно представить следующей схемой:
Графическое заполнение валентного энергетического слоя атома хлора можно представить следующей схемой:
Таким образом, внешний энергетический уровень атома хлора имеет свободные орбитали на 3d-подуровне, что позволяет электронам переходить в возбуждённое состояние (перемещаться на более высокие свободные орбитали). У атома хлора возможно три состояния перемещения электронов на более высокие свободные орбитали, электроны с s- и p-подуровней переходят на 3d-подуровень:
1) При затрате некоторой энергии один из 3p-электронов атома хлора может быть переведён на вакантную 3d-орбиталь, при этом энергия атома возрастает, так что возникающая электронная конфигурация (1s22s22p63s23p43d1) соответствует одному из возбуждённых состояний атома хлора. Графически это можно представить схемой:
В данном случае 3d-подуровень содержит четыре вакантные орбитали возбуждённого атома хлора.
2) При затрате некоторой энергии два из 3p-электронов атома хлора могут быть переведены на вакантные 3d-орбитали, при этом энергия атома возрастает, так что возникает электронная конфигурация (1s22s22p63s23p33d2), которая соответствует одному из возбуждённых состояний атома хлора. Графически это можно представить схемой:
Графически это можно представить схемой:
В таком возбуждённом состоянии атом хлора содержит три вакантные 3d-орбитали.
3) При затрате некоторой энергии один из 3s- и два 3p-электронов могут быть переведены на свободные 3d-орбитали, при этом энергия атома возрастает, так что возникающая конфигурация (1s22s22p63s13p33d3) также соответствует одному из возможных состояний хлора:
б) Электронная конфигурация валентного энергетического уровня атома ванадия имеет вид: …3d34s2. Графическая схема заполнения электронами имеет вид:
В возбуждённом состоянии атома ванадия один 4s-электрон может быть переведён на свободную 3d-орбиталь, так что возникающая электронная конфигурация валентного уровня (3d44s1) соответствует возбуждённому состоянию атома ванадия, что можно представить в виде схемы:
При возбуждении атома ванадия остаётся вакантной одна 3d-орбиталь.
в) Электронная конфигурация валентного энергетического уровня атома марганца имеет вид: …3d54s2. Графическая схема заполнения электронами имеет вид:
При возбуждении атома марганца один s-электрон переходит на 3d-орбиталь, при этом получается электронная конфигурация валентного уровня (3d64s1) соответствует возбуждённому состоянию атома марганца, что можно представить в виде схемы:
Из схемы вытекает, что при возбуждении атома марганца свободных d-орбиталей нет, так как на 3d-подуровне распределяются два спаренных электрона и четыре неспаренных. Таким образом, атом марганца ни в основном, ни в возбуждённом состоянии не имеет свободных d-орбиталей.
Задача 185.
Сколько неспаренных электронов содержат невозбужденные атомы: а) В; б) S; в) Аs; г) Сг; д) Нg; е) Еu?
Решение:
а) Электронная формула атома бора 1s22s22p1.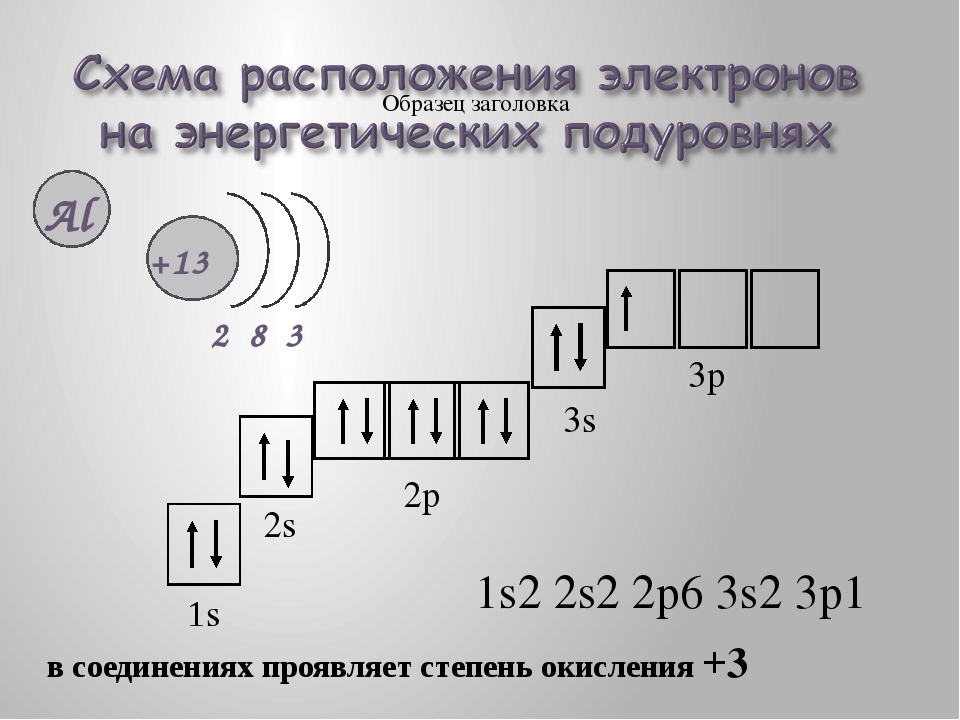 Валентность орбитали в этом атоме являются орбитали внешнего (второго) электронного, т.е. 2s-, 2p-орбитали. Графическая схема заполнения электронами этих орбиталей имеет следующий вид:
Валентность орбитали в этом атоме являются орбитали внешнего (второго) электронного, т.е. 2s-, 2p-орбитали. Графическая схема заполнения электронами этих орбиталей имеет следующий вид:
Следовательно, атом бора содержит один неспаренный 2p-электрон.
б) Электронная конфигурация валентного электронного слоя атома серы имеет вид: …2s22p4. Графическая схема заполнения электронами этого слоя имеет следующий вид:
Следовательно, атом серы в стационарном состоянии содержит два неспаренных электрона -, 2p-подуровне.
в) Электронная конфигурация валентного электронного слоя атома мышьяка имеет вид: …4s24p3. Графическая схема распределения валентных электронов имеет следующий вид:
Таким образом, атом мышьяка имеет три неспаренных электрона на 4p-подуровне.
г) Электронная конфигурация валентного электронного слоя атома хрома имеет вид: …3d5 4s1. Графическая схема заполнения электронами этого слоя имеет следующий вид:
Следовательно, атом хрома в стационарном состоянии содержит шесть неспаренных электронов, из которых пять на 3d-подуровне и один на 4s-подуровне.
д) Электронная конфигурация валентного электронного слоя атома ртути имеет вид: … 6s26p0. Графическая схема заполнения электронами этого слоя имеет следующий вид:
Атом ртути не содержит ни одного неспаренного электрона.
е) Электронная конфигурация валентного электронного слоя атома европия имеет вид: …4f7 6s2. Графическая схема заполнения электронами этого слоя имеет следующий вид:
Таким образом, атом европия содержит семь неспаренных 4f-электронов.
Ответ: а) 1; б) 2; в) 3; г) 6; д) 0; е) 7.
Задача 186.
Составить электронно-графические схемы ионов Ее2+ и Ее3+. Чем можно объяснить особую устойчивость электронной конфигурации иона Ее3+?
Решение:
Электронная формула атома железа имеет вид: 1s22s22p63s23p63d64s2. Графическая схема размещения электронов в квантовых ячейках атома железа будет иметь следующий вид:
Графическая схема размещения электронов в квантовых ячейках атома железа будет иметь следующий вид:
При отдаче двух 4s-электронов атомом железа образуется ион Ее2+, графическая схема размещения электронов в котором будет иметь вид:
При отдаче трёх электронов (двух 4s- и одного 3d) атомом железа образуется ион Ее3+, графическая схема размещения электронов в котором будет иметь вид:
Таким образом, на внешнем энергетическом уровне иона Ее2+ содержится два 3s-, шесть 3p- и шесть 3d-электронов. Причём на 3d-подуровне содержатся четыре неспаренных и два спаренных электрона. Ион Ее3+ отличается от Ее2+ тем, что содержит на 3d-подуровне на один электрон меньше, и все они неспаренные, такая система 3d-подуровня является энергетически более устойчивой. Электростатическое взаимодействие между ядром и электронной плотностью у иона Ее3+ больше, чем у иона Ее2+.
Задача 187.
Указать особенности электронных конфигураций меди и хрома. Сколько 4s-электронов содержат невозбужденные атомы этих элементов?
Решение:
Так как число электронов в атоме элемента равно его порядковому номеру, то общее число электронов в атоме меди и хрома соответственно равно 29 и 24.
Последовательность заполнения энергетических уровней и подуровней в атоме элемента определяется правилами Клечковского, согласно которым электрон занимает тот энергетический подуровень, на котором он обладает наименьшей энергией (меньшая сумма n + l). Порядок заполнения подуровней определяется правилом Хунда. Согласно правилу Хунда, минимальной энергии атома соответствует такое распределение электронов по атомным орбиталям данного подуровня, при котором абсолютное значение суммарного спина атома максимально.
Электронные формулы атомов хрома и меди можно выразить следующим образом:
Экспериментально установлено, что на внешнем энергетическом уровне у хрома и меди находится по одному электрону. Объясняется это тем, что произошёл «провал» одного 4s-электрона у атомов хрома и меди на 3d-подуровень. Происходит это потому, что энергетически выгодным состоянием является состояние атома, когда при четырёх неспаренных электронах на 3d-подуровне происходит заполнение пятой свободной атомной орбитали. Поэтому электронная формула атома хрома имеет следующий вид: 1s22s22p63s23p63d54s1.
Объясняется это тем, что произошёл «провал» одного 4s-электрона у атомов хрома и меди на 3d-подуровень. Происходит это потому, что энергетически выгодным состоянием является состояние атома, когда при четырёх неспаренных электронах на 3d-подуровне происходит заполнение пятой свободной атомной орбитали. Поэтому электронная формула атома хрома имеет следующий вид: 1s22s22p63s23p63d54s1.
У атома меди все атомные орбитали 3d-подуровня заполнены, причём четыре полностью, а на пятой находится один неспаренный электрон. Такая система 3d-подуровня, состоящая из девяти электронов является энергетически неустойчивой, и поэтому происходит «провал электрона с 4s-орбитали на 3d-орбиталь. Электронную формулу атома меди можно теперь представить следующим образом: 1s22s22p63s23p63d104s1.
Таким образом, атомы хрома и меди на внешних энергетических уровнях содержат по одному 4-электрону. Графические схемы распределения электронов по квантовым ячейкам у атомов хрома и меди в стационарном состоянии будут иметь следующий вид:
Графические схемы распределения электронов по квантовым ячейкам у атомов хрома и меди в стационарном состоянии будут иметь следующий вид:
как информация об элементе мышьяка: факты, свойства, тенденции, использование и сравнение – Периодическая таблица элементов
История мышьяка
Элемент мышьяк был открыт в бронзовом веке в год 1250 в неизвестном месте . мышьяк производное от английского слова (лат. arsenicum)
Присутствие мышьяка: изобилие в природе и вокруг нас
В таблице ниже показано содержание мышьяка во Вселенной, на Солнце, в метеоритах, Земная кора, океаны и тело человека.
Кристаллическая структура мышьяка
Твердотельная структура мышьяка представляет собой простой тригонал .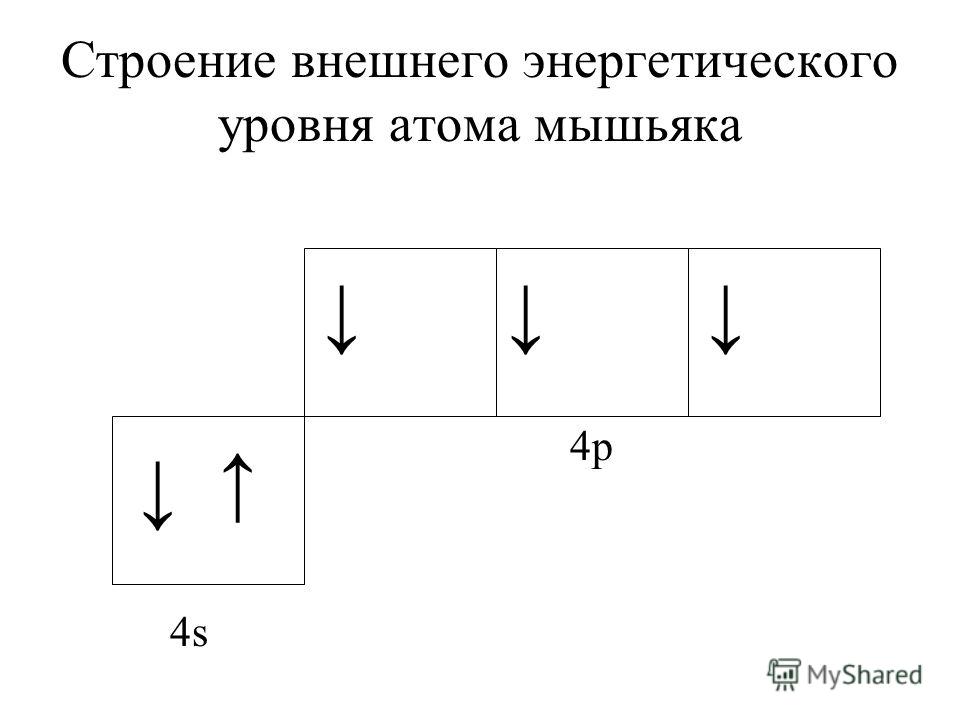
Кристаллическую структуру можно описать с точки зрения ее элементарной ячейки. Единичные клетки повторяются в три объемное пространство для формирования конструкции.
Параметры ячейки
Элементарная ячейка представлена в терминах ее параметров решетки, которые являются длинами ячейки края Постоянные решетки ( a , b и c )
| и | б | в |
|---|---|---|
| 375.98 | 375,98 | 1054,75 вечера |
и углы между ними Углы решетки (альфа, бета и гамма).
| альфа | бета | гамма |
|---|---|---|
| π/2 | №/2 | 2 π/3 |
Положения атомов внутри элементарной ячейки описываются набором положений атомов (
x i , y i , z i ), измеренные от опорной точки решетки.
Свойства симметрии кристалла описываются понятием пространственных групп. Все возможное симметричное расположение частиц в трехмерном пространстве описывается 230 пространственными группами (219 различных типов или 230, если хиральные копии считаются различными.
Атомные и орбитальные свойства мышьяка
Атомы мышьяка имеют 33 электрона и структура электронной оболочки [2, 8, 18, 5] с атомарным символом (квантовыми числами) 4 S 3/2 .
Оболочечная структура мышьяка – количество электронов на энергию уровень
| нет | с | р | д | ф | |
|---|---|---|---|---|---|
| 1 | К | 2 | |||
| 2 | л | 2 | 6 | ||
| 3 | М | 2 | 6 | 10 | |
| 4 | Н | 2 | 3 |
Электронная конфигурация мышьяка в основном состоянии – нейтральная Атом мышьяка
Электронная конфигурация нейтрального атома мышьяка в основном состоянии
[Ар] 3d10 4s2 4p3.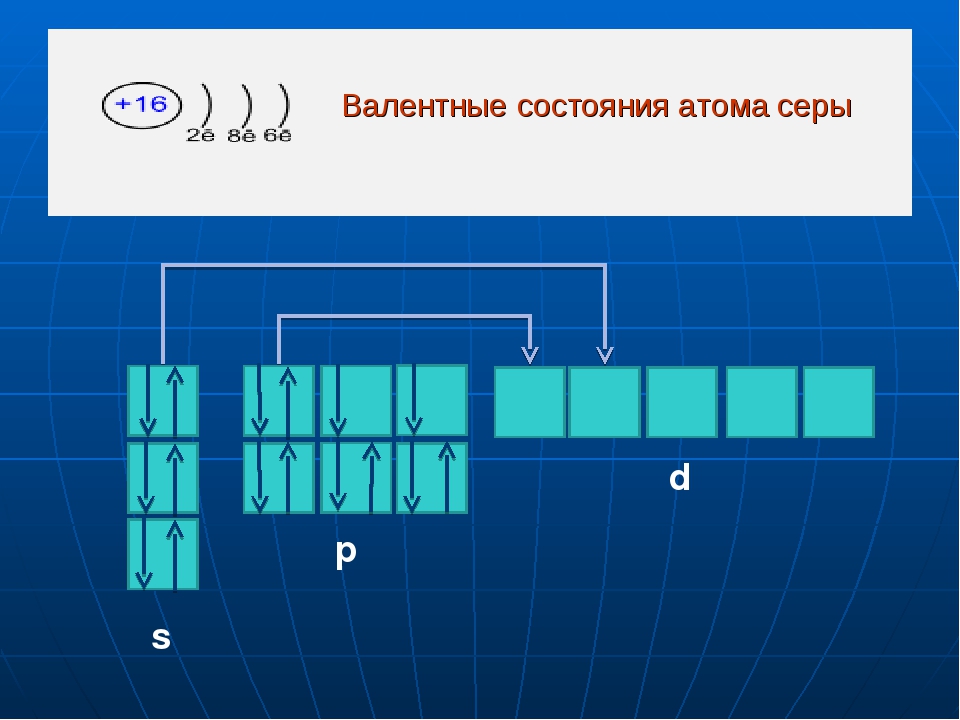 Часть конфигурации мышьяка, эквивалентная благородному газу
предшествующий период обозначается аббревиатурой [Ar]. Для атомов с большим количеством электронов это
нотация может стать длинной, поэтому используется сокращенная нотация. Это важно, поскольку это
валентные электроны 3d10 4s2 4p3, электроны в
внешняя оболочка, определяющая химические свойства элемента.
Часть конфигурации мышьяка, эквивалентная благородному газу
предшествующий период обозначается аббревиатурой [Ar]. Для атомов с большим количеством электронов это
нотация может стать длинной, поэтому используется сокращенная нотация. Это важно, поскольку это
валентные электроны 3d10 4s2 4p3, электроны в
внешняя оболочка, определяющая химические свойства элемента.
Расшифрованная электронная конфигурация нейтрального мышьяка
Полная электронная конфигурация в основном состоянии атома мышьяка, Полная электронная конфигурация
1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p3
Атомная структура мышьяка
Атомный радиус мышьяка составляет 114 пм, а его ковалентный радиус — 119 пм.
Атомный спектр мышьяка
Химические свойства мышьяка: Энергии ионизации мышьяка и сродство к электрону
Электронное сродство мышьяка составляет 78 кДж/моль.
Энергия ионизации мышьяка
Энергии ионизации мышьяка
см. в таблице ниже.| Номер энергии ионизации | Энтальпия – кДж/моль |
|---|---|
| 1 | 947 |
| 2 | 1798 |
| 3 | 2735 |
| 4 | 4837 |
| 5 | 6043 |
| 6 | 12310 |
Физические свойства мышьяка
Физические свойства мышьяка
см. в таблице ниже.| Плотность | 5. 727 г/см3 727 г/см3 |
| Молярный объем | 13.0821721669 см3 |
Упругие свойства
Твердость мышьяка. Испытания для измерения твердости элемента
Электрические свойства мышьяка
Мышьяк является проводником электричества. Ссылаться на Таблица ниже для электрических свойств мышьяка
Свойства тепла и проводимости мышьяка
Магнитные свойства мышьяка
Оптические свойства мышьяка
Акустические свойства мышьяка
Термические свойства мышьяка – энтальпии и термодинамика
См. таблицу ниже для термических свойств мышьяка
.Энтальпии мышьяка
Изотопы мышьяка – ядерные свойства мышьяка
Изотопы родия.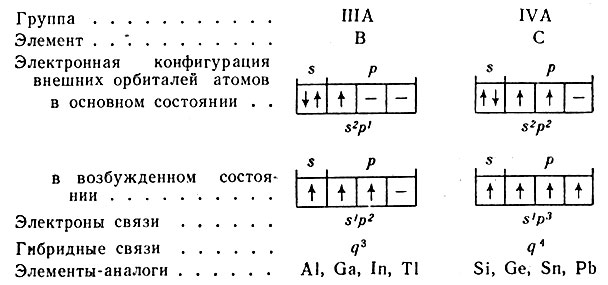 Встречающийся в природе мышьяк
1 стабильный изотоп –
75Ас.
Встречающийся в природе мышьяк
1 стабильный изотоп –
75Ас.
| Изотоп | Масса изотопов | % Изобилие | Т половина | Режим затухания |
|---|---|---|---|---|
| 60Ас | ||||
| 61Ас | ||||
| 62Ас | ||||
| 63Ас | ||||
| 64А | ||||
| 65Ас | ||||
| 66Ас | ||||
| 67Ас | ||||
| 68Ас | ||||
| 69Ас | ||||
| 70Ас | ||||
| 71Ас | ||||
| 72Ас | ||||
| 73Ас | ||||
| 74Ас | ||||
| 75Ас | 100% | Стабильный | Н/Д | |
| 76Ас | ||||
| 77Ас | ||||
| 78Ас | ||||
| 79Ас | ||||
| 80Ас | ||||
| 81Ас | ||||
| 82Ас | ||||
| 83Ас | ||||
| 84А | ||||
| 85А | ||||
| 86Ас | ||||
| 87А | ||||
| 88Ас | ||||
| 89Ас | ||||
| 90Ас | ||||
| 91Ас | ||||
| 92Ас |
Нормативно-правовое регулирование и здоровье – Параметры и рекомендации по охране здоровья и безопасности
| Количество CAS | КАС7440-38-2 |
| Номер РТЕКС | {Н/Д, RTECSCG0525000, Н/Д} |
| Класс опасности DOT | {Н/Д, 6. 1, н/д} 1, н/д} |
| Номера точек | “Н/Д”, {1558}, “Н/Д” |
| Номер ЕС | {Н/Д, Н/Д, Н/Д} |
| Рейтинг огнестойкости NFPA | {Н/Д, 2, Н/Д} |
| Опасности NFPA | Н/Д, Н/Д, Н/Д |
| Рейтинг здоровья NFPA | {Н/Д, 3, Н/Д} |
| Рейтинг реактивности NFPA | {Н/Д, Н/Д, Н/Д} |
Поиск по базе данных
Список уникальных идентификаторов для поиска элемента в различных базах данных химических реестров
Изучите нашу интерактивную периодическую таблицу
Сравнение элементов периодической таблицы
Мышьяк – информация об элементе, свойства и использование
Стенограмма:
Химия в ее стихии: мышьяк
Вы слушаете Химия в ее стихии, представленная вам Chemistry World , журналом Королевского химического общества.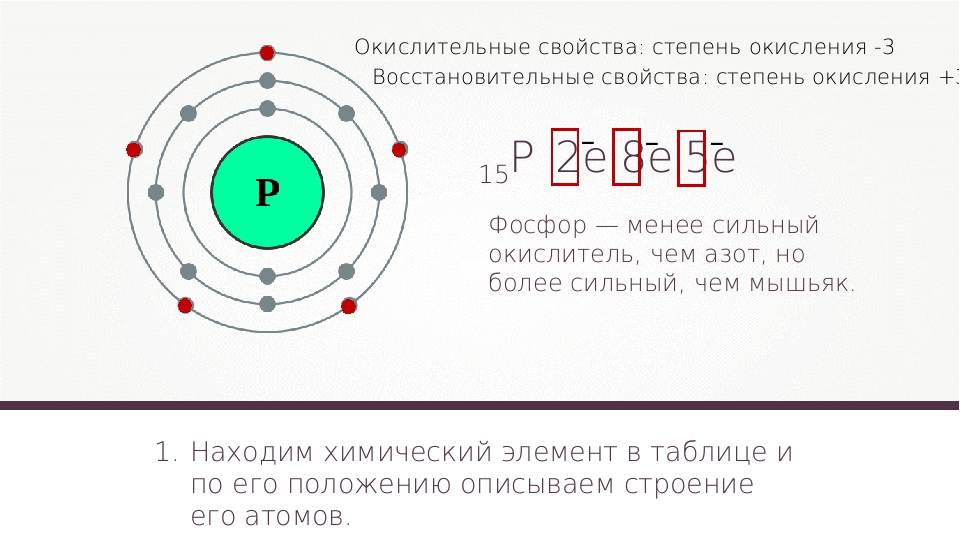
(Конец промо)
Крис Смит
На этой неделе яды в красках, фейерверки и афродизиаки, обои Наполеона и запах чеснока, какая связь? Вот Беа Перкс.
Bea Perks
Упомяните мышьяк любому, даже химику, первое слово, которое скорее всего придет на ум, это яд, это конечно смертельный яд, но его соединения также обнаружены или были обнаружены в инсектицидах, красителях агентов, консервантов для древесины, в кормах для животных, для лечения сифилиса и лечения рака, для лечения псориаза, в фейерверках и в качестве полупроводника.Ой! Так же может быть как афродизиак.
Мышьяк, атомный номер 33, находится между фосфором и сурьмой в группе 15, так называемой азотной группе периодической таблицы. Члены группы, включающей, конечно, азот, наряду с мышьяком, фосфором, сурьмой и висмутом, особенно стабильны в соединениях, поскольку они склонны образовывать двойные или тройные ковалентные связи. Это свойство также приводит к токсичности, особенно очевидной для фосфора, сурьмы и, что наиболее печально известно, мышьяка. Когда они реагируют с определенными химическими веществами в организме, они создают сильные свободные радикалы, которые не легко перерабатываются печенью, где они накапливаются.
Когда они реагируют с определенными химическими веществами в организме, они создают сильные свободные радикалы, которые не легко перерабатываются печенью, где они накапливаются.
Мышьяк не является ни металлом, ни неметаллом, а вместо этого присоединяется к избранной, но довольно плохо определенной группе элементов, называемых металлоидами. Они расположены в периодической таблице вдоль диагональной линии от бора вверху слева до полония внизу справа. Все, что находится справа от черты в периодической таблице, является неметаллом, а все, что находится слева, — металлом. Точные члены группы открыты для обсуждения, но мышьяк всегда входит в ее состав. Большинство металлоидов встречается в нескольких формах или аллотропах, где один может казаться металлическим, а другой – неметаллическим.Углерод не является металлоидом, потому что, несмотря на полупроводниковые свойства графита, все его аллотропы от графита до алмаза имеют неметаллический характер.
Мышьяк получил свое название от персидского слова, обозначающего желтый пигмент, теперь известный как аурипигмент. Для проницательных лексикографов очевидно, что рассматриваемое персидское слово зарних было впоследствии заимствовано греками для их слова арсеникон, что означает мужской или могущественный.
Для проницательных лексикографов очевидно, что рассматриваемое персидское слово зарних было впоследствии заимствовано греками для их слова арсеникон, что означает мужской или могущественный.
Аурипигмент или желтый трисульфид мышьяка представляет собой исторический пигмент, идентифицированный в древнеегипетских артефактах.Что касается пигмента, то они едва ли осмеливались упоминать об этом, такая заезженная история. Говорят, что обои Наполеона незадолго до его смерти включали в себя так называемую зелень Шееле, которая выделяла пары мышьяка, когда становилась влажной. Все хорошо, кроме того, что Наполеон также страдал язвой желудка, раком желудка, туберкулезом и т. д., так что делайте из этого что хотите!
Мышьяк не очень похож на металл в его так называемой желтой форме, но он также имеет серую форму, известную как металлический мышьяк.Желтый мышьяк имеет удельный вес 1,97, а серый мышьяк имеет удельный вес 5,73. Серый мышьяк представляет собой обычную стабильную форму с температурой плавления 817 градусов по Цельсию.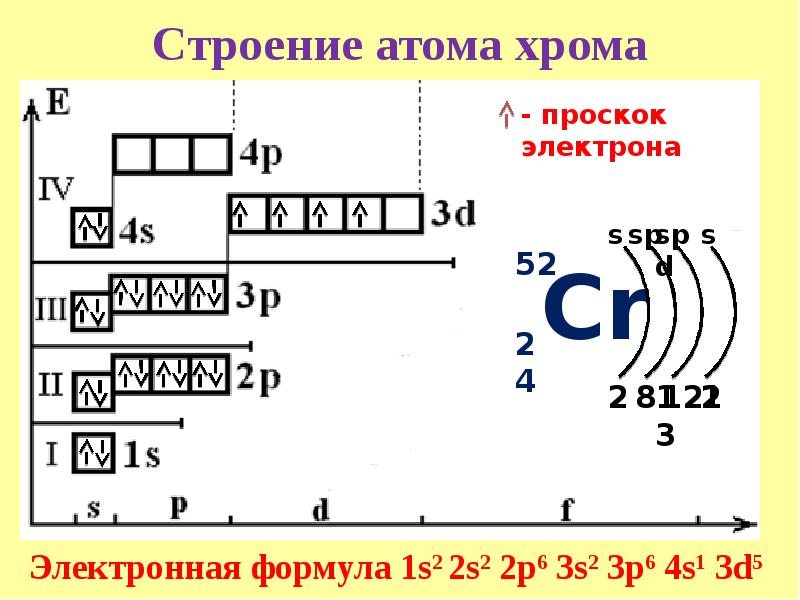 Это очень хрупкий полуметаллический твердый металл серо-стального цвета, который легко тускнеет на воздухе. Он быстро окисляется до оксида мышьяка, который пахнет чесноком, если вы достаточно смелы, чтобы почувствовать его запах при нагревании.
Это очень хрупкий полуметаллический твердый металл серо-стального цвета, который легко тускнеет на воздухе. Он быстро окисляется до оксида мышьяка, который пахнет чесноком, если вы достаточно смелы, чтобы почувствовать его запах при нагревании.
В дни, когда преднамеренное отравление мышьяком оставалось реальной угрозой и до прибытия тестов, которые могли предупредить власти о его наличии.Несколько раз диагностировали отравление на основании чесночного запаха изо рта пострадавшего. Совсем недавно исследователи из Индии показали, что употребление от 1 до 3 зубчиков чеснока в день может защитить людей от отравления мышьяком, связанного с загрязненной питьевой водой.
Повторное появление чеснока является случайным, и тип отравления, острое преднамеренное отравление и непреднамеренное длительное отравление питьевой водой, сильно различаются. Уровни мышьяка в грунтовых водах иногда повышены в результате эрозии местных пород.В Бангладеш есть особая проблема: повышение уровня мышьяка последовало за тем, что должно было стать улучшением водоснабжения. Местное население использовало питьевую воду из открытых источников, таких как пруды. Но около 30 лет назад воду начали получать из колодцев. Рытье колодцев привело к заметному снижению инфекций, передающихся через воду. К 1993 году было обнаружено, что в этих колодцах присутствует мышьяк. Первые симптомы, обнаруживаемые у людей, пьющих загрязненную мышьяком воду, включают изменения пигментации кожи и ее утолщение или гиперкератоз.После примерно 10 лет употребления этой воды симптомы распространяются на рак кожи и внутренних органов. Всемирная организация здравоохранения сообщает, что мышьяк в питьевой воде может стать причиной смерти от рака в Бангладеш от 200 000 до 270 000 человек. Уровни мышьяка, по-видимому, ниже в более мелких грунтовых водах или в гораздо более глубоких водоносных горизонтах, и мы надеемся, что эти знания должны способствовать снижению рисков в будущем.
Местное население использовало питьевую воду из открытых источников, таких как пруды. Но около 30 лет назад воду начали получать из колодцев. Рытье колодцев привело к заметному снижению инфекций, передающихся через воду. К 1993 году было обнаружено, что в этих колодцах присутствует мышьяк. Первые симптомы, обнаруживаемые у людей, пьющих загрязненную мышьяком воду, включают изменения пигментации кожи и ее утолщение или гиперкератоз.После примерно 10 лет употребления этой воды симптомы распространяются на рак кожи и внутренних органов. Всемирная организация здравоохранения сообщает, что мышьяк в питьевой воде может стать причиной смерти от рака в Бангладеш от 200 000 до 270 000 человек. Уровни мышьяка, по-видимому, ниже в более мелких грунтовых водах или в гораздо более глубоких водоносных горизонтах, и мы надеемся, что эти знания должны способствовать снижению рисков в будущем.
На более легкой ноте, я боюсь, что не так много доказательств, несмотря на его связь с греческим словом «мощный», что мышьяк является афродизиаком. Это позор, потому что это могло бы быть довольно полезно, если бы это было так. Препарат на основе мышьяка под названием Сальварсан был разработан в 1910 году лауреатом Нобелевской премии Паулем Эрлихом для лечения сифилиса, передающегося половым путем.
Это позор, потому что это могло бы быть довольно полезно, если бы это было так. Препарат на основе мышьяка под названием Сальварсан был разработан в 1910 году лауреатом Нобелевской премии Паулем Эрлихом для лечения сифилиса, передающегося половым путем.
Крис Смит
Химический мир Беа занимается наукой об элементе номер 33, мышьяке. И если вы думаете, что мышьяк опасен, подождите, пока вы не встретите на следующей неделе элемент
Питер Уотерс
Это звучит как монстр из «Доктора Кто», и во многих отношениях этот элемент действительно имеет несколько свойств, которые делают его подходящим для любого человека. Хороший космический научно-фантастический фильм ужасов.Во-первых, как и многие космические монстры, он происходит из слизи. У каждого хорошего монстра должно быть секретное оружие, и теллур не исключение. Он дает своим врагам чесночное дыхание. Действительно неприятный чесночный запах изо рта.
Крис Смит
Отлично! Это был Питер Уотерс, который будет здесь, чтобы рассказать историю о вонючем элементе теллуре на следующей неделе «Химия в его элементе». Я надеюсь, что вы можете присоединиться к нам. Я Крис Смит, спасибо за внимание и до свидания.
(Акция)
(Конец акции)
Исследование механизма взаимодействия различных атомных соотношений неодима, мышьяка и железа
Металлографический анализ
На рисунке 2 представлены металлографические изображения образцов при различных атомных соотношениях под оптическим микроскопом.При постоянной температуре нагрева и времени выдержки наблюдались три типа контраста (сероватый, серый и черный) при различных атомных соотношениях. Сероватая часть указывает на коллективную часть цилиндра, большую часть которой составляет промышленно чистое Fe, серая часть имеет более высокую долю As, а черная часть имеет более высокую долю Nd. На рисунке 2а показана соседняя область блока цилиндров, что указывает на то, что вся область была разделена на две разные части: матрица цилиндра слева и основной компонент справа.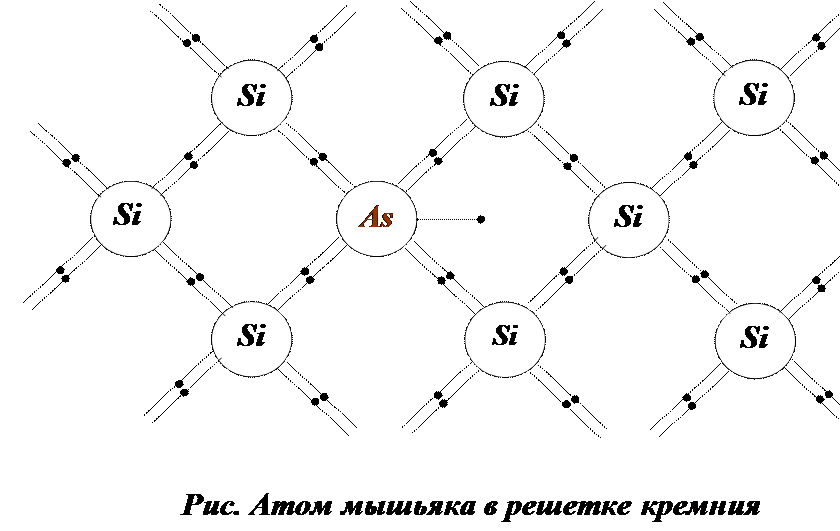 Кроме того, при всех атомных соотношениях (правая область) формировались неоднородные зернистые структуры, содержащие такой же белый лайнер, как и матрица цилиндра. С увеличением атомных отношений симметрия всей зернистой структуры сначала увеличивалась, а затем уменьшалась. Кроме того, с увеличением диффузии сероватая область диффузии отодвигалась все дальше от края, что, следовательно, уменьшало диффузию. В частности, с уменьшением расстояния между серой областью и краем границы доля серой области уменьшалась.При высоких температурах атом Fe диффундировал в центральную область образца, а атом Nd диффундировал в область матрицы, а атомы Fe и As диффундировали вместе, и, следовательно, атомы Fe постепенно образовывали кольцевую структуру.
Кроме того, при всех атомных соотношениях (правая область) формировались неоднородные зернистые структуры, содержащие такой же белый лайнер, как и матрица цилиндра. С увеличением атомных отношений симметрия всей зернистой структуры сначала увеличивалась, а затем уменьшалась. Кроме того, с увеличением диффузии сероватая область диффузии отодвигалась все дальше от края, что, следовательно, уменьшало диффузию. В частности, с уменьшением расстояния между серой областью и краем границы доля серой области уменьшалась.При высоких температурах атом Fe диффундировал в центральную область образца, а атом Nd диффундировал в область матрицы, а атомы Fe и As диффундировали вместе, и, следовательно, атомы Fe постепенно образовывали кольцевую структуру.
Металлографические изображения атомов с различным атомным соотношением, ( a ) Изображения прилегающей области блока цилиндров, ( b ) Изображения вокруг области его ядра.
Фазовый анализ
Для фазового анализа образец из зоны керна растирали в ступке в порошок. В дальнейшем фаза образцов была охарактеризована методом РФА, как показано на рис. 3. Основные дифракционные пики, наблюдаемые в спектрах РФА, можно отнести к образованию пяти типов соединений (Fe 12 As 5 , Fe 2 As, NdAs, Fe 17 Nd 2 и α-Fe) в тройной системе образцов высокотемпературного плавления. При атомном соотношении Nd и As 1:1 и 1:2 интенсивность дифракционных пиков была стабильной. В ходе эксперимента As возгонялся при высоких температурах, а высокореакционноспособный Nd реагировал с As.Следовательно, количество соединений (NdAs) увеличилось. В ходе эксперимента небольшое количество As диффундировало во внешнюю матрицу блока цилиндров, а Fe диффундировало в область его ядра и реагировало с As, образуя соединения As (Fe 2 As).
В дальнейшем фаза образцов была охарактеризована методом РФА, как показано на рис. 3. Основные дифракционные пики, наблюдаемые в спектрах РФА, можно отнести к образованию пяти типов соединений (Fe 12 As 5 , Fe 2 As, NdAs, Fe 17 Nd 2 и α-Fe) в тройной системе образцов высокотемпературного плавления. При атомном соотношении Nd и As 1:1 и 1:2 интенсивность дифракционных пиков была стабильной. В ходе эксперимента As возгонялся при высоких температурах, а высокореакционноспособный Nd реагировал с As.Следовательно, количество соединений (NdAs) увеличилось. В ходе эксперимента небольшое количество As диффундировало во внешнюю матрицу блока цилиндров, а Fe диффундировало в область его ядра и реагировало с As, образуя соединения As (Fe 2 As).
Спектры рентгеновской дифракции образцов при различном атомном соотношении.
РСА порошковых соединений Nd–Fe–As в тройной системе в соответствующей литературе не обнаружены. Однако анализ энергодисперсионной спектроскопии (EDS) предполагает образование тройных соединений (NdFeAs).
Однако анализ энергодисперсионной спектроскопии (EDS) предполагает образование тройных соединений (NdFeAs).
СЭМ-анализ был проведен на уменьшенном образце, а ЭДС-анализ был использован для анализа изображения при различных контрастах. Как показано на рис. 4, образцы в основном распределены по четырем типам контрастной фазы (черный, темно-серый, светло-серый и белый), которые обозначены буквами A, B, C и D, и каждая ткань контрастной фазы была исследованы с помощью анализа EDS; результаты представлены в таблице 3. Микроструктура черного, темно-серого и светло-серого контраста имела неправильную форму.Кроме того, серый и светло-серый компоненты в основном состоят из Nd и As, в сочетании со спектрами XRD Nd и As этот результат указывает на то, что структура контрастной фазы представляет собой кристаллическую структуру NdAs, тогда как структура черной контрастной фазы в основном представляет собой насыщенную структуру. В виде твердого раствора α-Fe.
Рисунок 4 Карты обратно рассеянных электронов образца при различных атомных соотношениях ( a ) 1:1, ( b ) 1:2, ( c ) 1:3.
Как обсуждалось выше, продукты Nd и As при различных атомных соотношениях (1:1, 1:2, 1:3) содержали Fe 12 As 5 , Fe 2 As, NdAs и Fe 17 Nd 2 во всех тройных системах. Однако количество различных фаз изменяется с увеличением атомных отношений, и различные структуры контрастных фаз демонстрируют симбиотическую связь.
Диффузионный анализ образцов
На рисунке 5 показан атласный анализ линейного сканирования переходных областей Nd и As при различных атомных соотношениях.Согласно графику, три элемента (Nd, Fe, As) находились в непрерывном распределении в полосчатом градиенте. Кроме того, количество Nd в области белого контраста было значительно выше, чем в других областях. Кроме того, количество Fe в черной контрастной области было самым высоким, а As присутствовал во всех контрастных фазах.
Спектр развертки краевой линии цилиндрических образцов при различном атомном соотношении.
В ходе эксперимента Fe диффундировало в центральную область блока цилиндров, тогда как энергия активации диффузии As была ниже, чем у Fe 31 .Кроме того, As диффундировал через образование соединений Fe и As, а Nd диффундировал через вакансионный механизм и образование соединений Fe и As. Поскольку химический потенциал Nd увеличивался с увеличением его содержания, а растворимость As поддерживалась на уровне 10% при температуре эксперимента, в процессе сублимации образовывались вакансии. При взаимодействии As и Nd образуются соединения NdAs, а оставшиеся Nd и Fe образуют соединения Fe 17 Nd 2 для заполнения вакансий.Кроме того, вакансии Fe формировались за счет тепловых колебаний; следовательно, эти вакансии создавали условия для диффузии Nd 32 . Кроме того, размер зерна постепенно уменьшался, что увеличивало площадь границы зерна. Одновременно соответственно увеличились зернограничные вакансии. Совместное воздействие генерируемых вакансий, соединений растворенных веществ с вакансиями, генерируемых Nd, и увеличение скорости термодиффузии приводит к сегрегации Nd на границе зерен.{i} }}} \right] \times 100$$
Одновременно соответственно увеличились зернограничные вакансии. Совместное воздействие генерируемых вакансий, соединений растворенных веществ с вакансиями, генерируемых Nd, и увеличение скорости термодиффузии приводит к сегрегации Nd на границе зерен.{i} }}} \right] \times 100$$
(1)
, где \(\delta\) — среднее значение трех несоответствий между \(\left( {hkl} \right)_{s}\) и \(\left( {hkl} \right)_{n }\) плоскости; \(d_{{\left[ {uvw} \right]_{s}}} \;{\text{and}}\;d_{{\left[{uvw} \right]_{n}}} \ ;{\ text{is}}\;{\text{}}\;{\text{межатомный}}\;{\text{интервал}}\;{\text{вдоль}}\;\left[ { uvw} \right]_{s}\) и \(\left[ {uvw} \right]_{n}\) соответственно; а θ — угол между двумя соответствующими направлениями.
Диаграмма согласования атомов поверхности между плоскостями Fe 12 As 5 (0001) и NdAs (111) представлена на рис. 6 и 7. Первое обозначено буквой «X», а второе обозначено буквой «O». Параметры кристалла, участвовавшие в расчетах, перечислены в таблице 4 34 , а конкретные расчетные данные показаны в таблице 5. Результат расчета двух несоответствующих плоскостей составил 17,86%, что указывает на то, что Fe 12 As 5 не может использоваться в качестве эффективного ядра гетерогенной нуклеации в пласте NdAs.
Результат расчета двух несоответствующих плоскостей составил 17,86%, что указывает на то, что Fe 12 As 5 не может использоваться в качестве эффективного ядра гетерогенной нуклеации в пласте NdAs.
Кристаллографические соотношения плоскостей Fe 12 As 5 (0001) и NdAs (111).
Рисунок 7Схема плоскости и направления кристалла NdAs (111).
Таблица 4 Кристаллографические параметры возможных соединений Nd и As в стали. Таблица 5 Детали расчета решетки между соединениями Fe 12 As 5 и NdAs. Результаты расчета рассогласования приведены в таблице 6.Несоответствие между Fe 2 As и NdFeAs составляет 8,33%, что указывает на высокую вероятность того, что Fe 2 As эффективно действует в качестве ядер гетерогенного зародышеобразования для образования тройного соединения NdFeAs.
Как нарисовать структуру Льюиса AsCl3?
Химическая формула трихлорида мышьяка: AsCl3. Рисовать структуру Льюиса AsCl3 очень легко, используя следующий метод.Здесь, в этом посте, мы описали пошаговый метод построения структуры Льюиса AsCl3. Элементы мышьяка и хлора являются членами групп семейства азота и галогена из периодической таблицы соответственно. Валентных электронов в мышьяке и хлоре пять и семь соответственно. Раздел химии соединений галогена мышьяка используется для производства химических реагентов для органических химических реакций.
Ключевые моменты, которые следует учитывать при рисовании структуры электронных точек AsCl3 Можно использовать трехэтапный подход для рисования структуры Льюиса AsCl3.Первым шагом является набросок структуры Льюиса молекулы AsCl3, чтобы добавить валентные электроны вокруг атома мышьяка; второй шаг – добавить валентные электроны к трем атомам хлора, а последний шаг – объединить шаг 1 и шаг 2, чтобы получить структуру Льюиса AsCl3.
Структура Льюиса AsCl3 представляет собой диаграмму, иллюстрирующую количество валентных электронов и пар связанных электронов в молекуле AsCl3. Затем геометрию молекулы AsCl3 можно предсказать с помощью теории отталкивания электронных пар валентной оболочки (теория VSEPR), которая утверждает, что молекулы будут выбирать геометрическую форму AsCl3, в которой электроны отличаются друг от друга.
Наконец, вы должны добавить полярности их связей, чтобы вычислить силу трех одинарных связей As-Cl (свойства дипольного момента молекулы AsCl3). Связи мышьяк-хлор в трихлориде мышьяка (AsCl3), например, поляризованы в сторону более электроотрицательного хлора в молекуле AsCl3, и поскольку обе связи имеют одинаковый размер и расположены вокруг трех хлорных концов тригональной пирамиды с одной неподеленной парой ( всего два электрона) на атоме мышьяка, их сумма дипольных моментов отлична от нуля из-за дипольного момента связи молекулы AsCl3 и большей полярности электронов по отношению к атомам хлора.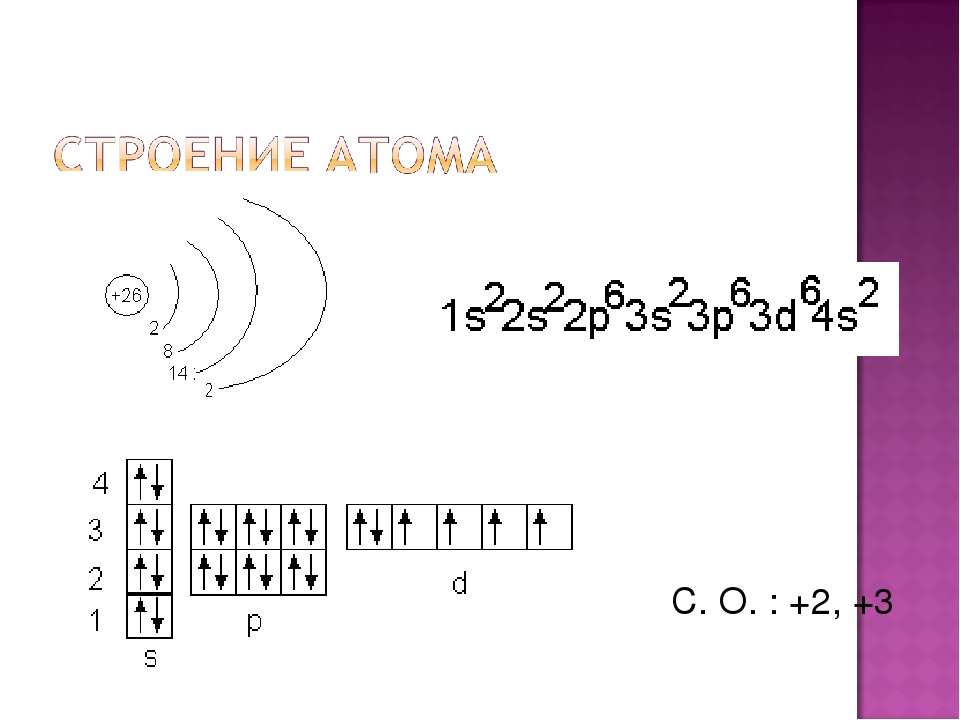 Потому что каждые три полярности связей As-Cl не компенсируют друг друга в молекуле AsCl3 благодаря наличию одной неподеленной пары электронов. Молекула трихлорида мышьяка (AsCl3) классифицируется как полярная молекула.
Потому что каждые три полярности связей As-Cl не компенсируют друг друга в молекуле AsCl3 благодаря наличию одной неподеленной пары электронов. Молекула трихлорида мышьяка (AsCl3) классифицируется как полярная молекула.
Молекула трихлорида мышьяка (с тригонально-пирамидальной молекулярной геометрией) наклонена, углы связи между мышьяком и хлором составляют 100 градусов. Он имеет разницу в значениях электроотрицательности между атомами мышьяка и хлора, при этом центральное притяжение мышьяка меньше, чем у концевого хлора в молекуле AsCl3.Но они не компенсировали друг друга благодаря несимметричной тригональной пирамидальности с одной неподеленной парой в молекулярной геометрии молекулы AsCl3.
В результате он имеет ненулевой дипольный момент. Молекула AsCl3 имеет ненулевой дипольный момент из-за неравномерного распределения отрицательных и положительных зарядов. Но и атомы мышьяка, и атомы хлора попадают в группы семейства азота и галогена в периодической таблице соответственно. Атом хлора является более электроотрицательным, чем мышьяк в молекуле AsCl3.Молекула AsCl3 имеет суммарный дипольный момент 2,17D в энергетическом состоянии основного состояния.
Атом хлора является более электроотрицательным, чем мышьяк в молекуле AsCl3.Молекула AsCl3 имеет суммарный дипольный момент 2,17D в энергетическом состоянии основного состояния.
Молекула AsCl3 имеет три одинарные связи As-Cl. Его дипольный момент в основном состоянии совершенно иной, чем в возбужденном состоянии. Если он поглощает свет, это может быть видимый или ультрафиолетовый свет. Он претерпевает переход от пи к пи-звезде и от п к пи-звезде с энергетического уровня основного состояния на энергетический уровень возбужденного состояния. На энергетическом уровне возбужденного состояния молекула AsCl3 имеет определенный дипольный момент.Но очень динамично.
Молекулы можно разделить на полярные и неполярные. Полярная молекула ведет себя иначе, чем неполярная.
Обзор: структура Льюиса AsCl3 Центральным атомом является мышьяк, который граничит с тремя концами с атомами хлора (в тригонально-пирамидальной геометрии) и одной неподеленной парой на центральном атоме мышьяка в тригонально-пирамидальной молекулярной геометрии.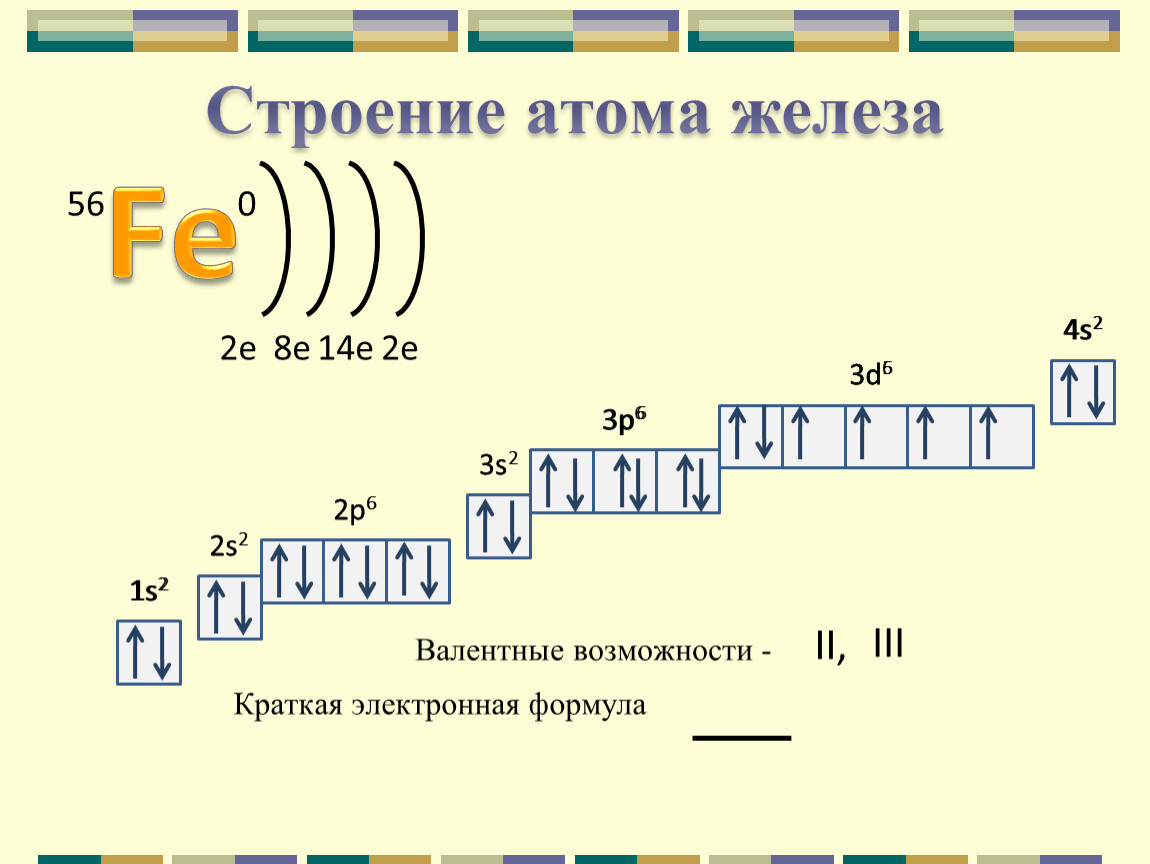 Мышьяк имеет пять самых внешних валентных электронов, что указывает на то, что он обладает пятью электронами на своей самой внешней оболочке, тогда как хлор также имеет семь валентных электронов на самой внешней оболочке.Для завершения октета атомов мышьяка и хлора требуется три и один валентный электрон на каждой их самой внешней оболочке соответственно.
Мышьяк имеет пять самых внешних валентных электронов, что указывает на то, что он обладает пятью электронами на своей самой внешней оболочке, тогда как хлор также имеет семь валентных электронов на самой внешней оболочке.Для завершения октета атомов мышьяка и хлора требуется три и один валентный электрон на каждой их самой внешней оболочке соответственно.
В результате три атома хлора устанавливают ковалентные связи с центральным атомом мышьяка, оставляя атом мышьяка с одной неподеленной парой. На центральном атоме мышьяка есть одна неподеленная пара электронов, которая сопротивляется парам связей трех связей As-Cl. Согласно теории VSEPR, полярность одиночных пар связей As-Cl приводит к тому, что молекула AsCl3 принимает структуру тригональной пирамидальной геометрии.
Три связи As-Cl в молекуле AsCl3 расположены в симметричном порядке полярности вокруг тригонально-пирамидальной молекулярной геометрии, что приводит к форме молекулы AsCl3. Молекула AsCl3 имеет тригонально-пирамидальную молекулярную геометрию, потому что существует электрическое отталкивание между неподеленными парами электронов в мышьяке и тремя парами одинарных связей (As-Cl) молекулы AsCl3.
Структура Льюиса AsCl3 имеет точечную электронную репрезентативную структуру. Валентные электроны атомов подвергаются смешению орбиталей в химических реакциях, что дает новые типы молекулярных частиц AsCl3.Молекула — это не что иное, как пучок валентных электронов атомов. Но он преобразуется в пары связей и неподеленные пары в молекулярной структуре.
Электроотрицательное значение Разница Расчет AsCl3 Молекула: Мышьяк и хлор Электроотрицательная разность в AsCl3:Атом мышьяка имеет электроотрицательность 2,19, а хлор имеет электроотрицательность 3,16 в молекуле AsCl3. Разницу в электроотрицательности мышьяка и хлора можно оценить с помощью приведенного ниже метода.
Электронгетивная разница величин между мышьяком и хлором в молекуле Ascl3
Значение электроотрицательности Arsenic = 2,19
Значение электроотрицательности хлора = 3,16
Разница в электрозвательном величине между мышьяк и хлор в ASCL3 молекула = 3,16 – 2.
Разность электроотрицательностей между связью As-Cl Расчет молекулы AsCl319 = 0,97
Электроотрицательная разница между мышьяком и хлором больше 0.5. Это указывало на то, что полярность связи приближается к полярной природе. Полярность связи As-Cl в молекуле AsCl3 полярная.
Из-за этой разницы в электроотрицательности атомов мышьяка и хлора связь As-Cl в молекуле AsCl3 становится полярной. Суммарный результирующий дипольный момент молекулы AsCl3 отличен от нуля из-за несокращения дипольного момента связи в тригонально-пирамидальной геометрии. Электроотрицательность атома — это сила, с которой он может притягивать на свою сторону связанные электронные пары.Полярность AsCl3 обсуждалась в нашем предыдущем посте.
В результате дипольный момент связи As-Cl высок из-за поляризации связей и одной неподеленной пары электронов на мышьяке, а все диполи связей As-Cl расположены в асимметричной молекулярной геометрии AsCl3. Молекула AsCl3 имеет ненулевой суммарный дипольный момент.
Молекула AsCl3 имеет ненулевой суммарный дипольный момент.
Электронно-точечная структура молекулы AsCl3 также известна как структура Льюиса AsCl3. Он определяет количество самых внешних валентных электронов, а также электронов, участвующих в образовании связи молекулы AsCl3.При рассмотрении льюисовской структуры молекулы необходимо понимать самые внешние валентные электроны молекулы AsCl3.
Атом мышьяка является средним элементом в молекулярной геометрии AsCl3 с пятью электронами на внешней оболочке валентных электронов, тогда как атом хлора имеет семь электронов на внешней оболочке валентных электронов. Атом хлора имеет семь валентных электронов.
AsCl3 имеет всего 26 валентных электронов в результате вышеприведенных рассуждений.С основным центральным атомом мышьяка три конца с тремя атомами хлора образуют ковалентные связи, оставляя атом мышьяка с одной неподеленной парой в середине тригональной пирамидальной геометрии.
Потому что неподеленные пары на концевых атомах хлора создают взаимодействие с парами связей As-Cl (но оно незначительно в основном состоянии молекулы AsCl3). Валентный угол связи Cl-As-Cl в тригонально-пирамидальной молекулярной геометрии составляет примерно 100 градусов. Этот угол меньше валентного угла молекулы Ch5.Длина связи As-Cl составляет 207 пм (пикометр).
Валентный угол связи Cl-As-Cl в тригонально-пирамидальной молекулярной геометрии составляет примерно 100 градусов. Этот угол меньше валентного угла молекулы Ch5.Длина связи As-Cl составляет 207 пм (пикометр).
Чтобы вычислить валентный электрон каждого атома в AsCl3, найдите его периодическую группу в периодической таблице. Семейства групп азота и галогена, которые являются 15-й и 17-й группами в периодической таблице, состоят из атомов мышьяка и хлора соответственно.В своих самых внешних оболочках хлор и мышьяк имеют семь и пять валентных электронов соответственно.
Рассчитайте общее число валентных электронов на внешней валентной оболочке молекулы AsCl3. Первый шаг — определить, сколько электронов находится в самой внешней валентной оболочке структуры Льюиса AsCl3. Электрон в самой внешней оболочке атома известен как валентный электрон. Он представлен точками на диаграмме Льюиса AsCl3. Ядро атома мышьяка молекулы AsCl3 можно представить следующим образом:
Электрон в самой внешней оболочке атома известен как валентный электрон. Он представлен точками на диаграмме Льюиса AsCl3. Ядро атома мышьяка молекулы AsCl3 можно представить следующим образом:
Общее количество электронов внешней валентной оболочки атома мышьяка в AsCl3= 5
Общее количество электронов внешней валентной оболочки атома хлора в AsCl3= 7
Молекула AsCl3 имеет один центральный атом мышьяка и три атома хлора.Тогда общее количество электронов внешней валентной оболочки можно рассчитать следующим образом:
∴ Общее количество электронов внешней валентной оболочки, доступных для структуры Льюиса AsCl3 (точечная структура) = 5+3*7= 26 валентных электронов в AsCl3.
расчет полного валентного электрона молекулы AsCl3
Выберите атом с наименьшим электроотрицательным значением и вставьте его в центр молекулярной геометрии AsCl3. Мы выберем атом с наименьшим электроотрицательным значением в молекуле AsCl3 и поместим его в центр структурной диаграммы Льюиса AsCl3 в этой фазе. Значение электроотрицательности в периодических группах растет слева направо в таблице Менделеева и падает сверху вниз.
Значение электроотрицательности в периодических группах растет слева направо в таблице Менделеева и падает сверху вниз.
Первый шаг — поместить пять валентных электронов вокруг атома мышьяка, как показано на рисунке.
Шаг 2: структура Льюиса AsCl3 для подсчета валентных электронов вокруг концевых атомов хлораВ результате мышьяк является третьим атомом в группе семейства азота периодической таблицы. Хлор является вторым членом семейства галогенов.Электроотрицательность атома хлора выше, чем у атома мышьяка в молекуле AsCl3. Кроме того, хлор имеет предел в семь электронов, поскольку мышьяк является менее электроотрицательным элементом в молекуле AsCl3.
На структурной диаграмме Льюиса AsCl3 атом мышьяка может быть центральным атомом молекулы. В результате центральный мышьяк в структуре Льюиса AsCl3 со всеми тремя атомами хлора расположен в тригонально-пирамидальной геометрии.
Добавьте валентные электроны вокруг атома хлора, как показано на рисунке.
Соедините внешний и центральный атомы ядра молекулы AsCl3 тремя одинарными связями As-Cl. На этом этапе используйте три атома хлора снаружи молекулы AsCl3 для центрального атома мышьяка в середине.
Подсчитайте, сколько электронов с самой внешней валентной оболочки уже было использовано в структуре AsCl3. Каждая одинарная связь As-Cl несет два электрона, потому что каждый атом мышьяка соединен с тремя атомами хлора тремя одинарными связями As-Cl.Связующие пары As-Cl — вот как они называются.
Таким образом, из 26 валентных электронов, доступных для структуры Льюиса AsCl3, мы использовали шесть электронов для трех одинарных связей As-Cl молекулы AsCl3. Молекула AsCl3 имеет одну неподеленную пару электронов в центральном атоме мышьяка.
Поместите валентные электроны в пары связей As-Cl, начиная с ядра мышьяка, три атома хлора в молекуле AsCl3. В структурной диаграмме Льюиса AsCl3 мы всегда начинаем с введения валентных электронов от центрального атома мышьяка (на шаге 1).В результате сначала оберните валентные электроны пары связи центрального атома мышьяка (см. рисунок для шага 1).
Атом мышьяка в молекуле получает только 8 электронов вокруг своей молекулярной структуры. Этот центральный атом мышьяка стабилен по октету. Но у него есть одна одинокая пара. Мышьяк представляет собой коричневатое твердое вещество. Мышьяк воспламеняется при контакте с воздухом. Но мышьяк используется в спичечных коробках и петардах.
Хлор (Cl2) находится в газообразном состоянии при нормальной температуре и давлении.Он используется в качестве хлорирующего агента в области органической химии. Это очень агрессивный газ. Он вызывает сухую коррозию металлических корпусов. Он очень реактивен по отношению к биомикроорганизмам. Он также используется в качестве дезинфицирующего средства на очистных сооружениях.
Мышьяку требуется 8 электронов в самой внешней валентной оболочке для обеспечения стабильности молекулярного октета, шесть электронных пар связи в трех одинарных связях As-Cl и одна неподеленная пара в центральном атоме мышьяка.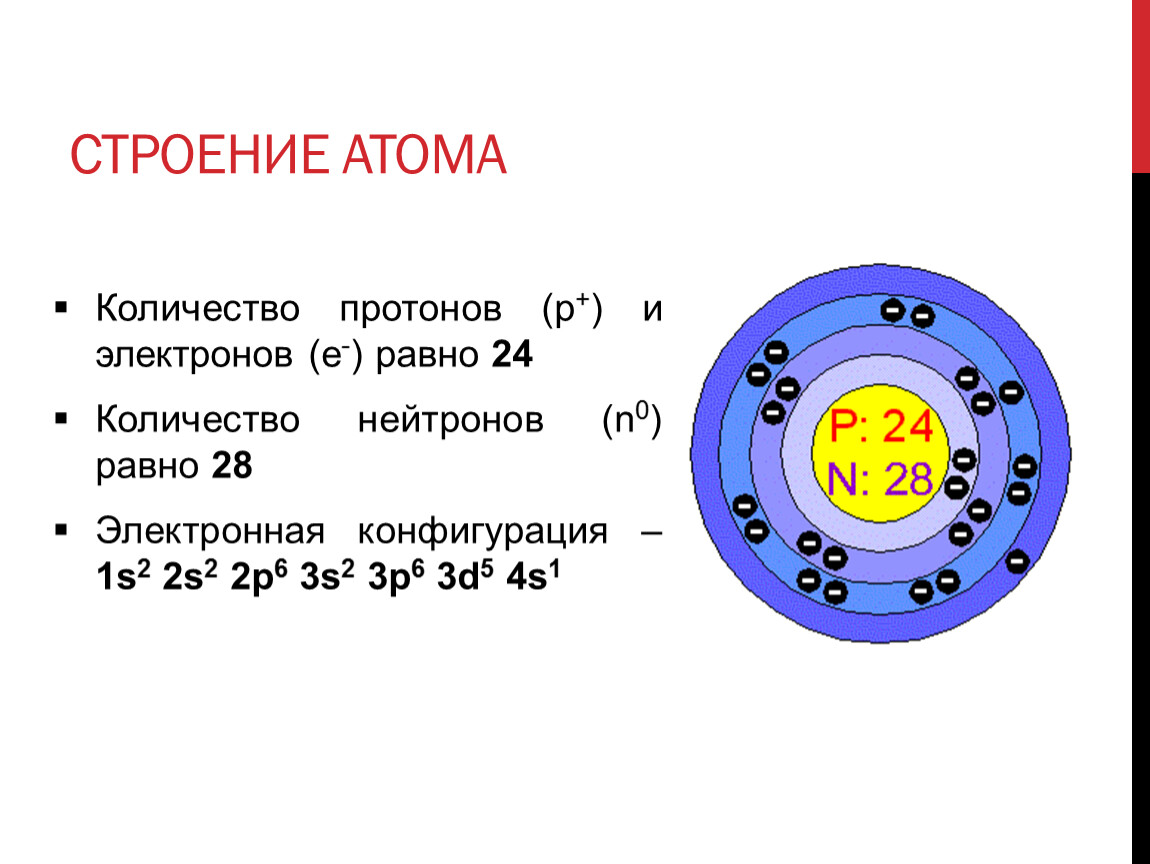 Затем неподеленная пара электронов на атомах хлора молекулы AsCl3 размещается в тригонально-пирамидальной геометрии.Мышьяк уже делит 8 электронов с тремя одинарными связями As-Cl. Затем поместите валентный электрон в атомы хлора, он разместил около семи электронов на каждом атоме (шаг 2). 18 валентных электронов были размещены вокруг трех атомов хлора в виде неподеленных пар электронов.
Затем неподеленная пара электронов на атомах хлора молекулы AsCl3 размещается в тригонально-пирамидальной геометрии.Мышьяк уже делит 8 электронов с тремя одинарными связями As-Cl. Затем поместите валентный электрон в атомы хлора, он разместил около семи электронов на каждом атоме (шаг 2). 18 валентных электронов были размещены вокруг трех атомов хлора в виде неподеленных пар электронов.
Мы разместили 18 электронов вокруг трехконцевых атомов хлора (шаг 3), которые представлены точкой в молекулярной структуре AsCl3 выше. Атом мышьяка завершает свою молекулярную стабильность октета в молекуле AsCl3, поскольку он обладает шестью электронами в своих парах связей (три одинарных связи As-Cl) с тремя атомами хлора в самой внешней валентной оболочке.
Подсчитайте, сколько электронов внешней валентной оболочки было использовано до сих пор, используя структуру Льюиса AsCl3. три пары электронных связей показаны точками в химической структуре AsCl3, тогда как каждая из трех одинарных связей содержит по два электрона. В результате расчета число электронов внешней валентной оболочки молекулы AsCl3 (пары связей) равно шести. Общее количество валентных электронов в атоме мышьяка равно 8,
В результате расчета число электронов внешней валентной оболочки молекулы AsCl3 (пары связей) равно шести. Общее количество валентных электронов в атоме мышьяка равно 8,
До сих пор мы использовали 26 из 26 электронов самой внешней валентной оболочки структуры AsCl3 Льюиса.Одна неподеленная пара электронов на атоме мышьяка в тригонально-пирамидальной геометрии молекулы AsCl3.
Завершить стабильность среднего атома мышьяка и, при необходимости, применить ковалентную связь. Центральный атом мышьяка подвергается стабильности октета (из-за трех пар одинарных связей электронов).
Основным атомом в структуре Льюиса AsCl3 является мышьяк, который связан с тремя атомами хлора одинарными связями (три As-Cl). С помощью трех одинарных связей он делит уже 8 электронов.В результате мышьяк следует правилу октета и имеет 8 электронов, окружающих его на трех концах тригонально-пирамидальной геометрии молекулы AsCl3.
Как рассчитать формальный заряд атомов мышьяка и хлора в структуре Льюиса AsCl3? Расчет формального заряда мышьяка молекулы AsCl3 : Формальный заряд центрального атома мышьяка молекулы AsCl3 часто соответствует фактическому заряду этого центрального атома мышьяка. В следующих вычислениях формальный заряд будет рассчитан для центрального атома мышьяка точечной структуры Льюиса AsCl3.
В следующих вычислениях формальный заряд будет рассчитан для центрального атома мышьяка точечной структуры Льюиса AsCl3.
Рассчитать формальный заряд центрального атома мышьяка молекулы AsCl3 по следующей формуле:
Формальный заряд атома мышьяка молекулы AsCl3= (V. E(P)– LE(P) – 1/ 2(BE))
VE (P) = валентный электрон в атоме мышьяка молекулы AsCl3
LE(P) = неподеленная пара электрона в атоме мышьяка молекулы AsCl3.
B.E = электрон пары связи в атоме P молекулы AsCl3
расчет формального заряда атома мышьяка в молекуле AsCl3
Атом ядра мышьяка (три одинарные связи, соединенные с тремя атомами хлора) молекулы AsCl3 имеет пять валентных электронов, одну неподеленную пару электронов (два электрона) и шесть связывающих парных валентных электронов. Поместите эти значения для атома мышьяка в формулу выше.
Формальный заряд атома мышьяка в молекуле AsCl3 = (5- 2-(6/2)) =0
В структуре Льюиса AsCl3 формальный заряд центрального атома мышьяка равен нулю.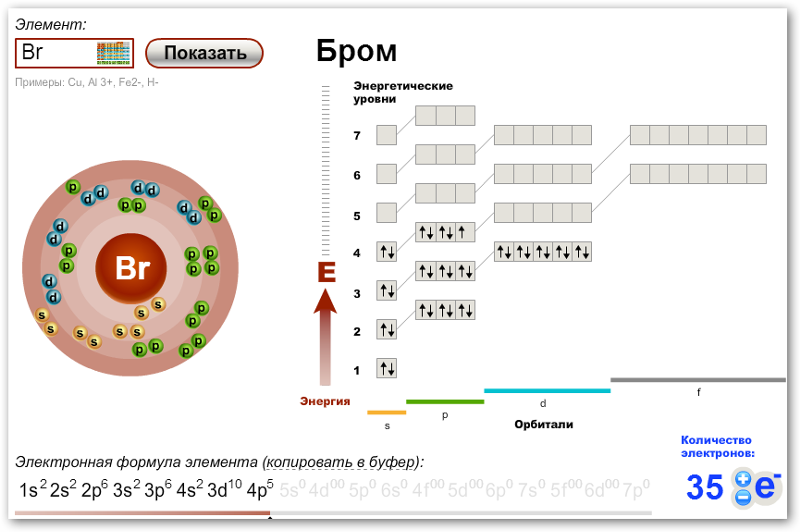
Формальный заряд концевых атомов хлора в молекуле AsCl3 часто соответствует фактическому заряду этих концевых атомов хлора. В следующих вычислениях формальный заряд будет рассчитываться на концевом атоме хлора в точечной структуре Льюиса AsCl3.
Для расчета формального заряда концевого атома хлора молекулы AsCl3 по следующей формуле:
Формальный заряд атома хлора молекулы AsCl3 = (V.E(Cl)– LE(Cl) – 1/2(BE))
VE (Cl) = валентный электрон в атоме хлора молекулы AsCl3
LE(Cl) = неподеленные пары электрона в атоме хлора молекула AsCl3.
B.E = электрон связи в атоме Cl в молекуле AsCl3
расчет формального заряда на атоме хлора в молекуле AsCl3
Концевые атомы хлора молекулы AsCl3 имеют семь валентных электронов, три неподеленные пары электронов (шесть электронов) и два связывающих спаренных валентных электрона (одинарная связь). Подставьте эти значения для атома хлора в приведенную выше формулу.
Подставьте эти значения для атома хлора в приведенную выше формулу.
Формальный заряд атома хлора в молекуле AsCl3 = (7- 6-(2/2)) =0
В структуре Льюиса AsCl3 формальный заряд на концевом атоме хлора равен нулю.
Сводка:В этом посте мы обсудили метод построения структуры Льюиса AsCl3. Во-первых, валентные электроны располагаются вокруг атома мышьяка. Во-вторых, поместите валентный электрон на атомы хлора.Наконец, когда мы объединили первый и второй шаги. Это дает структуру Льюиса AsCl3. Необходимо помнить, что если вы будете следовать описанному выше методу, вы сможете очень легко построить структуру молекулярных точек.
Что такое структура Льюиса AsCl3?
Структура Льюиса AsCl3 представляет собой точечное представление
Каков формальный заряд структуры Льюиса AsCl3?
Нулевые заряды на молекулярной структуре AsCl3
Полярность молекулПолярность молекул указана следующим образом
Структура Льюиса и молекулярная геометрияСтруктура Льюиса и молекулярная геометрия молекул перечислены ниже
Внешняя ссылка:Информация о PCl3
18.
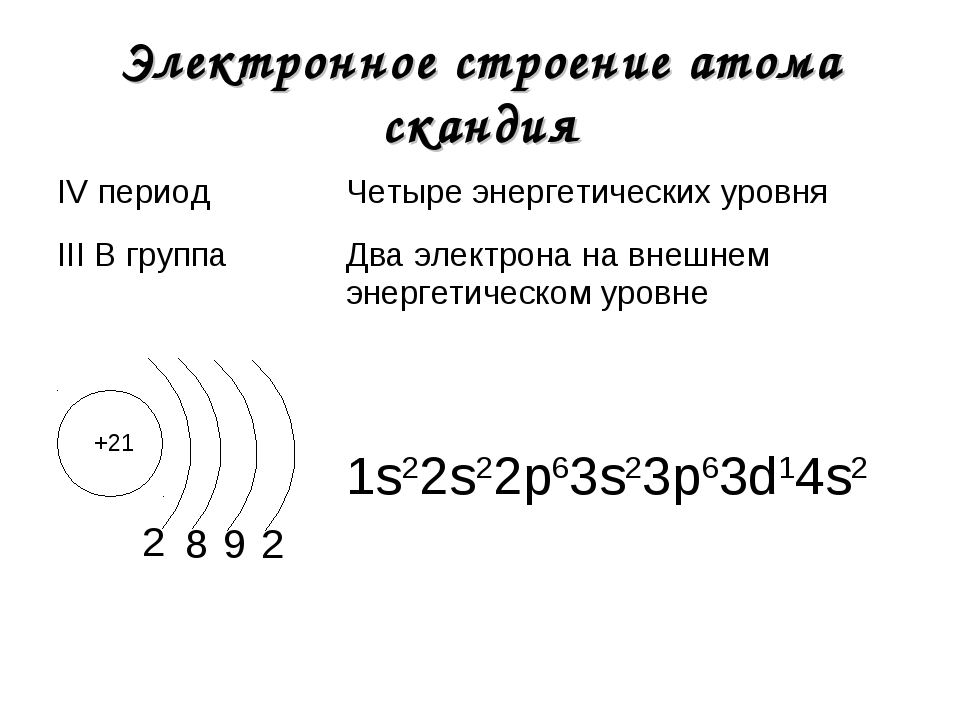 3 Структура и общие свойства металлоидов – Химия
3 Структура и общие свойства металлоидов – ХимияРяд из шести элементов, называемых металлоидами, отделяет металлы от неметаллов в периодической таблице. Металлоиды – бор, кремний, германий, мышьяк, сурьма и теллур. Эти элементы выглядят металлическими; однако они не проводят электричество так же хорошо, как металлы, поэтому они являются полупроводниками. Они являются полупроводниками, потому что их электроны более тесно связаны с их ядрами, чем у металлических проводников.Их химическое поведение находится между металлами и неметаллами. Например, чистые металлоиды образуют ковалентные кристаллы, подобно неметаллам, но, как и металлы, обычно не образуют одноатомных анионов. Это промежуточное поведение частично связано с их промежуточными значениями электроотрицательности. В этом разделе мы кратко обсудим химическое поведение металлоидов и рассмотрим два из этих элементов — бор и кремний — более подробно.
Металлоид бора имеет много общего со своим соседом углеродом и его диагональным соседом кремнием.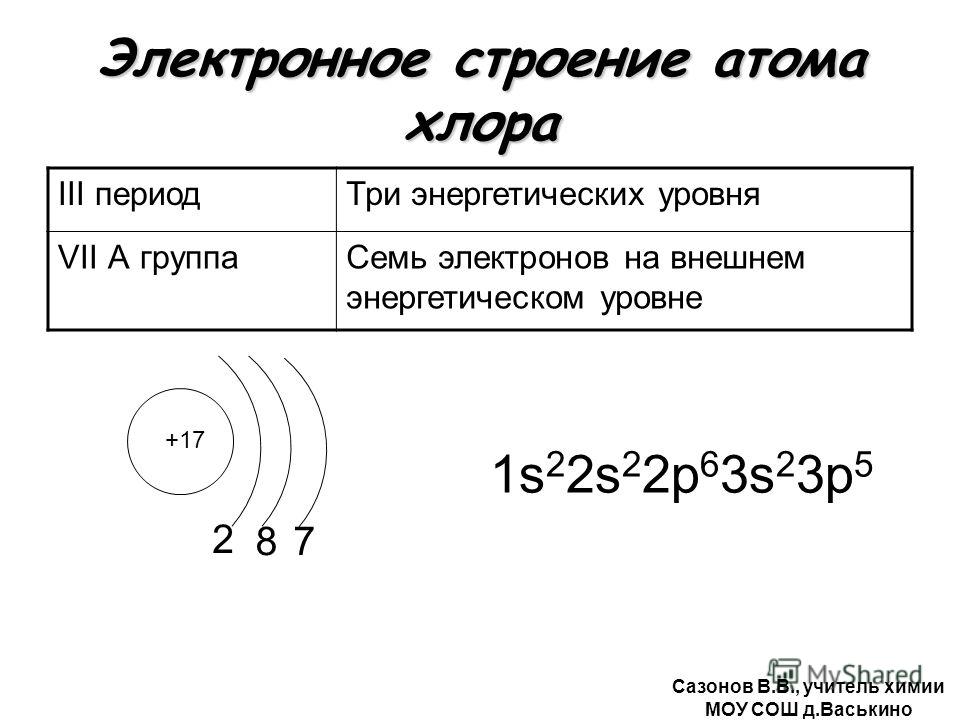 Все три элемента образуют ковалентные соединения. Однако у бора есть одно явное отличие: его внешняя электронная структура 2 s 2 2 p 1 дает ему на один валентный электрон меньше, чем он имеет валентные орбитали. Хотя бор проявляет степень окисления 3+ в большинстве своих стабильных соединений, этот недостаток электронов обеспечивает бору способность образовывать другие, иногда дробные, степени окисления, которые имеют место, например, в гидридах бора.
Все три элемента образуют ковалентные соединения. Однако у бора есть одно явное отличие: его внешняя электронная структура 2 s 2 2 p 1 дает ему на один валентный электрон меньше, чем он имеет валентные орбитали. Хотя бор проявляет степень окисления 3+ в большинстве своих стабильных соединений, этот недостаток электронов обеспечивает бору способность образовывать другие, иногда дробные, степени окисления, которые имеют место, например, в гидридах бора.
Кремний имеет электронную конфигурацию валентной оболочки 3 s 2 3 p 2 , и он обычно образует тетраэдрические структуры, в которых он sp 3 формально гибридизован с 4 a степенью окисления.Основные различия между химией углерода и кремния связаны с относительной прочностью связи углерод-углерод, способностью углерода образовывать стабильные связи с самим собой и наличием пустых орбиталей валентной оболочки 3 d в кремнии. Пустые орбитали d кремния и пустая орбиталь p бора позволяют тетраэдрическим соединениям кремния и тригональным плоским соединениям бора действовать как кислоты Льюиса. У углерода, с другой стороны, нет доступных орбиталей валентной оболочки; тетраэдрические соединения углерода не могут действовать как кислоты Льюиса.По своему химическому поведению германий очень похож на кремний.
Пустые орбитали d кремния и пустая орбиталь p бора позволяют тетраэдрическим соединениям кремния и тригональным плоским соединениям бора действовать как кислоты Льюиса. У углерода, с другой стороны, нет доступных орбиталей валентной оболочки; тетраэдрические соединения углерода не могут действовать как кислоты Льюиса.По своему химическому поведению германий очень похож на кремний.
Мышьяк и сурьма обычно образуют соединения, в которых проявляется степень окисления 3+ или 5+; однако мышьяк может образовывать арсениды со степенью окисления 3-. Эти элементы лишь слегка тускнеют в сухом воздухе, но легко окисляются при нагревании.
Теллур напрямую соединяется с большинством элементов. Наиболее устойчивыми соединениями теллура являются теллуриды — соли Te 2–, образованные с активными металлами и лантаноидами, а также соединения с кислородом, фтором и хлором, в которых теллур обычно проявляет степень окисления 2+ или 4+.Хотя соединения теллура (VI) известны (например, TeF 6 ), существует заметная устойчивость к окислению до этой максимальной степени группового окисления.
Бор составляет менее 0,001% по массе земной коры. В природе встречается только в соединениях с кислородом. Бор широко распространен в вулканических регионах в виде борной кислоты, B(OH) 3 , и в районах сухих озер, включая пустынные районы Калифорнии, в виде боратов и солей бороксикислот, таких как бура, Na 2 B . 4 О 7 ⋅10H 2 О.
Элементарный бор химически инертен при комнатной температуре, реагируя только с фтором и кислородом с образованием трифторида бора BF 3 и оксида бора B 2 O 3 соответственно. При более высоких температурах бор реагирует со всеми неметаллами, кроме теллура и инертных газов, и почти со всеми металлами; окисляется до B 2 O 3 при нагревании с концентрированной азотной или серной кислотой. Бор не реагирует с неокисляющими кислотами. Многие соединения бора легко реагируют с водой с образованием борной кислоты B(OH) 3 (иногда обозначаемой как H 3 BO 3 ).
Восстановление оксида бора порошком магния образует бор (чистота 95–98,5 %) в виде коричневого аморфного порошка:
[латекс]\текст{B}_2\текст{O}_3(s)\;+\;3\text{Mg}(s)\;{\longrightarrow}\;2\text{B}(s) \;+\;3\text{MgO}(т)[/латекс]
Аморфное вещество представляет собой материал, который кажется твердым, но не имеет дальнего порядка, как истинно твердое тело. Обработка соляной кислотой удаляет оксид магния. Дальнейшая очистка бора начинается с превращения нечистого бора в треххлористый бор.{\circ} = 253,7\;\text{кДж}[/латекс]
Кремний составляет почти четверть массы земной коры, уступая по распространенности только кислороду. Кора почти полностью состоит из минералов, в которых атомы кремния находятся в центре кремнекислородного тетраэдра, которые соединяются различными способами, образуя, среди прочего, цепочки, слои и трехмерные каркасы. Эти минералы составляют основную массу наиболее распространенных горных пород, почвы и глин. Кроме того, такие материалы, как кирпич, керамика и стекло, содержат соединения кремния.
Можно производить кремний путем высокотемпературного восстановления диоксида кремния сильными восстановителями, такими как углерод и магний:
[латекс]\текст{SiO}_2(s)\;+\;2\text{C}(s)\;\overset{\Delta}{\longrightarrow}\;\text{Si}(s)\ ;+\;2\text{CO}(g)[/латекс]
[латекс]\text{SiO}_2(s)\;+\;2\text{Mg}(s)\;\overset{\ Delta}{\longrightarrow}\;\text{Si}(s)\;+\;2\text{MgO}(s)[/latex]
Чрезвычайно чистый кремний необходим для производства полупроводниковых электронных устройств.Этот процесс начинается с превращения нечистого кремния в тетрагалогениды кремния или силан (SiH 4 ) с последующим разложением при высоких температурах. Зона очистки, показанная на рисунке 3, завершает очистку. В этом методе кремниевый стержень нагревается с одного конца источником тепла, который создает тонкое поперечное сечение расплавленного кремния. Медленное опускание стержня через источник тепла перемещает расплавленную зону с одного конца стержня на другой. По мере движения этой тонкой расплавленной области примеси в кремнии растворяются в жидком кремнии и перемещаются вместе с расплавленной областью.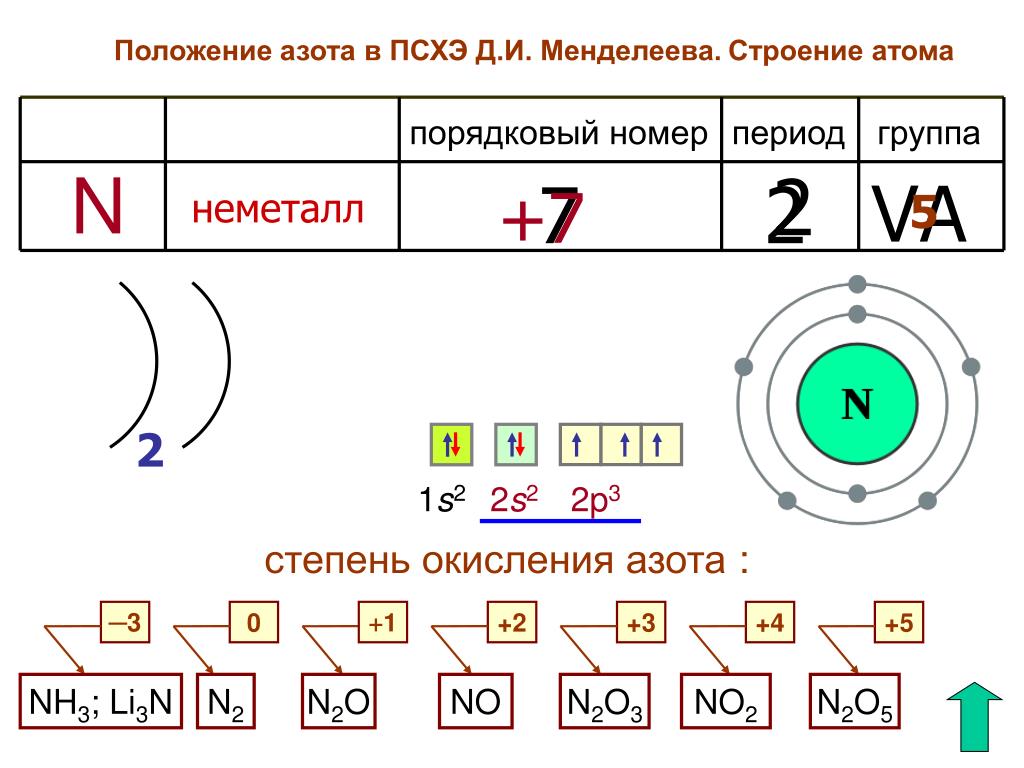 В конечном итоге примеси перемещаются к одному концу стержня, который затем отрезается.
В конечном итоге примеси перемещаются к одному концу стержня, который затем отрезается.
Этот высокоочищенный кремний, содержащий не более одной части примеси на миллион частей кремния, является наиболее важным элементом в компьютерной промышленности. Чистый кремний необходим в полупроводниковых электронных устройствах, таких как транзисторы, компьютерные чипы и солнечные элементы.
Как и у некоторых металлов, пассивация кремния происходит за счет образования очень тонкой пленки оксида (прежде всего диоксида кремния, SiO 2 ).{\;\;4-}(водный раствор)\;+\;2\text{H}_2(g)[/латекс]
Кремний реагирует с галогенами при высоких температурах с образованием летучих тетрагалогенидов, таких как SiF 4 .
В отличие от углерода, кремний плохо образует двойные или тройные связи. Соединения кремния общей формулы SiX 4 , где X представляет собой сильно электроотрицательную группу, могут действовать как кислоты Льюиса с образованием шестикоординированного кремния.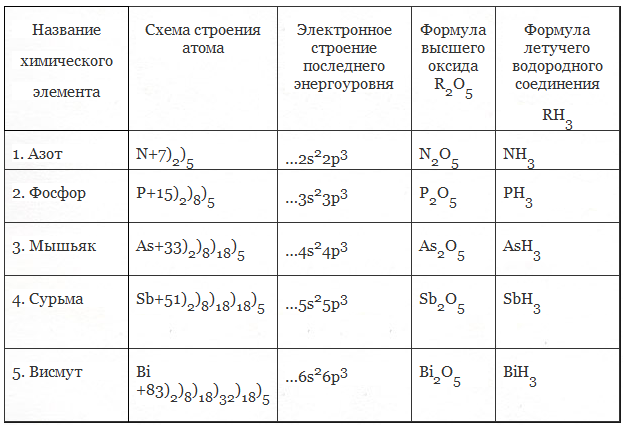 {2-}[/ латекс] ион, в котором кремний sp 3 d 2 гибридизован:
{2-}[/ латекс] ион, в котором кремний sp 3 d 2 гибридизован:
[латекс]2\текст{NaF}(s)\;+\;\text{SiF}_4(g)\;{\longrightarrow}\;\text{Na}_2\text{SiF}_6(s) [/латекс]
Сурьма легко реагирует со стехиометрическими количествами фтора, хлора, брома или йода с образованием тригалогенидов или с избытком фтора или хлора с образованием пентагалогенидов SbF 5 и SbCl 5 .В зависимости от стехиометрии при нагревании с серой образует сульфид сурьмы (III), Sb 2 S 3 или сульфид сурьмы (V). Как и ожидалось, металлическая природа элемента выше, чем у мышьяка, который находится непосредственно над ним в группе 15.
Галогениды бора и кремния
Тригалогениды бора — BF 3 , BCl 3 , BBr 3 и BI 3 — могут быть получены прямой реакцией элементов. Эти неполярные молекулы содержат бор с гибридизацией sp 2 и тригонально-плоской молекулярной геометрией. {\circ} = -191.2\;\текст{кДж}[/латекс]
{\circ} = -191.2\;\текст{кДж}[/латекс]
Плавиковая кислота — единственная распространенная кислота, которая реагирует с диоксидом кремния или силикатами. Эта реакция происходит потому, что связь кремний-фтор является единственной связью, образуемой кремнием, которая прочнее, чем связь кремний-кислород. По этой причине все распространенные кислоты, кроме плавиковой, можно хранить в стеклянных емкостях.
За исключением тетрафторида кремния, галогениды кремния чрезвычайно чувствительны к воде. Под воздействием воды SiCl 4 быстро реагирует с гидроксидными группами, заменяя все четыре атома хлора с образованием нестабильной ортокремниевой кислоты, Si(OH) 4 или H 4 SiO 4 , которая медленно разлагается на SiO 2 .
Оксиды бора и кремния и их производные
Бор сгорает при 700 °С в кислороде с образованием оксида бора, B 2 O 3 . Оксид бора необходим для производства термостойкого боросиликатного стекла, подобного показанному на рис. 4, и некоторых оптических стекол. Оксид бора растворяется в горячей воде с образованием борной кислоты B(OH) 3 :
4, и некоторых оптических стекол. Оксид бора растворяется в горячей воде с образованием борной кислоты B(OH) 3 :
[латекс]\текст{B}_2\текст{O}_3(s)\;+\;3\text{H}_2\текст{O}(l)\;{\longrightarrow}\;2\text {B(OH)}_3(водный)[/латекс]
Рис. 4. Лабораторная стеклянная посуда, такая как Pyrex и Kimax, изготовлена из боросиликатного стекла, поскольку оно не бьется при нагревании. Включение боратов в стекло помогает опосредовать эффекты теплового расширения и сжатия. Это снижает вероятность теплового удара, из-за которого силикатное стекло трескается при быстром нагревании или охлаждении. (кредит: «Tweenk»/Wikimedia Commons)Атом бора в B(OH) 3 является sp 2 гибридизованным и расположен в центре равностороннего треугольника с атомами кислорода в углах.{-10}[/латекс]
Рисунок 5. Борная кислота имеет плоскую структуру с тремя группами –OH, равномерно распределенными под углом 120° друг к другу.
При нагревании борной кислоты до 100 °C молекулы воды расщепляются между парами соседних групп –OH с образованием метаборной кислоты, HBO 2 . Примерно при 150 °C образуются дополнительные связи BO-B, соединяющие группы BO 3 вместе с общими атомами кислорода с образованием тетраборной кислоты H 2 B 4 O 7 .{\;\;3-}[/latex] до сложных частиц, содержащих цепочки и кольца трех- и четырехкоординированных атомов бора. Структуры анионов, обнаруженных в CaB 2 O 4 , K[B 5 O 6 (OH) 4 ]⋅2H 2 O (обычно пишут KB ⋅4h 2 o) и Na 2 [B 4 o 5 (OH) 4 ] ⋅8H 2 O (обычно написано NA 2 B 4 O 7 ⋅ 10H 2 O) показаны на рисунке 6.С коммерческой точки зрения наиболее важным боратом является бура, Na 2 [B 4 O 5 (OH) 4 ]⋅8H 2 O, которая является важным компонентом некоторых моющих средств для стирки. Большая часть поставок буры поступает непосредственно из высохших озер, таких как озеро Сирлс в Калифорнии, или производится из кернита, Na 2 B 4 O 7 ⋅4H 2 O.
Большая часть поставок буры поступает непосредственно из высохших озер, таких как озеро Сирлс в Калифорнии, или производится из кернита, Na 2 B 4 O 7 ⋅4H 2 O.
Диоксид кремния, диоксид кремния, встречается как в кристаллической, так и в аморфной формах. Обычной кристаллической формой диоксида кремния является кварц, твердое, хрупкое, прозрачное бесцветное твердое вещество. Он полезен во многих отношениях — для архитектурных украшений, полудрагоценных камней и управления частотой в радиопередатчиках. Кремнезем принимает в природе много кристаллических форм или полиморфов . Следовые количества Fe 3+ в кварце придают аметисту его характерный фиолетовый цвет. Термин кварц также используется для таких изделий, как трубки и линзы, изготовленные из аморфного кремнезема. Опал – это встречающаяся в природе форма аморфного кремнезема.
Термин кварц также используется для таких изделий, как трубки и линзы, изготовленные из аморфного кремнезема. Опал – это встречающаяся в природе форма аморфного кремнезема.
Интересен контраст в структуре и физических свойствах между диоксидом кремния и диоксидом углерода, как показано на рис. 7. Твердый диоксид углерода (сухой лед) содержит одиночные молекулы CO 2 с каждым из двух атомов кислорода, присоединенных к атому углерода двойные связи. Очень слабые межмолекулярные силы удерживают молекулы вместе в кристалле.Летучесть сухого льда отражает эти слабые силы между молекулами. Напротив, диоксид кремния представляет собой твердое вещество с ковалентной сеткой. В диоксиде кремния каждый атом кремния связан с четырьмя атомами кислорода одинарными связями, направленными к углам правильного тетраэдра, а тетраэдры SiO 4 имеют общие атомы кислорода. Такое расположение дает трехмерную непрерывную кремний-кислородную сеть. Кристалл кварца представляет собой макромолекулу диоксида кремния. Разница между этими двумя соединениями заключается в способности элементов 14 группы образовывать прочные π-связи.Элементы второго периода, такие как углерод, образуют очень сильные π-связи, поэтому углекислый газ образует небольшие молекулы с сильными двойными связями. Элементы ниже второго периода, такие как кремний, не образуют π-связи так легко, как элементы второго периода, а когда они образуются, π-связи слабее, чем связи, образованные элементами второго периода. По этой причине диоксид кремния не содержит π-связей, а только σ-связи.
Разница между этими двумя соединениями заключается в способности элементов 14 группы образовывать прочные π-связи.Элементы второго периода, такие как углерод, образуют очень сильные π-связи, поэтому углекислый газ образует небольшие молекулы с сильными двойными связями. Элементы ниже второго периода, такие как кремний, не образуют π-связи так легко, как элементы второго периода, а когда они образуются, π-связи слабее, чем связи, образованные элементами второго периода. По этой причине диоксид кремния не содержит π-связей, а только σ-связи.
При 1600 °C кварц плавится, образуя вязкую жидкость. Когда жидкость охлаждается, она не кристаллизуется легко, но обычно переохлаждается и образует стекло, также называемое кремнеземом. Тетраэдры SiO 4 в стекловидном кремнеземе имеют случайное расположение, характерное для переохлажденных жидкостей, а стекло обладает некоторыми очень полезными свойствами. Силикагель очень прозрачен как для видимого, так и для ультрафиолетового света.По этой причине он важен при производстве ламп, дающих излучение, богатое ультрафиолетовым светом, и в некоторых оптических приборах, работающих с ультрафиолетовым светом. Коэффициент расширения кварцевого стекла очень низкий; поэтому быстрые изменения температуры не вызывают его разрушения. CorningWare и другая керамическая посуда содержат аморфный кремнезем.
Когда жидкость охлаждается, она не кристаллизуется легко, но обычно переохлаждается и образует стекло, также называемое кремнеземом. Тетраэдры SiO 4 в стекловидном кремнеземе имеют случайное расположение, характерное для переохлажденных жидкостей, а стекло обладает некоторыми очень полезными свойствами. Силикагель очень прозрачен как для видимого, так и для ультрафиолетового света.По этой причине он важен при производстве ламп, дающих излучение, богатое ультрафиолетовым светом, и в некоторых оптических приборах, работающих с ультрафиолетовым светом. Коэффициент расширения кварцевого стекла очень низкий; поэтому быстрые изменения температуры не вызывают его разрушения. CorningWare и другая керамическая посуда содержат аморфный кремнезем.
Силикаты представляют собой соли, содержащие анионы, состоящие из кремния и кислорода. Почти во всех силикатах sp 3 -гибридизованные атомы кремния находятся в центрах тетраэдров с кислородом в углах. Существует вариация в соотношении кремния и кислорода, которая возникает из-за того, что тетраэдры кремний-кислород могут существовать как дискретные, независимые единицы или могут иметь общие атомы кислорода в углах различными способами. Кроме того, присутствие различных катионов приводит к образованию большого количества силикатных минералов.
Существует вариация в соотношении кремния и кислорода, которая возникает из-за того, что тетраэдры кремний-кислород могут существовать как дискретные, независимые единицы или могут иметь общие атомы кислорода в углах различными способами. Кроме того, присутствие различных катионов приводит к образованию большого количества силикатных минералов.
Многие виды керамики состоят из силикатов. Включая небольшие количества других соединений, можно изменить физические свойства силикатных материалов для производства керамики с полезными характеристиками.
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка браузера на прием файлов cookie
Существует множество причин, по которым файл cookie не может быть установлен правильно. Ниже приведены наиболее распространенные причины:
- В вашем браузере отключены файлы cookie.
Вам необходимо сбросить настройки браузера, чтобы принять файлы cookie, или спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файл cookie.
- Ваш браузер не поддерживает файлы cookie. Попробуйте другой браузер, если вы подозреваете это.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы это исправить, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Предоставить доступ без файлов cookie
потребует от сайта создания нового сеанса для каждой посещаемой вами страницы, что замедляет работу системы до неприемлемого уровня.
Предоставить доступ без файлов cookie
потребует от сайта создания нового сеанса для каждой посещаемой вами страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в файле cookie; никакая другая информация не фиксируется.
Как правило, в файле cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, если вы не решите ввести его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступ к остальной части вашего компьютера, и только сайт, создавший файл cookie, может его прочитать.
Arsenic Atom – обзор
11.1 ВВЕДЕНИЕ
Полупроводниковый сплав нитрида арсенида галлия (индия) в последние годы привлек значительное внимание. Когда небольшая часть атомов мышьяка в GaAs заменяется азотом, энергетическая щель сначала быстро уменьшается, примерно на 0,1 эВ на % N для x → 0,03 [1], при этом измеренная масса CBE также показывает неожиданно большие значения [2]. -6]. Такое поведение заметно отличается от обычных полупроводников и представляет интерес как с фундаментальной точки зрения, так и из-за его значительных потенциальных применений в устройствах.Сильный изгиб открывает возможность использования GaInNA для получения оптического излучения на подложке GaAs на технологически важных длинах волн 1,3 и 1,55 мкм, что значительно расширяет возможности GaAs для оптоэлектроники [7-10], как обсуждалось в других местах этой книги.
Когда небольшая часть атомов мышьяка в GaAs заменяется азотом, энергетическая щель сначала быстро уменьшается, примерно на 0,1 эВ на % N для x → 0,03 [1], при этом измеренная масса CBE также показывает неожиданно большие значения [2]. -6]. Такое поведение заметно отличается от обычных полупроводников и представляет интерес как с фундаментальной точки зрения, так и из-за его значительных потенциальных применений в устройствах.Сильный изгиб открывает возможность использования GaInNA для получения оптического излучения на подложке GaAs на технологически важных длинах волн 1,3 и 1,55 мкм, что значительно расширяет возможности GaAs для оптоэлектроники [7-10], как обсуждалось в других местах этой книги.
Наше понимание обычных сплавов III-V основано на ряде подходов. Большой прогресс основан на использовании и применении относительно простых моделей, таких как теория эффективной массы и метод огибающей [11-13], для описания электронных состояний в квантовых ямах и гетероструктурах. Эти простые и хорошо зарекомендовавшие себя модели подкрепляются более подробными и фундаментальными теоретическими расчетами, а также сравнением с широким спектром экспериментальных данных.
Эти простые и хорошо зарекомендовавшие себя модели подкрепляются более подробными и фундаментальными теоретическими расчетами, а также сравнением с широким спектром экспериментальных данных.
Рассматриваемый здесь вопрос заключается в разработке соответствующих моделей для описания электронной структуры разбавленных нитридных сплавов. Для объяснения их экстремального поведения были приняты два взаимодополняющих подхода: один основан на подробных расчетах зонной структуры [14-18], другой — на экспериментально наблюдаемом эффекте противопересечения зон (BAC) [19].Эти два подхода оказались весьма успешными при описании энергий краев зон и их изменения при отжиге [20, 21]. Модель BAC также успешно применялась для интерпретации измерений фотоотражения как объемных, так и квантовых ям (QW) образцов GaNAs, идентифицируя более высокую энергетическую характеристику ( E + ), наблюдаемую в объемных образцах [19,22,23], и также обеспечивает последовательную интерпретацию энергии перехода возбужденного состояния КЯ в широком диапазоне образцов и в зависимости от гидростатического давления [24,25]. Несмотря на широкий успех модели BAC, до недавнего времени имелся один важный набор экспериментальных данных, который оставался необъяснимым, а именно наблюдаемая зависимость эффективной массы CBE от состава в сплавах Ga(In)NAs. Как модель BAC, так и подробные расчеты предсказывают увеличение массы CBE по сравнению с GaAs. Модель BAC дает хорошую оценку измеренной массы при очень низких составах N [6] (x < 0,05%), а также в индийсодержащих образцах [5], но значительно занижает массу в GaN x As 1- х для х > 0.1% [3-6]. Относительная эффективная масса электрона, m c * , теперь определена с использованием ряда различных методов, при этом наблюдается постоянная тенденция неожиданно больших значений относительной массы в GaN x As 1-x , например м е * , 0,12 и даже 0,19 для х = 0,1% [6], 1,2% [4] и 2,0% [4]. Эти измеренные значения массы обеспечивают строгую проверку любой модели, описывающей электронную структуру GaN x As 1-x и родственных сплавов.
Несмотря на широкий успех модели BAC, до недавнего времени имелся один важный набор экспериментальных данных, который оставался необъяснимым, а именно наблюдаемая зависимость эффективной массы CBE от состава в сплавах Ga(In)NAs. Как модель BAC, так и подробные расчеты предсказывают увеличение массы CBE по сравнению с GaAs. Модель BAC дает хорошую оценку измеренной массы при очень низких составах N [6] (x < 0,05%), а также в индийсодержащих образцах [5], но значительно занижает массу в GaN x As 1- х для х > 0.1% [3-6]. Относительная эффективная масса электрона, m c * , теперь определена с использованием ряда различных методов, при этом наблюдается постоянная тенденция неожиданно больших значений относительной массы в GaN x As 1-x , например м е * , 0,12 и даже 0,19 для х = 0,1% [6], 1,2% [4] и 2,0% [4]. Эти измеренные значения массы обеспечивают строгую проверку любой модели, описывающей электронную структуру GaN x As 1-x и родственных сплавов.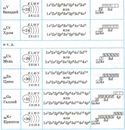
В этой главе мы рассмотрим, как эти значения массы и несколько других ранее нерешенных аспектов зонной структуры Ga(In)NxAs 1-x могут быть количественно поняты путем объединения идей и подхода эмпирической модели BAC с подробным информация, полученная в результате расчетов зонной структуры. Подход, который мы представляем, дает результаты в превосходном количественном согласии с экспериментом, обеспечивая ясное понимание наблюдаемых изменений в m e * и даже предсказывая в некоторых случаях немонотонное изменение массы с давлением.Наши результаты также ясно показывают, почему характеристика с более высокой энергией, обозначенная как E + , появляется только для x → 0,2% при измерении фотоотражения объемного GaN x As 1-x [22, 24]. Они также имеют отношение к недавнему прямому наблюдению дисперсии зоны проводимости в квантовых ямах GaN 0,0008 As 0,9992 с помощью магнитотуннельной спектроскопии [26] и обеспечивают дальнейшее понимание низких значений подвижности, обычно наблюдаемых в Ga(In)xAs 1 -х сплавов [2,27,28].
Хорошо известно, что когда одиночный атом N замещает атом As в GaAs, он образует уровень резонансного дефекта над CBE GaAs [29,30]. Этот уровень дефекта возникает из-за большой разницы в электроотрицательности и размерах атомов между N и As [31-33]. Крупный прорыв был достигнут для разбавленных нитридных сплавов с демонстрацией Валукевичем и его сотрудниками (с использованием методов гидростатического давления [19]), что уменьшение энергетической щели в Ga(In)NxAs 1-x происходит из-за взаимодействия BAC между CBE и вышележащими локализованными резонансными состояниями азота.Экспериментальные исследования сверхразбавленных нитридных сплавов показывают диапазон уровней резонансных дефектов выше CBE из-за образования комплексов N. К ним относятся, например. что атом галлия с двумя соседями N дает резонансный уровень дефекта, близкий к низкотемпературному КПЭ GaAs [23,24,30]. Подобные состояния обнаруживаются в эмпирических исследованиях псевдопотенциала [16,17] и сильной связи [34] N-комплексов. Такие расчеты подтверждают многие аспекты модели BAC, но также дают дополнительное представление о роли беспорядка и кластеризации азота в сплавах GaNA.Ниже мы покажем, что многие особенности зонной структуры разбавленных нитридных сплавов можно понять, модифицировав двухуровневую модель BAC, чтобы явно включить эффекты кластеров азота и взаимодействия между соседними атомами азота, случайно расположенными внутри сплава.
Такие расчеты подтверждают многие аспекты модели BAC, но также дают дополнительное представление о роли беспорядка и кластеризации азота в сплавах GaNA.Ниже мы покажем, что многие особенности зонной структуры разбавленных нитридных сплавов можно понять, модифицировав двухуровневую модель BAC, чтобы явно включить эффекты кластеров азота и взаимодействия между соседними атомами азота, случайно расположенными внутри сплава.
Подход, который мы используем здесь, состоит в том, чтобы сначала рассмотреть упорядоченные GaNA, анализируя информацию, которую мы получили, используя тщательно параметризованный метод сильной связи для описания электронной структуры [21,35]. Используя упорядоченные структуры, мы явно выводим двухуровневую модель BAC в разделе 11.2 для описания CBE, показывая, что концепция локализованных N резонансных состояний может оставаться справедливой даже до x ~ 0,25.
В разделе 11.3 мы обратимся к рассмотрению применения модели BAC для описания электронной структуры структур с квантовыми ямами GaNAs/GaAs. Мы представляем аналитическое выражение, с помощью которого можно рассчитать как энергию ограниченного состояния электронов, так и дисперсию зоны проводимости в структурах с квадратными квантовыми ямами Ga(In)NAs, показывая, что эти энергии ограниченного состояния очень хорошо согласуются с энергиями, полученными в результате более подробных расчетов. .Затем эту аналитическую двухуровневую модель можно использовать для обеспечения последовательного соответствия энергий перехода основного и возбужденного состояний, измеренных в широком диапазоне образцов. Аналитическая модель дает полезную информацию о нескольких аспектах поведения ограниченного состояния в гетероструктурах Ga(In)NAs/GaAs.
Мы представляем аналитическое выражение, с помощью которого можно рассчитать как энергию ограниченного состояния электронов, так и дисперсию зоны проводимости в структурах с квадратными квантовыми ямами Ga(In)NAs, показывая, что эти энергии ограниченного состояния очень хорошо согласуются с энергиями, полученными в результате более подробных расчетов. .Затем эту аналитическую двухуровневую модель можно использовать для обеспечения последовательного соответствия энергий перехода основного и возбужденного состояний, измеренных в широком диапазоне образцов. Аналитическая модель дает полезную информацию о нескольких аспектах поведения ограниченного состояния в гетероструктурах Ga(In)NAs/GaAs.
Мы используем гамильтониан сильной связи sp * s * в разделах 11.4 и 11.5, чтобы более подробно рассмотреть влияние беспорядка, исследуя, как неизбежный беспорядок в распределении N в Ga(In)NA изменяет BAC Модель и ее предсказания.В разделе 11.4 мы показываем, что даже в неупорядоченном сплаве изгиб запрещенной зоны и зависимость E – от состава могут быть очень точно описаны моделью BAC, но теперь BAC явно рассматривает случайное распределение N резонансных состояний. [34]. Затем мы расширим анализ в разделе 11.5, чтобы показать, что включение эффектов беспорядка может дать количественное понимание измеренного изменения эффективной массы с x в Ga(In)NxAs 1-x и поведения E + уровень в композициях с очень низким содержанием азота ( x → 0.2%) [36].
[34]. Затем мы расширим анализ в разделе 11.5, чтобы показать, что включение эффектов беспорядка может дать количественное понимание измеренного изменения эффективной массы с x в Ga(In)NxAs 1-x и поведения E + уровень в композициях с очень низким содержанием азота ( x → 0.2%) [36].
Мы меняем направление в разделе 11.6, чтобы рассмотреть, в частности, последствия сильного искривления запрещенной зоны для подвижности электронов в разбавленных нитридных полупроводниках. Мы показываем фундаментальную связь между энергией CBE и сечением рассеяния носителей n-типа в ультраразбавленном пределе, накладывая общие ограничения на подвижность носителей в таких сплавах [28,37]. В приближении независимого рассеяния подвижность носителей оценивается в ~ 1000 см 2 /В с при концентрации атомов N 1 %, что сравнимо с максимальной измеренной подвижностью в высококачественных образцах GaInNA при этих концентрациях N, но выше чем во многих образцах.
