8 класс. Химия. Электронная оболочка атома – Электронная оболочка атома
Комментарии преподавателяСостояние электронов в атоме
Выдающийся датский физик Нильс Бор (Рис. 1) предположил, что электроны в атоме могут двигаться не по любым, а по строго определенным орбитам.
Рис. 1. Бор Нильс Хендрих Давид (1885–1962)
При этом электроны в атоме различаются своей энергией. Как показывают опыты, одни из них притягиваются к ядру сильнее, другие – слабее. Главная причина этого заключается в разном удалении электронов от ядра атома. Чем ближе электроны к ядру, тем они прочнее связаны с ним и их труднее вырвать из электронной оболочки. Таким образом, по мере удаления от ядра атома запас энергии электрона увеличивается.
Электроны, движущиеся вблизи ядра, как бы загораживают (экранируют) ядро от других электронов, которые притягиваются к ядру слабее и движутся на большем удалении от него. Так образуются электронные слои.
Каждый электронный слой состоит из электронов с близкими значениями энергии; поэтому электронные слои называют еще энергетическими уровнями.
Правила распределения электронов
Ядро находится в центре атома каждого элемента, а электроны, образующие электронную оболочку, размещаются вокруг ядра слоями.
Число электронных слоев в атоме элемента равно номеру периода, в котором находится данный элемент.
Например, натрий Na – элемент 3-го периода, значит, его электронная оболочка включает 3 энергетических уровня. В атоме брома Br – 4 энергетических уровня, т. к. бром расположен в 4-м периоде (Рис. 2).
Модель атома натрия: Модель атома брома:
Рис. 2. Модели строения электронных оболочек атомов натрия и брома
Максимальное число электронов на энергетическом уровне рассчитывается по формуле: 2n2, где n – номер энергетического уровня.
Таким образом, максимальное число электронов на:
1 слое – 2
2 слое – 8
3 слое – 18 и т. д.
У элементов главных подгрупп номер группы, к которой относится элемент, равен числу внешних электронов атома.
Внешними называют электроны последнего электронного слоя.
Например, в атоме натрия – 1 внешний электрон (т. к. это элемент IА подгруппы). В атоме брома – 7 электронов на последнем электронном слое (это элемент VIIА подгруппы).
Строение электронных оболочек элементов 1–3 периодов
В атоме водорода заряд ядра равен +1, и этот заряд нейтрализуется единственным электроном (Рис. 3).
Рис. 3. Схема строения атома водорода
Следующий за водородом элемент – гелий, тоже элемент 1-го периода. Следовательно, в атоме гелия 1 энергетический уровень, на котором размещаются два электрона (Рис. 4). Это максимально возможное число электронов для первого энергетического уровня.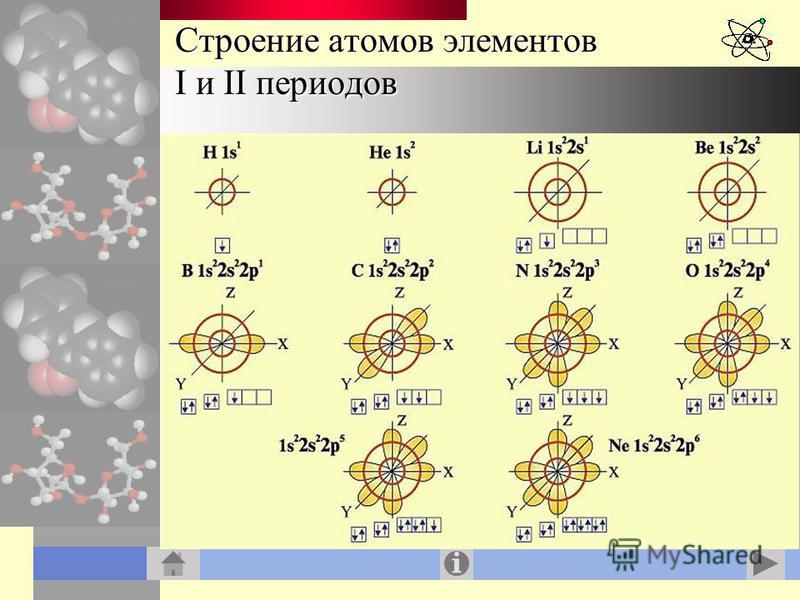
Рис 4. Схема строения атома гелия
Элемент № 3 – это литий. В атоме лития 2 электронных слоя, т. к. это элемент 2-го периода. На 1 слое в атоме лития находится 2 электрона (этот слой завершен), а на 2 слое –1 электрон. В атоме бериллия на 1 электрон больше, чем в атоме лития (Рис. 5).
Рис. 5. Схемы строения атомов лития и бериллия
Аналогично можно изобразить схемы строения атомов остальных элементов второго периода (Рис. 6).
Рис. 6. Схемы строения атомов некоторых элементов второго периода
В атоме последнего элемента второго периода – неона – последний энергетический уровень является завершенным (на нем 8 электронов, что соответствует максимальному значению для 2-го слоя). Неон – инертный газ, который не вступает в химические реакции, следовательно, его электронная оболочка очень устойчива.
Американский химик Гилберт Льюис дал объяснение этому и выдвинул правило октета, в соответствии с которым устойчивым является восьмиэлектронный слой (за исключением 1 слоя: т. к. на нем может находиться не более 2 электронов, устойчивым для него будет двухэлектронное состояние).
к. на нем может находиться не более 2 электронов, устойчивым для него будет двухэлектронное состояние).
После неона следует элемент 3-го периода – натрий. В атоме натрия – 3 электронных слоя, на которых расположены 11 электронов (Рис. 7).
Na
Рис. 7. Схема строения атома натрия
Натрий находится в 1 группе, его валентность в соединениях равна I, как и у лития. Это связано с тем, что на внешнем электронном слое атомов натрия и лития находится 1 электрон.
Свойства элементов периодически повторяются потому, что у атомов элементов периодически повторяется число электронов на внешнем электронном слое.
Строение атомов остальных элементов третьего периода можно представить по аналогии со строением атомов элементов 2-го периода.
Строение электронных оболочек элементов 4 периода
Четвертый период включает в себя 18 элементов, среди них есть элементы как главной (А), так и побочной (В) подгрупп. Особенностью строения атомов элементов побочных подгрупп является то, что у них последовательно заполняются предвнешние (внутренние), а не внешние электронные слои.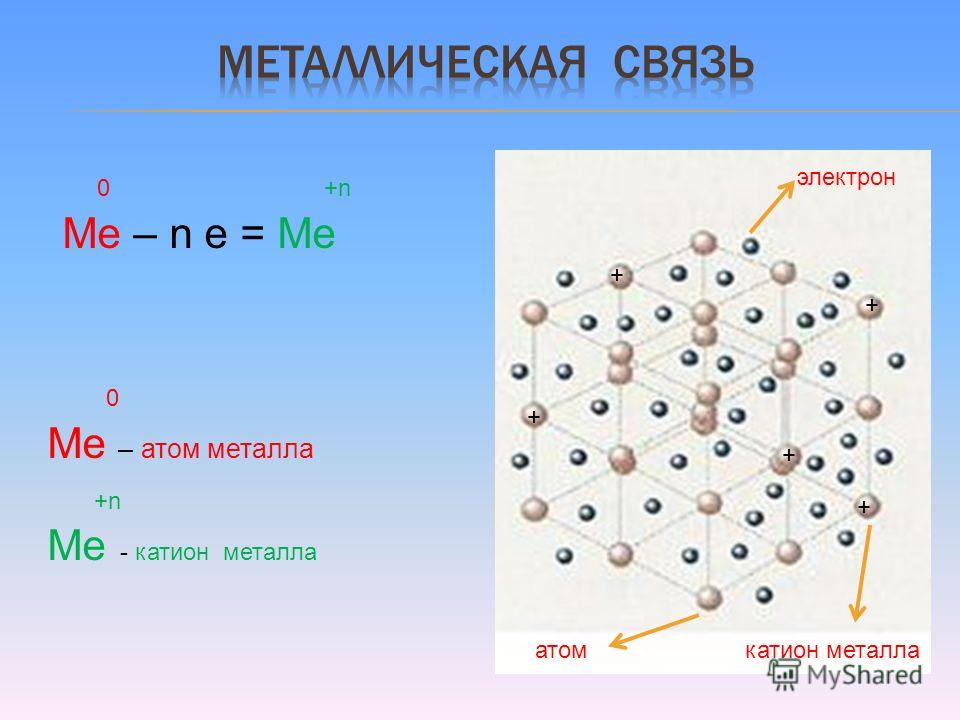
Четвертый период начинается с калия. Калий – щелочной металл, проявляющий в соединениях валентность I. Это вполне согласуется со следующим строением его атома. Как элемент 4-го периода, атом калия имеет 4 электронных слоя. На последнем (четвертом) электронном слое калия находится 1 электрон, общее количество электронов в атоме калия равно 19 (порядковому номеру этого элемента) (Рис. 8).
Рис. 8. Схема строения атома калия
Следующий за кальцием элемент – скандий. Это элемент побочной (В) подгруппы. Все элементы побочных подгрупп – это металлы. Особенностью строения их атомов является наличие не более 2-х электронов на последнем электронном слое, т. е. последовательно заполняться электронами будет предпоследний электронный слой.
Так, для скандия можно представить следующую модель строения атома (Рис.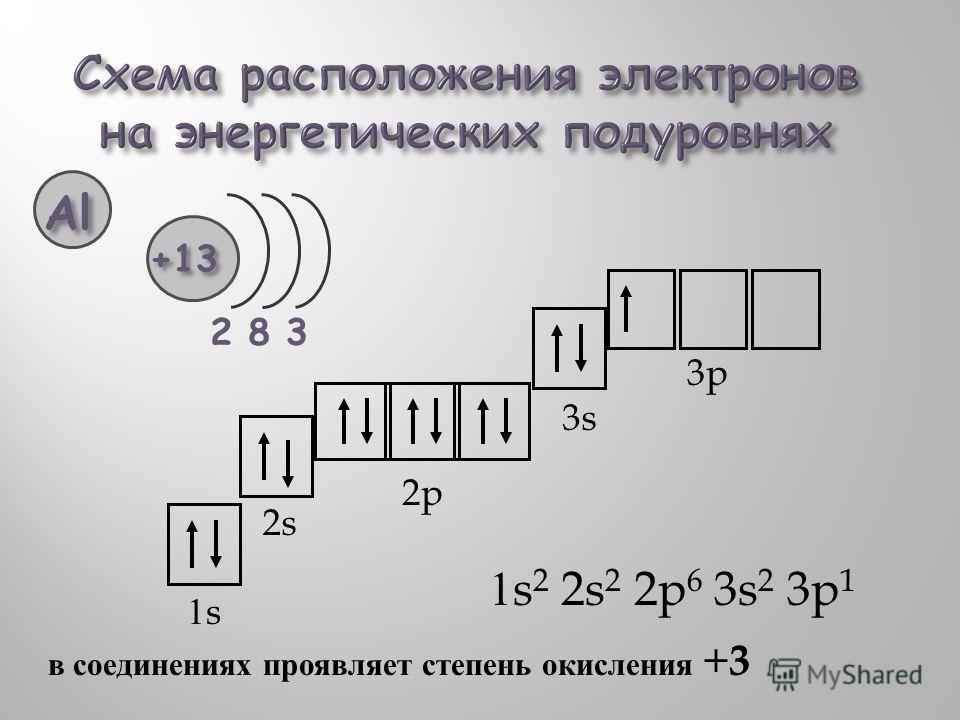
Рис. 9. Схема строения атома скандия
Такое распределение электронов возможно, т. к. на третьем слое максимально допустимое количество электронов – 18, т. е. восемь электронов на 3-м слое – это устойчивое, но не завершенное состояние слоя.
У десяти элементов побочных подгрупп 4-го периода от скандия до цинка последовательно заполняется третий электронный слой.
Схему строения атома цинка можно представить так: на внешнем электронном слое – два электрона, на предвнешнем – 18 (Рис. 10).
Рис. 10. Схема строения атома цинка
Следующие за цинком элементы относятся к элементам главной подгруппы: галлий, германий и т. д. до криптона. В атомах этих элементов последовательно заполняется 4-й (т. е. внешний) электронный слой. В атоме инертного газа криптона будет октет на внешней оболочке, т. е. устойчивое состояние.
Подведение итога урока
На этом уроке вы узнали, как устроена электронная оболочка атома и как объяснить явление периодичности. Познакомились с моделями строения электронных оболочек атомов, с помощью которых можно предсказать и объяснить свойства химических элементов и их соединений.
Познакомились с моделями строения электронных оболочек атомов, с помощью которых можно предсказать и объяснить свойства химических элементов и их соединений.
Источники
http://www.youtube.com/watch?t=7&v=xgPDyORYV_Q
http://www.youtube.com/watch?v=RNu0Ql4Htjg
http://www.youtube.com/watch?v=8h3nw8m3x6k
заставка http://www.youtube.com/watch?v=z0Muwg71Rmc
источник презентации – http://www.myshared.ru/slide/834600/#
Конспект http://interneturok.ru/ru/school/chemistry/8-klass
Бром
| Бром | |
|---|---|
| Атомный номер | 35 |
| Внешний вид простого вещества | красно-бурая жидкость с сильным неприятным запахом |
| Свойства атома | |
|
Атомная масса (молярная масса) |
79,904 а. е. м. (г/моль) е. м. (г/моль) |
| Радиус атома | n/a пм |
|
Энергия ионизации (первый электрон) |
1142,0 (11,84) кДж/моль (эВ) |
| Электронная конфигурация | |
| Химические свойства | |
| Ковалентный радиус | 114 пм |
| Радиус иона | (+5e)47 (-1e)196 пм |
|
Электроотрицательность (по Полингу) |
2,96 |
| Электродный потенциал | 0 |
| Степени окисления | 7, 5, 3, 1, -1 |
| Термодинамические свойства простого вещества | |
| Плотность | 3,12 г/см³ |
| Молярная теплоёмкость | 75,69 Дж/(K·моль) |
| Теплопроводность | 0,005 Вт/(м·K) |
| Температура плавления | 265,9 K |
| Теплота плавления | (Br—Br) 10,57 кДж/моль |
| Температура кипения | 331,9 K |
| Теплота испарения | (Br—Br) 29,56 кДж/моль |
| Молярный объём | 23,5 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | орторомбическая |
| Параметры решётки | a=6,67 b=4,48 c=8,72 Å |
| Отношение c/a | — |
| Температура Дебая | n/a K |
| Br | 35 |
| 79,904 | |
| [Ar]3d104s24p5 | |
| Бром | |
Бром — элемент главной подгруппы седьмой группы четвёртого периода периодической системы химических элементов Д.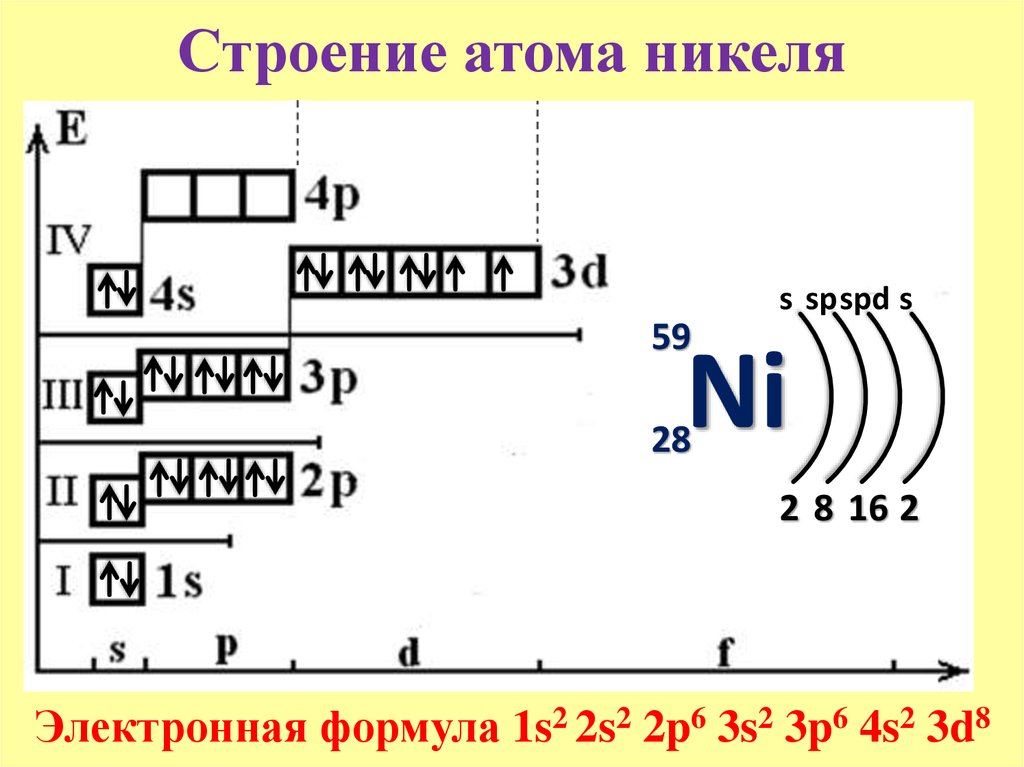 И. Менделеева, атомный номер 35. Обозначается символом Br (лат. Bromum). Химически активный неметалл, относится к группе галогенов. Простое вещество бром (CAS-номер: 7726-95-6) при нормальных условиях — тяжёлая жидкость красно-бурого цвета с сильным неприятным запахом. Молекула брома двухатомна (формула Br2).
И. Менделеева, атомный номер 35. Обозначается символом Br (лат. Bromum). Химически активный неметалл, относится к группе галогенов. Простое вещество бром (CAS-номер: 7726-95-6) при нормальных условиях — тяжёлая жидкость красно-бурого цвета с сильным неприятным запахом. Молекула брома двухатомна (формула Br2).
История
Схема атома брома
Бром был открыт в 1826 году молодым преподавателем колледжа города Монпелье А. Ж. Баларом. Открытие Балара сделало его имя известным всему миру. Из одной популярной книги в другую кочует утверждение, что огорченный тем, что в открытии брома никому неизвестный Антуан Балар опередил самого Юстуса Либиха, Либих воскликнул, что, дескать, не Балар открыл бром, а бром открыл Балара. Однако это неправда, или, точнее, не совсем правда. Фраза-то была, но принадлежала она не Ю. Либиху, а Шарлю Жерару, который очень хотел, чтобы кафедру химии в Сорбонне занял Огюст Лоран, а не избранный на должность профессора А. Балар.
Балар.
Происхождение названия
Название элемента происходит βρῶμος — зловоние.
Получение
Бром получают химическим путём из рассола Br–:
Физические свойства
При обычных условиях бром — красно-бурая жидкость с резким неприятным запахом, ядовит, при соприкосновении с кожей образуются ожоги. Плотность при 0 °C — 3, 19 г./см³. Температура плавления (затвердевания) брома −7,2 °C, кипения 58,8 °C, при кипении бром превращается из жидкости в буро-коричневые пары, при вдыхании раздражающие дыхательные пути. Стандартный электродный потенциал Br²/Вr– в водном растворе равен +1,065 В.
Обычный бром состоит из изотопов 79Br (50,56 %) и 81Br (49,44 %). Искусственно получены радиоактивные изотопы.
Химические свойства
В свободном виде существует в виде двухатомных молекул Br2. Заметная диссоциация молекул на атомы наблюдается при температуре 800 °C и быстро возрастает при дальнейшем росте температуры. Диаметр молекулы Br2 равен 0,323 нм, межъядерное расстояние в этой молекуле — 0,228 нм.
Диаметр молекулы Br2 равен 0,323 нм, межъядерное расстояние в этой молекуле — 0,228 нм.
Бром немного, но лучше других галогенов растворим в воде (3,58 г в 100 г воды при 20 °C), раствор называют бромной водой. В бромной воде протекает реакция с образованием бромоводородной и неустойчивой бромноватистой кислот:
Br2 + H2O → HBr + HBrO.
С большинством органических растворителей бром смешивается во всех отношениях, при этом часто происходит бромирование молекул органических растворителей.
По химической активности бром занимает промежуточное положение между хлором и иодом. При реакции брома с растворами иодидов выделяется свободный иод:
Br2 + 2KI → I2↓ + 2KBr.
Напротив, при действии хлора на бромиды, находящиеся в водных растворах, выделяется свободный бром:
Cl2 + 2NaBr → Br2 + 2NaCl.
При реакции брома с серой образуется S2Br2, при реакции брома с фосфором — PBr3 и PBr5. Бром реагирует также с неметаллами селеном и теллуром.
Бром реагирует также с неметаллами селеном и теллуром.
Реакция брома с водородом протекает при нагревании и приводит к образованию бромоводорода HBr. Раствор HBr в воде — это бромоводородная кислота, по силе близкая к соляной кислоте HCl. Соли бромоводородной кислоты — бромиды (NaBr, MgBr2, AlBr3 и др.). Качественная реакция на присутствие бромид-ионов в растворе — образование с ионами Ag+ светло-желтого осадка бромида серебра AgBr, практически нерастворимого в воде.
С кислородом и азотом бром непосредственно не реагирует. Бром образует большое число различных соединений с остальными галогенами. Например, со фтором бром образует неустойчивые BrF3 и BrF5, с иодом — IBr. При взаимодействии со многими металлами бром образует бромиды, например, AlBr3, CuBr2, MgBr2 и др. Устойчивы к действию брома тантал и платина, в меньшей степени — серебро, титан и свинец.
Бром — сильный окислитель, он окисляет сульфит-ион до сульфата, нитрит-ион — до нитрата и т. д.
д.
При взаимодействии с органическими соединениями, содержащими двойную связь, бром присоединяется, давая соответствующие дибромпроизводные:
C2H4 + Br2 → C2H4Br2.
Присоединяется бром и к органическим молекулам, в составе которых есть тройная связь. Обесцвечивание бромной воды при пропускании через нее газа или добавлении к ней жидкости свидетельствует о том, что в газе или в жидкости присутствует непредельное соединение.
При нагревании в присутствии катализатора бром реагирует с бензолом с образованием бромбензола C6H5Br (реакция замещения).
При взаимодействии брома с растворами щелочей и с растворами карбонатов натрия или калия образуются соответствующие бромиды и броматы, например:
3Br2 + 3Na2CO3 → 5NaBr + NaBrO3+ 3CO2↑.
Бромсодержащие кислоты
Помимо бескислородной бромоводородной кислоты HBr, бром образует ряд кислородных кислот: бромную HBrO4, бромноватую HBrO3, бромистую HBrO2, бромноватистую HBrO.
Применение
В химии
Вещества на основе брома широко применяются в основном органическом синтезе.
В технике
— Бромид серебра AgBr применяется в фотографии как светочувствительное вещество.
— Используется для создания антипиренов — добавок, придающих пожароустойчивость пластикам, древесине, текстильным материалам.
— Пентафторид брома иногда используется как очень мощный окислитель ракетного топлива.
— 1,2-дибромэтан в настоящее время применяют как антидетонирующую добавку в моторном топливе, взамен тетраэтилсвинца.
— Растворы бромидов используются в нефтедобыче.
В медицине
В медицине бромид натрия и бромид калия применяют как успокаивающие средства.
В производстве оружия
Со времен Первой Мировой войны бром используется для производства боевых отравляющих веществ.
Физиологическое действие
Уже при содержании брома в воздухе в концентрации около 0,001 % (по объёму) наблюдается раздражение слизистых оболочек, головокружение, а при более высоких концентрациях — спазмы дыхательных путей, удушье. ПДК паров брома 0,5 мг/м³. При попадании в организм токсическая доза составляет 3 г, летальная — от 35 г. При отравлении парами брома пострадавшего нужно немедленно вывести на свежий воздух; для восстановления дыхания можно на небольшое время пользоваться тампоном, смоченным нашатырным спиртом, на короткое время периодически поднося его к носу пострадавшего. Дальнейшее лечение должно проводиться под наблюдением врача. Жидкий бром при попадании на кожу вызывает болезненные ожоги.
ПДК паров брома 0,5 мг/м³. При попадании в организм токсическая доза составляет 3 г, летальная — от 35 г. При отравлении парами брома пострадавшего нужно немедленно вывести на свежий воздух; для восстановления дыхания можно на небольшое время пользоваться тампоном, смоченным нашатырным спиртом, на короткое время периодически поднося его к носу пострадавшего. Дальнейшее лечение должно проводиться под наблюдением врача. Жидкий бром при попадании на кожу вызывает болезненные ожоги.
Особенности работы
При работе с бромом следует пользоваться защитной спецодеждой, противогазом, специальными перчатками. Из-за высокой химической активности и токсичности, как паров брома, так и жидкого брома его следует хранить в стеклянной, плотно укупоренной толстостенной посуде. Склянки с бромом располагают в ёмкостях с песком, который предохраняет склянки от разрушения при встряхивании. Из-за высокой плотности брома склянки с ним ни в коем случае нельзя брать только за горло (горло может оторваться, и тогда бром окажется на полу).
Для нейтрализации пролитого брома поверхность с ним надо залить раствором сульфита натрия Na2SO3
Мифы и легенды
Существует широко распространенная легенда о том, что в армии будто бы добавляют бром в еду для снижения полового влечения. Этот миф не имеет под собой никаких оснований — влечение успешно снижают физические нагрузки, а действительно добавляемые в еду добавки чаще всего оказываются аскорбиновой кислотой для предотвращения авитаминоза. К тому же, препараты брома соленые на вкус и не влияют ни на влечение, ни на потенцию. Они обладают снотворным и успокаивающим эффектом.
Бром, свойства атома, химические и физические свойства
Бром, свойства атома, химические и физические свойства.
Br 35 Бром
79,901-79,907* 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p5
Бром — элемент периодической системы химических элементов Д. И. Менделеева с атомным номером 35. Расположен в 17-й группе (по старой классификации — главной подгруппе седьмой группы), четвертом периоде периодической системы.
И. Менделеева с атомным номером 35. Расположен в 17-й группе (по старой классификации — главной подгруппе седьмой группы), четвертом периоде периодической системы.
Атом и молекула брома. Формула брома. Строение атома брома
Изотопы и модификации брома
Свойства брома (таблица): температура, плотность, давление и пр.
Физические свойства брома
Химические свойства брома. Взаимодействие брома. Химические реакции с бромом
Получение брома
Применение брома
Таблица химических элементов Д.И. Менделеева
Атом и молекула брома. Формула брома. Строение атома брома:
Бром (лат. Bromum, от др.-греч. βρῶμος – «дурной запах, зловоние») – химический элемент периодической системы химических элементов Д. И. Менделеева с обозначением Br и атомным номером 35. Расположен в 17-й группе (по старой классификации – главной подгруппе седьмой группы), четвертом периоде периодической системы.
Бром – неметалл. Относится к группе галогенов.
Бром обозначается символом Br.
Как простое вещество бром при нормальных условиях представляет собой тяжёлую едкую жидкость красно-бурого цвета с сильным неприятным «тяжёлым» запахом, отдалённо напоминающим запах одновременно йода и хлора. Бром – летучее вещество. Бром является единственным жидким неметаллом при нормальных условиях.
Молекула брома двухатомна.
Химическая формула брома Br2.
Электронная конфигурация атома брома 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p5. Потенциал ионизации (первый электрон) атома брома равен 1139,86 кДж/моль (11,81381(6) эВ).
Строение атома брома. Атом брома состоит из положительно заряженного ядра (+35), вокруг которого по четырем оболочкам движутся 35 электронов. При этом 28 электронов находятся на внутреннем уровне, а 7 электронов – на внешнем. Поскольку бром расположен в четвертом периоде, оболочек всего четыре. Первая – внутренняя оболочка представлена s-орбиталью. Вторая – внутренняя оболочка представлены s- и р-орбиталями. Третья – внутренняя оболочка представлена s-, р- и d-орбиталями. Четвертая – внешняя оболочка представлена s- и р-орбиталями. На внешнем энергетическом уровне атома брома на 4s-орбитали находятся два спаренных электрона, на 4p-орбитали – четыре спаренных и один неспаренный электрон. В свою очередь ядро атома брома состоит из 35 протонов и 45 нейтронов. Бром относится к элементам p-семейства.
Радиус атома брома (вычисленный) составляет 94 пм.
Атомная масса атома брома составляет 79,901-79,907 а. е. м.
м.
Бром – химически активный неметалл. Ядовит.
Бром, свойства атома, химические и физические свойства
Изотопы и модификации брома:
Свойства брома (таблица): температура, плотность, давление и пр.:
Подробные сведения на сайте ChemicalStudy.ru
| 100 | Общие сведения | |
| 101 | Название | Бром |
| 102 | Прежнее название | |
| 103 | Латинское название | Bromum |
| 104 | Английское название | Bromine |
| 105 | Символ | Br |
| 106 | Атомный номер (номер в таблице) | 35 |
| 107 | Тип | Неметалл |
| 108 | Группа | Галоген |
| 109 | Открыт | Карл Якоб Лёвих, Германия, 1825 г. , Антуан Жером Балар, Франция, 1826 г. , Антуан Жером Балар, Франция, 1826 г. |
| 110 | Год открытия | 1825 г. |
| 111 | Внешний вид и пр. | Красно-бурая жидкость с сильным неприятным, «тяжёлым» запахом. Летуч, ядовит |
| 112 | Происхождение | Природный материал |
| 113 | Модификации | |
| 114 | Аллотропные модификации | |
| 115 | Температура и иные условия перехода аллотропных модификаций друг в друга | |
| 116 | Конденсат Бозе-Эйнштейна | |
| 117 | Двумерные материалы | |
| 118 | Содержание в атмосфере и воздухе (по массе) | 0 % |
| 119 | Содержание в земной коре (по массе) | 0,0003 % |
| 120 | Содержание в морях и океанах (по массе) | 0,0067 % |
| 121 | Содержание во Вселенной и космосе (по массе) | 7,0·10-7 % |
| 122 | Содержание в Солнце (по массе) | |
| 123 | Содержание в метеоритах (по массе) | 0,00012 % |
| 124 | Содержание в организме человека (по массе) | 0,00029 % |
| 200 | Свойства атома | |
| 201 | Атомная масса (молярная масса)* | 79,901-79,907 а. е. м. (г/моль) е. м. (г/моль) |
| 202 | Электронная конфигурация | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p5 |
| 203 | Электронная оболочка | K2 L8 M18 N7 O0 P0 Q0 R0
|
| 204 | Радиус атома (вычисленный) | 94 пм |
| 205 | Эмпирический радиус атома* | 115 пм |
| 206 | Ковалентный радиус* | 120 пм |
| 207 | Радиус иона (кристаллический) | Br– 182 (6) пм, Br7+ 53 (6) пм (в скобках указано координационное число – характеристика, которая определяет число ближайших частиц (ионов или атомов) в молекуле или кристалле) |
| 208 | Радиус Ван-дер-Ваальса | 185 пм |
| 209 | Электроны, Протоны, Нейтроны | 35 электронов, 35 протонов, 45 нейтронов |
| 210 | Семейство (блок) | элемент p-семейства |
| 211 | Период в периодической таблице | 4 |
| 212 | Группа в периодической таблице | 17-ая группа (по старой классификации – главная подгруппа 7-ой группы) |
| 213 | Эмиссионный спектр излучения | |
| 300 | Химические свойства | |
| 301 | Степени окисления | -1, 0, +1, +3, +4, +5, +7 |
| 302 | Валентность | I, III, V, VII |
| 303 | Электроотрицательность | 2,96 (шкала Полинга) |
| 304 | Энергия ионизации (первый электрон) | 1139,86 кДж/моль (11,81381(6) эВ) |
| 305 | Электродный потенциал | Br2 + 2e– → 2Br–, Eo = +1,065 В, Br3– + 2e– → 3Br–, Eo = +1,05 В |
| 306 | Энергия сродства атома к электрону | 324,5369(3) кДж/моль (3,363588(3) эВ) |
| 400 | Физические свойства | |
| 401 | Плотность | 3,4 г/см3 (при -7,3 °C и иных стандартных условиях, состояние вещества – твердое тело), 3,1193 г/см3 (при 20 °C и иных стандартных условиях, состояние вещества – жидкость), 3,102 г/см3 (при 25 °C и иных стандартных условиях, состояние вещества – жидкость), 3,0848 , г/см3 (при 30 °C и иных стандартных условиях, состояние вещества – жидкость) |
| 402 | Температура плавления* | -7,2 °C (265,8 K, 19 °F) |
| 403 | Температура кипения* | 58,8 °C (332,0 K, 137,8 °F) |
| 404 | Температура сублимации | |
| 405 | Температура разложения | |
| 406 | Температура самовоспламенения смеси газа с воздухом | |
| 407 | Удельная теплота плавления (энтальпия плавления ΔHпл)* | 10,571 кДж/моль |
| 408 | Удельная теплота испарения (энтальпия кипения ΔHкип)* | 29,96 кДж/моль |
| 409 | Удельная теплоемкость при постоянном давлении | |
| 410 | Молярная теплоёмкость* | 75,69 Дж/(K·моль) |
| 411 | Молярный объём | 25,610256 см³/моль |
| 412 | Теплопроводность | 0,122 Вт/(м·К) (при стандартных условиях), 0,005 Вт/(м·К) (при 300 K) |
| 500 | Кристаллическая решётка | |
| 511 | Кристаллическая решётка #1 | |
| 512 | Структура решётки | Орторомбическая
|
| 513 | Параметры решётки | a = 6,67 Å, b = 4,48 Å, c = 8,72 Å |
| 514 | Отношение c/a | |
| 515 | Температура Дебая | |
| 516 | Название пространственной группы симметрии | Cmca |
| 517 | Номер пространственной группы симметрии | 64 |
| 900 | Дополнительные сведения | |
| 901 | Номер CAS | 7726-95-6 |
Примечание:
201* Указан диапазон значений атомной массы в связи с различной распространённостью изотопов данного элемента в природе.
205* Эмпирический радиус атома брома согласно [1] составляет 120 пм.
206* Ковалентный радиус брома согласно [1] и [3] составляет 120±3 пм и 114 пм соответственно.
402* Температура плавления брома согласно [3] и [4] составляет -7,25 °С (265,9 K, 18,95 °F).
403* Температура кипения брома согласно [3] составляет 58,6 °С (331,9 K, 137,48 °F).
407* Удельная теплота плавления (энтальпия плавления ΔHпл) брома согласно [3] и [4] составляет 10,57 кДж/моль и 9,44 кДж/моль соответственно.
408* Удельная теплота испарения (энтальпия кипения ΔHкип) брома согласно [3] и [4] составляет 29,56 кДж/моль и 29,5 кДж/моль соответственно.
410* Молярная теплоёмкость брома согласно [3] составляет 75,69 Дж/(K·моль).
Физические свойства брома:
Химические свойства брома. Взаимодействие брома. Химические реакции с бромом:
Получение брома:
Применение брома:
Таблица химических элементов Д. И. Менделеева
И. Менделеева
- 1. Водород
- 2. Гелий
- 3. Литий
- 4. Бериллий
- 5. Бор
- 6. Углерод
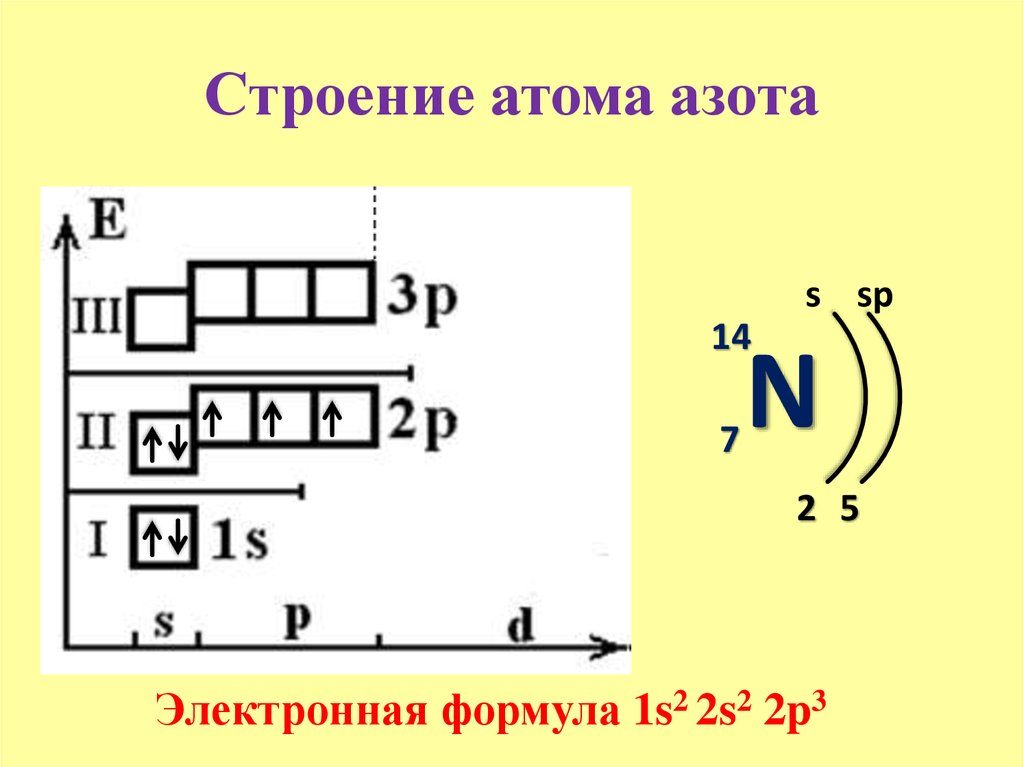
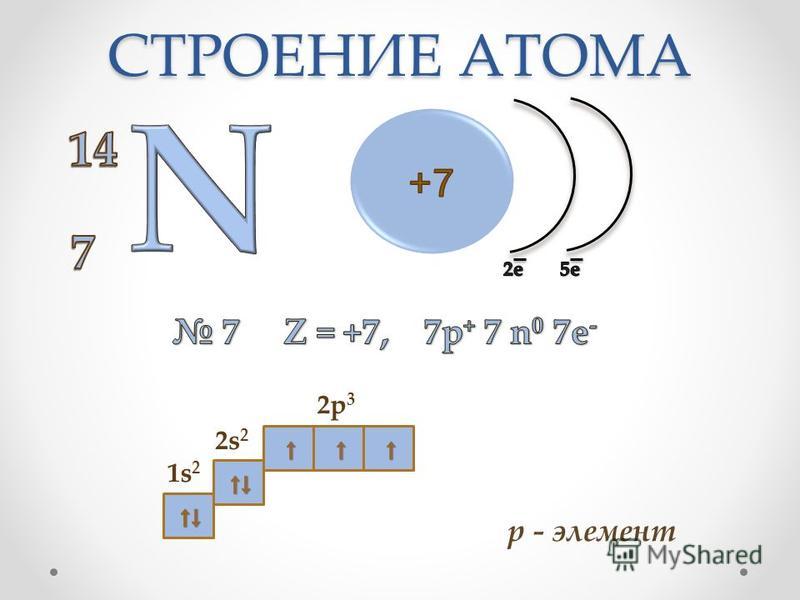
- 7. Азот
- 8. Кислород
- 9. Фтор
- 10. Неон
- 11. Натрий
- 12. Магний
- 13. Алюминий
- 14. Кремний
- 15. Фосфор
- 16. Сера
- 17. Хлор
- 18. Аргон
- 19. Калий
- 20. Кальций
- 21. Скандий
- 22. Титан
- 23. Ванадий
- 24. Хром
- 25. Марганец
- 26. Железо
- 27. Кобальт
- 28. Никель
- 29. Медь
- 30. Цинк
- 31. Галлий
- 32. Германий
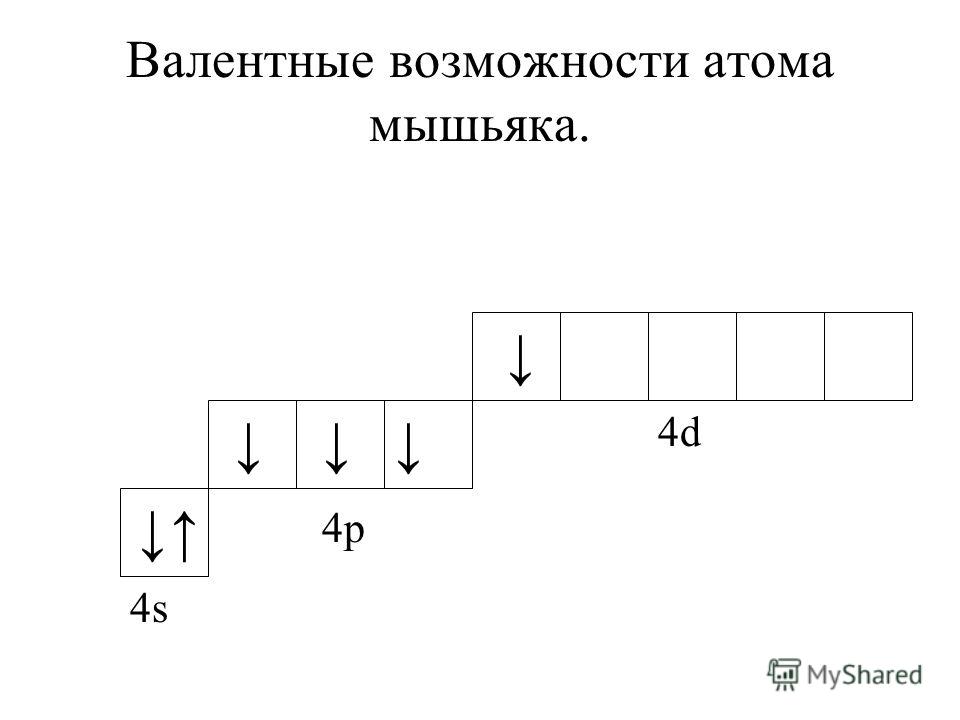
- 33. Мышьяк
- 34.
 Селен
Селен - 35. Бром
- 36. Криптон
- 37. Рубидий
- 38. Стронций
- 39. Иттрий
- 40. Цирконий
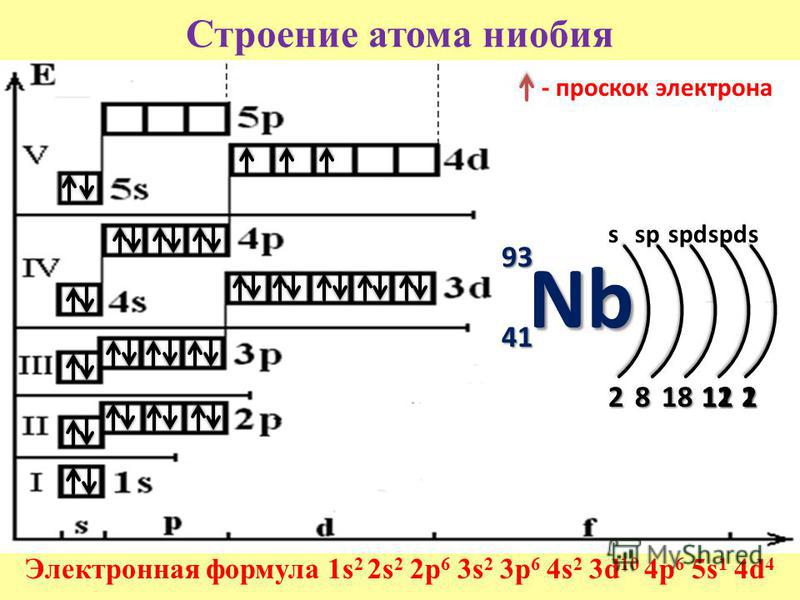
- 41. Ниобий
- 42. Молибден
- 43. Технеций
- 44. Рутений
- 45. Родий
- 46. Палладий
- 47. Серебро
- 48. Кадмий
- 49. Индий
- 50. Олово
- 51. Сурьма
- 52. Теллур
- 53. Йод
- 54. Ксенон
- 55. Цезий
- 56. Барий
- 57. Лантан
- 58. Церий
- 59. Празеодим
- 60. Неодим
- 61. Прометий
- 62. Самарий
- 63. Европий
- 64. Гадолиний
- 65. Тербий
- 66. Диспрозий
- 67.
 Гольмий
Гольмий - 68. Эрбий
- 69. Тулий
- 70. Иттербий
- 71. Лютеций
- 72. Гафний
- 73. Тантал
- 74. Вольфрам
- 75. Рений
- 76. Осмий
- 77. Иридий
- 78. Платина
- 79. Золото
- 80. Ртуть
- 81. Таллий
- 82. Свинец
- 83. Висмут
- 84. Полоний
- 85. Астат
- 86. Радон
- 87. Франций
- 88. Радий
- 89. Актиний
- 90. Торий
- 91. Протактиний
- 92. Уран
- 93. Нептуний
- 94. Плутоний
- 95. Америций
- 96. Кюрий
- 97. Берклий
- 98. Калифорний
- 99. Эйнштейний
- 100.
 Фермий
Фермий - 101. Менделеевий
- 102. Нобелий
- 103. Лоуренсий
- 104. Резерфордий
- 105. Дубний
- 106. Сиборгий
- 107. Борий
- 108. Хассий
- 109. Мейтнерий
- 110. Дармштадтий
- 111. Рентгений
- 112. Коперниций
- 113. Нихоний
- 114. Флеровий
- 115. Московий
- 116. Ливерморий
- 117. Теннессин
- 118. Оганесон
Таблица химических элементов Д.И. Менделеева
Источники:
- https://en.wikipedia.org/wiki/Bromine
- https://de.wikipedia.org/wiki/Brom
- https://ru.wikipedia.org/wiki/Бром
- http://chemister.ru/Database/properties.php?dbid=1&id=245
- https://chemicalstudy.ru/brom-svoystva-atoma-himicheskie-i-fizicheskie-svoystva/
Примечание: © Фото https://www. pexels.com, https://pixabay.com
pexels.com, https://pixabay.com
бром атомная масса степень окисления валентность плотность температура кипения плавления физические химические свойства структура теплопроводность электропроводность кристаллическая решетка
атом нарисовать строение число протонов в ядре строение электронных оболочек электронная формула конфигурация схема строения электронной оболочки заряд ядра состав масса орбита уровни модель радиус энергия электрона переход скорость спектр длина волны молекулярная масса объем атома
электронные формулы сколько атомов в молекуле брома
сколько электронов в атоме свойства металлические неметаллические термодинамические
Коэффициент востребованности 2 635
Bromine Bohr Model – Как нарисовать диаграмму Бора для атома брома (Br)
Главная > Bromine Bohr model
Боровская модель брома (Br) имеет ядро, которое содержит 45 нейтронов и 35 протонов. Это ядро окружено четырехэлектронными оболочками, называемыми K-оболочкой, L-оболочкой, М-оболочкой и N-оболочкой. Самая внешняя оболочка на диаграмме Бора брома содержит 7 электронов, которые также называются валентными электронами.
Это ядро окружено четырехэлектронными оболочками, называемыми K-оболочкой, L-оболочкой, М-оболочкой и N-оболочкой. Самая внешняя оболочка на диаграмме Бора брома содержит 7 электронов, которые также называются валентными электронами.
| Имя | Bromine Bohr Model |
| Number of neutrons | 45 |
| Number of protons | 35 |
| Number of electrons | 35 |
| Всего электронных оболочек | 4 |
| Электрон на первой оболочке (K) | 2 |
| Electrons in the Second shell(L) | 8 |
| Electrons in the Third shell(M) | 18 |
| Electrons in the Четвертая оболочка (n) | 7 |
| Общая валентная электроны в броме | 7 |
Модель Bohr Описывает модель визуализации. В нем использовались разные электронные оболочки, такие как K, L, M, N… и так далее. Эти оболочки содержат определенное количество электронов, электронная оболочка, ближайшая к ядру, имеет меньшую энергию, а электронная оболочка, наиболее удаленная от ядра, имеет большую энергию.
В нем использовались разные электронные оболочки, такие как K, L, M, N… и так далее. Эти оболочки содержат определенное количество электронов, электронная оболочка, ближайшая к ядру, имеет меньшую энергию, а электронная оболочка, наиболее удаленная от ядра, имеет большую энергию.
Диаграмма Бора очень интересна и легко рисуется. Здесь мы нарисуем диаграмму Бора атома брома с помощью нескольких простых шагов.
Этапы рисования Боровской модели атома брома1. Найдите количество протонов, электронов и нейтронов в атоме брома
Протоны — положительно заряженные частицы, нейтроны — незаряженные частицы, обе они составляющие ядра атома. Электроны — это отрицательно заряженные частицы, вращающиеся вокруг ядра атома 9.0005
Чтобы узнать количество протонов, содержащихся в атоме, просто посмотрите на его атомный номер.
Если атомный номер атома 37, то и протон будет 37, если атомный номер 39, то и протон будет 39.
протонов в атоме брома тоже 35.
Теперь, чтобы определить количество нейтронов в атоме, используйте эту формулу.
⇒ Количество нейтронов в атоме 9.0004 = Атомная масса атома (округленная до ближайшего целого числа) – Количество протонов в атоме
Например, атом имеет 59,998 атомную массу и 30 протонов.
Затем, чтобы найти число нейтронов, округлите атомную массу почти до целого числа, таким образом, атомная масса 59,998 округлите до 60.
= (60 – 30 протонов) = 30 число нейтронов в атоме
Теперь Чтобы получить количество нейтронов в атоме брома , посмотрите на его атомную массу, которая равна 79..904 округлить до 80, а число протонов в Броме равно 35.
∴ Отсюда число нейтронов в атоме Брома = (80 – 35) = 45
Следует отметить, что электронов в нейтральном атоме равно числу протонов».
Итак, атом брома нейтрален, следовательно, число его электронов будет равно числу протонов, которое равно 35 , как мы уже обсуждали.
⇒ Число электронов в атоме брома = 35,9.0005
⇒ Количество протонов в атоме брома = 35
⇒ Количество нейтронов в атоме брома = 45
Читаем подробно – Как найти количество протонов, электронов, нейтронов?
2. Нарисуйте ядро атома
Ядро представляет собой плотную и маленькую область, которая содержит количество протонов и нейтронов атома.
На этом шаге мы должны нарисовать маленький кружок, состоящий из числа протонов и числа нейтронов атома брома.
3. Нарисуйте первую электронную оболочку
«Электронную оболочку можно представить как орбиту, по которой следуют электроны вокруг ядра атома».
Первую электронную оболочку также называют К-оболочкой, это ближайшая к ядру атома оболочка, которая может содержать максимум два электрона.
Как мы знаем, атом брома имеет в общей сложности 35 электронов.
Итак, поместите два электрона из него, в первую оболочку, рядом друг с другом.
Мы успешно нарисовали первую оболочку атома брома, которая может содержать 2 электрона. Так как атом брома имеет всего 35 электронов, то из 35 электронов мы использовали два электрона на первой оболочке.
∴ (35 – 2) = 33 электрона
Следовательно, у нас осталось 33 электрона, поместим их в следующие оболочки атома Брома.
4. Нарисуйте вторую электронную оболочку
Вторая оболочка, также называемая L-оболочкой, может содержать максимум 8 электронов. Эта оболочка рисуется после первой электронной оболочки.
Во второй электронной оболочке электроны добавляются по одному, начиная с верхнего положения и затем двигаясь по часовой стрелке.
Во второй оболочке электроны добавляются по одному по часовой стрелке в положении часов – 12 часов, 3 часа, 6 часов, 9 часов.
После того, как вы разместите электроны по одному на каждой из четырех сторон (сверху – справа – снизу – слева), начните спаривать или удваивать их.
Итак, у нас осталось 33 электрона атома брома, а 2-я оболочка может удерживать максимум 8 электронов.
Таким образом, поместите 8 электронов атома брома во 2-ю электронную оболочку, начните с верхней позиции, размещайте электроны по одному и двигайтесь по часовой стрелке (сверху – справа – снизу – слева). И, наконец, соедините их.
Поскольку у нас всего 35 электронов для атома брома, мы разместили 2 электрона на первой оболочке и 8 электронов на второй оболочке.
∴ [35 – (2 + 8)] = 25 электронов
, следовательно, у нас осталось еще 25 электронов.
Поместим его в следующие ракушки.
5. Нарисуйте третью электронную оболочку
Третья оболочка также называется М-оболочкой и способна удерживать до 18 электронов, но для элементов первых нескольких периодов третья оболочка удерживает только до 8 электронов.
«Можно считать, что третья оболочка содержит 8 или 18 электронов, но всего третья оболочка может содержать 18 электронов».
Для первых нескольких элементов, скажем, до атомного номера 20 в периодической таблице, третья оболочка содержит до 8 электронов.
⇒ Для атомного номера 20 или меньше 20 третья оболочка может содержать максимум 8 электронов.
⇒ Для атомных номеров более 20, скажем, атомные номера 21, 22, 23, 24, 25, 26, 27 и т. д., третья оболочка заполнена более чем 8 электронами и до максимума 18 электронов.
Итак, у нас осталось 25 электронов атома брома, а третья оболочка будет содержать до 18 электронов, так как атомный номер брома равен 35.
Поэтому поместите 18 электронов брома в третью оболочку в положение, показанное на рисунке ниже.
Теперь, после размещения 18 электронов Брома в третьей оболочке, у нас осталось только 7 электронов.
Поместим их в следующую оболочку.
6. Нарисуйте четвертую электронную оболочку
Здесь нарисуйте четвертую электронную оболочку и поместите оставшиеся 7 электронов Брома таким образом, чтобы, начиная с верхней позиции, размещать электроны по одному, и идти в по часовой стрелке (сверху – справа – снизу – слева).
Боровская модель атома бромаИ, наконец, начать сопряжение.
Вот и все, это наша Боровская модель атома брома , которая содержит 35 протонов и 45 нейтронов в области ядра, и 35 электронов вращаются вокруг ядра, два электронов на первой оболочке, восемь электронов на второй оболочке, восемнадцать электронов на третьей оболочке и семь электронов на четвертой оболочке.
Читайте также:-
- Модель Oxygen Bohr
- Boron Bohr model
- Beryllium Bohr model
- Lithium Bohr model
- Helium Bohr model
- Nitrogen Bohr model
- Fluorine Bohr model
- Neon Bohr model
- Carbon Bohr model
- Sodium Bohr model
- Silicon Bohr model
- Магний Бор, модель
- Сера, Бор, модель
- Хлор, Бор, модель
- Фосфор, Бор, модель
- Алюминий, Бор, модель
- Аргон, Бор, модель
- Potassium Bohr model
- Calcium Bohr model
- Silver Bohr model
- Arsenic Bohr model
- Gold Bohr model
- Krypton Bohr model
- Iodine Bohr model
- Copper Bohr model
- Iron Bohr model
- Uranium Bohr model
- Никель, модель Бора
- Скандий, модель Бора
- Титан, модель Бора
- Ванадий, модель Бора
Найдите валентный электрон брома по его диаграмме БораТакже проверьте: Модель Бора для каждого элемента Периодической таблицы
Из диаграммы Бора атома мы можем легко найти количество валентных электронов в атоме, взглянув на его внешнюю оболочку.
Итак, нам нужно найти валентный электрон в атоме брома, для этого смотрим его диаграмму Бора.
Диаграмма Бора для брома имеет четыре электронных оболочки (K, L, M, N), внутренняя оболочка — это K-оболочка, а самая внешняя оболочка — это N-оболочка.
Следовательно, электроны, обнаруженные в N-оболочке атома брома, являются его валентными электронами, поскольку это самая внешняя оболочка, также называемая валентной оболочкой.
N-оболочка или внешняя оболочка модели Брома Бора содержит 7 электронов, следовательно, число валентных электронов в атоме брома также равно 7.
Электронная точечная диаграмма, также называемая структурой Льюиса, представляет собой валентные электроны атомов.
Как мы узнали из диаграммы Бора Брома, он имеет 7 валентных электронов.
Итак, просто представьте 7-валентный электрон вокруг атома брома в виде точки.
Электронная конфигурация бромаБром имеет атомный номер 35 и содержит 35 электронов.
Из боровской модели Брома мы знаем, что 2 электрона находятся в К-оболочке, 8 электронов — в L-оболочке, 18 электронов — в М-оболочке и 7 электронов — в N-оболочке.
Итак, исходя из оболочки, электронная конфигурация атома брома равна [2, 8, 18, 7].
Или электронная конфигурация брома : [Ar] 3d¹⁰ 4s² 4p⁵ , поскольку он содержит в общей сложности 35 электронов.
Читайте также:-
Часто задаваемые вопросы
- Как нарисовать орбитальную диаграмму любого атома
- Как написать электронную конфигурацию любого атома?
Сколько электронных оболочек содержит модель Брома Бора? Электронные оболочки, также называемые энергетическими уровнями. Вы можете найти количество электронных оболочек элемента, зная его номер периода в периодической таблице.
Элементы или атомы в первом периоде таблицы Менделеева имеют один энергетический уровень или одну электронную оболочку, так же как элементы во втором периоде имеют два энергетических уровня или двухэлектронную оболочку, и так далее…
Итак, атом брома относится к 4-му периоду периодической таблицы , следовательно, число электронных оболочек для боровской модели брома будет равно 4 (K-оболочка, L-оболочка, M-оболочка и N -оболочка).
Свойства брома
Какова внешняя оболочка диаграммы Бора атома брома? Самая внешняя оболочка, также называемая валентной оболочкой, содержит валентные электроны атома.
Согласно диаграмме Бора Брома, внешняя оболочка представляет собой N-оболочку, которая содержит семь валентных электронов.
Сводка
- Бром является третьим по легкости галогеном.
- Очень реакционноспособен по своей природе.
- Выглядит красновато-коричневым.
- До полного октета не хватает одного электрона.
- Образует орторомбическую кристаллическую структуру.
- Боровская модель брома (Br) нарисована с четырьмя электронными оболочками, первая оболочка содержит 2 электрона, вторая оболочка содержит 8 электронов, третья оболочка содержит 18 электронов и четвертая оболочка содержит 7 электронов.
- Бром нейтрален, и его атомный номер равен 35, следовательно, количество протонов и электронов, доступных для его диаграммы Бора, также равно 35.
- Число нейтронов для диаграммы Бора брома можно найти, вычитая количество протонов. от атомной массы (округленной до ближайшего целого).
- Электронная конфигурация брома с точки зрения оболочки [2, 8, 18, 7], или в нормальной форме это [Ar] 3d¹⁰ 4s² 4p⁵.
Br Информация об элементе брома: факты, свойства, тенденции, использование и сравнение – Периодическая таблица элементов
Кристаллическая структура брома
Структура твердого тела брома Орторомбическая с центром в основании .
Кристаллическая структура может быть описана с точки зрения ее элементарной ячейки. Единичные Клетки повторяются в трехмерном пространстве, образуя структуру.
Параметры элементарной ячейки
Элементарная ячейка представлена параметрами решетки, которые являются длинами ребер ячейки Постоянные решетки (a, b и c)
a b c6 672,65 пм 464,51 пм 870,23 пм и углы между ними Углы решетки (альфа, бета и гамма).
альфа бета Gamma π/2 π/2 π/2 Положения атомов внутри единичной клетки описаны по набору ATOMIC. y 90 569 i 90 570 , z 90 569 i 90 570 ), измеренные от опорной точки решетки.
Свойства симметрии кристалла описываются концепцией пространственных групп. Все возможные симметричные расположения частиц в трехмерном пространстве описываются 230 пространственными группами (219различные типы или 230, если хиральные копии считаются различными.
Space Group Name Cmca Oxidation States Space Group Number 64 Crystal Structure Base Centered Orthorhombic Bromine Atomic and Orbital Properties
Атомы брома имеют 35 электронов и структуру электронной оболочки [2, 8, 18, 7] с символом атомного термина (квантовые числа) 2 P 3/2 .
Atomic Number 35 Number of Electrons (with no charge) 35 Number of Protons 35 Mass Number 80 Number нейтронов 45 Структура оболочки (электронов на энергетический уровень) 2, 8, 18, 7 Электронная конфигурация [Ar] 3d10 4s2 4p5 Valence Electrons 4s2 4p5 Valence (Valency) 5 Main Oxidation States -1, 1, 3, 5 Состояния окисления -1, 1, 3, 4, 5, 7 Символ атомного термина (квантовые числа) 2 P 3/2 9000 2 9000 2 9015 9000 2 .
– Электронов на энергетический уровень
Электронная конфигурация основного состояния брома – нейтральный атом брома
Сокращенная электронная конфигурация брома
Сокращенная электронная конфигурация основного состояния нейтрального атома брома [Ar] 3d10 4s2 4p5. Часть конфигурации брома, эквивалентная благородному газу предыдущего периода, обозначается аббревиатурой [Ar]. Для атомов с большим количеством электронов это обозначение может стать длинным, поэтому используется сокращенное обозначение. Это важно, поскольку именно валентные электроны 4s2 4p5, электроны в самой внешней оболочке, определяют химические свойства элемента.
Полная электронная конфигурация нейтрального брома
Полная электронная конфигурация основного состояния атома брома, Полная электронная конфигурация
1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p5 , принцип запрета Паули и правило Хунда.
В соответствии с принципом Ауфбау электроны будут занимать орбитали с более низкой энергией, прежде чем занять орбитали с более высокой энергией. По этому принципу электроны заполняются в следующем порядке: 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, 5d, 6p, 7s, 5f, 6d, 7p. …
Принцип запрета Паули гласит, что максимум два электрона, каждый из которых имеет противоположные спины, могут разместиться на орбитали. Правило Хунда гласит, что каждая орбиталь в данной подоболочке занята электронами до того, как второй электрон заполнит орбиталь. Атомная структура брома
Атомный радиус брома составляет 94 пм, а его ковалентный радиус равен 114 пм.
Вычисленный атомный радиус 94 пм (0,94 Å)
Atomic Radius Empirical 115 pm (1.15 Å)
Atomic Volume 19.78 cm3/mol Covalent Radius 114 pm (1.14 Å) Van der Waals Radius 185 PM Нейтронный сечение 6,8 Поглощение массы нейтронной массы 0,002 Atomic Spectrum atomic
Atomic Spectrum
Atomic Spectrum
Atomic Spectrum
Atomic Spectrum
.
0519
Химические свойства брома: Энергия ионизации брома и сродство к электрону
Сродство к электрону брома составляет 324,6 кДж/моль.
Valence 5 Electronegativity 2.96 ElectronAffinity 324.6 kJ/mol Ionization Energy of Bromine
Refer to table below for Ionization energies of Bromine
Ionization energy number Enthalpy – kJ/mol 1st 1139.9 2nd 2103 3rd 3470 4th 4560 5th 5760 6th 8550 7th 9940 8th 18600 Физические свойства брома
См.
Ниже таблицы для физических свойств брома
Плотность 3,12 г/см3 (когда плотность M.P составляет 3,12 г/см3) м.П. mol Elastic Properties
Young Modulus – Shear Modulus – Bulk Modulus 1.9 GPa Poisson Ratio – Hardness of Bromine – Tests to Measure of Hardness of Element
Mohs Hardness – Vickers Hardness – Твердость по Бринеллю – Электрические свойства брома
Бром является проводником электричества. Обратитесь к таблице ниже для получения информации об электрических свойствах брома 9.0005
Electrical Conductivity 1e-10 S/m Resistivity 10000000000 m Ω Superconducting Point – Bromine Heat and Conduction Properties
Thermal Проводимость 0,12 Вт/(м·К) Тепловое расширение – Магнитные свойства брома
Magnetic Type Diamagnetic Curie Point – Mass Magnetic Susceptibility -4. 9e-9 m3/kg
Molar Magnetic Susceptibility -7.83e-10 m3/ моль Объемная магнитная восприимчивость -0,0000153 Оптические свойства брома
3 19012 3 0016 Акустические свойства Bromine
Скорость звука – .
265,8 K (-7,35°C, 18,77000000000006 °F) Температура кипения 332 K (58,85°C, 137,93000000009 00016 °F) 00013 Critical Temperature 588 K Superconducting Point – Enthalpies of Bromine
Heat of Fusion 5.8 kJ/mol Heat of Vaporization 14.8 kJ/ моль Теплота сгорания – Изотопы брома.
Ядерные свойства брома
Бром имеет 31 изотоп, от 67 до 97 нуклонов. Бром имеет 2 стабильных природных изотопа.
Изотопы брома – Встречающиеся в природе стабильные изотопы: 79Br, 81Br.
Isotope Z N Isotope Mass % Abundance T half Decay Mode 67Br 35 32 67 Synthetic 68Br 35 33 68 Synthetic 69Br 35 34 69 Synthetic 70Br 35 35 70 Synthetic 71Br 35 36 71 Synthetic 72Br 35 37 72 Synthetic 73Br 35 38 73 Synthetic 74Br 35 39 74 Synthetic 75Br 35 40 75 Synthetic 76Br 35 41 76 Synthetic 77Br 35 42 77 Synthetic 78Br 35 43 78 Synthetic 79Br 35 44 79 50,69% Стабильная N/A 80BR 35 45 80 Синтетические . 1140
81Br 35 46 81 49.31% Stable N/A 82Br 35 47 82 Synthetic 83Br 35 48 83 Синтетический 84BR 35 49 SYNTITITITIT0012 85Br 35 50 85 Synthetic 86Br 35 51 86 Synthetic 87Br 35 52 87 Synthetic 88Br 35 53 88 Synthetic 89Br 35 54 89 Synthetic 90Br 35 55 90 Synthetic 91Br 35 56 91 Synthetic 92Br 35 57 92 Synthetic 93Br 35 58 93 Synthetic 94Br 35 59 94 Synthetic 95Br 35 60 95 Synthetic 96Br 35 61 96 Синтетический 97BR 35 62 97 Синтетично 4014 14 14 0021 Вертикальная наука 7 класса
Валентные электроны и химические свойства
Вы узнали, что атомы в целом не очень стабильны.
На самом деле известно всего шесть химически стабильных атомов: благородные газы. Атомы благородных газов химически стабильны из-за их электронных конфигураций. Каждый из них имеет «полный» набор электронов на внешней оболочке.
Атом гелия (4He)
Атом неона (20Ne)
Атом аргона (40Ar)
Но подождите минутку. Атомы гелия и неона имеют полные внешние электронные оболочки… атом гелия имеет два электрона на своей первой (внешней) оболочке, а атом неона имеет восемь электронов на своей второй (внешней) оболочке… но атом аргона имеет только восемь электронов на своей первой (внешней) оболочке. третья (внешняя) оболочка, когда третья оболочка может содержать до восемнадцати электронов. Как внешняя оболочка атома аргона близка к полной?
девятнадцатый электрон в атоме калия (40K)
двадцатый электрон в атоме кальция (20Ca)
двадцать первый электрон в атоме скандия (45Sc)
Причина в том, что модель атома Бора, основанная на электронных оболочках, неточна.
Электроны не занимают электронные оболочки; они занимают атомные орбитали. Следующим после аргона элементом является калий (К). Атом калия имеет на один протон и на один электрон больше, чем атом аргона. Модель Бора предсказывает, что этот девятнадцатый электрон перейдет в третью электронную оболочку. Но на самом деле девятнадцатый электрон переходит на s-орбиталь четвертой электронной оболочки, хотя третья оболочка еще не полностью заполнена. Остальные орбитали в третьей оболочке заполняются только после того, как первой будет заполнена s-орбиталь в четвертой оболочке. (Диаграммы Бора точны только до аргона.)
Хотя третья электронная оболочка может содержать 18 электронов, четвертая электронная оболочка может содержать 32 электрона, пятая электронная оболочка может содержать 50 электронов, а шестая электронная оболочка может содержать 72 электрона, когда каждая из этих электронных оболочек заполняется 8 электронов, следующие два электрона перейдут в следующую более высокую электронную оболочку.
Это означает, что самая внешняя оболочка атома может иметь только от 1 до 8 электронов, прежде чем запустится новая внешняя оболочка, и эта оболочка вместо этого станет внутренней оболочкой. Электроны на внешней оболочке атома называются валентными электронами.
Если атом имеет только один электрон, то все атомные орбитали электронной оболочки эквивалентны и имеют одинаковую энергию, и не имеет значения, какую атомную орбиталь занимает электрон. Но когда атом имеет более одного электрона, геометрия атомных орбиталей и положения других электронов действительно влияют на энергию атомной орбитали и порядок их заполнения.
Первая электронная оболочка имеет одну атомную орбиталь: s-орбиталь. Все s-орбитали имеют форму сфер. Вторая электронная оболочка имеет четыре атомные орбитали: одну s-орбиталь и три р-орбитали. Р-орбитали имеют форму гантелей, чтобы максимально увеличить расстояние между электронами. Максимальное расстояние между электронами делает атом более стабильным, потому что электроны отрицательно заряжены и отталкиваются друг от друга.
s-орбиталь
pz-орбиталь
Два электрона на px-орбитали проводят большую часть своего времени в областях слева и справа от атомного ядра; два электрона на пи-орбитали проводят большую часть своего времени в областях выше и ниже атомного ядра; и два электрона на pz-орбитали проводят большую часть своего времени в областях перед и за атомным ядром. Геометрия этих орбиталей максимально рассеивает электроны, но все же есть некоторое перекрытие, которое снижает стабильность и немного увеличивает энергию p-орбиталей. Вот почему на самом деле s-орбиталь заполняется раньше p-орбиталей.
Третья электронная оболочка имеет девять атомных орбиталей: одну s-орбиталь, три p-орбитали и пять d-орбиталей. D-орбитали имеют еще более сложную и вытянутую форму, чтобы максимально увеличить расстояние между электронами, но они настолько сильно перекрываются, что s-орбиталь в четвертой электронной оболочке фактически заполняется раньше, чем пять d-орбиталей в третьей. электронная оболочка начинает заполняться.
В этой таблице показан порядок заполнения атомных орбиталей. 1s — s-орбиталь в первой электронной оболочке. 2s — s-орбиталь второй электронной оболочки. 2p — p-орбитали во второй электронной оболочке.
Правило октета и структуры Льюиса
Поскольку большинство атомов не очень стабильны, они склонны химически связываться с другими атомами, образуя стабильные молекулы. То, как связываются многие атомы, можно предсказать с помощью правила октетов. Правило октета гласит, что атомы имеют тенденцию терять, принимать или делиться электронами до тех пор, пока они не приобретут электронную конфигурацию с «полной» внешней оболочкой (в данном случае полной, что означает два электрона, если самая внешняя оболочка является первой оболочкой, и восемь электронов). если самая внешняя оболочка является второй или более высокой оболочкой). Это та же электронная конфигурация, что и у атомов благородных газов, которые являются единственными химически стабильными атомами в периодической таблице.
Правило октета не всегда работает, так как существует так много переменных, которые могут повлиять на стабильность атома. Как правило, правило октета не применяется к переходным или внутренним переходным металлам.
Как вы видели, диаграммы Бора могут немного вводить в заблуждение. Они также не очень полезны для предсказания химических свойств атомов. Химические свойства описывают, как атом или молекула реагирует в присутствии других атомов или молекул. Атомы реагируют, теряя, принимая или делясь электронами, и это почти всегда касается самых внешних (валентных) электронов атома, а не электронов во внутренних оболочках. Структура Льюиса — это диаграмма, на которой выделены валентные электроны атома. Это может быть очень полезно для предсказания того, как атомы будут реагировать друг на друга.
Чтобы нарисовать структуру Льюиса атома, найдите символ атома и положение в периодической таблице.
Символ брома — Br. У него 35 протонов и 35 электронов, и он находится в четвертом ряду и семнадцатом столбце периодической таблицы.
Начните заполнять валентные электроны брома. Поскольку бром находится в четвертой строке периодической таблицы, его валентные электроны будут находиться в четвертой электронной оболочке.
Начните с первого элемента в четвертой строке периодической таблицы (K) и начните отсчет. Девятнадцатый электрон брома переходит на 4s-орбиталь. Нарисуйте одну точку справа от символа брома.
Двадцатый электрон также переходит на 4s-орбиталь. Нарисуйте вторую точку справа от символа брома.
Теперь 4s-орбиталь заполнена, и следующие десять электронов переходят на 3d-орбитали. Поскольку эти электроны входят в третью электронную оболочку, они являются внутренними электронами, а не валентными электронами. Не добавляйте точки к символу брома.
Br
Тридцать первый электрон переходит на 4px-орбиталь. Нарисуйте одну точку над символом брома.
Тридцать второй электрон переходит на 4py-орбиталь. Нарисуйте одну точку слева от символа брома.
Тридцать третий электрон переходит на 4pz-орбиталь. Нарисуйте одну точку под символом брома. Каждая 4p-орбиталь теперь имеет один электрон.
Тридцать четвертый электрон переходит на 4px-орбиталь. Нарисуйте вторую точку над символом брома. Теперь орбиталь 4px заполнена.
Тридцать пятый (и последний) электрон переходит на 4py-орбиталь. Нарисуйте вторую точку слева от символа брома. Теперь 4py-орбиталь заполнена.
Структура Льюиса атома брома завершена. У него семь валентных электронов на внешней оболочке. Поскольку самая внешняя оболочка не является «полной» (у нее короткий один электрон), атом брома химически нестабилен и будет реагировать с другими атомами или молекулами до тех пор, пока его внешняя оболочка не заполнится.
Некоторые люди заполняют точки (валентные электроны) структуры Льюиса в разном порядке. Кажется, что нет единственно правильного способа сделать это, но это способ, который я предпочитаю. Начните с заполнения s-орбитальных электронов справа от символа атома, а затем заполните p-орбитальные электроны один за другим, двигаясь против часовой стрелки вокруг символа.
Группы элементов в периодической таблице
Если бы вы нарисовали структуры Льюиса для всех элементов в периодической таблице, вы бы обнаружили интересную закономерность. Все элементы семнадцатого столбца периодической таблицы имеют одинаковую структуру Льюиса.
Эти элементы вместе известны как галогены или группа фтора. Поскольку они имеют семь валентных электронов в одной и той же электронной конфигурации, они имеют схожие химические свойства. Галогены очень реакционноспособны и будут связываться с другими атомами, принимая или разделяя один электрон, чтобы заполнить их валентные оболочки.
На другом конце периодической таблицы находятся щелочные металлы или группа лития. Поскольку они имеют один валентный электрон в одной и той же электронной конфигурации, щелочные металлы также имеют схожие химические свойства. Они очень реактивны и будут связываться с другими атомами, теряя свой один валентный электрон. Это делает следующую более низкую (и полную) электронную оболочку самой внешней, валентной оболочкой.