Таблица менделеева – Электронный учебник K-tree
Электронный учебник
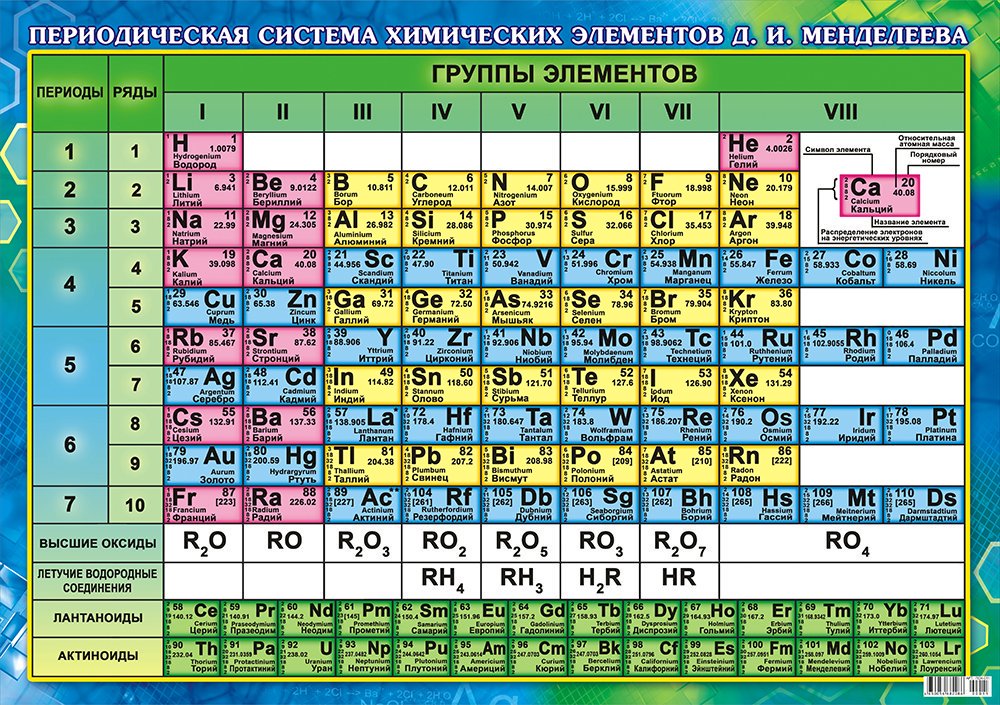
Периодический закон, открытый Д. И. Менделеевым был выражен в таблице. Периодическая таблица химических элементов, или таблица менделеева.
1
H
1.008
2
He
4.003
3
Li
6.938
4
Be
9.012
5
B
10.806
6
C
12.01
7
N
14.006
8
O
15.999
9
F
18.998
10
Ne
20.18
11
Na
22.99
12
Mg
24.304
13
Al
26.982
14
Si
28.084
15
P
30.974
16
S
32.059
17
Cl
35.446
18
Ar
39.948
19
K
39.098
20
Ca
40.078
21
Sc
44.956
22
Ti
47.867
23
V
50.942
24
Cr
51. 996
996
Mn
54.938
26
Fe
55.845
27
Co
58.933
28
Ni
58.693
29
Cu
63.546
30
Zn
65.38
31
Ga
69.723
32
Ge
72.63
33
As
74.922
34
Se
78.971
35
Br
79.901
36
Kr
83.798
37
Rb
85.468
38
Sr
87.62
39
Y
88.906
40
Zr
91.224
41
Nb
92.906
42
Mo
95.95
44
Ru
101.07
45
Rh
102.906
46
Pd
106.42
47
Ag
107.868
48
Cd
112.414
49
In
114.818
50
Sn
118.71
51
Sb
121.76
52
Te
127.6
53
I
126.904
54
Xe
131.293
55
Cs
132.905
56
Ba
137.327
57
La
138.905
72
Hf
178. 49
49
73
Ta
180.948
74
W
183.84
75
Re
186.207
76
Os
190.23
77
Ir
192.217
78
Pt
195.084
79
Au
196.967
80
Hg
200.592
81
Tl
204.382
82
Pb
207.2
83
Bi
208.98
58
Ce
140.116
59
Pr
140.908
60
Nd
144.242
62
Sm
150.36
63
Eu
151.964
64
Gd
157.25
65
Tb
158.925
66
Dy
162.5
67
Ho
164.93
68
Er
167.259
69
Tm
168.934
70
Yb
173.045
71
Lu
174.967
90
Th
232.038
91
Pa
231.036
92
U
238.029
В таблице менделеева колонки называются группами, строки называются периодами. Элементы в группах как правило имеют
одинаковые электронные конфигурации внешних оболочек, например, благородные газы – последняя группа, имеют законченную
электронную конфигурацию.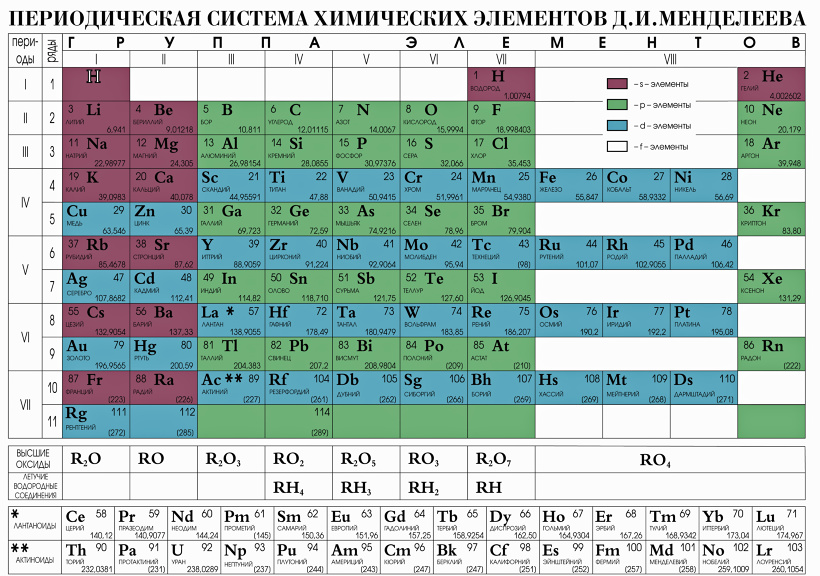
Как заполняется электронная конфигурация элементов подробно описано в статье
Скачать таблицу менделеева в хорошем качестве
© 2015-2022 – K-Tree.ru • Электронный учебник
По любым вопросам Вы можете связаться по почте [email protected]
Копия материалов, размещённых на данном сайте, допускается только по письменному разрешению владельцев сайта.
Химический элемент Олово: свойства и применение
Содержание
- История открытия
- Изотопы
- Нахождение в природе
- Формы нахождения
- Применение
- Биологическая роль
Олово представляет собой химический элемент, стоящий в 14 группе 5 периода под 50 атомным номером. В нормальных условиях показывает свойства пластичности, является ковким и легкоплавким металлом с характерным блеском и серебристым цветом.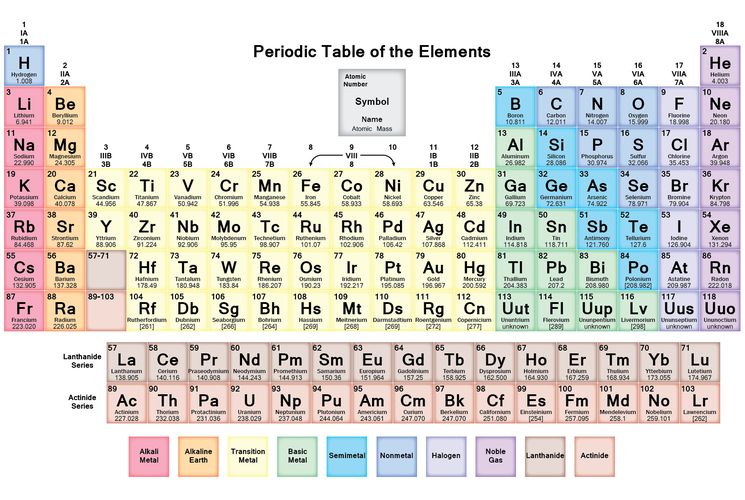
История открытия
Человек познакомился с оловом примерно в 4 тысячелетии до нашей эры. В чистом виде его удалось получить примерно в XII веке, этот факт стал известен из трудов Р. Бэкона. Название пришло из латинского языка, в переводе, если говорить дословно, оно обозначает «прочный». Непосредственно же слово «олово» обладает общеславянскими корнями и грубо говоря, обозначает «желтый».
Изотопы
В природе данный элемент составляют десять нуклидов являющиеся стабильными и обладающие следующими массовыми числами: 112Sn, 114Sn, 115Sn, 116Sn, 117Sn, 118Sn, 119Sn, 120Sn,122Sn,124Sn.
Он является представителем химических элементов, у которого в составе стабильных изотопов больше всего.
Нахождение в природе
Данное вещество представляет собой достаточно редкий элемент, который к тому же является еще и рассеянным. По распространению оно по праву занимает 47 место.
В поверхностных чистых водах олово содержится в качестве субмикрограммового концентрата, а если же говорить о подземных водах, то там оно достигает целых единиц микрограммов на 1 литр. В воде олово оказывается в результате разрушения минералов.
Формы нахождения
Данный элемент помимо рассеянной формы распространения способен также и к образованию минеральных форм.
- Твердая фаза. Существуют следующие формы элемента, в которых он встречается в природной среде: рассеянная; минеральная (чаще всего это минералы с содержанием железа).
- Собственно минеральные формы
- Самородные элементы
- Соединения олова в виде оксидов
- Касситерит
- Касситерит является основным минералом руд, который применяется для получения описываемого химического элемента.
- Синтез с водой
- Силикаты
- Шпинелиды
- Сульфидные соединения олова
- Станнин
- Коллоидная форма
Формы жидкого состояния вещества:
- Ионные соединения;
- Простые ионы;
- Галогениды;
- Гидроксильные сочетания;
- Сульфидные соединения.

Применение
Использование олова происходит в качестве безопасного, нетоксичного материала, который не подвержен коррозиям. Одними из немногих отраслей промышленности, где его используют, является производство посуды, трубопроводов. Одним из распространенных сплавов является бронза. Использование его происходит также для создания проводов с высокой скоростью передачи сигнала.
Сочетания олова с другими представителями периодической системы применяют для производства красок, оптических стекол.
Биологическая роль
О данной роли этого представителя таблицы Д. И. Менделеева практически нет никакой информации. Олово содержится в организме человека, а наибольшая его часть скапливается в кишечнике.
Вещество является опасным для человека, когда оно действует в виде паров или пыли, что может привести к болезням, одной из них может быть поражение легких.
Sn Информация об элементе олова: факты, свойства, тенденции, использование и сравнение – Периодическая таблица элементов
Кристаллическая структура олова
Твердотельная структура олова Центрированная тетрагональная .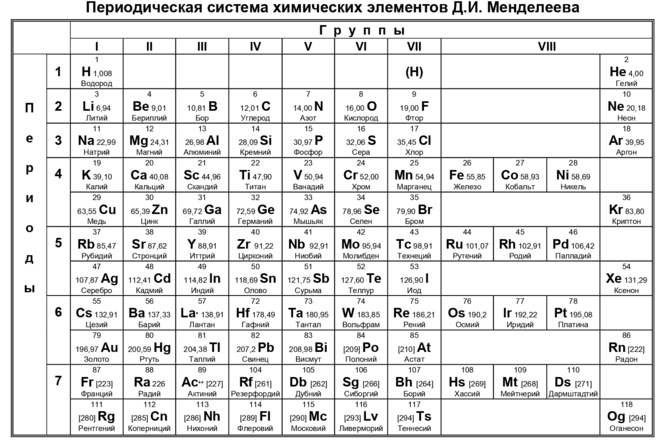
Кристаллическая структура может быть описана с точки зрения ее элементарной ячейки. Единичные Клетки повторяются в трехмерном пространстве, образуя структуру.
Параметры элементарной ячейки
Элементарная ячейка представлена в терминах ее параметров решетки, которые являются длинами ребер ячейки Константы решетки (a, b и c)
| A | B | C |
|---|---|---|
| 583.18 PM | 583.18 | 318.19 PM |
| alpha | beta | gamma |
|---|---|---|
| π/2 | π/2 | π/2 |
The positions of the atoms inside the unit cell are described by the set атомных позиций ( x i , y i , z i ), измеренные от опорной точки решетки.
Свойства симметрии кристалла описываются концепцией пространственных групп. Все возможные симметричные расположения частиц в трехмерном пространстве описываются 230 пространственными группами (219 различных типов или 230, если киральные копии считаются различными).
Tin Atomic и Orbital Properties
Атомы олова. 4] с символом атомного термина (квантовые числа) 3 P 0 .
| Атомный номер | 50 | |
| Количество электронов (бесплатно) | 50 | |
| Number of Protons | 50 | |
| Mass Number | 119 | |
| Number of Neutrons | 69 | |
| Shell structure (Electrons per energy level) | 2, 8, 18, 18, 4 | |
| Электронная конфигурация | [KR] 4D10 5S2 5P2 | |
| Валентные электроны | 5S2 5P2 | |
| Валентность (Валентность) | ||
| (Валентность) | ||
| (Валентность) | ||
| (Валентность) | ||
| (валентность) | ||
| (валентность)0028 | ||
| Основные степени окисления | -4, 2, 4 | |
| Степени окисления | -4, -3, -2, -1, 0, 1, 2, 3, 4 | 9002 Атомный термин Символ (квантовые номера)3 P 0 |
Атомная модель BOHR Atomic Tin Electrons
Наземное состояние.
 Олово
ОловоСокращенная электронная конфигурация основного состояния нейтрального атома олова: [Kr] 4d10 5s2 5p2. Часть конфигурации олова, эквивалентная благородному газу предыдущего периода, обозначается аббревиатурой [Kr]. Для атомов с большим количеством электронов это обозначение может стать длинным, поэтому используется сокращенное обозначение. Это важно, так как именно валентные электроны 5s2 5p2, электроны в самой внешней оболочке, определяют химические свойства элемента.
Полная электронная конфигурация нейтрального олова
Полная электронная конфигурация атома олова в основном состоянии. Полная электронная конфигурация
1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p2 Правило Хунда.
 …
…Атомная структура олова
Атомный радиус олова составляет 145 пм, а его ковалентный радиус составляет 141 пм.
| Расчетный атомный радиус | 145 пм (1,45 Å) |
| Радиус атомного радиуса Эмпирический | 145 вечера (1,45 Å) |
| Атомический объем | 16,239 CM3/моль |
| COVERED/239 CM3/моль | |
| COVERED/239 CM3/Мол | |
| COVLED | ())))))))))))). RADIUS217 PM |
| Нейтронный сечение | 0,63 |
| АБрапбция нейтрона | 0,0002 |
Ат -спектр0011
Химические свойства олова: Энергия ионизации олова и сродство к электрону
Сродство к электрону олова составляет 107,3 кДж/моль.
| Valence | 4 |
| Electronegativity | 1.96 |
| ElectronAffinity | 107.3 kJ/mol |
Ionization Energy of Tin
Refer to table below for Ionization energies of Tin
| Энергия ионизации номер | Enthalpy – kJ/mol |
|---|---|
| 1st | 708.6 |
| 2nd | 1411.8 |
| 3rd | 2943 |
| 4th | 3930.3 |
| 5th | 7456 |
Физические свойства олова
Физические свойства олова см. в таблице ниже.9 g/cm3)
Elastic Properties
| Young Modulus | 50 |
| Shear Modulus | 18 GPa |
| Bulk Modulus | 58 ГПа |
| Коэффициент Пуассона | 0,36 |
0027 Мохс.
 Твердость
ТвердостьTin Heat and Conduction Properties
| Thermal Conductivity | 67 W/(m K) |
| Thermal Expansion | 0.000022 /K |
Tin Magnetic Properties
| Магнитный тип | Диамагнитный |
| Точка Кюри | – |
| Масса Магнитная восприимчивость | -3.1e-9 м3/кг0028 |
| Molar Magnetic Susceptibility | -3.68e-10 m3/mol |
| Volume Magnetic Susceptibility | -0.0000227 |
Optical Properties of Tin
| Refractive Index | – |
Акустические свойства олова
| Скорость звука | 2500 м/с |
Тепловые свойства олова.
 Энтальпии и термодинамика
Энтальпии и термодинамикаСм. Таблицу ниже для термических свойств TIN
| Снятие плавления | 505,08 K (231,93 ° C, 449,474 ° F) |
| 449,478 | 28777.855.8555.855.855.855.855.855.85.85.85.85.85.85.85.85.85.8.855.8. |
| Критическая температура | – |
| Сверхпроводящая точка | 3,72 |
Энтуалпий
Hapt of LIN
|

 97%
97% 58%
58% 0027 50
0027 50 Олово имеет ряд применений, в первую очередь для покрытия стали в пищевых контейнерах или для изготовления листов фольги. Олово имеет кристаллическую структуру, и когда оловянный стержень сгибается, звук, похожий на визг, разрушает эту кристаллическую структуру, это известно как крик олова. Олово было известно людям как элемент уже давно, начиная с 3000 г. до н.э., когда оно использовалось для производства бронзы. Он был легирован медью для улучшения свойств. Он находится в группе 14 как металл. Он имеет температуру плавления 231°C и точку кипения 2620°C.
Олово имеет ряд применений, в первую очередь для покрытия стали в пищевых контейнерах или для изготовления листов фольги. Олово имеет кристаллическую структуру, и когда оловянный стержень сгибается, звук, похожий на визг, разрушает эту кристаллическую структуру, это известно как крик олова. Олово было известно людям как элемент уже давно, начиная с 3000 г. до н.э., когда оно использовалось для производства бронзы. Он был легирован медью для улучшения свойств. Он находится в группе 14 как металл. Он имеет температуру плавления 231°C и точку кипения 2620°C.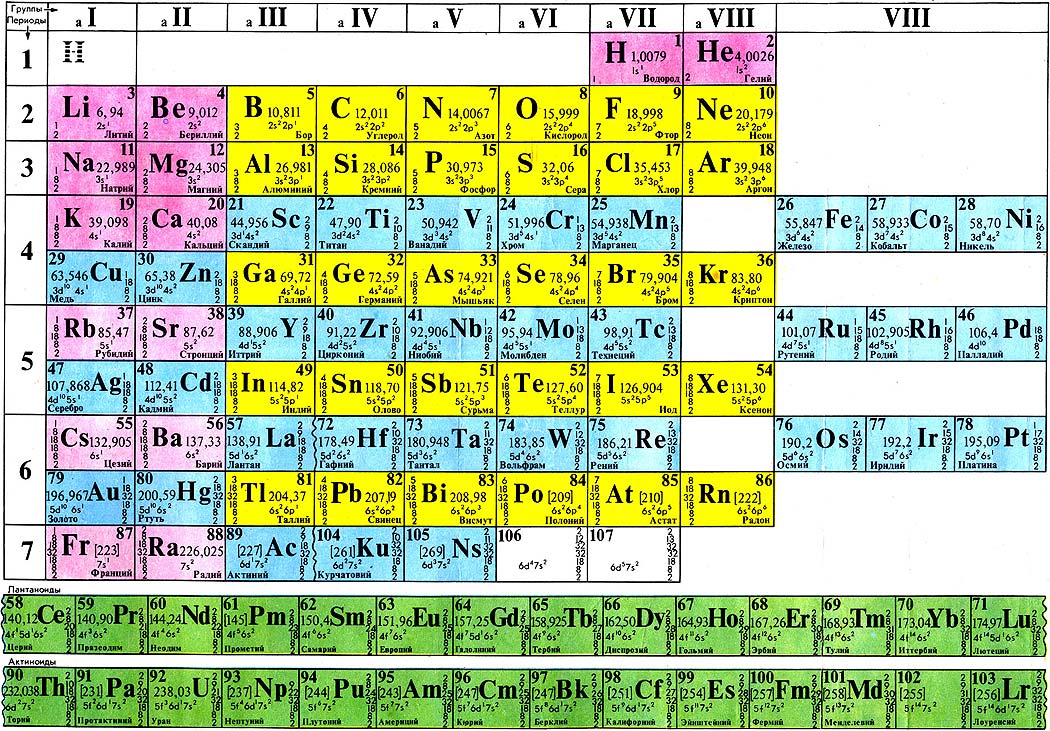
 Предмет Натана варьируется от общей химии до органической химии. Натан также создал учебную программу «Разрушение атома» на странице курса.
Предмет Натана варьируется от общей химии до органической химии. Натан также создал учебную программу «Разрушение атома» на странице курса.