Тайны Мироздания: факты об атомах и молекулах – Пипсик
В физике существуют целые разделы, изучающие строение и взаимодействие микроскопических структурных единиц. Однако когда мы начинаем изучать физику, то она почти неизбежно потащит за собой и химию, так что для детальных знаний придется разбираться в обеих науках. В этой статье мы раскроем интересные факты об атомах и молекулах, которые помогут лучше понять окружающий нас мир.
Если кратко, то вся окружающая нас материя, любые объекты как на Земле, так и в космосе, состоят из мельчайших частиц — атомов, которые образуют более сложные соединения — молекулы. Эти частицы могут иметь различные свойства (и даже менять их!), когда находятся в составе различных химических элементов, но при этом подчиняются законам физики. Простейший пример: вода имеет одни свойства, а лед или пар — уже иные. Между тем это одно вещество, правда находящееся в разных агрегатных состояниях.
1. Атомы состоят из ядра, образованного протонами и нейтронами. Вокруг этого ядра вращаются электроны. На плотное ядро приходится 99,9% массы частицы. Если представить целостную квантовую систему в виде футбольного поля, ядро окажется размером с горошину. Электроны — самые легкие компоненты атома, их орбита проходит настолько далеко от центра, что крошечную структуру фактически на 99% заполняет пустота.
Вокруг этого ядра вращаются электроны. На плотное ядро приходится 99,9% массы частицы. Если представить целостную квантовую систему в виде футбольного поля, ядро окажется размером с горошину. Электроны — самые легкие компоненты атома, их орбита проходит настолько далеко от центра, что крошечную структуру фактически на 99% заполняет пустота.
2. Субатомные частицы — составляющие ядра, удерживаются вместе ядерной силой. Природа этой силы ученым пока не понятна. Отрицательно заряженным электронам не дает сбиться с траектории движения электромагнитная сила, притягивающая их к протонам — частичкам с положительным зарядом. Ядерная сила почти в тысячу раз мощнее земной гравитации, но проявляется только в пределах микроструктур.
3. Протоны и электроны состоят из более мелких частичек, получивших название кварки. Они существуют исключительно в связанном состоянии и делятся на виды: нижний, верхний, странный, очаровательный, истинный, и красивый. Поведение этих точечных единиц такое же необычное, как и их названия, и законы, по которым они действуют, пока не изучены.
Долгое время кварки являлись лишь гипотезой, однако после строительства БАК (Большой Адронный Коллайдер) их существование было доказано экспериментальным путем. Здесь нужно все же оговориться, что доказательство это весьма косвенно, так как время жизни кварков измерятся долями секунд, но научный мир его принял.
4. Атомы химических элементов отличаются количеством протонов. Так, в ядре атома водорода всего одна частица, углерода — шесть, а алюминия — тринадцать. Причем материя не всегда однородна: например, золото образовано атомами одного типа, а хлорид натрия состоит из связанных между собой атомов двух веществ. Но здесь мы уже углубляемся больше в химию, чем в физику.
5. Ученые могут создавать атомы, искусственно добавляя протоны. Первым таким экспериментальным веществом был технеций, имеющий в ядре 43 частички. Этот радиоактивный порошкообразный металл был синтезирован в 1937 году, он не имеет стабильных изотопов, производится для нужд медицины и промышленности в ядерных реакторах.
Однако технеций был не изобретен, а «подсмотрен» у природы. Также техническим путем изготавливают и искусственные алмазы, помещая углерод под пресс с немыслимым давлением и температурой. Кстати, в современной промышленности 97% всех алмазов — синтетические. Всего науке известно около 100 видов атомов, из них более 90% можно встретить в природе, остальные “сконструированы” в лабораториях.
6. Тело человека весом 70 кг. формируется из 7 октиллионов атомов, среди которых большая часть — азот, кислород и углерод. Около 98% этих частиц заменяется ежегодно (см.интересные факты о человеке).
7. 73% атомов в пределах обозримой Вселенной — атомы водорода.
8. Атом не всегда мирный. Атомная бомба — оружие массового поражения, способное уничтожить миллионы. При расщеплении ядра высвобождается огромное количество энергии, направленной на разрушение. Ядерное оружие впервые использовали в конце Второй мировой войны американцы, сбросив 2 бомбы на Японию.
Результаты были катастрофическими: от двух американских бомб в Хиросиме и Нагасаки погибли сотни тысяч человек, а японское правительство немедленно подписало капитуляцию. Сейчас страны ядерного Клуба тщательно следят за своими бомбами и ракетами, чтобы они случайно не попали не в те руки. Ну а про Чернобыль и Фукусиму, печально известные атомные электростанции, все уже слышали.
Сейчас страны ядерного Клуба тщательно следят за своими бомбами и ракетами, чтобы они случайно не попали не в те руки. Ну а про Чернобыль и Фукусиму, печально известные атомные электростанции, все уже слышали.
9. Молекулы определенного вещества состоят из абсолютно идентичных атомов. Эти частицы невозможно увидеть в обычные микроскопы, только в современные электронные приборы последнего поколения с тысячекратным увеличением. Если говорить образно, молекула по размеру во столько раз меньше яблока, во сколько яблоко меньше земного шара. Одна песчинка — это 20 миллионов миллиардов микрочастичек.
10. Молекулы всегда находятся в движении. Это явление было открыто Р. Броуном в 1827 году и позже сформулировано А. Эйнштейном. Британский ботаник смешал капельку воды с пыльцой растений и поместил под микроскоп. Наблюдения показали: пыльца постоянно перемещается без видимых причин, что объяснили влиянием хаотично колеблющихся молекул воды. Явление получило название Броуновского движения.
Это конечно не все интересные факты об атомах и молекулах. Если вас заинтересовала данная тема, рекомендуем более подробно углубиться в нее и проштудировать школьные учебники по физике и химии. Быть может, из вас получится второй Эйнштейн или Нильс Бор? Кто знает.
Интересные факты, удивительные факты, неизвестные факты в музее фактов. Интересные факты о молекулах
Интересные факты о физике, естественной школьной науке, позволят вам узнать самые обычные, на первый взгляд, процессы с необычной стороны.
Капля дождя весит больше, чем комар. Но волоски, которые размещены на поверхности тела насекомого, практически, не передают импульс от капли к комару. Поэтому насекомое выживает даже под проливным дождем. Этому способствует еще один фактор. Столкновение воды с комаром происходит на незакрепленной поверхности. Поэтому если удар приходится в центр насекомого, оно некоторое время падает с каплей, а потом быстро освобождается. Если дождь попадает не в центр, траектория движения комара немного отклоняется.
Интересные факты об атоме
Расщепление атомов – это не только химический процесс, в некоторых случаях это может являться человеческим увлечением. И тому есть пример из Швеции – мужчина (по-видимому, от нечего делать) обустроил на своей небольшой кухне мини-лабораторию в виде “ядерного реактора” и там, собственно, ставил такие немудреные эксперименты, вложив всего менее 1000$ в эту увлекательную экспедицию.
Интересные факторы о температуре.
Знаете ли вы, что человек смог создать живому организму невероятно высокую температуру -4 млрд градусов Цельсия? А это, что бы вы смогли ориентироваться, в 250 раз более, нежели температура солнечного ядра!
Интересные факты о свете.
Свет обладает нулевой массой, но имеет огромную кинетическую энергию, оказывая давление на любой объект, который он освещает. Эту удивительную способность света конструкторы пытаются применить для перемещения спутников в космосе.
Интересный факт о грозе .
Не все знают, почему нельзя купаться во время грозы. Так как вода является великолепным проводником электричества, благодаря растворенным в ней различным минеральным солям, вероятность попадания молнии достаточно велика. Если же воду дистилировать, то она, напротив, превратится в диэлектрик.
Интересный факт о работе лифта.
Любой человек хоть раз в жизни ездил в лифте. И многим приходила в голову мысль о том, что делать, если он начнет падать с высоты. Большинство решили бы, что в таких обстоятельствах шансов выжить нет. Или что в момент удара необходимо подпрыгнуть. На самом деле рассчитать это время нереально. Но если сделать так, чтобы сила удара пришлась на как можно большую площадь поверхности тела, возможно, все обойдется. То есть попросту нужно лечь на пол. Как видно,
Почему сидящая на проводе птица не погибает от удара током?
Сидящая на проводе высоковольтной ЛЭП птица не страдает от тока, потому что её тело – плохой проводник тока.
Какие элементарные частицы названы в честь крика уток?
Мюррей Гелл-Манн, выдвинувший гипотезу о том, что адроны состоят из ещё более мелких частиц, решил назвать эти частицы звуком, который производят утки. Оформить этот звук в подходящее слово ему помог роман Джеймса Джойса «Поминки по Финнегану», а именно строка: «

Занимательный факт об инфразвуке.
Известно, что инфразвук это звук с колебаниями меньше 16 герц. Так вот, однажды для спектакля про средневековье, в театр где должно было происходить действия привезли трубу длиной почти в 40 метров. Так как известно, что чем длиннее труба, тем ниже получается звук, что она издает. Рассчитали, что частота звука новой трубы должна быть 8Гц, и по идее, человек не должен его услышать, но произошел аншлаг. Когда заиграли на трубе, звук вышел частотой 5 Гц, что соответствует альфа-ритму человеческого мозга. В зале случилась паника так, как данный звук вызвал у всех присутствующих страх.
Еще немного физики.
1) Ничто не может гореть еще раз, если уже сгорело.
2) Пузырь круглый, так как воздух внутри него одинаково давит на все его части, поверхность пузыря равноудалена от его центра.
3) Черный цвет притягивает тепло, белый отражает его.
4) Кнут издает щелчок, потому что его кончик двигается быстрее скорости звука.
5) Бензин не имеет определенной точки замерзания – он может замерзнуть при любой температуре от -118 С до -151 С. При замерзании бензин не становится полностью твердым, скорее напоминает резину или воск.
6) Яйцо будет плавать в воде, в которую добавили сахар.
7) Грязный снег тает быстрее, чем чистый.
8) Гранит проводит звук в десять раз быстрее воздуха.
9) Вода в жидкой форме имеет большую молекулярную плотность, чем в твердой. Поэтому лед плавает.
10) Если стакан с водой увеличить до размера Земли, то молекулы, из которых она состоит, будут размером с большой апельсин.
11) Если в атомах убрать свободное пространство и оставить только составляющие их элементарные частицы, то чайная ложка такого “вещества” будет весить 5.000.000.000.000 килограмм. Из него состоят так называемые нейтронные звезды.
12) Скорость света зависит от материала, в котором он распространяется. Ученым удалось замедлить движение фотонов до 17 метров в секунду, пропуская их через слиток рубидия, охлажденный до температуры, очень близкой к абсолютному нулю (-273 по Цельсию)
Cтраница 1
Интересная молекула F3NO также имеет тетраэдрическую структуру.
Эти интересные молекулы могут либо отдавать протон карбоксила, либо присоединять еще один протон к аминогруппе.
Ксенон образует ряд интересных молекул и ионов со фтором и кислородом. Укажите, на каких атомах в этих льюисовых структурах имеются отличные от нуля формальные заряды.
При попытке использовать измерения ЯЭО для более интересных молекул, чем приведенные в предыдущем разделе, мы столкнемся с некоторыми трудностями. Вероятно, большое число взаимодействующих протонов сделает невозможным расчет межъядерных расстояний. Предположение о равных корреляционных временах для всех межъядерных векторов, на котором основаны такие расчеты, скорее всего вообще не выполняется для больших молекул, и мы не должны забывать об этом.
Прогресс, достигнутый за последние годы в области современной структурной химии, сводится в основном к определению структур ряда особенно интересных молекул и кристаллов.
Вместе с тем метод газовой хроматографии для исследования адсорбции отличается высокой чувствительностью, позволяющей изучать область малых заполнений, возможностью работать на серийной аппаратуре в широкой области температур и, следовательно, изучить адсорбционные взаимодействия большого числа интересных молекул разного строения. Однако при этом используется приближение теории нелинейной равновесной хроматографии. Сопоставление со статическими исследованиями показывает, что обычно критерием достаточной близости к равновесным условиям в колонке при проявительной хроматографии является, во-первых, совпадение размытой границы пика для разных проб (от нуля до точки перегиба изотермы) и, во-вторых, вертикальность противоположной границы пика.
В анионе [ СЮ2 ] – угол ОС1О равен 110 5, длина связи хлор – кислород – 156 пм. Интересной молекулой с аналогичным угловым строением является С1С2, в которой угол OC1Q равен 117 4, а расстояние С1 – О – 147 пм. Эта молекула необычна, так как хотя она парамагнитна, но в противоположность NO2, димеров (см. с. Поскольку связи С1 – О в ней заметно короче связей в хлорид-ионе, порядок связей должен быть больше. Простейший способ описать образование связей – исходить из строения диоксида серы и считать, что дополнительный электрон находится на разрыхляющей орбитали.
Мы хотим теперь поговорить об одной из самых интересных молекул – о молекуле бензола, диаграмма которой приведена на фиг. В нее входят по шести весьма симметрично расположенных атомов углерода и водорода. Каждая черточка на диаграмме представляет пару электронов с противоположными спинами, пляшущих танец ковалентной связи. Каждый атом водорода вводит в игру по одному электрону, а каждый атом углерода – по четыре, образуя в общей сложности систему из 30 участвующих в игре электронов.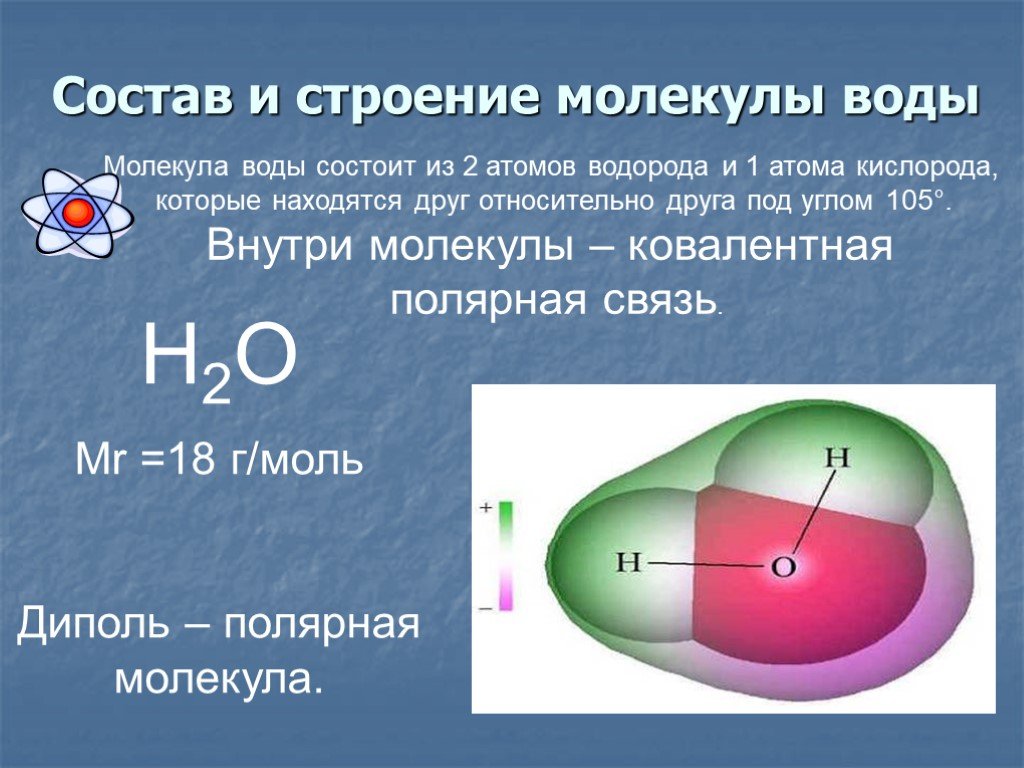
Таким образом, изооктан дает только два первичных продукта: грег-бутилкатион и изобутилен. Здесь следует отметить несколько важных моментов, делающих изооктан наиболее интересной молекулой с точки зрения исследования карбоний-ионного механизма превращения алканов.
Выше были рассмотрены спектры труднолетучих галогенидов различных элементов, однако еще более труднолетучими являются окислы. Одним из первых объектов исследований была окись бора, но до сих пор проблемы строения и спектров этой очень интересной молекулы не разрешены, поэтому остановимся несколько подробнее на истории и технике исследований.
Теперь на примере наиболее простой молекулы – молекулярного иона водорода Щ – мы сначала выявим наиболее существенные черты теории строения молекул, а затем обсудим более сложные и химически более интересные молекулы.
Сравнивая протонные химические сдвиги 1 6 8 13 – б с-метано аннулена (31) и данные для 1 6-метано аннулена, можно прийти к заключению, что в 31 нет кольцевого тока, существование которого можно предполагать, исходя из числа jt – электронов. Как показывает изучение молекулярных моделей, между центрами 6, 7, 8 и 13, 14, 1 происходит сильное скручивание углерод-углеродных связей, которое настолько затрудняет эффективное перекрывание 2рг – орбиталей углерода, что здесь впервые соединение, имеющее число л-электронов, точно соответствующее правилу ароматичности Хюккеля, проявляет олефиновые свойства. Позднее мы еще вернемся к этой интересной молекуле.
Как показывает изучение молекулярных моделей, между центрами 6, 7, 8 и 13, 14, 1 происходит сильное скручивание углерод-углеродных связей, которое настолько затрудняет эффективное перекрывание 2рг – орбиталей углерода, что здесь впервые соединение, имеющее число л-электронов, точно соответствующее правилу ароматичности Хюккеля, проявляет олефиновые свойства. Позднее мы еще вернемся к этой интересной молекуле.
Однако любая предлагаемая структура должна быть проверена путем сравнения спектра, предсказываемого на ее основании, с опытным. При этом следует указать на два обстоятельства. Для того чтобы такая сложная молекула, как [ Fe3 (CO) 12 ], имела сравнительно простой спектр, ее симметрия должна быть довольно высокой. Слабость полос представляется, таким образом, аргументом против наличия в молекуле кетонных мостиков. Однако тогда становится неясным вопрос о том, к чему же могут быть отнесены слабые полосы. Очевидно, что необходимы дальнейшие исследования этой интересной молекулы.
Страницы: 1
Несколько интересных фактов: … разведя 1 мл чернил в 1 л воды, а затем 1 мл этого раствора – в ещё одном литре воды, мы получим разбавление в миллион раз. Несмотря на это, получившийся раствор будет иметь вполне заметную окраску. Отсюда следует, что объём частичек чернил намного меньше, чем миллионная часть миллилитра! … сохранилось описание одного исторического опыта, в котором в свинцовый шар налили воду и прочно его запаяли. По шару ударили молотом, надеясь, что он сплющится и сожмёт воду. И что же? Шар сплющился, но вода не сжалась, она просочилась сквозь стенки шара. Молекулы воды были продавлены через промежутки между частицами свинца. … Молекула меньше яблока во столько же раз, во сколько раз яблоко меньше Земли. …Если представить, что растительное масло создаёт на поверхности воды плёнку толщиной в одну молекулу, то такая плёнка будет тоньше человеческого волоса в 40000 раз.
Слайд 29 из презентации «МКТ» к урокам физики на тему «МКТ»
Размеры: 960 х 720 пикселей, формат: jpg. Чтобы бесплатно скачать слайд для использования на уроке физики,
щёлкните на изображении правой кнопкой мышки и нажмите «Сохранить изображение как…».
Скачать всю презентацию «МКТ.ppt» можно
в zip-архиве размером 3625 КБ.
Чтобы бесплатно скачать слайд для использования на уроке физики,
щёлкните на изображении правой кнопкой мышки и нажмите «Сохранить изображение как…».
Скачать всю презентацию «МКТ.ppt» можно
в zip-архиве размером 3625 КБ.
Скачать презентацию
МКТ
«Урок физики Основное уравнение МКТ» – Задача №2. Микроскопические – параметры, которые измеряются косвенным путем. Урок №3 Основное уравнение МКТ. Чему равно давление азота? Задача №1. Давление кислорода равно 32 кПа. Имеются два одинаковых сосуда. Макроскопические – параметры, которые можно измерить с помощью приборов. Давление идеального газа прямо пропорционально средней кинетической энергии поступательного движения молекул, содержащихся в единице объема газа.
«Молекулярно-кинетическая теория» – Ионный проектор. Доказательства первого положения МКТ. Первое положение МКТ. Молекулярная физика. Частицы вещества непрерывно и хаотически движутся. Броуновское движение – беспорядочное движение частиц. Определение молекулярно-кинетической теории. Частицы вещества взаимодействуют друг с другом. Доказательства второго положения МКТ.
Определение молекулярно-кинетической теории. Частицы вещества взаимодействуют друг с другом. Доказательства второго положения МКТ.
««МКТ» физика» – Нормальное состояние. Кроссворд. Температура и внутренняя энергия тела. Миллиметр ртутного столба. Модель идеального газа. Температура. Материальные точки. Основы молекулярно-кинетической теории. Раздел физики. Кельвин. Молекулярная физика. Термодинамическая температурная шкала. Идеальный газ. Давление.
«Основы МКТ» – Атомная единица массы (а.е.м.): 1/12?12С (1/16?16О), 1.66?10-27 кг Относительная атомная масса – отношение массы атома к а.е.м.: mа.о.=mат./а.е.м. приблизительно равна числу нуклонов в ядре. Переход системы из неравновесного состояния в равновесное происходит за время релаксации, которое может зависеть от степени отклонения от равновесного состояния и свойств самой системы.
«Давление газа» – Рисунок 1.7. Жозеф Гей-Люссак. Величину T называют абсолютной темпе-ратурой и измеряют в градусах Кельвина (К). Рисунок 1.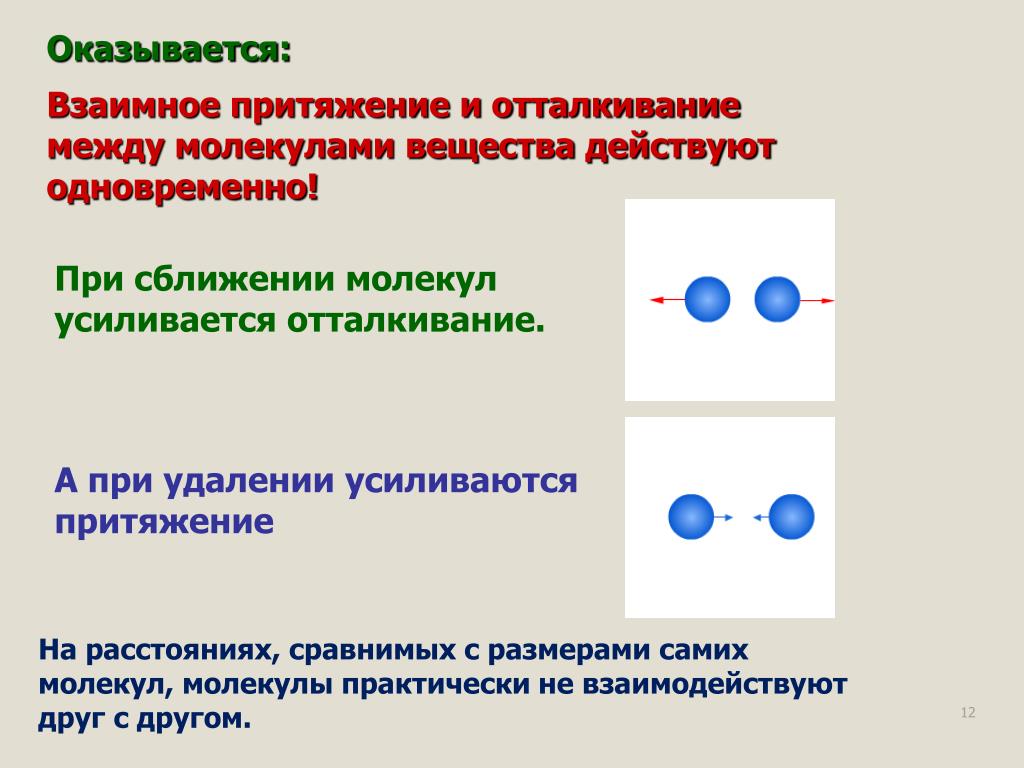 9. Единицы измерения давления. Менделеев Дмитрий Иванович (1834 – 1907) – русский ученый. Автомобиль имеет вес F2. 7. Закон Дальтона. Процесс, при котором теплоёмкость газа остаётся постоянной.
9. Единицы измерения давления. Менделеев Дмитрий Иванович (1834 – 1907) – русский ученый. Автомобиль имеет вес F2. 7. Закон Дальтона. Процесс, при котором теплоёмкость газа остаётся постоянной.
1. Но начнем мы совсем с другой стороны. Прежде чем отправиться в путешествие к глубинам материи, давайте обратим свой взор вверх.
Например, известно, что до Луны в среднем почти 400 тысяч километров, до Солнца – 150 миллионов, до Плутона (который уже не виден без телескопа) – 6 миллиардов, до ближайшей звезды Проксимы Центавра – 40 триллионов, до ближайшей крупной галактики туманности Андромеды – 25 квинтиллионов, и наконец до окраин обозримой Вселенной – 130 секстиллионов.
Впечатляюще, конечно, но разница между всеми этими «квадри-», «квинти-» и «сексти-» не кажется столь уж огромной, хотя они и различаются между собой в тысячу раз. Совсем другое дело микромир. Разве в нем может быть скрыто так уж много интересного, ведь ему просто негде там поместиться. Так говорит нам здравый смысл и ошибается .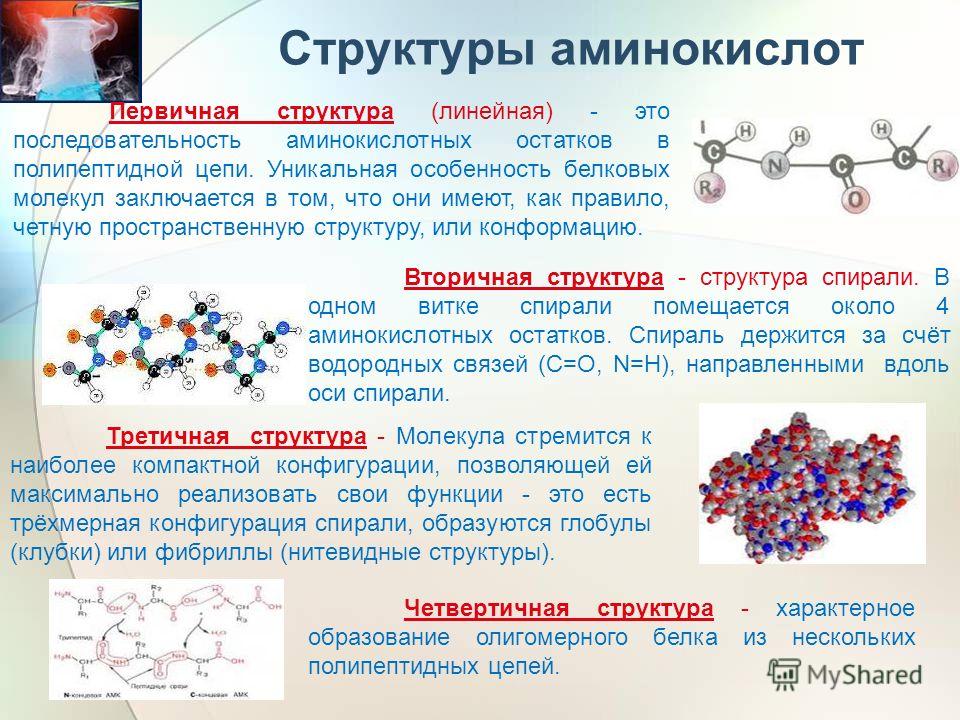
2. Если на одном конце логарифмической шкалы отложить самое маленькое известное расстояние во Вселенной, а на другом – самое большое, то посередине окажется… песчинка. Её диаметр – 0.1 мм.
3. Если положить в ряд 400 млрд песчинок, их ряд обогнёт весь земной шар по экватору. А если собрать эти же 400 млрд в мешок, весить он будет около тонны.
4. Толщина человеческого волоса – 50–70 микронам, то есть их 15–20 штук на миллиметр. Для того чтобы выложить ими расстояние до Луны, потребуется 8 триллионов волос (если складывать их не по длине, а по ширине, конечно). Поскольку на голове у одного человека их около 100 тысяч, то если собрать волосы у всего населения России, до Луны хватит с лихвой и даже еще останется.
5. Размер бактерий – от 0.5 до 5 микрон. Если увеличить среднюю бактерию до такого размера, что она удобно ляжет нам в ладонь (в 100 тысяч раз), толщина волоса станет равной 5 метрам.
6. Кстати, внутри человеческого тела обитает целый квадриллион бактерий, а их общий вес составляет 2 килограмма.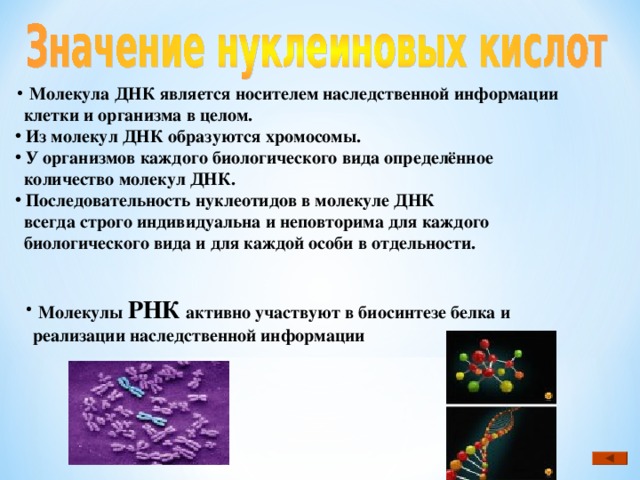 (-35) метра. Давайте проделаем наш стандартный «увеличительный» эксперимент в последний раз. Квантовая струна становится удобного размера, и мы держим ее в руке как карандаш. При этом нейтрино будет в 7 раз больше Солнца, а атом водорода в 300 раз превысит размеры Млечного Пути.
(-35) метра. Давайте проделаем наш стандартный «увеличительный» эксперимент в последний раз. Квантовая струна становится удобного размера, и мы держим ее в руке как карандаш. При этом нейтрино будет в 7 раз больше Солнца, а атом водорода в 300 раз превысит размеры Млечного Пути.
20. Наконец мы подошли к самой структуре мироздания – масштабу, на котором пространство становится похожим на время, время на пространство, и происходят разные другие причудливые штуки. Дальше уже ничего нет (наверное)…
Александр Таранов 06.08.2015
Понравился пост?
Поддержи Фактрум, нажми:
Большинство людей уверены, что физика — дело скучное и имеющее отдаленное отношение к жизни. Даже зная, что многим явлениям в ней есть именно научное объяснение, они считают понимание природы каждого из них доступным только специалистам.
На самом деле физика — не только уравнения, формулы и схемы. А изучающие ее люди отнюдь не покрытые книжной пылью существа. и ученых, занимающихся этой наукой, тому подтверждение.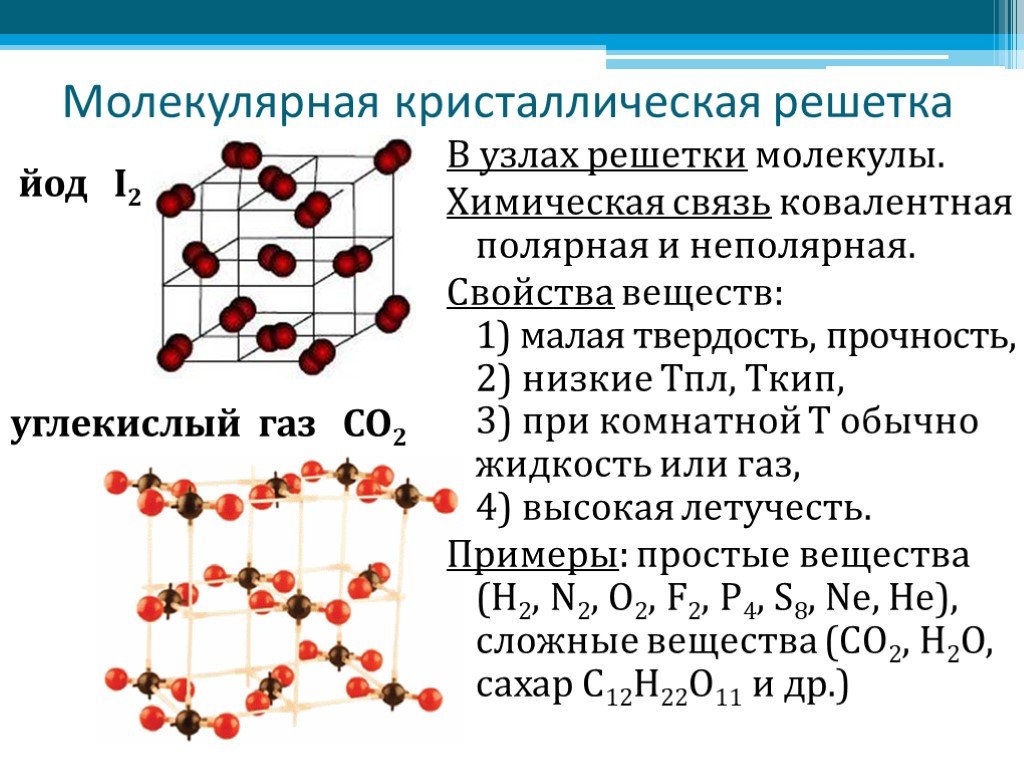
Бывает ли физика интересной?
Все, что есть на Земле и за ее пределами, подчиняется физическим законам. Люди не задумываются об этом, но пользуются в повседневной жизни. Например, всем известно, что не стоит купаться в реке в грозу, потому что нужно бояться удара молнии. Но ведь она опасна и на открытом сухом пространстве. Что же страшного именное в воде? А то, что она отлично проводит электричество, но только благодаря содержащимся примесям, ионам минеральных солей. Сами молекулы воды ток не воспринимают, но об этом несведущие люди не имеют представления. Хотя вряд ли знание подобных интересных фактов о физике сподвигло бы их наполнять бассейны дистиллированной жидкостью и купаться в грозу.
Любой человек хоть раз в жизни ездил в лифте. И многим приходила в голову мысль о том, что делать, если он начнет падать с высоты. Большинство решили бы, что в таких обстоятельствах шансов выжить нет. Или что в момент удара необходимо подпрыгнуть. На самом деле рассчитать это время нереально.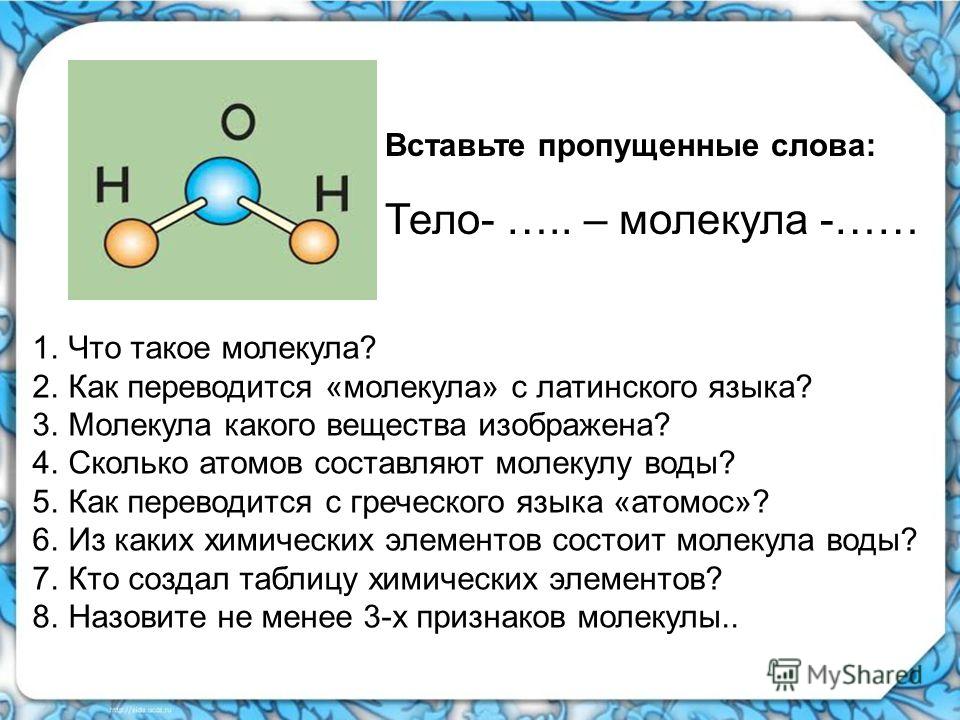 Но если сделать так, чтобы сила удара пришлась на как можно большую площадь поверхности тела, возможно, все обойдется. То есть попросту нужно лечь на пол. Как видно, интересные факты о физике способны спасти жизнь.
Но если сделать так, чтобы сила удара пришлась на как можно большую площадь поверхности тела, возможно, все обойдется. То есть попросту нужно лечь на пол. Как видно, интересные факты о физике способны спасти жизнь.
Иногда законы науки выглядят как чудо. Например, при открывании бутылки, запечатанной пробкой, о стену. Если прикрыть последнюю свернутой бумагой и ударить о нее дном сосуда строго под углом в 90 градусов, затычка выйдет настолько, что ее будет можно вынуть без штопора. Это возможно благодаря резкому изменению скорости потока жидкости в бутылке из-за столкновения со стеной. Удар приходится как раз на пробку.
Не пропусти! Интересные факты о грибах
А чтобы умельцы открывать бутылки и опустошать их в большом количестве знали в этом меру, Пифагор в свое время придумал особую кружку. Заполнить ее жидкостью можно только до определенного уровня. Все, что выше, вытекает наружу. Подобное возможно благодаря имеющейся внутри кружки изогнутой трубке, один край которой раскрыт со стороны дна, а другой имеет выход внутрь.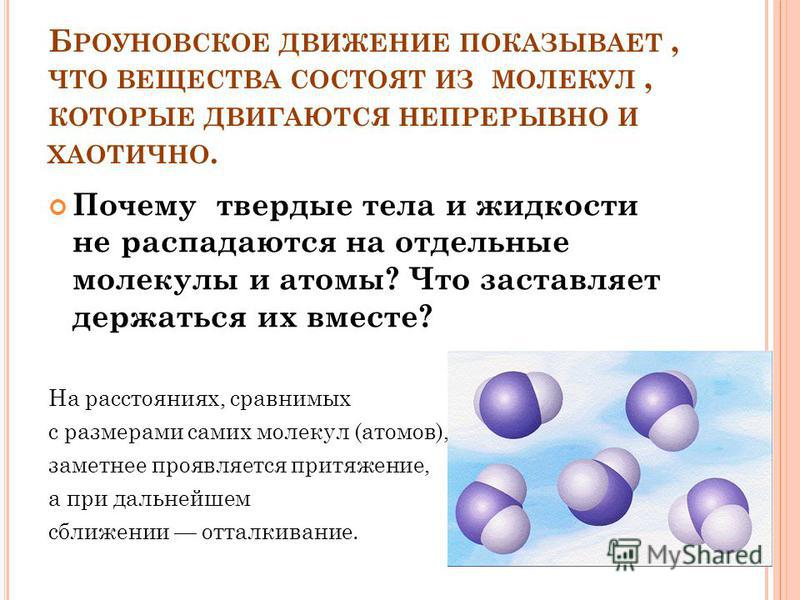 Это ничто иное как закон о сообщающихся сосудах, открытый Паскалем.
Это ничто иное как закон о сообщающихся сосудах, открытый Паскалем.
«Физик» — это звучит гордо
Изучающие эту науку люди обладают не только высоким интеллектом и интересом к необычному, но и самоотверженностью, чувством юмора и тягой к прекрасному. Свидетельства тому — :
- Кто мог предположить, что портреты нобелевских лауреатов, написанные великим художником, могут стоить мешок пшена? А ведь такое было в 1921 году. Позировали будущие знаменитые ученые Петр Капица и Николай Семенов, а писал Борис Кустодиев. Гонорар, переданный художнику, будущие светила науки заработали на ремонте мельницы. К Кустодиеву молодые ученые пришли потому, что считали именно его, пишущего портреты знаменитостей, достойным запечатлеть их самих;
- Есть физик, имеющий награды за самое замечательное и самое нелепое открытия в науке. Это голландец Андрей Гейм, который в 2000 году получил Шнобелевскую премию за изучение левитации лягушек и в 2010 Нобелевскую за открытие свойств графена;
- Среди интересных фактов о физиках не только забавные и курьезные, но и свидетельствующие о самоотверженности ученых, преданности делу.
 Василий Петров для экспериментов по изучению электрической дуги избавился от верхнего слоя кожи на пальцах, чтобы ощущать необходимые для этого слабые токи. А Ньютон, интересуясь возможностями сетчатки, вводил в собственный глаз зонд. Так он проверял значение давления света на нее.
Василий Петров для экспериментов по изучению электрической дуги избавился от верхнего слоя кожи на пальцах, чтобы ощущать необходимые для этого слабые токи. А Ньютон, интересуясь возможностями сетчатки, вводил в собственный глаз зонд. Так он проверял значение давления света на нее.
Не пропусти! Интересные факты о фильмах
Зачет(11 ) Пересдача(3 )
Не пропусти самое интересное
Определение, примеры, факты и диаграммы
Что такое молекула
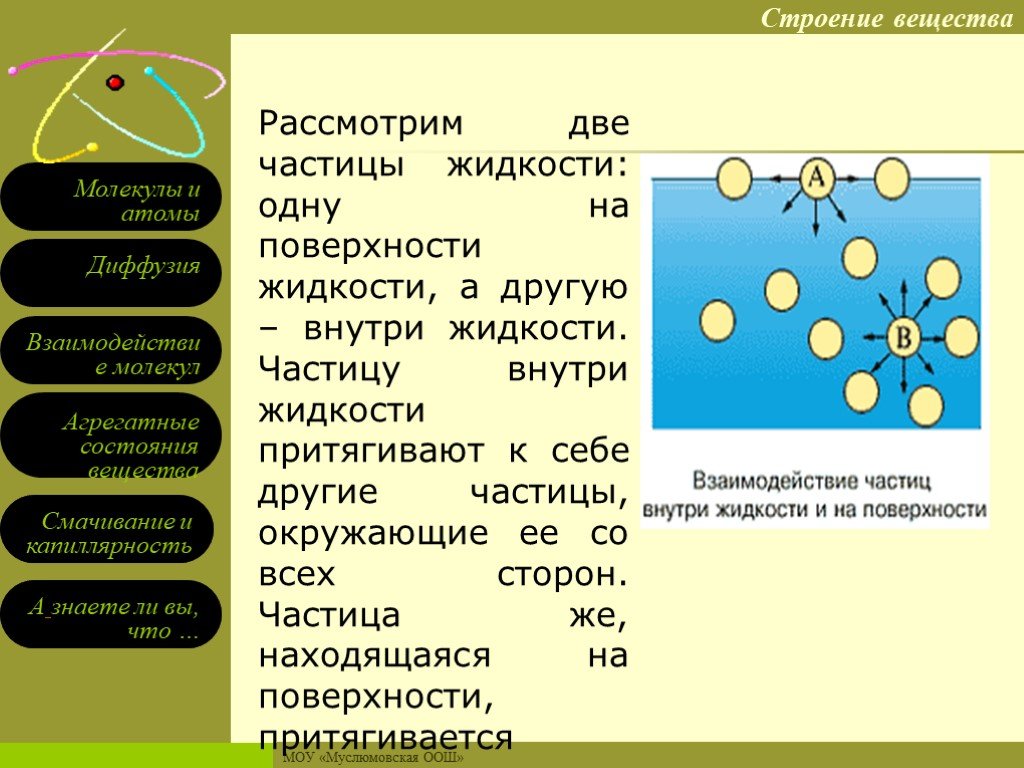
Атомы — это основные или фундаментальные единицы материи, которые редко существуют независимо друг от друга, но объединяются, образуя различные вещества. Всякий раз, когда два или более атома объединяются, они образуют молекулу. Это наименьшая единица химического вещества, обладающая всеми свойствами этого вещества. Молекулы нейтральны и не несут заряда. Если молекула распадается на более мелкие части, из нее получаются разные вещества.
Ниже показана молекула воды (H 2 О).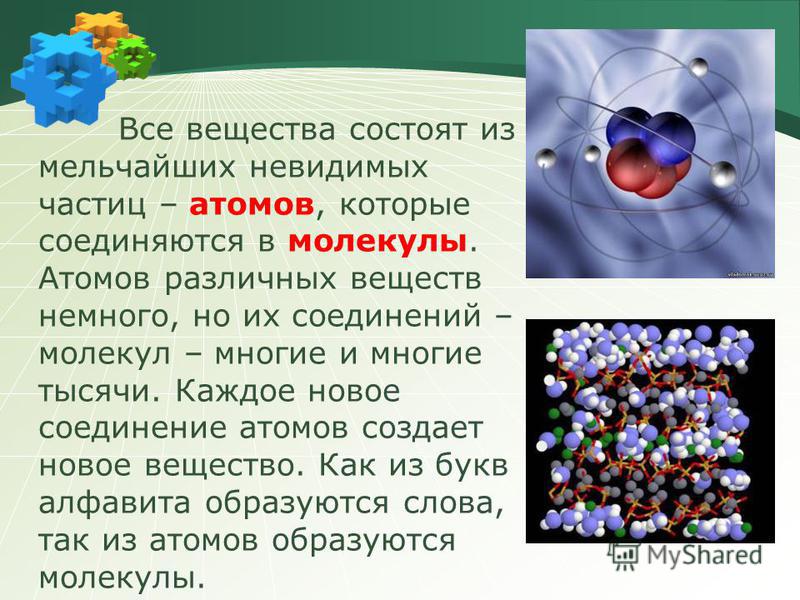
Все объекты, которые мы видим вокруг себя, состоят из молекул. Из живых объектов, таких как растения или животные, включая людей, неодушевленные предметы, такие как стул, стол, стена, дверь, окна, книги, компьютер и мобильные телефоны, состоят из молекул.
Examples
Oxygen (O 2 ), ozone (O 3 ), methane (CH 4 ), sodium chloride (NaCl), and glucose (C 6 H 12 O 6 ) — еще несколько распространенных примеров молекул.
Примеры молекулМолекулы и элементы
Элементы — это вещества, из которых состоит вся материя на Земле. Таким образом, все вещества состоят либо из чистого элемента, либо из комбинации двух или более элементов. Молекула состоит из атомов одного или нескольких элементов. Например, алюминий — это чистый элемент, молекула которого состоит из одного элемента. Точно так же молекула гелия состоит из одного атома элемента гелия. С другой стороны, молекула кислорода состоит из двух атомов элемента кислорода.
Молекулы и соединения
Иногда молекулы состоят из атомов двух или более различных элементов. Вещество, состоящее из таких молекул, называется химическим соединением. Метан является химическим соединением, поскольку его молекулы содержат один атом углерода и четыре атома водорода.
Что такое молекулярная формула
В каждом рецепте нужны ингредиенты. Когда ингредиенты смешиваются в определенной пропорции, получается блюдо. Химические вещества производятся таким же образом. Нам известно около сотни различных атомов, но мы знаем миллионы различных веществ на выходе. Как это возможно?
Это возможно, потому что каждое вещество состоит из разных типов атомов, а атомы уникальным образом объединяются в молекулы. Например, когда два атома кислорода и один атом углерода объединяются, они образуют молекулу углекислого газа, записанную как CO 2 . Опять же, молекула сахара или глюкозы с формулой C 6 H 12 O 6 состоит из шести атомов углерода, двенадцати атомов водорода и шести атомов кислорода.
Некоторыми другими примерами являются аммиак (NH 3 : один атом азота и три атома водорода), метан (CH 4 : один атом углерода и четыре атома водорода) и сахароза (C 12 H 22 O 11 : двенадцать атомов углерода, двадцать два атома водорода и одиннадцать атомов кислорода).
Таким образом, единственный способ образования конкретного вещества — это соединение точного числа и типа атомов в правильном порядке или ориентации.
Как образуются молекулы
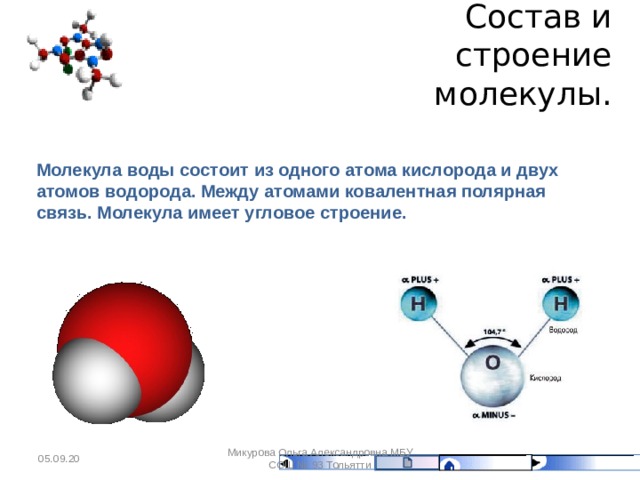
После соединения атомов крайне важно удерживать их вместе для стабильности молекулы. Силы, которые удерживают атомы в молекуле, известны как химические связи. В соединениях встречаются два основных типа химических связей: 1) ионные связи и 2) ковалентные связи. В то время как некоторые соединения имеют только один тип связи, другие обладают обоими.
В обоих типах связей участвуют электроны, представляющие собой отрицательно заряженные частицы, вращающиеся вокруг ядра по фиксированной траектории или оболочке. Оболочки в атоме следуют определенному правилу заполнения электронами, известному как правило октета. Самая внешняя оболочка играет решающую роль в образовании химической связи. Когда эта оболочка частично заполнена, атомы соединятся, чтобы заполнить оболочку электронами и сформировать химическую связь.
Оболочки в атоме следуют определенному правилу заполнения электронами, известному как правило октета. Самая внешняя оболочка играет решающую роль в образовании химической связи. Когда эта оболочка частично заполнена, атомы соединятся, чтобы заполнить оболочку электронами и сформировать химическую связь.
1) Ионные связи : Происходит, когда один участвующий атом отдает электрон другому атому. Другими словами, один атом получает электрон от другого атома, образуя стабильную молекулу или соединение.
2) Ковалентные связи : Возникают, когда два или более участвующих атома делят между собой свои электроны, образуя стабильную молекулу или соединение.
Некоторые забавные факты
- Геометрия и расположение атомов в молекуле определяют химические и физические свойства молекулы.
- Молекулы имеют широкий спектр форм, таких как длинная спираль, пирамидальная, сферическая и овальная.
- Почти 65% массы человеческого тела состоит из атомов кислорода.
 Остальные состоят из 18% углерода, 90,5% водорода и 3,2% атомов азота.
Остальные состоят из 18% углерода, 90,5% водорода и 3,2% атомов азота. - Белки, липиды, углеводы и нуклеиновые кислоты — это биологические молекулы, формирующие структуру нашего организма.
- ДНК, тип нуклеиновой кислоты, представляет собой длинную спиральную молекулу, содержащую информацию о живом существе.
- Идеальный алмаз — это молекула, состоящая из множества атомов углерода, расположенных в определенном порядке.
Часто задаваемые вопросы
Q1. В чем разница между атомом и молекулой?
Ответ . Разница в том, что атом — это самая маленькая и самая фундаментальная единица материи, которая может существовать независимо. Молекула, с другой стороны, состоит из двух или более атомов.
Q2. В чем разница между молекулой и соединением?
Ответ . Разница в том, что молекула представляет собой группу из двух или более атомов, удерживаемых вместе химическими связями. Напротив, соединение представляет собой вещество, образованное двумя или более различными типами элементов, объединенными в фиксированном соотношении.
Напротив, соединение представляет собой вещество, образованное двумя или более различными типами элементов, объединенными в фиксированном соотношении.
Список литературы
Последний раз статья была рассмотрена 12 февраля 2021 г.
Что такое молекула?
К
- Гэвин Райт
Молекула – это два или более атома, соединенных химическими связями, которые образуют наименьшую единицу вещества, сохраняющую состав и свойства этого вещества. Молекулы составляют основу химии. Молекулы отмечены символом элемента и нижним индексом с количеством атомов.
Атомы являются основной единицей элемента. Они состоят из ядра и окружающих его электронов. Когда атом имеет неполную электронную оболочку, говорят, что он имеет валентные электроны. Когда два или более атома объединяются, чтобы разделить валентные электроны внешней оболочки, образуется химическая (ковалентная) связь, и они переходят в более низкое энергетическое состояние. Когда атомы связываются, энергия высвобождается в экзотермической реакции. Если ковалентная связь разорвана и молекула расщеплена, она требует затрат энергии и, таким образом, является эндотермической.
Когда два или более атома объединяются, чтобы разделить валентные электроны внешней оболочки, образуется химическая (ковалентная) связь, и они переходят в более низкое энергетическое состояние. Когда атомы связываются, энергия высвобождается в экзотермической реакции. Если ковалентная связь разорвана и молекула расщеплена, она требует затрат энергии и, таким образом, является эндотермической.
Двухатомные молекулы — это когда объединяются только два атома. Примером двухатомной молекулы является монооксид углерода (СО), состоящий из одного атома углерода и одного атома кислорода. Если два атома представляют собой один и тот же элемент, он называется гомоядерной двухатомной молекулой , такой как кислород (O 2 ) и азот (N 2 ). Многоатомные молекулы имеют более двух атомов, например вода (H 2 O) и углекислый газ (CO 2 ). Более крупные молекулы называются полимерами и может состоять из тысяч атомов.
Атомы могут объединяться в молекулы разными способами.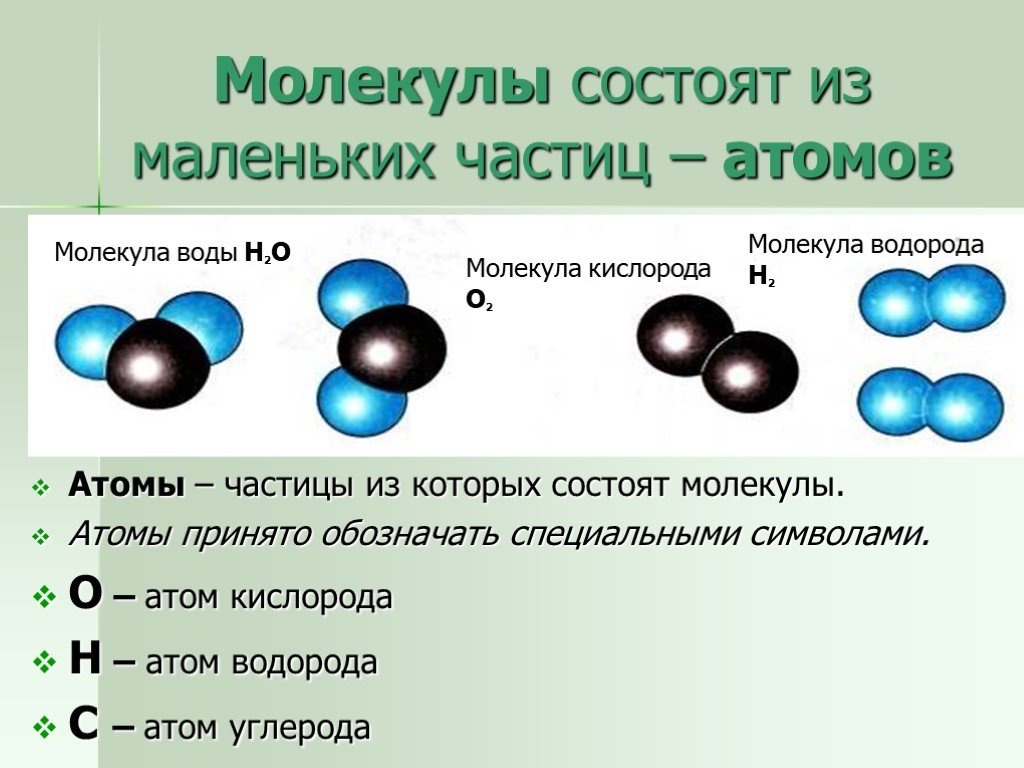 Одни и те же атомы могут соединяться в разных пропорциях, образуя разные молекулы. Например, два атома водорода и один атом кислорода образуют воду (H 2 O), а два атома водорода и два атома кислорода образуют перекись водорода (H 2 O 2 ). Также возможно сочетание одних и тех же элементов в тех же пропорциях, но в другой физической конфигурации. Физическая структура молекулы может определять ее свойства. Примером может служить вода: два атома водорода, расположенные на расстоянии 120 градусов друг от друга, создают небольшой направленный электрический заряд, придающий воде способность растворяться.
Одни и те же атомы могут соединяться в разных пропорциях, образуя разные молекулы. Например, два атома водорода и один атом кислорода образуют воду (H 2 O), а два атома водорода и два атома кислорода образуют перекись водорода (H 2 O 2 ). Также возможно сочетание одних и тех же элементов в тех же пропорциях, но в другой физической конфигурации. Физическая структура молекулы может определять ее свойства. Примером может служить вода: два атома водорода, расположенные на расстоянии 120 градусов друг от друга, создают небольшой направленный электрический заряд, придающий воде способность растворяться.
Молекулярная масса молекулы представляет собой сумму атомных масс всех составляющих ее атомов. Число Авогадро (6,02214076 × 10 23 ) — это число молекул, которое составляет атомный вес молекулы в граммах (г). Например, вода — это два атома водорода массой 1 г каждый и один атом кислорода массой 16 г, а это означает, что один моль молекул воды весит 18 г.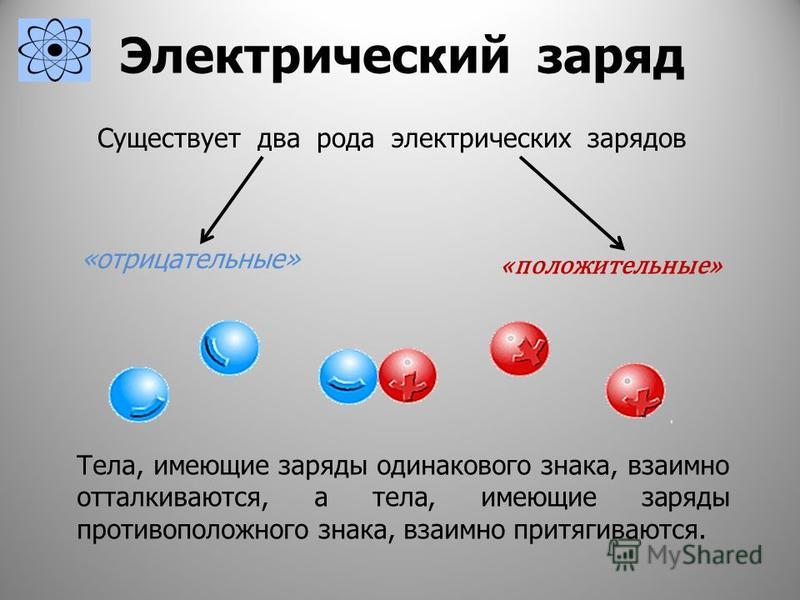
Слово «молекула» происходит от латинского molecula , означающего единицу массы. Это название должно было охватывать его первоначальное значение «наименьшая единица вещества, которая все еще сохраняет свойства этого вещества». В 1873 году Джеймс Максвелл определил атом и молекулу: «Атом — это тело, которое нельзя разрезать пополам; молекула — это наименьшая возможная часть определенного вещества». Поскольку молекулы были названы до того, как была открыта их истинная природа, это привело к тому, что сейчас определение является неточным и обсуждаемым.
Молекулы составляют основу химии
Немолекулярные соединенияМногие соединения не подходят под строгое определение молекулы, но широко распространены в химии и повседневной жизни. Некоторыми примерами структур, не являющихся молекулярными по своей природе, являются кристаллы, минералы и металлы.
Благородные газы — это элементы, не имеющие валентных электронов и, следовательно, не нуждающиеся в образовании ковалентных связей, чтобы стать стабильными. Некоторые могут считать их молекулой, состоящей всего из одного атома.
Некоторые могут считать их молекулой, состоящей всего из одного атома.
В солях и ионных связях нет обычных ковалентных связей, поэтому они не считаются молекулами. Например, поваренная соль (хлорид натрия) образует решетчатую структуру, удерживаемую ионными связями. В ионной связи электроны могут быть общими для многих атомов, а не только для двух, как в ковалентной связи. Эти химические связи не приводят к четкому разделению отдельных молекул. Эти химические структуры выражаются в виде соотношений составляющих их элементов.
Металлы не используют ковалентные связи и не считаются молекулами. Вместо этого они образуют металлические связи, в которых свободные валентные электроны распределяются между всеми различными атомами в делокализованных электронных облаках. Электроны могут свободно перемещаться по всей структуре, а не быть локализованными.
See also: matter , gas , solid , plasma and liquid .
Последнее обновление: июнь 2022 г.
Продолжить чтение о молекуле- Молекулярная память может повысить плотность жесткого диска
- Что нужно знать о хранении данных ДНК сегодня
- Стохастические точечные процессы и их практическое значение
- Технология AI COVID-19 поддерживает социальное дистанцирование и цепочки поставок
- Исследователи NUS разработали устройство памяти на основе мозга
словарь данных
Словарь данных — это набор описаний объектов данных или элементов в модели данных, на которые могут ссылаться программисты и другие лица.
Сеть
- доступность сети
Доступность сети — это время безотказной работы сетевой системы в течение определенного интервала времени.
- NFV MANO (управление и оркестрация виртуализации сетевых функций)
NFV MANO (управление виртуализацией и оркестровкой сетевых функций), также называемый MANO, представляет собой архитектурную основу для .
 ..
.. - Сетевой коммутатор
Сетевой коммутатор соединяет устройства в сети друг с другом, позволяя им общаться путем обмена пакетами данных.
Безопасность
- GPS-глушение
Подавление сигналов GPS — это действие устройства, передающего частоту, для блокирования или создания помех радиосвязи.
- контрольная сумма
Контрольная сумма — это значение, представляющее количество битов в передаваемом сообщении, которое используется ИТ-специалистами для обнаружения…
- информация о безопасности и управление событиями (SIEM)
Управление информацией о безопасности и событиями (SIEM) — это подход к управлению безопасностью, который объединяет информацию о безопасности …
ИТ-директор
- FMEA (анализ видов и последствий отказов)
FMEA (анализ видов и последствий отказов) представляет собой пошаговый подход к сбору сведений о возможных точках отказа в .
 ..
.. - доказательство концепции (POC)
Доказательство концепции (POC) — это упражнение, в котором работа сосредоточена на определении того, можно ли превратить идею в реальность.
- зеленые ИТ (зеленые информационные технологии)
Green IT (зеленые информационные технологии) — это практика создания и использования экологически устойчивых вычислений.
HRSoftware
- самообслуживание сотрудников (ESS)
Самообслуживание сотрудников (ESS) — это широко используемая технология управления персоналом, которая позволяет сотрудникам выполнять множество связанных с работой …
- платформа обучения (LXP)
Платформа обучения (LXP) — это управляемая искусственным интеллектом платформа взаимного обучения, предоставляемая с использованием программного обеспечения как услуги (…
- Поиск талантов
Привлечение талантов — это стратегический процесс, который работодатели используют для анализа своих долгосрочных потребностей в талантах в контексте бизнеса .


 Василий Петров для экспериментов по изучению электрической дуги избавился от верхнего слоя кожи на пальцах, чтобы ощущать необходимые для этого слабые токи. А Ньютон, интересуясь возможностями сетчатки, вводил в собственный глаз зонд. Так он проверял значение давления света на нее.
Василий Петров для экспериментов по изучению электрической дуги избавился от верхнего слоя кожи на пальцах, чтобы ощущать необходимые для этого слабые токи. А Ньютон, интересуясь возможностями сетчатки, вводил в собственный глаз зонд. Так он проверял значение давления света на нее. Остальные состоят из 18% углерода, 90,5% водорода и 3,2% атомов азота.
Остальные состоят из 18% углерода, 90,5% водорода и 3,2% атомов азота. ..
.. ..
..