Реферат на тему Строение атома
Содержание:
- Зарождение теории строения вещества
- Атомистическая теория Дальтона
- Катодные лучи и электроны
- Ядерная модель строения атома
- Состав атомных ядер
- Изотопы
- Электронные оболочки атомов. Теория Бора
- Фотоны
- Квантовая (волновая) механика. Характеристика поведения электронов в атомах
- Заключение
| Предмет: | Химия |
| Тип работы: | Реферат |
| Язык: | Русский |
| Дата добавления: | 24.06.2019 |
- Данный тип работы не является научным трудом, не является готовой работой!
- Данный тип работы представляет собой готовый результат обработки, структурирования и форматирования собранной информации, предназначенной для использования в качестве источника материала для самостоятельной подготовки учебной работы.

Если вам тяжело разобраться в данной теме напишите мне в whatsapp разберём вашу тему, согласуем сроки и я вам помогу!
По этой ссылке вы сможете найти рефераты по химии на любые темы и посмотреть как они написаны:
| Много готовых тем для рефератов по химии |
Посмотрите похожие темы возможно они вам могут быть полезны:
| Карбоновые кислоты |
| Коррозия металлов |
| Нефть – основное сырье для получения топлива и горюче – смазочных материалов |
| Лайнус Полинг |
Введение:
Атомизм-современная теория строения материи-произошел из Древней Греции. Древнегреческих мыслителей интересовал, казалось бы, абстрактный вопрос: Можно ли разделить проблему на бесконечно малые части или даже больше?
Основная идея древнегреческого философа согласно воззрениям Платона и Аристотеля была основана на идее непрерывности материи.
Зарождение теории строения вещества
Идея атомизма легла также в основу натурфилософии римского поэта и философа Лукреция, жившего в I веке до н. э. Он написал знаменитую поэму” о природе вещей”, в которой подробно развил свои атомные взгляды на свойства материи. Даже если было доказано, что материя имеет атомную структуру, возникает вопрос о том, как различаются атомы различных веществ. Лукреций считал, что атомы и вещества горького вкуса имеют на поверхности зарубки, которые царапают язык, но атомы веществ приятного вкуса должны иметь гладкую поверхность.
Атомистические представления о свойствах материи не очень далеко ушли в XVIII веке от Лукреция. Европейская научная мысль, атомистические идеи на протяжении веков подкреплялись философскими идеями Платона и Аристотеля, которые не разделяли атомистических взглядов на природу материи, иногда вспоминались, но в более ранние времена приверженцы некоторых теорий строения материи искали подтверждения своим взглядам главным образом интуицией.
Но даже в этот длительный период экспериментальные работы проводились медленно и с перерывами. Например, алхимики верили, что простые металлы, такие как свинец, могут быть превращены в драгоценные металлы. Однако накопилась информация о том, как реагируют химические вещества, и были разработаны более количественные методы изучения химических реакций. Это проложило путь к новым, более осмысленным формулировкам в рамках атомизма.
Атомистическая теория Дальтона
Джон Далтон (1766-1844) большую часть своей жизни преподавал в школах и колледжах Манчестера. Возможно, потому, что сам Далтон не был химиком, он подошел к ее проблемам с другой точки зрения, чем химик своего времени. Его атомизм, опубликованный в 1803-1807 годах, был твердо основан на экспериментальных наблюдениях. Она была настолько успешной, что с этого времени заняла доминирующее положение в науке и не требовала дальнейшего пересмотра.
Основными положениями теории Далтона были:
- Каждый элемент состоит из очень маленьких частиц, называемых атомами;
- Все атомы одного и того же элемента одинаковы;
- Атомы различных элементов обладают различными свойствами, в том числе и разной массой;
- Атомы одного элемента не превращаются химической реакцией в атомы другого;
- Соединение образуется в результате сочетания атомов двух и более элементов;
- Относительное число атомов данного соединения, различные степени и сорта этих атомов всегда постоянны.

Теория Дальтона позволяет мысленно нарисовать картину строения материи. Рассмотрим элемент, состоящий из мелких частиц, называемых атомами. Атомы являются основными структурными единицами материи. Это мельчайшие частицы элемента, которые могут быть объединены с другими элементами. Соединение состоит из атомов двух или более элементов, которые образуют определенные комбинации друг с другом.
Катодные лучи и электроны
До конца XIX века в химии господствовали метафизические представления, простая проблема мельчайших частиц атома-это вопрос о разделимости последнего предела. Далтон и его современники рассматривали атомы как неразделимые объекты. Считалось, что при всех химических превращениях разрушаются и воссоздаются только молекулы, но атом остается неизменным и не может быть разделен на более мелкие части. Однако все эти предположения в то время еще не могли быть подтверждены экспериментальными данными.
В конце XIX века были сделаны только открытия, показавшие сложность строения атома и возможность изменения одних атомов при определенных условиях на другие. На основе этих открытий стало быстро развиваться учение о строении атома.
На основе этих открытий стало быстро развиваться учение о строении атома.
Первым признаком сложной структуры атома является исследование лучей катода (от отрицательно заряженного электрода или катода), которое происходит, когда разряд происходит в сильно разбавленном газе. катодный луч распространяется перпендикулярно его поверхности от катода трубки, вызывая яркое зеленое свечение в местах их падения.
Катодный луч обладает способностью легко перемещаться в подвижном теле и отклоняться от первоначального пути в магнитном и электрическом полях (последнее идет к положительно заряженной пластине). Поскольку стекло непроницаемо для них, действие катодного луча обнаруживается только внутри трубки. Изучение свойств катодного луча привело к выводу, что это поток мелких частиц, которые несут отрицательный заряд и летят со скоростью, достигающей половины скорости света.
Масса частиц и величина их заряда не зависят от природы газа, остающегося в трубке, вещества, в котором образуется электрод, или других условий эксперимента. Эти частицы называются электронами. Согласно современным представлениям, заряд электрона – это наименьший заряд, наименьшее количество электричества, которое может существовать.
Эти частицы называются электронами. Согласно современным представлениям, заряд электрона – это наименьший заряд, наименьшее количество электричества, которое может существовать.
В катодной трубке электроны отделяются от катода под действием заряда, но они также могут возникать вне связи с зарядом. Например, все металлы испускают электроны при нагревании; пламя горелки также имеет электроны; многие вещества испускают электроны под действием ультрафиолетовых, рентгеновских лучей или широкого спектра веществ, освещенных лучом (лучевой эффект), поскольку выделение электронов указывает на то, что эти частицы являются частью целого, атомы построены из более мелких структурных единиц.
В 1897 году британский физик Дж. Дж. Томпсон (1856-1940) сумел измерить отношение заряда электрона к массе, равное 1,76 * 10КЛ/г.
В 1909 году Роберт Милликен из Чикагского университета определил электронный заряд: 1,60*10КЛ. Заменив это значение отношением заряда электрона к его массе, найденным Томсоном, можно вычислить массу электрона: 1,60*10КЛ/1,76*10КЛ/г=9,11*10г.
Ядерная модель строения атома
Изучение строения атома началось практически в 1897-1898 годах, после того как была окончательно установлена природа катодного луча как электронного потока, а также определены величина заряда и масса электрона. Тот факт, что электроны были разделены самыми разнообразными веществами, привел к выводу, что электроны являются частью всех атомов.
Но поскольку весь атом электрически нейтрален, он должен содержать еще один положительно заряженный компонент, заряд которого должен уравновешивать сумму отрицательных зарядов электрона. Эта положительно заряженная часть атома была открыта в 1911 году Эрнестом Резерфордом (1871-1937). Резерфорд предложил следующую схему строения атома.
В центре атома находится положительно заряженное ядро, вокруг которого электроны вращаются по разным орбитам. Центробежные силы, возникающие при их вращении, уравновешиваются притяжением между ядром и электроном, которое удерживает некоторое расстояние от ядра.
Общий отрицательный заряд электрона численно равен положительному заряду ядра, так что весь атом электрически нейтрален. Поскольку масса электрона ничтожна, почти вся масса атома сосредоточена в его ядре. И наоборот, размер ядра также очень мал по сравнению с размером самого атома. Поэтому ясно, что доля ядер и электронов, как мы увидим далее, занимает лишь малую часть всего пространства, занимаемого атомной системой.
Состав атомных ядер
Таким образом, открытие Резерфорда положило начало ядерной теории атома. Со времен Резерфорда физики узнали много подробностей о строении атомных ядер. Самый легкий атом-это атом водорода (H). Поскольку почти вся масса атома сосредоточена в ядре, предполагается, что ядро атома водорода представляет собой элементарную частицу положительного электричества, которая называется Протоном от греческого слова “Протос”.
Следовательно, протон – это масса атома водорода (ровно 1,00728 углеродных единиц) и заряд, равный 1 (если атомы электронов тяжелых элементов содержат ядра, которые имеют больший заряд и явно имеют большую массу.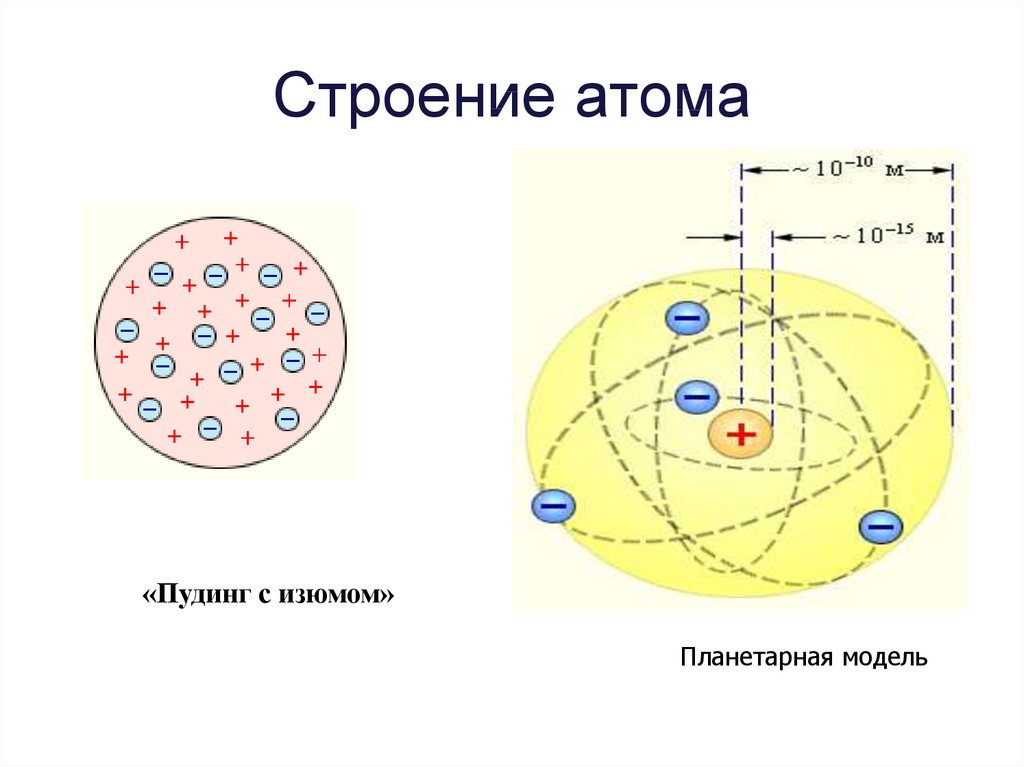
Измерение заряда атомного ядра показало, что заряд ядра атома в этих условных единицах численно равен атомному номеру или порядковому номеру элемента. Однако нельзя было предположить, что при одинаковом заряде последние неизбежно будут отталкиваться друг от друга, в результате чего такое ядро станет неустойчивым.
Кроме того, масса атомного ядра была в два и более раза больше общей массы протонов, что обуславливало заряд атомного ядра соответствующего элемента. Тогда ядро атома содержит число протонов, большее,чем атомное число элементов, и избыточный положительный заряд ядра, полученный таким образом, эти электроны, дополненные электронами, входящими в состав ядра, должны, очевидно, удерживать протоны отталкивающимися друг от друга в ядре.
Однако это предположение пришлось отвергнуть, поскольку нельзя было допустить сосуществования тяжелых (протонов) и легких (электронов) частиц в компактном ядре.
В 1932 году Чедвик открыл элементарные частицы без заряда, поэтому их назвали нейтронами. Масса нейтронов несколько больше массы протонов (ровно 1,008665 в углеродных единицах). После этого открытия Д. Д. Иваненко, Е. Н. Гапон, В. Гейзенберг самостоятельно предложили общепринятую теорию состава атомных ядер. Согласно этой теории, атомное ядро всех элементов (кроме водорода) состоит из протонов и нейтронов.
Масса нейтронов несколько больше массы протонов (ровно 1,008665 в углеродных единицах). После этого открытия Д. Д. Иваненко, Е. Н. Гапон, В. Гейзенберг самостоятельно предложили общепринятую теорию состава атомных ядер. Согласно этой теории, атомное ядро всех элементов (кроме водорода) состоит из протонов и нейтронов.
Число протонов в ядре определяет величину его положительного заряда, а также общее число протонов и нейтронов (величину их массы). Ядерные частицы – протоны и нейтроны – объединяются под общим названием нуклоны. Итак, число протонов соответствует атомному номеру элемента, а общее число нуклонов – это масса атома, сосредоточенного в атомном ядре, его массовое число, то есть округленное до ближайшей целой массы атома А:
N=AZ
Таким образом, протонно-нейтронная теория позволила разрешить ранее возникшие противоречия в концепции взаимосвязи состава атомного ядра с его порядковым номером и атомной массой.
Изотопы
Протонно-нейтронная теория позволила разрешить еще одно противоречие, возникшее при формировании теории атомов. Если предположить, что ядро элемента состоит из некоторого числа нуклонов, то атомная масса всех элементов должна быть выражена целым числом.
Если предположить, что ядро элемента состоит из некоторого числа нуклонов, то атомная масса всех элементов должна быть выражена целым числом.
Для многих элементов это верно, но небольшое отклонение от целого числа можно объяснить недостаточной точностью измерения. Однако для некоторых элементов значение атомной массы является целым числом, которое уже нельзя объяснить неточностью измерений и другими случайными причинами, например, атомная масса хлора (CL) равна 35,45. Оказалось, что около трех четвертей атомов хлора, присутствующих в природе, имеют массу 35, а четверть-37.
Таким образом, элементы, существующие в природе, состоят из смеси атомов с различными массами, но, очевидно, обладающих одинаковыми химическими свойствами, то есть массами различных целых чисел. Астону удалось разделить такую смесь на компоненты, называемые изотопами.
С точки зрения протонно-нейтронной теории, изотопы – это типы элементов, которые содержат разное количество нейтронов, но с одинаковым количеством протонов. Химические свойства элемента определяются числом протонов в атомном ядре и равны числу электронов в оболочке атома. Изменение числа нейтронов не влияет на химические свойства атома.
Химические свойства элемента определяются числом протонов в атомном ядре и равны числу электронов в оболочке атома. Изменение числа нейтронов не влияет на химические свойства атома.
Это позволяет сформулировать понятие химического элемента как своеобразного атома, который характеризуется специфическим зарядом ядра. Среди изотопов различных элементов были обнаружены те, которые содержат одинаковое общее число нуклонов в ядре при разном числе протонов, то есть те, в которых атомы имеют одинаковую массу.
Такой изотоп получил название Изобар. Различные химические свойства Изобары убедительно подтверждают, что свойства элемента не определяются массой его атомов. Для различных изотопов используются названия и символы самих элементов, указывающие на массовое число, следующее за названием элемента, или в качестве индекса в верхнем левом углу символа(например, хлор-35 различных изотопов отличается своей стабильностью.
Такой элемент называется моноизотопным, характеризуется главным образом нечетным числом атомов, а его атомная масса приблизительно равна целому числу. 55 элементов имеют некоторые стабильные изотопы – их называют полиизотопными, большое количество изотопов характерно для элементов преимущественно четных чисел.
55 элементов имеют некоторые стабильные изотопы – их называют полиизотопными, большое количество изотопов характерно для элементов преимущественно четных чисел.
Для других элементов известны только нестабильные радиоактивные изотопы. Это все тяжелые элементы, начиная с элемента № 84 (полоний) и относительно легких элементов №43 (технеций) и № 61 (прометий).
Однако радиоизотопы некоторых элементов относительно стабильны, характеризуются длительным периодом полураспада, и поэтому большинство из них, например торий и уран, содержат большое количество радиоизотопов стабильных элементов, радиоактивные изотопы которых получают искусственным путем.
Электронные оболочки атомов. Теория Бора
Согласно теории Резерфорда, каждый электрон вращается вокруг ядра, и притяжение ядра уравновешивается центробежной силой, возникающей при вращении электрона. Вращение электрона в точности совпадает с его быстрыми колебаниями, которые должны вызывать испускание электромагнитных волн.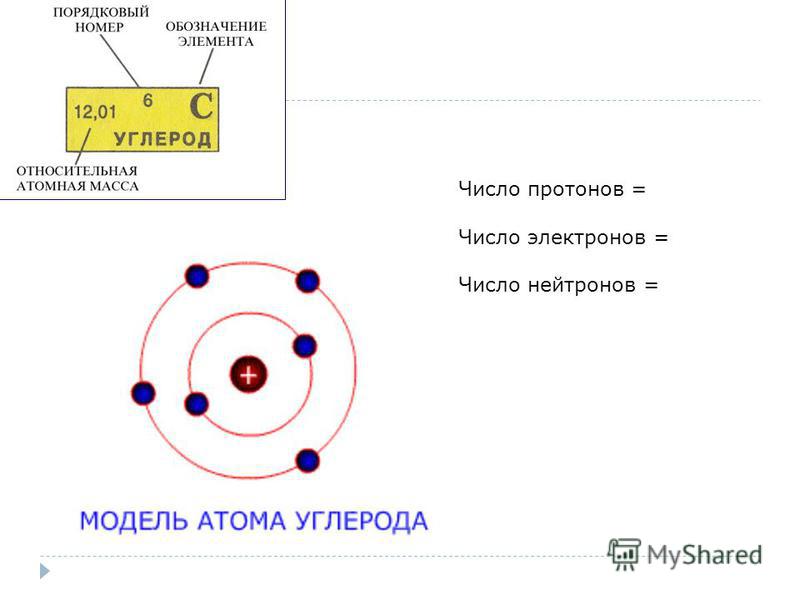
Таким образом, можно предположить, что вращающиеся электроны излучают свет определенной длины волны, зависящей от частоты орбиты электрона. Но когда электрон испускает свет, он теряет часть своей энергии, и равновесие между ним и ядром нарушается.
Чтобы восстановить равновесие, электроны должны постепенно приближаться к ядру, причем частота циркуляции электронов и характер испускаемого ими света также постепенно меняются. В конце концов, исчерпав всю энергию, электроны должны “упасть” в ядро, и свечение прекратится. Если такое непрерывное изменение в движении электронов действительно имело место, то его “распад” над ядром означает разрушение атома и его прекращение.
Таким образом, визуальная и простая ядерная модель атома, предложенная Резерфордом, была явно несовместима с классической электродинамикой. Электронная система, вращающаяся вокруг ядра, не является стабильной, так как электроны в этом вращении должны непрерывно высвобождать энергию. С другой стороны, атом-это стабильная система.
Эти существенные противоречия были частично разрешены выдающимся датским физиком Нильсом Бором (1885-1962), который в 1913 году разработал теорию атомов водорода на основе специального предположения, а суть классической квантовой теории заключается в том, что энергия не непрерывно высвобождается и поглощается, а является небольшой, но четко определенной частью энергетического тела, которая, как было принято ранее, является накопителем энергии, изменяющейся квант за квантом. Величина кванта энергии зависит от частоты излучения:чем выше частота излучения, тем больше величина кванта.
Фотоны
Квант лучистой энергии также называют фотоном. Применяя понятие кванта к вращению электронов вокруг ядра, Бор основывал свою теорию на очень смелом предположении, или постулате. Эти допущения противоречат законам классической электродинамики, но в полном согласии, обнаруженном между теоретическим результатом и огромным количеством экспериментальных фактов, они сводятся к следующим допущениям: электроны могут двигаться только в определенных условиях, вытекающих из квантовой теории, а не по произвольным орбитам.
Эти орбиты называются стабильными, стационарными или квантовыми. Когда электрон движется по одной из своих возможных стабильных орбит, он не испускает электромагнитной энергии. Переход электронов с дальней орбиты на близкую сопровождается потерей энергии. Энергия, теряемая атомом при каждом переходе, преобразуется в один квант лучистой энергии.
Частота испускаемого света в этом случае определяется радиусом двух орбит, по которым проходят электроны. Показано, что энергия атома в положении электрона через E ‘приближается к более удаленной орбите от ядра через E’, а потерянная энергия E ‘–E ‘ является постоянной Планка: =(Eí-Eǐ) / ч
Чем больше расстояние от орбиты, на которой находится электрон, до орбиты, по которой он проходит, тем больше частота излучения. Простейший из атомов-это атом водорода, вокруг ядра которого вращается только один электрон.
Исходя из вышеизложенного предположения, Бор вычислил радиусы возможных орбит этого электрона и выяснил, что они связаны как квадраты натуральных чисел: 1:2:3. .. значение n, n, называется главным квантовым числом.
.. значение n, n, называется главным квантовым числом.
В дальнейшем теория Бора была распространена на атомную структуру других элементов, но это было связано с некоторыми трудностями, обусловленными ее новизной. Она решает очень важные задачи, касающиеся расположения электронов в атомах различных элементов, устанавливает зависимость свойств элементов от строения электронных оболочек их атомов.
Однако следует отметить, что все эти схемы являются более или менее надежными гипотезами, позволяющими объяснить многие физико-химические свойства элементов. Как уже упоминалось ранее, число электронов, вращающихся вокруг ядра атома, соответствует порядковому номеру элемента в периодической таблице.
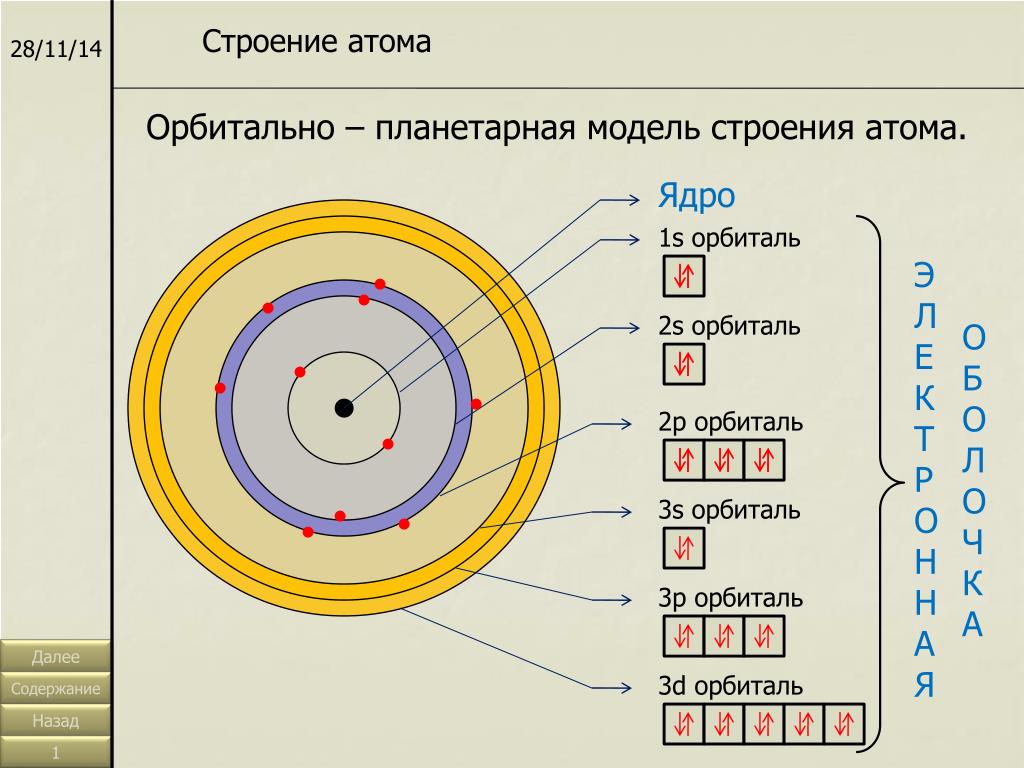
Электроны располагаются слоями, то есть каждый слой имеет определенное количество электронов, которые встречаются или насыщают его. Электроны одного и того же слоя имеют примерно одинаковый запас энергии, то есть находятся почти на одном энергетическом уровне. Вся оболочка атома распадается на несколько энергетических уровней.
Электроны каждого последующего слоя находятся на более высоком энергетическом уровне, чем электроны предыдущего слоя. Максимальное число n электронов, которые могут быть расположены на данном энергетическом уровне, равно квадрату числа слоев: N=2n, где n-номер слоя.
Итак, для 1-2, для 2-8, для 3-18, кроме того, оказывается, что число электронов во внешнем слое для всех элементов, кроме палладия, не превышает восьми, а в предпоследнем слое–восемнадцати. Поскольку электроны во внешнем слое находятся наиболее далеко от ядра, они не связаны с ядром наиболее сильно, так что атом, отделившийся от атома и связанный с другими атомами и потерявший один или несколько электронов, образующих часть внешнего слоя последнего, становится положительно заряженным, так как заряд ядра атома превышает сумму зарядов остальных электронов.
И наоборот, атомы, которые присоединяют электроны, заряжены отрицательно. Образовавшиеся таким образом заряженные частицы называются ионами, которые качественно отличаются от соответствующих атомов. Многие ионы могут потерять или присоединить электрон, превратившись в электрон-нейтральный атом или в новый с другим зарядом.
Многие ионы могут потерять или присоединить электрон, превратившись в электрон-нейтральный атом или в новый с другим зарядом.
Квантовая (волновая) механика. Характеристика поведения электронов в атомах
Теория Бора оказала большую услугу физике и химии. Однако в этой области все еще было много явлений, которые теория Бора не могла объяснить. Движение электронов в атоме Бор описывал в некоторой степени как простое механическое движение, но оно очень сложное и своеобразное.
Особенность движения электронов была раскрыта новой теорией-квантовой, или волновой, механикой. Квантовая механика показывает, что законы движения электронов имеют много общего с законами распространения волн. Для электронов с массой m и скоростью v можно записать: =h/(m * v), где-длина волны осколков, а h-постоянная Планка.
Заключение
Атомы различных элементов характеризуются определенным значением заряда ядра и равным числом электронов, распределенных по энергетическому уровню.
Основное квантовое число n определяет энергетический уровень, которому соответствует эта орбита, и расстояние от ядра. Это число может принимать значение нескольких натуральных чисел (в реальных атомах от одного до семи).
Орбитальное, латеральное или азимутальное квантовое число l характеризует момент количества движения электронов относительно центра орбиты. Она определяет форму электронного облака (форму орбиты), его непрерывность или прерывистость, а также его удлинение. Принимает целочисленные значения от 0 до (n-1). Для заданного значения n, n различных орбиталей, то есть числа значений l, определяют число атомарных орбиталей. Магнитное квантовое число М определяет положение плоскости орбиталей электронов в пространстве или, по выражению волновой механики, направление, в котором растягивается электронное облако. L l (включая 0), Total (2*l+1) может принимать целочисленные значения. Число M-значений определяет число орбит данного (s-,p-,d-,f-типа).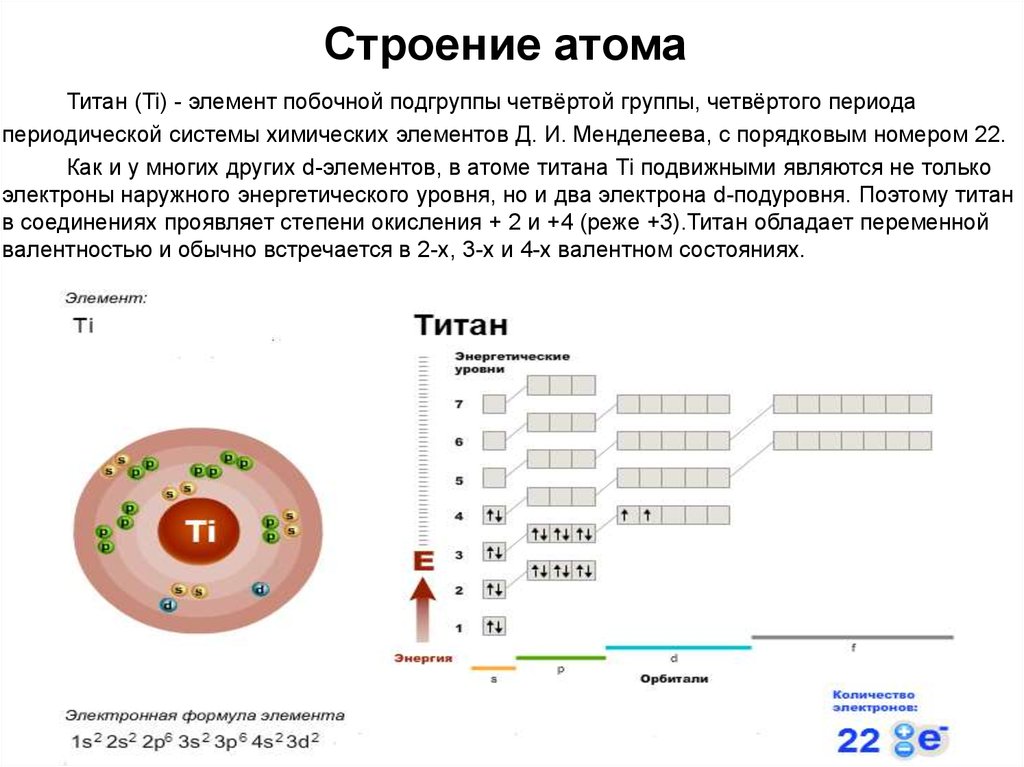
Спиновое квантовое число s определяет направление вращения электрона и может принимать только два значения: 1/2 и – 1/2. Поведение атомов в химических реакциях во многом зависит от того, насколько плотно электроны удерживаются на своих орбитах, поэтому трудно изучать распределение электронов в них.
Реферат – Строение атома
Реферат
- формат doc
- размер 92.5 КБ
- добавлен 03 июля 2011 г.
Москва 2009. стр. 10.
Введение.
Глава I. История атома. Исследования Резерфорда Эрнеста.
Исследования Нильса Бора. Глава II. Строение атома Природа
электричества. Электрон Свойства электрона.
 Ядра атомов. Атомная орбиталь. Атомная орбиталь
пространство вокруг ядра, в котором наиболее вероятно нахождение
электрона. Заключение.
Ядра атомов. Атомная орбиталь. Атомная орбиталь
пространство вокруг ядра, в котором наиболее вероятно нахождение
электрона. Заключение.Смотрите также
- формат pdf
- размер 189.25 КБ
- добавлен 05 июня 2010 г.
Для учащихся выпускных классов школ и лицеев с углублённым изучением естественных наук. Одесский государственный университет им И. И. Мечникова Учебно-производственный центр “Интеллект” Ришельевский лицей Корпускулярные свойства электромагнитного излучения Модели атома Томпсона, Резерфорда, Бора Гипотеза де-Бройля Соотношение неопределённостей Квантовая теория атома водорода, многоэлектронные атомы
- формат doc
- размер 218.5 КБ
- добавлен 04 мая 2011 г.
Электроны и протоны. Модели атома. Опыт Д. Томсона. Опыт Э. Резерфорда. Строение атомного ядра. Субатомные частицы. Элементы. Изотопы. Атомные веса природных элементов. Изотопный состав элементов. Дефект массы. Электронное строение атома. Средняя школа № 71
Модели атома. Опыт Д. Томсона. Опыт Э. Резерфорда. Строение атомного ядра. Субатомные частицы. Элементы. Изотопы. Атомные веса природных элементов. Изотопный состав элементов. Дефект массы. Электронное строение атома. Средняя школа № 71
- формат djvu
- размер 22.23 МБ
- добавлен 29 августа 2010 г.
В трех частях. Часть 3, 12-е изд. М.: Учпедгиз, 1965. – 385 с. В этой части учебника рассмотрены следующие темы: Раздел Электричество Значение учения об электрических явлениях для современной науки и техники Главы: Электрические заряды и электрическое поле. Постоянный электрический ток. Магнитное поле и электромагнитная индукция Переменный ток Электромагнитные колебания и волны. Раздел Оптика и строение атома Главы: Распространение света. Отр…
- формат pdf
- размер 19 МБ
- добавлен
29 января 2011 г.

Механика. Молекулярная физика. Основы электродинамики. Оптика. Квантовые свойства света. Строение атома. Тесты для итогового контроля. Ответы на тесты.
Реферат
- формат doc
- размер 13.24 КБ
- добавлен 23 октября 2011 г.
Феномен атома. Модель атома Резерфорда. Создание модели атома: квантовая теория и спектроскопия. Атомная энергетика. Радиоактивность: ее открытие и природа. Получение ядерной энергии. Ядерные реакторы: классификация. Термоядерная энергия – основа энергетики будущего. Атомное оружие. Современные атомные бомбы и снаряды. Современные термоядерные бомбы и снаряды. «Чистая» водородная бомба. Атом и экология.
Реферат
- формат doc
- размер 88.
 5 КБ
5 КБ - добавлен 24 января 2011 г.
Донецк, стр. 12. Развитие идеи о планетарной модели атома. Краткие исторические сведения. Электроны и позитроны. Открытие нейтрона. Открытие мезона.
Реферат
- формат doc
- размер 102.5 КБ
- добавлен 07 мая 2011 г.
Реферат для школы – 10 класс План Введение. Движение луны. Форма Луны. Фазы Луны. Поверхность Луны. Рельеф лунной поверхности. Происхождение Луны. Новый этап исследования Луны. Человек на Луне. Лунный грунт. Внутреннее строение Луны Международно-правовые проблемы Полеты космических кораблей Аполлон Использованная литература
Реферат
- формат rtf
- размер 115.
 5 КБ
5 КБ - добавлен 24 августа 2011 г.
Реферат по астрономии. 5 стр. 11 класс Содержание включает следующую информацию – Общие сведения. История открытия. Особенности вращения Урана. Химический состав, физические условия и строение Урана. Кольца Урана. Магнитосфера. Спутники Урана. Уран — седьмая планета от Солнца и третья по размеру. Интересно, что Уран хоть и больше в диаметре, но меньше массой, чем Нептун. Уран иногда едва видим невооруженным глазом в очень ясные ночи; его нетрудно…
Реферат
- формат doc
- размер 79.5 КБ
- добавлен 24 января 2011 г.
Москва. 2010 Зарождение теории строения вещества. Атомистическая теория Дальтона. Катодные лучи и электроны. Ядерная модель строения атомов. Состав атомных ядер. Изотопы. Электронные оболочки атомов. Теория Бора. Квантовая (волновая) механика. Характеристика поведения электронов в атомах.
Катодные лучи и электроны. Ядерная модель строения атомов. Состав атомных ядер. Изотопы. Электронные оболочки атомов. Теория Бора. Квантовая (волновая) механика. Характеристика поведения электронов в атомах.
- формат djvu
- размер 2.38 МБ
- добавлен 17 ноября 2010 г.
Цедрик М. С.,. Китунович Ф. Г,. Микулич А. С,. Качинский А. М Пособие по физике для поступающих в вузы. «Высшая школа» Минск 1966 279 с. Предисловие Механика Сложение и разложение сил. Условие равновесия тел Прямолинейное движение Законы Ньютона. Работа, мощность, энергия. Криволинейное движение Вращательное движение. Движение тела по окружности Механические колебания н волны. Звук Жидкости и газы Вопросы и задачи для самопроверки Теплота и мо…
Структура атома | Безграничная химия |
Обзор строения атома
Атомы состоят из частиц, называемых протонами, нейтронами и электронами, которые отвечают за массу и заряд атомов.
Цели обучения
Обсудить электронные и структурные свойства атома
Ключевые выводы
Ключевые моменты
- Атом состоит из двух частей: ядра, которое находится в центре атома и содержит протоны и нейтроны , и внешняя область атома, которая удерживает его электроны на орбите вокруг ядра.
- Протоны и нейтроны имеют примерно одинаковую массу, около 1,67 × 10-24 грамма, которую ученые определяют как одну атомную единицу массы (а.е.м.) или один дальтон.
- Каждый электрон имеет отрицательный заряд (-1), равный положительному заряду протона (+1).
- Нейтроны — это незаряженные частицы, находящиеся внутри ядра.
Ключевые термины
- атом : Наименьшее возможное количество вещества, которое все еще сохраняет свою идентичность как химический элемент, состоящий из ядра, окруженного электронами.
- протон : Положительно заряженная субатомная частица, входящая в состав ядра атома и определяющая атомный номер элемента.
 Он весит 1 а.е.м.
Он весит 1 а.е.м. - нейтрон : Субатомная частица, входящая в состав ядра атома. У него нет заряда. По массе он равен протону или весит 1 а.е.м.
Атом — это наименьшая единица вещества, сохраняющая все химические свойства элемента. Атомы объединяются, образуя молекулы, которые затем взаимодействуют, образуя твердые тела, газы или жидкости. Например, вода состоит из атомов водорода и кислорода, которые, объединившись, образуют молекулы воды. Многие биологические процессы посвящены расщеплению молекул на составные атомы, чтобы их можно было собрать в более полезную молекулу.
Атомные частицы
Атомы состоят из трех основных частиц: протонов, электронов и нейтронов. Ядро (центр) атома содержит протоны (положительно заряженные) и нейтроны (без заряда). Самые внешние области атома называются электронными оболочками и содержат электроны (отрицательно заряженные). Атомы обладают различными свойствами в зависимости от расположения и количества их основных частиц.
Атом водорода (H) содержит только один протон, один электрон и не содержит нейтронов. Это можно определить, используя атомный номер и массовое число элемента (см. понятие об атомных числах и массовых числах).
Структура атома : Элементы, такие как гелий, изображенные здесь, состоят из атомов. Атомы состоят из протонов и нейтронов, расположенных внутри ядра, с электронами на орбиталях, окружающих ядро.
Атомная масса
Протоны и нейтроны имеют примерно одинаковую массу, примерно 1,67 × 10 -24 грамм. Ученые определяют это количество массы как одну атомную единицу массы (аму) или один дальтон. Несмотря на то, что протоны имеют одинаковую массу, они заряжены положительно, а нейтроны заряда не имеют. Следовательно, количество нейтронов в атоме вносит значительный вклад в его массу, но не в его заряд.
Электроны намного меньше по массе, чем протоны, и весят всего 9,11 × 10 -28 граммов, или около 1/1800 атомной единицы массы. Следовательно, они не вносят большого вклада в общую атомную массу элемента. При рассмотрении атомной массы принято игнорировать массу любых электронов и вычислять массу атома, основываясь только на числе протонов и нейтронов.
Следовательно, они не вносят большого вклада в общую атомную массу элемента. При рассмотрении атомной массы принято игнорировать массу любых электронов и вычислять массу атома, основываясь только на числе протонов и нейтронов.
Электроны вносят большой вклад в заряд атома, так как каждый электрон имеет отрицательный заряд, равный положительному заряду протона. Ученые определяют эти заряды как «+1» и «-1». В незаряженном нейтральном атоме число электронов, вращающихся вокруг ядра, равно числу протонов внутри ядра. В этих атомах положительные и отрицательные заряды компенсируют друг друга, что приводит к атому без суммарного заряда.
Протоны, нейтроны и электроны : И протоны, и нейтроны имеют массу 1 а.е.м. и находятся в ядре. Однако протоны имеют заряд +1, а нейтроны не заряжены. Электроны имеют массу примерно 0 а.е.м., вращаются вокруг ядра и имеют заряд -1.
Изучение свойств электронов : Сравните поведение электронов с поведением других заряженных частиц, чтобы узнать свойства электронов, такие как заряд и масса.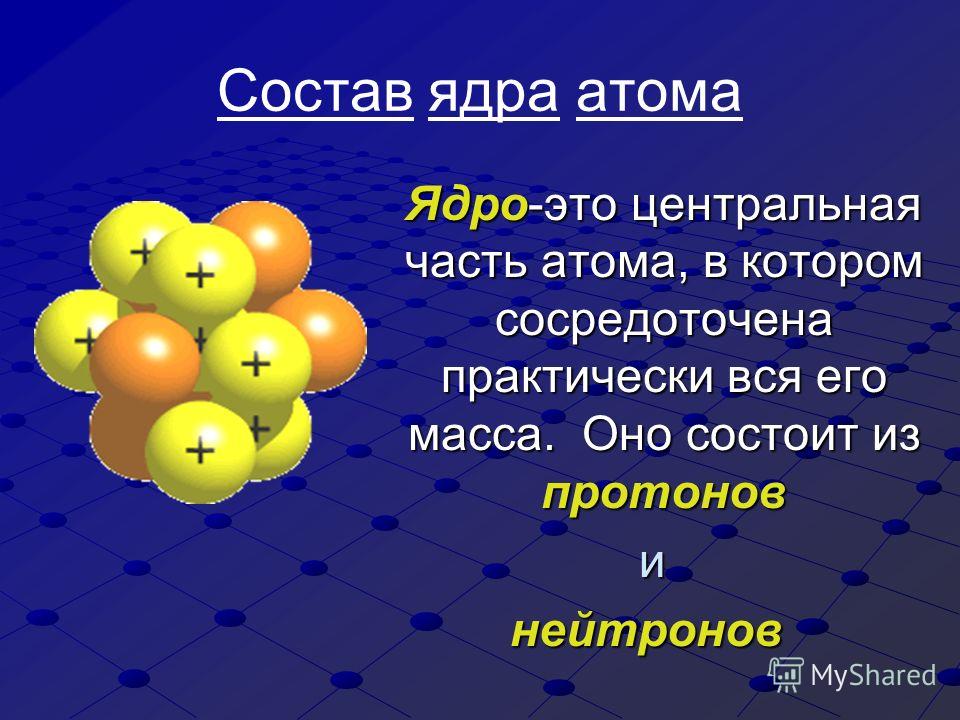
Объем атомов
Принимая во внимание размеры протонов, нейтронов и электронов, большая часть объема атома — более 99 процентов — фактически представляет собой пустое пространство. Несмотря на все это пустое пространство, твердые объекты не просто проходят друг через друга. Электроны, окружающие все атомы, заряжены отрицательно и заставляют атомы отталкиваться друг от друга, не позволяя атомам занимать одно и то же пространство. Эти межмолекулярные силы не позволяют вам провалиться сквозь такой объект, как ваш стул.
Интерактив: построй атом : построй атом из протонов, нейтронов и электронов и посмотри, как изменяются элементы, заряд и масса. Тогда сыграйте в игру, чтобы проверить свои идеи!
Атомный номер и массовое число
Атомный номер — это количество протонов в элементе, а массовое число — это количество протонов плюс количество нейтронов.
Цели обучения
Определить связь между массовым числом атома, его атомным номером, его атомной массой и числом субатомных частиц
Ключевые выводы
Ключевые моменты
- Нейтральные атомы каждого элемента содержат равное количество протонов и электронов.
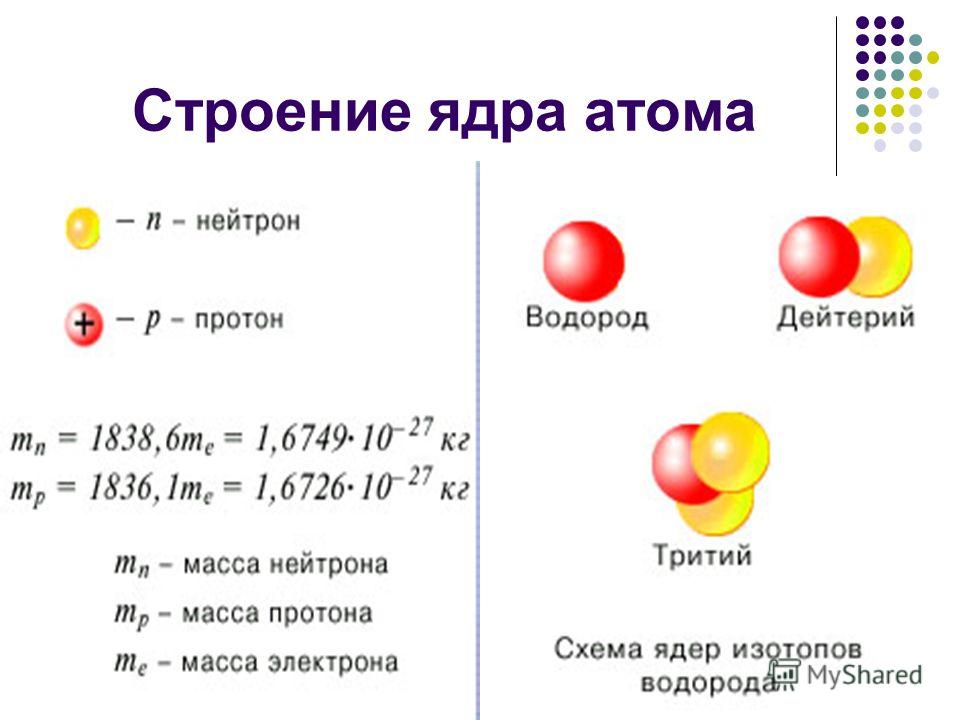
- Количество протонов определяет атомный номер элемента и используется для отличия одного элемента от другого.
- Количество нейтронов изменчиво, в результате чего изотопы, которые представляют собой различные формы одного и того же атома, различаются только количеством нейтронов, которыми они обладают.
- Вместе количество протонов и количество нейтронов определяют массовое число элемента.
- Поскольку изотопы элемента имеют немного разные массовые числа, атомная масса рассчитывается путем получения среднего значения массовых чисел для его изотопов.
Ключевые термины
- массовое число : Сумма числа протонов и числа нейтронов в атоме.
- атомный номер : Количество протонов в атоме.
- атомная масса : Средняя масса атома с учетом всех его природных изотопов.
Атомный номер
Нейтральные атомы элемента содержат равное количество протонов и электронов. Количество протонов определяет атомный номер элемента (Z) и отличает один элемент от другого. Например, атомный номер углерода (Z) равен 6, потому что у него 6 протонов. Количество нейтронов может варьироваться для получения изотопов, которые представляют собой атомы одного и того же элемента, имеющие разное количество нейтронов. Количество электронов также может быть разным в атомах одного и того же элемента, что приводит к образованию ионов (заряженных атомов). Например, железо Fe может существовать в нейтральном состоянии или в ионных состояниях +2 и +3.
Количество протонов определяет атомный номер элемента (Z) и отличает один элемент от другого. Например, атомный номер углерода (Z) равен 6, потому что у него 6 протонов. Количество нейтронов может варьироваться для получения изотопов, которые представляют собой атомы одного и того же элемента, имеющие разное количество нейтронов. Количество электронов также может быть разным в атомах одного и того же элемента, что приводит к образованию ионов (заряженных атомов). Например, железо Fe может существовать в нейтральном состоянии или в ионных состояниях +2 и +3.
Массовое число
Массовое число элемента (А) представляет собой сумму числа протонов и числа нейтронов. Небольшой вклад массы от электронов не учитывается при вычислении массового числа. Это приближение массы можно использовать, чтобы легко вычислить, сколько нейтронов имеет элемент, просто вычитая количество протонов из массового числа. Протоны и нейтроны весят примерно одну атомную единицу массы или а.е.м. Изотопы одного и того же элемента будут иметь одинаковый атомный номер, но разные массовые числа.
Атомный номер, химический символ и массовое число : Углерод имеет атомный номер шесть и два стабильных изотопа с массовыми числами двенадцать и тринадцать соответственно. Его средняя атомная масса составляет 12,11.
Ученые определяют атомную массу, вычисляя среднее значение массовых чисел для встречающихся в природе изотопов. Часто полученное число содержит десятичную дробь. Например, атомная масса хлора (Cl) составляет 35,45 а.е.м., поскольку хлор состоит из нескольких изотопов, некоторые из которых (большинство) имеют атомную массу 35 а.е.м. (17 протонов и 18 нейтронов), а некоторые — 37 а.е.м. (17 протонов и 20 нейтронов).
Зная атомный номер (Z) и массовое число (A), вы можете найти количество протонов, нейтронов и электронов в нейтральном атоме. Например, атом лития (Z=3, A=7 а.е.м.) содержит три протона (определено из Z), три электрона (поскольку число протонов равно числу электронов в атоме) и четыре нейтрона (7 – 3 = 4).
Изотопы
Изотопы — это различные формы элемента, которые имеют одинаковое количество протонов, но разное количество нейтронов.
Цели обучения
Обсудить свойства изотопов и их использование в радиометрическом датировании
Ключевые выводы
Ключевые моменты
- Изотопы — это атомы одного и того же элемента, которые содержат одинаковое количество протонов, но разное количество нейтронов.
- Несмотря на разное количество нейтронов, изотопы одного и того же элемента имеют очень похожие физические свойства.
- Некоторые изотопы нестабильны и подвергаются радиоактивному распаду, превращаясь в другие элементы.
- Предсказуемый период полураспада различных распадающихся изотопов позволяет ученым датировать материал на основе его изотопного состава, например, с помощью датирования по углероду-14.
Ключевые термины
- изотоп : Любая из двух или более форм элемента, в которых атомы имеют одинаковое количество протонов, но разное количество нейтронов в ядрах.
- период полураспада : Время, за которое половина исходной концентрации изотопа распадается обратно в более стабильную форму.

- радиоактивные изотопы : атом с нестабильным ядром, характеризующийся избыточной доступной энергией, который подвергается радиоактивному распаду и создает чаще всего гамма-лучи, альфа- или бета-частицы.
- радиоуглеродное датирование : Определение возраста объекта путем сравнения отношения обнаруженной в нем концентрации 14С к количеству 14С в атмосфере.
Что такое изотоп?
Изотопы — это различные формы элемента, которые имеют одинаковое количество протонов, но разное количество нейтронов. Некоторые элементы, такие как углерод, калий и уран, имеют несколько встречающихся в природе изотопов. Изотопы определяются сначала их элементом, а затем суммой присутствующих протонов и нейтронов.
- Углерод-12 (или 12 C) содержит шесть протонов, шесть нейтронов и шесть электронов; следовательно, он имеет массовое число 12 а.е.м. (шесть протонов и шесть нейтронов).
- Углерод-14 (или 14 C) содержит шесть протонов, восемь нейтронов и шесть электронов; его атомная масса составляет 14 а.
 е.м. (шесть протонов и восемь нейтронов).
е.м. (шесть протонов и восемь нейтронов).
Несмотря на то, что масса отдельных изотопов различна, их физические и химические свойства в основном остаются неизменными.
Изотопы отличаются своей стабильностью. Углерод-12 ( 12 C) является наиболее распространенным из изотопов углерода, на его долю приходится 98,89% углерода на Земле. Углерод-14 ( 14 C) нестабилен и встречается только в следовых количествах. Нестабильные изотопы чаще всего испускают альфа-частицы (He 2+ ) и электроны. Нейтроны, протоны и позитроны также могут быть испущены, а электроны могут быть захвачены для достижения более стабильной атомной конфигурации (более низкий уровень потенциальной энергии) посредством процесса, называемого радиоактивным распадом. Созданные новые атомы могут находиться в состоянии с высокой энергией и испускать гамма-лучи, которые снижают энергию, но сами по себе не превращают атом в другой изотоп. Эти атомы называются радиоактивными изотопами или радиоизотопами.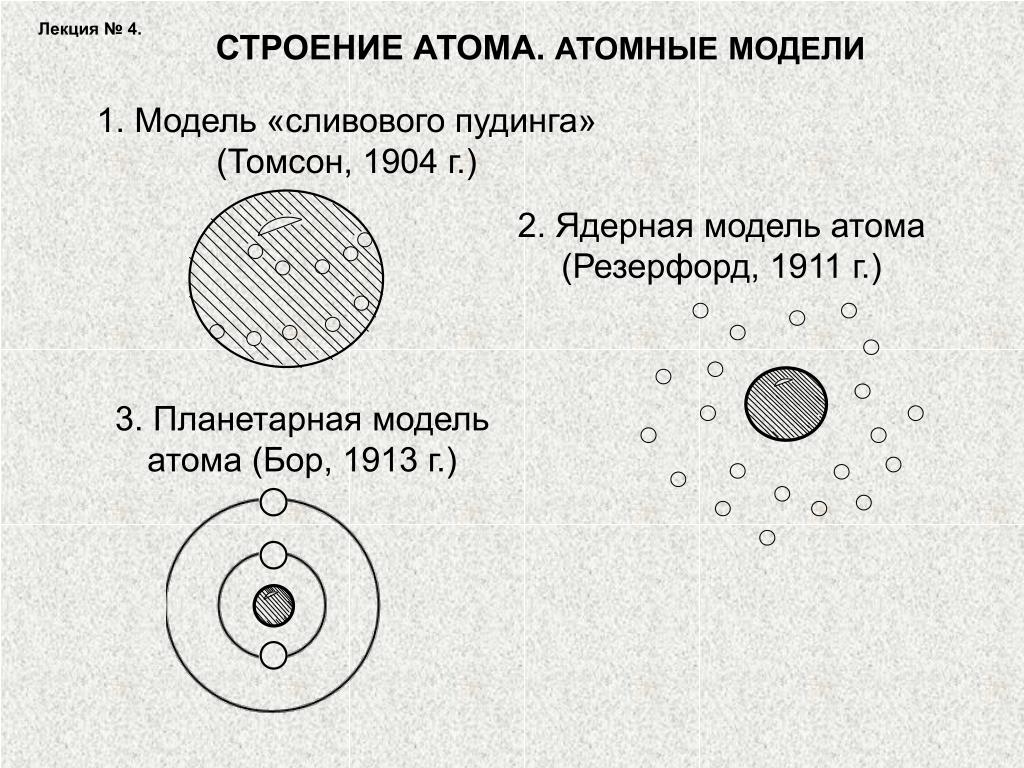
Радиоуглеродный анализ
Углерод обычно присутствует в атмосфере в виде газообразных соединений, таких как двуокись углерода и метан. Углерод-14 ( 14 C) представляет собой встречающийся в природе радиоизотоп, который создается из атмосферного 14 N (азота) путем добавления нейтрона и потери протона, что вызвано космическими лучами. Это непрерывный процесс, поэтому в атмосфере всегда создается больше 14 C. После производства 14 C часто соединяется с кислородом в атмосфере с образованием углекислого газа. Углекислый газ, образующийся таким образом, диффундирует в атмосферу, растворяется в океане и усваивается растениями посредством фотосинтеза. Животные поедают растения и, в конечном счете, радиоуглерод распространяется по всей биосфере.
В живых организмах относительное количество 14 С в их организме примерно равно концентрации 14 С в атмосфере. Когда организм умирает, он больше не поглощает 14 C, поэтому отношение между 14 C и 12 C будет уменьшаться по мере того, как 14 C постепенно распадается обратно до 14 N. Этот медленный процесс, называемый бета-распадом, высвобождает энергию за счет испускания электроны из ядра или позитроны.
Этот медленный процесс, называемый бета-распадом, высвобождает энергию за счет испускания электроны из ядра или позитроны.
Приблизительно через 5730 лет половина исходной концентрации 14 C превратится обратно в 14 N. Это называется периодом полураспада или временем, которое требуется для половины исходной концентрации 14 N. изотоп распадается до более стабильной формы. Поскольку период полураспада 14 C — длинный, он используется для датировки бывших живых объектов, таких как старые кости или дерево. Сравнивая отношение концентрации 14 С, обнаруженной в объекте, к количеству 14 С в атмосфере, можно определить количество еще не распавшегося изотопа. На основе этого количества можно точно рассчитать возраст материала, если считается, что возраст материала составляет менее 50 000 лет. Этот метод называется радиоуглеродным датированием, или сокращенно углеродным датированием.
Применение углеродного датирования : Возраст углеродосодержащих останков возрастом менее 50 000 лет, таких как этот карликовый мамонт, можно определить с помощью углеродного датирования.
Другие элементы имеют изотопы с разным периодом полураспада. Например, 40 K (калий-40) имеет период полураспада 1,25 миллиарда лет, а 235 U (уран-235) имеет период полураспада около 700 миллионов лет. Ученые часто используют эти другие радиоактивные элементы для датирования объектов старше 50 000 лет (предел углеродного датирования). С помощью радиометрического датирования ученые могут изучать возраст окаменелостей или других остатков вымерших организмов.
Лицензии и авторство
Контент под лицензией CC, совместно используемый ранее
- Курирование и пересмотр. Предоставлено : Boundless.com. Лицензия : CC BY-SA: Attribution-ShareAlike
Лицензионный контент CC, конкретное указание авторства
- OpenStax College, Biology. 16 октября 2013 г. Предоставлено : OpenStax CNX. Расположен по адресу : https://openstax.org/books/biology/pages/2-1-atoms-isotopes-ions-and-molecules-the-building-blocks.
 Лицензия : CC BY: Атрибуция
Лицензия : CC BY: Атрибуция - Сунил Кумар Сингх, Основные типы сил. 27 октября 2013 г. Предоставлено : OpenStax CNX. Лицензия : CC BY: Атрибуция
- нейтрон. Предоставлено : Викисловарь. Расположен по адресу : https://en.wiktionary.org/wiki/neutron. Лицензия : CC BY-SA: Attribution-ShareAlike
- электрон. Предоставлено : Викисловарь. Лицензия : CC BY-SA: Attribution-ShareAlike
- атом. Предоставлено : Викисловарь. Лицензия : CC BY-SA: Attribution-ShareAlike
- протон. Предоставлено : Викисловарь. Лицензия : CC BY-SA: Attribution-ShareAlike
- Колледж OpenStax, Биология. 30 октября 2013 г. Предоставлено : OpenStax CNX. Расположен по адресу : https://openstax.
 org/books/biology/pages/2-1-atoms-isotopes-ions-and-molecules-the-building-blocks. Лицензия : CC BY: Атрибуция
org/books/biology/pages/2-1-atoms-isotopes-ions-and-molecules-the-building-blocks. Лицензия : CC BY: Атрибуция - Колледж OpenStax, Атомы, изотопы, ионы и молекулы: строительные блоки. 16 октября 2013 г. Предоставлено : OpenStax CNX. Лицензия : CC BY: Attribution
- атомный номер. Предоставлено : Викисловарь. Лицензия : CC BY-SA: Attribution-ShareAlike
- Колледж OpenStax, Биология. 16 октября 2013 г. Предоставлено : OpenStax CNX. Расположен по адресу : https://openstax.org/books/biology/pages/2-1-atoms-isotopes-ions-and-molecules-the-building-blocks. Лицензия : CC BY: Атрибуция
- Химия уровня A/OCR/Атомы, связи и группы/Атомы и реакции/Атомы. Предоставлено : Wikibooks. Лицензия : CC BY-SA: Attribution-ShareAlike
- Безгранично.
 Предоставлено : Безграничное обучение. Лицензия : CC BY-SA: Attribution-ShareAlike
Предоставлено : Безграничное обучение. Лицензия : CC BY-SA: Attribution-ShareAlike - Колледж OpenStax, Биология. 30 октября 2013 г. Предоставлено : OpenStax CNX. Расположен по адресу : https://openstax.org/books/biology/pages/2-1-atoms-isotopes-ions-and-molecules-the-building-blocks. Лицензия : CC BY: Атрибуция
- Колледж OpenStax, Атомы, изотопы, ионы и молекулы: строительные блоки. 16 октября 2013 г. Предоставлено : OpenStax CNX. Лицензия : CC BY: Атрибуция
- Колледж OpenStax, Биология. 27 октября 2013 г. Предоставлено : OpenStax CNX. Расположен по адресу : https://openstax.org/books/biology/pages/2-1-atoms-isotopes-ions-and-molecules-the-building-blocks. Лицензия : CC BY: Атрибуция
- Колледж OpenStax, Биология. 16 октября 2013 г.
 Предоставлено : OpenStax CNX. Лицензия : CC BY: Attribution
Предоставлено : OpenStax CNX. Лицензия : CC BY: Attribution - Радиоуглеродное датирование. Предоставлено : Википедия. Лицензия : CC BY-SA: Attribution-ShareAlike
- изотоп. Предоставлено : Викисловарь. Лицензия : CC BY-SA: Attribution-ShareAlike
- Углерод-12. Предоставлено : Википедия. Лицензия : CC BY-SA: Attribution-ShareAlike
- Колледж OpenStax, Биология. 30 октября 2013 г. Предоставлено : OpenStax CNX. Расположен по адресу : https://openstax.org/books/biology/pages/2-1-atoms-isotopes-ions-and-molecules-the-building-blocks. Лицензия : CC BY: Атрибуция
- Колледж OpenStax, Атомы, изотопы, ионы и молекулы: строительные блоки. 16 октября 2013 г. Предоставлено : OpenStax CNX.
 Лицензия : CC BY: Атрибуция
Лицензия : CC BY: Атрибуция - Колледж OpenStax, Биология. 27 октября 2013 г. Предоставлено : OpenStax CNX. Расположен по адресу : https://openstax.org/books/biology/pages/2-1-atoms-isotopes-ions-and-molecules-the-building-blocks. Лицензия : CC BY: Attribution
- Колледж OpenStax, Атомы, изотопы, ионы и молекулы: строительные блоки. 16 октября 2013 г. Предоставлено : OpenStax CNX. Лицензия : CC BY: Attribution
Chem4Kids.com: Atoms: Structure
Материя | Атомы | Элементы | Периодическая таблица | Реакции | Биохимия | Все темы
Обзор | Структура | Орбиты | Электроны | Ионы | Нейтроны | Изотопы | Склеивание | Соединения | Составные имена | Радиоактивность и антивещество
Атомы являются основой химии.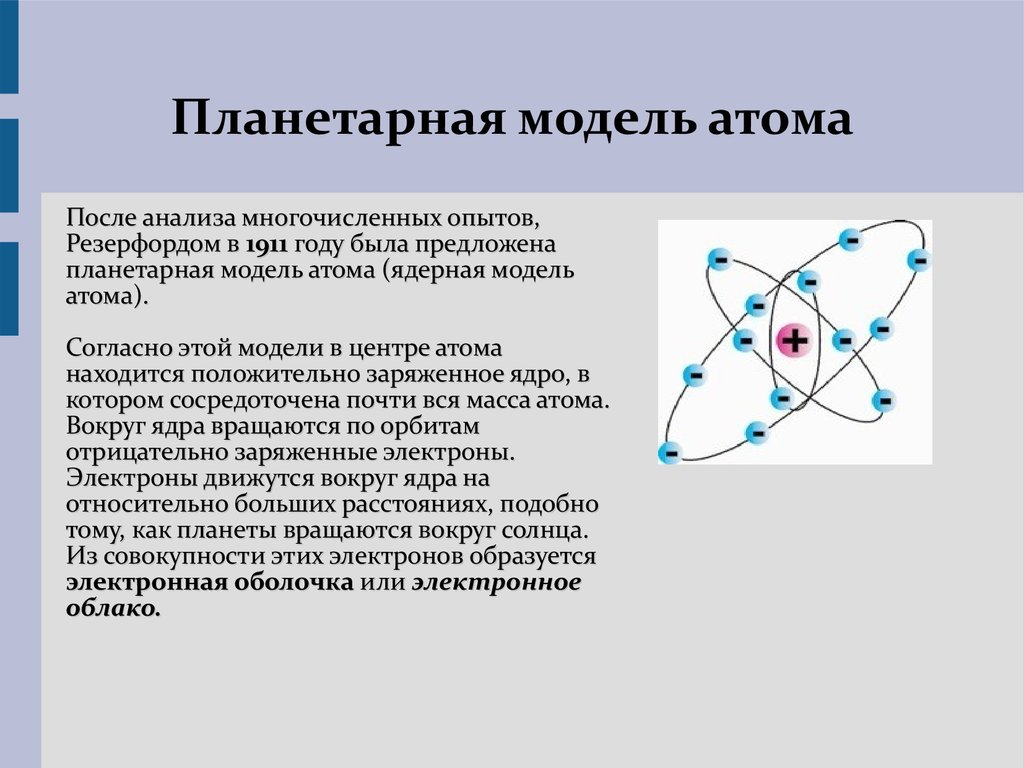 Они являются основой всего во Вселенной. Как известно, материя состоит из атомов. Твердые тела состоят из плотно упакованных атомов, в то время как газы имеют разбросанные атомы. Мы рассмотрим основы, такие как атомная структура и связи между атомами. Когда вы узнаете больше, вы можете перейти к страницам реакций и биохимии и посмотреть, как атомы образуют соединения, которые помогают биологическому миру выжить.
Они являются основой всего во Вселенной. Как известно, материя состоит из атомов. Твердые тела состоят из плотно упакованных атомов, в то время как газы имеют разбросанные атомы. Мы рассмотрим основы, такие как атомная структура и связи между атомами. Когда вы узнаете больше, вы можете перейти к страницам реакций и биохимии и посмотреть, как атомы образуют соединения, которые помогают биологическому миру выжить.
Существуют ли частицы материи, которые меньше атомов? Конечно есть. Сверхмалые частицы можно найти внутри кусочков атомов. Эти субатомные частицы включают нуклонов и кварков . Химики-ядерщики и физики работают вместе на ускорителях частиц , чтобы обнаружить присутствие этих крошечных, крошечных, крошечных частиц материи. Однако наука основана на атоме, потому что это мельчайшая отдельная единица материи.
Несмотря на то, что существует множество сверхмалых атомных частиц, вам нужно запомнить только три основные части атома: электроны, протоны и нейтроны. Что такое электроны, протоны и нейтроны? Электроны — самые маленькие из трех частиц, из которых состоят атомы. Электроны находятся в оболочках или орбиталях, окружающих ядро атома. Протоны и нейтроны находятся в ядро . Они группируются в центре атома. Это все, что вам нужно помнить. Три легких произведения!
Что такое электроны, протоны и нейтроны? Электроны — самые маленькие из трех частиц, из которых состоят атомы. Электроны находятся в оболочках или орбиталях, окружающих ядро атома. Протоны и нейтроны находятся в ядро . Они группируются в центре атома. Это все, что вам нужно помнить. Три легких произведения!
В таблице Менделеева почти 120 известных элементов. (117, пока мы это пишем) Химики и физики каждый день пытаются создавать новые в своих лабораториях. Атомы разных элементов имеют разное количество электронов, протонов и нейтронов. Каждый элемент уникален и имеет атомный номер. Это число говорит вам о количестве протонов в каждом атоме элемента. Атомный номер также называют числом протона.
Вы можете видеть, что каждая часть атома помечена знаком «+», «-» или «0». Эти символы относятся к заряду частицы. Вы когда-нибудь слышали о том, что вас может ударить током от розетки, статического электричества или молнии? Все это связано с электрическими зарядами. Заряды также обнаруживаются в мельчайших частицах материи.
Заряды также обнаруживаются в мельчайших частицах материи.
Электрон всегда имеет “-” или отрицательный заряд. Протон всегда имеет «+» или положительный заряд. Если заряд всего атома равен «0» или нейтральному, количество положительных и отрицательных зарядов равно. Нейтральные атомы имеют одинаковое количество электронов и протонов. Третья частица – нейтрон. Он имеет нейтральный заряд, также известный как нулевой заряд.
Поскольку количество протонов в атоме не меняется, меньшее количество или дополнительные электроны могут создать особый атом, называемый ионом. Катионы имеют меньше электронов и имеют положительный заряд. Анионы имеют дополнительные электроны, которые создают отрицательный заряд.
► СЛЕДУЮЩАЯ СТРАНИЦА ПО АТОМАМ
► СЛЕДУЮЩАЯ ОСТАНОВКА НА ОБЪЕКТЕ ОБЪЕКТА
► ВИКТОРИНА ПО СТРУКТУРЕ АТОМА
► ВЕРНУТЬСЯ НА НАЧАЛО СТРАНИЦЫ
► Или выполните поиск по сайтам.