Все металлы в таблице Менделеева – список, свойства
Металлы – обобщенное название химических элементов, объеденных по ряду признаков. В периодической таблице они занимают большую часть, однако до сих пор не существует документа, позволяющего разделить их на классы.
Отличаются металлы в первую очередь своими качественными характеристиками. Какие-то имеют высокую теплопроводимость, другие выдерживают высокие нагрузки на разрыв и растяжение. В зависимости от этих качеств определяется и сфера применения, но металлы в природном виде, даже очищенные, не обладают необходимыми показателями в достаточном виде, поэтому применяется технология сплавов, то есть соединения нескольких элементов в одну молекулярную решетку. Это позволяет существенно улучшить характеристики, и придать сплаву необходимые качества.
Простой пример: возьмем распространенный в промышленности сплав бронзу. Это соединение, где основным элементом выступает медь. В качестве легирующего, то есть улучшающего качество, компонента используется олово. В результате соединения получается новый металл, более твердый и упругий по сравнению с чистой медью, который часто используют для изготовления крепежа.
В результате соединения получается новый металл, более твердый и упругий по сравнению с чистой медью, который часто используют для изготовления крепежа.
Свойства
В группу черных металлов входит железо и все его сплавы. Они составляют около 90% всего материала, который используется в экономике. В природе они встречаются редко, поэтому добывают материал путем обработки железной руды. Главным отличием черных металлов является то, что в их составе всегда есть железо. Цветные его не содержат, обычно встречаются еще и в разных цветах. От этого и появилось такое название. Цветные металлы отличаются друг от друга техническими возможностями и составом, а черные все между собой похожи, поскольку в основном состоят из железа.
Свойства чермета появляются только после изменения его состава, перечислим главные достоинства этого материала:
- легкая свариваемость;
- высокий показатель твердости;
- повышенная прочность;
- низкая себестоимость;
- устойчивость к механическим повреждениям;
- достаточный объем для использования в производственных целях.

Благодаря этим качествам черный металл больше используют в строительстве для создания сооружений гражданского и промышленного масштаба. Здания выдерживают высокую нагрузку и имеют долгий срок службы.
Цветные металлы стоят дороже из-за того, что их мало, но сплавы используются для производства приборов и изделий с ограниченными свойствами.
Свойства цветмета:
- лом этого материала подходит для вторичного использования;
- он не подвергается коррозии;
- имеет высокую теплопроводность;
- легче весит, если сравнивать с черметом;
- более пластичен и гибок.
Никель – цветной металл или чёрный?
По физическим свойствам никель – это чёрный металл. Однако с технической точки зрения его причисляют к цветным металлам. Наряду с хромом, ванадием, молибденом, марганцем никель входит в первую пятёрку легирующих элементов по массовости их применения. Помимо этого, его используют в производстве широкого спектра сплавов, в которых он является основным или вторым по массовой доле элементом.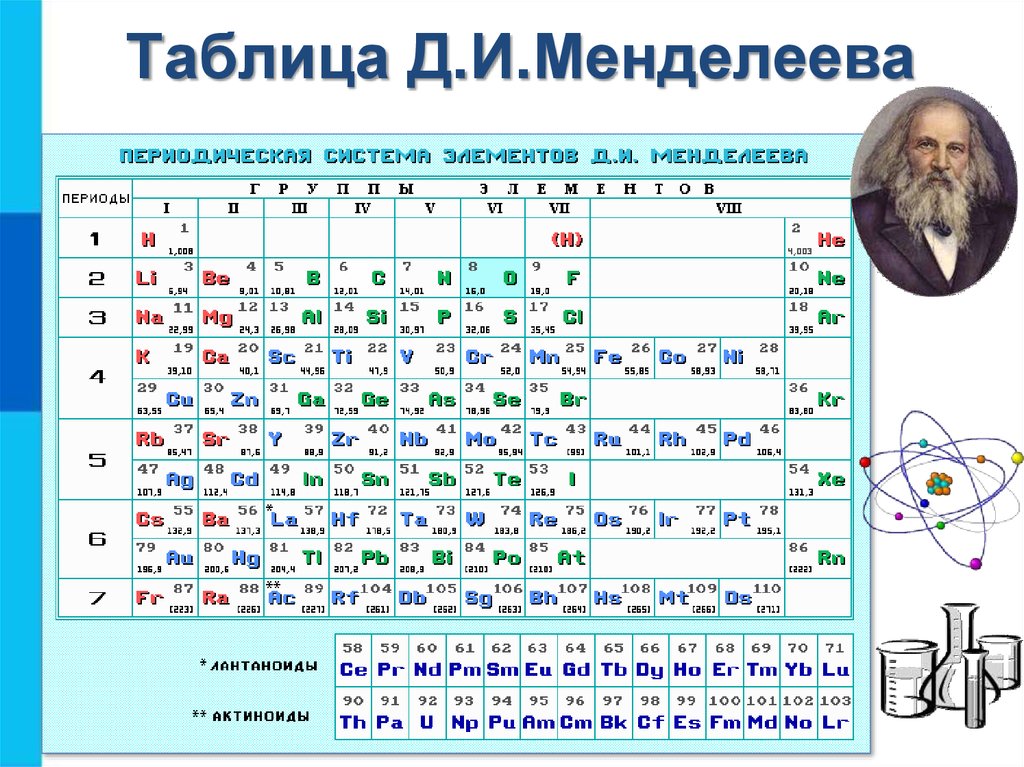
К ним относятся производимые согласно ГОСТ 492-73 и ГОСТ 19241-2016 сплавы. В их числе мельхиор, хромель, константан, манганин и другие ценные сплавы, которые отличает очень высокая коррозионная стойкость. Значительное содержание в углеродных сплавах никеля и хрома также обеспечивает им стойкость ко всем видам коррозии, в том числе в результате атмосферных и агрессивных воздействий.
Никель наряду с другими легирующими элементами придаёт углеродистым сплавам заданные специальные свойства. В их числе жаропрочность и жаростойкость, повышенная механическая прочность, стойкость к разным видам агрессивной среды и прочее. С учётом высокой ценности высоколегированных сплавов, в том числе имеющих магнитные свойства, их справедливо причисляют к цветным металлам.
Основные виды
В сравнении с черным, у цветного металла гораздо больше разновидностей. Добавление различных веществ в состав привело к тому, что материал стали классифицировать по семи группам. У цветного металла есть тугоплавкие, легкие и тяжелые, рассеянные, редкоземельные, радиоактивные, благородные, рассеянные материалы. Мы не будем перечислять все эти типы, а остановимся лишь на самых востребованных металлах и их свойствах:
Мы не будем перечислять все эти типы, а остановимся лишь на самых востребованных металлах и их свойствах:
- Медь. Входит в перечень элементов, которые составляют до 98% земной коры. Не имеет магнитных свойств, обладает высокой электропроводимостью. Используется для создания проводки, труб, технических элементов.
- Свинец. По распространенности этот сплав занимает четвертое место в производственных процессах. Подходит для электропроводных элементов, но применяется не так часто, поскольку считается токсичным.
- Латунь. Она превосходит медь по прочности. Используется для производства труб, листового металла, фольги, проволоки.
- Цинк. Относится к тяжелым цветным металлам. Применяется для создания сплавов и в качестве антикоррозийной защиты для черных металлов. В чистом виде используется только в фармацевтической и производственной отрасли.
- Алюминий. Чаще остальных берется для производства из-за легкого веса.
 Не видоизменяется от внешних факторов, поэтому распространен на потребительском рынке.
Не видоизменяется от внешних факторов, поэтому распространен на потребительском рынке.
У черного металла не так много сплавов, в промышленных целях используется только 2 разновидности:
- Сталь. Это используемый во многих отраслях черный металл. В нем содержится около 99% железа, остальное занимает углерод. При добавлении других веществ повышают прочность металла, защищают от коррозии, делают устойчивым к перепадам температуры. Некоторые марки стали используются для вторичного производства.
- Чугун. В нем содержится больше углерода (около 5%). Он используется в промышленности и производстве, но много весит, поэтому применим не везде. После эксплуатации чугун переливают в сталь.
Особенности состава и применения черных металлов
Черными называют металлы, в составе которых содержится железо. К ним относят мягкую, углеродистую и нержавеющую сталь, чугун. Их применяют для изготовления изделий для металлургической, пищевой, химической промышленности, строительства и других сфер жизни, начиная с многоэтажных зданий, закачивая маленьким шурупом для крепления.
В составе изделий в основном преобладает железо. Материал сохраняет прочность и долговечность после переработки. Нержавеющая сталь устойчива к коррозии, благодаря содержанию хрома. Большинство черных металлов обладают магнитными свойствами и успешно применяются в электротехнике.
Область применения
Из цветного металла создаются детали для автомобилей, кораблей и самолетов. С их помощью делают металлоконструкции, ювелирные украшения, предметы искусства. Сплавы цветметаллов применяют в промышленности и медицине. С их помощью создают оборудование, гиподермические иглы, инструменты для проведения операции. Иридий берется во время лучевой терапии, а золото с платиной используется в стоматологии.
Черные металлы активно применяют в пищевой отрасли, при создании электротехники и генерировании энергии. В строительстве домов, промышленных сооружений и автомобилей они используются чаще цветмета. Некоторые сплавы специально создают для суровых эксплуатационных условий, добавляя примеси, которые сделают материал устойчивей, надежней и пр.
Переработка
Из-за повышения оборотов производства и потребительского спроса все больше организаций занимается переработкой лома. Если не следить за отходами, то в скором времени экология и люди пострадают, поскольку некоторые материалы опасны для здоровья, окружающей среды.
Переработка доступна для черных и цветных металлов. Самое ценное для этого процесса сырье содержится в аккумуляторах, батареях и бытовой технике. Процесс переработки сырья подразумевает несколько этапов:
- Прием металлолома, взвешивание и оплата.
- Сортировка в специальном пункте по профилю и разновидности. Это самый трудоемкий этап, на который уходит много времени.
- Деление материала на мелкие фрагменты для удобной транспортировки и дальнейшей переработки.
- Очистка от примесей вручную или с использованием специальных приборов.
- Переплавка материала для его повторного использования.
Крупным предприятиям сдача металла позволяет сократить расходы. Именно такие организации в основном и влияют на экологическую обстановку, поскольку потребители не производят отходы в таких масштабах.
Именно такие организации в основном и влияют на экологическую обстановку, поскольку потребители не производят отходы в таких масштабах.
Цветные и черные металлы используются почти во всех отраслях жизни человека. Умение отличать их друг от друга позволит заранее принять во внимание слабые и сильные стороны материала, а также заранее спланировать их переработку и повторное использование.
Черная металлургия
Черная металлургия является важной отраслью промышленностью, специализируется на производстве черных металлов. Широкий спектр продукции используется в различных сферах деятельности. По изготовлению стали и металлопроката (основные виды металлургической продукции) Россия занимает 5 место. Размеры производства черной, а также цветной металлургии во всем мире постоянно увеличиваются. Это обусловлено тем, что спрос на продукцию стремительно повышается.
Компании, которые работают в отрасли черной металлургии, классифицируются на несколько категорий:
- Полного цикла.
 Предприятия этого типа выполняют все этапы производства, начиная с добычи сырья, заканчивая реализацией готовой продукции.
Предприятия этого типа выполняют все этапы производства, начиная с добычи сырья, заканчивая реализацией готовой продукции. - Передельные. Одну из стадий выделяют в отдельное производство. Это могут быть дочерние компании большого концерна или комбината.
- Малые. Этот вид представляет собой металлургические цеха, которые являются составными крупных комплексов.
Районов производства черной металлургии несколько. Каждый из них имеет свои особенности. В каждом из этих регионов располагаются предприятия, которые специализируются на добыче, переработке сырья и производстве черных металлов.
Объемы и особенности производства
Общий объем производства составляет около 9,8 %. Черная металлургия включает в себя более 1,5 тыс. организаций и предприятий.С каждым годом динамика экспорта продукции возрастает.Металлургические комбинаты традиционно размещаются на относительно небольшом расстоянии от тех мест, где залегает железная руда.
Объемы производства продукции черной металлургии довольно большие. В России расположено более 34 предприятия. Самыми крупными являются такие комбинаты:
В России расположено более 34 предприятия. Самыми крупными являются такие комбинаты:
- Оскольский;
- Западно-Сибирский;
- Новолипецкий;
- Череповецкий;
- Магнитогорский.
Особенности производства черной металлургии:
- потребление большого количества сырья;
- высокая трудоемкость процесса;
- большие энергозатраты;
- разнообразие выпускаемой продукции;
- высокая себестоимость производства.
Несмотря на эти трудности, отрасль развивается, ведь спрос на металлическую продукцию не снижается. В России производится металл, который не только используется в пределах страны, но и уходит на экспорт.
Факторы размещения
Заводы располагаются либо в непосредственной близости от источников сырья. Главными факторами размещения предприятий черной металлургии считаются такие:
- близость расположения к заводам, где осуществляется изготовление ферросплавов и электростали;
- доступность топливных и природных ресурсов.

Большинство производственных площадок локализируются в Московской области.Ферросплавы изготавливаются в специальных печах либо на заводах электротермическим способом.
Горно-обогатительные компании локализируются вблизи источников залегания сырья. Коксогазовые предприятия работают, находясь в составе металлургических концернов полного цикла. Предприятия полного цикла базируются там, где есть топливные и сырьевые ресурсы, а также источники электрической энергии.
География металлургии чёрных металлов
Рассмотрим особенности географии отраслей черной металлургии в России и районы развития. Наша страна хорошо снабжена сырьём для черной металлургии,вот только на территории размещение залежей неравномерное.
- РФ обладает большими запасами железной руды.
- В Якутии перспективные месторождения расположены в Алданской провинции,а также в Олекмо-Амгуньском районе.
- Залежи хрома и марганца незначительные. Марганец залегает в Свердловской и Кемеровской областях, а хром-в Пермском крае.

Доминирующим изготовителем стали и чугуна считается Уральская металлургическая база, которая функционирует с XVIII века.
Источник
Влияние чёрной металлургии на окружающую среду
К основным веществам,которые поступают в воздух и загрязняют его, относятся продукты, образующиеся в процессе сжигания топлива. Также негативно влияют и выбросы оксида железа. Выделение пыли образуется вследствие выполнения погрузки и разгрузки, а также при приготовлении шихты. Газообразование и пылевыделение происходят при производстве металлопроката и обжиге известняка.
Тенденции и стратегии развития черной металлургии заставляют задуматься. Влияние этой отрасли на окружающую среду колоссальное. Нужно разрабатывать эффективные меры защиты экологии, внедрять технологии, которые бы снизили пагубное воздействие на природу.
Перспективы развития отрасли
Спрос на металлическую продукцию не снижается. Металл сегодня применяется в разных отраслях человеческой деятельности. Сырьё и готовый металлопрокат используются не только в пределах РФ, но и поставляются в другие страны. Отрасль будет развиваться. Уже сейчас технологические процессы, связанные с добычей и переработкой сырья, модернизируются.
Сырьё и готовый металлопрокат используются не только в пределах РФ, но и поставляются в другие страны. Отрасль будет развиваться. Уже сейчас технологические процессы, связанные с добычей и переработкой сырья, модернизируются.
Источник
Чтобы максимально точно оценить ситуацию рынка на 2021 год и последующие два года, специалисты выдвинули три прогнозных сценария.
- Оптимистичный.Пандемия в мировом масштабе будет остановлена ориентировочно к концу 2021 года. Сначала произойдет восстановление мировых рынков, стабилизация цен, российский рынок выдаст незначительное падение (около 5%), но после снова продолжит расти.
- Пессимистичный. При вынужденном продлении карантина падение рынка станет более жестким и составит 15%. Долгая продолжительность остановки производств сможет даже вызвать финансовый кризис. И в этом случае рынок начнет расти только с 2022 года.
- Базовый. Этот вид сценария близок к пессимистичному.Здесь также предусмотрено падение рынка на 10% к 2021 году, после чего начнется медленный рост.

По мнению экспертов, при таких обстоятельствах большое преимущество получат крупные холдинги, которые имеют определенный запас прочности и широкий спектр выпускаемой продукции.
список, свойства, особенности и сферы применения
Этой группе металлов отдан весь второй столбец таблицы Менделеева. И атомщики, и ювелиры используют щелочноземельные металлы. С ними интересно экспериментировать, но требуется осторожность.
Содержание
- Что представляют собой
- История
- Формы нахождения в природе
- Физико-химические характеристики
- Где используются
- Биологическое значение
Что представляют собой
Щелочноземельные металлы – это вся вторая группа таблицы Менделеева.
К щёлочноземельным металлам относятся:
- бериллий,
Бериллий, чистота более 99%, поликристаллический фрагмент
- магний,
Металлический магний
- кальций.
Кальций в атмосфере аргона
Плюс:
- стронций,
- барий,
Барий металлический Ba 99,9%
- радий.

Советский армейский компас. Жёлтая краска содержит радий
То есть «щелочноземельный» список насчитывает шесть позиций, которые обычно располагаются по возрастанию атомного номера – от бериллия к радию.
История
Двойное название группы – отражение природы и характеристик входящих в нее элементов:
- Они способны образовывать щелочи.
- Ряд свойств их оксидов близки окислам алюминия и железа. Такие вещества еще средневековые алхимики именовали «землями».
Сегодняшний состав щелочноземельной группы сформировался не сразу: бериллий и магний отсутствовали.
Это объяснялось отличием свойств данных элементов от остальных:
- По большинству характеристик они ближе к алюминию, чем к другим элементам группы.
- Их гидроксиды – не щелочи.
- Магний взаимодействует с водой в замедленном режиме, у бериллия реакция в таком растворе нулевая. Та же картина при контакте с неметаллами.
Однако специалисты Международного союза теоретической и прикладной химии (IUPAC) решили все-таки причислить бериллий и магний к щелочноземельной группе.
Формы нахождения в природе
Щёлочноземельным металлам присуща чрезмерная активность, поэтому в природе они как самостоятельный элемент отсутствуют.
Почти всегда это составляющая минералов либо руд:
- Самый распространенный элемент щелочноземельной группы – кальций (2,9-12,9% по массе). Его получают из известняков, им насыщены мрамор, гранит.
- Почти три процента забирает магний.
- В сто раз реже в литосфере представлены барий со стронцием.
- Содержание остальных элементов измеряется тысячными долями процента.
Самым редким на планете щёлочноземельным металлом является радий. Но найти его легче других: это обязательный компонент урановых рудников.
Физико-химические характеристики
Элементы группы наделены общими физическими свойствами:
- Серебристый с сероватостью цвет.
- Твердость в стандартных условиях, ножом режется только стронций.
- Металлический блеск.
- Тускнение на воздухе с разной скоростью вследствие образования оксидной пленки.

- Хорошая пропускная способность для тепла и электричества.
- Два электрона на внешнем слое атома у каждого элемента, степень окисления – всегда +2. Это отражают формулы соединений, образованных металлами группы.
Самая тяжелая «щелочная земля» – радий. Кубик вещества с ребром в 1 см весит 5,5 грамма.
Более интересны химические свойства «земель».
Есть общие и оригинальные:
- Покрытый пленкой-оксидом бериллий способен на реакцию только при 600+°С (кроме фтора).
- Окисленный магний при средней температуре не реагирует ни с чем. Получение соединений металла возможно при температуре от 645°C.
- Кальций окисляется неспешно и только если воздух влажный. При незначительном нагреве горит, растворяется водой.
- Осмотрительности требуют барий, стронций, радий. На открытом пространстве взаимодействие этих металлов с кислородом и азотом чревато взрывом. Их держат в герметичных контейнерах, залив керосином.

Общие свойства щёлочноземельных металлов – растворение в кислотах, образование солей, щелочей при взаимодействии с водой.
Химическая активность щелочноземельных металлов усиливается с увеличением габаритов атома – от бериллия к радию.
Где используются
Свойства металлов щелочноземельной группы обусловили применение каждого во всех сегментах – от авиастроения до медицины и ювелирного дела:
- Бериллий. Исходник при выплавке сплавов, включая «атомные», получения ракетного топлива. Компонент ювелирных минералов первого ряда – аквамарина, гелиодора, изумруда.
- Кальций. Базис большинства огнеупоров, строительных материалов. Металл задействован при производстве топлива, аптечных препаратов.
- Магний. Самый легкий щелочноземельный металл. Как восстановитель нашел применение в металлургии. Без проблем куется, раскатывается.
 Чаще используется как «ингредиент» сплавов, снижающий их массивность, – материал корпусов и деталей ракет, самолетов, автомобилей, электроники. А также приборов для нужд оборонного комплекса и предприятий приборостроения.
Чаще используется как «ингредиент» сплавов, снижающий их массивность, – материал корпусов и деталей ракет, самолетов, автомобилей, электроники. А также приборов для нужд оборонного комплекса и предприятий приборостроения.
Сегодня на первое место по использованию магниевых сплавов выходят смартфоны, планшеты, другие гаджеты.
- Стронций. Металлургами используется как лигатура сплавов, очиститель сталей, чугуна, меди от серы, других вредных примесей. Сырье закупают производители радиоэлектроники, химических источников тока, атомщики, пиротехники. Продукция «высокого сегмента» из металла – чистый уран, керамика-сверхпроводник, вакуумный инструментарий.
Стронций создает насыщенно-красные оттенки огней салюта. Изотопом вещества лечат онкологию.
- Барий. Используются соединения металла. Главный потребитель – атомщики. Ассортимент: вакуумные, пьезоэлектрические приборы, жидкий теплоноситель, линзы, стекло для урановых стержней, керамика-сверхпроводник.
 Нетоксичный сульфат используется рентгенологами как контрастное вещество.
Нетоксичный сульфат используется рентгенологами как контрастное вещество.
На особом счету радий. Это самый редкий щелочноземельный металл: на планете его получено всего полтора килограмма.
Даже микродозы радиоактивного вещества смертельно опасны для человека. Однако это свойство используется исследователями ядерных процессов и для лечения онкологии.
Шкалы, стрелки компасов, бортовых приборов, изготовленных до 1970-х годов, покрыты краской, содержащей радий. Она светится в темноте, но с тех пор не используется как опасная для человека.
Биологическое значение
Значение щелочноземельных элементов разнообразно:
- Без кальция не формируется скелет, зубы, не сокращаются мышцы. Элемент «курирует» параметры крови.

- Магний – компонент биологических структур (к примеру, хлорофилла у растений). В организме человека содействует синтезу нуклеиновых кислот, работе ферментов, нервной системы.
- Микродозы стронция присутствуют в организме как аналог кальция. Особо важен щелочноземельный элемент для детей младше четырех лет.
Барий, радий, бериллий, их соединения ядовиты. Поэтому для биологических структур опасны.
Периодическая таблица – химия пищевых продуктов и кулинария
В 1800-х годах было открыто много ранее неизвестных элементов, и ученые отметили, что некоторые наборы элементов имеют схожие химические свойства. Например, хлор, бром и йод реагируют с другими элементами (такими как натрий) с образованием подобных соединений. Точно так же литий, натрий и калий реагируют с другими элементами (такими как кислород) с образованием подобных соединений. Почему это так?
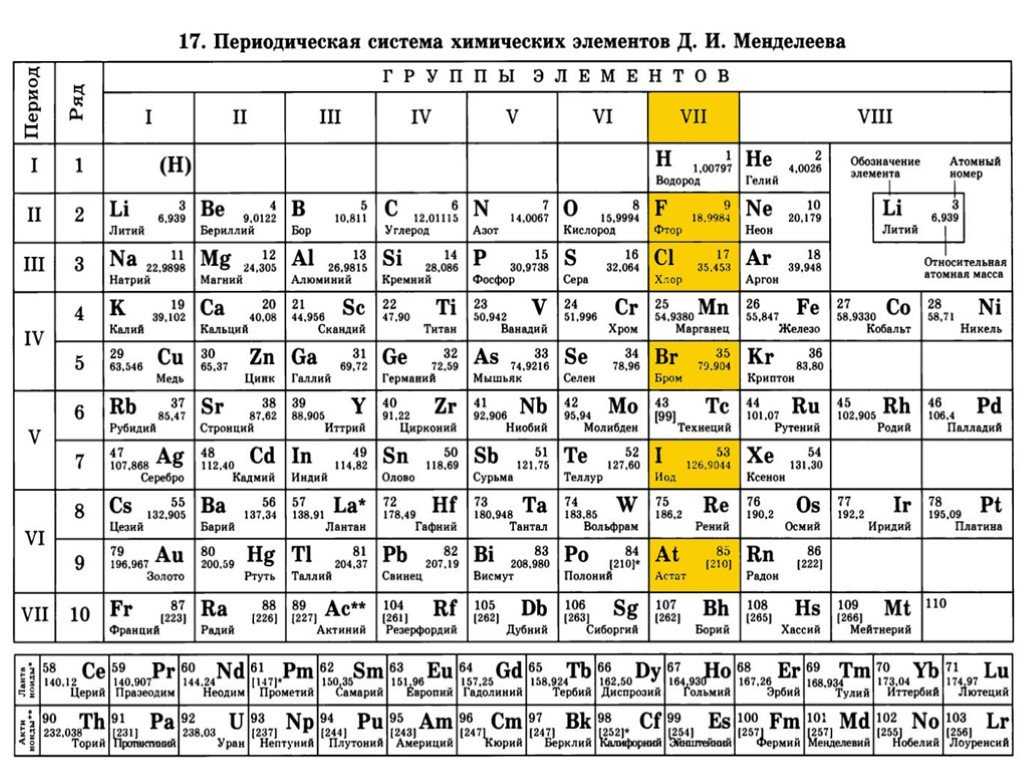
Дмитрий Менделеев в России (1869 г.) и Лотар Мейер в Германии (1870 г.) независимо друг от друга признали, что существует периодическая связь между свойствами элементов, известных в то время. В обеих опубликованных таблицах элементы расположены в порядке возрастания атомной массы. Но Менделеев пошел на шаг дальше Мейера: таблица Менделеева содержала пробелы для того, что, по его предположению, было неоткрытыми элементами. Он использовал свою таблицу и отношения к обнаруженным элементам, чтобы смело предсказать свойства этих неоткрытых элементов. Многие ученые в то время пренебрежительно относились к таблице Менделеева. Однако, когда позже были обнаружены элементы, свойства которых близко соответствовали предсказаниям Менделеева, его версия таблицы завоевала популярность в научном сообществе. На рисунке ниже вы можете видеть, что некоторые элементы, помещенные Менделеевым в его таблицу, имеют прочерк (-) вместо символа — эти элементы в то время еще не были открыты.
В обеих опубликованных таблицах элементы расположены в порядке возрастания атомной массы. Но Менделеев пошел на шаг дальше Мейера: таблица Менделеева содержала пробелы для того, что, по его предположению, было неоткрытыми элементами. Он использовал свою таблицу и отношения к обнаруженным элементам, чтобы смело предсказать свойства этих неоткрытых элементов. Многие ученые в то время пренебрежительно относились к таблице Менделеева. Однако, когда позже были обнаружены элементы, свойства которых близко соответствовали предсказаниям Менделеева, его версия таблицы завоевала популярность в научном сообществе. На рисунке ниже вы можете видеть, что некоторые элементы, помещенные Менделеевым в его таблицу, имеют прочерк (-) вместо символа — эти элементы в то время еще не были открыты.
Поскольку определенные свойства элементов регулярно повторяются по всей таблице (то есть они являются периодическими) , она стала известна как периодическая таблица
 Периодическая таблица является одним из краеугольных камней химии, поскольку в ней все известные элементы систематизированы на основе их химических свойств. В современных периодических таблицах элементы перечислены в порядке атомного номера, а не атомной массы. В современной периодической таблице элементы перечислены слева направо по атомному номеру.
Периодическая таблица является одним из краеугольных камней химии, поскольку в ней все известные элементы систематизированы на основе их химических свойств. В современных периодических таблицах элементы перечислены в порядке атомного номера, а не атомной массы. В современной периодической таблице элементы перечислены слева направо по атомному номеру. Атомный номер — это число протонов в ядре атома (подробнее о протонах и ядре атома см. главу 2 «Анатомия атома»). Это определяющая черта элемента: его значение определяет идентичность атома. Например, водород имеет атомный номер 1; все атомы водорода имеют в ядре 1 протон. Гелий имеет атомный номер 2; все атомы гелия имеют 2 протона в своих ядрах. Не бывает атома водорода с двумя протонами в ядре; ядро с 2 протонами было бы атомом гелия. Протоны были открыты после Менделеева в 19 г.10, и хотя он ничего не знал о протонах и атомных числах, элементы в его периодической таблице исключительно хорошо соответствовали системе упорядочения атомных чисел.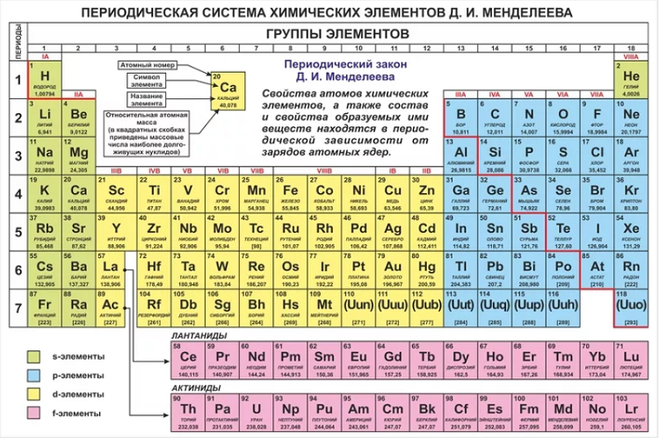
Элементы со схожими химическими свойствами сгруппированы в вертикальные столбцы, называемые группами (или семействами) . Каждое поле представляет собой элемент и содержит его атомный номер, символ, среднюю атомную массу и (иногда) имя. Каждая строка элементов периодической таблицы называется периодом . Периоды имеют разную длину; в первом периоде всего 2 элемента (водород и гелий), а во втором и третьем периодах по 8 элементов. Четвертый и пятый периоды содержат по 18 элементов каждый, а более поздние периоды настолько длинные, что сегмент каждого из них удаляется и помещается под основную часть таблицы.
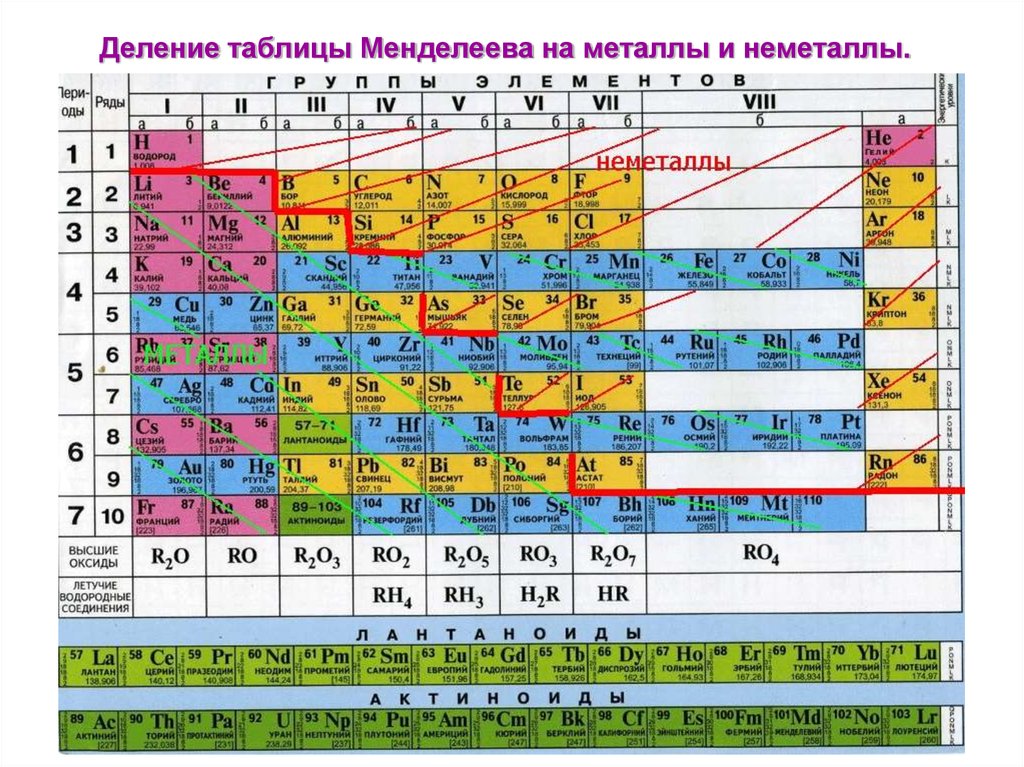
Многие элементы резко различаются по своим химическим и физическим свойствам, но некоторые элементы сходны по своему поведению. Например, многие элементы кажутся блестящими, податливыми (их можно формовать в тонкие листы, не ломая) и пластичными (можно вытягивать в провода), а также хорошо проводить тепло и электричество. Другие элементы не блестящие, ковкие или пластичные и являются плохими проводниками тепла и электричества. Мы можем отсортировать элементы по большим классам с общими свойствами:
Мы можем отсортировать элементы по большим классам с общими свойствами:
- металлы
- блестящие, пластичные элементы, хорошо проводящие тепло и электричество
- заштрихован желтым в периодической таблице ниже
- неметаллы
- элементы, которые кажутся тусклыми, могут быть хрупкими и плохо проводят тепло и электричество
- заштриховано зеленым цветом в таблице Менделеева ниже .
- металлоиды (или полуметаллы)
- элементы, которые умеренно хорошо проводят тепло и электричество и обладают некоторыми свойствами металлов и некоторыми свойствами неметаллов
- окрашен в фиолетовый цвет в таблице Менделеева ниже .
Атрибуция
Эта страница основана на публикации «Chemistry 2e» Пола Флауэрса, Клауса Теопольда, Ричарда Лэнгли, Уильяма Р. Робинсона, доктора философии, Openstax под лицензией CC BY 4.0. Бесплатный доступ на https://openstax.org/books/chemistry-2e/pages/1-introduction 9.0003
Эта страница основана на статье «Кулинарная химия» Сорангеля Родригеса-Веласкеса под лицензией CC BY-NC-SA 4.0. Бесплатный доступ на http://chemofcooking.openbooks.wpengine.com/
Эта страница основана на «Основах общей, органической и биологической химии» Дэвида В. Болла, Джона У. Хилла, Ронды Дж. Скотт, Сейлор, лицензия CC BY-NC-SA 4.0. Бесплатный доступ по адресу http://saylordotorg.github.io/text_the-basics-of-general-organic-and-biological-chemistry/index.html
List – Periodic Table
H
Hydrogen
1
He
Helium
2
Li
Lithium
3
Be
Beryllium
4
B
Boron
5
C
Carbon
6
N
Азот
7
O
Оксид
8
F
Флуорин
F
F
0002 Ne
Neon
10
Na
Sodium
11
Mg
Magnesium
12
Al
Aluminum
13
Si
Silicon
14
P
Phosphorus
15
S
Sulfur
16
CL
Хлор
17
AR
Аргон
18
K
18
K
0003
19
CA
Calcium
20
SC
Скандий
21
TI
V
9000 2 229000 2
9000 2 22.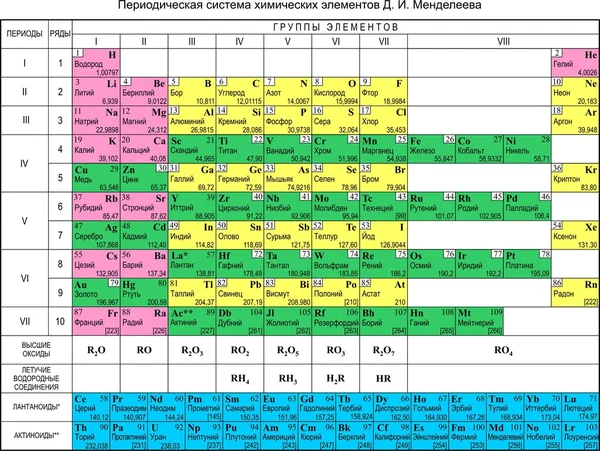

 Не видоизменяется от внешних факторов, поэтому распространен на потребительском рынке.
Не видоизменяется от внешних факторов, поэтому распространен на потребительском рынке. Предприятия этого типа выполняют все этапы производства, начиная с добычи сырья, заканчивая реализацией готовой продукции.
Предприятия этого типа выполняют все этапы производства, начиная с добычи сырья, заканчивая реализацией готовой продукции.




 Чаще используется как «ингредиент» сплавов, снижающий их массивность, – материал корпусов и деталей ракет, самолетов, автомобилей, электроники. А также приборов для нужд оборонного комплекса и предприятий приборостроения.
Чаще используется как «ингредиент» сплавов, снижающий их массивность, – материал корпусов и деталей ракет, самолетов, автомобилей, электроники. А также приборов для нужд оборонного комплекса и предприятий приборостроения.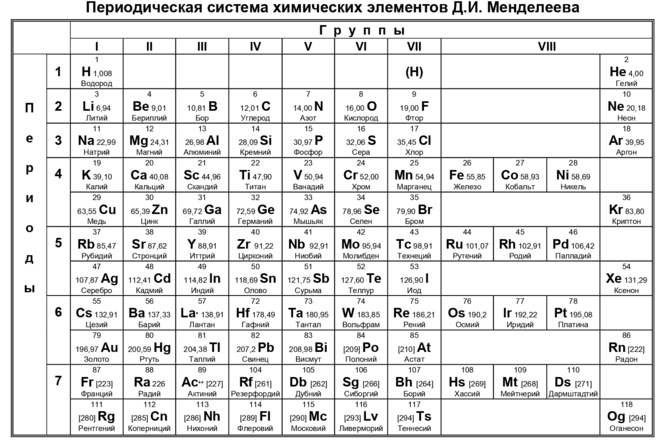 Нетоксичный сульфат используется рентгенологами как контрастное вещество.
Нетоксичный сульфат используется рентгенологами как контрастное вещество.