Строение атома кратко и понятно (химия, 8 класс), электронно-графическая формула
4.4
Средняя оценка: 4.4
Всего получено оценок: 3615.
4.4
Средняя оценка: 4.4
Всего получено оценок: 3615.
Атом – наименьшая частица вещества. Его изучение началось еще в Древней Греции, когда к строению атома было приковано внимание не только ученых, но и философов. Каково же электронное строение атома, и какие основные сведения известны об этой частице?
Строение атома
Уже древнегреческие ученые догадывались о существовании мельчайших химически частиц, из которых состоит любой предмет и организм. И если в XVII-XVIII вв. химики были уверены, что атом неделимая элементарная частица, то на рубеже XIX-XX вв., опытным путем удалось доказать, что атом не является неделимым.
Атом, будучи микроскопической частицей вещества, состоит из ядра и электронов. Ядро в 10000 раз меньше атома, однако практически вся его масса сосредоточена именно в ядре. Главной характеристикой атомного ядра, является то, что он имеет положительный заряд и состоит из протонов и нейтронов. Протоны заряжены положительно, а нейтроны не имеют заряда (они нейтральны).
Главной характеристикой атомного ядра, является то, что он имеет положительный заряд и состоит из протонов и нейтронов. Протоны заряжены положительно, а нейтроны не имеют заряда (они нейтральны).
Атом любого элемента можно обозначить электронной формулой и электронно графической формулой:
Рис. 1. Электронно-графическая формула атома.Единственным химическим элементом из периодической системы, в ядре которого не содержатся нейтроны, является легкий водород (протий).
Электрон является отрицательно заряженной частицей. Электронная оболочка состоит из движущихся вокруг ядра электронов. Электроны имеют свойства притягиваться к ядру, а между друг друг на них оказывает влияние кулоновское взаимодействие. Чтобы преодолеть притяжения ядра, электроны должны получать энергию от внешнего источника.
Модели атомов
На протяжении долго времени ученые стремились познать природу атома. На раннем этапе большой вклад внес древнегреческий философ Демокрит. Хотя сейчас его теория и кажется нам банальной и слишком простой, в тот период, когда представления об элементарных частицах только начинало зарождаться, его теория о кусочках материи воспринималась совершенно серьезно. Демокрит считал, что свойства любого вещества зависят от формы, массы и других характеристик атомов. Так, например, у огня, полагал он, острые атомы – поэтому огонь обжигает; у воды атомы гладкие, поэтому она способна течь; у твердых предметов, по его представлению, атомы были шереховатые.
Демокрит считал, что из атомов состоит абсолютно все, даже душа человека.
В 1904 году Дж. Дж. Томсон предложил свою модель атома. Основные положения теории сводились к тому, что атом представлялся положительно заряженным телом, внутри которого находились электроны с отрицательным зарядом.
Также в 1904 году японским физиком Х. Нагаока была предложена ранняя планетарная модель атома по аналогии с планетой Сатурн. Электроны по этой теории объединены в кольца и вращаются вокруг положительно заряженного ядра. Эта теория оказалась ошибочной.
В 1911 году Э. Резерфорд, проделав ряд опытов, сделал выводы, что атом по своему строению похож на планетную систему. Ведь электроны, словно планеты, движутся по орбитам вокруг тяжелого положительно заряженного ядра. Однако это описание противоречило классической электродинамике. Тогда датский физик Нильс Бор в 1913 году ввел постулаты, суть которых заключалась в том, что электрон, находясь в некоторых специальных состояниях, не излучает энергию. Таким образом, постулаты бора показали, что для атомов классическая механика неприменима. Планетарная модель, описанная Резерфордом и дополненная Бором, получила название – планетарная модель Бора-Резерфорда.
Дальнейшее изучение атома привело к созданию такого раздела, как квантовая механика, с помощью которого объяснялись многие научные факты. Современные представления об атоме развились из планетарной модели Бора-Резерфорда.
Что мы узнали?
В данной статье по химии (8 класс) рассказывается кратко и понятно о строении атома. На протяжении многих веков ученые разных стран изучали мельчайшие частицы вещества. Появлялись разные теории, модели и разные формулы строения атома. Современные представления об атоме основываются на модели Бора-Резерфорда, по которой атом состоит из ядра и электронного облака, в котором электроны движутся вокруг ядра.
Тест по теме
Доска почёта
Чтобы попасть сюда – пройдите тест.
Саша Николаев
10/10
Александр Котков
10/10
Павел Сафаров
6/10
Мир Грин
10/10
Юрий Филиппов
7/10
Александр Котков
10/10
Даниил Суханкин
10/10
Виктория Гудимова
10/10
Виктор Миронов
9/10
Сергей Ефремов
9/10
Оценка доклада
4. 4
4
Средняя оценка: 4.4
Всего получено оценок: 3615.
А какая ваша оценка?
Модели строения атома
Модель Томсона
Первая модель строения атома была предложена Дж. Томсоном в 1904 г., согласно которой атом – положительно заряженная сфера с вкрапленными в нее электронами. Несмотря на свое несовершенство томсоновская модель позволяла объяснить явления испускания, поглощения и рассеяния света атомами, а также установить число электронов в атомах легких элементов.
Рис. 1. Атом, согласно модели Томсона. Электроны удерживаются внутри положительно заряженной сферы упругими силами. Те из них, которые находятся на поверхности, могут легко «выбиваться» , оставляя ионизированный атом.
2.2 Модель Резерфорда
Модель
Томсона была опровергнута Э.
Рис. 2. Эта модель строения атома известна как планетарная, т. к. электроны вращаются вокруг ядра подобно планетам солнечной системы.
Согласно законам классической электродинамики, движение электрона по окружности вокруг ядра будет устойчивым, если сила кулоновского притяжения будет равна центробежной силе. Однако, в соответствии с теорией электромагнитного поля, электроны в этом случае должны двигаться по спирали, непрерывно излучая энергию, и падать на ядро. Однако атом устойчив.
К тому же при непрерывном излучении энергии у атома должен наблюдаться непрерывный, сплошной спектр. На самом деле спектр атома состоит из отдельных линий и серий.
Таким образом,
данная модель противоречит законам
электродинамики и не объясняет линейчатого
характера атомного спектра.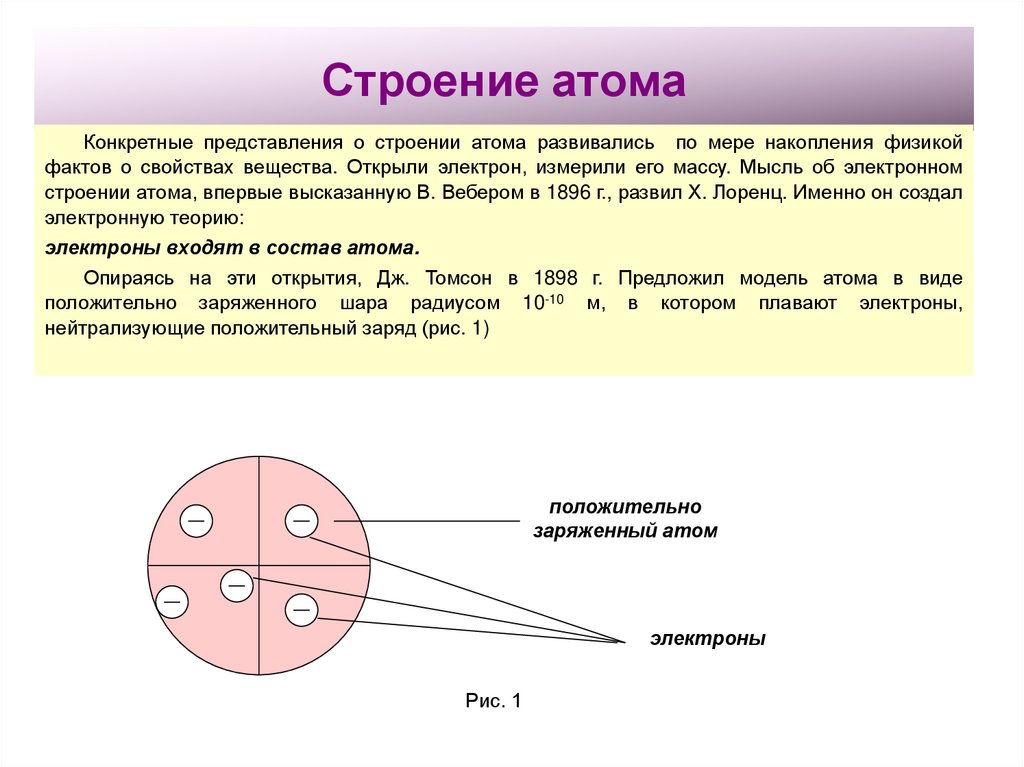
2.3. Модель Бора
В 1913 г. Н. Бор предложил свою теорию строения атома, не отрицая при этом полностью предыдущие представления. В основу своей теории Бор положил два постулата.
Первый постулат говорит о том, что электрон может вращаться вокруг ядра только по определенным стационарным орбитам. Находясь на них, он не излучает и не поглощает энергию (рис.3).
Рис. 3. Модель строения атома Бора. Изменение состояния атома при переходе электрона с одной орбиты на другую.
При
движении по любой стационарной орбите
запас энергии электрона (Е1, Е2 …) остается постоянным. Чем ближе к ядру
расположена орбита, тем меньше запас
энергии электрона Е1 ˂
где
m
– масса электрона, h
– постоянная Планка, n
– 1, 2, 3… (n=1
для 1-ой орбиты, n=2
для 2-ой и т. д.).
д.).
Второй постулат говорит о том, что при переходе с одной орбиты на другую электрон поглощает или выделяет квант (порцию) энергии.
Если подвергнуть атомы воздействию (нагреванию, облучению и др.), то электрон может поглотить квант энергии и перейти на более удаленную от ядра орбиту (рис. 3). В этом случае говорят о возбужденном состоянии атома. При обратом переходе электрона (на более близкую к ядру орбиту) энергия выделяется в виде кванта лучистой энергии – фотона. В спектре это фиксируется определенной линией. На основании формулы
,
где λ
– длина волны, n
= квантовые числа, характеризующие
ближнюю и дальнюю орбиты, Бор рассчитал
длины волн для всех серий в спектре
атома водорода. Полученные результаты
соответствовали экспериментальным
данным. Стало ясным происхождение
прерывистых линейчатых спектров. Они
– результат излучения энергии атомами
при переходе электронов из возбужденного
состояния в стационарное. Переходы
электронов на 1-ю орбиту образуют группу
частот серии Лаймана, на 2-ю – серию
Бальмера, на 3-ю серию Пашена (рис. 4,табл.
1).
Переходы
электронов на 1-ю орбиту образуют группу
частот серии Лаймана, на 2-ю – серию
Бальмера, на 3-ю серию Пашена (рис. 4,табл.
1).
Рис. 4. Соответствие между электронными переходами и спектральными линиями атома водорода.
Таблица 1
Проверка формулы Бора для серий водородного спектра
Название серии | λ, А Экспериментальная | λ, А Вычисленная Бором |
Пашена | 18751,3 12817,5 10938,0 10049,8 | 18756 12822 10941 10052 |
Бальмера | 6564,66 4862,71 4102,91 3971,20 3799,00 3712,70 | 6564,70 4862,80 4341,70 4102,93 3971,23 3799,01 3712,62 |
Лаймана | 1216 1028 972 | 1215,68 1025,73 972,5 |
Однако,
теория Бора не смогла объяснить
расщепление линий в спектрах
многоэлектронных атомов. Бор исходил
из того, что электрон – это частица, и
использовал для описания электрона
законы, характерные для частиц. Вместе
с тем накапливались факты, свидетельствующие
о том, что электрон способен проявлять
и волновые свойства. Классическая
механика оказалась не в состоянии
объяснить движение микрообъектов,
обладающих одновременно свойствами
материальных частиц и свойствами волны.
Эту задачу позволила решить квантовая
механика – физическая теория, исследующая
общие закономерности движения и
взаимодействия микрочастиц, обладающих
очень малой массой (табл. 2).
Бор исходил
из того, что электрон – это частица, и
использовал для описания электрона
законы, характерные для частиц. Вместе
с тем накапливались факты, свидетельствующие
о том, что электрон способен проявлять
и волновые свойства. Классическая
механика оказалась не в состоянии
объяснить движение микрообъектов,
обладающих одновременно свойствами
материальных частиц и свойствами волны.
Эту задачу позволила решить квантовая
механика – физическая теория, исследующая
общие закономерности движения и
взаимодействия микрочастиц, обладающих
очень малой массой (табл. 2).
Таблица 2
Свойства элементарных частиц, образующих атом
Частица | Заряд | Масса | ||
Кл | Условн. | г | А.е.м. | |
Электрон | – 1,6·10-19 | -1 | 9,10·10-28 | 0,00055 |
Протон | 1,6·10-19 | +1 | 1,67·10-24 | 1,00728 |
Нейтрон | 0 | 0 | 1,67·10-24 | 1,00866 |
АТОМА СТРОЕНИЕ | Энциклопедия Кругосвет
Содержание статьи- АТОМ КАК ЦЕЛОЕ
- Законы Дальтона.
- Число Авогадро.
- Открытие электрона.

- Масс-спектрограф Томсона.
- Другие доказательства сложной структуры атома.
- Модель атома Томсона.
- Опыты Резерфорда по рассеянию.
- Квантовая теория Бора.
- Квантовая механика атома.
- Спин электрона и принцип запрета Паули.
- Периодическая система элементов.
- Дальнейшее исследование структуры атомов.
АТОМА СТРОЕНИЕ, раздел физики, изучающий внутреннее устройство атомов. Атомы, первоначально считавшиеся неделимыми, представляют собой сложные системы. Они имеют массивное ядро, состоящее из протонов и нейтронов, вокруг которого в пустом пространстве движутся электроны. Атомы очень малы – их размеры порядка 10–10–10–9 м, а размеры ядра еще примерно в 100 000 раз меньше (10–15–10–14 м). Поэтому атомы можно «увидеть» только косвенным путем, на изображении с очень большим увеличением (например, с помощью автоэлектронного проектора). Но и в этом случае атомы не удается рассмотреть в деталях. Наши знания об их внутреннем устройстве основаны на огромном количестве экспериментальных данных, которые косвенно, но убедительно свидетельствуют в пользу сказанного выше.
Наши знания об их внутреннем устройстве основаны на огромном количестве экспериментальных данных, которые косвенно, но убедительно свидетельствуют в пользу сказанного выше.
Представления о строении атома радикально изменились в 20 в. под влиянием новых теоретических идей и экспериментальных данных. В описании внутреннего строения атомного ядра до сих пор остаются нерешенные вопросы, которые служат предметом интенсивных исследований. В следующих разделах излагается история развития представлений о строении атома как целого; строению ядра посвящена отдельная статья (АТОМНОГО ЯДРА СТРОЕНИЕ), поскольку эти представления развивались в значительной степени независимо. Энергия, необходимая для исследования внешних оболочек атома, относительно невелика, порядка тепловой или химической энергии. По этой причине электроны были экспериментально обнаружены задолго до открытия ядра.
Ядро же при его малых размерах очень сильно связано, так что разрушить и исследовать его можно только с помощью сил, в миллионы раз более интенсивных, нежели силы, действующие между атомами. Быстрый прогресс в понимании внутренней структуры ядра начался лишь с появлением ускорителей частиц. Именно это огромное различие размеров и энергии связи позволяет рассматривать структуру атома в целом отдельно от структуры ядра.
Быстрый прогресс в понимании внутренней структуры ядра начался лишь с появлением ускорителей частиц. Именно это огромное различие размеров и энергии связи позволяет рассматривать структуру атома в целом отдельно от структуры ядра.
Чтобы составить представление о размерах атома и незаполненности занимаемого им пространства, рассмотрим атомы, составляющие каплю воды диаметром 1 мм. Если мысленно увеличить эту каплю до размеров Земли, то атомы водорода и кислорода, входящие в молекулу воды, будут иметь в поперечнике 1–2 м. Основная же часть массы каждого атома сосредоточена в его ядре, поперечник которого при этом составил всего 0,01 мм.
АТОМ КАК ЦЕЛОЕ
Историю возникновения самых общих представлений об атоме обычно ведут со времен греческого философа Демокрита (ок. 460 – ок. 370 до н. э.), много размышлявшего о наименьших частицах, на которые можно было бы поделить любое вещество. Группу греческих философов, придерживавшихся того взгляда, что существуют подобные крошечные неделимые частицы, называли атомистами. Греческий философ Эпикур (ок. 342–270 до н.э.) принял атомную теорию, и в первом веке до н.э. один из его последователей, римский поэт и философ Лукреций Кар, изложил учение Эпикура в поэме «О природе вещей», благодаря которой оно и сохранилось для следующих поколений. Аристотель (384–322 до н.э.), один из крупнейших ученых древности, атомистическую теорию не принимал, и его взгляды на философию и науку преобладали впоследствии в средневековом мышлении. Атомистической теории как бы не существовало до самого конца эпохи Возрождения, когда на смену чисто умозрительным философским рассуждениям пришел эксперимент.
Греческий философ Эпикур (ок. 342–270 до н.э.) принял атомную теорию, и в первом веке до н.э. один из его последователей, римский поэт и философ Лукреций Кар, изложил учение Эпикура в поэме «О природе вещей», благодаря которой оно и сохранилось для следующих поколений. Аристотель (384–322 до н.э.), один из крупнейших ученых древности, атомистическую теорию не принимал, и его взгляды на философию и науку преобладали впоследствии в средневековом мышлении. Атомистической теории как бы не существовало до самого конца эпохи Возрождения, когда на смену чисто умозрительным философским рассуждениям пришел эксперимент.
В эпоху Возрождения начались систематические исследования в областях, именуемых ныне химией и физикой, принесшие с собой новые догадки о природе «неделимых частиц». Р.Бойль (1627–1691) и И.Ньютон (1643–1727) исходили в своих рассуждениях из представления о существовании неделимых частиц вещества. Однако ни Бойлю, ни Ньютону не потребовалось детальной атомистической теории для объяснения интересовавших их явлений, и результаты проведенных ими экспериментов не сказали ничего нового о свойствах «атомов».
Законы Дальтона.
Первым действительно научным обоснованием атомистической теории, убедительно продемонстрировавшим рациональность и простоту гипотезы о том, что всякий химический элемент состоит из мельчайших частиц, явилась работа английского школьного учителя математики Дж.Дальтона (1766–1844), статья которого, посвященная этой проблеме, появилась в 1803.
Дальтон изучал свойства газов, в частности отношения объемов газов, вступавших в реакцию образования химического соединения, например, при образовании воды из водорода и кислорода. Он установил, что отношения прореагировавших количеств водорода и кислорода всегда представляют собой отношения небольших целых чисел. Так, при образовании воды (H2O) в реакцию с 16 г кислорода вступают 2,016 г газообразного водорода, а при образовании пероксида водорода (H2O2) с 2,016 г водорода соединяются 32 г газообразного кислорода. Массы кислорода, реагирующие с одной и той же массой водорода при образовании этих двух соединений, соотносятся между собой как небольшие числа:
16:32 = 1:2.
На основе подобных результатов Дальтон сформулировал свой «закон кратных отношений». Согласно этому закону, если два элемента соединяются в разных пропорциях, образуя разные соединения, то массы одного из элементов, соединяющиеся с одним и тем же количеством второго элемента, соотносятся как небольшие целые числа. По второму закону Дальтона, «закону постоянных отношений», в любом химическом соединении соотношение масс входящих в него элементов всегда одно и то же. Большое количество экспериментальных данных, относящихся не только к газам, но также и к жидкостям и твердым соединениям, собрал Й.Берцелиус (1779–1848), который провел точные измерения реагирующих масс элементов для многих соединений. Его данные подтвердили сформулированные Дальтоном законы и убедительно продемонстрировали наличие у каждого элемента наименьшей единицы массы.
Атомные постулаты Дальтона имели то преимущество перед абстрактными рассуждениями древнегреческих атомистов, что его законы позволяли объяснить и увязать между собой результаты реальных опытов, а также предсказать результаты новых экспериментов. Он постулировал, что 1) все атомы одного и того же элемента тождественны во всех отношениях, в частности, одинаковы их массы; 2) атомы разных элементов имеют неодинаковые свойства, в частности, неодинаковы их массы; 3) в соединение, в отличие от элемента, входит определенное целое число атомов каждого из составляющих его элементов; 4) в химических реакциях может происходить перераспределение атомов, но ни один атом не разрушается и не создается вновь. (В действительности, как выяснилось в начале 20 в., эти постулаты не вполне строго выполняются, т.к. атомы одного и того же элемента могут иметь разные массы, например водород имеет три такие разновидности, называемые изотопами; кроме того, атомы могут претерпевать радиоактивные превращения и даже полностью разрушиться, но не в химических реакциях, рассматривавшихся Дальтоном.) Основанная на этих четырех постулатах атомная теория Дальтона давала самое простое объяснение законов постоянных и кратных отношений.
Он постулировал, что 1) все атомы одного и того же элемента тождественны во всех отношениях, в частности, одинаковы их массы; 2) атомы разных элементов имеют неодинаковые свойства, в частности, неодинаковы их массы; 3) в соединение, в отличие от элемента, входит определенное целое число атомов каждого из составляющих его элементов; 4) в химических реакциях может происходить перераспределение атомов, но ни один атом не разрушается и не создается вновь. (В действительности, как выяснилось в начале 20 в., эти постулаты не вполне строго выполняются, т.к. атомы одного и того же элемента могут иметь разные массы, например водород имеет три такие разновидности, называемые изотопами; кроме того, атомы могут претерпевать радиоактивные превращения и даже полностью разрушиться, но не в химических реакциях, рассматривавшихся Дальтоном.) Основанная на этих четырех постулатах атомная теория Дальтона давала самое простое объяснение законов постоянных и кратных отношений.
Хотя законы Дальтона лежат в основе всей химии, ими не определяются фактические размеры и массы атомов. Они ничего не говорят о числе атомов, содержащихся в определенной массе элемента или соединения. Молекулы простых веществ слишком малы, чтобы их можно было взвесить по отдельности, поэтому для определения масс атомов и молекул приходится прибегать к косвенным методам.
Они ничего не говорят о числе атомов, содержащихся в определенной массе элемента или соединения. Молекулы простых веществ слишком малы, чтобы их можно было взвесить по отдельности, поэтому для определения масс атомов и молекул приходится прибегать к косвенным методам.
Число Авогадро.
В 1811 А.Авогадро (1776–1856) выдвинул гипотезу, которая значительно упрощала анализ того, как из элементов образуются соединения, и устанавливала различие между атомами и молекулами. Его мысль состояла в том, что равные объемы газов, находящиеся при одинаковых температуре и давлении, содержат одно и то же число молекул. В принципе намек на это можно найти в более ранней работе Ж.Гей-Люссака (1778–1850), который установил, что отношение объемов газообразных элементов, вступающих в химическую реакцию, выражается целыми числами, хотя и отличными от отношений масс, полученных Дальтоном. Например, 2 л газообразного водорода (молекулы H2), соединяясь с 1 л газообразного кислорода (молекулы O2), образуют 1 л паров воды (молекулы H2O).
Истинное число молекул в данном объеме газа чрезвычайно велико, и до 1865 его не удавалось определить с приемлемой точностью. Однако уже во времена Авогадро проводились грубые оценки на основе кинетической теории газов. Очень удобной единицей измерения количества вещества является моль, т.е. количество вещества, в котором столько же молекул, сколько атомов в 0,012 кг самого распространенного изотопа углерода 12С. Один моль идеального газа при нормальных условиях (н.у.), т.е. стандартных температуре и давлении, занимает объем 22,4 л. Число Авогадро – это полное число молекул в одном моле вещества или в 22,4 л газа при н.у. Другие методы, такие, как рентгенография, дают для числа Авогадро N0 более точные значения, нежели полученные на основе кинетической теории. Значение, принятое в настоящее время, таково: 6,0221367Ч1023 атомов (молекул) в одном моле. Следовательно, в 1 л воздуха содержится примерно 3Ч1022 молекул кислорода, азота и других газов.
Важная роль числа Авогадро для физики атома связана с тем, что оно позволяет определить массу и приблизительные размеры атома или молекулы. Поскольку масса 22,4 л газообразного H2 составляет 2,016Ч10–3 кг, масса одного атома водорода равна 1,67Ч10–27 кг. Если считать, что в твердом теле атомы расположены вплотную друг к другу, то число Авогадро позволит приближенно оценить радиус r, скажем, атомов алюминия. Для алюминия 1 моль равен 0,027 кг, а плотность – 2,7Ч103 кг/м3. При этом имеем
откуда r » 1,6Ч10–10 м. Так первые оценки числа Авогадро дали представление об атомных размерах.
Открытие электрона.
Экспериментальные данные, связанные с образованием химических соединений, подтверждали существование «атомных» частиц и позволили судить о малых размерах и массе отдельных атомов. Однако реальная структура атомов, в том числе и существование еще меньших частиц, составляющих атомы, оставалась неясной до открытия Дж. Дж.Томсоном электрона в 1897. До той поры атом считался неделимым и различие в химических свойствах различных элементов не имело своего объяснения. Еще до открытия Томсона был выполнен ряд интересных экспериментов, в которых другие исследователи изучали электрический ток в стеклянных трубках, наполненных газом при низких давлениях. Такие трубки, названные трубками Гейсслера по имени немецкого стеклодува Г.Гейсслера (1815–1879), который первым начал изготовлять их, испускали яркое свечение, будучи подключены к высоковольтной обмотке индукционной катушки. Этими электрическими разрядами заинтересовался У.Крукс (1832–1919), который установил, что характер разряда в трубке меняется в зависимости от давления, и разряд полностью исчезает при высоком вакууме. Более поздние исследования Ж.Перрена (1870–1942) показали, что вызывающие свечение «катодные лучи» представляют собой отрицательно заряженные частицы, которые движутся прямолинейно, но могут отклоняться магнитным полем. Однако заряд и масса частиц оставались неизвестны и было неясно, одинаковы ли все отрицательные частицы.
Дж.Томсоном электрона в 1897. До той поры атом считался неделимым и различие в химических свойствах различных элементов не имело своего объяснения. Еще до открытия Томсона был выполнен ряд интересных экспериментов, в которых другие исследователи изучали электрический ток в стеклянных трубках, наполненных газом при низких давлениях. Такие трубки, названные трубками Гейсслера по имени немецкого стеклодува Г.Гейсслера (1815–1879), который первым начал изготовлять их, испускали яркое свечение, будучи подключены к высоковольтной обмотке индукционной катушки. Этими электрическими разрядами заинтересовался У.Крукс (1832–1919), который установил, что характер разряда в трубке меняется в зависимости от давления, и разряд полностью исчезает при высоком вакууме. Более поздние исследования Ж.Перрена (1870–1942) показали, что вызывающие свечение «катодные лучи» представляют собой отрицательно заряженные частицы, которые движутся прямолинейно, но могут отклоняться магнитным полем. Однако заряд и масса частиц оставались неизвестны и было неясно, одинаковы ли все отрицательные частицы.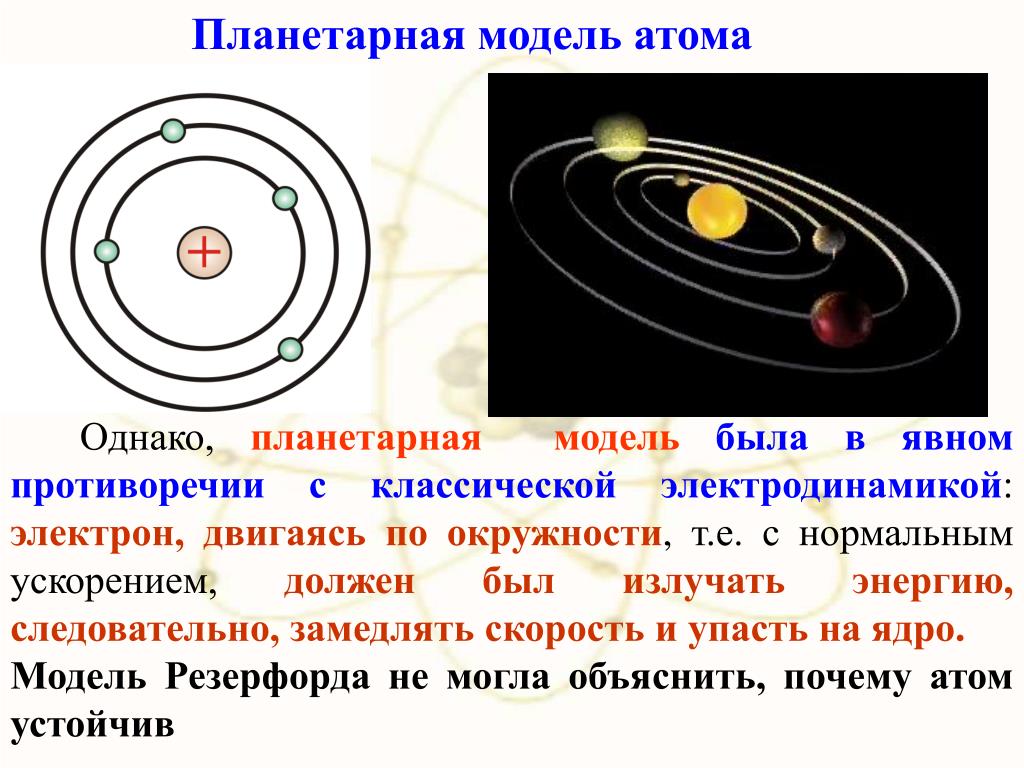
Огромной заслугой Томсона явилось доказательство того, что все частицы, образующие катодные лучи, тождественны друг другу и входят в состав вещества. С помощью разрядной трубки особого типа, изображенной на рис. 1, Томсон измерил скорость и отношение заряда к массе частиц катодных лучей, позднее названных электронами. Электроны вылетали из катода под действием высоковольтного разряда в трубке. Через диафрагмы D и E проходили только те из них, что летели вдоль оси трубки.
В нормальном режиме эти электроны попадали в центр люминесцентного экрана. (Трубка Томсона была первой «электронно-лучевой трубкой» с экраном, предшественницей телевизионного кинескопа.) В трубке находилась также пара пластин электрического конденсатора, которые, если на них подавалось напряжение, могли отклонять электроны. Электрическая сила FE, действующая на заряд e со стороны электрического поля E, дается выражением
FE = eE.
Кроме того, в той же области трубки с помощью пары катушек с током могло создаваться магнитное поле, способное отклонять электроны в противоположном направлении. Сила FH, действующая со стороны магнитного поля H, пропорциональна напряженности поля, скорости частицы v и ее заряду e:
FH = Hev.
Томсон отрегулировал электрическое и магнитное поля так, чтобы полное отклонение электронов было равно нулю, т.е. электронный пучок вернулся в первоначальное положение. Поскольку в этом случае обе силы FE и FHравны, скорость электронов дается выражением
v = E/H.
Томсон установил, что эта скорость зависит от напряжения на трубке V и что кинетическая энергия электронов mv2/2 прямо пропорциональна этому напряжению, т.е. mv2/2 = eV. (Отсюда термин «электрон-вольт» для энергии, приобретаемой частицей с зарядом, равным заряду электрона при ускорении разностью потенциалов 1 В.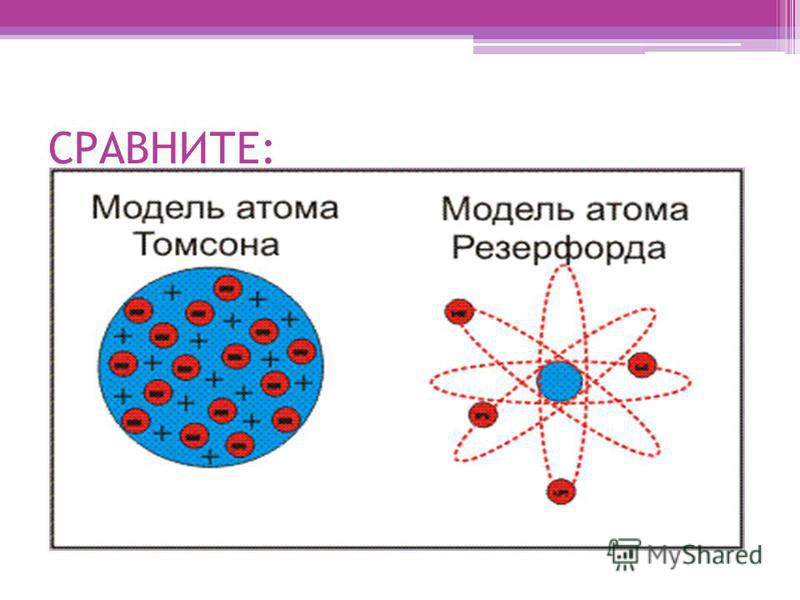 ) Комбинируя это уравнение с выражением для скорости электрона, он нашел отношение заряда к массе:
) Комбинируя это уравнение с выражением для скорости электрона, он нашел отношение заряда к массе:
Эти опыты позволили определить отношение e/m для электрона и дали приближенное значение заряда e. Точно величина e была измерена Р.Милликеном, который в своих опытах добивался, чтобы заряженные капельки масла висели в воздухе между пластинами конденсатора. В настоящее время характеристики электрона известны с большой точностью:
Таким образом, масса электрона значительно меньше массы атома водорода:
Эксперименты Томсона показали, что электроны в электрических разрядах могут возникать из любого вещества. Поскольку все электроны одинаковы, элементы должны различаться лишь числом электронов. Кроме того, малая величина массы электронов указывала на то, что масса атома сосредоточена не в них.
Масс-спектрограф Томсона.
Вскоре и оставшуюся часть атома с положительным зарядом удалось наблюдать с помощью той же, хотя и модифицированной, разрядной трубки, позволившей открыть электрон. Уже первые эксперименты с разрядными трубками показали, что если катод с отверстием помещается посередине трубки, то через «канал» в катоде проходят положительно заряженные частицы, вызывая свечение люминесцентного экрана, расположенного в противоположном от анода конце трубки. Эти положительные «каналовые лучи» тоже отклонялись магнитным полем, но в направлении, противоположном электронам.
Уже первые эксперименты с разрядными трубками показали, что если катод с отверстием помещается посередине трубки, то через «канал» в катоде проходят положительно заряженные частицы, вызывая свечение люминесцентного экрана, расположенного в противоположном от анода конце трубки. Эти положительные «каналовые лучи» тоже отклонялись магнитным полем, но в направлении, противоположном электронам.
Томсон решил измерить массу и заряд этих новых лучей, также используя для отклонения частиц электрическое и магнитное поля. Его прибор для изучения положительных лучей, «масс-спектрограф», схематически изображен на рис. 2. Он отличается от прибора, представленного на рис. 1, тем, что электрическое и магнитное поля отклоняют частицы под прямым углом друг к другу, а потому «нулевое» отклонение получить не удается. Положительно заряженные атомы на пути между анодом и катодом могут потерять один или несколько электронов, и по этой причине могут ускоряться до различных энергий. Атомы одного типа с одинаковыми зарядом и массой, но с некоторым разбросом конечных скоростей, вычертят на люминесцентном экране или фотопластинке кривую линию (отрезок параболы). При наличии атомов с различной массой более тяжелые атомы (с тем же зарядом) будут отклоняться от центральной оси слабее, чем более легкие. На рис. 3 приведена фотография парабол, полученных на масс-спектрографе Томсона. Самая узкая парабола соответствует самому тяжелому однократно ионизованному атому (атому ртути), у которого выбит один электрон. Две самые широкие параболы соответствуют водороду, одна – атомарному H+, а другая – молекулярному H2+, причем оба однократно ионизованы. В некоторых случаях теряются два, три и даже четыре заряда, однако атомарный водород никогда не наблюдался ионизованным более чем однократно. Данное обстоятельство было первым указанием на то, что в атоме водорода только один электрон, т.е. это самый простой из атомов.
При наличии атомов с различной массой более тяжелые атомы (с тем же зарядом) будут отклоняться от центральной оси слабее, чем более легкие. На рис. 3 приведена фотография парабол, полученных на масс-спектрографе Томсона. Самая узкая парабола соответствует самому тяжелому однократно ионизованному атому (атому ртути), у которого выбит один электрон. Две самые широкие параболы соответствуют водороду, одна – атомарному H+, а другая – молекулярному H2+, причем оба однократно ионизованы. В некоторых случаях теряются два, три и даже четыре заряда, однако атомарный водород никогда не наблюдался ионизованным более чем однократно. Данное обстоятельство было первым указанием на то, что в атоме водорода только один электрон, т.е. это самый простой из атомов.
Другие доказательства сложной структуры атома.
В то самое время, когда Томсон и другие исследователи экспериментировали с катодными лучами, открытие рентгеновского излучения и радиоактивности принесло дополнительные доказательства сложной структуры атома. В 1895 В.Рентген (1845–1923) случайно обнаружил таинственное излучение («Х-лучи»), проникавшее сквозь черную бумагу, которой он оборачивал трубку Крукса при исследовании зеленой люминесцирующей области электрического разряда. Х-лучи вызывали свечение удаленного экрана, покрытого кристаллическим платиноцианидом бария. Рентген выяснил, что различные вещества разной толщины, введенные между экраном и трубкой, ослабляют свечение, но не гасят его полностью. Это свидетельствовало о чрезвычайно высокой проникающей способности Х-лучей. Рентген установил также, что эти лучи распространяются прямолинейно и не отклоняются под действием электрических и магнитных полей. Возникновение такого невидимого проникающего излучения при бомбардировке электронами различных материалов было чем-то совершенно новым. Было известно, что видимый свет от трубок Гейсслера состоит из отдельных «спектральных линий» с определенными длинами волн и, значит, связан с «колебаниями» атомов, имеющими дискретные частоты.
В 1895 В.Рентген (1845–1923) случайно обнаружил таинственное излучение («Х-лучи»), проникавшее сквозь черную бумагу, которой он оборачивал трубку Крукса при исследовании зеленой люминесцирующей области электрического разряда. Х-лучи вызывали свечение удаленного экрана, покрытого кристаллическим платиноцианидом бария. Рентген выяснил, что различные вещества разной толщины, введенные между экраном и трубкой, ослабляют свечение, но не гасят его полностью. Это свидетельствовало о чрезвычайно высокой проникающей способности Х-лучей. Рентген установил также, что эти лучи распространяются прямолинейно и не отклоняются под действием электрических и магнитных полей. Возникновение такого невидимого проникающего излучения при бомбардировке электронами различных материалов было чем-то совершенно новым. Было известно, что видимый свет от трубок Гейсслера состоит из отдельных «спектральных линий» с определенными длинами волн и, значит, связан с «колебаниями» атомов, имеющими дискретные частоты. Существенная особенность нового излучения, отличавшая его от оптических спектров, помимо высокой проникающей способности, состояла в том, что оптические спектры элементов с последовательно возраставшим числом электронов полностью отличались друг от друга, тогда как спектры X-лучей очень незначительно изменялись от элемента к элементу.
Существенная особенность нового излучения, отличавшая его от оптических спектров, помимо высокой проникающей способности, состояла в том, что оптические спектры элементов с последовательно возраставшим числом электронов полностью отличались друг от друга, тогда как спектры X-лучей очень незначительно изменялись от элемента к элементу.
Еще одним открытием, имеющим отношение к строению атома, было то, что атомы некоторых элементов могут спонтанно испускать излучение. Это явление было обнаружено в 1896 А.Беккерелем (1852–1908). Беккерель открыл радиоактивность, используя соли урана в процессе изучения люминесценции солей под действием света и ее связи с люминесценцией стекла в рентгеновской трубке. В одном из опытов наблюдалось почернение фотопластинки, завернутой в черную бумагу и находившейся около урановой соли в полной темноте. Это случайное открытие стимулировало интенсивные поиски других примеров естественной радиоактивности и постановку опытов по определению природы испускаемого излучения. В 1898 П.Кюри (1859–1906) и М.Кюри (1867–1934) обнаружили еще два радиоактивных элемента – полоний и радий. Э.Резерфорд (1871–1937), исследовав проникающую способность излучения урана, показал, что имеются два типа излучений: очень «мягкое» излучение, которое легко поглощается веществом и которое Резерфорд назвал альфа-лучами, и более проникающее излучение, которое он назвал бета-лучами. Бета-лучи оказались тождественными обычным электронам, или «катодным лучам», возникающим в разрядных трубках. Альфа-лучи, как выяснилось, имеют такие же заряд и массу, как и атомы гелия, лишенные двух своих электронов. Третий тип излучения, названный гамма-лучами, оказался сходен с X-лучами, но обладал еще большей проникающей способностью.
В 1898 П.Кюри (1859–1906) и М.Кюри (1867–1934) обнаружили еще два радиоактивных элемента – полоний и радий. Э.Резерфорд (1871–1937), исследовав проникающую способность излучения урана, показал, что имеются два типа излучений: очень «мягкое» излучение, которое легко поглощается веществом и которое Резерфорд назвал альфа-лучами, и более проникающее излучение, которое он назвал бета-лучами. Бета-лучи оказались тождественными обычным электронам, или «катодным лучам», возникающим в разрядных трубках. Альфа-лучи, как выяснилось, имеют такие же заряд и массу, как и атомы гелия, лишенные двух своих электронов. Третий тип излучения, названный гамма-лучами, оказался сходен с X-лучами, но обладал еще большей проникающей способностью.
Все эти открытия ясно показали, что атом не является «неделимым». Он не только состоит из более мелких частей (электронов и более тяжелых положительных частиц), но эти и другие субчастицы, по-видимому, самопроизвольно испускаются при радиоактивном распаде тяжелых элементов. Кроме того, атомы не только испускают излучение в видимой области с дискретными частотами, но и могут так возбуждаться, что начинают испускать более «жесткое» электромагнитное излучение, а именно X-лучи.
Кроме того, атомы не только испускают излучение в видимой области с дискретными частотами, но и могут так возбуждаться, что начинают испускать более «жесткое» электромагнитное излучение, а именно X-лучи.
Модель атома Томсона.
Дж.Томсон, внесший огромный вклад в экспериментальное изучение строения атома, стремился найти модель, которая позволила бы объяснить все его известные свойства. Поскольку преобладающая доля массы атома сосредоточена в его положительно заряженной части, он принял, что атом представляет собой сферическое распределение положительного заряда радиусом примерно 10–10 м, а на его поверхности находятся электроны, удерживаемые упругими силами, позволяющими им колебаться (рис. 4). Суммарный отрицательный заряд электронов в точности компенсирует положительный заряд, так что атом электрически нейтрален. Электроны находятся на сфере, но могут совершать простые гармонические колебания относительно положения равновесия. Такие колебания могут происходить лишь с определенными частотами, которым соответствуют узкие спектральные линии, наблюдающиеся в газоразрядных трубках. Электроны можно довольно легко выбить с их позиций, в результате чего возникают положительно заряженные «ионы», из которых состоят «каналовые лучи» в опытах с масс-спектрографом. X-лучи соответствуют очень высоким обертонам основных колебаний электронов. Альфа-частицы, возникающие при радиоактивных превращениях, – это часть положительной сферы, выбитая из нее в результате какого-то энергичного разрывания атома.
Электроны можно довольно легко выбить с их позиций, в результате чего возникают положительно заряженные «ионы», из которых состоят «каналовые лучи» в опытах с масс-спектрографом. X-лучи соответствуют очень высоким обертонам основных колебаний электронов. Альфа-частицы, возникающие при радиоактивных превращениях, – это часть положительной сферы, выбитая из нее в результате какого-то энергичного разрывания атома.
Однако эта модель вызывала ряд возражений. Одно из них было связано с тем, что, как обнаружили спектроскописты, измерявшие линии испускания, частоты этих линий не являются простыми кратными низшей частоты, как должно быть в случае периодических колебаний заряда. Вместо этого они сближаются с увеличением частоты, как если бы стремились к пределу. Уже в 1885 И.Бальмеру (1825–1898) удалось найти простую эмпирическую формулу, связывающую частоты линий видимой части спектра водорода:
где n – частота, c – скорость света (3Ч108 м/с), n – целое число и RH – некий постоянный множитель. Согласно этой формуле, в данной серии спектральных линий водорода должны отсутствовать линии с длиной волны l меньше 364,56 нм (или с более высокими частотами), отвечающей n = Ґ. Так оно и оказалось, и это стало серьезным возражением против модели атома Томсона, хотя и делались попытки объяснить расхождение различием упругих возвращающих сил для разных электронов.
Согласно этой формуле, в данной серии спектральных линий водорода должны отсутствовать линии с длиной волны l меньше 364,56 нм (или с более высокими частотами), отвечающей n = Ґ. Так оно и оказалось, и это стало серьезным возражением против модели атома Томсона, хотя и делались попытки объяснить расхождение различием упругих возвращающих сил для разных электронов.
Исходя из модели атома Томсона, было также крайне трудно объяснить испускание атомами рентгеновского или гамма-излучения.
Затруднения в модели атома Томсона вызвало и отношение e/m заряда к массе для атомов, потерявших свои электроны («каналовых лучей»). Самый простой атом – атом водорода с одним электроном и сравнительно массивной сферой, несущей один положительный заряд. Значительно раньше, в 1815, У.Праут высказал предположение, что все более тяжелые атомы состоят из атомов водорода, и было бы понятно, если бы масса атома возрастала пропорционально числу электронов. Однако измерения показали, что отношение заряда к массе для разных элементов неодинаково. Например, масса атома неона примерно в 20 раз больше массы атома водорода, тогда как заряд составляет лишь 10 единиц положительного заряда (у атома неона 10 электронов). Дело обстояло так, как если бы положительный заряд имел переменную массу или же электронов было действительно 20, но 10 из них находились внутри сферы.
Например, масса атома неона примерно в 20 раз больше массы атома водорода, тогда как заряд составляет лишь 10 единиц положительного заряда (у атома неона 10 электронов). Дело обстояло так, как если бы положительный заряд имел переменную массу или же электронов было действительно 20, но 10 из них находились внутри сферы.
Опыты Резерфорда по рассеянию.
Затем возникла еще одна трудность. В 1903 Ф.Ленард (1862–1947) ставил опыты с прохождением пучка быстрых электронов сквозь тонкие металлические фольги. В модели атома Томсона почти все пространство заполнено веществом (положительно заряженной частью атома), а потому можно было думать, что сквозь фольгу сможет проникать лишь очень мало электронов. Ленард же обнаружил, что сквозь фольгу проходят почти все электроны. Хотя в эксперименте имелись трудности, связанные с малой массой бомбардирующих частиц, Ленард выдвинул предположение, что масса атома сосредоточена в «динамиде» – его центральной области, значительно меньшей, чем предполагалось.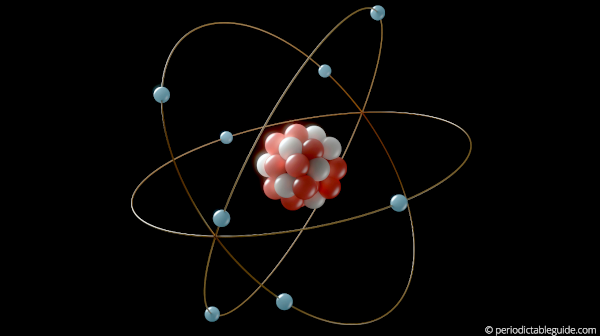
Решающий эксперимент, совершенно изменивший представления о пространственной структуре атома, был проведен Э.Резерфордом и его сотрудниками Х.Гейгером (1882–1945) и Э.Марсденом (1889–1970). Вместо электронов они использовали альфа-частицы, т.к. благодаря своей большей массе (в 7350 раз больше массы электрона) эти частицы не претерпевают заметного отклонения при столкновении с атомными электронами, что позволяет регистрировать только столкновения с положительной частью атома. В качестве источника альфа-частиц был взят радий, а частицы, претерпевавшие рассеяние в тонкой металлической фольге, например золотой, регистрировались по «сцинтилляционным» вспышкам на экране из сульфида цинка, находящемся в затемненной комнате. Схема опыта представлена на рис. 5.
Согласно модели Томсона, практически все альфа-частицы должны оказываться в пределах очень малого угла относительно своего первоначального направления, поскольку большую часть времени они должны были бы проходить в области почти равномерно распределенного положительного заряда.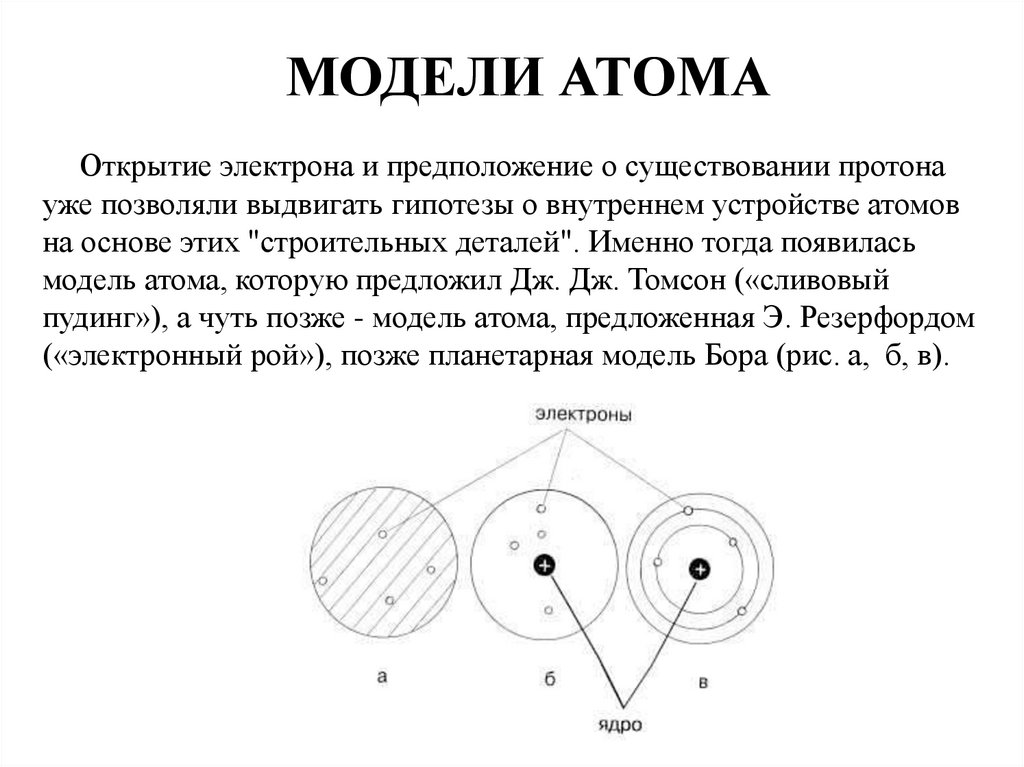 Хотя результаты Резерфорда согласовались с ожидаемым распределением в области малых отклонений, было зарегистрировано очень много отклонений на углы, гораздо большие, чем предсказывала модель атома Томсона. Столь большие отклонения можно было объяснить лишь тем, что положительная «сердцевина» атома значительно меньше размеров его электронной структуры и, следовательно, альфа-частицы могут очень близко подходить к этой малой положительной сердцевине, встречая при этом очень большие кулоновские силы. Опыты Резерфорда убедительно показали, что весь атом, кроме очень малой массивной сердцевины, или «ядра», как и предполагал Ленард, почти полностью пуст. Исходя из полученных им экспериментальных данных, Резерфорд заключил, что диаметр ядра атома золота составляет не более 6Ч10–15 м – значение, довольно близкое к современному.
Хотя результаты Резерфорда согласовались с ожидаемым распределением в области малых отклонений, было зарегистрировано очень много отклонений на углы, гораздо большие, чем предсказывала модель атома Томсона. Столь большие отклонения можно было объяснить лишь тем, что положительная «сердцевина» атома значительно меньше размеров его электронной структуры и, следовательно, альфа-частицы могут очень близко подходить к этой малой положительной сердцевине, встречая при этом очень большие кулоновские силы. Опыты Резерфорда убедительно показали, что весь атом, кроме очень малой массивной сердцевины, или «ядра», как и предполагал Ленард, почти полностью пуст. Исходя из полученных им экспериментальных данных, Резерфорд заключил, что диаметр ядра атома золота составляет не более 6Ч10–15 м – значение, довольно близкое к современному.
Резерфорду удалось, упрощенно рассматривая ядро как точечный центр рассеяния, на основе только электростатики и механики Ньютона вывести формулу для углового распределения рассеянных частиц. Между альфа-частицей с массой M и зарядом 2e, где e – заряд электрона, и ядром с зарядом Ze, где Z – атомный номер элемента, из которого состоит рассеивающее вещество, действует сила электростатического отталкивания 2Ze2/r2, где r – расстояние между зарядами. Угол j, на который происходит рассеяние, зависит от параметра столкновения p, т.е. минимального расстояния, на котором частица прошла бы мимо ядра, если бы не отклонилась.
Между альфа-частицей с массой M и зарядом 2e, где e – заряд электрона, и ядром с зарядом Ze, где Z – атомный номер элемента, из которого состоит рассеивающее вещество, действует сила электростатического отталкивания 2Ze2/r2, где r – расстояние между зарядами. Угол j, на который происходит рассеяние, зависит от параметра столкновения p, т.е. минимального расстояния, на котором частица прошла бы мимо ядра, если бы не отклонилась.
Как видно из рис. 6, наибольшему углу отклонения отвечает наименьший параметр столкновения. Доля альфа-частиц, отклоняющихся на угол j и более, дается выражением
где n – число атомов в 1 см3, t – толщина фольги, M и v – масса и скорость альфа-частицы и Z – заряд ядра. Этот закон рассеяния Резерфорда чаще записывают в виде доли частиц df, которая рассеивается в телесный угол dw в интервале углов от j до j + dj:
Эти выражения получили количественное подтверждение для широкого диапазона углов и разных рассеивающих материалов и позволили измерить заряд ядра.
Резерфордовская, или ядерная, модель атома, вытеснив томсоновскую модель, явилась важным этапом на пути создания квантовой механики. Детальные эксперименты, выполненные Гейгером и Марсденом в 1913, не оставили и тени сомнения в том, что картина атома с малым массивным ядром в центре электронной структуры значительно больших размеров верна не только качественно, но и количественно. Некоторые детали, перенесенные из томсоновской модели, такие, как существование в ядре электронов, позднее также были отброшены.
Квантовая теория Бора.
Н.Бор (1885–1962) работал в 1912–1913 у Резерфорда, когда тот проводил опыты по рассеянию, и вернулся в 1913 в Копенгаген с множеством новых идей. Требовал своего объяснения ряд явлений, помимо только что открытых в «ядерных» экспериментах по рассеянию. Теперь, когда была отвергнута томсоновская модель атома, узкие, дискретные спектральные линии в излучении разрядных трубок и эмпирические закономерности в их частотах казались еще менее понятными.
Был и другой атомный эффект, открытый в 1887 Г.Герцем (1857–1894), а именно фотоэффект. Суть его в том, что свет, падающий на свежеочищенную поверхность металла, выбивает из нее электроны, если частота света достаточно высока. Для каждого металла имеется своя пороговая частота. Опыты показали, что тормозящее электростатическое поле, уменьшающее до нуля ток фотоэлектронов, не зависит от интенсивности света, но зависит от его длины волны. Электромагнитная теория, согласно которой свет представляет собой электромагнитные волны, оказалась не в состоянии объяснить это, поскольку по этой теории для испускания электрона с любой скоростью атому нужно только достаточно долго поглощать энергию. В 1905 А.Эйнштейн (1879–1955) предложил объяснение фотоэффекта, которое полностью согласовалось с экспериментальными данными, но требовало коренного пересмотра существовавшей концепции света как волнового процесса. Эйнштейн предположил, что свет переносит энергию порциями, которые называются фотонами или квантами света, причем их энергия дается выражением E = hn, где n – частота света, а h – «постоянная Планка», равная 6,626Ч10–34 ДжЧс. Попадая на поверхность металла, фотон передает всю свою энергию электрону. Поскольку электрон связан с поверхностью электростатическими силами, ему для вылета необходима энергия W («работа выхода»), а остальная часть полученной электроном энергии превращается в его кинетическую энергию, т.е. hn = W + 1/2mv2. Гипотеза Эйнштейна объясняла, почему кинетическая энергия фотоэлектронов зависит от частоты света, а число испускаемых электронов – от его интенсивности.
Попадая на поверхность металла, фотон передает всю свою энергию электрону. Поскольку электрон связан с поверхностью электростатическими силами, ему для вылета необходима энергия W («работа выхода»), а остальная часть полученной электроном энергии превращается в его кинетическую энергию, т.е. hn = W + 1/2mv2. Гипотеза Эйнштейна объясняла, почему кинетическая энергия фотоэлектронов зависит от частоты света, а число испускаемых электронов – от его интенсивности.
Как часто происходит с научными открытиями, оказалось, что гипотеза «квантов» Эйнштейна имеет в своей основе более раннюю теорию. М.Планк (1858–1947) первым привлек идею квантования для объяснения наблюдаемого спектрального состава излучения нагретых тел. Ему удалось объяснить спектр, предположив, что гармонические осцилляторы поглощают и излучают лишь дискретные порции энергии hn.
Бор блестяще применил квантовую гипотезу к описанию орбит электронов в атомах и их излучения. Он отбросил идею о том, что электроны ведут себя подобно осцилляторам, а вместо этого представил динамику атома в виде движения электронов по орбитам вокруг ядра, наподобие движения планет по орбитам вокруг Солнца. Сила электростатического притяжения электрона ядром является центростремительной силой, заставляющей электрон двигаться по круговой орбите радиуса r со скоростью v. В общем случае ядра с зарядом Ze имеем
Он отбросил идею о том, что электроны ведут себя подобно осцилляторам, а вместо этого представил динамику атома в виде движения электронов по орбитам вокруг ядра, наподобие движения планет по орбитам вокруг Солнца. Сила электростатического притяжения электрона ядром является центростремительной силой, заставляющей электрон двигаться по круговой орбите радиуса r со скоростью v. В общем случае ядра с зарядом Ze имеем
В таком силовом поле (когда сила обратно пропорциональна расстоянию до центра притяжения) кинетическая энергия движения всегда равна – 1/2 потенциальной энергии:
а полная энергия, т.е. сумма кинетической и потенциальной энергий, равна:
Эти соотношения следуют из обычных законов механики и электростатики. Бор, в дополнение к ним, сформулировал следующие постулаты, составляющие основу квантовой теории атома.
I. Разрешены только такие круговые орбиты, для которых момент импульса равен целому числу в единицах постоянной Планка, деленной на 2p. (Момент импульса тела l, движущегося по круговой орбите, равен произведению его массы m на скорость v и радиус орбиты r.) Таким образом,
(Момент импульса тела l, движущегося по круговой орбите, равен произведению его массы m на скорость v и радиус орбиты r.) Таким образом,
II. Хотя, согласно электромагнитной теории, любая заряженная частица, движущаяся с ускорением, должна испускать излучение, электроны не испускают излучения, двигаясь по своим орбитам внутри атома. Излучение возникает только при переходе электрона с одной квантованной орбиты на другую.
III. Частота этого излучения определяется изменением полной энергии, т.е. разностью энергий атома в начальном и конечном состояниях:
hn = E2 – E1.
Эти условия квантования энергии приводят к дискретным орбитам электронов. Решая уравнение (2) относительно скорости и подставляя в (4), получаем
или, если ввести «боровский радиус» a0 = h2/4p2me2 » 5,29Ч10–11 м,
На рис. 7 изображены первые шесть орбит электронов в атоме водорода, соответствующие теории Бора. Показаны также переходы, сопровождающиеся испусканием дискретных спектральных линий. Каждая серия спектральных линий носит имя ее открывателя; из всех серий лишь часть серии Бальмера лежит в видимой области спектра.
7 изображены первые шесть орбит электронов в атоме водорода, соответствующие теории Бора. Показаны также переходы, сопровождающиеся испусканием дискретных спектральных линий. Каждая серия спектральных линий носит имя ее открывателя; из всех серий лишь часть серии Бальмера лежит в видимой области спектра.
На рис. 8 показано, как выглядят линии серии Бальмера на фотопластинке спектрографа. Нетрудно видеть, что линии сгущаются вблизи границы серии.
Энергии состояний атома, отвечающих каждому целому значению n, также квантованы:
Используя третий постулат Бора и соотношение с = ln между скоростью, длиной волны и частотой, можно теперь объяснить эмпирическую формулу, найденную Бальмером для его серии линий:
просто как частный случай формулы Бора. С ее помощью можно вычислить «постоянную Ридберга» RH :
Значение RH, найденное Бальмером, составляло 10967776 м–1; используя имевшиеся в то время значения m, e, c и h, Бор получил RH = 1,03Ч107 м–1. Современное значение RH составляет 10979708 м–1. Таким образом, соответствие теории Бора с экспериментом достаточно хорошее. Расхождение в величине RH объясняется неточностью значений фундаментальных констант m, e, c, h, которыми пользовался Бор, а также необходимостью учета ряда поправок, главной из которых является поправка на движение ядра (см. ниже).
Современное значение RH составляет 10979708 м–1. Таким образом, соответствие теории Бора с экспериментом достаточно хорошее. Расхождение в величине RH объясняется неточностью значений фундаментальных констант m, e, c, h, которыми пользовался Бор, а также необходимостью учета ряда поправок, главной из которых является поправка на движение ядра (см. ниже).
Таким образом, Бор своей теорией с самого начала добился значительного успеха, дав не только качественное, но и количественное объяснение линиям водородного спектра и применив представления Планка и Эйнштейна о квантах в теории оптических спектров.
В 1914 Дж.Франк (1882–1964) и Г.Герц (1887–1975) экспериментально подтвердили правильность представления о квантовании энергетических уровней, бомбардируя атомы паров ртути электронами с известной энергией. Они измеряли энергию, теряемую электронами при рассеянии на атомах ртути. Электроны с энергией ниже определенного порогового значения вообще не передавали энергию атомам ртути; но, как только энергия электронов оказывалась достаточной для возбуждения перехода атома ртути на ближайший уровень с более высокой энергией, электроны интенсивно передавали свою энергию. Это было убедительным доказательством существования квантованных энергетических уровней.
Это было убедительным доказательством существования квантованных энергетических уровней.
Теория Бора позволила объяснить и происхождение рентгеновского излучения (X-лучей): это излучение испускается в результате выбивания (бомбардирующим атом электроном) электрона с внутренней орбиты атома: на освободившееся место переходят электроны с внешних оболочек атома. Поскольку энергия при этом изменяется значительно больше, чем при оптическом переходе, рентгеновское излучение оказывается более коротковолновым, нежели видимый свет, и более проникающим. Теория Бора объяснила не только линии Бальмера, наблюдаемые в видимой части спектра, но и другие серии линий в ультрафиолетовой (серию Лаймана) и инфракрасной (серию Пашена) области, которые были обнаружены с помощью фотографических методов.
Хотя масса M ядра водорода (протона) значительно больше массы электрона, движущегося по орбите в атоме, было бы неправильным считать, что в этой «динамической» модели атома протон покоится. Как указал А.Зоммерфельд (1868–1951), в силу законов сохранения энергии и импульса ядро и электрон должны вращаться относительно общего центра масс с одинаковой угловой скоростью (при этом ядро расположено гораздо ближе к центру масс). Влияние этого движения ядра на энергию электронных состояний можно учесть, просто заменив массу электрона m «приведенной массой»
Как указал А.Зоммерфельд (1868–1951), в силу законов сохранения энергии и импульса ядро и электрон должны вращаться относительно общего центра масс с одинаковой угловой скоростью (при этом ядро расположено гораздо ближе к центру масс). Влияние этого движения ядра на энергию электронных состояний можно учесть, просто заменив массу электрона m «приведенной массой»
где M – масса ядра рассматриваемого атома. В случае водорода величина m меньше m на 1/1837. Однако точность спектроскопических измерений такова, что такая поправка заметно улучшает согласие теории с экспериментом.
Эффектной демонстрацией возможностей модифицированной теории Бора для атома водорода явилось открытие «тяжелого водорода» (дейтерия) 2Н. Масса ядра дейтерия почти вдвое превышает массу протона, и хотя дейтерий составляет всего 1/4500 часть обычного газообразного водорода, его наличие проявляется на фотоснимках спектра, сделанных с высоким разрешением, в виде очень слабых линий, сдвинутых относительно основных линий из-за различия в величине m. После того как Ф.Астон (1977–1945) обнаружил в 1931 очевидное расхождение в значениях атомной массы водорода, Р.Бёрдж (1887–1980) и Д.Менцель выдвинули гипотезу о существовании двух разновидностей водорода с разными массами изотопов. В 1932 Г.Юри (1893–1981), Дж.Мерфи и Ф.Брикведде (1903–1989) провели серию экспериментов, в которых спектр водорода фотографировался с помощью вогнутой дифракционной решетки радиусом 6,4 м. Они обнаружили слабые дейтериевые линии там, где их предсказывали (длина волны, отвечающая линии Ha , была смещена на 179,3 нм), и, взяв образцы, обогащенные тяжелым изотопом, получили не вызывающие сомнения яркие линии.
После того как Ф.Астон (1977–1945) обнаружил в 1931 очевидное расхождение в значениях атомной массы водорода, Р.Бёрдж (1887–1980) и Д.Менцель выдвинули гипотезу о существовании двух разновидностей водорода с разными массами изотопов. В 1932 Г.Юри (1893–1981), Дж.Мерфи и Ф.Брикведде (1903–1989) провели серию экспериментов, в которых спектр водорода фотографировался с помощью вогнутой дифракционной решетки радиусом 6,4 м. Они обнаружили слабые дейтериевые линии там, где их предсказывали (длина волны, отвечающая линии Ha , была смещена на 179,3 нм), и, взяв образцы, обогащенные тяжелым изотопом, получили не вызывающие сомнения яркие линии.
Зоммерфельд развил далее теорию Бора, указав на то, что круговые орбиты – это лишь частный случай и что постулаты Бора могут быть введены и в случае эллиптических орбит. (При движении по эллиптической орбите скорость наряду с азимутальной имеет и радиальную составляющую. При этом движение происходит в одной плоскости, а центр притяжения располагается в одном из фокусов. ) Таким образом, на обобщенный импульс pi налагаются два условия квантования, связанные с «периодическими координатами» qi. (Область изменения периодических координат повторяется с определенным периодом; например, угловое положение электрона относительно ядра представляет собой периодическую координату.) В общем случае
) Таким образом, на обобщенный импульс pi налагаются два условия квантования, связанные с «периодическими координатами» qi. (Область изменения периодических координат повторяется с определенным периодом; например, угловое положение электрона относительно ядра представляет собой периодическую координату.) В общем случае
Таким образом, для того чтобы орбита существовала, интеграл от импульса по координате за период должен быть равен целому числу постоянных Планка. При движении по эллиптической орбите существуют два независимых уравнения
где pj – азимутальный, а pr – радиальный импульс. (Радиальный импульс prравен произведению массы на радиальную скорость, которая в случае круговой орбиты равна нулю.) Классическая механика движения по эллиптическим орбитам, справедливая для описания движения планет, была хорошо известна, и, следовательно, ее можно было непосредственно использовать в случае атомных орбит. Согласно механике Ньютона, переход от эллиптической орбиты к круговой не сопровождается изменением энергии уровня, поскольку в случае эллипса энергия зависит только от большой полуоси эллипса, которая в свою очередь зависит лишь от
Согласно механике Ньютона, переход от эллиптической орбиты к круговой не сопровождается изменением энергии уровня, поскольку в случае эллипса энергия зависит только от большой полуоси эллипса, которая в свою очередь зависит лишь от
Таким образом, число n («главное квантовое число») отвечает одной и той же энергии для некоего набора эллиптических орбит, включающего в себя и круговую, для которой nY = 0.
Измерения, проведенные с более высоким разрешением, показали существование «тонкой структуры» спектральных линий (одна широкая «линия» в действительности состоит из нескольких линий). Частично это было связано с тем, как было показано Зоммерфельдом, что электроны движутся со скоростями, сравнимыми со скоростью света и, следовательно, вместо механики Ньютона следует использовать релятивистскую механику Эйнштейна. В результате в энергиях эллиптических орбит возникает небольшое различие, поскольку скорости меняются в зависимости от эсцентриситета.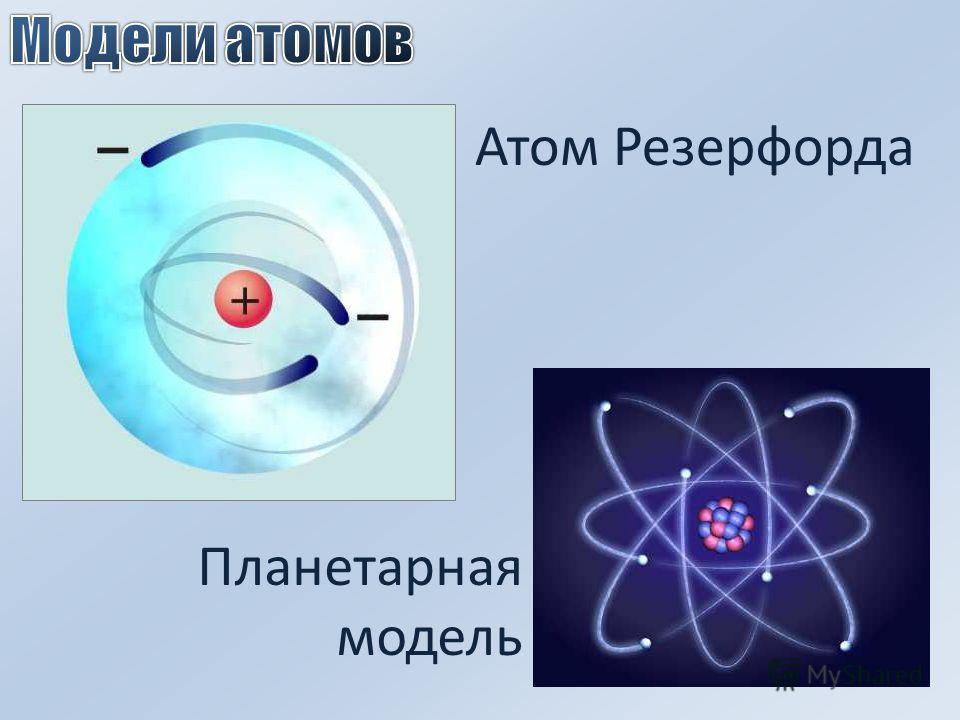 Поправка может быть выражена через квантовые числа n и nj:
Поправка может быть выражена через квантовые числа n и nj:
где величина
есть так называемая постоянная тонкой структуры, или постоянная Зоммерфельда. Существование этих небольших поправок, зависящих от эллиптичности орбиты, значительно увеличивает число возможных переходов. Чтобы учесть отсутствие некоторых из предсказанных спектральных линий, пришлось ввести «правила отбора», допускающие изменение азимутального квантового числа nj только на +1 или -1.
Таким образом, квантовая теория Бора, дополненная более точной механикой орбитального движения Зоммерфельда, оказалась способной объяснить широкий круг явлений. Стало понятным существование серий спектральных линий водорода, наличие их тонкой структуры, характеристики неупругого рассеяния электронов в газах и изотопическое смещение спектральных линий. Кроме того, удалось точно вычислить потенциал ионизации водорода (энергию, необходимую для выбивания электрона из атома).
Однако трудности все же остались. Теория Бора давала хорошие результаты в случае одноэлектронных атомов типа водорода, однократно ионизованного гелия, дважды ионизованного лития, а также, например, натрия (благодаря тому, что в атоме натрия есть один слабо связанный электрон, котрый в основном и определяет как спектр, так и химические свойства натрия), но она плохо описывала обычный атом гелия с двумя электронами и другие многоэлектронные атомы. Неудачными оказались также попытки Бора объяснить хорошо известные изменения химических и физических свойств при переходе от атома к атому. Наконец, и постулаты Бора, например, квантование момента импульса на электронных орбитах, выглядели совершенно произвольными.
Дело в том, что в то время были неизвестны два положения, без которых понять строение сложных атомов невозможно, – принцип запрета Паули и существование у электрона спина. Эти положения наряду с созданием новой механики, названной волновой, или квантовой, были необходимы для полного понимания строения атома.
Квантовая механика атома.
Недостатки теории Бора, основанной на механике классических частиц с дополнением в виде квантовых постулатов, высветили фундаментальную проблему правильного описания движения электронов на малых расстояниях, например, внутри атома. Опираясь на то, что свет имеет как корпускулярные, так и волновые свойства (в некторых явлениях, например, при фотоэффекте, он ведет себя как поток частиц, а в некоторых, например, при интерференции, как волна), Л.де Бройль (1892–1987) в 1923 выдвинул гипотезу о том, что корпускулярно-волновой дуализм свойствен также и веществу. Поскольку квантовая теория приписывает световым фотонам при фотоэффекте корпускулярное поведение, можно допустить, что электроны в атомах могут вести себя на своих «орбитах» подобно волнам. Де Бройль пришел к выводу, что с движением любого вида частиц можно «ассоциировать» распространение волны, если приписать частице с массой m и скоростью v длину волны
l = h/mv.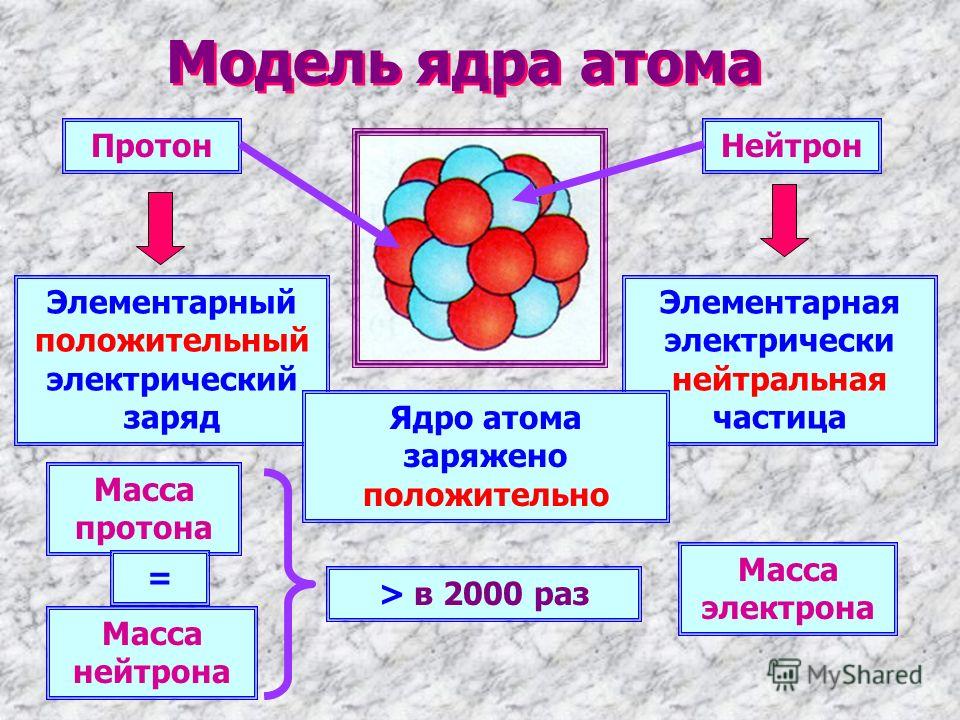
Экспериментальным подтверждением волновых свойств частиц явилось открытое в 1927 К.Дэвиссоном (1881–1958) и Л.Джермером (1896–1971) явление дифракции электронов. Угловое распределение электронов при отражении пучка электронов от поверхности кристалла можно объяснить лишь на основе волновых представлений, причем наблюдалось согласие с постулированным де Бройлем соотношением между длиной волны и скоростью.
Разработка квантовой механики В.Гейзенбергом (1901–1976), Э.Шрёдингером (1887–1961) и другими теоретиками в период, последовавший за высказанной де Бройлем гипотезой, привела к прояснению ситуации с теорией Бора. Например, в теории Бора условие «стационарных состояний»
mvЧ2pr = nh
носило характер произвольного требования. Теперь же оно выступает как требование, чтобы на периодической орбите электрона укладывалось целое число длин волн де Бройля. Разрешенными оказываются именно те орбиты, которые удовлетворяют этому требованию.
При решении волнового уравнения Шрёдингера для атома водорода естественным образом возникают три квантовых числа, обычно обозначаемые символами n, l и ml. Здесь n – целое число, принимающее любые значения, большие 0, которое называется главным квантовым числом электрона. Оно соответствует числу n, обозначавшему различные боровские орбиты. Число l (орбитальное квантовое число) тоже целое и может принимать любые значения от 0 до (n – 1). Оно характеризует орбитальный момент импульса электрона и тесно связано с nj в модели Бора. Из решения волнового уравнения следует, что разрешены только значения орбитального момента импульса электрона, равные:
Здесь n – целое число, принимающее любые значения, большие 0, которое называется главным квантовым числом электрона. Оно соответствует числу n, обозначавшему различные боровские орбиты. Число l (орбитальное квантовое число) тоже целое и может принимать любые значения от 0 до (n – 1). Оно характеризует орбитальный момент импульса электрона и тесно связано с nj в модели Бора. Из решения волнового уравнения следует, что разрешены только значения орбитального момента импульса электрона, равные:
При максимально допустимое значение l равно нулю, и, следовательно, орбитальный момент импульса электрона тоже должен быть равен нулю.
Третье квантовое число ml называется «магнитным квантовым числом» и играет важную роль, когда атом находится в магнитном поле H. В этом случае квантуется не только орбитальный момент импульса pj, но и его проекция на направление магнитного поля. Проекция квантового числа l на направление поля H также должна быть целым числом, ml. Таким образом, ml может принимать (2l + 1) значений: +l, (l – 1), (l – 2),…, –(l – 1), –l. В рамках модели Бора это соответствует заданию угла q наклона плоскости электронной орбиты относительно направления магнитного поля, как показано на рис. 9:
Проекция квантового числа l на направление поля H также должна быть целым числом, ml. Таким образом, ml может принимать (2l + 1) значений: +l, (l – 1), (l – 2),…, –(l – 1), –l. В рамках модели Бора это соответствует заданию угла q наклона плоскости электронной орбиты относительно направления магнитного поля, как показано на рис. 9:
cosq = ml/l.
Если l = 3, то существует (2l + 1), т.е. 7 различных дискретных значений угла, которые могут составлять боровские орбиты с направлением H (рис. 9,б).
Еще одно следствие правил квантования ml состоит в том, что магнитный момент m может принимать значения
m = leh/4pmc = lm,
где величина m0, так называемый магнетон Бора, равна 9,27Ч10–24 Дж/Тл. Изменение энергии электрона, обусловленное взаимодействием его момента с магнитным полем, равно:
Изменение энергии электрона, обусловленное взаимодействием его момента с магнитным полем, равно:
DE = m0Hml.
Таким образом, магнитное поле приводит к расщеплению уровней и увеличению числа переходов и спектральных линий, т.е. к эффекту Зеемана.
Спин электрона и принцип запрета Паули.
В то время, когда формировались идеи квантовой механики, для объяснения характеристик линейчатых спектров атомов была выдвинута гипотеза спина электрона. Спектроскопия более высокого разрешения показала, что многие линии представляют собой дублеты, которые не удается объяснить, исходя из орбитального движения электронов. Особенно показательный пример – дублет желтых линий натрия 589,0 и 589,6 нм, который четко разделяется даже простыми спектрометрическими приборами.
Для объяснения частого появления дублетов в линейчатых спектрах Дж.Уленбек (1900–1988) и С.Гаудсмит (1902–1978) выдвинули в 1925 предположение, что электрон имеет собственный момент импульса, или спин, т. е. его можно представить себе вращающимся вокруг собственной оси одновременно с вращением по орбите вокруг ядра, аналогично вращению Земли при ее движении вокруг Солнца. Спин характеризуется еще одним квантовым числом, s. Поскольку вектор спинового момента импульса имеет (2s + 1) различных ориентаций, а наблюдаемая кратность энергетических уровней равна двум, имеем (2s + 1) = 2, или s = 1/2. Проекции вектора s на некое выделенное направление (направление внешнего магнитного поля) характеризуются спиновым магнитным квантовым числом ms, которое может быть равно либо +1/2, либо -1/2. Вращающийся вокруг собственной оси электрон подобен крошечному магниту с магнитным моментом
е. его можно представить себе вращающимся вокруг собственной оси одновременно с вращением по орбите вокруг ядра, аналогично вращению Земли при ее движении вокруг Солнца. Спин характеризуется еще одним квантовым числом, s. Поскольку вектор спинового момента импульса имеет (2s + 1) различных ориентаций, а наблюдаемая кратность энергетических уровней равна двум, имеем (2s + 1) = 2, или s = 1/2. Проекции вектора s на некое выделенное направление (направление внешнего магнитного поля) характеризуются спиновым магнитным квантовым числом ms, которое может быть равно либо +1/2, либо -1/2. Вращающийся вокруг собственной оси электрон подобен крошечному магниту с магнитным моментом
В конечном итоге получается 4 независимых квантовых числа, характеризующих состояние электрона в атоме:
n – главное квантовое число;
l – орбитальное квантовое число;
ml – орбитальное магнитное квантовое число;
ms – спиновое магнитное квантовое число.
Хотя квантовая механика позволяет, если заданы квантовые числа, определить энергию состояния и пространственное распределение электронной плотности вероятностей (заменяющее орбиты в модели Бора), для фиксации числа электронов в каждом состоянии требуются дальнейшие предположения.
В 1925 В.Паули (1900–1958) сформулировал «принцип запрета», который сразу внес ясность в очень многие атомные явления. Он предложил простое правило: в каждом отдельном квантовом состоянии может находиться только один электрон. Это означает, что набор чисел, отвечающих данным n, l и ml, зависит от n. Например, при n = 1 возможно лишь l = 0; следовательно, ml = 0 и единственное различие состояний связано с ms = +1/2 и -1/2. В таблице приведены возможности, отвечающие различным n. Отметим, что в первой «оболочке» (n = 1) имеются 2 электрона, в следующей оболочке (n = 2) имеется 8 электронов, образующих две подоболочки, и т. д. Максимальное число электронов в подоболочке равно 2(2l + 1), а максимальное число подоболочек составляет n. Для каждого n полностью заполненная оболочка содержит 2n2 электронов.
д. Максимальное число электронов в подоболочке равно 2(2l + 1), а максимальное число подоболочек составляет n. Для каждого n полностью заполненная оболочка содержит 2n2 электронов.
| ВОЗМОЖНОЕ ЧИСЛО ЭЛЕКТРОНОВ В ДАННОЙ ОБОЛОЧКЕ | |||||
| n | l | ml | ms | Число электронов в подоболочке | Число электронов в заполненной оболочке |
| 1 1 | 0 0 | 0 0 | +1/2 –1/2 | 2 | 2 |
| 2 2 | 0 0 | 0 0 | +1/2 –1/2 | 2 | |
| 2 2 2 2 2 2 | 1 1 1 1 1 1 | –1 –1 0 0 1 1 | +1/2 –1/2 +1/2 –1/2 +1/2 –1/2 | 6 | 8 |
| 3 3 | 0 0 | 0 0 | +1/2 –1/2 | 2 | |
| 3 3 3 3 3 3 | 1 1 1 1 1 1 | –1 –1 0 0 1 1 | +1/2 –1/2 +1/2 –1/2 +1/2 –1/2 | 6 | |
| 3 3 3 3 3 3 3 3 3 3 | 2 2 2 2 2 2 2 2 2 2 | –2 –2 –1 –1 0 0 1 1 2 2 | +1/2 –1/2 +1/2 –1/2 +1/2 –1/2 +1/2 –1/2 +1/2 –1/2 | 10 | 18 |
Соответствие принципа Паули эксперименту было подтверждено огромным числом спектроскопических наблюдений, а также многочисленными данными электронной теории металлов, физики ядерных процессов, низкотемпературных явлений. Это один из наиболее фундаментальных объединяющих принципов физики, открывший путь к пониманию электронной структуры сложных атомов. Правда, принципом Паули определяется лишь возможность заполнения различных электронных оболочек, а для проверки фактического заполнения тех или иных состояний необходимы данные, полученные на основе оптических и рентгеновских спектров. Но в атомах вплоть до аргона с Z = 18 каждый дополнительный электрон просто добавляется в низшую из незаполненных подоболочек. Отступления от этого порядка наблюдаются у более сложных атомов, оболочки которых частично перекрываются. Квантовая механика объясняет это отступление тем, что в первую очередь заполняются состояния с самой низкой энергией.
Это один из наиболее фундаментальных объединяющих принципов физики, открывший путь к пониманию электронной структуры сложных атомов. Правда, принципом Паули определяется лишь возможность заполнения различных электронных оболочек, а для проверки фактического заполнения тех или иных состояний необходимы данные, полученные на основе оптических и рентгеновских спектров. Но в атомах вплоть до аргона с Z = 18 каждый дополнительный электрон просто добавляется в низшую из незаполненных подоболочек. Отступления от этого порядка наблюдаются у более сложных атомов, оболочки которых частично перекрываются. Квантовая механика объясняет это отступление тем, что в первую очередь заполняются состояния с самой низкой энергией.
Детальный анализ электронной структуры и распределения электронов с точки зрения квантовой механики и принципа Паули в более тяжелых атомах весьма сложен. Для состояния 1s (n = 1, l = 0) возможно только сферически симметричное распределение (причем наиболее вероятным оказывается положение электрона в центре атома).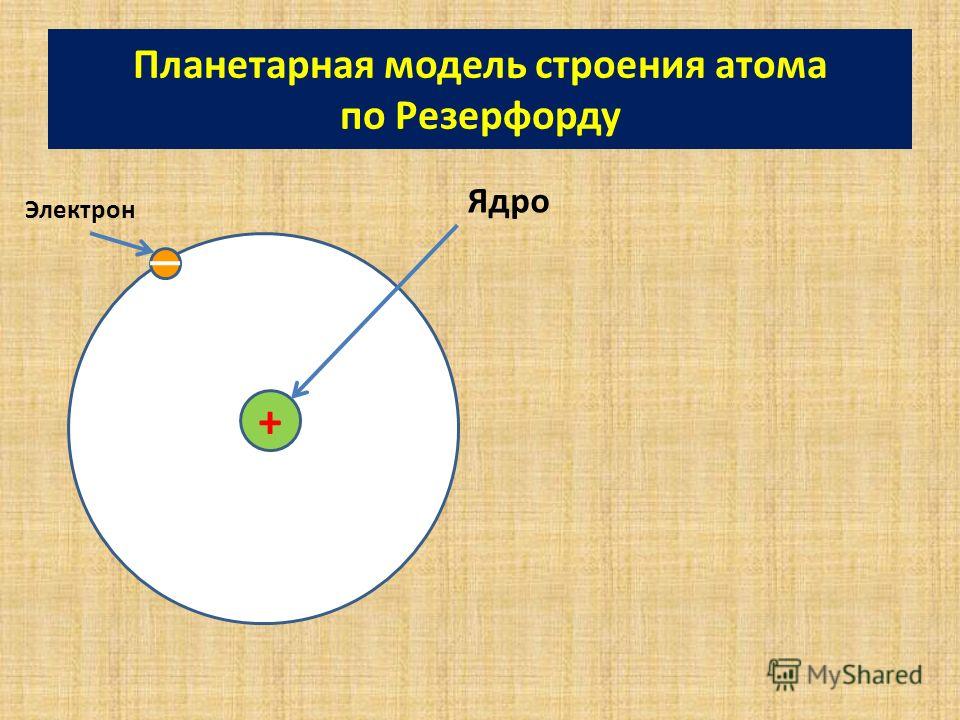 В состоянии 2p (n = 2, l = 1) момент импульса электрона уже не равен нулю, и поэтому масимум плотности находится на ненулевом расстоянии от ядра. Распределение электронной плотности зависит от квантового числа ml в соответствии с требованием квантования компонент момента импульса вдоль направления магнитного поля.
В состоянии 2p (n = 2, l = 1) момент импульса электрона уже не равен нулю, и поэтому масимум плотности находится на ненулевом расстоянии от ядра. Распределение электронной плотности зависит от квантового числа ml в соответствии с требованием квантования компонент момента импульса вдоль направления магнитного поля.
Периодическая система элементов.
Число электронов, находящихся в оболочках нейтрального атома, равное числу протонов в его ядре, называется атомным номером элемента. Периодическая система элементов, предложенная в 1869 Д.И.Менделеевым (1834–1907) – это таблица, в которой элементы располагаются в порядке возрастания атомного номера и распределяются по периодам так, что атомы со сходными химическими свойствами попадают в одну и ту же группу. Например, группа, содержащая гелий, неон, аргон, криптон, ксенон и радон, составляет группу инертных газов; это атомы с заполненными электронными оболочками, а из заполненной оболочки почти так же трудно удалить электрон, как и добавить в нее лишний. Кроме того, эти газы – одноатомные, их молекулы представляют собой один атом (см. также ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ).
Кроме того, эти газы – одноатомные, их молекулы представляют собой один атом (см. также ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ).
Химические свойства атомов в значительной степени определяются внешними электронами. Простой характер таблицы вплоть до аргона (атомный номер которого Z = 18) обусловлен тем, что при добавлении очередного электрона вплоть до Z = 18 последовательно заполняется низшая подоболочка. Значительное же усложнение таблицы после Z = 18 объясняется усложнением последовательности заполнения подоболочек. Для случая, когда имеется большое число электронов, точные решения уравнений квантовой механики получить не удается, и используются приближенные методы. Одно из приближений состоит в том, что атом с единственным электроном сверх заполненной оболочки, такой, как натрий, Z = 11, рассматривается как «одноэлектронный» атом. И действительно, упрощенная теория Бора (модифицированная с учетом значения n = 3 для состояния электрона) дает довольно точные значения для энергии уровней (но не для расщепления линий).
Дальнейшее исследование структуры атомов.
В настоящее время электронная структура атомов в принципе получила свое объяснение, хотя свойства многоэлектронных атомов удается рассчитать лишь приближенно. Квантовая механика объясняет все известные свойства отдельных атомов. Активно изучается взаимодействие атомов, особенно в твердых телах. Строению атомного ядра посвящена статья.
Атом: ядро плюс электроны – Учебник по Химии. 8 класс. Григорович
Учебник по Химии. 8 класс. Григорович – Новая программа
Открытие сложного строения атомов
Вам уже известно, что все вещества состоят из атомов, молекул или ионов. В свою очередь, молекулы и ионы образованы из атомов.
Долгое время считалось, что атом невозможно разделить на более мелкие частицы. До начала XX в. была известна только одна количественная характеристика атомов — относительная атомная масса, которая была взята за основу классификации химических элементов. Но, используя только массу атомов, нельзя было объяснить причины периодичности изменения их свойств. Было непонятно, почему атомы с близкими массами, например Алюминий и Силиций, существенно отличаются по свойствам, тогда как атомы с разными массами обладают сходными свойствами. Таким образом, для характеристики атомов знания одной лишь их массы недостаточно. Все это наводило ученых на мысль о том, что атом имеет сложное строение. В начале XX в. было выдвинуто множество гипотез и моделей строения атома, некоторые из которых представлены на рисунке 9.1.
Было непонятно, почему атомы с близкими массами, например Алюминий и Силиций, существенно отличаются по свойствам, тогда как атомы с разными массами обладают сходными свойствами. Таким образом, для характеристики атомов знания одной лишь их массы недостаточно. Все это наводило ученых на мысль о том, что атом имеет сложное строение. В начале XX в. было выдвинуто множество гипотез и моделей строения атома, некоторые из которых представлены на рисунке 9.1.
Рис. 9.1. а — «кексовая» модель атома Уильяма Томсона (1902), который представлял атом сгустком положительно заряженной материи, где равномерно распределены электроны, как изюм в кексе; б — «кексовая» модель, усовершенствованная Джозефом Джоном Томпсоном (1904), в которой электроны расположены в одной плоскости и образуют концентрические кольца; в — модель атома Хантаро Нагаока (1904), предположившего, что атом похож на планету Сатурн — половину объема занимает положительно заряженный шар, вокруг которого спутники-электроны образуют кольцо
Наибольших успехов в исследовании атома достиг английский ученый Эрнест Резерфорд. В 1909 г. он провел эксперимент, в котором бомбардировал золотую фольгу положительно заряженными альфа-частицами. Большинство из них, проходя сквозь фольгу, не отклонялись от начального направления, некоторые незначительно отклонялись, а небольшое число альфа-частиц существенно отклонялись от первоначальной траектории и иногда даже летели в обратном направлении. Резерфорд писал, что это было так удивительно, как будто вы выстреливаете из пушки в лист бумаги, а пушечное ядро отталкивается от него и летит назад вам в лоб.
В 1909 г. он провел эксперимент, в котором бомбардировал золотую фольгу положительно заряженными альфа-частицами. Большинство из них, проходя сквозь фольгу, не отклонялись от начального направления, некоторые незначительно отклонялись, а небольшое число альфа-частиц существенно отклонялись от первоначальной траектории и иногда даже летели в обратном направлении. Резерфорд писал, что это было так удивительно, как будто вы выстреливаете из пушки в лист бумаги, а пушечное ядро отталкивается от него и летит назад вам в лоб.
Эрнест Резерфорд (1871-1937)
Английский физик, лауреат Нобелевской премии по химии 1908 г. Является основателем нового направления науки — ядерной физики. Он создал учение о радиоактивности и строении атома. Предложил новую, революционную для того времени теорию строения атома, которая сегодня является общепризнанной. Этим он опроверг мнение о неделимости атома и ошеломил весь мир идеей, что все тела (даже самые твердые) преимущественно являются пустым пространством, в котором движутся крохотные частицы. Осуществил первую искусственную ядерную реакцию и продемонстрировал возможности использования ядерной энергии. Предсказал существование нейтрона.
Осуществил первую искусственную ядерную реакцию и продемонстрировал возможности использования ядерной энергии. Предсказал существование нейтрона.
Результаты этого эксперимента противоречили популярным в то время моделям атомов. Если бы «кексовая» модель атома соответствовала действительности, то альфа-частицы должны были бы свободно проходить сквозь атомы золотой фольги (рис. 9.2). Поскольку альфа-частицы заряжены положительно, то для того чтобы отражаться от фольги, они должны сталкиваться с другими положительно заряженными частицами в составе атомов, образующих золотую фольгу. Основываясь на результатах своего эксперимента, Резерфорд доказал, что положительный заряд в атоме сконцентрирован в центре атома в очень небольшом объеме, который он назвал ядром. В ходе эксперимента чем ближе к ядру пролетали альфа-частицы, тем сильнее искривлялась их траектория, а частицы, попавшие прямо в ядро, отталкивались от него и летели назад (рис. 9.3).
Рис. 9.2. Если бы атомы фольги соответствовали «кексовой» модели, то альфа-частицы свободно проходили бы сквозь пластинку
Рис.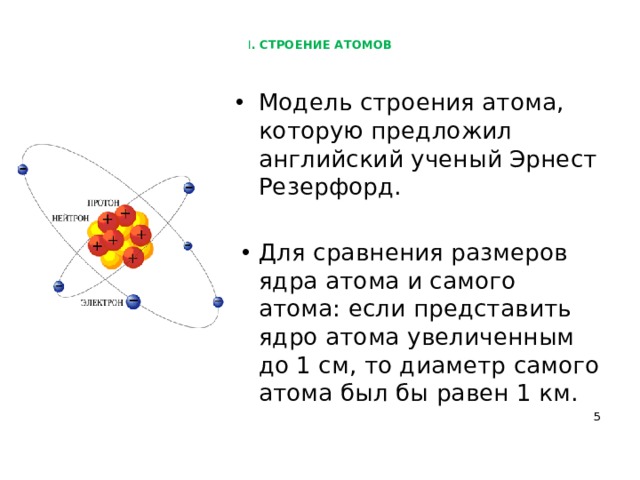 9.3. Изменение траектории альфа-частиц связано с отталкиванием от положительно заряженного ядра
9.3. Изменение траектории альфа-частиц связано с отталкиванием от положительно заряженного ядра
Резерфорд предложил планетарную модель строения атома, которой с небольшими изменениями мы пользуемся и сегодня (рис. 9.4). Согласно этой модели, весь положительный заряд атома сосредоточен в центре — ядре, которое окружено отрицательно заряженными электронами. Электроны движутся вокруг ядра по определенным орбитам, как планеты вокруг Солнца.
Рис. 9.4. Планетарная модель строения атома, предложенная Резерфордом
Атом — это электронейтральная химически неделимая частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов.
Модель атома Резерфорда, без сомнения, лучше всех остальных отображала истинное строение атома, но и она имела существенное противоречие: по известным тогда законам физики электрон, если он вращается вокруг ядра, должен непрерывно излучать энергию и со временем упасть на ядро. Модель атома Резерфорда усовершенствовал датский физик Нильс Бор. Он утверждал, что электроны могут вращаться не на любой орбите, а только на определенных расстояниях от ядра, образуя концентрические сферы из электронов. Поэтому иногда планетарную модель атома называют моделью Бора-Резерфорда.
Модель атома Резерфорда усовершенствовал датский физик Нильс Бор. Он утверждал, что электроны могут вращаться не на любой орбите, а только на определенных расстояниях от ядра, образуя концентрические сферы из электронов. Поэтому иногда планетарную модель атома называют моделью Бора-Резерфорда.
Состав атомов
Итак, атомы состоят из положительно заряженного ядра и отрицательно заряженных электронов.
Заряд электрона называют элементарным, так как он наименьший из всех известных зарядов и потому его абсолютную величину принимают за условную единицу измерения. Именно в этих условных единицах обычно указывают заряды всех частиц: электронов, протонов, ядер, ионов и т. д. Заряд самого электрона принимают за -1.
Электрон — самая легкая из известных элементарных частиц. Его масса составляет 9,1 • 10-28 г, это в 1837 раз меньше массы самого легкого из атомов — атома Гидрогена. Часто в расчетах массой электрона пренебрегают (считают равной нулю).
Таблица 5. Частицы, из которых состоит атом
После открытия сложного строения атома выяснили, что ядро атома также имеет сложное строение. Оно состоит из частиц двух видов — протонов и нейтронов (рис. 9.5). Протоны и нейтроны называют нуклонами. Протоны являются положительно заряженными частицами с зарядом +1, а нейтроны не имеют заряда (табл. 5). Это означает, что весь положительный заряд ядра образован только протонами — их число равно заряду ядра:
Любой атом является электронейтральным, следовательно, число протонов с зарядом +1 всегда равно числу электронов с зарядом -1:
Ядро — самая тяжелая часть атома: его масса составляет около 99,97 % от массы атома и определяется числом протонов и нейтронов в ядре. Массы протона и нейтрона почти одинаковы и приблизительно равны 1 а. е. м. Таким образом,
Пример. Ядро атома содержит 5 протонов и 5 нейтронов.
1. Определим заряд ядра и число электронов в атоме:
Число протонов в ядре = 5 —> Заряд ядра = +5 —> Число электронов = 5
2. Определим атомную массу:
Определим атомную массу:
И хотя именно в ядре сосредоточена вся масса атома, тем не менее размеры ядра чрезвычайно малы: его радиус приблизительно в сто тысяч раз меньше радиуса атома (рис. 9.5). Представьте, если размер ядра увеличить до размера яблока, то сам атом будет размером с земной шар.
Рис. 9.5. Ядро атома состоит из положительно заряженных протонов и нейтральных нейтронов. Вокруг ядра вращаются электроны, образуя электронную оболочку атома
Порядковый номер химического элемента
У всех атомов одного химического элемента число протонов всегда одинаковое (и равно заряду ядра), а число нейтронов может быть разным, поэтому масса атомов одного элемента также может отличаться. Это означает, что не масса, а именно заряд ядра является основной характеристикой, отличающей атомы одного вида от атомов другого вида. Именно поэтому в начале XX в. изменилось определение понятия химического элемента:
Химический элемент — это разновидность атомов с одинаковым зарядом ядра.
После открытия сложного строения атома была изменена и формулировка Периодического закона:
Свойства химических элементов, а также образованных ими веществ находятся в периодической зависимости от зарядов их атомных ядер.
Дальнейшее изучение строения атома показало, что протонов в атомах содержится не произвольное число, а равное порядковому номеру химического элемента в Периодической системе химических элементов Д. И. Менделеева. Следовательно, и заряд ядра также равен порядковому номеру:
Оказалось, что, даже не догадываясь о сложном строении атомов, Менделеев при составлении своей Периодической системы расположил элементы в порядке возрастания зарядов их атомных ядер.
• Физики уверены, что протоны, нейтроны и другие частицы состоят из кварков — подлинно элементарных частиц. Однако ученым никак не удается выделить кварки и таким образом подтвердить их существование. Но электрон до сих пор считается элементарной частицей.
• Эрнест Резерфорд проводил исследования в основном в области физики и однажды заявил, что все науки можно разделить на две группы — на физику и коллекционирование марок. Однако Нобелевскую премию Резерфорд получил именно по химии. Позднее он отметил, что из всех превращений, которые ему удалось наблюдать, самым быстрым оказалось его собственное превращение из физика в химика.
Выводы
1. Общепринятой является планетарная модель строения атомов, согласно которой атом состоит из положительно заряженного ядра, вокруг которого на определенном расстоянии вращаются отрицательно заряженные электроны, образуя электронную оболочку атома.
2. Ядро атома состоит из нуклонов: положительно заряженных протонов и нейтральных нейтронов. Число протонов в ядре определенного атома равно порядковому номеру химического элемента в Периодической системе. Поскольку атом электронейтрален, то число протонов в ядре атома равно числу электронов в его электронной оболочке.
Контрольные вопросы
1. Охарактеризуйте планетарную модель атома Резерфорда.
2. Какие частицы входят в состав: а) атома; б) атомного ядра? Каковы их заряд и масса?
3. Ядро атома: а) имеет отрицательный заряд; б) имеет положительный заряд; в) не имеет заряда.
4. Какие характеристики атома вам известны?
5. Как определить число протонов в ядре атома: а) по порядковому номеру элемента в Периодической системе; б) по номеру периода; в) по номеру группы?
6. Дайте определение понятиям «атом» и «химический элемент».
7. Приведите современную формулировку Периодического закона. Чем она отличается от той, которую вы изучали ранее?
Задания для усвоения материала
1. Ядро атома Гелия имеет заряд +2. Сколько электронов в атоме Гелия?
2. Атом Карбона содержит 6 электронов. Чему равен заряд; а) атома Карбона; б) ядра атома Карбона?
3. Определите число протонов в ядрах и заряды атомов; а) Лития; б) Сульфура; в) Феррума; г) Плюмбума.
4. Определите заряд ядра, число электронов и массу атома, если ядро содержит: а) 8 протонов и 9 нейтронов; б) 25 протонов и 30 нейтронов; в) 89 протонов и 117 нейтронов. Назовите соответствующие химические элементы.
5*. Опишите суть эксперимента Резерфорда по установлению строения атома. Какие результаты опыта позволили ему сделать выводы о планетарном строении атома?
Попередня
СторінкаНаступна
СторінкаЗміст
Строение атома. Модели Резерфорда и Бора реферат по естествознанию | Сочинения Нейропсихология
Скачай Строение атома. Модели Резерфорда и Бора реферат по естествознанию и еще Сочинения в формате PDF Нейропсихология только на Docsity! Введение. Мысль о том, что вещество построено из мельчайших частиц, высказывалась еще древнегреческими учеными. Они-то и назвали эти частицы атомами (от греческого слова, означающего «неделимый»). Древние греки предполагали, что атомы имеют форму правильных многогранников: куба («атомы земли»), тетраэдра («атомы огня»), октаэдра («атомы воздуха»), икосаэдра («атомы воды»). Поэтому и состоящий из них мир неисчерпаемо богат в своих свойствах и качествах. Цепляясь друг за друга крючками и крючочками, атомы образуют твердые тела. Атомы воды гладкие и скользкие, поэтому она растекается и не имеет формы. Атомы вязких веществ обладают заусеницами. Воздух – это пустота, в которой носятся отдельные редкие атомы. Атомы огня острые и колючие, поэтому огонь жжется. Прошло почти более двадцати столетий, прежде чем были получены экспериментальные подтверждения идеи атомистического строения вещества. Представления о строении атома до Резерфорда. Развитие исследований радиоактивности излучения, с одной стороны, и квантовой теории – с другой, привели к созданию квантовой модели атома Резерфорда-Бора. Но созданию этой теории предшествовали попытки построить модель атома на основе представлений классической электродинамики и механики. В 1904 году появились публикации о строении атома, принадлежащие одна японскому физику Хантаро Нагаока (1865-1950), другая английскому физику Дж.
Поэтому и состоящий из них мир неисчерпаемо богат в своих свойствах и качествах. Цепляясь друг за друга крючками и крючочками, атомы образуют твердые тела. Атомы воды гладкие и скользкие, поэтому она растекается и не имеет формы. Атомы вязких веществ обладают заусеницами. Воздух – это пустота, в которой носятся отдельные редкие атомы. Атомы огня острые и колючие, поэтому огонь жжется. Прошло почти более двадцати столетий, прежде чем были получены экспериментальные подтверждения идеи атомистического строения вещества. Представления о строении атома до Резерфорда. Развитие исследований радиоактивности излучения, с одной стороны, и квантовой теории – с другой, привели к созданию квантовой модели атома Резерфорда-Бора. Но созданию этой теории предшествовали попытки построить модель атома на основе представлений классической электродинамики и механики. В 1904 году появились публикации о строении атома, принадлежащие одна японскому физику Хантаро Нагаока (1865-1950), другая английскому физику Дж. Дж. Томсону. Нагаока исходил из исследований Максвелла об устойчивости колец Сатурна и представил строение атома аналогичным строению солнечной системы: роль Солнца играет положительно заряженная часть атома, вокруг которой по установленным орбитам движутся «планеты» – электроны. При незначительных смещениях электроны возбуждают электромагнитные волны, периоды которых, по расчетам Нагаоки, того же порядка, что и частоты спектральных линий некоторых элементов. «Система состоит из большого числа частиц одинаковой массы, расположенных по кругу через равные угловые интервалы и взаимоотталкивающиеся с силой, обратно пропорциональной квадрату расстояния между ними; в центре круга помещается большая частица, которая притягивает другие частицы, образующие кольцо, по тому же закону». (Нагаока) В атоме Томсона положительное электричество «размазано» по сфере, в которую вкраплены, как изюм в пудинг, электроны. В простейшем атоме водорода электрон находится в центре положительно заряженной сферы. При смещении из центра на электрон действует квазиупругая сила электростатического напряжения, под действием которой электрон совершает колебания.
Дж. Томсону. Нагаока исходил из исследований Максвелла об устойчивости колец Сатурна и представил строение атома аналогичным строению солнечной системы: роль Солнца играет положительно заряженная часть атома, вокруг которой по установленным орбитам движутся «планеты» – электроны. При незначительных смещениях электроны возбуждают электромагнитные волны, периоды которых, по расчетам Нагаоки, того же порядка, что и частоты спектральных линий некоторых элементов. «Система состоит из большого числа частиц одинаковой массы, расположенных по кругу через равные угловые интервалы и взаимоотталкивающиеся с силой, обратно пропорциональной квадрату расстояния между ними; в центре круга помещается большая частица, которая притягивает другие частицы, образующие кольцо, по тому же закону». (Нагаока) В атоме Томсона положительное электричество «размазано» по сфере, в которую вкраплены, как изюм в пудинг, электроны. В простейшем атоме водорода электрон находится в центре положительно заряженной сферы. При смещении из центра на электрон действует квазиупругая сила электростатического напряжения, под действием которой электрон совершает колебания. Частота этих колебаний определяется радиусом сферы, зарядом и массой электрона, и если радиус сферы имеет порядок радиуса атома, частота этих колебаний совпадает с частотой колебания спектральной линии атома. В многоэлектронных атомах электроны располагаются по устойчивым конфигурациям, рассчитанным Томсоном. Томсон считал каждую такую конфигурацию Резерфорд, продолжая свою работу над магнитным детектором, вместе с тем заинтересовался исследованиями Томсона по электропроводимости газов. В 1896 году появляется совместная работа Томсона и Резерфорда «О прохождении электричества через газы, подвергнутые действию лучей Рентгена». В 1897 году выходит в свет заключительная статья Резерфорда «Магнитный детектор электрических волн и некоторые его применения». После этого он полностью сосредоточивает свои силы на исследовании нового разряда. В том же, 1897 году появляется его новая работа «Об электризации газов, подверженных действию рентгеновских лучей, и о поглощении рентгеновского излучения газами и парами».
Частота этих колебаний определяется радиусом сферы, зарядом и массой электрона, и если радиус сферы имеет порядок радиуса атома, частота этих колебаний совпадает с частотой колебания спектральной линии атома. В многоэлектронных атомах электроны располагаются по устойчивым конфигурациям, рассчитанным Томсоном. Томсон считал каждую такую конфигурацию Резерфорд, продолжая свою работу над магнитным детектором, вместе с тем заинтересовался исследованиями Томсона по электропроводимости газов. В 1896 году появляется совместная работа Томсона и Резерфорда «О прохождении электричества через газы, подвергнутые действию лучей Рентгена». В 1897 году выходит в свет заключительная статья Резерфорда «Магнитный детектор электрических волн и некоторые его применения». После этого он полностью сосредоточивает свои силы на исследовании нового разряда. В том же, 1897 году появляется его новая работа «Об электризации газов, подверженных действию рентгеновских лучей, и о поглощении рентгеновского излучения газами и парами». Вероятно, Резерфорд и Томсон вообще были одними из первых ученых, проявивших интерес к рентгеновским лучам и считавших открытие Рентгена исключительно важным и многообещающим. В воскресенье 1 марта 1896 года Анри Беккерель обнаружил, что уран непрерывно испускает проникающее излучение неизвестной природы, которая оказалась совершенно отличной от природы рентгеновских лучей. Тем самым он обнаружил существование радиоактивности, начавшее новую эпоху в истории науки и человечества. Сообщение об открытии Беккерелем радиоактивности произвело большой эффект в Кавендишской лаборатории, и Резерфорд решил немедленно заняться изучением этих загадочных лучей. Сначала ему казалось, что существует какая-то связь между урановыми и рентгеновскими лучами. Излучение урановых препаратов, как и рентгеновские лучи, производило ионизацию воздуха. Такое сходство в воздействии излучений на окружающую среду привело Резерфорда к мысли об опытном сравнении рентгеновских и беккерелевых лучей, что могло дать наиболее достоверные и точные сведения об их физических свойствах.
Вероятно, Резерфорд и Томсон вообще были одними из первых ученых, проявивших интерес к рентгеновским лучам и считавших открытие Рентгена исключительно важным и многообещающим. В воскресенье 1 марта 1896 года Анри Беккерель обнаружил, что уран непрерывно испускает проникающее излучение неизвестной природы, которая оказалась совершенно отличной от природы рентгеновских лучей. Тем самым он обнаружил существование радиоактивности, начавшее новую эпоху в истории науки и человечества. Сообщение об открытии Беккерелем радиоактивности произвело большой эффект в Кавендишской лаборатории, и Резерфорд решил немедленно заняться изучением этих загадочных лучей. Сначала ему казалось, что существует какая-то связь между урановыми и рентгеновскими лучами. Излучение урановых препаратов, как и рентгеновские лучи, производило ионизацию воздуха. Такое сходство в воздействии излучений на окружающую среду привело Резерфорда к мысли об опытном сравнении рентгеновских и беккерелевых лучей, что могло дать наиболее достоверные и точные сведения об их физических свойствах. Результатом этого явилась большая статья «Излучение урана и созданная им электропроводность». Опыты продолжались почти год. Они показали, что сходства между двумя исследовавшимися излучениями, несмотря на их одинаковое ионизирующее действие, нет. Резерфорд также смог убедиться также в том, что предположение Беккереля о сходстве урановых лучей со световыми ошибочно. Излучение урана вопреки заявлению Беккереля (правда, не подкрепленному опытами) не обнаружило свойств, характерных для света. Оно не подчинялось законам световой оптики: отражению, преломлению и поляризации. В результате этих работ Резерфорда были открыты F 06 1- частицы. Резерфорд поместил радиоактивный источник в магнитное поле и получил три вида излучений, испускаемых ураном: F 06 1-, F 06 2-частицы и F 06 7-лучи. Уже при проведении этих опытов Резерфорд предвидел, что F 06 1-частицы помогут исследовать структуру атома в качестве мощных инструментов для проникновения в атом. В сентябре 1898 года Резерфорд был приглашен в университет Мак-Гила в Монреале (Канада) в качестве профессора кафедры теоретической физики.
Результатом этого явилась большая статья «Излучение урана и созданная им электропроводность». Опыты продолжались почти год. Они показали, что сходства между двумя исследовавшимися излучениями, несмотря на их одинаковое ионизирующее действие, нет. Резерфорд также смог убедиться также в том, что предположение Беккереля о сходстве урановых лучей со световыми ошибочно. Излучение урана вопреки заявлению Беккереля (правда, не подкрепленному опытами) не обнаружило свойств, характерных для света. Оно не подчинялось законам световой оптики: отражению, преломлению и поляризации. В результате этих работ Резерфорда были открыты F 06 1- частицы. Резерфорд поместил радиоактивный источник в магнитное поле и получил три вида излучений, испускаемых ураном: F 06 1-, F 06 2-частицы и F 06 7-лучи. Уже при проведении этих опытов Резерфорд предвидел, что F 06 1-частицы помогут исследовать структуру атома в качестве мощных инструментов для проникновения в атом. В сентябре 1898 года Резерфорд был приглашен в университет Мак-Гила в Монреале (Канада) в качестве профессора кафедры теоретической физики. В Монреале он пробыл до 1907 года. Здесь он сделал фундаментальные открытия: им была открыта эманация теория и разгадана природа так называемой «индуцированной радиоактивности»; совместно с Содди он открыл радиоактивный распад и его закон. Здесь им была написана книга «Радиоактивность». В Монреале он начал тщательные исследования природы F 06 1- частиц, закончившееся уже в Манчестере полной разгадкой их природы. Здесь же он начал свои исследования по происхождению F 06 1-частиц через вещество. Огромный размах научной работы Резерфорда в Монреале принес ему славу первоклассного исследователя. Им было опубликовано как лично, так и совместно с другими учеными 66 статей, не считая книги «Радиоактивность». Он получает приглашение занять кафедру в Манчестере. 24 мая 1907 года Резерфорд вернулся в Европу. Начался новый период в его жизни. Почти немедленно по прибытии в Манчестер Резерфорд начал систематические исследования рассеяния F 06 1-частиц веществом. Он установил, что каждая F 06 1-частица, попадая на экран из сернистого цинка, создает вспышку света.
В Монреале он пробыл до 1907 года. Здесь он сделал фундаментальные открытия: им была открыта эманация теория и разгадана природа так называемой «индуцированной радиоактивности»; совместно с Содди он открыл радиоактивный распад и его закон. Здесь им была написана книга «Радиоактивность». В Монреале он начал тщательные исследования природы F 06 1- частиц, закончившееся уже в Манчестере полной разгадкой их природы. Здесь же он начал свои исследования по происхождению F 06 1-частиц через вещество. Огромный размах научной работы Резерфорда в Монреале принес ему славу первоклассного исследователя. Им было опубликовано как лично, так и совместно с другими учеными 66 статей, не считая книги «Радиоактивность». Он получает приглашение занять кафедру в Манчестере. 24 мая 1907 года Резерфорд вернулся в Европу. Начался новый период в его жизни. Почти немедленно по прибытии в Манчестер Резерфорд начал систематические исследования рассеяния F 06 1-частиц веществом. Он установил, что каждая F 06 1-частица, попадая на экран из сернистого цинка, создает вспышку света. Поэтому для исследования рассеяния F 06 1-частиц был сконструирован прибор, изображенный схематически на рис.1 (стр. 18). С помощью свинцового коллиматора выделялся узкий конус F 06 1- частиц из радиоактивного источника. Испытав рассеивание в золотой фольге, F 06 1-частицы ударялись затем в экран из сернистого цинка и регистрировались с помощью небольшого микроскопа, в который можно было наблюдать вспышки света. Вращая детектор, можно было изменять относительное число F 0 6 1-частиц, рассеянных под различными углами F 07 1. Прибор помещался внутри откачанной камеры с целью устранить косеканса» был проверен экспериментально Гейгером, и был найден справедливым в пределах экспериментальных ошибок. Важным следствием теории Резерфорда было указание на заряд атомного центра, который Резерфорд положил равным F 0 B 1Ne. Заряд оказался пропорциональным атомному весу. «Точное значение заряда центрального ядра не было определено,–писал Резерфорд,–но для атома золота оно приблизительно равно 100 единицам заряда».
Поэтому для исследования рассеяния F 06 1-частиц был сконструирован прибор, изображенный схематически на рис.1 (стр. 18). С помощью свинцового коллиматора выделялся узкий конус F 06 1- частиц из радиоактивного источника. Испытав рассеивание в золотой фольге, F 06 1-частицы ударялись затем в экран из сернистого цинка и регистрировались с помощью небольшого микроскопа, в который можно было наблюдать вспышки света. Вращая детектор, можно было изменять относительное число F 0 6 1-частиц, рассеянных под различными углами F 07 1. Прибор помещался внутри откачанной камеры с целью устранить косеканса» был проверен экспериментально Гейгером, и был найден справедливым в пределах экспериментальных ошибок. Важным следствием теории Резерфорда было указание на заряд атомного центра, который Резерфорд положил равным F 0 B 1Ne. Заряд оказался пропорциональным атомному весу. «Точное значение заряда центрального ядра не было определено,–писал Резерфорд,–но для атома золота оно приблизительно равно 100 единицам заряда». В 1913 году Гейгер и Марсден предприняли новую экспериментальную проверку формулы Резерфорда, подсчитывая рассеивание частиц по производимым ими сцинтиляционным вспышкам. «Это была трудная, кропотливая работа, – характеризовал Резерфорд работу своих сотрудников, – так как нужно было считать много тысяч частиц. Результаты Гейгера и Марсдена весьма близко согласуются с теорией». Из этих утомительных и кропотливых исследований и возникло представление о ядре как устойчивой части атома, несущей в себе почти всю массу атома и обладающей положительным (Резерфорд еще в 1913 году считал знак заряда неопределенным) зарядом. При этом число элементарных зарядов оказалось пропорциональным атомному весу. Тем не менее классические модели строения атома страдали весьма глубокими недостатками. С их помощью никак не удавалось объяснить спектральные закономерности и устойчивость движения электронов внутри атома. Рано или поздно электроны в модели Резерфорда должны были прекратить движение, что прекращало существование атома.
В 1913 году Гейгер и Марсден предприняли новую экспериментальную проверку формулы Резерфорда, подсчитывая рассеивание частиц по производимым ими сцинтиляционным вспышкам. «Это была трудная, кропотливая работа, – характеризовал Резерфорд работу своих сотрудников, – так как нужно было считать много тысяч частиц. Результаты Гейгера и Марсдена весьма близко согласуются с теорией». Из этих утомительных и кропотливых исследований и возникло представление о ядре как устойчивой части атома, несущей в себе почти всю массу атома и обладающей положительным (Резерфорд еще в 1913 году считал знак заряда неопределенным) зарядом. При этом число элементарных зарядов оказалось пропорциональным атомному весу. Тем не менее классические модели строения атома страдали весьма глубокими недостатками. С их помощью никак не удавалось объяснить спектральные закономерности и устойчивость движения электронов внутри атома. Рано или поздно электроны в модели Резерфорда должны были прекратить движение, что прекращало существование атома. В действительности же атомы существовали, не обращая внимания на мрачные пророчества теории. Налицо было вопиющее противоречие между теорией и действительностью, причем противоречие на уровне самой исходной, самой бедной по содержанию – категорией существования. Спектральные закономерности еще можно было как-то надеяться вывести, представляя очень хитрым образом движение электронов вокруг ядра. Здесь же теория подрубалась под корень. Атом Бора. Идеи о непримиримости законов классической механики и электродинамики во всей их полноте к исследованию внутреннего строения атома высказывались и до Бора. Мысли о необходимости учета квантового характера излучения были также не новыми. Тем не менее именно Нильс Бор заслуженно считается пионером квантовой теории атома. Имена его предшественников на этом пути – Никольсона, Штарка, Бьеррума и других, на которых Бор не устает ссылаться в своих первых статьях, сейчас мало кому известны. Это можно объяснить тем, что упомянутые авторы достигали только частных результатов, не объединенных в сколько-нибудь стройную систему, которая могла бы служить программой целого круга исследований и допускала бы количественную проверку на опыте.
В действительности же атомы существовали, не обращая внимания на мрачные пророчества теории. Налицо было вопиющее противоречие между теорией и действительностью, причем противоречие на уровне самой исходной, самой бедной по содержанию – категорией существования. Спектральные закономерности еще можно было как-то надеяться вывести, представляя очень хитрым образом движение электронов вокруг ядра. Здесь же теория подрубалась под корень. Атом Бора. Идеи о непримиримости законов классической механики и электродинамики во всей их полноте к исследованию внутреннего строения атома высказывались и до Бора. Мысли о необходимости учета квантового характера излучения были также не новыми. Тем не менее именно Нильс Бор заслуженно считается пионером квантовой теории атома. Имена его предшественников на этом пути – Никольсона, Штарка, Бьеррума и других, на которых Бор не устает ссылаться в своих первых статьях, сейчас мало кому известны. Это можно объяснить тем, что упомянутые авторы достигали только частных результатов, не объединенных в сколько-нибудь стройную систему, которая могла бы служить программой целого круга исследований и допускала бы количественную проверку на опыте. Нильс Бор родился 7 октября 1885 года в семье профессора физиологии Копенгагенского университета Христиана Бора. В 1903 году Бор поступил в Копенгагенский университет. Еще в студенческие годы Бор выполнил конкурсную работу по поверхностному натяжению. Работа была удостоена золотой медали Датской Академии наук. В 1909 году, спустя два года после окончания Бором университета, эта работа – «Определение поверхностного натяжения воды методом колебания струи» – была опубликована в трудах Лондонского Королевского общества. Весной 1911 года состоялась защита докторской диссертации Бора на тему «Анализ электронной теории металла», в сентябре того же года Бор приехал на стажировку в Кембридж к Дж.Дж. Томсону. Томсон в это время занимался анализом положительных лучей. Им был разработан метод точного анализа – метод парабол, с помощью которого он впервые обнаружил у неона существование двух разновидностей атомов: с атомным весом 20 и 22. Продолжая эти исследования уже после войны, ученик Томсона Астон открыл изотопы многих стабильных элементов.
Нильс Бор родился 7 октября 1885 года в семье профессора физиологии Копенгагенского университета Христиана Бора. В 1903 году Бор поступил в Копенгагенский университет. Еще в студенческие годы Бор выполнил конкурсную работу по поверхностному натяжению. Работа была удостоена золотой медали Датской Академии наук. В 1909 году, спустя два года после окончания Бором университета, эта работа – «Определение поверхностного натяжения воды методом колебания струи» – была опубликована в трудах Лондонского Королевского общества. Весной 1911 года состоялась защита докторской диссертации Бора на тему «Анализ электронной теории металла», в сентябре того же года Бор приехал на стажировку в Кембридж к Дж.Дж. Томсону. Томсон в это время занимался анализом положительных лучей. Им был разработан метод точного анализа – метод парабол, с помощью которого он впервые обнаружил у неона существование двух разновидностей атомов: с атомным весом 20 и 22. Продолжая эти исследования уже после войны, ученик Томсона Астон открыл изотопы многих стабильных элементов. Исследования самого Томсона были обобщены им в монографии «Лучи положительного электричества и их применение к химическому анализу», вышедшей в 1913 году. Томсон поручил и Бору провести эксперимент с положительными лучами. Бор собрал вакуумную установку, однако дело дальше не пошло, и он начал готовить к изданию свою докторскую диссертацию. Томсон отнесся без внимания к работе Бора и не прочитал ее. В том же, 1911 году, когда Бор приехал в Кембридж, сотрудник Томсона Чарльз Томас Рис Вильсон (1869-1959) изобрел замечательный прибор, известный ныне под названием «камера Вильсона». Этот прибор позволяет видеть частицу по оставляемому ею туманному следу. Резерфорд, приехавший на традиционный ежегодный обед в Кембридж, в своей речи с энтузиазмом отозвался о приборе Вильсона и полученных первых результатах. Бор, который впервые увидел Кроме того, с моделью Резерфорда было не совместимо допущение о квазиупругом характере сил связи электрона с ядром, поскольку все силы взаимодействия между частями атома изменялись согласно закону Кулона обратно пропорционально квадрату расстояния.
Исследования самого Томсона были обобщены им в монографии «Лучи положительного электричества и их применение к химическому анализу», вышедшей в 1913 году. Томсон поручил и Бору провести эксперимент с положительными лучами. Бор собрал вакуумную установку, однако дело дальше не пошло, и он начал готовить к изданию свою докторскую диссертацию. Томсон отнесся без внимания к работе Бора и не прочитал ее. В том же, 1911 году, когда Бор приехал в Кембридж, сотрудник Томсона Чарльз Томас Рис Вильсон (1869-1959) изобрел замечательный прибор, известный ныне под названием «камера Вильсона». Этот прибор позволяет видеть частицу по оставляемому ею туманному следу. Резерфорд, приехавший на традиционный ежегодный обед в Кембридж, в своей речи с энтузиазмом отозвался о приборе Вильсона и полученных первых результатах. Бор, который впервые увидел Кроме того, с моделью Резерфорда было не совместимо допущение о квазиупругом характере сил связи электрона с ядром, поскольку все силы взаимодействия между частями атома изменялись согласно закону Кулона обратно пропорционально квадрату расстояния.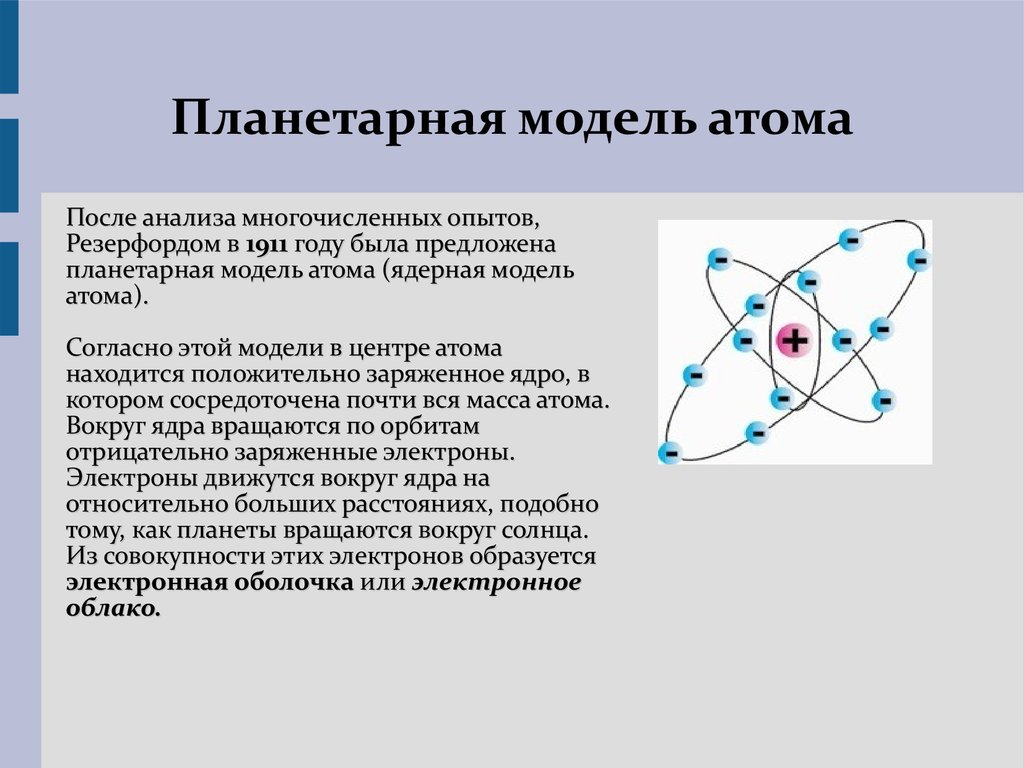 Модель Томсона, в которой электрон находился внутри положительно заряженного «ядра», допускала существование таких сил. Тем не менее, несмотря на все эти соображения, эксперимент убедительно говорил в пользу Резерфорда. Если бы физика целиком осталась на классических позициях, то ей вряд ли удалось бы достигнуть разрешения противоречий между опытом и «очевидными» физическими соображениями. Поэтому Нильс Бор утверждает: «Каким бы ни было изменение законов движения электронов, представляется необходимым ввести в эти законы величину, чуждую классической электродинамике, то есть постоянную Планка, или, как ее часто называют, элементарный квант действия. Благодаря введению этой величины вопрос об устойчивых конфигурациях электронов в атоме существенным образом изменяется, так как эта постоянная обладает такой размерностью и значением, что может в комбинации с зарядом и массой частиц определить длину требуемого порядка величины». Постоянная Планка символизировала в теории элементарное количество действия, которое было сложным по структуре выражением, что видно уже из ее размерности.
Модель Томсона, в которой электрон находился внутри положительно заряженного «ядра», допускала существование таких сил. Тем не менее, несмотря на все эти соображения, эксперимент убедительно говорил в пользу Резерфорда. Если бы физика целиком осталась на классических позициях, то ей вряд ли удалось бы достигнуть разрешения противоречий между опытом и «очевидными» физическими соображениями. Поэтому Нильс Бор утверждает: «Каким бы ни было изменение законов движения электронов, представляется необходимым ввести в эти законы величину, чуждую классической электродинамике, то есть постоянную Планка, или, как ее часто называют, элементарный квант действия. Благодаря введению этой величины вопрос об устойчивых конфигурациях электронов в атоме существенным образом изменяется, так как эта постоянная обладает такой размерностью и значением, что может в комбинации с зарядом и массой частиц определить длину требуемого порядка величины». Постоянная Планка символизировала в теории элементарное количество действия, которое было сложным по структуре выражением, что видно уже из ее размерности. Элементарность действия имеет поэтому другой статус (чисто количественный) по сравнению с элементарностью свойств и отношений, которая носила преимущественно качественный характер. Действие (а вместе с ним и совпадающий с действием по размерности момент количества движения), если встать на точку зрения теории Планка, могло принимать только значения, кратные h. Это означало, что из непрерывного множества всех возможных с точки зрения классики орбит электронов – а были возможны орбиты любого радиуса – отбиралось дискретное множество орбит. Нильс Бор назвал их стационарными орбитами, соответствовавшими стационарным состояниям атома. Все возражения против модели Резерфорда, по словам Бора, можно устранить, если допустить, «(1) что динамическое равновесие систем в стационарных состояниях может обсуждаться с помощью обычной механики, в то время как переход систем между различными стационарными состояниями не может трактоваться на этой основе; (2) что последний процесс сопровождается испусканием гомогенного излучения, для которого соотношение между частотой и количеством испущенной энергии дается теорией Планка».
Элементарность действия имеет поэтому другой статус (чисто количественный) по сравнению с элементарностью свойств и отношений, которая носила преимущественно качественный характер. Действие (а вместе с ним и совпадающий с действием по размерности момент количества движения), если встать на точку зрения теории Планка, могло принимать только значения, кратные h. Это означало, что из непрерывного множества всех возможных с точки зрения классики орбит электронов – а были возможны орбиты любого радиуса – отбиралось дискретное множество орбит. Нильс Бор назвал их стационарными орбитами, соответствовавшими стационарным состояниям атома. Все возражения против модели Резерфорда, по словам Бора, можно устранить, если допустить, «(1) что динамическое равновесие систем в стационарных состояниях может обсуждаться с помощью обычной механики, в то время как переход систем между различными стационарными состояниями не может трактоваться на этой основе; (2) что последний процесс сопровождается испусканием гомогенного излучения, для которого соотношение между частотой и количеством испущенной энергии дается теорией Планка». Это и есть знаменитые постулаты Бора, вокруг которых вплоть до 1925 года концентрировалось развитие теоретической атомной физики. Итак, в модели Бора существовало строго определенное множество дозволенных орбит, выделенных квантовыми условиями. При этом каждая стационарная орбита была устойчивой по определению, и каждой стационарной орбите соответствовало определенное состояние атома. Вообще говоря, в любом стационарном состоянии атом мог находиться неограниченно долго, что ликвидировало единственность устойчивого состояния атома «самого по себе». Среди бесконечного множества стационарных состояний только одно – основное состояние – было абсолютно устойчивым в рамках модели. Для нахождения атома в других состояниях, устойчивых лишь относительно, существовала некоторая вероятность спонтанного перехода атома в другое, менее возбужденное состояние. Возможность таких спонтанных переходов была посторонней – в сторону уменьшения энергии состояния, уменьшения степени возбуждения атома. Спонтанно увеличивать свою энергию атом не мог.
Это и есть знаменитые постулаты Бора, вокруг которых вплоть до 1925 года концентрировалось развитие теоретической атомной физики. Итак, в модели Бора существовало строго определенное множество дозволенных орбит, выделенных квантовыми условиями. При этом каждая стационарная орбита была устойчивой по определению, и каждой стационарной орбите соответствовало определенное состояние атома. Вообще говоря, в любом стационарном состоянии атом мог находиться неограниченно долго, что ликвидировало единственность устойчивого состояния атома «самого по себе». Среди бесконечного множества стационарных состояний только одно – основное состояние – было абсолютно устойчивым в рамках модели. Для нахождения атома в других состояниях, устойчивых лишь относительно, существовала некоторая вероятность спонтанного перехода атома в другое, менее возбужденное состояние. Возможность таких спонтанных переходов была посторонней – в сторону уменьшения энергии состояния, уменьшения степени возбуждения атома. Спонтанно увеличивать свою энергию атом не мог. Это делало его гораздо менее «забывчивым». Одно только основное состояние «не помнило» о прошлом поведении атома. Для других же стационарных состояний сам факт их существования напоминал о прошлом поведении атома, который мог начать существовать в этом состоянии, только либо увеличив свою энергию под влиянием внешнего воздействия, либо уменьшить энергию в результате перехода из более возбужденного состояния – спонтанного или вынужденного. Находясь в любом состоянии, кроме основного, атом сохраняет в «снятом виде» отпечаток прошлого своего поведения. Опираясь на свои допущения, Бор выводит далее новые закономерности для спектра водорода, принимавшиеся ранее просто как эмпирический факт: формулу Бальмера и закон Ридберга-Ритца. Очень скоро известные опыты Франка и Герца, по словам одного из авторов, «так убедительно доказали представления Бора о стационарных состояниях атома и о появлении излучения при переходе из одного состояния в другое с определением частоты из уравнения h F 06 E=E1-E2 (где h– понимание квантовой теории».
Это делало его гораздо менее «забывчивым». Одно только основное состояние «не помнило» о прошлом поведении атома. Для других же стационарных состояний сам факт их существования напоминал о прошлом поведении атома, который мог начать существовать в этом состоянии, только либо увеличив свою энергию под влиянием внешнего воздействия, либо уменьшить энергию в результате перехода из более возбужденного состояния – спонтанного или вынужденного. Находясь в любом состоянии, кроме основного, атом сохраняет в «снятом виде» отпечаток прошлого своего поведения. Опираясь на свои допущения, Бор выводит далее новые закономерности для спектра водорода, принимавшиеся ранее просто как эмпирический факт: формулу Бальмера и закон Ридберга-Ритца. Очень скоро известные опыты Франка и Герца, по словам одного из авторов, «так убедительно доказали представления Бора о стационарных состояниях атома и о появлении излучения при переходе из одного состояния в другое с определением частоты из уравнения h F 06 E=E1-E2 (где h– понимание квантовой теории». Теория атома после открытия Зоммерфельда стала называться теорией Бора–Зоммерфельда. По возвращении в Копенгаген Бор обнаружил пакет со статьей Эренфеста, содержащей теорию адиабатических вариантов. Эта теория давала критерий квантующихся величин и до создания квантовой механики была единственной руководящей нитью при применении правил квантования, предвосхищавшей многие выводы, следующие из статьи Бора. К 1916 году теория Бора начала разрабатываться многими физиками. Была создана квантовая теория эффекта Зеемана и открытого в 1913 году Штарком (1874-1957) эффекта влияния электрического поля на спектры. «Область нашей работы, – писал Бор Резерфорду, – после получения статьи Эренфеста превратилась из страны с довольно малочисленным населением в донельзя перенаселенное государство». Продолжая развивать свои идеи, Бор сформулировал принцип соответствия (1918), означавший шаг вперед в ответе на вопросы, поставленные Резерфордом. Чрезвычайно существенно, что благодаря Бору Копенгаген превратился в центр теоретической физики.
Теория атома после открытия Зоммерфельда стала называться теорией Бора–Зоммерфельда. По возвращении в Копенгаген Бор обнаружил пакет со статьей Эренфеста, содержащей теорию адиабатических вариантов. Эта теория давала критерий квантующихся величин и до создания квантовой механики была единственной руководящей нитью при применении правил квантования, предвосхищавшей многие выводы, следующие из статьи Бора. К 1916 году теория Бора начала разрабатываться многими физиками. Была создана квантовая теория эффекта Зеемана и открытого в 1913 году Штарком (1874-1957) эффекта влияния электрического поля на спектры. «Область нашей работы, – писал Бор Резерфорду, – после получения статьи Эренфеста превратилась из страны с довольно малочисленным населением в донельзя перенаселенное государство». Продолжая развивать свои идеи, Бор сформулировал принцип соответствия (1918), означавший шаг вперед в ответе на вопросы, поставленные Резерфордом. Чрезвычайно существенно, что благодаря Бору Копенгаген превратился в центр теоретической физики.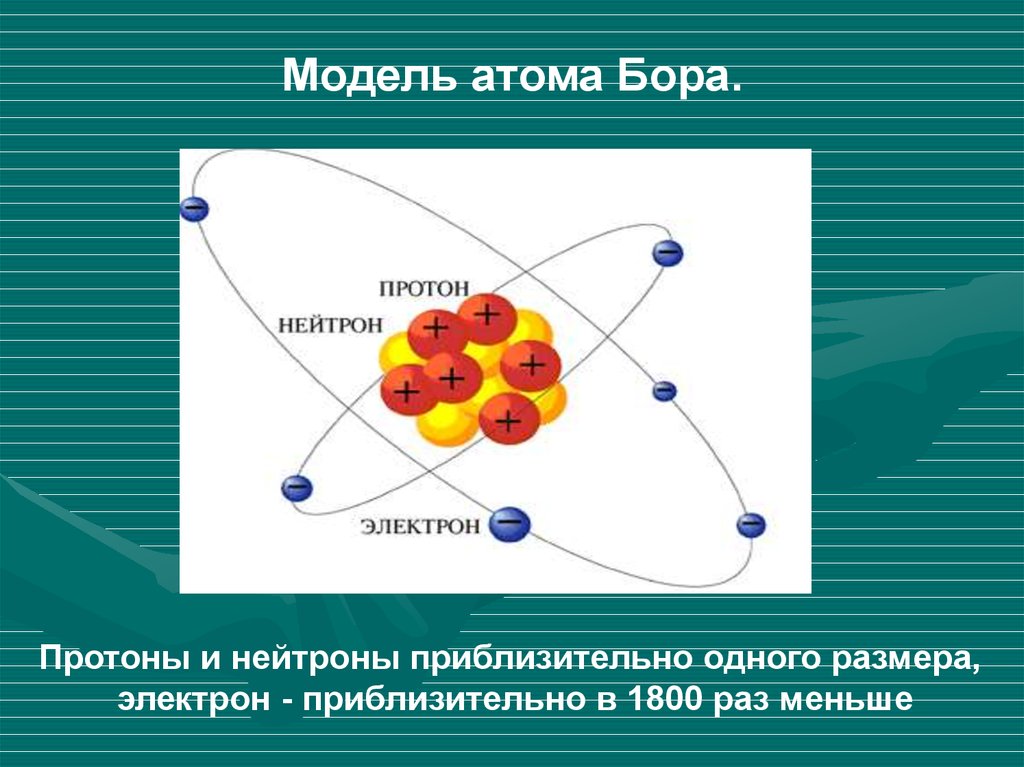 К Бору примкнул молодой физик, ставший его ассистентом, Гендрик Антон Крамерс (1894-1952). Бор создал институт теоретической физики, в организации которого ему деятельную поддержку оказывал Резерфорд. В 1922 году Бор получил Нобелевскую премию по физике. В прочитанном им 11 декабря 1922 года в Стокгольме нобелевском докладе он развернул картину состояния атомной теории к этому времени. Одним из наиболее существенных успехов теории было нахождение ключа к периодической системе элементов, которая объяснялась наличием электронных оболочек, окружающих ядра атомов. Огромная физическая интуиция позволила Бору, еще не зная принципа Паули и спина электрона, наметить правильную картину построения периодической системы, исправить ошибку химиков в классификации редких земель и предсказать существование нового элемента, который и был открыт Костером и Хевеши, давшими ему название гафний. Нильс Бор посвятил всю свою жизнь изучению свойств атома и его строения, 18 ноября 1962 года он неожиданно скончался.
К Бору примкнул молодой физик, ставший его ассистентом, Гендрик Антон Крамерс (1894-1952). Бор создал институт теоретической физики, в организации которого ему деятельную поддержку оказывал Резерфорд. В 1922 году Бор получил Нобелевскую премию по физике. В прочитанном им 11 декабря 1922 года в Стокгольме нобелевском докладе он развернул картину состояния атомной теории к этому времени. Одним из наиболее существенных успехов теории было нахождение ключа к периодической системе элементов, которая объяснялась наличием электронных оболочек, окружающих ядра атомов. Огромная физическая интуиция позволила Бору, еще не зная принципа Паули и спина электрона, наметить правильную картину построения периодической системы, исправить ошибку химиков в классификации редких земель и предсказать существование нового элемента, который и был открыт Костером и Хевеши, давшими ему название гафний. Нильс Бор посвятил всю свою жизнь изучению свойств атома и его строения, 18 ноября 1962 года он неожиданно скончался. Заключение. Таким образом, открытия Резерфорда и Бора являются фундаментальными и имеют огромное значение для современной физики и для всего человечества. История науки учит, что всякий раз, когда человечество овладевает очередной ступенькой лестницы, ведущей в глубь вещества, это приводит к открытию нового, еще более мощного вида энергии. Горение и взрыв связаны с перестройкой молекул. Внутриатомные процессы сопровождаются выделением в миллионы раз большей энергии. Еще большее выделение энергии происходит на уровне элементарных частиц. А что будет на следующих ступенях? Открытия Резерфорда и Бора доказали, что атом не есть неделимая частица, и дают возможность современной физике ответить на этот вопрос. Список использованной литературы: Алексеев И. С. Развитие представлений о структуре атома. М.,1975. Бор Нильс. Три статьи о спектрах и строении атомов. Москва-Петроград, Госиздат, 1922. Кедров Ф. Эрнест Резерфорд. М.: Атомиздат, 1965. Кудрявцев Л. С. Курс истории физики. М., 1982. Льоцци Марио.
Заключение. Таким образом, открытия Резерфорда и Бора являются фундаментальными и имеют огромное значение для современной физики и для всего человечества. История науки учит, что всякий раз, когда человечество овладевает очередной ступенькой лестницы, ведущей в глубь вещества, это приводит к открытию нового, еще более мощного вида энергии. Горение и взрыв связаны с перестройкой молекул. Внутриатомные процессы сопровождаются выделением в миллионы раз большей энергии. Еще большее выделение энергии происходит на уровне элементарных частиц. А что будет на следующих ступенях? Открытия Резерфорда и Бора доказали, что атом не есть неделимая частица, и дают возможность современной физике ответить на этот вопрос. Список использованной литературы: Алексеев И. С. Развитие представлений о структуре атома. М.,1975. Бор Нильс. Три статьи о спектрах и строении атомов. Москва-Петроград, Госиздат, 1922. Кедров Ф. Эрнест Резерфорд. М.: Атомиздат, 1965. Кудрявцев Л. С. Курс истории физики. М., 1982. Льоцци Марио.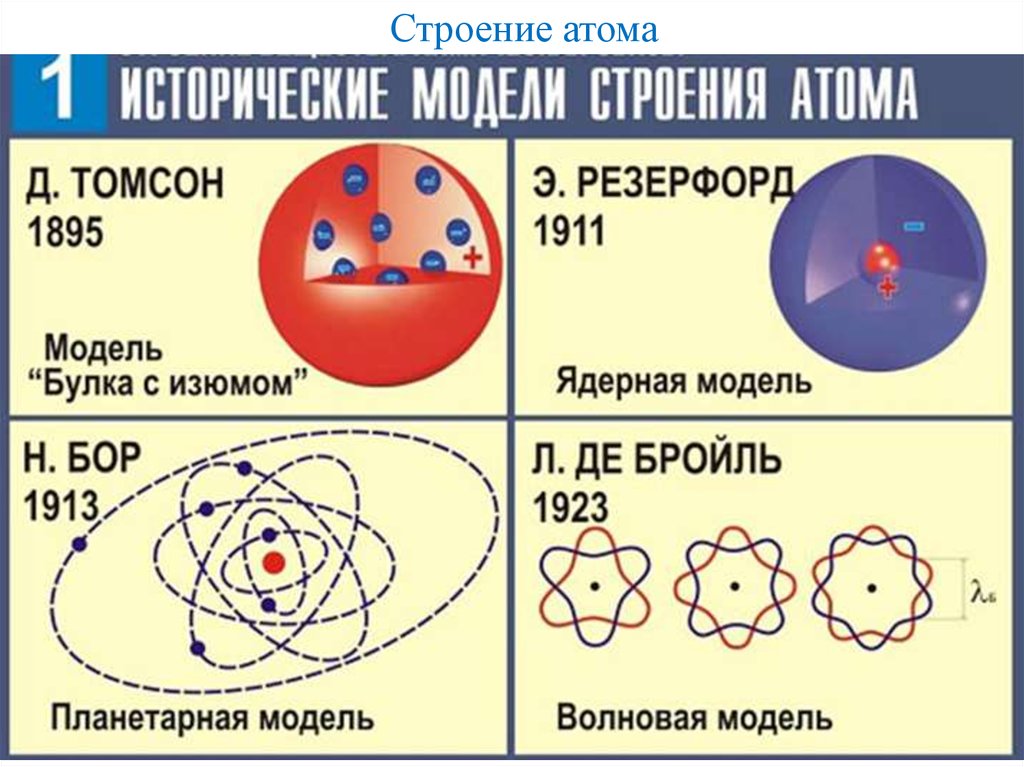 История физики. М., 1970. Мэрион Дж. Б. Физика и физический мир. М., 1975. Резерфорд Эрнест. Избранные научные труды. М., 1971.
История физики. М., 1970. Мэрион Дж. Б. Физика и физический мир. М., 1975. Резерфорд Эрнест. Избранные научные труды. М., 1971.
Модели атомов. Опыт Резерфорда 9 класс онлайн-подготовка на Ростелеком Лицей
Введение
На предыдущем уроке мы обсудили, что в результате радиоактивности образуются различные виды излучений: a-, b-, и g-лучи. Появился инструмент, при помощи которого можно было изучать строение атома.
Модель Томсона
После того, как стало ясно, что атом тоже имеет сложную структуру, как-то по-особенному устроен, необходимо было исследовать само строение атома, объяснить, как он устроен, из чего состоит. И вот ученые приступили к этому изучению.
Первые идеи о сложном строении были высказаны Томсоном, который в 1897 году открыл электрон. В 1903 году Томсон впервые предложил модель атома. По теории Томсона, атом представлял собой шар, по всему объему которого «размазан» положительный заряд. А внутри, как плавающие элементы, находились электроны. В целом, по Томсону, атом был электронейтрален, т. е. заряд такого атома был равен 0. Отрицательные заряды электронов компенсировали положительный заряд самого атома. Размер атома составлял приблизительно 10-10м. Модель Томсона получила название «пудинг с изюмом»: сам «пудинг» – это положительно заряженное «тело» атома, а «изюм» – это электроны (рис. 1).
А внутри, как плавающие элементы, находились электроны. В целом, по Томсону, атом был электронейтрален, т. е. заряд такого атома был равен 0. Отрицательные заряды электронов компенсировали положительный заряд самого атома. Размер атома составлял приблизительно 10-10м. Модель Томсона получила название «пудинг с изюмом»: сам «пудинг» – это положительно заряженное «тело» атома, а «изюм» – это электроны (рис. 1).
Рис. 1. Модель атома Томсона («пудинг с изюмом»)
Модель Резерфорда
Первый достоверный опыт по определению строения атома удалось провести Э. Резерфорду. На сегодняшний день мы твердо знаем, что атом представляет собой структуру, напоминающую планетную солнечную систему. В центре находится массивное тело, вокруг которого вращаются планеты. Такая модель атома получила название планетарной модели.
Опыт Резерфорда
Давайте обратимся к схеме опыта Резерфорда (рис. 2) и обсудим результаты, которые привели к созданию планетарной модели.
2) и обсудим результаты, которые привели к созданию планетарной модели.
Рис. 2. Схема опыта Резерфорда
Внутрь свинцового цилиндра с узким отверстием был заложен радий. При помощи диафрагмы создавался узкий пучок a-частиц, которые, пролетая через отверстие диафрагмы, попадали на экран, покрытый специальным составом, при попадании возникала микро-вспышка. Такое свечение при попадании частиц на экран называется «сцинтиляционная вспышка». Такие вспышки наблюдались на поверхности экрана при помощи микроскопа. В дальнейшем до тех пор, пока в схеме не было золотой пластины, все частицы, которые вылетали из цилиндра, попадали в одну точку. Когда же внутрь экрана на пути летящих a-частиц была поставлена очень тонкая пластинка из золота, стали наблюдаться совершенно непонятные вещи. Как только была поставлена золотая пластина, начались отклонения a-частиц. Были замечены частицы, которые отклонялись от своего первоначального прямолинейного движения и уже попадали в совершенно другие точки этого экрана.
Более того, когда экран сделали почти замкнутым, выяснилось, что есть частицы, которые каким-то образом летят в обратную сторону. Они отклоняются под углом 90° и больше. Эти наблюдения были проанализированы Резерфордом, и выяснилась следующая довольно любопытная вещь.
Анализ результатов опыта Резерфорда
В первую очередь здесь потерпела крах теория Томсона. По теории Томсона, атом представляет собой шар размером 10-10м, в котором положительный заряд размазан и есть электрон. Так вот, электроны – это очень маленькие частицы, они не могут препятствовать a-частицам, летящим с приличной скоростью. Скорость a-частиц в данном случае составляла около 10000 км/с.
Представьте себе ситуацию, когда грузовик столкнется с игрушечным автомобилем. Понятно, что грузовик даже не заметит такого автомобиля. Это мы можем привести как аналогию столкновения электрона с a-частицей. Значит, необходимо было сделать вывод, что атом устроен иначе, не так, как утверждал Томсон. И, видимо, в атоме золота есть объект более массивный, чем a-частица, имеющий положительный заряд.
И, видимо, в атоме золота есть объект более массивный, чем a-частица, имеющий положительный заряд.
Давайте посмотрим еще одну картину, которая характеризует рассеивание a-частиц на той массивной частице, наличие которой предсказал Резерфорд в атоме (рис. 3).
Рис. 3. Рассеивание альфа-частиц По результатам опытов можно было говорить, что в атоме есть массивный положительно заряженный объект. a-частица, сталкиваясь с этой большой частицей, может отразиться обратно. Те частицы, которые пролетают рядом, отклоняются на разные углы. Чем дальше a-частица пролетает от этого объекта, тем на меньший угол они отклоняются. Такое явление получило название «рассеивание a-частиц».
Ядро и планетарная модель атома
Крупную частицу, которая находится внутри атома, Резерфорд назвал ядром. И даже оценил его размеры. По оценке Резерфорда, размеры ядра составили 10-14–10-15м. Этот объект был очень и очень мал по своим размерам по сравнению с атомом.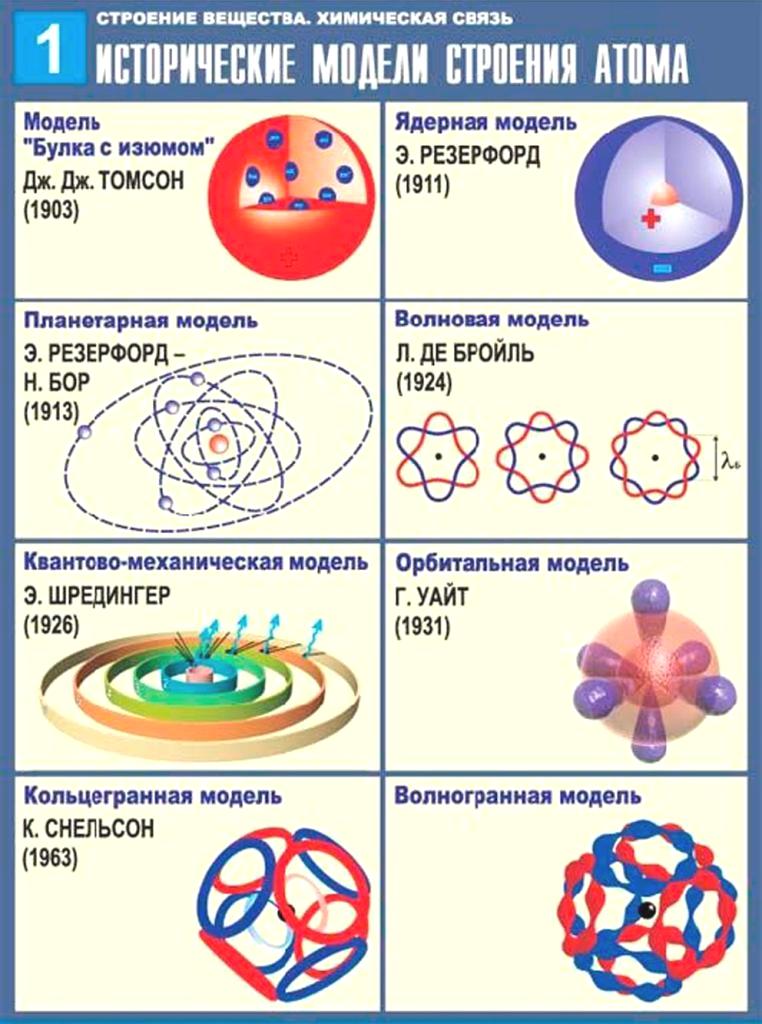 Атом имеет размер порядка 10-10м. При этом практически вся масса атома была сосредоточена именно в ядре. И именно вокруг ядра обращаются электроны.
Атом имеет размер порядка 10-10м. При этом практически вся масса атома была сосредоточена именно в ядре. И именно вокруг ядра обращаются электроны.
Отсюда следует планетарная модель Резерфорда, которая утверждает, что атом представляет собой массивное положительно заряженное ядро, вокруг которого по своим орбитам обращаются электроны (рис. 4). В целом атом электронейтрален, т. е. заряд атома равен нулю. Если у атома избыток или недостаток электронов, то его называют ион.
Рис. 4. Планетарная модель атома
Заключение
Конечно, были и другие теории, представляющие интерес. На сегодняшний день общепринятой, с некоторыми оговорками, о которых поговорим позднее, является именно планетарная модель атома, предложенная Эрнестом Резерфордом.
Список литературы
- Бронштейн М.П. Атомы и электроны. «Библиотечка “Квант”». Вып. 1. – М.: Наука, 1980.
- Кикоин И.
 К., Кикоин А.К. Физика: Учебник для 9 класса средней школы. – М.: «Просвещение».
К., Кикоин А.К. Физика: Учебник для 9 класса средней школы. – М.: «Просвещение». - Китайгородский А.И. Физика для всех. Фотоны и ядра. Книга 4. – М.: Наука.
- Мякишев Г.Я., Синякова А.З. Физика. Оптика Квантовая физика. 11 класс: учебник для углубленного изучения физики. – М.: Дрофа.
- Ньютон И. Математические начала натуральной философии. – М.: Наука, 1989.
- Резерфорд Э. Избранные научные труды. Радиоактивность. – М.: Наука.
- Резерфорд Э. Избранные научные труды. Строение атома и искусственное превращение элементов. – М.: Наука.
- Эйнштейн А., Инфельд Л. Эволюция физики. Развитие идей от первоначальных понятий до теории относительности и квантов. – М.: Наука, 1965.
атомов | Определение, структура, история, примеры, схема и факты
модель атомной оболочки
Посмотреть все медиа
- Ключевые люди:
- Эрнест Резерфорд
Нильс Бор
Лев Давидович Ландау
Стивен Чу
Уильям Д.
 Филлипс
Филлипс
- Похожие темы:
- субатомная частица радиоактивность изотоп атомизм периодическая таблица
Просмотреть весь связанный контент →
Популярные вопросы
Что такое атом?
Атом является основным строительным элементом химии. Это наименьшая единица, на которую можно разделить материю без высвобождения электрически заряженных частиц. Это также наименьшая единица материи, обладающая характерными свойствами химического элемента.
Все ли атомы одного размера?
Все атомы примерно одинакового размера, независимо от того, имеют ли они 3 или 90 электронов. Приблизительно 50 миллионов атомов твердого вещества, выстроенных в ряд, будут иметь размер 1 см (0,4 дюйма). Удобная единица длины для измерения размеров атомов — ангстрем, определяемый как 10 −10 метра.
Из чего состоит масса атома?
Масса атома состоит из массы ядра плюс массы электронов. Это означает, что единица атомной массы не совсем такая же, как масса протона или нейтрона.
Это означает, что единица атомной массы не совсем такая же, как масса протона или нейтрона.
Как определяется атомный номер атома?
Единственной наиболее важной характеристикой атома является его атомный номер (обычно обозначаемый буквой Z), который определяется как количество единиц положительного заряда (протонов) в ядре. Например, если атом имеет Z, равный 6, это углерод, а Z, равный 92, соответствует урану.
Сводка
Прочтите краткий обзор этой темы
атом , наименьшая единица, на которую можно разделить материю без высвобождения электрически заряженных частиц. Это также наименьшая единица материи, обладающая характерными свойствами химического элемента. Таким образом, атом является основным строительным блоком химии.
Исследование различных конфигураций электронов в электронных оболочках вокруг ядра атома
Просмотреть все видео к этой статье Большая часть атома представляет собой пустое пространство. Остальное состоит из положительно заряженного ядра протонов и нейтронов, окруженного облаком отрицательно заряженных электронов. Ядро маленькое и плотное по сравнению с электронами, которые являются самыми легкими заряженными частицами в природе. Электроны притягиваются к любому положительному заряду своей электрической силой; в атоме электрические силы связывают электроны с ядром.
Остальное состоит из положительно заряженного ядра протонов и нейтронов, окруженного облаком отрицательно заряженных электронов. Ядро маленькое и плотное по сравнению с электронами, которые являются самыми легкими заряженными частицами в природе. Электроны притягиваются к любому положительному заряду своей электрической силой; в атоме электрические силы связывают электроны с ядром.
Из-за природы квантовой механики ни одно изображение не было полностью удовлетворительным для визуализации различных характеристик атома, что вынуждает физиков использовать дополнительные изображения атома для объяснения различных свойств. В некотором отношении электроны в атоме ведут себя как частицы, вращающиеся вокруг ядра. В других электроны ведут себя как волны, застывшие вокруг ядра. Такие волновые структуры, называемые орбиталями, описывают распределение отдельных электронов. Эти орбитальные свойства сильно влияют на поведение атома, а его химические свойства определяются орбитальными группировками, известными как оболочки.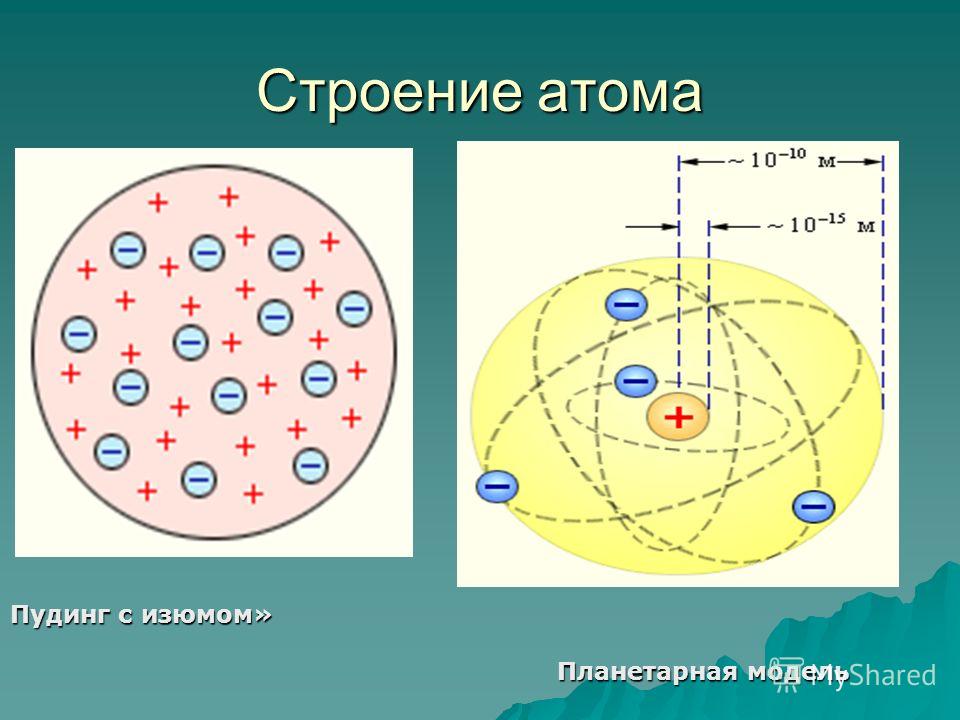
Эта статья начинается с широкого обзора фундаментальных свойств атома и составляющих его частиц и взаимодействий. После этого обзора следует исторический обзор наиболее влиятельных концепций об атоме, которые были сформулированы на протяжении веков. Для получения дополнительной информации, касающейся структуры ядра и элементарных частиц, см. субатомные частицы.
Викторина “Британника”
Наука: правда или вымысел?
Вас увлекает физика? Устали от геологии? С помощью этих вопросов отделите научный факт от вымысла.
Большая часть материи состоит из скоплений молекул, которые можно относительно легко разделить. Молекулы, в свою очередь, состоят из атомов, соединенных химическими связями, которые труднее разорвать. Каждый отдельный атом состоит из более мелких частиц, а именно электронов и ядер. Эти частицы электрически заряжены, и электрические силы на заряде ответственны за удержание атома вместе. Попытки разделить эти более мелкие составляющие частицы требуют все большего количества энергии и приводят к созданию новых субатомных частиц, многие из которых заряжены.
Как отмечалось во введении к этой статье, атом в основном состоит из пустого пространства. Ядро является положительно заряженным центром атома и содержит большую часть его массы. Он состоит из протонов, имеющих положительный заряд, и нейтронов, не имеющих заряда. Протоны, нейтроны и окружающие их электроны являются долгоживущими частицами, присутствующими во всех обычных атомах природного происхождения. Другие субатомные частицы могут быть обнаружены в ассоциации с этими тремя типами частиц. Однако они могут быть созданы только с добавлением огромного количества энергии и очень недолговечны.
Оформите подписку Britannica Premium и получите доступ к эксклюзивному контенту. Подпишитесь сейчас
Все атомы примерно одинакового размера, независимо от того, имеют ли они 3 или 90 электронов. Приблизительно 50 миллионов атомов твердого вещества, выстроенных в ряд, будут иметь размер 1 см (0,4 дюйма). Удобная единица длины для измерения размеров атомов — ангстрем (Å), определяемый как 10 −10 метра.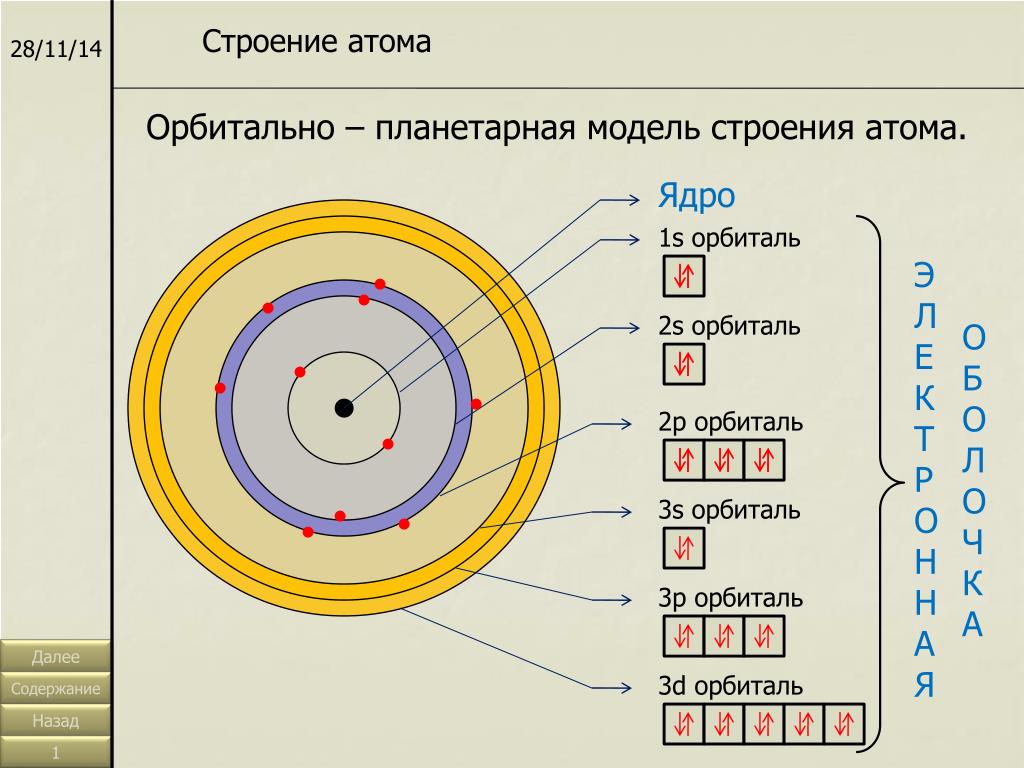 Радиус атома составляет 1–2 Å. По сравнению с общим размером атома ядро еще меньше. Он находится в такой же пропорции к атому, как шарик к футбольному полю. По объему ядро занимает всего 10 −14 метра пространства в атоме, т. е. 1 часть на 100 000. Удобная единица длины для измерения размеров ядер — фемтометр (фм), который равен 10 −15 метра. Диаметр ядра зависит от числа содержащихся в нем частиц и колеблется примерно от 4 фм для легкого ядра, такого как углерод, до 15 фм для тяжелого ядра, такого как свинец. Несмотря на малые размеры ядра, в нем сосредоточена практически вся масса атома. Протоны — это массивные положительно заряженные частицы, тогда как нейтроны не имеют заряда и немного массивнее протонов. Тот факт, что ядра могут иметь от 1 до почти 300 протонов и нейтронов, объясняет их большие различия в массе. Самое легкое ядро, атом водорода, в 1836 раз массивнее электрона, а тяжелые ядра почти в 500 000 раз массивнее.
Радиус атома составляет 1–2 Å. По сравнению с общим размером атома ядро еще меньше. Он находится в такой же пропорции к атому, как шарик к футбольному полю. По объему ядро занимает всего 10 −14 метра пространства в атоме, т. е. 1 часть на 100 000. Удобная единица длины для измерения размеров ядер — фемтометр (фм), который равен 10 −15 метра. Диаметр ядра зависит от числа содержащихся в нем частиц и колеблется примерно от 4 фм для легкого ядра, такого как углерод, до 15 фм для тяжелого ядра, такого как свинец. Несмотря на малые размеры ядра, в нем сосредоточена практически вся масса атома. Протоны — это массивные положительно заряженные частицы, тогда как нейтроны не имеют заряда и немного массивнее протонов. Тот факт, что ядра могут иметь от 1 до почти 300 протонов и нейтронов, объясняет их большие различия в массе. Самое легкое ядро, атом водорода, в 1836 раз массивнее электрона, а тяжелые ядра почти в 500 000 раз массивнее.
Основные свойства
Единственной наиболее важной характеристикой атома является его атомный номер (обычно обозначаемый буквой Z ), который определяется как количество единиц положительного заряда (протонов) в ядре. Например, если атом имеет Z из 6, это углерод, а Z из 92 соответствует урану. Нейтральный атом имеет равное количество протонов и электронов, поэтому положительные и отрицательные заряды точно уравновешиваются. Поскольку именно электроны определяют, как один атом взаимодействует с другим, в конечном итоге именно количество протонов в ядре определяет химические свойства атома.
Например, если атом имеет Z из 6, это углерод, а Z из 92 соответствует урану. Нейтральный атом имеет равное количество протонов и электронов, поэтому положительные и отрицательные заряды точно уравновешиваются. Поскольку именно электроны определяют, как один атом взаимодействует с другим, в конечном итоге именно количество протонов в ядре определяет химические свойства атома.
Что такое атом? Определение и структура
По
- Бен Луткевич, Технический писатель
Атом — это частица вещества, однозначно определяющая химический элемент. Атом состоит из центрального ядра, окруженного одним или несколькими отрицательно заряженными электронами. Ядро заряжено положительно и содержит одну или несколько относительно тяжелых частиц, известных как протоны и нейтроны.
Атомы являются основными строительными блоками материи. Все, что занимает пространство, и все, что имеет массу, состоит из атомов.
Что такое протоны и нейтроны?Протоны и нейтроны — субатомные частицы, составляющие центр атома или его атомное ядро.
- протон заряжен положительно. Число протонов в ядре атома является атомным номером химического элемента. Атомные номера различных элементов можно найти в Периодической таблице элементов. Например, у натрия 11 протонов, а его атомный номер равен 11. Протон имеет массу покоя, обозначаемую m p , приблизительно 1,673 x 10 -27 килограмма (кг).
- Нейтрон электрически нейтрален и имеет массу покоя, обозначенную m n , приблизительно 1,675 x 10 -27 .
Масса протона или нейтрона увеличивается, когда частица достигает предельной скорости, например, в циклотроне или линейном ускорителе.
Общая масса атома, включая протоны, нейтроны и электроны, является атомной массой или атомным весом. Атомная масса или вес измеряется в атомных единицах массы.
Протоны и нейтроны составляют ядро атома и орбиту электронов.Электроны составляют лишь крошечную часть массы атомной структуры, однако они играют важную роль в химических реакциях, в результате которых образуются молекулы. Для большинства целей атомный вес можно рассматривать как количество протонов плюс количество нейтронов. Поскольку количество нейтронов в атоме может варьироваться, для большинства элементов может быть несколько различных атомных весов.
Протоны и электроны имеют одинаковые и противоположные заряды. Протоны имеют положительный заряд, а электроны – отрицательный. Обычно атомы имеют одинаковое количество протонов и электронов, что придает им нейтральный заряд.
Ион — это атом с другим числом электронов, чем у протонов, и он электрически заряжен. Ион с дополнительными электронами имеет отрицательный заряд и называется анионом , а ион с недостатком электронов имеет положительный заряд и называется катионом .
Ион с дополнительными электронами имеет отрицательный заряд и называется анионом , а ион с недостатком электронов имеет положительный заряд и называется катионом .
Атомы, имеющие одинаковое количество протонов, но разное количество нейтронов, представляют один и тот же элемент и известны как изотопы этого элемента. Изотоп элемента определяется суммой количества протонов и нейтронов. Например, следующие два изотопа атома углерода:
- Углерод-12 — наиболее распространенный нерадиоактивный изотоп углерода.
- Углерод-14 — менее распространенный радиоактивный изотоп углерода.
Единственный нейтральный атом без нейтронов — это атом водорода. Он имеет один электрон и один протон.
История атома По данным CERN, Европейского совета по ядерным исследованиям, атомы были созданы 13,7 миллиарда лет назад в первые несколько минут после Большого взрыва. Новая Вселенная остыла и расширилась, создав условия для образования электронов и кварков — меньших частиц, из которых состоят протоны и нейтроны. Миллионные доли секунды спустя кварки объединились, чтобы сформировать протоны и нейтроны, которые объединились, чтобы сформировать ядра атомов.
Новая Вселенная остыла и расширилась, создав условия для образования электронов и кварков — меньших частиц, из которых состоят протоны и нейтроны. Миллионные доли секунды спустя кварки объединились, чтобы сформировать протоны и нейтроны, которые объединились, чтобы сформировать ядра атомов.
Физик Эрнест Резерфорд разработал раннюю модель атома в 1912 году. Он был первым, кто предположил, что атомы подобны миниатюрным солнечным системам, за исключением того, что вместо гравитации, действующей как сила притяжения, эту функцию выполняют противоположные электрические заряды. В резерфордовском атоме атомной теории электроны вращаются вокруг ядра по круговым траекториям.
Другой физик, Нильс Бор, пересмотрел модель атома Резерфорда в 1913 году.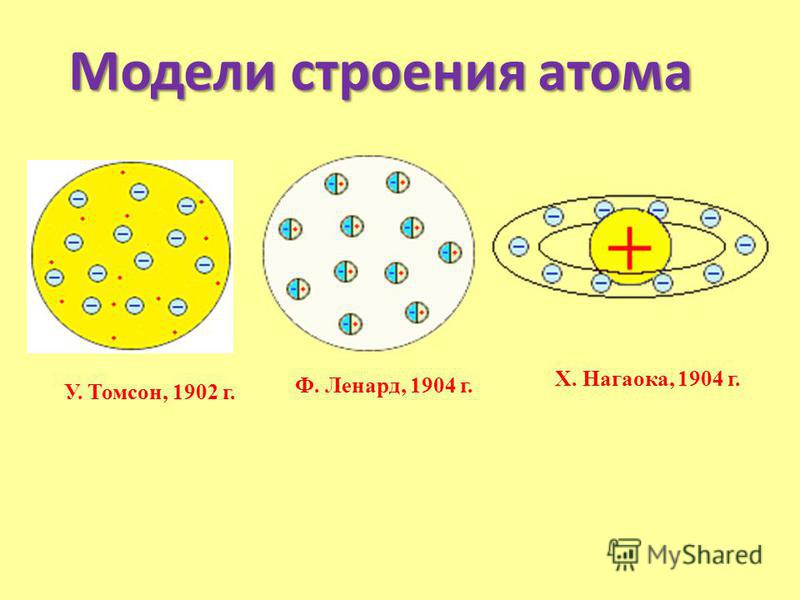 Атом Бора включал отрицательно заряженные электроны, вращающиеся вокруг ядра на определенных срединных расстояниях. Эти расстояния представлены сферами, называемыми оболочками , окружающими ядро. Электроны могут переходить с оболочки на оболочку. Когда электрон поглощает достаточно энергии, он перемещается на большую или более высокую оболочку. Когда он теряет определенное количество энергии, он падает на меньшую, более низкую оболочку.
Атом Бора включал отрицательно заряженные электроны, вращающиеся вокруг ядра на определенных срединных расстояниях. Эти расстояния представлены сферами, называемыми оболочками , окружающими ядро. Электроны могут переходить с оболочки на оболочку. Когда электрон поглощает достаточно энергии, он перемещается на большую или более высокую оболочку. Когда он теряет определенное количество энергии, он падает на меньшую, более низкую оболочку.
Константа радиуса Бора основана на модели атома Бора.
Атомная энергия Сильное ядерное взаимодействие удерживает вместе протоны и нейтроны в ядре атома. Эта сила преодолевает силу отталкивания между положительно заряженными частицами. Сильное ядерное взаимодействие, иногда называемое сильным взаимодействием или сильным взаимодействием, действует только на очень близких расстояниях. Сильное взаимодействие является самым сильным из четырех фундаментальных сил в природе; остальные три — гравитационное, электромагнитное и слабое ядерное взаимодействие.
Когда связь между частицами в ядре разрывается, высвобождается большое количество энергии. Процесс разрыва этих связей известен как деление ядра. Атомные электростанции используют деление для расщепления атомов урана и выработки электроэнергии. Уран используется для деления, потому что его атомы относительно легко расщепляются.
Атомная энергетика считается чистым источником энергии, поскольку при делении не образуются парниковые газы. Это возможный источник энергии для ИТ-центров обработки данных, стремящихся уменьшить свой углеродный след.
Узнайте о роли атомной физики в квантовых вычислениях и о том, почему вам следует обратить внимание на эти разработки.
Последнее обновление: август 2022 г.
- Каково текущее состояние квантовых вычислений?
- 5 быстрых терминов квантовых вычислений для изучения
- Устойчивое развитие в деловой практике: Что следует знать ИТ-специалистам
- Глобальное состояние устойчивого развития центров обработки данных
- Ключевая роль ИТ-директора в обеспечении экологической устойчивости
электрон
Автор: Роберт Шелдон
атомная единица массы (АМД или а.е.м.)
Автор: Рахул Авати
материя
Автор: Рахул Авати
твердый
Автор: Эндрю Зола
SearchCloudComputing
- Упростите управление пакетами с помощью этого руководства по Azure Artifacts
Расширение службы Azure DevOps, Azure Artifacts, может помочь разработчикам управлять пакетами и обмениваться ими, чтобы оптимизировать общую.
 ..
.. - Oracle оптимизирует расходы на AWS, поддержку многооблачных баз данных
Oracle разрешает пользователям своих баз данных получать доступ к этим сервисам в конкурирующих облаках, активно преследуя клиентов AWS в …
- Сравните AWS Glue и Azure Data Factory
AWS Glue и Фабрика данных Azure имеют ключевые отличия, несмотря на то, что являются схожими сервисами. Узнайте, что лучше всего подходит для вашей организации …
ПоискMobileComputing
- Apple преследует растущий премиальный рынок с iPhone 14
Apple переключила свое внимание на смартфоны премиум-класса в новейшей линейке iPhone 14 с такими функциями, как режим блокировки, который IT …
- Предотвращение атак на мобильные приложения на предприятии
По мере того, как мобильные устройства становятся все более популярными в качестве корпоративных устройств, мобильные приложения становятся все большей мишенью для хакеров.
 Поймите риски…
Поймите риски… - Лучшие мобильные приложения для малого и среднего бизнеса
Хотя существует множество вариантов мобильных приложений, которые могут помочь организациям достичь бизнес-целей, некоторые …
SearchDataCenter
- Дорожная карта Arm Neoverse нацелена на корпоративную инфраструктуру, облако
Дорожная карта
Arm для ядра Neoverse V2 предназначена для работы с 5G, высокопроизводительными вычислениями и периферийными рабочими нагрузками. Nvidia включит это предложение в свой …
- IBM нацеливает энергосберегающие мейнфреймы на пользователей Linux
Новое поколение мейнфреймов IBM на базе Linux может значительно снизить энергопотребление для компаний, желающих заменить серверы x86 …
- План подписки IBM iSeries направлен на упрощение ИТ-бюджетов
Вслед за конкурентами, включая Dell и HPE, IBM представила комплексный план подписки на iSeries, который .
 ..
..
4.2 Модели атома | Атом
Предыдущий 4.1 Введение | Следующий 4.3 Атомная масса и диаметр |
4.2 Модели атома (ESAAN)
Важно понимать, что многое из того, что мы знаем о структуре атомов, развивалось в течение долгого времени. промежуток времени. Часто так развивается научное знание, когда один человек опирается на идеи другого. еще. Мы собираемся посмотреть, как наше современное понимание атома эволюционировало с течением времени.
Идея атомов была придумана двумя греческими философами Демокритом и Левкиппом в пятом веке до нашей эры.
Греческое слово ατoμoν (атом) означает неделимых , потому что считалось, что атомы
нельзя было разбить на более мелкие части.
Сегодня мы знаем, что атомы состоят из положительно заряженных ядер в центре. в окружении отрицательно заряженных электронов . Однако в прошлом, до создания структуры атом был правильно понят, ученые придумали множество различных модели или картинки , чтобы описать, как выглядят атомы.
- Модель
Модель — это представление системы в реальном мире. Модели помогают нам понять системы и их характеристики.
Например, модель атома представляет, как могла бы выглядеть структура атома на основе что мы знаем о том, как ведут себя атомы. Это не обязательно верное представление о точной структуре атома.
Модели часто упрощаются. Маленькие игрушечные машинки, с которыми вы, возможно, играли в детстве, — это модели. Они дают
Вы хорошо представляете, как выглядит настоящий автомобиль, но они намного меньше и намного проще. Модель не всегда может
быть абсолютно точным, и важно, чтобы мы это осознавали, чтобы у нас не сложилось неправильное представление
о чем-нибудь.
Модель не всегда может
быть абсолютно точным, и важно, чтобы мы это осознавали, чтобы у нас не сложилось неправильное представление
о чем-нибудь.
Модель атома Дальтона (ESAAO)
Джон Дальтон предположил, что вся материя состоит из очень маленьких частиц, которые он назвал атомами. Это не было совершенно новая концепция, поскольку древние греки (особенно Демокрит) предположили, что вся материя состоит из маленькие, неделимые (нельзя разделить) объекты. Когда Дальтон предложил свою модель, электроны и ядро были неизвестный.
Рисунок 4.2: Атом по Дальтону.
Модель атома Томсона (ESAAP)
После открытия электрона Дж.Дж. Томсоном в 1897 году люди поняли, что атомы состоят даже из
более мелкие частицы, чем они думали ранее. Однако атомное ядро еще не было открыто.
так в 1904 году была выдвинута «модель сливового пудинга». В этой модели атом состоит из отрицательных
электроны, плавающие в «супе» с положительным зарядом, подобно сливам в пудинге или изюму в
фруктовый торт (рис. 4.3). В 1906, Томсон был награжден
Нобелевскую премию за работу в этой области. Однако даже с моделью сливового пудинга все еще не было
понимание того, как устроены эти электроны в атоме.
4.3). В 1906, Томсон был награжден
Нобелевскую премию за работу в этой области. Однако даже с моделью сливового пудинга все еще не было
понимание того, как устроены эти электроны в атоме.
Рисунок 4.3: Атом в соответствии с моделью сливового пудинга.
Открытие излучения стало следующим шагом на пути к построению точной картины атомная структура. В начале ХХ века Мария и Пьер Кюри открыли, что некоторые элементы (т. радиоактивных элемента) испускают частицы, способные проходить сквозь вещество подобно Рентген (подробнее об этом читайте в 11 классе). Эрнест Резерфорд в 1911 году использовал это открытие для пересмотреть модель атома.
Двумя другими моделями, предложенными для атома, были кубическая модель и модель Сатурна. В кубической модели
предполагалось, что электроны лежат в углах куба. В модели Сатурна электроны представлялись
вращаться вокруг очень большого тяжелого ядра.
Модель атома Резерфорда (ESAAQ)
Резерфорд провел несколько экспериментов, которые привели к изменению представлений об атоме. Его новая модель описана атом как крошечное, плотное, положительно заряженное ядро, называемое ядром, окруженное более легким, отрицательно заряженным электроны. Другой взгляд на эту модель заключался в том, что атом рассматривался как мини-солнечная система. где электроны вращаются вокруг ядра, как планеты вокруг Солнца. Упрощенная картина этого показано рядом. Эту модель иногда называют планетарной моделью атома.
Рис. 4.4: Резерфордовская модель атома.
Модель атома Бора (ESAAR)
Однако с моделью Резерфорда были некоторые проблемы: например, она не могла объяснить саму
интересное наблюдение, что атомы излучают свет только на определенных длинах волн или частотах. Нильс Бор решил эту
проблему, предполагая, что электроны могут вращаться вокруг ядра только по определенным специальным орбитам при разных
энергетические уровни вокруг ядра.
Рис. 4.5: Боровская модель атома.
Джеймс Чедвик (ESAAS)
Резерфорд предсказал (в 1920 г.), что в ядре наряду с протон. Он предсказал это потому, что если бы в ядре были только положительно заряженные протоны, то оно должно было бы разорвутся на части из-за сил отталкивания между одноименно заряженными протонами! Чтобы убедиться, что атом остается электрически нейтральной, эта частица сама должна быть нейтральной. В 1932 Джеймс Чедвик открыл нейтрона и измерил его массу.
Другие модели атома (ESAAT)
Хотя наиболее часто используемой моделью атома является модель Бора, ученые все еще разрабатывают новые и
усовершенствованные теории о том, как выглядит атом. Один из самых важных вкладов в атомную теорию (т.
область науки, изучающая атомы) была развитием квантовой теории. Шредингер, Гейзенберг, Борн и
многие другие сыграли роль в развитии квантовой теории.
Модели атома
Учебник Упражнение 4.1
Сопоставьте информацию в столбце A с ключом для обнаружения в столбце B.
Колонна А | Столбец В |
1. Открытие электронов и модель сливового пудинга | А. Нильс Бор |
2. Расположение электронов | Б. Мария и Пьер Кюри |
3. Атомы как мельчайшие строительные блоки материи | C. |
4. Открытие ядра | Д. Дж.Дж. Томсон |
5. Открытие радиации | E. Резерфорд |
Решение пока недоступно.
Предыдущий 4.1 Введение | Оглавление | Следующий 4.3 Атомная масса и диаметр |
Atom Diagram – Bilder und Stockfotos
5. 155Bilder
155Bilder
- Bilder
- Fotos
- Grafiken
- Vektoren
- Videos
Niedrigster Preis
SignatureBeste Qualität
Durchstöbern Sie 5.155
atom diagram Фото и фотографии. Oder starten Sie eine neuesuche, um noch mehr Stock-Photografie und Bilder zu entdecken. атом и молекула векторная иллюстрация. Диаграмма связей меченых соединений. – Атомная диаграмма сток-график, -клипарт, -мультфильмы и -символАтом и молекула вектор-иллюстрация. Меченые соединения Связи…
bohr-atommodelle eines stickstoffatoms. векторная иллюстрация для умственного труда – атомная диаграмма, графика, клипарт, мультфильмы и символыBohr-Atommodelleeines Stickstoffatoms. Векторная иллюстрация для…
атомная структура zeichnung – атомная диаграмма, графика, клипарт, мультфильмы и символыAtom Struktur Zeichnung
zeitleiste der atommodelle. – Атомная диаграмма – графика, -клипарт, -мультфильмы и -символ
– Атомная диаграмма – графика, -клипарт, -мультфильмы и -символZeitleiste der Atommodelle.
атомоструктура, анатомия, модель. атом лучший из самых древних: протонов, электронов, нейтронов. керн. электронная орбитальная форма. красный, синий, зеленый кугель. abbildungsvektor – атомная диаграмма, графика, клипарт, мультфильмы и символыAtomstruktur, Anatomie, Modell. Atome bestehen aus drei…
helle vektor-design – атомная диаграмма, графика, клипарт, мультфильмы и символыHelle Vektor-design
Kohlenstoff-Atom auf Weißem Hintergrund. структура – диаграмма атома фондовая графика, -клипарт, -мультфильмы и -символKohlenstoff-атом на Weißem Hintergrund. Struktur
Penetrationsleistung von alpha-, beta- und gammastrahlung – атомная диаграмма стоковая графика, -клипарт, -мультфильмы и -символ -cartoons und -symboleКомпоненты кернреакторов
Nuclear Gekritzel – атомная диаграмма стоковые графики, -клипарты, -мультфильмы и -символыNuclear Gekritzel
fünf schritte atom modellvorlage folie – атомные диаграммы стоковые графики, -клипарты, -мультфильмы и -символыFünf Schritte Atom Modellvorlage Folie
abstrakte netzwerk verbindung Hintergrund. – атомная диаграмма фото и фотографии
– атомная диаграмма фото и фотографииAbstrakte Netzwerk Verbindung Hintergrund.
molekül und netzwerk weiße textur. – атомная диаграмма сток-график, -клипарт, -мультфильмы и -символMolekül und Netzwerk weiße Textur.
Структура атома и молекулы с sauerstoff- und wasserumrissdiagramm – диаграмма атома фондовая графика, -клипарт, -мультфильмы и -символСтруктурная схема атома и молекулы с Sauerstoff-…
Strompreise und Energiekonzepte
kernspaltungsprozess vektorbild – атомная диаграмма, графика, клипарт, мультфильмы и символыKernspaltungsprozess Vektorbild
eine tafel zeigt steigende energiekosten – atom diagram stock-fotos und bilderEine Tafel zeigt steigende Energiekosten
taschenrechner und steigende energiekosten – atom diagram stock-fotos und bilderTaschenrechner und steigende Energiekosten
steigende energiekosten – rising energy costs – atom diagram stock- фотографии и изображенияSteigende Energiekosten – Рост стоимости энергии
молекулярная структура триптофана. 3D-иллюстрация – атомная диаграмма, стоковые фотографии и изображения
3D-иллюстрация – атомная диаграмма, стоковые фотографии и изображенияМолекулярная структура триптофана. 3D-иллюстрация
абстрактный инфографический шаблон – атомная диаграмма сток-график, -клипарт, -мультфильмы и -символАбстрактный инфографический шаблон
структура атомов – атомная диаграмма сток-график, -клипарт, -мультфильмы и -символСтруктура атомов
Periodensystem der Elemente – диаграмма атома сток-график, -клипарт, -мультфильмы и -символPeriodensystem der Elemente
диаграмма атомной структуры – атом диаграмма сток-график, -клипарт, -мультфильмы и -символDiagramm der Atomstruktur
rolle von molekül zu quark. – атомная диаграмма сток-график, -клипарт, -мультфильмы и -символRolle von Molekül zu Quark.
veränderung von materiezuständen – атомная диаграмма сток-график, -клипарт, -мультфильмы и -символ -Vektorillustration milchsäure-molekülstruktur. 3D-иллюстрация – атомная диаграмма, стоковые фотографии и изображения Milchsäure-Molekülstruktur. 3D-иллюстрация
3D-иллюстрация
h3O, Wassermolekül, Planetenmodell, chemische und strukturelle… графика, клипарт, мультфильмы и символы
Lebhafte Netzwerkverbindungen
норадреналин-молекюльструктура. 3D-иллюстрация – атомная диаграмма, фото и изображениеНорадреналин-молекулярная структура. 3D-иллюстрация
молекулярная структура холестерина. 3D-иллюстрация – атомная диаграмма стоковые фотографии и изображенияCholesterin-Molekülstruktur. 3D-иллюстрация
литий-атом – диаграмма атома сток-график, -клипарт, -мультфильмы и -символлитий-атом
векторная диаграмма мит sich ändernden zuständen der materie, drei zuständen der materie mit unterschiedlichen molekularen anordnungen – fest, flussungen. gefrieren, schmelzen, конденсация, verdampfung, сублимация, абшайдунг. – атомная диаграмма сток-график, -клипарт, -мультфильмы и -символ Vektordiagramm mit sich ändernden Zuständen der Materie, drei. ..
..
Ebenen der Proteinstruktur von Aminosäuren bis zum Komplex des…
nukleare fusion – атомная диаграмма сток-график, -клипарт, -мультфильмы и -символNukleare Fusion
chemie-illustration zeigt formweise atomorbital, die die die elektronenverteilung beschreiben (s, p, d) – атомная диаграмма stock-grafiken, -clipart, -cartoons und -symboleChemie-Illustration zeigt formweise Atomorbital, die die…
химические иконки — серия monoline — атомная диаграмма сток-график, —клипарт, —мультфильмы и —символХимия иконки — монолайн серия
ethylenmolekül-symbol — атомная диаграмма сток-графика, —клипарт, —мультфильмы и —символEthylenmolekül-Symbol
vektordiagramm mit sich ändernden zuständen der materie, drei zuständen der materie mit unterschiedlichen molekularen anordnungen – fest, flussig, gasförmig. gefrieren, schmelzen, конденсация, verdampfung, сублимация, абшайдунг. – атомная диаграмма стоковая графика, -клипарт, -мультфильмы и -символ
gefrieren, schmelzen, конденсация, verdampfung, сублимация, абшайдунг. – атомная диаграмма стоковая графика, -клипарт, -мультфильмы и -символВекторные диаграммы с этими изображениями материи, дрей…
kernkraftprozess – атомная диаграмма стоковая графика, -клипарт, -мультфильмы и -символKernkraftprozess
vorlage fürlage fürlage fürlage anleihen – атомная диаграмма сток-график, -клипарт, -мультфильмы и -символVorlage für Anleihen
state der angelegenheit – атомная диаграмма фондовая графика, -clipart, -cartoons und -symboleТрехмерная изометрическая флеш-память Vektordardarstellung der Kreislaufwirtschaft
junge lehrerin (wissenschaftlerin, biochemikerin) unterrichtet naturwissenschaften (онлайн-эксперимент и wissenschaftliches Experiment) aus der ferne mit Laptop, kamera und whiteboard -koneptarningits im work (klesenzimmer-), eund стоковые графики, клипарты, мультфильмы и символыJunge Lehrerin (Wissenschaftlerin, Biochemikerin) unterrichtet…
Vergleich der относительный größe von partikeln und zellen auf biologischem maßstab – атомная диаграмма фондовая графика, -клипарт, -мультфильмы и -символ Vergleich der relativen Größe von Partikeln und Zellen. ..
..
Chemischen Periodensystem der Elemente mit Farbe Zellen Vektor-ill
диаграмма атомной структуры – диаграмма атома стоковая графика, -клипарт, -мультфильмы и -символДиаграмма атомной структуры
химическая структура тетраэдрических винкелей, линейная и абстрактная – диаграмма атома стоковая графика, -клипарт, -мультфильмы и -символХимическая Struktur des tetraedrischen Winkels, linear und Abstoßun
quad-icon-packet mit science-liniensatz – атомная диаграмма сток-графика, -клипарт, -мультфильмы и -символQuad-Icon-Paket mit Science-Liniensatz
molekül – атомная диаграмма сток- фотографии и изображенияMolekül
Абстрактные данные Hintergrund – атомная диаграмма фото и фотографии – атомная диаграмма фондовых графиков, -клипарт, -мультфильмы и -символ Struktur von Natriumchlorid auf weißem Hintergrund.
cm Curium Element Information – Fakten, Eigenschaften, Trends,…
porträt eines geschäftsmannes, der mit einem диаграмма arbeitet. halten sie einen stift, finanzanalyse, berechnen sie das einkommen mit einem taschenrechner. и ноутбук в бюро – атомная диаграмма стоковые фотографии и изображенияПортреты Geschäftsmannes, der mit einem Diagramm arbeitet….
chemische reaktivität: 5 bis 7 valenzelektronen – атомная диаграмма стоковые графики, -клипарты, -мультфильмы и -символыChemische Reaktivität: 5 bis 7 Valenzelektronen
molekulares bg – атомная диаграмма, графика, клипарт, мультфильмы и символы – атомная диаграмма сток-график, -клипарт, -мультфильмы и -символStruktur дер ДНК на Weißem Hintergrund.
фон 86Модель Бора: Знаменитое, но неверное изображение атома
Космос поддерживается аудиторией. Когда вы покупаете по ссылкам на нашем сайте, мы можем получать партнерскую комиссию. Вот почему вы можете доверять нам.
Когда вы покупаете по ссылкам на нашем сайте, мы можем получать партнерскую комиссию. Вот почему вы можете доверять нам.
Модель Бора, представленная датским физиком Нильсом Бором в 1913 году, стала ключевым шагом на пути к пониманию атомов.
Древнегреческие мыслители уже считали, что материя состоит из мельчайших элементарных частиц, которые невозможно разделить дальше. Науке потребовалось более 2000 лет, чтобы доказать правильность этой теории. Путь к пониманию атомов и их внутренней работы был долгим и сложным.
Британский химик Джон Дальтон в начале 19 века возродил представления древних греков о том, что материя состоит из мельчайших неделимых частиц, называемых атомами. Дальтон считал, что каждый химический элемент состоит из атомов с различными свойствами, которые могут быть объединены в различные соединения, согласно Britannica .
Теории Дальтона были верны во многих аспектах, за исключением той основной посылки, что атомы являются мельчайшим компонентом материи, который нельзя разбить на что-то еще меньшее. Примерно через сто лет после Дальтона физики начали открывать, что атом на самом деле очень сложен внутри.
Примерно через сто лет после Дальтона физики начали открывать, что атом на самом деле очень сложен внутри.
Связанный: Внутри каждого атома во Вселенной скрывается гигантская тайна
Модель Бора: путешествие в поисках структуры атомов
Британский физик Джозеф Джон Томсон совершил первый крупный прорыв в понимании атомов в 1897 году когда он обнаружил, что атомы содержат крошечные отрицательно заряженные частицы, которые он назвал электронами . Томсон считал, что электроны плавают в положительно заряженном «супе» внутри атомной сферы, согласно 9.0678 Академия Хана (откроется в новой вкладке).
14 лет спустя уроженец Новой Зеландии Эрнест Резерфорд, бывший ученик Томсона, поставил под сомнение это представление об атоме, когда в ходе экспериментов обнаружил, что в центре атома должно находиться небольшое положительно заряженное ядро.
Основываясь на этом открытии, Резерфорд затем разработал новую модель атома, модель Резерфорда. Согласно этой модели, атом больше не состоял только из электронов, плавающих в бульоне, а имел крошечное центральное ядро, которое содержало большую часть массы атома. Вокруг этого ядра электроны вращались подобно планетам, вращающимся вокруг солнце в нашей солнечной системе , согласно Британника (откроется в новой вкладке).
Согласно этой модели, атом больше не состоял только из электронов, плавающих в бульоне, а имел крошечное центральное ядро, которое содержало большую часть массы атома. Вокруг этого ядра электроны вращались подобно планетам, вращающимся вокруг солнце в нашей солнечной системе , согласно Британника (откроется в новой вкладке).
Однако некоторые вопросы остались без ответа. Например, как могло случиться, что электроны не столкнулись с ядром, поскольку их противоположный заряд означал бы, что они должны притягиваться к нему? Несколько физиков пытались ответить на этот вопрос, включая ученика Резерфорда Нильса Бора.
Нильс Бор и квантовая теория
Бор был первым физиком, обратившимся к появившейся тогда квантовая теория попытаться объяснить поведение частиц внутри самого простого из всех атомов; атом водорода. Атомы водорода состоят из тяжелого ядра с одним положительно заряженным протоном, вокруг которого вращается один, гораздо меньший и легкий, отрицательно заряженный электрон. Вся система немного похожа на Солнце, вокруг которого вращается только одна планета.
Вся система немного похожа на Солнце, вокруг которого вращается только одна планета.
Бор пытался объяснить связь между расстоянием электрона от ядра, энергией электрона и светом, поглощаемым атомом водорода, используя одно великое новшество физики той эпохи: постоянную Планка.
Постоянная Планка появилась в результате исследования немецким физиком Максом Планком свойств электромагнитного излучения гипотетического совершенного объекта, называемого черным телом.
Как ни странно, Планк обнаружил, что это излучение, включая свет, испускается не в континууме, а скорее в виде дискретных пакетов энергии, которые могут быть только кратны определенному фиксированному значению, согласно Physics World . Это фиксированное значение стало постоянной Планка. Макс Планк назвал эти пакеты квантов энергии, дав имя совершенно новому типу физики, который должен был перевернуть представление ученых о нашем мире с ног на голову.
Модель Бора и атом водорода
Какую роль играет постоянная Планка в атоме водорода? Несмотря на красивое сравнение, атом водорода не совсем похож на Солнечную систему. Электрон не вращается вокруг своего солнца — ядра — на фиксированном расстоянии, но может перескакивать с одной орбиты на другую в зависимости от того, сколько энергии он несет, постулировал Бор. Он может вращаться на расстоянии Меркурия , затем прыгнуть на Землю , затем на Марс .
Электрон не вращается вокруг своего солнца — ядра — на фиксированном расстоянии, но может перескакивать с одной орбиты на другую в зависимости от того, сколько энергии он несет, постулировал Бор. Он может вращаться на расстоянии Меркурия , затем прыгнуть на Землю , затем на Марс .
Электрон не скользит между орбитами постепенно, а совершает дискретные скачки, когда достигает правильного энергетического уровня, что вполне соответствует теории Планка, объясняет физик Али Хайек в своем Канал YouTube (откроется в новой вкладке).
Бор считал, что существует фиксированное количество орбит, по которым может двигаться электрон. Когда электрон поглощает энергию, он перескакивает на более высокую орбитальную оболочку. Когда он теряет энергию, излучая ее, он падает на более низкую орбиту. Если электрон достигнет высшей орбитальной оболочки и продолжит поглощать энергию, он вообще вылетит из атома.
Отношение между энергией электрона и частотой испускаемого им излучения равно постоянной Планка. Согласно Али Хайеку, энергия излучаемого или поглощаемого света точно равна разнице между энергиями орбит и обратно пропорциональна длине волны света, поглощаемого электроном.
Согласно Али Хайеку, энергия излучаемого или поглощаемого света точно равна разнице между энергиями орбит и обратно пропорциональна длине волны света, поглощаемого электроном.
Используя свою модель, Бор смог рассчитать спектральные линии — линии в непрерывном спектре света — которые будут поглощать атомы водорода.
Недостатки модели Бора
Модель Бора, казалось, довольно хорошо работала для атомов с одним электроном. Но, кроме водорода, все остальные атомы в периодической таблице имеют больше электронов, вращающихся вокруг ядер. Например, у атома кислорода восемь электронов, у атома железа 26 электронов.
Как только Бор попытался использовать свою модель для предсказания спектральных линий более сложных атомов, результаты стали все больше искажаться.
Есть две причины, по которым модель Бора не работает для атомов с более чем одним электроном, согласно Chemistry Channel . Во-первых, взаимодействие нескольких атомов затрудняет предсказание их энергетической структуры.
Модель Бора также не принимала во внимание некоторые ключевые принципы квантовой физики, в первую очередь тот странный и ошеломляющий факт, что частицы также являются волнами, согласно образовательному веб-сайту 9.0678 Академия Хана (откроется в новой вкладке).
Квантовая механика не позволяет точно предсказать движение электронов вокруг ядра. Невозможно точно определить скорость и положение электрона в любой момент времени. Таким образом, оболочки, в которых вращаются эти электроны, представляют собой не простые линии, а скорее расплывчатые, менее определенные облака.
Истории по теме:
Всего через несколько лет после публикации модели физики начали улучшать работу Бора на основе вновь открытых принципов поведения частиц. В конце концов, появилась гораздо более сложная квантово-механическая модель, заменившая модель Бора. Но поскольку все становится гораздо менее четким, когда действуют все квантовые принципы, модель Бора, вероятно, по-прежнему остается первой вещью, которую большинство студентов-физиков открывают в своем стремлении понять, что управляет материей в микромире.
Дополнительные ресурсы:
Узнайте больше о модели атома Бора на веб-сайте Национальной ассоциации преподавателей естественных наук (открывается в новой вкладке) или смотрите это видео (открывается в новой вкладке).
Библиография
Heilbron, J.L., Rutherford-Bohr atom, American Journal of Physics 49, 1981 https://aapt.scitation.org/doi/abs/10.1119/1.12521
Olszewski, Станислав, Новый взгляд на модель атома водорода Бора, Обзоры по теоретической науке, том 4, номер 4, декабрь 2016 г. https://www.ingentaconnect.com/contentone/asp/rits/2016/00000004/00000004/art00003 (открывается в новой вкладке)
Крагм Хельге, Нильс Бор между физикой и химией, Physics Today, 2013 http:/ /materias.df.uba.ar/f4Aa2013c2/files/2012/08/bohr2.pdf (открывается в новой вкладке)
Следите за Терезой Путаровой в Твиттере: @TerezaPultarova . Подпишитесь на нас в Твиттере @Spacedotcom и на Facebook .
Присоединяйтесь к нашим космическим форумам, чтобы продолжать обсуждать последние миссии, ночное небо и многое другое! А если у вас есть новость, исправление или комментарий, сообщите нам об этом по адресу: [email protected].
Тереза — лондонский журналист, работающий в области науки и техники, начинающий писатель-фантаст и гимнастка-любитель. Родом из Праги, Чешская Республика, она провела первые семь лет своей карьеры, работая репортером, сценаристом и ведущей различных телепрограмм Чешского общественного телевидения. Позже она сделала перерыв в карьере, чтобы продолжить образование, и добавила степень магистра естественных наук Международного космического университета во Франции к степени бакалавра журналистики и магистра культурной антропологии Карлова университета в Праге. Она работала репортером в журнале Engineering and Technology, работала внештатным сотрудником в ряде изданий, включая Live Science, Space.com, Professional Engineering, Via Satellite and Space News, а также работала научным редактором в Европейском космическом агентстве.
5 различных атомных моделей — теории, схема и структура атома
Дом »https://testbook.com/learn/chemistry/
Приянка Вагмаре | Обновлено: 16 сентября 2021 г., 16:23 IST
-1
Сохранить
Скачать публикацию в формате PDFАтом — мельчайшая частица любого элемента. Слово атом произошло от греческого слова Atomos, что означает неделимый. Атомы состоят из электронов, протонов и нейтронов. Протоны и нейтроны находятся в ядре атома, а электроны вращаются вокруг ядра. Атомы всегда имеют одинаковое количество протонов и электронов, и количество нейтронов и протонов обычно также одинаково. Протоны и нейтроны удерживаются вместе в ядре сильной силой, называемой сильной ядерной силой.
Структура атомов — недавнее открытие. Различные модели атомов постулировались и отбрасывались до того, как была открыта правильная. В этой статье мы изучим самые известные атомные модели, которые постулировались и отбрасывались до тех пор, пока не была принята окончательная.
Проверьте разработку периодической таблицы здесь.
Модель атома Дальтона- Дальтон выдвинул очень известную теорию, в которой говорилось:
- Материя состоит из очень маленьких частиц, известных как атомы.
- Атомы неделимы (которые не могут быть разделены) и не могут быть разрушены в результате химических реакций.
- Все атомы элемента имеют одинаковые химические свойства и массу.
Однако эта теория имела некоторые ограничения и недостатки.
Недостатки теории Дальтона:- Дальтон сказал, что атомы одного и того же элемента подобны во всех отношениях, а атомы разных элементов во всех отношениях различны.
- Различные другие ученые обнаружили, что атомы состоят из электронов, протонов и нейтронов.
- Томсон предложил теорию, согласно которой он определил атомы как рождественский пудинг.

- Он утверждал, что атомы состоят из положительно заряженной сферы, в которую встроены электроны.
- Он также сказал, что отрицательные и положительные заряды равны по величине, поэтому атом в целом электрически нейтрален.
- Не удалось объяснить, как положительный заряд удерживается на электроне внутри атома.
- Не удалось также объяснить причины стабильности атома.
Узнайте все о решениях, их компонентах, типах и свойствах здесь.
Модель атома Резерфорда- Резерфорд использовал эксперимент по рассеянию α-частиц на листе золота.
- Он заметил, что большая часть α– частиц прошла сквозь золотую фольгу, не отклонившись.
- Некоторые α-частицы отклонились на малые углы, а некоторые почти на 180°.
- На основании этого эксперимента Резерфорд установил, что в атоме есть положительно заряженный сферический центр, называемый ядром, и почти вся масса атома (имеющего радиус 10-10 м) упакована в ядре (имеющем радиус 10-10 м).
 радиус 10–15 м).
радиус 10–15 м). - Теория говорит, что размер ядра очень мал по сравнению с размером атома.
- Он заявил, что электроны вращаются вокруг ядра по четко определенной траектории, называемой «орбитой».
- Благодаря этому эксперименту мы пришли к выводу, что модель, предложенная Дж. Дж. Томсоном, не может быть правильной, поскольку согласно его модели атом не является полым. Положительный заряд атома равномерно распределен по всему объему. Если это так, то большинство альфа-частиц должны рассеиваться из-за силы отталкивания между положительно заряженным ядром и альфа-частицами.
- Но мы получаем прямо противоположный результат. Большинство альфа-частиц проходят через золотую фольгу без отклонений, что позволяет нам понять, что весь положительный заряд плотно сконцентрирован в центре атома, и это согласие поддерживает гипотезу ядра, предложенную ядерной моделью Резерфорда.
- В нем говорится, что весь положительный заряд плотно сжат и сконцентрирован в центре атома, и все электроны будут вращаться вокруг них, как планеты вращаются вокруг Солнца.

- Позже, из-за нескольких проблем, таких как стабильность ядра, была принята модель Бора.
Также подробнее об адсорбции читайте здесь.
Теория Нила Бора- Бор использовал концепцию квантования и выдвинул следующие положения своей теории.
- Электроны вращаются по своим орбитам, не теряя энергии.
- Электрон переходит из более низких состояний в более высокие, приобретая энергию, и переходит из более высоких энергетических состояний в более низкие энергетические состояния, теряя энергию.
- Самый низкий энергетический уровень электрона называется основным состоянием.
- Уровни энергии представлены целым числом, известным как квантовое число. Эти квантовые числа начинаются с n=1, 2, 3, ….. и обозначаются как K, L, M, N,…. Раковины.
- Модель Бора не могла определить влияние магнитного поля и электрического поля на спектры атомов.

- Атомная модель Бора сделала правильные предсказания для атомов меньшего размера, таких как водород, но плохие спектральные предсказания были получены, когда рассматривались более крупные атомы.
Ознакомьтесь с более важными разделами химии здесь.
Итак, это все о различных атомных моделях. Попрактикуйтесь в том же в нашем бесплатном приложении Testbook. Скачать сейчас!
Часто задаваемые вопросы о различных атомных моделяхВ.1 Каковы 4 атомные модели?
Ans.1 Модель атома Дальтона, Модель атома Дж. Дж. Томсона, Модель атома Резерфорда и Теория атома Нила Бора.
Q.2 Какая атомная модель является наиболее точной?
Ответ 2 Модель атома Нила Бора является наиболее точной моделью атома.
Q.3 Какая была первая атомная модель?
Ответ 3 Модель атома Дальтона была первой моделью атома.

 ед.
ед.