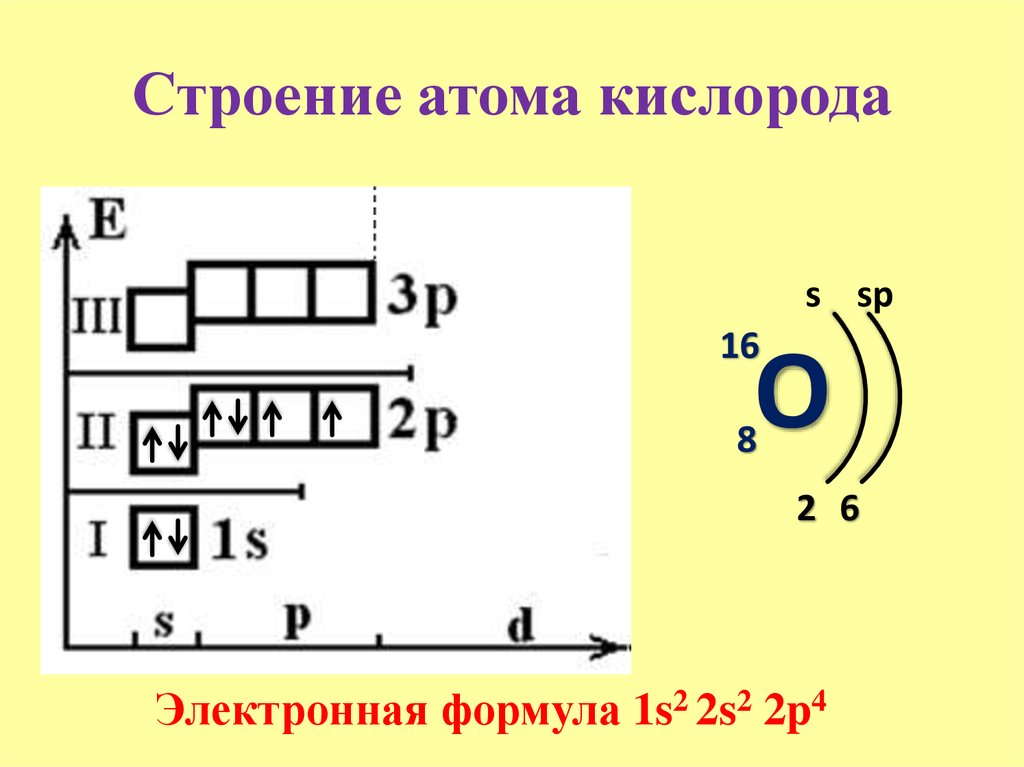
Строение атома – материалы для подготовки к ЕГЭ по Химии
Автор статьи — профессиональный репетитор И. Давыдова (Юдина).
Атом – в переводе с древнегреческого – неделимый – это наименьшая частица химического элемента, являющаяся носителем его свойств. Современные представления о строении атома требуют для понимания знаний основ квантовой механики, поэтому мы ограничимся упрощенной моделью.
Атом состоит из ядра (в составе которого протоны и нейтроны) и электронов. Несмотря на то, что ядро составляет большую часть массы атома, оно очень мало.
| Заряд z | Масса m | |
| Протон p+ | +1 | 1 |
| Нейтрон n0 | 0 | 1 |
| Электрон e– | -1 | 0 |
Количество протонов равно количеству электронов и равно номеру атома в периодической таблице.
Бор – пятый элемент периодической таблицы, в его атоме 5 протонов и 5 электронов. Атомная масса ≈ 11, количество нейтронов равно 11 – 5 = 6.
Элементы, имеющие одинаковое количество протонов в ядре, но различающиеся числом нейтронов, называются изотопами.
Например, 35Cl и 37Cl – изотопы, различающиеся атомной массой и количеством нейтронов.
| Число протонов | Число нейтронов | Число электронов | |
| 35Cl | 17 | 18 | 17 |
| 37Cl | 17 | 20 | 17 |
Вокруг ядра по различным траекториям – орбиталям движутся электроны. Каждой орбитали соответствует определенный уровень энергии, чем ближе орбиталь к ядру, тем меньшей энергией должен обладать электрон, чтобы находиться на ней.
Порядок заполнения орбиталей:
Электроны располагаются на орбиталях в соответствии со следующими правилами:
- Принцип наименьшей энергии: в первую очередь электроны заполняют наиболее низкие по энергии уровни (ближайшие к ядру).
Энергия орбиталей на уровнях и подуровнях изменяется следующим образом: 1s < 2s < 2р < Зs < Зр < 4s < 3d < 4р < 5s <4d < 5р < 6s < 4f ≈ 5d < 6p < 7s < 5f ≈6d < 7p . (●)
| Тип орбитали | Число орбиталей на энергетическом уровне | Максимальное количество электронов на этих орбиталях |
| s | 2 | |
| p | 3 | 6 |
| d | 5 | 10 |
| f | 7 | 14 |
Перед оставшимися двумя принципами введем понятие спина электрона. Спин – характеристика самого электрона, представить его (это упрощенная модель, а ненастоящий физический смысл понятия спин!) можно как направление движения электрона вокруг своей оси: по или против часовой стрелки. Возможных значений всего два: +1/2 и -1/2.
Спин – характеристика самого электрона, представить его (это упрощенная модель, а ненастоящий физический смысл понятия спин!) можно как направление движения электрона вокруг своей оси: по или против часовой стрелки. Возможных значений всего два: +1/2 и -1/2.
- Принцип Паули: на каждой орбитали может быть не более двух электронов, причем их спины должны быть различными.
- Правило Хунда: суммарный спин системы должен быть максимально возможным.
Рассмотрим заполнение орбиталей электронами на нескольких примерах. У каждого следующего элемента таблицы Менделеева на один протон и один электрон больше, чем у предыдущего. У элементов n-го периода заполнены предыдущие n-1 электронные уровни.
– магний – двенадцатый элемент, имеет по 12 протонов и электронов. Распределим эти электроны в соответствии с (●), не забывая, что на каждом подуровне может быть не более двух электронов.
Магний – элемент третьего периода, следовательно, первый и второй энергетические уровни полностью заполнены – 1s22s22p6.Магний находится во второй группе, значит, на третьем уровне у него два электрона – 3s2. Итого получаем1s22s22p63s2.
В атоме магния в основном состоянии нет неспаренных электронов.
Если атому сообщили дополнительную энергию (например, нагрели), то электронная пара может распарится и один из электронов переходит на свободную орбиталь того же энергетического уровня. В возбужденном состоянии атом магния имеет два неспаренных электрона и может образовать две связи (валентность II).
– фосфор – пятнадцатый элемент, распределяем 15 электронов: Фосфор – элемент третьего периода, следовательно, первый и второй энергетические уровни полностью заполнены – 1s22s22p6.Фосфор находится в пятой группе, значит, на третьем уровне у него пять электронов – 3s23p3. Итого получаем1s22s22p63s
Итого получаем1s22s22p63s
В атоме фосфора в основном состоянии 3 неспаренных электрона. В возбужденном состоянии атом фосфора имеет пять неспаренных электронов и может образовать пять связей (валентность V).
– цирконий – сороковой элемент, распределяем 40 электронов. Цирконий – элемент пятого периода, следовательно, первые четыре энергетических уровня полностью заполнены – 1s22s22p63s23p64s23d104p6.Заполнение пятого уровня начинается с 5s2. Цирконий – второй d – элемент в пятом периоде, значит, он содержит 2 электрона на 4d – подуровне. Итого получаем: 1s2
В атоме циркония в основном состоянии 2 неспаренных электрона.
В возбужденном состоянии цирконий имеет четыре неспаренных электрона.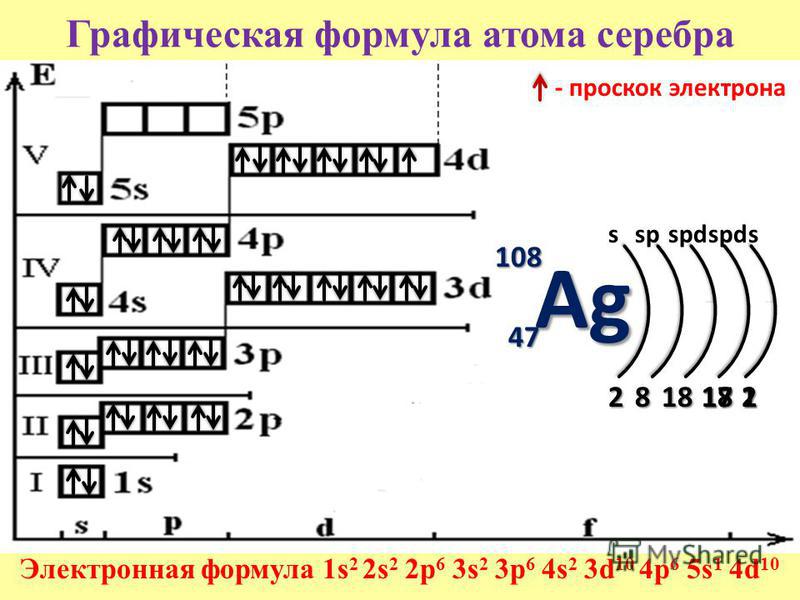
Исключениями из общего порядка заполнения электронных подуровней являются хром, марганец, медь, серебро и золото – у них наблюдается «провал» электрона с внешного s – подуровня на предвнешний d. Например, электронные конфигурации хрома и меди вместо 4s23d4 и 4s23d9 имеют вид 4s
Задания для тренировки:
- Сколько протонов и электронов содержит ион NO2–
1) 46p, 46e
2) 23p, 24e
3) 23р, 23e
4) 46p, 47e - Чем отличаются изотопы одного и того же химического элемента?
1) Числом протонов
2) Числом электронов
3) Зарядом ядра
4) Массовым числом - Укажите атом, в котором больше всего электронов:
1) 2Н
2) 40Аr
3) 41Ar
4) 39К - Изобразить электронно-графическую схему атома хлора в основном и всех возможных возбужденных состояниях.

- Объяснить, почему сера проявляет валентность VI, а кислород – не проявляет, хотя оба эти элемента содержат по 6 электронов на внешнем слое.
Строение атома | CHEMEGE.RU
Темы кодификатора ЕГЭ: Строение электронных оболочек атомов элементов первых четырех периодов: s-, p- и d-элементы. Электронная конфигурация атомов и ионов. Основное и возбужденное состояние атомов.
Тренировочные тесты в формате ЕГЭ по теме «Строение атома» (задание 1 ЕГЭ по химии) ( с ответами)
Одну из первых моделей строения атома — «пудинговую модель
 Модель, конечно, оригинальная, но неверная. Зато модель Томсона стала отличным стартом для дальнейших работ в этой области.
Модель, конечно, оригинальная, но неверная. Зато модель Томсона стала отличным стартом для дальнейших работ в этой области.
И дальнейшая работа оказалась эффективной. Ученик Томсона, Эрнест Резерфорд, на основании опытов по рассеянию альфа-частиц на золотой фольге предложил новую, планетарную модель строения атома.
Согласно модели Резерфорда, атом состоит из массивного, положительно заряженного ядра и частиц с небольшой массой — электронов, которые, как планеты вокруг Солнца, летают вокруг ядра, и на него не падают.
Модель Резерфорда оказалась следующим шагом в изучении строения атома. Однако современная наука использует более совершенную модель, предложенную Нильсом Бором в 1913 году. На ней мы и остановимся подробнее.
Атом — это мельчайшая, электронейтральная, химически неделимая частица вещества, состоящая из положительно заряженного ядра и отрицательно заряженной электронной оболочки.
При этом электроны двигаются не по определенной орбите, как предполагал Резерфорд, а довольно хаотично. Совокупность электронов, которые двигаются вокруг ядра, называется электронной оболочкой.
Совокупность электронов, которые двигаются вокруг ядра, называется электронной оболочкой.
Атомное ядро, как доказал Резерфорд — массивное и положительно заряженное, расположено в центральной части атома. Структура ядра довольно сложна, и изучается в ядерной физике. Основные частицы, из которых оно состоит — протоны и нейтроны. Они связаны ядерными силами (сильное взаимодействие).
Рассмотрим основные характеристики протонов, нейтронов и электронов:
| Протон | Нейтрон | Электрон | |
| Масса | 1,00728 а.е.м. | 1,00867 а.е.м. | 1/1960 а.е.м. |
| Заряд | + 1 элементарный заряд | 0 | — 1 элементарный заряд |
1 а. е.м. (атомная единица массы) = 1,66054·10-27 кг
е.м. (атомная единица массы) = 1,66054·10-27 кг
1 элементарный заряд = 1,60219·10-19 Кл
И — самое главное. Периодическая система химических элементов, структурированная Дмитрием Ивановичем Менделеевым, подчиняется простой и понятной логике: номер атома — это число протонов в ядре этого атома. Причем ни о каких протонах Дмитрий Иванович в XIX веке не слышал. Тем гениальнее его открытие и способности, и научное чутье, которое позволило перешагнуть на полтора столетия вперёд в науке.
Следовательно, заряд ядра Z равен числу протонов, т.е. номеру атома в Периодической системе химических элементов.
Атом — это электронейтральная частица, следовательно, число протонов равно числу электронов: Ne = Np = Z.
Масса атома (массовое число A) примерно равна суммарной массе крупных частиц, которые входят в состав атома — протонов и нейтронов.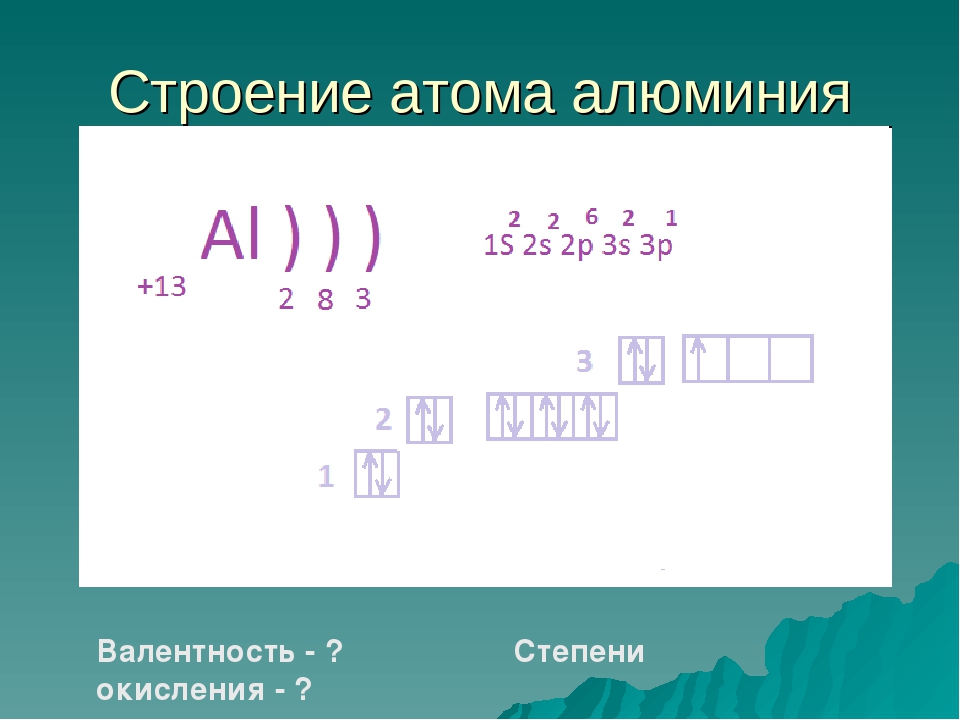 Поскольку масса протона и нейтрона примерно равна 1 атомной единице массы, можно использовать формулу:
Поскольку масса протона и нейтрона примерно равна 1 атомной единице массы, можно использовать формулу:
M = Np + Nn
Массовое число указано в Периодической системе химических элементов в ячейке каждого элемента.
Обратите внимание! При решении задач ЕГЭ массовое число всех атомов, кроме хлора, округляется до целого по правилам математики. Массовое число атома хлора в ЕГЭ принято считать равным 35,5.
Таким образом, рассчитать число нейтронов в атоме можно, вычтя из массового числа номер атома: Nn = M – Z.
В Периодической системе собраны химические элементы — атомы с одинаковым зарядом ядра. Однако, может ли меняться у этих атомов число остальных частиц? Вполне. Например, атомы с разным числом нейтронов называют изотопами данного химического элемента. У одного и того же элемента может быть несколько изотопов.
Попробуйте ответить на вопросы. Ответы на них — в конце статьи:
- У изотопов одного элемента массовое число одинаковое или разное?
- У изотопов одно элемента число протонов одинаковое или разное?
Химические свойства атомов определяются строением электронной оболочки и зарядом ядра. Таким образом, химические свойства изотопов одного элемента практически не отличаются.
Поскольку атомы одного элемента могут существовать в форме разных изотопов, в названии часто указывается массовое число, например, хлор-35, и принята такая форма записи атомов:
Еще немного вопросов:
3. Определите количество нейтронов, протонов и электронов в изотопе брома-81.
4. Определите число нейтронов в изотопе хлора-37.
Строение электронной оболочки
Согласно квантовой модели строение атома Нильса Бора, электроны в атоме могут двигаться только по определенным (стационарным) орбитам, удаленным от ядра на определенное расстояние и характеризующиеся определенной энергией.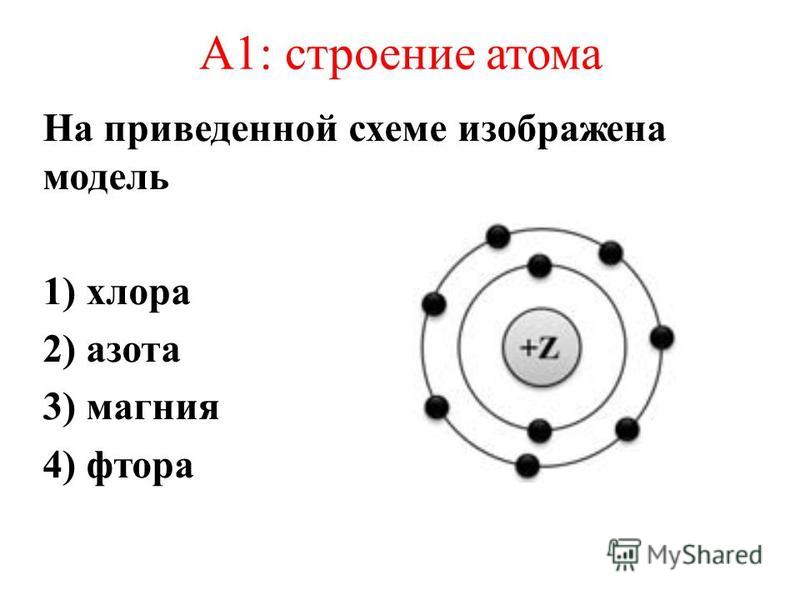 Другое название стационарны орбит — электронные слои или энергетические уровни.
Другое название стационарны орбит — электронные слои или энергетические уровни.
Электронные уровни можно обозначать цифрами — 1, 2, 3, …, n. Номер слоя увеличивается мере удаления его от ядра. Номер уровня соответствует главному квантовому числу n.
В одном слое электроны могут двигаться по разным траекториям. Траекторию орбиты характеризует электронный подуровень. Тип подуровня характеризует орбитальное квантовое число l = 0,1, 2, 3 …, либо соответствующие буквы — s, p, d, g и др.
В рамках одного подуровня (электронных орбиталей одного типа) возможны варианты расположения орбиталей в пространстве. Чем сложнее геометрия орбиталей данного подуровня, тем больше вариантов их расположения в пространстве. Общее число орбиталей подуровня данного типа l можно определить по формуле: 2l+1.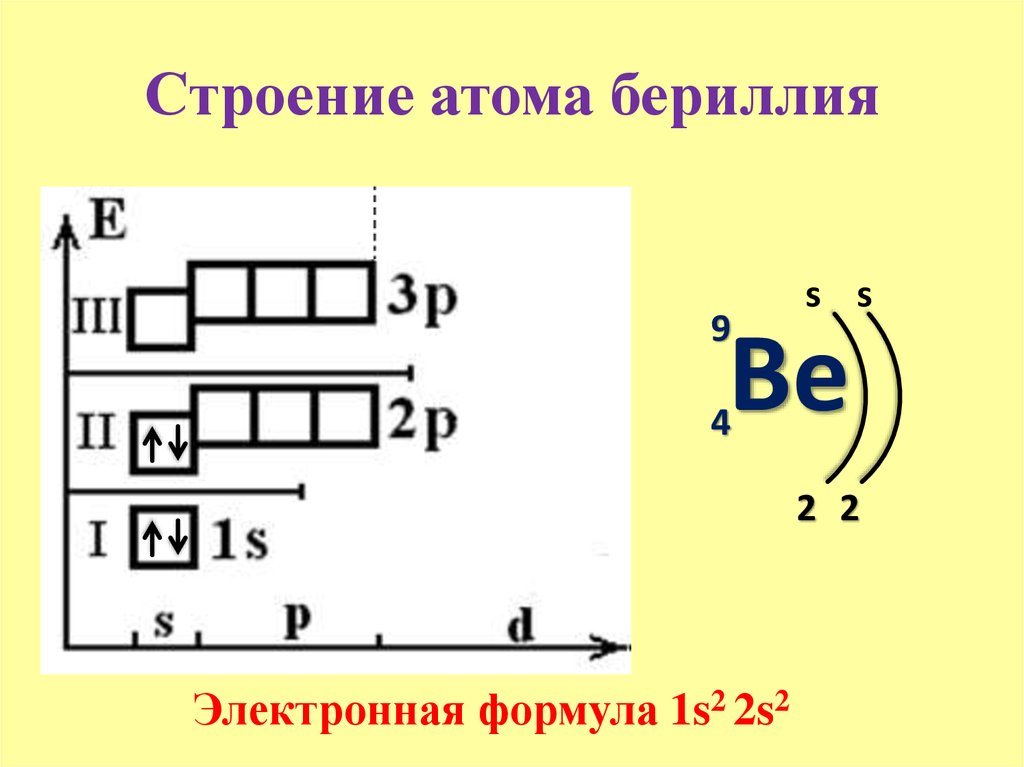 На каждой орбитали может находиться не более двух электронов.
На каждой орбитали может находиться не более двух электронов.
| Тип орбитали | s | p | d | f | g |
| Значение орбитального квантового числа l | 0 | 1 | 2 | 3 | 4 |
| Число атомных орбиталей данного типа 2l+1 | 1 | 3 | 5 | 7 | 9 |
| Максимальное количество электронов на орбиталях данного типа | 2 | 6 | 10 | 14 | 18 |
Получаем сводную таблицу:
Номер уровня, n | Подуровень | Число АО | Максимальное количество электронов |
| 1 | 1s | 1 | 2 |
| 2 | 2s | 1 | 2 |
| 2p | 3 | 6 | |
3 | 3s | 1 | 2 |
| 3p | 3 | 6 | |
| 3d | 5 | 10 | |
4 | 4s | 1 | 2 |
| 4p | 3 | 6 | |
| 4d | 5 | 10 | |
| 4f | 7 | 14 |
Заполнение электронами энергетических орбиталей происходит согласно некоторым основным правилам. Давайте остановимся на них подробно.
Давайте остановимся на них подробно.
Принцип Паули (запрет Паули): на одной атомной орбитали могут находиться не более двух электронов с противоположными спинами (спин — это квантовомеханическая характеристика движения электрона).
Правило Хунда. На атомных орбиталях с одинаковой энергией электроны располагаются по одному с параллельными спинами. Т.е. орбитали одного подуровня заполняются так: сначала на каждую орбиталь распределяется по одному электрону. Только когда во всех орбиталях данного подуровня распределено по одному электрону, занимаем орбитали вторыми электронами, с противоположными спинами.
Таким образом, сумма спиновых квантовых чисел таких электронов на одном энергетическом подуровне (оболочке) будет максимальной.
Например, заполнение 2р-орбитали тремя электронами будет происходить так: , а не так:
Принцип минимума энергии. Электроны заполняют сначала орбитали с наименьшей энергией. Энергия атомной орбитали эквивалентна сумме главного и орбитального квантовых чисел: n + l. Если сумма одинаковая, то заполняется первой та орбиталь, у которой меньше главное квантовое число n.
Энергия атомной орбитали эквивалентна сумме главного и орбитального квантовых чисел: n + l. Если сумма одинаковая, то заполняется первой та орбиталь, у которой меньше главное квантовое число n.
| АО | 1s | 2s | 2p | 3s | 3p | 3d | 4s | 4p | 4d | 4f | 5s | 5p | 5d | 5f | 5g |
| n | 1 | 2 | 2 | 3 | 3 | 3 | 4 | 4 | 4 | 4 | 5 | 5 | 5 | 5 | 5 |
| l | 0 | 0 | 1 | 0 | 1 | 2 | 0 | 1 | 2 | 3 | 0 | 1 | 2 | 3 | 4 |
| n + l | 1 | 2 | 3 | 3 | 4 | 5 | 4 | 5 | 6 | 7 | 5 | 6 | 7 | 8 | 9 |
Таким образом, энергетический ряд орбиталей выглядит так:
1s < 2s < 2 p < 3s < 3p < 4s < 3d < 4p < 5s < 4d < 5p < 6s < 4f~5d < 6p < 7s <5f~6d …
Электронную структуру атома можно представлять в разных формах — энергетическая диаграмма, электронная формула и др. Разберем основные.
Разберем основные.
Энергетическая диаграмма атома — это схематическое изображение орбиталей с учетом их энергии. Диаграмма показывает расположение электронов на энергетических уровнях и подуровнях. Заполнение орбиталей происходит согласно квантовым принципам.
Например, энергетическая диаграмма для атома углерода:
Электронная формула — это запись распределения электронов по орбиталям атома или иона. Сначала указывается номер уровня, затем тип орбитали. Верхний индекс справа от буквы показывает число электронов на орбитали. Орбитали указываются в порядке заполнения. Запись 1s2 означает, что на 1 уровне s-подуровне расположено 2 электрона.
Например, электронная формула углерода выглядит так: 1s22s22p2.
Для краткости записи, вместо энергетических орбиталей, полностью заполненных электронами, иногда используют символ ближайшего благородного газа (элемента VIIIА группы), имеющего соответствующую электронную конфигурацию.
Например, электронную формулу азота можно записать так: 1s22s22p3 или так: [He]2s22p3.
1s2 = [He]
1s22s22p6 = [Ne]
1s22s22p63s23p6 = [Ar] и так далее.
Электронные формулы элементов первых четырех периодов
Рассмотрим заполнение электронами оболочки элементов первых четырех периодов. У водорода заполняется самый первый энергетический уровень, s-подуровень, на нем расположен 1 электрон:
+1H 1s1 1s
У гелия 1s-орбиталь полностью заполнена:
+2He 1s2 1s
Поскольку первый энергетический уровень вмещает максимально 2 электрона, у лития начинается заполнение второго энергетического уровня, начиная с орбитали с минимальной энергией — 2s.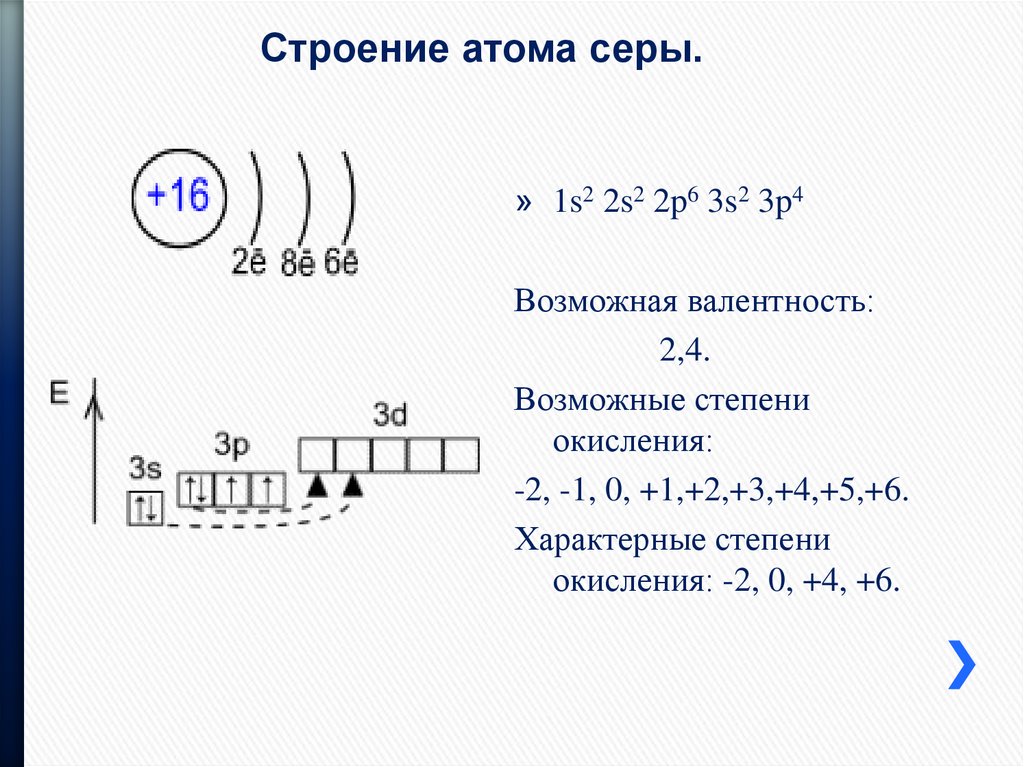 При этом сначала заполняется первый энергетический уровень:
При этом сначала заполняется первый энергетический уровень:
+3Li 1s22s1 1s 2s
У бериллия 2s-подуровень заполнен:
+4Be 1s22s2 1s 2s
Далее, у бора заполняется p-подуровень второго уровня:
+5B 1s22s22p1 1s 2s 2p
У следующего элемента, углерода, очередной электрон, согласно правилу Хунда, заполняет вакантную орбиталь, а не заполняет частично занятую:
+6C 1s22s22p2 1s 2s 2p
Попробуйте составить электронную и электронно-графическую формулы для следующих элементов, а затем можете проверить себя по ответам конце статьи:
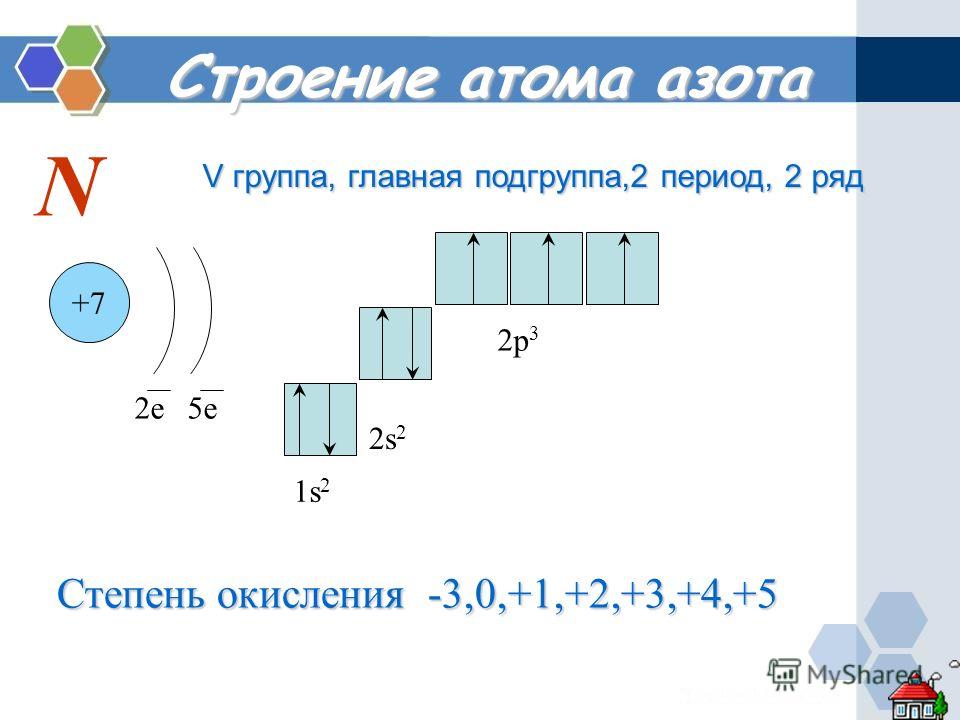
5. Азот
Азот
6. Кислород
7. Фтор
У неона завершено заполнение второго энергетического уровня:
+10Ne 1s22s22p6 1s 2s 2p
У натрия начинается заполнение третьего энергетического уровня:
+11Na 1s22s22p63s1 1s 2s 2p 3s
От натрия до аргона заполнение 3-го уровня происходит в том же порядке, что и заполнение 2-го энергетического уровня. Предлагаю составить электронные формулы элементов от магния до аргона самостоятельно, проверить по ответам.
8. Магний
9. Алюминий
10. Кремний
11. Фосфор
12. Сера
13. Хлор
Хлор
14. Аргон
А вот начиная с 19-го элемента, калия, иногда начинается путаница — заполняется не 3d-орбиталь, а 4s. Ранее мы упоминали в этой статье, что заполнение энергетических уровней и подуровней электронами происходит по энергетическому ряду орбиталей, а не по порядку. Рекомендую повторить его еще раз. Таким образом, формула калия:
+19K 1s22s22p63s23p64s11s 2s 2p3s 3p4s
Для записи дальнейших электронных формул в статье будем использовать сокращенную форму:
+19K [Ar]4s1 [Ar] 4s
У кальция 4s-подуровень заполнен:
+20Ca [Ar]4s2 [Ar] 4s
У элемента 21, скандия, согласно энергетическому ряду орбиталей, начинается заполнение 3d-подуровня:
+21Sc [Ar]3d14s2 [Ar] 4s 3d
Дальнейшее заполнение 3d-подуровня происходит согласно квантовым правилам, от титана до ванадия:
+22Ti [Ar]3d24s2 [Ar] 4s 3d
+23V [Ar]3d34s2 [Ar] 4s 3d
Однако, у следующего элемента порядок заполнения орбиталей нарушается. Электронная конфигурация хрома такая:
Электронная конфигурация хрома такая:
+24Cr [Ar]3d54s1 [Ar] 4s 3d
В чём же дело? А дело в том, что при «традиционном» порядке заполнения орбиталей (соответственно, неверном в данном случае — 3d44s2) ровно одна ячейка в d-подуровне оставалась бы незаполненной. Оказалось, что такое заполнение энергетически менее выгодно. А более выгодно, когда d-орбиталь заполнена полностью, хотя бы единичными электронами. Этот лишний электрон переходит с 4s-подуровня. И небольшие затраты энергии на перескок электрона с 4s-подуровня с лихвой покрывает энергетический эффект от заполнения всех 3d-орбиталей. Этот эффект так и называется — «провал» или «проскок» электрона. И наблюдается он, когда d-орбиталь недозаполнена на 1 электрон (по одному электрону в ячейке или по два).
И наблюдается он, когда d-орбиталь недозаполнена на 1 электрон (по одному электрону в ячейке или по два).
У следующих элементов «традиционный» порядок заполнения орбиталей снова возвращается. Конфигурация марганца:
+25Mn [Ar]3d54s2
Аналогично у кобальта и никеля. А вот у меди мы снова наблюдаем провал (проскок) электрона — электрон опять проскакивает с 4s-подуровня на 3d-подуровень:
+29Cu [Ar]3d104s1
На цинке завершается заполнение 3d-подуровня:
+30Zn [Ar]3d104s2
У следующих элементов, от галлия до криптона, происходит заполнение 4p-подуровня по квантовым правилам. Например, электронная формула галлия:
Например, электронная формула галлия:
+31Ga [Ar]3d104s24p1
Формулы остальных элементов мы приводить не будем, можете составить их самостоятельно.
Некоторые важные понятия:
Внешний энергетический уровень — это энергетический уровень в атоме с максимальным номером, на котором есть электроны.
Например, у меди ([Ar]3d104s1) внешний энергетический уровень — четвёртый.
Валентные электроны — электроны в атоме, которые могут участвовать в образовании химической связи. Например, у хрома (+24Cr [Ar]3d54s1) валентными являются не только электроны внешнего энергетического уровня (4s1), но и неспаренные электроны на 3d-подуровне, т.к. они могут образовывать химические связи.
Основное и возбужденное состояние атома
Электронные формулы, которые мы составляли до этого, соответствуют основному энергетическому состоянию атома. Это наиболее выгодное энергетически состояние атома.
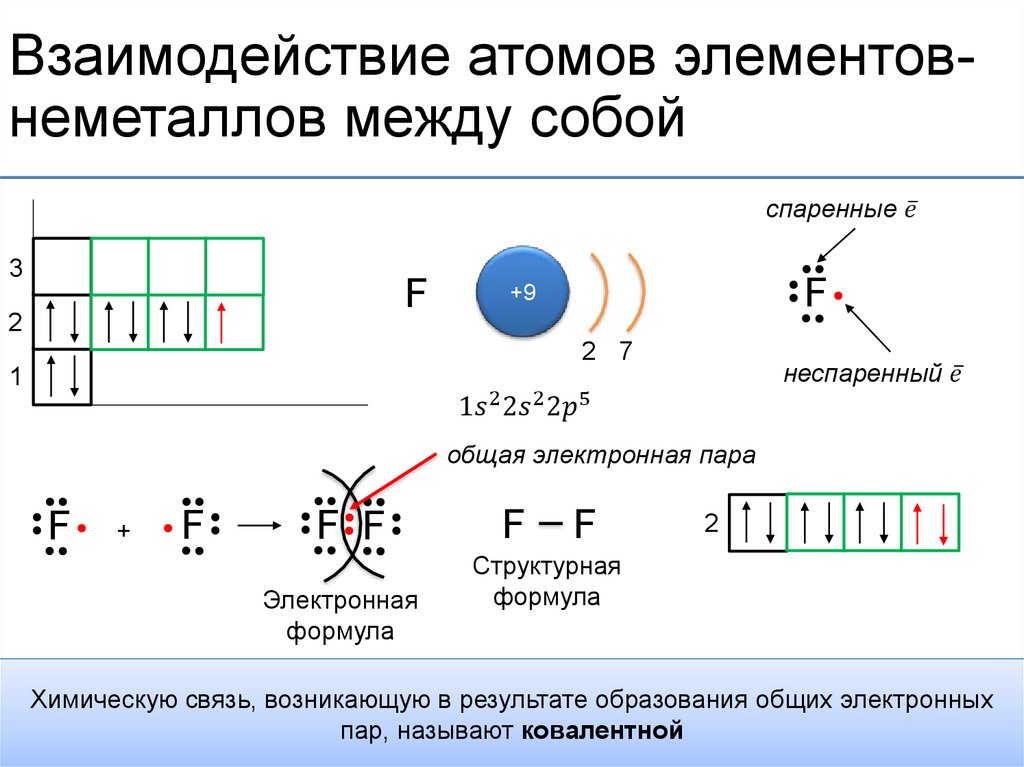
Однако, чтобы образовывать химические связи, атому в большинстве ситуаций необходимо наличие неспаренных (одиночных) электронов. А химические связи энергетически очень для атома выгодны. Следовательно, чем больше в атоме неспаренных электронов — тем больше связей он может образовать, и, как следствие, перейдёт в более выгодное энергетическое состояние.
Поэтому при наличии свободных энергетических орбиталей на данном уровне спаренные пары электронов могут распариваться, и один из электронов спаренной пары может переходить на вакантную орбиталь. Таким образом число неспаренных электронов увеличивается, и атом может образовать больше химических связей, что очень выгодно с точки зрения энергии. Такое состояние атома называют возбуждённым и обозначают звёздочкой.
Такое состояние атома называют возбуждённым и обозначают звёздочкой.
Например, в основном состоянии бор имеет следующую конфигурацию энергетического уровня:
+5B 1s22s22p1 1s 2s 2p
На втором уровне (внешнем) одна спаренная электронная пара, один одиночный электрон и пара свободных (вакантных) орбиталей. Следовательно, есть возможность для перехода электрона из пары на вакантную орбиталь, получаем возбуждённое состояние атома бора (обозначается звёздочкой):
+5B* 1s22s12p2 1s 2s 2p
Попробуйте самостоятельно составить электронную формулу, соответствующую возбуждённому состоянию атомов. Не забываем проверять себя по ответам!
15. Углерода
16. Бериллия
17. Кислорода
Кислорода
Электронные формулы ионов
Атомы могут отдавать и принимать электроны. Отдавая или принимая электроны, они превращаются в ионы.
Ионы — это заряженные частицы. Избыточный заряд обозначается индексом в правом верхнем углу.
Если атом отдаёт электроны, то общий заряд образовавшейся частицы будет положительный (вспомним, что число протонов в атоме равно числу электронов, а при отдаче электронов число протонов будет больше числа электронов). Положительно заряженные ионы — это катионы. Например: катион натрия образуется так:
+11Na 1s22s22p63s1 -1е = +11Na+ 1s22s22p63s0
Если атом принимает электроны, то приобретает отрицательный заряд. Отрицательно заряженные частицы — это анионы. Например, анион хлора образуется так:
Отрицательно заряженные частицы — это анионы. Например, анион хлора образуется так:
+17Cl 1s22s22p63s23p5 +1e = +17Cl— 1s22s22p63s23p6
Таким образом, электронные формулы ионов можно получить добавив или отняв электроны у атома. Обратите внимание, при образовании катионов электроны уходят с внешнего энергетического уровня. При образовании анионов электроны приходят на внешний энергетический уровень.
Попробуйте составить самостоятельно электронный формулы ионов. Не забывайте проверять себя по ключам!
18. Ион Са2+
19. Ион S2-
20. Ион Ni2+
Ион Ni2+
В некоторых случаях совершенно разные атомы образуют ионы с одинаковой электронной конфигурацией. Частицы с одинаковой электронной конфигурацией и одинаковым числом электронов называют изоэлектронными частицами.
Например, ионы Na+ и F—.
Электронная формула катиона натрия: Na+ 1s22s22p6, всего 10 электронов.
Электронная формула аниона фтора: F— 1s22s22p6, всего 10 электронов.
Таким образом, ионы Na+ и F— — изоэлектронные. Также они изоэлектронны атому неона.
Тренажер по теме «Строение атома» — 10 вопросов, при каждом прохождении новые.
1096
Создан на По Admin
Тренировочный тест “Строение атома”
Тренировочный тест по теме “Строение атома”
1 / 10
1) Zn 2) S 3) Si 4) Fe 5) Mg
Определите элементы, атомы которых в основном состоянии не содержат неспаренных электронов.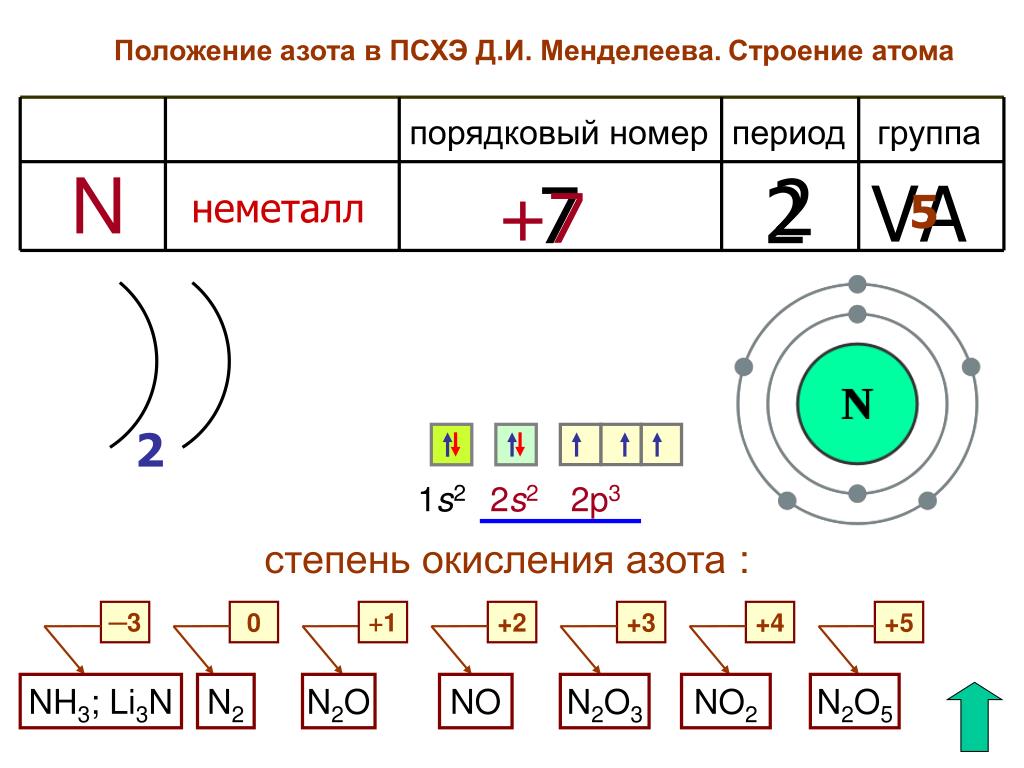
2 / 10
1) Al 2) V 3) P 4) H 5) Cl
Определите элементы, атомы которых в основном состоянии содержат три неспаренных электрона.
3 / 10
1) Li 2) F 3) N 4) As 5) Br
Определите, атомы каких из указанных в ряду элементов в основном состоянии имеют электронную конфигурацию внешнего энергетического уровня ns2np5.
4 / 10
1) Y 2) V 3) Al 4) Be 5) Ar
Определите, атомы каких из указанных в ряду элементов в основном энергетическом состоянии содержат 6 s-электронов.
5 / 10
1) Na 2) Cl 3) Si 4) Mn 5) Cr
Определите, атомы каких из указанных в ряду элементов в основном состоянии содержат одинаковое число валентных электронов.
6 / 10
1) H 2) Mg 3) Si 4) S 5) Mn
Определите, атомы каких из указанных в ряду элементов в основном состоянии содержат во внешнем слое одинаковое число электронов.
7 / 10
1) P 2) Cl 3) B 4) Ca 5) He
Определите элементы, атомы которых в основном состоянии содержат один неспаренный электрон.
8 / 10
1) Ca 2) C 3) Fe 4) Pb 5) K
Определите, атомы каких из указанных в ряду элементов в основном состоянии имеют на внешнем энергетическом уровне ровно два электрона.
9 / 10
1) Li 2) Si 3) S 4) Al 5) F
Какие из указанных элементов в основном состоянии имеют на внешнем уровне больше s-электронов, чем p-электронов? Запишите в поле ответа номера выбранных элементов в порядке возрастания.
10 / 10
1) V 2) Cl 3) As 4) P 5) Nb
Определите, атомы каких из указанных в ряду элементов в основном состоянии имеют электронную формулу внешнего энергетического уровня ns2np3.
Ваша оценка
Средний балл 40%
Ответы на вопросы:
1. У изотопов одного химического элемента массовое число всегда разное, т.к. массовое число складывается из числа протонов и нейтронов. А у изотопов различается число нейтронов.
2. У изотопов одного элемента число протонов всегда одинаковое, т. к. число протонов характеризует химический элемент.
к. число протонов характеризует химический элемент.
3. Массовое число изотопа брома-81 равно 81. Атомный номер = заряд ядра брома = число протонов в ядре = 35. Вычитаем из массового числа число протонов, получаем 81-35=46 нейтронов.
4. Массовое число изотопа хлора равно 37. Атомный номер, заряд ядра и число протонов в ядре равно 17. Получаем число нейтронов = 37-17 =20.
5. Электронная формула азота:
+7N 1s22s22p3 1s 2s 2p
6. Электронная формула кислорода:
+8О 1s22s22p4 1s 2s 2p
7. Электронная формула фтора:
8. Электронная формула магния:
+12Mg 1s22s22p63s2 1s 2s 2p 3s
9. Электронная формула алюминия:
Электронная формула алюминия:
+13Al 1s22s22p63s23p1 1s 2s 2p 3s 3p
10. Электронная формула кремния:
+14Si 1s22s22p63s23p2 1s 2s 2p 3s 3p
11. Электронная формула фосфора:
+15P 1s22s22p63s23p3 1s 2s 2p 3s 3p
12. Электронная формула серы:
+16S 1s22s22p63s23p4 1s 2s 2p 3s 3p
13. Электронная формула хлора:
Электронная формула хлора:
14. Электронная формула аргона:
+18Ar 1s22s22p63s23p6 1s 2s 2p 3s 3p
15. Электронная формула углерода в возбуждённом состоянии:
+6C* 1s22s12p3 1s 2s 2p
16. Электронная формула бериллия в возбуждённом состоянии:
+4Be 1s22s12p1 1s 2s 2p
17. Электронная формула кислорода в возбуждённом энергетическом состоянии соответствует формуле кислорода в основном энергетическом состоянии, т. к. нет условий для перехода электрона — отсутствуют вакантные энергетические орбитали.
к. нет условий для перехода электрона — отсутствуют вакантные энергетические орбитали.
18. Электронная формула иона кальция Са2+: +20Ca2+ 1s22s22p63s23p6
19. Электронная формула аниона серы S2-: +16S2- 1s22s22p63s23p6
20. Электронная формула катиона никеля Ni2+: +28Ni2+ 1s22s22p63s23p63d84s0. Обратите внимание! Атомы отдают электроны всегда сначала с внешнего энергетического уровня. Поэтому никель отдаёт электроны сначала с внешнего 4s-подуровня.
Тренировочные тесты в формате ЕГЭ по теме «Строение атома» (задание 1 ЕГЭ по химии) ( с ответами)
Понравилось это:
Нравится Загрузка. ..
..
ЕГЭ. Периодический закон и Периодическая система химических элементов Д.И. Менделеева. Строение атома 11 класс
Тема 2: Строение атома. Периодический закон
Урок 4: ЕГЭ. Периодический закон и Периодическая система химических элементов Д.И. Менделеева. Строение атома
- Видео
- Тренажер
- Теория
Заметили ошибку?
Задания с выбором ответов
|
Вопрос |
Комментарий |
|
А1. Из каких частиц состоит атомное ядро?
|
Атом – это электронейтральная частица, состоящая из протонов, нейтронов и электронов. Протоны и нейтроны входят в состав ядра атома, а электроны вращаются вокруг. Правильный ответ 2. |
|
А2. Что такое изотопы?
|
Изотопы – это атомы одного химического элемента. У них одинаковое число электронов и протонов в атоме, но разное число нейтронов и поэтому разная масса. Правильный ответ 3. |
|
А3. Что называется химическим элементом?
|
Химический элемент – это совокупность атомов с одинаковым зарядом ядра.
Правильный ответ 1. |
|
А4. Какая частица состоит из 8 протонов, 10 нейтронов и 8 электронов?
|
Находим в периодической системе элемент № 8. Это кислород. Прибавив к 8 протонам 10 нейтронов, получим массу атома 18. Это 18О. Правильный ответ 2. |
|
А5. Электронная формула атома химического элемента – 1s22s22p63s23p4. Укажите знак элемента и формулу его высшего оксида.
|
Нужно просуммировать количество электронов, которое равно количеству протонов.
Правильный ответ 3. |
|
А6. Наиболее сильно выражены металлические свойства у:
|
Чем левее и ниже элемент расположен в Периодической системе, тем ярче выражены его металлические свойства. Все приведенные элементы, кроме фосфора, находятся в 6 группе. Фосфор – это типичный неметалл. Теллур (Те) находится ниже всех в группе. Правильный ответ 4. |
|
А7. Число электронов в атоме равно:
|
Атом – это электронейтральная частица, поэтому число электронов равно числу протонов. Правильный ответ 2. |
|
А8. К р-элементам относится:
|
Al находится в III-A группе. Электронное строение внешнего энергетического уровня …3s23p1. Правильный ответ 4. |
|
А9. В каком ряду химические элементы расположены в порядке возрастания их атомного радиуса?
|
По группе сверху вниз атомные радиусы увеличиваются, а по периоду слева направо – уменьшаются.
Правильный ответ 2. |
|
А10. Химический элемент расположен в IV периоде I-A группе.
|
Это 19К. Сумма электронов в ряду должна быть равна 19.
Правильный ответ 3. |
|
А11. Бром – это элемент
|
Бром – это галоген, элемент главной подгруппы VII группы.
Правильный ответ 3. |
|
А12. Элементу с зарядом ядра +12 соответствует высший оксид:
|
По заряду ядра находим этот элемент в Периодической системе.
Правильный ответ 1. |
|
А13. Электроное строение внешнего энергeтического уровня атома кремния: 1. …2s22p2 2. …3s23p2 3. …2s22p4 4. …3s23p4 |
Кремний находится в 3-ем периоде, поэтому у него три энергетических уровня. Не учитываем варианты с цифрой 2. Так как Si – в IV группе, то валентных электронов 4. Только во втором варианте сумма электрона равна 4.
Правильный ответ 2. |
Задания на соответствие
Задания с кратким ответом
В3. Химический элемент железо представлен в природе несколькими изотопами: 54Fe, 56Fe, 57Fe, 58Fe. Определить, сколько протонов содержат атомы всех этих изотопов.
Определить, сколько протонов содержат атомы всех этих изотопов.
При обозначении изотопов вверху пишется массовое число, т. е. сумма масс протонов и нейтронов. Для определения числа протонов нужно посмотреть положение железа в Периодической системе. Порядковый номер железа – 26, значит, ядро атома железа содержит 26 протонов.
Правильный ответ 26.
В4. Определить, сколько нейтронов содержит ядро атома изотопа неона-22.
Для определения числа нейтронов нужно посмотреть положение неона в Периодической системе. Порядковый номер неона – 10. Это количество протонов. Вычитаем из массового числа количество протонов, получаем число нейтронов. Это 12.
Правильный ответ 12.
В5. Какой заряд ядра имеют изотопы химического элемента фтора?
Порядковый номер фтора – 9. Значит, заряд его ядра будет равен +9.
Правильный ответ +9
В6. Ядро атома одного из изотопов калия содержит 21 нейтрон. Определить массовое число данного изотопа.
Определить массовое число данного изотопа.
Массовое число равно сумме количества нейтронов и протонов. Нужно сложить число протонов (19) и число нейтронов (21).
Правильный ответ 40.
В7. Определить число нейтронов в ядре атома фосфора -31.
Вычитаем из массового числа (31) его порядковый номер (15) получаем число нейтронов. Это 16.
Правильный ответ 16.
В8. Под номерами 1-3 в колонке слева приведены ряды химических элементов. Укажите, какими буквами в колонке справа обозначены закономерности, на основе которых составлен каждый из этих рядов.
|
1. Na, Mg, Al, Si, P, S, Cl |
А) Электроотрицательность уменьшается |
|
2. F, O, N, Cl |
Б) Изменяется характер химических свойств высших оксидов: основные свойства ослабевают, кислотные усиливаются |
|
3. |
В) Неметалличность свойств простых веществ, образованных химическими элементами, усиливается |
|
|
Г) Степени окисления атомов химических элементов в соединении с кислородом увеличиваются |
|
|
Д) Степени окисления атомов химических элементов в соединении с водородом увеличиваются |
|
|
Е) Радиусы атомов увеличиваются |
|
|
Ж) Степень окисления атомов в высших оксидах одинакова |
Комментарий к В8. При решении этого задания нужно вспомнить таблицу, которая приводилась в предыдущем уроке.
Закономерности изменения периодических свойств приведены в Табл. 1.
1.
|
Параметр |
По группе вниз |
По периоду вправо |
|
Заряд ядра |
Увеличивается |
Увеличивается |
|
Число валентных электронов |
Не меняется |
Увеличивается |
|
Число энергетических уровней |
Увеличивается |
Не меняется |
|
Радиус атома |
Увеличивается |
Уменьшается |
|
Электроотрицательность |
Уменьшается |
Увеличивается |
|
Металлические свойства |
Увеличиваются |
Уменьшаются |
|
Степень окисления в высшем оксиде |
Не меняется |
Увеличивается |
|
Степень окисления в водородных соединениях (для элементов IV-VII групп) |
Не меняется |
Увеличивается |
Табл. 1.
1.
Представленные в вопросе элементы находятся либо в одном периоде, либо в одной группе.
- Na, Mg, Al, Si, P, S, Cl соответствуют варианты Б, В, Г
- F, O, N, Cl не соответствуют ни один из вариантов
- Be, Mg, Ca, Sr, Ba соответствуют варианты А, Е, Ж
Правильный ответ 1-Б В Г; 2-; 3-А Е Ж.
Задания с развернутым ответом
|
Вопрос |
Комментарий |
|
С1. Опишите химические свойства элемента с порядковым номером 23 по его положению в Периодической системе. |
Элемент № 23 – это ванадий V. Это металл, т. к. он находится в побочной подгруппе V группы, в 4-ом периоде. Его электронная конфигурация: 1s22s22p63s23p64s23d3. Летучих водородных соединений не образует. Высший оксид V2O5 – кислотный оксид. Как металл отдает свои валентные электроны. |
|
С2. Элемент образует высший оксид состава ЭО3. В летучем водородном соединении массовая доля водорода составляет 5,88 %. Рассчитайте относительную атомную массу элемента и назовите его. |
По формуле высшего оксида понятно, что элемент находится в VI группе. Формула водородного соединения – Н2Э. Массовая доля равна отношению массы элемента к суммарной массе соединения. Пусть атомная масса элемента будет Х. Тогда , отсюда Х = 200 : 5,88 – 2 = 32. Значит этот элемент – сера S. |
Подведение итога урока
На уроке были рассмотрены задачи ЕГЭ по теме «Периодический закон и Периодическая система химических элементов Д. И. Менделеева. Строение атома». Мы научились характеризовать общие свойства химических элементов и их соединений на основе положения в химической системе Д. И. Менделеева.
Список литературы
- Рудзитис Г.
 Е. Химия. Основы общей химии. 11 класс: учебник для общеобразовательных учреждений: базовый уровень / Г. Е. Рудзитис, Ф. Г. Фельдман. – 14-е изд. – М.: Просвещение, 2012.
Е. Химия. Основы общей химии. 11 класс: учебник для общеобразовательных учреждений: базовый уровень / Г. Е. Рудзитис, Ф. Г. Фельдман. – 14-е изд. – М.: Просвещение, 2012. - Попель П. П. Химия: 8 кл.: учебник для общеобразовательных учебных заведений / П. П. Попель, Л. С.Кривля. – К.: ИЦ «Академия», 2008. – 240 с.: ил.
- Учебно-тренировочные материалы для подготовки к единому государственному экзамену. Химия / Каверина А. А., Добротин Д. Ю., Медведев Ю. Н., Корощенко А. С. – М.: Интеллект- Центр, 2011.
Дополнительные рекомендованные ссылки на ресурсы сети Интернет
- Официальный информационный портал Единого Государственного Экзамена (Источник)
- Интернет-портал «chemport.ru» (Источник)
- Интернет-портал «Химик» (Источник)
Домашнее задание
- №№ 1-3 (с. 7) Рудзитис Г. Е. Химия. Основы общей химии. 11 класс: учебник для общеобразовательных учреждений: базовый уровень / Г.
 Е. Рудзитис, Ф. Г. Фельдман. – 14-е изд. – М.: Просвещение, 2012.
Е. Рудзитис, Ф. Г. Фельдман. – 14-е изд. – М.: Просвещение, 2012. - Какие закономерности наблюдают в изменении атомных радиусов в периодах слева направо и при переходе от одного периода к другому?
- Высший оксид состава RO3 образует элемент с электронной конфигурацией внешнего электронного слоя: 1) ns2np1; 2) ns2np3; 3) ns2np4; 4) ns2np6. Назовите этот элемент.
Заметили ошибку?
Расскажите нам об ошибке, и мы ее исправим.Видеоурок: ЕГЭ. Периодический закон и Периодическая система химических элементов Д.И. Менделеева. Строение атома по предмету Химия за 11 класс.
Строение атома и электронные конфигурации 1.0
На этой странице вы узнаете- Чем атом похож на Солнечную систему?
- Один водород, но три лучше: что такое изотопы?
- Как умеет скакать электрон?
Атом можно представить как конструктор «Лего», который можно собрать из более простых “элементарных” частиц.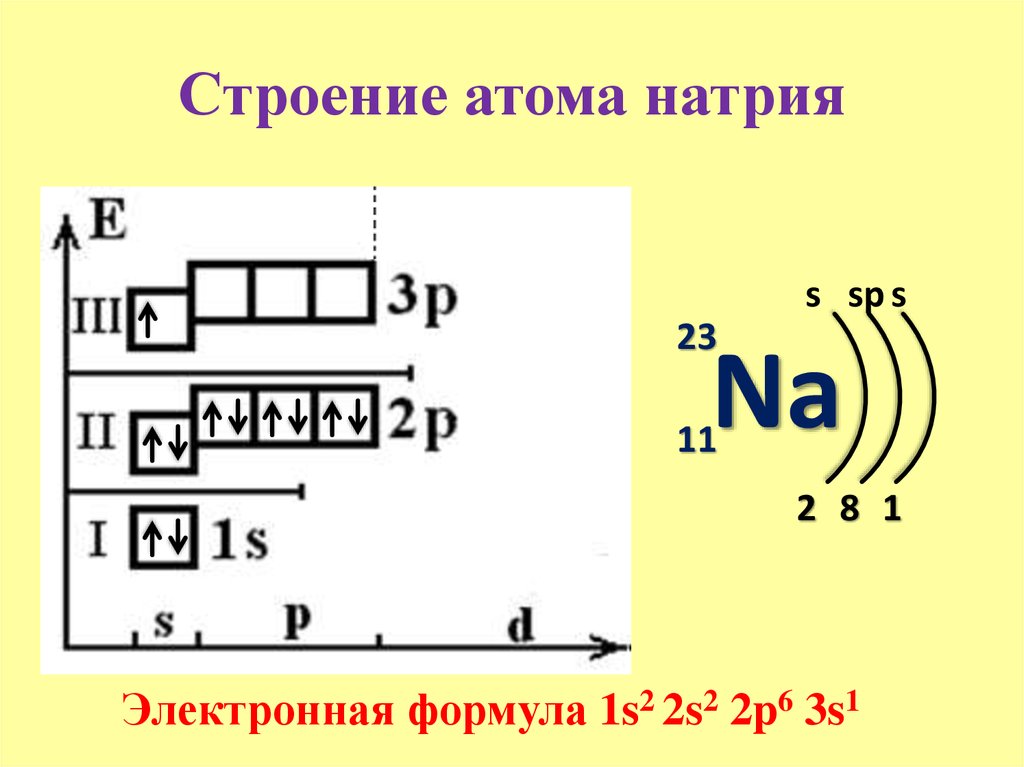 У каждого атома число “деталек” может быть различным. Об этом и о других особенностях строения атома поговорим в статье.
У каждого атома число “деталек” может быть различным. Об этом и о других особенностях строения атома поговорим в статье.
Великие ученые и философы древности упорно бились над вопросом, из чего же состоят вещества, которые их окружают. Впервые идею о том, что все тела живой и неживой природы состоят из мельчайших частиц — атомов — высказал древнегреческий ученый Демокрит целых 2500 лет назад!
Что же из себя представляет атом?
Атом — это мельчайшая химически неделимая частица вещества.
Атомы могут соединяться друг с другом с помощью химических связей в различной последовательности, образуя более сложные частицы — молекулы. Можно провести аналогию:
- атом — отдельный человек,
- молекулы — группы людей, объединенные общим признаком (семья, одноклассники, коллеги, любители кошек, любители собак).

Молекула — это мельчайшие частицы, которые состоят из атомов. Они являются химически делимыми.
Долгое время считалось, что атом нельзя разделить далее на составляющие. Но с развитием науки учёные-физики выяснили, что атом состоит из более мелких, или элементарных частиц — протонов (p), нейтронов (n) и электронов (ē).
В центре атома располагается ядро, которое состоит из протонов и нейтронов (их общее название нуклоны), а вокруг ядра вращаются электроны.
| Чем атом похож на Солнечную систему? Можно представить атом как Солнечную систему, где вокруг ядра (Солнца) по орбитам вращаются электроны (планеты). Это так называемая планетарная модель атома. В реальности атом намного сложнее, но для запоминания нам удобнее пользоваться этими представлениями. |
Тогда более точно определение атома будет звучать так:
Атом — электронейтральная химически неделимая частица, которая состоит из положительно заряженного ядра и вращающихся вокруг него отрицательно заряженных электронов.
Каждая из элементарных частиц в атоме имеет свой заряд и массу:
Характеристика элементарных частицИз таблички видно, что вся масса атома сосредоточена в протонах и нейтронах, то есть в ядре. При этом само ядро положительно заряжено, а вокруг ядра вращаются отрицательно заряженные электроны.
В разновидностях одного и того же химического элемента может быть различное число элементарных частиц. Давай рассмотрим это на примере атома водорода.
Первый случай: ядро атома водорода состоит из одного протона (масса ядра = 1 а.е.м.). Такой атом называется протием, именно он указан в периодической системе Д.И. Менделеева.
Добавим к этому ядру один нейтрон, тогда масса ядра будет равна 2 а.е.м.. Мы получили вторую разновидность атома водорода — дейтерий.
Если добавить второй нейтрон к такому ядру, то мы получим тритий. Так вот, разновидности одного и того же химического элемента, которые различаются числом нейтронов в ядре, называются изотопами.
Так вот, разновидности одного и того же химического элемента, которые различаются числом нейтронов в ядре, называются изотопами.
| Один водород, но три лучше: что такое изотопы? Изотопы — атомы одного химического элемента с разным числом нейтронов: равные заряды ядра, равное число e и p, но разное число n! |
Сейчас мы научимся определять количество протонов, нейтронов и электронов в атоме любого химического элемента. В этом нам поможет периодическая система Д.И. Менделеева.
Давай рассмотрим ячейку в периодической системе с углеродом:
В верхней части ячейки располагается порядковый номер элемента (это целое число), под ним располагается относительная атомная масса. Она является нецелым числом, поэтому её легко определять.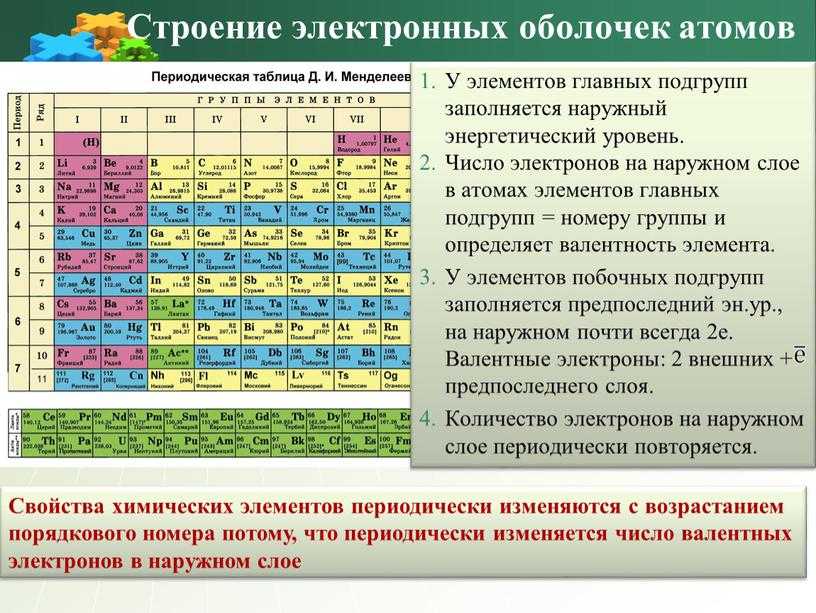 Относительная атомная масса, округленная до целого числа, называется массовым числом.
Относительная атомная масса, округленная до целого числа, называется массовым числом.
Эти характеристики связаны с количеством элементарных частиц в атоме следующим образом:
| Порядковый номер элемента = число протонов в ядре = заряд ядра атома = число электронов в атоме (№ элемента = p = Z = ē) Число нейтронов = массовое число – порядковый номер (n = Ar — № элемента) |
Давай рассмотрим основные определения и положения, связанные с характеристикой элемента и числовыми операциями:
- Орбиты, на которых располагаются электроны, называются электронными слоями (или энергетическими уровнями). Нумерация слоев начинается с ближайшего к ядру электронного слоя.
- На каждом электронном слое может находиться не более 2N2 электронов (где N — номер слоя).
- Число занятых электронами слоев в атоме элемента совпадает с номером периода, в котором он находится.
- Последний энергетический уровень называют внешним (максимальное число ē на внешнем уровне = 8). Обычно на нем находятся валентные электроны, то есть электроны на внешней (валентной) оболочке атома.
- Число валентных электронов, как правило, совпадает с номером группы, в котором находится элемент.
На примере атома углерода определим количество элементарных частиц в его атоме.
Порядковый номер углерода равен 6, значит, заряд его атома + 6, число протонов и число электронов совпадает и тоже равно 6.
Относительная атомная масса равна 12,01, а число нейтронов равно 12 – 6 = 6.
Углерод находится во втором периоде, IV группе. Это показывает нам, что занято лишь 2 электронных слоя, при этом на внешнем электронном уровне располагаются 4 электрона.
При заполнении электронами ячеек мы описываем так называемое основное состояние. Это такое состояние атома, при котором энергия системы минимальна. Его состояние можно определить как “веселое”: в атоме всё спокойно и в порядке.
Но может быть и другая ситуация, когда на электроны оказывается какое-то воздействие. Тогда происходит процесс, похожий на развод пары в человеческом мире. В результате воздействия те электроны, которые находились на орбитали вдвоем и были спаренными, могут друг с другом “поссориться” и “разъехаться” по разным орбиталям.
Тогда атом можно определить как “грустный”: электроны ссорятся, атома грустит. В химии это состояние и называется возбужденным. Такой “развод” возможен только в пределах одного энергетического уровня.
Атомные подуровни заполняются электронами в порядке увеличения их энергии. Этот порядок выглядит следующим образом:
Этот порядок выглядит следующим образом:
| 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → … |
| Как умеет скакать электрон? Иногда при заполнении энергетических подуровней мы нарушаем порядок заполнения подуровней. В первую очередь, это связано с заполнением s- и d-подуровней . Электрон перемещается с внешнего s- на предвнешний d-подуровень. Так образуется более устойчивая заполненная или полузаполненная конфигурация. |
Это явление характерно для элементов IB и VIB групп, например, Cr, Cu, Ag.
Например, у меди электронная оболочка должна выглядеть как ..3d94s2. Но так как для заполнения d-подуровня не хватает одного электрона, то более выгодной становится ситуация, когда с s-подуровня электрон “перепрыгивает” на внутренний d-подуровень.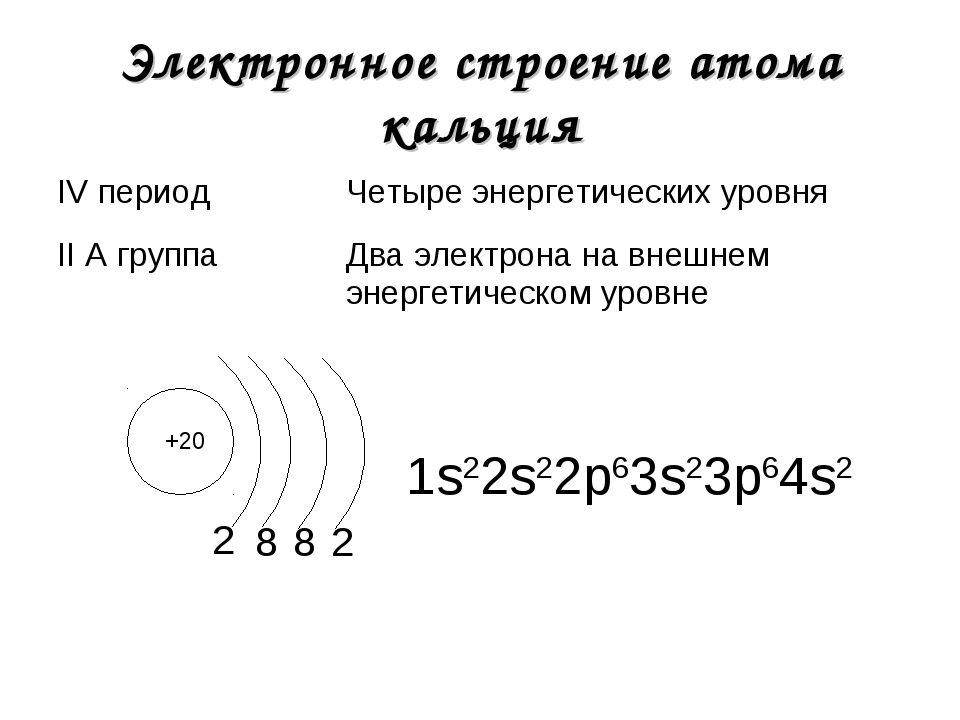 В результате, конфигурация меди выглядит как 3d104s11
В результате, конфигурация меди выглядит как 3d104s11
| Итог: иметь конфигурации nd5 и nd10 более энергетически выгодно, чем nd4 и nd9. Поэтому у таких элементов, как Cu, Cr, Ag, Au, Nb, Mo, Ru, Pt, Pd происходит проскок (провал) электрона: электрон с верхнего “этажа” как будто проваливается на нижний. |
Классификация химических элементов: s-,p-,d-,f-элементы
В зависимости от положения “последнего электрона” бывают s-, p-, d-, f-элементы:
- s-элементы: IA и IIA группы;
- p-элементы: IIIA-VIIIA группы;
- d-элементы: элементы побочных подгрупп;
- f-элементы: вынесены в отдельную группу лантаноидов и актиноидов.
У s- и p-элементов валентные электроны находятся на внешнем уровне.
У d-элементов — на внешнем s- и на предвнешнем d-подуровнях.
Далее приведены электронные формулы атомов элементов первых четырех периодов. Благодаря этой шпаргалке всегда можно сверить свой вариант электронной конфигурации и проверить себя.
Продолжение темы читайте в статье «Строение атома и электронные конфигурации 2.0».
Фактчек- Атом — электронейтральная частица, состоящая из ядра и вращающихся вокруг него электронов.
- Электроны располагаются на электронных подуровнях, причем их число определяется порядковым номером элемента.
- Существует группа атомов одного и того же химического элемента, у которых имеется разное число нейтронов. Такие элементы называют изотопами.
- Электроны располагаются по ячейкам так, чтобы энергия системы была минимальна.
- Иногда для достижения минимума энергии некоторые правила нарушаются — таковым является проскок электрона.

Задание 1.
Ядро атома состоит из:
- Протонов и нейтронов
- Протонов и электронов
- Нейтронов и электронов
- Протонов, нейтронов и электронов
Задание 2.
У изотопов различается число:
- Протонов
- Нейтронов
- Электронов
- Нейтронов и электронов
Задание 3.
Проскок электрона характерен для элемента:
- Натрия
- Алюминия
- Ксенона
- Меди
Задание 4.
На третьем электронном слое может находиться максимально:
- 8 электронов
- 18 электронов
- 2 электрона
- 32 электрона
Ответы: 1. — 1; 2. — 2; 3. — 4; 4. — 2.
основные теории и модели, кратко о составе частиц, электронный заряд
Химия
12.11.21
11 мин.
В школьном курсе химии и физики изучается теория строения атома. Кратко описать структуру внутреннего устройства веществ помогает периодический закон Д. И. Менделеева в современной трактовке. Изменения свойств элементов и их соединений напрямую зависят от строения составляющих их частиц.
Кратко описать структуру внутреннего устройства веществ помогает периодический закон Д. И. Менделеева в современной трактовке. Изменения свойств элементов и их соединений напрямую зависят от строения составляющих их частиц.
Оглавление:
- Как устроен атом
- Исторические модели
- Строение электронных оболочек
- Примеры описания
- Современные направления исследований
Как устроен атом
Слово ἄτоμоς на древнегреческом языке означает «неделимый, неразрезаемый». Так с древних времен называли наименьшую частицу вещества. Атом состоит из ядра и электронов. Эту систему можно сравнить с Солнцем и планетами. Большую часть массы составляет ядро (более чем 99.9%). Оно состоит из протонов — положительно заряженных частиц, и нейтронов, которые не имеют заряда. Оболочку ядра составляют электроны, которые практически не имеют веса. Эти частицы заряжены отрицательно.
Устройство ядра
Протоны, нейтроны и электроны — 3 главные составляющие атома. Количество этих частиц для каждого элемента можно найти в периодической таблице Д. И. Менделеева. Численность протонов и электронов равна порядковому номеру в системе. Это определяет его принадлежность к определенному веществу. Число нейтронов равно разности относительной атомной массы и порядкового номера. Это количество может варьироваться от нуля до нескольких десятков:
- Протоны — элементарные частицы, обладающие положительным зарядом и имеющие массу 1,675 * 10 (в степени -24) г. Они участвуют в образовании ядра и принимают участие в термоядерных реакциях.
- Нейтроны — электронейтральные (не имеющие заряда) частицы ядра атома с массой равной 1,673 * 10 (в степени -24) г. Они входят в состав центральной части.
- Электроны — отрицательно заряженные частицы, расположенные на энергетических уровнях вокруг ядра. Они образуют электронную оболочку атома.

Основные свойства
Каждый химический элемент состоит из атомов, имеющих определенный заряд ядра (количество протонов). Однако часто встречаются разновидности, которые, будучи одинаково заряженными, имеют разную атомную массу. Такие вещества называют изотопами, они определены и известны для каждого элемента. Это понятие происходит от греческого isos — «равный», topos — «место», так как они занимают одно и то же положение в периодической системе, поэтому атомные массы в периодической таблице являются средним значением всех изотопов определенного вида атомов.
Из этого важного факта следует, что самой важной отличительной чертой химического элемента является заряд ядра и количество протонов и электронов. Атомные массы не могут быть основной характеристикой, поскольку они подвержены изменениям. Численность нейтронов (n) в каждом изотопе разная, именно поэтому появляется разница в весе.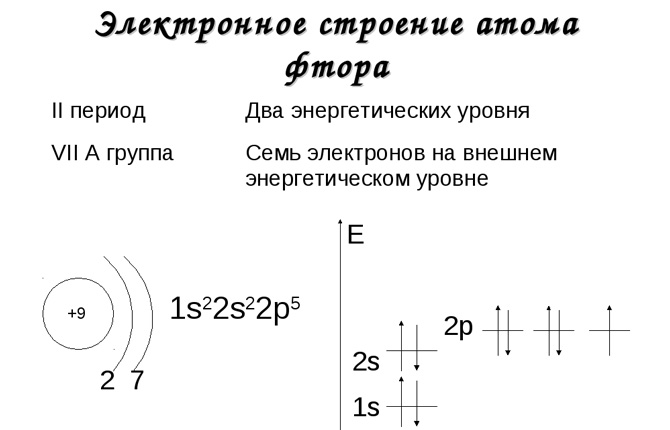
Некоторые атомы обладают свойством непроизвольно излучать невидимые глазу частицы. Это явление называется радиоактивностью и проявляется у нестабильных изотопов, когда радиус ядра больше длины действия сильных взаимодействий.
Исторические модели
В течение долгого времени ученые пытались наглядно представить, как могут выглядеть атомы. Чтобы доказать верность модели, необходимо выдвинуть теорию, обосновать ее и подтвердить экспериментами. Ученый выдвигает предположения, что должно происходить, если его идея верна. Если в ходе эксперимента эти прогнозы подтверждаются, теорию можно считать правильной. По мере поступлений новых сведений об устройстве веществ, представления науки меняются:
- В 1904 году Дж. Томсон предложил свою модель атома — «Пудинг с изюмом». Теория предполагала, что внутри положительно заряженного тела находились отрицательные электроны. Необычное название происходит от сходства частиц с изюмом в традиционном английском пудинге по их произвольному расположению в нем.
 Позже Резерфорд опроверг эту модель.
Позже Резерфорд опроверг эту модель. - Почти одновременно с Томсоном разработал свою идею японский физик Нагаока. Он построил раннюю планетарную модель атома (она имела сходство с планетой Сатурн). По схеме кольца, состоящие из электронов, вращались вокруг ядра с положительным зарядом. Позже было доказано, что теория неверна.
- В 1911 году Э. Резерфорд после многих опытов пришел к выводу, что атом по своему строению напоминает планетарную систему, так как электроны перемещаются вокруг ядра по осям, подобно планетам.
Парадокс заключался в том, что, несмотря на опытные доказательства, модель противоречила правилам классической науки. По законам обычной механики электроны должны были бы падать на ядро вследствие потери энергии. После этого датский физик Нильс Бор доказал, что они удерживаются на «орбите» ядра за счет его положительного заряда. Электроны не излучают энергию.
Таким образом, люди выяснили, что внутри атомов действуют совсем другие законы природы.
Это послужило началом новой отрасли науки — квантовой механики, правила которой отличаются от классической. А планетарная теория получила название модель Бора-Резерфорда.
Строение электронных оболочек
Электроны, вращаясь вокруг ядра, расположены на определенных уровнях, отдаленно напоминающим орбиты, по которым планеты вращаются вокруг Солнца. Сходство это чисто условное, так как большую часть времени эти частицы летают по непредсказуемым траекториям. Но все-таки хаотичное движение электронов происходит внутри определенной области, которую ученые называют орбиталь. Количество их у разных элементов разное. Число орбиталей для какого-то определенного элемента совпадает с номером периода, в котором он расположен в периодической таблице.
Также установлено максимальное количество заряженных частиц на определённых электрических уровнях. На первом (самом близком к ядру) слое могут находиться максимум 2 электрона, во втором — 8, в третьем — 18, в четвертом — 32. Максимальное число отрицательно заряженных частиц можно определить по формуле 2 (n*n), где n — номер энергетического уровня.
Максимальное число отрицательно заряженных частиц можно определить по формуле 2 (n*n), где n — номер энергетического уровня.
Слой, в котором находиться максимальное для него количество электронов, называется завершенным электронным уровнем.
С таким представлением об электронной оболочке связано свойство валентности. По определению, термин означает способность атомов вступать в химические связи с другими элементами. Это происходит за счет незаполненных мест электронных оболочек. Электроны способны отрываться и улетать, подобно кометам в космосе. Атомов всегда стремятся заполнить эти пустоты за счет свободных электронов других веществ. Таким образом происходит процесс химических связей и образования новых соединений.
Примеры описания
Атом водорода (H) имеет в периодической системе Д. И. Менделеева порядковый номер 1, соответственно, заряд ядра равен +1, элемент имеет один энергетический слой, в котором движется 1 электрон (e). Так как на первом s-уровне могут находиться 2 e, а у H он только 1, значит, здесь незавершенный электронный уровень.
Так как на первом s-уровне могут находиться 2 e, а у H он только 1, значит, здесь незавершенный электронный уровень.
Следующий элемент в периоде под номером 1 — гелий (He), следовательно он имеет заряд ядра +2, один электронный уровень, но с двумя отрицательно заряженными частицами и энергетический уровень завершен.
Современные направления исследований
В настоящее время ученые работают на субатомном уровне, то есть изучают частицы, которые во много раз меньше атомов. К ним относятся кварки, фотоны, глюоны. Эти, казалось бы, совсем незаметные частицы способны выделять огромную энергию. Свойства их еще практически не исследованы. Ученые ставят сложнейшие опыты, сталкивая частицы друг с другом в огромных установках-ускорителях.
СТРОЕНИЕ АтОмА реферат по химии | Сочинения Химия
Скачай СТРОЕНИЕ АтОмА реферат по химии и еще Сочинения в формате PDF Химия только на Docsity! Министерство общего и профессионального образования
Российской Федерации
Управление Образования Администрации Аксайского района
Вечерняя общеобразовательная школа
РЕФЕРАГ
н
на тему «СТРОЕНИЕАТОМА»
н
сн
нс м:
нс сн
“7. 7
Выполнила: |Попова Ольга Сергеевна
Проверила:
Аксай 2007 г. Содержание: Введение………………………………………………………….. стр. 3 Основные законы и понятия химии ……………………………. стр. 4 Ядерная модель строения атома………………………………… стр. 8 Атом Резерфорда…………………………………………………. стр. 8 Модель атома Бор-Резерфорд……………………………………. стр. 10 Модель кристалла………………………………………………. стр.11 Характеристика поведения электронов в атомах………………. стр. 14 Представление о содержащихся в веществах электрических частицах…………………………………………………………… стр. 15 Свойства электрона………………………………………………. стр. 16 Общие принципы заполнения электронных оболочек атомов элементов по периодам…………………………………………… стр. 16 Ядра атомов……………………………………………………… стр. 17 Протон и нейтрон………………………………………………… стр. 18 Строение атомных ядер…………………………………………. стр. 18 Атомная орбиталь………………………………………………… стр. 18 Заключение……………………………………………………….. стр. 18 Список использованной литературы……………………………. стр. 20 Основные законы и понятия химии. Закон сохранения массы. Исключительное значение для химии имело 0 0 1 Fустановление закона сохранения массы, являющегося след ствием 0 0 1 Fвсеобщего естественного закона сохранения материи и дви жения, сформулированного М.
7
Выполнила: |Попова Ольга Сергеевна
Проверила:
Аксай 2007 г. Содержание: Введение………………………………………………………….. стр. 3 Основные законы и понятия химии ……………………………. стр. 4 Ядерная модель строения атома………………………………… стр. 8 Атом Резерфорда…………………………………………………. стр. 8 Модель атома Бор-Резерфорд……………………………………. стр. 10 Модель кристалла………………………………………………. стр.11 Характеристика поведения электронов в атомах………………. стр. 14 Представление о содержащихся в веществах электрических частицах…………………………………………………………… стр. 15 Свойства электрона………………………………………………. стр. 16 Общие принципы заполнения электронных оболочек атомов элементов по периодам…………………………………………… стр. 16 Ядра атомов……………………………………………………… стр. 17 Протон и нейтрон………………………………………………… стр. 18 Строение атомных ядер…………………………………………. стр. 18 Атомная орбиталь………………………………………………… стр. 18 Заключение……………………………………………………….. стр. 18 Список использованной литературы……………………………. стр. 20 Основные законы и понятия химии. Закон сохранения массы. Исключительное значение для химии имело 0 0 1 Fустановление закона сохранения массы, являющегося след ствием 0 0 1 Fвсеобщего естественного закона сохранения материи и дви жения, сформулированного М. В.Ломоносовым (1711-1765 гг.) как всеобщий естественный закон в 1748 г. в письме к Д. Эйлеру: “Все перемены, в натуре случающиеся, такого суть состояния, что, сколько чего у одного тела отнимется, столько присовокупится к другому, ежели, где убудет несколько материи, то умножится в другом месте… Сей всеобщий закон простирается и в самые пра 0 01 Fвила движения; ибо тело, движущее своей силой другое, столько же он у себя теряет, сколько сообщает другому, которое от него движе ние получает.” Это положение, высказанное в виде философской концепции. М. В. Ломоносов подтвердил экспериментально в 1756 г., повторив опыты Р. Боиля по прокаливанию металлов в запаянных стеклянных сосудах (ретортах). Русс кий ученый установил, что если сосуд, содержащий металл, взвесить до и после прокаливания, не вскрывая его, то масса остается без изменений. При нагревании же металла во вскрытой реторте масса увеличивается за счет его с оединения с воздухом, проникающим в сосуд. Аналогичных выводы на основе экспериментом по прокаливанию м еталлов сделал в 1777 г.
В.Ломоносовым (1711-1765 гг.) как всеобщий естественный закон в 1748 г. в письме к Д. Эйлеру: “Все перемены, в натуре случающиеся, такого суть состояния, что, сколько чего у одного тела отнимется, столько присовокупится к другому, ежели, где убудет несколько материи, то умножится в другом месте… Сей всеобщий закон простирается и в самые пра 0 01 Fвила движения; ибо тело, движущее своей силой другое, столько же он у себя теряет, сколько сообщает другому, которое от него движе ние получает.” Это положение, высказанное в виде философской концепции. М. В. Ломоносов подтвердил экспериментально в 1756 г., повторив опыты Р. Боиля по прокаливанию металлов в запаянных стеклянных сосудах (ретортах). Русс кий ученый установил, что если сосуд, содержащий металл, взвесить до и после прокаливания, не вскрывая его, то масса остается без изменений. При нагревании же металла во вскрытой реторте масса увеличивается за счет его с оединения с воздухом, проникающим в сосуд. Аналогичных выводы на основе экспериментом по прокаливанию м еталлов сделал в 1777 г. и А. Лавуазье (1743-1794 гг.), который (после открыт ия и 1774 г. Д. Пристли кислорода) уже знал качественный и количественный состав воздуха. Например, оксид углерода (IV) можно получить по любой и 0 01 Fз ука занных ниже реакций: С+О2=СО2; 2СО+02=2С02; СаСОз=С02+СаО В химически чистом образце этого оксида всегда содержится 27,29% С и 72,71% 0 01 F О. Отклонение от указанного состава свидетель ствует о присутствии примесей. Утверждение, обратное закону о постоянстве состава 0 0 1 Fвеществ: каждому определенному составу отве чает только одно химическое соединение, неверно. Действительно, диметиловый эфир и этиловый спирт имеют одинаковый химический состав – С2НбО, но отличаются друг от друга структурой молекул, т. е. порядком соединения в них атомов (изомеры). Закон эквивалентов. Химические элементы соединяются друг с другом в строго определенных количествах, соответствующих их эквивалентам (В. Рихтер, 1792-1794 гг.). Понятие эквивалента введено в химию для 0 0 1 Fсопоставления соединительной способности раз личных элементов.
и А. Лавуазье (1743-1794 гг.), который (после открыт ия и 1774 г. Д. Пристли кислорода) уже знал качественный и количественный состав воздуха. Например, оксид углерода (IV) можно получить по любой и 0 01 Fз ука занных ниже реакций: С+О2=СО2; 2СО+02=2С02; СаСОз=С02+СаО В химически чистом образце этого оксида всегда содержится 27,29% С и 72,71% 0 01 F О. Отклонение от указанного состава свидетель ствует о присутствии примесей. Утверждение, обратное закону о постоянстве состава 0 0 1 Fвеществ: каждому определенному составу отве чает только одно химическое соединение, неверно. Действительно, диметиловый эфир и этиловый спирт имеют одинаковый химический состав – С2НбО, но отличаются друг от друга структурой молекул, т. е. порядком соединения в них атомов (изомеры). Закон эквивалентов. Химические элементы соединяются друг с другом в строго определенных количествах, соответствующих их эквивалентам (В. Рихтер, 1792-1794 гг.). Понятие эквивалента введено в химию для 0 0 1 Fсопоставления соединительной способности раз личных элементов.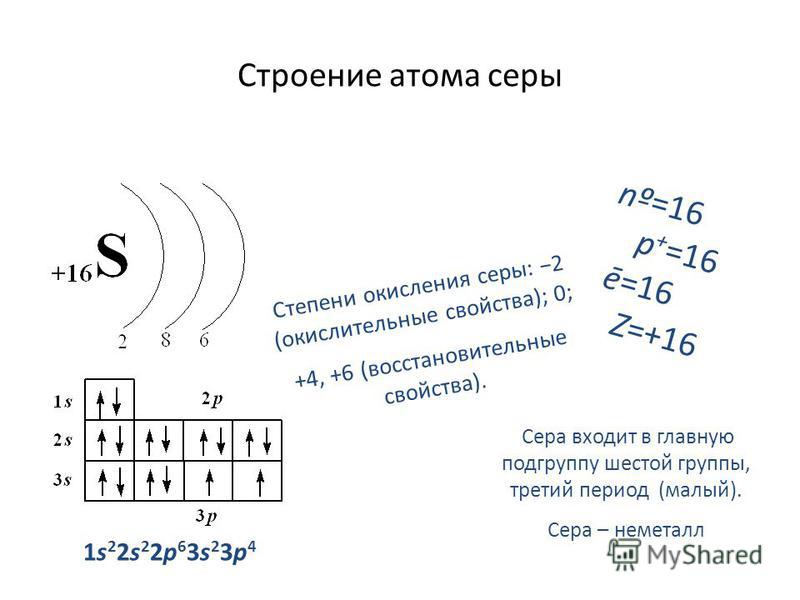 Эквивалентом химического элемента называют такую его массу, которая соединяется с 1,008 ч. м. 0 01 F (части массы) во дорода или 8 ч. м. кислорода или з 0 0 1 Fамещает эти массы в соедине ниях* Отметим, что один и тот же элемент может иметь не один, а 0 01 Fне сколько эквивалентов. Так, эквивалент углерода в оксиде углерода (IV) равен трем, а в оксиде углерода (II) – шести. 0 0 1 FПонятие эквивалента можно распространить и на сложные соеди нения типа кислот, солей и оснований. Эквивалентом сложного соединения называют массу этого 0 0 1 Fсоеди нения, содержащую эквивалент водорода (кислоты) или эквивалент металлической составной части (основания, соли). 0 0 1 FВ общем виде закон эквивалентов можно сформулировать следую щим образом: Во всех химических реакциях взаимодействие различных веществ друг 0 0 1 Fс другом происходит в соответствии с их эквивалентами, неза висимо от того, являются ли эти вещества простыми или сложными. Закон кратных отношений. Если два элемента образуют друг с Другом несколько химических соединений, то на одну и ту же массу одного из них приходятся такие массы другого, которые относятся между собой как простые целые числа (Д.
Эквивалентом химического элемента называют такую его массу, которая соединяется с 1,008 ч. м. 0 01 F (части массы) во дорода или 8 ч. м. кислорода или з 0 0 1 Fамещает эти массы в соедине ниях* Отметим, что один и тот же элемент может иметь не один, а 0 01 Fне сколько эквивалентов. Так, эквивалент углерода в оксиде углерода (IV) равен трем, а в оксиде углерода (II) – шести. 0 0 1 FПонятие эквивалента можно распространить и на сложные соеди нения типа кислот, солей и оснований. Эквивалентом сложного соединения называют массу этого 0 0 1 Fсоеди нения, содержащую эквивалент водорода (кислоты) или эквивалент металлической составной части (основания, соли). 0 0 1 FВ общем виде закон эквивалентов можно сформулировать следую щим образом: Во всех химических реакциях взаимодействие различных веществ друг 0 0 1 Fс другом происходит в соответствии с их эквивалентами, неза висимо от того, являются ли эти вещества простыми или сложными. Закон кратных отношений. Если два элемента образуют друг с Другом несколько химических соединений, то на одну и ту же массу одного из них приходятся такие массы другого, которые относятся между собой как простые целые числа (Д. Дальтон, 1803 г.). Д. Дальтон (1776-1844 гг.) в дальнейшем, используя 0 4 3 E 0 4 4 2 0 4 3 A 0 4 4 0 0 4 4 B тый им закол кратных отношений, закон эквивалентов и закон 0 0 1 Fпосто янства состава, создал новую версию атомистической теории, основан ную на количественных соотношениях, возникающих при 0 0 1 Fвзаимодей ствии между химическими элементами. Нетрудно убедиться, что закон кратных отношений представляет собой дальнейшее развитие закона эквивалентов, 0 4 3 E 0 4 4 1 0 4 3 D 0 4 3 E 0 4 3 2 0 4 3 0 0 4 3 D 0 4 3 D 0 4 3 E 0 4 3 5 0 4 3 D 0 4 3 0 0 4 3 F 0 4 3 E 0 4 4 1 ледовательном анализе рядов химических соединений, образующихся при взаимодействии друг с другом двух 0 4 3 B 0 4 4 E 0 4 3 1 0 4 4 B 0 4 4 5 0 4 4 5 0 4 3 8 0 4 3 C 0 4 3 8 0 4 4 7 0 4 3 5 0 4 4 1 0 4 3 A 0 4 3 8 0 4 4 5 0 4 4 D 0 4 3 B 0 4 3 5 0 4 3 C 0 4 3 5 0 4 3 D тов. В простейшем случае указанный ряд может состоять из двух соединений. Например, при вз аимодействии углерода и кислорода: образуются два соединения: оксид углерода (II) и оксид углерода- (IV).
Дальтон, 1803 г.). Д. Дальтон (1776-1844 гг.) в дальнейшем, используя 0 4 3 E 0 4 4 2 0 4 3 A 0 4 4 0 0 4 4 B тый им закол кратных отношений, закон эквивалентов и закон 0 0 1 Fпосто янства состава, создал новую версию атомистической теории, основан ную на количественных соотношениях, возникающих при 0 0 1 Fвзаимодей ствии между химическими элементами. Нетрудно убедиться, что закон кратных отношений представляет собой дальнейшее развитие закона эквивалентов, 0 4 3 E 0 4 4 1 0 4 3 D 0 4 3 E 0 4 3 2 0 4 3 0 0 4 3 D 0 4 3 D 0 4 3 E 0 4 3 5 0 4 3 D 0 4 3 0 0 4 3 F 0 4 3 E 0 4 4 1 ледовательном анализе рядов химических соединений, образующихся при взаимодействии друг с другом двух 0 4 3 B 0 4 4 E 0 4 3 1 0 4 4 B 0 4 4 5 0 4 4 5 0 4 3 8 0 4 3 C 0 4 3 8 0 4 4 7 0 4 3 5 0 4 4 1 0 4 3 A 0 4 3 8 0 4 4 5 0 4 4 D 0 4 3 B 0 4 3 5 0 4 3 C 0 4 3 5 0 4 3 D тов. В простейшем случае указанный ряд может состоять из двух соединений. Например, при вз аимодействии углерода и кислорода: образуются два соединения: оксид углерода (II) и оксид углерода- (IV).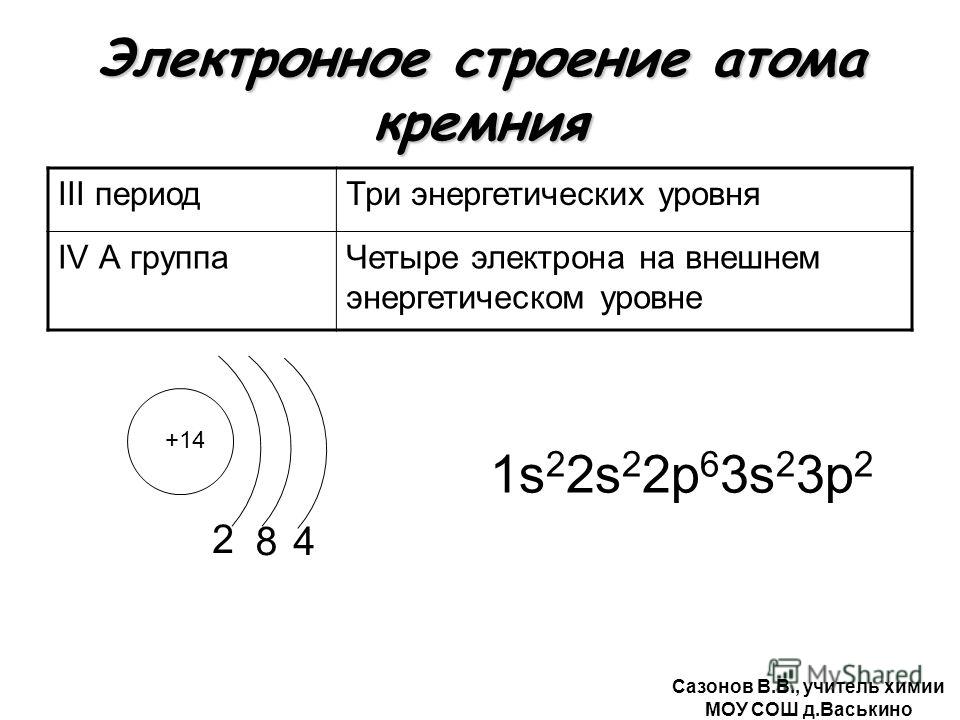 Доказательство постоянства состава для самых разнообразных хими ческих соединении уже являлось само по себе свидетельством в пользу дискретного строения материи. Применение же закона постоянства состава для анализа любого из указанных рядов показывает, что существование дв 0 0 1 Fух (или нескольких) соединений, обра зующихся при взаимодействии любой пары химических элементов, возможно лишь в том случае, когда состав соединений буде 0 01 Fт отли чаться один от другого на целые атомы. Естественно, что эти разли 0 01 Fчия в составе химических соединений ряда, впрочем, как и сами основные законы химии, справедливы лишь при условии, что материя действительно состоит из мельчайших неделимых частиц. Выдвигая новую версию атомистической теории, опирающуюся на основные химические законы, и отдавая дань 0 01 F уважения древнегре ческим философам- атомистам, Д. 0 01 F Дальтон сохранил предложен ное ими название для мельчайших неделимых частиц материи – атом. И наконец, использование закона постоянства состава и закона кратных отношений позволило Д.
Доказательство постоянства состава для самых разнообразных хими ческих соединении уже являлось само по себе свидетельством в пользу дискретного строения материи. Применение же закона постоянства состава для анализа любого из указанных рядов показывает, что существование дв 0 0 1 Fух (или нескольких) соединений, обра зующихся при взаимодействии любой пары химических элементов, возможно лишь в том случае, когда состав соединений буде 0 01 Fт отли чаться один от другого на целые атомы. Естественно, что эти разли 0 01 Fчия в составе химических соединений ряда, впрочем, как и сами основные законы химии, справедливы лишь при условии, что материя действительно состоит из мельчайших неделимых частиц. Выдвигая новую версию атомистической теории, опирающуюся на основные химические законы, и отдавая дань 0 01 F уважения древнегре ческим философам- атомистам, Д. 0 01 F Дальтон сохранил предложен ное ими название для мельчайших неделимых частиц материи – атом. И наконец, использование закона постоянства состава и закона кратных отношений позволило Д. Дальтону установить значения относительных атомных масс элементов, принимая за единичную – массу атома водорода. Так, том Дальтона, обладающий конкретным материальным 0 01 Fсвой ством – атомной массой, из отвлеченной модели превратился в 0 01 Fконк ретное химическое понятие. С введением в химию понятия “атомная масса” наука переходит на более высокую ступень своего развития. 0 0 1 FВместе с тем атомистика Дальтона еще не свободна от недос татков: в ней нет места молекулам, а существуют только “сложные атомы ”. Закон объемных отношений и закон Авогадро. 0 01 F Объемы вступаю щих в 0 0 1 Fреакцию газов относятся друг к другу, а также к объему полу чающихся газообразных продуктов как простые целые числа (Ж. Гей-Люссак, 1805 г.). 0 0 1 FЭтот закон находится в серьезном про тиворечии с выводами атомистики Дальтона. Для объяснения наблюдавшихся Ж. Гей-Люссаком 0 01 F законо мерностей соединения газов оказалось необходимым предположить следующее: 1) любые газы (в том числе и простые) состоят не из атомов, а из молекул; 2) 0 01 F в равных объемах различных газов при одинаковых темпера туре и давлении содержится одинаковое число молекул.
Дальтону установить значения относительных атомных масс элементов, принимая за единичную – массу атома водорода. Так, том Дальтона, обладающий конкретным материальным 0 01 Fсвой ством – атомной массой, из отвлеченной модели превратился в 0 01 Fконк ретное химическое понятие. С введением в химию понятия “атомная масса” наука переходит на более высокую ступень своего развития. 0 0 1 FВместе с тем атомистика Дальтона еще не свободна от недос татков: в ней нет места молекулам, а существуют только “сложные атомы ”. Закон объемных отношений и закон Авогадро. 0 01 F Объемы вступаю щих в 0 0 1 Fреакцию газов относятся друг к другу, а также к объему полу чающихся газообразных продуктов как простые целые числа (Ж. Гей-Люссак, 1805 г.). 0 0 1 FЭтот закон находится в серьезном про тиворечии с выводами атомистики Дальтона. Для объяснения наблюдавшихся Ж. Гей-Люссаком 0 01 F законо мерностей соединения газов оказалось необходимым предположить следующее: 1) любые газы (в том числе и простые) состоят не из атомов, а из молекул; 2) 0 01 F в равных объемах различных газов при одинаковых темпера туре и давлении содержится одинаковое число молекул. Последнее утверждение, высказанное итальянским ученым А. А во га дров 1811 г., вошло в химию под именем закона Авогадро. Однако в начале 19 в. 0 0 1 Fэти воззрения не получили должно го признания: даже крупные химики того времени Д. Дальтон и И. Берцелиус отрицали возможность существования молекул, состоящих из нескольких одинаковых атомов. Прошло еще полвека, прежде чем на 1 Международном съезде химиков, состоявшемся в Карлсруэ (Германия) в сентябре 1860 г., были окончате 0 01 Fльно приня ты основные 0 0 1 Fхимические представления (понятия об атомах и моле кулах), зародившиеся в виде философского учения в Древней Греции (Левкипп, Демокрит, Эпикур), 0 0 1 Fвпервые развитые в виде на учной концепции Д. Дальтоном, подтвержденные опытами Ж. Пруста, Ж. Гей-Люссака и окончательно 0 0 1 Fсформулирован ные в трудах А. Авогадро и его ученика С.Канниццаро. Таким образом, основные положения атомно-молекулярного учения можно сформулировать следующим образом: Все вещества состоят из атомов. Атомы каждого вида одинаковы между собой, но отличаются от атомов любого другого вида.
Последнее утверждение, высказанное итальянским ученым А. А во га дров 1811 г., вошло в химию под именем закона Авогадро. Однако в начале 19 в. 0 0 1 Fэти воззрения не получили должно го признания: даже крупные химики того времени Д. Дальтон и И. Берцелиус отрицали возможность существования молекул, состоящих из нескольких одинаковых атомов. Прошло еще полвека, прежде чем на 1 Международном съезде химиков, состоявшемся в Карлсруэ (Германия) в сентябре 1860 г., были окончате 0 01 Fльно приня ты основные 0 0 1 Fхимические представления (понятия об атомах и моле кулах), зародившиеся в виде философского учения в Древней Греции (Левкипп, Демокрит, Эпикур), 0 0 1 Fвпервые развитые в виде на учной концепции Д. Дальтоном, подтвержденные опытами Ж. Пруста, Ж. Гей-Люссака и окончательно 0 0 1 Fсформулирован ные в трудах А. Авогадро и его ученика С.Канниццаро. Таким образом, основные положения атомно-молекулярного учения можно сформулировать следующим образом: Все вещества состоят из атомов. Атомы каждого вида одинаковы между собой, но отличаются от атомов любого другого вида. каждой частицы равнялась 0,00055 углеродной частицы. Заряд равняется 1,602 на 10 в минус 19 степени. Особенно замечательно, что масса частиц и величина их заряда не зависит ни от природы газа, остающегося в трубке, ни от вещества из которого сделаны электроды, ни от прочих условий опыта. Кроме того, катодные частицы известны только в заряженном состоянии и не могут существовать без своих зарядов, не могут быть превращены в электронейтральные частицы: электрический заряд составляет, самую сущность их природы. Эти частицы получили название электронов. В катодных трубках электроны отделяются от катода под влиянием электрического заряда. Но они могут возникать и вне всякой связи с электрическим зарядом. Так, например при электронной эмиссии металлы испускают электроны; при фотоэффекте многие вещества также выбрасывают электроны. Выделение электронов самыми разнообразными веществами указывает на то, что эти частицы входят в состав всех атомов; следовательно атомы являются сложными образованиями, построенными из более мелких «составных частей».
каждой частицы равнялась 0,00055 углеродной частицы. Заряд равняется 1,602 на 10 в минус 19 степени. Особенно замечательно, что масса частиц и величина их заряда не зависит ни от природы газа, остающегося в трубке, ни от вещества из которого сделаны электроды, ни от прочих условий опыта. Кроме того, катодные частицы известны только в заряженном состоянии и не могут существовать без своих зарядов, не могут быть превращены в электронейтральные частицы: электрический заряд составляет, самую сущность их природы. Эти частицы получили название электронов. В катодных трубках электроны отделяются от катода под влиянием электрического заряда. Но они могут возникать и вне всякой связи с электрическим зарядом. Так, например при электронной эмиссии металлы испускают электроны; при фотоэффекте многие вещества также выбрасывают электроны. Выделение электронов самыми разнообразными веществами указывает на то, что эти частицы входят в состав всех атомов; следовательно атомы являются сложными образованиями, построенными из более мелких «составных частей». Изучение строения атома практически началось в 1897-1898 гг., после того как была окончательно установлена природа катодных лучей как потока электронов и были определены величина заряда и масса электрона. Факт выделения электронов самыми разнообразными веществами приводил к выводу, что электроны входят в состав всех атомов. Но атом, как известно, электрически нейтрален, из этого следовало, что в его состав должна была входить ещё одна составная часть, уравновешивавшая сумму отрицательных зарядов электронов. Эта положительно заряженная часть атома была открыта в 1911 г. Резерфордом при исследовании движения α – частиц в газах и других веществах. α – частицы, выбрасываемые веществами активных элементов представляют собой положительно заряженные ионы гелия, скорость движения которых достигает 20000 км/сек. Благодаря такой огромной скорости α -частицы, пролетая через воздух и сталкиваясь с молекулами газов, выбивают из них электроны. Молекулы, потерявшие электроны, становятся заряженными положительно, выбитые же электроны тотчас присоединяются к другим молекулам, заряжая их отрицательно.
Изучение строения атома практически началось в 1897-1898 гг., после того как была окончательно установлена природа катодных лучей как потока электронов и были определены величина заряда и масса электрона. Факт выделения электронов самыми разнообразными веществами приводил к выводу, что электроны входят в состав всех атомов. Но атом, как известно, электрически нейтрален, из этого следовало, что в его состав должна была входить ещё одна составная часть, уравновешивавшая сумму отрицательных зарядов электронов. Эта положительно заряженная часть атома была открыта в 1911 г. Резерфордом при исследовании движения α – частиц в газах и других веществах. α – частицы, выбрасываемые веществами активных элементов представляют собой положительно заряженные ионы гелия, скорость движения которых достигает 20000 км/сек. Благодаря такой огромной скорости α -частицы, пролетая через воздух и сталкиваясь с молекулами газов, выбивают из них электроны. Молекулы, потерявшие электроны, становятся заряженными положительно, выбитые же электроны тотчас присоединяются к другим молекулам, заряжая их отрицательно.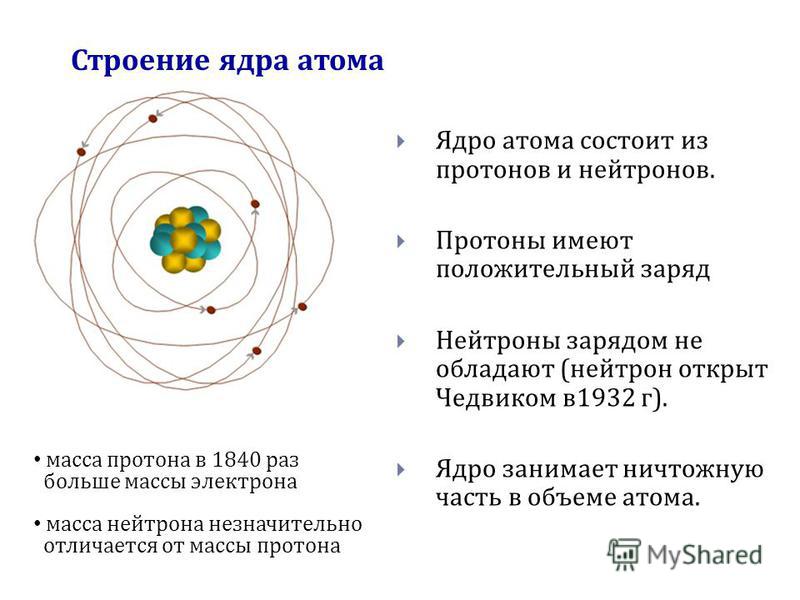 Таким образом, в воздухе на пути α – частиц образуются положительно и отрицательно заряженные ионы газа. Способность α -частиц ионизировать воздух была использована английским физиком Вильсоном для того, чтобы сделать видимыми пути движения отдельных частиц и сфотографировать их. Впоследствии аппарат для фотографирования частиц получил название камеры Вильсона. (Первый трековый детектор заряженных частиц. Изобретена Ч. Вильсоном в 1912. Действие Вильсона камеры основано на конденсации пересыщенного пара (образовании мелких капелек жидкости) на ионах, возникающих вдоль следа (трека) заряженной частицы. В дальнейшем вытеснена другими трековыми детекторами.) Исследуя пути движения частиц с помощью камеры, Резерфорд заметил, что в камере они параллельны (пути), а при пропускании пучка параллельных лучей через слой газа или тонкую металлическую пластинку, они выходят не параллельно, а несколько расходятся, т.е. происходит отклонение частиц от их первоначального пути. Некоторые частицы отклонялись очень сильно, некоторые вообще не проходили через тонкую пластинку.
Таким образом, в воздухе на пути α – частиц образуются положительно и отрицательно заряженные ионы газа. Способность α -частиц ионизировать воздух была использована английским физиком Вильсоном для того, чтобы сделать видимыми пути движения отдельных частиц и сфотографировать их. Впоследствии аппарат для фотографирования частиц получил название камеры Вильсона. (Первый трековый детектор заряженных частиц. Изобретена Ч. Вильсоном в 1912. Действие Вильсона камеры основано на конденсации пересыщенного пара (образовании мелких капелек жидкости) на ионах, возникающих вдоль следа (трека) заряженной частицы. В дальнейшем вытеснена другими трековыми детекторами.) Исследуя пути движения частиц с помощью камеры, Резерфорд заметил, что в камере они параллельны (пути), а при пропускании пучка параллельных лучей через слой газа или тонкую металлическую пластинку, они выходят не параллельно, а несколько расходятся, т.е. происходит отклонение частиц от их первоначального пути. Некоторые частицы отклонялись очень сильно, некоторые вообще не проходили через тонкую пластинку. Модель атома Бор-Резерфорд. Исходя из этих наблюдений, Резерфорд предложил свою схему строения атома: в центре атома находится положительное ядро, вокруг которого по разным орбиталям вращаются отрицательные электроны. Центростремительные силы, возникающие при их вращении удерживают их на своих орбиталях и не дают им улететь. Эта модель атома легко объясняет явление отклонения α – частиц. Размеры ядра и электронов очень малы по сравнению с размерами всего атома, которые определяются орбитами наиболее удаленных от ядра электронов; поэтому большинство α -частиц пролетает через атомы без заметного отклонения. Только в тех случаях, когда α -частицы очень близко подходит к ядру, электрическое отталкивание вызывает резкое отклонение ее от первоначального пути. Таким образом, изучение рассеяние α -частиц положило начало ядерной теории атома. Одной из задач, стоявших перед теорией строения атома в начале ее развития, было определение величины заряда ядра различных атомов. Так как атом в целом электрически нейтрален, то, определив заряд ядра, можно было бы установить и число окружающих ядро электронов.
Модель атома Бор-Резерфорд. Исходя из этих наблюдений, Резерфорд предложил свою схему строения атома: в центре атома находится положительное ядро, вокруг которого по разным орбиталям вращаются отрицательные электроны. Центростремительные силы, возникающие при их вращении удерживают их на своих орбиталях и не дают им улететь. Эта модель атома легко объясняет явление отклонения α – частиц. Размеры ядра и электронов очень малы по сравнению с размерами всего атома, которые определяются орбитами наиболее удаленных от ядра электронов; поэтому большинство α -частиц пролетает через атомы без заметного отклонения. Только в тех случаях, когда α -частицы очень близко подходит к ядру, электрическое отталкивание вызывает резкое отклонение ее от первоначального пути. Таким образом, изучение рассеяние α -частиц положило начало ядерной теории атома. Одной из задач, стоявших перед теорией строения атома в начале ее развития, было определение величины заряда ядра различных атомов. Так как атом в целом электрически нейтрален, то, определив заряд ядра, можно было бы установить и число окружающих ядро электронов. В решении этой задачи этой большую помощь оказало изучение спектров рентгеновских лучей. Рентгеновские лучи возникают при ударе быстро летящих электронов о какое-либо твердое тело и отличаются от лучей видимого света только значительно меньшей длиной волны. В то время как короткие световые волны имеют длину около 4000 ангстремов (фиолетовые лучи), длины волн рентгеновских лучей лежат в пределах от 20 до 0,1 ангстрема. Чтобы получить спектр рентгеновских лучей, нельзя пользоваться обыкновенной призмой или дифракционной решеткой. (Дифракционная РЕШЕТКА, оптический прибор; совокупность большого количества параллельных щелей в непрозрачном экране или отражающих зеркальных полосок (штрихов), равноотстоящих друг от друга, на которых происходит дифракция света. Дифракционная решетка разлагает падающий на нее пучок света в спектр, что используется в спектральных приборах. ) Для рентгеновских лучей требовалась решётка с очень большим количеством делений на один миллиметр (примерно 1млн./1мм.). Такую решётку искусственно приготовить было невозможно.
В решении этой задачи этой большую помощь оказало изучение спектров рентгеновских лучей. Рентгеновские лучи возникают при ударе быстро летящих электронов о какое-либо твердое тело и отличаются от лучей видимого света только значительно меньшей длиной волны. В то время как короткие световые волны имеют длину около 4000 ангстремов (фиолетовые лучи), длины волн рентгеновских лучей лежат в пределах от 20 до 0,1 ангстрема. Чтобы получить спектр рентгеновских лучей, нельзя пользоваться обыкновенной призмой или дифракционной решеткой. (Дифракционная РЕШЕТКА, оптический прибор; совокупность большого количества параллельных щелей в непрозрачном экране или отражающих зеркальных полосок (штрихов), равноотстоящих друг от друга, на которых происходит дифракция света. Дифракционная решетка разлагает падающий на нее пучок света в спектр, что используется в спектральных приборах. ) Для рентгеновских лучей требовалась решётка с очень большим количеством делений на один миллиметр (примерно 1млн./1мм.). Такую решётку искусственно приготовить было невозможно.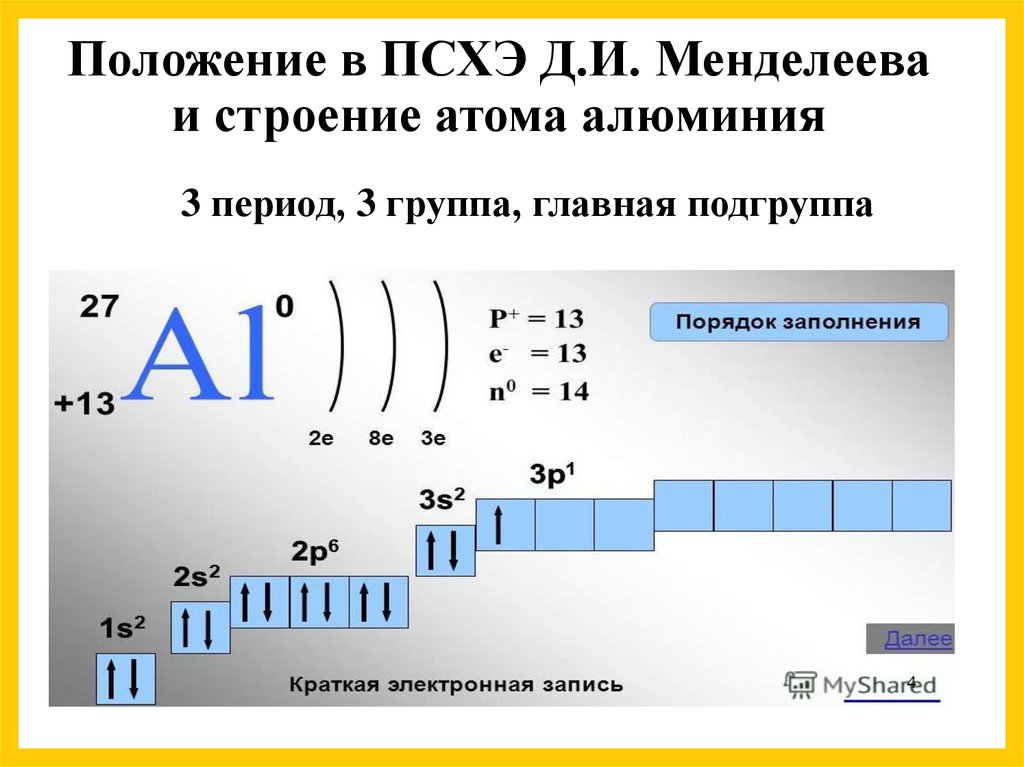 В 1912 г. у швейцарского физика Лауэ возникла мысль использовать кристаллы в качестве дифракционной решетки для рентгеновских лучей. Модель кристалла. Упорядоченное расположение атомов в кристалле и малое расстояние между ними давало повод предполагать что как раз кристаллы и подойдут на роль требуемой дифракционной решётки. Опыт блестяще подтвердил предположение Лауэ, вскоре удалось построить приборы, которые давали возможность получать спектр рентгеновских лучей почти всех элементов. Для получения рентгеновских спектров антикатод в рентгеновских трубках делают из того металла, спектр которого хотят получить, или же наносят соединение исследуемого элемента. Экраном для спектра служит фотобумага; после проявления на ней видны все линии спектра. В 1913 г. английский ученый Мозли, изучая рентгеновские спектры нашел соотношение между длинами волн рентгеновских лучей и порядкового номерами соответствующих элементов – это носит название закона Мозли и может быть сформулировано следующим образом: Корни квадратные из обратных значений длин волн находятся в линейной зависимости от порядковых номеров элементов.
В 1912 г. у швейцарского физика Лауэ возникла мысль использовать кристаллы в качестве дифракционной решетки для рентгеновских лучей. Модель кристалла. Упорядоченное расположение атомов в кристалле и малое расстояние между ними давало повод предполагать что как раз кристаллы и подойдут на роль требуемой дифракционной решётки. Опыт блестяще подтвердил предположение Лауэ, вскоре удалось построить приборы, которые давали возможность получать спектр рентгеновских лучей почти всех элементов. Для получения рентгеновских спектров антикатод в рентгеновских трубках делают из того металла, спектр которого хотят получить, или же наносят соединение исследуемого элемента. Экраном для спектра служит фотобумага; после проявления на ней видны все линии спектра. В 1913 г. английский ученый Мозли, изучая рентгеновские спектры нашел соотношение между длинами волн рентгеновских лучей и порядкового номерами соответствующих элементов – это носит название закона Мозли и может быть сформулировано следующим образом: Корни квадратные из обратных значений длин волн находятся в линейной зависимости от порядковых номеров элементов. Еще до работ Мозли некоторые учёные предполагали, что порядковый номер элемента указывает число зарядов ядра его атома. В тоже время Резерфорд, изучая рассеивание F 06 1-частиц при прохождении через тонкие металлические пластинки, выяснил, что если заряд электрона принять за единицу, то выражаемый в таких единицах заряд ядра приблизительно равен половине атомного веса элемента. Порядковый номер, по крайне мере более легких элементов, тоже равняется примерно половине атомного веса. Все вместе взятое привело к выводу, что Заряд ядра численно равен порядковому номеру элемента. Таким образом, закон Мозли позволил определить заряды атомных ядер. Тем самым, ввиду нейтральности атомов, было установлено и число электронов, вращающихся вокруг ядра в атоме каждого элемента. Модель Нильса Бора N=2n*n где n-номер слоя. Кроме того, установлено, что число электронов в наружном слое для всех элементов, кроме палладия, не превышает восьми, а в предпоследнем – восемнадцати. Электроны наружного слоя, как наиболее удаленные от ядра и, следовательно, наименее прочно связанные с ядром, могут отрываться от атома и присоединяться к другим атомам, входя в состав наружного слоя последних.
Еще до работ Мозли некоторые учёные предполагали, что порядковый номер элемента указывает число зарядов ядра его атома. В тоже время Резерфорд, изучая рассеивание F 06 1-частиц при прохождении через тонкие металлические пластинки, выяснил, что если заряд электрона принять за единицу, то выражаемый в таких единицах заряд ядра приблизительно равен половине атомного веса элемента. Порядковый номер, по крайне мере более легких элементов, тоже равняется примерно половине атомного веса. Все вместе взятое привело к выводу, что Заряд ядра численно равен порядковому номеру элемента. Таким образом, закон Мозли позволил определить заряды атомных ядер. Тем самым, ввиду нейтральности атомов, было установлено и число электронов, вращающихся вокруг ядра в атоме каждого элемента. Модель Нильса Бора N=2n*n где n-номер слоя. Кроме того, установлено, что число электронов в наружном слое для всех элементов, кроме палладия, не превышает восьми, а в предпоследнем – восемнадцати. Электроны наружного слоя, как наиболее удаленные от ядра и, следовательно, наименее прочно связанные с ядром, могут отрываться от атома и присоединяться к другим атомам, входя в состав наружного слоя последних. Атомы, лишившиеся одного или нескольких электронов, становятся заряженные положительно, так как заряд ядра атома превышает сумму зарядов оставшихся электронов. Наоборот атомы присоединившие электроны становятся заряженные отрицательно. Образующиеся таким путем заряженные частицы, качественно отличные от соответствующих атомов. называются ионами. Многие ионы в свою очередь могут терять или присоединять электроны, превращаясь при этом или в электронейтральные атомы, или в новые ионы с другим зарядом. Теория Бора оказала огромные услуги физике и химии, подойдя, с одной стороны, к раскрытию законов спектроскопии и объяснению механизма лучеиспускания, а с другой – к выяснению структуры отдельных атомов и установлению связи между ними. Однако оставалось еще много явлений в этой области, объяснить которые теория Бора не могла. Движение электронов в атомах Бор представлял как простое механическое, однако оно является сложным и своеобразным. Это своеобразие было объяснено новой квантовой теорией.
Атомы, лишившиеся одного или нескольких электронов, становятся заряженные положительно, так как заряд ядра атома превышает сумму зарядов оставшихся электронов. Наоборот атомы присоединившие электроны становятся заряженные отрицательно. Образующиеся таким путем заряженные частицы, качественно отличные от соответствующих атомов. называются ионами. Многие ионы в свою очередь могут терять или присоединять электроны, превращаясь при этом или в электронейтральные атомы, или в новые ионы с другим зарядом. Теория Бора оказала огромные услуги физике и химии, подойдя, с одной стороны, к раскрытию законов спектроскопии и объяснению механизма лучеиспускания, а с другой – к выяснению структуры отдельных атомов и установлению связи между ними. Однако оставалось еще много явлений в этой области, объяснить которые теория Бора не могла. Движение электронов в атомах Бор представлял как простое механическое, однако оно является сложным и своеобразным. Это своеобразие было объяснено новой квантовой теорией. Отсюда и пошло: «Карпускулярно- вролновой дуализм». Характеристика поведения электронов в атомах. Теория Бора оказала огромные услуги физике и химии. Однако оставалось еще много явлений в этой области, объяснить которые теория Бора не могла. Движение электронов в атомах рисовалось Бору до известной степени как простое механическое перемещение, между тем как оно является весьма сложным и своеобразным. Своеобразие движения электронов было раскрыто новой теорией – квантовой, или волновой, механикой. Квантовая механика показывает, что законы движения электронов имеют много общего с законами распространения волн. Атомы различных элементов характеризуются определенным значением заряда ядра и равным ему числом электронов, которые распределяются по энергетическим уровням. Поведение электронов в атоме характеризуется четырьмя квантовыми числами: 1) Главное квантовое число n определяет уровень энергии, которому отвечает данная орбита, и ее удаленность от ядра. Число может принимать значения ряда натуральных чисел (в реальных атомах от одного до семи).
Отсюда и пошло: «Карпускулярно- вролновой дуализм». Характеристика поведения электронов в атомах. Теория Бора оказала огромные услуги физике и химии. Однако оставалось еще много явлений в этой области, объяснить которые теория Бора не могла. Движение электронов в атомах рисовалось Бору до известной степени как простое механическое перемещение, между тем как оно является весьма сложным и своеобразным. Своеобразие движения электронов было раскрыто новой теорией – квантовой, или волновой, механикой. Квантовая механика показывает, что законы движения электронов имеют много общего с законами распространения волн. Атомы различных элементов характеризуются определенным значением заряда ядра и равным ему числом электронов, которые распределяются по энергетическим уровням. Поведение электронов в атоме характеризуется четырьмя квантовыми числами: 1) Главное квантовое число n определяет уровень энергии, которому отвечает данная орбита, и ее удаленность от ядра. Число может принимать значения ряда натуральных чисел (в реальных атомах от одного до семи).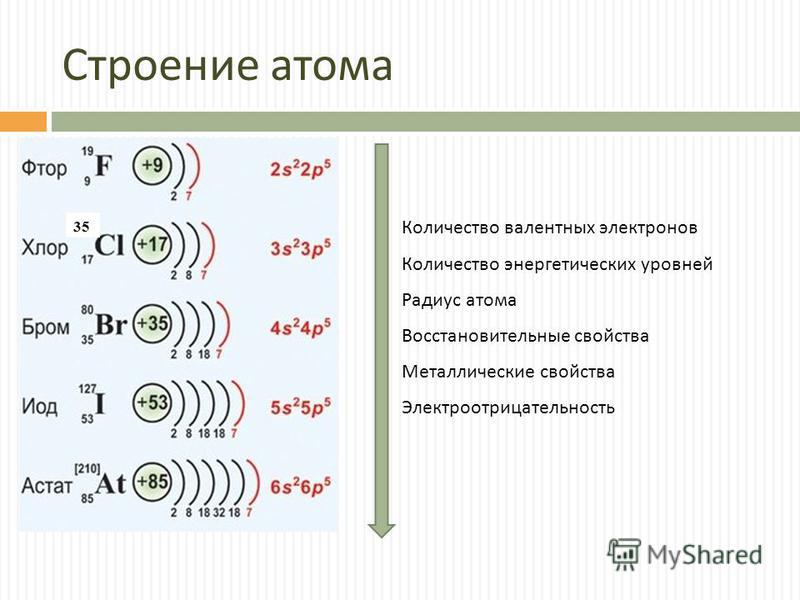 Эти числа соответствуют электронным слоям атома или его энергетическим уровням, которые обозначаются прописными буквами латинского алфавита: 1 2 3 4 5 6 7 К L M N O P Q Помимо главного квантового числа, состояние электрона в атоме характеризуется еще тремя другими квантовыми числами: l, m, s. 2) Орбитальное, побочное или азимутальное квантовое число l характеризует момент количества движения электрона относительно центра орбиты. Оно определяет форму электронного облака (форму орбиты), его сплошность или разрывы и его вытянутость. Принимает целые значения от 0 до (n-1). Для данного значения n имеется n различных орбиталей, т.е. число значений l определяет количество атомных орбиталей. Энергетические подуровни обозначаются следующим образом: 0 1 2 3 s p d f 3) Магнитное квантовое число m определяет положение плоскости орбиты электрона в пространстве или, в соответствии с представлениями волновой механики, то направление, в котором вытянуто электронное облако. Может принимать целые значения от -l до l (включая 0), всего (2*l+1) значений.
Эти числа соответствуют электронным слоям атома или его энергетическим уровням, которые обозначаются прописными буквами латинского алфавита: 1 2 3 4 5 6 7 К L M N O P Q Помимо главного квантового числа, состояние электрона в атоме характеризуется еще тремя другими квантовыми числами: l, m, s. 2) Орбитальное, побочное или азимутальное квантовое число l характеризует момент количества движения электрона относительно центра орбиты. Оно определяет форму электронного облака (форму орбиты), его сплошность или разрывы и его вытянутость. Принимает целые значения от 0 до (n-1). Для данного значения n имеется n различных орбиталей, т.е. число значений l определяет количество атомных орбиталей. Энергетические подуровни обозначаются следующим образом: 0 1 2 3 s p d f 3) Магнитное квантовое число m определяет положение плоскости орбиты электрона в пространстве или, в соответствии с представлениями волновой механики, то направление, в котором вытянуто электронное облако. Может принимать целые значения от -l до l (включая 0), всего (2*l+1) значений. Число значений m определяет число орбиталей данного (s-, p-, d-, f- типа). 4) Спиновое квантовое число s определяет направление вращения электрона, может принимать только два значения: 1/2 и -1/2. Изучению распределения электронов в атомах уделяется большое внимание, так как поведение атомов в химических реакциях в значительной мере зависит от того, насколько прочно их электроны удерживаются на своих орбиталях. Представление о содержащихся в веществах электрических частицах. Представление о содержащихся в веществах электрических частицах было высказано в качестве гипотезы английским ученым Г. Джонстоном Стонеем. Стоней знал, что вещества можно разложить электрическим током, – например, воду можно разложить таким способом на водород и кислород. Ему было известно также о работах Майкла Фарадея, установившего, что для получения некоторого количества элемента из того или иного его соединения требуется определенное количество электричества. Обдумывая эти явления, Стоней в 1874г. пришел к выводу о том, что они указывают на существование электричества в виде дискретных единичных зарядов, причем эти единичные заряды связаны с атомами.
Число значений m определяет число орбиталей данного (s-, p-, d-, f- типа). 4) Спиновое квантовое число s определяет направление вращения электрона, может принимать только два значения: 1/2 и -1/2. Изучению распределения электронов в атомах уделяется большое внимание, так как поведение атомов в химических реакциях в значительной мере зависит от того, насколько прочно их электроны удерживаются на своих орбиталях. Представление о содержащихся в веществах электрических частицах. Представление о содержащихся в веществах электрических частицах было высказано в качестве гипотезы английским ученым Г. Джонстоном Стонеем. Стоней знал, что вещества можно разложить электрическим током, – например, воду можно разложить таким способом на водород и кислород. Ему было известно также о работах Майкла Фарадея, установившего, что для получения некоторого количества элемента из того или иного его соединения требуется определенное количество электричества. Обдумывая эти явления, Стоней в 1874г. пришел к выводу о том, что они указывают на существование электричества в виде дискретных единичных зарядов, причем эти единичные заряды связаны с атомами. В 1891г. Стоней предложил название электрон для постулированной им единицы электричества. Экспериментально электрон был открыт в 1897г Дж. Дж. Томсоном (1856-1940) в Кембриджском университете. Свойства электрона. Электрон представляет собой частицу с отрицательным зарядом величиной –0,1602 10-18 Кл. Масса электрона равна 0,9108 10-30кг, что составляет 1/1873 массы атома водорода. Электрон имеет очень небольшие размеры. Радиус электрона точно не определен, но известно, что он значительно меньше 1·10-15м. В 1925г. было установлено, что электрон вращается вокруг собственной оси и что он имеет магнитный момент. Общие принципы заполнения электронных оболочек атомов элементов по периодам. Число электронов в электронейтральном атоме закономерно повышается при переходе элемента от Z к Z + 1. Эта закономерность подчиняется квантовой теории строения атома. Максимальная устойчивость атома, как системы электрических частиц, отвечает минимуму его полной энергии. Потому электроны при заполнении энергетических уровней в электромагнитном поле ядра будут занимать (застраивать) в первую очередь наиболее низкий из них (К – уровень; n=1).
В 1891г. Стоней предложил название электрон для постулированной им единицы электричества. Экспериментально электрон был открыт в 1897г Дж. Дж. Томсоном (1856-1940) в Кембриджском университете. Свойства электрона. Электрон представляет собой частицу с отрицательным зарядом величиной –0,1602 10-18 Кл. Масса электрона равна 0,9108 10-30кг, что составляет 1/1873 массы атома водорода. Электрон имеет очень небольшие размеры. Радиус электрона точно не определен, но известно, что он значительно меньше 1·10-15м. В 1925г. было установлено, что электрон вращается вокруг собственной оси и что он имеет магнитный момент. Общие принципы заполнения электронных оболочек атомов элементов по периодам. Число электронов в электронейтральном атоме закономерно повышается при переходе элемента от Z к Z + 1. Эта закономерность подчиняется квантовой теории строения атома. Максимальная устойчивость атома, как системы электрических частиц, отвечает минимуму его полной энергии. Потому электроны при заполнении энергетических уровней в электромагнитном поле ядра будут занимать (застраивать) в первую очередь наиболее низкий из них (К – уровень; n=1). В электронейтральном невозбужденном атоме электрон в этих условиях имеет наименьшую энергию (и, соответственно, наибольшую связь с ядром). Когда К – уровень будет заполнен (1s2 – состояние, характерное для атома гелия), электроны начнут застраивать уровень L (n = 2), затем M – уровень (n=3). При данном n электроны должны застраивать сначала s-, затем p-, d- и т. д. подуровни. Вначале в качестве примера рассмотрим дейтрон. Это ядро атома тяжелого водорода, или атома дейтерия. Дейтрон имеет такой же электрический заряд, как и протон, но его масса приблизительно вдвое электрический заряд, как и протон, но его масса приблизительно вдвое превышает массу протона. Полагают, что дейтрон состоит из одного протона и одного нейтрона. Ядро атома гелия, которое также называют альфа – частицей или гелионом, имеет электрический заряд, в два раза превышающий заряд протона, и массу приблизительно в четыре раза больше массы протона. Считают, что альфа- частица состоит из двух протонов и двух нейтронов. Заключение.
В электронейтральном невозбужденном атоме электрон в этих условиях имеет наименьшую энергию (и, соответственно, наибольшую связь с ядром). Когда К – уровень будет заполнен (1s2 – состояние, характерное для атома гелия), электроны начнут застраивать уровень L (n = 2), затем M – уровень (n=3). При данном n электроны должны застраивать сначала s-, затем p-, d- и т. д. подуровни. Вначале в качестве примера рассмотрим дейтрон. Это ядро атома тяжелого водорода, или атома дейтерия. Дейтрон имеет такой же электрический заряд, как и протон, но его масса приблизительно вдвое электрический заряд, как и протон, но его масса приблизительно вдвое превышает массу протона. Полагают, что дейтрон состоит из одного протона и одного нейтрона. Ядро атома гелия, которое также называют альфа – частицей или гелионом, имеет электрический заряд, в два раза превышающий заряд протона, и массу приблизительно в четыре раза больше массы протона. Считают, что альфа- частица состоит из двух протонов и двух нейтронов. Заключение. Открытия Резерфорда и Бора являются фундаментальными и имеют огромное значение для современной физики и для всего человечества. История науки учит, что всякий раз, когда человечество овладевает очередной ступенькой лестницы, ведущей в глубь вещества, это приводит к открытию нового, еще более мощного вида энергии. Горение и взрыв связаны с перестройкой молекул. Внутриатомные процессы сопровождаются выделением в миллионы раз большей энергии. Еще большее выделение энергии происходит на уровне элементарных частиц. А что будет на следующих ступенях? Открытия Резерфорда и Бора доказали, что атом не есть неделимая частица, и дают возможность современной физике ответить на этот вопрос. Список использованной литературы: Кедров Ф. Эрнест Резерфорд. М.: Атомиздат, 1965. Кульман А. Г., Общая химия- М: Наука, 1982. Некрасов Б. В., Основы общей химии-М: Химия, 1973. Полинг Л., Полинг П. Химия –М: Мир, 1978. Резерфорд Эрнест. Избранные научные труды. М., 1971.
Открытия Резерфорда и Бора являются фундаментальными и имеют огромное значение для современной физики и для всего человечества. История науки учит, что всякий раз, когда человечество овладевает очередной ступенькой лестницы, ведущей в глубь вещества, это приводит к открытию нового, еще более мощного вида энергии. Горение и взрыв связаны с перестройкой молекул. Внутриатомные процессы сопровождаются выделением в миллионы раз большей энергии. Еще большее выделение энергии происходит на уровне элементарных частиц. А что будет на следующих ступенях? Открытия Резерфорда и Бора доказали, что атом не есть неделимая частица, и дают возможность современной физике ответить на этот вопрос. Список использованной литературы: Кедров Ф. Эрнест Резерфорд. М.: Атомиздат, 1965. Кульман А. Г., Общая химия- М: Наука, 1982. Некрасов Б. В., Основы общей химии-М: Химия, 1973. Полинг Л., Полинг П. Химия –М: Мир, 1978. Резерфорд Эрнест. Избранные научные труды. М., 1971.
Атомная структура Определение и значение
- Основные определения
- Викторина
- Примеры
- Британский
Показывает уровень сложности слова.
Сохрани это слово!
Показывает уровень сложности слова.
сущ. Физика.
структура атома, теоретически состоящая из положительно заряженного ядра, окруженного и нейтрализованного отрицательно заряженными электронами, вращающимися по орбитам на различных расстояниях от ядра, строение ядра и расположение электронов различаются у различных химических элементов.
ВИКТОРИНА
Сыграем ли мы в «ДОЛЖЕН» ПРОТИВ. “ДОЛЖЕН” ВЫЗОВ?
Должны ли вы пройти этот тест на «должен» или «должен»? Это должно оказаться быстрым вызовом!
Вопрос 1 из 6
Какая форма используется для указания обязательства или обязанности кого-либо?
Происхождение атомной структуры
Впервые записано в 1895–1900 гг. , атомизм
Dictionary.com Полный текст На основе Random House Unabridged Dictionary, © Random House, Inc. 2022
Как использовать атомную структуру в предложении
«Он учится исключительно на атомной структуре, не используя никакой другой информации… и не делает никаких предположений о том, какая структура особенности могут быть важны», — говорят авторы.

Глубокое обучение решает еще одну ключевую загадку биологии: структура РНК|Веер ракушек|31 августа 2021 г.|Центр Singularity
Итак, один из ключей к созданию материалов с худшими проводниками и лучшими изоляторами — это изменение атомной структуры материала.
Худший в мире проводник может изменить правила игры в условиях климатического кризиса|Клэр Мальдарелли|23 июля 2021 г.|Popular-Science
Атомная структура графита не подходит для удержания жидкостей на месте, алмазы превращаются в графит, эти жидкости выделяются в виде газа.
Алмазы содержат остатки древней атмосферы Земли|Монро Хаммонд|20 июля 2021 г.|Popular-Science
Как химические примеси, так и атомная структура играют роль в цвете из-за того, как они изменяют спектр поглощения света минералом.
Как минералы и горные породы отражают радугу, светятся в темноте и поражают воображение|Лорен Леффер|28 июня 2021|Популярная наука
одетые модели, демонстрирующие последние достижения европейского минимализма.

Самый трагический призрак Нью-Йорка любит минималистскую шведскую моду|Нина Строхлич|8 января 2015 г.|DAILY BEAST
Черных американцев считают расой; другой — расизм как социальная структура.
Ни богов, ни копов, ни господ|Джеймс Пулос|1 января 2015|DAILY BEAST
Следуя этой цепочке рассуждений до ее логического завершения, путь к достижению мира во всем мире состоит в том, чтобы дать всем атомные бомбы.
Санта терпит неудачу еще раз|P. Дж. О’Рурк|27 декабря 2014 г.|DAILY BEAST
Это происходит не из-за плохих лидеров или поляризованной политики, а из-за того, что структура управления имеет фатальные недостатки.
Красная лента душит добрых самаритян|Филип К. Ховард|27 декабря 2014|DAILY BEAST
И структура аккордов для тех из вас, кто играет на музыкальных инструментах, неожиданна и заслуживает внимания.
Да, я люблю рождественскую музыку. Перестаньте смеяться.|Майкл Томаски|24 декабря 2014 г.
 |DAILY BEAST
|DAILY BEASTНо жилище означает особый вид строения – здание, занимаемое человеком, – место, где он живет.
Ассимиляционная память|Маркус Дуайт Ларроу (он же профессор А. Луазетта)
Здание, похожее на мечеть значительных размеров, располагалось посреди манговой рощи.
Красный год|Луи Трейси
Не успел я наступить на хрупкую конструкцию, как она внезапно и необъяснимо рухнула посередине.
The Pit Town Coronet, Volume I (из 3)|Charles James Wills
Однако в обычной работе безопаснее основывать различие на размере, чем на структуре.
Руководство по клинической диагностике|Джеймс Кэмпбелл Тодд
Они сочетают фиксацию с процессом окрашивания и по-разному окрашивают каждую нормальную и аномальную структуру в крови.
Руководство по клинической диагностике|Джеймс Кэмпбелл Тодд
Британский словарь определений атомной структуры
атомная структура
существительное
понятие атома как центрального положительно заряженного ядра, состоящего из протонов и нейтронов количество электронов. Количество электронов равно количеству протонов: таким образом, вся сущность электрически нейтральна
Количество электронов равно количеству протонов: таким образом, вся сущность электрически нейтральна
Английский словарь Коллинза – полное и полное цифровое издание 2012 г. © William Collins Sons & Co. Ltd., 1979, 1986 © HarperCollins Издатели 1998, 2000, 2003, 2005, 2006, 2007, 2009, 2012
Атомная структура и изотопы | Химия на количественном языке: основы общих химических расчетов
Фильтр поиска панели навигации Oxford AcademicChemistry in Quantitative Language: Fundamentals of General Chemistry CalculationsAnalytical ChemistryBooksJournals Термин поиска мобильного микросайта
Закрыть
Фильтр поиска панели навигации Oxford AcademicChemistry in Quantitative Language: Fundamentals of General Chemistry CalculationsAnalytical ChemistryBooksJournals Термин поиска на микросайте
Расширенный поиск
Иконка Цитировать Цитировать
Разрешения
- Делиться
- Твиттер
- Подробнее
Cite
Ориахи, Кристофер О,
‘Atomic Structure and Isotopes’
,
Chemistry in Quantitative Language: Fundamentals of General Chemistry Calculations
(
New York,
2009;
online edn,
Oxford Academic
, 12 Nov. 2020
2020
), https://doi.org/10.1093/oso/9780195367997.003.0007,
, по состоянию на 30 сентября 2022 г.
Выберите формат Выберите format.ris (Mendeley, Papers, Zotero).enw (EndNote).bibtex (BibTex).txt (Medlars, RefWorks)
Закрыть
Фильтр поиска панели навигации Oxford AcademicChemistry in Quantitative Language: Fundamentals of General Chemistry CalculationsAnalytical ChemistryBooksJournals Термин поиска мобильного микросайта
Закрыть
Фильтр поиска панели навигации Oxford AcademicChemistry in Quantitative Language: Fundamentals of General Chemistry CalculationsAnalytical ChemistryBooksJournals Термин поиска на микросайте
Advanced Search
Abstract
Джон Дальтон предложил свою теорию атома в 1808 году на основе экспериментальных данных и химических законов, известных в его время. Теория утверждает, что: 1. Все химические элементы состоят из крошечных неделимых частиц, называемых атомами. 2. Атомы не могут быть созданы или уничтожены. Химические реакции только меняют способ соединения атомов. 3. Атомы одного и того же элемента во всех отношениях одинаковы и имеют одинаковые массы и физико-химические свойства. Атомы разных элементов имеют разную массу, а также разные физические и химические свойства. 4. Соединение элементов с образованием соединения происходит между небольшими целочисленными соотношениями атомов. Теория Дальтона привела к формулировке закона сохранения массы и закона кратных пропорций. В химической реакции вещество не создается и не разрушается. Масса продуктов равна массе реагентов. Если два элемента образуют между собой более одного соединения, массы одного элемента, которые соединяются с фиксированной массой второго элемента, находятся в отношении целых чисел. Азот и кислород объединяются, образуя различные соединения, такие как NO, NO2 и N2O.
Теория утверждает, что: 1. Все химические элементы состоят из крошечных неделимых частиц, называемых атомами. 2. Атомы не могут быть созданы или уничтожены. Химические реакции только меняют способ соединения атомов. 3. Атомы одного и того же элемента во всех отношениях одинаковы и имеют одинаковые массы и физико-химические свойства. Атомы разных элементов имеют разную массу, а также разные физические и химические свойства. 4. Соединение элементов с образованием соединения происходит между небольшими целочисленными соотношениями атомов. Теория Дальтона привела к формулировке закона сохранения массы и закона кратных пропорций. В химической реакции вещество не создается и не разрушается. Масса продуктов равна массе реагентов. Если два элемента образуют между собой более одного соединения, массы одного элемента, которые соединяются с фиксированной массой второго элемента, находятся в отношении целых чисел. Азот и кислород объединяются, образуя различные соединения, такие как NO, NO2 и N2O. Согласно этому закону число атомов азота к кислороду в этих соединениях должно быть простым отношением двух небольших целых чисел. Это один из основных законов стехиометрии, как мы увидим в главе 9.. Атом состоит из центрального ядра, которое содержит примерно 99,9% общей массы атома, и окружающего его облака электронов. Ядро состоит из двух видов частиц, протонов и нейтронов, которые в совокупности известны как нуклоны. Протон заряжен положительно, а нейтрон электрически нейтрален. Электроны имеют отрицательный заряд и окружают ядро «оболочками» определенных энергетических уровней. (Примечание: уровень энергии будет обсуждаться в главе 10.) В нейтральном (непрореагировавшем) атоме число электронов равно числу протонов, поэтому атом имеет нулевой заряд.
Согласно этому закону число атомов азота к кислороду в этих соединениях должно быть простым отношением двух небольших целых чисел. Это один из основных законов стехиометрии, как мы увидим в главе 9.. Атом состоит из центрального ядра, которое содержит примерно 99,9% общей массы атома, и окружающего его облака электронов. Ядро состоит из двух видов частиц, протонов и нейтронов, которые в совокупности известны как нуклоны. Протон заряжен положительно, а нейтрон электрически нейтрален. Электроны имеют отрицательный заряд и окружают ядро «оболочками» определенных энергетических уровней. (Примечание: уровень энергии будет обсуждаться в главе 10.) В нейтральном (непрореагировавшем) атоме число электронов равно числу протонов, поэтому атом имеет нулевой заряд.
Ключевые слова: атомный номер (Z), нейтрон, протон
Предмет
Аналитическая химия
В настоящее время у вас нет доступа к этой главе.
Войти
Получить помощь с доступом
Получить помощь с доступом
Доступ для учреждений
Доступ к контенту в Oxford Academic часто предоставляется посредством институциональных подписок и покупок. Если вы являетесь членом учреждения с активной учетной записью, вы можете получить доступ к контенту одним из следующих способов:
Доступ на основе IP
Как правило, доступ предоставляется через институциональную сеть к диапазону IP-адресов. Эта аутентификация происходит автоматически, и невозможно выйти из учетной записи с IP-аутентификацией.
Войдите через свое учреждение
Выберите этот вариант, чтобы получить удаленный доступ за пределами вашего учреждения. Технология Shibboleth/Open Athens используется для обеспечения единого входа между веб-сайтом вашего учебного заведения и Oxford Academic.
- Нажмите Войти через свое учреждение.
- Выберите свое учреждение из предоставленного списка, после чего вы перейдете на веб-сайт вашего учреждения для входа.
- Находясь на сайте учреждения, используйте учетные данные, предоставленные вашим учреждением. Не используйте личную учетную запись Oxford Academic.
- После успешного входа вы вернетесь в Oxford Academic.
Если вашего учреждения нет в списке или вы не можете войти на веб-сайт своего учреждения, обратитесь к своему библиотекарю или администратору.
Войти с помощью читательского билета
Введите номер своего читательского билета, чтобы войти в систему. Если вы не можете войти в систему, обратитесь к своему библиотекарю.
Члены общества
Доступ члена общества к журналу достигается одним из следующих способов:
Войти через сайт сообщества
Многие общества предлагают единый вход между веб-сайтом общества и Oxford Academic.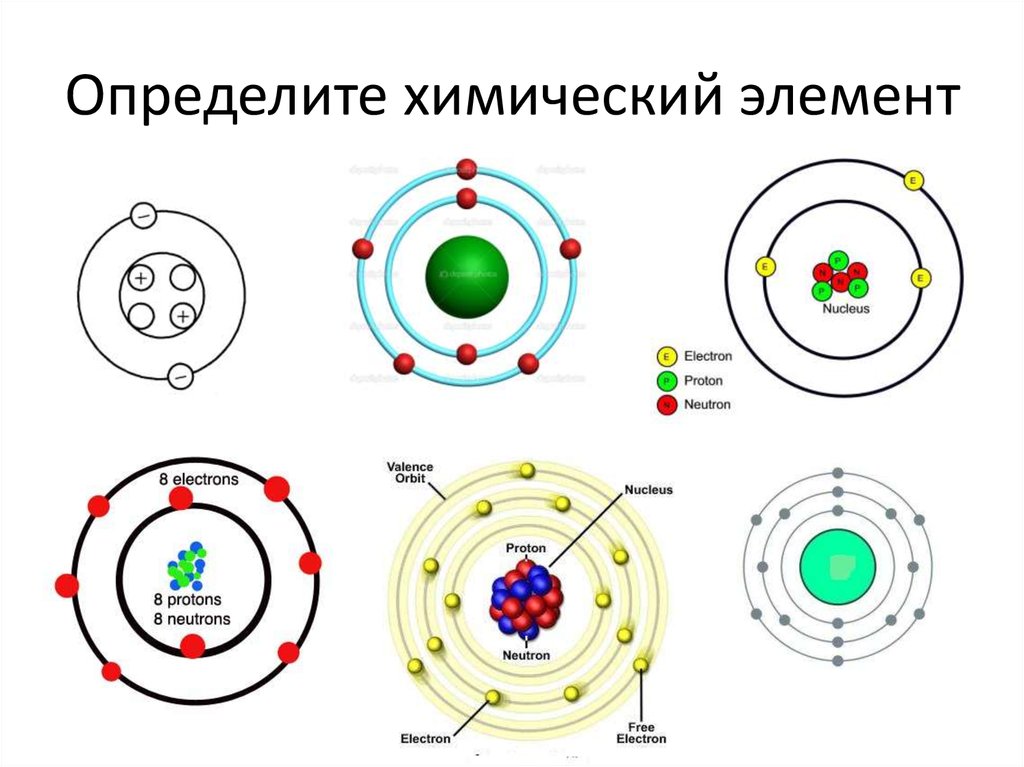 Если вы видите «Войти через сайт сообщества» на панели входа в журнале:
Если вы видите «Войти через сайт сообщества» на панели входа в журнале:
- Щелкните Войти через сайт сообщества.
- При посещении сайта общества используйте учетные данные, предоставленные этим обществом. Не используйте личную учетную запись Oxford Academic.
- После успешного входа вы вернетесь в Oxford Academic.
Если у вас нет учетной записи сообщества или вы забыли свое имя пользователя или пароль, обратитесь в свое общество.
Вход через личный кабинет
Некоторые общества используют личные аккаунты Oxford Academic для предоставления доступа своим членам. Смотри ниже.
Личный кабинет
Личную учетную запись можно использовать для получения оповещений по электронной почте, сохранения результатов поиска, покупки контента и активации подписок.
Некоторые общества используют личные аккаунты Oxford Academic для предоставления доступа своим членам.
Просмотр ваших зарегистрированных учетных записей
Щелкните значок учетной записи в правом верхнем углу, чтобы:
- Просмотр вашей личной учетной записи и доступ к функциям управления учетной записью.
- Просмотр институциональных учетных записей, предоставляющих доступ.
Выполнен вход, но нет доступа к содержимому
Oxford Academic предлагает широкий ассортимент продукции. Подписка учреждения может не распространяться на контент, к которому вы пытаетесь получить доступ. Если вы считаете, что у вас должен быть доступ к этому контенту, обратитесь к своему библиотекарю.
Ведение счетов организаций
Для библиотекарей и администраторов ваша личная учетная запись также предоставляет доступ к управлению институциональной учетной записью. Здесь вы найдете параметры для просмотра и активации подписок, управления институциональными настройками и параметрами доступа, доступа к статистике использования и т.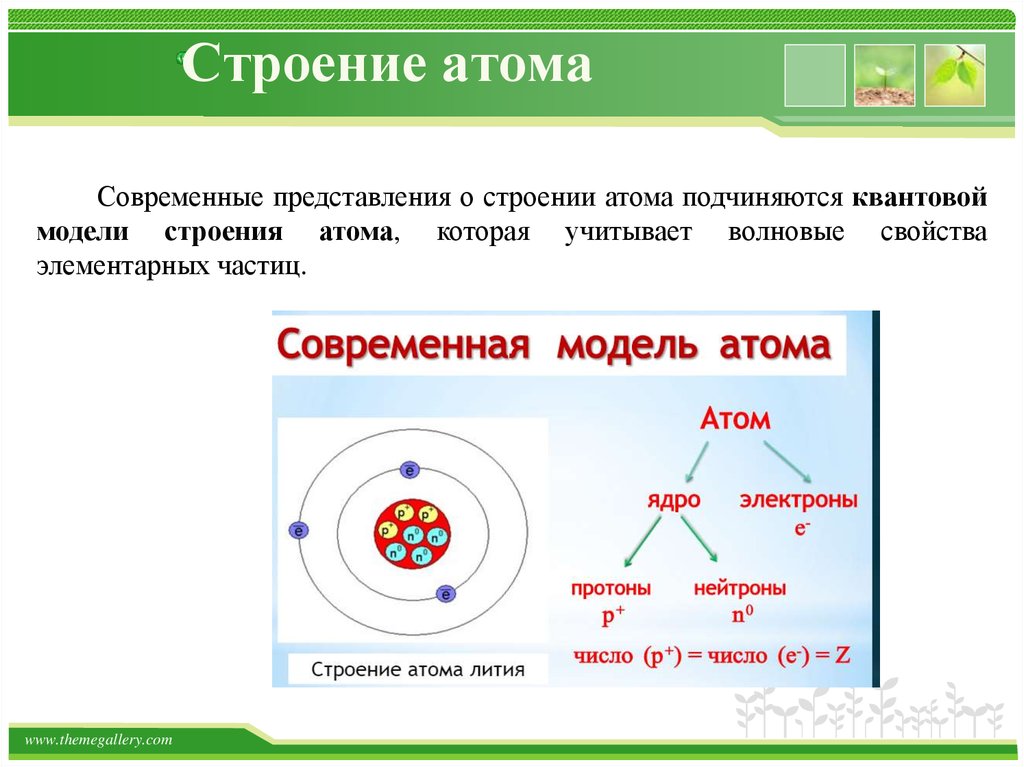 д.
д.
Покупка
Наши книги можно приобрести по подписке или приобрести в библиотеках и учреждениях.
Информация о покупке
Atomic Structure — Beautiful Chemistry
От атомной теории к квантовой механике
Атомная теория существует уже давно. Однако с момента создания древнегреческими философами в V веке до нашей эры и до возрождения такими учеными, как Бойль и Ньютон в эпоху Возрождения, атомная теория казалась более актуальной для философии и физики, но не очень полезной для объяснения химических свойств материи.
В начале 19 века теория химических элементов Лавуазье и закон постоянной пропорции химических соединений Пруста легли в основу теории атома Дальтона. В 1803 году Дальтон ясно описал свою теорию в своей записной книжке: 1) Химические элементы состоят из очень маленьких неделимых атомов. 2) Все атомы элемента одинаковы, атомы разных элементов различны, и разница заключается в весе атома. 3) Соотношения различных атомов в соединениях представляют собой простые числовые соотношения, такие как 1 : 2 или 2 : 3. Теория Дальтона дала четкое микроскопическое объяснение закону постоянной пропорции Пруста, и она была быстро принята химиками. Позже, с развитием аналитической химии, были определены все атомные массы и химические формулы соединений.
3) Соотношения различных атомов в соединениях представляют собой простые числовые соотношения, такие как 1 : 2 или 2 : 3. Теория Дальтона дала четкое микроскопическое объяснение закону постоянной пропорции Пруста, и она была быстро принята химиками. Позже, с развитием аналитической химии, были определены все атомные массы и химические формулы соединений.
Открытие электрона в конце 19 века аннулировало неделимость атома Дальтона. В начале 20 века было предложено множество моделей внутреннего строения атома. В 1913 году Бор представил революционный квантовый атом, основанный на модели ядра Резерфорда и квантовой теории Планка. С помощью модели Бора спектр излучения атомарного водорода можно прекрасно объяснить с помощью очень простых математических уравнений. Модель Бора была триумфом квантовой теории в начале 20 века. Позднее создание квантовой механики полностью изменило наше представление об атомном мире. Сегодня ученые продолжают исследования строения атома. Физики-ядерщики работают над такими проблемами, как расположение протонов и нейтронов внутри ядра и каков предельный размер ядра.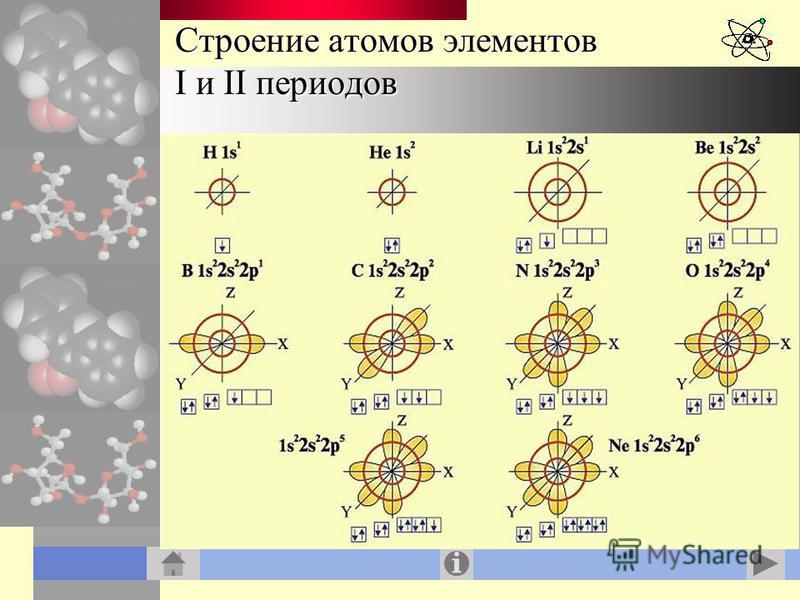 Теперь мы знаем, что протоны и нейтроны состоят из еще более мелких основных частиц (кварков). Проводя высокоэнергетические эксперименты в великолепных ускорителях частиц, физики частиц теперь ищут основные частицы материи и излучения (такие как видимый свет), чтобы ответить на главный вопрос: откуда берется материя?
Теперь мы знаем, что протоны и нейтроны состоят из еще более мелких основных частиц (кварков). Проводя высокоэнергетические эксперименты в великолепных ускорителях частиц, физики частиц теперь ищут основные частицы материи и излучения (такие как видимый свет), чтобы ответить на главный вопрос: откуда берется материя?
Верхняя диаграмма: волна де Бройля.
Теория атома Дальтона. Греческие философы впервые представили примитивную атомистическую теорию в V веке до нашей эры. После эпохи Возрождения ученые, такие как Бойль и Гук, снова взялись за атомистическую теорию или п-что и использовали ее для объяснения природных явлений. Дальтон впервые подробно изложил свою атомную теорию в 1803 году. Два основных отличия его теории от предыдущих: 1) разные элементы состоят из разных атомов, 2) разные атомы имеют разный вес. В начале 1919 веке теория Дальтона получила широкое признание среди химиков, что способствовало развитию химии на теоретическом уровне. В своей книге «Новая система химической философии », опубликованной в 1808 году, Дальтон разработал круговой символ для каждого элемента, известного в его время, и использовал комбинацию этих символов для обозначения соединений (выше). Поскольку было трудно определить точные атомные массы, атомные отношения Дальтона для многих соединений были неверными. Здесь мы показываем только несколько его составных представлений с правильным соотношением атомов. [Ссылка на рисунок: Далтон, Дж. Новая система химической философии (1808 г.)].
Поскольку было трудно определить точные атомные массы, атомные отношения Дальтона для многих соединений были неверными. Здесь мы показываем только несколько его составных представлений с правильным соотношением атомов. [Ссылка на рисунок: Далтон, Дж. Новая система химической философии (1808 г.)].
Ранние модели строения атома. Атомы Дальтона представляют собой неделимые твердые сферы. Однако с тех пор, как Томсон открыл электрон в 1897 году, новые экспериментальные данные заставили ученых понять, что атомы могут иметь сложную внутреннюю структуру. В начале 20 века появилось много атомных моделей. Четыре из них представлены на рисунке выше, причем красный и синий цвета обозначают положительные и отрицательные заряды соответственно. Модель динамида, предложенная Ленардом в 1903 атом представляет собой пустую оболочку с динамидами в центре. Динамид состоит из одного положительного заряда и одного отрицательного заряда, соединенных вместе. Модель Сатурна, предложенная Хантаро Нагуока в 1904 году, атом похож на Сатурн, с электронами, вращающимися вокруг положительно заряженной сферы в центре. В модели сливового пудинга, предложенной Дж. Дж. Томсоном в 1904 г., атом состоит из положительно заряженной оболочки и электронов, встроенных в оболочку. В модели ядра, предложенной Резерфордом в 1911 году, атом состоит из положительно заряженного ядра в центре и электронов, движущихся вокруг него. Ядро очень маленькое, но содержит почти всю массу атома. [Ссылка на рисунок: Ихде, А. Дж. Развитие современной химии (1964)]
В модели сливового пудинга, предложенной Дж. Дж. Томсоном в 1904 г., атом состоит из положительно заряженной оболочки и электронов, встроенных в оболочку. В модели ядра, предложенной Резерфордом в 1911 году, атом состоит из положительно заряженного ядра в центре и электронов, движущихся вокруг него. Ядро очень маленькое, но содержит почти всю массу атома. [Ссылка на рисунок: Ихде, А. Дж. Развитие современной химии (1964)]
Квантовый атом Бора. В 1913 году Бор предложил новую квантовую модель атома, которая была одной из самых революционных теоретических моделей в истории науки. Квантовый атом Бора похож на микроскопическую солнечную систему с серией электронных орбиталей, вращающихся вокруг положительно заряженного ядра в центре. Каждая орбиталь характеризуется определенной энергией, причем орбитали с более низкой энергией ближе к ядру, а орбитали с более высокой энергией дальше от ядра. Электрон должен принадлежать определенной орбитали с такой же энергией, что и орбиталь.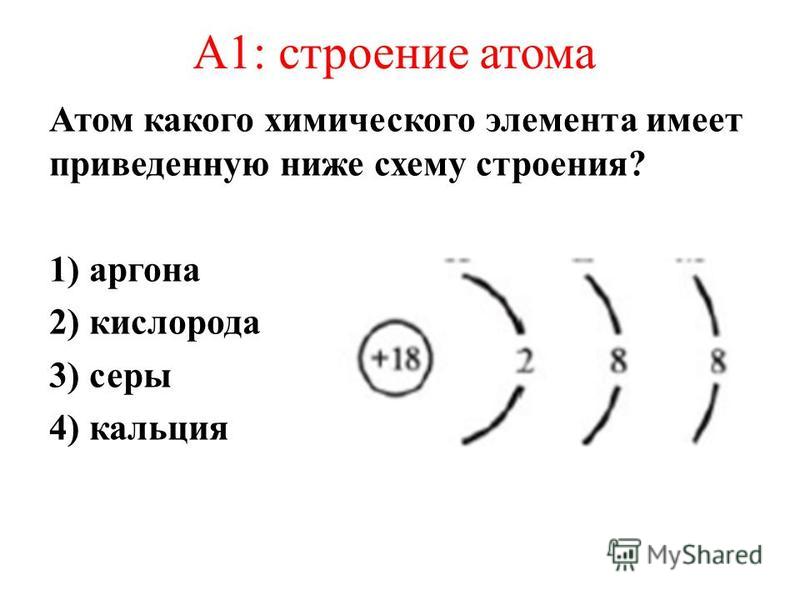 Электрон может переходить с одной орбитали на другую только в том случае, если он поглощает (с низкоэнергетической орбитали на высокоэнергетическую) или испускает (с высокоэнергетической орбитали на низкоэнергетическую) фотон и энергия фотона равна разность энергий двух орбиталей. Модель Бора дала прекрасное объяснение атомному спектру водорода (выше мы показали соответствующий электронный переход серий спектра водорода Лаймана, Бальмера и Пашена) и заложила основу для теории химической связи Льюиса. В 1922 декабря Бор был удостоен Нобелевской премии по физике за вклад в квантовую модель атома. [Ссылка на рисунок: Бор, Н. Фил. Маг. 26, 1 (1913)]
Электрон может переходить с одной орбитали на другую только в том случае, если он поглощает (с низкоэнергетической орбитали на высокоэнергетическую) или испускает (с высокоэнергетической орбитали на низкоэнергетическую) фотон и энергия фотона равна разность энергий двух орбиталей. Модель Бора дала прекрасное объяснение атомному спектру водорода (выше мы показали соответствующий электронный переход серий спектра водорода Лаймана, Бальмера и Пашена) и заложила основу для теории химической связи Льюиса. В 1922 декабря Бор был удостоен Нобелевской премии по физике за вклад в квантовую модель атома. [Ссылка на рисунок: Бор, Н. Фил. Маг. 26, 1 (1913)]
Атомные орбитали квантовой механики. Хотя квантовая модель Бора успешно объяснила некоторые свойства атомов водорода и других одноэлектронных ионов, таких как ион He, она была очень ограничена для многоэлектронных атомов. В 1920—30 де Бройль, В. Гейзенберг, И. Шрёдингер и другие физики создали квантовую механику, ставшую фундаментальной теорией для понимания атомного и молекулярного мира. В квантовой механике атомная орбиталь интерпретируется как возможность нахождения электрона вокруг ядра, которую можно рассчитать с помощью элегантного уравнения Шредингера. Чтобы сделать эти абстрактные математические понятия более интуитивными, химики обычно используют графику для представления атомных орбиталей. Для указанных выше орбиталей 3D-поверхности выбираются на основе изоповерхностей, внутри которых вероятность появления электрона равна 90%. (Ссылка на рисунок: трехмерные модели атомных орбит доктора С. Иммеля из Дармштадтского университета прикладных наук и технологий)
В квантовой механике атомная орбиталь интерпретируется как возможность нахождения электрона вокруг ядра, которую можно рассчитать с помощью элегантного уравнения Шредингера. Чтобы сделать эти абстрактные математические понятия более интуитивными, химики обычно используют графику для представления атомных орбиталей. Для указанных выше орбиталей 3D-поверхности выбираются на основе изоповерхностей, внутри которых вероятность появления электрона равна 90%. (Ссылка на рисунок: трехмерные модели атомных орбит доктора С. Иммеля из Дармштадтского университета прикладных наук и технологий)
Другие темы
Химические символы
Атомная структура
Химические связки
Кристаллическая структура
Органическая молекулярная структура
Полимеры
Биомакромолекулы
Наночастицы
Углеродная наноструктура
Структура поверхности
Классные ресурсы | План подразделения атомной структуры
ПЛАН УРОКА по атомным спектрам, модели атома, изотопам, атомной теории, субатомным частицам, спектру излучения, электронам, орбиталям, ионам, планам единиц.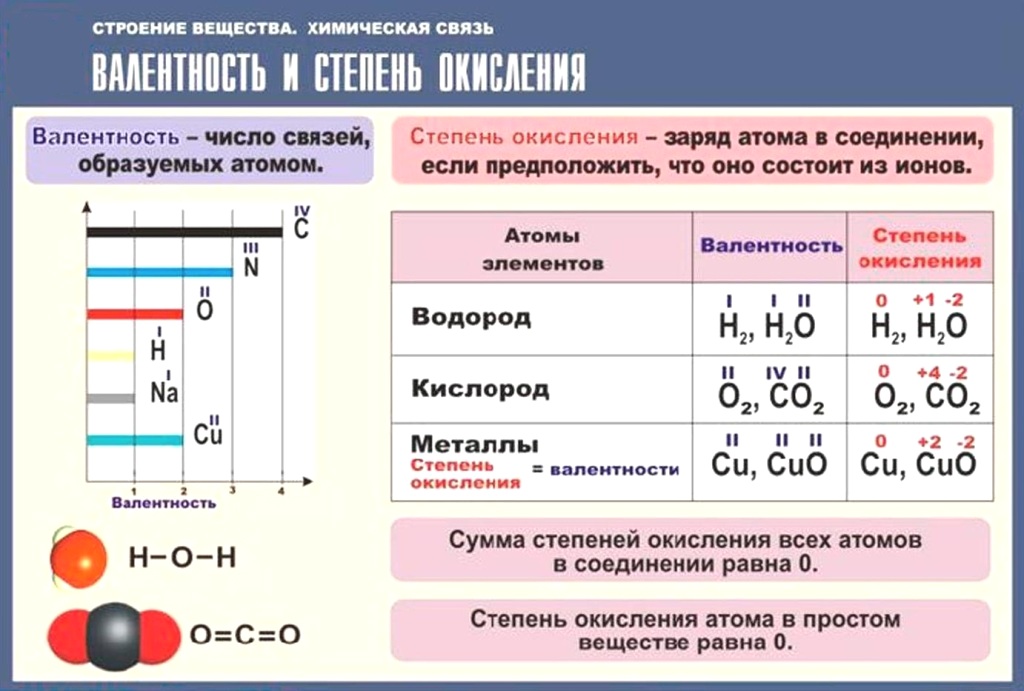 Последнее обновление: 10 мая 2021 г.
Последнее обновление: 10 мая 2021 г.
Резюме
В библиотеке ресурсов AACT для занятий в средней школе есть все, что вам нужно для составления учебного плана для вашего класса: уроки, занятия, лабораторные работы, проекты, видео, модели и анимации. Мы создали модульный план, используя ресурсы AACT, который предназначен для обучения ваших студентов атомарной структуре.
Класс
Средняя школа
Цели
К концу этого раздела учащиеся должны уметь
- Объясните конкретные вклады Демокрита, Аристотеля, Джона Дальтона, Дж.Дж. Томсон, Эрнест Резерфорд, Нильс Бор, Эдвин Шредингер, Альберт Эйнштейн и Вернер Гейзенберг.
- Понимать прошлые и современные теории строения атома.
- Используйте количество протонов, нейтронов и электронов в элементе, чтобы предсказать идентичность атома.
- Вычислите атомную массу.
- Рассчитать атомный номер.
- Понять значение иона .

- Рассчитайте молярную массу вещества.
- Рассчитайте количество молей соединения в данной массе.
- Рассчитайте количество молекул соединения в заданной массе.
- Поймите концепцию крота.
- Преобразование данных массы элемента или соединения в значения молей, атомов или молекул.
- Объясните, как была определена атомная масса элемента в таблице Менделеева.
- Дайте определение изотопа .
- Точно рассчитайте среднюю атомную массу элемента, зная атомную массу каждого изотопа и его распространенность.
- Объясните значение средневзвешенного значения и вычислить его.
- Определите, какие субатомные частицы влияют на атомную массу атома.
- Определите атомную массу по смеси изотопов.
- Обсудите массовое число по отношению к протонам и нейтронам атома.
- Понять закон сохранения материи.
- Визуализируйте, как орбитали накладываются друг на друга внутри атома.

- Объясните смысл сохранения энергии.
- Опишите, что когда к атому добавляется энергия, его электрон(ы) могут временно переходить в возбужденное состояние. Энергия излучается, когда атом возвращается в свое основное состояние.
- Поймите, что энергия квантуется.
- Используйте испытания пламенем, чтобы идентифицировать металл или металлическую соль по цвету, который они производят, когда их помещают в пламя.
- Рассчитайте частоту света, зная его длину волны.
- Рассчитайте длину волны света, зная его частоту.
- Определите неизвестный металл по цвету, который он излучает при прохождении через пламя.
Темы по химии
Этот модуль помогает учащимся понять
- Атомная структура
- Атомная теория
- Модель атома
- Субатомные частицы
- Атомная масса
- Атомный номер
- Изотопы
- Орбиты
- Электроны
- Атомные спектры
- Электромагнитный спектр
- Количественная химия
- Концепция крота
- Молярная масса
- Кроты
- Измерение
- Размерный анализ
- История химии
- Химические реакции
- Уравновешивание химических уравнений
- Закон сохранения материи
- Закон сохранения энергии
- Серия действий
Время
Подготовка учителя : См.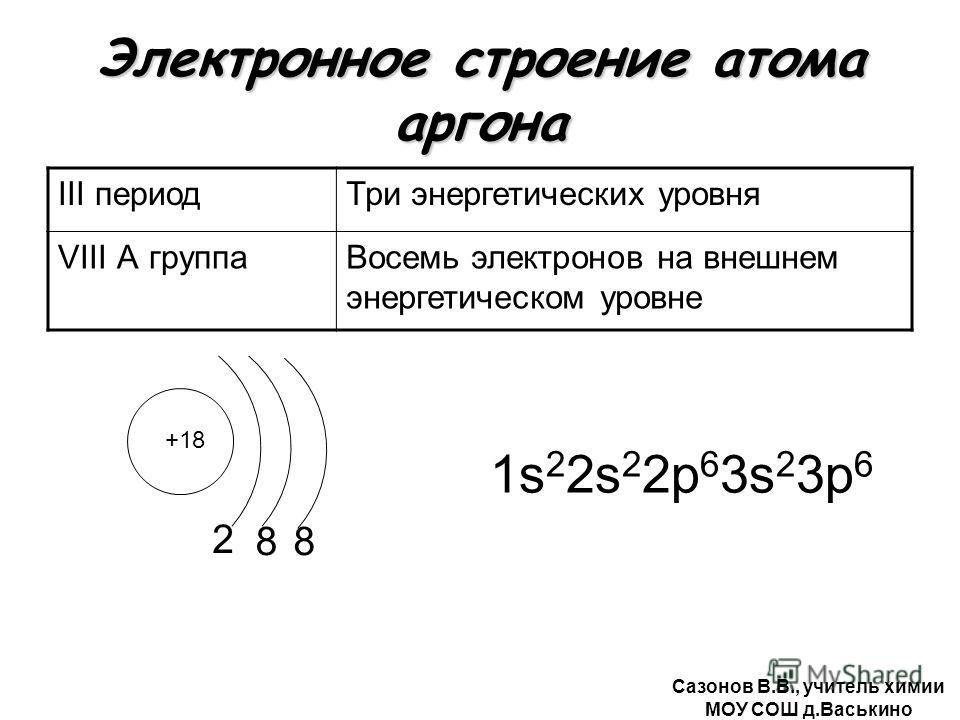 отдельные ресурсы.
отдельные ресурсы.
Урок : 7-10 академических часов, в зависимости от уровня класса.
Материалы
- См. список материалов, прилагаемый к каждому отдельному виду деятельности.
Безопасность
- См. инструкции по технике безопасности для каждого отдельного действия.
Заметки учителя
- Действия, показанные ниже, перечислены в том порядке, в котором они должны быть выполнены.
- Заметки учителя, раздаточные материалы для учащихся и дополнительные материалы доступны на странице для каждого отдельного занятия.
- Обратите внимание, что большинство этих ресурсов предоставляются участникам AACT.
Атомная теория:
- Серия Founders of Chemistry: расскажите о развитии атомной теории, используя один или несколько наших видеороликов Founders of Chemistry. The Ancient Chemistry Video прослеживает историю химии от открытия огня через различные эпохи металлов и, наконец, до великих философов.
 Студенты могут узнать о первоначальном исследовании Резерфордом альфа-частиц в видеоролике Эрнеста Резерфорда и услышать о том, как он выдвинул гипотезу о том, что это ядра гелия. Нильс Бор Видео рассказывает историю Нильса Бора, великого ученого, который изменил наше представление об атомах и электроне. Каждый из них включает в себя лист с заданиями, в котором есть вопросы, на которые учащиеся должны ответить во время просмотра видео.
Студенты могут узнать о первоначальном исследовании Резерфордом альфа-частиц в видеоролике Эрнеста Резерфорда и услышать о том, как он выдвинул гипотезу о том, что это ядра гелия. Нильс Бор Видео рассказывает историю Нильса Бора, великого ученого, который изменил наше представление об атомах и электроне. Каждый из них включает в себя лист с заданиями, в котором есть вопросы, на которые учащиеся должны ответить во время просмотра видео. - Ученые, стоящие за проектом атома: после просмотра видеороликов используйте этот проект, чтобы ваши ученики создали цифровую или бумажную книгу об ученых, которые внесли свой вклад в наше понимание атома. Этот проект поможет учащимся объяснить конкретный вклад нескольких ученых и понять прошлые и современные теории относительно структуры атома.
- Создание имитации атома. Кроме того, используйте эту симуляцию, чтобы ваши учащиеся манипулировали количеством протонов, нейтронов и электронов в элементе и определяли, как они влияют на массовое число, атомный номер и другие свойства атома.
 Этот урок, основанный на моделировании PhET, позволяет учащимся увидеть, как они могут использовать количество протонов, нейтронов и электронов в элементе для предсказания его идентичности.
Этот урок, основанный на моделировании PhET, позволяет учащимся увидеть, как они могут использовать количество протонов, нейтронов и электронов в элементе для предсказания его идентичности.
Концепция крота:
- Амедео Авогадро Видео: Покажите своим ученикам еще одно видео из нашей коллекции «Основатели химии», чтобы начать изучение концепции крота. В нем рассказывается история Амедео Авогадро, ученого, получившего признание за концепцию крота в результате своего исследования газов. Он также включает в себя лист с заданиями, в котором есть вопросы, на которые учащиеся должны отвечать во время просмотра видео.
- Пришло время молей: затем ваши ученики могут выполнить эту лабораторную работу, чтобы узнать, как рассчитать молярную массу вещества, количество молей соединения в заданной массе и количество молекул соединения в заданной массе. Во время лабораторной работы студенты определяют количество молей мела, использованных для написания их имени, количество молей сахарозы, проглоченной при жевании резинки, и количество молей спирта, испарившегося при использовании дезинфицирующего средства для рук.
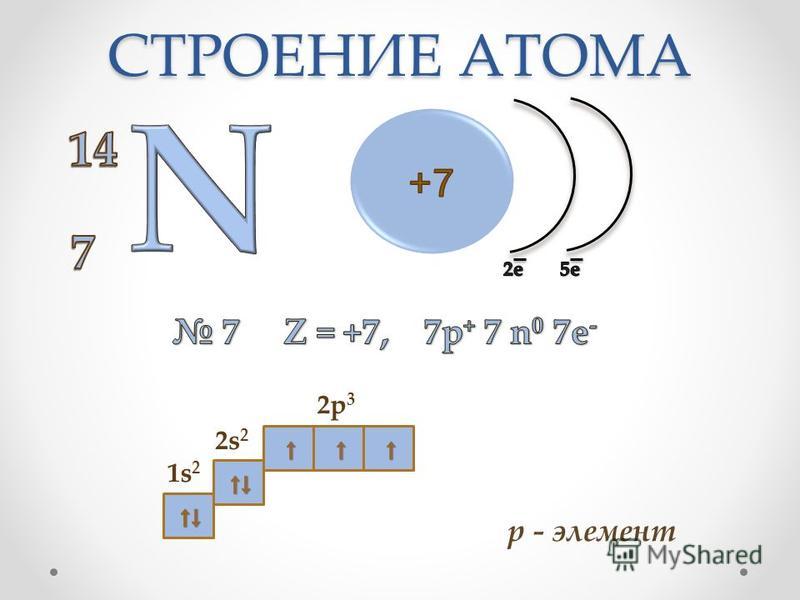
- Расчет кротов в повседневной жизни: Это простое в настройке и недорогое лабораторное задание — еще один хороший вариант для давая учащимся дополнительную практику с расчетами преобразования молей с использованием монеты и обычные предметы домашнего обихода.
- Вычисление молей: если вашим учащимся нужно немного больше практики, попросите их использовать эту лабораторную работу, чтобы помочь им понять концепцию кротов и преобразовать данные о массе в значения кротов, атомов или молекул. Студенты могут работать индивидуально или с партнером, чтобы попрактиковаться в использовании размерного анализа для решения задач преобразования родинок.
Изотопы и средняя атомная масса:
- Познакомить с понятием изотопов с помощью задания Что такое изотопы? Видео Вопросы. Учащиеся смотрят видео из серии видео Американского химического общества Химия Основы , а затем ответить на вопросы об изотопах. Это задание поможет им узнать об открытии изотопов, разнице между химическими и ядерными реакциями, различных видах радиоактивного распада и некоторых областях применения радиоактивных изотопов.
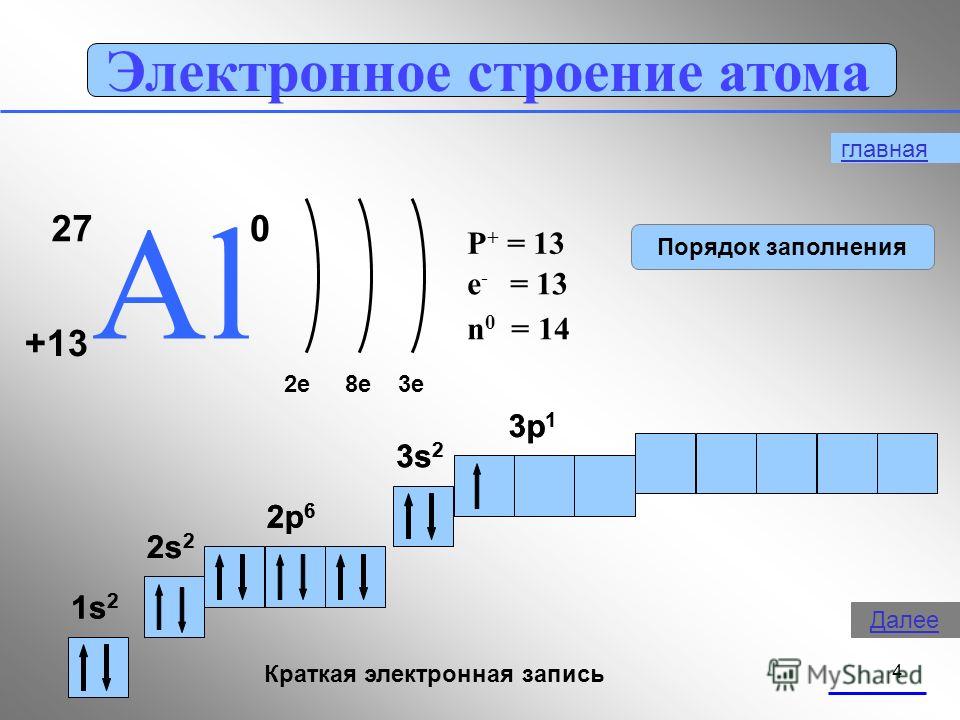
- Изотопы и расчет средней атомной массы: учащиеся могут узнать, как определяется средняя атомная масса, с помощью учебного пособия, основанного на содержании изотопов углерода с помощью этой симуляции. Затем они выбирают количество изотопов, массу каждого изотопа, а также содержание каждого из них, чтобы успешно построить загадочный элемент и вычислить его среднюю атомную массу.
- Изотопы фасоли: Если вы предпочитаете практическую деятельность, эта лабораторная работа проведет ваших студентов через шаги, которые они предпримут для расчета средней атомной массы воображаемого элемента под названием фасоль.
- Candy Isotopes & Atomic Mass: Это альтернативное задание, которое вы можете использовать, чтобы представить концепцию средней атомной массы. Этот простой и недорогой урок использует конфеты M&M для моделирования отношений, которые приблизительно соответствуют реальным значениям атомной массы в периодической таблице. Ресурс можно использовать с учащимися средних и старших классов, и он включает согласование с ожиданиями производительности NGSS.

Сохранение массы:
- Антуан Лавуазье: Познакомьте с концепцией сохранения массы и законом определенной пропорции с помощью этого видеоролика «Основатели химии», в котором рассказывается история о том, как, которого многие считают отцом современной химии, открыли кислород и водород и впервые предложил Закон сохранения массы. Он также включает в себя лист с заданиями, который включает вопросы, на которые учащиеся должны ответить во время просмотра видео.
- Балансировка лего: следуя видео, попросите учащихся использовать это практическое задание для моделирования реагентов и продуктов химической реакции. Затем они используют эти «атомы» и «молекулы», чтобы сбалансировать химическую реакцию, чтобы продемонстрировать закон сохранения материи.
- Химия в мешочке: используйте этот урок как упражнение или демонстрацию, чтобы ваши ученики сделали наблюдения о Законе сохранения массы.
Электроны, электронные конфигурации и электромагнитное излучение:
- Орбиты Анимация: Используя модель Бора для представления структуры атома, учащиеся визуализируют электроны, «вращающиеся» вокруг ядра.
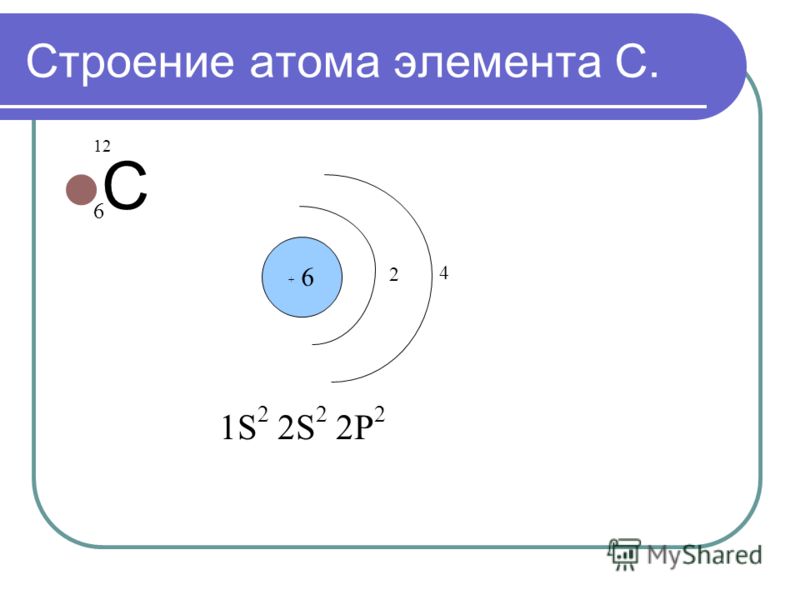 Помогите им расширить свои знания с помощью этой анимации, которая позволяет учащимся визуализировать, как орбитали накладываются друг на друга внутри атома в трех измерениях. На этой анимации изображены орбитали 1s, 2s, 2p, 3s, 3p, 4s и 3d.
Помогите им расширить свои знания с помощью этой анимации, которая позволяет учащимся визуализировать, как орбитали накладываются друг на друга внутри атома в трех измерениях. На этой анимации изображены орбитали 1s, 2s, 2p, 3s, 3p, 4s и 3d.- Продолжите урок «Электроны и орбитали», чтобы помочь учащимся различать энергетические уровни, подуровни, орбитали и электроны. Студенты часто путают эти термины, связанные с электронами, и это упражнение помогает им лучше понять, как их различать.
- Расширьте тему электронов и орбиталей с помощью анимации «Электромагнитный спектр» и плана урока. Анимация помогает учащимся узнать об электромагнитном спектре, уделяя особое внимание видимому спектру. В нем рассматривается взаимосвязь между цветом, длиной волны, частотой и энергией световых волн, а также то, как объект поглощает и отражает определенные длины волн света, чтобы внести свой вклад в воспринимаемый нами цвет.
- Захватывающие электроны: тогда используйте эту симуляцию из мартовского номера 9 2015 года.
 0327 Chemistry Solutions , чтобы позволить вашим учащимся изучить, что происходит, когда электроны в обычном атоме возбуждаются из своего основного состояния. Они увидят, что когда электрон возвращается в свое основное состояние из возбужденного состояния, выделяется энергия в виде электромагнитного излучения.
0327 Chemistry Solutions , чтобы позволить вашим учащимся изучить, что происходит, когда электроны в обычном атоме возбуждаются из своего основного состояния. Они увидят, что когда электрон возвращается в свое основное состояние из возбужденного состояния, выделяется энергия в виде электромагнитного излучения.
- Flame Test (Rainbow Demo): завершите изучение электронов этой более безопасной версией традиционной демонстрации, которая обычно используется на уроках химии в средней школе. Его можно использовать, чтобы показать учащимся разнообразие цветов, которые образуются при нагревании различных солей металлов в пламени. Вы можете просмотреть видео этой демонстрации на странице The Flame Test веб-сайта ACS. Подробнее об этом читайте в предупреждении о безопасности ACS о демонстрации Rainbow.
- Испытание пламенем: идем дальше: В дополнение к демонстрации попросите учащихся исследовать цвета, возникающие при помещении в пламя нескольких смесей ионов металлов.
 Обратите внимание, что в этой процедуре также используются деревянные шины и водные растворы вместо традиционного легковоспламеняющегося растворителя.
Обратите внимание, что в этой процедуре также используются деревянные шины и водные растворы вместо традиционного легковоспламеняющегося растворителя.
Структура атома – Уроки Византа
И ты думал, что ты странный…
Вот возмутительная мысль: Вся материя вокруг вас состоит из атомов, а все атомы состоят только из трех типов субатомных частиц, протонов, электронов , и нейтроны. Более того, все протоны абсолютно одинаковы, все нейтроны абсолютно одинаковы, и все электроны абсолютно одинаковы. Протоны и нейтроны имеют почти одинаковую массу. Масса электрона составляет примерно 1/1835 массы протона. Электроны имеют единичный отрицательный заряд. Каждый протон имеет положительный заряд. Эти заряды являются настоящими электрическими зарядами. Нейтроны не имеют никакого заряда.
Еще более возмутительной является форма атомов с тремя субатомными частицами. Нейтроны и протоны находятся в центре атома в ядре. Электроны находятся вне ядра в электронных оболочках различной формы на разном расстоянии от ядра.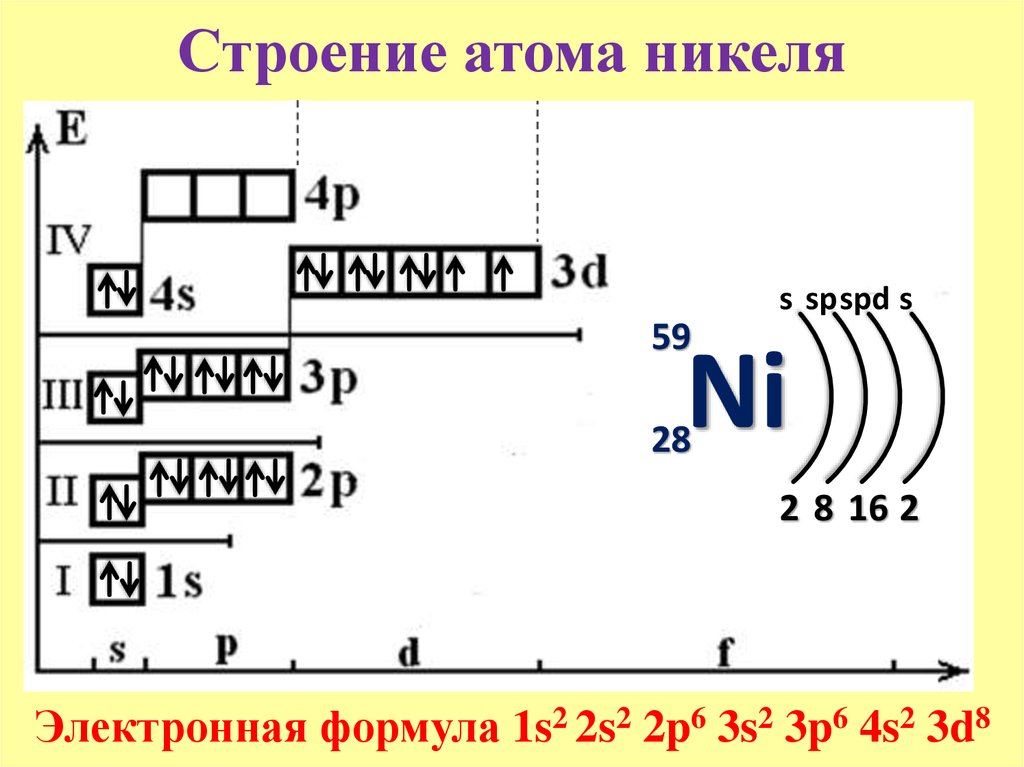 Атом в основном представляет собой пустое пространство. Эрнест Резерфорд стрелял субатомными частицами в очень тонкий кусок золота. Большинство частиц прошли прямо через золото. Это было все равно, что стрелять из винтовки в тонкую линию деревьев. Часть частиц отскочила, часть застряла внутри, но основная их часть прошла сквозь золотую фольгу. По расчетам Резерфорда, ядро в атоме похоже на BB в товарном вагоне. Это действительно возмутительная идея. Почти вся масса атома сосредоточена в крошечном ядре. Масса протона или нейтрона равна 1,66 Е -24 грамма или одной АМЕ, атомной единицы массы. Масса электрона 9.05 Е -28 грамм. Это число составляет одну миллиардную миллиардной миллиардной грамма. Никто и ни одна машина, использующая свет, не может увидеть протон в видимом свете. Длина волны света слишком велика, чтобы можно было обнаружить что-то настолько маленькое.
Атом в основном представляет собой пустое пространство. Эрнест Резерфорд стрелял субатомными частицами в очень тонкий кусок золота. Большинство частиц прошли прямо через золото. Это было все равно, что стрелять из винтовки в тонкую линию деревьев. Часть частиц отскочила, часть застряла внутри, но основная их часть прошла сквозь золотую фольгу. По расчетам Резерфорда, ядро в атоме похоже на BB в товарном вагоне. Это действительно возмутительная идея. Почти вся масса атома сосредоточена в крошечном ядре. Масса протона или нейтрона равна 1,66 Е -24 грамма или одной АМЕ, атомной единицы массы. Масса электрона 9.05 Е -28 грамм. Это число составляет одну миллиардную миллиардной миллиардной грамма. Никто и ни одна машина, использующая свет, не может увидеть протон в видимом свете. Длина волны света слишком велика, чтобы можно было обнаружить что-то настолько маленькое.
Открытие, структура и применение
Джон Дальтон: отец атома
Ближе к концу 18 века Джон Дальтон наблюдал три фундаментальных аспекта всей материи:
1.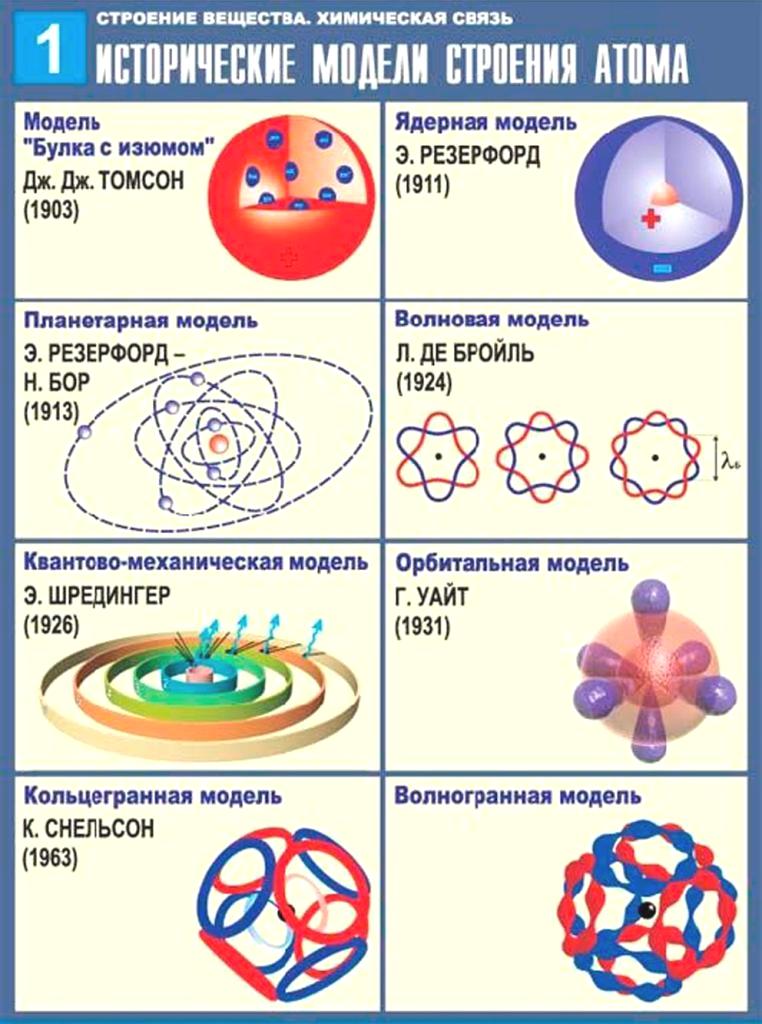 Массовое сохранение : Материя не может быть создана или уничтожена
Массовое сохранение : Материя не может быть создана или уничтожена
2. Определенный состав : Независимо от происхождения, конкретное соединение состоит из одной и той же материи/элементов в одинаковых фракциях.
3. Множественные пропорции : Когда один или несколько элементов объединяются вместе для образования соединения, это всегда делается в одной и той же пропорции.
Открытие: электричество?!
Чтобы понять природу атома, нужно вернуться к началу и проанализировать наблюдения, которые привели к нашей современной схеме. 19Ученые 19-го века начали свою одиссею в понимании атома, наблюдая за электричеством. Понятие материи и электрического заряда было понято, но фактические компоненты тока были преданы анафеме. Первым среди многих экспериментов являются эксперименты с электронно-лучевой трубкой. Эти катодные лучи исходят от отрицательного катода и направляются к положительному катоду. Однако, как только ученые ввели в обстановку магнит, они заметили, что эти лучи не распространяются прямолинейно.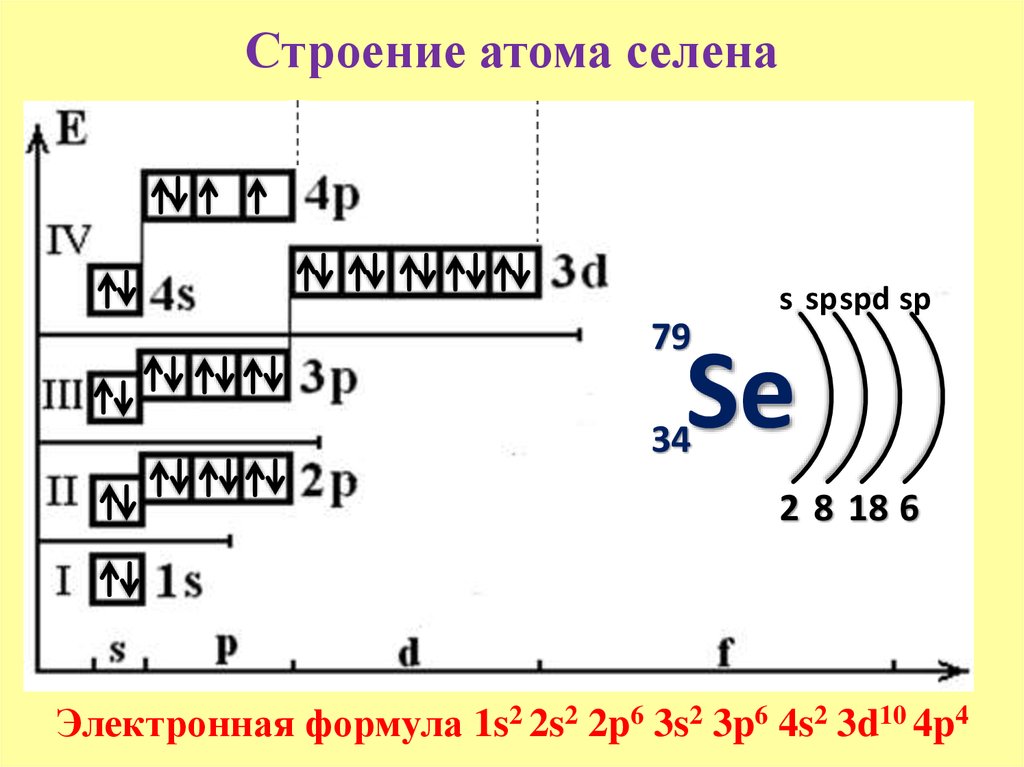 Скорее, лучи притягивались к положительному магниту, из-за чего они казались изогнутыми. Ученые поняли, что противоположности притягиваются, и ток, изгибающийся к положительному концу, должен состоять из отрицательно заряженных «вещей» (позже мы назовем их электронами).
Скорее, лучи притягивались к положительному магниту, из-за чего они казались изогнутыми. Ученые поняли, что противоположности притягиваются, и ток, изгибающийся к положительному концу, должен состоять из отрицательно заряженных «вещей» (позже мы назовем их электронами).
Открытие: от электрона к ядру!
После открытия электрона физики Дж.Дж. Томпсон и Роберт Милликен также проиллюстрировали заряд (-1,602×10 -19 Кл) и массу (9,109×10 -28 г) электронов. Следуя своим наблюдениям, Томпсон представил модель «сливового пудинга», как показано ниже, где атом — это просто положительная сфера с отрицательно заряженными частицами, находящимися внутри.
Ученый интуитивно понимает, что природа требует равновесия, и что если атом содержит отрицательные части (электроны), он также должен состоять из положительно заряженных частей, чтобы обеспечить равновесие. Кроме того, если электроны чрезвычайно малы, то из чего состоит масса самого атома? Введите Эрнеста Резерфорда и его эксперименты с золотой фольгой.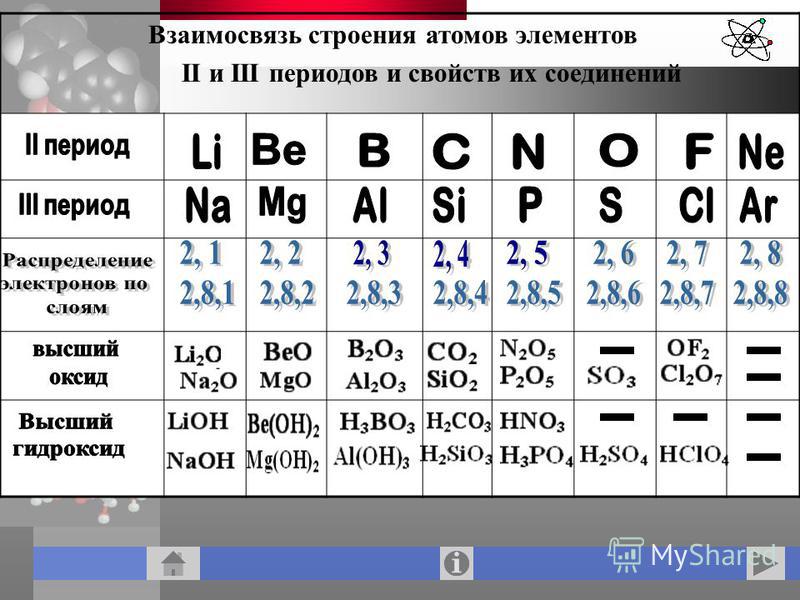
Приближаясь к концу 20-го века, Резерфорд использовал альфа-частицы (также известные как гелий) и направлял их на тонкий лист золотой фольги. Он заметил, что не все атомы проходят сквозь фольгу, а некоторые начинают отскакивать. Характер отскока этих нескольких альфа-атомов подразумевал, что, возможно, отрицательно заряженные части не были частью самого ядра и что центр содержал положительную часть со значительной массой. Электроны, будучи очень маленькими, не могли отражать громоздкие альфа-частицы, поэтому в центре должна быть большая часть, имеющая значительную массу с электронами, вращающимися вокруг этого центра. Резерфорд первым ввел термин «ядро» по отношению к атомному центру.
Вслед за Резерфордом Джеймс Чедвик в 1932 году обнаружил наличие незаряженной части ядра, называемой нейтроном. Эти разработки привели к современной структуре атома. А именно, ядро, содержащее протоны/нейтроны, представляющие основную часть массы атома, с электронами, вращающимися вокруг центра, является современным представлением атома.
Современная структура атома
Современный атом представляет собой сферическое существо, состоящее из положительно заряженного ядра, состоящего из протонов/нейтронов, окруженных одним или несколькими отрицательно заряженными электронами. Эти электроны вращаются вокруг ядра и составляют наибольшую часть 9 атома.0157 том . Однако именно чрезвычайно плотный центр, состоящий из протонов и нейтронов, содержит основную массу атома . Протоны имеют заряд +1, электроны -1, а нейтроны не заряжены, но имеют массу, почти равную массе протонов. Нейтральное состояние атомов существует потому, что заряды протонов и электронов компенсируют друг друга. Все атомы уникального элемента имеют одинаковый атомный номер, и каждый элемент имеет уникальный атомный номер, отличный от других элементов. Каждый атом имеет заданный атомный номер (Z), массовое число (A) и атомный символ (X), как показано ниже.
Важность этих чисел нельзя недооценивать, и нужно понимать, как их рассчитать.
I. Атомный номер (Z)
a. Это число протонов в атоме
b. Число протонов каждого атома уникально для элемента
i. Пр.) Углерод: Z=6, потому что у него 6 протонов в ядре
ii. Пр) Кислород Z=8, потому что у него 8 протонов в ядре
c. Формирует основу организации периодических таблиц
II. Массовое число (A)
a. Это общая сумма протонов и нейтронов, находящихся в ядре
b. Протоны = 1 единица массы; Нейтроны = 1 единица массы
i. Пример) Углерод: A=12
1. 6 протонов + 6 нейтронов = 12 единиц массы
ii. Пример) Кислород: A=14
1. 8 протонов + 8 нейтронов = 16 единиц массы
c. Чтобы рассчитать количество нейтронов:
i. A – Z = N (нейтроны)
III. Атомный символ (X)
a. Каждый элемент имеет уникальный символ
i. Кислород: O
ii. Углерод: C
Углерод: C
Изотопы, ионы и атомная масса…
Все атомы одного и того же элемента имеют одинаковое количество протонов, но могут иметь разное количество нейтронов, что приводит к разным атомным массам. Атомы с одинаковым числом протонов, но разным числом нейтронов называются изотопами. Изотопы приводят к тому, что атомная масса элемента отличается от его массового числа, потому что атомный номер представляет собой среднее значение масс изотопов, тогда как атомный номер представляет собой сумму протонов и нейтронов. Например:
I. Углерод: массовое число = 12, НО атомная масса = 12,01… почему?
а. Массовое число = нейтроны (N) + протоны (P) = 6+6=12
b. Атомная масса – это среднее значение масс изотопов
, основанное на содержании, i. 12 C (98,88%), 13 C (1,11%), 14 C (0,01%)
ii. Атомная масса = 12 (0,9988) + 13 (0,0111) + 14 (0,0001) = 12,01 а. е.м.
е.м.
Но подождите, откуда взялось понятие атомной массы? Атомная единица массы (а.е.м.) основана на стандарте атома углерода-12 и гласит, что 1/12 атома углерода-12 составляет одну а.е.м.
С атомной массой и изотопами, влияющими на массу атома, следующая часть касается заряда атома. Ионы – это атомы с одинаковым числом протонов, но разным числом электронов. При расчете заряда атома протоны равны +1, электроны -1, а нейтроны нейтральны. Процесс потери электрона делает атом более положительным, а приобретение электрона делает его более отрицательным. Заряд атома указан в верхней правой части символа атома.
I. Ex) Углерод
a. 12 C: 6 протонов, 6 электронов
i. (+6) + (-6) = 0
б. 12 C +1 : 6 протонов, 5 электронов
i. (+6) + (-5)= +1
c. 12 C -1 : 6 протонов, 7 электронов
i.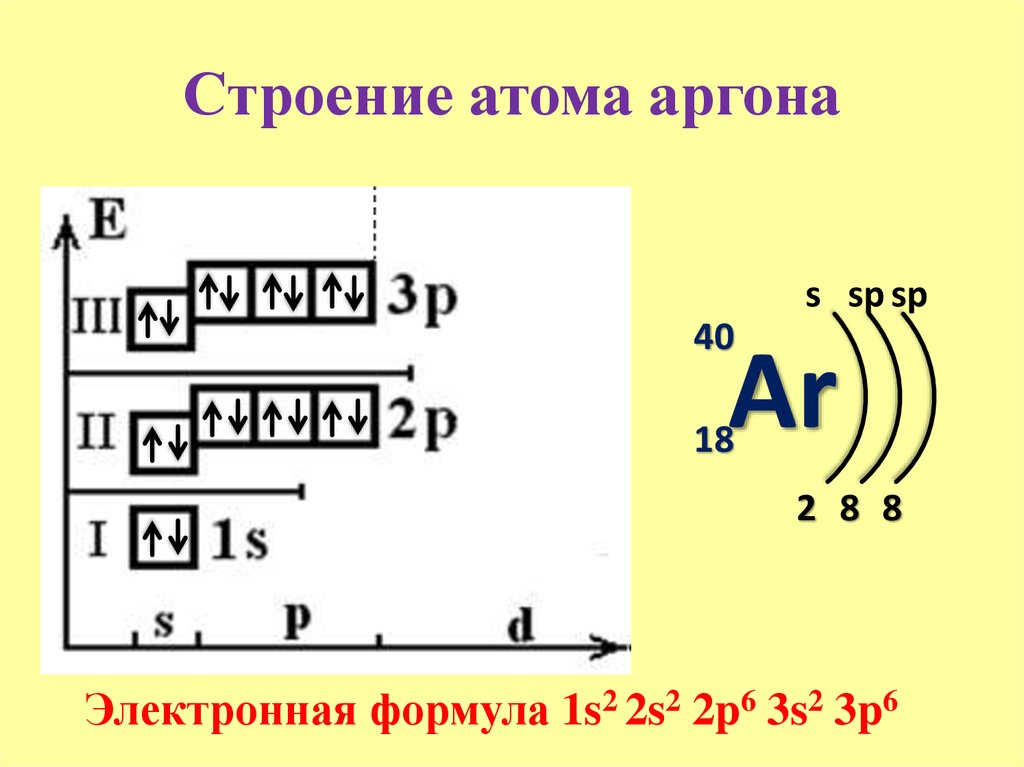 (+6) + (-7)= -1
(+6) + (-7)= -1
Атомные веса и атомные номера
Целое число, которое вы найдете в каждом поле периодической таблицы, является атомным номером. Атомный номер – это количество протонов в ядре каждого атома. Обратите внимание, что в каждом поле элемента есть одно и только одно целое число от 1 до 110 или около того, поэтому мы нашли все элементы. Каждый элемент аккуратно вписывается в свою нишу в периодической таблице.
Еще одно число, которое часто можно встретить в поле с символом элемента, обычно не является целым числом. Было бы немного упрощением сказать, что это число равно количеству протонов плюс среднее число нейтронов в этом элементе. Число называется атомным весом или атомной массой.
Как может элемент иметь усредненный атомный вес? Количество протонов определяет тип элемента. Если атом имеет шесть протонов, это углерод. Если у него 92 протона, то это уран. Однако количество нейтронов в ядре элемента может быть разным. Углерод 12 является наиболее распространенным типом углерода. У углерода 12 шесть протонов (естественно, иначе это был бы не углерод) и шесть нейтронов. Масса электронов пренебрежимо мала. Углерод 12 имеет массу двенадцать. У углерода 13 шесть протонов и семь нейтронов. У углерода 14 шесть протонов и восемь нейтронов. Углерод 14 радиоактивен, потому что, как и другие атомы с неправильным процентным соотношением нейтронов и протонов, он нестабилен. Ядро имеет тенденцию разрываться. Правильное соотношение протонов к нейтронам составляет примерно один к одному для малых элементов и примерно один протон к полутора нейтронам для более крупных элементов. Типы элементов, в которых каждый атом имеет одинаковое количество протонов и одинаковое количество нейтронов, называются изотопами. Углерод 14 — радиоактивный изотоп углерода. Углерод-14, образовавшийся во время образования Земли, почти полностью исчез. Углерод 14 непрерывно производится из высокоэнергетического электромагнитного излучения, воздействующего на атомы азота в озоновом слое земли. Этот углерод-14, поступающий в растения в виде CO2, также попадает в организм животных.
У углерода 12 шесть протонов (естественно, иначе это был бы не углерод) и шесть нейтронов. Масса электронов пренебрежимо мала. Углерод 12 имеет массу двенадцать. У углерода 13 шесть протонов и семь нейтронов. У углерода 14 шесть протонов и восемь нейтронов. Углерод 14 радиоактивен, потому что, как и другие атомы с неправильным процентным соотношением нейтронов и протонов, он нестабилен. Ядро имеет тенденцию разрываться. Правильное соотношение протонов к нейтронам составляет примерно один к одному для малых элементов и примерно один протон к полутора нейтронам для более крупных элементов. Типы элементов, в которых каждый атом имеет одинаковое количество протонов и одинаковое количество нейтронов, называются изотопами. Углерод 14 — радиоактивный изотоп углерода. Углерод-14, образовавшийся во время образования Земли, почти полностью исчез. Углерод 14 непрерывно производится из высокоэнергетического электромагнитного излучения, воздействующего на атомы азота в озоновом слое земли. Этот углерод-14, поступающий в растения в виде CO2, также попадает в организм животных.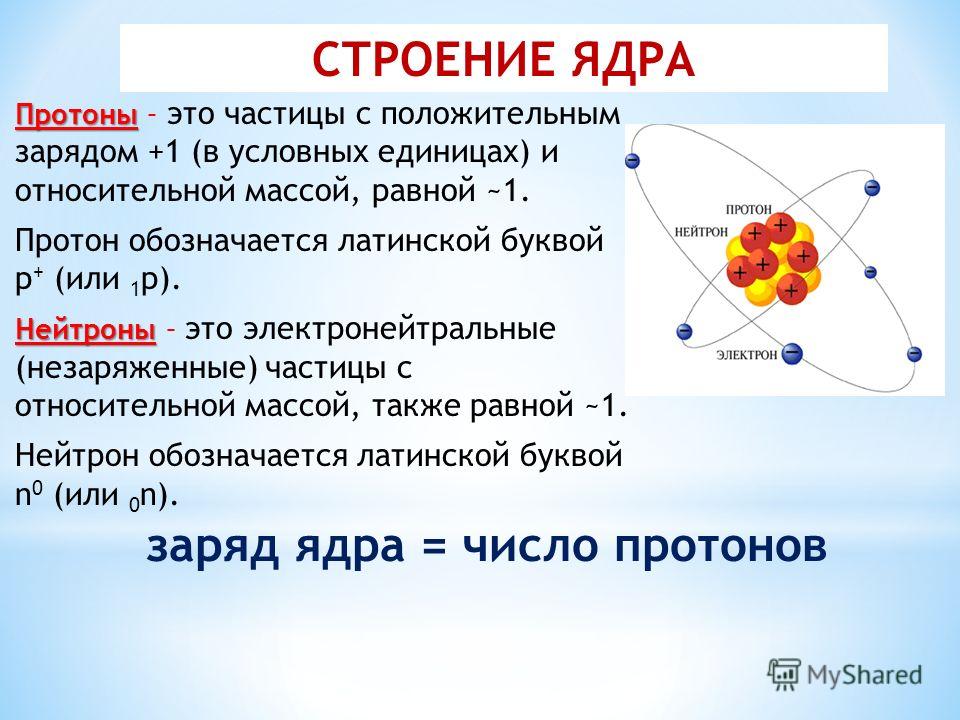 Мы можем узнать, сколько углерода-14 обычно содержится в живом растении или животном, а оттуда мы можем найти фактическое количество углерода-14, оставшееся в давно умершем растении или животном. Мы можем получить очень хорошее представление о том, как давно жило это растение или животное, по количеству углерода-14, оставшемуся в мертвом теле. Этот процесс называется «углеродным датированием». Стабильные, нерадиоактивные изотопы углерода не играют в этом никакой роли. Как целостный элемент углерод имеет более или менее постоянную пропорцию различных изотопов углерода. По этой причине мы можем определить средневзвешенное содержание изотопов для всех элементов. На периодической диаграмме вы можете увидеть некоторые атомные веса, которые являются целыми числами или заключены в круглые скобки. Обычно это очень крупные, очень редкие или очень радиоактивные элементы. На самом деле это не целочисленный атомный вес, но атомный вес был оценен с точностью до ближайшего целого числа.
Мы можем узнать, сколько углерода-14 обычно содержится в живом растении или животном, а оттуда мы можем найти фактическое количество углерода-14, оставшееся в давно умершем растении или животном. Мы можем получить очень хорошее представление о том, как давно жило это растение или животное, по количеству углерода-14, оставшемуся в мертвом теле. Этот процесс называется «углеродным датированием». Стабильные, нерадиоактивные изотопы углерода не играют в этом никакой роли. Как целостный элемент углерод имеет более или менее постоянную пропорцию различных изотопов углерода. По этой причине мы можем определить средневзвешенное содержание изотопов для всех элементов. На периодической диаграмме вы можете увидеть некоторые атомные веса, которые являются целыми числами или заключены в круглые скобки. Обычно это очень крупные, очень редкие или очень радиоактивные элементы. На самом деле это не целочисленный атомный вес, но атомный вес был оценен с точностью до ближайшего целого числа.
Вес по формуле или молекулярный вес или масса по формуле или молярная масса
Теперь, имея информацию об атомном весе, мы можем рассмотреть сопоставление атомов по массе. Возьмем хлористый водород, HCl. К одному атому хлора присоединен один атом водорода, но они имеют разные массы. Атом водорода имеет массу 1,008 а.е.м., а атом хлора имеет массу 35,453 а.е.м. С практической точки зрения, один AMU слишком мал для того, чтобы мы могли его взвесить в лаборатории. Мы можем взвесить 1,008 грамма водорода и 35,453 грамма хлора, и они точно совпадут. Атомов водорода будет столько же, сколько атомов хлора. Они могли бы объединиться, чтобы получить HCl без остатка водорода или хлора. Если мы возьмем один грамм материала на каждую АМЕ массы в атомах только одного из них, у нас будет моль (или моль) этого материала. Таким образом, один моль любого материала содержит такое же количество частиц названного материала, и это число является числом Авогадро, 6,022 E 23,9.0013
Возьмем хлористый водород, HCl. К одному атому хлора присоединен один атом водорода, но они имеют разные массы. Атом водорода имеет массу 1,008 а.е.м., а атом хлора имеет массу 35,453 а.е.м. С практической точки зрения, один AMU слишком мал для того, чтобы мы могли его взвесить в лаборатории. Мы можем взвесить 1,008 грамма водорода и 35,453 грамма хлора, и они точно совпадут. Атомов водорода будет столько же, сколько атомов хлора. Они могли бы объединиться, чтобы получить HCl без остатка водорода или хлора. Если мы возьмем один грамм материала на каждую АМЕ массы в атомах только одного из них, у нас будет моль (или моль) этого материала. Таким образом, один моль любого материала содержит такое же количество частиц названного материала, и это число является числом Авогадро, 6,022 E 23,9.0013
Масса формулы является наиболее общим термином, который включает атомную массу и молекулярную массу. В случае с HCl мы можем сложить атомные массы элементов в соединении и получить молекулярную массу. Молекулярная масса HCl составляет 36,461 г/моль, сумма атомных масс водорода и хлора. Единицей молекулярной массы является грамм на моль. Чтобы рассчитать молекулярную массу любой формулы, нужно сложить атомные массы всех атомов в формуле. CuSO4 · 5h3O – формула пентагидрата сульфата меди II. В формуле есть один атом меди, один атом серы, девять атомов кислорода и десять атомов водорода. Чтобы получить формулу веса этого соединения, мы должны сложить атомные веса. Пентагидрат сульфата меди II, строго говоря, не является молекулой, но вы услышите термин «молекулярная масса», используемый для него, а не более правильный «масса формулы». Поскольку единицей формульного веса являются граммы на моль, имеет смысл использовать формульный вес материала в качестве коэффициента преобразования между массой материала и количеством молей материала.
Молекулярная масса HCl составляет 36,461 г/моль, сумма атомных масс водорода и хлора. Единицей молекулярной массы является грамм на моль. Чтобы рассчитать молекулярную массу любой формулы, нужно сложить атомные массы всех атомов в формуле. CuSO4 · 5h3O – формула пентагидрата сульфата меди II. В формуле есть один атом меди, один атом серы, девять атомов кислорода и десять атомов водорода. Чтобы получить формулу веса этого соединения, мы должны сложить атомные веса. Пентагидрат сульфата меди II, строго говоря, не является молекулой, но вы услышите термин «молекулярная масса», используемый для него, а не более правильный «масса формулы». Поскольку единицей формульного веса являются граммы на моль, имеет смысл использовать формульный вес материала в качестве коэффициента преобразования между массой материала и количеством молей материала.
Электронная конфигурация
Протоны имеют положительный заряд, а электроны — отрицательный. Свободные (неприкрепленные) незаряженные атомы имеют такое же количество электронов, как и протоны, чтобы быть электрически нейтральными. Протоны находятся в ядре и не изменяются и не меняются, за исключением некоторых ядерных реакций. Электроны находятся в дискретных путях или оболочках вокруг ядра. Существует ранжирование или иерархия оболочек, обычно с более удаленными от ядра оболочками, имеющими более высокую энергию. Рассматривая электронную конфигурацию атомов, мы будем описывать положение электронов в основном состоянии. Когда электроны имеют более высокую энергию, они могут перемещаться от ядра в более высокоэнергетические оболочки.
Протоны находятся в ядре и не изменяются и не меняются, за исключением некоторых ядерных реакций. Электроны находятся в дискретных путях или оболочках вокруг ядра. Существует ранжирование или иерархия оболочек, обычно с более удаленными от ядра оболочками, имеющими более высокую энергию. Рассматривая электронную конфигурацию атомов, мы будем описывать положение электронов в основном состоянии. Когда электроны имеют более высокую энергию, они могут перемещаться от ядра в более высокоэнергетические оболочки.
Атом водорода имеет только один протон и один электрон. Электрон атома водорода движется вокруг ядра протона в оболочке сферической формы. Два электрона гелия, элемента номер два, имеют одинаковую сферическую форму вокруг ядра. Первая оболочка имеет только одну подоболочку, и эта подоболочка имеет только одну орбиталь или путь для электронов. На каждой орбитали есть место для двух электронов. Сферическая форма одинокой орбитали на первом энергетическом уровне дала ей название «s»-орбиталь. Гелий — последний элемент первого периода. Будучи инертным элементом, он указывает на то, что эта оболочка заполнена. Оболочка номер один имеет только одну подоболочку s, а все подоболочки s имеют только одну орбиталь. На каждой орбитали есть место только для двух электронов. Итак, первая оболочка, называемая К-оболочкой, имеет только два электрона.
Гелий — последний элемент первого периода. Будучи инертным элементом, он указывает на то, что эта оболочка заполнена. Оболочка номер один имеет только одну подоболочку s, а все подоболочки s имеют только одну орбиталь. На каждой орбитали есть место только для двух электронов. Итак, первая оболочка, называемая К-оболочкой, имеет только два электрона.
Начиная с лития, электронам не хватает места на первой оболочке или энергетическом уровне. Литий имеет два электрона на первой оболочке и один электрон на следующей оболочке. Первая оболочка заполняется первой, а остальные более или менее по порядку по мере увеличения размера элемента периодической диаграммы, но последовательность не сразу очевидна. На втором энергетическом уровне есть место для восьми электронов. Второй энергетический уровень имеет не только s-орбиталь, но и p-подоболочку с тремя орбиталями. Подоболочка p может содержать шесть электронов. Подоболочка p имеет форму трех гантелей, расположенных под углом 90 градусов друг к другу, причем каждая форма гантели представляет собой одну орбиталь.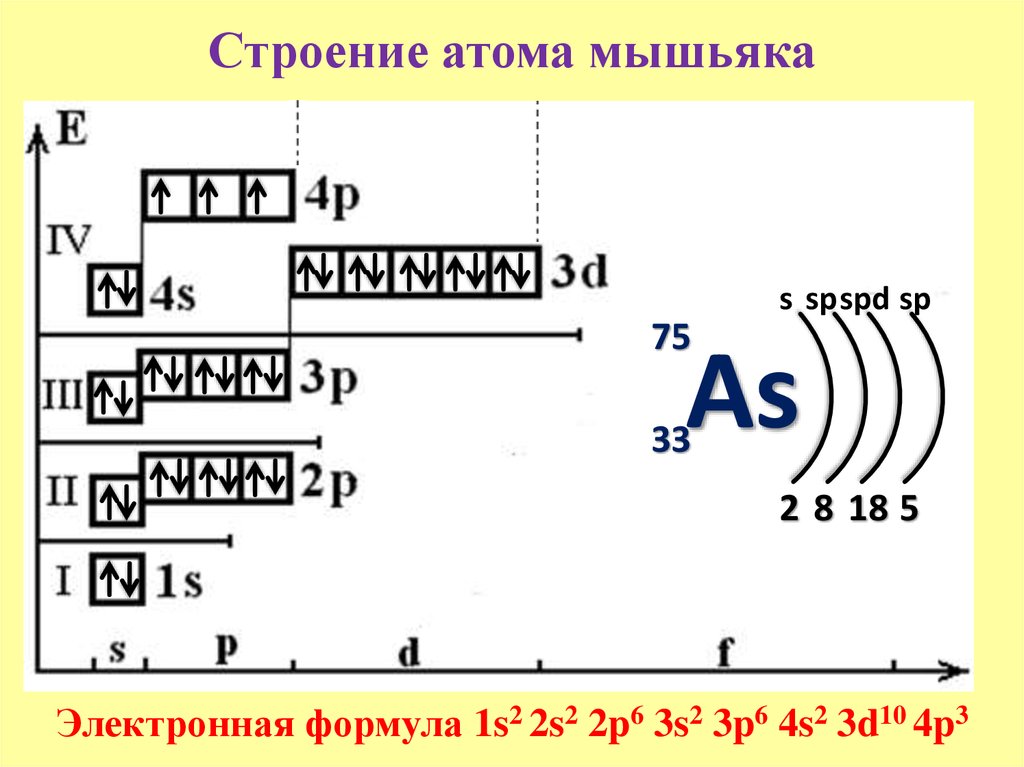 С подоболочками s и p вторая оболочка, L-оболочка, может содержать в общей сложности восемь электронов. Вы можете увидеть это на периодической диаграмме. Литий имеет один электрон на внешней оболочке, L-оболочке. Бериллий имеет два электрона на внешней оболочке. Подоболочка s заполняется первой, поэтому все остальные электроны, добавляющиеся к этой оболочке, переходят в подоболочку p. У бора три внешних электрона, у углерода — четыре, у азота — пять, у кислорода — шесть, у фтора — семь. Неон имеет полную оболочку из восьми электронов во внешней оболочке, L-оболочке, что означает, что неон — инертный элемент, конец периода.
С подоболочками s и p вторая оболочка, L-оболочка, может содержать в общей сложности восемь электронов. Вы можете увидеть это на периодической диаграмме. Литий имеет один электрон на внешней оболочке, L-оболочке. Бериллий имеет два электрона на внешней оболочке. Подоболочка s заполняется первой, поэтому все остальные электроны, добавляющиеся к этой оболочке, переходят в подоболочку p. У бора три внешних электрона, у углерода — четыре, у азота — пять, у кислорода — шесть, у фтора — семь. Неон имеет полную оболочку из восьми электронов во внешней оболочке, L-оболочке, что означает, что неон — инертный элемент, конец периода.
Начиная снова с натрия с одним электроном на внешней оболочке, М-оболочка заполняет свои подоболочки s и p восемью электронами. Аргон, восемнадцатый элемент, имеет два электрона на К-оболочке, восемь на L-оболочке и восемь на М-оболочке. Четвертый период снова начинается с калия и кальция, но здесь есть разница. После добавления 4s-электронов и до добавления 4p-электронов последовательность возвращается к третьему энергетическому уровню, чтобы вставить электроны в d-оболочку.
Оболочки или энергетические уровни пронумерованы или обозначены буквами, начиная с К. Итак, К — это один, L — два, М — три, N — четыре, О — пять, Р — шесть и Q — семь. Поскольку s-оболочки могут иметь только два электрона, а p-оболочки могут иметь только шесть электронов, d-оболочки могут иметь только десять электронов, а f-оболочки могут иметь только четырнадцать электронов. Последовательность добавления электронов по мере увеличения атомного номера выглядит следующим образом: первое число — это номер оболочки, s, p, d или f — тип подоболочки, а последнее число — количество электронов в атомной оболочке. подоболочка.
1 S 2 2 S 2 2 P 6 3 S 2 3 P 6 4 S 2 3 D 10 4 S 2 3 D 10 4 S 2 3 D 10 4 . 10 5 p 6 6 s 2 4 f 14 5 d 10 6 p 6 7 s 2 5 f 14 6 d 10 7 p 6
It заманчиво поставить 8s2 в конце последовательности, но у нас нет доказательств наличия R-оболочки.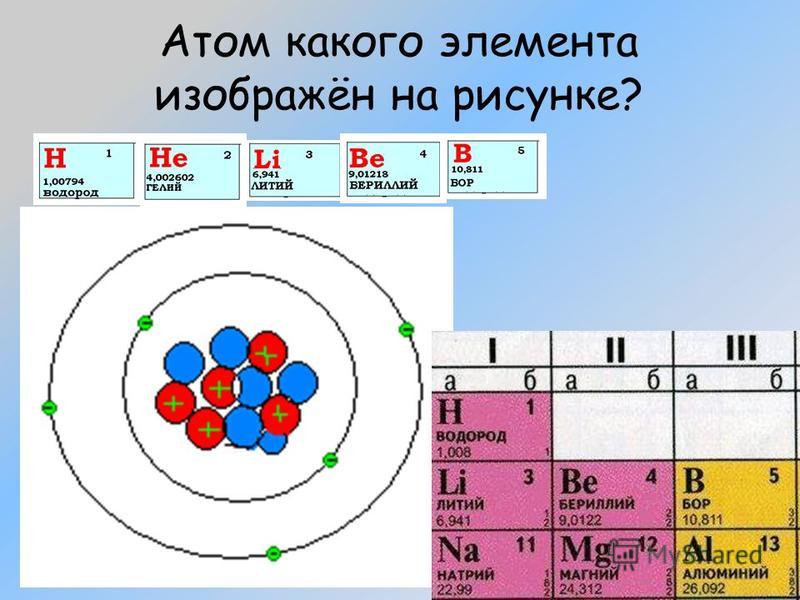 Один из способов узнать эту последовательность — запомнить ее. В нем есть некая закономерность. Следующий способ узнать эту последовательность — ВИДЕТЬ ЕЕ НА ПЕРИОДИЧЕСКОЙ ДИАГРАММЕ. Если двигаться от водорода вниз по диаграмме, группы 1 и 2 представляют заполнение подоболочки s. Заполнение p-подоболочки показано в группах с 3 по 8. Заполнение d-подоболочки представлено переходными элементами (десять элементов), а заполнение f-подоболочки показано в ряду лантанидов и актинидов (четырнадцать элементов).
Один из способов узнать эту последовательность — запомнить ее. В нем есть некая закономерность. Следующий способ узнать эту последовательность — ВИДЕТЬ ЕЕ НА ПЕРИОДИЧЕСКОЙ ДИАГРАММЕ. Если двигаться от водорода вниз по диаграмме, группы 1 и 2 представляют заполнение подоболочки s. Заполнение p-подоболочки показано в группах с 3 по 8. Заполнение d-подоболочки представлено переходными элементами (десять элементов), а заполнение f-подоболочки показано в ряду лантанидов и актинидов (четырнадцать элементов).
Вот копия периодической диаграммы, какой вы ее обычно видели.
А вот та же таблица, перестроенная с лантанидами и актинидами на своих местах, а затем с группами I и II. Обе эти диаграммы имеют цветовую кодировку, поэтому элементы с подоболочкой 2s снаружи (H и He) окрашены в бирюзовый цвет. Все остальные элементы с подоболочкой s снаружи (группы I и II) обведены синим цветом. Лантаниды и актиниды выделены серым цветом. Другие переходные элементы выделены желтым цветом, а все элементы, у которых подоболочка p является последней снаружи, окрашены в лососевый цвет.
Возможно, вам будет лучше видно с помеченными областями подоболочки.
Есть несколько других схем, которые помогут вам запомнить последовательность.
Форма подоболочек s сферическая. Форма подоболочек р представляет собой форму трех штанг под углом девяносто градусов друг к другу. Форма подоболочек д и ф очень сложная.
Электронная конфигурация — это «форма» электронов вокруг атома, то есть, на каком энергетическом уровне (оболочке) и на какой орбитали он находится. первые (внутренние) оболочки. Их имена начинались с «К» для первой оболочки, затем «Л», затем «М», поэтому последующие энергетические уровни продолжались вверх по алфавиту. С тех пор буквы заменены цифрами от одного до семи. Обратите внимание, что я включил оболочку «R» (#8), которая является чисто фантастической, но делает диаграмму симметричной.
Электронная конфигурация записывается с первой (большой) цифрой в качестве номера оболочки.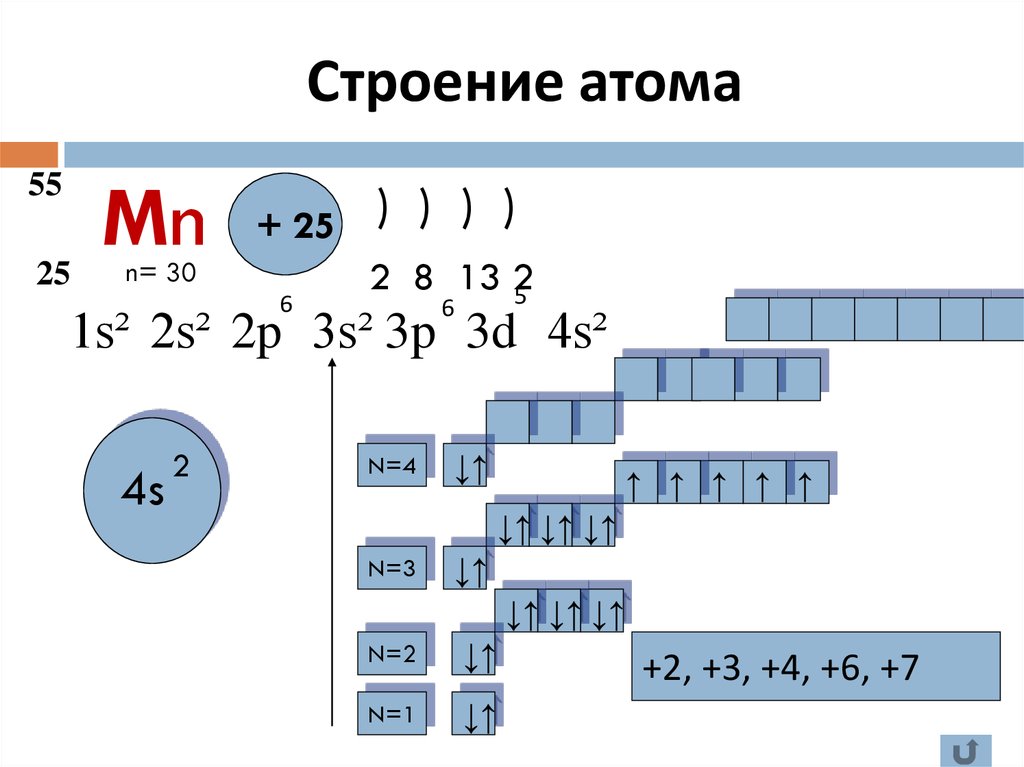 Буква орбитального типа (либо s , p , d , либо f ). Меньшее число в верхнем индексе – это количество электронов на этой орбитали.
Буква орбитального типа (либо s , p , d , либо f ). Меньшее число в верхнем индексе – это количество электронов на этой орбитали.
Используйте эту схему следующим образом. Сначала вы должны знать орбитали. Орбиталь s имеет только 2 электрона. Орбиталь p имеет шесть электронов. Орбиталь d имеет 10 электронов. f орбиталь имеет 14 электронов. Вы можете определить тип орбитали по номеру на графике. Единственным исключением из этого является то, что «8» на диаграмме — это «2» плюс «6», то есть s и p орбиталь. Диаграмма читается слева направо, а затем вниз к следующей строке, как в английском языке. Любой элемент с более чем 20 электронами в электрически нейтральном неприсоединенном атоме будет иметь все электроны в первой строке на диаграмме. Например, скандий, элемент № 21, будет иметь все электроны в первом ряду и один из второго. Электронная конфигурация скандия: 1 S 2 2 S 2 2 P 6 3 S 2 3 P 6 4 S 2 3 D 1 Обратите внимание, что 2 S 2 2 2 2 2 2 2 2 . s 2 3 p 6 произошли от восьмерок на графике (2+6). Обратите внимание, что другой электрон должен быть взят из следующей точки на диаграмме, а следующая точка — это первая точка слева в следующем ряду. Это пятно 3 d из-за «10» там, и нужен только один дополнительный электрон, следовательно, 3 d 1.
s 2 3 p 6 произошли от восьмерок на графике (2+6). Обратите внимание, что другой электрон должен быть взят из следующей точки на диаграмме, а следующая точка — это первая точка слева в следующем ряду. Это пятно 3 d из-за «10» там, и нужен только один дополнительный электрон, следовательно, 3 d 1.
Итоги справа указывают на использование целых строк. Если атомный номер элемента больше тридцати восьми, возьмите все первые две строки и все, что больше, из третьей строки. Йод номер пятьдесят три. Для его электронной конфигурации вы использовали бы все электроны в первых двух рядах и еще пятнадцать электронов. 1 S 2 2 S 2 2 P 6 3 S 2 3 P 6 4 S 2 3 D 10 4 P 6 5 D 10 4 P 6 5 D 10 4 P 6 5 D 2. и 4 д 10 5 р 5 с третьего ряда. Вы можете сложить итоги для каждой оболочки внизу. Полные раковины дадут вам итоги на дне.
Мы включили оболочку R (#8), несмотря на то, что ее существование еще не доказано. Диаграмма выглядит более симметричной с включенной оболочкой. Два электрона из оболочки R указаны в скобках. Мы еще даже не создали элементы, у которых есть электроны в подоболочке p Q-оболочки.
Диаграмма выглядит более симметричной с включенной оболочкой. Два электрона из оболочки R указаны в скобках. Мы еще даже не создали элементы, у которых есть электроны в подоболочке p Q-оболочки.
Схема конфигурации электрона
| К | л | М | Н | О | Р | В | Р | |
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | |
| с | сп | скорость | spdf | spdf | скорость | сп | с | |
| 2 | 8 | 8 | 2 | 20 | ||||
| 10 | 6 | 2 | 38 | |||||
| 10 | 6 | 2 | 56 | |||||
| 14 | 10 | 6 | 2 | 88 | ||||
| 14 | 10 | 6 | 2 | |||||
| — | — | — | — | — | — | — | — | |
| 2 | 8 | 18 | 32 | 32 | 18 | 8 | 2 | ИТОГО |
Вот еще один вариант рассмотрения той же схемы. Инертные элементы появляются в конце либо первых двух, либо восьмерки, либо шестерки. Везде, где есть шестерка подоболочки p , над ней есть две подоболочки s , образующие восемь электронов во внешней полной оболочке благородного газа. Электронная конфигурация ксенона:
Инертные элементы появляются в конце либо первых двух, либо восьмерки, либо шестерки. Везде, где есть шестерка подоболочки p , над ней есть две подоболочки s , образующие восемь электронов во внешней полной оболочке благородного газа. Электронная конфигурация ксенона:
1 s 2 2 s 2 2 p 6 3 s 2 3 p 6 4 s
| K | л | М | Н | О | Р | В | Р | |
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | |
| с | сп | скорость | spdf | spdf | скорость | сп | с | |
| 2 /ГЕЛИЙ | 8 /НЕОН | 8 /АРГОН | 2 | 20 | ||||
| 10 | 6 /КРИПТОН | 2 | 38 | |||||
| 10 | 6 /КСЕНОН | 2 | 56 | |||||
| 14 | 10 | 6 /РАДОН | 2 | 88 | ||||
| 14 | 10 | 6 /УНД | 2 | |||||
| — | — | — | — | — | — | — | — | |
| 2 | 8 | 18 | 32 | 32 | 18 | 8 | 2 | ВСЕГО |
«UND» — неоткрытый инертный элемент, который в периодической таблице находится ниже радона.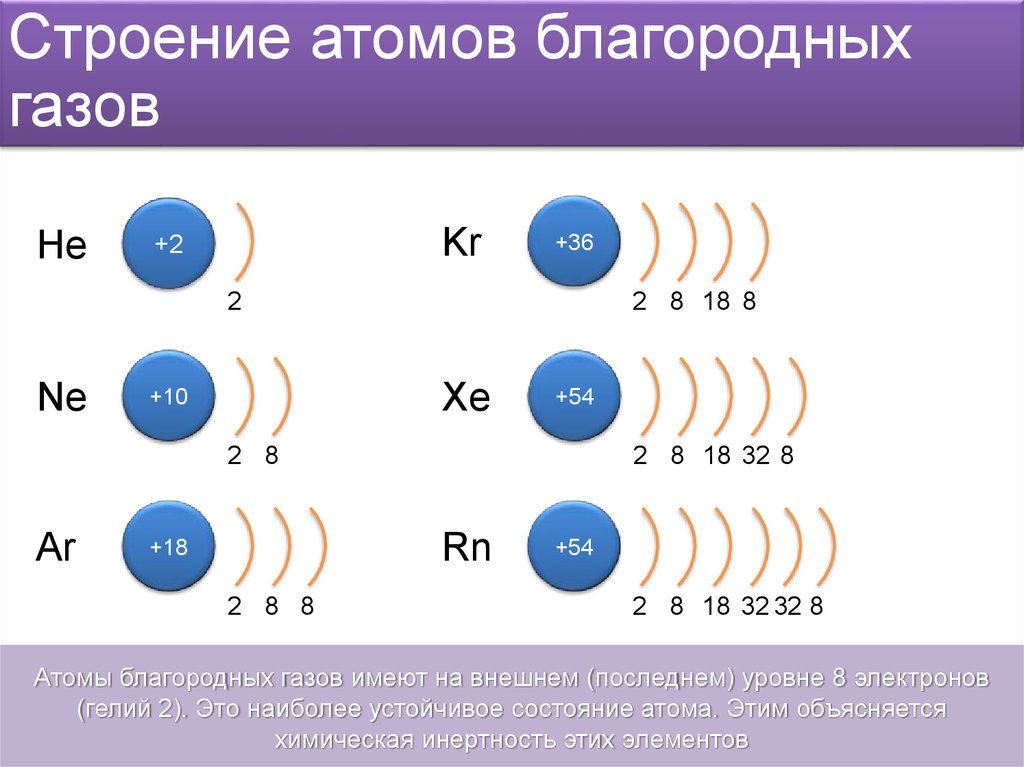
Общие схемы конфигурации электронов
Это более известные схемы. Все, что вам нужно сделать, это следовать стрелкам через точки, чтобы найти последовательность. Складывайте количество электронов по ходу дела и останавливайтесь, когда вы сравняетесь или почти превысите это число. Было много вариаций этой идеи, но все они работают одинаково. Расположите подоболочки в наклонном порядке и пройдите через массив прямыми линиями, как в первой схеме, или расположите подоболочки в прямую линию и пройдите через массив наклонными линиями, как во второй схеме. В этих схемах инертные элементы появляются после первой s подоболочки и после каждой p подоболочки. Как и другой тип, этот тип схемы имеет свои преимущества и недостатки, но все они ведут к одной и той же последовательности.
Схема А
| —» | 1 с 2 | |||
| —» | 2 с 2 | |||
| —» | 2 р 6 | |||
| —» | 3 с 2 | |||
| —» | 3 р 6 | |||
| —» | 4 с 2 | 3 г 10 | ||
| —» | 4 р 6 | |||
| —» | 5 с 2 | 4 г 10 | ||
| —» | 5 р 6 | |||
| —» | 6 с 2 | 4 ж 14 | ||
| —» | 5 д 10 | |||
| —» | 6 р 6 | |||
| —» | 7 с 2 | 5 ж 14 | ||
| —» | 6 д 10 | |||
| —» | 7 р 6 |
Схема Б
Любая из этих схем при правильном использовании даст вам одно и то же, последовательность добавления электронов к оболочкам. Эта закономерность верна для всех элементов, которые не являются переходными элементами, лантаноидами или актинидами. Из переходных элементов, лантанидов и актинидов около трети элементов не соответствуют этому образцу. Периодическая диаграмма ниже расположена боком, чтобы показать конфигурацию электрона по оболочке. Работая со схемами нахождения электронной конфигурации элементов, вы можете проверить правильность своего ответа, добавляя электроны в каждой оболочке (внизу в первой схеме) и сравнивая с боковой периодической диаграммой. Элементы, не вписывающиеся в шаблон, отмечены звездочкой. В переходных элементах, которые не следуют схеме, только подоболочка s внешней оболочки и подоболочка d предпоследней оболочки имеют некоторый обмен между собой. В ряду лантанидов и актинидов любой обмен электронами происходит между подоболочкой d предпоследней оболочки и f подоболочка предпоследней оболочки, которая заполняется по мере того, как элементы продвигаются вверх по этой серии.
Эта закономерность верна для всех элементов, которые не являются переходными элементами, лантаноидами или актинидами. Из переходных элементов, лантанидов и актинидов около трети элементов не соответствуют этому образцу. Периодическая диаграмма ниже расположена боком, чтобы показать конфигурацию электрона по оболочке. Работая со схемами нахождения электронной конфигурации элементов, вы можете проверить правильность своего ответа, добавляя электроны в каждой оболочке (внизу в первой схеме) и сравнивая с боковой периодической диаграммой. Элементы, не вписывающиеся в шаблон, отмечены звездочкой. В переходных элементах, которые не следуют схеме, только подоболочка s внешней оболочки и подоболочка d предпоследней оболочки имеют некоторый обмен между собой. В ряду лантанидов и актинидов любой обмен электронами происходит между подоболочкой d предпоследней оболочки и f подоболочка предпоследней оболочки, которая заполняется по мере того, как элементы продвигаются вверх по этой серии.
Правило октета в периодической таблице
Правило октетов утверждает, что атомы наиболее стабильны, когда они имеют полную электронную оболочку во внешнем электронном кольце. Первая оболочка имеет только два электрона в одной подоболочке s . Гелий имеет полную оболочку, поэтому он стабильный, инертный элемент. Однако водород имеет только один электрон. Он может потерять электрон, чтобы стать H+, ионом водорода, или может получить электрон, чтобы стать H-, ионом гидрида. Все остальные снаряды имеют s и подоболочка p , что дает им по крайней мере восемь электронов снаружи. Подоболочки s и p часто являются единственными валентными электронами, поэтому правило октетов названо в честь восьми электронов s и p .
Первая оболочка имеет только два электрона в одной подоболочке s . Гелий имеет полную оболочку, поэтому он стабильный, инертный элемент. Однако водород имеет только один электрон. Он может потерять электрон, чтобы стать H+, ионом водорода, или может получить электрон, чтобы стать H-, ионом гидрида. Все остальные снаряды имеют s и подоболочка p , что дает им по крайней мере восемь электронов снаружи. Подоболочки s и p часто являются единственными валентными электронами, поэтому правило октетов названо в честь восьми электронов s и p .
На периодической диаграмме с итоговыми значениями оболочки вы можете легко увидеть правило октетов. Валентность – это вероятный заряд иона элемента. Все элементы группы 1 имеют один электрон на внешней оболочке, и все они имеют валентность плюс один. Элементы группы 1 потеряют один и только один электрон, этот единственный внешний электрон превратится в один положительный ион с полной электронной оболочкой из восьми электронов (октет) в с и р подоболочки под него.
Все элементы группы 2 имеют два электрона на внешней оболочке и все имеют валентность плюс два. Бериллий может немного отличаться в этом отношении, но все остальные элементы группы 2 могут потерять два электрона, чтобы стать ионами +2. Они теряют не один электрон, а два или ни одного.
Переходные элементы, лантаноиды и актиноиды — все это металлы. Многие из них имеют разную валентность, потому что они могут обмениваться электронами с внешней оболочки на внутреннюю 9.0157 d или f незаполненные подоболочки. По этой причине иногда кажется, что они нарушают схему присоединения электронов.
Элементы группы 3 имеют валентность плюс три. Бор является исключением из этого правила, потому что он настолько мал, что имеет тенденцию образовывать ковалентные связи. Алюминий имеет валентность +3, но некоторые из более крупных элементов Группы 3 имеют более одной валентности.
Наименьшие элементы группы 4, углерод и кремний, являются неметаллами, потому что четыре электрона трудно потерять все четыре электрона во внешней оболочке. Малые элементы группы 4, как правило, образуют только ковалентные связи, разделяя электроны. Более крупные элементы группы 4 имеют более одной валентности, обычно включая +4.
Малые элементы группы 4, как правило, образуют только ковалентные связи, разделяя электроны. Более крупные элементы группы 4 имеют более одной валентности, обычно включая +4.
Элементы малой группы 5, азот и фосфор, являются неметаллами. Они имеют тенденцию либо получать три электрона, чтобы образовать октет, либо связываться ковалентно. Более крупные элементы группы 5 имеют более металлический характер.
Элементы малой группы 6, кислород и сера, склонны либо приобретать два электрона, либо связываться ковалентно. Более крупные элементы группы 6 имеют более металлический характер.
Все элементы группы 7 имеют семь электронов на внешней оболочке и либо получают один электрон, чтобы стать ионом -1, либо образуют одну ковалентную связь. Элементы группы 7 представляют собой двухатомные газы из-за сильной склонности связываться друг с другом ковалентной связью.
Все инертные элементы, благородные газы, имеют полный октет во внешней оболочке (или два в первой оболочке) и, таким образом, не соединяются естественным образом химически с другими элементами.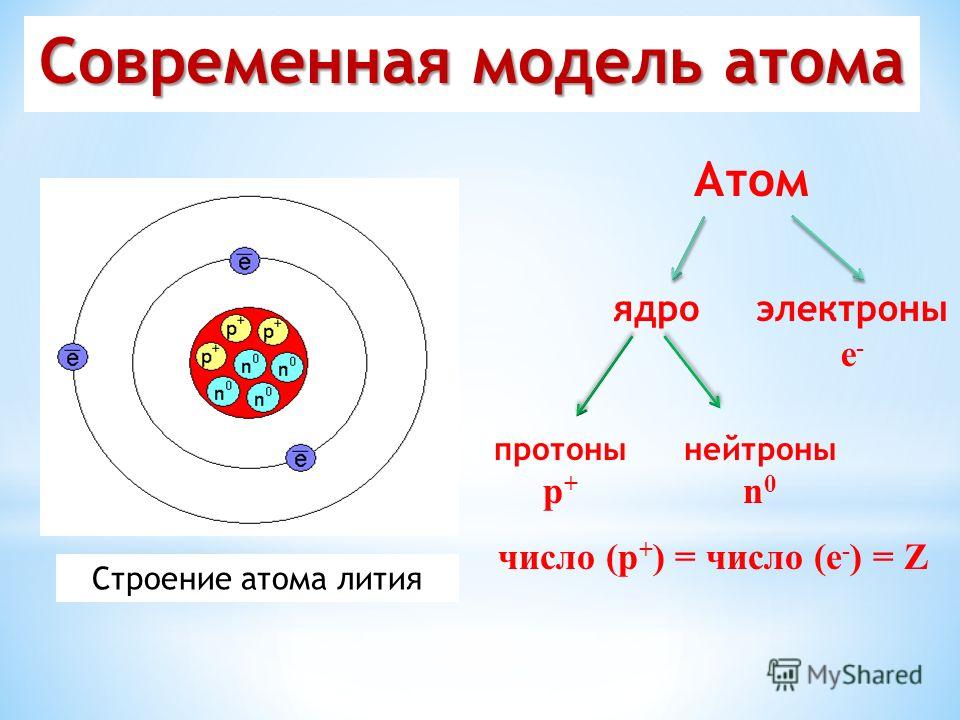
| Пт #87 | CS # 55 | Руб #37 | К № 19 | На № 11 | Ли #3 | H#1 | |||
| 2 8 18 32 18 8 1 | 2 8 18 18 8 1 | 2 8 18 8 1 | 2 8 8 1 | 2 8 1 | 2 1 | 1 | |||
| Ра #88 | Ба#56 | Старший № 38 | № 20 | Мг#12 | Бе # 4 | ||||
| 2 8 18 32 18 8 2 | 2 8 18 18 8 2 | 2 8 18 8 2 | 2 8 8 2 | 2 8 2 | 2 2 | ||||
| Ас №89 | Ла #57 | Lr #103 | Лу #71 | Г # 39 | Sc # 21 | ||||
| 2 8 18 32 18 9 2* | 2 8 18 18 9 2 * | 2 8 18 32 32 9 2 | 2 8 18 32 9 2 | 2 8 18 9 2 | 2 8 9 2 | ||||
| Тб #90 | Се № 58 | Дб#104 | Hf #72 | Zr #40 | Ти № 22 | ||||
| 28 18 32 18 10 2* | 2 8 18 19 9 2 * | 28 18 32 32 10 2 | 2 8 18 32 10 2 | 2 8 18 10 2 | 2 8 10 2 | ||||
| Па № 91 | Пр #59 | Jl #105 | Та # 73 | № № 41 | В #23 | ||||
| 2 8 18 32 20 9 2* | 2 8 18 21 8 2 | 28 18 32 32 11 2 | 2 8 18 32 11 2 | 2 8 18 12 1 * | 2 8 11 2 | ||||
| U #92 | Nd#60 | Rf#106 | Вт #74 | Мо # 42 | Кр # 24 | ||||
| 2 8 18 32 21 9 2* | 2 8 18 22 8 2 | 28 18 32 32 12 2 | 2 8 18 32 12 2 | 2 8 18 13 1 * | 2 8 13 1 * | ||||
| Np#93 | ПМ#61 | Бх#107 | Ре#75 | ТК #43 | № 25 | ||||
| 2 8 18 32 22 9 2* | 2 8 18 23 8 2 | 28 18 32 32 13 2 | 2 8 18 32 13 2 | 2 8 18 13 2 | 2 8 13 2 | ||||
| Пу#94 | См#62 | Hn#108 | Ос#76 | Ру #44 | Fe #26 | ||||
| 2 8 18 32 24 8 2 | 2 8 18 24 8 2 | 2 8 18 32 32 14 2 | 28 18 32 14 2 | 2 8 18 15 1 * | 2 8 14 2 | ||||
| Ам#95 | ЕС#63 | Мт # 109 | Ир № 77 | Правая #45 | Co #27 | ||||
| 2 8 18 32 25 8 2 | 2 8 18 25 8 2 | 28 18 32 32 15 2 | 2 8 18 32 15 2 | 2 8 18 16 1 * | 2 8 15 2 | ||||
| см#96 | Gd#64 | #110 | Часть № 78 | Pd № 46 | Ni #28 | ||||
| 2 8 18 32 25 9 2* | 2 8 18 25 9 2 * | 28 18 32 17 1 * | 2 8 18 18 0 * | 2 8 16 2 | |||||
| Бк #97 | Тб #65 | #111 | Au#79 | Аг #47 | Cu#29 | ||||
| 2 8 18 32 26 9 2* | 2 8 18 27 8 2 | 28 18 32 18 1 * | 2 8 18 18 1 * | 2 8 18 1 * | |||||
См. № 98 № 98 | Dy #66 | #112 | рт.ст.#80 | CD #48 | Zn #30 | ||||
| 2 8 18 32 28 8 2 | 2 8 18 28 8 2 | 2 8 18 32 18 2 | 2 8 18 18 2 | 2 8 18 2 | |||||
| Эс #99 | Хо #67 | #113 | TL #81 | В № 49 | Га № 31 | Ал #13 | Б №5 | ||
| 2 8 18 32 29 8 2 | 2 8 18 29 8 2 | 2 8 18 32 18 3 | 2 8 18 18 3 | 2 8 18 3 | 2 8 3 | 2 3 | |||
| FM#100 | Эр № 68 | #114 | Pb #82 | Серийный #50 | Ge #32 | Си #14 | С #6 | ||
| 2 8 18 32 30 8 2 | 2 8 18 30 8 2 | 2 8 18 32 18 4 | 2 8 18 18 4 | 2 8 18 4 | 2 8 4 | 2 4 | |||
| Мд#101 | Тм#69 | #115 | Би #83 | Сб № 51 | Как № 33 | Р № 15 | №7 | ||
| 2 8 18 32 31 8 2 | 2 8 18 31 8 2 | 2 8 18 32 18 5 | 2 8 18 18 5 | 2 8 18 5 | 2 8 5 | 2 5 | |||
| № 102 | Ыб #70 | #116 | По #84 | Те #52 | Se # 34 | S #16 | О #8 | ||
| 2 8 18 32 32 8 2 | 2 8 18 32 8 2 | 2 8 18 32 18 6 | 2 8 18 18 6 | 2 8 18 6 | 2 8 6 | 2 6 | |||
| #117 | Номер 85 | I #53 | Бр #35 | Кл #17 | F #9 | ||||
| 2 8 18 32 18 7 | 2 8 18 18 7 | 2 8 18 7 | 2 8 7 | 2 7 | |||||
| #118 | Рн#86 | Хе#54 | Кр #36 | Ар #18 | Ne#10 | He#2 | |||
| 2 8 18 32 18 8 | 2 8 18 18 8 | 2 8 18 8 | 2 8 8 | 2 8 | 2 | ||||
Структуры элементов по Льюису
Снова изучите боковую периодическую диаграмму с номерами электронных оболочек. Все элементы группы I и водород (верхний ряд диаграммы) имеют один и только один электрон на внешней оболочке. Именно этот единственный электрон придает этим элементам отличительный характер группы. Структуры Льюиса – это просто попытка графически показать эти валентные электроны, поскольку они используются для объединения с другими элементами. Символ элемента находится в центре, и до четырех групп из двух электронов показаны точками сверху, снизу, справа и слева от символа элемента, чтобы показать валентные электроны. Все инертные газы (благородные газы) имеют все восемь электронов вокруг символа элемента, за исключением гелия, у которого есть только два электрона даже при полной оболочке. Ниже приведена демонстрация благородных газов, записанных в структуре Льюиса. Обратите внимание, что электроны выделены красным, чтобы подчеркнуть их.
Все элементы группы I и водород (верхний ряд диаграммы) имеют один и только один электрон на внешней оболочке. Именно этот единственный электрон придает этим элементам отличительный характер группы. Структуры Льюиса – это просто попытка графически показать эти валентные электроны, поскольку они используются для объединения с другими элементами. Символ элемента находится в центре, и до четырех групп из двух электронов показаны точками сверху, снизу, справа и слева от символа элемента, чтобы показать валентные электроны. Все инертные газы (благородные газы) имеют все восемь электронов вокруг символа элемента, за исключением гелия, у которого есть только два электрона даже при полной оболочке. Ниже приведена демонстрация благородных газов, записанных в структуре Льюиса. Обратите внимание, что электроны выделены красным, чтобы подчеркнуть их.
Все остальные элементы имеют менее восьми электронов на внешней оболочке. Эти электроны могут занимать позиции восьми электронов инертных газов, но есть некоторые предположения о том, где они должны находиться. Элементы группы I имеют только один электрон на внешней оболочке, поэтому на самом деле не имеет значения, где находится точка электрона: над, под, справа или слева от символа элемента.
Элементы группы I имеют только один электрон на внешней оболочке, поэтому на самом деле не имеет значения, где находится точка электрона: над, под, справа или слева от символа элемента.
Элементы группы II имеют два электрона. Некоторые авторы помещают две точки электрона вместе на любой стороне символа элемента, потому что электроны действительно вместе находятся в s-подоболочке.
Некоторые авторы показывают, что электроны отделены друг от друга в любом из двух положений, но только по одному электрону в каждом положении. Причина этого в том, что электроны действительно пытаются двигаться как можно дальше друг от друга.
Бор и элементы ниже него в периодической таблице имеют три электрона на внешней оболочке. Эти электроны могут быть сгруппированы как каждый электрон в отдельности в одном из положений вокруг символа элемента или как группа из двух ( s ) электроны в одном положении и один электрон в другом. Бор обычно изображается с отдельными электронами, потому что он связан в основном ковалентно. Ковалентные связи, как мы знаем из формы молекул, обычно объединяют подоболочки s и p в sp орбитали с одной s и одной p орбиталью, sp2 орбиталью с одной s орбиталью. и две смешанные орбитали p или орбитали sp3 с использованием одной s орбиталь со всеми тремя p орбиталями. Орбитали sp2 бора имеют тенденцию иметь плоскую треугольную форму, то есть связи расположены под углом 120 градусов друг к другу в виде плоского круга вокруг атома бора в центре. Структура Льюиса бора представляет собой любую из приведенных ниже форм.
Бор обычно изображается с отдельными электронами, потому что он связан в основном ковалентно. Ковалентные связи, как мы знаем из формы молекул, обычно объединяют подоболочки s и p в sp орбитали с одной s и одной p орбиталью, sp2 орбиталью с одной s орбиталью. и две смешанные орбитали p или орбитали sp3 с использованием одной s орбиталь со всеми тремя p орбиталями. Орбитали sp2 бора имеют тенденцию иметь плоскую треугольную форму, то есть связи расположены под углом 120 градусов друг к другу в виде плоского круга вокруг атома бора в центре. Структура Льюиса бора представляет собой любую из приведенных ниже форм.
Углерод и элементы под ним имеют четыре электрона на внешней оболочке. В структурах Льюиса обычно показано, что углерод и кремний имеют четыре отдельных электрона, опять же потому, что эти элементы связаны исключительно ковалентными связями. sp3 орбитали углерода и кремния имеют тетраэдрическую форму.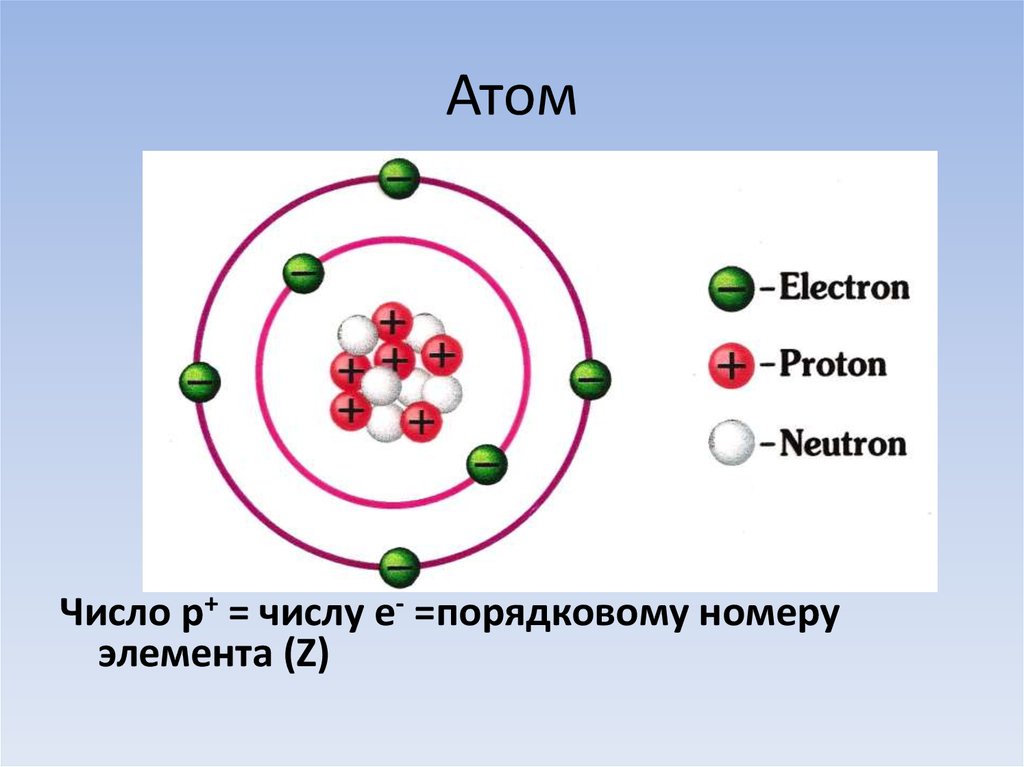
Азот и элементы ниже него имеют пять электронов на валентной оболочке, поэтому они должны быть показаны с одной парой (где угодно) и тремя одиночными электронами.
Кислород и элементы ниже него имеют шесть валентных электронов и поэтому должны иметь две пары и два одиночных электрона.
Все элементы группы галогенов, группы VII, имеют семь электронов на внешней оболочке, поэтому только три группы по два и один электрон находятся в последнем положении.
Переходные элементы и элементы ряда лантанидов и актинидов не часто используются в ковалентных связях, которые обычно изображают структуры Льюиса, но эти металлические элементы можно изобразить таким образом, используя количество электронов во внешней оболочке, которое соответствует с валентностью элемента.
Существует разница между структурой Льюиса соединения и фактической трехмерной структурой. Структура Льюиса показывает элементы как их символы, а связи (тире) от каждого атома располагаются на девяносто градусов от символа. Электроны, не связанные связями, показаны точками (здесь квадратами) рядом с элементом. (См. первый рисунок.) Трехмерная структура пытается показать реальную форму молекулы.
Электроны, не связанные связями, показаны точками (здесь квадратами) рядом с элементом. (См. первый рисунок.) Трехмерная структура пытается показать реальную форму молекулы.
В трехмерной структуре справа. электроны, присоединенные к атому азота, показаны красным. Атом азота синий, а атомы водорода черные. Связи от азота к водороду также выделены черным цветом. Была попытка показать молекулу в 3D, так что связь сзади, кажется, уходит на экран. Каждая связь имеет два электрона, поэтому учитываются все электроны от всех участников этой молекулы.
Атомная теория | Общая химия 1
Глава 2
В этой главе изучаются атомы: химические элементы, атомная теория, строение атома, различие между изотопами и ионами, катионы и анионы, химическая номенклатура ионов и кислот
Атомы и элементы
Элемент:
Вещество , которое нельзя разложить на более простые вещества. Элементы можно разделить на 2 широких класса: металлы (хорошие проводники электричества и тепла, ковкие, пластичные) и неметаллы. Только 7 элементов встречаются в природе в виде двухатомных молекул: H 2 , N 2 , O 2 , F 2 , Cl 2 , Br 2 , I 2 ; остальные элементы одноатомные. Химические символы — это аббревиатуры, используемые для обозначения элементов
Элементы можно разделить на 2 широких класса: металлы (хорошие проводники электричества и тепла, ковкие, пластичные) и неметаллы. Только 7 элементов встречаются в природе в виде двухатомных молекул: H 2 , N 2 , O 2 , F 2 , Cl 2 , Br 2 , I 2 ; остальные элементы одноатомные. Химические символы — это аббревиатуры, используемые для обозначения элементов
H = водород, He = гелий, Li = литий
Атом:
Наименьшая составная единица материи, которая еще сохраняет свойства материи. Атом состоит из протонов, нейтронов и электронов:
- Протон: расположен в ядре, заряд = +1, масса ~ 1 а.е.м. = 1,661 x 10 -27 кг
- Нейтрон: расположен в ядре, заряд = 0, масса ~ 1 а.е.м.
- Электрон: расположен вне ядра, заряд = -1, масса = 5,5 x 10 -4 а.е.м. << 1 а.е.м.
⇒ большая часть массы атома сосредоточена в его ядре. Соединение или молекула, состоящая всего из 2 атомов, называется двухатомной молекулой 9.0013
Соединение или молекула, состоящая всего из 2 атомов, называется двухатомной молекулой 9.0013
Атомная теория
Атомная теория была сформулирована Джоном Дальтоном. Вот основные пункты:
- Материя состоит из атомов, малых и неделимых частиц
- Все атомы одного и того же элемента идентичны и имеют одинаковую массу
- Атомы различных элементов различаются по размеру, массе и химическому поведению
- Химические соединения состоят как минимум из 2 атомов различных элементов. Образовавшаяся частица называется молекулой
- В химической реакции атомы перестраиваются, разделяются или рекомбинируются с образованием новых соединений, но атом не создается и не разрушается
Атомная структура
Ядерная обозначения:
X: Символ элемента
Z: Atomic Число = число протонов
. Каждый элемент inember AIMBER AIMAIS AIMAIS AIMAIS AIMICAIS AIMICAIS AIMICAIN AIMICAIS AIMICAIS AIMAIN AIMIC AIMICAIN AIMIC AIMBICES AIMAIN AIMIC AIMICAIS AIMICAIS AIMICAIN AMIC AIMBICEN AIMICAIN AMIC AIMBICATE AIMAIN AOM57 количество протонов + нейтронов = количество нуклонов
Количество нейтронов = A-Z
Количество электронов = количество протонов – заряд
Изотопы:
Атомы одного и того же элемента, содержащие разное количество нейтронов. Большинство элементов встречается в природе в виде смесей изотопов
Большинство элементов встречается в природе в виде смесей изотопов
Все атомы углерода имеют одинаковое количество протонов Z = 6
Однако они могут иметь разное количество нейтронов: C612 (6 нейтронов) и C613 (7 нейтронов)
C612 и C613 – два изотопа углерода
Ионы – Катионы и анионы
Ион:
Атом или молекула, которые приобрели или потеряли один или несколько электронов, что придает им отрицательный или положительный заряд: число протонов (положительный заряд) отличается от количество электронов (отрицательный заряд). Количество электронов, которые получает или теряет атом, связано с его положением в периодической таблице ⇒ атом будет приобретать или терять электроны, образуя ионы с таким же количеством электронов, как у ближайшего благородного газа
Катион против аниона:
Потеря электрона в атоме или молекуле дает катион, ион с чистым положительным зарядом, в то время как приобретение электрона дает анион, ион с чистым отрицательный заряд
Атомный номер натрия Na равен Z = 11 ⇒ 11 протонов
Na нейтрален ⇒ 11 электронов
Катион Na + заряжен положительно ⇒ потеря 1 электрона
Наименование ионов
Одноатомные ионы:
Одноатомные катионы:
- названы путем добавления слова ион к названию элементов
- , если имеется более одного возможного заряда (особенно для переходных металлов), после названия элементов добавляется римская цифра для обозначения заряда
Mg 2+ = ион магния
Fe 2+ = ион железа(II)
Fe 3+ = ион железа(III)
Одноатомные анионы:
- названы путем изменения окончания названия элемента на -ide и добавления слова ion
Cl – = хлорид-ион
O 2- = оксид-ион
Оксоанионы:
Многоатомные анионы, содержащие один или несколько атомов кислорода и один центральный атом другого элемента. Они часто встречаются в виде серий из 2 или более ионов с одним и тем же центральным атомом, но с разным количеством атомов кислорода 9.0013
Они часто встречаются в виде серий из 2 или более ионов с одним и тем же центральным атомом, но с разным количеством атомов кислорода 9.0013
Наиболее распространенная форма оксоанионов в серии названа путем изменения окончания названия центрального элемента на -ate и добавления слова ион
- ион с на 1 меньше кислорода, чем наиболее распространенная ионная форма называется -ите ион
- ион, содержащий на 2 атома кислорода меньше, чем наиболее распространенная ионная форма, называется гипо- … -ит ион
- ион, содержащий на 1 кислород больше, чем самая распространенная ионная форма, называется пер- … -ат ион
CLO 3 – = ион хлората = наиболее распространенная форма
CLO 2 – = Ион хлорита
CLO – = Гипохлорский ион
CLO 65 – = Гипохлорский ион
CLO 7 40720 4 40720 40720 40720 40720 40720 – .
Наименование кислот
Бинарные кислоты:
Кислоты, образованные анионом и водородом H + . Они называются:
- путем добавления префикса 9.0327 гидро- перед названием аниона
- , заменив -ide окончание аниона на -ic .
- на добавление слова кислота в конце
HCl = соляная кислота
Оксокислоты:
Кислоты, образующие ионы водорода и соответствующие оксоанионы при растворении в воде. Оксокислота на основе иона -ate называется … -овая кислота в то время как оксокислота на основе -ite иона называется … -ous кислота
NO 3 – = нитрат ⇒ HNO 3 = азотная кислота
Проверьте свои знания об этой главе
Элемент является простейшей формой вещества и не может быть разбит на более простые вещества, пока атом является частью элемента. Только 7 элементов встречаются в природе в виде двухатомных молекул: H 2 , N 2 , O 2 , F 2 , Cl 2 , Br 2 , I 2 ; остальные элементы одноатомные. Химические символы — это аббревиатуры, используемые для обозначения элементов.
Только 7 элементов встречаются в природе в виде двухатомных молекул: H 2 , N 2 , O 2 , F 2 , Cl 2 , Br 2 , I 2 ; остальные элементы одноатомные. Химические символы — это аббревиатуры, используемые для обозначения элементов.
Элемент — это вещество, которое нельзя разбить на более простые вещества, в то время как соединение — это вещество, содержащее 2 или более элементов.
Атом — это наименьшая составная единица материи, которая сохраняет свойства материи. Он состоит из протонов (заряд = +1, масса ~ 1 а.е.м.) и нейтронов (заряд = 0, масса ~ 1 а.е.м.) в ядре и электронов (заряд = -1, масса = 5,5 х 10 -4 а.е.м.) вне ядра.
Существование нейтрона было доказано английским физиком Джеймсом Чедвиком, бомбардировавшим тонкую пластинку бериллия α-частицами. Металл испускал излучение очень высокой энергии, которое не отклонялось ни электрическими, ни магнитными полями.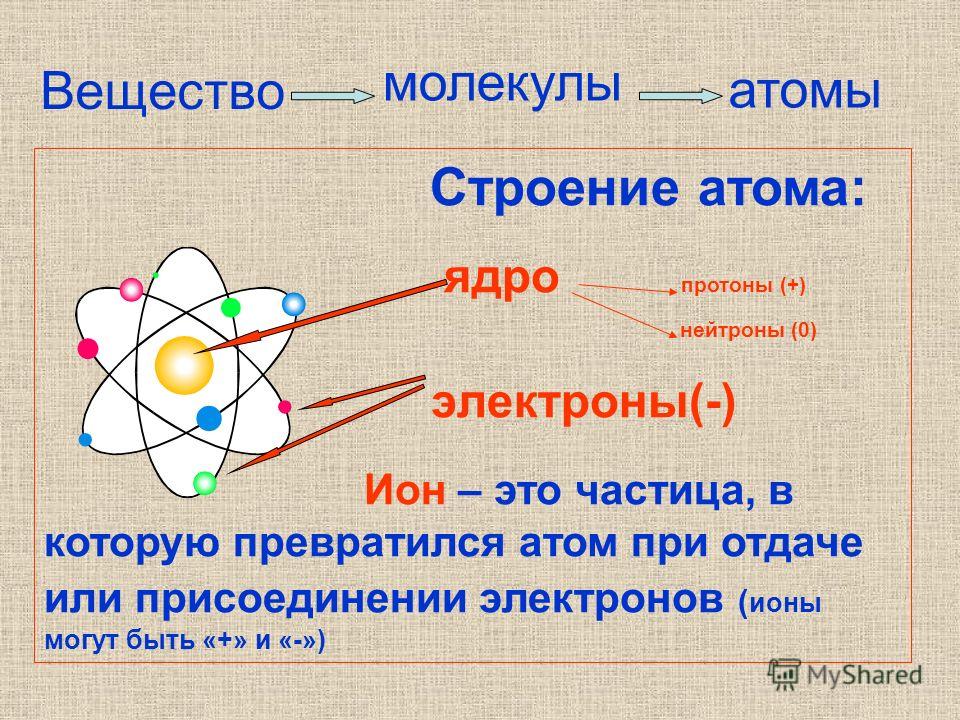 Этот эксперимент доказал существование третьего типа субатомных частиц, которые Чедвик назвал нейтронами, потому что они электрически нейтральны.
Этот эксперимент доказал существование третьего типа субатомных частиц, которые Чедвик назвал нейтронами, потому что они электрически нейтральны.
Атомная теория утверждает, что вся материя состоит из очень маленьких частиц, называемых атомами, которые не могут быть разделены, созданы или уничтожены. Атомы данного элемента одинаковы по размеру, массе и другим свойствам, тогда как атомы разных элементов различны. Эта теория дает объяснение как закона постоянного состава, так и закона сохранения массы.
- Материя состоит из атомов, малых и неделимых частиц
- Все атомы одного и того же элемента идентичны и имеют одинаковую массу
- Атомы различных элементов различаются по размеру, массе и химическому поведению
- Химические соединения состоят как минимум из 2 атомов различных элементов. Образовавшаяся частица называется молекулой .
- В химической реакции атомы перестраиваются, разделяются или рекомбинируются с образованием новых соединений, но атом не создается и не разрушается
Атомный номер (Z) — это количество протонов в атоме элемента. Каждый атом элемента имеет одинаковое количество протонов.
Каждый атом элемента имеет одинаковое количество протонов.
Количество протонов равно атомному номеру (Z) элемента. Чтобы найти количество нейтронов, вычтите количество протонов из массового числа (А). Чтобы найти количество электронов, вычтите заряд элемента из числа протонов.
Два изотопа — это атомы одного и того же элемента, содержащие разное количество нейтронов. Большинство элементов встречается в природе в виде смесей изотопов.
Ион – это атом или молекула, которые приобрели или потеряли один или несколько электронов, что придает ему отрицательный или положительный заряд: количество протонов (положительный заряд) отличается от количества электронов (отрицательный заряд).
Заряд атома равен количеству протонов минус количество электронов.
Чтобы найти количество электронов, вычтите заряд иона из числа протонов. Если заряд положительный, то в ионе протонов больше, чем электронов. Если заряд отрицательный, электронов больше, чем протонов.
Катион — это ион с чистым положительным зарядом из-за потери электрона, а анион — это ион с чистым отрицательным зарядом из-за присоединения электрона.
Одноатомные катионы называются путем добавления слова ион к названию элементов. Если существует более одного возможного заряда (особенно для переходных металлов), после названия элементов добавляется римская цифра, чтобы указать заряд.
Одноатомные анионы называются путем изменения окончания названия элемента на -ide и добавив слово ion .
Оксоанион – это многоатомный анион , который содержит один или несколько атомов кислорода и центральный атом другого элемента. Оксоанионы часто встречаются в виде серий из 2 или более ионов с одним и тем же центральным атомом, но с разным количеством атомов кислорода.
Наиболее распространенная форма оксоанионов в серии названа путем изменения окончания названия центрального элемента на -ate и добавления слова ион
- Ион с на 1 меньше кислорода, чем наиболее распространенная ионная форма называется -ите ион
- Ион, содержащий на 2 атома кислорода меньше, чем наиболее распространенная ионная форма, называется гипо- .


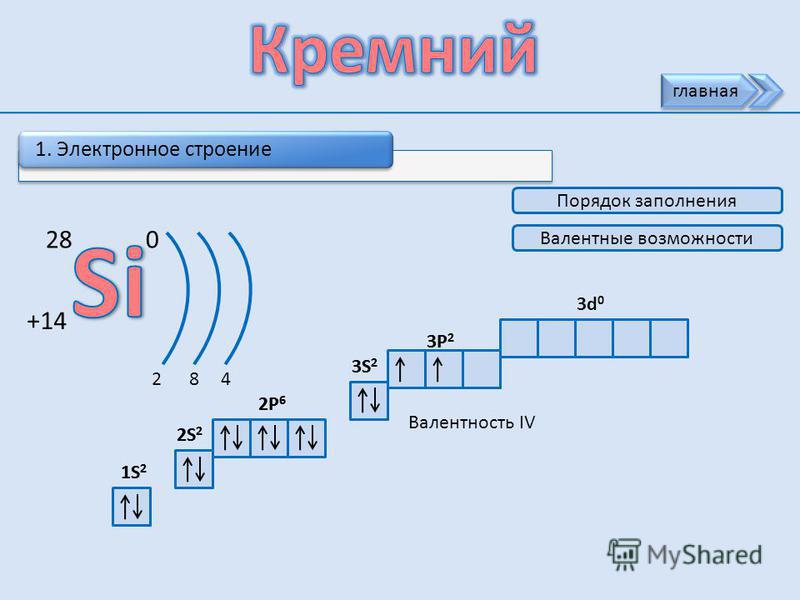

 Это число 16. Это сера S, формула её высшего оксида – SO3.
Это число 16. Это сера S, формула её высшего оксида – SO3.
 Распределению электронов в атоме этого элемента соответствует ряд чисел:
Распределению электронов в атоме этого элемента соответствует ряд чисел: Это Mg. Ему соответствует оксид ЭО.
Это Mg. Ему соответствует оксид ЭО.  Be, Mg, Ca, Sr, Ba
Be, Mg, Ca, Sr, Ba