Химический элемент – характеристика, формулы и свойства (химия, 8 класс)
4.2
Средняя оценка: 4.2
Всего получено оценок: 1137.
4.2
Средняя оценка: 4.2
Всего получено оценок: 1137.
Все многообразие окружающей нас природы состоит из сочетаний сравнительно небольшого числа химических элементов. Так какова же характеристика химического элемента, и чем он отличается от простого вещества?
Химический элемент: история открытия
В различные исторические эпохи в понятие «элемент» вкладывался различный смысл. Древнегреческие философы в качестве таких «элементов» рассматривали 4 «стихии» – тепло, холод, сухость и влажность. Сочетаясь попарно они образовывали четыре «начала» всего на свете – огонь, воздух, воду и землю.
В XVII веке Р. Бойль указал на то, что все элементы носят материальный характер и их число может быть достаточно велико.
В 1787 году французский химик А. Лавуазье создал «Таблицу простых тел». В нее вошли все известные к тому времени элементы. Под последними понимались простые тела, которые не удавалось разложить химическими методами на еще более простые. Впоследствии выяснилось, что в таблицу вошли и некоторые сложные вещества.
Под последними понимались простые тела, которые не удавалось разложить химическими методами на еще более простые. Впоследствии выяснилось, что в таблицу вошли и некоторые сложные вещества.
К моменту, когда Д. И. Менделеев открыл периодический закон, было известно всего 63 химических элементов. Открытие ученого не только привело к упорядоченной классификации химических элементов, а также помогло предсказать существование новых, еще не открытых элементов.
Рис. 1. А. Лавуазье.Что такое химический элемент?
Химическим элементом называют определенный вид атомов. В настоящее время известно 118 химических элементов. Каждый элемент обозначают символом, который представляет одну или две буквы из его латинского названия. Например, элемент водород обозначают латинской буквой H и формулой H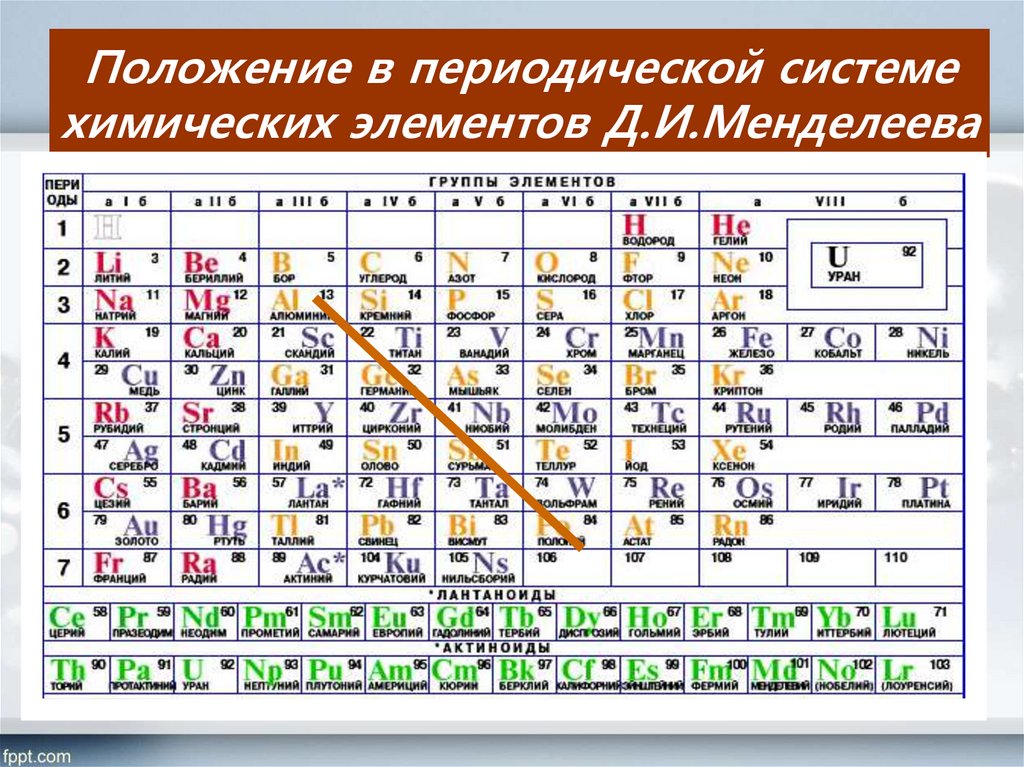
Cуществует много видов систем, но общепринятой является Периодическая система химических элементов Д. И. Менделеева, которая является графическим выражением Периодического закона Д. И. Менделеева. Обычно используют короткую и длинную формы Периодической системы.
Рис. 2. Периодическая система элементов Д. И. Менделеева.По современным представлениям, главным свойством атома, относящим его к определенному элементу, является заряд ядра. Таким образом, химический элемент – это вид атомов, характеризующихся определенным значением (величиной) части химического элемента – положительного заряда ядра.
Из всех существующих 118 химических элементов большую часть (около 90) можно обнаружить в природе.
Все элементы делятся на металлы и неметаллы. Более 80 элементов относятся к металлам. Однако это деление условное. При определенных условиях некоторые металлы могут проявлять неметаллические свойства, а некоторые неметаллы – металлические свойства.
Содержание различных элементов в природных объектах колеблется в широких пределах. 8 химических элементов (кислород, кремний, алюминий, железо, кальций, натрий, калий, магний) составляют 99% земной коры по массе, все остальные – менее 1%. Большинство химических элементов имеют природное происхождение (95), хотя некоторые из них изначально были выведены искусственно (например, прометий).
Следует различать понятия «простое вещество» и «химический элемент». Простое вещество характеризуется определенными химическими и физическими свойствами. В процессе химического превращения простое вещество утрачивает часть своих свойств и входит в новое вещество в виде элемента. Например, азот и водород, входящие в состав аммиака, содержатся в нем не в виде простых веществ, а в виде элементов.
Простое вещество характеризуется определенными химическими и физическими свойствами. В процессе химического превращения простое вещество утрачивает часть своих свойств и входит в новое вещество в виде элемента. Например, азот и водород, входящие в состав аммиака, содержатся в нем не в виде простых веществ, а в виде элементов.
Некоторые элементы объединяются в группы, такие как органогены (углерод, кислород, водород, азот), щелочные металлы (литий, натрий, калий и т.д.), лантаноиды (лантан, церий и т.д.), галогены (фтор, хлор, бром и т.д.), инертные элементы (гелий, неон, аргон)
Рис. 3. Галогены таблица.Что мы узнали?
При введении в курс химии 8 класса в первую очередь необходимо изучить понятие «химический элемент». в настоящее время известно 118 химических элементов, расположенных в таблице Д. И. Менделеева согласно возрастанию атомной массы, и имеющих основно-кислотные свойства.
Тест по теме
Доска почёта
Чтобы попасть сюда – пройдите тест.
Егор Митряшкин
8/10
Маргарита Побытова
10/10
Александр Котков
10/10
Александр Котков
10/10
Регина Медникова
10/10
Александр Котков
10/10
Сергей Ефремов
8/10
Анастасия Меркер
7/10
Сергей Макаров
10/10
Настя Хон
6/10
Оценка доклада
4.2
Средняя оценка: 4.2
Всего получено оценок: 1137.
А какая ваша оценка?
Презентация по химии Периодическая таблица Менделеева (8 класс) доклад, проект
ГБОУРК «Евпаторийская санаторная
школа-интернат»
Урок химии
8 класс
13.04.2018
Д. И. Менделеев (1834-1907)
И. Менделеев (1834-1907)
Тема Урока: Периодическая таблица химических элементов. Группы и периоды
Девиз урока:
У научного изучения предметов две основные или конечные цели: предвиденье и польза.
Д.И.Менделеев
Цели урока:
-Изучить структуру таблицы химических элементов;
– научиться давать характеристику элемента, пользуясь таблицей химических элементов.
Мир сложен. Он полон событий, сомнений,
И тайн бесконечных, и смелых догадок,
Как чудо природы является гений
И в этом хаосе находит порядок…
Весь мир большой: жара и стужа,
Планет круженье, свет зари…
Всё то, что видим мы снаружи,
Законом связано внутри…
Найдётся ль правило простое,
Что целый мир объединит?
Таблицу Менделеев строит,
Природы ищет алфавит.
Три буквы плода треугольного,
“П” между этими фрагментами…
Все вместе – столбик с элементами!
Птичий мех, но не пух,
И без букв последних двух,
Плюс раствор для смазки ссадин,
Что сажают дети за день;
Вместе – ряд горизонтальный
Получаем моментально.
Период – это горизонтальный ряд элементов.
Периоды обозначаются арабскими цифрами.
В периодической системе всего 7 периодов.
Группа – это вертикальный ряд элементов.
В периодической системе всего восемь групп.
Группы обозначаются римскими цифрами.
Каждая группа подразделяется на главную и побочную подгруппы.
Физкультминутка
Характеристика элемента
(примерный план)
1. Название элемента.
Название элемента.
2. Период.
4. Подгруппа.
5. Высший оксид.
6. Характер оксида.
7. Летучее водородное соединение.
8. Относительная атомная масса
Дайте характеристику элементам
1 группа
№16
3 группа
№ 35
2 группа
№19
4 группа
№56
1 вариант 2вариант
1 вариант 2 вариант
1) Б; г 1) В; г
2) Д; б 2) Д; а
3)А; д 3) А; в
4) В; а 4) Б; д
5) Г; в 5) Г; б
Задача
Элемент расположен в VII группе Периодической системы. Относительная молекулярная масса его высшего оксида 183. Найдите элемент.
Относительная молекулярная масса его высшего оксида 183. Найдите элемент.
Ответ:
Cl
Задача
«Потерялся»
Некий жилец II подъезда пришел в гости в квартиру №8 поиграть в шахматы. Кто из них кому пешку не уступил или шах поставил – неизвестно. Но только они крупно повзаимодействовали, в результате чего жилец массой 0,8 г исчез, а вместо него образовалось 1,12 г его оксида. Определите, как звали пропавшего жильца, который любил ходить в гости?
Ответ:
Ca
«Au Ni N Na I Eu – S I Li Ar»
79 28 7 11 53 63 16 53 3 18
Если вы правильно назовёте химические элементы, знаки которых записаны на доске, то из первых букв этих названий получится крылатая фраза.
ЗНАНИЕ –СИЛА!
Домашнее задание:
§51 – читать, определения учить.
География + химия
Запишите названия химических элементов, связанных с названием материков, стран, городов
Скачать презентацию
Периодический закон и Периодическая система химических элементов Д.И. Менделеева 11 класс онлайн-подготовка на
Предпосылки открытия периодического закона
В период становления науки химии ученые пытались привести в систему сведения об известных к тому времени нескольких десятков химических элементов. Эта проблема увлекла и Д. И. Менделеева. Он искал закономерности и взаимосвязи, которые бы охватывали все элементы, а не только часть из них. Менделеев считал важнейшей характеристикой элемента массу его атома. Проанализировав все известные к тому времени сведения о химических элементах и расположив их в порядке возрастания их атомных масс, в 1869 году он сформулировал периодический закон.
Формулировка закона: свойства химических элементов, простых веществ, а также состав и свойства соединений находятся в периодической зависимости от значения атомных масс.
К моменту формулировки периодического закона еще не было известно строение атома и существования элементарных частиц. Также впоследствии было установлено, что от атомных масс свойства вещества не зависят, как это предполагал Менделеев. Хотя, не обладая этими сведениями, Д. И. Менделеев не сделал в своей таблице ни единой ошибки.
После открытия Мозли, который установил экспериментально, что заряд ядра атома совпадает с порядковым номером химического элемента, указанным Менделеевым в его таблице, в формулировку его закона внесли изменения.
Описание периодической системы
Современная формулировка закона: свойства химических элементов, простых веществ, а также состав и свойства соединений находятся в периодической зависимости от значений зарядов ядер атомов.
Графическим выражением периодического закона является Периодическая система химических элементов Д. И. Менделеева (рис. 1).
Рис. 1
Рассмотрим принятые в ней обозначения на примере рубидия (рис. 2).
Рис. 2
В каждой ячейке, соответствующей элементу, представлены: химический символ, название, порядковый номер, соответствующий числу протонов в атоме, относительная атомная масса. Число электронов в атоме соответствует числу протонов. Количество нейтронов в атоме можно найти по разности между относительной атомной массой и количеством протонов, т. е. порядкового номера.
| N(n0) | = | Ar | – | Z |
| Количество нейтронов |
относительная атомная масса |
порядковый номер элемента |
Например, для изотопа хлора 35Cl количество нейтронов равно: 35-17 = 18
Составными частями периодической системы являются группы и периоды.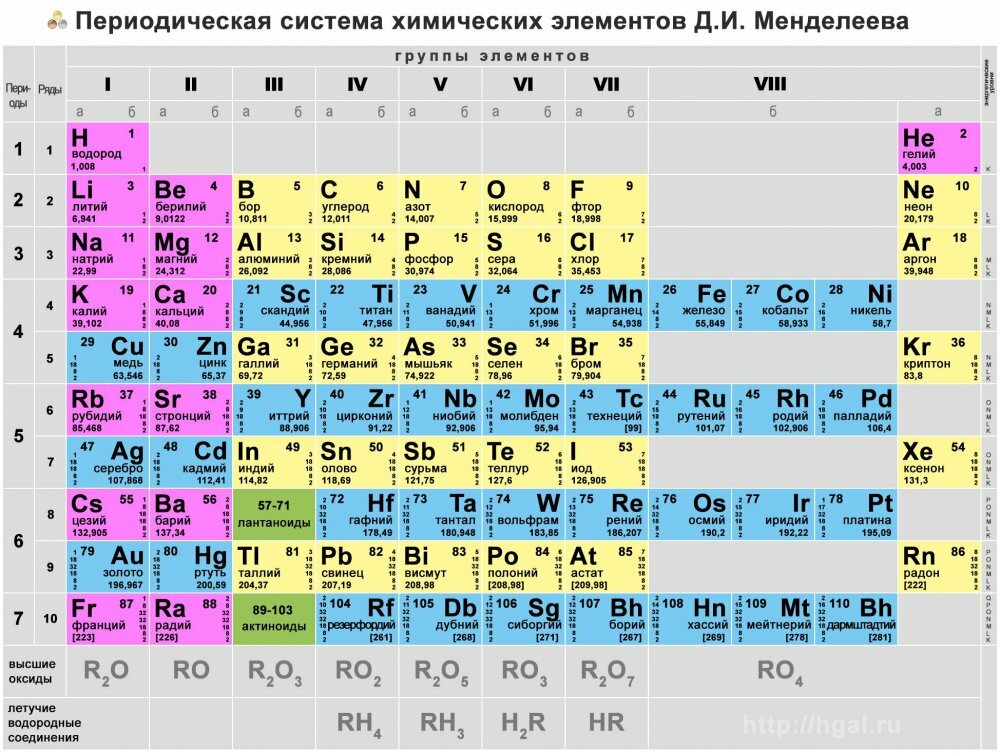
Периодическая система содержит восемь групп элементов. Каждая группа состоит их двух подгрупп: главной и побочной. Главные обозначены буквой а, а побочные – буквой б. Главная подгруппа содержит больше элементов, чем побочная. В главной подгруппе содержатся s- и p-элементы, в побочной – d-элементы.
Понятия о группах и периодах
Группа – столбец периодической системы, в котором объединены химические элементы, обладающие химическим сходством вследствие сходных электронных конфигураций валентного слоя. Это основополагающий принцип построения периодической системы. Рассмотрим это на примере элементов первых двух групп.
Табл. 1
|
Элемент |
Конфигурация валентных электронов |
Элемент |
Конфигурация валентных электронов |
|
H |
1s1 |
|
|
|
Li |
2s1 |
Be |
2s2 |
|
Na |
3s1 |
Mg |
3s2 |
|
K |
4s1 |
Ca |
4s2 |
|
Rb |
5s1 |
Sr |
5s2 |
|
Cs |
6s1 |
Ba |
6s2 |
Из таблицы видно, что элементы первой группы главной подгруппы имеют один валентный электрон. Элементы второй группы главной подгруппы имеют два валентных электрона.
Элементы второй группы главной подгруппы имеют два валентных электрона.
Некоторые главные подuруппы имеют свои особенные названия:
Табл. 2
|
I-a |
Щелочные металлы |
|
II-a |
Щелочноземельные металлы |
|
V-a |
Пниктогены |
|
VI-a |
Халькогены |
|
VII-a |
Галогены |
|
VIII-a |
Благородные (инертные) газы |
Строка, называемая периодом, – это последовательность элементов, расположенных в порядке увеличения зарядов их ядер, которая начинается с щелочного металла (или водорода) и заканчивается благородным газом.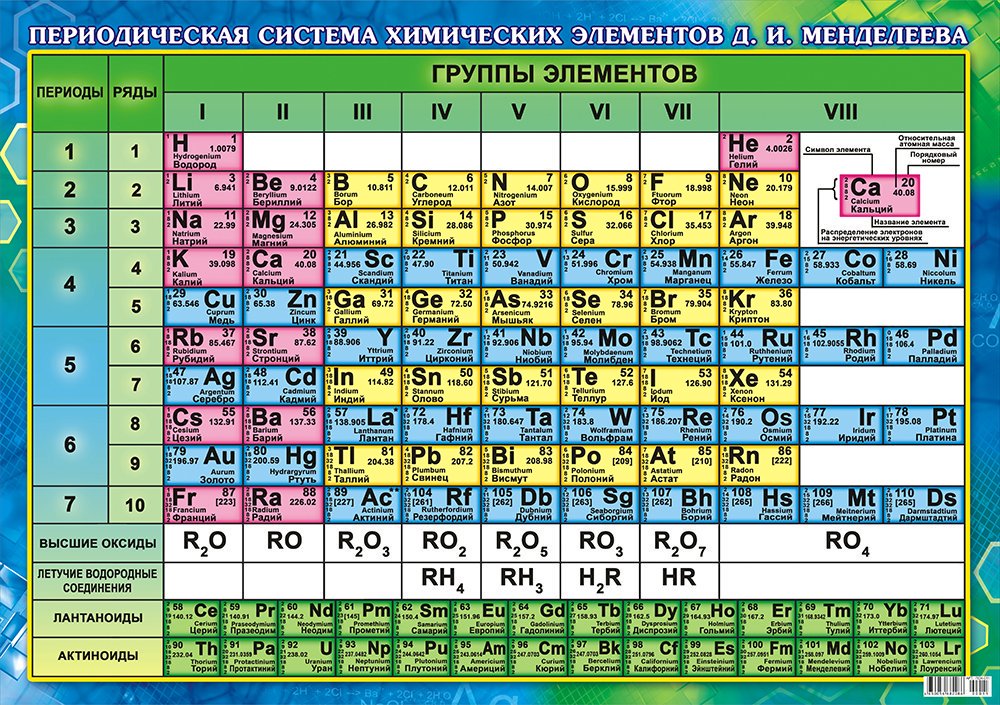
Номер периода равен количеству электронных уровней в атоме.
Существует два основных варианта представления периодической системы: длиннопериодный, в котором выделяют 18 групп (рис. 3) и короткопериодный, в котором групп 8, но вводится понятие главной и побочной подгрупп (рис. 1).
Рис. 3
Электронные конфигурации валентного слоя некоторых атомов
Периодическая повторяемость строения валентных электронов в атоме – это важнейший критерий, который объясняет и предсказывает свойства многих элементов (см. табл. 3).
Табл. 3
|
Электронные конфигурации валентного слоя атомов элементов от лития до кальция |
||||||
|
Элемент |
Li |
Be |
B |
C |
N |
O |
|
Z |
3 |
4 |
5 |
6 |
7 |
8 |
|
Электронная конфигурация |
2s1 |
2s2 |
2s22p1 |
2s22p2 |
2s22p3 |
2s22p4 |
|
Элемент |
F |
Ne |
Na |
Mg |
Al |
Si |
|
Z |
9 |
10 |
11 |
12 |
13 |
14 |
|
Электронная конфигурация |
2s22p5 |
2s22p6 |
3s1 |
3s2 |
3s23p1 |
3s23p2 |
|
Элемент |
P |
S |
Cl |
Ar |
K |
Ca |
|
Z |
15 |
16 |
17 |
18 |
19 |
20 |
|
Электронная конфигурация |
3s23p3 |
3s23p4 |
3s23p5 |
3s23p6 |
4s1 |
4s2 |
У каждой группы есть формула высшего оксида, т.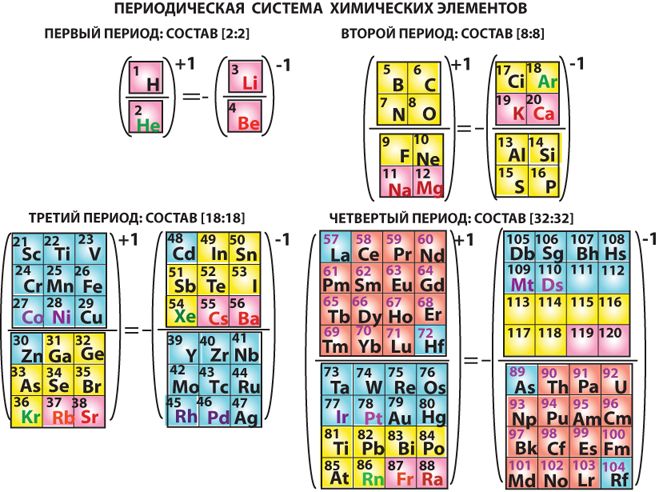 е. оксида с максимальной степенью окисления элементов. Эта информация написана внизу таблицы. Например, для элементов V группы формула высшего оксида – R2O5. Это N2O5, P2O5, As2O5,V2O5….По составу высшего оксида элемента можно определить его свойства. Оксиды состава R2O, RO основные. R2O3 – чаще всего амфотерные. Остальные оксиды – кислотные. Чем выше степень окисления элемента R,чем ярче выраженными кислотными свойствами обладает его оксид. Таким образом, кислотность высших оксидов элементов главных подгрупп увеличивается по периоду слева направо.
е. оксида с максимальной степенью окисления элементов. Эта информация написана внизу таблицы. Например, для элементов V группы формула высшего оксида – R2O5. Это N2O5, P2O5, As2O5,V2O5….По составу высшего оксида элемента можно определить его свойства. Оксиды состава R2O, RO основные. R2O3 – чаще всего амфотерные. Остальные оксиды – кислотные. Чем выше степень окисления элемента R,чем ярче выраженными кислотными свойствами обладает его оксид. Таким образом, кислотность высших оксидов элементов главных подгрупп увеличивается по периоду слева направо.
В таблице отражен состав летучих водородных соединений. Такие соединения образуют элементы IV-VII групп, причем только легких.
Изменение атомного радиуса
В группах: для элементов главных подгрупп сверху вниз увеличивается число энергетических уровней. Энергетический уровень – это и есть расстояние, на котором находится электрон от ядра. Значит, по группе вниз атомный радиус увеличивается.
Энергетический уровень – это и есть расстояние, на котором находится электрон от ядра. Значит, по группе вниз атомный радиус увеличивается.
В периодах: по периоду номер энергетического уровня, на котором находятся валентные электроны, остается неизменным, но число валентных электронов увеличивается, а также растет и заряд ядра. Значит, электроны электростатически сильнее притягиваются к ядру. Поэтому радиус атома уменьшается.
Электроотрицательность
Электроотрицательность – это способность атома перетягивать на себя электроны связи.
Это величина, которая отражает «желание» атома отдать свои валентные электроны или принять чужие валентные электроны. Чем выше электроотрицательность, тем сильнее атом хочет принять чужие валентные электроны. Существует несколько основных шкал электроотрицательности. Электроотрицательность можно выразить количественно и выстроить элементы в ряд по ее возрастанию. Наиболее часто используют шкалу электроотрицательностей, предложенную американским химиком Л. Полингом. Электроотрицательность (X) измеряется в относительных величинах (таблица 4).
Электроотрицательность можно выразить количественно и выстроить элементы в ряд по ее возрастанию. Наиболее часто используют шкалу электроотрицательностей, предложенную американским химиком Л. Полингом. Электроотрицательность (X) измеряется в относительных величинах (таблица 4).
|
Элемент |
Х |
Элемент |
Х |
|
Cs |
0,79 |
H |
2,20 |
|
K |
0,82 |
C |
2,55 |
|
Na |
0,93 |
S |
2,58 |
|
Li |
0,98 |
I |
2,66 |
|
Ca |
1,00 |
Br |
2,96 |
|
Mg |
1,31 |
N |
3,04 |
|
Be |
1,57 |
Cl |
3,16 |
|
Si |
1,90 |
O |
3,44 |
|
B |
2,04 |
F |
3,98 |
|
P |
2,19 |
|
|
Таблица 4.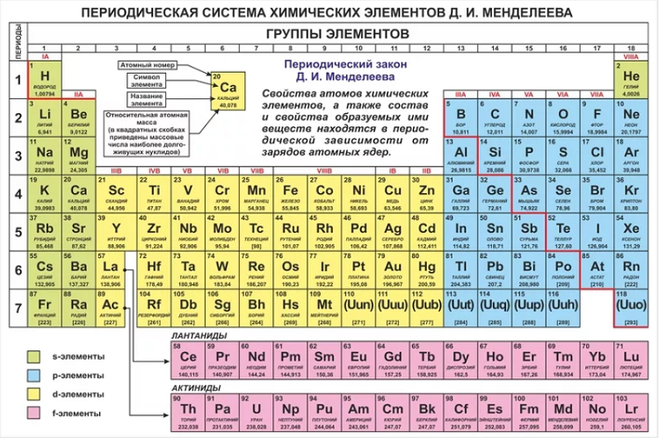 Электроотрицательности (X) некоторых элементов. Данные из справочника: CRS Handbook of Chemistry and Physics (издание 2007 года).
Электроотрицательности (X) некоторых элементов. Данные из справочника: CRS Handbook of Chemistry and Physics (издание 2007 года).
Электроотрицательность по Полингу – это свойство атомов, связанных химическими связями, т. е. находящихся в составе химических соединений. Соединения таких благородных элементов, как гелий, неон и аргон до сих пор не получены, поэтому не определена и ЭО этих элементов. Однако в полной таблице в приложении VII уже можно найти значения для ксенона (Xe), соединения которого с фтором и кислородом известны с 60-х годов ХХ века.
Наибольшей электроотрицательностью обладают элементы, находящиеся в правом верхнем углу Периодической системы. Соответственно, наименьшей – элементы, находящиеся в нижнем левом углу. Аналогично меняются и металлические свойства простых веществ, образованных данными элементами. Металлы легко отдают свои валентные электроны, соответственно, они имеют низкую электроотрицательность. Поэтому металлы находятся в нижнем левом углу Периодической системы, а типичные неметаллы – в правом верхнем.
Обобщение закономерностей изменения свойств в таблице
Закономерности изменения периодических свойств приведены в табл. 5.
|
Параметр |
По группе вниз |
По периоду вправо |
|
Заряд ядра |
Увеличивается |
Увеличивается |
|
Число валентных электронов |
Не меняется |
Увеличивается |
|
Число энергетических уровней |
Увеличивается |
Не меняется |
|
Радиус атома |
Увеличивается |
Уменьшается |
|
Электроотрицательность |
Уменьшается |
Увеличивается |
|
Металлические свойства |
Увеличиваются |
Уменьшаются |
|
Степень окисления в высшем оксиде |
Не меняется |
Увеличивается |
|
Степень окисления в водородных соединениях (для элементов IV-VII групп) |
Не меняется |
Увеличивается |
Табл. 5
5
Подведение итога урока
Вы узнали о строении Периодической системы элементов Д. И. Менделеева, а также о закономерностях изменения основных свойств химических элементов по ней.
Список литературы
- Рудзитис Г. Е. Химия. Основы общей химии. 11 класс: учебник для общеобразовательных учреждений: базовый уровень / Г. Е. Рудзитис, Ф. Г. Фельдман. – 14-е изд. – М.: Просвещение, 2012.
- Попель П. П. Химия: 8 кл.: учебник для общеобразовательных учебных заведений / П. П. Попель, Л. С.Кривля. – К.: ИЦ «Академия», 2008. – 240 с.: ил.
- Мануйлов А. В., Родионов В. И. Основы химии. Интернет-учебник.
Дополнительные рекомендованные ссылки на ресурсы сети Интернет
- Интернет-портал «internerurok.ru» (Источник)
- Интернет-портал «hemi.nsu.ru» (Источник)
- Интернет-портал «chemport.ru» (Источник)
- Интернет-портал «Химик» (Источник)
Домашнее задание
- №№3-5 (с.
 22) Рудзитис Г. Е. Химия. Основы общей химии. 11 класс: учебник для общеобразовательных учреждений: базовый уровень / Г. Е. Рудзитис, Ф. Г. Фельдман. – 14-е изд. – М.: Просвещение, 2012.
22) Рудзитис Г. Е. Химия. Основы общей химии. 11 класс: учебник для общеобразовательных учреждений: базовый уровень / Г. Е. Рудзитис, Ф. Г. Фельдман. – 14-е изд. – М.: Просвещение, 2012. - Сравните электронную конфигурацию атомов углерода и кремния. Какую валентность и степени окисления они могут проявлять в химических соединениях? Приведите формулы соединений этих элементов с водородом. Приведите формулы их соединений с кислородом в высшей степени окисления.
- Напишите электронные формулы внешних оболочек следующих элементов: 14Si, 15P, 16S, 17Cl, 34Se, 52Te. Три элемента из этого ряда являются химическими аналогами (проявляют похожие химические свойства). Какие это элементы?
Периодическая таблица элементов, используемых для 8 класса и старшей школы: Заполните и подпишите онлайн Периодическая таблица элементов
, используемая для 8 класса и старшей школы: Заполните и подпишите онлайн | докхаб- org/BreadcrumbList”>
- Дом
- Периодическая таблица элементов, используемая для 8 класса и старшей школы
4.7 из 5
43 голоса
DocHub Отзывы
44 отзыва
DocHub Отзывы
23 оценки
15 005
10 000 000+
303
100 000+ пользователей
Вот как это работает
01. Редактируйте свою периодическую таблицу элементов для восьмого класса и старшей школы Калифорнии онлайн
Введите текст, добавьте изображения, затемните конфиденциальные данные, добавьте комментарии, выделение и многое другое.
02. Подпишите в несколько кликов
Нарисуйте свою подпись, введите ее, загрузите изображение или используйте мобильное устройство в качестве панели для подписи.
03. Поделитесь своей формой с другими
Отправьте периодическую таблицу элементов 8 класса по электронной почте, ссылке или факсу. Вы также можете скачать его, экспортировать или распечатать.
Как редактировать периодическую таблицу элементов, используемых в 8 классе и старшей школе с помощью DocHub
9.5Простота настройки
Рейтинги пользователей DocHub на G2
9.0Простота использования
Рейтинги пользователей DocHub на G2
Как редактировать периодические таблица используемых элементов для 8 класса и старшей школы в формате PDF онлайн
Работать с документами с помощью нашего универсального и удобного PDF-редактора очень просто. Следуйте приведенным ниже инструкциям, чтобы легко и быстро заполнить периодическую таблицу элементов, используемых для 8 класса и старшей школы онлайн:
- Войдите в свою учетную запись .
 Войдите под своими учетными данными или зарегистрируйте бесплатную учетную запись, чтобы попробовать продукт перед обновлением подписки.
Войдите под своими учетными данными или зарегистрируйте бесплатную учетную запись, чтобы попробовать продукт перед обновлением подписки. - Импорт формы . Перетащите файл со своего устройства или импортируйте его из других служб, таких как Google Диск, OneDrive, Dropbox или по внешней ссылке.
- Редактировать периодическую таблицу элементов, используемых для 8 класса и старшей школы . С легкостью добавляйте и выделяйте текст, вставляйте изображения, галочки и символы, удаляйте новые заполняемые поля, а также переупорядочивайте или удаляйте страницы из документа.
- Получите периодическую таблицу элементов, используемую для 8 класса и старшей школы . Загрузите скорректированный документ, экспортируйте его в облако, распечатайте из редактора или поделитесь им с другими с помощью общей ссылки или в виде вложения электронной почты.
Воспользуйтесь преимуществами DocHub, самого простого редактора для быстрого управления документацией в Интернете!
будьте готовы получить больше
Заполните эту форму за 5 минут или меньше
Получить форму
Есть вопросы?
У нас есть ответы на самые популярные вопросы наших клиентов. Если вы не можете найти ответ на свой вопрос, пожалуйста, свяжитесь с нами.
Если вы не можете найти ответ на свой вопрос, пожалуйста, свяжитесь с нами.
Свяжитесь с нами
Сколько элементов всего 2021?
Сегодня, когда известно 118 элементов, он считается одним из самых значительных достижений в науке.
Есть ли 119элементы?
Унуненний, также известный как эка-франций или элемент 119, является гипотетическим химическим элементом с символом Uue и атомным номером 119…. Какой самый новый элемент в периодической таблице 2022?
По состоянию на 2022 год элементом с самым высоким известным атомным номером является оганесон (Z = 118), который завершает седьмой период (строку) в периодической таблице.
Как называются элементы 13 и 14 группы?
Элементы группы 13 также известны как элементы Р-блока, это – бор, алюминий, галлий, индий, таллий. Элементы блока P или элементы группы 13 подробно обсуждаются в разделе 11, называемом элементами блока P, в книге NCERT по химии класса 11.
Каково использование класса 8 периодической таблицы?
Ученые используют периодическую таблицу для быстрого поиска информации об элементе, такой как атомная масса и химический символ. Устройство периодической таблицы также позволяет ученым различать тенденции в свойствах элементов, включая электроотрицательность, энергию ионизации и атомный радиус.
периодическая таблица элементов, используемых в 8 классе и старшей школе
периодическая таблица cr
Связанные формы
будьте готовы получить больше
Заполните эту форму менее чем за 5 минут
Получить форму
Люди также спрашивают
Что такое 13-й элемент в периодической таблице?
Алюминий. Информация об элементе, свойства и использование | Периодическая таблица.
Информация об элементе, свойства и использование | Периодическая таблица.
Как вы объясняете периодическую таблицу учащимся?
Периодическая таблица упорядочивает элементы в строках и столбцах. В строках элементы располагаются в порядке их порядкового номера. Столбцы образуют группы элементов со схожими химическими свойствами. Например, некоторые газы находятся в одной колонке, а металлы — в другой.
Что такое класс 8 периодической таблицы?
Что такое периодическая таблица? Периодическая таблица представляет собой расположение всех элементов, известных человеку, в соответствии с их возрастающим атомным номером и повторяющимися химическими свойствами. Они расположены в виде таблицы, где строка представляет собой точку, а столбец — группу.
Сколько элементов в периодической таблице 2022 года?
Это список из 118 химических элементов, идентифицированных по состоянию на 2022 год. Химический элемент, часто называемый просто элементом, представляет собой тип атома, который имеет одинаковое количество протонов в атомном ядре (т. е. атомный номер или Z).
Почему мы используем периодическую таблицу?
Резюме. Подводя итог, можно сказать, что периодическая таблица важна, потому что она организована таким образом, чтобы предоставить большой объем информации об элементах и о том, как они соотносятся друг с другом, в одном простом в использовании справочнике. Таблицу можно использовать для предсказания свойств элементов, даже тех, которые еще не открыты.
Периодическая таблица элементов, используемых в 8 классе и старшей школе
Свойства металлов, металлоидов и неметаллов – Википедия
Химические элементы можно разделить на металлы, металлоиды и неметаллы в соответствии с их общими физическими и химическими свойствами .
Подробнее
ERIC – Результаты поиска – Департамент образования
Результаты 1 – 15 из 50 — Эта работа посвящена изучению способности учащихся старших классов использовать периодическую таблицу элементов для решения проблемных задач.
Узнать больше
Периодическая таблица элементов — Американское химическое общество
Периодическая таблица химических элементов, которую часто называют периодической таблицей, объединяет все обнаруженные химические элементы в строки (называемые периодами) и столбцы .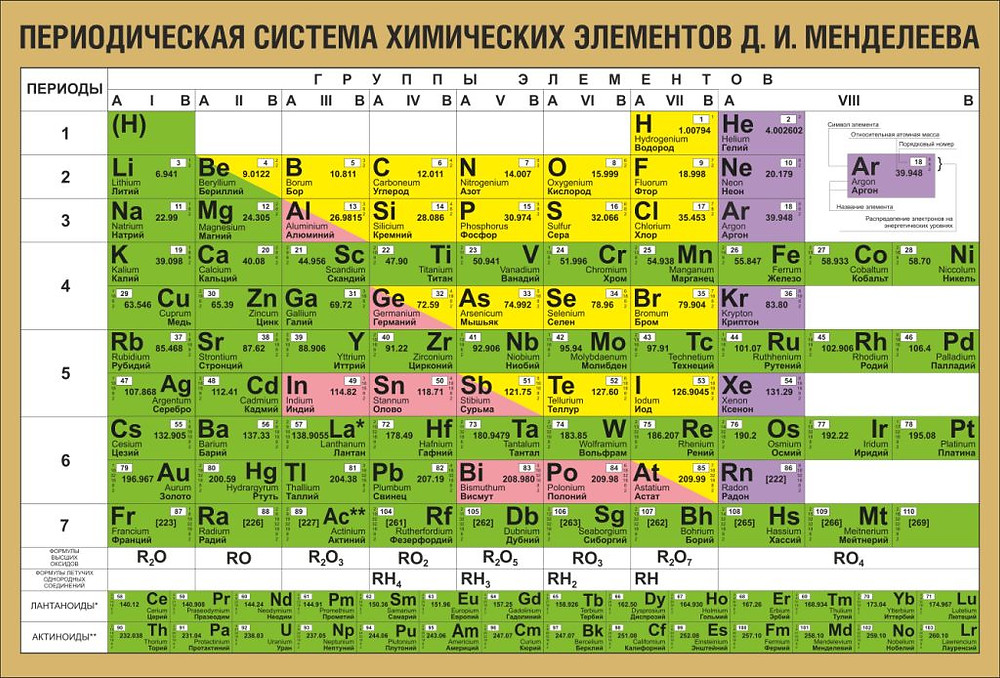 ..
..
Узнать больше
Попробуйте другие инструменты PDF
© 2022 ООО «ДокХаб»
открытых учебников | Siyavula
Загрузите наши открытые учебники в различных форматах, чтобы использовать их так, как вам удобно. Нажмите на обложку каждой книги, чтобы увидеть доступные для загрузки файлы на английском и африкаанс. Лучше, чем просто бесплатные, эти книги также имеют открытую лицензию! См. различные открытые лицензии для каждой загрузки и пояснения к лицензиям в нижней части страницы.
Математика
- Читать онлайн
Учебники
Английский
- 7A PDF (CC-BY-ND)
- 7B PDF (CC-BY-ND)
Африкаанс
- 7A PDF (CC-BY-ND)
- 7B PDF (CC-BY-ND)
- Читать онлайн
Учебники
Английский
- 8A PDF (CC-BY-ND)
- 8B PDF (CC-BY-ND)
Африкаанс
- 8A PDF (CC-BY-ND)
- 8B PDF (CC-BY-ND)
- Читать онлайн
Учебники
Английский
- 9A PDF (CC-BY-ND)
- 9B PDF (CC-BY-ND)
Африкаанс
- 9A PDF (CC-BY-ND)
- 9B PDF (CC-BY-ND)
- Читать онлайн
Учебники
Английский
- PDF (CC-BY-ND)
- ePUB (CC-BY-ND)
- ePUB (CC-BY)
Африкаанс
- PDF (CC-BY-ND)
- ePUB (CC-BY-ND)
- ePUB (CC-BY)
Пособия для учителя
Английский
- PDF (CC-BY-ND)
Африкаанс
- PDF (CC-BY-ND)
- Читать онлайн
Учебники
Английский
- PDF (CC-BY-ND)
- ePUB (CC-BY-ND)
- ePUB (CC-BY)
Африкаанс
- PDF (CC-BY-ND)
- ePUB (CC-BY-ND)
- ePUB (CC-BY)
Пособия для учителя
Английский
- PDF (CC-BY-ND)
Африкаанс
- PDF (CC-BY-ND)
- Читать онлайн
Учебники
Английский
- PDF (CC-BY-ND)
- ePUB (CC-BY-ND)
- ePUB (CC-BY)
Африкаанс
- PDF (CC-BY-ND)
- ePUB (CC-BY-ND)
- ePUB (CC-BY)
Пособия для учителя
Английский
- PDF (CC-BY-ND)
Африкаанс
- PDF (CC-BY-ND)
- Читать онлайн
Учебники
Английский
- PDF (CC-BY-ND)
- ePUB (CC-BY-ND)
- ePUB (CC-BY)
Африкаанс
- PDF (CC-BY-ND)
- ePUB (CC-BY-ND)
- ePUB (CC-BY)
Пособия для учителя
Английский
- PDF (CC-BY-ND)
Африкаанс
- PDF (CC-BY-ND)
Наука
- Читать онлайн
Учебники
Английский
- PDF (CC-BY-ND)
- ePUB (CC-BY-ND)
- ePUB (CC-BY)
Африкаанс
- PDF (CC-BY-ND)
Пособия для учителя
Английский
- PDF (CC-BY-ND)
Африкаанс
- PDF (CC-BY-ND)
- Читать онлайн
Учебники
Английский
- PDF (CC-BY-ND)
- ePUB (CC-BY-ND)
- ePUB (CC-BY)
Африкаанс
- PDF (CC-BY-ND)
- ePUB (CC-BY-ND)
- ePUB (CC-BY)
Пособия для учителя
Английский
- PDF (CC-BY-ND)
Африкаанс
- PDF (CC-BY-ND)
- Читать онлайн
Учебники
Английский
- PDF (CC-BY-ND)
- ePUB (CC-BY-ND)
- ePUB (CC-BY)
Африкаанс
- PDF (CC-BY-ND)
- ePUB (CC-BY-ND)
- ePUB (CC-BY)
Пособия для учителя
Английский
- PDF (CC-BY-ND)
Африкаанс
- PDF (CC-BY-ND)
- Читать онлайн
Учебники
Английский
- PDF (CC-BY-ND)
- ePUB (CC-BY-ND)
- ePUB (CC-BY)
Африкаанс
- PDF (CC-BY-ND)
- ePUB (CC-BY-ND)
- ePUB (CC-BY)
Пособия для учителя
Английский
- PDF (CC-BY-ND)
Африкаанс
- PDF (CC-BY-ND)
- Читать онлайн
Учебники
Пособия для учителя
Английский
Класс 7А
- PDF (CC-BY-ND)
Класс 7Б
- PDF (CC-BY-ND)
Африкаанс
Граад 7А
- PDF (CC-BY-ND)
Граад 7Б
- PDF (CC-BY-ND)
- Читать онлайн
Учебники
Пособия для учителя
Английский
Класс 8А
- PDF (CC-BY-ND)
Класс 8Б
- PDF (CC-BY-ND)
Африкаанс
Граад 8А
- PDF (CC-BY-ND)
Граад 8Б
- PDF (CC-BY-ND)
- Читать онлайн
Учебники
Пособия для учителя
Английский
Класс 9А
- PDF (CC-BY-ND)
Класс 9Б
- PDF (CC-BY-ND)
Африкаанс
Граад 9А
- PDF (CC-BY-ND)
Граад 9Б
- PDF (CC-BY-ND)
- Читать онлайн
Учебники
Пособия для учителя
Английский
Класс 4А
- PDF (CC-BY-ND)
Класс 4Б
- PDF (CC-BY-ND)
Африкаанс
Граад 4А
- PDF (CC-BY-ND)
Граад 4Б
- PDF (CC-BY-ND)
- Читать онлайн
Учебники
Пособия для учителя
Английский
Класс 5А
- PDF (CC-BY-ND)
Класс 5Б
- PDF (CC-BY-ND)
Африкаанс
Граад 5А
- PDF (CC-BY-ND)
Граад 5Б
- PDF (CC-BY-ND)
- Читать онлайн
Учебники
Пособия для учителя
Английский
Класс 6А
- PDF (CC-BY-ND)
Класс 6Б
- PDF (CC-BY-ND)
Африкаанс
Граад 6А
- PDF (CC-BY-ND)
Граад 6Б
- PDF (CC-BY-ND)
Лицензирование наших книг
Лучше, чем просто бесплатные, эти книги также имеют открытую лицензию! Один и тот же контент, но разные версии (фирменные или нет) имеют разные лицензии, как объяснено:
CC-BY-ND (фирменные версии)
Вам разрешается и поощряется свободное копирование этих версий. Вы можете копировать, распечатывать и распространять их столько раз, сколько захотите. Вы можете загрузить их на свой мобильный телефон, iPad, ПК или флешку. Вы можете записать их на компакт-диск, отправить по электронной почте или загрузить на свой веб-сайт. Единственное ограничение заключается в том, что вы не можете каким-либо образом адаптировать или изменять эти версии учебников, их содержание или обложки, поскольку они содержат соответствующие бренды Siyavula, логотипы спонсоров и одобрены Департаментом базового образования. Для получения дополнительной информации посетите сайт Creative Commons Attribution-NoDerivs 3.0 Unported.
Вы можете копировать, распечатывать и распространять их столько раз, сколько захотите. Вы можете загрузить их на свой мобильный телефон, iPad, ПК или флешку. Вы можете записать их на компакт-диск, отправить по электронной почте или загрузить на свой веб-сайт. Единственное ограничение заключается в том, что вы не можете каким-либо образом адаптировать или изменять эти версии учебников, их содержание или обложки, поскольку они содержат соответствующие бренды Siyavula, логотипы спонсоров и одобрены Департаментом базового образования. Для получения дополнительной информации посетите сайт Creative Commons Attribution-NoDerivs 3.0 Unported.
Узнайте здесь больше о спонсорстве и партнерстве с другими, которые сделали возможным выпуск каждого из открытых учебников.
CC-BY (версии без торговой марки)
Эти версии одного и того же контента без торговой марки доступны для вас, чтобы вы могли делиться ими, адаптировать, преобразовывать, изменять или развивать их любым способом, при этом единственным требованием является предоставление соответствующей ссылки на Siyavula. Для получения дополнительной информации посетите Creative Commons Attribution 3.0 Unported.
Для получения дополнительной информации посетите Creative Commons Attribution 3.0 Unported.
Восьмой класс (8 класс) Таблица Менделеева и элементы Вопросы для тестов и рабочих листов
Выбрать все вопросыВодород находится в группе Периодической таблицы.
- 1
- 2
- 3
- 4
Количество протонов в ядре атома этого элемента равно .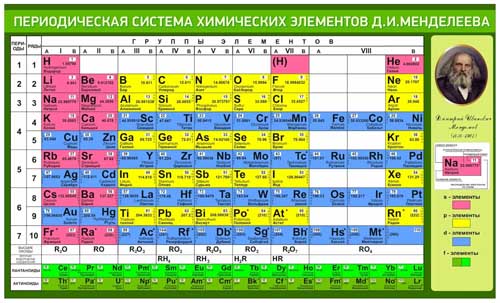
- атомный номер
- атомный вес
- массовое число
- изотопы
A(n) — это чистое вещество, которое нельзя разложить на более простые вещества химическими или физическими средствами.
- сложный
- элемент
- молекула
- смесь
Что лучше всего описывает кислород?
- Кислород – это галоген.

- Кислород неметалл.
- Кислород – благородный газ.
- Кислород — редкоземельный элемент.
В современной Периодической таблице элементы расположены
- по атомной массе.
- по атомному номеру.
- в алфавитном порядке.
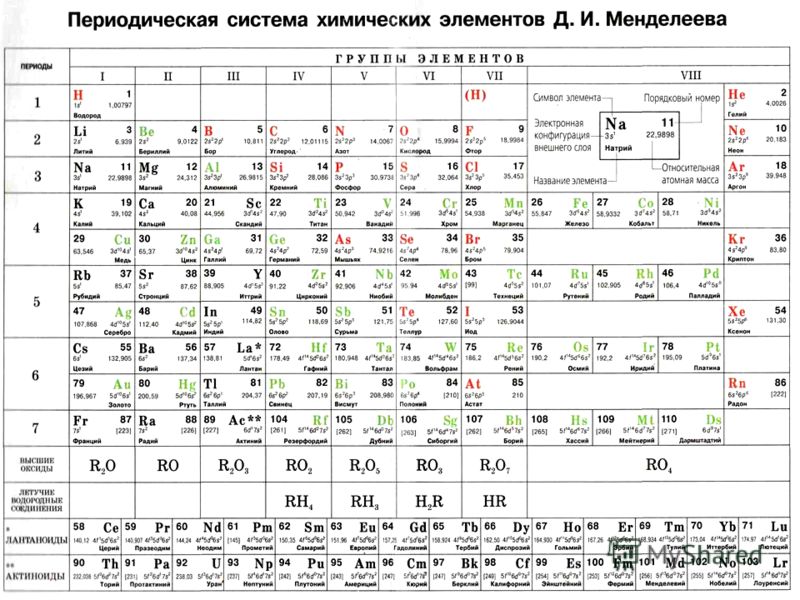
- по количеству нейтронов в их ядрах.
Атомный номер атома определяется числом .
- протоны
- нейтроны
- электроны
- изотопы
Периодическая таблица состоит из 7 групп.
- Истинный
- ЛОЖЬ
Сколько нейтронов в атоме хлора?
- 16
- 17
- 18
- 35
Что такое медь?
- Медь
- Цинк
Наименьшая единица элемента, сохраняющая свойства этого элемента, — это a(n) .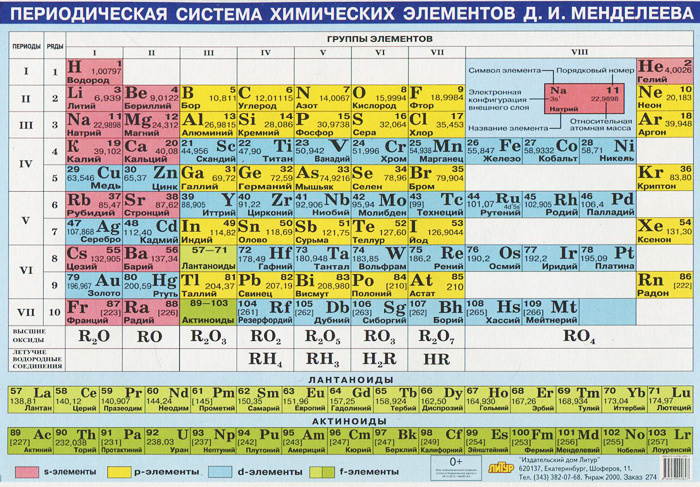
- атом
- молекула
- сложный
- коллоид
Какой атомный номер водорода?
- 0
- 1
- 2
- 3
В Периодической таблице вертикальные столбцы, идущие вниз по Периодической таблице, называются .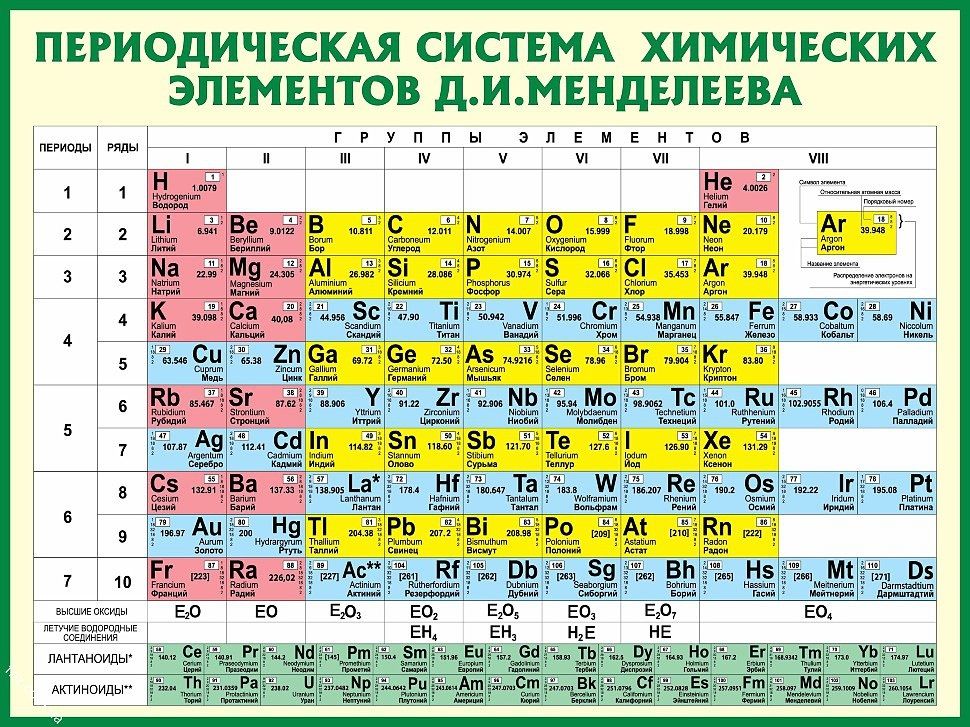
- периоды
- группы
- классы
Символ олова Sb.
- Истинный
- ЛОЖЬ
Медь находится в группе 4 и периоде 11 периодической таблицы.
- Истинный
- ЛОЖЬ
Первая Периодическая таблица была составлена .
- атомный номер
- атомная масса
- химический символ
Алюминий — это металл, находящийся в четвертом столбце периодической таблицы. Какое утверждение верно относительно алюминия и других элементов в этой колонке?
- Все элементы нереакционноспособны.
- Все элементы находятся в одном периоде.
- Все элементы имеют одинаковое количество протонов.
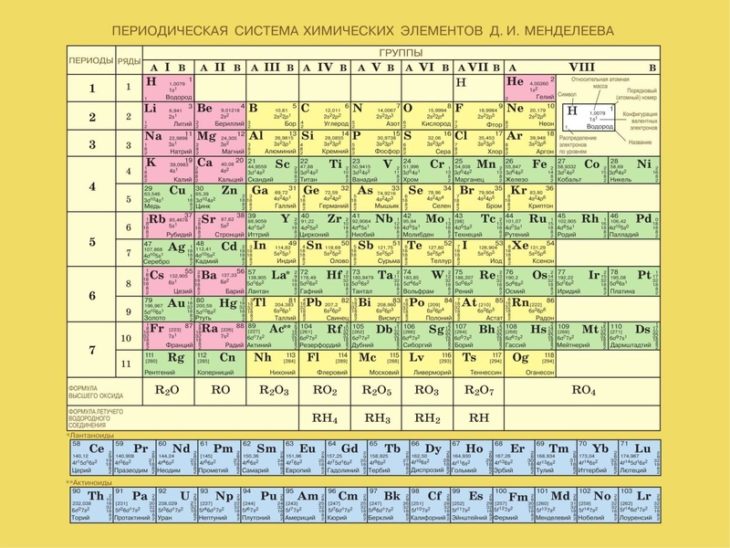
- Все элементы имеют схожие химические свойства.
Атомный номер золота 79.
- Истинный
- ЛОЖЬ
Этот вопрос является частью группы с общими инструкциями. Посмотреть группу »
Периодическая таблица организована таким образом, что периоды пронумерованы и пронумерованы
- по горизонтали.
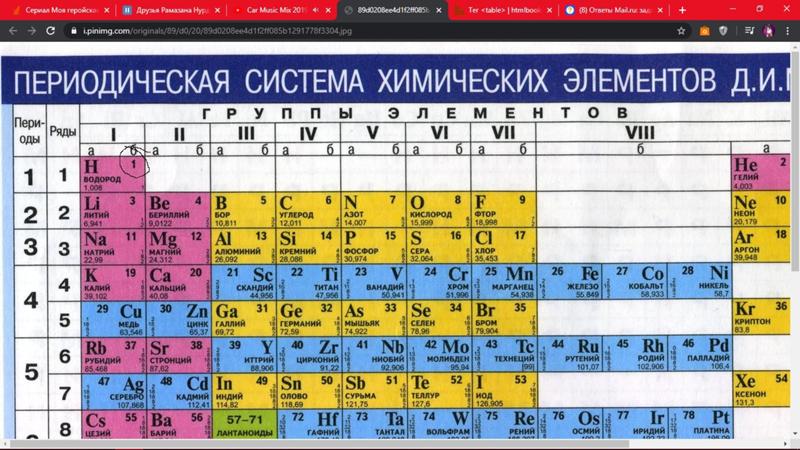
- вертикально.
- по диагонали.
- в восьмерке.
Какой элемент имеет 4 нейтрона?
- элемент с атомным номером 2 и атомной массой 4
- элемент с атомным номером 3 и атомной массой 7
- элемент с атомным номером 4 и атомной массой 9
- элемент с атомным номером 7 и атомной массой 14
Современная Периодическая таблица организована .
