Периодическая таблица в пространстве и времени
Борис Шустов
В 2019 году мы празднуем 150‑летие открытия великого Периодического закона, суть которого выражена в Периодической таблице химических элементов. Выдающийся русский ученый Дмитрий Иванович Менделеев по праву считается отцом Периодического закона, и у россиян есть повод для гордости.
К 1 марта 1869 года (официальная дата открытия закона) было известно немногим более 60 элементов, причем часть сведений являлась ошибочной. Но Менделееву удалось сложить этот замысловатый пазл и построить основу системного знания, на котором строится современная наука и, в общем-то, современная цивилизация.
Периодическая таблица химических элементов — одно из наиболее значительных достижений в науке, охватывающих суть не только химии, но и физики, и астрофизики, и даже биологии. Это уникальный инструмент, позволяющий изучать свойства вещества во всей Вселенной, включая Землю и нас самих.
Основной закон Вселенной состоит в том, что она постоянно меняется. Все ее свойства: структурные, тепловые, ионизационные и, конечно же, химические, изменяются на протяжении уже почти 13,8 миллиардов лет (это современная оценка возраста Вселенной). Временные и пространственные шкалы этих изменений очень сильно отличаются. И всё это происходило, происходит и будет происходить взаимосвязано. В студенческие годы мы все знакомились с принципом материального единства мира. Это были немного абстрактные (а временами скучноватые) философские положения, но с накоплением научных знаний углублялось понимание сложного и эволюционного переплетения взаимосвязей во Вселенной.
Начало (первичный нуклеосинтез)
В самом начале (когда возраст Вселенной составлял малые доли секунды) вещество было разогрето до столь высоких температур, и в нем присутствовало настолько много мощных фотонов, что эти фотоны разбивали любые микроструктуры вещества Вселенной, и оно представляло собой простейшую смесь элементарных частиц, поведение и состав которых определяются Стандартной моделью физики элементарных частиц.

Для составления первой таблицы химических элементов было бы достаточно лишь нескольких ячеек, но космологи заинтересованы в точном знании содержания элементов в этой таблице, поскольку точное содержание этих самых первых химических элементов является критически важным для космологических теорий.
Нуклеосинтез в первых звездах
Вещество первичного состава, то есть, практически полностью лишенное тяжелых элементов (по традиции все элементы тяжелее 4He называют металлами), часто называют «космологическим». Считается, что именно из такого вещества примерно через сто миллионов лет после Большого взрыва образовались первые звезды (ПЗ) во Вселенной, называемые также «населением III».
По-видимому, эпоха ПЗ была очень короткой, так как время жизни звезд с такой массой составляло несколько миллионов лет, после чего они взрывались и выбрасывали продукты звездного нуклеосинтеза в окружающий водородно-гелиевый газ. Вновь образующиеся из этого газа звезды (их называют звездами населения II) уже имели в своем составе некоторое количество металлов. Металлы — прекрасные охладители, так что практически скачком произошел переход от необычных звезд населения III к «обычным».
Звездный нуклеосинтез
В популярной песне поется: «Мы — дети Галактики». Это не совсем точно. Мы все — дети звезд (космических объектов). Дети звезд эстрады, спорта, политики и так далее в этом плане «как все». Большая часть химических элементов родились в недрах звезд — этих природных ядерных реакторах. С появлением звезд начался процесс ядерного синтеза, и в результате мы получили такое удивительное разнообразие химических элементов.
Сейчас она содержит 118 элементов. Восемьдесят стабильных элементов и четыре радиоактивных считаются первичными, то есть космического происхождения. Остальные 34 обнаружены после того, как они были получены синтетически. Современные представления об источниках отдельных (групп) химических элементов представлены на известной диаграмме (из https://commons.wikimedia.org/wiki/File:Elements-origin-ru.svg).
Эта красивая картинка — не икона. Здесь кроется еще множество нерешенных проблем.
Как путешествуют в космосе элементы периодической таблицы
Итак, элементы тяжелее гелия рождаются в звездах, которые обычно сосредоточены в галактиках. Часть этого богатства навсегда погребена в недрах потухших звезд, но значительная часть была выброшена в космос в результате потери массы звездами и грандиозных звездных взрывов. Эти элементы входят в межзвездное вещество (газ и пыль), из которого образовались и образуются новые звезды и планеты. Значительная часть тяжелых элементов покидает галактики и улетает в глубины межгалактического пространства. Интересно, что даже очень далеко от галактик в пустотах (англ. voids), которые считаются самыми пустыми областями Вселенной, обнаруживаются тяжелые элементы. Поскольку элементы не могли там родиться, нужно объяснить, как они переносятся в межгалактическую среду (МГС) и гораздо дальше, в пустоты.
Эти элементы входят в межзвездное вещество (газ и пыль), из которого образовались и образуются новые звезды и планеты. Значительная часть тяжелых элементов покидает галактики и улетает в глубины межгалактического пространства. Интересно, что даже очень далеко от галактик в пустотах (англ. voids), которые считаются самыми пустыми областями Вселенной, обнаруживаются тяжелые элементы. Поскольку элементы не могли там родиться, нужно объяснить, как они переносятся в межгалактическую среду (МГС) и гораздо дальше, в пустоты.
Основными механизмами потери тяжелых элементов из галактик и выброса их в МГС являются: (1) галактический ветер и (2) вынос пыли давлением звездного излучения из галактик. После выброса из галактик тяжелые элементы переносятся в остальную Вселенную. Наблюдения показывают наличие тяжелых элементов даже в огромных (10 — 100 мегапарсек) пустотах при красных смещениях z ≥ 3. Ни галактический ветер, ни выброс пыли, который мы наблюдаем в нашу эпоху, не способны принести вещество так далеко. Так что и здесь можно отметить сакраментальное «проблемы остаются».
От атомов к молекулам
Разнообразие химических элементов обусловило развитие различных процессов образования и разрушения соединений химических элементов, то есть молекул. Одним из важнейших результатов химической эволюции (для нас, а не для самой Вселенной) стало появление живых существ, которые пытаются понять, как все это произошло. Астрохимики изучают космические источники происхождения около 200 молекул (и 400 молекулярных изотопологов), наблюдаемых в космосе, включая важнейшие органические соединения, а также очень сложные химические процессы в космосе. В конечном счете, чтобы понять происхождение жизни, это знание может быть решающим.
В рамках большого химического конгресса (Менделеевского съезда), посвященного 150‑летию таблицы Менделеева и проводимого в Санкт-Петербурге в сентябре 2019 года обсуждаются многие вопросы по проблемам космического происхождения, точнее наполнения, периодической таблицы химических элементов. Название симпозиума «Периодическая таблица сквозь пространство и время» (The Periodic Table through Space and Time) говорит само за себя. На этом симпозиуме ведущие космологи, астрофизики и астрохимики планеты обсуждают современное состояние представленных выше вопросов и обмениваются новыми идеями и перспективами. Празднование 150‑летия периодической таблицы химических элементов является очень важным шагом в научном прогрессе, который никогда не остановится.
Название симпозиума «Периодическая таблица сквозь пространство и время» (The Periodic Table through Space and Time) говорит само за себя. На этом симпозиуме ведущие космологи, астрофизики и астрохимики планеты обсуждают современное состояние представленных выше вопросов и обмениваются новыми идеями и перспективами. Празднование 150‑летия периодической таблицы химических элементов является очень важным шагом в научном прогрессе, который никогда не остановится.
Шустов Борис Михайлович, член-корреспондент РАН, научный руководитель Института астрономии РАН.
как аспирант РУДН научился использовать навыки в химии для приготовления кулинарных блюд
Химию отличает от других естественных наук возможность творчески подойти к делу и найти удивительные решения давно известных задач.
Аспирант РУДН Тшепо Дифеко из Южной Африки прививает окружающим любовь к науке. Он делает это незаметно, просто ненароком напоминает, что химия окружает человека абсолютно везде — в теле, мозге, в одежде, еде, предметах быта. По мнению студента, невозможно оставаться равнодушным, ведь: «Химия — это все. Мы сталкиваемся с ней, когда пьем кофе или чай, держим в руках бумажный стаканчик или запускаем фейерверки на Новый год».
Он делает это незаметно, просто ненароком напоминает, что химия окружает человека абсолютно везде — в теле, мозге, в одежде, еде, предметах быта. По мнению студента, невозможно оставаться равнодушным, ведь: «Химия — это все. Мы сталкиваемся с ней, когда пьем кофе или чай, держим в руках бумажный стаканчик или запускаем фейерверки на Новый год».
Тшепо влюбился в химию еще в школе: поразили не только результаты красочных химических реакций, например, «фараонова змея», но и структура таблицы Менделеева, четкие химические уравнения — с химией жизнь упорядочивалась по формулам, элементам и реакциям.
Страсть к порядку и точным измерениям порошков и жидкостей плавно переместилась на кухню: «Я не лучший повар, которого вы встретите на своем пути, но зато приготовлю все с душой». Похоже, аспирант подходит к приготовлению блюд точно так же, как к подготовке исхода реакции в лаборатории: все эффектно, правильно проведено, и по-научному точно выверены объемы веществ. Но он прямо говорит, что «творчеством здесь и не пахнет». В кулинарии нужно придерживаться принципа всех серьезных ученых в белых халатах: смешивать вещества только по четкой инструкции — без лишней самодеятельности.
В кулинарии нужно придерживаться принципа всех серьезных ученых в белых халатах: смешивать вещества только по четкой инструкции — без лишней самодеятельности.
«В ЮАР не хватает специалистов в области химии, — говорит Тшепо. — С каждым годом нам нужно больше и больше людей с такими навыками для развития химической отрасли страны».
После аспирантуры Тшепо ждет работа в химической промышленности и постдокторантура — исследования открывают широчайшие возможности для продолжения научной деятельности.
Яркие научные события в России 2019: Год Менделеева
В преддверии новогодних праздников “Научная Россия” рассказала
о самых ярких событиях уходящего года в отечественной науке.
2019-й год оказался очень плодотворным для российской науки, в особенности для естественных наук. В этом году произошло беспрецедентное по своей значимости событие: объявление 2019 года Международным годом Периодической таблицы им.Д.И.Менделеева. Парадоксально, что далеко не во всех странах мира Периодическая таблица носит имя ее создателя — Дмитрия Менделеева.
Популяризация величайшего достижения в отечественной науке —
Периодического закона — и имени Менделеева стала важной
актуальной задачей для российских ученых. Именно поэтому
российская сторона обратилась к международному сообществу
с инициативой. Решение объявить 2019 год Международным годом
Периодической таблицы химических элементов было принято
Генеральной ассамблеей ООН. Год проходил под эгидой ЮНЕСКО
в России, Франции, Германии, США, Японии и других странах
мира. Провести мероприятия, посвященные 150-летию
Таблицы Менделеева, решили более 80 государств, 295 городов.
Имя российского ученого звучало на выставках и открытых уроках,
на конференциях, научных фестивалях и других событиях, проводимых
по всему земному шару.
30 января 2019 года, в Париже, в штаб-квартире ЮНЕСКО прошла Церемония открытия Международного года Периодической таблицы химических элементов. Участниками и гостями открытия стали более 1300 человек из 80 стран мира. Среди них – ученые, политики, руководители международных, научных, образовательных организаций, представители бизнес-компаний и общественных объединений.
Теме 150-летия Периодической таблицы Менделеева была посвящена одна из научных сессий общего собрания РАН, которое проходило в ноябре:
“Текущий 2019-й год объявлен годом 150-летия Периодической таблицы химических элементов Д.И.Менделеева. Эта инициатива была предложена Россией и единогласно поддержана ООН. Периодическая таблица носит имя Менделеева не везде. Поэтому подобная инициатива очень важна, чтобы закрепить этот приоритет за российской наукой”, – рассказал на общем собрании президент РАН Александр Сергеев.
“В мире были проведены десятки тысяч мероприятий. Участвовали
все шесть континентов, включая Антарктиду. Это миллионы людей,
которые слушали, делали и познавали новое. Практически все
мероприятия сопровождались докладами о биографии Менделеева. Этот
Международный год позволил сделать шаг на пути к преодолению
хемофобии”, — рассказала сопредседатель
Международного комитета по проведению Года Периодической таблицы
химических элементов, директор Института химии и проблем
устойчивого развития Наталия Тарасова.
Участвовали
все шесть континентов, включая Антарктиду. Это миллионы людей,
которые слушали, делали и познавали новое. Практически все
мероприятия сопровождались докладами о биографии Менделеева. Этот
Международный год позволил сделать шаг на пути к преодолению
хемофобии”, — рассказала сопредседатель
Международного комитета по проведению Года Периодической таблицы
химических элементов, директор Института химии и проблем
устойчивого развития Наталия Тарасова.
В России за год прошли сотни научно-популярных и образовательных мероприятий, посвященных 150-летию Таблицы Менделеева. Среди наиболее ярких — Всероссийский фестиваль NAUKA 0+, Всероссийский съезд учителей химии, XXI Менделеевский съезд по общей и прикладной химии и другие.
Периодическая система химических элементов Дмитрия Ивановича
Менделеева — одно из величайших достижений в истории.
Открытие Менделеева изменило всю мировую науку;
особенно сильно, помимо химии, оно повлияло на физику,
космологию, геохимию.
В честь ученого назван 101-й элемент Периодической таблицы — менделевий (Md). 2019 год объявлен Международным годом Периодической таблицы химических элементов Д.И.Менделеева. Финальное закрытие Международного года Таблицы Менделеева состоялось в Токио 5 декабря. В России же оно проходило 28 ноября в стенах МГУ.
На закрытии Международного года Периодической таблицы Менделеева в Токио ряд выступлений глав крупнейших научных союзов был посвящен тому, чтобы объявить 2022 год международным годом фундаментальной науки.
“Предварительные переговоры в ЮНЕСКО по этому предложению уже прошли. Заявку на год фундаментальной науки будут готовить несколько объединений, в том числе Международный союз чистой физики. Считаю, что в этом процессе Россия должна играть одну из ключевых ролей”, – сообщил глава РАН Александр Сергеев.
«В 1869 году Д.И. Менделеев впервые опубликовал свою первую
схему Периодической таблицы в статье «Соотношение свойств с
атомным весом элементов» в журнале Русского химического
общества.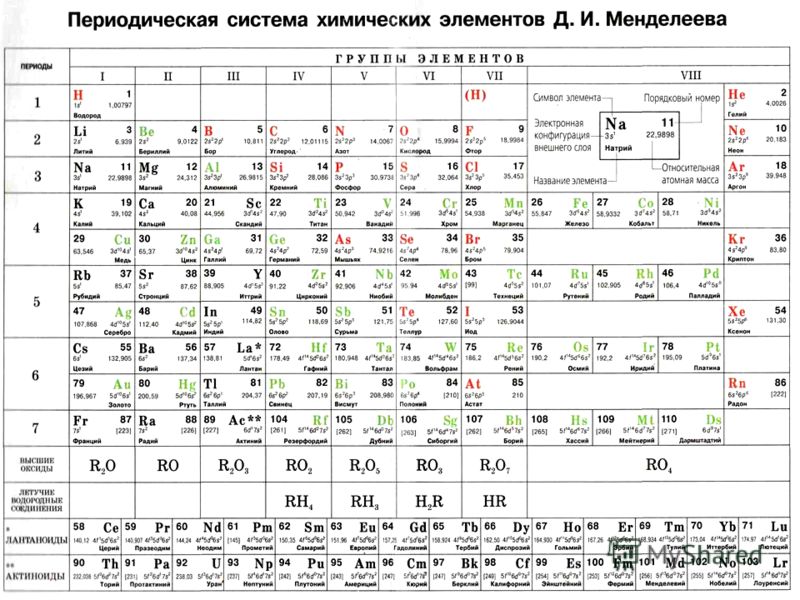 С тех пор Периодическая таблица химических элементов
является одним из самых значительных достижений в науке,
охватывая сущность не только химии, но и всех естественных
наук. Это уникальный инструмент, позволяющий ученым
прогнозировать внешний вид и свойства материи на Земле и в
остальной части Вселенной».
С тех пор Периодическая таблица химических элементов
является одним из самых значительных достижений в науке,
охватывая сущность не только химии, но и всех естественных
наук. Это уникальный инструмент, позволяющий ученым
прогнозировать внешний вид и свойства материи на Земле и в
остальной части Вселенной».
Янина Хужина
Видео
Музей-архив Д.И. Менделеева | izi.TRAVEL
Музей-архив Д.И. Менделеева на сайте СПбГУ
Музей-архив Д.И. Менделеева ВКонтакте
Музей-архив Д.И. Менделеева на Facebook
Мемориальный кабинет Д.И. Менделеева открыт в 1911 году в бывшей казенной квартире Университета в здании Двенадцати коллегий, где ученый жил с семьей с 1866 по 1890 год. Здесь открыт Периодический закон, написаны «Основы химии», выполнены работы по физике газов, экономике, промышленности и пр.
21 декабря 1911 года состоялось открытие и освящение кабинета Д. И. Менделеева (первое название музея). Кабинет скорее был хранилищем разнообразных менделеевских документов и предметов, чем музеем в полном смысле слова. В 1934 году, в связи с подготовкой к 100–летнему юбилею ученого, Кабинет Д. И. Менделеева пополнился новыми экспонатами и был открыт как музей. В подготовительной работе активное участие принял сын Дмитрия Ивановича — Иван Дмитриевич Менделеев.
Кабинет скорее был хранилищем разнообразных менделеевских документов и предметов, чем музеем в полном смысле слова. В 1934 году, в связи с подготовкой к 100–летнему юбилею ученого, Кабинет Д. И. Менделеева пополнился новыми экспонатами и был открыт как музей. В подготовительной работе активное участие принял сын Дмитрия Ивановича — Иван Дмитриевич Менделеев.
Великая Отечественная война лишь ненадолго прервала работу музея. Сразу же по возвращении из эвакуации младшая дочь ученого — Мария Дмитриевна Менделеева-Кузьмина приступила к систематизации и описанию архива и библиотеки. Новый этап в изучении наследия ученого начался с принятием 22 июля 1952 года Постановления Совета Министров СССР за подписью И. В. Сталина о сосредоточении всех материалов, связанных с жизнью и деятельностью ученого, в Музее-архиве Д. И. Менделеева. Кроме того, в начале 1950–х годов музей был расширен. Он дополнительно получил ряд помещений, относившихся ранее к квартире Менделеева и его лаборатории. Музею была также возвращена комната, в которой помещался рабочий кабинет ученого в бытность его профессором Петербургского университета.
Уже в 1956 году музей открылся для широкой публики. Экспозиция размещалась в семи залах. Во второй половине 1980-х годов Музей-архив был реконструирован и расширен. В новом виде он начал функционировать с весны 1993 года.
Линию дизайнерской одежды разработали к празднованию юбилея таблицы Менделеева в Подмосковье
По заказу Министерства культуры Московской области Игорь Чапурин разработал линию одежды, выполненную с использованием авторского дизайна, посвященного празднованию 150-летния периодической таблицы химических элементов в музее-усадьбе Менделеева и Блока в Шахматово, сообщили в пресс-службе регионального ведомства.
«В коллекцию в стилистике smart casual вошли стильные свитшоты, мягкие брюки, комфортные куртки-бомберы, футболки и жилеты нейтральных оттенков, выполненные из хлопка и неопрена. Ключевым дизайнерским приемом стало использование элементов таблицы, переосмысленных Игорем Чапуриным в русле современных трендов и эстетике марки Chapurin», – сообщается в материале.
Дизайнер отметил, что впервые участвует в подобном проекте.
«Мне было очень любопытно интегрировать в дизайн великое творение русского ученого. По сути, мы буквально соединили “химию” и “моду”, и, наверно, это едва ли не единственный случай в моей карьере, когда моя inspiration-база была столь четкой и совершенной по организации», – добавил Чапурин.
Объединяет коллекцию общий хэштег #150леттаблицеменделеева, который нанесли на все модели коллекции. Базовые цвета юбилейной серии – белоснежный, черный, серый и специальный сиреневый цвет, в котором объединен спектр оттенков, используемых в химической таблице.
«Подмосковье – территория новых форматов, свежего подхода и поиска, поэтому объединение Менделеева и Чапурина – как раз наш стиль. Конечно, нам хотелось максимально вовлечь в эту историю молодых, – их должен увлечь такой креативный процесс, как создание новой коллекции. Менделеев – на редкость интересная фигура, – и все, что связано в его жизни с Блоком, и тот факт, что он сам увлекался дизайном аксессуаров, делает образ великого ученого еще более привлекательным», – резюмировала министр культуры Московской области Нармин Ширалиева.
Таблица Менделеева для чайников – HIMI4KA
Еще в школе, сидя на уроках химии, все мы помним таблицу на стене класса или химической лаборатории. Эта таблица содержала классификацию всех известных человечеству химических элементов, тех фундаментальных компонентов, из которых состоит Земля и вся Вселенная. Тогда мы и подумать не могли, что таблица Менделеева бесспорно является одним из величайших научных открытий, который является фундаментом нашего современного знания о химии.
Периодическая система химических элементов Д. И. Менделеева
На первый взгляд, ее идея выглядит обманчиво просто: организовать химические элементы в порядке возрастания веса их атомов. Причем в большинстве случаев оказывается, что химические и физические свойства каждого элемента сходны с предыдущим ему в таблице элементом. Эта закономерность проявляется для всех элементов, кроме нескольких самых первых, просто потому что они не имеют перед собой элементов, сходных с ними по атомному весу. Именно благодаря открытию такого свойства мы можем поместить линейную последовательность элементов в таблицу, очень напоминающую настенный календарь, и таким образом объединить огромное количество видов химических элементов в четкой и связной форме. Разумеется, сегодня мы пользуемся понятием атомного числа (количества протонов) для того, чтобы упорядочить систему элементов. Это помогло решить так называемую техническую проблему «пары перестановок», однако не привело к кардинальному изменению вида периодической таблицы.
Именно благодаря открытию такого свойства мы можем поместить линейную последовательность элементов в таблицу, очень напоминающую настенный календарь, и таким образом объединить огромное количество видов химических элементов в четкой и связной форме. Разумеется, сегодня мы пользуемся понятием атомного числа (количества протонов) для того, чтобы упорядочить систему элементов. Это помогло решить так называемую техническую проблему «пары перестановок», однако не привело к кардинальному изменению вида периодической таблицы.
В периодической таблице Менделеева все элементы упорядочены с учетом их атомного числа, электронной конфигурации и повторяющихся химических свойств. Ряды в таблице называются периодами, а столбцы группами. В первой таблице, датируемой 1869 годом, содержалось всего 60 элементов, теперь же таблицу пришлось увеличить, чтобы поместить 118 элементов, известных нам сегодня.
Периодическая система Менделеева систематизирует не только элементы, но и самые разнообразные их свойства. Химику часто бывает достаточно иметь перед глазами Периодическую таблицу для того, чтобы правильно ответить на множество вопросов (не только экзаменационных, но и научных).
Химику часто бывает достаточно иметь перед глазами Периодическую таблицу для того, чтобы правильно ответить на множество вопросов (не только экзаменационных, но и научных).
The YouTube ID of 1M7iKKVnPJE is invalid.
Периодический закон
Существуют две формулировки периодического закона химических элементов: классическая и современная.
Классическая, в изложении его первооткрывателя Д.И. Менделеева: свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величин атомных весов элементов.
Современная: свойства простых веществ, а также свойства и формы соединений элементов находятся в периодической зависимости от заряда ядра атомов элементов (порядкового номера).
Графическим изображением периодического закона является периодическая система элементов, которая представляет собой естественную классификацию химических элементов, основанную на закономерных изменениях свойств элементов от зарядов их атомов.
Периодическая система химических элементов Д.И. Менделеева 2.2
Программа, написанная Феофановым Александром, представляет собой длиннопериодный вариант таблицы и содержит подробные сведения по каждому элементу, которые легко получить, наведя курсор мыши на любой из них. Приводятся название элемента на 9 языках (русский, английский, японский, немецкий, французский, испанский, китайский, греческий, арабский), электронная конфигурация, атомная масса, электроотрицательность, потенциалы ионизации, содержание в земной коре, кем и когда открыт, а также многое другое. Программа абсолютно бесплатная для некоммерческого использования. Заявлено, что программа будет работать под операционными системами Windows 98, Me, Xp, и, судя по отзывам, она также прекрасно работает и под Windows 7.
Размер программы: 693 Кб;
Группы и периоды Периодической системы
Группами называют вертикальные ряды в периодической системе. В группах элементы объединены по признаку высшей степени окисления в оксидах. Каждая группа состоит из главной и побочной подгрупп. Главные подгруппы включают в себя элементы малых периодов и одинаковые с ним по свойствам элементы больших периодов. Побочные подгруппы состоят только из элементов больших периодов. Химические свойства элементов главных и побочных подгрупп значительно различаются.
Периодом называют горизонтальный ряд элементов, расположенных в порядке возрастания порядковых (атомных) номеров. В периодической системе имеются семь периодов: первый, второй и третий периоды называют малыми, в них содержится соответственно 2, 8 и 8 элементов; остальные периоды называют большими: в четвёртом и пятом периодах расположены по 18 элементов, в шестом — 32, а в седьмом (пока незавершенном) — 31 элемент. Каждый период, кроме первого, начинается щелочным металлом, а заканчивается благородным газом.
Физический смысл порядкового номера химического элемента: число протонов в атомном ядре и число электронов, вращающихся вокруг атомного ядра, равны порядковому номеру элемента.
Длиннопериодный вариант (современный).
Отличный современный вариант. К сожалению качество изображения слегка ужато. Видимо автор использует оригинальную версию где-то в коммерческих целях. Подойдёт для черно-белой печати на формате А4.
Включает 114 элементов, по каждому из них вы можете видеть название элемента на русском, английском и латинском, номер, атомная масса, температуры плавления и кипения, электроотрицательность по Полингу и Аллреду, распределение электронов по энергетическим уровням;
Размер изображения: 1796х1111;
Формат файла: JPG;
Размер — файла: 590 Кб.
Периодическая система от американского химика-коллекционера, автора книги «Сумасшедшая наука». Особенность данного издания заключается в том, что в каждой клетке элемента содержится изображение простого вещества, соответствующего ему, либо изделие из простого вещества данного элемента. В случае с трансурановыми короткоживущими элементами мы видим портрет учёного в честь которого он назван.
Включает 118 элементов с минимальной информацией: символ элемента, название, номер и внешний вид. Очень хорошо изображение подходит в качестве обоев на рабочий стол.
Размер изображения: 1173х605;
Формат файла: JPG;
Размер файла: 239 Кб.
Вариант периодической системы в стиле нашумевшего сериала Breaking Bad (Во все тяжкие). Выполнен дизайнером Ciaran Nash. Несмотря на такой, казалось бы, минималистический дизайн, данная таблица содержит все необходимые данные о каждом элементе: символ элемента, номер, относительная атомная масса, распределение электронов по уровням. Однако, при этом таблица не содержит названий элементов так что в качестве пособия для обучения не годится.
Изображение содержит 118 элементов, даже ливерморий и флеровий на ней обозначены, в отличие от других вариантов. Неплохо подойдёт тем, кто уже неплохо знает химию, а также в качестве красивых обоев на рабочий стол.
Размер изображения:2560х1309;
Формат файла: JPG;
Размер файла: 538 Кб.
Свойства таблицы Менделеева
Напомним, что группами называют вертикальные ряды в периодической системе и химические свойства элементов главных и побочных подгрупп значительно различаются.
Свойства элементов в подгруппах закономерно изменяются сверху вниз:
- усиливаются металлические свойства и ослабевают неметаллические;
- возрастает атомный радиус;
- возрастает сила образованных элементом оснований и бескислородных кислот;
- электроотрицательность падает.
Все элементы, кроме гелия, неона и аргона, образуют кислородные соединения, существует всего восемь форм кислородных соединений. В периодической системе их часто изображают общими формулами, расположенными под каждой группой в порядке возрастания степени окисления элементов: R2O, RO, R2O3, RO2, R2O5, RO3, R2O7, RO4, где символом R обозначают элемент данной группы. Формулы высших оксидов относятся ко всем элементам группы, кроме исключительных случаев, когда элементы не проявляют степени окисления, равной номеру группы (например, фтор).
Оксиды состава R2O проявляют сильные основные свойства, причём их основность возрастает с увеличением порядкового номера, оксиды состава RO (за исключением BeO) проявляют основные свойства. Оксиды состава RO2, R2O5, RO3, R2O7 проявляют кислотные свойства, причём их кислотность возрастает с увеличением порядкового номера.
Элементы главных подгрупп, начиная с IV группы, образуют газообразные водородные соединения. Существуют четыре формы таких соединений. Их располагают под элементами главных подгрупп и изображают общими формулами в последовательности Rh5, Rh4, Rh3, RH.
Соединения Rh5 имеют нейтральный характер; Rh4 — слабоосновный; Rh3 — слабокислый; RH — сильнокислый характер.
Напомним, что периодом называют горизонтальный ряд элементов, расположенных в порядке возрастания порядковых (атомных) номеров.
В пределах периода с увеличением порядкового номера элемента:
- электроотрицательность возрастает;
- металлические свойства убывают, неметаллические возрастают;
- атомный радиус падает.
Элементы таблицы Менделеева
Щелочные и щелочноземельные элементы
К ним относятся элементы из первой и второй группы периодической таблицы. Щелочные металлы из первой группы — мягкие металлы, серебристого цвета, хорошо режутся ножом. Все они обладают одним-единственным электроном на внешней оболочке и прекрасно вступают в реакцию. Щелочноземельные металлы из второй группы также имеют серебристый оттенок. На внешнем уровне помещено по два электрона, и, соответственно, эти металлы менее охотно взаимодействуют с другими элементами. По сравнению со щелочными металлами, щелочноземельные металлы плавятся и кипят при более высоких температурах.
Показать / Скрыть текст
| Щелочные металлы | Щелочноземельные металлы |
| Литий Li 3 | Бериллий Be 4 |
| Натрий Na 11 | Магний Mg 12 |
| Калий K 19 | Кальций Ca 20 |
| Рубидий Rb 37 | Стронций Sr 38 |
| Цезий Cs 55 | Барий Ba 56 |
| Франций Fr 87 | Радий Ra 88 |
Лантаниды (редкоземельные элементы) и актиниды
Лантаниды — это группа элементов, изначально обнаруженных в редко встречающихся минералах; отсюда их название «редкоземельные» элементы. Впоследствии выяснилось, что данные элементы не столь редки, как думали вначале, и поэтому редкоземельным элементам было присвоено название лантаниды. Лантаниды и актиниды занимают два блока, которые расположены под основной таблицей элементов. Обе группы включают в себя металлы; все лантаниды (за исключением прометия) нерадиоактивны; актиниды, напротив, радиоактивны.
Показать / Скрыть текст
| Лантаниды | Актиниды |
| Лантан La 57 | Актиний Ac 89 |
| Церий Ce 58 | Торий Th 90 |
| Празеодимий Pr 59 | Протактиний Pa 91 |
| Неодимий Nd 60 | Уран U 92 |
| Прометий Pm 61 | Нептуний Np 93 |
| Самарий Sm 62 | Плутоний Pu 94 |
| Европий Eu 63 | Америций Am 95 |
| Гадолиний Gd 64 | Кюрий Cm 96 |
| Тербий Tb 65 | Берклий Bk 97 |
| Диспрозий Dy 66 | Калифорний Cf 98 |
| Гольмий Ho 67 | Эйнштейний Es 99 |
| Эрбий Er 68 | Фермий Fm 100 |
| Тулий Tm 69 | Менделевий Md 101 |
| Иттербий Yb 70 | Нобелий No 102 |
Галогены и благородные газы
Галогены и благородные газы объединены в группы 17 и 18 периодической таблицы. Галогены представляют собой неметаллические элементы, все они имеют семь электронов во внешней оболочке. В благородных газахвсе электроны находятся во внешней оболочке, таким образом с трудом участвуют в образовании соединений. Эти газы называют «благородными, потому что они редко вступают в реакцию с прочими элементами; т. е. ссылаются на представителей благородной касты, которые традиционно сторонились других людей в обществе.
Показать / Скрыть текст
| Галогены | Благородные газы |
| Фтор F 9 | Гелий He 2 |
| Хлор Cl 17 | Неон Ne 10 |
| Бром Br 35 | Аргон Ar 18 |
| Йод I 53 | Криптон Kr 36 |
| Астат At 85 | Ксенон Xe 54 |
| — | Радон Rn 86 |
Переходные металлы
Переходные металлы занимают группы 3—12 в периодической таблице. Большинство из них плотные, твердые, с хорошей электро- и теплопроводностью. Их валентные электроны (при помощи которых они соединяются с другими элементами) находятся в нескольких электронных оболочках.
Показать / Скрыть текст
| Переходные металлы |
| Скандий Sc 21 |
| Титан Ti 22 |
| Ванадий V 23 |
| Хром Cr 24 |
| Марганец Mn 25 |
| Железо Fe 26 |
| Кобальт Co 27 |
| Никель Ni 28 |
| Медь Cu 29 |
| Цинк Zn 30 |
| Иттрий Y 39 |
| Цирконий Zr 40 |
| Ниобий Nb 41 |
| Молибден Mo 42 |
| Технеций Tc 43 |
| Рутений Ru 44 |
| Родий Rh 45 |
| Палладий Pd 46 |
| Серебро Ag 47 |
| Кадмий Cd 48 |
| Лютеций Lu 71 |
| Гафний Hf 72 |
| Тантал Ta 73 |
| Вольфрам W 74 |
| Рений Re 75 |
| Осмий Os 76 |
| Иридий Ir 77 |
| Платина Pt 78 |
| Золото Au 79 |
| Ртуть Hg 80 |
| Лоуренсий Lr 103 |
| Резерфордий Rf 104 |
| Дубний Db 105 |
| Сиборгий Sg 106 |
| Борий Bh 107 |
| Хассий Hs 108 |
| Мейтнерий Mt 109 |
| Дармштадтий Ds 110 |
| Рентгений Rg 111 |
| Коперниций Cn 112 |
Металлоиды
Металлоиды занимают группы 13—16 периодической таблицы. Такие металлоиды, как бор, германий и кремний, являются полупроводниками и используются для изготовления компьютерных чипов и плат.
Показать / Скрыть текст
| Металлоиды |
| Бор B 5 |
| Кремний Si 14 |
| Германий Ge 32 |
| Мышьяк As 33 |
| Сурьма Sb 51 |
| Теллур Te 52 |
| Полоний Po 84 |
Постпереходными металлами
Элементы, называемые постпереходными металлами, относятся к группам 13—15 периодической таблицы. В отличие от металлов, они не имеют блеска, а имеют матовую окраску. В сравнении с переходными металлами постпереходные металлы более мягкие, имеют более низкую температуру плавления и кипения, более высокую электроотрицательность. Их валентные электроны, с помощью которых они присоединяют другие элементы, располагаются только на внешней электронной оболочке. Элементы группы постпереходных металлов имеют гораздо более высокую температуру кипения, чем металлоиды.
Показать / Скрыть текст
| Постпереходные металлы |
| Алюминий Al 13 |
| Галлий Ga 31 |
| Индий In 49 |
| Олово Sn 50 |
| Таллий Tl 81 |
| Свинец Pb 82 |
| Висмут Bi 83 |
Smell-O-Mints (для MacOs)
Для обладателей персонального компьютера с операционной системой Mac Os прекрасно подойдёт приложение Smell-O-Mints. При нажатии на любой элемент, данная программа также отображает подробные сведения о нём. Имеется возможность подсвечивания отдельных групп элементов, например по агрегатному состоянию: твёрдые, жидкие, газообразные. Имеется возможность самому группировать химические элементы по каким-либо признакам.
Размер программы: 844 Кб;
История и перспективы периодического закона и периодической системы Д.И. Менделеева.
«История и перспективы периодического закона и периодической системы элементов Д.И.Менделеева»
Автор работы: Часовских Вероника Игоревна
ученица 11-А класса
Руководитель: Замурий Ирина Владимировна
Содержание
Введение.
Глава 11.1. Первые попытки систематизации элементов.
1.2.Систематизация элементов до открытия Д.И. Менделеева.
1.3. Открытие периодического закона и периодической системы элементов Дмитрием Ивановичем Менделеевым.
Первый вариант системы элементов ученого.
1.4.Второй вариант системы элементов ученого.
Глава 2
2.1.Взгляд и вклад ученого мира Запада на открытие Менделеевской системы.
2.2. Включение в периодическую систему инертных элементов.
2.3.Таблица Менделеева в конце XIX– начале XX века.
Перспективы развития таблицы Менделеева.
Глава 3. Значение периодической системы.
Вывод.
Литература.
Приложения.
Введение
Тема моей работы: «История и перспективы периодического закона и периодических элементов Д.И. Менделеева».
Я выбрала эту тему для исследования, потому что каждый из нас, в частности я, неоднократно пользовались таблицей Менделеева, но мало кто задумывался о том, как она появилась, и, каковы ее перспективы. В современном мире периодическая система и периодический закон имеют большое значение, так как открытие, сделанное величайшим химиком – Д.И. Менделеевым, сыграло важнейшую роль в развитии науки и промышленности. Исходя из этого, стоит сделать вывод, что нельзя останавливаться на достигнутом. Периодическая система требует развития.
Цели данной работы:
– первые попытки систематизации элементов;
– подробно изучить историю изобретения и структуру таблицы Менделеева;
-определить перспективы развития периодической системы.
Достижение цели с помощью решения таких задач:
-анализ истории возникновения периодической системы элементов;
-изучив материал по этой теме, выдвинуть свои собственные размышления по поводу дальнейшего развития периодической системы.
Гипотеза исследования построена на предположении о том, что изучив периодическую систему элементов более углубленно, можно открыть новые элементы.
Детальное изучение литературы по этой теме дало возможность проанализировать такие противоречия:
– между учениями и представлением системы элементов, которые были выдвинуты до Д.И.Менделеева;
-между традиционной формой периодической системы химических элементов и её дальнейшем усовершенствованием с точки зрения современного человека.
Данная исследовательская работа, все материалы и особенности исследования были обусловлены целью, задачами, степенью изученности проблемы.
ГЛАВ
1.1.Первые попытки систематизации элементов.
Всем нам давно известен тот факт, что людям, свойственно наблюдать за окружающим миром, а также изменениями и различными явлениями природы. Бывает и так, что эти изменения могут навредить человечеству, как, например, землетрясение, засухи, затопления, смерчи и многое другое. Но чаще всего случается то, чего мы можем просто не замечать в повседневной жизни: испарение, замерзание жидкости, а также распад на мелкие кусочки какого-либо твёрдого тела. Наблюдая и изучая подобные процессы люди задумываются: почему происходит так, а не иначе, начинают более углубленно исследовать причины и пытаются выявить сущность всех этих явлений. Стоит отметить, что с древних времен люди смогли отыскать и изучить одиннадцать элементов: медь, серебро, золото, олово, свинец, сурьму, цинк, ртуть, железо, углерод и серу. Так же исследуя материал по этой теме, мне удалось узнать, что по мере развития цивилизации, некоторые философы, путем наблюдений, выдвигали свои собственные теории. Что же это за теории и в чем их суть? Нельзя оставить незаметным тот факт, что каждый из этих ученых приходил к одним и тем же умозаключениям. А именно, что, во-первых, существуют какие-то первичные вещества или материи, чье сочетание образует всё то разнообразие веществ, которое нас окружает. Подтвердить данный факт я бы хотела убеждениями древнегреческих философов: Фалес считал первоматерией воду, Анаксимен – воздух, Ксенофан – землю, а Гераклит – огонь. Отдельно хотелось бы отметить философа Эмпедокла, который смог изучить, что сочетая вышеперечисленные материи в различных пропорциях, мы можем получить все остальные вещества. Так же был и ряд других ученых, которые утверждали, что первоматерией является неопределенная субстанция. Анализируя свои доводы, философы вдруг обнаружили, что все вещества состоят из мельчайших частиц под названием атомы. Еще один философ – Аристотель, имел свою точку зрения на этот счет. Он был уверен в том, что те 4 материи не просто субстанции, как считал Эмпедокла, а символы, которые являются носителями таких качеств, как сухость, влажность, тепло и холод. Таким образом, можно отследить следующую цепочку наложений качества на материю: тепло + сухость = огонь, влажность + холод = вода, сухость + холод = земля, а тепло + влажность = воздух. Во многом с Аристотелем были согласны представители алхимии (ложной химии). Алхимия была целиком основана на «системе элементов» Аристотеля. Пытаясь дополнить «систему элементов» (Приложение 1), прогресс так и не был достигнут в полном объеме.
В эпоху Возрождения снова стали возрождаться атомистические представления. Так философ Джордано Бруно считал, что элемент – это любое вещество, которое не способно раскладываться на более простые вещества. Английский ученый Р. Бойль в очень четкой форме высказал свое отрицательное отношение к «элементам» алхимиков. Чуть позже этими вопросами был заинтересовался Михаил Васильевич Ломоносов. Он разделял мысли Бойля, но в тоже время был не согласен с тем, что элемент – простое вещество. Сам Ломоносов воспринимал понятие «элемент», как отдельный вид атома. Но, к сожалению, Михаил Васильевич не был услышан своими заграничными коллегами. Однако, позднее, один из них – Дж. Дольтон, дал определение элементу и ввел свою символику элементов взамен той, которой пользовались алхимики. Стоит также отметить химика из Швеции – Якоба Берцелиуса, который изобрел символику химических элементов, которой мы пользуемся. Ее достоинством является то, что за каждым символом элемента скрывается не только его название, но и подразумевается атомная масса (Приложение 2)
1.2.Систематизация элементов до открытия Д.И. Менделеева
Год за годом число элементов стало возрастать, на тот период их число достигло тридцати трёх, поэтому появилась острая необходимость в их систематизации и классификации. Основоположником первой классификации стал французский ученый А.Лавуазье.
Газы и «флюиды»;
Неметаллы;
Металлы;
«земли» (это те вещества, которые являются оксидами элементов).
Чуть позже свою версию выдвинул уже немецкий ученый по фамилии Доберейнер, который расположил элементы триадами (Приложение 3). Это открытие сделало огромный толчок в науке, и уже на основании этого в 1857 году Е.Ленссен располагает все элементы так, что получилось двадцать, так называемых триад.
В свою очередь другие ученые, стали понимать, что все закономерности не случайны. Исходя из этого, уже в 50-х годах появились мысли систематизации элементов по группам. Таким образом, уже в 1864-1965 годах свои открытия в виде таблицы сделал Дж. Ньюлендс, расположив все элементы в восьми вертикальных столбцах – октавах, сходные элементы расположены по горизонтали. Его таблица была негармонична, потому что, как мы можем увидеть (Приложение 4), нет никакого сходства между такими элементами, как Cl и Pb, S и Fe. Но стоит отметить, что ученый подметил повторяемость свойств элементов на восьмом элементе. Однако, Дж. Ньюлендс не сделал ожидаемого результата, в отличие от Л.Мейера. Он как никто другой приблизился к открытию периодического закона. В своей таблице он разместил элементы по их валентности по водороду. Всего в таблице ученого было 6 столбцов, которые содержали в себе 44 элемента, расположенных по валентности (Приложение 5). Проследив, что в каждом столбце атомная масса, рядом стоящих, элементов закономерно отличается на: 16, 45 и 90, Л.Мейер, к сожалению, не делает никакого вывода.
Суммируя все попытки химиков отследить логическую цепочку, они так и не смогли обнаружить ту самую единую систему элементов.
1.3.Открытие периодического закона и периодической системы элементов Дмитрием Ивановичем Менделеевым. Первый вариант системы элементов ученого
Д.И.Менделеев начал изучение материала по созданию системы элементов, работая над своим собственным учебником «Основы химии». И уже 1 марта 1869 химиком был представлен первый вариант системы элементов под названием «Опыт системы элементов, основанной на их атомной массе и химическом сходстве», который сделал огромный прогресс для науки и вошел в ее историю. Как же Менделеев смог добиться таких результатов? История гласит, что ученый был в поисках константы. Перебирая такие свойства элементов, как плотность, температура плавления и кипения, автор данного открытия не нашел ничего подходящего. Тогда химик решил, как он сам это называл, раскладывать свой «карточный пасьянс», на котором были указаны элементы, по их атомному весу. Именно тогда Д.И. Менделеев обнаружил сходство элементов. Какой же вид имела таблица, сделавшая огромный толчок научному прогрессу? Все элементы в ней были расставлены по 19-и рядам и по 6 столбцам (Приложение 6). Так же, анализируя информацию из различных пособий, стоит отметить, что горизонтальные ряды обозначали сходство элементов между собой, а атомная масса элементов, стоявших в каждом ряду, возрастала слева направо. Столбцы, в свою очередь, указывали на характер изменения атомных масс с некой периодичностью в среднем 2,5 единицы. Разработав свою таблицу, Менделеев обнаружил четыре пропуска. Это подтолкнуло его на мысль о том, что в природе существуют еще четыре, неизвестных элемента. По мнению ученого, эти элементы должны были стоять в 1-ом, 9-ом, в 10-ом, и 16-ом ряду. Тот элемент, чье «окно» находилось в 9-ом ряду, должен был стать аналогом бора и алюминия, имея при этом относительную атомную массу равную 68; в 1-ом ряду, как утверждал химии, нужен элемент, который смог бы стать аналогом титана и циркония с относительной атомной массой 180; в 10-ом – аналог углерода и кремния с относительной атомной массой равной, приблизительно, 70; и в 16-ом – аналог церия с относительной атомной массой 45. В будущем этими элементами стали: галлий, германий, гафний и скандий.
Какой вывод можно сделать из исследования ученым своей собственной таблицы?
Все элементы расположены по атомной массе и имеют периодичность свойств.
Атомная масса определяет характер и свойства элементов.
С помощью аналогов и их атомных масс можно иногда исправлять атомные массы.
Можно предположить открытие еще многих простых тел (элементов).
1.4. Второй вариант системы элементов ученого
Работая долгих полтора года, уже в 1870 году Д.И. Менделеев обнародует второй вариант под названием «Естественная система элементов» (Приложение 7). Я задаюсь простым вопросом, что же изменилось с тех пор?
Те горизонтальные ряды, о которых я упоминала выше, стали вертикальными.
Произошло их уплотнение, что привело к образованию восьми групп элементов.
Столбцы обратились в периоды.
Валентность элементов стала определяться по их номеру группы.
Периоды начинались с активных щелочных металлов, а заканчивались нетипичным металлом – галогеном.
В отличие от первого варианта таблицы ученого, появились группы, а также химик предполагал, что существуют лантаноиды и заурановые элементы. Расположение элементов в таблице:
Благородные газы – гелий, неон, аргон, криптон, ксенон и радон неохотно реагируют с другими элементами и проявляют низкую химическую активность и потому находятся в крайней правой колонке. В противоположность этому элементы самой левой колонки — литий, натрий, калий и прочие реагируют с другими веществами бурно, процесс носит взрывной характер. Аналогично ведут себя элементы в других колонках таблицы — внутри колонки эти свойства подобны, но варьируются при переходе от одной колонки к другой.
Усложнив и усовершенствовав своё учение, его автор сумел предположить, что существует не 4, а уже 11 элементов. Сейчас эти элементы называются так: скандий (2-й ряд), галлий и германий (3-й ряд), технеций (4-й ряд), гафний и рений (8-й ряд), астат (9-й ряд), франций, радий, актиний, протактиний (10-й ряд). Это привело к тому, что Менделееву пришлось изменять относительные атомные массы некоторых элементов. И тут же в 1871 году химии сформулировал открытый закон:
«Свойства простых тел, также формы и свойства соединений элементов находятся в периодической зависимости от величины атомных весов элементов». Доказать всем, что, открытый им закон, действительно работает, Менделеев решил на примере названный им же элементов – экабора, экаалюминия и экасилиция описать их свойства, свойства их соединений и методы, которыми они могут быть получены. Дальнейшие открытия этих элементов подтвердили правильность менделеевского приема наименования элементов. Этот прием используется и в настоящее время.
ГЛАВА 2
2.1.Взгляд и вклад ученого мира Запада на открытие Менделеевской системы
Отношение западных ученых к таблице Менделеева было скептическим, многие просто оставляли данное без внимания только потому, что это открытие было совершенно их русским коллегой. И только лишь в 1875 году началась череда открытий новых элементов. Французский ученый Лекол де-Буабодран, открыл элемент под названием «галлий». Менделеев, ознакомившись с открытием ученого, указал на то, что плотность элемента рассчитана неточно, так как открытый галлий – это экаалюминий. После этого, уже в 1879 году свой элемент под названием «скандий» открыл шведский химик Ларс Нильсон, свойства которого совпали со свойствами экабора. Следующий свой вклад в науку внес немец Кл. Винклер, открыв германий, предсказанный Менделеевым экасилиций. И каждое новое открытие подтверждало правильность учения Менделеева. Именно с тех пор таблица Менделеева стала активно развиваться и пополняться всё новыми и новыми элементами.
Как говорил сам Менделеев о своем достижении в тот период: «Наука есть достояние общее, а потому справедливость требует не тому отдать наибольшую научную славу, кто первый высказал известную истину, а тому, кто сумел убедить в ней других, показал ее достоверность и сделал ее применимою в науке».
2.2. Включение в периодическую систему инертных элементов.
Д.И.Менделеев внимательно анализировал атомные массы элементов и обратил внимание на то, что разрыв между атомными массами элементов – галогенов и щелочными металлами ненормально велик, поэтому между ними возможен какой – то промежуточный элемент. Поэтому Менделеев предвидел наличие этих элементов, но каковы будут их свойства еще более неметаллического характера, чем у галогенов или более металлического характера, че у щелочных металлов он не мог смог определить. И третьего варианта, что эти элементы будут инертны, Д.И. Менделеев не предугадал.
В 1884 году революционер Н.А. Морозов, заключенный царским правительством пожизненно в Шлиссельбургскую крепость, начинает изучать химию. Он знакомиться с системой Менделеева и по образу и подобию создает свою таблицу для углеводородов. Таблица состоит из 8 вертикальных рядов – классов углеводородов и их радикалов и 7 горизонтальных рядов. Сравнивая свою таблицу с таблицей Менделеева, он приходит к выводу, что в его таблице есть химически инертные
( малоактивные) углеводороды, а в таблице Менделеева инертных элементов нет. И вот Н.А. Морозов предсказывает, что такие элементы должны быть в природе, и скорее всего в воздухе. Первым был открыт английским ученым У. Рамзаем аргон, а вскоре были открыты и другие элементы и в 1901 году был открыт уже шестой химический элемент – радон.
Следовательно, на основе системы Д. И. Менделеева, Н.А. Морозову удалось предсказать то, что не удалось сделать автору периодического закона. Известно, что Д.И. Менделеев называл ученых, открывавших предсказанные им элементы «укрепителями» периодического закона.
И вот когда в конце XIX века к Д. И. Менделееву пришла мировая слава и известность, начинаются попытки приписать открытие этого закона другим ученым.
Много испытаний выпало на долю и периодической системы:
– открытие радиоактивности, когда для атомов продуктов распада не находилось, как бы места, в системе;
– отрицание реального существования атомов;
– открытие явления изотопии;
– размещение в системе лантаноидов и актиноидов по мере их открытия;
– открытие строения атома и ядра;
– открытие возможности искусственного превращения элементов и другие.
Но, все эти испытания периодическая система преодолела.
2.3.Таблица Менделеева в конце XIX – начале XXI века.
Перспективы развития таблицы Менделеева
По-особенному продуктивным для выявления новых элементов стал XIX век. Это было обусловлено успехами электрохимии и спектрального анализа. В середине XIX века учеными было получено 62 элемента. Но уже в начале ХХ века это число стало достигать 88. В последствие стали появляться всё новые и новые пропуски в таблице, которые заполнялись теми элементами, которых в природе не существует. Их получение производилось искусственным путем при помощи ядерной реакции. Так же данная реакция поспособствовала образованию заурановых элементов, которых насчитывается тринадцать. Так же стоит отметить то, что для элементов, полученных искусственным путем, понятие «относительная атомная масса» теряет свой смысл, т.к. ее роль в таких ситуациях – заряд ядра, равный атомному номеру и числу электронов, распределение которых по электронным оболочкам атома элемента определяет его химические свойства. Химические элементы вплоть до урана (содержит 92 протона и 92 электрона) встречаются в природе. Начиная с номера 93 идут искусственные элементы, созданные в лабораторных условиях. Нельзя скрыть тот факт, что работа по получению новых элементов проходит при тесном сотрудничестве физиков и химиков. Задача физиков – получить тот или иной элемент искусственным путем. Задача химиков: установить химическую природу элемента и уточнить его место в системе элементов. Постепенно таблица стала заполняться, и к 2010 году был завершен период под номером семь. Число открытых на данный момент элементов достигло 118-ти. 113-й, 115-й, 117-й и 118-й элементы были задекларированы (Международным союзом теоретической и прикладной химии) совсем недавно, 30-го декабря 2015 года (Приложение 8). Так, например, элемент с порядковым номером 113 получил от открывших его японских ученых название “нихоний” (символ Nh), что переводится на русский язык как “Страна восходящего солнца”.115-й элемент получил название “московий” (Mc) в честь Московского региона, где располагается Объединенный институт ядерных исследований г. Дубна. Новый элемент с атомным числом 117 внесли в таблицу под названием “теннессин” (Ts). Наконец, 118-й элемент, которому было присвоено временное название “унуктоний”, сменил его на постоянное и официальное “оганессий” (Og) в честь академика Российской академии наук Юрия Цолаковича Оганесяна.
Описание элементов:
Нихоний входит в группу бора, но ведёт себя как переходный металл. Согласно расчётам, температура плавления и кипения нихония составляет 430°С и 1100°С, что делает его непохожим на другие элементы, которые плавятся и кипят при существенно более низких температурах.
Московий входит в группу пниктогенов (группа азота): ближайший к нему элемент той же группы – висмут. Московий предположительно является плотным металлом, вторым в группе после висмута. По физическим свойствам он напоминает нихоний, поскольку электроны московия также испытывают сильное спин-орбитальное взаимодействие. По химическим свойствам московий скорее напоминают щелочной таллий.
Теннессин – самый «молодой» элемент Он принадлежит к галогенам, стоя в их группе сразу после йода и астата. В его поведении преобладают металлические свойства. Температура плавления и кипения теннессина существенно ниже, чем у других элементов этой же группы – он должен кипеть около 210–350°С, поскольку, в отличие от других галогенов, способен существовать в одноатомной форме, без образования типичных для галогенов двухатомных молекул.
Четвёртый элемент – оганессий назван в честь Юрия Оганесяна –профессора ядерной физики и научного руководителя Лаборатории ядерных реакций им. Г.Н. Флёрова в Объединённом институте ядерных исследований в Дубне. Это второй случай в истории, когда химический элемент назван в честь всё ещё живущего исследователя. Такой прогресс способствовал не только развитию химии и физики, способствуя открытию новых разделов – физики атома, физике ядра, но и др. отраслей науки.
Каждый из нас хоть раз задавался вопросом: есть ли конец периодической системы? Предел получения элементов искусственным путем?
Можно предположить предел периодической системы, исходя из теоретических соображений закономерностей возрастания радиоактивности атомов по мере их усложнения. Но, как нам всем известно, видов радиоактивности целое множество. Предел существованию атомов, вызываемый каким-либо одним видом неустойчивости, может не совпадать с переделом, вызываемым другим видом. Так, например, можно сделать вывод, что, исходя из всех закономерностей, полученных при исследовании спонтанного деления ядер, следует, что предел располагается приблизительно между элементами №108-116; исходя из закономерностей электронного захвата, предел стоит ожидать на элементе №137; исходя из закономерностей α- излучения, предел расположен в районе элементов под номерами 104- 106. Изучив всё вышесказанное, можно сделать вывод, возможно существование элемента, например, №130.
На сегодняшний день ученые смеют предположить, что на каком- то из элементов система практически оборвется, но спустя некоторое количество номеров после последнего элемента может быть синтезирован атом элемента со значительно большим номером. И так далее всё по тому же алгоритму.
На самом деле, получение элементов искусственным путем, которые давно исчезли с лица Земли, является огромным достижением науки. Из изученного мною материала можно сделать вывод, что те люди, которые изучают химические элементы, поневоле сталкиваются с географией, историей, астрономией, минералогией, мифологией и т.д.
Подводя итог, стоит только отметить то, что важно различать открытия:
1)открытие элемента, как определенного вида атомов;
2)выделение элемента в виде простого вещества для определения его свойств.
Очень часто случается так, что между этими открытиями проходят десятки лет, но ученые всё равно добиваются нужного им результата.
Глава 3.Значение периодической системы.
Первоначальная цель разработки системы элементов Д.И. Менделеева была прикладная, узкая, имела учебно – педагогическое значение. Научное же значение было огромно. Вот только часть того, какую роль она сыграла:
Создание системы элементов привело к развитию учения об атоме и учения об элементе.
Открылась новая эра в химии, биологии, физике, металловедении, геохимии, астрохимии и в ряде других наук.
Периодическая система элементов заставила ученых работать над исправлением и уточнением атомных масс, над получением оксидов, водородных соединений, предпринять поиски элементов, предсказанных Д.И. Менделеевым и других элементов.
Создание периодической системы элементов побудило ученых к выяснению причин периодичности свойств, к выяснению физического смысла понятий «группа», «подгруппа», «период», «номер элемента», «номер группы», «номер периода», то есть к выяснению строения атома.
На базе периодической системы изучают и объясняют те или иные аномалии в свойствах отдельных веществ, создаются новые вещества, сплавы.
Периодическая система элементов позволяет более четко понимать распределение элементов на земном шаре, во вселенной, в живых организмах.
Периодическая система показала, что материя постоянно развивается, что устанавливается взаимосвязь и взаимообусловленность явлений.
Многие ученые мира высоко оценили труд Д. И. Менделеева. Английский ученый У. Рамзай называл периодическую систему «компасом для исследователя», Нильс Бор называл ее « путеводной звездой для исследований». Сам же Д.И. Менделеев сказал: «Периодическому закону будущее не грозит разрушением, а только надстройка и развитие обещаются». Это пророческие слова. Многие видные ученые мира утверждают, что все развитие химии идет на основе менделеевской системы.
Вывод.
Данная работа помогла мне узнать больше полезной информации о таблице Менделеева. Например, то, как долгие столетия отдельно друг от друга развивались учения об атоме и об элементе. И только Д.И. Менделеев смог слить их воедино. Ученый смог доказать, что элемент – это всего лишь отдельный вид атома и, что атом этот можно охарактеризовать по его месту в системе элементов. С созданием периодической системы началась новая эра в целом ряде наук: химия, физика, биохимия и др. Значение периодической системы элементов бесценно. Поэтому нужно не останавливаться на достигнутом, а развивать и дополнять периодическую систему с целью увеличения пользы химии в жизни человечества.
Литература
http://uznay-skolko.ru/skolko-elementov-v-tablitse-mendeleeva-118-ili-126
https://slavikap.livejournal.com/26129672.html
http://lediznaet.ru/lichnoe/samorazvitie/skolko-elementov-v-tablice-mendeleeva-na-segodnya.html
https://ru.wikipedia.org/wiki/Периодическая_система_химических_элементов
http://edu.glavsprav.ru/info/tablica-mendeleeva
Приложение 1. Система «философских элементов» Аристотеля (пятая сущность)
Приложение 2. Развитие химической символики
Приложение 3. Закон триад
Приложение 4. Закон октав
Приложение 5. Таблица Майера
Приложение 6. Первый вариант системы элементов Д.И. Менделеева
Приложение 7. «Естественная система элементов»
Приложение 8. Периодическая система элементов Д.И.Менделеева
Периодическая таблица элементовBW
% PDF-1.5 % 1 0 объект > / OCGs [8 0 R 9 0 R 10 0 R] >> / Страницы 3 0 R / Тип / Каталог >> эндобдж 2 0 obj > поток application / pdf
Ученые предлагают совершенно новую таблицу Менделеева, и это путешествие
Периодическая таблица элементов, созданная главным образом русским химиком Дмитрием Менделеевым (1834–1907), в прошлом году отметила свое 150-летие. Трудно переоценить его важность как организующего принципа в химии – все начинающие химики знакомятся с ним с самых ранних этапов своего образования.
Учитывая важность таблицы, можно простить мысль, что порядок элементов больше не является предметом обсуждения.Однако два ученых из Москвы, Россия, недавно опубликовали предложение о новом порядке.
Давайте сначала рассмотрим, как была разработана таблица Менделеева. К концу 18 века химики ясно понимали разницу между элементом и соединением: элементы были химически неделимы (например, водород, кислород), тогда как соединения состояли из двух или более элементов в комбинации, обладающих свойствами, совершенно отличными от составляющих их элементов.
К началу 19 века имелись хорошие косвенные доказательства существования атомов.А к 1860-м годам стало возможно перечислять известные элементы в порядке их относительной атомной массы – например, водород был равен 1, а кислород 16.
Простые списки, конечно, одномерны по своей природе. Но химики знали, что некоторые элементы имеют довольно похожие химические свойства: например, литий, натрий и калий или хлор, бром и йод.
Казалось, что-то повторяется, и, помещая химически похожие элементы рядом друг с другом, можно построить двухмерную таблицу.Так родилась таблица Менделеева.
Важно отметить, что периодическая таблица Менделеева была получена эмпирическим путем на основе наблюдаемого химического сходства определенных элементов. Только в начале 20-го века, после того, как была установлена структура атома и вслед за развитием квантовой теории, появилось теоретическое понимание его структуры.
Элементы теперь упорядочены по атомному номеру (количеству положительно заряженных частиц, называемых протонами в атомном ядре), а не по атомной массе, но также по химическому сходству.
Но последнее теперь следует из расположения электронов, повторяющихся в так называемых «оболочках» через равные промежутки времени. К 1940-м годам в большинстве учебников была периодическая таблица, аналогичная той, что мы видим сегодня, как показано на рисунке ниже.
Сегодняшняя таблица Менделеева. (Offnfopt / Wikipedia)
Можно было бы подумать, что на этом все кончено. Однако это не так. Простой поиск в Интернете покажет всевозможные версии таблицы Менделеева.
Есть короткие версии, длинные версии, круглые версии, спиральные версии и даже трехмерные версии.Конечно, многие из них представляют собой просто разные способы передачи одной и той же информации, но по-прежнему существуют разногласия по поводу того, где следует разместить некоторые элементы.
Точное размещение определенных элементов зависит от того, какие конкретные свойства мы хотим выделить. Таким образом, периодическая таблица, которая отдает приоритет электронной структуре атомов, будет отличаться от таблиц, для которых основными критериями являются определенные химические или физические свойства.
Эти версии не сильно различаются, но есть определенные элементы, например водород, которые можно расположить по-разному в зависимости от конкретного свойства, которое нужно выделить.В некоторых таблицах водород помещен в группу 1, тогда как в других он находится в верхней части группы 17; некоторые столы даже включают его в отдельную группу.
Более радикально, однако, мы также можем рассмотреть упорядочение элементов совершенно другим способом, который не включает атомный номер и не отражает электронную структуру – возвращаясь к одномерному списку.
Новое предложение
Последняя попытка упорядочить элементы таким образом была недавно опубликована в журнале « Journal of Physical Chemistry » учеными Захедом Аллахьяри и Артемом Огановым.
(Allahyari et al., Journal of Physical Chemistry, 2020)
Их подход, основанный на более ранней работе других, заключается в присвоении каждому элементу так называемого числа Менделеева (MN).
Есть несколько способов получить такие числа, но последнее исследование использует комбинацию двух фундаментальных величин, которые можно измерить напрямую: атомного радиуса элемента и свойства, называемого электроотрицательностью, которое описывает, насколько сильно атом притягивает электроны к себе.
Если упорядочить элементы по их MN, у ближайших соседей, что неудивительно, будут довольно похожие MN. Но гораздо полезнее сделать еще один шаг и построить двумерную сетку на основе MN составляющих элементов в так называемых «бинарных соединениях».
Это соединения, состоящие из двух элементов, таких как хлорид натрия, NaCl.
В чем преимущество такого подхода? Важно отметить, что это может помочь предсказать свойства бинарных соединений, которые еще не были созданы.Это полезно при поиске новых материалов, которые могут понадобиться как для будущих, так и для существующих технологий. Со временем, без сомнения, это будет распространено на соединения с более чем двумя элементарными компонентами.
Хороший пример важности поиска новых материалов можно оценить, рассматривая периодическую таблицу, показанную на рисунке ниже.
Периодическая таблица, показывающая относительное содержание элементов. (Европейское химическое общество / Википедия / CC BY-SA)
В этой таблице показано не только относительное содержание элементов (чем больше прямоугольник для каждого элемента, тем его больше), но также освещены потенциальные проблемы поставок, связанные с технологиями. которые стали повсеместными и важными в нашей повседневной жизни.
Возьмем, к примеру, мобильные телефоны. Все элементы, используемые при их производстве, обозначены значком телефона, и вы можете видеть, что некоторые необходимые элементы становятся дефицитными – их будущие поставки неизвестны.
Если мы хотим разработать заменяющие материалы, в которых не используются определенные элементы, то понимание, полученное при упорядочивании элементов их MN, может оказаться ценным в этом поиске.
Спустя 150 лет мы видим, что периодические таблицы являются не просто жизненно важным образовательным инструментом, они остаются полезными для исследователей в их поисках необходимых новых материалов.Но мы не должны думать о новых версиях как о замене более ранних изображений. Наличие множества разных таблиц и списков только помогает нам лучше понять, как ведут себя элементы.
Ник Норман, профессор химии, Бристольский университет.
Эта статья переиздана из The Conversation под лицензией Creative Commons. Прочтите оригинальную статью.
Лучшая периодическая таблица 2021 года (пересмотренная, ранжированная и сравненная)
Для студентов, изучающих естественные науки, наличие таблицы Менделеева в сгибе книги является обязательным условием.Студентам, изучающим химию или физику, очень важно знать природу, характеристики и взаимосвязь всех химических элементов, которые были открыты до сих пор.
Но как вы думаете, легко ли запомнить все свойства химических элементов и их отношения друг с другом? Надеюсь, ты этого не сделаешь. И периодическая таблица, таблица, отображающая химические элементы, отсортированные по идентичным свойствам, – это лист бумаги, который значительно упрощает процесс, объединяя все химические элементы и их свойства в одном месте.
Всякий раз, когда вам нужно узнать природу или характеристики элемента, просто посмотрите на таблицу и выполните свое задание.
Но для этого вы должны найти лучшую таблицу Менделеева со всей обновленной информацией. Итак, в этой статье мы собрали некоторые из самых популярных периодических таблиц, которые заслуживают вашего внимания, прежде чем вы их купите.
Palace Learning Периодическая таблица элементов | ||||||||||||||||||||||||||||||||||||||||||||||||||||
Периодическая таблица элементов графического образования | ||||||||||||||||||||||||||||||||||||||||||||||||||||
Подставка для безболезненного обучения периодической таблицы | ||||||||||||||||||||||||||||||||||||||||||||||||||||
1. Palace Learning Periodic Table of Elements | Bigiodic Table of Elements | 3 9024 | |||||
3. Периодическая таблица элементов графического образования | |||||||
4.Подставка для безболезненного обучения периодической таблицы | |||||||
5. Янг Н. Новое определение периодической таблицы элементов | |||||||
6. Наследие Периодическая таблица элементов | 63Периодическая таблица элементов наследия | ||||||
8. Usborne Book and Jigsaw | |||||||
9.Периодическая таблица элементов Bigtime Signs | Универсальные – все емкостные устройства с сенсорным экраном | ||||||
11. Sunlit Periodic Table of Elements | 09 Учебный комплект Периодическая таблица | Ячейка | |||||
13. Периодическая таблица элементов LiFe Chem | Плакат и органайзер. |
Часто задаваемый вопрос
На этом этапе статьи мы собрали некоторые из наиболее часто задаваемых вопросов о таблице Менделеева. Мы надеемся, что эти вопросы и ответы укрепят ваши знания о периодической таблице и ее различных применениях.
1. Вопрос: Что такое определение Периодической таблицы?
Ответ: Согласно Википедии, периодическая таблица – это таблица химических элементов, организованная в порядке атомного номера, обычно в строках, так что элементы с аналогичной атомной структурой (и аналогичными химическими свойствами) отображаются в вертикальных столбцах.
2. Вопрос: Сколько элементов в периодической таблице?
Ответ: До декабря 2015 года элементов в периодической таблице было 114. Но в декабре 2015 года в периодическую таблицу были добавлены 4 новых элемента – Московий, Теннессин, Нихониум, Оганессон. Пока это самый обновленный список.
3. Вопрос: Какая польза от периодической таблицы?
Ответ: Таблица Менделеева поможет вам узнать свойства элемента и то, как они связаны друг с другом.В прежние времена таблица Менделеева могла сказать вам свойства элемента, который уже был обнаружен. Но в наши дни использование таблицы Менделеева изменилось. Теперь он может помочь вам предсказать свойства элемента, который еще не был обнаружен.
4. Вопрос: Кто первым открыл периодическую таблицу Менделеева?
Ответ: Дмитрий Менделеев впервые опубликовал общепринятую таблицу Менделеева в 1859 году.
5. Вопрос: Каковы основные тенденции в периодической таблице Менделеева?
Ответ: Наиболее значительными и основными периодическими тенденциями являются энергия ионизации, сродство к электрону, металлический характер, электроотрицательность и атомный радиус.
Заключительные слова
Таблица Менделеева облегчает процесс изучения и понимания химии. С помощью таблицы Менделеева вы можете узнать химические элементы и их свойства, даже не запоминая их. В этом обзоре мы представили лучшие периодические таблицы, чтобы убедиться, что поиск идеальной таблицы, соответствующей вашим требованиям, не займет много времени.
Никто не станет спорить с тем, что наличие идеальной таблицы Менделеева может облегчить выполнение задач и сделать их увлекательными. Поскольку вы уже прошли обзор раздела, теперь вы знаете, сколько типов периодической таблицы мы принесли туда.Никто не идеален. Один лучше всего подходит для одной конкретной задачи, возможно, тот же продукт даже не попадает в список для другой задачи. Выбирайте продукт только в зависимости от вашего конкретного применения и предпочтений.
Мы уверены, что после подробного изучения статьи покупка плаката с таблицей Менделеева не будет для вас сложной задачей. Удачи!
Также читайте:
% PDF-1.4 % 7 0 объект > эндобдж xref 7 530 0000000016 00000 н. 0000010962 00000 п. 0000011032 00000 п. 0000011726 00000 п. 0000012326 00000 п. 0000014224 00000 п. 0000014367 00000 п. 0000014495 00000 п. 0000014623 00000 п. 0000014754 00000 п. 0000014883 00000 п. 0000015014 00000 п. 0000015146 00000 п. 0000015279 00000 п. 0000015411 00000 п. 0000015543 00000 п. 0000015675 00000 п. 0000015803 00000 п. 0000015932 00000 п. 0000016062 00000 п. 0000016192 00000 п. 0000016337 00000 п. 0000016467 00000 п. 0000016596 00000 п. 0000016726 00000 п. 0000016857 00000 п. 0000016985 00000 п. 0000017116 00000 п. 0000017244 00000 п. 0000017373 00000 п. 0000017503 00000 п. 0000017633 00000 п. 0000017763 00000 п. 0000017896 00000 п. 0000018029 00000 п. 0000018162 00000 п. 0000018295 00000 п. 0000018428 00000 п. 0000018561 00000 п. 0000018691 00000 п. 0000018821 00000 п. 0000018951 00000 п. 0000019081 00000 п. 0000019211 00000 п. 0000019341 00000 п. 0000019472 00000 п. 0000019603 00000 п. 0000019734 00000 п. 0000019865 00000 п. 0000019996 00000 п. 0000020127 00000 н. 0000020257 00000 п. 0000020387 00000 п. 0000020517 00000 п. 0000020647 00000 п. 0000020777 00000 п. 0000020907 00000 п. 0000021037 00000 п. 0000021167 00000 п. 0000021297 00000 п. 0000021427 00000 н. 0000021560 00000 п. 0000021690 00000 н. 0000021821 00000 п. 0000021952 00000 п. 0000022083 00000 п. 0000022214 00000 п. 0000022346 00000 п. 0000022477 00000 п. 0000022607 00000 п. 0000022737 00000 п. 0000022867 00000 п. 0000023000 00000 п. 0000023130 00000 п. 0000023260 00000 п. 0000023393 00000 п. 0000023523 00000 п. 0000023653 00000 п. 0000023786 00000 п. 0000023919 00000 п. 0000024052 00000 п. 0000024183 00000 п. 0000024315 00000 п. 0000024448 00000 п. 0000024581 00000 п. 0000024714 00000 п. 0000024847 00000 п. 0000024974 00000 п. 0000025104 00000 п. 0000025234 00000 п. 0000025364 00000 н. 0000025494 00000 п. 0000025624 00000 п. 0000025755 00000 п. 0000025888 00000 п. 0000026021 00000 п. 0000026154 00000 п. 0000026287 00000 п. 0000026420 00000 н. 0000026553 00000 п. 0000026687 00000 п. 0000026821 00000 п. 0000026955 00000 п. 0000027089 00000 п. 0000027223 00000 п. 0000027357 00000 п. 0000027490 00000 н. 0000027623 00000 п. 0000027756 00000 п. 0000027889 00000 н. 0000028022 00000 п. 0000028155 00000 п. 0000028289 00000 п. 0000028423 00000 п. 0000028557 00000 п. 0000028691 00000 п. 0000028825 00000 п. 0000028959 00000 п. 0000029092 00000 п. 0000029225 00000 п. 0000029358 00000 п. 0000029492 00000 п. 0000029626 00000 п. 0000029760 00000 п. 0000029898 00000 н. 0000030044 00000 п. 0000030187 00000 п. 0000030332 00000 п. 0000030473 00000 п. 0000030613 00000 п. 0000030755 00000 п. 0000030896 00000 п. 0000031039 00000 п. 0000031180 00000 п. 0000031322 00000 п. 0000031464 00000 п. 0000031606 00000 п. 0000031747 00000 п. 0000031888 00000 п. 0000032030 00000 п. 0000032174 00000 п. 0000032318 00000 п. 0000032462 00000 п. 0000032605 00000 п. 0000032748 00000 н. 0000032892 00000 п. 0000033033 00000 п. 0000033176 00000 п. 0000033320 00000 п. 0000033464 00000 п. 0000033608 00000 п. 0000033752 00000 п. 0000033895 00000 п. 0000034038 00000 п. 0000034182 00000 п. 0000034326 00000 п. 0000034470 00000 п. 0000034614 00000 п. 0000034758 00000 п. 0000034902 00000 п. 0000035046 00000 п. 0000035189 00000 п. 0000035332 00000 п. 0000035476 00000 п. 0000035616 00000 п. 0000035758 00000 п. 0000035901 00000 п. 0000036044 00000 п. 0000036187 00000 п. 0000036330 00000 п. 0000036472 00000 н. 0000036614 00000 п. 0000036757 00000 п. 0000036900 00000 п. 0000037043 00000 п. 0000037186 00000 п. 0000037329 00000 п. 0000037472 00000 п. 0000037615 00000 п. 0000037757 00000 п. 0000037899 00000 н. 0000038042 00000 п. 0000038182 00000 п. 0000038324 00000 п. 0000038467 00000 п. 0000038610 00000 п. 0000038753 00000 п. 0000038895 00000 п. 0000039037 00000 н. 0000039180 00000 п. 0000039323 00000 п. 0000039466 00000 п. 0000039609 00000 п. 0000039752 00000 п. 0000039895 00000 п. 0000040038 00000 п. 0000040180 00000 п. 0000040322 00000 п. 0000040465 00000 п. 0000040606 00000 п. 0000040749 00000 п. 0000040893 00000 п. 0000041037 00000 п. 0000041181 00000 п. 0000041324 00000 п. 0000041467 00000 п. 0000041611 00000 п. 0000041755 00000 п. 0000041899 00000 н. 0000042043 00000 п. 0000042187 00000 п. 0000042331 00000 п. 0000042475 00000 п. 0000042618 00000 п. 0000042761 00000 п. 0000042905 00000 п. 0000043046 00000 п. 0000043190 00000 п. 0000043334 00000 п. 0000043478 00000 п. 0000043621 00000 п. 0000043764 00000 п. 0000043908 00000 п. 0000044052 00000 п. 0000044196 00000 п. 0000044340 00000 п. 0000044484 00000 п. 0000044628 00000 п. 0000044772 00000 п. 0000044915 00000 п. 0000045058 00000 п. 0000045202 00000 п. 0000045344 00000 п. 0000045486 00000 п. 0000045628 00000 п. 0000045769 00000 п. 0000045910 00000 п. 0000046052 00000 п. 0000046194 00000 п. 0000046336 00000 п. 0000046478 00000 п. 0000046620 00000 н. 0000046762 00000 н. 0000046904 00000 н. 0000047045 00000 п. 0000047186 00000 п. 0000047328 00000 п. 0000047472 00000 п. 0000047935 00000 п. 0000048433 00000 п. 0000048723 00000 п. 0000048993 00000 н. 0000049385 00000 п. 0000049673 00000 п. 0000049954 00000 н. 0000049984 00000 н. 0000050276 00000 н. 0000050563 00000 п. 0000050794 00000 п. 0000050817 00000 п. 0000059726 00000 п. 0000059749 00000 п. 0000062644 00000 п. 0000062668 00000 п. 0000079367 00000 п. 0000079391 00000 п. 0000096085 00000 п. 0000096108 00000 п. 0000101748 00000 н. 0000101771 00000 н. 0000106486 00000 н. 0000106509 00000 н. 0000111225 00000 н. 0000111248 00000 н. 0000117551 00000 н. 0000151143 00000 н. 0000178018 00000 н. 0000183578 00000 н. 0000206713 00000 н. 0000213583 00000 н. 0000213642 00000 п. 0000213778 00000 н. 0000213985 00000 п. 0000214093 00000 н. 0000214200 00000 н. 0000214309 00000 н. 0000214416 00000 н. 0000214525 00000 н. 0000214631 00000 н. 0000214739 00000 н. 0000214847 00000 н. 0000214954 00000 н. 0000215060 00000 н. 0000215166 00000 н. 0000215273 00000 н. 0000215380 00000 н. 0000215490 00000 н. 0000215599 00000 н. 0000215708 00000 н. 0000215816 00000 н. 0000215922 00000 н. 0000216029 00000 н. 0000216136 00000 н. 0000216243 00000 н. 0000216352 00000 н. 0000216458 00000 н. 0000216564 00000 н. 0000216671 00000 н. 0000216777 00000 н. 0000216887 00000 н. 0000216994 00000 н. 0000217101 00000 п. 0000217212 00000 н. 0000217318 00000 н. 0000217424 00000 н. 0000217530 00000 н. 0000217639 00000 н. 0000217746 00000 н. 0000217853 00000 н. 0000217960 00000 н. 0000218066 00000 н. 0000218175 00000 н. 0000218283 00000 н. 0000218392 00000 н. 0000218499 00000 н. 0000218606 00000 н. 0000218714 00000 н. 0000218820 00000 н. 0000218926 00000 н. 0000219032 00000 н. 0000219138 00000 н. 0000219247 00000 н. 0000219355 00000 н. 0000219462 00000 н. 0000219572 00000 н. 0000219679 00000 н. 0000219785 00000 н. 0000219892 00000 н. 0000219998 00000 н. 0000220105 00000 н. 0000220214 00000 н. 0000220321 00000 н. 0000220429 00000 н. 0000220536 00000 н. 0000220642 00000 н. 0000220749 00000 н. 0000220855 00000 н. 0000220961 00000 н. 0000221068 00000 н. 0000221176 00000 н. 0000221285 00000 н. 0000221392 00000 н. 0000221499 00000 н. 0000221607 00000 н. 0000221713 00000 н. 0000221821 00000 н. 0000221930 00000 н. 0000222040 00000 н. 0000222146 00000 н. 0000222253 00000 н. 0000222360 00000 н. 0000222469 00000 н. 0000222577 00000 н. 0000222684 00000 н. 0000222790 00000 н. 0000222899 00000 н. 0000223005 00000 н. 0000223115 00000 н. 0000223222 00000 н. 0000223329 00000 н. 0000223435 00000 н. 0000223541 00000 н. 0000223649 00000 н. 0000223756 00000 н. 0000223862 00000 н. 0000223969 00000 н. 0000224077 00000 н. 0000224184 00000 п. 0000224292 00000 н. 0000224399 00000 н. 0000224505 00000 н. 0000224612 00000 н. 0000224722 00000 н. 0000224830 00000 н. 0000224937 00000 н. 0000225044 00000 н. 0000225151 00000 н. 0000225260 00000 н. 0000225367 00000 н. 0000225473 00000 н. 0000225580 00000 н. 0000225688 00000 н. 0000225795 00000 н. 0000225903 00000 н. 0000226011 00000 н. 0000226122 00000 н. 0000226228 00000 н. 0000226334 00000 н. 0000226441 00000 н. 0000226549 00000 н. 0000226655 00000 н. 0000226747 00000 н. 0000226855 00000 н. 0000226960 00000 н. 0000227068 00000 н. 0000227176 00000 н. 0000227285 00000 н. 0000227392 00000 н. 0000227499 00000 н. 0000227605 00000 н. 0000227712 00000 н. 0000227818 00000 н. 0000227925 00000 н. 0000228032 00000 н. 0000228139 00000 н. 0000228247 00000 н. 0000228355 00000 н. 0000228461 00000 п. 0000228568 00000 н. 0000228675 00000 н. 0000228782 00000 н. 0000228891 00000 н. 0000229000 00000 н. 0000229106 00000 н. 0000229214 00000 н. 0000229322 00000 н. 0000229430 00000 н. 0000229537 00000 н. 0000229644 00000 н. 0000229752 00000 н. 0000229858 00000 н. 0000229969 00000 н. 0000230076 00000 н. 0000230183 00000 п. 0000230292 00000 н. 0000230398 00000 н. 0000230507 00000 н. 0000230614 00000 н. 0000230720 00000 н. 0000230827 00000 н. 0000230933 00000 п. 0000231039 00000 п. 0000231146 00000 н. 0000231252 00000 н. 0000231358 00000 н. 0000231464 00000 н. 0000231571 00000 н. 0000231679 00000 н. 0000231787 00000 н. 0000231896 00000 н. 0000232002 00000 н. 0000232108 00000 н. 0000232215 00000 н. 0000232322 00000 н. 0000232429 00000 н. 0000232536 00000 н. 0000232643 00000 н. 0000232750 00000 н. 0000232856 00000 н. 0000232962 00000 н. 0000233068 00000 н. 0000233176 00000 н. 0000233284 00000 н. 0000233390 00000 н. 0000233496 00000 н. 0000233604 00000 н. 0000233712 00000 н. 0000233820 00000 н. 0000233926 00000 н. 0000234033 00000 н. 0000234140 00000 н. 0000234247 00000 н. 0000234354 00000 п. 0000234461 00000 п. 0000234567 00000 н. 0000234673 00000 п. 0000234779 00000 н. 0000234888 00000 н. 0000234996 00000 н. 0000235102 00000 п. 0000235211 00000 н. 0000235317 00000 н. 0000235424 00000 н. 0000235530 00000 н. 0000235638 00000 п. 0000235745 00000 н. 0000235851 00000 п. 0000235957 00000 н. 0000236064 00000 н. 0000236171 00000 н. -Q2Bbzg $ +] uM? 0g # w * Z \ `s_ \ PUtdi 1l0 Ո f7kd Co [OHt TbToPFwnm3A ݑ ww: 5-z ߃ > с bAuȕF_
Периодическая таблица меняется на 150.Пожалуйста, хлопайте в ладоши.
В 1669 году Хенниг Бранд, немецкий торговец и алхимик, провел новый эксперимент, который, как он надеялся, приведет к получению мифического «философского камня» – способа прядения неблагородных металлов в золото. Его точная формула утеряна для истории, но мы знаем, что он нагревал мочу в реторте или стеклянной камере до тех пор, пока сосуд не засветился и капающая жидкость не загорелась. Оказалось, что моча не была источником золота. Это был источник фосфора, ранее неизвестного элемента, который был впервые выделен в лаборатории.Чтобы превратить открытие в прибыль, если не в буквальное золото, потребовались бы более сообразительные деловые умы, но его усилия не были потрачены зря. Бранд использовал светящийся экстракт в самодельных лампах, которые он использовал для чтения алхимических текстов после наступления темноты.
Если вы не слышали, 2019 год объявлен «Международным годом Периодической таблицы химических элементов (IYPT 2019)». Подайте сигнал фейерверку.
Так идет марш науки. Два столетия спустя, в 1869 году, гений сибирского происхождения по имени Дмитрий Менделеев, вдохновленный мечтой или крайним сроком публикации, организовал известные тогда 63 элемента в ряды и столбцы в соответствии с их весом и химическими свойствами.(Он обозначил фосфор как №15.) И вот настоящий гениальный штрих: он оставил поля-заполнители для элементов, где они, как ожидалось, должны были существовать, но еще не были обнаружены.
Как, спросите вы, Менделеев знал то, чего не знал? Проще говоря, он расположил все известные элементы в порядке от самых легких до самых тяжелых, начиная с водорода. Затем он организовал их в семь горизонтальных рядов или периодов и 18 вертикальных столбцов или групп, члены которых имеют схожие физические и химические свойства – как «щелочные металлы» в первой группе, которые известны своей пластичностью и электропроводностью.Затем, когда он установил четкие шаблоны свойств и поведения, он понял, что в его таблице есть пробелы, места, где должно быть других элементов – и особые виды элементов с предсказуемыми свойствами. Неважно, что такие вещества никогда не были обнаружены или обработаны в алхимии – Менделеев понимал, что целостность его системы зависит от существования этих отсутствующих в то время элементов.
Умный сибиряк изобрел свою гениальную таблицу до открытия электронов, квантовой теории или 16 радиоактивных элементов, созданных Гленном Сиборгом и другими в Калифорнийском университете в Беркли.Тем не менее, с некоторыми изменениями, его проницательное расположение элементов выдержало – в отличие, скажем, от волнистого представления Аристотеля о том, что мир состоит из четырех элементов: земли, воды, огня и воздуха – принесло Менделееву бесспорный титул «отца периодического света». стол.”
ПОЧЕМУ НАПИСАТЬ ОБ ЭТОМ СЕЙЧАС? Что ж, если вы не слышали, 2019 год объявлен Генеральной Ассамблеей Организации Объединенных Наций и ЮНЕСКО «Международным годом Периодической таблицы химических элементов (IYPT 2019)».
Подайте фейерверк.
Человек в Белом доме не писал в Твиттере о IYPT 2019, что могло бы помочь объяснить, почему слухи о праздновании так долго не доходили до Твиттерсферы. С другой стороны, в последний раз большинство американцев видели периодическую таблицу Менделеева, когда она висела в классе Уолтера Уайта на Во все тяжкие, . Скорее всего, вы его почти не заметили, как и тот, что на вашем уроке химии. Более того, жаль, потому что, по выражению ООН, таблица – это «одно из самых значительных достижений в науке, отражающее суть не только химии, но также физики и биологии».”
Как, спросите вы, Менделеев знал то, чего не знал? Проще говоря, он расположил все известные элементы в порядке от самых легких до самых тяжелых, начиная с
водорода.
Химик из Беркли Джон Арнольд попал под чары стола, когда еще учился в старшей школе в Ланкашире, Англия. Для Арнольда, ныне профессора и декана химического колледжа, в творении Менделеева есть что-то волшебное. «Я считаю, что это действительно одно из величайших научных достижений всех времен», – говорит Арнольд.«Мы можем связать то, что происходит в нашей жизни каждый день, с этой простой двумерной картиной».
Как и Арнольд, Ли Бернштейн, профессор ядерной инженерии, руководитель группы ядерных данных в лаборатории Беркли и Калифорнийском университете в Беркли, благоговейно относится к столу Менделеева. «Это повторение, эта идея, что вы достигнете одного конца, а затем начнете снова с другого, – это великолепно. Однако это не просто великолепно. Это прекрасно. И это красиво, я бы сказал, так же красиво, как солнце встает утром.”
Имейте в виду, Менделеева не первая и не единственная таблица Менделеева. Примечательно, что немецкий химик Лотар Мейер опубликовал аналогичную модель всего через несколько месяцев после Менделеева. Но так же, как Дарвину приписывают теорию эволюции – в отличие от его соперника, Альфреда Рассела Уоллеса, – история помнит Менделеева, а не Мейера. Тем не менее, Мейер разделил крупную награду со своим российским коллегой за их независимую работу по установлению периодического закона, который гласит, что, когда элементы расположены в порядке атомной массы, физические и химические свойства будут периодически повторяться.
Арнольд называет это явление «танцем электронов» и говорит о «магическом числе восемь». Как в восьми электронах.
Он объясняет: «Есть очень сильная тенденция попадания вещей в число восемь так или иначе. Один из способов сделать это – потерять или приобрести электроны в своей валентной оболочке. И вы очень ясно видите на периодической таблице, что, начиная с левой стороны, наблюдается очень сильная тенденция к потере электронов ».
Рассмотрим, например, случай натрия (Na), крайний слева, и хлора (Cl) в группе 17, один справа.(На фото выше.)
Социальная жизнь элементов, кажется, – это химия, изучение того, как атомы соединяются с другими атомами, образуя соединения.
«Каждый из них недоволен», – говорит Арнольд. «У одного есть семь электронов» – говоря здесь о внешней оболочке хлора, орбитали, которая определяет, скажем так, беспокойство атома, – «а у одного есть только один. И вот они делают эту сделку. Они говорят: «Хорошо, у меня есть электрон, который мне не нужен, а вы действительно хотите его». И вы получаете что-то, что находится в океанах, и вы можете его выкопать, и это очень стабильно.«Удачный результат – хлорид натрия (NaCl), широко известный как поваренная соль.
«Это разница между числом электронов, которое имеет элемент, и числом электронов, которое он хотел бы иметь, чтобы иметь стабильную конфигурацию, подобную благородному газу», – объясняет Бернштейн. «Менделеев понял, что, например, элементы группы 1А» или щелочные металлы – крайний левый столбец таблицы – «все обладают очень похожими свойствами, они взрываются при контакте с водой или сгорают вместе с кислородом. Он не обязательно знал почему.Но он знал, что в этом отношении все они были общими ».
Гонка до восьми очевидна даже при взгляде на кислород в столбце 16, всего в двух позициях от неона, у самого восточного края стола.
«Кислород хочет быть неоном», – объясняет Бернштейн, признавая, казалось бы, универсальную привычку химиков и ученых-ядерщиков антропоморфизировать элементы. «Природа стремится минимизировать энергию. Сказать, что атом хочет что-то сделать, – это то же самое, что сказать, что происходит высвобождение энергии.И чем больше он этого хочет, тем больше выделяется энергии ».
Так почему же кислород хочет быть неоном?
«Неон стабилен. Все элементы в этом ряду, – он проводит пальцем по правому краю таблицы Менделеева ручной работы, подаренной ему бывшим студентом, – стабильны. Они благородные, у них низкоэнергетическая конфигурация “. Другими словами, у них есть полный набор из восьми валентных электронов. «Они не хотят взаимодействовать».
Самый верхний элемент в этом столбце – гелий, единственный элемент в верхнем ряду, кроме водорода.Водород сидит один в верхнем левом углу благодаря своему единственному протону. Это тоже несчастливо.
«Идея о том, что вы достигнете одного конца, а затем начнете снова с другого, – это великолепно. Однако это не просто великолепно. Это прекрасно. И это прекрасно, я бы сказал, так же красиво, как солнце, восходящее утром ».
«Один – одинокое число, – говорит Бернштейн, – потому что природе нравится иметь вещи парами. Итак, если я перейду к двум протонам – гелию, – он станет гораздо менее химически активным.Очень стабильно. На самом деле это заносчиво. Он не любит играть с другими элементами. Поэтому мы называем это благородным газом ».
Социальная жизнь элементов, кажется, – это химия, изучение того, как атомы соединяются с другими атомами, образуя соединения. И, как демонстрирует собственная работа Бернштейна, таблица Менделеева достаточно обширна, чтобы охватить даже ядерную физику, изучение того, как атомы могут быть разнесены на части или преобразованы – если хотите, алхимически преобразованы – в форму новых радиоактивных элементов.У нас есть искусственная радиоактивность, за которую стоит благодарить светящиеся циферблаты часов, ПЭТ-сканирование и радиотерапию, а также проклинать ядерное оружие. (Когда дело доходит до ядерной энергии, кажется, популярными вариантами являются и благодарность, и проклятие.)
Совместное использование электронов в своих внешних оболочках – это то, как элементы связываются со своими соседями. Если их количество протонов изменится, они фактически станут своими соседями. В отличие от электронов, протоны находятся с нейтронами внутри ядра атома, что является областью не химии, а ядерной физики.Представьте электроны как планеты, вращающиеся вокруг Солнца – ядра.
Ускоритель элементарных частиц, изобретенный Эрнестом О. Лоуренсом, тезкой лабораторий Ливермора и Беркли, позволил его коллегам и академическим потомкам создавать странные новые элементы путем реструктуризации самих атомов. Эта глава табличной истории началась в 1937 году с технеция, который Менделеев не определил, но ожидал как элемент 43. Менделеев даже предвидел тяжелые радиоактивные элементы, которые расширили число известных элементов далеко за пределы 88, обнаруженных в природе.(Некоторые источники приводят доводы в пользу 92 или 94, но многие ученые-ядерщики, в том числе Бернштейн, не приписывают радиоактивным элементам такие короткие периоды полураспада, что они скорее отсутствуют, чем присутствуют в природе.) Шестнадцать из этих так называемых трансурановых элементов, включая берклий, калифорний, лоуренсий и сиборгий, были открыты (и, как вы, наверное, догадались, получили название) учеными из Беркли. (Подробнее о берклиуме здесь.)
Это Сиборг, не случайно, ответственен за две отколовшиеся строки, обнаруженные в современных интерпретациях таблицы Менделеева.Это лантаноиды и актиниды, которые математически связывают барий (56) и гафний (72) в строке 6, а также радий (88) и резерфорд (104) в строке 7 соответственно. Достаточно сказать, что это вводит нас в сферу квантовой механики и открытия орбитальных форм. Без резиновых перчаток и защитных очков не рекомендуется более глубокое исследование нижних областей стола.
«Это просто потрясающая, удивительная вещь, которую слишком многие люди принимают как должное. Я могу придумать очень мало с научной точки зрения.”
Дело, когда мы празднуем IYPT 2019, заключается в том, что периодическая таблица включает в себя даже те элементы, которые Менделеев никогда не мог себе представить, те, которые созданы только путем разбивания атомов с непостижимой скоростью субатомными частицами из машины, которая не существовала до десятилетий после его смерти. . Общее количество известных элементов в настоящее время составляет 118, но, вероятно, их количество будет еще больше.
«Я уверен, что мы откроем для себя новые элементы», – говорит Арнольд, – «119, 120 находятся в поле зрения людей в России и в США.S., и, вероятно, Япония. Если у нас будет достаточно времени и усилий, мы доберемся туда ».
И какие бы новые элементы ни появлялись, всем им будет место за столом Менделеева, несмотря на неизбежные попытки понять, где именно их усадить.
«Это просто потрясающая, удивительная вещь, которую слишком многие люди принимают как должное», – говорит Арнольд. «С научной точки зрения я могу придумать очень немногое. E = mc 2 , Думаю, почти все знают, потому что это легко и быстро, а однажды услышав это, трудно забыть.Таблица Менделеева примерно такая же. Это очень похоже на мем, это в некотором смысле стало частью всего. Это – это всего, наверное, поэтому ».
Итак, имея это в виду, давайте склоним сосуд с русской водкой к 150 годам периодической таблицы Менделеева, включим “Стихии” Тома Лерера на караоке-машине и устроим вечеринку, как в 1869 году.
Людям с благородным газом настоятельно рекомендуется держаться от себя высокомерных, чтобы не погубить кайф для остальных из нас.
Барри Бергман занимает особое место в своем сердце для The Elements of Style. Он женат на научном журналисте.
Кто изобрел Периодическую таблицу?
- дом
- Блог
- Кто изобрел периодическую таблицу?
Периодическая таблица Менделеева занимает центральное место в изучении химии и используется для последовательной организации химических элементов. Разработка периодической таблицы имеет долгую историю, в которой участвовали многие ученые на протяжении сотен лет.Но кто это на самом деле придумал? Как менялась периодическая таблица Менделеева с годами? Почему изобретатель таблицы организовал ее так, как мы ее используем сегодня?
Было много людей, которые внесли свой вклад в идеи, лежащие в основе периодической таблицы Менделеева, но некоторые цифры заслуживают большего доверия, чем другие.
События древности
Возвращаясь к древним временам, мы можем увидеть корни нашего понимания элементов, составляющих периодическую таблицу.В Древней Греции Аристотель и Платон считали, что все на планете происходит из четырех источников. Это были огонь, вода, воздух и земля. Таким образом, мы можем сказать, что древние греки действительно понимали природу элементов и их сущность. Но они мало что сделали для улучшения нашего понимания материи; это будет позже.
Открытия XVII и XVIII веков
Именно в 17-18 веках мы можем начать видеть происхождение периодической таблицы Менделеева, которая связана с открытием первых химических элементов.Хенниг Бранд провел эксперименты, которые привели к открытию фосфора в 1669 году. Это было первое открытие элемента. Антуан-Лоран де Лавуазье написал первый современный учебник по химии в 1789 году. В этой книге перечислены основные элементы, которые были определены как мельчайшие частицы материи, которые нельзя было подразделить дальше. Это было основой нашего современного понимания элементов.
Вклад Джона Ньюлендса
Джон Ньюлендс был очень важной фигурой в химии XIX века.Он был первым химиком, который взял список известных в то время элементов и разделил их на разные группы. Это то, что позже станет очень важным, когда будет создана первая правильная таблица Менделеева. Он предложил закон октав для разделения и разделения элементов. Это произошло потому, что он заметил сходство атомного веса и физических свойств химикатов в каждых 8 химикатах в своем списке. Его открытия были впервые опубликованы в Chemistry News в середине 1860-х годов.
Слово «периодический» происходит от его работ и открытий, поэтому его влияние на современную таблицу Менделеева явно очень важно.Есть даже люди, которые до сих пор считают его главной движущей силой разработки периодической таблицы элементов. В последние годы Королевское химическое общество официально признало его влияние и вклад. Однако он не считается самым важным автором периодической таблицы Менделеева.
Другие пожертвования XIX века
В 1862 году французский геолог по имени Александр-Эмиль Бегуйе де Шанкуртуа был первым, кто заметил периодичность химических элементов.Его открытия предшествовали открытиям Джона Ньюлендса, который проделал аналогичную работу в этой области химии. Он написал другую раннюю форму таблицы Менделеева, которая была организована по атомному весу, но она не такая, как та, которую мы знаем и признаем сегодня.
Иоганн Вольфганг Доберейнер работал за несколько лет до Александра-Эмиля Бегуайера де Шанкуртуа, и он также пытался объединить химические элементы. Он был одним из первых, кто это сделал. Он использовал группы из трех человек, чтобы организовать элементы, и назвал эти группировки триадами.Например, он сгруппировал бы вместе хлор, бром и йод. Они были сгруппированы по химически аналогичным элементам, и их атомный вес увеличился. Эта работа была выполнена в конце 1820-х годов и оказала влияние на последовавших за ним химиков и выполнила другие работы по группировке химических элементов.
Дмитрий Менделеев: человек, которого считают изобретателем Периодической таблицы
Это имя чаще всего ассоциируется с изобретением периодической таблицы Менделеева.До этого момента в начале 19 века наблюдалось явное продвижение к концепции периодической таблицы. Дмитрий Иванович Менделеев, однако, был первым человеком, который составил таблицу Менделеева, очень близкую к той, что мы делаем сегодня. Таблица Менделеева состояла из 60 элементов, известных в то время. Он был русским химиком и сосредоточился на расположении элементов в соответствии с их атомной массой. Формальное изложение его идей 1869 года называлось «Зависимость между свойствами атомного веса элементов».Позже в том же году его таблица Менделеева была опубликована в одном из российских журналов.
Он обнаружил, что, когда его таблица Менделеева была устроена в порядке возрастания атомной массы, в элементах таблицы появлялись закономерности через равные промежутки времени. Это означало, что можно было делать прогнозы относительно физических свойств элементов, которые еще даже не были обнаружены. Кроме того, он также предсказал, что в будущем будут обнаружены другие элементы с различной атомной массой, и оставил места для этих элементов в своей таблице.
Лотар Мейер: соавтор Периодической таблицы?
Хотя Менделеев считается главным человеком, стоящим за изобретением таблицы Менделеева, это не решенный вопрос. В то же время были другие люди, которые выполняли аналогичную работу. Многие люди считают Лотара Мейера законным соавтором современной таблицы Менделеева. В его таблице элементы упорядочены по повторяющимся образцам и физическим свойствам, как и в таблице Менделеева. Работа Мейера по-прежнему очень впечатляет и важна.Однако эти две таблицы не были одинаковыми, и Мейеру не хватало некоторых ключевых моментов.
Например, таблица Мейера не была упорядочена по атомному весу. Вместо этого таблица Мейера была организована по валентности, которая является мерой того, насколько легко элементы объединяются с другими элементами для образования соединений. Его работа была опубликована примерно на 5 лет раньше Менделеева и состояла из таблицы из 28 элементов. В конце концов, Менделеев считается изобретателем периодической таблицы, потому что его расположение элементов позволило точно предсказать свойства элементов, которые в то время не были известны.
Дополнительные взносы ХХ века
Разработка таблицы Менделеева не остановилась в конце 19 века. Были дальнейшие разработки и открытия, которые произошли совсем недавно, в первой половине 20 века. Генри Мозли – самый выдающийся автор периодической таблицы в 20 веке. За год до своей смерти в Первой мировой войне Мозли обнаружил, что длина волны рентгеновского излучения элемента связана с его атомным номером.
Это привело его к тому, что он разместил кобальт и никель в периодической таблице в правильном порядке. Его открытие также привело его к выводу, что в периодической таблице должно быть больше пробелов, и теперь они заполнены другими элементами, которые с тех пор были обнаружены. В 1940-х годах Гленн Т. Сиборг во время работы над Манхэттенским проектом обнаружил правильное расположение рядов актинидов и лантанидов в современной периодической таблице.
Почему Периодическая таблица Менделеева устроена именно так?
Возникает естественный вопрос: почему периодическая таблица Менделеева устроена именно так? Все сводится к группировке элементов.Когда таблица организована в соответствии с атомной массой элемента, физические свойства элементов проявляются периодически. Около двух третей таблицы слева занимают металлы. И правая часть таблицы посвящена неметаллам. Эти две секции разделяет небольшая полоса элементов, известных как металлоиды.
Периодическая таблица Менделеева постоянно пересматривается, и свойства элементов постоянно открываются. Периодическая таблица изменяется по мере открытия новых элементов, что происходит, когда новые элементы мгновенно создаются в ускорителях частиц и других ядерных экспериментах.Периодическая таблица Менделеева – это инструмент, который используется во всех областях науки и техники и облегчает решение сложных проблем.
Периодическая таблица – обзор
I.A Элементарные и атомные концепции
Периодическая таблица, великая классификационная схема химии, основана на двух наиболее фундаментальных концепциях в физической науке – элементах и атомах. В своих зачаточных формах обе эти идеи были изобретением досократических греческих философов.Первым из этих мыслителей был Фалес Милетский (ок. 624–545 до н. Э.), Который разделял идею о том, что вся материя происходит из одной субстанции. В то время как он считал воду элементарной субстанцией, другие, такие как Анаксимен, Гераклит и Анаксимандр, отдавали предпочтение воздуху, огню и апейрону (вечному, неограниченному элементу) соответственно.
Где-то около 450 г. до н. Э. Эмпедокл (ок. 490–430 до н. Э.), Кажется, синтезировал некоторые из этих идей в своем аргументе о том, что вся материя состоит из различных смесей четырех первичных веществ – земли, воздуха, огня и воды.Два величайших философа классической античности, Платон (428–347 до н.э.) и Аристотель (384–322 до н.э.), переняли четыре элемента Эмпедокла, хотя Аристотель добавил пятый, quita essentia , который составлял кристаллические сферы небес. . Хотя некоторые ученые признали эти элементы еще в 17 веке, важно понимать, что эти четыре элемента были скорее философскими конструкциями, чем конкретными сущностями с химическими последствиями.
Точно так же древние греки предложили атомы не столько для объяснения конкретных природных явлений, сколько для объяснения постоянства среди изменений.Такие атомисты, как Демокрит из Абдеры (ок. 460–370 до н. Э.), Утверждали, что тело не может быть бесконечно разделено на части. В конечном итоге процесс должен был остановиться на уровне «неразрезанной» частицы, буквально ατ oμ os. Римский поэт Лукреций (ок. 100–55 до н. Э.) Утверждал, что атомы и пустота составляют все вещи, и развил эту идею для объяснения метеорологии и геологии, ощущений и секса, космологии и социологии и даже жизни и разума. Несмотря на столь амбициозную всесторонность, атомы не получили такого широкого признания, как четыре земных элемента, в основном потому, что Аристотель отверг их.Тем не менее, концепция элементарных частиц материи иногда использовалась в качестве рабочей гипотезы такими учеными, как Гассенди, Галилей, Бойль и Ньютон. Действительно, Ньютон зашел так далеко, что выразил это мнение: «Мне кажется вероятным, что Бог в Начальной форме имел Материю в твердых, массивных, твердых, непроницаемых, подвижных Частицах».
Таким образом, к 1700 году успехи химии поставили идею четырех элементов под серьезный вопрос, в то время как идея атомов получила научное распространение.Последовавший за этим век сделал многое для дальнейшего утверждения последнего и свержения первого. Антуан Лоран Лавуазье (1743–1794), француз, которого часто считают «отцом современной химии», сформулировал рабочее определение «простой субстанции» в своем тексте 1789 года, Traité Élementaire de Chimie . Первое издание включало таблицу из 33 элементарных веществ, которые не могли быть разложены химическими операциями. В этой таблице элементы были разделены на группы, такие как métalliques и non métalliques .Большинство металлов, перечисленных Лавуазье (например, сурьма, серебро, медь и железо), были известны и использовались веками. То же самое было и с некоторыми неметаллами, такими как углерод и сера. Однако список Лавуазье также включал водород, кислород и азот – три газа, которые были недавно изолированы и, благодаря его теоретической системе, правильно идентифицированы как специфические элементарные вещества. По сути, все 33 исходных вещества Лавуазье все еще присутствуют в современной периодической таблице.Предположение Лавуазье о том, что пять «земель», которые он включает – известь, магнезия, барита, алюмний и кремнезем, – на самом деле могут быть сложными веществами, подтвердилось. Теперь мы знаем, что это оксиды кальция, магния, бария, алюминия и кремния. Две его записи, свет и тепло, вообще не являются материалами. Тем не менее концепция простых веществ Лавуазье и его предварительный список оказались очень важными для развития химии и периодической классификации элементов.
Например, четко определенная рабочая концепция элемента была необходима для разработки атомной теории Джоном Далтоном (1766–1844). В 1808 году этот английский школьный учитель опубликовал A New System of Chemical Philosophy , в котором изложил свои постулаты о структуре материи. Каждый элемент, утверждал Дальтон, состоит из идентичных, неизменных и уникально характерных атомов. Когда элементы объединяются в соединения, их атомы объединяются в фиксированном соотношении, которое характерно для соединения.Поскольку эти числа фиксированы, элементарный состав соединения по массе также постоянен. Это последнее свойство можно было довольно точно определить даже во времена Дальтона. Однако у Дальтона не было прямого способа установить правильное атомное соотношение элементов любого соединения. Как следствие, он не мог с уверенностью вычислить относительные массы атомов различных элементов – их атомные массы или атомные веса. Атомные массы элементов и атомные отношения, характерные для конкретных соединений, проявляются в элементарном массовом составе соединений.Как только правильное атомное соотношение известно, атомные массы могут быть легко вычислены на основе массового состава. В качестве альтернативы, знание атомных масс позволяет преобразовать состав по массе в состав по атомному соотношению. Однако Далтон столкнулся с дилеммой уравнения с двумя неизвестными.
Эта дилемма продолжала преследовать химию в течение 50 лет и, следовательно, ограничивала полезность атомной теории. Из-за важности массовых соотношений в химических реакциях был консенсус, что характерная атомная масса элемента была важным свойством.Однако не было единого мнения о том, какие значения были правильными. Водород обычно считался самым «легким» элементом и, следовательно, ему обычно приписывалась атомная масса 1.
