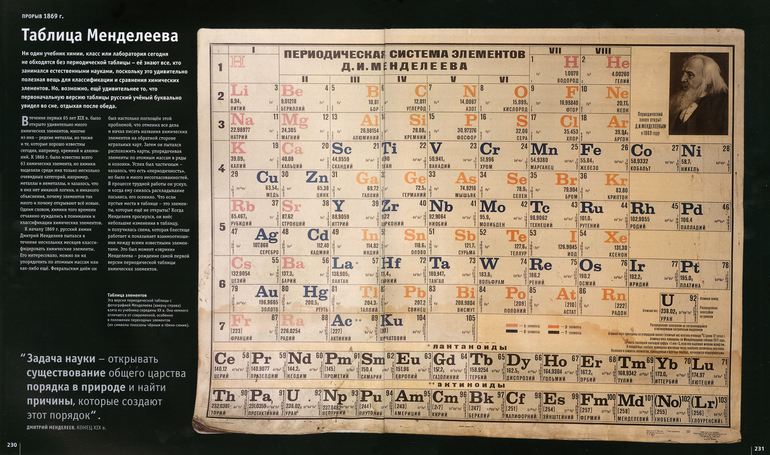
20 фактов, которые скрываются за таблицей Менделеева. Теперь вы не скажете, что химия — скучная наука
150 лет назад (в 1869 году) Д.И. Менделеев выступил с докладом об открытии периодического закона — взаимосвязи между свойствами химических элементов и их атомной массой. Но окончательно его вклад в науку признали только в середине 80-х годов XIX века, когда сбылись предсказания ученого об открытии новых веществ (галлия, скандия, германия). С тех пор таблица Менделеева существенно расширилась, а любая клетка в ней — результат многих лет работы исследователей из разных веков и стран.
AdMe.ru подготовил подборку фактов о таблице Менделеева, отобранных свежим взглядом. Вы даже узнаете, как она связана с географией Земли, если дочитаете до бонуса в конце статьи.
1. Названия лишь 2 элементов в таблице связаны с реальными женщинами
2. Литий — металл, который не тонет в воде (и керосине)
3. Соединения неодима меняют цвет в зависимости от освещения
4.
 Кристаллы йода — черные, его спиртовой раствор — желто-коричневый, а пары — фиолетовые
Кристаллы йода — черные, его спиртовой раствор — желто-коричневый, а пары — фиолетовые5. Индий настолько мягкий, что его можно откусить зубами
6. И название «индий» не имеет отношения к Индии. Все из-за цвета индиго, в который он окрашивает пламя горелки
7. О плотности элементов наглядно. Вот как выглядит 1 г разных металлов
8. Задолго до нашей эры сурьмой и ее сульфитом (антимонитом) подводили глаза и чернили брови. Жаль, что эта красота токсична
9. Селен выглядит как эритроцит, борется с перхотью и даже отметился при создании красного стекла для рубиновых звезд Московского Кремля
10. Аргон — самый распространенный инертный газ на земле. С его помощью создают атмосферу, в которой не происходят реакции у элементов, чувствительных к воздуху и воде
11. Цезий невероятно химически активен (поэтому его хранят в ампулах с аргоном)
12. Уран выглядит как обычный серый металл, но его соединения действительно светятся зеленым в ультрафиолете
13.
 Вольфрам расплавить труднее, чем все остальные металлы. Понадобится температура около 3 400 °C (для сравнения: железо плавится при 1 500 °C)
Вольфрам расплавить труднее, чем все остальные металлы. Понадобится температура около 3 400 °C (для сравнения: железо плавится при 1 500 °C)14. Как выглядит отбеливание хлором
15. Всего лишь 2 ученых увековечили в таблице Менделеева еще при жизни
16. Ксенон считается допингом: при его вдыхании увеличивается выносливость спортсменов и эффективность тренировок
17. Европий напоминает золотистые перья. Вещества на его основе используют для защиты банкнот евро от подделок
18. Титан — один из самых твердых металлов. Его диоксид переливается всеми цветами радуги, поэтому им покрывают камни для украшений
19. В списке элементов отметился бог: в честь Тора назван торий. И древнегреческий титан Прометей, который дал имя прометию
20. Серебряная кнопка от YouTube сделана из цинка и покрыта настоящим серебром (по версии блогера-химика)
Бонус: химическая география
Названия многих химических элементов связаны со странами и географическими объектами в них:
1. США: Bk — берклий, Cf — теннессин, Lv — ливерморий.
США: Bk — берклий, Cf — теннессин, Lv — ливерморий.
2. Америка: Am — америций.
3. Франция: Fr — франций, Lu — лютеций, Ga — галлий.
4. Скандинавия: Sc — скандий.
5. Дания: Hf — гафний.
6. Великобритания: Sr — стронций.
7. Европа: Eu — европий.
8. Швеция: Ho — гольмий, Tb — тербий, Er — эрбий, Y — иттрий.
9. Германия: Ge — германий, Ds — дармштадтий, Hs — хассий, Re — рений.
10. Россия: Db — дубний, Mc — московий, Ru — рутений.
11. Индия: Be — бериллий.
12. Япония: Nh — нихоний.
Удалось ли нам вас удивить? Если бы в школе на уроках химии больше рассказывали о таких фактах, вы бы связали свою жизнь с этой наукой?
Интересные факты о современной таблице Менделеева
Генеральная ассамблея ООН провозгласила 2019 год Международным годом периодической таблицы химических элементов. Дмитрий Менделеев представил ее еще в 1869 году — с тех пор она остается актуальной и постоянно обновляется (например, только в 2016 году в нее включили четыре новых элемента).
 Издание Science News опубликовало подборку занимательных фактов. T&P пересказывают самое интересное.
Издание Science News опубликовало подборку занимательных фактов. T&P пересказывают самое интересное.Уран
Когда в 1896 году французский физик Анри Беккерель поместил соли урана на фотопластинку, он случайно обнаружил, что вещество радиоактивно, — и позже получил за это Нобелевскую премию. Уран — последний элемент в таблице Менделеева (номер 92), который встречается в природе. Все остальные синтезируют в лаборатории.
Золото
Специальная теория относительности Альберта Эйнштейна объясняет цвет золота. Из-за смещения уровней энергии электронов металл поглощает синий цвет, придавая отраженному свету желтый оттенок.
Ртуть
Когда путешественники Мериуэзер Льюис и Уильям Кларк в начале XIX века отправились в экспедицию к Тихому океану через всю Америку, они прихватили с собой 1300 доз ртутного слабительного (известного как «слабительное доктора Раша»). Двести лет спустя исследователи смогли точно установить, где находился лагерь путешественников в штате Монтана, благодаря следам неразлагающейся ртути.
Галлий
Менделеев оставил в первой версии периодической таблицы пустые места, чтобы дополнить ее новыми открытиями. Первым заполненным пробелом оказался галлий (номер 31), который открыли в 1875 году. Металлический галлий (остается твердым при комнатной температуре, но плавится при температуре выше 29,7° С) стал звездой благодаря химическому трюку, в котором сделанная из него ложка тает прямо в руке или стакане чая.
Гелий
Гелий обнаружили во время исследования хромосферы Солнца в 1868 году. Это случилось за 30 лет до того, как элемент впервые нашли на Земле. А в 2018 году ученые обнаружили гелий в атмосфере экзопланеты.
Оганесон
Оганесон — последний в колонке благородных газов. Однако он не такой надменный, как соседи: в отличие от того же гелия или аргона, оганесон с готовностью отдает свои и берет чужие электроны, а его атомы могут слипаться (по крайней мере, в теории).
Где можно учиться по теме #химия
Факты о Периодической системе химических элементов, которые вы не знали
Вы, вероятно, уже видели Периодическую таблицу элементов раньше. Возможно, она все еще является вам во снах, или, может быть, он канула для вас в небытие, будучи не более чем украшением стены класса, призванной сделать кабинет более солидным. Однако в этой системе, казалось бы, случайно расположенных ячеек есть нечто большее, чем кажется на первый взгляд.
Возможно, она все еще является вам во снах, или, может быть, он канула для вас в небытие, будучи не более чем украшением стены класса, призванной сделать кабинет более солидным. Однако в этой системе, казалось бы, случайно расположенных ячеек есть нечто большее, чем кажется на первый взгляд.10. Менделееву помогли
Фото: Wikimedia
Периодическая таблица используется с 1869 года, когда ее создал бородатый Димитрий Менделеев. Большинство людей думают, что Менделеев был единственным, кто изобрел таблицу и стал гениальным химиком века. Тем не менее, его усилия поддержали несколько европейских ученых, которые внесли важный вклад, чтобы сделать эту колоссальную диаграмму элементов полной.
Менделеев, как и положено, широко известен как отец Периодической таблицы, но он не документировал каждый известный нам элемент.
9. Новые дополнения
Фото: IUPAC
Хотите верьте, хотите нет, но Периодическая таблица не сильно изменилась с 1950-х годов. Однако 2 декабря 2016 года были добавлены четыре новых элемента: нихоний (элемент 113), московий (элемент 115), теннесин (элемент 117) и оганесон (элемент 118). Эти новые дополнения были озвучены в июне 2016 года, но, чтобы их можно было официально добавить в ПТ, потребовалось пять месяцев анализа.
Каждый из этих элементов был назван в честь города или государства, в котором они были обнаружены, за исключением оганесона, который был назван в честь российского физика-ядерщика Юрия Оганесяна за его усилия по документированию этого элемента.
8. Нет буквы «J»
В английском алфавите есть 26 замечательных букв, и каждая из них не менее важна, чем предыдущая и последующая. Однако Менделеев смотрел на это иначе. Попробуйте угадать, какая несчастная буква ни разу не встречается в ПТ? Вот подсказка: произносите буквы и загибайте пальцы на руках, пока не загнете все (если у вас есть все десять). Угадали? Правильно, это буква «J», которой ни разу не появилась в ПТ.
Однако Менделеев смотрел на это иначе. Попробуйте угадать, какая несчастная буква ни разу не встречается в ПТ? Вот подсказка: произносите буквы и загибайте пальцы на руках, пока не загнете все (если у вас есть все десять). Угадали? Правильно, это буква «J», которой ни разу не появилась в ПТ.
Говорят, один в поле не воин? Тогда, возможно, J – самая одинокая буква. Однако вот забавный факт: буква «J» чаще всего используется в именах для мальчиков, начиная с 2000 года. Итак, «J» получает достаточно внимания, не переживайте.
7. Искусственные элементы
Фото: Popocatomar
Как вы только что узнали, в Периодической таблице теперь есть целых 118 элементов. Можете догадаться, сколько из этих 118 сделано человеком? Из 118 элементов 90 можно найти в красивом месте, которое мы называем природой.
Как 28 элементов могут быть искусственными? Это, действительно, так. Мы синтезировали элементы с 1937 года и продолжаем делать это и сейчас. Хорошая новость заключается в том, что ПТ удивительна, и эти искусственные элементы можно легко обнаружить, если вам когда-нибудь станет любопытно. Просто посмотрите на элементы с 93 по 118. Полное разоблачение: этот диапазон включает в себя несколько элементов, которые очень редко встречаются в природе и поэтому почти всегда создаются в лабораториях, что также верно для элементов 43, 61, 85 и 87.
Просто посмотрите на элементы с 93 по 118. Полное разоблачение: этот диапазон включает в себя несколько элементов, которые очень редко встречаются в природе и поэтому почти всегда создаются в лабораториях, что также верно для элементов 43, 61, 85 и 87.
6. Элемент 137
В середине 20-го века, известный ученый по имени Ричард Фейнман (Richard Feynman) сделал серьезное заявление, которое задело за живое ученых всего мира, заставив их вечно ломать голову. Он сказал, что, если мы когда-нибудь обнаружим 137-й элемент, у нас не будет никакого способа количественно определить его протоны и электроны. 137 элемент отличается тем, что это значение константы тонкой материи, определяемой как вероятность того, что электрон поглотит фотон. Теоретически, 137 элемент будет иметь 137 электронов и 100-процентную вероятность поглощения фотона. Его электроны вращались бы со скоростью света. Еще более безумно, что электроны элемента 139, если такое вещество существует, должны вращаться быстрее скорости света.
Достаточно физики? Обдумайте это, и вам станет интересно (ну, так же интересно, как чтение об электронах). Элемент 137 в теории может объединить три важные части физики: скорость света, квантовую механику и электромагнетизм. С начала 1900-х годов физики предположили, что элемент 137 может лежать в основе Великой Единой Теории, которая могла бы соединить воедино все три вышеупомянутые области. По общему мнению, это звучит так же безумно, как Зона 51 с инопланетянами или Бермудский треугольник.
5. Что необычного в названии?
Почти все названия элементов имеют больше смысла и значения, чем вы могли бы представить. Они выбираются на случайно. Мы бы, например, назвали элемент первым словом, пришедшим нам в голову. «Керфлумп». Да, отлично.
Далее, свои истоки названия элементов берут в одной из пяти основных категорий. Одна из них – имена известных ученых, классический пример эйнштейниум. Элементы также могут быть названы в честь мест, где их задокументировали, например, германий, америций, галлий и так далее. Вариантом для названий могут служить названия небесных тел, таких как планеты. Уран впервые был обнаружен вскоре после открытия планеты Уран. Элементы могут получить имена из мифологии: например, есть титан в честь греческих Титанов и торий в честь скандинавского Бога грома—или Звездного Мстителя, что вам больше нравится.
Вариантом для названий могут служить названия небесных тел, таких как планеты. Уран впервые был обнаружен вскоре после открытия планеты Уран. Элементы могут получить имена из мифологии: например, есть титан в честь греческих Титанов и торий в честь скандинавского Бога грома—или Звездного Мстителя, что вам больше нравится.
Наконец, есть названия, которые описывают свойства элементов. Аргон происходит от греческого слова argos, что означает «ленивый» или «праздный». Сейчас вы решите, что аргон самый ленивый элемент. Эй, аргон, иди работать. Бром – еще одно такое название от греческого слова bromos, что означает «зловоние», что очень точно описывает ужасный запах брома.
4. Вряд ли это было вдохновение
Если вы хороши в картах, то этот факт только для вас. Менделееву необходимо было каким-то образом сортировать все элементы, и для этого нужен был системный подход. Естественно, чтобы разбить таблицу по категориям, он обратился к игре в пасьянс. Менделеев написал на отдельных картах атомный вес каждого элемента, и приступил к безумной игре в пасьянс, так сказать. Он укладывал элементы в соответствии со специфическими свойствами, которые формировали тип «масти». Затем он смог распределить эти вошедшие в определенную категорию элементы в колонки в соответствии с их атомным весом.
Многие из нас с трудом могут пройти уровни обычной игры в пасьянс, поэтому этот парень-игрок 1000-го уровня, очень впечатляет. Что дальше? Кто-то решит обратиться к шахматам, чтобы произвести революцию в астрофизике, а также построить ракету, которая сможет совершить полет к краю галактики и обратно, оставаясь при этом абсолютно стабильной? Это вполне возможно, если такой сумасшедший профессор, как Менделеев, смог систематизировать нечто огромное с помощью карточной игры.
3. “Нет” инертным газам
Фото: Wikimedia
Помните, как мы классифицировали аргон как самый ленивый и скучный элемент в истории Вселенной? Менделеев чувствовал нечто подобное. Когда в 1894 году аргон удалось впервые выделить, он не вписывался ни в одну из колонок новой таблицы, поэтому вместо того, чтобы найти способ внести дополнение, ученый решил отрицать существование этого элемента.
Еще более удивительно, что аргон не единственный несчастный элемент, который настигла подобная участь. Еще пяти элементам было оказано в существовании, как и неклассифицированному аргону. Просто какая-то дискриминация элементов. Шутки в сторону, радон, неон, криптон, гелий, ксенон – всем им было отказано в существовании, только потому, что Менделеев не смог найти для них место в таблице. После многих лет реконфигурации и повторной классификации эти счастливые элементы (называемые инертными газами) смогли войти в элитный клуб под названием «Существующие элементы».
2. Романтические соединения
Этот факт для вас, романтики. Если взять бумажную копию Периодической таблицы и вырезать средние столбцы, то получится периодическая таблица, в которой отсутствуют элементы. Сложите ее один раз в середине IV группы, и тадам – вы узнали, какие элементы могут образовывать соединения друг с другом.
Элементы, которые при этом «поцеловались», образуют стабильные соединения. У них дополняющие друг друга электронные структуры, которые позволяют их объединять. Если это не настоящая любовь, такая же как у Ромео и Джульетты, или даже Шрека и Фионы, тогда что это?
У них дополняющие друг друга электронные структуры, которые позволяют их объединять. Если это не настоящая любовь, такая же как у Ромео и Джульетты, или даже Шрека и Фионы, тогда что это?
1. Углерод главный
Углерод желает быть самым главным. Вы думаете, что знаете об углероде все, но нет. Этот плохой парень способен на большее, чем вы когда-либо думали. Знаете ли вы, что большее количество соединений содержит углерод, чем не содержит его? Как насчет того, что 20% веса живых организмов составляет углерод? Еще более странно, что каждый атом углерода в вашем теле был когда-то частью доли углекислого газа в атмосфере. Углерод не только является практически суперэлементом, но и четвертым по распространенности элементом во всей Вселенной.
Если бы Периодическая таблица была вечеринкой, вы бы захотели оказаться на ней рядом с углеродом. Кажется, этот элемент действительно умеет веселиться. Это также основной элемент алмазов, поэтому добавьте немного блеска в список его удивительных качеств.
7 малоизвестных фактов о химических элементах и таблице Менделеева
Генеральная ассамблея ООН провозгласила 2019 год Международным годом Периодической таблицы химических элементов.
Дело в том, что именно в этом году мы отпраздновали юбилей – 150 лет со дня открытия Дмитрием Ивановичем Менделеевым Периодического закона.
Во времена Менделеева уже было открыто больше шести десятков разных химических элементов, но всё ещё не было единой понятной и удобной классификации. Хотя многие учёные не раз пытались придумать концепцию для систематизации. Например, химик и музыкант Джон Александр Ньюленд предложил схему элементов, схожую с той, что впоследствии придумал Менделеев, но научное сообщество не восприняло всерьёз эту попытку, хотя бы потому, что там чрезмерно много внимания было уделено гармонии и связи с музыкой. Ещё один химик – Лотар-Юлиус Мейер – сначала старался расположить элементы по возрастанию степеней их окисления. Он предложил объединять элементы в «группы», но никак не раскрыл это понятие.
Он предложил объединять элементы в «группы», но никак не раскрыл это понятие.
В 1868 году в журнале Русского химического общества была опубликована схема периодической таблицы Менделеева. Извещение об этом получили все именитейшие учёные того времени. Суть открытия была в том, что изменения в свойствах веществ происходят не монотонно, а периодически, то есть свойства в группах элементов начинают повторяться. В 1871 году все свои идеи Менделеев объединил в один периодический закон. Это позволило не только упорядочить известные элементы, но и увидеть тенденцию и предсказать некоторые на тот момент ещё не открытые вещества.
Вокруг этого открытия, как и вокруг самой личности Дмитрия Ивановича, до сих пор вьётся много слухов и домыслов. Самые известные из них уже множество раз опровергнуты, но всё равно почему-то упорно повторяются в анекдотах. Например, принято считать, что Менделеев увидел концепцию своей таблицы во сне. То, что это далеко от истины, говорил и сам Менделеев. Он возмущался, что на протяжении двадцати лет бился над упорядочиванием элементов, это не было каким-то спонтанным озарением, и думать так, значит, обесценивать многолетний труд учёного. Ещё есть байка о том, что Менделеев якобы изобрёл водку. На самом же деле, это всего лишь локальная шутка, возникшая из-за темы его диссертации: «Рассуждение о соединении спирта с водой». Водку изобрели задолго до Менделеева.
Он возмущался, что на протяжении двадцати лет бился над упорядочиванием элементов, это не было каким-то спонтанным озарением, и думать так, значит, обесценивать многолетний труд учёного. Ещё есть байка о том, что Менделеев якобы изобрёл водку. На самом же деле, это всего лишь локальная шутка, возникшая из-за темы его диссертации: «Рассуждение о соединении спирта с водой». Водку изобрели задолго до Менделеева.
В общем, всё, что касается жизни самого Менделеева, очень часто вспоминается и обсуждается. Но мы сегодня попробуем рассказать немного больше о его периодической таблице и о некоторых элементах, открытие которых было интересным или курьёзным.
Вашему вниманию представляются 7 фактов о химических элементах, их свойствах и об их отношениях с таблицей Менделеева.
При чём здесь петух?
Шёл 1875 год. Молодой химик Лекок-де-Буабодран в совершенстве владел таким умением как спектральный анализ веществ. Это значит, что он отлично разбирался в том, какие цвета получаются при разложении света, пропускаемого через раскалённые вещества. Лекок практически наизусть знал все спектры, на которые можно разложить тот или иной элемент.
Лекок практически наизусть знал все спектры, на которые можно разложить тот или иной элемент.
И вот однажды Буабодран изучал минерал сфалерит – цинковую обманку. Химик обнаруживает в его спектре новый цвет. Ярко-фиолетовая линия, которую увидел Лекок, ранее ещё никем не была описана, а значит вполне возможно, что французскому учёному удалось открыть новый элемент.
Лекок-де-Буабодран сразу же описал своё открытие и поместил в конверт. Конверт отдал своему учителю – академику Вюрцу, но попросил его не вскрывать, а просто сохранить. Почему? Потому что прежде, чем делать громкое заявление об открытии нового элемента, он хотел это ещё много раз перепроверить, чтобы со своими преждевременными выводами не прослыть опрометчивым. Но осторожный Лекок боялся, что пока он будет перепроверять, кто-нибудь другой заявит о таком же открытии и опередит его, так что описанное и датированное описание эксперимента в запечатанном конверте было доказательством, что Лекок обнаружил это первым.
И вот, Лекок полностью убедился в своей правоте, множество перепроверок доказали, что он действительно открыл новый, неизвестный до этого химический элемент. Имя этому элементу он дал в честь своей родины – Франции, что по-латински «Галлия». По крайнее мере, это официальная версия. Некоторые же считают, что элемент галлий так назван из-за латинского слова «галлус» – петух. Почему петух? Потому что именно так переводится имя Лекок с французского.
Кстати, галлий – один из тех элементов, существование которых предсказал Менделеев. Так что этот элемент, найденный ещё при его жизни, доказал, что открытый им периодический закон работает.
Галлий плавится при очень низкой температуре: всего 30 градусов. Если взять в руку кусочек галлия, он расплавится. Зато если вы захотите этот кусочек испарить, то придётся нагреть его аж до 2200°C.
Металл против монахов
Антимониум – серебристо-белый металл, среди химиков больше известный как сурьма. Этот металл известен уже много тысяч лет. Например, археологами доказано, что примерно три тысячи лет назад в Вавилоне из сурьмы делали сосуды. Но чаще, конечно, применялся не чистый металл, а его сульфид – «сурьмяный блеск».
В 1604 году появилось первое описание получения сурьмы из соединений. Это описание было в книге довольно известного монаха, а по совместительству алхимика, Василия Валентина.
Василий Валентин верил, что соединения сурьмы могут помочь очистить организм от «вредоносных начал». Он пытался применять сурьму в качестве лекарства. Например, он считал отличным «рвотным средством» вино, которое было выдержано в сурьмяных сосудах. А как вам «вечные пилюли», которые можно было использовать много раз – они просто проходили весь кишечный тракт? Все эти лекарства Василий использовал на монахах, и некоторых из них забирала мучительная смерть. Вот откуда взялось название «антимониум» – противомонашеский металл.
Сегодня есть мнение, что такого человека как Василий Валентин не существовало, ведь его не было в списках монахов ордена, к которому он себя причислял. Вполне возможно, что все его книги – коллективный труд нескольких алхимиков.
Вполне возможно, что все его книги – коллективный труд нескольких алхимиков.
И ещё интересный факт про сурьму: в России это название произошло от турецкой косметической процедуры – «чернение бровей». И хотя в качестве краски для бровей сурьму употребляли редко, выражение насурьмить брови» довольно часто можно было услышать в быту.
Ленивый элемент, которому не нашли места
Здесь речь пойдёт о газе аргоне, который был впервые обнаружен английским химиком Кавендишем. Он установил, что в воздухе помимо всех известных находится ещё какой-то газ, но какой именно, установить ему не удалось.
Чуть позже, в 1892 году, в совершенно другом эксперименте этот газ снова был обнаружен, теперь уже физиком Джоном-Уильямом Страттом.
Уже в 1894 два химика выступили с публичным обращением и рассказали миру о своём открытии. Но вот что интересно: когда впервые удалось получить чистый аргон (что в переводе означает «ленивый» или «медленный»), он никак не вписывался в уже существовавшую периодическую таблицу. Казалось, что Менделеев просто решил это открытие проигнорировать, раз оно не вписывалось в его концепцию.
Казалось, что Менделеев просто решил это открытие проигнорировать, раз оно не вписывалось в его концепцию.
Точно такая же ситуация была с радоном, неоном, криптоном, гелием и ксеноном – люди поначалу не признавали эти газы, потому что было непонятно, куда их пристроить в таблице. Понадобилось несколько лет, чтобы выделить их в отдельную группу инертных газов и перестать отрицать их существование.
Цвета в названиях элементов
Вообще названия химическим элементам дают всегда примерно одинаково: в основном либо по каким-то внешним свойствам, либо по месту открытия, либо по имени учёного, которому мир обязан новым элементом.
И если обратить внимание конкретно на элементы, названные по каким-то своим свойствам, то очень частое явление – «цветное» название, как будто именно разнообразие цветов больше всего впечатляло химиков.
Например, название «хлор» происходит от греческого слова «хлорус», что в переводе гласит «жёлто-зелёный». А элемент йод – «йодес» с греческого – это фиолетовый. Здесь надо пояснить, что имеется в виду не цвет самого вещества, а, как и в первой истории про Лекока-де-Буабодрана, цвет спектральный линий в спектрах излучения соединений.
Иридий тоже был назван в соответствии с греческим языком: слово «ирис» означает радуга. Соли иридия имеют множество разнообразных окрасок.
«Таллос» в переводе означает «молодая зелёная ветка», вот и элемент таллий так назван из-за ярко-зелёной линии в спектре излучения его соединений.
«Цезиум» – голубой цвет «небесного свода», соответственно, у цезия в спектре излучения солей были найдены именно голубые линии. А у серы такое название потому, что в древнеиндийском языке «сира» означает светло-жёлтый цвет.
И это далеко не всё, с цветами связано огромное количество названий элементов.
А вот названий в честь запаха элемента всего два: бром – «бромос» – «зловоние», и осмий – «осме» – «запах».
Кстати, довольно логично, но по вкусу элементы ни разу не называли.
Элементы, открытые случайно
Так или иначе, почти все элементы были открыты незапланированно./imgs/2019/08/05/10/3489939/b210986d372c08253b7647f6928441111a87d79b.jpg) Просто, например, не сходились расчёты, или внезапно проявлялись неожиданные свойства. Но некоторые пробелы в таблице Менделеева были заполнены как будто не учёными, а чередой обстоятельств. Совпадение? Абсолютное.
Просто, например, не сходились расчёты, или внезапно проявлялись неожиданные свойства. Но некоторые пробелы в таблице Менделеева были заполнены как будто не учёными, а чередой обстоятельств. Совпадение? Абсолютное.
Вот, скажем, фосфор был открыт солдатом Хённинг Брандом в 1669 году. Правда, он не искал фосфор, он вообще пытался синтезировать философский камень, и для этого он занимался выпариванием солдатской мочи. В какой-то момент он заметил уже привычное для нас зеленоватое свечение в сосуде. Но Бранд так никогда и не узнал, что его открытие было важным, ведь в его время ещё даже не было представления о химических элементах.
А ещё одно открытие было фактически сделано котом! У одного известного химика был кот, имевший обыкновение сидеть на плече своего хозяина. И вот однажды, испугавшись чего-то в лаборатории, кот спрыгнул с плеча на пол и задел стоявшие там бутылки с веществами. В одной бутылке была концентрированная серная кислота, а в другой – суспензия золы для водорослей в этаноле. В общем, жидкости случайно смешались, появился сине-фиолетовый пар, и постепенно на всех близстоящих предметах начали образовываться небольшие фиолетовые кристаллики с особыми свойствами. Оказалось, что это был новый на тот момент элемент – йод. А фамилия учёного, который с помощью кота его открыл, – Куртуа.
В общем, жидкости случайно смешались, появился сине-фиолетовый пар, и постепенно на всех близстоящих предметах начали образовываться небольшие фиолетовые кристаллики с особыми свойствами. Оказалось, что это был новый на тот момент элемент – йод. А фамилия учёного, который с помощью кота его открыл, – Куртуа.
Открытие несуществующих элементов
Довольно часто в науке были курьёзные ситуации, когда казалось, что открыт новый элемент, но при подробнейшем изучении это «новшество» оказывалось всего лишь очередным изотопом чего-нибудь уже давно известного.
Вот, например, истории открытия таких элементов как «небулий» и «короний».
Астрономы исследовали солнечную систему, точнее «корону» Солнца – внешний атмосферный слой нашей звезды. Во время этих исследований были найдены спектральные линии, совершенно ни на что не похожие, по крайней мере, их раньше не видели на Земле. Логично было предположить, что они принадлежат какому-то новому элементу. Его назвали «короний» в честь места, где нашли его спектральный линии.
Точно так же нашли ещё один «новый элемент», теперь уже при изучении спектров газовых туманностей. Ещё один новый элемент был назван небулием.
Оба эти элемента не вписывались в таблицу Менделеева, для веществ с такими свойствами там просто не было места. И при более подробном исследовании оказалось, что это вовсе не необычные новые элементы, а в первом случае сильно ионизированное железо, а во втором – обычный земной кислород.
Могут ли химические элементы «вымереть»?
В принципе, большая часть химических элементов на нашей планете довольно устойчива. Но есть среди них и те, содержание которых в атмосфере, гидросфере и земной коре исчезающе мало.
Например, сравнительно мало радиоактивных элементов. Технеций, астат, актиний, полоний или франций уже считаются «вымершими». Учёные полагают, что раньше этих элементов было гораздо больше, но именно в силу своей радиоактивности и стремления к распаду их количество уменьшается.
Сейчас есть несколько элементов, находящихся на грани «вымирания»: атомы калия-40, астата-211 и актиния-235.
Такая же судьба ждёт и уран, хотя вымирать он будет гораздо дольше. По примерным расчётам, в каждом килограмме урана за сто лет образовывается тринадцать граммов свинца и два грамма гелия. А это значит, что всему урану, который сегодня есть на Земле, осталось примерно четыре миллиарда лет. Когда он полностью исчезнет, все урановые месторождения будут свинцовыми, а атмосфера заметно обогатится гелием.
Таблица Менделеева – Интересные факты
В конце августа 1875 г. в кабинет акад. Вюрца входит его ученик, молодой французский химик Лекок-де-Буабодран. н долго не решается объяснить причину своего отменного прихода. Наконец он вынимает нз бокового кармана запечатанный зеленый конверт н вручает Вюрцу с просьбой сохранить его, не вскрывая. Получив заверения, что желание его будет нсполнено, Буа бодрен уходит.
Несмотря на свою молодость, Лекок-де-Буабодран уже в совершенстве овладел спектральным анализом веществ. Он знал наизусть спектры всех элементов. Эти цветные полоски, которые получаются при разложении света, испускаемого раскаленными веществами, давали ключ к определению состава тел. Ведь каждый элемент обладает строго определенным сочетанием спектральных линий.
Он знал наизусть спектры всех элементов. Эти цветные полоски, которые получаются при разложении света, испускаемого раскаленными веществами, давали ключ к определению состава тел. Ведь каждый элемент обладает строго определенным сочетанием спектральных линий.
Однажды, изучая спектр минерала цинковой обманки. Буабодран, к своему удивлению, обнаруживает в спектре новую, никому доселе не известную ярко-фиолетовую линию. Ученый решает, что эта линия принадлежит новому, неизвестному еще элементу. Опасаясь, что кто-либо другой оповестит мир об этом открытии, Буабодран записывает все происшедшее и в запечатанном конверте передает Вюрцу в Академию наук. Возвратившись в лабораторию, Буабодран продолжает упорно проверять свое открытие, так как боится сделать преждевременный, опрометчивый вывод.
Настает наконец день, когда все сомнения отброшены, когда он полностью убедился в правильности своих наблюдений…
В конце сентября того же года, во время очередного заседания Парижской Академии наук, Вюри при напряженном вниманиивсех присутствующих оглашает от имени своего ученика Лекока-дс-Буабодраия документ. хранящийся в запечатанном конверте В документе написано, что 27 августа 1875 г., между 3 и 4 часами пополудни. Лекок-де-Буабодран путем спектрального анализа обнаружил в цинковой обманке новый, неизвестный еще элемент. Этот элемент был назван галлием, в честь старинного названия родины Буабодрана — Франции.
хранящийся в запечатанном конверте В документе написано, что 27 августа 1875 г., между 3 и 4 часами пополудни. Лекок-де-Буабодран путем спектрального анализа обнаружил в цинковой обманке новый, неизвестный еще элемент. Этот элемент был назван галлием, в честь старинного названия родины Буабодрана — Франции.
Открытие галлия нашло отклик далеко за пределами Франции и помогло утверждению одного из основных законов химии.
Далеко от солнечной Франции, в далеком, хмуром Петербурге, проф. Дмитрий Иванович Менделеев сразу же оценил всю важность открытия молодого ученого. Узнав из протокола Парижской Академии об открытии галлия и о некоторых его свойствах, которые удалось установить Буабодраку. Менделеев сразу же решает, что галлий и есть тот самый элемент, существование которого он еще так недавно предсказывал на основании открытого им периодического закона.
Во времена Менделеева было известно всего 63 химических элемента. Несмотря на столь небольшое, казалось бы, число их, они не были систематизированы, распределены.
Не было единой точки зрения на природу элементов, на причины их сходства и различия. Все попытки классификации химических элементов неизменно кончались неудачей. Объяснялось это тем, что их авторы не смогли найти такого признака, общего для всех элементов, который можно было бы положить в основу классификация.
В 1867 г. Менделеев приступает к чтению лекций по курсу неорганической химии в Петербургском университете. Излагая студентам совокупность сведений о химических веществах, Менделеев все чаще и чаще задумывается над взаимными отношениями элементов и основой их классификации. Он все больше и больше склоняется к мысли о том, что наиболее важным, наиболее всеобщим свойством всех химических элементов является вес, или точнее, масса их атома. Постепенно крепнет убеждение Менделеева в том, что именно в атомных весах нужно искать причину сходства и различия элементов. Этот путь был уже отчасти испробован другими, но никто не пошел дальше предчувствия того великого закона природы, открытие и утверждение которого обессмертили имя Менделеева.
Однажды, придя поздно ночью домой, Менделеев решительно направляется в кабинет. Убеждения и мысли его созрели. Этой ночью он должен проверить, насколько правильны те взгляды, которые мучительно трудно вынашивались им в течение долгого времени. Он вынимает из шкафа лист картона и аккуратно нарезает 63 карточки, по числу химических элементов. На каждой карточке он пишет атомный вес элементе, название и важнейшие его свойства. Через некоторое время все 63 карточки заполнены. Теперь Дмитрий Иванович раскладывает их в ряд в порядке нарастания атомных весов элементов
Внимательно всматриваясь в длинный ряд карточек, Менделеев замечает, что свойства химических элементов изменяются но мере возрастания их атомного веся. Он берет первые 8 карточек, на которых нанесены элементы от водорода до фтора, и ставит их одну под другой так, чтобы атомные веса элементов возрастали сверху вниз.
Всю ночь раскладывал Менделеев карточки.
Образовавшийся вертикальный ряд карточек открывался водородом — самым легким нз всех элементов. Вес его атома принят за единицу при вычислении атомных весов. Под водородом поставлен литии, с атомным весом, равным семи. Это самый легкий нз известных металлов. Он очень энергично соединяется с кислородом н обладает ярко выраженными металлическими свойствами. У следующих за литнем элементов — бериллия и бора — по мере возрастания атомных весов металлические свойства слабеют. Дальше вниз следуют углерод, азот, кислород и фтор — уже не металлы, а металлоиды, причем фтор оказался ярко выраженным металлоидом. По своим свойствам он является полной противоположностью лития. Таким образом, свойства этих 8 элементов по мере увеличения их атомных весов изменяются от металлических к металоидным.
Вес его атома принят за единицу при вычислении атомных весов. Под водородом поставлен литии, с атомным весом, равным семи. Это самый легкий нз известных металлов. Он очень энергично соединяется с кислородом н обладает ярко выраженными металлическими свойствами. У следующих за литнем элементов — бериллия и бора — по мере возрастания атомных весов металлические свойства слабеют. Дальше вниз следуют углерод, азот, кислород и фтор — уже не металлы, а металлоиды, причем фтор оказался ярко выраженным металлоидом. По своим свойствам он является полной противоположностью лития. Таким образом, свойства этих 8 элементов по мере увеличения их атомных весов изменяются от металлических к металоидным.
Следующий за фтором элемент — натрий — оказался опять резко выраженным металлом Он как бы нарушал найденную закономерность. Вместо плавного изменения свойств здесь был резкий скачок от ярко выраженного металлоида — фтора — к типичному металлу — натрию. Однако свойства следующих за натрием 7 элементов опять плавно изменялись от металлических к металлоидным. Пятнадцатый элемент — хлор — оказался опять резко выраженным металлоидом.
Пятнадцатый элемент — хлор — оказался опять резко выраженным металлоидом.
Теперь уже сомнений не было. Свойства элементов действительно зависят от их атомного веса, но зависимость эта не простая, а периодическая, повторяющаяся.
Когда Менделеев приставил первый вертикальный ряд элементов ко второму так. чтобы в первой строчке против лития оказался натрий, по всех остальных строчках оказались элементы, очень сходные между собой. Литий н натрий, углерод и кремний, азот и фосфор, фтор и хлор начинали собой естественные группы семейства элементов.
Дальше Дмитрий Иванович продолжил начало строк, подставив к ним сходные элементы так. что они стояли в порядке возрастания их атомных весов. Получилась таблица, названная впоследствии периодической системой элементов.
70 лет назад. 1 марта 1869 г.. Менделеев напечатал составленную таблицу и разослал ее многим ученым. Это был первый опыт составления периодической системы элементов. В дальнейшем Дмитрий Иванович видоизменил ее, сделал периоды горизонтальными, а ряды, в которых стоят сходные элементы, вертикальными. В этом виде система существует и в наши дни.
В этом виде система существует и в наши дни.
Надо было обладать гением Менделеева, для того чтобы в то время, когда атомные веса ряда элементов были вычислены неправильно, а о существовании многих элементов вообще не было известно, напасть на сдлед периодического закона. НО в XV было глубоко верить в свое открытие, чтобы, несмотря на кажущиеся непреодолимыми возражения, настаивать на безусловной правильности периодического закона.
Элементы, атомный вес которых был определен неверно, путали при помещении их в таблицу все карты. Место их в таблице не соответствовало их атомному весу. Менделеев смело преодолевает это препятствие, решив, что атомные веся этих элементов определены неправильно. Он исправляет атомные веса этих элементов в соответствии с их местом в периодической системе.
Стройности периодической таблицы очень мешало также отсутствие многих элементов, которые тогда не были известны. Вследствие этого таблица имела много пустых клеточек.
Из 63 элементов Менделееву удалось с полной уверенностью разместить в таблице только 36. Остальные элементы бы и им размещены лишь после того, как он уточнил их атомные веса И все же места 7 элементов казались самому Менделееву сомнительными.
Остальные элементы бы и им размещены лишь после того, как он уточнил их атомные веса И все же места 7 элементов казались самому Менделееву сомнительными.
Все это, однако, не могло поколебать глубочайшего убеждения Менделеева в том, что нм открыт один из важнейших законов природы. Его уверенность была настолько велика, что он решается на смелое предсказание 3 новых элементов, которые называет экабором, зкаялюмниием и экакремннем.
Проходит еще несколько лет после открытия Лекок-де-Буабодраном первого нз предсказанных Менделеевым элементов — экаалюмнння (галлия). Дмитрий Иванович занимается новыми исследованиями и очень активной педагогической работой в университете. Он упорно и много работает над дальнейшим уточнением открытого нм периодического закона н совсем не предполагает, что ему предстоит скоро получить новую радостную весть, на этот раз с севера — из Швеции.
В 1884 г. известный шведский хнмик Ннльсон сообщает, что им открыт второй из предсказанных Менделеевым элементов.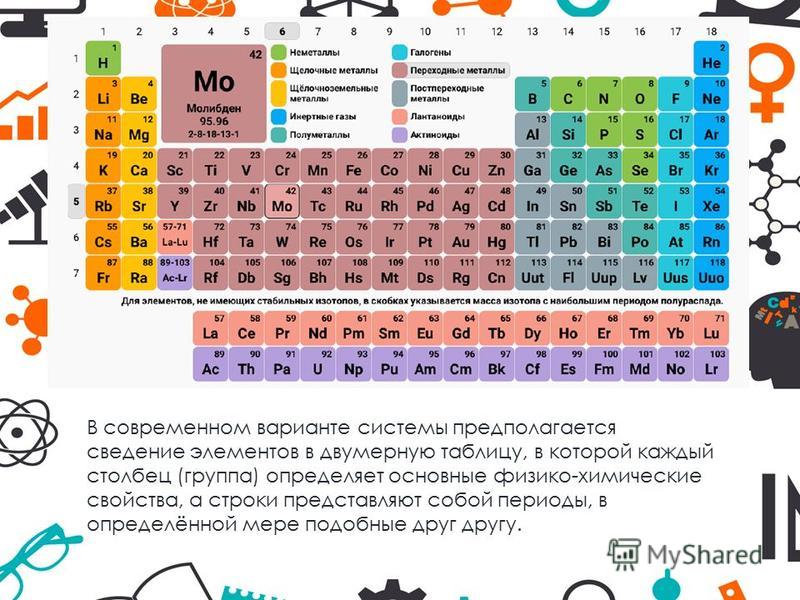 Новый металл Ннльсон назвал скандием. Свойства вполне отвечали предсказанному Менделеевым экабору
Новый металл Ннльсон назвал скандием. Свойства вполне отвечали предсказанному Менделеевым экабору
«Таким образом, — заканчивает свое сообщение Ннльсон, — подтверждаются соображения русского химика, которые не только дали вовзможность предсказать существование названных элементов — скандия и галлия, но и предвидеть заранее их важнейшие свойства».
Наконец, п 1886 г.. немецкий ученый Винклер открывает третий предугаданный Менделеевым элемент. Винклер считает, что новый элемент — германий — как раз н есть предсказанный Менделеевым эка кремний. Чтобы еще больше убедить читателей в этом, ученый заканчивает свое сообщение таблицей сравнения свойств экакремння н германия.
В своем сообщении Вннклер говорит: «Нельзя требовать более очевидного доказательства правильности периодического закона, чем поразительное совпадение свойств экакремння и гермпння Это не простое подтверждение искусной теории — это блестящее расширение химического кругозора, великий шаг в области познаний».
Гениальное открытие Менделеева не сразу получило признание. Причиной этому служили, главным образом, слабые места менделеевской таблицы. Так например, было известно, что атомный вес никеля меньше атомного веса кобальта, между тем кобальт стоит в таблице раньше никеля; другая пара элементов — иол и теллур — также была примером такого же нарушения периодического закона.
Менделеев сознательно допустил такое нарушение своей системы Он считал, что свойства этих «спорных» элементов вполне достаточно определяют их место в таблице, в то время как атомный вес их мог быть определен неточно.
В 1894 г. весь ученый мир был поражен сенсационным открытием английского ученого Рамзая. Он нашел в воздухе новый, абсолютно недеятельный газ н назвал его аргоном (что значит «ленивый») Далее, один за другим были открыты еще четыре недеятельных газа: криптон, ксенон, гелий н неон. Вновь открытые элементы образовали новую группу, существование которой как будто нарушало стройность периодической таблицы.
Вслед за работой Рамзая последовало открытие так называемых редкоземельных элементов. Менделеев не знает, куда поместить их в своей таблице, н откровенно признает: «Тут мое личное мнение еще ин на чем не остановилось, и тут я вижу одну из труднейших задач, представляемых периодической закономерностью».
Несмотря на эти противоречия н трудности. Дмитрий Иванович уверен в своей правоте. Он считает, что наука пока еще не может объяснить этих нарушений периодической системы. При дальнейшем изучении свойств инертных газов было найдено, что эти элементы представляют собой переходную группу между металлами и галлондами. Поэтому Менделеев охотно согласился с бельгийским ученым Эррером и поместил инертные газы в новую, дополнительную группу своей таблицы — нулевую.
Осталось последнее возражение против менделеевской таблицы — несоответствие атомных весов некоторых элементов их месту в системе кобальт и никель, теллур и иод). Это возражение отпало только совсем недавно, когда наука вплотную подошла к разрешению загадки строения атома.
Во времена Менделеева атом считался неделимым. Ученые же пате-го века доказали, что атом состоит из ядра, заряженного положительно, и окружающих его электронов, заряженных отрицательно. В 1913 г. английский ученый Г. Моэли занялся изучением рентгеновских спектров элементов. Он нашел, что эти спектры очень просты и состоят из немногих линий. Для каждого элемента длина волны этих линий оказалась в очень простой математической связи с порядковым числом, т. е. номером его места в общем ряду элементов. Таким образом, оказалось возможным определить по порядковые числа всех элементов. Полученные числа определяли положение каждого элемента в менделеевской системе и объясняли все до сих пор спорные се места Порядковые номера кобальта н никеля, теллура и иоде подтвердили гениальную догадку Менделеева, который поставил кобальт раньше никеля и теллур раньше иода, хотя атомные веса этих элементов не соответствовали их месту в системе.
Открытие Мозлн сильно преобразило периодическую систему, н периодический закон формулируется теперь так – свойства элементов находятся в периодической зависимости от их порядковых номеров
Развитие науки о строении атоме позволило нейти место в системе и для редкоземельных элементов, разрешив задачу которую сам Менделеев не смог решить. Так одно за другим отпали все возражения против периодической системы, и закон Менделеева занимает почетное место среди важнейших законов естествознания.
Так одно за другим отпали все возражения против периодической системы, и закон Менделеева занимает почетное место среди важнейших законов естествознания.
|
1. Барфилд, М. Элементарно! : вся таблица Менделеева у тебя дома : [для старшего школьного возраста] / Майк Барфилд ; иллюстрации Лорен Хамфри ; перевод с английского Вадима Цилинского. – 2-е изд. – Москва : Манн, Иванов и Фербер, 2020. – 62, [1] с. : ил. – (Миф детство). – Алф. указ. в конце кн. – 3000 экз. – ISBN 978-5-00169-023-8 Ж2-20/68851 Аннотация |
|
|
2. Курамшин, А. И. Химические элементы для безнадежных гуманитариев [сильно влюбленных в них] / Аркадий Курамшин. – Москва : АСТ, 2020. – 414, [1] с. : ил. – (Безнадежный гуманитарий). – 2000 экз. – ISBN 978-5-17-123412-6 Д10-20/78268 Аннотация |
|
|
3. Периодическая система. От философского камня к 118 элементам / Энн Руни ; [пер. с англ. Макояна А. С.]. – Москва : Аванта : Изд-во АСТ, 2020. – 204, [1] с. : ил. – (Наука для всех). – Авт. и пер. указ. в вып. дан. – 2000 экз. – ISBN 978-5-17-114752-5 Д10-20/79114 Аннотация |
|
|
4. Руни, Э. Химия. От таблицы Менделеева к нанотехнологиям / Э. Д10-20/76453 Аннотация |
|
|
5. Иванов, А. Химические элементы : [для среднего школьного возраста] / А. Иванов, И. Гордий. – Москва : Аванта : АСТ, 2018. – 120, [11] с. : ил. – (Химия просто) (Хочу всё знать!). – 3000 экз. – ISBN 978-5-17-108044-0 Ж2-18/65481 Аннотация |
|
|
6. Курамшин, А. Элементы: замечательный сон профессора Менделеева / А. Курамшин. – Москва : Изд-во АСТ : Времена, 2019. – 414, [1] с. : ил. – (Научпоп Рунета). – 5000 экз. – ISBN 978-5-17-113353-5 Д10-19/63246 Аннотация |
|
|
7. Иванов, А. Б. Химические элементы / А. Б. Иванов, И. В. Гордий. – Москва : Аванта, 2018. – 205 с. : ил. – (Простая наука для детей). – Авт. указ. в вып. дан. – 4000 экз. – ISBN 978-5-17-105368-0 Д10-18/51625 Аннотация |
|
|
8. Олдерси-Уильямс, Х. Научные сказки периодической таблицы: занимательная история химических элементов от мышьяка до цинка : [перевод с английского] / Х. Д10-19/64698 Аннотация |
|
| 9. Химические элементы : энциклопедический словарь : учебное пособие / В. В. Лунин [и др. ; научный редактор Н. В. Шелемина] ; Химический факультет Московского государственного университета. – Москва : Энциклопедия, 2019. – 382 с. – Авт. указ. на обороте тит. л. – 300 экз. – ISBN 978-5-94802-070-9
Д10-19/63112 Аннотация |
|
|
10. Кин, С. Исчезающая ложка, или Удивительные истории из жизни периодической таблицы Менделеева / Сэм Кин ; [перевод с английского М. А. Райтман]. – Москва : БОМБОРА™ : Изд-во “Эксмо”, 2020. – 601, [4] с. : ил. – (Бомборий. Новый элемент знаний). – Библиогр. в конце кн. – Пер. изд.: disappearing spoon: and other true tales of madness, love, and the history of the world from the periodic table of the elements / Sam Kean. – 2010. – 2000 экз. – ISBN 978-5-04-111267-7 Д10-20/78887 Аннотация |
Дмитрий Менделеев: «Я думал над ней 20 лет …»
2 февраля 2017 года исполнилось 110 лет со дня смерти гениального химика, «отца» периодической таблицы химических элементов Дмитрия Менделеева.
Редакция портала «Российское образование» вспомнила историю формирования периодической таблицы и интересные факты, связанные с ее открытием.
В поисках единой концепции
Ушло не одно столетие на безуспешные поиски ученых всех стран обнаружить закономерность среди химических элементов. Исследователи старались «подогнать» их под имевшиеся схемы, что, само собой, не приносило желаемых результатов. Менделеев же был уверен, что существует общий закон природы, который связан с массой атома и определяет все сходства и различия элементов между собой.
Советский публицист Олег Писаржевский описывает работу ученого таким образом:
«Он помог успеху своих поисков простым и наглядным приемом. Он воспользовался запасом ненужных визитных карточек – узеньких полосок картона. Из этих картонных карточек он составил нечто вроде подвижной картотеки элементов. На обороте каждой карточки он записал под названием элемента его атомный вес и формулы основных соединений, которые данный элемент образует с другими. <…> Разложив перед собой эти карточки, комбинируя их во всевозможных сочетаниях, сопоставляя их между собой по свойствам элементов, он с большой легкостью мог охватить умственным взором всю совокупность элементов со всем сложным переплетением их свойств. Все более отчетливо проявлялись в его сознании признаки системы, которой подчинялось все это пестрое разнородное собрание земных тел».
<…> Разложив перед собой эти карточки, комбинируя их во всевозможных сочетаниях, сопоставляя их между собой по свойствам элементов, он с большой легкостью мог охватить умственным взором всю совокупность элементов со всем сложным переплетением их свойств. Все более отчетливо проявлялись в его сознании признаки системы, которой подчинялось все это пестрое разнородное собрание земных тел».
Вокруг открытия ученого сочиняли множество легенд. Одна из них – знаменитая таблица Менделееву приснилась. Сложно поверить в то, что можно с такой легкостью совершать научные открытия. Менделеев только смеялся над абсурдностью этого предположения.
«Я над ней, может быть, двадцать лет думал, а вы говорите: сидел и вдруг … готово!», – комментировал он.
Писаржевский писал по этому поводу:
«Менделеев действительно не раз вспоминал о том, как он часами переставлял элементы в рядах, вчитываясь в свои заметки до ряби в глазах. Голова у него кружилась от напряжения. Ведь когда с места на место перекладывались легкие карточки с названиями веществ, в сознании исследователя приходили в движение целые эшелоны сведений об этих веществах. <…> И даже когда, утомленный, он засыпал за своими размышлениями, неугомонная, бессонная мысль продолжала биться в мозгу исследователя. И весьма возможно, что именно в тот момент, когда более поверхностные, мешающие раздражители были заторможены сном, свободно и до конца оформилось то наблюдение, которое было подготовлено годами труда и уже складывалось в сознании».
<…> И даже когда, утомленный, он засыпал за своими размышлениями, неугомонная, бессонная мысль продолжала биться в мозгу исследователя. И весьма возможно, что именно в тот момент, когда более поверхностные, мешающие раздражители были заторможены сном, свободно и до конца оформилось то наблюдение, которое было подготовлено годами труда и уже складывалось в сознании».
В 1869 году таблица имела пустующие ячейки. Менделеев специально оставил свободные места для новых элементов, которые, по его предположению, должны были найти в будущем. Основываясь на свойствах «соседей» по периодической таблице, ученый даже довольно точно описал еще неоткрытых три элемента. И вскоре свободные ячейки заняли галлий, скандий и германий.
Появление радия
Еще в течение многих лет периодическая таблица дополнялось новыми элементами. 26 декабря 1898 года лауреат Нобелевской премии по физике Пьер Кюри представил во Французской Академии наук радий в виде смеси с барием. Вместе со своей супругой Марией они получили из отходов, остающихся после выделения урана из урановой руды, сильнорадиоактивный элемент – радий.
Вместе со своей супругой Марией они получили из отходов, остающихся после выделения урана из урановой руды, сильнорадиоактивный элемент – радий.
В то время никто не знал о смертельной опасности радиации, и новый элемент сделали панацеей чуть ли не от всех болезней. Радий включили в состав пищевых продуктов, зубной пасты, кремов для лица. Его рекомендовали врачи в качестве средства для снятия стресса. А богачи щеголяли в часах, циферблат которых был окрашен краской, содержащей радий.
Сегодня этот элемент используют в медицине для кратковременного облучения при лечении ряда злокачественных заболеваний.
«Лжеэлементы»: небулий и короний
Некоторые химические элементы не укладывались в концепцию периодического закона и были признаны несуществующими. Так в начале 20 века случилось с небулием и коронием.
При исследовании солнечной атмосферы астрономы обнаружили спектральные линии, которые им не удалось отождествить ни с одним из известных на земле химических элементов. Ученые предположили, что эти линии принадлежат новому элементу, который получил название короний (потому что линии были обнаружены при исследовании «короны» Солнца – внешнего слоя атмосферы звезды).
Ученые предположили, что эти линии принадлежат новому элементу, который получил название короний (потому что линии были обнаружены при исследовании «короны» Солнца – внешнего слоя атмосферы звезды).
Спустя несколько лет астрономы сделали еще одно открытие, изучая спектры газовых туманностей. Обнаруженные линии, которые снова не удалось отождествить ни с чем земным, приписали другому химическому элементу – небулию.
Открытия подверглись критике, поскольку в периодической таблице Менделеева уже не оставалось места для элементов, обладающих свойствами небулия и корония. После проверки обнаружилось, что небулий является обычным земным кислородом, а короний – сильно ионизированное железо.
Дмитрий Менделеев считал, что «периодическому закону – будущее не грозит разрушением, а только надстройки и развитие обещает». Его изобретение и по сей день по всеобщему признанию является основным законом химии.
15 забавных и удивительных фактов о периодической таблице элементов
К сожалению, для многих людей таблица Менделеева – это то, что им велят монотонно запоминать в школьные годы. Но правда в том, что этот маленький столик – незаменимая дорожная карта для ученых всего мира.
Но правда в том, что этот маленький столик – незаменимая дорожная карта для ученых всего мира.
Вот несколько забавных, интересных и малоизвестных фактов о таблице Менделеева, написанных как энтузиастами науки, так и всеми студентами, изучающими химию.
1.Дмитрий Менделеев является изобретателем современной таблицы Менделеева
Дмитрий Менделеев представил свою периодическую таблицу элементов, основанную на возрастании атомного веса, 6 марта 1869 года в Русском химическом обществе.
Дмитрий Менделеев, Источник: Public domain / Wikimedia CommonsХотя его часто называют изобретателем современной периодической таблицы, знаете ли вы, что его таблица не была первой попыткой организовать элементы в соответствии с периодическими свойствами? В 1864 году Лотар Мейер опубликовал периодическую таблицу, в которой описывалось расположение 28 элементов.
2. Ученые использовали полярность батареи для взвешивания элементов.
Чтобы определить вес каждого из 63 известных в то время элементов, ученые пропустили ток через несколько растворов, чтобы разбить их на атомы определенных элементов.
Батарейки использовались для разделения атомов – их полярность заставляла атомы одного элемента двигаться в одном направлении, а другие – в другом. Затем атомы собирали в отдельные контейнеры и взвешивали.
3.Таблица Менделеева отражает любовь ее создателя к карточным играм.
Дмитрий Менделеев очень любил карточные игры. Вот почему он записал вес каждого элемента на отдельной карточке и отсортировал их, как если бы они были организованы в пасьянс.
Источник: Джек Гамильтон / UnsplashЭлементы с аналогичными свойствами затем сформировали «костюм» и были помещены в столбцы, упорядоченные по возрастанию атомного веса.
4. Он использовался для правильного предсказания элементов, которые не были обнаружены.
Когда Менделеев сложил свою оригинальную таблицу Менделеева, в ней было несколько пробелов.Оценивая их свойства по сравнению с другими элементами рядом с полями на столе, Менделеев смог правильно предсказать открытие нескольких элементов.
СВЯЗАННЫЕ: ЗДЕСЬ РЕАЛЬНОЕ ИСПОЛЬЗОВАНИЕ КАЖДОГО ЭЛЕМЕНТА ПЕРИОДИЧЕСКОЙ ТАБЛИЦЫ В ЖИЗНИ
Он правильно предсказал вес и химическое поведение галлия, скандия и германия до того, как они были обнаружены.
5. Он также использовался для неправильного отрицания существования определенных элементов
Несмотря на впечатляющее предсказание существования нескольких элементов, Менделеев также использовал свою таблицу, чтобы неверно отрицать существование нескольких других элементов после того, как они были обнаружены.
Он отрицал существование аргона после его открытия в 1894 году, поскольку он не помещался в его колонки, и он сделал то же самое после открытия гелия, неона, криптона, ксенона и радона.
6. Периодическая таблица Менделеева периодически пересматривается.
Международный союз чистой прикладной химии (IUPAC) несет ответственность за поддержание и обновление таблицы Менделеева в случае, если любые научные открытия требуют изменений.
Последняя редакция таблицы Менделеева была опубликована в декабре 2018 года.
7. Технеций был первым искусственно созданным элементом
Сегодня в периодической таблице 118 подтвержденных элементов. 90 из этих элементов обычно встречаются в природе, другие в основном производятся синтетическим путем.
Технеций был первым синтезированным элементом. Впервые он был произведен в 1937 году. Сегодня есть еще 24 элемента, которые в основном производятся синтетическим путем.
8. Современная таблица Менделеева разработана в порядке возрастания атомного номера
Периодическая таблица Менделеева разработана в порядке возрастания атомного веса.У современной таблицы Менделеева есть одно ключевое отличие.
Современная таблица Менделеева была разработана в соответствии с возрастающим атомным номером.
9. Четыре элемента в таблице были названы совсем недавно.
28 ноября 2016 года Международный союз теоретической и прикладной химии утвердил название и символы для четырех элементов, которые ранее назывались элементами 113, 115, 117 и 118.
Элементы получили названия нихоний (Nh), московий (Mc), теннессин (Ts) и оганессон (Og).
10. Большинство элементов – металлы.
Почти 75 процентов таблицы Менделеева состоит из металлов.
Источник: vubp / PixabayЩелочные металлы, щелочноземельные, основные металлы, переходные металлы, лантаноиды и актиноиды – все это группы металлов.
11. Некоторые элементы названы в честь известных ученых, планет или мифологических фигур
Эйнштейний назван в честь Альберта Эйнштейна, а германий, америций и галлий были названы в честь мест, в которых они были обнаружены.Уран был назван вскоре после открытия Урана.
Названия некоторых элементов взяты из мифологии. Например, торий назван в честь скандинавского бога грома Тора. Между тем, титан назван в честь греческих титанов.
12. Остальным элементам дается греческое слово, которое лучше всего их описывает.
Затем идут элементы, названные греческим словом, которое лучше всего описывает их свойства. Аргон происходит от греческого слова «Аргос», что означает «ленивый» или «праздный».«Бром, который производит ужасный запах, точно назван в честь греческого слова« бромос », что означает« зловоние ».
Аргон происходит от греческого слова «Аргос», что означает «ленивый» или «праздный».«Бром, который производит ужасный запах, точно назван в честь греческого слова« бромос », что означает« зловоние ».
13. Противоположности таблицы притягиваются
Если взять современную таблицу Менделеева, вырезать сложные средние столбцы и сложить ее один раз по центру элементов группы 4, группы, которые «целуются», – это те, которые могут быть стабильно срослись.
Эти элементы имеют дополнительные электронные структуры, которые позволяют их комбинировать. Так романтично.
14. Углерод – король
Атомы углерода из группы 4 могут образовывать четыре ковалентные связи с другими элементами, а также с самим собой. Это означает, что атомы углерода могут объединяться с другими атомами углерода с образованием самых разнообразных соединений с высокой молекулярной массой. Это также означает, что образующиеся молекулы могут существовать в огромном разнообразии трехмерных структур, включая кольца и решетки. Эта гибкость делает их ключевой молекулой в самом нашем существовании.
Эта гибкость делает их ключевой молекулой в самом нашем существовании.
Знаете ли вы, что мы на 20 процентов состоим из углерода, и что большинство известных соединений содержат углерод? Это также четвертый по численности элемент во всей вселенной.
15. Периодическая таблица Менделеева может не расшириться до 137 элементов
Физик Ричард Фейнман предсказал, что, если она существует, мы никогда не сможем наблюдать 137-й элемент.
Отчасти потому, что теоретически электроны элемента 137 должны вращаться по орбите со скоростью света. Гипотетически говоря, электроны элемента 139 будут вращаться быстрее скорости света, что делает это невозможным с учетом сегодняшних научных знаний.
11 интересных фактов о периодической таблице Менделеева
Знаете ли вы, что таблица Менделеева на самом деле была шпаргалкой? Прокрутите, чтобы узнать больше.Периодическая таблица
Имена четырех недавно обнаруженных элементов не доступны для всеобщего ознакомления. Элементам 113, 115, 117 и 118 даны названия – Nihonium, Moscovium, Tennessine и Oganesson соответственно. Публичное рассмотрение завершится 8 ноября.
Элементам 113, 115, 117 и 118 даны названия – Nihonium, Moscovium, Tennessine и Oganesson соответственно. Публичное рассмотрение завершится 8 ноября.
По этому поводу мы представляем вам 11 интересных фактов о периодической таблице Менделеева:
- Вы знаете, почему они называют ее периодической таблицей? Это потому, что строки называются периодами
- Ужасная Периодическая таблица на стене вашего класса на самом деле является гигантской шпаргалкой.Создатель таблицы Дмитрий Менделеев опоздал с представлением работы по всем 63 элементам. Чтобы ускорить процесс, он составил базу данных всех элементов в соответствии с их атомными массами
- В периодической таблице 118 подтвержденных элементов. Из них 90 элементов можно найти в природе, а остальные созданы руками человека. Технеций был первым искусственным элементом
- Водород – самый легкий элемент с атомным весом 1, поэтому его можно найти в верхнем левом углу периодической таблицы.
 атомный вес 238
атомный вес 238
- Гелий, неон, аргон, криптон, ксенон и радон известны как благородные газы, поскольку считались инертными.Но недавние исследования показали реактивные соединения ксенона, криптона и радона
- Международный союз чистой прикладной химии (IUPAC) несет ответственность за поддержание периодической таблицы Менделеева
- Большинство элементов в периодической таблице – металлы – почти 75 процентов
- Различные формы чистых элементов называются аллотропами. Например, алмаз, графит, бакминстерфуллерен и аморфный углерод являются аллотропами одного чистого элемента – углерода
- Таблица Менделеева была разработана в порядке возрастания атомного веса, в то время как современная таблица Менделеева разработана в соответствии с увеличивающимся атомным номером .
- Единственные два элемента, которые являются жидкими при комнатной температуре, – это ртуть и бром.
Заинтересованы в общих знаниях и текущих делах? Щелкните здесь, чтобы быть в курсе событий и узнавать, что происходит во всем мире с нашими G. K. и раздел «Текущие события».
K. и раздел «Текущие события».
Щелкните здесь, чтобы получить полный охват IndiaToday.in о пандемии коронавируса.
20 фактов о периодической таблице Менделеева, которых вы не знали
1.Вы можете помнить Периодическую таблицу элементов как унылую диаграмму на стене в классе. Если это так, то вы никогда не догадались, что это настоящее предназначение: это огромная шпаргалка.
2. Стол обслуживает студентов-химиков с 1869 года, когда его создал Дмитрий Менделеев, капризный профессор Петербургского университета.
3. С приближением крайнего срока для издателя Менделеев не успел описать все 63 известных тогда элемента. Поэтому он обратился к набору данных об атомных весах, тщательно собранным другими.
4. Чтобы определить эти веса, ученые пропустили токи через различные растворы, чтобы разбить их на составляющие их атомы. В зависимости от полярности батареи атомы одного элемента уходят в сторону, а атомы другого – в другую сторону. Атомы собирали в отдельные контейнеры и затем взвешивали.
В зависимости от полярности батареи атомы одного элемента уходят в сторону, а атомы другого – в другую сторону. Атомы собирали в отдельные контейнеры и затем взвешивали.
5. На основе этого процесса химики определили относительные веса, которые были всем, что требовалось Менделееву для создания полезного ранжирования.
6. Увлекался карточными играми, записывал вес каждого элемента на отдельной карточке и сортировал их, как в пасьянсе.Элементы с похожими свойствами образовали «костюм», который он разместил в столбцах, упорядоченных по возрастанию атомного веса.
7. Теперь у него был новый Периодический закон («Элементы, упорядоченные в соответствии со значением их атомного веса, демонстрируют явную периодичность свойств»), который описывал один образец для всех 63 элементов.
8. Там, где в таблице Менделеева были пробелы, он правильно предсказал вес и химическое поведение некоторых недостающих элементов – галлия, скандия и германия.
9.Но когда в 1894 году был открыт аргон, он не вписался ни в одну из колонок Менделеева, поэтому он отрицал его существование – как и гелий, неон, криптон, ксенон и радон.
10. В 1902 году он признал, что не ожидал существования этих недооцененных, невероятно инертных элементов – благородных газов – которые теперь составляют всю восьмую группу таблицы.
(Источник: Nerdist72 / Shutterstock)
11. Теперь мы сортируем элементы по количеству протонов, или «атомному номеру», который определяет конфигурацию атома из противоположно заряженных электронов и, следовательно, его химические свойства.
12. Благородные газы (крайний справа в периодической таблице) имеют замкнутые оболочки из электронов, поэтому они почти инертны.
13. Атомная любовь. Возьмите современную таблицу Менделеева, вырежьте сложные средние столбцы и сложите ее один раз по центру элементов четвертой группы. Группы, которые целуются, имеют дополнительные электронные структуры и будут объединяться друг с другом.
14. Натрий касается хлора – поваренной соли! Вы можете предсказать другие распространенные соединения, такие как хлорид калия, которые используются в очень больших дозах как часть смертельной инъекции.
15. Элементы группы 4 (обозначенные выше как IVA) в средней части легко связываются друг с другом и сами с собой. Кремний + кремний + кремний до бесконечности соединяется в кристаллические решетки, используемые для изготовления полупроводников для компьютеров.
16. Атомы углерода – также группа 4 – связываются в длинные цепи, и вуаля: сахара. Химическая гибкость углерода делает его ключевой молекулой жизни.
17. Менделеев ошибочно полагал, что все элементы неизменны. Но радиоактивные атомы имеют нестабильные ядра, что означает, что они могут перемещаться по диаграмме.Например, уран (элемент 92) постепенно распадается на целый ряд более легких элементов, заканчивающихся свинцом (элемент 82).
18. За гранью: атомы с атомными номерами выше 92 не существуют в природе, но они могут быть созданы путем бомбардировки элементов другими элементами или их частями.
19. Два новейших члена периодической таблицы Менделеева, до сих пор безымянные элементы 114 и 116, были официально признаны в июне прошлого года. Число 116 распадается и исчезает за миллисекунды. (Три элемента, от 110 до 112, также были официально названы ранее в этом месяце.)
Число 116 распадается и исчезает за миллисекунды. (Три элемента, от 110 до 112, также были официально названы ранее в этом месяце.)
20. Физик Ричард Фейнман однажды предсказал, что число 137 определяет внешний предел таблицы; добавление дополнительных протонов приведет к получению энергии, которую можно количественно измерить только мнимым числом, что сделает невозможным элемент 138 и выше. Может быть.
Интересные факты об элементах
Мир Периодической таблицы и химических элементов всегда был для меня очень привлекательным. Элементы – это простейшие формы материи, и Дмитрий Менделеев разработал способ организовать их в табличной форме.Каждый из этих элементов обладает уникальными свойствами, и есть много интересных фактов, связанных с Периодической таблицей и химическими элементами. Сегодня мы расскажем вам несколько очень интересных и интересных фактов об элементах. Сделайте решительный шаг и учитесь, пока развлекаетесь!
Факты об элементах и периодической таблице
- На данный момент в Периодической таблице всего 118 элементов .

- Первый элемент – это Водород (H), а последний элемент – Оганессон (Og).
- Русский химик Дмитрий Менделеев создал оригинальную таблицу Менделеева. В таблице Менделеева элементы были организованы в соответствии с их возрастающим атомным весом – в современной Периодической таблице элементы располагаются по возрастанию атомного номера.
- Международный союз чистой прикладной химии, IUPAC, является международной организацией, которая управляет Периодической таблицей.
- Водород (H) – самый распространенный элемент во Вселенной . Это около 75% всей наблюдаемой Вселенной.
- Гелий – второй по распространенности элемент во Вселенной. Водород и гелий вместе составляют более 99% наблюдаемой Вселенной.
- Технеций (Tc) был первым элементом , который был искусственно произведен . Впервые синтезирован в 1937 году.
- J – единственная буква, отсутствующая во всех символах элементов таблицы Менделеева.

- Число 113, 115, 117 и 118 – это четыре элемента , последний из которых был назван . 28 ноября 2016 года Международный союз теоретической и прикладной химии утвердил названия и символы для этих элементов: Nihonium (Nh), Moscovium (Mc), Tennessine (Ts) и Oganesson (Og).
- Тор твой любимый супергерой? Что ж, Торий (Th) назван в честь нордического бога грома – Тора!
- Хотя гелий (He) присутствует на Земле – он был открыт при наблюдении за Солнцем!
- Ричард Фейнман , знаменитый физик, предсказал, что Периодическая таблица не может выходить за рамки 137 элементов . Причина? Что ж, теоретически электроны элемента номер 137 будут вращаться вокруг его ядра со скоростью света. Итак, это означает, что электроны элемента 138 будут двигаться со скоростью выше скорости света, что невозможно.
- Строки Периодической таблицы называются периодами . Номер периода элемента – это наивысший невозбужденный уровень энергии электрона этого элемента.

- Столбцы элементов помогают различать групп в Периодической таблице. Элементы внутри группы имеют несколько общих свойств и часто имеют одинаковое внешнее расположение электронов.
- Фтор (F) – это самый электроотрицательный элемент в Периодической таблице. Это означает, что фтор сильно притягивает к себе электроны.
- Франций (Fr) – самый электроположительный элемент в Периодической таблице.
- Углерод (C) уникален тем, что, как известно, он образует до 10 миллионов различных соединений .
- Астатин (At) – это самый редкий природный элемент в земной коре.
- Знаете ли вы, какой элемент составляет большую часть вашего тела? Это кислород! Кислород (O) – самый распространенный элемент в организме человека.
- Какой элемент наиболее реактивный ? Ну, это фтор (F).
- Осмий (Os) имеет самую высокую плотность среди всех элементов.
- Иридий (Ir) наименее коррозионный элемент – это означает, что его меньше всего беспокоит реакция с водой, кислотой, воздухом или другими химическими веществами.
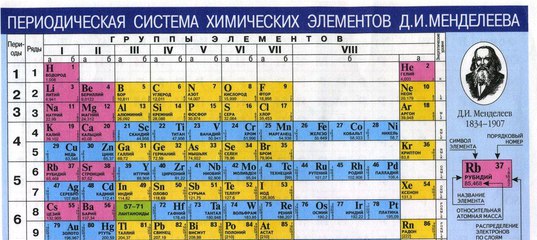
- Есть только два жидких элемента в Периодической таблице. Это ртуть (Hg) и бром (Br). Они остаются в жидком виде при комнатной температуре.
- Самый тяжелый элемент , встречающийся в природе, – это уран (U) с атомным номером 92 и атомным весом 238.0289.
- Многие элементы были названы в честь ученых, лауреатов Нобелевской премии. Например:
- Некоторые элементы также были названы в честь ученых, не получивших Нобелевской премии:
- Некоторые элементы получили свои названия из мест на Земле. Например:
- Полоний (Po) имени Польши
- Франций и Галлий, оба названы в честь Франции
- Нихоний (Nh) имени Японии
- Германий по имени Германии
- Америций назван в честь Америки
- Европий им. Европы
- Символы некоторых элементов не являются английскими.Например:
- Свинец (Pb) происходит от plumbum на латинском языке
- Вольфрам (W) происходит от вольфрама на немецком языке
- Гелий (He) происходит от hḗlios по-гречески, что означает «солнце»
- Золото (Au) происходит от aurum на латыни
Надеемся, вам понравились эти интересные, веселые и в то же время важные для запоминания факты об элементах, из которых состоит наш мир. Мы будем продолжать обновлять этот список.Вы также можете внести свой вклад в раздел комментариев.
Мы будем продолжать обновлять этот список.Вы также можете внести свой вклад в раздел комментариев.
Цитата
Используйте ссылку ниже, чтобы добавить эту статью в свою библиографию
Энн Мари Хелменстайн – ЛЮБОПЫТНЫЕ факты о Периодической таблице
10 фактов о периодической таблицеЭнн Мари Хелменстайн, доктор философии.
Периодическая таблица – это таблица, в которой химические элементы расположены в удобном и логичном порядке. Элементы перечислены в порядке возрастания атомного номера, выровнены так, чтобы элементы, обладающие схожими свойствами, располагались в одной строке или столбце друг с другом.Таблица Менделеева – один из самых полезных инструментов химии и других наук. Вот 10 забавных и интересных фактов о Таблице Менделеева:
1. Хотя Дмитрия Менделеева чаще всего называют изобретателем современной таблицы Менделеева, его таблица была только первой, получившей научное доверие, а не первой таблицей, в которой организованы элементы. по периодическим свойствам.
2. В таблице Менделеева 90 элементов, встречающихся в природе. Все остальные элементы созданы руками человека.
3. Технеций был первым элементом, созданным искусственно.
4. Международный союз чистой прикладной химии, ИЮПАК, пересматривает периодическую таблицу по мере появления новых данных. На момент написания самая последняя версия таблицы Менделеева была утверждена 19 февраля 2010 года.
5. Строки таблицы Менделеева называются периодами. Номер периода элемента – это наивысший невозбужденный уровень энергии электрона этого элемента.
6. Столбцы элементов помогают различать группы в периодической таблице.Элементы внутри группы имеют несколько общих свойств и часто имеют одинаковое внешнее расположение электронов.
7. Большинство элементов в таблице Менделеева – металлы. Щелочные металлы, щелочноземельные металлы, основные металлы, переходные металлы, лантаноиды и актиниды – все это группы металлов.
8. Настоящая таблица Менделеева вмещает 118 элементов.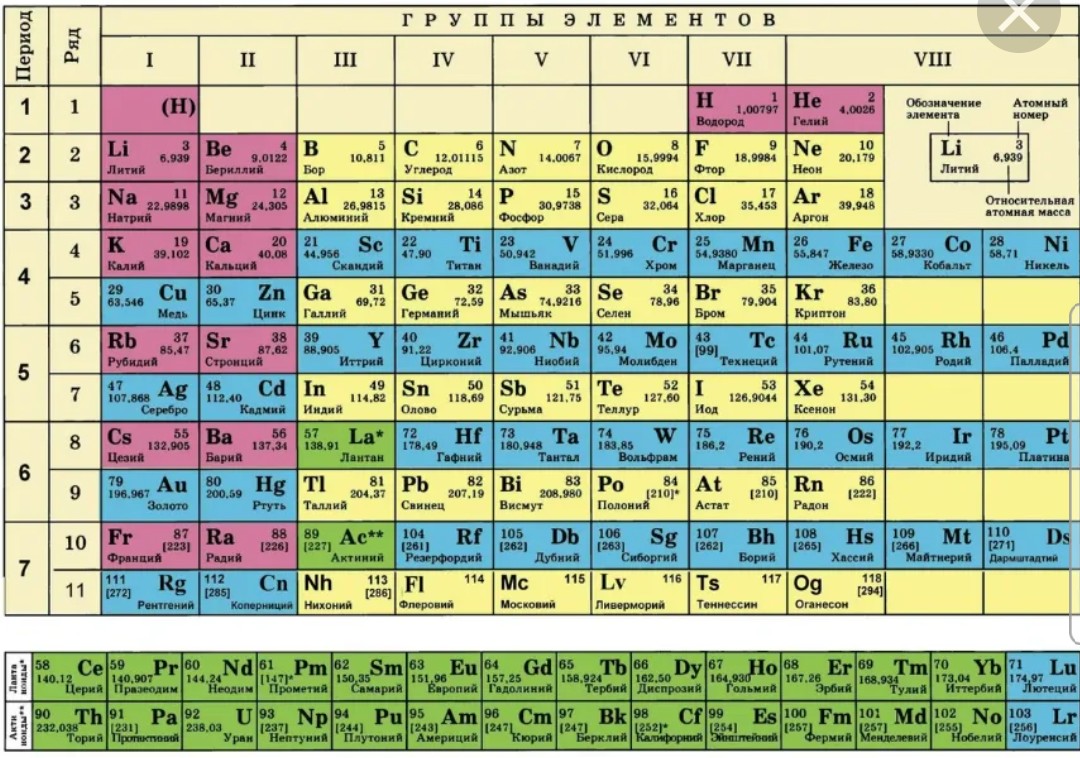 Элементы не обнаруживаются и не создаются в порядке их атомного номера. Ученые работают над созданием и проверкой элемента 120, который изменит внешний вид таблицы.
Элементы не обнаруживаются и не создаются в порядке их атомного номера. Ученые работают над созданием и проверкой элемента 120, который изменит внешний вид таблицы.
9. Хотя можно ожидать, что атомы элемента станут больше по мере увеличения их атомного номера, это не всегда происходит, потому что размер атома определяется диаметром его электронной оболочки. Фактически, атомы элементов обычно уменьшаются в размере при перемещении слева направо по строке или периоду.
10. Основное различие между современной таблицей Менделеева и таблицей Менделеева состоит в том, что в таблице Менделеева элементы расположены в порядке возрастания атомного веса, в то время как в современной таблице элементы упорядочены по возрастанию атомного номера.
103 Элементы и их интересные факты (Часть 2) Люсинда Чу
Встречая новый год, я надеюсь, что одной из ваших новогодних резолюций будет «узнать больше о таблице Менделеева». Стонать от разочарования? Не волнуйтесь, это сообщение в блоге познакомит вас с еще двадцатью четырьмя элементами, каждый из которых содержит интересный факт. (Вы можете прочитать часть 1 здесь).
(Вы можете прочитать часть 1 здесь).
7. Азот
Химия обычно не смешная, но азот заставит вас смеяться весь день! Азот используется дантистом как веселящий газ, чтобы отвлечь вас от болезненных стоматологических процедур и помочь вам расслабиться! По крайней мере, это лучше, чем шутки моего отца…
Источник: https://www.coolkidfacts.com/nitrogen-facts/
8. Кислород
Избранник природы любит цвета. Твердый и жидкий кислород обычно имеют светло-голубой цвет, но он также может иметь красный, оранжевый, розовый и черный цвета!
Источник: https://www.oughttco.com/fun-oxygen-facts-for-kids-3975945
9. Фтор
Этот взрывоопасный элемент – заклятый враг углерода. Фтор – один из немногих элементов, которые могут повредить алмаз.Кто-нибудь хочет посмотреть Carbonman Vs. Fluorineman ?
Источник: https://www.oughttco.com/interesting-fluorine-element-facts-603361
10. Neon
Neon
Вспышка новостей: Неон, новый гелий? Если вы всегда обнаруживаете, что ваши гелиевые шары продолжают улетать от вас, возможно, вы захотите рассмотреть газовый неон в качестве своего нового парня. Если вы наполните шар неоном, он поднимется в воздух, но будет делать это гораздо медленнее, чем наполненный гелием. Но небо, крадущее воздушные шары, не будет счастливым…
Источник: http://www.sciencekids.co.nz/sciencefacts/chemistry/neon.html
11. Натрий
Сэр Хэмфри Дэви был гением химии не зря. Большинству химиков требуются годы (или десятилетия), чтобы найти новый элемент. Обнаружив калий, он обнаружил натрий в течение нескольких дней. Поговорим о умных!
Источник: https://www.ducksters.com/science/chemistry/sodium.php
12. Магний
Как углеродный алмаз, магний почти непобедим.Что бы вы сделали, если бы увидели огонь из магния? Распылить азот или углекислый газ? Не получится! Налить воду, чтобы потушить? Это только сделает хуже ! Пожары магния трудно потушить, потому что они могут прожечь углекислый газ и воду азота.
Источник: https://www.ducksters.com/science/chemistry/magnesium.php
13. Алюминий
Вы когда-нибудь задумывались, почему вы не видите тринадцатый элемент в биологии? Из-за невезения числа 13! Алюминий не играет никакой роли в биологии.
Источник: https://www.ducksters.com/science/chemistry/aluminium.php
14. Кремний
У алмаза есть побочный эффект, и он называется карбид кремния (SiC). SiC почти такой же твердый, как алмаз.
Источник: https://www.ducksters.com/science/chemistry/silicon.php
15. Фосфор
Ах, фосфор, элемент, который делает химию самым сложным тестом на правописание. Есть два суперзлодея – Белый фосфор и Черный фосфор.Белый фосфор относится к типу «уничтожить все, что находится в пределах досягаемости», прикосновение к нему может вызвать серьезные ожоги. Черный фосфор – это тип «злых самозванцев», который выглядит как графитовый порошок и проводит электричество, хотя и не является металлом. Берегитесь красочных братьев Фосфор!
Берегитесь красочных братьев Фосфор!
Источник: https://www.ducksters.com/science/chemistry/phosphorus.php61
16. Сера
Сера захватывает Луну! Вернее, одна из спутников Юпитера Ио. Он кажется желтым из-за большого количества серы на его поверхности.Эта сера поступает из его многочисленных действующих вулканов.
Источник: https://www.ducksters.com/science/chemistry/sulfur.php
17. Хлор
Угх. Вонючие вещества в бассейне. Видимо это тоже смертельно! Газообразный хлор использовался немцами во время Первой мировой войны для отравления солдат союзников.
Источник: https://www.ducksters.com/science/chemistry/chlorine.php
18. Аргон
Удивительно, но аргон очень похож на людей. Это бездельник, расслабляющий и бездельник, которому все равно.В прямом смысле. Название аргон происходит от греческого слова «аргос», означающего «ленивый» или «бездействующий». (Он также лучше всех дружит с алюминием, потому что он тоже не имеет ничего общего с биологией!)
Источник: https://www. ducksters.com/science/chemistry/argon.php
ducksters.com/science/chemistry/argon.php
19. Калий
Где как вы думаете, мы можем найти калий в нашей пище? Картофель ? (Потому что она называется “ pota ssium”) Правильно! Его также можно найти в бананах, авокадо, орехах, петрушке и шоколаде.(Ммм …)
Источник: https://www.ducksters.com/science/chemistry/potassium.php
20. Кальций
Кальций и известь – родственные души. Кальций назван в честь греческого названия извести, «калькс», который представляет собой оксид кальция.
Источник: https://www.ducksters.com/science/chemistry/calcium.php
21. Скандий
Похоже, вы не единственный, кто потерпел неудачу в географии! Хотя скандий был открыт шведским химиком, который назвал его в честь своей родины Скандинавия (Швеция является частью Скандинавии), он обычно находится в Норвегии (родине викингов, которая является другой частью Скандинавии) и на Мадагаскаре (вплоть до Африки. !).Передай от меня привет лемурам, Сканн!
Источник: https://www. ducksters.com/science/chemistry/scandium.php
ducksters.com/science/chemistry/scandium.php
22. Титан
Подобно скандию, титан – еще один путешественник. Вернее, космический рысак! Титан содержится в метеоритах, на Луне и в некоторых типах звезд, но он также встречается в земной коре (хотя и не в чистом виде. Из него делают что угодно, от клюшек для гольфа и теннисных ракеток до покрытые плиткой города в музее в Испании.
Источник: https://www.ducksters.com/science/chemistry/titanium.php
23. Ванадий
Всегда жалуетесь, что названия элементов от до сложного? Что ж, могло быть намного хуже! Ванадий изначально не предполагалось называть ванадием. Предлагаемые названия для Элемента 23 включают рионий, панхром и эритроний. Лично я рад, что ванадий легче произносить по буквам!
Источник: https://www.ducksters.com/science/chemistry/vanadium.php, http://www.softschools.com/facts/periodic_table/vanadium_facts/200/
24. Хроний
Розы красные, а фиалки синие. Рубины красные, а хромий черный / серый / синий / фиолетовый / оранжевый / зеленый / желтый / фиолетовый / другие цвета / красный тоже! На самом деле, рубины получают красный цвет из-за небольших следов хрома!
Рубины красные, а хромий черный / серый / синий / фиолетовый / оранжевый / зеленый / желтый / фиолетовый / другие цвета / красный тоже! На самом деле, рубины получают красный цвет из-за небольших следов хрома!
Источник: https://www.ducksters.com/science/chemistry/chromium.php, https://chem.libretexts.org/Bookshelves/Inorganic_Chemistry/Supplemental_Modules_(Inorganic_Chemistry)/BDescriptive_Chemistry/Elements_lements_Organized/Elements_lements_Organized % 3A_Transition_Metals / Chemistry_of_Chromium
25. Марганец
В периодической таблице у нас есть друзья, такие как h3O (вода), и враги, такие как ртуть или свинец. Однако марганец (нет, это не язык манги!) Считается заклятым врагом – хотя он нужен нам для выживания, например, для работы печени и почек, наши тела не могут его хранить!
Источник: https://www.ducksters.com/science/chemistry/manganese.php
26. Железо
Всем известно, что нельзя есть такие вещи, как железные болты или винты. Однако знаете ли вы, что на самом деле вы едите его почти каждый день, даже не зная об этом? Пищевые источники железа, которые полезны для вашего организма, включают красное мясо, фасоль, рыбу и зеленые листовые овощи. (Примечание: эти источники пищи НЕ включают железные магниты в вашей научной лаборатории!)
Однако знаете ли вы, что на самом деле вы едите его почти каждый день, даже не зная об этом? Пищевые источники железа, которые полезны для вашего организма, включают красное мясо, фасоль, рыбу и зеленые листовые овощи. (Примечание: эти источники пищи НЕ включают железные магниты в вашей научной лаборатории!)
Источник: https://www.ducksters.com/science/chemistry/iron.php
27. Cobalt
Привет, любители фэнтези! Если вы ненавидите химию (а это, наверное, все, кроме меня), то этот факт для вас! Название кобальт происходит от немецкого слова kobold, что означает «гоблинская руда».«Как волшебно!
Источник: http://www.softschools.com/facts/periodic_table/cobalt_facts/203/
28. Никель
Предупреждение: впереди бомба! Почему никель и медь смертельные враги? Вот эксклюзивный совок! Хотя американская пятицентовая монета называется «никель», на самом деле она на три четверти сделана из меди! Только 25% из нее сделано из никеля, поэтому никель украл кредит, и технически ее следует называть «никелем». медь »! Этот подлец!
медь »! Этот подлец!
Источник: https: // www.ducksters.com/science/chemistry/nickel.php
29. Медь
А теперь жертва никелевого дурачества: 29 элемент. Медь – лучший сотрудник, и это товарищ по команде, который всегда поддерживает вас! Медь легко образует сотни сплавов с другими металлами, такими как латунь (медь и цинк) и бронза (медь и олово). Он даже достаточно великодушен, чтобы работать с тем самым элементом, который украл его славу, – никелем! Оу … Это мой новый любимый элемент! Я плачу, потому что история слишком трогательна… Просто шучу:).
Источник: https://www.oughttco.com/interesting-copper-element-facts-603357, https://copperalliance.eu/about-copper/copper-and-its-alloys/alloys/
30. Цинк
Да! Последний элемент дня (заметьте, не для всей таблицы), он также начинается с последней буквы алфавита! Правильно: это цинк! Вы, вероятно, думали, что не можете есть металл (по крайней мере, не ваши железные болты и латунные тубы, сделанные из меди и цинка, как упоминалось выше), и поэтому вы, вероятно, ужаснулись, когда услышали мой факт о железе. «Ну что ж, – вы, наверное, вздохнули, – жизнь такая! По крайней мере, мой младший брат / сестра не проглотит эти отвратительные металлы. Они слишком молоды, чтобы жевать!» В таком случае вы ошибаетесь: цинк иногда используют в зубной пасте и детской присыпке! (Крики ужаса.) Не волнуйтесь, цинк им не повредит! Зато будут медные тубы. (Просто говорю.)
«Ну что ж, – вы, наверное, вздохнули, – жизнь такая! По крайней мере, мой младший брат / сестра не проглотит эти отвратительные металлы. Они слишком молоды, чтобы жевать!» В таком случае вы ошибаетесь: цинк иногда используют в зубной пасте и детской присыпке! (Крики ужаса.) Не волнуйтесь, цинк им не повредит! Зато будут медные тубы. (Просто говорю.)
Источник: https://www.ducksters.com/science/chemistry/zinc.php
На сегодня все! Класс распущен!
Какой факт вас заинтересовал больше всего? Прокомментируйте ниже!
Интересные факты о Периодической таблице
Периодическая таблица – это таблица химических элементов, расположенных в порядке атомных номеров, обычно в строках, так что элементы с аналогичной атомной структурой (и, следовательно, схожими химическими свойствами) отображаются в вертикальных столбцах.
Обязательно к прочтению: известные химики
Факты о Периодической таблице
- Хотя Дмитрия Менделеева чаще всего называют изобретателем современной таблицы Менделеева, его таблица была всего лишь первой, получившей научную достоверность, а не первой таблицей, в которой элементы организованы в соответствии с периодическими свойствами
.
- В периодической таблице 90 элементов, встречающихся в природе. Все остальные элементы созданы руками человека.
- Технеций был первым элементом, созданным искусственно.
- Международный союз чистой прикладной химии, IUPAC, пересматривает периодическую таблицу по мере появления новых данных. На момент написания самая последняя версия таблицы была утверждена 19 февраля
2010. - Строки периодической таблицы называются периодами. Номер периода элемента – это наивысший невозбужденный уровень энергии электрона этого элемента.
- Столбцы элементов помогают различать группы в периодической таблице. Элементы внутри группы имеют несколько общих свойств и часто имеют одинаковое внешнее расположение электронов.
- Большинство элементов на столе – металлы. Щелочные металлы, щелочноземельные металлы, основные металлы, переходные металлы, лантаноиды и актиниды – все это группы металлов.
- В настоящей таблице Менделеева помещено 118 элементов.
 Элементы не обнаруживаются и не создаются в порядке их атомного номера. Ученые работают над созданием и проверкой элемента 120, который изменит внешний вид таблицы
Элементы не обнаруживаются и не создаются в порядке их атомного номера. Ученые работают над созданием и проверкой элемента 120, который изменит внешний вид таблицы
. - Хотя можно ожидать, что атомы элемента будут становиться больше по мере увеличения их атомного номера, это не всегда происходит, потому что размер атома определяется диаметром его электронной оболочки.Фактически, атомы элементов обычно уменьшаются в размере при перемещении слева направо по строке или периоду.
- Основное различие между современной таблицей Менделеева и таблицей Менделеева состоит в том, что в таблице Менделеева элементы расположены в порядке возрастания атомного веса, в то время как современная таблица упорядочивает элементы
путем увеличения атомного номера. - Углерод уникален тем, что, как известно, он образует до 10 миллионов различных соединений. Углерод важен для существования жизни.
- Франций – самый редкий элемент на Земле. Вероятно, в любой момент времени на Земле может быть не более нескольких унций этого вещества.

- Единственная буква, отсутствующая в периодической таблице, – это буква J.
- Страна Аргентина названа в честь элемента серебро (символ Ag), которое на латыни означает Argentum.
- Хотя на Земле есть гелий, он был впервые обнаружен при наблюдении за Солнцем.
- В таблице Менделеева были пустые места, он правильно предсказал вес и химическое поведение некоторых недостающих элементов – галлия, скандия и германия.
- Когда в 1894 году был открыт аргон, он не подходил ни для одной из колонок Менделеева, поэтому он отрицал его существование, как и гелий, неон, криптон, ксенон и радон.
Обязательно к прочтению:
Известные химики
Глоссарий и термины по химии
Законы физики и химии
.

 Это весело! В книге Вы найдете интересные факты об элементах, узнаете, как провести химические опыты, а на страницах с комиксами познакомитесь с великими учеными.
Это весело! В книге Вы найдете интересные факты об элементах, узнаете, как провести химические опыты, а на страницах с комиксами познакомитесь с великими учеными. Руни, Э.
Руни, Э. Руни ; [перевод с английского А. Банкрашкова]. – Москва : Аванта : Изд-во АСТ, 2020. – 206, [1] с. : ил. – (Наука для всех). – Авт. указ. в вып. дан. – 3000 экз. – ISBN 978-5-17-114753-2
Руни ; [перевод с английского А. Банкрашкова]. – Москва : Аванта : Изд-во АСТ, 2020. – 206, [1] с. : ил. – (Наука для всех). – Авт. указ. в вып. дан. – 3000 экз. – ISBN 978-5-17-114753-2