Таблица кислот и кислотных остатков
Справочники
support
Таблица кислот и кислотных остатков.
Поделитесь информацией:
Таблица кислот и кислотных остатков (1 часть):
| Формула кислоты | Название кислоты | Формула кислотного остатка | Название кислотного остатка |
| HN3 | Азотистоводородная (Азоимид, Азидоводород) | N3– | Азид |
| HNO2 | Азотистая | NO2– | Нитрит |
| HNO3 | Азотная | NO3– | Нитрат |
| HBrO2 | Бромистая | BrO2– | Бромит |
| HBrO3 | Бромноватая | BrO3– | Бромат |
| HBrO | Бромноватистая (Гипобромистая кислота) | BrO– | Гипобромит |
| HBr | Бромоводород (Бромистоводородная кислота) | Br– | Бромид |
| HVO3 | Ванадиевая | VO3– | Ванадат |
| H2WO4 | Вольфрамовая | WO42– | Вольфрамат |
| H4GeO4 или Ge(OH) | Германиевая кислота (Гидроксид германия (IV)) | GeO44– | Германат |
| H2S2O7 | Дисерная | S2O72– | Дисульфат |
| H4P2O7 | Дифосфорная | P2O74– | Пирофосфат или дифосфат (по номенклатуре IUPAC) |
| H2Cr2O7 | Дихромовая | Cr2O72– | Дихромат |
| HIO4 | Йодная | IO4– | |
| HIO | Йодноватистая | IO– | Гипоиодит |
| HI | Йодоводород (Йодоводородная кислота) | I– | Йодид |
| H2SiO3 | Кремниевая | SiO32– | Силикат |
| H2MnO4 | Марганцовистая | MnO42– | Манганат |
| HMnO4 | Марганцовая | MnO4– | Перманганат |
| HCOOH | Метановая (Муравьиная кислота) | HCOO– | Формиат |
| HBO | Метаборная | BO– | Метаборат |
| HAsO2 | Метамышьяковистая | AsO2– | Метаарсенит |
| HPO3 | Метафосфорная | PO3– | Метафосфат |
Таблица кислот и кислотных остатков (2 часть):
| H2MoO4 | Молибденовая | MoO42– | Молибдат |
| H3BO3 | Ортоборная (Борная кислота) | BO33– | Бораты |
| H3AsO4 | Ортомышьяковая | Арсенат | |
| H3AsO3 | Ортомышьяковистая | AsO33– | Ортоарсенит |
| H2PbO4 | Ортосвинцовая кислота | PbO42– | Ортоплюмбат или плюмбат |
| H3PO4 | Ортофосфорная (Фосфорная кислота) | PO43– | Фосфат |
| HNCS | Роданистоводородная (Тиоциановая кислота) | SCN– | Тиоцианат |
| C7H6O3 | Салициловая | C7H6O3– | Салицилат |
| H2SO4 | Серная | SO42– | Сульфат |
| H2SO3 | Сернистая | SO32– | Сульфит |
| H2S | Сероводород (Сероводородная кислота) | S2– | Сульфид |
| H2SO3S | Тиосерная | SO3S2– | Тиосульфат |
| H2CO3 | Угольная | CO32– | Карбонат |
| HF | Фтороводород (Плавиковая кислота) | F– | Фторид |
| HCl | Хлороводород (Соляная кислота) | Cl– | Хлорид |
| H2CrO4 | Хромовая | CrO42– | Хромат |
| HClO2 | Хлористая | ClO2– | Хлорит |
| HClO4 | Хлорная | ClO4– | Перхлорат |
| HClO3 | Хлорноватая | ClO3– | Хлорат |
| HClO | Хлорноватистая | ClO– | Гипохлорит |
| HCN | Циановодород (Синильная кислота) | CN— | Цианид |
| H2C2O4 | Этандиовая (Щавелевая кислота) | C2O42– | Оксалат |
| CH3COOH | Этановая (Уксусная кислота) | CH3COO– | Ацетат |
| C4H6O5 | Яблочная (Оксиянтарная, Гидроксибутандиовая кислота) | C4H4O52– | Малат |
Коэффициент востребованности 9 156
классификация, номенклатура, физические и химические свойства
Из материалов урока Вы познакомитесь с разными способами классификации кислот, расширите свои знания о физических и химических свойствах кислот.
I. Посмотрите видео-презентацию
Кислоты – сложные вещества, состоящие из одного или нескольких атомов водорода, способных замещаться на атома металлов, и кислотных остатков.
Состав кислот отражен в их названии. Например, у бескислородных кислот название всегда включает название элемента и слово «водородная»:
HCl – хлороводородная, h3S – сероводородная.
Названия кислородсодержащих кислот тоже подчиняются определенным правилам. К названию химического элемента прибавляется суффикс н или ов(ев) и окончание –ая, если число атомов кислорода в молекуле кислоты наибольшее:
H2SO4 – серная
HNO3 – азотная
H2SiO3 – кремниевая
Если в молекуле кислоты число атомов кислорода меньше максимального, то часто в названии используют суффикс ист:
H2SO3 – сернистая
HNO2 – азотистая
Это интересно
Всегда ли кислоты называли кислотами?
Названия неорганических кислот долгое время никак не были связаны с присущим им кислым вкусом. Так, серную кислоту называли купоросным маслом или купоросным спиртом, хлороводородную (соляную) кислоту — соляным спиртом или кислым спиртом, азотную кислоту — селитряной дымистой водкой или крепкой водкой; смесь азотной и хлороводородной кислот называли царской водкой. Названия эти пришли из языка алхимиков и не отражали особенностей строения кислот.
Так, серную кислоту называли купоросным маслом или купоросным спиртом, хлороводородную (соляную) кислоту — соляным спиртом или кислым спиртом, азотную кислоту — селитряной дымистой водкой или крепкой водкой; смесь азотной и хлороводородной кислот называли царской водкой. Названия эти пришли из языка алхимиков и не отражали особенностей строения кислот.
II. Классификация кислот
1. По числу атомов водорода: число атомов водорода (n) определяет основность кислот:
n = 1 одноосновная
n = 2 двухосновная
n = 3 трехосновная
2. По составу:
а) Таблица кислород содержащих кислот, кислотных остатков и соответствующих кислотных оксидов:
|
Кислота (НnА) |
Кислотный остаток (А) |
Соответствующий кислотный оксид |
|
HClO4 хлорная |
ClO4 (I) перхлорат |
Cl2O7 |
|
H2SO4 серная |
SO4 (II) сульфат |
SO3 оксид серы (VI ), серный ангидрид |
|
HNO3 азотная |
NO3 (I) нитрат |
N2O5 оксид азота ( V ) |
|
HMnO4 марганцовая |
MnO4 (I) перманганат |
Mn2O7 оксид марганца (VII ) |
|
H2SO3 сернистая |
SO3 (II) сульфит |
SO2 оксид серы (IV ) |
|
H3PO4 ортофосфорная |
PO4 (III) ортофосфат |
P2O5 оксид фосфора (V ) |
|
HNO2 азотистая |
NO2 (I) нитрит |
N2O3 оксид азота (III ) |
|
H2CO3 угольная |
CO3 (II) карбонат |
CO2 оксид углерода ( IV), углекислый газ |
|
H2SiO3 кремниевая |
SiO3 (II) силикат |
SiO2 оксид кремния (IV) |
б) Таблица бескислородных кислот
|
Кислота (НnА) |
Кислотный остаток (А) |
|
HCl соляная, хлороводородная |
Cl (I) хлорид |
|
H2S сероводородная |
S(II) сульфид |
|
HBr бромоводородная |
Br (I) бромид |
|
HI йодоводородная |
I(I) йодид |
|
HF фтороводородная, плавиковая |
F(I) фторид |
III. Физические свойства кислот
Физические свойства кислот
Многие кислоты, например серная, азотная, соляная – это бесцветные жидкости. известны также твёрдые кислоты: ортофосфорная, метафосфорная HPO3, борная H3BO3. Почти все кислоты растворимы в воде. Пример нерастворимой кислоты – кремниевая H2SiO3. Растворы кислот имеют кислый вкус. Так, например, многим плодам придают кислый вкус содержащиеся в них кислоты. Отсюда названия кислот: лимонная, яблочная и т.д.
H2SO3 HClO4 HNO3
IV. Способы получения кислот
|
Бескислородные |
Кислородсодержащие |
|
HCl, HBr, HI, HF, H2S |
HNO3, H2SO4 и другие |
|
ПОЛУЧЕНИЕ |
|
|
1. H2 + Cl2 = 2 HCl |
1. Кислотный оксид + вода = кислота SO3 + H2O = H2SO4 |
|
2. Реакция обмена между солью и менее летучей кислотой 2 NaCl (тв.) + H2SO4(конц.) = Na2SO4 + 2HCl |
|
V. Химические свойства кислот
1. Изменяют окраску индикаторов
|
Название индикатора |
Нейтральная среда |
Кислая среда |
|
Лакмус |
Фиолетовый |
Красный |
|
Фенолфталеин |
Бесцветный |
Бесцветный |
|
Метилоранж |
Оранжевый |
Красный |
|
Универсальная индикаторная бумага |
Оранжевая |
Красная |
2. Реагируют с металлами в ряду активности до H2 (искл. HNO3 –азотная кислота)
Реагируют с металлами в ряду активности до H2 (искл. HNO3 –азотная кислота)
Видео: “Взаимодействие кислот с металлами”
Ме + КИСЛОТА =СОЛЬ + H2↑ (р. замещения)
Zn + 2 HCl = ZnCl2 + H2
3. С основными (амфотерными) оксидами – оксидами металлов
Видео: “Взаимодействие оксидов металлов с кислотами”
МехОу + КИСЛОТА= СОЛЬ + Н2О (р. обмена)
CuO + H2SO4 = Cu SO4 + H2O
4. Реагируют с основаниями – реакция нейтрализации
КИСЛОТА + ОСНОВАНИЕ= СОЛЬ+ H2O ( р. обмена)
обмена)
H3PO4 + 3NaOH = Na3PO4 + 3H2O
5. Реагируют с солями слабых, летучих кислот – если образуется кислота, выпадающая в осадок или выделяется газ:
2NaCl (тв.) + H2SO4(конц.) = Na2SO4 + 2HCl↑ ( р. обмена)
|
Сила кислот убывает в ряду: HI > HClO4 > HBr > HCl > H2SO4 > HNO3 > HMnO4 > H2SO3 > H3PO4 > HF > HNO2>H2CO3 > H2S > H2SiO3 . Каждая предыдущая кислота может вытеснить из соли последующую |
Видео: “Взаимодействие кислот с солями”
6. Разложение кислородсодержащих кислот при нагревании ( искл. H2SO4; H3PO4 )
Разложение кислородсодержащих кислот при нагревании ( искл. H2SO4; H3PO4 )
КИСЛОТА = КИСЛОТНЫЙ ОКСИД + ВОДА (р. разложения )
Запомните! Неустойчивые кислоты (угольная и сернистая) – разлагаются на газ и воду:
H2CO3 ↔ H2O + CO2↑
H2SO3 ↔ H2O + SO2↑
Сероводородная кислота в продуктах выделяется в виде газа: СаS + 2HCl = H2S↑ + CaCl2
Видео: “Химические свойства соляной кислоты”
VI. Значение кислот
Роль кислот в нашей жизни трудно не заметить. Во-первых, в желудочном соке человека и животных содержится слабый раствор соляной кислоты. Муравьиная кислота, которая относится к группе органических кислот, содержится в жидкости, выделяемой муравьями, и ожог от крапивы обусловлен действием на кожу именно этой кислоты.
Муравьиная кислота, которая относится к группе органических кислот, содержится в жидкости, выделяемой муравьями, и ожог от крапивы обусловлен действием на кожу именно этой кислоты.
Рис. 1. Кислоты в природе (в лимонном соке содержится лимонная кислота; в жидкости, выделяемой муравьями – муравьиная кислота)
На этикетке многих газированных фруктовых напитков написано, что в их состав входит фосфорная кислота. Азотная кислота используется в производстве минеральных удобрений и взрывчатых веществ. Серную кислоту применяют в производстве аккумуляторных батарей.
VII. Техника безопасности приработе с кислотами
Анимация: Оказание первой помощи при попадании кислот на кожу
Анимация: Правила техники безопасности при работе с кислотами
Анимация: Правило разбавления концентрированной серной кислоты водой
VIII. Задания для закрепления
Задания для закрепления
Задание №1. Распределите химические формулы кислот в таблицу. Дайте им названия:
LiOH, Mn2O7, CaO, Na3PO4, H2S, MnO, Fe(OH)3, Cr2O3, HI, HClO4, HBr, CaCl2, Na2O, HCl, H2SO4, HNO3, HMnO4, Ca(OH)2, SiO2, H2SO3, Zn(OH)2, H3PO4, HF, HNO2,H2CO3, N2O, NaNO3, H2S, H2SiO3
|
Кислоты |
||||||
|
Бескислородные |
Кислородосодержащие |
Растворимые
|
Нерастворимые |
Одноосновные |
Двухосновные |
Трёхосновные |
Задание №2. Составьте уравнения реакций:
Составьте уравнения реакций:
Ca + HCl =
Na + H2SO4 =
Al + H2S =
Ca + H3PO4 =
Назовите продукты реакции.
Задание №3. Составьте уравнения реакций, назовите продукты:
Na2O + H2CO3 =
ZnO + HCl =
CaO + HNO3 =
Fe2O3 + H2SO4 =
Задание №4. Составьте уравнения реакций взаимодействия кислот с основаниями и солями:
KOH + HNO3 =
NaOH + H2SO3 =
Ca(OH)2 + H2S =
Al(OH)3 + HF =
HCl + Na2SiO3 =
H2SO4 + K2CO3 =
HNO3 + CaCO3 =
Назовите продукты реакции.
IX. Тренажеры
Тренажёр №1. “Формулы и названия кислот”
Тренажёр №2. ” Установление соответствия: формула кислоты – формула оксида”
” Установление соответствия: формула кислоты – формула оксида”
Тренажёр №3. “Действие кислот на индикаторы”
Тренажёр №4. “Классификация кислот по наличию кислорода в кислотном остатке”
Тренажёр №5. “Классификация кислот по основности”
Тренажёр №6. “Классификация кислот по растворимости в воде”
Тренажёр №7. “Классификация кислот по стабильности”
Интерактивное задание LearningApps.org по теме: “Химические свойства кислот и оснований”
Выполните тест
Выполните итоговый контроль по теме: “Кислоты”
ЦОРы
Видео-презентация: “Кислоты”
Видео-опыт: “Действие кислот на индикаторы”
Видео-опыт: “Взаимодействие кислот с металлами”
Видео-опыт: “Взаимодействие оксидов металлов с кислотами”
Практическая работа: “Реакция обмена между оксидом меди (II) и серной кислотой”
Видео-опыт: “Реакция нейтрализации”
Видео-опыт: “Взаимодействие кислот с солями”
Видео-опыт: “Химические свойства соляной кислоты”
Анимация: “Оказание первой помощи при попадании кислот на кожу”
Анимация: “Правила техники безопасности при работе с кислотами”
Анимация: “Правило разбавления концентрированной серной кислоты водой”
Раздел недели: Плоские фигуры. Свойства, стороны, углы, признаки, периметры, равенства, подобия, хорды, секторы, площади и т.д. | |||||||||||
| Поиск на сайте DPVA Поставщики оборудования Полезные ссылки О проекте Обратная связь Ответы на вопросы. Оглавление Таблицы DPVA.ru – Инженерный Справочник | Адрес этой страницы (вложенность) в справочнике dpva.ru: главная страница / / Техническая информация/ / Химический справочник / / Таблица силы кислот и оснований. Относительная сила кислот и оснований. Значения констант кислотности и констант основности.
Поделиться:
 Введите свой запрос: Введите свой запрос: | ||||||||||
Если Вы не обнаружили себя в списке поставщиков, заметили ошибку, или у Вас есть дополнительные численные данные для коллег по теме, сообщите , пожалуйста. | |||||||||||
Коды баннеров проекта DPVA.ru Консультации и техническая | Проект является некоммерческим. Информация, представленная на сайте, не является официальной и предоставлена только в целях ознакомления. Владельцы сайта www.dpva.ru не несут никакой ответственности за риски, связанные с использованием информации, полученной с этого интернет-ресурса. Free xml sitemap generator | ||||||||||
Периодическая кислота | American Elements ®
Посмотреть историю американских элементов на Wikipedia
| Продукт | Код продукта | Порядок | Данные о безопасности | Технические данные | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
(2N) 99%. | IP-H-02-C | Цены > | Паспорт безопасности > | Спецификация > | ||||||||||
| (3N) 99,9% йодная кислота | IP-H-03-C | Цена> | SDS> | Лист данных> | ||||||||||
| (4N) 99,99% Периодика | 9 1 199000.-H-H-H-H-H-HAIN | 1111119 | 9 | 9 | 9. 14.04.04.03222 2 | 1111119 | 9 | 9. 19.049% | 11111111119 | 9 | 9. 999%. | Pricing > | SDS > | Data Sheet > |
| (5N) 99.999% Periodic Acid | IP-H-05-C | Pricing > | SDS > | Data Sheet > |
Periodic Acid Properties (Theoretical)
| Compound Formula | H 5 IO 6 |
|---|---|
| Molecular Weight | 227. 938 g/mol 938 g/mol |
| Appearance | Colorless to белые кристаллы или кристаллический порошок |
| Температура плавления | 122-130 °C |
| Температура кипения | Н/Д |
| Density | N/A |
| Solubility in h3O | Soluble |
| Exact Mass | 227.913 g/mol |
| Monoisotopic Mass | 227.913 g/mol |
Periodic Acid Health Информация о безопасности
| Сигнальное слово | Опасность |
|---|---|
| Заявления об опасности | h371-h414-h510 | Коды опасности0008 | O, C, N |
| Precautionary Statements | P210-P260-P280-P305 + P351 + P338-P370 + P378-P371 + P380 + P375 |
| RTECS Number | N/A |
| Transport Information | UN 3085 8(5. 1) / PGII 1) / PGII |
| WGK Germany | 3 |
| GHS Pictograms | |
| MSDS / SDS | Request MSDS / SDS |
О периодной кислоте
Периодическая кислота является сильным окислителем, используемым в многочисленных химических реакциях, таких как окрашивание гликопротеинов и метод Шиффа периодической кислоты (PAS) внутриклеточного анализа полисахаридов. American Elements производит материалы многих стандартных сортов, когда это применимо, включая Mil Spec (военный класс), ACS, реактивный и технический классы; Продукт предназначен для пищевой, сельскохозяйственной и фармацевтической, оптической, полупроводниковой и электронной промышленности и соответствует применимым стандартам испытаний USP, EP/BP и ASTM. Большинство материалов можно производить в формах высокой и сверхвысокой чистоты (99%, 99,9%, 99,99%, 99,999% и выше). Возможна стандартная и индивидуальная упаковка. Доступна дополнительная техническая информация, информация об исследованиях и безопасности (SDS). Пожалуйста, запросите котировку выше, чтобы получить информацию о ценах на основе ваших спецификаций.
Доступна дополнительная техническая информация, информация об исследованиях и безопасности (SDS). Пожалуйста, запросите котировку выше, чтобы получить информацию о ценах на основе ваших спецификаций.
Синонимы периодической кислоты
Ортопериодная кислота, тетрагидроксийодистая кислота, парапериодная кислота, пентагидрокси-λ 5 -оксид йода, пентагидрокси(оксо)-ламда-7-йодан, UNII AK1D44L87G, CAS 13444-71-8 (метапериодная кислота, HIO)
Chemical Identifiers
| Linear Formula | H 5 IO 6 |
|---|---|
| MDL Number | MFCD00011344 |
| EC No. | 233-937-0 |
| Pubchem CID | 25289 |
| IUPAC Name | pentahydroxy(oxo)-λ 7 -iodane |
| SMILES | OI(=O)(O)(O)(O)O |
| Идентификатор InchI | InChI=1S/H5IO6/c2-1(3,4,5,6)7/h(H5,2,3,4,5,6,7) |
| Ключ InchI | TWLXDPFBEPBAQB -UHFFFAOYSA-N |
Customers For Periodic Acid Have Also Viewed
Formamidinium Iodide | Tetraiodoethylene | Methylammonium Iodide | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Silver Iodide Solution | Magnesium Октагидрат йодида | Хексагидрат йодида никеля | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Gram’s йод раствор | Silver (II). Типичная оптовая упаковка включает пластиковые поддоны на 5 галлонов/25 кг. ведра, волокнистые и стальные барабаны до 1-тонных супермешков в количестве полного контейнера (FCL) или загрузки грузовика (T/L). Исследования и образцы, а также гигроскопичные, окисляющие или другие чувствительные к воздуху материалы могут быть упакованы в аргоне или вакууме. Отгрузочная документация включает сертификат анализа и паспорт безопасности (SDS). Растворы упаковываются в полипропиленовые, пластиковые или стеклянные банки, вплоть до контейнеров для жидкостей на поддонах емкостью 440 галлонов и автоцистерн на 36 000 фунтов. Сопутствующие элементы53 I 126.0000 Йод Посмотреть другие продукты с йодом. Йод (атомный символ: I, атомный номер: 53) представляет собой элемент блока P, группы 17, периода 5 с атомным радиусом 126,. Количество электронов в каждой из оболочек йода равно 2, 8, 18, 18, 7, а его электронная конфигурация [Kr] 4d 10 5s 2 5p 5 . Недавние исследованияМягкий флюс периодической кислоты и гидротермальные методы синтеза кристаллических соединений йода, содержащих f-элемент. Объективное сравнение выявляемости поражений на изображениях с коллиматорами низкой и средней энергии с йодом-123 mIBG с использованием канального наблюдателя Хотеллинга. Катализируемые переходными металлами йод(iii)-опосредованные реакции переноса нитрена: эффективные инструменты для сложных синтезов. Повидон-йодная мазь продемонстрировала in vitro эффективность против образования биопленки. Катализируемое йодом прямое C-H алкенилирование N-оксидов азагетероцикла алкенами. Добавочная селезенка в сравнении с лимфатическим узлом: значение количественного определения йода с помощью двухэнергетической компьютерной томографии. Иодид-йодаты M3[IO3]12·Ag4I, M = Bi, Tb, с каркасной структурой и высоким оптическим откликом генерации второй гармоники. Получение и характеристика высокорентгеноконтрастного композита, армированного стекловолокном Е, с йодсодержащим метакрилатным мономером. Краниопластика аутогенными костными лоскутами, криоконсервированными в повидон-йоде: долгосрочное наблюдение. Лечение и наблюдение за метастатическим, устойчивым к йоду дифференцированным раком щитовидной железы.
|

 Прямое взаимодействие неметаллов
Прямое взаимодействие неметаллов Относительная сила кислот и оснований. Значения констант кислотности и констант основности. Амфолиты. Кислые соли
Относительная сила кислот и оснований. Значения констант кислотности и констант основности. Амфолиты. Кислые соли Амфолиты. Кислые соли
Амфолиты. Кислые соли

 Соли, в состав которых входят такие анионы, называются кислыми солями.
Соли, в состав которых входят такие анионы, называются кислыми солями. Спецификации
Спецификации Атом йода имеет радиус 140 пм и радиус Ван-дер-Ваальса 198 пм. В своей элементарной форме йод имеет блестящий металлический серый цвет в виде твердого вещества и фиолетовый вид в виде газа или жидкого раствора. Йод образует соединения со многими элементами, но менее активен, чем другие галогены. Он легко растворяется в хлороформе, четыреххлористом углероде или сероуглероде. Соединения йода важны в органической химии и очень полезны в области медицины. Йод был открыт и впервые выделен Бернаром Куртуа в 1811 году. Название «йод» происходит от греческого слова «iodes», означающего фиолетовый.
Атом йода имеет радиус 140 пм и радиус Ван-дер-Ваальса 198 пм. В своей элементарной форме йод имеет блестящий металлический серый цвет в виде твердого вещества и фиолетовый вид в виде газа или жидкого раствора. Йод образует соединения со многими элементами, но менее активен, чем другие галогены. Он легко растворяется в хлороформе, четыреххлористом углероде или сероуглероде. Соединения йода важны в органической химии и очень полезны в области медицины. Йод был открыт и впервые выделен Бернаром Куртуа в 1811 году. Название «йод» происходит от греческого слова «iodes», означающего фиолетовый.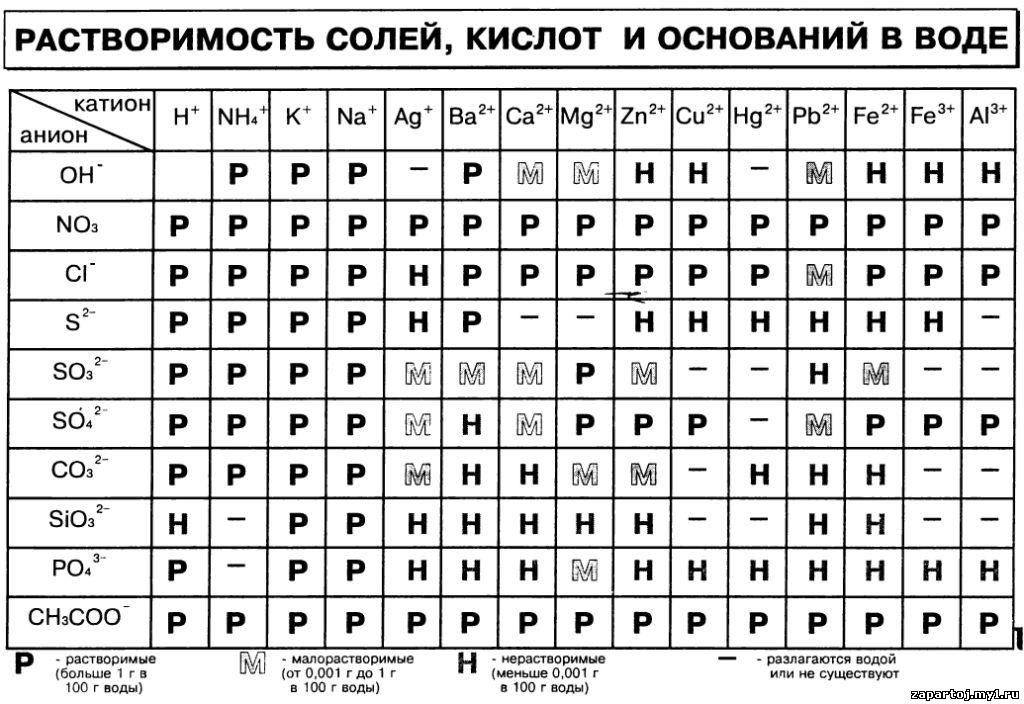
 Как и все перйодаты, он может существовать в двух формах: ортопериодная кислота с химической формулой H 5 IO 6 и метапериодная кислота, имеющая формулу HIO 4 . Периодическая кислота была открыта Генрихом Густавом Магнусом и К. Ф. Аммермюллером в 1833 году.
Как и все перйодаты, он может существовать в двух формах: ортопериодная кислота с химической формулой H 5 IO 6 и метапериодная кислота, имеющая формулу HIO 4 . Периодическая кислота была открыта Генрихом Густавом Магнусом и К. Ф. Аммермюллером в 1833 году. чем ожидаемый ангидрид гептоксида дийода (I 2 O 7 ). Метапериодная кислота также может быть получена из различных ортопериодов обработкой разбавленной азотной кислотой.
чем ожидаемый ангидрид гептоксида дийода (I 2 O 7 ). Метапериодная кислота также может быть получена из различных ортопериодов обработкой разбавленной азотной кислотой.
 Этот процесс часто используется для мечения сахаридов флуоресцентными молекулами или другими метками, такими как биотин. Поскольку для этого процесса требуются вицинальные диолы, периодатное окисление часто используется для селективной маркировки 3′-концов РНК (у рибозы есть вицинальные диолы) вместо ДНК, поскольку дезоксирибоза не имеет вицинальных диолов.
Этот процесс часто используется для мечения сахаридов флуоресцентными молекулами или другими метками, такими как биотин. Поскольку для этого процесса требуются вицинальные диолы, периодатное окисление часто используется для селективной маркировки 3′-концов РНК (у рибозы есть вицинальные диолы) вместо ДНК, поскольку дезоксирибоза не имеет вицинальных диолов. Ф. Холлеманом; продолжил Эгон Виберг; перевод Мэри Иглсон, Уильям Брюэр; в редакции Бернхарда Дж. (2001). Неорганическая химия (1-е английское изд., [под редакцией] Нильса Виберга, изд.). Сан-Диего, Калифорния: Берлин: Academic Press, W. de Gruyter. п. 453. ISBN 0123526515.
Ф. Холлеманом; продолжил Эгон Виберг; перевод Мэри Иглсон, Уильям Брюэр; в редакции Бернхарда Дж. (2001). Неорганическая химия (1-е английское изд., [под редакцией] Нильса Виберга, изд.). Сан-Диего, Калифорния: Берлин: Academic Press, W. de Gruyter. п. 453. ISBN 0123526515. /вес. водн. раствор., Thermo Scientific™
9{7}-йодан SMILES: O[I](O)(O)(O)(O)=O
/вес. водн. раствор., Thermo Scientific™
9{7}-йодан SMILES: O[I](O)(O)(O)(O)=O

 C.S. Реагент, J.T.Baker™
C.S. Реагент, J.T.Baker™