Металлы и различные неметаллы в периодической таблице Менделеева: признаки и свойства
Природа имеет некую цикличность и повторяемость в своих проявлениях. На это обращали внимание и древнегреческие ученые, когда пытались разложить природу вещей на составляющие: стихии, геометрические фигуры и даже атомы. На признаки повторяемости также обращают внимание и ученые современности. Например, Карл Линней на основе фенотипичного сходства смог выстроить систему живых существ.
…
Оглавление:
- Металлы и их отличительные свойства
- Какие же признаки являются общими для всех металлов?
- Неметаллы
- Аллотропия
Долгое время химия как наука оставалась без системы, которая могла бы упорядочить великое множество открытых веществ. Знания древних алхимиков дали богатейший материал для построения такой системы. Многие учёные предпринимали попытки выстроить гармоничную схему, но все попытки оказались тщетными. Так было вплоть до 1869 года, когда великий русский химик Дмитрий Иванович Менделеев представил миру своё детище — периодическую таблицу химических элементов. Говорят, что таблица приснилась учёному. Во сне он увидел, как таблица выстроилась в виде змеи и обвилась вокруг его ног. Достоверность этого факта сомнительна, но как бы то ни было, это был настоящий прорыв в науке.
Так было вплоть до 1869 года, когда великий русский химик Дмитрий Иванович Менделеев представил миру своё детище — периодическую таблицу химических элементов. Говорят, что таблица приснилась учёному. Во сне он увидел, как таблица выстроилась в виде змеи и обвилась вокруг его ног. Достоверность этого факта сомнительна, но как бы то ни было, это был настоящий прорыв в науке.
Менделеев расположил элементы по мере возрастания их атомной массы. Этот принцип актуален и сейчас, правда, сейчас в основе лежит количество протонов и нейтронов в ядре.
Это интересно: анионы и катионы в химии, таблица растворимости.
Металлы и их отличительные свойства
Все химические элементы можно довольно условно поделить на металлы и неметаллы. Что же их отличает друг от друга? Как отличить металл от неметалла?
Из 118 открытых веществ 94 относят к группе металлов. Группа представлена разнообразными подгруппами:
- Щелочные
- Щелочноземельные
- Переходные металлы
- Легкие
- Полуметаллы
- Лантаноиды
- Актиноиды
- Неопределенные — Бериллий и Магний.

Какие же признаки являются общими для всех металлов?
- Все металлы при комнатной температуре являют твёрдыми веществами. Это справедливо для всех элементов, кроме ртути, которая тверда до минус 39 градусов Цельсия. В комнатных условиях ртуть — это жидкость.
- Большинство из элементов этой группы имеют довольно высокую температуру плавления. Например, Вольфрам плавится при температуре 3410 градусов Цельсия. По этой причине его используют для изготовления нити в лампах накаливания.
- Все металлы пластичны. Это проявляется в том, что кристаллическая решетка металла позволяет атомам смещаться. В результате металлы могут гнуться без физической деформации, поддаются ковке. Особой пластичностью обладают медь, золото и серебро. Именно поэтому исторически они были первыми металлами, которые обрабатывал человек. Далее он научился обрабатывать железо.
- Все металлы очень хорошо проводят электричество, что опять же связано со строением металлической кристаллической решетки, имеющей подвижные электроны.
 Кроме всего прочего, эти элементы очень легко проводят тепло.
Кроме всего прочего, эти элементы очень легко проводят тепло. - Ну и, наконец, все металлы имеют характерный, ни с чем не сравнимый металлический блеск. Цвет чаще всего сероватой с голубым отливом. Au, Cu или Cs имеют желтый и красный оттенки.
Не пропустите: механизм образования металлической связи, конкретные примеры.
Неметаллы
Все неметаллы расположены в правом верхнем углу периодической таблицы по диагонали, которую можно провести от водорода до астата и радона. Кстати говоря, водород при определенных условиях также может проявлять металлические свойства.
Основное отличие от металлов заключается в строении кристаллической решетки. Если у металлов кристаллическая решетка металлическая, то у неметаллов она может быть атомной или молекулярной. Молекулярной решеткой обладают некоторые газы — кислород, хлор, сера, азот. Вещества с атомной решеткой имеют твёрдое агрегатное состояние, относительно высокую температуру плавления.
Это интересно: водородная связь — примеры, механизм образования.
Физические свойства неметаллов довольно разнообразны, неметаллы могут быть твердыми (йод, углерод, сера, фосфор), жидкими (только бром), газообразными (фтор, хлор, азот, кислород, водород) веществами с абсолютно разнообразным цветом. Агрегатное состояние может меняться под действием температуры.
С химической точки зрения, неметаллы могут выступать в роли окислителей и восстановителей. Неметаллы могут взаимодействовать между собой и с металлами. Кислород, к примеру, со всеми веществами выступает в роли окислителя, а вот с фтором выступает в роли восстановителя.
Аллотропия
Еще одно удивительное свойство неметаллов заключается в явлении, которое назвали аллотропией — видоизменение веществ, приводящее к различным аллотропным модификациям одного и того же химического элемента. С греческого можно перевести слово «аллотропия» как «другое свойство». Так оно и есть.
Это интересно: типы кристаллических решеток — таблица различных материалов.
Рассмотрим более подробно на примере списка некоторых простых веществ:
- Водород — при различной температуре это вещество может быть в виде орто-водорода и пара-водорода.
- Углерод имеет огромное множество аллотропных модификаций — алмаз, графит, графен, карбин. Строение кристаллических решеток этих веществ различается.
- Фосфор — встречается более 11 модификаций этого вещества. Интересен тот факт, что при модификации цвет вещества также меняется. Наиболее известны белый, черный и красный фосфор. Белый фосфор наиболее реакционный — он может самовоспламеняться, светится в темноте. Необходимо помнить, что белый фосфор очень ядовит для человеческого организма. В связи с этим не рекомендуется держать в доме различные предметы с фосфором. В советские годы очень популярны были статуэтки оленей или птиц, выполненные с применением белого фосфора. Они, конечно, очень красивы, но при этом ядовиты.

- Кислород может существовать в виде формы О2 — это стандартный кислород, которым мы дышим, и О3 — озон. Озон — это не очень устойчивая форма. В стратосфере озон формирует озоновый экран, защищающий атмосферу от проникновения вредного солнечного ультрафиолета. Озон имеет особый запах, который мы ассоциируем с запахом свежести после грозы. По этому запаху можно определить озон. Дело в том, что под действием электрический разрядов в атмосфере образуются молекулы озона.
Это интересно: как определить валентность по таблице Менделеева?
Модификации имеют и другие вещества — сера, селен, бор, мышьяк, бор, кремний, сурьма. При различных температурах многие металлы также обладают этими свойствами.
Конечно, деление всех простых веществ на группы металлов и неметаллов довольно условно. Это деление облегчает понимание свойств химических веществ, создает иллюзию их разделения на обособленные вещества. Как и все в мире, это деление относительное и зависит от внешних факторов окружающей среды — давления, температуры, света и т.д.
Как и все в мире, это деление относительное и зависит от внешних факторов окружающей среды — давления, температуры, света и т.д.
Таблица менделеева металлы и неметаллы отмечены цветом.
Полупроводниками называются неметаллы, которые имеют некоторые металлические свойства. Металлы и полупроводники имеют схожесть в том, что и те, и другие способны проводить ток.
Но полупроводники имеют отличительную особенность, которая заключается в том, что их электропроводность может возрастать в несколько раз в зависимости от внешних факторов. Таким образом, полупроводник проводит ток лучше при повышении температуры. У металлов электропроводность с повышением температуры уменьшается. Также на электропроводность может повлиять наличие посторонних примесей. Так, в металлах примеси понижают электропроводность, а в полупроводниках повышают.
Полупроводники в отличие от металлов могут обладать позитивной и негативной электропроводимостью. Сами по себе полупроводники по способности пропускать сквозь себя ток стоят между металлом и элементами, которые не проводят ток совсем.
Сами по себе полупроводники по способности пропускать сквозь себя ток стоят между металлом и элементами, которые не проводят ток совсем.
Определение металла и его свойства
Каждый день мы имеем дело с металлами и это неспроста. Большинство элементов таблицы Менделеева являются ими. Все они имеют свои характеристики и свойства.
Как правило, металлы — это такие элементы, которые хорошо проводят тепло и электричество. Также металлы очень пластичны, что позволяет изменять их форму путем ковки, еще они имеют высокий коэффициент твердости. Отличительной особенностью этого элемента является блеск, который называется металлическим. Свойства металла делятся на две основные фракции, такие как:
- Физические свойства.
- Химические свойства.
Чем металлы отличаются от металлов по физическим характеристикам? К физическим свойствам относится:
- Цвет. Металлы, как правило, имеют плотную структуру, которая не пропускает сквозь себя свет. А их цвет определяется отражением света от его поверхности.
 Так, металлы в большинстве случаев имеют расцветку от серого до серебристого. Но есть и исключения, как, например, медь, которая имеет красный цвет, и золото, имеющее желтый окрас.
Так, металлы в большинстве случаев имеют расцветку от серого до серебристого. Но есть и исключения, как, например, медь, которая имеет красный цвет, и золото, имеющее желтый окрас. - Состояние формы, твердость и плотность. Сами по себе металлы имеют твердое агрегатное состояние, но способны переходить в жидкое при высоких температурах. Так, металлы плавятся при температуре от 40 до 3400 градусов по Цельсию. Но встречаются металлы, чье основное агрегатное состояние — жидкое. К таким элементам относят ртуть.
- Электропроводимость. Особенностью является ее снижение при повышении температуры вещества.
- Теплопроводность и температура кипения/плавления.
Чем металлы отличаются от металлов по химическим свойствам? В этой группе выделяют:
- Окисляемость. Также металлы окисляются, и оксидная пленка на поверхности может придать им другой оттенок.
- Вступление в реакцию с неметаллами, кислотами, водой, солями.
Таблица Менделеева для чайников – HIMI4KA
Еще в школе, сидя на уроках химии, все мы помним таблицу на стене класса или химической лаборатории.
Эта таблица содержала классификацию всех известных человечеству химических элементов, тех фундаментальных компонентов, из которых состоит Земля и вся Вселенная.
Тогда мы и подумать не могли, что таблица Менделеева бесспорно является одним из величайших научных открытий, который является фундаментом нашего современного знания о химии.
Периодическая система химических элементов Д. И. Менделеева
На первый взгляд, ее идея выглядит обманчиво просто: организовать химические элементы в порядке возрастания веса их атомов. Причем в большинстве случаев оказывается, что химические и физические свойства каждого элемента сходны с предыдущим ему в таблице элементом.
Эта закономерность проявляется для всех элементов, кроме нескольких самых первых, просто потому что они не имеют перед собой элементов, сходных с ними по атомному весу.
Именно благодаря открытию такого свойства мы можем поместить линейную последовательность элементов в таблицу, очень напоминающую настенный календарь, и таким образом объединить огромное количество видов химических элементов в четкой и связной форме.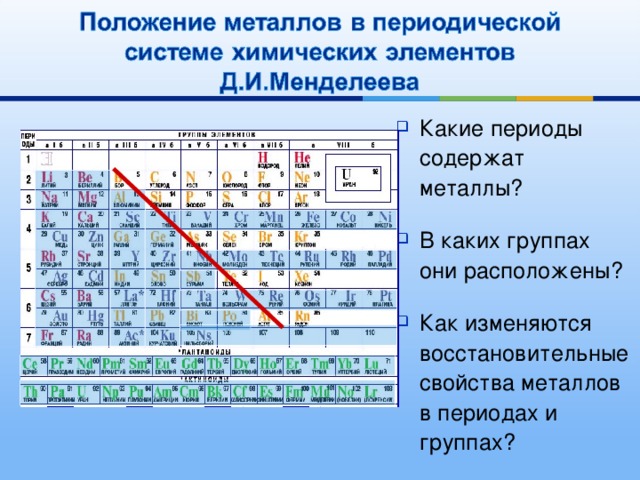
Разумеется, сегодня мы пользуемся понятием атомного числа (количества протонов) для того, чтобы упорядочить систему элементов. Это помогло решить так называемую техническую проблему «пары перестановок», однако не привело к кардинальному изменению вида периодической таблицы.
В периодической таблице Менделеева все элементы упорядочены с учетом их атомного числа, электронной конфигурации и повторяющихся химических свойств. Ряды в таблице называются периодами, а столбцы группами. В первой таблице, датируемой 1869 годом, содержалось всего 60 элементов, теперь же таблицу пришлось увеличить, чтобы поместить 118 элементов, известных нам сегодня.
Периодическая система Менделеева систематизирует не только элементы, но и самые разнообразные их свойства. Химику часто бывает достаточно иметь перед глазами Периодическую таблицу для того, чтобы правильно ответить на множество вопросов (не только экзаменационных, но и научных).
The ID of 1M7iKKVnPJE is invalid.
Периодический закон
Существуют две формулировки периодического закона химических элементов: классическая и современная.
Классическая, в изложении его первооткрывателя Д.И. Менделеева: свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величин атомных весов элементов.
Современная: свойства простых веществ, а также свойства и формы соединений элементов находятся в периодической зависимости от заряда ядра атомов элементов (порядкового номера).
Графическим изображением периодического закона является периодическая система элементов, которая представляет собой естественную классификацию химических элементов, основанную на закономерных изменениях свойств элементов от зарядов их атомов. Наиболее распространёнными изображениями периодической системы элементов Д.И. Менделеева являются короткая и длинная формы.
Группы и периоды Периодической системы
Группами называют вертикальные ряды в периодической системе. В группах элементы объединены по признаку высшей степени окисления в оксидах. Каждая группа состоит из главной и побочной подгрупп.
В группах элементы объединены по признаку высшей степени окисления в оксидах. Каждая группа состоит из главной и побочной подгрупп.
Главные подгруппы включают в себя элементы малых периодов и одинаковые с ним по свойствам элементы больших периодов. Побочные подгруппы состоят только из элементов больших периодов.
Химические свойства элементов главных и побочных подгрупп значительно различаются.
Периодом называют горизонтальный ряд элементов, расположенных в порядке возрастания порядковых (атомных) номеров.
В периодической системе имеются семь периодов: первый, второй и третий периоды называют малыми, в них содержится соответственно 2, 8 и 8 элементов; остальные периоды называют большими: в четвёртом и пятом периодах расположены по 18 элементов, в шестом — 32, а в седьмом (пока незавершенном) — 31 элемент. Каждый период, кроме первого, начинается щелочным металлом, а заканчивается благородным газом.
Физический смысл порядкового номера химического элемента: число протонов в атомном ядре и число электронов, вращающихся вокруг атомного ядра, равны порядковому номеру элемента.
Свойства таблицы Менделеева
Напомним, что группами называют вертикальные ряды в периодической системе и химические свойства элементов главных и побочных подгрупп значительно различаются.
Свойства элементов в подгруппах закономерно изменяются сверху вниз:
- усиливаются металлические свойства и ослабевают неметаллические;
- возрастает атомный радиус;
- возрастает сила образованных элементом оснований и бескислородных кислот;
- электроотрицательность падает.
Все элементы, кроме гелия, неона и аргона, образуют кислородные соединения, существует всего восемь форм кислородных соединений.
В периодической системе их часто изображают общими формулами, расположенными под каждой группой в порядке возрастания степени окисления элементов: R2O, RO, R2O3, RO2, R2O5, RO3, R2O7, RO4, где символом R обозначают элемент данной группы.
Формулы высших оксидов относятся ко всем элементам группы, кроме исключительных случаев, когда элементы не проявляют степени окисления, равной номеру группы (например, фтор).
Оксиды состава R2O проявляют сильные основные свойства, причём их основность возрастает с увеличением порядкового номера, оксиды состава RO (за исключением BeO) проявляют основные свойства. Оксиды состава RO2, R2O5, RO3, R2O7 проявляют кислотные свойства, причём их кислотность возрастает с увеличением порядкового номера.
Элементы главных подгрупп, начиная с IV группы, образуют газообразные водородные соединения. Существуют четыре формы таких соединений. Их располагают под элементами главных подгрупп и изображают общими формулами в последовательности Rh5, Rh4, Rh3, RH.
Соединения Rh5 имеют нейтральный характер; Rh4 — слабоосновный; Rh3 — слабокислый; RH — сильнокислый характер.
Напомним, что периодом называют горизонтальный ряд элементов, расположенных в порядке возрастания порядковых (атомных) номеров.
В пределах периода с увеличением порядкового номера элемента:
- электроотрицательность возрастает;
- металлические свойства убывают, неметаллические возрастают;
- атомный радиус падает.

К ним относятся элементы из первой и второй группы периодической таблицы. Щелочные металлы из первой группы — мягкие металлы, серебристого цвета, хорошо режутся ножом. Все они обладают одним-единственным электроном на внешней оболочке и прекрасно вступают в реакцию.
Щелочноземельные металлы из второй группы также имеют серебристый оттенок. На внешнем уровне помещено по два электрона, и, соответственно, эти металлы менее охотно взаимодействуют с другими элементами.
По сравнению со щелочными металлами, щелочноземельные металлы плавятся и кипят при более высоких температурах.
Показать / Скрыть текст
| Щелочные металлы | Щелочноземельные металлы |
| Литий Li 3 | Бериллий Be 4 |
| Натрий Na 11 | Магний Mg 12 |
| Калий K 19 | Кальций Ca 20 |
| Рубидий Rb 37 | Стронций Sr 38 |
| Цезий Cs 55 | Барий Ba 56 |
| Франций Fr 87 | Радий Ra 88 |
Лантаниды (редкоземельные элементы) и актиниды
Лантаниды — это группа элементов, изначально обнаруженных в редко встречающихся минералах; отсюда их название «редкоземельные» элементы.
Впоследствии выяснилось, что данные элементы не столь редки, как думали вначале, и поэтому редкоземельным элементам было присвоено название лантаниды. Лантаниды и актиниды занимают два блока, которые расположены под основной таблицей элементов.
Обе группы включают в себя металлы; все лантаниды (за исключением прометия) нерадиоактивны; актиниды, напротив, радиоактивны.
Показать / Скрыть текст
| Лантаниды | Актиниды |
| Лантан La 57 | Актиний Ac 89 |
| Церий Ce 58 | Торий Th 90 |
| Празеодимий Pr 59 | Протактиний Pa 91 |
| Неодимий Nd 60 | Уран U 92 |
| Прометий Pm 61 | Нептуний Np 93 |
| Самарий Sm 62 | Плутоний Pu 94 |
| Европий Eu 63 | Америций Am 95 |
| Гадолиний Gd 64 | Кюрий Cm 96 |
| Тербий Tb 65 | Берклий Bk 97 |
| Диспрозий Dy 66 | Калифорний Cf 98 |
| Гольмий Ho 67 | Эйнштейний Es 99 |
| Эрбий Er 68 | Фермий Fm 100 |
| Тулий Tm 69 | Менделевий Md 101 |
| Иттербий Yb 70 | Нобелий No 102 |
Галогены и благородные газы
Галогены и благородные газы объединены в группы 17 и 18 периодической таблицы. Галогены представляют собой неметаллические элементы, все они имеют семь электронов во внешней оболочке.
Галогены представляют собой неметаллические элементы, все они имеют семь электронов во внешней оболочке.
В благородных газахвсе электроны находятся во внешней оболочке, таким образом с трудом участвуют в образовании соединений. Эти газы называют «благородными, потому что они редко вступают в реакцию с прочими элементами; т. е.
ссылаются на представителей благородной касты, которые традиционно сторонились других людей в обществе.
Показать / Скрыть текст
| Галогены | Благородные газы |
| Фтор F 9 | Гелий He 2 |
| Хлор Cl 17 | Неон Ne 10 |
| Бром Br 35 | Аргон Ar 18 |
| Йод I 53 | Криптон Kr 36 |
| Астат At 85 | Ксенон Xe 54 |
| — | Радон Rn 86 |
Переходные металлы
Переходные металлы занимают группы 3—12 в периодической таблице. Большинство из них плотные, твердые, с хорошей электро- и теплопроводностью. Их валентные электроны (при помощи которых они соединяются с другими элементами) находятся в нескольких электронных оболочках.
Большинство из них плотные, твердые, с хорошей электро- и теплопроводностью. Их валентные электроны (при помощи которых они соединяются с другими элементами) находятся в нескольких электронных оболочках.
Показать / Скрыть текст
| Переходные металлы |
| Скандий Sc 21 |
| Титан Ti 22 |
| Ванадий V 23 |
| Хром Cr 24 |
| Марганец Mn 25 |
| Железо Fe 26 |
| Кобальт Co 27 |
| Никель Ni 28 |
| Медь Cu 29 |
| Цинк Zn 30 |
| Иттрий Y 39 |
| Цирконий Zr 40 |
| Ниобий Nb 41 |
| Молибден Mo 42 |
| Технеций Tc 43 |
| Рутений Ru 44 |
| Родий Rh 45 |
| Палладий Pd 46 |
| Серебро Ag 47 |
| Кадмий Cd 48 |
| Лютеций Lu 71 |
| Гафний Hf 72 |
| Тантал Ta 73 |
| Вольфрам W 74 |
| Рений Re 75 |
| Осмий Os 76 |
| Иридий Ir 77 |
| Платина Pt 78 |
| Золото Au 79 |
| Ртуть Hg 80 |
| Лоуренсий Lr 103 |
| Резерфордий Rf 104 |
| Дубний Db 105 |
| Сиборгий Sg 106 |
| Борий Bh 107 |
| Хассий Hs 108 |
| Мейтнерий Mt 109 |
| Дармштадтий Ds 110 |
| Рентгений Rg 111 |
| Коперниций Cn 112 |
Металлоиды
Металлоиды занимают группы 13—16 периодической таблицы.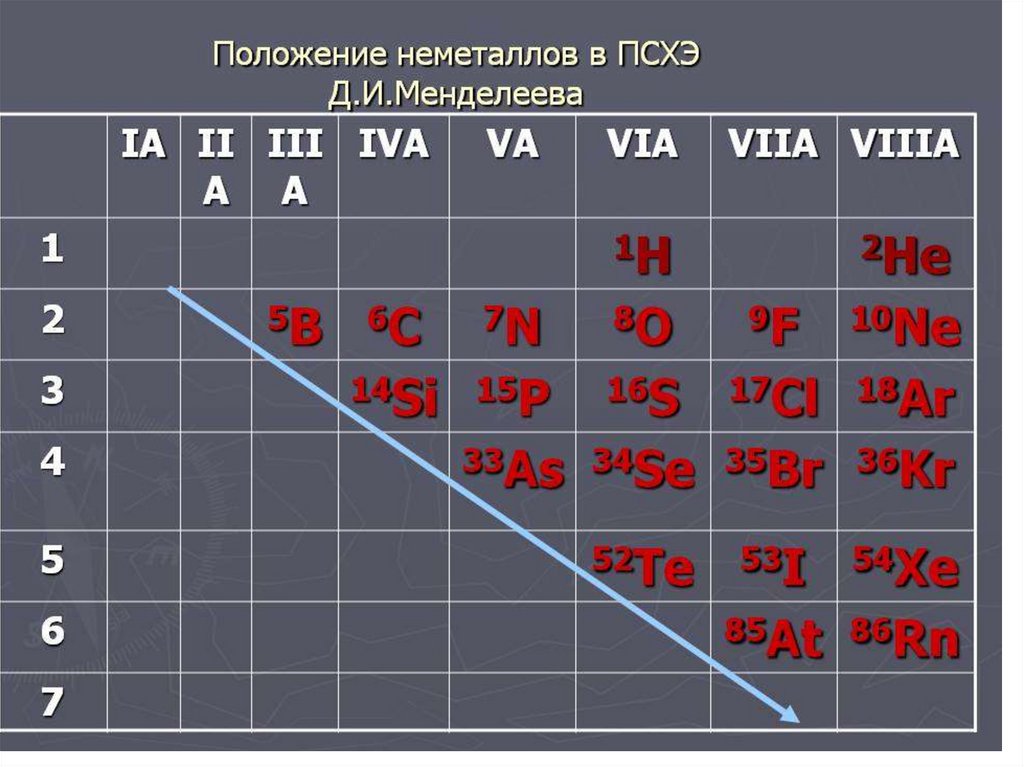 Такие металлоиды, как бор, германий и кремний, являются полупроводниками и используются для изготовления компьютерных чипов и плат.
Такие металлоиды, как бор, германий и кремний, являются полупроводниками и используются для изготовления компьютерных чипов и плат.
Показать / Скрыть текст
| Металлоиды |
| Бор B 5 |
| Кремний Si 14 |
| Германий Ge 32 |
| Мышьяк As 33 |
| Сурьма Sb 51 |
| Теллур Te 52 |
| Полоний Po 84 |
Постпереходными металлами
Элементы, называемые постпереходными металлами, относятся к группам 13—15 периодической таблицы. В отличие от металлов, они не имеют блеска, а имеют матовую окраску.
В сравнении с переходными металлами постпереходные металлы более мягкие, имеют более низкую температуру плавления и кипения, более высокую электроотрицательность. Их валентные электроны, с помощью которых они присоединяют другие элементы, располагаются только на внешней электронной оболочке.
Элементы группы постпереходных металлов имеют гораздо более высокую температуру кипения, чем металлоиды.
Показать / Скрыть текст
| Постпереходные металлы |
| Алюминий Al 13 |
| Галлий Ga 31 |
| Индий In 49 |
| Олово Sn 50 |
| Таллий Tl 81 |
| Свинец Pb 82 |
| Висмут Bi 83 |
Неметаллы
Из всех элементов, классифицируемых как неметаллы, водород относится к 1-й группе периодической таблицы, а остальные — к группам 13—18. Неметаллы не являются хорошими проводниками тепла и электричества. Обычно при комнатной температуре они пребывают в газообразном (водород или кислород) или твердом состоянии (углерод).
Показать / Скрыть текст
| Неметаллы |
| Водород H 1 |
| Углерод C 6 |
| Азот N 7 |
| Кислород O 8 |
| Фосфор P 15 |
| Сера S 16 |
| Селен Se 34 |
| Флеровий Fl 114 |
| Унунсептий Uus 117 |
А теперь закрепите полученные знания, посмотрев видео про таблицу Менделеева и не только.
Отлично, первый шаг на пути к знаниям сделан. Теперь вы более-менее ориентируетесь в таблице Менделеева и это вам очень даже пригодится, ведь Периодическая система Менделеева является фундаментом, на котором стоит эта удивительная наука.
Источник: https://himi4ka.ru/tablica-mendeleeva
Чем дерево похоже на металл и в чем их отличия
Дерево — это растительное сырье. Металл же это результат природного химического соединения. Чем отличается дерево от металла:
- Древесина не проводит электричество и возгорается при довольно низкой температуре по сравнению с металлами.
- Древесина не плавится при воздействии высоких температур.
- Также дерево плохо проводит тепло, в отличие от металлов.
- Древесина упругая, но не гибкая. Металлы же имеют более низкий коэффициент упругости, но они более пластичны. Так сложить пополам проволоку и не сломать ее можно легко, древесина при таком воздействии сломается пополам.
- Также отличительной чертой древесины от металла является то, что она не покрывается коррозией.
 Есть породы дерева, которые могут долгое время находиться в воде и не гнить. Металлы же при таких условиях покрываются ржавчиной.
Есть породы дерева, которые могут долгое время находиться в воде и не гнить. Металлы же при таких условиях покрываются ржавчиной. - Плотность древесины достаточно низкая по сравнению с металлами. Хотя некоторые металлы имеют плотность ниже дерева, они относятся к легким металлам.
Периодическая система Менделеева
Периодическая таблица химических элементов была составлена Д. И. Менделеевым во второй половине XIX века. Что такое это, и для чего она нужна? Она объединяет все химические элементы по возрастанию атомного веса, причем, все они расставлены так, что их свойства изменяются периодическим образом.
Периодическая система Менделеева в свела в единую систему все существующие элементы, прежде считавшиеся просто отдельными веществами.
На основании ее изучения были предсказаны, а впоследствии — синтезированы новые химические вещества. Значение этого открытия для науки невозможно переоценить
, оно значительно опередило свое время и дало толчок к развитию химии на многие десятилетия.
Существует три наиболее распространенных варианта таблицы, которые условно именуются «короткая», «длинная» и «сверхдлинная».
Основной считается длинная таблица, она
утверждена официально.
Отличием между ними является компоновка элементов и длина периодов.
Что такое период
Система содержит 7 периодов
. Они представлены графически в виде горизонтальных строк. При этом, период может иметь одну или две строки, называемые рядами. Каждый последующий элемент отличается от предыдущего возрастанием заряда ядра (количества электронов) на единицу.
Если не усложнять, период — это горизонтальная строка периодической таблицы. Каждый из них начинается металлом и заканчивается инертным газом. Собственно, это и создает периодичность — свойства элементов изменяются внутри одного периода, вновь повторяясь в следующем. Первый, второй и третий периоды — неполные, они называются малыми и содержат соответственно 2, 8 и 8 элементов. Остальные — полные, они имеют по 18 элементов.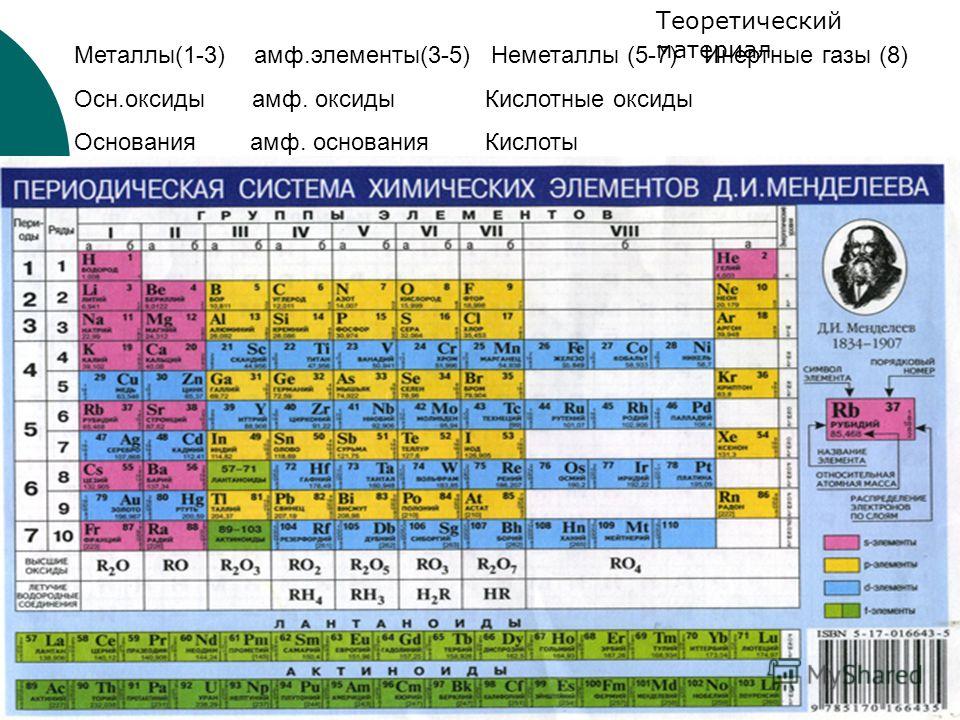
Что такое группа
Группа — это вертикальный столбец
, содержащий элементы с одинаковым электронным строением или, говоря проще, с одинаковой высшей . Официально утвержденная длинная таблица содержит 18 групп, которые начинаются со щелочных металлов и заканчиваются инертными газами.
Каждая группа имеет свое название, облегчающее поиск или классификацию элементов. Усиливаются металлические свойства в независимости от элемента по направлению сверху-вниз. Это связано с увеличением количества атомных орбит — чем их больше, тем слабее электронные связи, что делает более ярко выраженной кристаллическую решетку.
Что такое металл? Свойства и особенности металлов
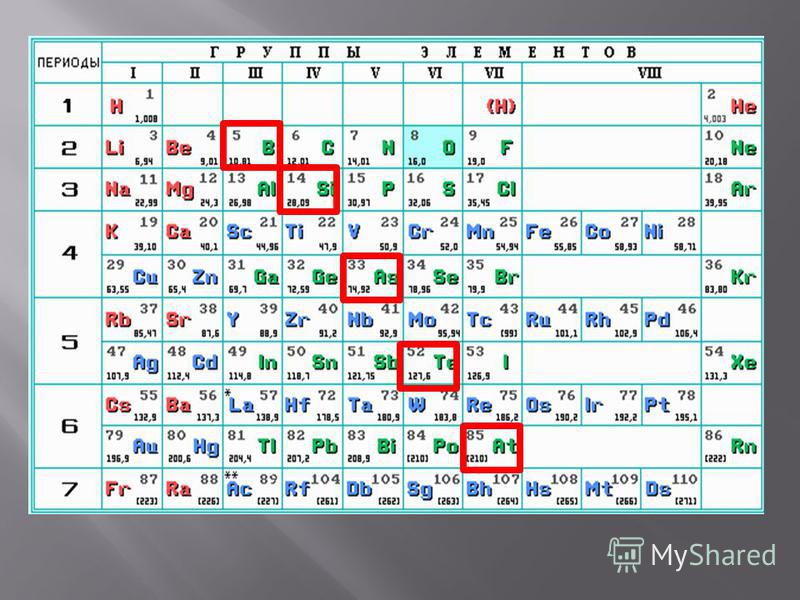
Если в периодической таблице элементов Д.И.Менделеева провести диагональ от бериллия к астату, то слева внизу по диагонали будут находиться элементы-металлы (к ним же относятся элементы побочных подгрупп, выделены синим цветом), а справа вверху – элементы-неметаллы (выделены желтым цветом).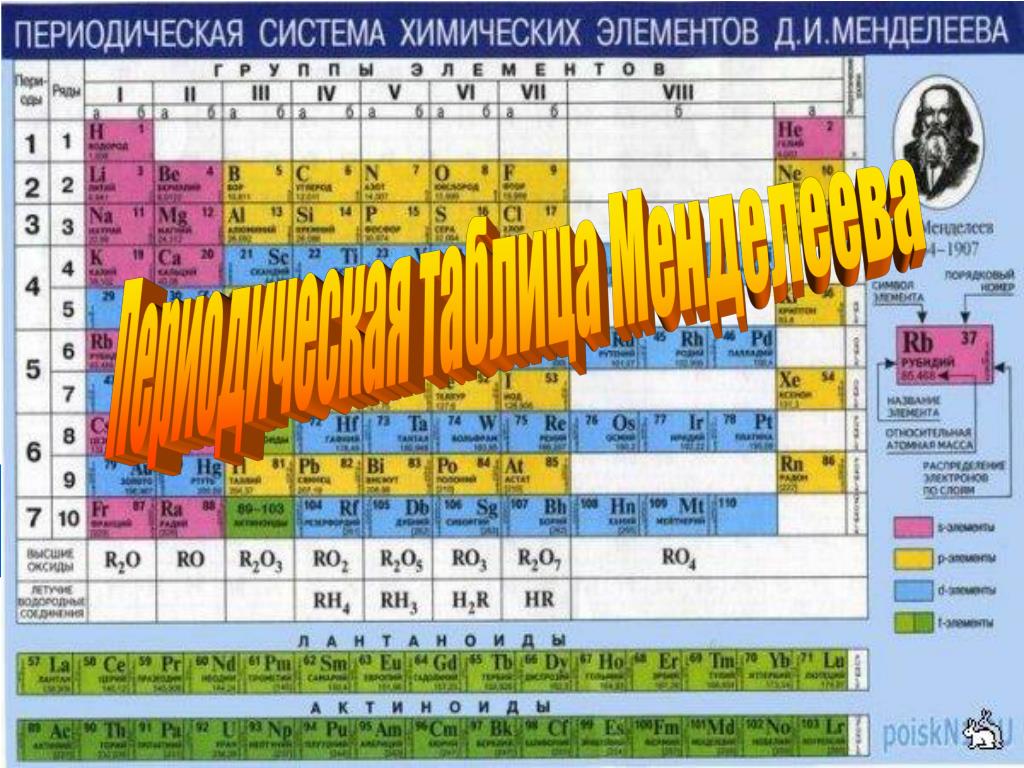 Элементы, расположенные вблизи диагонали – полуметаллы или металлоиды (B, Si, Ge, Sb и др.), обладают двойственным характером (выделены розовым цветом).
Элементы, расположенные вблизи диагонали – полуметаллы или металлоиды (B, Si, Ge, Sb и др.), обладают двойственным характером (выделены розовым цветом).
Как видно из рисунка, подавляющее большинство элементов являются металлами.
По своей химической природе металлы – это химические элементы, атомы которых отдают электроны с внешнего или предвнешнего энергетического уровней, образуя при этом положительно заряженные ионы.
Практически все металлы имеют сравнительно большие радиусы и малое число электронов (от 1 до 3) на внешнем энергетическом уровне. Для металлов характерны низкие значения электроотрицательности и восстановительные свойства.
Наиболее типичные металлы расположены в начале периодов (начиная со второго), далее слева направо металлические свойства ослабевают. В группе сверху вниз металлические свойства усиливаются, т.к увеличивается радиус атомов (за счет увеличения числа энергетических уровней). Это приводит к уменьшению электроотрицательности (способности притягивать электроны) элементов и усилению восстановительных свойств (способность отдавать электроны другим атомам в химических реакциях).
Типичными
металлами являются s-элементы (элементы IА-группы от Li до Fr. элементы ПА-группы от Мg до Rа). Общая электронная формула их атомов ns1-2. Для них характерны степени окисления + I и +II соответственно.
Небольшое число электронов (1-2) на внешнем энергетическом уровне атомов типичных металлов предполагает легкую потерю этих электронов и проявление сильных восстановительных свойств, что отражают низкие значения электроотрицательности. Отсюда вытекает ограниченность химических свойств и способов получения типичных металлов.
Характерной особенностью типичных металлов является стремление их атомов образовывать катионы и ионные химические связи с атомами неметаллов. Соединения типичных металлов с неметаллами — это ионные кристаллы «катион металлаанион неметалла», например К+ Вг—, Сa2+ О2-. Катионы типичных металлов входят также в состав соединений со сложными анионами — гидроксидов и солей, например Мg2+(OН—)2, (Li+)2СO32-.
Металлы А-групп, образующие диагональ амфотерности в Периодической системе Ве-Аl-Gе-Sb-Ро, а также примыкающие к ним металлы (Gа, In, Тl, Sn, Рb, Вi) не проявляют типично металлических свойств. Общая электронная формула их атомов ns2np0-4
Общая электронная формула их атомов ns2np0-4
предполагает большее разнообразие степеней окисления, большую способность удерживать собственные электроны, постепенное понижение их восстановительной способности и появление окислительной способности, особенно в высоких степенях окисления (характерные примеры — соединения Тl III, РbIV, Вiv). Подобное химическое поведение характерно и для большинства (d-элементов, т. е. элементов Б-групп Периодической системы (типичные примеры — амфотерные элементы Сr и Zn).
Это проявление двойственности (амфотерности) свойств, одновременно металлических (основных) и неметаллических, обусловлено характером химической связи. В твердом состоянии соединения нетипичных металлов с неметаллами содержат преимущественно ковалентные связи (но менее прочные, чем связи между неметаллами). В растворе эти связи легко разрываются, а соединения диссоциируют на ионы (полностью или частично). Например, металл галлий состоит из молекул Ga2, в твердом состоянии хлориды алюминия и ртути (II) АlСl3 и НgСl2 содержат сильно ковалентные связи, но в растворе АlСl3 диссоциирует почти полностью, а НgСl2 — в очень малой степени (да и то на ионы НgСl+ и Сl—).
Что такое металл?
Наибольшее число элементов в таблице Менделеева относится к металлам. В настоящее время человеку известно только 96 их видов. Каждый из них обладает своими особенностями, многие из которых ещё не изучены.
Что такое металл? Это простое вещество, для которого характерны большие электро- и теплопроводность, положительный температурный коэффициент проводимости. Большинство металлов обладает высокой прочностью, пластичностью и поддаются ковке. Одной из отличительных особенностей является наличие металлического блеска.
Значение слова «металл» связано с греческим métallion, где оно означает «выкапывать из земли», а также «рудник, копи». В русскую терминологию оно пришло в период правления Петра I из немецкого языка (нем. Metall), в который слово перебралось с латинского.
Свойства таблицы Менделеева
Напомним, что группами называют вертикальные ряды в периодической системе и химические свойства элементов главных и побочных подгрупп значительно различаются.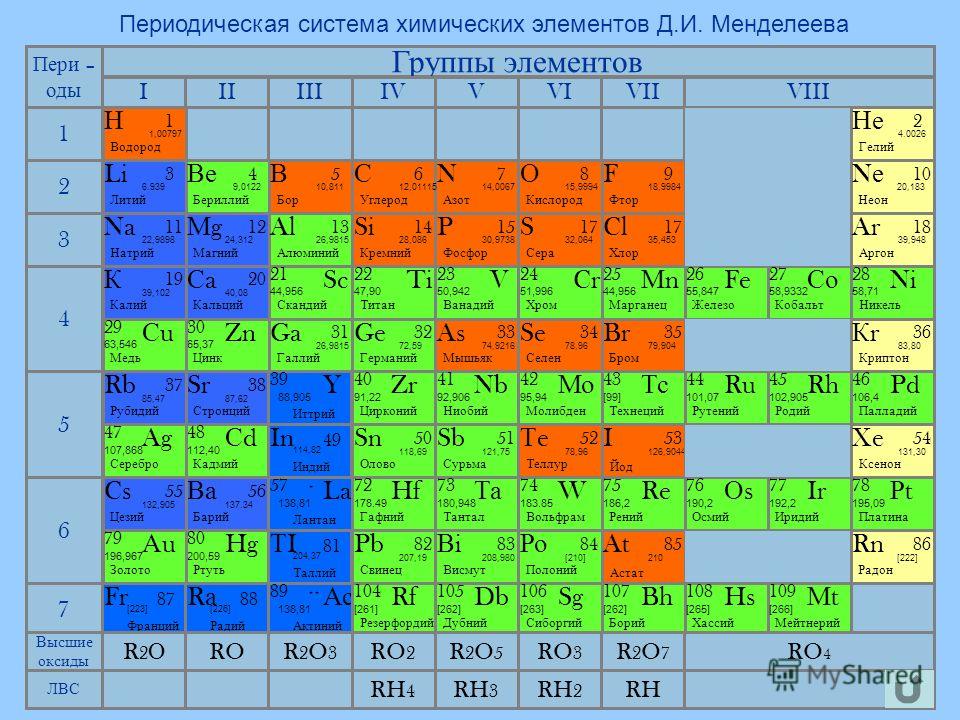
Свойства элементов в подгруппах закономерно изменяются сверху вниз:
- усиливаются металлические свойства и ослабевают неметаллические;
- возрастает атомный радиус;
- возрастает сила образованных элементом оснований и бескислородных кислот;
- электроотрицательность падает.
Все элементы, кроме гелия, неона и аргона, образуют кислородные соединения, существует всего восемь форм кислородных соединений. В периодической системе их часто изображают общими формулами, расположенными под каждой группой в порядке возрастания степени окисления элементов: R2O, RO, R2O3, RO2, R2O5, RO3, R2O7, RO4, где символом R обозначают элемент данной группы. Формулы высших оксидов относятся ко всем элементам группы, кроме исключительных случаев, когда элементы не проявляют степени окисления, равной номеру группы (например, фтор).
Оксиды состава R2O проявляют сильные основные свойства, причём их основность возрастает с увеличением порядкового номера, оксиды состава RO (за исключением BeO) проявляют основные свойства. Оксиды состава RO2, R2O5, RO3, R2O7 проявляют кислотные свойства, причём их кислотность возрастает с увеличением порядкового номера.
Оксиды состава RO2, R2O5, RO3, R2O7 проявляют кислотные свойства, причём их кислотность возрастает с увеличением порядкового номера.
Элементы главных подгрупп, начиная с IV группы, образуют газообразные водородные соединения. Существуют четыре формы таких соединений. Их располагают под элементами главных подгрупп и изображают общими формулами в последовательности Rh5, Rh4, Rh3, RH.
Соединения Rh5 имеют нейтральный характер; Rh4 — слабоосновный; Rh3 — слабокислый; RH — сильнокислый характер.
Напомним, что периодом называют горизонтальный ряд элементов, расположенных в порядке возрастания порядковых (атомных) номеров.
В пределах периода с увеличением порядкового номера элемента:
- электроотрицательность возрастает;
- металлические свойства убывают, неметаллические возрастают;
- атомный радиус падает.
Физические свойства
Элементы металлы обычно обладают хорошей пластичностью, исключение составляют олово, цинк, марганец. По плотности они разделяются на легкие (алюминий, литий) и тяжелые (осмий, вольфрам). Большинство имеет высокую температуру плавления, общий диапазон колеблется от – 39 у ртути до 3410 градусов по Цельсию у вольфрама.
По плотности они разделяются на легкие (алюминий, литий) и тяжелые (осмий, вольфрам). Большинство имеет высокую температуру плавления, общий диапазон колеблется от – 39 у ртути до 3410 градусов по Цельсию у вольфрама.
В нормальных условиях все металлы, кроме ртути и франция, являются твердыми. Степень их твердости определяют в баллах по шкале Мосса, где максимумом считается 10 баллов. Так, самыми твердыми являются вольфрам и уран (6.0), наиболее мягким является цезий (0.2). Многие металлы обладают серебристым, голубоватым и серым оттенками, только некоторым свойственны желтый и красноватый цвета.
В их кристаллических решетках находятся подвижные электроны, благодаря чему они отлично проводят электрический ток и тепло. Лучше всего с этим справляется серебро и медь. Наименьшую теплопроводность имеет ртуть.
Химические свойства
По химическим свойствам металлы разделяются на множество групп. Среди них щелочные, щелочноземельные, легкие, актиний и актиноиды, лантан и лантаноиды, полуметаллы. Отдельно находятся магний и бериллий.
Отдельно находятся магний и бериллий.
Как правило, металлы выступают в качестве восстановителей для неметаллов. Они обладают различной активностью, поэтому реакции на вещества неодинаковы. Наиболее активными являются щелочные металлы, они легко взаимодействуют с водородом, водой.
При определенных условиях почти всегда происходит взаимодействие металлов с кислородом. Реакция на него отсутствует только у золота и платины. Они также не реагируют на серу и хлор, в отличие от других металлов. Щелочная группа окисляется в обыкновенной среде, остальные при воздействии высоких температур.
Группы и периоды Периодической системы
Группами называют вертикальные ряды в периодической системе. В группах элементы объединены по признаку высшей степени окисления в оксидах. Каждая группа состоит из главной и побочной подгрупп. Главные подгруппы включают в себя элементы малых периодов и одинаковые с ним по свойствам элементы больших периодов. Побочные подгруппы состоят только из элементов больших периодов. Химические свойства элементов главных и побочных подгрупп значительно различаются.
Химические свойства элементов главных и побочных подгрупп значительно различаются.
Периодом называют горизонтальный ряд элементов, расположенных в порядке возрастания порядковых (атомных) номеров. В периодической системе имеются семь периодов: первый, второй и третий периоды называют малыми, в них содержится соответственно 2, 8 и 8 элементов; остальные периоды называют большими: в четвёртом и пятом периодах расположены по 18 элементов, в шестом — 32, а в седьмом (пока незавершенном) — 31 элемент. Каждый период, кроме первого, начинается щелочным металлом, а заканчивается благородным газом.
Физический смысл порядкового номера химического элемента: число протонов в атомном ядре и число электронов, вращающихся вокруг атомного ядра, равны порядковому номеру элемента.
Нахождение в природе
В природе металлы встречаются в основном в рудах или соединениях, например, оксидах, солях, карбонатах. Перед использованием они проходят длительные этапы очистки. Многие металлы сопровождают месторождения минералов. Так, кадмий входит в состав цинковых руд, скандий и тантал соседствуют с оловом.
Многие металлы сопровождают месторождения минералов. Так, кадмий входит в состав цинковых руд, скандий и тантал соседствуют с оловом.
Сразу в чистом виде встречаются только инертные, то есть неактивные металлы. Из-за слабой подверженности к окислениям и коррозиям они завоевали звание благородных. К ним относят золото, платину, серебро, рутений, осмий, палладий и т. д. Благородные металлы очень пластичны и обладают характерным ярким блеском в готовых изделиях.
Металлы окружают нас повсюду. В больших количествах они находятся в земной коре. Самыми распространенными являются алюминий, железо, натрий, магний, кальций, титан и калий. Они содержатся в морской воде (натрий, магний), являются частью живых организмов. В теле человека металлы присутствуют в костях (кальций), в крови (железо), нервной системе (магний), мышцах (магний) и других органах.
Дизайн интерьера и архитектура
Для успешного создания декоративных изделий необходимо знать основные свойства исходного материала, а также технологию работы с ним.
В наши дни для изготовления посуды, украшений и различных предметов дизайна интерьера могут использоваться как металлы в чистом виде, так и их сплавы.
Художественное изделие — ваза из серебра
Все металлы и сплавы, созданные на их основе, делятся на две большие группы, обладающие различными свойствами:
- Черные металлы — сталь
- Цветные металлы — медь, бронза, латунь, цинк, олово, алюминий, свинец и серебро.
Именно эти виды металлов наиболее часто используются для изготовления декоративных предметов, посуды и многого другого. Поэтому давайте рассмотрим их свойства и особенности обработки металлов.
Сталь
Сталь относится к черным металлам. Для художественной обработки лучше всего подходит углеродистая сталь, которая представляет собой сплав железа с углеродом и другими элементами. Сталь обладает высокими качественными характеристиками, среди которых можно назвать следующие:
- Упругость
- Прочность
- Способность к закаливанию — кусок стали нагревается при высокой температуре докрасна, а затем опускают в воду.
 Благодаря этому металл приобретает различные степени твердости и упругости.
Благодаря этому металл приобретает различные степени твердости и упругости. - Возможность » отпускания» посредством нагревания до красного каления и последующего медленного охлаждения.
- Способность к обработке кузнечным молотом в нагретом состоянии, так как сталь отлично куется.
- Возможность к разрезанию металла на тонкие полосы.
Мягкость стали прямо пропорциональная количеству углерода в ее составе. Чем меньше в металле углерода, тем он мягче и легче в обработке. Мягкость стали повышается при отжиге, то есть » отпускании» металла. Для этого сталь нагревают докрасна, а затем подвергают процедуре медленного охлаждения.
Сталь для изготовления различных изделий и художественной обработки производят в виде сортового материала. Для гравирования и чеканки чаще всего используют стали У8 и У10, где буквой » У» обозначено количество углерода в составе сплава.
Лезвие ножей изготовлено из нержавеющей углеродистой стали
Цветные металлы
Цветные металлы стоят намного дороже черных, потому что они обладают множеством уникальных свойств. Главным из них является отсутствие реакции с магнитом, то есть цветные металлы не притягиваются и не намагничиваются. Кроме этого, большинство из них практически не поддаются окислению, поэтому изделия характеризуются длительностью срока службы.
Главным из них является отсутствие реакции с магнитом, то есть цветные металлы не притягиваются и не намагничиваются. Кроме этого, большинство из них практически не поддаются окислению, поэтому изделия характеризуются длительностью срока службы.
Выпуск цветных металлов для художественной обработки осуществляется в различных видах:
- Ленты
- Полосы
- Чушки
- Трубки
- Проволока
- Прутки
- Листы
Давайте рассмотрим характерные особенности наиболее популярных среди мастеров цветных металлов:
- Медь — достаточно мягкий металл красивого красно — оранжевого оттенка, характеризующийся повышенной способностью к ковке и обладающий большой электропроводностью и способностью проводить тепло. Обработка меди не представляет особой сложности, но мастер должен иметь в виду большую вязкость данного металла.

Медь можно паять с помощью олова и твердого припоя, Листовая медь является основным материалом для выполнения чеканки и граверных работ. Медная проволока используется для изготовления декоративных изделий и ажурных скульптур.
Медная раковина
- Бронза — это сплав меди с оловом. Количественное содержание олова влияет на цвет сплава, который может приобретать розовые, красные, желтые или серые оттенки. Если бронзовое изделие покрыть слоем патины ( декоративным налетом из оксида меди), то она приобретает благородный дымчато — зеленоватый оттенок и выглядит старинной и по — настоящему дорогой. Бронза чаще всего используется для инкрустации и литейных работ.
Листовая бронза
- Латунь — это сплав меди с цинком. Оттенок металла зависит от количества цинка. По своим качественным характеристикам латунь является более твердым сплавом, чем чистая красная медь, поэтому степень ее ковкости значительно ниже. По сравнению с медью латунь обладает некоторой хрупкостью, но вместе с тем она более упруга.

Латунь легко поддается различным видам обработки, в частности, ее можно использовать для изготовления тонких деталей в инкрустациях, а также украшений различной конфигурации. Для чеканных работ используется в листовом виде.
Чеканка на латуни
- Цинк — прекрасно подходит для литья как в чистом виде, так и в сплавах с другими металлами. Чистый цинк куется плохо, однако его легко паять, гравировать и обрабатывать различными инструментами. Температура плавления составляет 419* С.
Листовой цинк
- Олово — цветной металл, с давних пор известный своей мягкостью и пластичностью. Температура его плавления составляет всего 252* С. В качестве компонента олово входит в состав различных видов бронзы. На изломе олово издает характерный, узнаваемый хруст. Чистое олово и его сплавы идеально подходят для изготовления инкрустаций. А еще олово используется для лужения и пайки посуды как в чистом виде, так и в сплавах со свинцом.
 При этом продукты его окисления безвредны.
При этом продукты его окисления безвредны.
Набор оловянных солдатиков
- Алюминий — цветной металл серебристо — белого цвета, который плавится при температуре около 658* С. Характерной особенностью алюминия является его легкость и простота в обработке металла. Литой алюминий достаточно хрупкий, а в прокатном ( отожженном) виде он приобретает желаемую пластичность.
Алюминиевые изделия ремесленников Мадагаскара
- Свинец — мягкий цветной металл, имеющий синевато — серый оттенок. Он плавится при температуре 327* С, и хорошо противостоит коррозии. Однако следует отметить, что оксиды свинца являются ядовитыми. Свинец пригоден для литейных работ и изготовления формовых изделий.
Свинец ( эталон)
- Серебро — также относится к цветным, но при этом является еще и драгоценным металлом. Чистое серебро слишком мягкое, и поэтому его неудобно обрабатывать. Для изготовления изделий применяется в виде сплавов с медью.
 Серебряные вставки используются в инкрустациях, в гравировке, чеканке и черни.
Серебряные вставки используются в инкрустациях, в гравировке, чеканке и черни.
Антикварные серебряные изделия
Свойства металлов
Рассмотрим некоторые свойства металлов, влияющие на качество выполнения художественных изделий:
- Ковкость металла — ковкие пластичные металлы требуют большей силы резания, но при этом необходимо учитывать их вязкость. Кусок меди или свинца нужно рубить до конца, а латунь, цинк или сталь можно надколоть зубилом, а после просто сломать. Более твердая латунь при обточке дает гладкую поверхность, в то время как алюминий или медь как бы тянутся за резцом.
- Хрупкость — это способность твердых материалов разрушаться вследствие механического воздействия без заметной пластической деформации. Это свойство противоположно пластичности. Сильно закаленная сталь, а также многие сорта латуни и бронзы являются очень хрупкими, и от сильных ударов раскалываются на куски. Хрупкость металла не всегда является признаком его твердости, например, отливка из цинка хрупкая, но не твердая.
 Закаленный стальной нож одновременно и тверд, и хрупок.
Закаленный стальной нож одновременно и тверд, и хрупок. - Упругость — это свойство металлов восстанавливать свою форму и объем после прекращения действия внешних сил или нагревания, вызвавших деформацию. В большой степени этим свойством обладают специальные сорта стали.
- Плавление при нагревании — способность металла плавиться при нагревании является важным качеством, так как плавление считается одним из самых доступных и дешевых способов получения изделий из металла. Детали огромных машин и маленькие металлические скульптуры изготовляются одинаковым способом.
Если возникает необходимость закалить деталь, и при этом сохранить вязкость металла, мастера используют токи высокой частоты. При этом деталь закаляется в глубину на несколько миллиметров. Однако вся остальная масса металла внутри изделия остается без изменений. И, наконец, металлические детали можно обрабатывать без нагревания — например, способом гравировки и резьбы по металлу.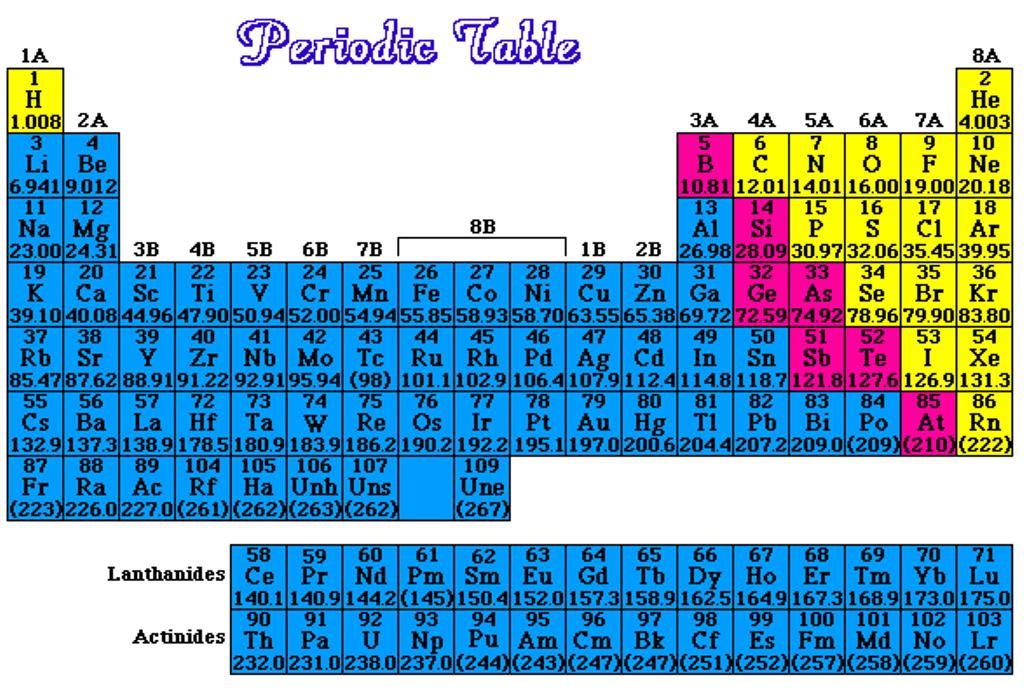
Серебряные изделия
Изучение и использование
Что такое металл знали ещё древние цивилизации. Среди египетских археологических находок, датируемых 3-4 тысячелетиями до нашей эры, были найдены изделия из благородных металлов. Первыми человек открыл золото, медь, серебро, свинец, железо, олово, ртуть. Они служили для изготовления украшений, орудий труда, ритуальных предметов и оружия.
В эпоху Средневековья были обнаружены сурьма, мышьяк, висмут, цинк. Им нередко придавали магические свойства, связывали с космосом, движением планет. Алхимики проводили многочисленные опыты в надежде превратить ртуть в воду или золото. Постепенно число открытий возрастало, и к XXI веку были открыты все известные на сегодняшний день металлы.
Сейчас их применяют практически во всех сферах жизни. Металлы используют для изготовления украшений, техники, кораблей, автомобилей. Из них делают каркасы для строительства зданий, изготовляют мебель, различные мелкие детали.
Отличная электропроводность сделала металл незаменимым для изготовления проводов, именно благодаря ему, мы пользуемся электрическим током.
Как определить металлы в таблице Менделеева
Металлы и неметаллы периодической таблицы
Корпускуляризм
Корпускуляризм — это теория, предложенная Декартом, согласно которой вся материя состоит из мельчайших частиц.
Рене Декарт
Рене Декарт был известным математиком и философом 16-го века, который выдвинул теорию корпускуляризма об атоме.
Полупроводники
Полупроводники — это термин для описания металлоидов, которые способны проводить ток при подаче электрической энергии за счет движения электронов, но измерения проводимости не такие высокие, как у металлов, из-за меньшего количества электронов, несущих заряд, или менее упорядоченной структура.
Ионное соединение
Ионное соединение представляет собой связь, которая образуется между металлами и неметаллами с образованием большой ионной решетки. Атомы водорода под действием большого количества тепла и давления вынуждены объединяться, образуя более крупный атом гелия 9. 0003
0003
Принцип неопределенности
Принцип неопределенности Гейзенберга используется для описания взаимосвязи между импульсом и положением электрона. Где, если точное положение электрона известно, импульс будет неопределенным.
Гейзенберг
Вернер Гейзенберг был немецким физиком, пионером в области квантовой механики. Он разработал принцип неопределенности относительно импульса и положения электрона.
Лепестки
Лепестки относятся к форме электронных волн и области с наибольшей вероятностью, где этот электрон как частица может быть найден.
Принцип исключения Паули
Исключение Паули относится к теории, согласно которой каждый электрон может иметь только уникальный набор из 4 квантовых чисел, и никакие два электрона не могут иметь одинаковые квантовые числа
Квантовые числа
Квантовые числа — это используемый термин описать присвоение чисел электронам как математическую функцию для описания их импульса и энергии.
Модель Бора
Модель Бора относится к трактовке электронов как частиц, вращающихся вокруг ядра.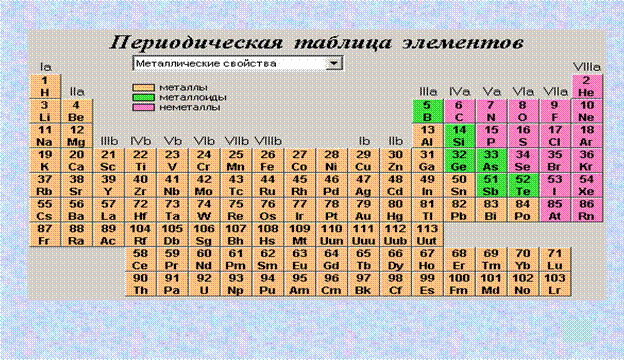
Квантовая механика
Термин квантовая механика относится к уровням энергии и теоретической области физики и химии, где математика используется для объяснения поведения субатомных частиц.
Впадина
Впадина — самая нижняя точка поперечной волны.
Пик
Пик — это самая высокая точка поперечной волны.
Колебательные моды
Колебательные моды — это термин, используемый для описания постоянного движения в молекуле. Обычно это вибрации, вращения и перемещения.
Erwin Schrodinger
Эрвин Шредингер был австрийским физиком, который использовал математические модели для усовершенствования модели Бора об электроне и создал уравнение для предсказания вероятности нахождения электрона в заданном положении.
Щелочной металл
Щелочные металлы, находящиеся в группе 1 периодической таблицы (ранее известной как группа IA), настолько реакционноспособны, что обычно встречаются в природе в сочетании с другими элементами. Щелочные металлы — это блестящие, мягкие, высокореактивные металлы при стандартной температуре и давлении.
Щелочные металлы — это блестящие, мягкие, высокореактивные металлы при стандартной температуре и давлении.
Щелочноземельные металлы
Щелочноземельные металлы являются второй по реакционной способности группой элементов в периодической таблице. Они находятся в группе 2 периодической таблицы (формально известной как группа IIA).
Неизвестные элементы
Неизвестные элементы (или трансактиниды) являются самыми тяжелыми элементами периодической таблицы. Это мейтнерий (Mt, атомный номер 109), дармштадтий (Ds, атомный номер 110), рентгений (Rg, атомный номер 111), нихоний (Nh, атомный номер 113), московий (Mc, атомный номер 115), ливерморий (Lv , атомный номер 116) и теннессин (Ts, атомный номер 117).
Постпереходный металл
Постпереходные металлы находятся между переходными металлами (слева) и металлоидами (справа). К ним относятся алюминий (Al), галлий (Ga), индий (In), таллий (Tl), олово (Sn), свинец (Pb) и висмут (Bi).
Oganesson
Oganesson (Og) — радиоактивный элемент с атомным номером 118 в периодической таблице, его внешний вид полностью неизвестен из-за мизерных количеств, которые он производит. Он находится в группе 18. Он имеет символ Og.
Он находится в группе 18. Он имеет символ Og.
Теннессин
Теннессин (Ts) — радиоактивный элемент с атомным номером 117 в периодической таблице, его внешний вид полностью неизвестен из-за мизерных количеств, которые он производит. Он находится в группе 17. Он имеет символ Ts.
Ливерморий
Ливерморий (Lv) — радиоактивный элемент с атомным номером 116 в периодической таблице, его внешний вид полностью неизвестен из-за мизерных количеств, которые он производит. Он находится в группе 16. Он имеет символ Lv.
Московий
Московий (Mc) — радиоактивный металл с атомным номером 115 в таблице Менделеева, его внешний вид полностью неизвестен из-за незначительных количеств его производства. Он находится в группе 15. Он имеет символ Mc.
Флеровий
Флеровий (Fl) — радиоактивный металл с атомным номером 114 в периодической таблице, его внешний вид полностью неизвестен из-за мизерных количеств его производства. Он находится в группе 14. Он имеет символ Fl.
Нихоний
Нихоний (Nh) — радиоактивный металл с атомным номером 112 в периодической таблице, его внешний вид полностью неизвестен из-за незначительных количеств его производства. Он находится в группе 13. Он имеет символ Nh.
Copernicium
Copernicium (Cr) — радиоактивный металл с атомным номером 112 в таблице Менделеева, его внешний вид полностью неизвестен из-за незначительных количеств его производства. Это переходный металл группы 11. Он имеет символ Rg.
Рентгений
Рентгений (Rg) — радиоактивный металл с атомным номером 111 в периодической таблице, его внешний вид полностью неизвестен из-за мизерных количеств его производства. Это переходный металл группы 11. Он имеет символ Rg.
Darmstadtium
Darmstadtium (Ds) — радиоактивный металл с атомным номером 110 в таблице Менделеева, его внешний вид полностью неизвестен из-за незначительных количеств его производства. Это переходный металл группы 10. Он имеет символ Ds 9.0003
Мейтнерий
Мейтнерий (Mt) — радиоактивный металл с атомным номером 109 в таблице Менделеева, его внешний вид полностью неизвестен из-за незначительных количеств его производства. Это переходный металл группы 9. Он имеет символ Mt
Это переходный металл группы 9. Он имеет символ Mt
Хассий
Хассий (Hs) — радиоактивный металл с атомным номером 108 в периодической таблице, его внешний вид полностью неизвестен из-за ничтожных количеств производится из него. Это переходный металл группы 8. Он имеет символ Hs.
Борий
Борий (Bh) — радиоактивный металл с атомным номером 107 в периодической таблице, его внешний вид полностью неизвестен из-за незначительных количеств его производства. Это переходный металл группы 7. Он имеет символ Bh.
Сиборгий
Сиборгий (Sg) — радиоактивный металл с атомным номером 106 в периодической таблице, его внешний вид полностью неизвестен из-за мизерных количеств его производства. Это переходный металл группы 6. Он имеет символ Sg.
Дубний
Дубний (Db) — радиоактивный металл с атомным номером 105 в периодической таблице, его внешний вид полностью неизвестен из-за незначительных количеств его производства. Это переходный металл группы 5. Он имеет символ Db.
Он имеет символ Db.
Резерфордий
Резерфордий (Rf) — радиоактивный металл с атомным номером 104 в таблице Менделеева, его внешний вид полностью неизвестен из-за незначительных количеств его производства. Это переходный металл группы 4. Он имеет символ Rf.
Lawrencium
Lawrencium (Lr) — серебристо-белый радиоактивный металл с атомным номером 103 в периодической таблице. Это актиноидный металл с символом Lr.
Нобелий
Нобелий (No) — радиоактивный металл с атомным номером 102 в таблице Менделеева, его внешний вид полностью неизвестен из-за незначительных количеств его производства. Это актиноидный металл с символом №
Менделевий
Менделевий (Md) — радиоактивный металл с атомным номером 101 в таблице Менделеева, его внешний вид полностью неизвестен из-за незначительных количеств его производства. Это актиноидный металл с символом Md. 9.0003
Фермий
Фермий (Fm) — серебристо-белый радиоактивный металл с атомным номером 100 в периодической таблице. Это актиноидный металл с символом Fm.
Это актиноидный металл с символом Fm.
Эйнштейний
Эйнштейний (Es) — серебристо-белый радиоактивный металл с атомным номером 99 в периодической таблице. Это актиноидный металл с символом Es.
Калифорний
Калифорний (Cf) — серебристо-белый радиоактивный металл с атомным номером 98 в периодической таблице. Это актиноидный металл с символом Cf.
Берклий
Берклий (Bk) — серебристый радиоактивный металл, имеющий атомный номер 97 в периодической таблице. Это актиноидный металл с символом Bk.
Кюрий
Кюрий (Cm) — серебристо-белый радиоактивный металл с атомным номером 96 в периодической таблице. Это актиноидный металл с символом Cm.
Америций
Америций (Am) представляет собой серебристый радиоактивный металл с атомным номером 95 в периодической таблице. Это актиноидный металл с символом Am.
Плутоний
Плутоний (Pu) представляет собой серебристый радиоактивный металл, имеющий атомный номер 94 в периодической таблице. Это актиноидный металл с символом Pu.
Это актиноидный металл с символом Pu.
Нептуний
Нептуний (Np) — серебристый радиоактивный металл с атомным номером 93 в периодической таблице. Это актиноидный металл с символом Np.
Протактиний
Протактиний (Па) представляет собой блестящий серебристый радиоактивный металл с атомным номером 91 в периодической таблице. Это актиноидный металл с символом Pa.
Торий
Торий (Th) — серебристо-белый радиоактивный металл с атомным номером 90 в периодической таблице. Это актиноидный металл с символом Th.
Актиний
Актиний (Ac) представляет собой серебристый радиоактивный металл с атомным номером 89 в периодической таблице. Это актиноидный металл с символом Ac.
Радий
Радий (Ra) — металл серебристо-белого цвета, имеющий атомный номер 88 в периодической таблице. Это щелочноземельный металл с символом Ra, расположенный во 2-й группе периодической таблицы.
Франций
Франций (Fr) считается металлом серого цвета, имеющим атомный номер 87 в периодической таблице. Это щелочной металл с символом Fr, расположенный в группе 1 периодической таблицы.
Это щелочной металл с символом Fr, расположенный в группе 1 периодической таблицы.
Радон
Радон (Rn) представляет собой бесцветный радиоактивный газ без запаха, неметалл, имеющий атомный номер 86 в периодической таблице в 18-й группе. Он имеет символ Rn.
Астатин
Астатин (At) — радиоактивный неметалл, имеющий атомный номер 85 в периодической таблице в 17-й группе. Он имеет символ At.
Полоний
Полоний (Po) — серебристо-серый металл с атомным номером 84 в периодической таблице в 16-й группе. Он имеет символ Po.
Висмут
Висмут (Bi) — твердый стальной серый металл, имеющий атомный номер 83 в периодической таблице в 15-й группе. Он имеет символ Bi.
Свинец
Свинец (Pb) — мягкий серый металл, имеющий атомный номер 82 в периодической таблице в 14-й группе. Он имеет символ Pb.
Таллий
Таллий (Tl) — мягкий серый металл, имеющий атомный номер 81 в периодической таблице в 13-й группе. Он имеет символ Tl.
Ртуть
Ртуть (Hg) представляет собой жидкий металл серебристого цвета, имеющий атомный номер 80 в периодической таблице. Это переходный металл группы 12. Он имеет символ Hg.
Золото
Золото (Au) — это мягкий металл золотистого цвета, имеющий атомный номер 79 в периодической таблице. Это переходный металл группы 11. Он имеет символ Au.
Платина
Платина (Pt) — тяжелый белый металл с атомным номером 78 в периодической таблице. Это переходный металл группы 10. Он имеет символ Pt.
Иридий
Иридий (Ir) — тяжелый белый металл с атомным номером 77 в периодической таблице. Это переходный металл группы 9. Он имеет символ Ir.
Осмий
Осмий (Os) представляет собой твердый мелкий черный порошок или сине-белый металл с атомным номером 76 в периодической таблице. Это переходный металл группы 8. Он имеет символ Os.
Рений
Рений (Re) — металл серебристо-белого цвета, имеющий атомный номер 75 в периодической таблице. Это переходный металл группы 7. Он имеет символ Re.
Это переходный металл группы 7. Он имеет символ Re.
Вольфрам
Вольфрам (W) — металл серо-стального цвета, имеющий атомный номер 74 в периодической таблице. Это переходный металл группы 6. Он имеет символ W.
Тантал
Тантал (Ta) — металл серого цвета с атомным номером 73 в периодической таблице. Это переходный металл группы 5. Он имеет символ Та.
Гафний
Гафний (Hf) — металл серебристого цвета с атомным номером 72 в периодической таблице. Это переходный металл группы 4. Он имеет символ Hf.
Лютеций
Лютеций (Lu) — металл серебристо-белого цвета, имеющий атомный номер 71 в периодической таблице. Это лантаноидный металл. Он имеет символ Лу.
Иттербий
Иттербий (Yb) представляет собой металл серебристого цвета с атомным номером 70 в периодической таблице. Это лантаноидный металл. Он имеет символ Yb.
Тулий
Тулий (Tm) представляет собой металл серебристого цвета с атомным номером 69 в периодической таблице. Это лантаноидный металл. Он имеет обозначение Tm.
Это лантаноидный металл. Он имеет обозначение Tm.
Эрбий
Эрбий (Er) — металл серебристого цвета, имеющий атомный номер 68 в периодической таблице. Это лантаноидный металл. Он имеет символ Er.
Гольмий
Гольмий (Но) — металл серебристого цвета, имеющий атомный номер 67 в периодической таблице. Это лантаноидный металл. Он имеет символ Хо.
Диспрозий
Диспрозий (Dy) представляет собой серебристый металл с атомным номером 66 в периодической таблице. Это лантаноидный металл. Он имеет символ Dy.
Тербий
Тербий (Tb) представляет собой металл серебристо-серого цвета, имеющий атомный номер 65 в периодической таблице. Это лантаноидный металл. Он имеет символ Tb.
Гадолиний
Гадолиний (Gd) — металл серебристо-белого цвета, имеющий атомный номер 64 в периодической таблице. Это лантаноидный металл. Он имеет символ Gd.
Европий
Европий (Eu) — металл серебристо-белого цвета, имеющий атомный номер 63 в периодической таблице.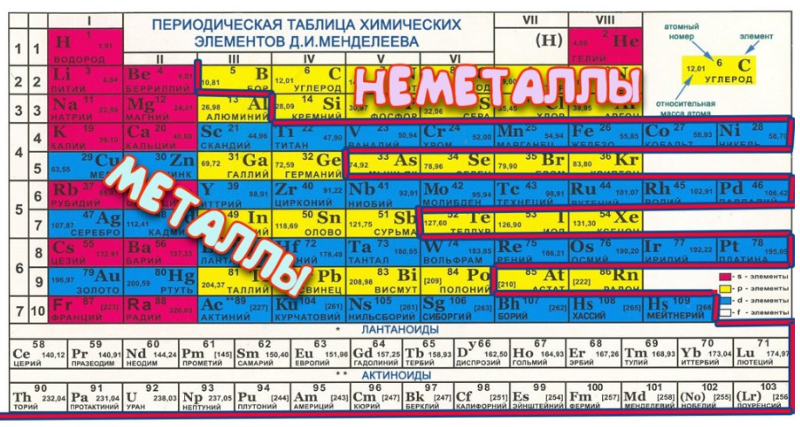 Это лантаноидный металл. Он имеет символ Eu.
Это лантаноидный металл. Он имеет символ Eu.
Самарий
Самарий (Sm) представляет собой металл серебристого цвета с атомным номером 62 в периодической таблице. Это лантаноидный металл. Он имеет символ Sm.
Прометий
Прометий (Pm) — редкий металл с атомным номером 61 в периодической таблице. Это лантаноидный металл. Он имеет символ Pm.
Неодим
Неодим (Nd) — металл серебристо-белого цвета, имеющий атомный номер 60 в периодической таблице. Это лантаноидный металл. Он имеет символ Nd.
Празеодим
Празеодим (Pr) представляет собой серебристо-белый металл с атомным номером 59 в периодической таблице. Это лантаноидный металл. Он имеет обозначение Pr.
Церий
Церий (Ce) представляет собой металл серо-железного цвета, имеющий атомный номер 58 в периодической таблице. Это лантаноидный металл. Он имеет символ Ce.
Лантан
Лантан (La) — мягкий серебристо-белый металл с атомным номером 57 в периодической таблице. Это лантаноидный металл. Имеет обозначение La.
Это лантаноидный металл. Имеет обозначение La.
Барий
Барий (Ba) — мягкий серебристо-белый металл с атомным номером 56 в периодической таблице. Это щелочноземельный металл, расположенный во 2-й группе периодической таблицы. он имеет символ Ba.
Цезий
Цезий (Cs) — мягкий металл серого цвета, имеющий атомный номер 55 в периодической таблице. Это щелочной металл и находится в группе 1 периодической таблицы. он имеет символ Cs.
Ксенон
Ксенон (Хе) существует в виде бесцветного газа без запаха и химически инертен. Он имеет атомный номер 54 в периодической таблице и принадлежит к группе 18, Благородные газы. Это неметалл с символом Xe.
Йод
Йод (I) представляет собой пурпурно-серый твердый неметалл. Он имеет атомный номер 53 в периодической таблице. Он расположен в группе 17, галогены. Он имеет символ I.
Теллур
Теллур (Te) — серебристо-белый полуметалл с атомным номером 52 в периодической таблице. Он расположен в 16 группе периодической таблицы. Он имеет символ Те.
Он имеет символ Те.
Сурьма
Сурьма (Sb) представляет собой твердый хрупкий серебристо-белый полуметалл с атомным номером 51 в периодической таблице. Он расположен в 15 группе периодической таблицы. Он имеет символ Sb.
Олово
Олово (Sn) — серебристо-белый металл с атомным номером 50 в периодической таблице. Он расположен в 14 группе периодической таблицы. Он имеет обозначение Sn.
Индий
Индий (In) — серебристо-белый металл с атомным номером 49 в периодической таблице. Он расположен в 13 группе периодической таблицы. Он имеет символ В.
Кадмий
Кадмий (Cd) — бело-голубой металл с атомным номером 48 в периодической таблице. Это переходный металл, расположенный в 12-й группе периодической таблицы. Он имеет обозначение Cd.
Серебро
Серебро (Ag) — металл серебра, имеющий атомный номер 47 в периодической таблице. Это переходный металл, расположенный в 11-й группе периодической таблицы. Он имеет символ Ag.
Палладий
Палладий (Pd) — серебристо-белый металл с атомным номером 46 в периодической таблице. Это переходный металл, расположенный в 10-й группе периодической таблицы. Он имеет обозначение Pd.
Это переходный металл, расположенный в 10-й группе периодической таблицы. Он имеет обозначение Pd.
Родий
Родий (Rh) — хрупкий серебристо-белый металл с атомным номером 45 в периодической таблице. Это переходный металл, расположенный в группе 9.периодической таблицы. Он имеет обозначение Rh.
Рутений
Рутений (Ru) представляет собой хрупкий металл серебристо-серого цвета, имеющий атомный номер 44 в периодической таблице. Это переходный металл, расположенный в 8-й группе периодической таблицы. Имеет обозначение Ru.
Технеций
Технеций (Tc) представляет собой серебристо-серый металл с атомным номером 43 в периодической таблице. Это переходный металл, расположенный в 7-й группе периодической таблицы. Он имеет символ Tc.
Молибден
Молибден (Мо) — серебристо-белый металл с атомным номером 42 в периодической таблице. Это переходный металл, расположенный в 6-й группе периодической таблицы. Он имеет обозначение Mb.
Ниобий
Ниобий (Nb) — блестящий белый металл с атомным номером 41 в периодической таблице. Это переходный металл, расположенный в группе 5 периодической таблицы. Он имеет символ Nb.
Это переходный металл, расположенный в группе 5 периодической таблицы. Он имеет символ Nb.
Цирконий
Цирконий (Zr) представляет собой серо-белый металл с атомным номером 40 в периодической таблице. Это переходный металл, расположенный в 4-й группе периодической таблицы. Он имеет символ Zr.
Иттрий
Иттрий (Y) — серебристый металл с атомным номером 39 в периодической таблице. Это переходный металл, расположенный в группе 3 периодической таблицы. Он имеет символ Y.
групп и периодов Периодической таблицы ——————– Металлы, неметаллы и металлоиды ———- ——————
Группы и периоды в Периодической таблице
Периодическая таблица химических элементов. Столбцы представляют группы, а строки представляют периоды.
Группа
В химии группа (также известная как семейство ) представляет собой столбец элементов в периодической таблице химических элементов. В периодической таблице 18 пронумерованных групп, но столбцы f-блока (между группами 2 и 3) не нумеруются. Элементы в группе имеют схожие физические или химические характеристики самых внешних электронных оболочек своих атомов (т. е. одинаковый заряд ядра), поскольку большинство химических свойств определяется орбитальным положением самого внешнего электрона. Существует три системы нумерации групп. Современная нумерация группа 1 – группа 18
В периодической таблице 18 пронумерованных групп, но столбцы f-блока (между группами 2 и 3) не нумеруются. Элементы в группе имеют схожие физические или химические характеристики самых внешних электронных оболочек своих атомов (т. е. одинаковый заряд ядра), поскольку большинство химических свойств определяется орбитальным положением самого внешнего электрона. Существует три системы нумерации групп. Современная нумерация группа 1 – группа 18
Период
Период – это горизонтальная строка в периодической таблице. Хотя группы обычно имеют более значимые периодические тренды, есть регионы, где горизонтальные тренды более значимы, чем вертикальные групповые тренды, такие как f-блок, где лантаниды и актиниды формируют два существенных горизонтальных ряда элементов.
Элементы того же периода демонстрируют тенденции изменения атомного радиуса, энергии ионизации, сродства к электрону и электроотрицательности. При движении слева направо по периоду радиус атома обычно уменьшается. Это происходит потому, что каждый последующий элемент имеет добавленный протон и электрон, которые заставляют электрон приближаться к ядру. Это уменьшение атомного радиуса также приводит к увеличению энергии ионизации при движении слева направо по периоду. Чем прочнее связан элемент, тем больше энергии требуется для отрыва электрона. Электроотрицательность увеличивается так же, как энергия ионизации, из-за притяжения, оказываемого на электроны ядром. Сродство к электрону также показывает небольшую тенденцию в течение периода. Металлы (левая часть точки) обычно имеют более низкое сродство к электрону, чем неметаллы (правая часть точки), за исключением инертных газов.
В соответствии с их общими физическими и химическими свойствами элементы можно разделить на основные категории металлы, металлоиды и неметаллы .
Металлы
Большинство элементов — это металлы. Металлы обладают следующими свойствами:
- обычно твердые при комнатной температуре (исключением является ртуть)
- сильный блеск (блестящий)
- металлический внешний вид
- хорошие проводники тепла и электричества
- ковкий (можно согнуть и растолочь в тонкие листы)
- пластичный (можно вытянуть в проволоку)
- корродирует или окисляется на воздухе и в морской воде
- обычно плотный (исключения включают литий, калий и натрий)
- может имеют очень высокую температуру плавления
- легко теряют электроны
Металлоиды или полуметаллы
Металлоиды обладают некоторыми свойствами металлов и некоторыми неметаллическими характеристиками.
- тусклый или блестящий
- обычно проводят тепло и электричество, хотя и не так хорошо, как металлы
- часто являются хорошими полупроводниками
- часто существуют в нескольких формах
- часто пластичны
- часто пластичны
- могут приобретать или терять электроны в реакциях 78
- тусклый вид
- обычно хрупкие
- плохие проводники тепла и электричества
- обычно менее плотные по сравнению с металлами
- обычно имеют низкую температуру плавления твердых тел по сравнению с металлами
- склонны приобретать электроны в химических реакциях
Неметаллы
Свойства неметаллов сильно отличаются от свойств металлов. Неметаллы обладают некоторыми или всеми из следующих характеристик:
Неметаллы обладают некоторыми или всеми из следующих характеристик:
неметаллы могут быть дополнительно классифицированы на подкатегории, которые показывают градацию от металлических до неметаллических свойств, если двигаться слева направо в рядах. Металлы подразделяются на высокореакционноспособные щелочные металлы, менее реакционноспособные щелочноземельные металлы, лантаноиды и актиноиды, архетипические переходные металлы и заканчиваются физически и химически слабыми постпереходными металлами. Неметаллы просто подразделяются на многоатомные неметаллы , которые, будучи ближайшими к металлоидам, проявляют некоторый зарождающийся металлический характер; двухатомные неметаллы, которые по существу неметаллы; и одноатомные благородные газы, неметаллические и почти полностью инертные.
Металлические настенные рисунки с периодическими таблицами / Металлические гравюры с периодическими таблицами
Результаты: 105
Результаты: 105
Периодическая таблица элементов металлической печати
76 долларов
61 доллар
Периодическая таблица элементов Green Metal Print
$81
65 долларов
Периодическая таблица элементов в черной металлической печати
81$
65$
Периодическая таблица элементов металлической печати
81$
65$
Периодическая таблица элементов – металлическая печать
81$
65$
Периодическая таблица элементов – металлическая печать
81$
65$
Фото со стока – Periodic Table Of Elements Metal Print
81 $
65 $
Периодическая таблица химических элементов металлической печати
81$
65$
Периодическая таблица рок-музыки Metal Print
71$
57$
Периодическая таблица элементов, черный Metal Print
86 долларов
69 долларов
Периодическая таблица элементов металлической печати
97 долларов
78 долларов
Батмантиум Элемент Периодической Таблицы Диаграмма Ботаник Химия Студент Супергерой Юмор Металл Печать
$76
61$
Периодическая таблица элементов Металл Печать
86 долларов
69 долларов
Tableau Periodiques Периодическая Таблица Элементов Старинные Диаграммы Сепия Красный Оттенок Металла Печать
71$
57$
Tableau Periodiques Периодическая Таблица Элементов Старинные Диаграммы Сепия Металл Печать
71$
57$
Научный эксперимент в научно-исследовательской лаборатории Metal Print
101$
81$
Металлическая печать с редкоземельными металлами
101 доллар
81 доллар
Металлическая печать с редкоземельными металлами
101 доллар
81 доллар
Периодическая таблица жанров фильмов Metal Print
71$
57$
Доктор Кто Периодическая таблица элементов металлическая печать
71$
57$
Tableau Periodiques Периодическая Таблица Элементов Старинные Диаграммы Серебряный Металл Печать
71$
57$
Периодическая таблица элементов. Винтажная диаграмма. Теплая металлическая печать.
Винтажная диаграмма. Теплая металлическая печать.
71$
57$
В твоих руках металлический принт
109 долларов
87 долларов
Мужчина сдает онлайн-экзамен по металлу
92 доллара
74 доллара
Периодическая Таблица Элементов Старинные Диаграммы Науки Химии Учитель Студент Школы Металла Печать
71$
57$
Tableau Periodiques Периодическая Таблица Элементов Старинные Диаграммы Синий Металл Печать
71$
57$
Периодическая таблица элементов металлической печати
86 долларов
69 долларов
Металлическая печать периодической таблицы
106 долларов
85 долларов
Металлическая печать периодической таблицы
106 долларов
85 долларов
Периодическая таблица элементов Vintage Chart Black Metal Print
71$
57$
Периодическая Таблица Элементов Старинные Диаграммы Науки Учитель Химии Студент Школы Черный Металл Печать
71$
57$
Япония Японская периодическая таблица элементов. Винтажная диаграмма. Серебряный металлический принт.
Винтажная диаграмма. Серебряный металлический принт.
71$
57$
Периодическая таблица элементов. Винтажная диаграмма. Теплая винтажная металлическая печать.
81$
65$
Периодическая таблица элементов. Винтажная диаграмма. Черная ретро-металлическая печать.
81$
65$
Подарки учителю естествознания, Компьютерщик, Ботаник Периодическая таблица элементов Старинный металлический принт
71$
57$
Подарки ученого, Подарки науки Периодическая таблица элементов Металлическая печать
71$
57$
Подарки науки, Подарки химии Периодическая таблица элементов Металлическая печать
71$
57$
Подарки для ботаников, Подарки для гиков Периодическая таблица элементов Старинный металлический принт
71$
57$
Tabla Periodica De Los Elementos Периодическая таблица элементов Винтажная диаграмма Серебряный металлический принт
71$
57$
Редкоземельные металлы, концептуальное изображение металлической печати
$101
$81
Редкоземельные металлы, концептуальное изображение металлической печати
101 доллар
81 доллар
Редкоземельные металлы, концептуальное изображение металлической печати
101 доллар
81 доллар
Фон круга математического линейного математического образования с геометрическим металлическим принтом
81$
65$
Футболка Ah The Element of Surprise в подарок для любителей науки Футболка унисекс с коротким рукавом с металлическим принтом
71$
57$
Футболка Ah The Element of Surprise в подарок для любителей науки Футболка унисекс с коротким рукавом Черный металлический принт
66 долларов
53 доллара
Диаграмма на металлической доске для печати
86 долларов
69 долларов
Протопериодическая таблица, металлическая гравюра 1760 г.
127 долларов
102 доллара
Протопериодическая таблица, металлическая гравюра 1760 г.
127 долларов
102 доллара
Периодическая таблица эмоций металлическая печать
71$
57$
Карта звездного неба и созвездий A3 Metal Print
86 долларов
69 долларов
Звезда и созвездие карта неба B1 металлический принт
81$
65$
Звезда и созвездие карта неба B2 металлический принт
81$
65$
научная сука металлический принт
66 долларов
53 доллара
Сарказм Элементы Юмора Периодическая Таблица Элементов Винтажная Диаграмма Теплая Металлическая Печать
71$
57$
Периодическая таблица элементов Vintage Chart Metal Print
66 долларов
53 доллара
Периодическая таблица элементов Vintage Chart Metal Print
66 долларов
53 доллара
Периодическая таблица элементов Vintage Chart Metal Print
66 долларов
53 доллара
Дилитиевый металлический принт
66 долларов
53 доллара
Изношенный дебоширский металлический принт
72 доллара
58 долларов
Элемент кобальт, в периодической таблице элементов, символ элемента Co Metal Print
64 доллара
51 доллар
Элемент никель, в периодической таблице элементов, символ элемента Ni Metal Print
64 доллара
51 доллар
Элемент меди, в периодической таблице элементов, символ элемента Cu Metal Print
64 доллара
51 доллар
Элемент железа, в периодической таблице элементов, символ элемента Fe Metal Print
64 доллара
51 доллар
Уран, химический элемент периодической таблицы элементов Metal Print
64 доллара
51 доллар
Плутоний, химический элемент периодической таблицы элементов Metal Print
64 доллара
51 доллар
Золото, элемент и драгоценный металл с символом Au в периодической таблице Metal Print
64 доллара
51 доллар
Серебро, элемент и драгоценный металл с символом Ag в периодической таблице Metal Print
64 доллара
51 доллар
Биткойн Периодическая таблица Криптовалюта Биткойн Рубашка Металл Печать
66 $
53 $
Next
Wall Art
0003
Home Decor
Throw PillowsFleece BlanketsDuvet CoversShower CurtainsBath TowelsHand TowelsCoffee MugsOrnaments
Apparel
Men’s T-ShirtsMen’s Tank TopsWomen’s T-ShirtsWomen’s Tank TopsLong Sleeve T-ShirtsSweatshirtsKid’s T-ShirtsBaby OnesiesFace Masks
Phone Cases
iPhone CasesGalaxy CasesPortable Battery Chargers
Канцелярские товары
Поздравительные открыткиНоутбукиНаклейки
Стиль жизни
Коврики для йогиСумкиСумки для выходных днейСумки Carry-AllCouchКофейные кружкиГоловоломки
Beach
Beach Totelssround Beach Totelsweekender Tote Bagscarry-All Couckesportable Bagsweekend
Все Картины Фотографии Чертежи Цифровое искусство Смешанная техника
Репродукции из цельного металла
Мы отправили миллионы товаров по всему миру для более чем 1 миллиона художников.

