Таблица П. Соединения элементов III группы
Между положением в периодической таблице легких элементов и их химическими свойствами не всегда обнаруживается закономерная взаимосвязь. Например, бериллий (II группа) во многих отношениях напоминает алюминий (группа ША) много общего также между бором и кремнием. Степени окисления этих элементов соответствуют номерам их групп, но, судя по свойствам образуемых ими соединений, по кислотно-основным характеристикам этих элементов и их физическим свойствам, между ними существует необычная для периодической системы диагональная связь. Причиной этого является сходство так называемых ионных потенциалов у диагонально расположенных в периодической таблице пар элементов. Ионным потенциалом (не пу- [c.105] Разделив все элементы иа периоды и располагая одн,н период под другим так, чтобы сходные ио свойствам и типу образуемых соединений элементы приходились друг под другом, Менделеев составил таблицу, названную им периодической системой элементов по группам и рядам.

Приведенная здесь таблица содержит данные о стандартных энтальпиях (АЯ”) и свободных энергиях (AG°) образования соединений из элементов в их стандартных состояниях, выраженные в килоджоулях на моль, а также термодинамические (вычисленные из третьего закона), или абсолютные, энтропии (S”) соединений в джоулях на кельвин на моль все эти данные относятся к температуре 298 К. Фазовое состояние соединения указывается следующим образом (г.)-газ, (ж.)-жидкость, (тв.)-твердое вещество, (водн.) – водный раствор в некоторых случаях указывается также кристаллическая форма твердого вещества. Соединения расположены в таблице по номерам групп главного элемента, при установлении которого металлам отдается предпочтение перед неметаллами, а О и Н рассматриваются как наименее важные элементы.
Периодическое изменение свойств элементов представлено в периодической таблице современного вида. При расположении элементов в порядке возрастания атомных номеров и группировке на основании общих свойств они образуют семь горизонтальных рядов, называемых периодами. Каждый вертикальный столбец – группа элементов – содержит элементы с близкими свойствами. Группа лития (Ы), состоит, например, из шести элементов. Все эти элементы – крайне реакционноспособные металлы, образующие хлориды и оксиды общей формулы ЭС1 и Э2О соответственно. Так же, как хлорид натрия, все хлориды и оксиды этих элементов — ионные соединения. В противоположность этому группа гелия, расположенная по правому краю таблицы, состоит из крайне инертных элементов (к настоящему времени известны соединения только ксенона и криптона). Элементы группы гелия известны под названием благородные газы.
.jpg) Кислоты — это соединения, содержащие обычно водород, кислород и еще какой-нибудь элемент. Характерные свойства кислот обусловлены ионом водорода, т. е. атомом водорода, несущим единичный положительный заряд. Основания — это соединения водорода и кислорода с каким-либо другим элементом, в которых кислород и водород соединяются и образуют гидроксильную группу. Гидроксильная группа несет единичный отрицательный заряд и обусловливает характерные свойства оснований. Свойство образовывать кислоту или основание определяется положением элемента в периодической таблице. Например, элементы группы I таблицы Менделеева образуют сильные основания, элементы группы II— умеренно-сильные основания, элементы групп Ш и IV могут образовывать слабо основные или слабо кислые соединения, а элементы групп V, VI и VII дают сильные кислоты, например фосфорную, серную или соляную. Вообще элементы, расположенные в левой части таблицы, образуют сильные основания, расположенные в правой части — сильные кислоты, а находящиеся между ними — либо слабые кислоты, либо слабые основания.
Кислоты — это соединения, содержащие обычно водород, кислород и еще какой-нибудь элемент. Характерные свойства кислот обусловлены ионом водорода, т. е. атомом водорода, несущим единичный положительный заряд. Основания — это соединения водорода и кислорода с каким-либо другим элементом, в которых кислород и водород соединяются и образуют гидроксильную группу. Гидроксильная группа несет единичный отрицательный заряд и обусловливает характерные свойства оснований. Свойство образовывать кислоту или основание определяется положением элемента в периодической таблице. Например, элементы группы I таблицы Менделеева образуют сильные основания, элементы группы II— умеренно-сильные основания, элементы групп Ш и IV могут образовывать слабо основные или слабо кислые соединения, а элементы групп V, VI и VII дают сильные кислоты, например фосфорную, серную или соляную. Вообще элементы, расположенные в левой части таблицы, образуют сильные основания, расположенные в правой части — сильные кислоты, а находящиеся между ними — либо слабые кислоты, либо слабые основания.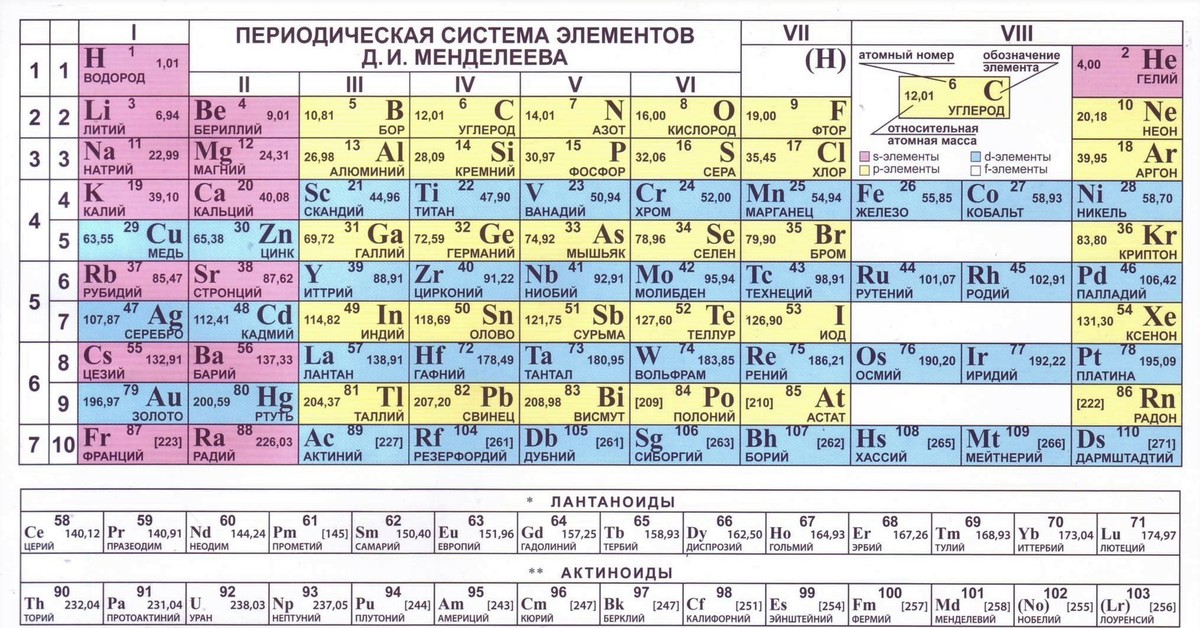
Расположение соединений. В таблице соединения расположены в алфавитном порядке названий элементов. Соединения аммония выделены в самостоятельную группу. [c.10]
В настоящее время изучается обширная группа полупроводниковых материалов, представляющих собой химические (большей частью бинарные ) соединения. Интересно отметить, что среди этих соединений хорошими проводниковыми свойствами обладают соединения элементов, равноотстоящих от середины таблицы Менделеева, например вещества состава A i , где А — элемент III группы, а В — элемент V группы. Примеры полупроводников подобного рода фосфиды галлия и индия (GaP, InP), арсениды тех же метал-
Развитие химии в период творческой деятельности Д. И. Менделеева привело ученого к выводу, что свойства химических элементов определяются их атомной массой, т. е. величиной, характеризующей относительную массу атома. Поэтому в основу систематики элементов он положил именно атомный вес, как фактор, от которого зависят физические и химические свойства элементов. Д. И. Менделеев сформулировал периодический закон так свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величины атомных весов элементов . Вслед за открытием закона Д. И. Менделеев опубликовал периодическую систему элементов, в которой вертикальные ряды сходных элементов назвал группами, а горизонтальные ряды, в пределах которых закономерно изменяются свойства элементов от типичного металла до типичного неметалла,— периодами. Современная периодическая система химических элементов Д. И. Менделеева состоит из семи периодов и восьми групп и содержит 105 элементов. Порядковый номер элемента в периодической системе не только определяет его положение в таблице, но и отражает важнейшее свойство атомов — величину заряда их ядер. Поэтому периодический закон Д. И. Менделеева в настоящее время формулируется так свойства элементов и образуемых ими простых и сложных веществ находятся в периодической зависимости от заряда ядер атомов элементов.
Поэтому в основу систематики элементов он положил именно атомный вес, как фактор, от которого зависят физические и химические свойства элементов. Д. И. Менделеев сформулировал периодический закон так свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величины атомных весов элементов . Вслед за открытием закона Д. И. Менделеев опубликовал периодическую систему элементов, в которой вертикальные ряды сходных элементов назвал группами, а горизонтальные ряды, в пределах которых закономерно изменяются свойства элементов от типичного металла до типичного неметалла,— периодами. Современная периодическая система химических элементов Д. И. Менделеева состоит из семи периодов и восьми групп и содержит 105 элементов. Порядковый номер элемента в периодической системе не только определяет его положение в таблице, но и отражает важнейшее свойство атомов — величину заряда их ядер. Поэтому периодический закон Д. И. Менделеева в настоящее время формулируется так свойства элементов и образуемых ими простых и сложных веществ находятся в периодической зависимости от заряда ядер атомов элементов.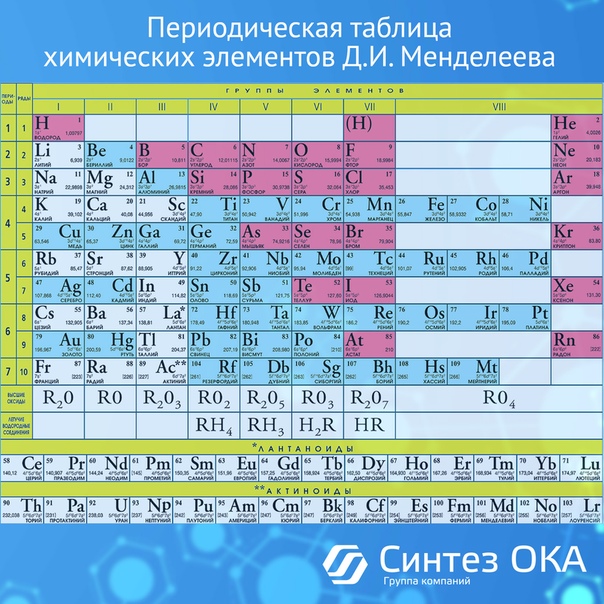
Общие формулы водородных соединений по группам периодической системы химических элементов приведены в таблице 31. [c.137]
Колебательные спектры (главным образом ИК-) известны для достаточно широкого круга соединений элементов главной и побочной подгрупп 1-1У фупп Периодической таблицы, а именно для Л-, N3-, К-солей гидропероксидов для магний-, цинк-, кадмий-, ртутьсодержащих пероксидов для пероксидных соединений алюминия,таллия и таллия, а также для органических пероксидов элементов IV группы — кремния, германия, олова, свинца и титана (литературу см. в [23], а также в 138-141]). В табл. 2.54 приведены частоты наиболее характерных поглощений некоторых элементоорганических пероксидных соединений.

Разработанная систематика представлена в сокращенном виде в табл. 1. Первичным элементом ее является каталитическая система реакция — катализатор. Совокупность таких систем, включающая данную реакцию и ряд однотипных катализаторов этой реакции, образует каталитическую серию. Однотипные серии, состоящие из сходных реакций, объединяются в каталитические типы по признаку сходства рядов каталитической активности и, следовательно, оптимальных катализаторов реакций, относящихся к данным сериям. Совокупности каталитических типов охватываются каталитическими подклассами по следующему принципу оптимальные катализаторы реакций данного подкласса содержат элементы или соединения элементов, которые принадлежат к одним и тем же группам таблицы Менделеева. Данные подклассы в сумме составляют единый класс газовых гетерогенно-каталитических процессов с участием Оа-
В каждом разделе молекулы располагаются в ряд от соединений щелочных металлов до соединений восьмой группы. При этом формулы молекул записываются согласно химической традиции. Соединения элементов одной группы внутри раздела сведены в отдельную таблицу. Внутри таблицы расположены сперва соединения главной группы, затем побочной, в порядке, которому следуют элементы в периодической системе элементов Д. И, Менделеева, Мы предпочли естественный для химика порядок расположения материала в таблицах алфавитному порядку, так как в первом случае резко проступает связь между
При этом формулы молекул записываются согласно химической традиции. Соединения элементов одной группы внутри раздела сведены в отдельную таблицу. Внутри таблицы расположены сперва соединения главной группы, затем побочной, в порядке, которому следуют элементы в периодической системе элементов Д. И, Менделеева, Мы предпочли естественный для химика порядок расположения материала в таблицах алфавитному порядку, так как в первом случае резко проступает связь между
 В промышленных масштабах кислород также получают одновременно с водородом в нроцессе электролиза воды. Некоторые свойства кислорода и родственных ему элементов приведены в табл. 7.6. Значения энтальпии образования соединений кислорода указаны в табл. 7.1 и в других таблицах, а соответствующие величины для соединений элементов группы кислорода приведены в табл. 7.7. [c.195]
В промышленных масштабах кислород также получают одновременно с водородом в нроцессе электролиза воды. Некоторые свойства кислорода и родственных ему элементов приведены в табл. 7.6. Значения энтальпии образования соединений кислорода указаны в табл. 7.1 и в других таблицах, а соответствующие величины для соединений элементов группы кислорода приведены в табл. 7.7. [c.195] VI групп, примыкающие к диагонали бор — астат,— типичные полупроводники (т. е. их электрическая проводимость с повышением температуры увеличивается, а не уменьшается). Характерная черта этих элементов — образование амфотерных гидроксидов (с. 151). Наиболее многочисленны d-металлы. В периодической таблице химических элементов Д. И. Менделеева они расположены между S- и р-элементами и получили название переходных металлов. У атомов d-элементов происходит достройка d-орбиталей. Каждое семейство состоит из десяти d-элементов. Известны четыре d-семейства 3d, 4d, 5d, и 6d. Кроме скандия и цинка, все переходные металлы могут иметь несколько степеней окисления. Максимально возможная степень окисления d-металлов +8 (у осмия, например, OsOj). С ростом порядкового номера максимальная степень окисления возрастает от III группы до первого элемента VIII группы, а затем убывает. Эти элементы — типичные металлы. Химия изоэлектронных соединений d-элементов весьма похожа. Элементы разных периодов с аналогичной электронной структурой d-слоев образуют побочные подгруппы периодической системы (например, медь — серебро — золото, цинк — кадмий — ртуть и т. п.). Самая характерная особенность d-элементов — исключительная способность к комплексообра-зованию. Этим они резко отличаются от непереходных элементов. Химию комплексных соединений часто называют химией переходных металлов. [c.141]
Максимально возможная степень окисления d-металлов +8 (у осмия, например, OsOj). С ростом порядкового номера максимальная степень окисления возрастает от III группы до первого элемента VIII группы, а затем убывает. Эти элементы — типичные металлы. Химия изоэлектронных соединений d-элементов весьма похожа. Элементы разных периодов с аналогичной электронной структурой d-слоев образуют побочные подгруппы периодической системы (например, медь — серебро — золото, цинк — кадмий — ртуть и т. п.). Самая характерная особенность d-элементов — исключительная способность к комплексообра-зованию. Этим они резко отличаются от непереходных элементов. Химию комплексных соединений часто называют химией переходных металлов. [c.141]
Особенно важно применение графопроектора при изучении систематики химических элементов и их соединений. Возможность демонстрировать таблицы, показывающие закономерное изменение свойств элементов и их соединений по группам и периодам, позволяет использовать метод сопоставления и сравнения. Так, при изучении галогенов, халькогенов, элементов V группы весьма эффективны обобщающие таблицы по характеристике свойств одиночных атомов (радиус, электроотрицательность, энергия ионизации и пр.), свойств простых веществ (плотность, температуры кипения, плавления, агрегатное состояние, цвет, масса [c.132]
Так, при изучении галогенов, халькогенов, элементов V группы весьма эффективны обобщающие таблицы по характеристике свойств одиночных атомов (радиус, электроотрицательность, энергия ионизации и пр.), свойств простых веществ (плотность, температуры кипения, плавления, агрегатное состояние, цвет, масса [c.132]
Если исключить соединения элементов, расположенных в начале периодов таблицы Д. И. Менделеева (например, ЫааО в ряду оксидов первой группы), то совпадение с экспериментальными данными часто достаточно удовлетворительно для ориентировочной оценки теплот образования еще не изученных соединений. [c.73]
К переходным элементам периодической таблицы химических элементов Д. И. Менделеева относят те из них, у которых заполняется предвнешняя й-оболочка. За исключением цинка, кадмия и ртути, все они имеют недостроенную -оболочку. Цинк, кадмий и ртуть относят к переходным элементам, поскольку они близки им по ряду свойств. Отличаются же они проявлением единственной степени окисления + 2 и в этом отношении похожи на з-элемен-ты — щелочноземельные металлы, с которыми они находятся в одной группе. Как отмечалось в предыдущей главе, переходные элементы побочной подгруппы III группы также имеют одну степень окисления +3. Все же остальные переходные элементы отличает разнообразие проявляемых степеней окисления, обилие окислительновосстановительных реакций, широкое изменение кислотно-основных свойств в соединениях. Наличие неспаренных й-электронов приводит к проявлению широкого круга магнитных, электрических и оптических свойств этих элементов. [c.154]
Как отмечалось в предыдущей главе, переходные элементы побочной подгруппы III группы также имеют одну степень окисления +3. Все же остальные переходные элементы отличает разнообразие проявляемых степеней окисления, обилие окислительновосстановительных реакций, широкое изменение кислотно-основных свойств в соединениях. Наличие неспаренных й-электронов приводит к проявлению широкого круга магнитных, электрических и оптических свойств этих элементов. [c.154]
Структурные типы соединении элементов III группы периодической системы с N, Р и т. д. указаны в таблице ниже. В то время как BN является, по-видимому, ковалентным веществом, связи в A1N, GaN, InN имеют, вероятно, в значительной мере ионный характер, а соединения с более тяжелыми элементами V группы по типу связей близки к металлическим. (Информация о InBi приведена в табл. 6.6, разд. 6.7.1.) Структура BeSiN2 представляет собой сверхструктуру вютрцитовой структуры AIN и т. д. [146]. [c.599]
Рассмотренные опытные данные по каталитическим свойствам веществ в отношении окисления органических соединений указывают на существование определенной взаимосвязи между типом катализируемой реакции и положением в таблице Менделеева элементов, входящих в состав соответствующих оптимальных катализаторов. Так, наиболее активные металлические и окисные катализаторы глубокого окисления различных веществ обычно содержат элементы УИ1 групп — платину, палладий, кобальт, никель, а также элемены соседних побочных подгрупп УИ и I групп (медь, марганец). Неполное окисление различных соединений в органические кислоты или их ангидриды, а также ароматических веществ и спиртов в карбонильные соединения лучше всего катализируют окисные контакты на основе ванадия и молибдена — переходных элементов У и У1 групп. Мягкое окисление олефинов эффективно ускоряется катализаторами, содержащими элементы побочной погруппы I группы (Си, А ), а окислительное дегидрирование — сложными окис- [c.212]
Так, наиболее активные металлические и окисные катализаторы глубокого окисления различных веществ обычно содержат элементы УИ1 групп — платину, палладий, кобальт, никель, а также элемены соседних побочных подгрупп УИ и I групп (медь, марганец). Неполное окисление различных соединений в органические кислоты или их ангидриды, а также ароматических веществ и спиртов в карбонильные соединения лучше всего катализируют окисные контакты на основе ванадия и молибдена — переходных элементов У и У1 групп. Мягкое окисление олефинов эффективно ускоряется катализаторами, содержащими элементы побочной погруппы I группы (Си, А ), а окислительное дегидрирование — сложными окис- [c.212]
Принятое расположение материала Справочника. В распределении материала по главам V—XXXI тома I Справочника, а также в расположении таблиц II тома выдержан принцип, по которому составлены современные термохимические справочники (см. том II, рис. 1). В соответствии с этим вначале приводятся данные для кислорода, затем для водорода, его изотопов и их соединений с кислородом, затем следует гелий и другие элементы группы инертных газов, фтор и другие галогены и далее элементы всех групп Периодической системы вплоть до элементов первой группы. Для каждого элемента приводятся его соединения со всеми предыдущими, причем вначале следуют одноатомные соединения, затем двухатомные и т. д. по мере увеличения числа атомов в соединении. [c.22]
Для каждого элемента приводятся его соединения со всеми предыдущими, причем вначале следуют одноатомные соединения, затем двухатомные и т. д. по мере увеличения числа атомов в соединении. [c.22]
А. Процессы, активно ускоряемые катализаторами на основе элементов или соединений элементов, принадлежащих преимущественно к VIII (а также 16) группе таблицы Менделеева (Pt. Pd, Со, Ni. u) [c.109]
В. Процессы, активно ускоряемые катализаторами на основе соединений элементов, пршадлежащих преимущественно к 1б, 1Уа и Уа группам таблицы Менделеева (Мо, У, В , 5п, 5Ь, Р) В. I. Окислительное дегидрирование олефннов на окисных катализаторах Висмут-молибденовый окисный катализатор [c.110]
Г. Процессы, активно ускоряемые катализаторами на основе элементов или соединений элементов, принадлежащих преимущест-всгшо к 16 группе таблицы. Аенделеева (Си, Ag) Г. I. Окисление олефинов (диолефинов) и их производных в ненасыщенные карбонильные соединения Закись меди [c. 110]
110]
54008-13: МТП типа МП на МО, МП на НТО, НТП на МО, НТП на НТО Меры толщины покрытий натурные
Назначение
Меры толщины покрытий натурные МТП типа МП на МО, МП на НТО, НТП на МО, НТП на НТО (далее – меры) предназначены для воспроизведения толщины покрытия.
Описание
Меры представляют собой основание круглой, прямоугольной или квадратной формы с нанесенным в центре покрытием заданной толщины.
Меры различаются материалами покрытий и оснований:
– МП на МО – магнитное покрытие на магнитном основании;
– МП на НТО – магнитное покрытие на немагнитном токопроводящем основании;
– НТП на МО – немагнитное токопроводящее покрытие на магнитном основании;
– НТП на НТО – немагнитное токопроводящее покрытие на немагнитном токопроводящем основании.
Материалы оснований и покрытий для мер приведены в таблице 1. Таблица 1
|
Тип меры |
Материал | |
|
Покрытие [обозначение] |
Основание [обозначение] | |
|
МП на МО |
Никель [Нм] |
Сталь конструкционная [Сталь 20] |
|
МП на НТО |
Никель [Нм] |
Латунь [ЛС59-1] |
|
НТП на МО |
Хром [Хм. |
Сталь конструкционная [Сталь 20] |
|
Медь [Мм] |
Сталь конструкционная [Сталь 20] | |
|
Цинк [Цм хим.хр.бц] |
Сталь конструкционная [Сталь 20] | |
|
Кадмий [Кд хим.хр.бц] |
Сталь конструкционная [Сталь 20] | |
|
Олово-Висмут [О-Ви б] |
Сталь конструкционная [Сталь 20] | |
|
НТП на НТО |
Хром [Хб] |
Латунь [ЛС59-1], Латунь [Л63], Медь [М0] |
|
Медь [Мм] |
Латунь [ЛС59-1], Латунь [Л63] | |
|
Олово-Висмут [О-Ви м] |
Латунь [ЛС59-1], Латунь [Л63], Медь [МО] | |
Технические характеристики
1. Номинальные значения толщин покрытий мер, допускаемые отклонения толщин покрытий мер от номинальных значений, пределы допускаемых среднеквадратических отклонений (СКО) результатов измерений толщин покрытий мер представлены в таблице 2. Таблица 2
Таблица 2
|
Тип меры / покрытие |
Номинальное значение толщины покрытия меры и допускаемое отклонение толщины покрытия меры от номинального значения, мкм |
Предел допускаемого среднеквадратического отклонения (СКО) результатов измерений толщины покрытия меры, мкм |
|
МП на МО и МП на НТО / Никель [Нм] |
5±2; 10±3; 20±5; 50±7; 75±10 |
0,4; 0,5; 0,8; 1,0; 1,5 |
|
НТП на МО / Хром [Хм.тв] |
5±2; 10±3; 20±5; 50±7; 75±10 |
0,4; 0,5; 0,8; 1,0; 1,5 |
|
НТП на НТО / Хром [Хб] |
5±2; 10±3; 20±5; 50±7; 75±10 |
0,4; 0,5; 0,8; 1,0; 1,5 |
|
НТП на МО / Цинк [Цм.хим.хр.бц] |
5±2; 10±3; 20±5; 50±7; 75±10 |
0,4; 0,5; 0,8; 1,0; 1,5 |
|
НТП на МО / Кадмий [Кд хим. |
5±2; 10±3; 20±5; 50±7; 75±10 |
0,4; 0,5; 0,8; 1,0; 1,5 |
|
НТП на МО / Олово-Висмут [О-Ви б] |
5±2; 10±3; 20±5; 50±7; 75±10 |
0,4; 0,5; 0,8; 1,0; 1,5 |
|
НТП на НТО / Олово-Висмут [О-Ви м] |
5±2; 10±3; 20±5; 50±7; 75±10 |
0,4; 0,5; 0,8; 1,0; 1,5 |
|
НТП на МО / Медь [Мм] |
5±2; 10±3; 20±5; 50±7; 75±10 |
0,4; 0,5; 0,8; 1,0; 1,5 |
|
НТП на НТО / Медь [Мм] |
5±2; 10±3; 20±5; 35±7 |
0,4; 0,5; 0,8; 1,1 |
2. Отклонения от плоскостности рабочей поверхности оснований, отклонения от параллельности поверхностей оснований, шероховатости поверхностей оснований, габаритные размеры и массы представлены в таблице 3.
Таблица 3
|
Наименование параметра |
Значение параметра |
|
Отклонение от плоскостности рабочей поверхности основания, мкм, не более |
3 |
|
Отклонение от параллельности поверхностей основания, мкм, не более |
5 |
|
Шероховатость поверхности основания Ra, мкм, не более |
0,2 |
|
Г абаритные размеры, мм, не более |
50х50х10/050х10 |
|
Масса, кг, не более |
0,2 |
3. +0,3)*
+0,3)*
Шероховатость поверхности покрытия меры Ra, мкм, не более
0,2
Г абаритные размеры зоны покрытия меры, мм, не менее
13х13
Размер рабочей зоны меры, мм, не менее
5х5
* Тд – измеряемая величина в мкм.
4. Средний срок службы, лет
10.
3000.
5. Наработка на отказ, ч
6. Условия эксплуатации:
о/~’
– диапазон температуры окружающего воздуха, С
– диапазон относительной влажности окружающего воздуха, %
Знак утверждения типа
наносится типографским способом на титульный лист паспорта и на футляр.
Комплектность
Комплектность мер представлена в таблице 5.
Таблица 5
|
№ п/п |
Наименование |
Количество, шт. |
|
1 |
Мера |
от 1 |
|
2 |
Футляр |
1 |
|
3 |
Паспорт |
1 |
|
4 |
Методика поверки МП 2512-0006-2013 |
1 |
Поверка
осуществляется по документу МП 2512-0006-2013 «Меры толщины покрытий натурные МТП типа МП на МО, МП на НТО, НТП на МО, НТП на НТО. Методика поверки», утвержденному ГЦИ СИ ФГУП «ВНИИМ им. Д.И. Менделеева» в марте 2013 г. Основными средствами поверки являются: прибор для поверки концевых мер длины Микрон-02 (Государственный реестр № 44269-10), профилометр по ГОСТ 19300-86.
Методика поверки», утвержденному ГЦИ СИ ФГУП «ВНИИМ им. Д.И. Менделеева» в марте 2013 г. Основными средствами поверки являются: прибор для поверки концевых мер длины Микрон-02 (Государственный реестр № 44269-10), профилометр по ГОСТ 19300-86.
Сведения о методах измерений
Методика измерений приведена в документе «Меры толщины покрытий натурные МТП. Паспорт», 2013 г.
Нормативные и технические документы, устанавливающие требования к мерам толщины покрытий натурным МТП
1. Р 50.2.006-2001 «ГСИ. Государственная поверочная схема для средств измерений толщины покрытий в диапазоне от 1 до 20000 мкм».
2. ТУ 4276-032-27449627-11 «Меры толщины покрытий натурные МТП типа МП на МО, МП на НТО, НТП на МО, НТП на НТО. Технические условия».
Химия
Начальный курс химии:http://www.alhimik.ru/teleclass/glava1/gl-1-0.shtml
ВНО – 2017 на Яндексе https://zno.yandex.ua/ru/chemistry/
АЛХИМИК http://www.alhimik.ru/ Программы школьного и вузовского курса химии, методические находки, вести из мира дистанционного образования, анонсы новых книг. Интернет-класс (начальный курс химии), химическая кунсткамера, читальный зал, виртуальный консультант, электронные учебные пособия по курсу неорганической химии, задачник, практикум, химический справочник, методические статьи, химия на каждый день: в саду, на кухне, наука о чистоте, домашняя аптечка, косметика, домашний мастер, экология дома. «Химическая всячина»: полезные ссылки, ответы на вопросы. Химические новости. Веселая химия.
Интернет-класс (начальный курс химии), химическая кунсткамера, читальный зал, виртуальный консультант, электронные учебные пособия по курсу неорганической химии, задачник, практикум, химический справочник, методические статьи, химия на каждый день: в саду, на кухне, наука о чистоте, домашняя аптечка, косметика, домашний мастер, экология дома. «Химическая всячина»: полезные ссылки, ответы на вопросы. Химические новости. Веселая химия.
Журнал “Химия и химики”http://chemistry-chemists.com/
Дистанционные курсы при МГУ для подготовки абитуриентовhttp://do.chem.msu.ru/rus/abitur/dl/
Виртуальная химическая школа http://maratakm.narod.ru/
Портал “Сеть творческих учителей” http://it-n.ru/default.aspx
Сообщество взаимопомощи учителей. Химия http://pedsovet.su/load/97
Газета “Химия” и сайт для учителя “Я иду на урок химии” http://him.1september.ru/
WebElements: онлайн-справочник химических элементов http://webelements.narod.ru/
Химия для всех: иллюстрированные материалы по общей, органической и неорганической химии
http://school-sector. relarn.ru/nsm/
relarn.ru/nsm/
Химический справочник http://tehtab.ru/Guide/GuideChemistry/
Chemnet – портал фундаментального химического образования России http://www.chemnet.ru
Химия: открытый колледж http://college.ru/chemistry/ (Интерактивный курс химии, включающий учебник, большое количество моделей и демонстраций, справочные материалы, тестирование, обратную связь с учениками).
Химия для всех. Серия “Обучающие энциклопедии” http://www.informika.ru/text/database/chemy/START.html Разделы: общая химия, неорганическая химия, органическая химия, тесты, справочные материалы, стереомодели молекул.
Химия для всех. Электронный учебник
http://school-sector.relarn.ru/nsm/chemistry/Rus/chemy.html Иллюстрированные материалы по разделам: общая, органическая и неорганическая химия. Справочник, Тесты, видео (демо).
Органическая химия. Электронный учебник для средней школы.http://cnit.ssau.ru/organics/index.htm:
Нобелевские лауреаты по химии http://n-t.ru/nl/hm/ Биографический электронный справочник, снабженный гиперссылками, списками литературы.
Этимология химических элементов http://www.biochem.nm.ru/science/element.htmНазвания химических элементов – связь со свойствами, географическими и астрономическими объектами, учеными, мифологическими персонажами. В разделе история химии все великие открытия, биографические очерки о великих химиках различных времен, интерактивные ссылки, иллюстрации.
Элементы жизни http://school2.kubannet.ru/. Сайт можно использовать как пособие для уроков химии в школе и дополнительном образовании.
Сайт о химии XuMuK.ru http://www.xumuk.ru/?_openstat=ZGlyZWN0LnlhbmRleC5ydTs4Njcw Химические справочники, энциклопедии, статьи.
Химический раздел http://www.websib.ru/noos/chemistry/cheerful.htm Интересный сайт, на котором собраны материалы для учителей и учеников. Разделы сайта: Программы; Органическая химия; Учительская; ХимSoft; Из истории; Это интересно; Советы химикам; Веселые химики; Химия и жизнь; Абитуриенту; Книги, журналы, статьи; Химические ресурсы.
Дистанционное обучение по химии http://chem. olymp.mioo.ru/ Сайт химического факультета Московского государственного университета. Среди материалов сайта особый интерес представляют разделы: Консультации по химии для школьников; Консультации для учителей химии. Кроме того представлены материалы для подготовки к олимпиаде по химии. Имеются материалы для подготовки к поступлению в вузы.
olymp.mioo.ru/ Сайт химического факультета Московского государственного университета. Среди материалов сайта особый интерес представляют разделы: Консультации по химии для школьников; Консультации для учителей химии. Кроме того представлены материалы для подготовки к олимпиаде по химии. Имеются материалы для подготовки к поступлению в вузы.
КонТрен – Химия для всех http://kontren.narod.ru/ Сайт химического факультета Тюменского государственного университета. Учебно-информационный сайт, предназначенный для студентов химических факультетов, учителей химии, школьников и абитуриентов.
Химия. Образовательный сайт для школьников http://www.hemi.nsu.ru/ Очень хороший сайт по химии, с подробным изложением различных ее разделов. Полезен не только для школьников, но и для студентов (возможно, и для преподавателей). Все хорошо оформлено, много ссылок. Иллюстрации, словарь терминов, задачи, периодическая система Менделеева и т.д. Постоянно обновляется.
HimHelp.ru: химический сервер http://www. himhelp.ru/ Полный курс химии: теоретические основы, неорганическая и органическая химия. Информация о великих ученых. Многофункциональная периодическая система элементов Д. И. Менделеева, химический калькулятор. Новости.
himhelp.ru/ Полный курс химии: теоретические основы, неорганическая и органическая химия. Информация о великих ученых. Многофункциональная периодическая система элементов Д. И. Менделеева, химический калькулятор. Новости.
Школьная химия http://schoolchemistry.by.ru/ Истории возникновения химии, события и хронология. Материалы для учащихся: рефераты, химический калькулятор, сборник упражнений и задач, тесты по химии. Учебно-справочные материалы. Сборник таблиц по химии. Мультимедийные приложения. Коллекция химических опытов.
Химия: пособие для абитуриентов http://chemi.org.ru/ Материалы по основам неорганической и органической химии. Словарь, биография ученых, каталог полезных сайтов и форум.
Занимательная химия: проект по методике преподавания химии. http://home.uic.tula.ru/~zanchem/Материалы сайта: интересные опыты, химические истории и курьёзы, рассказы о великих учёных-химиках и др. Электронная версия таблицы Менделеева. Большое количество материала, имеется поиск по сайту, особый интерес представляет раздел «полезные ссылки», в котором представлены адреса наиболее информативных сайтов по химии.
Справочник по химии для школьников.http://www.chemworld.narod.ru/referance.html Таблица атомных свойств химических элементов. Электронный вариант таблицы Д.И. Менделеева. Краткий химический словарь. Таблица растворимости кислот, щелочей и оснований. Биографии известных химиков. Тривиальные названия некоторых веществ.
Галерея великих химиков http://www.chemnet.ru/zorkii/istkhim/veliki1.htm Портреты и краткие биографические справки о 48 выдающихся химиках мира.
Всё о химии: методические и дидактические материалы http://www.chemistry-43school.narod.ru/Тренировочные и проверочные задания по химии для 8-11 классов; программа подготовки к экзаменам по химии, материалы ЕГЭ; творческие и занимательные задания; решения задач повышенной сложности. Материалы о жизни и открытиях великих ученых в области химии; тематические новости. Ссылки на образовательные ресурсы.
Электронная библиотека по химии и технике http://rushim.ru/books/books.htmКоллекция электронных версий учебников, учебных пособий, научных статьей, задачников, журналов, справочников, нормативных документов и инструкций по всем разделам химии.
Учебное пособие «Краткий очерк истории химии» http://www.physchem.chimfak.rsu.ru/Source/History/big_index.html Интерактивный учебник с большим количеством приложений, слайдами для презентаций и вопросами для самопроверки. Биографии и портреты известных химиков в алфавитном порядке. Приложения и дополнения (статьи, исторические факты; химические схемы и таблицы).
БУК МО Матвеевский район «Централизованная библиотечная система»
ТЕАТРАЛЬНЫЙ КАЛЕЙДОСКОП
Список сценариев
Общие работы
Аполлонова, Г. В. У истоков театра : мероприятие, посвященное русскому народному театру, с включением кукольного представления / Г. В. Аполлонова // Читаем. Учимся. Играем. – 2010. – № 12. – С. 8-13.
Бирюкова, Е. А. Заглянем в закулисье : 27 марта – Всемирный день театра / Е. А. Бирюкова // Читаем, учимся, играем. – 2017. – № 12. – C. 96-99.
– 2017. – № 12. – C. 96-99.
Виноградова, Е. В. От старинной шарманки до современного плеера : интерактивная театрализованная программа / Е. В. Виноградова // Читаем. Учимся. Играем. – 2016. – № 1. – С. 102.
Вовнейко, Е. В. Отец русского театра : пьеса о русском актере Ф. Волкове, основателе постоянного русского театра / Е. В. Вовнейко // Читаем. Учимся. Играем. – 2013. – № 11. – С. 68-69.
Давыдова, М. А. Такие разные жанры : представление, рассказывающее о разных театральных жанрах / М. А. Давыдова // Читаем. Учимся. Играем. – 2010. – № 12. – С. 14 – 17.
Козлова, Г. Ф. У истоков театра : театрализованный рассказ об истории театра у разных народов с игровыми включениями / Г. Ф. Козлова // Читаем. Учимся. Играем. – 2010. – № 8. – С. 96 – 98.
Кочеткова, Е. Ю. Хозяин кукольного дома : театрализованный рассказ об актере и режиссере [Государственного Академического Центрального Театра кукол] С. В. Образцове : к 150-летию со дня рождения / Е. Ю. Кочеткова // Читаем. Учимся. Играем. – 2016. – № 4 . – С. 48-52. – Библиогр.: с. 52.
Ю. Кочеткова // Читаем. Учимся. Играем. – 2016. – № 4 . – С. 48-52. – Библиогр.: с. 52.
Марченко, Н. Н. Браво, актер! : познавательно-игровая программа о театральных профессиях / Н. Н. Марченко, В. В. Файт, Е. Е. Хитрова // Читаем, учимся, играем. – 2007. – № 1. – С. 83-88.
Неволина, Г. А. Роскошные потешные огни : театрализованный рассказ об истории возникновения салютов и фейерверков / Г. А. Неволина // Читаем. Учимся. Играем. – 2010. – № 9. – С. 28-35.
Панфилов, В. Как написать сценарий игрового театрализованного представления : методические рекомендации / В. Панфилов // Сценарии и репертуар. – 2013. –№ 17. – С. 4-10. – (Ее величество Игра).
Перепелица, В. «И, взвившись, занавес шумит…» : сценарий вечера для учащихся среднего школьного возраста, посвященного истории русского театра / В. Перепелица // Сценарии и репертуар. – 2019. – № 4. – С. 4-31.
Перепелица, В. Михаил Щепкин – артист по призванию : театральная гостиная для старшеклассников, посвященная жизни и творчеству артиста / В. Перепелица // Сценарии и репертуар. – 2019. – № 4. – С. 32-47. – Библиогр.: с. 47 (5 назв.).
Перепелица // Сценарии и репертуар. – 2019. – № 4. – С. 32-47. – Библиогр.: с. 47 (5 назв.).
Романова, Н. Н. Здесь оживают грезы, сказки : сценарий для детей об искусстве театра / Н. Н. Романова // Начальная школа. – 2008. – № 3. – (Библиотечка учителя. – 2008. – № 3. – С. 25-27).
Савонова, Н. Н. Театральная мозаика : познавательно-игровая программа, посвященная театральному искусству, для старшеклассников / Н. Н. Савонова // Читаем, учимся, играем. – 2005. – №11. – С. 95-98.
Сценарии о пьесах и драматургах
Агапова, И. А. Триллеры, которые написал Пушкин : театрализованный вечер, посвященный «Маленьким трагедиям» А. С. Пушкина, для старшеклассников / И. А. Агапова // Читаем, учимся, играем. – 2006. – № 5. – С. 20-23.
Аполлонова, Г. В. «Чайка» А. П. Чехова : совсем не смешная комедия : театрализованное мероприятие, посвященное пьесе А. П. Чехова / Г. В. Аполлонова // Читаем, учимся, играем. – 2016. –№ 10. – С. 6-9 : ил., фот. – Библиогр.: с. 9.
– 2016. –№ 10. – С. 6-9 : ил., фот. – Библиогр.: с. 9.
Аполлонова, Г. В. Пушкин и театр : литературный вечер, посвященный драматическим произведениям поэта / Г. В. Аполлонова // Читаем. Учимся. Играем. – 2013. – № 8. – С. 24-29.
Аполлонова, Г. В. Тургенев как драматург / Г. В. Аполлонова // Читаем, учимся, играем. – 2014. – № 4. – С. 31-35 : ил., фот. – Библиогр.: с. 35.
Аполлонова, Г. В. Предчувствие будущего : сценарий о жизни и творчестве драматурга А. П. Чехова / Г. В. Аполлонова // Читаем, учимся, играем. – 2014. – № 9. – С. 22-26 : ил., фот. – Библиогр.: с. 26.
Аполлонова, Г. В. «Сатиры смелый властелин» : сценарий о жизни и творчестве русского драматурга Д. И. Фонвизина / Г. В. Аполлонова // Читаем, учимся, играем. – 2015. –№ 1. – С. 19-27 : ил., портр. – Библиогр.: с. 27.
Аполлонова, Г. В. Пламенное сердце драмы : сценарий о жизни и творчестве английского драматурга У. Шекспира / Г. В. Аполлонова // Читаем, учимся, играем. – 2014. – № 1. – С. 16-25 : ил., портр. – Библиогр.: с. 25.
– 2014. – № 1. – С. 16-25 : ил., портр. – Библиогр.: с. 25.
Опарина, Н. День Грибоедова : сценарий проведения мероприятий в течение всего учебного дня для средних классов, посвященного жизни и творчеству А. С. Грибоедова / Н. Опарина // Сценарии и репертуар. – 2018. – № 10. – С. 38-52.
Халяпина, М. Гроза над темным царством : вечер-портрет, посвященный А. Н. Островскому / М. Халяпина // Сценарии и репертуар. – 2019. – № 3. – С. 14-30. – Библиогр.: с. 30 (7 назв.). – (В твоих глазах восторг читаю…).
Издания, представленные в списке, доступны в фондах областной библиотеки.
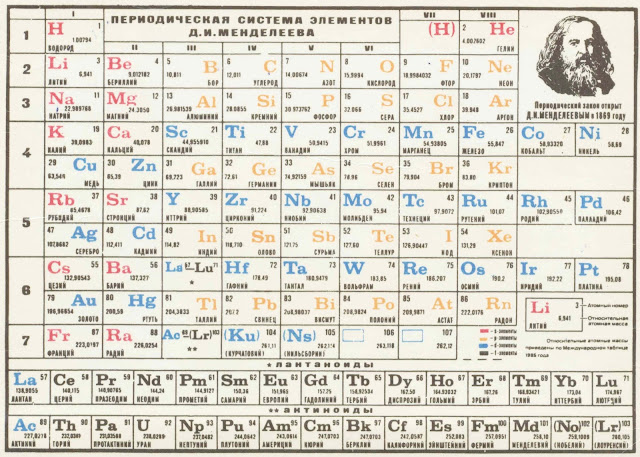
В 2019 году исполнилось 185 лет со дня рождения Д. И. Менделеева и 150 лет со дня открытия Периодической таблицы химических элементов. Это важнейшее событие в химии, которое сыграло огромную роль в развитии всей мировой химической науки. Поэтому Генеральная Ассамблея ООН объявила 2019 год Международным годом Периодической таблицы химических элементов.
В рамках проведения мероприятий к Международному году Периодической таблицы химических элементов, специалистами Информационно-библиографического отдела ОУНБ им. Н. К. Крупской, подготовлен список литературы «Великий закон природы»,который поможет Вам в проведении мероприятий приуроченных к Международному году Периодической таблицы химических элементов.
Издания, представленные в списке доступны в фондах областной библиотеки.
ВЕЛИКИЙ ЗАКОН ПРИРОДЫ
Список литературы
Одночастные монографические ресурсы
Книжные издания
Агафошин, Н. П. Периодический закон и периодическая система элементов Д. И. Менделеева / Н. П. Агафошин. – 2-е изд. – Москва : Просвещение, 1982. – 192 с.
Кедров, Б. М. День одного великого открытия / Б. М. Кедров. – Москва : Эдиториал УРСС, 2001. – 640 с. – (Философы России XX века).
Самин, Д. К. Сто великих научных открытий / Д. К. Самин. – Москва. : Вече, 2000, 2002. – 473, [6] с. : ил. – (100 великих).
Семишин, В. И. Периодическая система химических элементов Д. И. Менделеева / В. И. Семишин. – М. : Химия, 1972. – 188 с.
Степанов, Б. И. История великого закона / Б. И. Степанов. – Москва. : Учпедгиз, 1956. – 190 с. : ил.
————-
Великий закон природы : к 100-летию периодического закона Д. И. Менделеева: рекомендательный указатель литературы / Всесоюз. о-во “Знание”; Центр. политехн. б-ка. – Москва : Знание, 1969. – 16 с. – (В помощь лектору).
Сериальные ресурсы
Общие работы
Баландин, Р. Таблица приумножения знаний / Р. Баландин // Техника-молодежи. – 2018. – № 11. – С. 36-41 : фот. – (Сделано в России).
Физический смысл таблицы Менделеева и ее применимость для мира элементарных частиц.
Баринов, В. А. Титан : жизнь и деятельность Д. И. Менделеева в контексте российских библиотек / В. А. Баринов, К. В. Баринова // Библиотечное дело. – 2013. – № 19. – С. 32-38. – Окончание. Начало: № 17. – Примеч.: с. 38. – (Культурный контекст).
А. Титан : жизнь и деятельность Д. И. Менделеева в контексте российских библиотек / В. А. Баринов, К. В. Баринова // Библиотечное дело. – 2013. – № 19. – С. 32-38. – Окончание. Начало: № 17. – Примеч.: с. 38. – (Культурный контекст).
Дмитриев, И. С. Открытие периодического закона: три загадки и одна легенда / И. С. Дмитриев // Природа. – 2019. – № 2. – С. 34-43 : 8 ил., 6 портр. – Библиогр.: с. 43 (18 назв.). – (Международный год Периодической таблицы химических элементов).
Дроздов, А. М. Новый подход в исследовании верхней границы Периодической системы / А. М. Дроздов, А. А. Макареня, Т. В. Старова // Химия в школе. – 2012. – № 9. – С. 4-9 : 4 рис. – Библиогр.: с. 8-9 (11 назв.). – (Наука и промышленность).
Евдокимов, Ю. К истории периодического закона / Ю. Евдокимов // Наука и жизнь. – 2009. – № 5. – С. 12-15 : 6 фот., 3 портр., 6 табл. – Библиогр.: с. 15. – (Из истории науки).
К 175-летию со дня рождения Д. И. Менделеева. Книжно-иллюстративная выставка в РГБ // Библиотековедение. – 2009. – № 3. – С. 132-133 : 2 фот. – (Информация).
– 2009. – № 3. – С. 132-133 : 2 фот. – (Информация).
Оганесян, Ю. Ц. “Мы приблизились к границам применимости периодического закона”: интервью Ю. Ц. Оганесяна / беседовала Е. В. Сидорова // Природа. – 2019. – № 2. – С. 4-11 : 6 ил. – (Международный год Периодической таблицы химических элементов).
Беседа с директором Объединенного института ядерных исследований, академиком Ю. Ц. Оганесяном о выводах, сделанных учеными при исследовании свойств сверхтяжелых элементов, и об их влиянии на дальнейшее использование периодического закона.
Портнягина, М. Табличный вклад / М. Портнягина // Огонек. – 2019. – № 9. – С. 4. – (Неделя: эпицентр).
Савченко М. М. Гордость и слава России / М. М. Савченко // Наука в России. – 2004. – № 1. – С. 36 – 41.
Сайфуллин, Р. Современная форма таблицы Менделеева / Р. Сайфуллин, А. Сайфуллин // Наука и жизнь. – 2004. – № 7. – С. 2-7. – Библиогр.: с. 7.
Стрельникова, Л. Элементарно / Л. Стрельникова // Химия и жизнь – XXI век. – 2019. – № 1. – С. 2-3 : ил. – (Хемофилия).
Элементарно / Л. Стрельникова // Химия и жизнь – XXI век. – 2019. – № 1. – С. 2-3 : ил. – (Хемофилия).
2019 год ООН объявила Международным годом Периодической таблицы химических элементов в честь ее 150-летия.
Фадеев, Г. Н. Периодический закон: история и современность = Periodic law: history and modern interpretation / Г. Н. Фадеев, Ю. А. Лебедев // Химия в школе. – 2019. – № 1. – С. 71-78 : фот., табл. – Библиогр.: с. 78 (7 назв.). – (Из истории химии) (К 150-летию периодической таблицы).
Химики о Периодической таблице: профессиональный инструмент, научная икона, открытая книга? : интервью Е. В. Антипова [и др.] / беседовала Е. В. Сидорова // Природа. – 2019. – № 2. – С. 17-33 : 14 ил., 7 портр. – Библиогр.: с. 33 (19 назв.). – (Международный год Периодической таблицы химических элементов).
Интервью ведущих российских химиков о Периодической таблице Д. И. Менделеева.
Чугаев, Л. А. Дмитрий Иванович Менделеев. Биография русского гения : к 175-летию со дня рождения Д.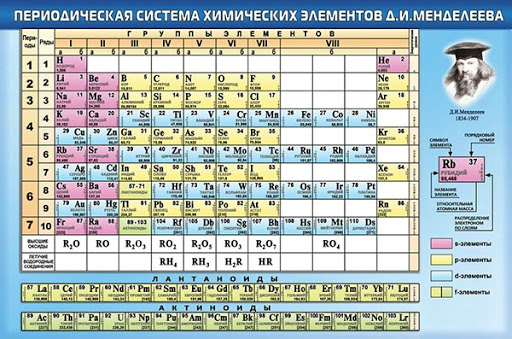 И. Менделеева / Л. А. Чугаев // Экология и жизнь. – 2009. – № 1. – С. 12-19. – Библиогр.: с. 19. – (Экология. Человек. Общество).
И. Менделеева / Л. А. Чугаев // Экология и жизнь. – 2009. – № 1. – С. 12-19. – Библиогр.: с. 19. – (Экология. Человек. Общество).
Занимательная химия
Арканова, В. Н. Кроссворд “Памяти Д. И. Менделеева” / В. Н. Арканова // Химия – Первое сентября. – 2014. – № 9. – С. 58-59 : 1 ил. – Библиогр.: с. 59. – (Кроссворды, головоломки).
Барнаковский, Н. А. Театрализованное представление “История открытия Периодического закона” / Н. А. Барнаковский // Химия в школе. – 2018. – № 9. – С. 46-52 : рис. – Библиогр.: с. 52. – (Внеурочная деятельность).
Интеллектуальная игра “Великий русский химик” / М. П. Неводчикова [и др.] // Химия в школе. – 2009. – № 1. – С. 60-69 : рис. – (Внеклассная работа).
Кабардина, Е. А. Городская интеллектуальная игра “Химия и жизнь” / Е. А. Кабардина, Г. И. Змановская // Химия в школе. – 2014. – № 8. – С. 56-59. – Библиогр.: с. 59. – (Внеклассная работа).
Игра по химии, приуроченная ко дню рождения Д. И. Менделеева.
И. Менделеева.
Костенчук, И. А. Химические шарады / И. А. Костенчук // Химия в школе. – 2011. – № 1. – С. 35.
Крюкова, Н. С. Дмитрий Менделеев. Как всё начиналось : сценарий мероприятия о жизни и творчестве учёного-химика Д. И. Менделеева / Н. С. Крюкова // Читаем, учимся, играем. – 2015. – № 3. – С. 70-73 : ил., портр.
Крюкова, Н. С. Викторина, посвященная Д. И. Менделееву / Н. С. Крюкова // Химия – Первое сентября. – 2015. – № 2. – С. 31 : 1 ил. – (Ко дню рождения…).
Махнева, М. В. Театрализованная постановка “Чертова трясина” / М. В. Махнева // Химия в школе. – 2009. – № 9. – С.74-79. – (Внеклассная работа).
Сценарий тематического зачета по теме “Периодическая система химических элементов”, который проходит как спектакль с химическим содержанием.
Пенькова, Г. А. Разработка и проведение игры “Что? Где? Когда?” / Г. А. Пенькова // Химия в школе. – 2011. – № 6. – С.75-79. – Окончание. Начало в № 5. – (Внеклассная работа).
– (Внеклассная работа).
Потапова, Е. А. Открытию периодического закона посвящается… : устный журнал / Е. А. Потапова // Химия – Первое сентября. – 2013. – № 2. – С. 7-10 : 5 ил. – (Внеклассное мероприятие).
Молибден | химический элемент
Молибден (Мо) , химический элемент , серебристо-серый тугоплавкий металл группы 6 (VIb) периодической таблицы , используемый для придания стали и другим сплавам превосходной прочности при высоких температурах.
Британская викторина
118 Имена и символы викторины с периодической таблицей
Таблица Менделеева состоит из 118 элементов. Насколько хорошо вы знаете их символы? В этой викторине вам будут показаны все 118 химических символов, и вам нужно будет выбрать название химического элемента, который представляет каждый из них.
Шведский химик Карл Вильгельм Шееле продемонстрировал ( около 1778 г.), что минерал молибдаина (нынемолибденит ), долгое время считавшийся свинцовой рудой или графитом , безусловно, содержит серу и, возможно, ранее неизвестный металл. По предложению Шееле другой шведский химик Питер Якоб Хьельм успешно выделил этот металл (1782 г.) и назвал его молибденом, от греческого « молибдос» – «свинец».
Молибден в природе не встречается в свободном виде. Относительно редкий элемент, он почти так же богат, как вольфрам , на который он похож. Для молибдена основной рудой является молибденит – дисульфид молибдена, MoS 2 – но также встречаются молибдаты, такие как молибдат свинца, PbMoO 4 (вульфенит) и MgMoO 4 . В основном промышленная добыча ведется из руд, содержащих минерал молибденит. Концентрированный минерал обычно обжигают в избытке воздуха, чтобы получить триоксид молибдена (MoO 3 ), также называемыйтехнический оксид молибдена , который после очистки может быть восстановлен водородом до металла. Последующее лечение зависит от конечного использования молибдена. Молибден можно добавлять в сталь в печи в виде технического оксида илиферромолибден . Ферромолибден (содержащий не менее 60 процентов молибдена) получают путем воспламенения смеси технического оксида и оксида железа . Металлический молибден получают в виде порошка путем восстановления водородом химически чистого оксида молибдена или молибдата аммония (NH 4 ) 2 MoO 4 . Порошок превращается в массивный металл с помощью процесса порошковой металлургии или процесса литья под давлением.
Последующее лечение зависит от конечного использования молибдена. Молибден можно добавлять в сталь в печи в виде технического оксида илиферромолибден . Ферромолибден (содержащий не менее 60 процентов молибдена) получают путем воспламенения смеси технического оксида и оксида железа . Металлический молибден получают в виде порошка путем восстановления водородом химически чистого оксида молибдена или молибдата аммония (NH 4 ) 2 MoO 4 . Порошок превращается в массивный металл с помощью процесса порошковой металлургии или процесса литья под давлением.
Сплавы на основе молибдена и сам металл обладают полезной прочностью при температурах, выше которых расплавляются большинство других металлов и сплавов. Однако в основном молибден используется в качестве легирующего агента при производстве сплавов черных и цветных металлов, которым он однозначно способствует высокой прочности и прочности.коррозионная стойкость, например, в реактивных двигателях, гильзах сгорания и деталях камеры дожигания. Это один из наиболее эффективных элементов для повышения закаливаемости чугуна и стали, а также способствует повышению ударной вязкости закаленных и отпущенных сталей. Высокая коррозионная стойкость, необходимая для нержавеющих сталей, используемых для обработки фармацевтических препаратов, и хромистых сталей для отделки автомобилей, уникально усиливается небольшими добавками молибдена. Металлический молибден используется для изготовления таких электрических и электронных деталей, как опоры для нитей накала, аноды и сетки. Пруток или проволока используются для нагревательных элементов в электрических печах, работающих при температуре до 1700 ° C (3092 ° F). Покрытия из молибдена прочно сцепляются со сталью, железом, алюминием., и другие металлы и демонстрируют отличную износостойкость.
Это один из наиболее эффективных элементов для повышения закаливаемости чугуна и стали, а также способствует повышению ударной вязкости закаленных и отпущенных сталей. Высокая коррозионная стойкость, необходимая для нержавеющих сталей, используемых для обработки фармацевтических препаратов, и хромистых сталей для отделки автомобилей, уникально усиливается небольшими добавками молибдена. Металлический молибден используется для изготовления таких электрических и электронных деталей, как опоры для нитей накала, аноды и сетки. Пруток или проволока используются для нагревательных элементов в электрических печах, работающих при температуре до 1700 ° C (3092 ° F). Покрытия из молибдена прочно сцепляются со сталью, железом, алюминием., и другие металлы и демонстрируют отличную износостойкость.
Молибден довольно устойчив к воздействию кислот, для смесей концентрированных азотной и плавиковой кислот , за исключением того , и она может быть быстро атакованы щелочных окислительных расплавов, таких как расплавленных смесей калия нитрата и натрия гидроксида натрия или пероксида; водные щелочи, однако, не действуют. Он инертен по отношению к кислороду при нормальной температуре, но легко соединяется с ним при нагревании красного цвета с образованием триоксидов и подвергается действию фтора при комнатной температуре с образованием гексафторидов.
Он инертен по отношению к кислороду при нормальной температуре, но легко соединяется с ним при нагревании красного цвета с образованием триоксидов и подвергается действию фтора при комнатной температуре с образованием гексафторидов.
Природный молибден представляет собой смесь семи стабильных изотопов : молибден-92 (15,84 процента), молибден-94 (9,04 процента), молибден-95 (15,72 процента), молибден-96 (16,53 процента), молибден-97 (9,46 процента), молибден-98 (23,78%) и молибден-100 (9,13%). Молибден проявляет степень окисления от +2 до +6 и, как считается, демонстрирует нулевую степень окисления в карбониле Mo (CO) 6 . Молибден (+6) присутствует в триоксиде, наиболее важном соединении , из которого получают большинство других его соединений , и в молибдатах (содержащих анион MoO 4 2- ), используемых для производства пигментов и красителей.Дисульфид молибдена (MoS 2 ), напоминающий графит, используется в качестве твердой смазки или добавки к консистентным смазкам и маслам. Молибден образует твердые, тугоплавкие и химически инертные межузельные соединения с бором , углеродом , азотом и кремнием при прямой реакции с этими элементами при высоких температурах.
Молибден образует твердые, тугоплавкие и химически инертные межузельные соединения с бором , углеродом , азотом и кремнием при прямой реакции с этими элементами при высоких температурах.
Молибден – важный микроэлемент в растениях; в бобовых в качестве катализатора он помогает бактериям связывать азот. Триоксид молибдена и молибдат натрия (Na 2 MoO 4 ) использовались в качестве питательных микроэлементов.
Крупнейшими производителями молибдена являются Китай, США , Чили , Перу , Мексика и Канада.
| атомный номер | 42 |
|---|---|
| атомный вес | 95,94 |
| температура плавления | 2610 ° С (4730 ° F) |
| точка кипения | 5,560 ° С (10,040 ° F) |
| удельный вес | 10,2 при 20 ° C (68 ° F) |
| состояния окисления | 0, +2, +3, +4, +5, +6 |
| электронная конфигурация | [Kr] 4 д 5 5 с 1 |
The Periodic Table at KnowledgeDoor
Ссылки (Нажмите рядом со значением выше, чтобы увидеть полную информацию о цитировании для этой записи)
Оллред, А. Л. «Значения электроотрицательности на основе термохимических данных». Журнал неорганической и ядерной химии, том 17, номера 3–4, 1961 г., стр. 215–221. doi:10.1016/
Л. «Значения электроотрицательности на основе термохимических данных». Журнал неорганической и ядерной химии, том 17, номера 3–4, 1961 г., стр. 215–221. doi:10.1016/
Андерс, Эдвард и Николя Гревесс. «Изобилие элементов: метеоритных и солнечных». Geochimica et Cosmochimica Acta, том 53, номер 1, 1989 г., стр.197–214. doi:10.1016/ -X
Андерсен Т., Х.К. Хауген и Х. Хотоп. «Энергии связи в атомных отрицательных ионах: III». Журнал физических и Химические справочные данные, том 28, номер 6, 1999 г., стр. 1511–1533.
Барсан, Майкл Э., редактор. Карманный справочник NIOSH по химическим опасностям. Цинциннати, Огайо: публикации NIOSH, 2007.
.Бацанов С.С. “Ван-дер-ваальсовы радиусы элементов”. Неорганические материалы, том 37, номер 9, 2001 г., стр. 871–885.См. реферат
Bedford, R. E., G. Bonnier, H. Maas и F. Pavese. «Рекомендуемые значения
Температура по Международной температурной шкале 1990 г. для избранного набора вторичных контрольных точек». Метрология, том 33, номер 2, 1996 г., стр. 133–154.
для избранного набора вторичных контрольных точек». Метрология, том 33, номер 2, 1996 г., стр. 133–154.
Боуэн, Х. Дж. М. Экологическая химия элементов. Лондон: Academic Press, Inc., 1979.
Кэмпбелл, Дж. Л. «Урожайность флуоресценции и вероятности Костера-Кронига для атомных L подоболочек.Таблицы атомных и ядерных данных, том 85, номер 2, 2003 г., стр. 291–315. doi: 10.1016/
Кардарелли, Франсуа. Справочник по материалам: краткий настольный справочник , 2-е издание. Лондон: Springer-Verlag, 2008.
Клементи, Э., Раймонди Д.Л., Рейнхардт В.П. Константы атомного скрининга из функций SCF. II. Атомы с 37–86 электронами». Журнал химической физики, том 47, номер 4, 1967 г.,
стр. 1300–1307. doi:10.1063/
Коэн, Э. Ричард, Дэвид Р. Лайд и Джордж Л. Тригг, редакторы. Справочник по физике AlP, 3-е издание. Нью-Йорк: Springer-Verlag New York, Inc., 2003.
. Коннелли, Нил Г. , Туре Дамхус, Ричард М. Хартсхорн и Алан Т. Хаттон. Номенклатура неорганической химии: Рекомендации IUPAC 2005. Кембридж: RSC Publishing, 2005.
, Туре Дамхус, Ричард М. Хартсхорн и Алан Т. Хаттон. Номенклатура неорганической химии: Рекомендации IUPAC 2005. Кембридж: RSC Publishing, 2005.
Кордеро, Беатрис, Вероника Гомес, Ана Э. Платеро-Пратс, Марк Ревес, Хорхе
Эчеверрия, Эдуард Кремадес, Флавия Барраган и Сантьяго Альварес.«Возвращение ковалентных радиусов». Dalton Transactions, номер 21, 2008 г., стр. 2832–2838. doi:10.1039/
де Подеста, Майкл. Понимание свойств Материя, 2-е издание. Лондон: Taylor & Francis, 2002.
Desai, PD, TK Chu, HM James и CY Ho. «Удельное электрическое сопротивление выбранных элементов». Журнал физических и химических справочных данных, том 13, номер 4, 1984 г., стр. 1069–1096.
Дронсковски, Ричард. Вычислительная химия твердотельных материалов.Вайнхайм, Германия: WILEY-VCH Verlag GmbH & Co. KGaA, 2005.
Эмсли, Джон. Строительные блоки природы: Путеводитель по элементам от А до Я . Оксфорд: Издательство Оксфордского университета, 2003.
Эмсли, Джон. Элементы, 3-е издание. Оксфорд: Издательство Оксфордского университета, 1998.
Элементы, 3-е издание. Оксфорд: Издательство Оксфордского университета, 1998.
Файрстоун, Ричард Б. Таблица изотопов, 8-е издание, том 2. Под редакцией Вирджинии С. Ширли с помощниками редактора Корал М. Бэглин, С. Ю. Фрэнк Чу и Джин Зипкин. Нью-Йорк: John Wiley & Sons, Inc., 1996.
Галассо, Фрэнсис С. Структура и свойства неорганических твердых тел. Oxford: Pergamon Press, 1970.
Гош, Дулал К. и Картик Гупта. «Новая шкала электроотрицательности 54 элементов периодической таблицы, основанная на поляризуемости атомов». Журнал теоретической и вычислительной химии, том 5,
№ 4, 2006 г., стр. 895–911. doi:10.1142/
Гринвуд, Н. Н. и А. Эрншоу. Химия элементов, 2-е издание. Оксфорд: Баттерворт-Хайнеманн, 1997.
Ганион, Роберт Ф., Сент-Джон Диксон-Уоррен, В. Карл Линебергер и Майкл Д. Морс. «Ультрафиолетовая фотоэлектронная спектроскопия анионов молибдена и монооксида молибдена». Журнал химической физики, том 104, номер 5, 1996 г. , стр. 1765–1773. doi:10.1063/
, стр. 1765–1773. doi:10.1063/
Гвин Уильямс. Энергии связи электронов. http://
Ho, C. Y., R. W. Powell, and P.Э. Лилей. «Теплопроводность элементов: всесторонний обзор». Журнал физических и химических справочных данных, том 3, приложение 1, 1974 г., стр. с I–1 по I–796.
Хорват, А.Л. «Критическая температура элементов и периодическая система».
Журнал химического образования, том 50, номер 5, 1973 г., стр. 335–336. doi:10.1021/
Хьюи, Джеймс Э., Эллен А. Кейтер и Ричард Л. Кейтер. Неорганическая химия: принципы строения и реакционной способности, 4-е издание.Нью-Йорк: Издательство HarperCollins College Publishers, 1993.
Ихде, Аарон Дж. Развитие современной химии. Нью-Йорк: Dover Publications, Inc., 1984.
Международная организация труда (МОТ). Международная карта химической безопасности для молибдена. http: //
http: //
Международная организация труда (МОТ). Международная карта химической безопасности для молибдена. http: //
Jr., Элберт Дж. Литтл и Марк М. Джонс. «Полная таблица
Электроотрицательности.Журнал химического образования, том 37, номер 5, 1960, стр. 231–233. doi:10.1021/
Каширас, Эфтимиос. Атомная и электронная структура
Твердые вещества. Кембридж: Издательство Кембриджского университета, 2003.
Киттель, Чарльз. Введение в физику твердого тела, 8-е издание. Хобокен, Нью-Джерси: John Wiley & Sons, Inc., 2005.
Киттель, Чарльз. Введение в физику твердого тела, 5-е издание. Нью-Йорк: John Wiley & Sons, Inc., 1976.
Краузе, М.О. «Атомно-радиационная и Безрадиационные выходы для оболочек K и L». Журнал физических и химических справочных данных, том 8, номер 2, 1979 г., стр. 307–327.
Ли, Ю.-Х. и Дж. Э. Шунмейкер. «Химический состав и минералогия». морских отложений». стр. 1–36 в книге «Осадки, диагенез и осадочные породы». Под редакцией Фреда Т. Маккензи. Оксфорд: Elsevier Ltd., 2005.
Либофф, Ричард Л. Введение в квантовую механику, 3-е издание. Рединг, Массачусетс: Addison Wesley Longman, Inc., 1998.
Лиде, Дэвид Р., изд. Справочник CRC по химии и физике, 88-е издание. Бока-Ратон, Флорида: Taylor & Francis Group, 2008.
Манн, Джозеф Б., Терри Л. Мик, Юджин Т. Найт, Джозеф Ф. Капитани и Леланд К. Аллен. «Энергии конфигурации элементов d-блока». Журнал Американского химического общества, том 122, номер 21, 2000 г., стр. 5132–5137. doi:10.1021/
Журнал Американского химического общества, том 122, номер 21, 2000 г., стр. 5132–5137. doi:10.1021/
Мануэль О., изд. Происхождение элементов в Солнечном Система: последствия наблюдений после 1957 года.Нью-Йорк: Kluwer Academic Publishers, 2000.
Маршалл, Джеймс Л. Открытие элементов: поиск фундаментальных принципов Вселенной, 2-е издание. Бостон, Массачусетс: Pearson Custom Publishing, 2002.
Мартин, В. К. «Электронная структура элементов». Европейский физический журнал C — Частицы и поля, том 15, номера 1–4, 2000 г., стр. 78–79. doi: 10.1007/
McDonough, WF «Композиционная модель ядра Земли». стр. 547–568 в «Мантии и ядре».Под редакцией Ричарда В. Карлсона. Оксфорд: Elsevier Ltd., 2005.
. Мечтли, Юджин А. «Свойства материалов». стр. 4–1–4–33 в Справочные данные для инженеров: радио, электроника, компьютер и связь. Мак Э. Ван Валкенбург, под редакцией Венди М. Миддлтон. Woburn, MA: Butterworth-Heinemann, 2002. doi:10.1016/
doi:10.1016/
Miessler, Gary L., and Donald A. Tarr. Неорганическая химия, 3-е издание. Река Аппер-Сэдл, Нью-Джерси: Pearson Prentice Hall, 2004.
Нэгл, Джеффри К. «Атомная поляризуемость и электроотрицательность». Журнал Американского химического общества, том 112, номер 12, 1990 г., стр. 4741–4747. doi:10.1021/
Национальный институт охраны труда и здоровья (NIOSH). Международная карта химической безопасности для молибдена. http://
Национальный институт охраны труда и здоровья (NIOSH).Международная карта химической безопасности для молибдена. http://
Национальный институт охраны труда и здоровья (NIOSH). Реестр токсического действия химических веществ на молибден.
Орем, У. Х. и Р. Б. Финкельман. «Углеобразование и геохимия.» стр. 191–222 в Осадки, диагенез, и осадочные породы. Под редакцией Фреда Т. Маккензи. Оксфорд: Elsevier Ltd., 2005.
Окстоби, Дэвид В., Х. П. Гиллис и Алан Кэмпион. Основы современной химии, 6-е издание. Бельмонт, Калифорния: Thomson Brooks/Cole, 2008.
Пальме, Х. и Х. Бир. «Метеориты и состав солнечной фотосферы». стр. 204–206 в Ландольте-Бёрнштейне – Группа VI: астрономия и астрофизика. Под редакцией HH Voigt. Нью-Йорк: Springer-Verlag, 1993. doi:10.1007/
Пальме Х. и Хью Сент-К. О’Нил. «Космохимические оценки состава мантии». стр. 1–38 в Мантии и Ядре. Под редакцией Ричарда В. Карлсона. Оксфорд: Elsevier Ltd., 2005.
.Полинг, Лайнус. Природа химической связи, 3-е издание. Итака, Нью-Йорк: Издательство Корнельского университета, 1960.
Пирсон, Ральф Г. «Абсолютная электроотрицательность и твердость: приложение к неорганической химии». Неорганическая химия, том 27, номер 4, 1988 г., стр. 734–740.doi:10.1021/
«Абсолютная электроотрицательность и твердость: приложение к неорганической химии». Неорганическая химия, том 27, номер 4, 1988 г., стр. 734–740.doi:10.1021/
Пекка Пюйккё. Самосогласованные ковалентные радиусы 2009 года. http://
Пюикко, Пекка и Мичико Атсуми. «Ковалентные радиусы молекулярных двойных связей для элементов Li-E112». Химия – Европейский журнал, том 15, номер 46, 2009 г., стр. 12770–12779. doi:10.1002/
Пьюкко, Пекка и Митико Атсуми.«Ковалентные радиусы молекулярных одинарных связей для элементов 1-118». Химия – Европейский журнал, том 15, номер 1, 2009 г., стр. 186–197. doi:10.1002/
Pyykkö, Pekka, Sebastian Riedel, and Michael Patzschke. «Ковалентные радиусы тройной связи». Химия – Европейский журнал, том 11, номер 12, 2005 г., стр. 3511–3520. doi:10. 1002/
1002/
Ringnes, Vivi. «Происхождение названий химических элементов». Журнал химического образования, том 66, номер 9, 1989 г., стр.731–738. doi: 10.1021/
Робертс, Б.В. «Обзор сверхпроводящих материалов и критическая оценка выбранных свойств». Журнал физических и химических справочных данных, том 5, номер 3, 1976 г., стр. 581–821.
Рорер, Грегори С. Структура и связь в кристаллических материалах. Кембридж: Издательство Кембриджского университета, 2001.
Самсонов Г.В., изд. Справочник по физико-химическим свойствам элементов. Нью-Йорк: Plenum Publishing Corporation, 1968.
Сандерсон, Р. Т. Простые неорганические вещества. Малабар, Флорида: Robert E. Krieger Publishing Co., Inc., 1989.
. Сандерсон, Р. Т. «Принципы электроотрицательности: Часть I. Общая природа». Журнал химического образования, том 65, номер 2, 1988 г., стр. 112–118. дои: 10.1021/
Сансонетти, Дж. Э. и В. К. Мартин. «Справочник по основным данным атомной спектроскопии». Журнал физических и химических справочных данных, том 34, номер 4, 2005 г., стр. 1559–2259.doi: 10.1063/
Э. и В. К. Мартин. «Справочник по основным данным атомной спектроскопии». Журнал физических и химических справочных данных, том 34, номер 4, 2005 г., стр. 1559–2259.doi: 10.1063/
Шеннон, Р. Д. «Пересмотренные эффективные ионные радиусы и систематические исследования межатомных расстояний в галогенидах и халькогенидах». Acta Crystallographica Section A, том 32, номер 5, 1976 г., стр. 751–767. doi:10.1107/
Силби, Роберт Дж., Роберт А. Альберти и Мунги Г. Бавенди. Физическая химия, 4-е издание. Хобокен, Нью-Джерси: John Wiley & Sons, Inc., 2005.
. Сингман, Чарльз Н. «Атомный объем и аллотропия элементов.Журнал химического образования, том 61, номер 2, 1984 г., стр. 137–142. doi:10.1021/
Слейтер, Дж. К. «Атомные радиусы в кристаллах».
Химическая физика, том 41, номер 10, 1964, стр. 3199–3204. doi: 10.1063/
Смит, Дерек В. «Электроотрицательность в двух измерениях: переоценка и разрешение парадокса Пирсона-Полинга».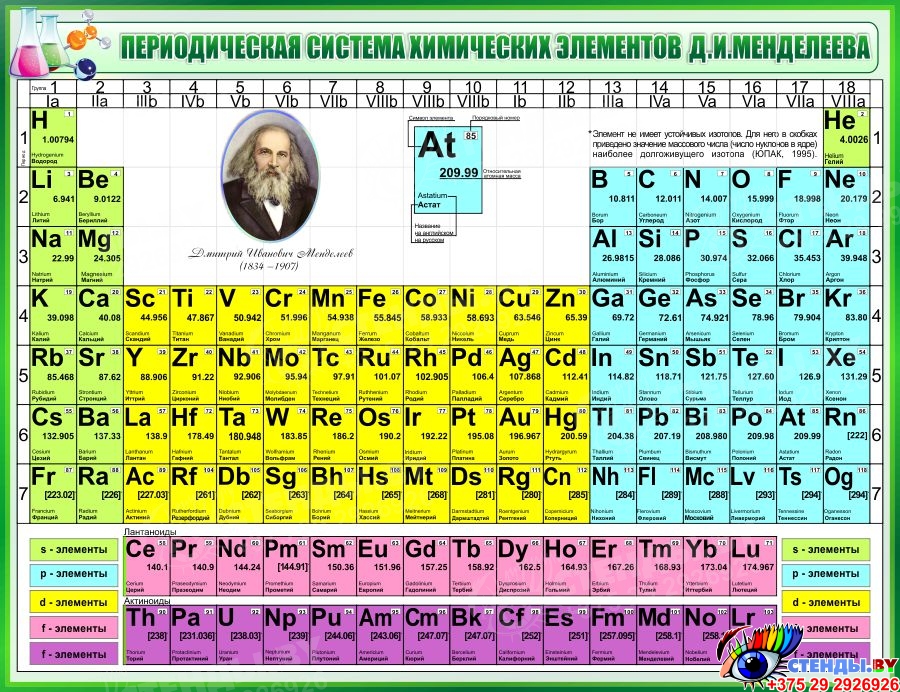 Журнал химических
Образование, том 67, номер 11, 1990 г., стр. 911–914. doi:10.1021/
Журнал химических
Образование, том 67, номер 11, 1990 г., стр. 911–914. doi:10.1021/
Смит, Дерек В.Неорганические вещества: прелюдия к изучению описательной неорганической химии. Кембридж: Кембриджский университет Press, 1990.
Стюарт, Г. Р. «Измерение низкотемпературной удельной теплоемкости». Обзор научных инструментов, том 54, номер 1, 1983 г., стр. 1–11. дои: 10.1063/
Стюарт, Г. Р. «Измерение низкотемпературной удельной теплоемкости». Обзор научных инструментов, том 54, номер 1, 1983 г., стр. 1–11. doi:10.1063/
Шугар, Джек и Арлин Масгроув.«Уровни энергии молибдена, от Mo I до Mo XLII». Журнал физических и химических справочных данных, том 17, номер 1, 1988 г., стр. 155–239.
Тари А. Удельная теплоемкость вещества при низких температурах. Лондон: Imperial College Press, 2003.
Вайнштейн, Борис К., Владимир М. Фридкин и Владимир Л. Инденбом. Структура кристаллов, 2-е издание. Современная кристаллография 2. Под редакцией Бориса К. Вайнштейна, А.А. Чернова и Л.А. Шувалова. Берлин: Springer-Verlag, 1995.
Современная кристаллография 2. Под редакцией Бориса К. Вайнштейна, А.А. Чернова и Л.А. Шувалова. Берлин: Springer-Verlag, 1995.
Voigt, H.Х., редактор. Ландольт-Бёрнштейн – Группа VI Астрономия и астрофизика. Берлин: Springer-Verlag, 1993.
. Вабер, Дж. Т. и Дон Т. Кромер. «Орбитальные радиусы атомов и ионов». Журнал химической физики, том 42, номер 12, 1965 г., стр. 4116–4123. doi:10.1063/
Вагман, Дональд Д., Уильям Х. Эванс, Вивиан Б. Паркер, Ричард Х. Шумм, Ива Халоу, Сильвия М. Бейли, Кеннет Л. Чёрни и Ральф Л. Наттолл. «Теплопроводность элементов: всесторонний обзор.Журнал физических и химических справочных данных, том 11, приложение 2, 1982 г., стр. 2–1–2–392.
Уолдрон, Кимберли А., Эрин М. Ферингер, Эми Э. Стриб, Дженнифер Э. Троски, и Джошуа Дж. Пирсон. «Скрининг процентов на основе эффективного заряда ядра Слейтера как универсальный инструмент для обучения периодическим тенденциям». Журнал химического образования, том 78, номер 5, 2001 г. , стр. 635–639.
, стр. 635–639.
Уикс, Мэри Эльвира и Генри М. Лестер, «Открытие элементов», 7-е издание.Истон, Пенсильвания: Журнал химического образования, 1968.
Визер, Майкл Э. и Тайлер Б. Коплен. «Атомные массы элементов 2009 г. (Технический отчет IUPAC)». Чистая и прикладная химия, том 83, номер 2, 2011 г., стр. 359–396. doi: 10.1351/
Йос, Карл Л. «Плотность жидкости элементов». Химическая инженерия, том 114, номер 12, 2007 г., стр. 44–46.
Yaws, Карл Л. Справочник Yaws по физическим свойствам углеводородов и химических веществ.Хьюстон, Техас: Gulf Publishing Company, 2005.
Факты о молибдене, символ, открытие, свойства, использование
.Что такое молибден
Молибден (произношение: meh-LIB-deh-nem) представляет собой блестящий серебристый элемент, принадлежащий к семейству переходных металлов и представленный химическим символом Mo [1, 2, 3]
Символ молибдена
. Пластичный металл с высокой коррозионной стойкостью, молибден легко реагирует с другими элементами с образованием соединений [2] .
Он имеет семь встречающихся в природе изотопов, из которых 98 Mo является наиболее распространенным, составляющим около 24,39% всего молибдена, обнаруженного на Земле [4] . Из семи встречающихся в природе изотопов 90 327 100 90 328 Mo не считается стабильным и имеет период полураспада 7,8 X 10 90 327 18 90 328 лет 90 327 [4] 90 328 .
Где содержится молибден
Молибденит (также известный как дисульфид молибдена или MoS 2 ) является основной минеральной рудой, из которой металл извлекается путем окислительного обжига с последующим восстановлением полученного оксида молибдена [1] .Небольшое количество молибдена также встречается в качестве побочного продукта при производстве меди и вольфрама [1] . В тройку крупнейших запасов молибдена входят Китай, США и Чили, а в тройку крупнейших производителей входят Китай, США и Чили [1] .
Молибден
История
Происхождение его названия : Название элемента происходит от слова «молибдос», греческого слова «свинец» [1, 2] .
Кто его открыл : Шведский химик Петер Якоб Хьелм является первооткрывателем молибдена [1] .
Когда и как он был открыт
Мягкая черная молибденитовая руда похожа на графит по внешнему виду и поэтому ошибочно считалась свинцовой рудой, пока не была проанализирована немецко-шведским химиком Карлом Вильгельмом Шееле в 1778 году [1] . Хотя он не смог идентифицировать вещество, его исследования показали, что это не был ни графит, ни свинец [1] .
Предполагалось, что минеральная руда содержит неизвестный элемент, но исследователи не смогли восстановить и выделить металл [1] .Они обнаружили, что новый элемент может окисляться и образовывать кислоту при смешивании с водой, называемую молибденовой кислотой (H 2 MoO 4 ) [1] . В 1781 году Петер Якоб Хьельм измельчил углерод и молибденовую кислоту вместе с льняным маслом и образовал пасту [1] . Он нагрел смесь в тигле и получил металлический молибден [1, 5] .
Он нагрел смесь в тигле и получил металлический молибден [1, 5] .
Молибден Идентификация | |||
| Атомный номер | 42 [1] | ||
| Номер CAS | 7439-98-7 [1] | ||
| Позиция в периодической таблице | Группа | Период | Блок |
| 6 [1] | 5 [1] | д [1] | |
Место молибдена в периодической таблице
Свойства и характеристики молибдена
Общие свойства | ||||||||||||||||
| Относительная атомная масса | 95.95 [1] | |||||||||||||||
| Атомная масса | 95,95 а. е.м. [1] е.м. [1] | |||||||||||||||
| Молярная масса | 95,96 г/моль [9, 10] | |||||||||||||||
Физические свойства | ||||||||||||||||
| Цвет | Серебристо-белый [1, 5] | |||||||||||||||
| Температура плавления/замерзания | 2622 °C, 4752 °F [1] | |||||||||||||||
| Температура кипения | 4639 °C, 8382 °F [1] | |||||||||||||||
| Плотность | 10.2 г см -3 [1] | |||||||||||||||
| Состояние вещества при комнатной температуре (твердое/жидкое/газообразное) | Твердый [1, 5] | |||||||||||||||
| Твердость | ||||||||||||||||
| – Бринелль | 1500 МПа [6] | |||||||||||||||
| – Мооса | 5,5 [6] | |||||||||||||||
| – Виккерс | 1530 МПа [6] | |||||||||||||||
| Электропроводность | 2X10 7 Ш/м [6] | |||||||||||||||
| Теплопроводность | 139 Вт/(м·К) [6] | |||||||||||||||
| Удельная теплоемкость | 251 Дж кг -1 К -1 [1] | |||||||||||||||
| Объемный модуль | 231 ГПа [1] | |||||||||||||||
| Модуль сдвига | Неизвестно [1] | |||||||||||||||
| Модуль Юнга | Неизвестно [1] | |||||||||||||||
| Давление паров | ||||||||||||||||
| – Температура (К) | 400 | 600 | 800 | 1000 | 1200 | 1400 | 1600 | 1800 | 2000 | 2200 | 2400 | |||||
| – Давление (Па) | – | – | – | – | – | – | 1. 83X 10 -9 83X 10 -9 | 4,07X 10 -7 | 3,03X 10 -5 | 1,02X 10 -5 | 1,89X 10 -2 | |||||
Химические свойства | ||||||||||||||||
| Степени окисления | 6, 5, 4, 3, 2, 0 [1] | |||||||||||||||
| Изотопы | Изотоп | Масса | Численность (%) | Период полураспада | Режим распада | |||||||||||
| 92 Пн | 91.907 | 14,53 | > 3 х 10 17 у | β+-EC | ||||||||||||
| 94 Пн | 93,905 | 9,15 | – | – | ||||||||||||
| 95 Пн | 94. 906 906 | 15,8 | – | – | ||||||||||||
| 96 Пн | 95,905 | 16.67 | – | – | ||||||||||||
| 97 Пн | 96,906 | 9,60 | – | – | ||||||||||||
| 98 Пн | 97,905 | 24,39 | – | – | ||||||||||||
| 100 Пн | 99,907 | 9,82 | 6 х 10 20 у | β-β- | ||||||||||||
Атомные данные молибдена (элемент 42)
| Валентные электроны | 6 [7] | |||||||
| Квантовые числа | ||||||||
| – № | 4 [7] | |||||||
| – ℓ | 2 [7] | |||||||
| – м л | 2 [7] | |||||||
| – м с | +1/2 [7] | |||||||
| Электронная конфигурация (конфигурация благородных газов) | [Кр] 4d 5 5s 1 [1] | |||||||
| Атомная структура | ||||||||
| – Количество электронов | 42 [5] | |||||||
| – Количество нейтронов | 54 [5] | |||||||
| – Количество протонов | 42 [5] | |||||||
| Радиус атома | ||||||||
| – Атомный радиус | 2. 17 Å [1] 17 Å [1] | |||||||
| – Ковалентный радиус | 1,46 Å [1] | |||||||
| Электроотрицательность (шкала Полинга) | 2,16 [1] | |||||||
| Сродство к электрону | 72,171 кДж моль -1 [1] | |||||||
| Энергия связи | 6,8 эВ (656,098 кДж моль -1 ) [11] | |||||||
| Энергия ионизации (кДж моль -1 ) | 1-й | 2-й | 3-й | 4-й | 5-й | 6-й | 7-й | 8-я |
| 684.316 | 1559.2 | 2617,65 | 4476,9 | 5257,49 | 6640,85 | 12124. 73 73 | 13855.3 | |
Электронная конфигурация молибдена (модель Бора)
Для чего используется молибден
Использование в промышленности
- Поскольку он имеет высокую температуру плавления, он используется для производства серого порошка, который прессуется при очень высоком давлении для изготовления тепловых, вакуумных и рентгеновских трубок [1] .
- Элемент 42 используется при изготовлении сплавов, в том числе стали, для повышения ее твердости, прочности, коррозионной стойкости и электропроводности [1, 5] .
- Сплавы молибдена используются в авиационных двигателях, турбинах для производства электроэнергии и атомных электростанциях, а также в нагревательных элементах, таких как пилы и сверла [1, 5] .
- Оксид молибдена, молибдаты и дисульфид молибдена используются в рецептурах высокоэффективных смазочных материалов [1, 8] .
- Поскольку молибден может выдерживать высокие температуры, он считается подходящим материалом для изготовления электродов для плавки стекла [5] .
- Используется в качестве катализатора в нефтяной промышленности, способствует удалению органической серы в процессах сжижения газа и угля [1, 5] .
Биологическая роль в растениях, животных и человеке
- Молибден является важным компонентом различных ферментов, включая нитрогеназу, позволяющую азотфиксирующим бактериям поглощать азот из воздуха, делая его доступным для растений [1, 5] .
- Он присутствует в растениях и животных в следовых количествах, помогая в синтезе и использовании белков, а также в других метаболических процессах [2] .
- Он действует как катализатор в организме человека для производства ферментов и расщепления аминокислот [2] .
Роль в научных исследованиях
- Хотя в настоящее время в океане много молибдена, в прошлом его было намного меньше.
 Таким образом, это четкий индикатор древней океанической химии и помогает исследователям оценить количество кислорода, которое могло присутствовать в течение определенного периода [2] .
Таким образом, это четкий индикатор древней океанической химии и помогает исследователям оценить количество кислорода, которое могло присутствовать в течение определенного периода [2] .
Молибден Токсичность
Хотя об острой токсичности молибдена у людей не сообщалось, исследования на животных показали, что высокие уровни элемента 42 могут влиять на способность организма поглощать медь и вызывать дефицит меди [12] . Горнодобывающие или металлурги, регулярно подвергающиеся воздействию молибденовой пыли и паров, могут страдать от головной боли, утомляемости, слабости, тремора, потливости, головокружения, потери веса, болей в суставах и мышцах и потери аппетита [13] .По данным NIOSH, IDLH (немедленная опасность для жизни и здоровья) для соединений молибдена составляет 5000 мг/м 3 [14] .
Интересные факты
- Молибден не реагирует с водой или кислородом при комнатной температуре [5] .

- Его оксид растворяется в щелочной воде и образует молибдатные соли [5] .
- Когда он встречается в соединениях, он обычно существует в степенях окисления (IV) и (VI) [5] .
- Вместо вольфрама в стальных сплавах часто используется молибден, потому что он имеет такой же металлический эффект, несмотря на то, что его плотность и атомный вес в два раза меньше, чем у вольфрама [2] .
- «Большая Берта», 47-тонное сверхтяжелое артиллерийское орудие, использовавшееся Германией в Первой и Второй мировых войнах, имело молибден в качестве одного из составных элементов своей стали [2] .
- Элемент графически представлен вентильным колесом, что указывает на его использование в котлах и вентилях [1] .
- В США добавки прописывают тем, кто не получает достаточного количества молибдена с пищей [15] .
Молибденовая проволока
Цена молибдена
Стоимость чистого молибдена составляет около 0,44 доллара США за грамм [5] .
Каталожные номера
- http://www.rsc.org/periodic-table/element/42/молибден
- https://www.livescience.com/34687-molybdenum.html
- https://образование.jlab.org/itselemental/ele042.html
- https://education.jlab.org/itselemental/iso042.html
- https://www.chemicool.com/elements/molybdenum.html
- http://periodictable.com/Elements/042/data.html
- http://chemistry-reference.com/q_elements.asp?Symbol=Mo
- https://www.imoa.info/molybdenum/molybdenum-products.php
- https://www.webqc.org/молекулярно-вес-оф-Мо.html
- https://webbook.nist.gov/cgi/inchi/InChI%3D1S/Mo
- http://веб.utk.edu/~prac/mse201/chp2.pdf
- https://www.msdvetmanual.com/toxicology/molybdenum-poisoning/overview-of-molybdenum-poisoning
- https://web.archive.org/web/20070919204536/http://rais.ornl.gov/tox/profiles/molybdenum_f_V1.shtml
- https://www.cdc.gov/niosh/npg/npgd0433.
 html
html - https://articles.mercola.com/sites/articles/archive/2016/10/17/molybdenum.aspx
Молибден, периодическая таблица, периодическая таблица элементов, периодическая таблица элементов, таблица
Интерактивная периодическая таблица 2001 – 2008 от ePeriodicTable.ком
Нам нужна ваша помощь! ePeriodicTable.com был разработан для быть бесплатным ресурсом, предназначенным для содействия пониманию химии, и быть полезный справочный инструмент для исследователей, студентов и ученых во всем мире. Мы ничего не берем на этом сайте , , но вы можете поддержать нас чрезвычайно, разместив ссылку на вашем сайте на нас. Вы можете копировать и вставлять этот код для ссылки на нас: таблица Менделеева
Мы очень благодарны за вашу поддержку!
Официальные интернет-ресурсы:
А
оптовая
дистрибьютор уникальных и натуральных
оптовая
продукты и товары для здоровья, такие как жидкие витамины натуральные пищевые добавки, помимо натуральных таблетки для похудения и стиральный порошок альтернатива шарикам для стирки. Попробуйте это очень эффективно бросить курить и продукт для отказа от курения, а также курить и прочее
здоровье
продукты прямо сейчас. Если вам нужно натуральное таблетки для похудения натуральные таблетки для похудения, содержащие худия гордони, специальность диетические продукты или даже информацию о на основе кортизола продукты для похудения и пищевые добавки, а также информация о оптовые пищевые добавки у них есть информация, которая вам нужна.
Попробуйте это очень эффективно бросить курить и продукт для отказа от курения, а также курить и прочее
здоровье
продукты прямо сейчас. Если вам нужно натуральное таблетки для похудения натуральные таблетки для похудения, содержащие худия гордони, специальность диетические продукты или даже информацию о на основе кортизола продукты для похудения и пищевые добавки, а также информация о оптовые пищевые добавки у них есть информация, которая вам нужна.
Получить бесплатно
информацию о том, как бросить курить, и узнать о таких продуктах, как никотиновая жевательная резинка и
никотиновый пластырь.Наслаждаться жидкие добавки и витамины
и популярный жидкие поливитамины. Посетите дистрибьютора шарик для стирки, используемый в качестве замены моющего средства. Вы можете получить
останавливаться
информация о курении, а также информация о всех натуральных
масса
таблетки потери. Получите специализацию
кортизол
информация о продукты для похудения, такие как кортислим и расслабиться и
прачечная
Сервисы.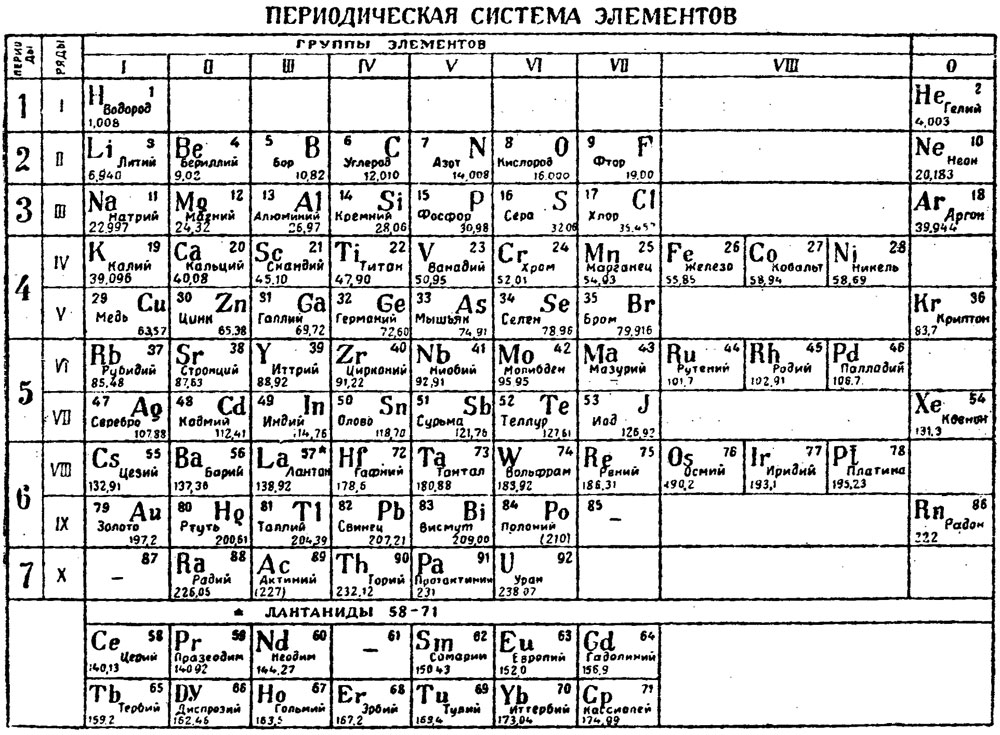
Вы можете наслаждаться зависимостью онлайн игры и ты можешь играть бесплатные игры на лучшем сайте игровых автоматов для увлекательные игры во всей сети.Для налогового сезона сравните налог программные продукты. Большое спасибо за посещение ePeriodicTable.com!
информация здесь доступна для только в образовательных целях. Мы не несем ответственности за неправильное использование или неправильное применение любую информацию, содержащуюся в настоящем документе, а также любые неточности.
Таблица Менделеева
Эй, ребята! Добро пожаловать в это видео Mometrix по периодической таблице.
Периодическая таблица элементов, несомненно, является одним из самых важных инструментов, которые вы будете использовать в химии.Благодаря своей инновационной организационной структуре таблица дает нам краткую и фундаментальную информацию не только о каждом отдельном элементе, но и о тенденциях, происходящих во всех элементах.
Давайте посмотрим на краткую историю Периодической таблицы.
История Периодической таблицы
В 1789 году французский химик Антуан Лоран Лавуазье определил элемент как фундаментальное вещество, которое нельзя разрушить никакими известными химическими средствами. Затем он приступил к составлению списка из 33 элементов, которые на самом деле не являются элементами; но он действительно подстегнул эту идею систематизации и понимания элементов.
В 1803 году английский химик Джон Дальтон использовал общее научное признание того, что элементы соединяются друг с другом в различных весовых соотношениях, для создания атомной теории, согласно которой все элементы состоят из переменного числа атомов водорода. Благодаря этой теории Дальтон создал шкалу атомного веса на основе атома водорода.
В 1869 году русский химик Дмитрий Менделеев систематически расположил элементы в таблице в соответствии с их атомным весом.Менделеев заметил то, чего не было ни у кого другого. Он понял, что существует ряд неизвестных элементов с атомным весом между уже открытыми элементами. Просто оставив отверстия для элементов, которые, по его мнению, не были обнаружены, он разработал организационную схему, которая вертикально группировала элементы с одинаковыми свойствами. Он обнаружил, что элементы с низким атомным весом имеют сходные химические характеристики, повторяющиеся через каждые семь элементов. Среди более тяжелых элементов он обнаружил, что характеристики повторяются через каждые семнадцать элементов.
Просто оставив отверстия для элементов, которые, по его мнению, не были обнаружены, он разработал организационную схему, которая вертикально группировала элементы с одинаковыми свойствами. Он обнаружил, что элементы с низким атомным весом имеют сходные химические характеристики, повторяющиеся через каждые семь элементов. Среди более тяжелых элементов он обнаружил, что характеристики повторяются через каждые семнадцать элементов.
Захватывающее открытие того, что физические и химические характеристики элементов являются периодическими функциями их атомного веса, стало известно как периодический закон. В 1879 году периодическая таблица Менделеева получила широкое признание, когда она предсказала существование галлия, германия и скандия.
С тех пор в таблицу были внесены небольшие изменения, и было добавлено много-много элементов.
Теперь давайте посмотрим, как читать периодическую таблицу.
Чтение таблицы Менделеева
| \ (\ DownArrow \) | |||||||||||||||||
| \ (\ DownArrow \) | |||||||||||||||||
Вертикальные столбцы, которые идут вверх и вниз, называются группами. Горизонтальные ряды, идущие из стороны в сторону, называются периодами. Есть 18 групп и 7 периодов.
Горизонтальные ряды, идущие из стороны в сторону, называются периодами. Есть 18 групп и 7 периодов.
Теперь давайте посмотрим на все содержимое отдельных коробок. Число в верхней части поля представляет собой атомный номер. Атомный номер водорода равен 1, а атомный номер урана — 92. Буква в середине — это атомный символ. Таким образом, для водорода это H, а для урана это U. Важно знать атомный символ, потому что не все таблицы имеют имена, перечисленные ниже; плюс, именно так ученые обозначают элементы в своих письмах.Как правило, символ атома соответствует названию, как C относится к углероду, но иногда это не так. Например, ртуть обозначается как Hg. Число внизу обозначает атомную массу. Водород имеет атомную массу 1,0079, а уран имеет атомную массу 238,029.
При последовательном перемещении из левого верхнего угла в правый нижний по таблице Менделеева атомный номер увеличивается. Атомный номер представляет собой точное место в периодической таблице элемента. Но, самое главное, атомный номер такой же, как и количество протонов в ядре атома элемента, а также столько же электронов, которые окружают ядро, когда оно находится в нейтральном состоянии. Например, водород имеет один протон и один электрон, а уран имеет 92 протона и 92 электрона.
Например, водород имеет один протон и один электрон, а уран имеет 92 протона и 92 электрона.
Атом также содержит нейтроны, наряду с протонами внутри своего ядра. Атомная масса или атомный вес элемента представляет собой общее количество протонов и нейтронов в ядре.
Важно отметить, что атомы некоторых элементов имеют разные версии, что просто означает, что элементы содержат атомы с разным числом нейтронов в ядре. Их называют изотопами.Атомный вес в этом случае представляет собой среднее значение атомных массовых чисел различных изотопов.
Металлы, неметаллы и полуметаллы
Элементы могут быть организованы по группам или периодам, но их также можно разделить на три основные категории: металлы, неметаллы и полуметаллы.
Металлы обычно представляют собой блестящие твердые вещества (хотя ртуть является жидкостью при комнатной температуре) и часто ковкие.Более половины из неметаллов являются газообразными при нормальных температурах.
Полуметаллы или металлоиды, как следует из названия, существуют между металлами и неметаллами.
Я описал более общие тенденции. Существует ряд дополнительных периодических тенденций, таких как сродство к электрону, электроотрицательность , размер атома и энергия ионизации .
Надеюсь, это видео поможет вам лучше ориентироваться в периодической таблице! Увидимся в следующий раз!
Молибден Электронная конфигурация (Mo) с орбитальной диаграммой
Электронная конфигурация молибдена : В нынешнем сценарии, когда новые химические элементы открываются очень быстрыми темпами, более важно исследовать эти химические элементы.Электронная конфигурация — единственный способ понять и упростить химическую реакцию этих элементов. Сегодня в этой статье мы собираемся обсудить электронную конфигурацию молибдена.
Электронная конфигурация молибдена
Молибден — это химический элемент, который не встречается в естественной форме на Земле, поскольку он образуется в результате окисления минералов. Этот химический элемент используется в качестве твердых и стабильных карбидов в сплаве.
Этот химический элемент используется в качестве твердых и стабильных карбидов в сплаве.
Электронная конфигурация молибдена подразумевает распределение электронов молибдена в атомных молекулах.Эта электронная конфигурация молибдена помогает химику и другому ученому понять химическую реакцию молибдена, чтобы его можно было использовать в соответствующих целях.
Электронная конфигурация молибдена?
Электронная конфигурация молибдена может быть представлена как молибден, имеющий атомный номер 42 и расположенный в группе 6 периода 5 периодической таблицы.
Эта электронная конфигурация Мо находится в конденсированной форме и в основном состоянии.Молибден дополнительно удерживает 42 электрона в своей оболочечной структуре 2.8.18.13.1
.Сколько валентных электронов у молибдена?
Молибден является одним из таких элементов, который имеет очень мягкую физическую структуру и считается очень пластичным. Этот химический элемент способен удерживать один Электрон в 5S и еще пять Электронов в 4d оболочках. Вся эта структура придает молибдену валентность 0,2+,3+,4+,5+ и 6+.
Этот химический элемент способен удерживать один Электрон в 5S и еще пять Электронов в 4d оболочках. Вся эта структура придает молибдену валентность 0,2+,3+,4+,5+ и 6+.
Молибден Число валентных электронов
Как мы объяснили выше, молибден имеет валентность 0,2+,3+,4+,5+ и 6+.
Простым объяснением этой валентности молибдена является способность этого химического элемента. Он может использовать один электрон в оболочке 5s, а затем он может использовать 5 электронов в оболочке 4d из-за его чрезвычайной гибкости, уникальной в своем роде.
.

 тв]
тв] хр.бц]
хр.бц]