Таблица Менделеева online – Ni
Ni
28
2
16
8
2
58.69±1
3d84s2
Никель
| Относительная электроотрицательность (по Полингу): | 1,75 |
| Температура плавления: | 1042°C |
| Температура кипения: | 3000°C |
| Теплопроводность: | 0 |
| Плотность: | 6,475 г/см3 |
| Открыт: | Д. Маринский, Л. Гленденин, К. Д. Корьелл |
| Цвет в твёрдом состоянии: | Металлический |
| Тип: | Редкоземельный |
| Орбитали: | 1s22s22p63s23p63d104s24p64d104f55s25p65d05f06s2 |
| Электронная формула: |
Ni – 1s2 2s2 2p Ni – [Ar] 4s2 3d8 |
| Валентность: | (+1), +2, (+3), (+4) |
| Степени окисления: | 0, +II, III |
| Сверхпроводящее состояние при температуре: | 0 К |
| Потенциалы ионизации: | 10,903 В 22,283 В |
Электропроводность в тв. фазе: фазе: |
|
| Ковалентный радиус: | 1,63 Å |
| Атомный объем: | 22,39 см3/моль |
| Атомный радиус: | 2,62 Å |
| Теплота распада: | |
| Теплота парообразования: | |
| Кристаллическая структура: | Гексагональная. Радиус описанной вокруг основания окружности не равен высоте фигуры. Боковая сторона перпендикулярна основанию |
Реклама
Изотопы
| Символ нуклида |
Z(p) | N(n) | Масса изотопа (а. е. м.) |
Период полураспада |
Спин и чётность ядра |
|---|---|---|---|---|---|
| Энергия возбуждения | |||||
| 48Ni | 28 | 20 | 48,01975 | 10 мс | 0+ |
| 49Ni | 28 | 21 | 49,00966 | 13 мс | 7/2- |
| 50Ni | 28 | 22 | 49,99593 | 9,1 мс | 0+ |
| 51Ni | 28 | 23 | 50,98772 | 30 мс | 7/2- |
| 52Ni | 28 | 24 | 51,97568 | 38 мс | 0+ |
| 53Ni | 28 | 25 | 52,96847 | 45 мс | 7/2- |
| 54Ni | 28 | 26 | 53,95791 | 104 мс | 0+ |
| 55Ni | 28 | 27 | 54,951330 | 204,7 мс | 7/2- |
| 56Ni | 28 | 28 | 55,942132 | 6,075 сут | 0+ |
| 57 |
28 | 29 | 56,9397935 | 35,60 ч | 3/2- |
| 58Ni | 28 | 30 | 57,9353429 | стабилен | 0+ |
| 59Ni | 28 | 31 | 58,9343467 | 76 тыс. лет лет |
3/2- |
| 60Ni | 28 | 32 | 59,9307864 | стабилен | 0+ |
| 61Ni | 28 | 33 | 60,9310560 | стабилен | |
| 62Ni | 28 | 34 | 61,9283451 | стабилен | 0+ |
| 63Ni | 28 | 35 | 62,9296694 | 100,1 лет | 1/2- |
| 63mNi | 87,15 кэВ | 1,67 мкс | 5/2- | ||
| 64Ni | 28 | 36 | 63,9279660 | стабилен | 0+ |
| 65Ni | 28 | 37 | 64,9300843 | 2,5172 h | 5/2- |
| 65mNi | 69 мкс | 1/2- | |||
| 66Ni | 28 | 38 | 65,9291393 | 54,6 ч | 0+ |
| 67Ni | 28 | 39 | 66,931569 | 21 с | 1/2- |
| 67mNi | 1,007 МэВ | 13,3 мкс | 9/2+ | ||
| 68Ni | 28 | 40 | 67,931869 | 29 с | 0+ |
| 68m1Ni | 1,7700 МэВ | 276 нс | 0+ | ||
| 68m2Ni | 2,8491 МэВ | 860 мкс | 5- | ||
| 69Ni | 28 | 41 | 68,935610 | 11,5 с | 9/2+ |
| 69m1Ni | 321 кэВ | 3,5 с | 1/2- | ||
| 69m2Ni | 2,701 МэВ | 439 нс | 17/2- | ||
| 70Ni | 28 | 42 | 69,93650 | 6,0 с | 0+ |
| 70mNi | 2,860 МэВ | 8+ | |||
| 71Ni | 28 | 43 | 70,94074 | 2,56 с | 1/2- |
| 72Ni | 28 | 44 | 71,94209 | 1,57 с | 0+ |
| 73Ni | 28 | 45 | 72,94647 | 840 мс | 9/2+ |
| 74Ni | 28 | 46 | 73,94807 | 680 мс | 0+ |
| 75Ni | 28 | 47 | 74,95287 | 600 мс | 7/2+ |
| 76Ni | 28 | 48 | 75,95533 | 470 мс | 0+ |
| 77Ni | 28 | 49 | 76,96055 | 300 мс | 9/2+ |
| 78Ni | 28 | 50 | 77,96318 | 110 мс | 0+ |
Самая большая в Европе таблица Менделеева
23 июля в рамках мероприятий, посвященных 65-летнему юбилею ОИЯИ и города Дубны, состоится торжественное открытие панно «Периодическая таблица Д. И. Менделеева». Ее площадь составляет более 284 кв. м, что делает ее самой большой в Европе.
И. Менделеева». Ее площадь составляет более 284 кв. м, что делает ее самой большой в Европе.
Таблица расположена на стене плавательного бассейна «Архимед» на набережной Волги и будет хорошо видна как жителям и гостям города, так и пассажирам многочисленных круизных теплоходов, проплывающих по реке. Таблица отражает выдающийся вклад ученых подмосковной Дубны в открытие новых химических элементов и призвана способствовать повышению интереса общества к достижениям современной науки.
Об идее создания панно мы побеседовали с Юрием Цолаковичем Оганесяном – специалистом в области экспериментальной ядерной физики, академиком РАН, научным руководителем Лаборатории ядерных реакций имени Г. Н. Флерова в Объединенном институте ядерных исследований. Под руководством Юрия Цолаковича в Дубне получены все известные к настоящему времени сверхтяжелые элементы от 113-го до 118-го, последний из которых назван в честь ученого – оганесон.
— Юрий Цолакович, в день рождения нашего наукограда состоится знаковое событие – открытие в Дубне самой большой в мире таблицы Менделеева на фасаде бассейна «Архимед».
— Да, это панно станет новой достопримечательностью нашего города. У Дубны славная история: когда построили канал, то здесь установили памятник Ленину работы великого скульптора С. Д. Меркурова, затем был снят кинофильм «Волга-Волга» с Любовью Орловой – часть съемок прошла на канале Москва-Волга и Московском море, а теперь на набережной будет столь знаменательный объект – панно «Периодическая таблица Менделеева».
— Панно – не просто украшение, это прежде всего популяризация науки, своеобразный рассказ дубненцам и гостям города о достижениях ОИЯИ.
— Именно так. Здесь, в Дубне, великое открытие Менделеева имело продолжение – учеными ОИЯИ синтезированы новые химические элементы. Таблица, которую будет видно пассажирам всех проплывающих по Волге теплоходов, отражает выдающийся вклад ученых нашего города в развитие науки и, надеюсь, будет способствовать повышению интереса прежде всего молодежи к новым научным достижениям.
Достопримечательность всегда имеет много граней. На панно можно смотреть с архитектурной, документальной, познавательной, с глубоко научной точек зрения. Мы увидим, как Таблица будет меняться, какие элементы еще будут появляться и так далее.
На панно можно смотреть с архитектурной, документальной, познавательной, с глубоко научной точек зрения. Мы увидим, как Таблица будет меняться, какие элементы еще будут появляться и так далее.
— На Ваш взгляд, наступит ли время, когда Периодическая таблица Менделеева заполнится и замкнется?
— Вообще, ядерной физике сто с небольшим лет. Говоря об элементах, следует вспомнить, что, когда в марте 1869 года Менделеев отдал свой труд в печать, считалось, что элементы, сколько бы их ни было, являются кирпичиками мироздания, и мир построен из этих элементов. И они, эти кирпичики, неделимы. Их еще Демокрит за 400 лет до нашей эры назвал атомами, тогда это было чисто философское понятие.
А у великого ученого Дальтона – 1808 год, когда было известно всего 36 элементов, – кирпичики соединяются в молекулы, далее в более сложные формы – кристаллы. Всего 36 элементов, как буквы алфавита. И этими буквами вы можете описать все что угодно.
Но, когда Менделеев начал исследовать свойства этих элементов, их было уже 63, он заметил, что свойства этих элементов периодически повторяются. Однако такое поведение явно не согласуется с понятием «кирпичики мироздания». Буквы в алфавите не должны быть похожи друг на друга! А если они похожи, подчиняясь какой-то закономерности, то это значит, что они сами имеют сложную структуру, которая, собственно, и дает эту периодичность…
Однако такое поведение явно не согласуется с понятием «кирпичики мироздания». Буквы в алфавите не должны быть похожи друг на друга! А если они похожи, подчиняясь какой-то закономерности, то это значит, что они сами имеют сложную структуру, которая, собственно, и дает эту периодичность…
Менделеев понял, что рассматриваемый набор элементов – это не кирпичики мироздания. Он стал искать эфир, в котором рождаются элементы, и был целиком поглощен поисками этих истоков материального мира. А таблица осталась. И теперь, как ни странно, 150 лет спустя, мы стали задаваться теми же вопросами: что такое таблица и как толкуется периодичность, что будет дальше, могут ли быть какие-то элементы более тяжелыми, можно ли считать элементы, которые созданы искусственно, настоящими?
Если мы пойдем дальше, то сам закон будет видоизменяться, потому что, согласно теории относительности, если электроны будут двигаться вокруг этого ядра со скоростью, близкой к скорости света, то станет расти их масса, и это должно быть учтено. По этой причине орбиты будут уплотняться, и тогда самая последняя орбита, где крутится тот самый электрон, который ответственен за химические свойства, изменит свои характеристики.
По этой причине орбиты будут уплотняться, и тогда самая последняя орбита, где крутится тот самый электрон, который ответственен за химические свойства, изменит свои характеристики.
Благодаря этим открытиям весь научный мир еще раз убедился, что можно сделать то, что раньше казалось невозможным. Большой прогресс случится, когда начнут строить квантовые компьютеры, это уже мы говорим о технике, а вот как это будет выглядеть… Есть разные сценарии, они зависят от указанного взаимодействия и эффектов теории относительности. Этим мы будем заниматься, это большой путь, сейчас пока мы поняли, что те средства, которые использовали для открытия новых элементов, не годятся, чтобы идти дальше. Сейчас все развивается очень быстро: то, что на данный момент считается передним краем науки, через 10 лет будет обычным делом.
— То есть процесс поиска новых элементов бесконечен…
— Таблица сама по себе неисчерпаема. Она продолжает жить в научном мире, будут добавляться элементы, открываться новые ее формы, строиться новые лаборатории по поиску элементов.
— Юрий Цолакович, любопытно, при каких обстоятельствах возникла сама идея? С чем связан выбор пространства для размещения панно?
— Подобные таблицы уже есть в мире, в Испании, например, она занимает площадь 150 квадратных метров – наша будет больше! Я показал эту таблицу Виктору Анатольевичу Матвееву в 2017 году, тогда мы обсуждали возможность ее появления на заднем фасаде Дома культуры «Мир». Я иногда гуляю по этому парку, сажусь на скамейку как раз напротив. И однажды подходит ко мне Андрей Владимирович Тамонов, и мы обсуждаем, что бы такое монументальное сделать на этой стене. И я посвящаю его в свою идею. А когда я поделился мыслями с Григорием Владимировичем Трубниковым, то он уже имел это в планах, только имел в виду фасад бассейна, чтобы было видно с Волги.
— Если говорить о деталях создания панно – как разрабатывался дизайн, почему он именно такой? Познавательный аспект превыше остального и главенствует в данном объекте?
— Если Вы поищете таблицу Менделеева в интернете – там их огромное количество, по-моему, 1500 видов. Таблица имеет разные формы, из всех мы с Сергеем Николаевичем Дмитриевым выбрали ту, которая имеет научное содержание. Панно «Периодическая таблица имени Д. И. Менделеева» сделано не просто декоративно, но и содержательно с точки зрения науки.
Таблица имеет разные формы, из всех мы с Сергеем Николаевичем Дмитриевым выбрали ту, которая имеет научное содержание. Панно «Периодическая таблица имени Д. И. Менделеева» сделано не просто декоративно, но и содержательно с точки зрения науки.
Наша Таблица будет очень хорошо смотреться ночью, с подсветкой. Кроме того, рядом слева есть свободное поле, на нем можно транслировать лекции, рассказывать об истории открытия элементов, об их химических свойствах, а на правой стороне демонстрировать различные элементы Таблицы.
— Юрий Цолакович, круг Ваших научных интересов описан не в одной статье. А что помогает Вам отвлекаться от рабочего процесса, от науки. Может быть, театральное, музыкальное искусство?
— Все, о чем Вы сейчас сказали, – это все духовное: и мышление, и творчество связаны с духовностью человека. Вы знаете, мне часто задают вопрос, на который сложно отвечать. Меня спрашивают о пользе открытия элементов. Это неосязаемое понимание, которое нельзя купить или продать, оно приходит как открытие, ты вдруг по-новому видишь мир.
— Насколько, на Ваш взгляд, взаимосвязаны наука и культура?
— Одно без другого очень бедно, и, безусловно, они взаимосвязаны. Поэтому своим ученикам я говорю – оставьте ваши книги, забудьте о них на некоторое время, идите в театр, послушайте музыку, посмотрите, что делается вокруг. Это так важно, это расширяет горизонты.
— После соприкосновения с искусством ученые возвращаются к работе уже другими людьми?
— Именно так: я им говорю, что могу все простить, но не могу простить того, если они ничего не знают, кроме своей области. Тогда они и в будущем мало что узнают и откроют.
Если посмотреть на ученых прошлого, они были многогранны. Тот же Менделеев – он не был членом Академии наук, а был членом Академии художеств! Он жил в квартире, выделенной петербургским университетом, и в ней по субботам принимал гостей, накрывая стол белой скатертью. А потом, когда они собирались расходиться, Дмитрий Иванович просил, чтобы они на этой скатерти расписались. А дальше его жена вышивала эти подписи – Репин, Мусоргский, кто только там не был! Это потрясающе. Он устраивал на Соловках раз в месяц семинары. И один из них был посвящен цвету. Приглашал физиков, химиков, артистов, художников, театральных деятелей, и каждый из них выступал на этом семинаре, рассказывал, что он понимает под словом «цвет».
А дальше его жена вышивала эти подписи – Репин, Мусоргский, кто только там не был! Это потрясающе. Он устраивал на Соловках раз в месяц семинары. И один из них был посвящен цвету. Приглашал физиков, химиков, артистов, художников, театральных деятелей, и каждый из них выступал на этом семинаре, рассказывал, что он понимает под словом «цвет».
Физик говорит, что это излучение, химик – что это смешение таких-то компонентов, художник рассуждал, как красный цвет напоминает ему кровь и он не может спокойно смотреть на красные полотнища. И это все интересно людям. В этом смысле, конечно, то что в Дубне будет такая достопримечательность – панно «Периодическая таблица Менделеева» – это замечательно. Будут разные люди смотреть на нее со своей точки зрения, по-разному воспринимать – это очень хорошо!
Беседовала Элеонора Ямалеева
Фотографии Елены Пузыниной
Источник – еженедельник ОИЯИ «Дубна: Наука. Содружество. Прогресс»
Дмитрий Менделеев: «Я думал над ней 20 лет …»
2 февраля 2017 года исполнилось 110 лет со дня смерти гениального химика, «отца» периодической таблицы химических элементов Дмитрия Менделеева.
Редакция портала «Российское образование» вспомнила историю формирования периодической таблицы и интересные факты, связанные с ее открытием.
В поисках единой концепции
Ушло не одно столетие на безуспешные поиски ученых всех стран обнаружить закономерность среди химических элементов. Исследователи старались «подогнать» их под имевшиеся схемы, что, само собой, не приносило желаемых результатов. Менделеев же был уверен, что существует общий закон природы, который связан с массой атома и определяет все сходства и различия элементов между собой.
Советский публицист Олег Писаржевский описывает работу ученого таким образом:
«Он помог успеху своих поисков простым и наглядным приемом. Он воспользовался запасом ненужных визитных карточек – узеньких полосок картона. Из этих картонных карточек он составил нечто вроде подвижной картотеки элементов. На обороте каждой карточки он записал под названием элемента его атомный вес и формулы основных соединений, которые данный элемент образует с другими. <…> Разложив перед собой эти карточки, комбинируя их во всевозможных сочетаниях, сопоставляя их между собой по свойствам элементов, он с большой легкостью мог охватить умственным взором всю совокупность элементов со всем сложным переплетением их свойств. Все более отчетливо проявлялись в его сознании признаки системы, которой подчинялось все это пестрое разнородное собрание земных тел».
<…> Разложив перед собой эти карточки, комбинируя их во всевозможных сочетаниях, сопоставляя их между собой по свойствам элементов, он с большой легкостью мог охватить умственным взором всю совокупность элементов со всем сложным переплетением их свойств. Все более отчетливо проявлялись в его сознании признаки системы, которой подчинялось все это пестрое разнородное собрание земных тел».
Вокруг открытия ученого сочиняли множество легенд. Одна из них – знаменитая таблица Менделееву приснилась. Сложно поверить в то, что можно с такой легкостью совершать научные открытия. Менделеев только смеялся над абсурдностью этого предположения.
«Я над ней, может быть, двадцать лет думал, а вы говорите: сидел и вдруг … готово!», – комментировал он.
Писаржевский писал по этому поводу:
«Менделеев действительно не раз вспоминал о том, как он часами переставлял элементы в рядах, вчитываясь в свои заметки до ряби в глазах. Голова у него кружилась от напряжения. Ведь когда с места на место перекладывались легкие карточки с названиями веществ, в сознании исследователя приходили в движение целые эшелоны сведений об этих веществах. <…> И даже когда, утомленный, он засыпал за своими размышлениями, неугомонная, бессонная мысль продолжала биться в мозгу исследователя. И весьма возможно, что именно в тот момент, когда более поверхностные, мешающие раздражители были заторможены сном, свободно и до конца оформилось то наблюдение, которое было подготовлено годами труда и уже складывалось в сознании».
<…> И даже когда, утомленный, он засыпал за своими размышлениями, неугомонная, бессонная мысль продолжала биться в мозгу исследователя. И весьма возможно, что именно в тот момент, когда более поверхностные, мешающие раздражители были заторможены сном, свободно и до конца оформилось то наблюдение, которое было подготовлено годами труда и уже складывалось в сознании».
В 1869 году таблица имела пустующие ячейки. Менделеев специально оставил свободные места для новых элементов, которые, по его предположению, должны были найти в будущем. Основываясь на свойствах «соседей» по периодической таблице, ученый даже довольно точно описал еще неоткрытых три элемента. И вскоре свободные ячейки заняли галлий, скандий и германий.
Появление радия
Еще в течение многих лет периодическая таблица дополнялось новыми элементами. 26 декабря 1898 года лауреат Нобелевской премии по физике Пьер Кюри представил во Французской Академии наук радий в виде смеси с барием. Вместе со своей супругой Марией они получили из отходов, остающихся после выделения урана из урановой руды, сильнорадиоактивный элемент – радий.
В то время никто не знал о смертельной опасности радиации, и новый элемент сделали панацеей чуть ли не от всех болезней. Радий включили в состав пищевых продуктов, зубной пасты, кремов для лица. Его рекомендовали врачи в качестве средства для снятия стресса. А богачи щеголяли в часах, циферблат которых был окрашен краской, содержащей радий.
Сегодня этот элемент используют в медицине для кратковременного облучения при лечении ряда злокачественных заболеваний.
«Лжеэлементы»: небулий и короний
Некоторые химические элементы не укладывались в концепцию периодического закона и были признаны несуществующими. Так в начале 20 века случилось с небулием и коронием.
При исследовании солнечной атмосферы астрономы обнаружили спектральные линии, которые им не удалось отождествить ни с одним из известных на земле химических элементов. Ученые предположили, что эти линии принадлежат новому элементу, который получил название короний (потому что линии были обнаружены при исследовании «короны» Солнца – внешнего слоя атмосферы звезды).
Спустя несколько лет астрономы сделали еще одно открытие, изучая спектры газовых туманностей. Обнаруженные линии, которые снова не удалось отождествить ни с чем земным, приписали другому химическому элементу – небулию.
Открытия подверглись критике, поскольку в периодической таблице Менделеева уже не оставалось места для элементов, обладающих свойствами небулия и корония. После проверки обнаружилось, что небулий является обычным земным кислородом, а короний – сильно ионизированное железо.
Дмитрий Менделеев считал, что «периодическому закону – будущее не грозит разрушением, а только надстройки и развитие обещает». Его изобретение и по сей день по всеобщему признанию является основным законом химии.
Точное место элементов в таблице Менделеева. О чем рассказывает свет
Точное место элементов в таблице Менделеева
Некоторые химические элементы стоят в таблице Менделеева не в порядке возрастания атомных весов. Таковы три группы элементов: № 18 — аргон (атомный вес 39,9) и № 19 — калий (атомный вес его меньше — 39,1), далее № 27 — кобальт (атомный вес 58,9) и № 28 — никель (атомный вес его меньше — 58,7), а также № 52 — теллур (атомный вес — 127,1) и № 53 — иод (атомный вес его меньше — 126,9).
Менделеев поставил указанные элементы в свою таблицу сообразно их химическим свойствам, в той последовательности, в какой они здесь перечислены. Атомные веса соседних элементов (например, кобальта и никеля) мало отличаются друг от друга. Среди химиков долго шли споры. Одни говорили, что в этих случаях нарушается периодический закон. Другие утверждали, что нарушения периодического закона нет, а просто у этих элементов неправильно определен атомный вес. Но сколько ни уточняли химики атомные веса этих элементов, всегда оказывалось, что аргон, кобальт и теллур соответственно тяжелее калия, никеля и иода. И все же в таблице Менделеева они стояли впереди калия, никеля и иода в нарушение стройности всей таблицы, как тогда думали.
В те времена и до конца жизни Менделеева (1910) наука еще ничего не знала ни о зарядах атомных ядер, ни о частотах рентгеновских излучений и тем более о законе возрастания этих частот с увеличением заряда атомных ядер. Закон Мозели был открыт уже после смерти Менделеева.
Когда все эти открытия были сделаны, рентгеновские спектры показали, что Менделеев совершенно правильно определил последовательность указанных элементов. Как теперь установлено, данная Менделеевым последовательность элементов соответствует возрастанию зарядов атомных ядер. Химические свойства элементов больше зависят от заряда атомных ядер, чем от атомных весов. Позднее ученые обнаружили даже такие элементы, у которых атомный вес немного отличался, но заряд ядер был один и тот же. И химические свойства их были тоже почти одинаковы. Такие элементы называют изотопами. Все изотопы стоят в одной клетке таблицы Менделеева (изотоп — слово греческое, означает «занимающий то же место»). Почти каждый элемент имеет несколько изотопов. Химики же определяли ранее не точный атомный вес элемента, а лишь средний атомный вес, т. е. атомный вес для смеси, состоящей из изотопов. Нарушив в своей таблице в трех случаях порядок возрастания атомных весов, Менделеев сохранил порядок, соответствующий закону периодичности химических свойств элементов. Но тем самым, как оказалось впоследствии, Менделеев сохранил последовательность возрастания ядерных зарядов.
Но тем самым, как оказалось впоследствии, Менделеев сохранил последовательность возрастания ядерных зарядов.
Вот замечательный пример того, как важно быть объективным в науке и не поддаваться соблазну подогнать факты (атомные веса) под «закон» (возрастания атомных весов в периодической таблице), который, казалось бы, был уже вот-вот нащупан, так как оправдывался для 97% элементов! В этой объективности проявляется сила подлинной науки и мужество настоящих ученых.
Это также и пример того, что в науке исключения из установленных ранее правил всегда ведут к раскрытию новых, более общих, закономерностей.
Уверенность Менделеева в справедливости открытого им великого закона природы — закона (периодичности химических свойств — оправдалась и в этом случае. Она была подтверждена также и спектральным анализом рентгеновских излучений.
Мысли Менделеева о структуре атома
1869 год. 6 марта
«Менделеев… совершил научный подвиг, который смело можно поставить рядом с открытием Леверье, вычислившего орбиту еще неизвестной планеты — Нептун».Ф. ЭНГЕЛЬС
Был или не был порядок?
о второй половине прошлого века наука какому пила уже довольно много
6 марта
«Менделеев… совершил научный подвиг, который смело можно поставить рядом с открытием Леверье, вычислившего орбиту еще неизвестной планеты — Нептун».Ф. ЭНГЕЛЬС
Был или не был порядок?
о второй половине прошлого века наука какому пила уже довольно много
Одно и то же место или нет?
Одно и то же место или нет? Нередко мы говорим, что, дескать, такие-то два события произошли в одном и том же месте, и так привыкли к этому, что склонны приписывать своему утверждению абсолютный смысл. А на самом деле оно ровно ничего не значит! Это все равно что сказать:
Спектрограф подтверждает предсказания Менделеева
Спектрограф подтверждает предсказания Менделеева В эти же годы великий русский ученый Д. И. Менделеев (1834—1907) изучал связь химических свойств элементов с их атомными весами. Он нашел, что если расположить все элементы в один ряд по возрастающим весам их атомов, начиная с
Рентгеновский спектр неоткрытых элементов
Рентгеновский спектр неоткрытых элементов
Наконец изучение закономерностей рентгеновских спектров привело к открытиям новых элементов. Мы видим, что по частоте рентгеновского излучения серии К у какого-нибудь элемента можно установить, каков заряд ядра у его атомов, в
Мы видим, что по частоте рентгеновского излучения серии К у какого-нибудь элемента можно установить, каков заряд ядра у его атомов, в
Заполнение пробелов в менделеевской таблице
Заполнение пробелов в менделеевской таблице Уже были открыты и получены заурановые элементы нептуний и плутоний, уже нашли им область применения, а в менделеевской таблице по-прежнему оставались незаполненные клетки.К двадцатым годам нашего столетия учёным были
ГЛАВА 17. ВАКАНТНОЕ МЕСТО ТОП–МОДЕЛИ
ГЛАВА 17. ВАКАНТНОЕ МЕСТО ТОП–МОДЕЛИ В январе 2010 г. мои коллеги собрались в Южной Калифорнии на конференцию, чтобы обсудить проблемы физики элементарных частиц и поиск скрытой массы в эпоху БАКа. Организатор конференции Мария Спиропулу — ученый–экспериментатор на CMS и
Вторая глава Место геометрии в мироздании
Вторая глава Место геометрии в мироздании На протяжении почти двух с половиной тысяч лет в европейской, точнее, в западной традиции изучение геометрии было обязательным, поскольку сложно себе представить более изящную, безупречную, образцовую истину, доступную нам вне
7.
 1. Определение предварительной орбиты и ее последующие уточнения. Оценка точности элементов орбиты
1. Определение предварительной орбиты и ее последующие уточнения. Оценка точности элементов орбиты7.1. Определение предварительной орбиты и ее последующие уточнения. Оценка точности элементов орбиты Для выделения потенциально опасных астероидов из общего числа АСЗ, для оценки вероятности столкновения их с Землей и предотвращения столкновений первостепенное
«Рабочее место» физиков в XVII–XIX ВЕКАХ
«Рабочее место» физиков в XVII–XIX ВЕКАХ Ничего похожего на современные лаборатории в то время не было. В прошлом физик работал в одиночку. Приборы обычно покупались на собственные деньги или изготовлялись самими учеными. Нередко лабораториями служили частные комнаты.
Таблица Менделеева: значение и структура
Добавлено: 17 сентября 2021 в 18:40
Содержание
Таблица Менделеева — форма записи, которая в удобной форме объединяет обнаруженные человеком химические элементы (в том числе и вновь открываемые и официально признанные международным сообществом). Это азбука химии, которая дает представление о свойствах и разнообразии «простейших веществ».
Это азбука химии, которая дает представление о свойствах и разнообразии «простейших веществ».
Таблица или Периодическая система химических элементов — то, что должен уметь «читать» современный выпускник школы. Именно с нее начинается погружение в предмет на уроках или курсах химии для школьников.
В 1869 году Дмитрий Менделеев работал над вторым томом своего учебника. Первый том был сдан «в печать», но над вторым пришлось призадуматься, ведь ученый не знал, как лучше классифицировать химические элементы. Впрочем, проблема позже превратилась в колоссальное открытие, которое прославило фамилию Менделеева не только в химической науке.
Все школьники помнят, что автор увидел свою таблицу во сне, а многие думают, что на этом заслуга химика и оканчивается.
В реальности все оказалось совсем не так, ведь за первым вариантом таблицы стоит колоссальный умственный труд по систематизации свойств элементов. Плоды этого труда были представлены в докладе Русскому химическому обществу, где прозвучал основной принцип организации таблицы: периодический, отражающий общность свойств сгруппированных в ней элементов.
Естественно, до Менделеева многие химики пытались упорядочить химические элементы (или то, что они считали таковыми) в поисках определенной закономерности. Менделеев понял, что физические и химические свойства элементов связаны с их атомной массой «периодическим» способом, и расположил их так, что группы элементов с аналогичными свойствами попадали в вертикальные столбцы в его таблице.
Таблица Менделеева: значение и структура
Предложенная автором система также не стала однозначным ответом, но она содержала признаки научного закона. При работе над таблицей Менделеев в определенных местах оставил пробелы, так как не нашел подходящего кандидата на конкретную позицию. Вместе с тем химику в голову пришла еще одна блестящая идея: он понял, что нужный элемент просто не открыли.
На основании своего подхода он смог определить атомную массу недостающих элементов и, таким образом, предсказать их свойства. Например, он предсказал свойства галлия, который был открыт в 1875 году.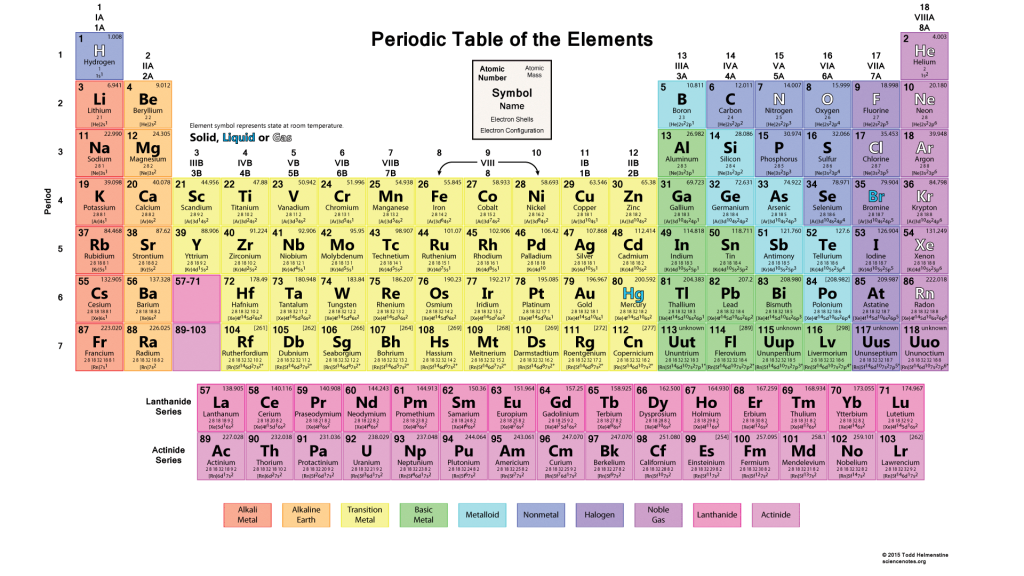 Позже были обнаружены два других предсказанных элемента, что еще раз подтвердило адекватность таблицы Менделеева. Когда ученые обнаружили недостающие части паззла с предсказанными Менделеевым характеристиками, периодическая система стала не просто таблицей, а инструментом для изучения химии.
Позже были обнаружены два других предсказанных элемента, что еще раз подтвердило адекватность таблицы Менделеева. Когда ученые обнаружили недостающие части паззла с предсказанными Менделеевым характеристиками, периодическая система стала не просто таблицей, а инструментом для изучения химии.
Характеристики таблицы Менделеева
Ни первая попытка ученого построить периодическую систему, ни его самая популярная таблица 1870 года не очень похожа на таблицу Менделеева, которая сегодня висит на стене большинства кабинетов химии или появляется на обложках учебников. Существует около тысячи различных ее версий. Современные таблицы расширены за пределы первоначальных 63 элементов. Большинство текущих вариантов содержит 108 или 109 элементов.
Таблица Менделеева: значение и структура
В таблице химические элементы располагаются в порядке возрастания атомного номера. Они сгруппированы в столбцы (группы) и строки (периоды), что отражает их особенности:
- в группах представлены элементы со сходными химическими свойствами, что обусловлено электронными конфигурациями на их валентных оболочках.
 К примеру, в 1-й группе собраны щелочные металлы от лития до франция, у которых на внешней оболочке имеется один электрон. Его очень легко «оторвать» от атома, поэтому щелочные металлы являются сильными восстановителями. С ростом порядкового номера элемента в группах растут металлические и восстановительные свойстваа, увеличивается атомный радиус, снижается электроотрицательность;
К примеру, в 1-й группе собраны щелочные металлы от лития до франция, у которых на внешней оболочке имеется один электрон. Его очень легко «оторвать» от атома, поэтому щелочные металлы являются сильными восстановителями. С ростом порядкового номера элемента в группах растут металлические и восстановительные свойстваа, увеличивается атомный радиус, снижается электроотрицательность; - в периодах элементы расположены по мере возрастания их атомных или порядковых номеров. При этом, как правили, слева направо уменьшаются металлические свойства и атомные радиусы, растут окислительные свойства и электроотрицательность.
Таблица Менделеева: значение и структура
Существует три вида таблицы:
- короткая — с лантаноидами и актиноидами, вынесенными в отдельный блок, и группировкой периодов, начиная с четвертого. Эта форма записи отменена ИЮПАК (международной организацией химиков), но широко используется в школьных учебниках, поскольку более наглядна с точки зрения анализа химических свойств.
 В ней ;
В ней ; - длинная — с лантаноидами и актиноидами, вынесенными в отдельный блок;
- сверхдлинная — в этом варианте каждый период занимает свою строку.
Каждая клеточка в таблице Менделеева содержит важную информацию:
- символ химического элемента в соответствии с международной классификацией, например, N — азот, Fe — железо (феррум) и т.д. Всего в таблице насчитывается 118 элементов. Из символы используются для обозначения элементов при записи химических реакций, формул веществ и в других случаях;
- атомный номер — число протонов, которое возрастает от первого элемента (водорода) к последующим. Количество электронов у каждого элемента может изменяться, а число протонов остается неизменным, определяя его основные свойства;
- относительная атомная масса — величина, которая показывает, во сколько раз масса атома конкретного элемента больше массы атома водорода — самого легкого элемента. Такой подход позволяет отойти от привычных граммов и килограммов, которые в масштабах атома неприменимы.
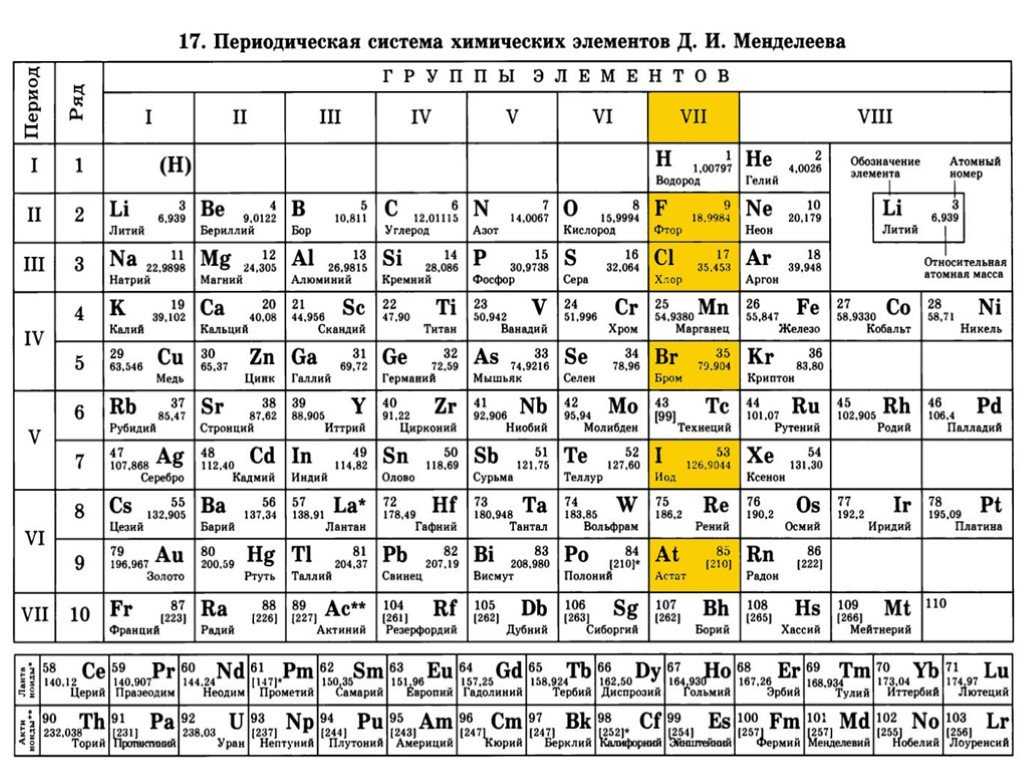
Анализ каждого элемента в таблице Менделеева и всего массива данных позволяет узнать многое о каждом из них и «предсказать», как будут вести себя вещества, составленные из них. Недаром на ОГЭ по химии разрешается пользоваться Периодической системой, ведь это умение также многое говорит о квалификации участника государственного экзамена.
Занимайтесь на курсах ЕГЭ и ОГЭ в паре TwoStu и получите максимум баллов на экзамене:
Владислав Барышников
Эксперт по подготовке к ЕГЭ, ОГЭ и ВПР
Задать вопрос
Закончил Московский физико-технический институт (Физтех) по специальности прикладная физика и математика. Магистр физико-математических наук. Преподавательский стаж более 13 лет. Соучредитель курсов ЕГЭ и ОГЭ в паре TwoStu.
Читайте также:
Краткая история химических элементов
От древних греков до ускорителей частиц
Античность V век до н.э.— II век н.э.
Атомы и элементы
«В мире нет ничего, кроме атомов и пустоты, всё существующее разрешается в бесконечное множество первоначальных неде- лимых вечных и неизменных частиц, которые вечно движутся
в бесконечном пространстве, то сцепляясь, то разлучаясь друг с другом» — это слова вовсе не Стивена Хокинга, а греческо-
го философа Демокрита, жившего в V–IV веках до нашей эры. Древние греки были очень прозорливы: понятия «атом» и «эле- мент» появились ещё в ранней Античности, причём значение этих слов не так уж отличалось от современного.
Древние греки были очень прозорливы: понятия «атом» и «эле- мент» появились ещё в ранней Античности, причём значение этих слов не так уж отличалось от современного.
Эпоха алхимии II–XVII века
В поисках золота
Причудливый гибрид науки, мистики и астрологии был предметом увлечения лучших умов Европы, Китая, арабского Востока. И конеч- но, алхимики оказались не совсем бесполезны. Вот, например, жил
в Гамбурге некто Хенниг Бранд, предавался популярнейшей алхими- ческой забаве — пытался получить золото из чего ни попадя. Источ- ник для синтеза драгоценного металла он выбрал по цветовой гамме, а именно мочу. Золота, конечно, не добыл, но в результате ряда реак- ций в 1669 году открыл фосфор.
Промышленная революция Сер. XVIII—перв. пол. XIX века
Век новых металлов
Подъём промышленности, развитие горного дела заметно расши- рили список известных элементов. В 1735 году из руды удалось выделить новый металл — кобальт, названный так в честь горно-
го духа Кобольда. А дальше понеслось: платина, никель, марга-
А дальше понеслось: платина, никель, марга-
нец, молибден, вольфрам, цирконий, титан, ниобий, литий, алю- миний… К середине XIX века была открыта большая часть метал- лов, используемых сегодня в производстве. Сторонники алхимии переживали: дескать, металлы должны быть связаны с небесными телами, а их получается явно больше, чем планет. Но вскоре алхимия исчезла, уступив место науке.
Великая химическая революция 1789 год
Начало современной науки
В 1789 году французский учёный Антуан Лавуазье публикует «Эле- ментарный курс химии», в котором приводит первый в истории спи- сок химических элементов, разделённых на несколько типов. В ка- честве «простых тел» указаны кислород, азот, водород, сера, фосфор, уголь и все известные к тому времени металлы. Возможно, Лавуазье сделал бы ещё немало открытий, если бы в 1794-м не был казнён якобинцами. Странно, что в честь него до сих пор не назвали ни од- ного химического элемента.
Наведение порядка 1814 год
Имена и символы
Шведский химик Йёнс Берцелиус предложил систе- му названий и символов для химических элементов. Именно его мы должны благодарить за буквы в клет- ках таблицы: H, O, C, Pb, Fe, Na, Mg и т. д. Ещё Берце- лиус открыл элементы церий, селен и торий, а также впервые выделил в чистом виде кремний, титан, тан- тал и цирконий.
Именно его мы должны благодарить за буквы в клет- ках таблицы: H, O, C, Pb, Fe, Na, Mg и т. д. Ещё Берце- лиус открыл элементы церий, селен и торий, а также впервые выделил в чистом виде кремний, титан, тан- тал и цирконий.
Спектральный анализ XIX век
Цвет химии
С середины XIX века для определения химического состава нача-
ли использовать спектральный анализ — метод, основанный на изучении взаимодействия материи с излучением: каждое веще- ство поглощает или излучает свет строго на определённых ча- стотах. Таким образом в 1860 году был открыт цезий, в 1861-м — рубидий (спектральные линии рубинового цвета), в 1863-м — ин- дий (давал цвет индиго, как наши джинсы). В 1868 году этим же методом в солнечной короне обнаружили гелий (на Земле его на- шли гораздо позже). С названием, правда, вышла ошибка: сначала гелий сочли металлом — отсюда окончание «-ий». Когда поняли, что это инертный газ, переименовывать было уже поздно.
Главная таблица 1869 год
Открытие периодического закона
Дмитрий Менделеев опубликовал первый вариант таблицы.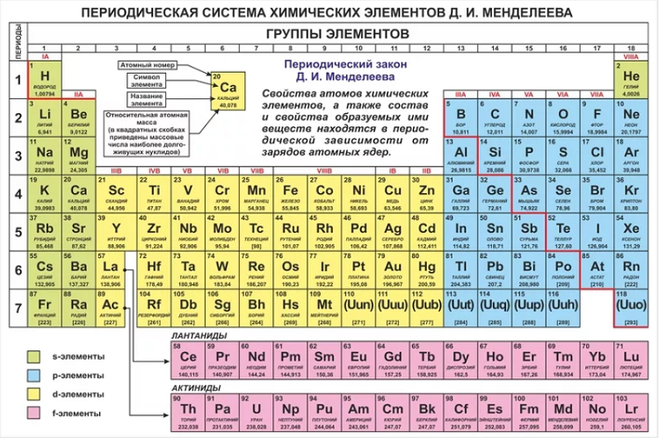 Важ- но не то, что он предложил удачную схему оформления извест- ных на тот момент элементов, а то, что вывел закон, который в со- временной трактовке звучит так: «Свойства химических элемен- тов, а также формы и свойства образуемых ими простых веществ и соединений находятся в периодической зависимости от величи- ны зарядов ядер их атомов». Открытие Менделеева позволило предсказывать новые элементы и их свойства.
Важ- но не то, что он предложил удачную схему оформления извест- ных на тот момент элементов, а то, что вывел закон, который в со- временной трактовке звучит так: «Свойства химических элемен- тов, а также формы и свойства образуемых ими простых веществ и соединений находятся в периодической зависимости от величи- ны зарядов ядер их атомов». Открытие Менделеева позволило предсказывать новые элементы и их свойства.
Радиоактивность Конец XIX— начало XX века
Тот, кто долго не живёт
Один за другим начали открывать элементы, которые со- держатся на планете в ничтожных количествах, поскольку распадаются за считаные годы, а то и часы. В 1898 году са- мая знаменитая супружеская пара науки — Мария Склодов- ская-Кюри и Пьер Кюри — получила радий и полоний. Чуть позже были обнаружены радон и актиний. Ни один из них не имеет стабильных изотопов.
Время большой физики Первая половина XX века
Понять атом
Это время запомнится не только войнами, революциями и дик- татурами. Первая половина ХХ столетия ознаменована гран- диозным прорывом в физике. В 1911 году Эрнест Резерфорд от- крыл атомное ядро. Учёные стали строить модели атома, были открыты нейтроны и прочие фундаментальные штуки. Появи- лась квантовая механика. Большая физика теперь могла объяс- нять, почему элементы имеют именно такие свойства и всту- пают в те, а не иные реакции.
Первая половина ХХ столетия ознаменована гран- диозным прорывом в физике. В 1911 году Эрнест Резерфорд от- крыл атомное ядро. Учёные стали строить модели атома, были открыты нейтроны и прочие фундаментальные штуки. Появи- лась квантовая механика. Большая физика теперь могла объяс- нять, почему элементы имеют именно такие свойства и всту- пают в те, а не иные реакции.
Начало эпохи ускорителей 1937 год
Первый искусственный элемент
О существовании элемента с порядковым номером 43 писал ещё Мен- делеев. Но найти его в природе не получалось. На помощь пришли тех- нологии. В созданном Эрнестом Лоуренсом ускорителе-циклотроне образцы молибдена обстреливали ядрами тяжёлого водорода и в ито- ге обнаружили новый радиоактивный элемент, получивший название технеций. Позднее, правда, его удалось найти в естественном виде — в спектрах некоторых звёзд.
Исчерпание природы 1939 год
Франция, девушка, радиоактивность
Список элементов, существующих в природе, закрыт — в 1939 го- ду Маргарита Перей, тридцатилетняя ученица Марии Склодов- ской-Кюри, открыла франций.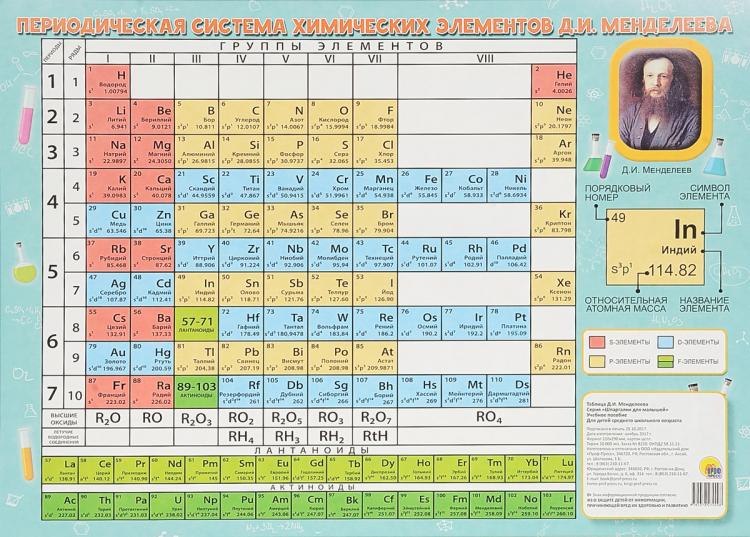 Этот радиоактивный элемент яв- ляется промежуточным продуктом распада более тяжёлых ядер. Суммарные запасы франция в земной коре составляют чуть больше трёхсот граммов и могли бы уместиться в кофейной чашке. Правда, через двадцать с небольшим минут этого эле- мента в чашке было бы уже в два раза меньше: он очень быстро распадается.
Этот радиоактивный элемент яв- ляется промежуточным продуктом распада более тяжёлых ядер. Суммарные запасы франция в земной коре составляют чуть больше трёхсот граммов и могли бы уместиться в кофейной чашке. Правда, через двадцать с небольшим минут этого эле- мента в чашке было бы уже в два раза меньше: он очень быстро распадается.
Начало трансуранов 40-e—60-е годы XX века
Нейтронами по мишени
В 1940 году в Университете Беркли (Калифорния, США) при облуче- нии урана-238 быстрыми нейтронами получен принципиально но- вый искусственный элемент — тяжёлый металл нептуний. Его по- рядковый номер 93, место в таблице — следующая после урана ячей- ка. Это первый трансурановый элемент. В том же году был синтези- рован плутоний (номер 94), который вскоре научились производить
в промышленных масштабах: он используется в атомных бомбах, электростанциях и космических батареях. С 1944 года под руковод- ством Гленна Сиборга в Беркли начали синтезировать новые элемен- ты — с чисто научными целями.
Подъём советской физики Начало 1960-х
В дело вступает Дубна
С 1961 года новые элементы создают и в Объединённом институте ядерных исследований в Дубне. У истоков этого процесса стоял Геор- гий Флёров. Параллельно с американцами наши физики синтезиро- вали элементы с номерами 101, 102, 103, 104, 105 и 106. Мировое со- общество признало успехи советской науки. Так, решением IUPAC (Международный союз теоретической и прикладной химии) 105-й элемент получил имя дубний, 114-й назвали флеровием, а 115-й — московием (в честь Московской области, где расположена Дубна). Позже к трансурановой гонке подключились Германия и Япония.
Вера в будущее 1969 год
Расширенная таблица Менделеева
Руководитель работ по созданию новых элементов
Гленн Сиборг предложил расширить периодическую таблицу элементов, включив в неё атомы, которые ещё не удалось синтезировать. Докуда может простираться эта таблица, спорят до сих пор.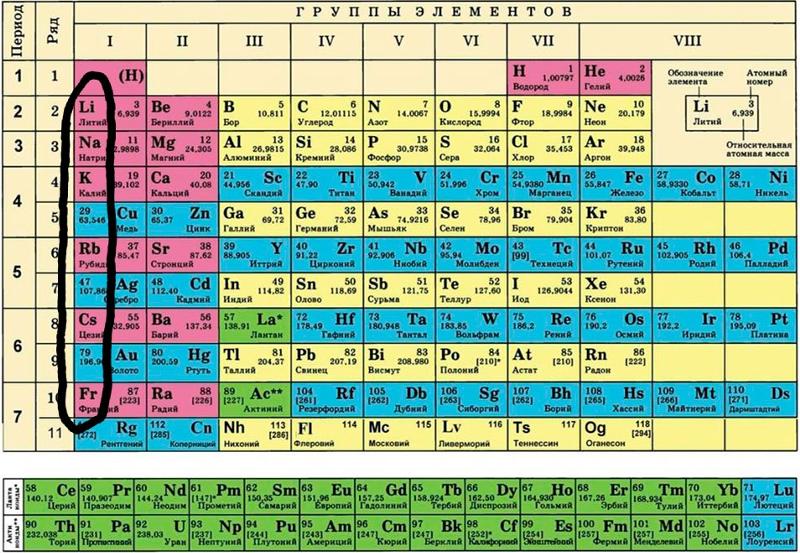 Одни считают, что эле- ментов не может быть больше 130, другие доходят до 143 и даже 218. Есть версия, что таблица Менделеева вообще не имеет границ.
Одни считают, что эле- ментов не может быть больше 130, другие доходят до 143 и даже 218. Есть версия, что таблица Менделеева вообще не имеет границ.
Современность Конец XX— начало XXI века
Наши элементы
Россия становится лидером трансурановой гонки.
В 1998 году группа учёных из ОИЯИ под руководством Юрия Оганесяна первой синтезирует 114-й элемент. Через несколько лет при участии американцев в Дуб- не получены 115-й, 116-й, 117-й и 118-й. В прошлом го- ду году IUPAC присвоил 118-му элементу имя огане- сон. Второй раз в истории элемент был назван в честь здравствующего учёного (первый был Гленн Сиборг — сиборгий). А, например, рентгений появился спустя во- семьдесят лет после смерти Вильгельма Рентгена.
никель | Определение, свойства, символы, использование и факты
никель
Посмотреть все СМИ
- Ключевые люди:
- Аксель Фредрик Кронстедт Поль Сабатье Шарль Эдуард Гийом
- Похожие темы:
- химический элемент переходный металл обработка никеля нейзильбер никель Ренея
Просмотреть весь соответствующий контент →
Резюме
Прочтите краткий обзор этой темы
никель (Ni) , химический элемент, ферромагнитный металл группы 10 (VIIIb) периодической таблицы Менделеева, заметно стойкий к окислению и коррозии.
| атомный номер | 28 |
|---|---|
| атомный вес | 58,69 |
| 1,453 °C (2,647 °F) | |
| boiling point | 2,732 °C (4,950 °F) |
| density | 8.902 (25 °C) |
| oxidation states | 0, + 1, +2, +3 |
| Электронная конфигурация | [AR] 3 D 8 4 S 2 |
Proterties, OckRest, и использует и использует
, Ockrandence, и использует и использует
, и использует
, и использует
, и использует
Серебристо-белый, прочный и более твердый, чем железо, никель широко известен из-за его использования в чеканке монет, но более важен как чистый металл, так и в виде сплавов для многих бытовых и промышленных применений. Элементарный никель очень редко встречается вместе с железом в земных и метеоритных отложениях. Металл был выделен (1751 г.) шведским химиком и минералогом бароном Акселем Фредриком Кронштедтом, который приготовил неочищенный образец из руды, содержащей никколит (арсенид никеля). Ранее руда этого же типа называлась Kupfernickel в честь «Старого Ника» и его озорных гномов, потому что, хотя он и напоминал медную руду, но давал хрупкий, незнакомый металл. Вдвое больше, чем медь, никель составляет около 0,007 процента земной коры; это довольно распространенный компонент магматических пород, хотя очень немногие месторождения по концентрации, размеру и доступности могут представлять коммерческий интерес. Считается, что центральные районы Земли содержат значительные количества. Важнейшие источники — пентландит, встречающийся с никельсодержащим пирротином, некоторые разновидности которого содержат 3—5% никеля, и халькопирит, а также никельсодержащие латериты (гарниерит — магниево-никелевый силикат переменного состава).
Элементарный никель очень редко встречается вместе с железом в земных и метеоритных отложениях. Металл был выделен (1751 г.) шведским химиком и минералогом бароном Акселем Фредриком Кронштедтом, который приготовил неочищенный образец из руды, содержащей никколит (арсенид никеля). Ранее руда этого же типа называлась Kupfernickel в честь «Старого Ника» и его озорных гномов, потому что, хотя он и напоминал медную руду, но давал хрупкий, незнакомый металл. Вдвое больше, чем медь, никель составляет около 0,007 процента земной коры; это довольно распространенный компонент магматических пород, хотя очень немногие месторождения по концентрации, размеру и доступности могут представлять коммерческий интерес. Считается, что центральные районы Земли содержат значительные количества. Важнейшие источники — пентландит, встречающийся с никельсодержащим пирротином, некоторые разновидности которого содержат 3—5% никеля, и халькопирит, а также никельсодержащие латериты (гарниерит — магниево-никелевый силикат переменного состава).
Britannica Викторина
118 Названий и символов периодической таблицы Викторина
Периодическая таблица состоит из 118 элементов. Насколько хорошо вы знаете их символы? В этом тесте вам будут показаны все 118 химических символов, и вам нужно будет выбрать название химического элемента, который представляет каждый из них.
Металлургия никеля сложна в деталях, многие из которых сильно различаются в зависимости от конкретной обрабатываемой руды. Обычно руда превращается в трисульфид диникеля, Ni 2 S 3 (с никелем в степени окисления +3), который обжигают на воздухе с получением оксида никеля NiO (состояние +2), который затем восстанавливают углеродом для получения металла. Некоторое количество никеля высокой чистоты получают с помощью упомянутого ранее карбонильного процесса. (Для получения информации о добыче, переработке и производстве никеля, см. обработка никеля.)
Никель (атомный номер 28) напоминает железо (атомный номер 26) по прочности и ударной вязкости, но больше похож на медь (атомный номер 29). ) в стойкости к окислению и коррозии, что объясняет многие из его применений. Никель обладает высокой электро- и теплопроводностью. Более половины произведенного никеля используется в сплавах с железом (особенно в нержавеющих сталях), а большая часть остального используется в коррозионно-стойких сплавах с медью (включая монель, который содержит 60-70% никеля, 30-40% медь и небольшое количество других металлов, таких как железо) и в жаропрочных сплавах с хромом. Никель также используется в электрически резистивных, магнитных и многих других сплавах, таких как нейзильбер (с медью и цинком, но без серебра). Нелегированный металл используется для формирования защитных покрытий на других металлах, особенно гальванопокрытием. Мелкоизмельченный никель используется для катализа гидрирования ненасыщенных органических соединений (например, жиров и масел).
) в стойкости к окислению и коррозии, что объясняет многие из его применений. Никель обладает высокой электро- и теплопроводностью. Более половины произведенного никеля используется в сплавах с железом (особенно в нержавеющих сталях), а большая часть остального используется в коррозионно-стойких сплавах с медью (включая монель, который содержит 60-70% никеля, 30-40% медь и небольшое количество других металлов, таких как железо) и в жаропрочных сплавах с хромом. Никель также используется в электрически резистивных, магнитных и многих других сплавах, таких как нейзильбер (с медью и цинком, но без серебра). Нелегированный металл используется для формирования защитных покрытий на других металлах, особенно гальванопокрытием. Мелкоизмельченный никель используется для катализа гидрирования ненасыщенных органических соединений (например, жиров и масел).
можно легко изготовить с использованием стандартных методов горячей и холодной обработки. Никель медленно реагирует с фтором, в конечном итоге образуя защитное покрытие из фторида, и поэтому используется в чистом виде или в виде сплавов, таких как монель, в оборудовании для работы с газообразным фтором и коррозионно-активными фторидами. Никель ферромагнитен при обычных температурах, хотя и не так сильно, как железо, и менее электроположителен, чем железо, но легко растворяется в разбавленных минеральных кислотах.
Никель ферромагнитен при обычных температурах, хотя и не так сильно, как железо, и менее электроположителен, чем железо, но легко растворяется в разбавленных минеральных кислотах.
Природный никель состоит из пяти стабильных изотопов: никеля-58 (68,27%), никеля-60 (26,10%), никеля-61 (1,13%), никеля-62 (3,59%) и никеля-64 (0,91%). Он имеет гранецентрированную кубическую кристаллическую структуру. Никель ферромагнитен до 358 ° C или 676 ° F (точка Кюри). Металл обладает уникальной стойкостью к действию щелочей и часто используется для изготовления емкостей для концентрированных растворов едкого натра. Никель медленно реагирует с сильными кислотами в обычных условиях с выделением водорода и образованием Ni 2 + ионы.
Оформите подписку Britannica Premium и получите доступ к эксклюзивному контенту. Подпишитесь сейчас
Китай является крупнейшим в мире производителем никеля. Другие крупные страны-производители никеля включают Россию, Японию, Австралию и Канаду.
Соединения
В своих соединениях никель проявляет степени окисления -1, 0, +1, +2, +3 и +4, хотя состояние +2 является наиболее распространенным. Ni 2+ образует большое количество комплексов, охватывающих координационные числа 4, 5 и 6 и все основные структурные типы, например октаэдрические, тригонально-бипирамидальные, тетраэдрические и квадратные.
Соединения с никелем в состоянии +2 имеют множество промышленных применений. Например, хлорид никеля, NiCl 2 , нитрат никеля, Ni(NO 3 ) 2 ·6H 2 O, и сульфамат никеля, Ni(SO 3 NH 2 0 ) 2 900 4H 2 O, используются главным образом в ваннах для гальваники никеля. Сульфат никеля, NiSO 4 , также используется при никелировании, а также при приготовлении катализаторов, грунтовочных эмалей и протрав (закрепителей) для окрашивания и текстильной печати. Оксид никеля, NiO, и пероксид никеля, Ni 2 O 3 , подготовлены для использования в топливных элементах и аккумуляторных батареях соответственно. Ферриты никеля используются в качестве магнитных сердечников для различных типов электрооборудования, таких как антенны и трансформаторы.
Ферриты никеля используются в качестве магнитных сердечников для различных типов электрооборудования, таких как антенны и трансформаторы.
Типичными соединениями никеля в природе, в которых он встречается главным образом в виде минералов в сочетании с мышьяком, сурьмой и серой, являются сульфид никеля, NiS; арсенид никеля, NiAs; антимонид никеля, NiSb; диарсенид никеля, NiAs 2 ; тиоарсенид никеля, NiAsS; и тиоантимонид никеля, NiSbS. В сульфиде никель находится в степени окисления +2, а во всех других приведенных соединениях — в степени +3.
Среди других важных коммерческих соединений карбонил никеля или тетракарбонилникель, Ni(CO) 4 . Это соединение, в котором никель проявляет нулевую степень окисления, используется в основном как носитель оксида углерода при синтезе акрилатов (соединений, используемых в производстве пластмасс) из ацетилена и спиртов. Это было первое открытое из класса соединений, называемых карбонилами металлов (1890 г.). Бесцветная летучая жидкость образуется при воздействии монооксида углерода на мелкодисперсный никель и характеризуется электронной конфигурацией, в которой атом никеля окружен 36 электронами. Этот тип конфигурации вполне сравним с конфигурацией атомов инертных газов.
Этот тип конфигурации вполне сравним с конфигурацией атомов инертных газов.
Эта статья была недавно пересмотрена и обновлена Адамом Августином.
Ni Никель Информация об элементе: факты, свойства, тенденции, использование и сравнение – Периодическая таблица элементов
Кристаллическая структура никеля
Твердотельная структура никеля Гранецентрированная кубическая .
Кристаллическая структура может быть описана с точки зрения ее элементарной ячейки. Единичные Клетки повторяются в трехмерном пространстве, образуя структуру.
Параметры элементарной ячейки
Элементарная ячейка представлена параметрами решетки, которые являются длинами ребер ячейки Постоянные решетки (a, b и c)
| a | b | c |
|---|---|---|
| 352,4 пм | 352,4 пм | 352,4 пм |
и углы между ними Углы решетки (альфа, бета и гамма).
| альфа | бета | Gamma |
|---|---|---|
| π/2 | π/2 | π/2 |
. y i , z i ) измеряется от опорной точки решетки.
Свойства симметрии кристалла описываются концепцией пространственных групп. Все возможные симметричные расположения частиц в трехмерном пространстве описываются 230 пространственными группами (219различные типы или 230, если хиральные копии считаются различными.
| Space Group Name | Fm_ 3m | |
| Oxidation States | Space Group Number | 225 |
| Crystal Structure | Face Centered Cubic |
Nickel Atomic and Orbital Properties
Атомы никеля имеют 28 электронов и структуру электронной оболочки [2, 8, 16, 2] с символом атомного термина (квантовые числа) 3 Ф 4 .
| Atomic Number | 28 |
| Number of Electrons (with no charge) | 28 |
| Number of Protons | 28 |
| Mass Number | 59 |
| Number нейтронов | 31 |
| Структура оболочки (электронов на энергетический уровень) | 2, 8, 16, 2 |
| Электронная конфигурация | [Ar] 3d8 4s2 |
| Valence Electrons | 3d8 4s2 |
| Valence (Valency) | 2 |
| Main Oxidation States | 2 |
| Oxidation States | -2, – 1, 0, 1, 2, 3, 4 |
| Atomic Term Symbol (Quantum Numbers) | 3 F 4 |
Bohr Atomic Model of Nickel – Electrons per energy level
Электронная конфигурация основного состояния никеля – нейтральный атом никеля
Сокращенная электронная конфигурация никеля
Сокращенная электронная конфигурация основного состояния нейтрального атома никеля [Ar] 3d8 4s2. Часть конфигурации никеля, эквивалентная благородному газу предыдущего периода, обозначается аббревиатурой [Ar]. Для атомов с большим количеством электронов это обозначение может стать длинным, поэтому используется сокращенное обозначение. Это важно, поскольку именно валентные электроны 3d8 4s2, электроны в самой внешней оболочке, определяют химические свойства элемента.
Часть конфигурации никеля, эквивалентная благородному газу предыдущего периода, обозначается аббревиатурой [Ar]. Для атомов с большим количеством электронов это обозначение может стать длинным, поэтому используется сокращенное обозначение. Это важно, поскольку именно валентные электроны 3d8 4s2, электроны в самой внешней оболочке, определяют химические свойства элемента.
Полная электронная конфигурация нейтрального никеля
Полная электронная конфигурация основного состояния атома никеля. Полная электронная конфигурация
1s2 2s2 2p6 3s2 3p6 3d8 4s2 Принцип запрета Паули и правило Хунда.

Атомная структура никеля
Атомный радиус никеля составляет 149 пм, а его ковалентный радиус составляет 121 пм.
| Вычисленный атомный радиус | 149 пм (1,49 Å) |
| Эмпирический радиус | 135 вечера (1,35 Å) |
| Атом | 6,588888888/Мол |
| 6,58888888888 гг. Waals Radius | 163 PM |
| Нейтронный сечение | 37,2 |
| Абсорбция нейтронной массы | 0,0026 |
ATOMIC.0171
Никель Химические свойства: Энергия ионизации никеля и сродство к электрону
Сродство к электрону никеля составляет 112 кДж/моль.
| Valence | 2 |
| Electronegativity | 1. 91 91 |
| ElectronAffinity | 112 kJ/mol |
Ionization Energy of Nickel
Refer to table below for Ionization energies of Nickel
| Ionization energy number | Enthalpy – kJ/mol |
|---|---|
| 1st | 737.1 |
| 2nd | 1753 |
| 3rd | 3395 |
| 4th | 5300 |
| 5th | 7339 |
| 6th | 10400 |
| 7th | 12800 |
| 8th | 15600 |
| 9th | 18600 |
| 10th | 21670 |
| 11th | 30970 |
| 12th | 34000 |
| 13th | 37100 |
| 14th | 41500 |
| 15th | 44800 |
| 16th | 48100 |
| 17th | 55101 |
| 18th | 585770 | 585770 | 8899
| 58570 | |
| 0036 19th | 148700 |
| 20th | 159000 |
| 21st | 169400 |
| 22nd | 182700 |
| 23rd | 1 |
| 24th | 205600 |
| 25th | 221400 |
| 26th | 231490 |
| 27th | 9 |
| 28th | 1039668 |
Физические свойства никеля
См. Ниже таблицы для физических свойств никеля
Ниже таблицы для физических свойств никеля
| Плотность | 8,908 г/см3 (когда жидкость при М.П. cm3/mol |
Elastic Properties
| Young Modulus | 200 |
| Shear Modulus | 76 GPa |
| Bulk Modulus | 180 GPa |
| Poisson Ratio | 0.31 |
Hardness of Nickel – Tests to Measure of Hardness of Element
| Mohs Hardness | 4 MPa |
| Vickers Hardness | 638 MPa |
| Твердость по Бринеллю | 700 МПа |
Никель Электрические свойства
Никель является проводником электричества. Электрические свойства никеля 9 см. в таблице ниже.0003
| Electrical Conductivity | 14000000 S/m |
| Resistivity | 7e-8 m Ω |
| Superconducting Point | – |
Nickel Heat and Conduction Properties
| Thermal Проводимость | 91 Вт/(м·К) |
| Тепловое расширение | 0,0000134 /K |
Никель Магнитные свойства
| Magnetic Type | Ferromagnetic |
| Curie Point | 631 K |
| Mass Magnetic Susceptibility | – |
| Molar Magnetic Susceptibility | – |
| Volume Magnetic Susceptibility | – |
Оптические свойства никеля
| Показатель преломления | – |
Акустические свойства никеля
| Speed of Sound | 4970 m/s |
Nickel Thermal Properties – Enthalpies and thermodynamics
Refer to table below for Thermal properties of Nickel
| Melting Point | 1728 K (1454. 85 °C, 2650.73 °F) 85 °C, 2650.73 °F) |
| Boiling Point | 3186 K (2912.85°C, 5275.129999999999 °F) |
| Critical Temperature | – |
| Superconducting Point | – |
Enthalpies of Nickel
| Heat of Fusion | 17.2 kJ/mol |
| Heat of Vaporization | 378 kJ/mol |
| Heat of Combustion | – |
Изотопы никеля – Ядерные свойства никеля
Никель состоит из 31 изотопа, содержащего от 48 до 78 нуклонов. Никель имеет 5 стабильных естественных изотопов.
Изотопы никеля – Встречающиеся в природе стабильные изотопы: 58Ni, 60Ni, 61Ni, 62Ni, 64Ni.
| Isotope | Z | N | Isotope Mass | % Abundance | T half | Decay Mode |
|---|---|---|---|---|---|---|
| 48Ni | 28 | 20 | 48 | Synthetic | ||
| 49Ni | 28 | 21 | 49 | Synthetic | ||
| 50Ni | 28 | 22 | 50 | Synthetic | ||
| 51Ni | 28 | 23 | 51 | Synthetic | ||
| 52Ni | 28 | 24 | 52 | Synthetic | ||
| 53Ni | 28 | 25 | 53 | Synthetic | ||
| 54Ni | 28 | 26 | 54 | Synthetic | ||
| 55Ni | 28 | 27 | 55 | Synthetic | ||
| 56Ni | 28 | 28 | 56 | Synthetic | ||
| 57Ni | 28 | 29 | 57 | Synthetic | ||
| 58Ni | 28 | 30 | 58 | 68. 0769% 0769% | Stable | N/A |
| 59Ni | 28 | 31 | 59 | Synthetic | Stable | |
| 60Ni | 28 | 32 | 60 | 26.2231% | Stable | N/A |
| 61Ni | 28 | 33 | 61 | 1.1399% | Stable | N/A |
| 62Ni | 28 | 34 | 62 | 3.6345% | Stable | N/A |
| 63Ni | 28 | 35 | 63 | Synthetic | ||
| 64Ni | 28 | 36 | 64 | 0.9256% | Stable | N/A |
| 65Ni | 28 | 37 | 65 | Synthetic | ||
| 66Ni | 28 | 38 | 66 | Synthetic | ||
| 67Ni | 28 | 39 | 67 | Synthetic | ||
| 68Ni | 28 | 40 | 68 | Synthetic | ||
| 69Ni | 28 | 41 | 69 | Synthetic | ||
| 70Ni | 28 | 42 | 70 | Synthetic | ||
| 71Ni | 28 | 43 | 71 | Synthetic | ||
| 72Ni | 28 | 44 | 72 | Synthetic | ||
| 73Ni | 28 | 45 | 73 | Synthetic | ||
| 74Ni | 28 | 46 | 74 | Synthetic | ||
| 75Ni | 28 | 47 | 75 | Synthetic | ||
| 76Ni | 28 | 48 | 76 | Synthetic | ||
| 77Ni | 28 | 49 | 77 | Synthetic | ||
| 78Ni | 28 | 50 | 78 | Synthetic |
Никель – Периодическая таблица
1
H
ГВД
Немамелаллы
HOUTER
Discoverer: Cavendish, Henry
Celection Catelection: Non Metall
| 6. в структуре атома 34 протона и 34 электрона. Химический символ для селена — это Se . Селен является неметаллом со свойствами, которые занимают промежуточное положение между элементами выше и ниже в периодической таблице, серой и теллуром, а также имеет сходство с мышьяком. 78.96 amu 35 Br Bromine Nonmetal Bromine Discoverer: Balard, Antoine-Jérôme Element Category: Nonmetal Bromine is a chemical element with atomic number 35 which означает, что в атомной структуре 35 протонов и 35 электронов. Химический символ для брома — это Br . Бром является третьим по легкости галогеном и представляет собой дымящую красно-коричневую жидкость при комнатной температуре, которая легко испаряется с образованием газа аналогичного цвета. Таким образом, его свойства занимают промежуточное положение между свойствами хлора и йода. 79,90 AMU 36 KR Krypton Noble Gas Krypton Discoverer: Ramsay, Sir William и Travers, Morris Категория элементов: Noble Gas KRYPOT 9002 KRYPOT. число 36 означает, что в структуре атома 36 протонов и 36 электронов. Химический символ для криптона равен Kr . Криптон является элементом группы 18 (благородные газы). Бесцветный благородный газ без запаха и вкуса, криптон встречается в следовых количествах в атмосфере и часто используется с другими инертными газами в люминесцентных лампах. 83,79 AMU 37 RB Rubidium Alkali Metals Rubidium Discoverer: Bunsen, Robert Wilhelm и Kirchhoff, Gustav Robert Elementle Catelecty: ALKALI MateLim и Kirchhoff, Gustav Robert Elemel атомный номер 37 , что означает, что в структуре атома 37 протонов и 37 электронов. Химический символ для рубидия равен Rb . Рубидий — мягкий серебристо-белый металлический элемент группы щелочных металлов с атомной массой 85,4678. 85,47 AMU 38 SR Strontium Алочные металлы Земля Стронтий Discoming: Crawford, Adair Категория элементов: Alkaline Earth Metals . Стр. , что означает, что в структуре атома 38 протонов и 38 электронов. Химический символ для стронция — это Sr . Стронций — щелочноземельный металл, стронций — мягкий серебристо-белый желтоватый металлический элемент, обладающий высокой химической активностью. 87.62 amu 39 Y Yttrium Transition metals Yttrium Discoverer: Gadolin, Johan Element Category: Transition metals Yttrium is a chemical element with atomic number 39 which означает, что в структуре атома 39 протонов и 39 электронов. Иттрий представляет собой серебристо-металлический переходный металл, химически сходный с лантанидами, и его часто относят к «редкоземельным элементам». 88,91 AMU 40 ZR Цирконий Переходные металлы Цирконий Discidenter: Klaproth, Martin Heinrich Категория элементов: Transition Metals 91.22 AMU 41 NB Niobium переходные металлы Niobium Discoverer: Hateket, Charles Категория: переход Metals NIOBIUM 666666 2 IS CHIMICAIM 2 AMICIMICAIM 2. ЧИМИМИЧЕСКИЙ НАМЕНИЧЕСКИЙ НАМЕНИЧЕСКИЙ НАМЕНИЧЕСКИЙ НА СИМИЧЕСКИЙ НАМЕНИЧЕСКИЙ НА СИМИЧЕСКИЙ ЭМИЧЕСКОМ. означает, что в структуре атома 41 протон и 41 электрон. Химический символ для ниобия — это Nb . Ниобий — мягкий, серый, пластичный переходный металл, часто встречающийся в минералах пирохлоре (главный коммерческий источник ниобия) и колумбите. 92.91 amu 42 Mo Molybdenum Transition metals Molybdenum Discoverer: Scheele, Carl Welhelm Element Category: Transition metals Molybdenum is a chemical element with atomic number 42 что означает, что в структуре атома 42 протона и 42 электрона. Молибден, серебристый металл с серым оттенком, имеет шестую самую высокую температуру плавления среди всех элементов. Он легко образует твердые устойчивые карбиды в сплавах, поэтому большая часть мирового производства элемента (около 80%) используется в стальных сплавах, в том числе в высокопрочных сплавах и суперсплавах. 95.94 AMU 43 TC Technetium Переход Metals Technetium Discoverer: Perrier, Carlo and Segrè, Emilio Категория элементов: переход Metals Технеций — самый легкий элемент, все изотопы которого радиоактивны; ни один не стабилен. Почти весь технеций производится синтетическим путем, и в земной коре его обнаруживают лишь в незначительных количествах. 98 AMU 44 RU Ruthenium Переход Metals Рутений Discireder: Klaus, Karl Karlovich Категория элементов: 40003 12626262 -й Chimmium 26262. Семалист 9002 Рутений — редкий переходный металл, относящийся к платиновой группе периодической таблицы. Как и другие металлы платиновой группы, рутений инертен к большинству других химических веществ. 101.07 AMU 45 RH Rhodium Переходные металлы Rhodium Discoverer: Wollaston, William Hyde Категория элементов: Metom. Rhodium 6. что означает, что в структуре атома 45 протонов и 45 электронов. Химический символ для родия равен Rh . Родий — редкий, серебристо-белый, твердый, устойчивый к коррозии и химически инертный переходный металл. Это благородный металл, член платиновой группы. 102.91 AMU 46 PD Palladium Переходные металлы Палладий Discoverer: Wollaston, William Hyde Категория элементов: Metom. . что означает, что в структуре атома 46 протонов и 46 электронов. Химический символ для палладия — это Pd . Палладий, платина, родий, рутений, иридий и осмий образуют группу элементов, называемых металлами платиновой группы (МПГ). Они имеют схожие химические свойства, но палладий имеет самую низкую температуру плавления и является наименее плотным из них. 106,42 AMU 47 AG Silver Переходные металлы Silver Discoverer: Unknown Категория элементов: переходной металлы Silver является химическим элементом с Atomic 9002 Silver является химическим элементом с Atomic Silver является химическим элементом с Atomic № Silver является химическим элементом. Серебро — мягкий, белый, блестящий переходный металл, обладающий самой высокой электропроводностью, теплопроводностью и отражательной способностью среди всех металлов. Металл встречается в земной коре в чистом, свободном элементном виде («самородное серебро»), в виде сплава с золотом и другими металлами, а также в таких минералах, как аргентит и хлораргирит. 107,87 AMU 48 CD Cadmium переходные металлы Cadmium Discoverer: Stromeyer, Prof. Friedrich Категория элементов: 40003 Cadmium 6. , что означает, что в структуре атома 48 протонов и 48 электронов. Химический символ для кадмия — это Cd . Кадмий — мягкий голубовато-белый металл, химически сходный с двумя другими стабильными металлами группы 12, цинком и ртутью. 112,41 AMU 49 в Индий Пост-трансфер. элемент с атомным номером 49 , что означает, что в атомной структуре 49 протонов и 49 электронов. Химический символ для индия равен In . Индий — это постпереходный металл, составляющий 0,21 части на миллион в земной коре. Очень мягкий и ковкий, индий имеет температуру плавления выше, чем у натрия и галлия, но ниже, чем у лития и олова. Химически индий похож на галлий и таллий. 114,82 AMU 50 SN TIN Пост-трансфер. , что означает, что в структуре атома 50 протонов и 50 электронов. Химический символ для олова – это Sn . Олово является постпереходным металлом в группе 14 периодической таблицы. 118,71 AMU 51 SB Отвания Металлоиды Ответ Discoverer: Неизвестный Категория: Metalloids Antimony. протонов и 51 электрон в структуре атома. Химический символ для сурьмы — это Sb . Сурьма представляет собой блестящий серый металлоид, встречается в природе в основном в виде сульфидного минерала антимонита. Соединения сурьмы были известны с древних времен и применялись в виде порошка для использования в качестве лекарств и косметики, часто известных под арабским названием коль. 121,76 AMU 52 TE Tellurium Metalloids Tellurium Discoverer: Müller Von Reichenstein, Franz Joseph Категори что означает, что в структуре атома 52 протона и 52 электрона. Теллур — хрупкий, умеренно токсичный, редко встречающийся серебристо-белый металлоид. Теллур химически связан с селеном и серой. Иногда его находят в естественной форме в виде элементарных кристаллов. Теллур гораздо более распространен во Вселенной в целом, чем на Земле. Крайняя редкость его в земной коре, сравнимая с платиной. 127,6 53 I йод НЕМЕЛАЛЬ йод Discoverer: Courtois, Bernard Категория: Нематал Iodine , который является химическим элементом с помощью ATMELIC Йод является самым тяжелым из стабильных галогенов. Он существует в виде блестящего пурпурно-черного металлического твердого вещества при стандартных условиях, который легко возгоняется с образованием фиолетового газа. 126,90 AMU 54 XE Xenon Noble Gas Xenon Discoverer: Ramsay, William and Travers, Morris William Категория элементов: Noble Gas 5. XEN Ксенон представляет собой бесцветный, плотный благородный газ без запаха, обнаруженный в атмосфере Земли в следовых количествах. Название ксенон для этого газа происходит от греческого слова ξένον [ксенон], формы среднего единственного числа от ξένος [ксенос], что означает «чужой (er)», «странный (r)» или «гость». В атомной промышленности особенно искусственный ксенон-135 оказывает огромное влияние на работу ядерного реактора. 131.29 AMU 55 CS Цезий Алкальские металлы Цезий Открытие: Alkali Metalle . Comemice Amelection с Alkali Metall с Alkali Metall с Alkali Metall с Alkali Metall с Alkali Metall с Alkali Metalli с Alkali Metall с Alkali Metalli с Alkali Metalli с Alkali Metall с Alkali Metalli с Alkali Malli. 55 , что означает, что в структуре атома 55 протонов и 55 электронов. Химический символ для цезия — это Cs . Цезий — мягкий щелочной металл серебристо-золотистого цвета с температурой плавления 28,5 °C, что делает его одним из пяти элементарных металлов, находящихся в жидком состоянии при комнатной температуре или близкой к ней. По физическим и химическим свойствам цезий подобен рубидию и калию. 132,91 AMU 56 BA Barium Алочные металлы Земля Barium Desciveer: Davy, Sir Humphry Категория элементов: Alkaline Metals Barium . Барий — пятый элемент группы 2, мягкий щелочноземельный металл серебристого цвета. Из-за своей высокой химической активности барий никогда не встречается в природе в виде свободного элемента. Наиболее вероятные массы осколков деления составляют около 9 масс.5 (криптон) и 137 (барий). 137,33 AMU 57-71 Lanthanoids Lanthanoids Discongerer:- Категория элементов: Lanthanoids составляют 9000-letments с Atmif с ATOMIC с ATAMIC с ATOMIC с ATOMIC с ATOMIC с ATOMIC с ATOMIC с ATOMIC: LANTHANIODS составляют 9000-letments с ATOMIC с ATOMIC. Эти элементы, наряду с химически подобными элементами скандием и иттрием, часто вместе известны как редкоземельные элементы. 72 HF Hafnium Переходные металлы Hafnium Discoverer: Coster, Dirk и De Hevesy, Джордж Чарльз Категория элементов: переходной металлы Hafnium является химическим элементом с Atomic Number . 178,49 73 TA Tantalum переходные металлы Tantalum Discoverer: Ekeberg, Anders Gustav Категория элементов: 40003 TANTAL 2. означает, что в структуре атома 73 протона и 73 электрона. Химический символ для тантала — это Ta . Тантал — редкий, твердый, голубовато-серый, блестящий переходный металл, обладающий высокой коррозионной стойкостью. 180,95 AMU 74 W В вольважении переходные металлы В вольвательство Discoverer: Elhuyar, Juan José и Elhuyar, Fausto Celection Catelecty: Transsition Metals Вольфрам — редкий металл, встречающийся в природе на Земле почти исключительно в виде химических соединений. Вольфрам по своей природе хрупкий и твердый материал, что затрудняет работу с ним. 183,84 AMU 75 RE Rhenium Переходные металлы Rhenium Discoverer: Noddack, Walter и Berg, Otto Carl и Tacke, IDA Категория: Transsition Metals 9002 555. RHENIUST ASTARIIME ASTARIES IDA . химический элемент с атомным номером 75 , что означает, что в атомной структуре 75 протонов и 75 электронов. Рений — серебристо-белый тяжелый переходный металл третьего ряда в группе 7 периодической таблицы. 186.21 AMU 76 OS OSMIUM Переход Metals OSMIUM Discoverer: Tennant, Smithson Категория элементов: переход Metals OSMIUM IS AIMICAIMIC 9002 . означает, что в структуре атома 76 протонов и 76 электронов. Химический символ для осмия равен Os . Осмий — твердый, хрупкий, голубовато-белый переходный металл платиновой группы, который встречается в качестве микроэлемента в сплавах, в основном в платиновых рудах. Осмий — самый плотный природный элемент с плотностью 22,59.г/см3. Но его плотность меркнет по сравнению с плотностью экзотических астрономических объектов, таких как белые карлики и нейтронные звезды. 190.23 AMU 77 IR IRIDIUM Переход Metals IRIDIUM Discoverer: Tennant, Smithson Категория элементов: переход Metals Iridium IS AIMICE AMICAL 9002 . Иридий — очень твердый, хрупкий, серебристо-белый переходный металл платиновой группы. Обычно иридий считается вторым по плотности элементом (после осмия). Это также самый устойчивый к коррозии металл даже при температурах до 2000 °C. 192.22 78 Pt Платина Переходные металлы Платина Первооткрыватель: Уллоа, Антонио де Категория элемента: переходные металлы Платина — это химический элемент с атомным номером 78 , что означает, что в атомной структуре 78 протонов и 78 электронов. Химический символ для платины — это Pt . Платина — это плотный, ковкий, пластичный, крайне нереакционноспособный, драгоценный серебристо-белый переходный металл. Платина является одним из наименее реакционноспособных металлов. 195.08 AMU 79 AU Gold Переходные металлы Gold Discoverer: Unknown Категория элементов: переходной металлы Gold является химическим элементом с Atomic № 9002 Gold является химическим элементом с Atomic Gold является химическим элементом с Atomic Number Gold является химическим элементом. 79 протонов и 79 электронов в атомной структуре. Химический символ для золота — это Au . Золото — яркий, слегка красновато-желтый, плотный, мягкий, ковкий и пластичный металл. 196,97 AMU 80 HG Mercury Переходные металлы Mercury Discount: Unknown Категория элементов: переходной металлы Merculy является химическим элементом с At Atomic Number Ртуть широко известна как ртуть и ранее называлась гидраргирум. Ртуть — это тяжелый серебристый элемент d-блока. Ртуть — единственный металлический элемент, который находится в жидком состоянии при стандартных условиях температуры и давления. 200,59 AMU 81 TL Thallium Пост-трансляция металлов Thallium Discoverer: Crookes, William Категория элементов: пост-перенос. 81 , что означает, что в структуре атома 81 протон и 81 электрон. Химический символ для таллия — это Tl . Таллий представляет собой мягкий серый постпереходный металл, который не встречается в природе в свободном виде. В промышленных масштабах таллий производится как побочный продукт переработки сульфидных руд тяжелых металлов. Примерно 60–70% производимого таллия используется в электронной промышленности. 204,38 AMU 82 PB ВЫДЕЛА Пост-трансфер. , что означает, что в структуре атома 82 протона и 82 электрона. Химический символ для свинца — это Pb . Свинец — тяжелый металл, более плотный, чем большинство обычных материалов. Свинец мягкий и пластичный, имеет относительно низкую температуру плавления. 207,2 AMU 83 BI Bismuth Пост-трансляция металлов Bismuth Discoverer: Geoffroy, Claude Категория элементов: пост-транзис. 83 , что означает, что в структуре атома 83 протона и 83 электрона. Химический символ для висмута — это Bi . Висмут представляет собой хрупкий металл серебристо-белого цвета в свежем виде, но поверхностное окисление может придать ему розовый оттенок. Висмут представляет собой пятивалентный постпереходный металл и один из пниктогенов, химически напоминающий его более легкие гомологи мышьяк и сурьму. 208,98 AMU 84 PO Polonium Пост-трансляция металлов Polonium Discoverer: Curie, Marie and Pierre Категория элементов: пост-транзитный металль . Полоний — редкий и высокорадиоактивный металл, не содержащий стабильных изотопов. По химическому составу полоний подобен селену и теллуру, хотя по своим металлическим свойствам напоминает своих горизонтальных соседей по периодической таблице: таллия, свинца и висмута. 209 AMU 86 RN Radon Noble Gas Radon Discoverer: Dorn, Friedrich Ernst Категория элементов: Nobal Gas Радон — радиоактивный бесцветный благородный газ без вкуса и запаха. Радон встречается в природе как промежуточный этап в обычных цепочках радиоактивного распада, посредством которых торий и уран медленно распадаются на свинец. 222 amu 87 Fr Francium Alkali metal Francium Discoverer: Perey, Marguerite Element Category: Alkali metal Francium is a chemical element with atomic number 87 which означает, что в структуре атома 87 протонов и 87 электронов. Химический символ для франция равен Fr . Франций — щелочной металл с одним валентным электроном. Франций является вторым наименее электроотрицательным элементом после цезия и вторым по редкости встречающимся в природе элементом (после астата). Франций — высокорадиоактивный металл, распадающийся на астат, радий и радон. 223 AMU 88 RA Radium Алкалиновый металлический металл Радий Discoverer: Curie, Marie and Pierre Категория элементов: щелочный металл Radium IS A -A -A -A -A -A -Amicic Came -Ciemic At At Amicic Amearic At Amicic Amemic Arate Cemicic At At Amicic Amearic Atemic Amearic Amearic Amearic Atemical Antamic At Amicical. Чистый радий представляет собой серебристо-белый щелочноземельный металл. Все изотопы радия высокорадиоактивны, наиболее стабильным из них является радий-226. 226 AMU 89-103 Актиноиды Актиноиды Disconder:- Категория элементов: Актиноид или актиноидные серии охватывают 15 металлических химических элементов с 89-й серией. актиний через лоуренсий. 104 Rf Резерфордий Переходный металл Резерфордий Первооткрыватель: ученые из Дубны, Россия (1964)/Альберт Гиорсо и др. др. (1969) Категория элемента: переходный металл Резерфордий — это химический элемент с атомным номером 104 , что означает, что в атомной структуре 104 протона и 104 электрона. Категория элемента: переходный металл Дубний — это химический элемент с атомным номером 105 , что означает, что в атомной структуре 105 протонов и 105 электронов. Химический символ для дубния — это Db . 268 а.е.м. 106 Sg Сиборгий Переходный металл Сиборгий Первооткрыватель: Albert Ghiorso et. др. Категория элемента: переходный металл Сиборгий — это химический элемент с атомным номером 106 , что означает, что в атомной структуре 106 протонов и 106 электронов. Химический символ для Seaborgium — Sg . 269 а.е.м. 107 Bh Борий Переходный металл Борий Первооткрыватель: Ученые из Дубны, Россия Элемент Переходный металл0003 Борий — это химический элемент с атомным номером 107 , что означает, что в атомной структуре 107 протонов и 107 электронов. 270 AMU 108 HS Hassium Переходный металл Hassium Discoverer: Armbruster, Paula and Muenzenberg, Dr. Gottfred Категория: переходной металл 555555555. .0026 — это химический элемент с атомным номером 108 , что означает, что в атомной структуре 108 протонов и 108 электронов. Химический символ для Hassium — Hs . Это синтетический элемент (впервые синтезированный в Хассе в Германии) и радиоактивный. Самый стабильный известный изотоп 269 Hs имеет период полураспада примерно 9,7 секунды. Расчетная плотность составляет 40,7 x 10 3 кг/м 3 . Плотность Hassium определяется его с высоким атомным весом и из-за значительного уменьшения ионных радиусов элементов в ряду лантанидов, известного как лантанид и сокращение актинидов . 269 AMU 109 MT Meitnerium Meitnerium Discoverer: Armbruster, Paula и Muenzenberg, Dr. Gottfred Категория элементов: Неизвестный, вероятно, A Transition Metalel 278 AMU 110 DS Darmstadtium Darmstadtium Discoverer: Armbruster, Paula и Muenzenberg, Dr. Gottfred Celecti элемент с атомным номером 110 , что означает, что в структуре атома 110 протонов и 110 электронов. Химический символ для Darmstadtium — Ds . 281 AMU 111 RG ROENTGENIUM ROENTGENIUM Discoverer: David Anderson, Ruhani Rabin, Team Houndraft Категория элементов: Неизвестный, вероятно, транспортный металл 282 AMU 112 CN Copernicium Copernicium Discoverer: Armbruster, Paula и Muenzenberg, Dr. Gottfred Категория элементов: Неизвестный, Вероятно, трансфер . элемент с атомным номером 112 , что означает, что в структуре атома 112 протонов и 112 электронов. Химический символ для Copernicium — это Cn . 285 а.е.м. 113 Nh Нигоний Нигоний Первооткрыватель: Ю. Т. Оганесян и др. др. Категория элемента: неизвестна, вероятно, переходный металл Нигоний — это химический элемент с атомным номером 113 , что означает, что в атомной структуре 113 протонов и 113 электронов. 286 AMU 114 FL Flerovium Flerovium Обнаружение: ученые из Дубны, Россия Категория элементов: Неизвестный, вероятно, металл после транспорта Flerovium . атомный номер 114 означает, что в атомной структуре 114 протонов и 114 электронов. Химический символ для флеровиума Fl . 289 а.о. др. Категория элемента: неизвестна Московий — это химический элемент с атомным номером 115 , что означает, что в атомной структуре 115 протонов и 115 электронов. Химический символ для Moscovium — это Mc . 290 AMU 116 LV Livermorium Livermorium Обнаружение: ученые в Дубне, Россия Категория элементов: Неизвестный Livermorium – это химический элемент с Antonship 9. 293 а.е.м. 117 Ц Tennessine Tennessine Disconger: – Элементы Категория: неизвестный Теннесин – химический элемент с атомным числом 117 , что означает, что в атомной структуре состоит 117 протонов и 117 электронов. Химический символ для Теннессина равен Ts . 294 а.м.у. др. Категория элемента: неизвестна Оганесон это химический элемент с атомным номером 118 , что означает, что в атомной структуре 118 протонов и 118 электронов. Химический символ для Оганесона равен Og . 295 а.е.м. 57 Ла Лантан Лантаноиды Лантан Первооткрыватель: Мосандер, Карл Густав Лантаноид 3 Категория Элементы0002 Лантан — это химический элемент с атомным номером 57 , что означает, что в атомной структуре 57 протонов и 57 электронов. Лантан — мягкий, пластичный металл серебристо-белого цвета, который быстро тускнеет на воздухе и достаточно мягкий, чтобы его можно было разрезать ножом. Это эпоним ряда лантанидов, группы из 15 подобных элементов между лантаном и лютецием в периодической таблице, из которых лантан является первым и прототипом. Его также иногда считают первым элементом переходных металлов 6-го периода и традиционно причисляют к редкоземельным элементам. 138,9 AMU 58 CE Cerium Lanthanoids Cerium Discoverer: Hisinger, Wilhelm и Berzelius, Jöns Jacob/Klaproth, Martin Heinrich Element: Lans Jacob/Klaproth, Martin Heinrich Ementle: Lans Jacob/Klaproth, Martin Heinrich . элемент с атомным номером 58 , что означает, что в атомной структуре 58 протонов и 58 электронов. Церий — мягкий, пластичный металл серебристо-белого цвета, который тускнеет на воздухе и достаточно мягкий, чтобы его можно было резать ножом. Церий — второй элемент в ряду лантанидов. Церий также традиционно считается одним из редкоземельных элементов. 140,1 59 PR Praseodymium Lanthanoids Praseodymium Discoverer: Von Welsbach, Baron Auer Категория элементов 9002 9002 9002 9002 9002 9002 9002 9002 9002 9002 9002 9002 9002 9002 9002 9002 9002 9002 9002 9002 9002 9002 9002 Празеодим — мягкий, серебристый, ковкий и пластичный металл, ценимый за свои магнитные, электрические, химические и оптические свойства. Празеодим является третьим членом ряда лантанидов и традиционно считается одним из редкоземельных металлов. 140,9 AMU 60 ND Neodymium Lanthanoids Neodymium Discoverer: Von Welsbach, Baron Auer Catelector: Lanthanes Неодим — мягкий серебристый металл, который тускнеет на воздухе. Неодим не встречается в природе в металлической форме или в несмешанном виде с другими лантаноидами, и его обычно очищают для общего использования. Хотя неодим относится к редкоземельным элементам, он довольно распространен. 144,24 а.е.м. 61 Pm Прометий Лантаноиды Прометий Первооткрыватель: Маринский, Джейкоб А. и Кориелл, Лоуэр, Чарльз Д. и Гленсенденин. E. Категория элемента: лантаноиды Прометий — это химический элемент с атомным номером 61 , что означает, что в атомной структуре 61 протон и 61 электрон. Прометий — один из двух таких элементов, за которыми в периодической таблице следуют элементы со стабильными формами. Все его изотопы радиоактивны. В ядерных реакторах равновесие по прометию существует при работе на мощности. Это равновесие также известно как «резервуар самария-149», поскольку весь этот прометий должен подвергнуться распаду до самария. 145 а.о.0003 Категория элемента: лантаноиды Самарий — это химический элемент с атомным номером 62 , что означает, что в атомной структуре 62 протона и 62 электрона. Химический символ для самария — это Sm . Самарий — типичный представитель ряда лантанидов, это серебристый металл средней твердости, легко окисляющийся на воздухе. Самарий назван в честь минерала самарскита, из которого он был выделен. Хотя самарий классифицируется как редкоземельный элемент, он занимает 40-е место по распространенности в земной коре и встречается чаще, чем такие металлы, как олово. 150,36 AMU 63 EU Europium Lanthanoids Europium Discoverer: Demarçay, Eugène-Antole Категория элементов: Lanthanoids Европий — умеренно твердый металл серебристого цвета, который легко окисляется на воздухе и в воде. Являясь типичным членом ряда лантанидов, европий обычно принимает степень окисления +3. Европий — один из наименее распространенных элементов во Вселенной. Только около 5 × 10−8% всей материи во Вселенной составляет европий. 151,96 ам.0003 Категория элемента: лантаноиды Гадолиний — это химический элемент с атомным номером 64 , что означает, что в атомной структуре 64 протона и 64 электрона. Химический символ для гадолиния равен Gd . Гадолиний относится к редкоземельным элементам (это один из семнадцати химических элементов периодической таблицы). В ядерной промышленности гадолиний обычно используется в качестве поглотителя нейтронов из-за очень высокого поперечного сечения поглощения нейтронов двух изотопов 155Gd и 157Gd. На самом деле их сечения поглощения самые высокие среди всех стабильных изотопов. 157,25 AMU 65 TB Тербий Lanthanoids Terbium Discongerer: Mosander, Carl Gustav Категория элементов: Lanthanoids Тербий — серебристо-белый редкоземельный металл, ковкий, пластичный и достаточно мягкий, чтобы его можно было разрезать ножом. Тербий, девятый член ряда лантанидов, является довольно электроположительным металлом, который реагирует с водой с выделением газообразного водорода. 158.92 amu 66 Dy Dysprosium Lanthanoids Dysprosium Discoverer: Lecoq de Boisbaudran, Paul-Émile Element Category: Lanthanoids Dysprosium is a chemical element with atomic number 66 , что означает, что в структуре атома 66 протонов и 66 электронов. Химический символ для диспрозия — это Dy . — редкоземельный элемент с металлическим серебряным блеском. Диспрозий используется из-за его высокого поперечного сечения поглощения тепловых нейтронов при изготовлении управляющих стержней в ядерных реакторах из-за его высокой магнитной восприимчивости в приложениях для хранения данных. 162,5 AMU 67 HO Holmium Lanthanoids Holmium Discoverer: Cleve, Per Theodor Категория элементов: Lanthanoids Holmium 6. в структуре атома 67 протонов и 67 электронов. Химический символ для гольмия равен Ho . Гольмий относится к ряду лантанидов, гольмий относится к редкоземельным элементам. Гольмий — относительно мягкий и ковкий металл серебристо-белого цвета. 164.94 AMU 68 ER ERBIUM Lanthanoids Erbium Discoverer: Mosander, Carl Gustav Категория элементов: Lanthanoids 26266 2 -й Chim -Emlection 2626262626266 2 -й. в структуре атома 68 протонов и 68 электронов. Химический символ для эрбия равен Er . Эрбий представляет собой серебристо-белый твердый металл при искусственном выделении, природный эрбий всегда находится в химическом сочетании с другими элементами. 167,25 AMU 69 TH Thulium Lanthanoids Thulium Discoverer: Cleave, Per Teodor Категория элементов: Lanthanoids Thulail 66.9.6 2.6 2 -й. в структуре атома 69 протонов и 69 электронов. Химический символ для тулия — это Tm . Тулий — легко обрабатываемый металл с ярким серебристо-серым блеском. Он довольно мягкий и медленно тускнеет на воздухе. Несмотря на высокую цену и редкость, тулий используется в качестве источника излучения в портативных рентгеновских аппаратах. Тулий является тринадцатым и третьим последним элементом в ряду лантаноидов. 168.93 amu 70 Yb Ytterbium Lanthanoids Ytterbium Discoverer: De Marignac, Jean Charles Galissard Element Category: Lanthanoids Ytterbium is a chemical element with atomic number 70 что означает, что в структуре атома 70 протонов и 70 электронов. Из-за его электронной конфигурации с замкнутой оболочкой его плотность, а также температуры плавления и кипения значительно отличаются от большинства других лантаноидов. 173.04 71 Lu Lutetium Lanthanoids Lutetium Discoverer: Hurbain, Georges категория: Lanthanoids Лютеций представляет собой серебристо-белый металл, устойчивый к коррозии в сухом воздухе, но не во влажном. Лютеций является последним элементом в ряду лантаноидов и традиционно считается одним из редкоземельных элементов. 174.96 amu 89 Ac Actinium Actinoids Actinium Discoverer: Debierne, André Element Category: Actinoids Actinium is a chemical element with atomic number 89 which means there 89 протонов и 89 электронов в атомной структуре. Актиний — мягкий серебристо-белый радиоактивный металл. Актиний дал название ряду актинидов, группе из 15 подобных элементов между актинием и лоуренцием в периодической таблице. 227 AMU 90 TH Thorium Actinoids Thorium Discoverer: Berzelius, Jöns Jacob Категория элементов: Actinoids Thor 262. в структуре атома 90 протонов и 90 электронов. Химический символ для тория равен Th . Металлический торий имеет серебристый цвет и тускнеет на воздухе, образуя диоксид. Торий умеренно твердый, ковкий и имеет высокую температуру плавления. Торий является природным элементом, и, по оценкам, его примерно в три раза больше, чем урана. Торий обычно встречается в монацитовых песках (редкоземельные металлы, содержащие фосфатный минерал). 232.03 AMU 91 PA Protactinium Actinoids Protactinium Discoverer: Göhring, Otto и Fajans, Kasimir Категори , что означает, что в структуре атома 91 протон и 91 электрон. Протактиний – плотный серебристо-серый металл, легко реагирующий с кислородом, парами воды и неорганическими кислотами. 231.03 AMU 92 U Уран Actinoids Уран Discoverer: Klaproth, Martin Heinrich Категория элементов: Actinoids 626262626262626262626262626262626262. в структуре атома 92 протона и 92 электрона. Химический символ для урана равен U . Уран — серебристо-белый металл актинидного ряда периодической таблицы. Уран слаборадиоактивен, потому что все изотопы урана нестабильны, а период полураспада колеблется между 159,200 лет и 4,5 миллиарда лет. Уран имеет самый высокий атомный вес среди первично встречающихся элементов. Его плотность примерно на 70% выше, чем у свинца, и немного ниже, чем у золота или вольфрама. 238,03 AMU 93 NP NEPTUNIUM Actinoids NEPTUNIUM Discoverer: McMillan, Edwin M. Celection: Actinoids 555.metrint Alementile Alementile Amele. атомный номер 93 , что означает, что в структуре атома 93 протона и 93 электрона. Химический символ для нептуния – Np . Металлический нептуний имеет серебристый цвет и тускнеет на воздухе. Нептуний — первый трансурановый элемент. 237 а.е.м. 94 Pu Плутоний Актиноиды Плутоний Первооткрыватель: Гленн Т. Сиборг, Джозеф У.0002 Категория элемента: актиноиды Плутоний — это химический элемент с атомным номером 94 , что означает, что в атомной структуре 94 протона и 94 электрона. Химический символ для плутония равен Pu . Плутоний представляет собой актинидный металл серебристо-серого цвета, который тускнеет на воздухе и образует матовое покрытие при окислении. 244 а. 95 Ам Америций Актиноиды Америций Первооткрыватель: Гленн Т. Сиборг, Ральф А. Джеймс, Леон О. Морган, Альберт Гиорсо 95 протонов и 95 электронов в атомной структуре. Химический символ для америция — Am . Америций является трансурановым членом ряда актинидов, в периодической таблице расположен под лантанидным элементом европием, и поэтому по аналогии был назван в честь Америки. 243 AMU 96 CM Curium Актиноиды Curium Discoverer: Гленн Т. Seaborg, Ralph A. James, Albert Ghiorso Категори с атомным номером 96 , что означает, что в атомной структуре 96 протонов и 96 электронов. Химический символ для кюрия равен см . Кюрий — твердый, плотный, серебристый металл с относительно высокой температурой плавления и кипения для актинида. 247 AMU 97 BK Berkelium Actinoids Berkelium Discoverer: Stanley G. Elementsemory: Atbertid2 9000.3 : 3 : 3 . Берклий — это химический элемент с атомным номером 97 , что означает, что в атомной структуре 97 протонов и 97 электронов. Химический символ для Berkelium — это Bk . Берклий относится к ряду актиноидов и трансурановых элементов. 247 98 CF Californium Actinoids Californium Discoverer: Stanley G. Thompson, Glenn T. Seaborg, Kenneth Street, Jr., Albert Ghiorso Category: Acteth Street, Jr., Albert Ghiorso : Actethtsthers Калифорний является актинидным элементом, шестым трансурановым элементом, который был синтезирован, и имеет вторую по величине атомную массу из всех элементов, которые были произведены в количествах, достаточно больших, чтобы их можно было увидеть невооруженным глазом (после эйнштейния). 251 а.е.м. 99 Es Эйнштейний Актиноиды Эйнштейний Первооткрыватель: Albert Ghiorso et. др. Категория элемента: актиноиды Эйнштейний — это химический элемент с атомным номером 99 , что означает, что в атомной структуре 99 протонов и 99 электронов. Химический символ для эйнштейния — это Es . Эйнштейний — седьмой трансурановый элемент и актинид. 252 а.е.м. 100 Fm Фермиум Актиноиды Фермиум Первооткрыватель: Albert Ghiorso et. др. Категория элемента: актиноиды Фермий — это химический элемент с атомным номером 100 , что означает, что в атомной структуре 100 протонов и 100 электронов. Химический символ для Фермия равен Fm . Фермий относится к ряду актинидов. Это самый тяжелый элемент, который может быть образован нейтронной бомбардировкой более легких элементов, и, следовательно, последний элемент, который можно получить в макроскопических количествах. 257 AMU 101 MD Mendelevium Actinoids Mendelevium Discoverer: Stanley G. Thompson, Glenn T. Seaborg, Bernard G. Harvey, Gregory R. Choppin, Albert. Ghiors 2 Менделевий — это химический элемент с атомным номером 101 , что означает, что в атомной структуре 101 протон и 101 электрон. Химический символ для менделевия равен 9.0025 Мд . Менделевий — металлический радиоактивный трансурановый элемент из ряда актинидов, это первый элемент, который в настоящее время не может быть произведен в макроскопических количествах. 258 AMU 102 NO NOBELIUM Актиноиды НОБЕЛИЙ Discoverer: Albert Ghiorso, Glenn T. Seaborg, Torbørn Sikkeland, John R. Walton . химический элемент с атомным номером 102 , что означает, что в структуре атома 102 протона и 102 электрона. Химический символ для нобелия — это № . Нобелий — десятый трансурановый элемент и предпоследний член ряда актинидов. Как и все элементы с атомным номером более 100, нобелий можно получить только в ускорителях частиц путем бомбардировки более легких элементов заряженными частицами. 259 а.е.м. 103 Lr Лоренсиум актиноиды Lawrencium Discoverer: Albert Ghiorso, Torbjørn Sikkeland, Almon E. Larsh, Robert M. Latimer Категория: Actinoids Lawrencium является химическим элементом с Atomic Number . 103 протона и 103 электрона в структуре атома. Лоуренсиум — последний член серии актинидов. Как и все элементы с атомным номером более 100, лоуренсий можно получить только в ускорителях частиц путем бомбардировки более легких элементов заряженными частицами. 262 а.е.м. Никель – серебристо-белый блестящий металл с легким золотистым оттенком. Никель относится к переходным металлам, тверд и пластичен. Никель это химический элемент с атомным номером 28 , что означает, что в атомной структуре 28 протонов и 28 электронов. Атом состоит из небольшого, но массивного ядра , окруженного облаком быстро движущихся электронов . Ядро состоит из протонов и нейтронов. Общее количество протонов в ядре называется атомный номер атома и обозначен символом Z . Таким образом, общий электрический заряд ядра равен +Ze, где e (элементарный заряд) равен 1,602 x 10 -19 кулонов . В нейтральном атоме электронов столько же, сколько протонов, движущихся вокруг ядра. Именно электроны ответственны за химическое поведение атомов и определяют различные химические элементы. См. также: Атомный номер – сохраняется ли он в ядерной реакции? Каждое твердое тело, жидкость, газ и плазма состоят из нейтральных или ионизированных атомов. Химические свойства атома определяются количеством протонов, фактически количеством и расположением электронов. Это принцип запрета Паули , который требует, чтобы электроны в атоме занимали разные энергетические уровни вместо того, чтобы все они конденсировались в основном состоянии. Упорядочивание электронов в основном состоянии многоэлектронных атомов начинается с самого низкого энергетического состояния (основного состояния) и постепенно перемещается оттуда вверх по энергетической шкале, пока каждому из электронов атома не будет присвоен уникальный набор квантовых чисел. Этот факт имеет ключевое значение для построения периодической таблицы элементов. Массовые числа типичных изотопов Никеля равны 60; 61; 62; 64. Общее число нейтронов в ядре атома называется числом нейтронов атома и обозначается символом N . Число нейтронов плюс атомный номер равняется атомному массовому числу: N+Z=A . Разница между числом нейтронов и атомным номером известна как избыток нейтронов 9.0026 : Д = Н — Z = А — 2Z. Номер нейтрона редко записывается явно в виде символа нуклида, но появляется в виде нижнего индекса справа от символа элемента. Нуклиды, имеющие одинаковое число нейтронов, но разное число протонов, называются изотонами. Различные виды атомов, ядра которых содержат определенное количество протонов и нейтронов, называются нуклидами . Каждый нуклид обозначается химическим символом элемента (это указывает Z) с номером атомной массы в качестве верхнего индекса. Поэтому мы не можем определить нейтронное число, например, урана. Мы можем определить число нейтронов определенного изотопа. Например, нейтронное число урана-238 равно 238-9. Свойства атомных ядер (атомная масса, ядерные сечения) определяются числом протонов и числом нейтронов (нейтронным числом). Следует отметить, что особенно ядерные сечения могут варьироваться на много порядков от нуклида с числом нейтронов N до нуклида с числом нейтронов N+1. Например, актиниды с нечетным числом нейтронов обычно делящиеся (делящиеся медленными нейтронами), в то время как актиниды с четным числом нейтронов обычно не делящиеся (но могут делиться быстрыми нейтронами). Тяжелые ядра с четным числом протонов и четным числом нейтронов (из-за принципа запрета Паули) очень стабильны благодаря возникновению «парного спина». С другой стороны, ядра с нечетным числом протонов и нейтронов в основном нестабильны. Ядерная стабильность – это понятие, которое помогает определить стабильность изотопа. Атомные ядра состоят из протонов и нейтронов, которые притягиваются друг к другу ядерной силой , а протоны отталкиваются друг от друга электрической силой из-за их положительного заряда. Эти две силы конкурируют, что приводит к различной устойчивости ядер. Нейтроны стабилизируют ядро , потому что они притягивают друг друга и протоны , что помогает компенсировать электрическое отталкивание между протонами. В результате, по мере увеличения числа протонов требуется возрастающее отношение нейтронов к протонам , чтобы сформировать стабильное ядро. Если нейтронов слишком много или слишком мало для данного количества протонов, полученное ядро не является стабильным и подвергается радиоактивному распаду. Нестабильные изотопы распадаются по различным путям радиоактивного распада, чаще всего альфа-распаду, бета-распаду, гамма-распаду или захвату электронов. Известно много других редких типов распада, таких как спонтанное деление или испускание нейтронов. Атомная масса никеля составляет 58,6934 ед. Атомная масса – это масса атома. Атомная масса или относительная изотопная масса относится к массе отдельной частицы и, следовательно, привязана к определенному конкретному изотопу элемента. Атомная масса переносится атомным ядром, которое занимает всего около 10 -12 от общего объема атома или меньше, но содержит весь положительный заряд и не менее 99,95% от общей массы атома. Обратите внимание, что каждый элемент может содержать больше изотопов, поэтому результирующая атомная масса рассчитывается на основе встречающихся в природе изотопов и их распространенности. Размер и масса атомов настолько малы, что использование обычных единиц измерения, хотя и возможно, часто неудобно. Единицы измерения массы и энергии были определены в атомном масштабе, чтобы сделать измерения более удобными для выражения. Единицей измерения массы является атомная единица массы (а.е.м.) . Одна атомная единица массы равна 1,66 х 10 -24 граммов. Для 12 C атомная масса точно равна 12u, так как из нее определяется единица атомной массы. Для других изотопов изотопная масса обычно отличается и обычно находится в пределах 0,1 ед от массового числа. Например, 63 Cu (29 протонов и 34 нейтрона) имеет массовое число 63, а изотопная масса в его ядерном основном состоянии составляет 62, ед. Различие между массовым числом и изотопной массой, известное как дефект массы, объясняется двумя причинами: Это увеличивает массу ядер с большим количеством нейтронов, чем протонов, относительно шкалы единиц атомной массы, основанной на 12 C с равным количеством протонов и нейтронов. Заметим, что была найдена масса покоя атомного ядра заметно меньше, чем сумма масс покоя составляющих его протонов, нейтронов и электронов. Масса больше не считалась неизменной в замкнутой системе. Разница является мерой ядерной энергии связи , которая удерживает ядро вместе. Согласно соотношению Эйнштейна (E=mc 2 ), эта энергия связи пропорциональна этой разности масс и известна как дефект массы . См. также: Атомное массовое число – сохраняется ли оно в ядерной реакции? Атомный радиус атома никеля составляет 124 пм (ковалентный радиус). Следует отметить, что атомы не имеют четкой внешней границы. Атомный радиус химического элемента является мерой расстояния, на которое простирается электронное облако от ядра. В периодической таблице элементов атомный радиус имеет тенденцию увеличиваться при перемещении вниз по столбцам, но уменьшается при перемещении по строкам (слева направо). Объем атома примерно На 15 порядков больше , чем объем ядра. Для атома урана Ван-дер-Ваальсов радиус составляет около 186 пм = 1,86 × 10 −10 м . Радиус Ван-дер-Ваальса, r w , атома — это радиус воображаемой твердой сферы, представляющий расстояние наибольшего сближения с другим атомом. Принимая сферическую форму, атом урана имеет объем около 26,9 × 10 −30 м 3 . Может показаться, что пространство и на самом деле материя пусто , но это не . Из-за квантовой природы электронов электроны не являются точечными частицами, они размазаны по всему атому. Классическое описание нельзя использовать для описания вещей на атомном уровне. В атомном масштабе физики обнаружили, что квантовая механика очень хорошо описывает вещи в этом масштабе. Расположение частиц в квантовой механике не находится в точном положении, они описываются функция плотности вероятности . Поэтому пространство в атоме (между электронами и атомным ядром) не пусто, а заполнено функцией плотности вероятности электронов (обычно известной как « электронных облаков »). Плотность Никель составляет 8,908 г/см 3 . Типичные плотности различных веществ даны при атмосферном давлении. Плотность определяется как масса на единицу объема . Это интенсивное свойство , которое математически определяется как масса, деленная на объем: ρ = m/V Другими словами, плотность (ρ) вещества равна общей массе (m) этого вещества. разделить на общий объем (V), занимаемый этим веществом. Стандартная единица СИ составляет килограммов на кубический метр ( кг/м 3 ). Стандартной английской единицей измерения является масса фунтов на кубический фут ( фунтов/фут 3 ). Поскольку плотность (ρ) вещества равна общей массе (m) этого вещества, деленной на общий объем (V), занимаемый этим веществом, очевидно, что плотность вещества сильно зависит от его атомной массы, а также от атомного номера плотности (N; атомов/см 3 ), Поскольку нуклонов ( протонов и нейтронов обычной материи) составляют большую часть массы обычного вещества . Если учесть элементы, созданные человеком, то самым плотным на данный момент является Hassium . Хассий — это химический элемент с символом Hs и атомным номером 108. Это синтетический элемент (впервые синтезированный в Хассе в Германии) и радиоактивный. Самый стабильный известный изотоп, 269 Hs имеет период полураспада примерно 9,7 секунды. Расчетная плотность составляет 40,7 x 10 3 кг/м 3 . Плотность хассия обусловлена его высоким атомным весом и значительным уменьшением ионных радиусов элементов в ряду лантаноидов, известных как лантанид и сокращение актинидов . Плотность материала зависит от температуры и давления. Это изменение обычно мало для твердых тел и жидкостей, но значительно больше для газов. Большинство материалов расширяются при повышении температуры. Повышение температуры заставляет жидкость в трубчатом термометре расширяться и изгибать биметаллические полоски. В результате этого расширения плотность большинства материалов уменьшается. Этот эффект вызван уменьшением плотности атомных номеров. Эта зависимость обычно выражается коэффициент линейного или объемного расширения . Увеличение давления на материал (особенно для жидкостей или газов) уменьшает объем объекта и, таким образом, увеличивает его плотность за счет плотности атомного числа. Сжимаемость (также известная как коэффициент сжимаемости — это мера относительного изменения объема жидкости или твердого тела в ответ на изменение давления (или среднего напряжения). См. См. также: Самые плотные материалы Земли Электронная конфигурация Никель : [Ar] 3d8 4s2 . Возможные степени окисления: +2,3 . Периодическая таблица представляет собой табличное отображение химических элементов, организованных на основе их атомных номеров, электронных конфигураций и химических свойств. Электронная конфигурация — это распределение электронов атома или молекулы (или другой физической структуры) на атомных или молекулярных орбиталях. Знание электронных конфигураций различных атомов полезны для понимания структуры периодической таблицы элементов. Каждое твердое тело, жидкость, газ и плазма состоят из нейтральных или ионизированных атомов. Химические свойства атома определяются количеством протонов, фактически количеством и расположением электронов . Это принцип запрета Паули , который требует, чтобы электроны в атоме занимали разные энергетические уровни вместо того, чтобы все они конденсировались в основном состоянии. Упорядочивание электронов в основном состоянии многоэлектронных атомов начинается с самого низкого энергетического состояния (основного состояния) и постепенно перемещается оттуда вверх по энергетической шкале, пока каждому из электронов атома не будет присвоен уникальный набор квантовых чисел. Этот факт имеет ключевое значение для построения периодической таблицы элементов. Первые два столбца в левой части таблицы Менделеева занимают s подоболочки. Для атомов с большим количеством электронов это обозначение может стать длинным, поэтому используется сокращенное обозначение. Электронная конфигурация может быть представлена как остовные электроны, эквивалентные инертным газам предыдущего периода, и валентные электроны (например, [Xe] 6s2 для бария). Степени окисления обычно представляются целыми числами, которые могут быть положительными, нулевыми или отрицательными. Текущее определение степени окисления в Золотой книге ИЮПАК: «Степень окисления атома — это заряд этого атома после ионной аппроксимации его гетероядерных связей…» , и термин «степень окисления» является почти синонимом. Элемент, который не сочетается ни с какими другими элементами, имеет степень окисления 0. Степень окисления 0 встречается у всех элементов — это просто элемент в его элементарной форме. Атом элемента в соединении будет иметь положительную степень окисления, если у него удалены электроны. Точно так же добавление электронов приводит к отрицательной степени окисления. Мы также различаем возможные и распространенные степени окисления каждого элемента. Например, кремний имеет девять возможных целочисленных степеней окисления от -4 до +4, но только -4, 0 и +4 являются обычными степенями окисления. Сродство к электрону Никель составляет 112 кДж/моль . Электроотрицательность никеля составляет 1,91 . В химии и атомной физике сродство к электрону атома или молекулы определяется как: изменение энергии (в кДж/моль) нейтрального атома или молекулы (в газообразном фаза), когда электрон присоединяется к атому, образуя отрицательный ион . X + e – → X – + энергия Сродство = – ∆H Другими словами, это можно выразить как вероятность нейтрального атома получить электрон . Обратите внимание, что энергия ионизации измеряет тенденцию нейтрального атома сопротивляться потере электронов. Сродство к электрону измерить труднее, чем энергию ионизации. Например, атом никеля в газовой фазе отдает энергию, когда он получает электрон, образуя ион никеля. Ni + e – → Ni – – ∆H = сродство = 112 кДж/моль Чтобы правильно использовать сродство к электрону, важно следить за знаком. При присоединении электрона к нейтральному атому выделяется энергия. Это сродство известно как сродство к первому электрону, и эти энергии отрицательны. По соглашению отрицательный знак показывает высвобождение энергии. Однако для присоединения электрона к отрицательному иону требуется больше энергии, что подавляет любое высвобождение энергии в процессе присоединения электрона. Это сродство известно как сродство ко второму электрону, и эти энергии положительны. Сродство к электрону может быть как положительным, так и отрицательным значением. Чем больше отрицательное значение, тем стабильнее анион. Хотя сродство сильно различается в периодической таблице, возникают некоторые закономерности. Как правило, элементы в правой части периодической таблицы имеют большое отрицательное сродство к электрону. Сродство неметаллов и сродство металлов Электроотрицательность , символ χ, представляет собой химическое свойство, которое описывает тенденцию атома притягивать электроны к этому атому. Для этой цели чаще всего используется безразмерная величина шкала Полинга , символ χ. Электроотрицательность никеля: χ = 1,91 В общем случае на электроотрицательность атома влияет как его атомный номер, так и расстояние, на котором его валентные электроны находятся от заряженного ядра. Чем выше связанное число электроотрицательности, тем больше элемент или соединение притягивает к себе электроны. Наиболее электроотрицательному атому, фтору, присвоено значение 4,0, а значения варьируются до цезия и франция, которые являются наименее электроотрицательными при 0,7. Электроотрицательность связана с энергией ионизации и сродством к электрону. Первая энергия ионизации никеля составляет 7,6398 эВ . Энергия ионизации , также называемая потенциалом ионизации , представляет собой энергию, необходимую для удаления электрона из нейтрального атома. X + энергия → X + + e − , где X — любой атом или молекула, способная к ионизации, X + — атом или молекула с удаленным электроном (положительный ион), и е – – удаленный электрон. Атому никеля, например, требуется следующая энергия ионизации для удаления самого внешнего электрона. Ni + IE → Ni + + e − IE = 7,6398 эВ Чаще всего используется энергия ионизации, связанная с удалением первого электрона. Энергия ионизации n th относится к количеству энергии, необходимой для удаления электрона из частиц с зарядом ( n -1). 1 -й Ионизационная энергия x → x + + E – 2 -я энергия ионизации x + → X 2+ + E – Энергия ионизации для различных элементов Для каждого последующего удаленного электрона существует энергия ионизации. Электроны, вращающиеся вокруг ядра, движутся по довольно четко определенным орбитам. Как правило, энергия ионизации увеличивается при движении вверх по группе и при перемещении слева направо по периоду. Энергия ионизации связана с электроотрицательностью и сродством к электрону. Электроны с низкими энергиями ионизации имеют низкую электроотрицательность, потому что их ядра не оказывают сильного притяжения на электроны. Элементы с высокой энергией ионизации имеют высокую электроотрицательность из-за сильного притяжения, оказываемого положительным ядром на отрицательные электроны. Следовательно, электроотрицательность максимальна в правом верхнем углу периодической таблицы и уменьшается в левом нижнем углу. Более того: Например, для ионизации натрия требуется всего 496 кДж/моль или 5,14 эВ/атом. С другой стороны, неон, благородный газ, непосредственно предшествующий ему в периодической таблице, требует 2081 кДж/моль или 21,56 эВ/атом. Температура плавления никеля 1455°C . Температура кипения никеля 2730°C . Обратите внимание, что эти точки связаны со стандартным атмосферным давлением. В общем, кипение представляет собой фазовый переход вещества из жидкой фазы в газовую. Температура кипения вещества – это температура, при которой происходит это фазовое превращение (кипение или испарение). Как видно, температура кипения жидкости варьируется в зависимости от давления окружающей среды. В периодической таблице элементов гелий имеет самую низкую температуру кипения. Обе точки кипения рения и вольфрама превышают 5000 К при стандартном давлении. Поскольку трудно точно и беспристрастно измерить экстремальные температуры, в литературе упоминаются оба вещества с более высокой температурой кипения. Вообще говоря, плавление представляет собой фазовый переход вещества из твердого состояния в жидкое. Температура плавления вещества — это температура, при которой происходит это фазовое превращение. См. также: Депрессия точки плавления Первая теория, объясняющая механизм плавления в объеме, была предложена Линдеманном, который использовал колебания атомов в кристалле для объяснения плавления. Твердые тела похожи на жидкости тем, что оба находятся в конденсированном состоянии, а частицы находятся гораздо ближе друг к другу, чем частицы газа. Как и в случае с точками кипения, точка плавления твердого тела зависит от силы этих сил притяжения. Ковалентные связи часто приводят к образованию небольших наборов лучше связанных атомов, называемых молекулами, которые в твердых телах и жидкостях связаны с другими молекулами силами, которые часто намного слабее, чем ковалентные связи, удерживающие молекулы вместе внутри. Такие слабые межмолекулярные связи придают органическим молекулярным веществам, таким как воски и масла, их мягкий объемный характер и низкие температуры плавления (в жидкостях молекулы должны прекратить наиболее структурированный или ориентированный контакт друг с другом). Теплопроводность никеля составляет 90,7 Вт/(м·К). Характеристики теплопередачи твердого материала измеряются свойством, называемым теплопроводностью , k (или λ), измеряемой в Вт/м·K . Это мера способности вещества передавать тепло через материал путем теплопроводности. Обратите внимание, что закон Фурье применим ко всей материи, независимо от ее состояния (твердое, жидкое или газообразное), поэтому он также определен для жидкостей и газов. Теплопроводность большинства жидкостей и твердых тел зависит от температуры. Для паров это также зависит от давления. В общем: Большинство материалов почти однородны, поэтому обычно мы можем написать k = k (T) . Аналогичные определения связаны с теплопроводностями в направлениях y и z (ky, kz), но для изотропного материала теплопроводность не зависит от направления переноса, kx = ky = kz = k. Перенос тепловой энергии в твердых телах обычно может быть обусловлен двумя эффектами: Когда электроны и фононы переносят тепловую энергию, приводящую к теплопроводности в твердом теле, теплопроводность может быть выражена как: их структура связана с наличием носителей заряда, в частности электронов . Электрическая и теплопроводность металлов обусловлена тем фактом, что их внешних электронов делокализованы . Их вклад в теплопроводность обозначается как электронная теплопроводность , k e . Фактически, в чистых металлах, таких как золото, серебро, медь и алюминий, тепловой ток, связанный с потоком электронов, намного превышает небольшой вклад, обусловленный потоком фононов. Напротив, для сплавов вкладом k ph в k уже нельзя пренебречь. Для неметаллические твердые вещества , k определяется в первую очередь k ph , которое увеличивается по мере уменьшения частоты взаимодействий между атомами и решеткой. квантов колебательного поля кристалла называются « фононами ». Фонон представляет собой коллективное возбуждение в периодическом упругом расположении атомов или молекул в конденсированных средах, таких как твердые тела и некоторые жидкости. Фононы играют важную роль во многих физических свойствах конденсированного вещества, таких как теплопроводность и электропроводность. В физике жидкость — это вещество, которое постоянно деформируется (течет) под действием приложенного напряжения сдвига. Флюиды являются подмножеством фаз материи и включают жидкости , газы , плазма и, в некоторой степени, твердые пластмассы. Поскольку межмолекулярное расстояние намного больше, а движение молекул более хаотично для жидкого состояния, чем для твердого состояния, перенос тепловой энергии менее эффективен. Следовательно, теплопроводность газов и жидкостей обычно меньше, чем у твердых тел. В жидкостях теплопроводность обусловлена атомной или молекулярной диффузией. Теплопроводность газов Влияние температуры, давления и химических соединений на теплопроводность газа можно объяснить с точки зрения кинетической теории газов . Воздух и другие газы обычно являются хорошими изоляторами при отсутствии конвекции. Таким образом, многие изоляционные материалы (например, полистирол) функционируют просто благодаря большому количеству заполненных газом карманов , которые предотвращают широкомасштабную конвекцию . Чередование газового кармана и твердого материала приводит к тому, что тепло должно передаваться через множество поверхностей раздела, что приводит к быстрому снижению коэффициента теплопередачи. Теплопроводность газов прямо пропорциональна плотности газа, средней скорости молекул и особенно длине свободного пробега молекулы. Как правило, теплопроводность газов увеличивается с повышением температуры. Теплопроводность жидкостей Как уже писалось, в жидкостях теплопроводность обусловлена атомной или молекулярной диффузией, но физические механизмы объяснения теплопроводности жидкостей изучены недостаточно. Жидкости, как правило, обладают лучшей теплопроводностью, чем газы, а способность течь делает жидкость подходящей для отвода избыточного тепла от механических компонентов. Тепло можно отводить, пропуская жидкость через теплообменник. Теплопроводность неметаллических жидкостей обычно уменьшается с повышением температуры. Коэффициент линейного теплового расширения Никель равен 13,4 мкм/(м·K) Тепловое расширение – это обычно тенденция материи изменять свои размеры в ответ на изменение в температуре. Обычно его выражают в виде доли изменения длины или объема на единицу изменения температуры. Тепловое расширение характерно для твердых тел, жидкостей и газов. В отличие от газов или жидкостей, твердые материалы, как правило, сохраняют свою форму при тепловом расширении. А 9Коэффициент линейного расширения 0025 обычно используется для описания расширения твердого тела, в то время как коэффициент объемного расширения более полезен для жидкости или газа. Коэффициент линейного теплового расширения определяется как: , где L — это конкретная длина, а dL/dT — скорость изменения этого линейного размера на единицу изменения температуры. Коэффициент объемного теплового расширения является основным коэффициентом теплового расширения и наиболее важным для жидкостей. Как правило, вещества расширяются или сжимаются при изменении их температуры, причем расширение или сжатие происходит во всех направлениях. Коэффициент объемного теплового расширения определяется как: , где л — объем материала, а dV/dT — скорость изменения этого объема на единицу изменения температуры. В твердом теле или жидкости существует динамическое равновесие между силами сцепления, удерживающими атомы или молекулы вместе, и условиями, создаваемыми температурой. Поэтому более высокие температуры предполагают большее расстояние между атомами. Разные материалы имеют разную силу сцепления и, следовательно, разные коэффициенты расширения. Если кристаллическое твердое тело изометрично (имеет во всем одинаковую структурную конфигурацию), расширение будет равномерным во всех измерениях кристалла. Удельная теплоемкость никеля 0,44 Дж/г K . Скрытая теплота плавления никеля 17,47 кДж/моль . Скрытая теплота испарения никеля 370,4 кДж/моль . Удельная теплоемкость или удельная теплоемкость — это свойство, связанное с внутренней энергией , которое очень важно в термодинамике. Интенсивные свойства C V и C P определены для чистых, простых сжимаемых веществ в виде частичных производных Энергии U (T, T, V) 666625 EILPY U (T, V, V) 666666626. , где индексы v и p обозначают переменные, удерживаемые фиксированными во время дифференцирования. Свойства c v и c p называются удельной теплоемкостью (или теплоемкостью ), поскольку при определенных особых условиях они связывают изменение температуры системы с количеством энергии, добавленной теплопередача. Их единицы СИ Дж/кг K или Дж/моль K . Различные вещества подвергаются воздействию различных величин за счет добавления тепла . При подводе к разным веществам определенного количества теплоты их температуры увеличиваются на разную величину. Теплоемкость – это экстенсивное свойство материи, означающее, что она пропорциональна размеру системы. Теплоемкость C имеет единицу измерения энергии на градус или энергию на кельвин. Обычно, когда материал изменяет фазу из твердой в жидкую или из жидкой в газообразную, на это фазовое изменение затрачивается определенное количество энергии. В случае фазового перехода жидкости в газ это количество энергии известно как энтальпия испарения , (символ ∆H vap ; единица измерения: Дж), также известный как (скрытая) теплота испарения или теплота испарения. В качестве примера см. рисунок, на котором показаны фазовые переходы воды. Скрытая теплота – это количество теплоты, добавляемое к веществу или отводимое от него для изменения фазы. Эта энергия разрушает силы межмолекулярного притяжения, а также должна обеспечивать энергию, необходимую для расширения газа (работа pΔV ). Температура, при которой начинает происходить испарение (кипение) при заданном давлении, также известна как температура насыщения , и при этих условиях смесь пара и жидкости может существовать вместе. Можно сказать, что жидкость насыщена тепловой энергией. Любое добавление тепловой энергии приводит к фазовому переходу. При температуре кипения две фазы вещества, жидкость и пар, имеют одинаковую свободную энергию и, следовательно, с одинаковой вероятностью существуют. Ниже точки кипения жидкость является более стабильным состоянием из двух, тогда как выше предпочтительна газообразная форма. В случае перехода из твердого состояния в жидкое изменение энтальпии, необходимое для изменения его состояния, известно как энтальпия плавления (обозначение ∆H fus ; единица измерения: Дж), также известное как (скрытая) теплота плавления . Жидкая фаза имеет более высокую внутреннюю энергию, чем твердая фаза. Это означает, что к твердому телу должна быть подведена энергия, чтобы расплавить его, а энергия высвобождается из жидкости при ее замерзании, потому что молекулы в жидкости испытывают более слабые межмолекулярные силы и, следовательно, имеют более высокую потенциальную энергию (своего рода энергия диссоциации связи). для межмолекулярных сил). Температура, при которой происходит фазовый переход, является точкой плавления . точка плавления также определяет состояние, при котором твердое тело и жидкость могут существовать в равновесии. Добавление тепла превратит твердое тело в жидкость без изменения температуры. Удельное электрическое сопротивление Никель составляет 69,3 нОм·м . Удельное электрическое сопротивление и его обратное значение, электропроводность , является фундаментальным свойством материала, которое количественно определяет, насколько сильно он сопротивляется или проводит поток электрического тока. Вещества, в которых может течь электричество, называются проводниками . Проводники изготавливаются из материалов с высокой проводимостью, таких как металлы, в частности медь и алюминий. Изоляторы , с другой стороны, изготавливаются из самых разных материалов в зависимости от таких факторов, как требуемое сопротивление. Полупроводники – это материалы, неорганические или органические, которые обладают способностью контролировать свою проводимость в зависимости от химической структуры, температуры, освещения и наличия примесей. Чтобы понять разницу между металлами , полупроводниками и электрическими изоляторами , мы должны определить следующие термины из физики твердого тела: Возможная кристаллическая структура никеля представляет собой гранецентрированную кубическую структуру . В металлах и многих других твердых телах атомы расположены в виде правильных рядов, называемых кристаллами. Три наиболее распространенных основных кристаллических узора: – Никель серебристо-белого цвета. твердый, ковкий и пластичный металл. Он относится к группе железа и приобретает высокую полировку. Это довольно хороший проводник тепла и электричества. В своих привычных соединениях никель двухвалентен, хотя и принимает другие валентности. Он также образует ряд сложных соединений. Большинство соединений никеля имеют синий или зеленый цвет. Области применения Никель в основном используется для получения сплавов. Никелевые сплавы характеризуются прочностью, пластичностью, стойкостью к коррозии и нагреву. Около 65 % никеля, потребляемого в западном мире, используется для производства нержавеющей стали, состав которой может варьироваться, но обычно это железо с примерно 18 % хрома и 8 % никеля. 12 % всего потребляемого никеля идет на жаропрочные сплавы. Остальные 23% потребления распределяются между легированной сталью, аккумуляторами, катализаторами и другими химическими веществами, чеканкой монет, литейными изделиями и гальванопокрытием. 9Никель 5408 прост в обработке и может быть вытянут в проволоку. Он устойчив к коррозии даже при высоких температурах и по этой причине используется в газовых турбинах и ракетных двигателях. Монель представляет собой сплав никеля и меди (например, 70% никеля, 30% меди со следами железа, марганца и кремния), который не только твердый, но и может противостоять коррозии в морской воде, поэтому он идеально подходит для изготовления гребных валов на лодках. Никель в окружающей среде Большая часть никеля на Земле недоступна, потому что она заперта в железо-никелевом расплавленном ядре планеты, которое на 10% состоит из никеля. Общее количество никеля, растворенного в море, оценивается примерно в 8 миллиардов тонн. Органические вещества обладают сильной способностью поглощать металл, поэтому уголь и нефть содержат значительные количества. Содержание никеля в почве может составлять от 0,2 до 450 частей на миллион в некоторых глинистых и суглинистых почвах. В среднем около 20 частей на миллион. Никель содержится в некоторых бобах, где он является важным компонентом некоторых ферментов. Другим относительно богатым источником никеля является чай, содержащий 7,6 мг/кг сухих листьев. Никель представляет собой соединение, которое встречается в окружающей среде только в очень малых количествах. Люди используют никель для самых разных целей. Наиболее распространенным применением никеля является использование в качестве ингредиента стали и других металлических изделий. Его можно найти в обычных металлических изделиях, таких как ювелирные изделия. Пищевые продукты естественным образом содержат небольшое количество никеля. Шоколад и жиры, как известно, содержат очень много. Поглощение никеля увеличится, когда люди будут есть большое количество овощей из загрязненных почв. Известно, что растения накапливают никель, и в результате поглощение никеля из овощей будет значительным. Курильщики имеют более высокое поглощение никеля через легкие. Наконец, никель можно найти в моющих средствах. Люди могут подвергаться воздействию никеля при вдыхании воздуха, питьевой воде, употреблении пищи или курении сигарет. Контакт кожи с почвой или водой, загрязненной никелем, также может привести к воздействию никеля. В небольших количествах никель необходим, но когда поглощение слишком велико, он может представлять опасность для здоровья человека. Поглощение слишком больших количеств никеля имеет следующие последствия: Пары никеля раздражают дыхательные пути и могут вызывать пневмонит. Воздействие никеля и его соединений может привести к развитию дерматита, известного как «никелевый зуд», у сенсибилизированных людей. Канцерогенность. Никель и некоторые соединения никеля внесены в список Национальной токсикологической программы (NTP) как канцерогены. Международное агентство по изучению рака (IARC) отнесло соединения никеля к группе 1 (есть достаточные доказательства канцерогенности для человека) и никель к группе 2B (агенты, которые могут быть канцерогенными для человека). OSHA не регулирует никель как канцероген. Никель включен в Уведомление ACGIH о предполагаемых изменениях как категория A1, подтвержденный канцероген для человека. Никель выбрасывается в воздух электростанциями и мусоросжигательными заводами. Затем он осядет на землю или упадет после реакции с каплями дождя. Обычно удаление никеля из воздуха занимает много времени. Большая часть всех соединений никеля, выбрасываемых в окружающую среду, адсорбируется на отложениях или частицах почвы и в результате становится неподвижной. Однако в кислых грунтах никель становится более подвижным и часто вымывается в грунтовые воды. Существует немного информации о воздействии никеля на другие организмы, кроме человека. Мы знаем, что высокие концентрации никеля в песчаных почвах могут нанести вред растениям, а высокие концентрации никеля в поверхностных водах могут снизить скорость роста водорослей. Микроорганизмы также могут страдать от снижения роста из-за присутствия никеля, но обычно через некоторое время у них развивается устойчивость к никелю. Никель в небольших количествах является важным пищевым продуктом для животных. Но никель благоприятен не только как необходимый элемент; это также может быть опасно, когда превышены максимально допустимые количества. Никель не накапливается в растениях или животных. В результате никель не будет биоувеличивать пищевую цепочку. Now check out our page on nickel and water Back to periodic chart Recommended daily intake of nickel 111Bilder Niedrigster Preis Beste Qualität никель-материал Nickel-chemisches Element, Zeichen mit Ordnungszahl und … Chemisches Element Nickel, Vorzeichen mit Ordnungszahl und Ordnungsgewicht, Periodensystemelement Kupfer-Element Химические элементы никеля в периодической системе… Focus auf chemisches Element Nickel beleuchtet im Periodensystem… Wirklich und pure Chemical Elemente-hier abgebildet Nickel-Ni Sammlung einiger Reiner Chemischer Elemente mit 99,9% Klarheit. 3D Render Weiß Blau Lithium Batterien abstraktes Konzept – печать никель в периодической системе элементов, металл с символом Ni Element Nickel, im Periodensystem der Elemente, Elementsymbol Ni Stück Nickel auf Periodensystem von Elementen Никель-символ. Periodensystemsymbol für Nickel Химический элементсимвол – серый Серия Никель-символ. Chemisches Element des Periodensystems…. Ni Nickel Element Information – Fakten, Eigenschaften, Trends,… Infografik des Elements Nickel Химический элемент Symbole Set Kreis Serie 2-Farbe Chemische Element Symbole Set 2 Farbkreis Serie Vektor EPS10 Datei. Periodensystem der chemischen Elemente, abstrakte Wissenschaft Realistische Schaltfläche mit niccolum Symbol. Химический… Никель-Символ. Химический элемент периодической системы. Вектор-Stoc Химический элемент-силуэт-символ-набор 4 Das Periodensystemelement Nickel. Detaillierte Infografik von Nickel Infografik des Nickelelements Große und bunte Infografik zum Element Nickel. Никель-символ-Ni. Element der Periodensystem der Elemente Zeit… Nickel-Symbol – Ni. Element des Periodensystems mit Lupe gezoomt Nickel ist ein chemisches Element, reindustrieller Einsatz. Nickel-Periodensystem Elementsymbol auf weißem Hintergrund Vektor 3 d серебряный элемент “Неодим-Магнит” на деревянном фоне. Минеральный комплекс с химической формулой. Минерал мг, Магнийкомплекс с химическим элементом Elementsymbol. Pharmazeutischer, medizinischer Hintergrund mit Platz für Text. Набор символов химического элемента, 2-цветная серия Chemische Element Symbole Set 2 Farbserie Vektor EPS10 Datei. Das Periodensystemelement Nickel. Вектор-иллюстрация Das Periodensystem Element Nickel.Vector. Ni символ 28 материал для никелевого химического элемента Ni-Symbol 28 Материал для никелевого химического элемента Набор символов химических элементов Kreis Serie 2-Schwarz Набор символов химических элементов 2 Black Circle Series Vector EPS-Datei. Химический элемент Никель. Design-Konzept der Kohlebergbau. Vektor dreidigitale handgezeichnete chemische Silbergrau… Векторный гель Символ элемента Никель Ni. Weißes, ferromagnetisches, formbares, duktiles und hauptsächlich giftiges Metall, das als Teil von Legierungen verwendet wird. Element ist auf weißem Hintergrund isoliert. никель ни химический элемент символ никель ни химический элемент символ – векторная иллюстрация Übergang metals Набор символов химического элемента 2-weiße Serie Schwermetalle – Konzept Bild mit Hand ein Stop-Schild gegen ein. Никель. Убергангсметалле. Химический элемент Менделеева… никель. Убергангсметалле. Chemisches Element des Mendelejewschen Periodensystems. Никель в квадратной форме Würfel kreatives Konzept. Химический элемент никель. Genie mit Element Symbolen ausgeschrieben Das Wort “GENIUS” wird mit Elementsymbolen geschrieben, die von Pyrexlaborgeräten und molekularen Modellen umgeben sind Джин с элементом Symbolen Ausgeschrieben Химический элемент никеля. Символ для химического элемента в никеле Das Periodensystemelement Nickel. Vektor-Illustration Element von Nickel mit Lupe Nickel aus dem Periodensystem der Elemente mit Lupe никель-элемент Periodensystem der Elemente Периодическая таблица элементов никеля символ Abbildung. Infografik des Elements Nickel Große und bunte Infografik zum Element Nickel. Химический элемент Никель. Никель (произношение NICK-‘l [2] 90), представленный химической формулой 7 или 90 Ni [1] , представляет собой твердый, пластичный и ковкий элемент, принадлежащий к семейству переходных металлов [3, 5] . Никель Символ Хотя этот металл иногда встречается в природе в свободном виде, в основном он встречается в рудах, состоящих в основном из пирротина и пентландита (сульфиды никеля и железа), миллерита и гарниерита. Извлекается из полезных ископаемых методами обжига и восстановления [1, 3] . Большое количество никеля попало на Землю через метеориты, попавшие в нее [1] . Происхождение названия: Название представляет собой краткую форму немецкого «kupfernickel», что означает «медь святого Николая» или «медь дьявола» [1] . Кто открыл никель: Шведский химик Аксель Фредрик Кронстедт [1, 2] . Когда он был обнаружен: Год его открытия — 1751 [1] . Как это было обнаружено Кронстедт, работая в Стокгольме в 1751 году, исследовал новый минерал (который сейчас называется никелином), который был найден в шахте в Лос, Хельсингланд в Швеции. Он предположил, что он содержит медь, но то, что он извлек, было новым металлом, который он назвал и объявил никелем в 1754 году. Однако многие химики придерживались мнения, что это был сплав мышьяка, кобальта, меди и железа, хотя на самом деле, они присутствовали только в виде следовых примесей. Чистый никель удалось получить и подтвердить его элементарную природу только в 1775 г. другим шведским химиком, Торберном Бергманом 9 .0075 [1] Металлический никель Где встречается никель в периодической таблице (кДжмоль -1 ) [1] Электронная конфигурация никеля (модель Бора) Никель Изображение Никель является канцерогеном. Это может вызвать кожную и астматическую аллергию. При вдыхании или контакте может неблагоприятно воздействовать на кожу, глаза, нос и легкие [3, 15] . Серьезные состояния здоровья, такие как сердечно-сосудистые заболевания, неврологические расстройства и т. д., также вызываются отравлением никелем [18]. Никель Никелевая монета Чистый металл стоит 7,7 доллара за каждые 100 грамм, оптом такое же количество стоит 1,9 доллара [3] . Ссылки | ||||||||||||||||||||
