Таблица Менделеева online – No
No
102
2
8
32
32
18
8
2
259.1009
5f147s2
Нобелий
| Относительная электроотрицательность (по Полингу): | |
| Температура плавления: | |
| Температура кипения: | |
| Теплопроводность: | 0 |
| Плотность: | |
| Открыт: | |
| Цвет в твёрдом состоянии: | |
| Тип: | Редкоземельный |
| Орбитали: | 1s22s22p63s23p63d104s24p64d104f145s25p65d105f146s26p66d07s2 |
| Электронная формула: |
No – 1s2 2s2 2p6 3s2 3p6 4s2 3d10 No – [Rn] 5f14 7s2 |
| Валентность: | |
| Степени окисления: | 0, +II, III |
| Сверхпроводящее состояние при температуре: | |
| Потенциалы ионизации: | |
Электропроводность в тв. фазе: фазе: |
|
| Ковалентный радиус: | |
| Атомный объем: | |
| Атомный радиус: | |
| Теплота распада: | |
| Теплота парообразования: | |
| Кристаллическая структура: |
Реклама
Изотопы
| Символ нуклида |
Z(p) | N(n) | Масса изотопа (а. е. м.) |
Период полураспада (T1/2) |
Спин и чётность ядра |
|---|---|---|---|---|---|
| Энергия возбуждения | |||||
| 248No | 102 | 146 | 248,08660 | 2 мкс | 0+ |
| 249No | 102 | 147 | 249,08783 | 57 мкс | 5/2+ |
| 250No | 102 | 148 | 250,08751 | 5,7 мкс | 0+ |
| 251No | 102 | 149 | 251,08901 | 780 мс | 7/2+ |
| 251mNo | 110 кэВ | 1,7 с | 9/2- | ||
| 252No | 102 | 150 | 252,088977 | 2,27 с | 0+ |
| 253No | 102 | 151 | 253,09068 | 1,62 мин | 9/2- |
| 253mNo | 129 кэВ | 31 мкс | 5/2+ | ||
| 254No | 102 | 152 | 254,090955 | 51 с | 0+ |
| 254mNo | 500 кэВ | 280 мс | 0+ | ||
| 255No | 102 | 255,093241 | 3,1 мин | 1/2+ | |
| 256No | 102 | 154 | 256,094283 | 2,91 с | 0+ |
| 257No | 102 | 155 | 257,096877 | 25 с | 7/2+ |
| 258No | 102 | 156 | 258,09821 | 1,2 мс | 0+ |
| 259No | 102 | 157 | 259,10103 | 58 мин | 9/2+ |
| 260No | 102 | 158 | 260,10264 | 0+ | |
| 261No | 102 | 159 | 261,10575 | 3 ч | 3/2+ |
| 262No | 102 | 160 | 262,10730 | 5 мс | 0+ |
| 263No | 102 | 161 | 263,11055 | 20 мин | |
| 264No | 102 | 162 | 264,11235 | 1 мин | 0+ |
Таблица менделеева – Электронный учебник K-tree
Электронный учебник
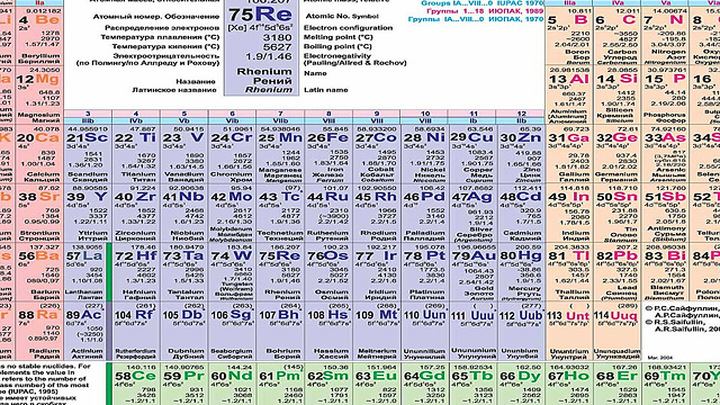
Периодический закон, открытый Д.
1
H
1.008
2
He
4.003
3
Li
6.938
4
Be
9.012
5
B
10.806
6
C
12.01
7
N
14.006
8
O
15.999
9
F
18.998
10
Ne
20.18
11
Na
22.99
12
Mg
24.304
13
Al
26.982
14
Si
28.084
15
P
30.974
16
S
32.059
17
Cl
35.446
18
Ar
39.948
19
K
39.098
20
Ca
40.078
21
Sc
44.956
22
Ti
47.867
23
V
50.942
24
Cr
51.996
25
Mn
54.938
26
Fe
55.845
27
Co
58.933
28
Ni
58.693
29
Cu
63.546
30
Zn
65. 38
38
31
Ga
69.723
32
Ge
72.63
33
As
74.922
34
Se
78.971
35
Br
79.901
36
Kr
83.798
37
Rb
85.468
38
Sr
87.62
39
Y
88.906
40
Zr
91.224
41
Nb
92.906
42
Mo
95.95
44
Ru
101.07
45
Rh
102.906
46
Pd
106.42
47
Ag
107.868
48
Cd
112.414
49
In
114.818
50
Sn
118.71
51
Sb
121.76
52
Te
127.6
53
I
126.904
54
Xe
131.293
55
Cs
132.905
56
Ba
137.327
57
La
138.905
72
Hf
178.49
73
Ta
180.948
74
W
183.84
75
Re
186.207
76
Os
190.23
77
Ir
192.217
78
Pt
195. 084
084
79
Au
196.967
80
Hg
200.592
81
Tl
204.382
82
Pb
207.2
83
Bi
208.98
58
Ce
140.116
59
Pr
140.908
60
Nd
144.242
62
Sm
150.36
63
Eu
151.964
64
Gd
157.25
65
Tb
158.925
66
Dy
162.5
67
Ho
164.93
68
Er
167.259
69
Tm
70
Yb
173.045
71
Lu
174.967
90
Th
232.038
91
Pa
231.036
92
U
238.029
В таблице менделеева колонки называются группами, строки называются периодами. Элементы в группах как правило имеют одинаковые электронные конфигурации внешних оболочек, например, благородные газы – последняя группа, имеют законченную электронную конфигурацию.
Как заполняется электронная конфигурация элементов подробно описано в статье
Скачать таблицу менделеева в хорошем качестве
© 2015-2022 – K-Tree.
По любым вопросам Вы можете связаться по почте [email protected]
Копия материалов, размещённых на данном сайте, допускается только по письменному разрешению владельцев сайта.
нобелия | химический элемент | Британика
nobelium
Посмотреть все СМИ
- Ключевые люди:
- Гленн Т. Сиборг
- Похожие темы:
- химический элемент
Просмотреть все связанные материалы →
нобелий (No) , синтетический химический элемент актиноидного ряда периодической таблицы, атомный номер 102. Элемент назван в честь шведского химика Альфреда Нобеля.
Не встречающийся в природе нобелий был впервые заявлен международной группой ученых, работавших в Нобелевском институте физики в Стокгольме в 1957 году. Они сообщили о синтезе изотопа элемента 102 (изотоп 253 или 255), который распадался с испусканием альфа частицы с периодом полураспада около 10 минут.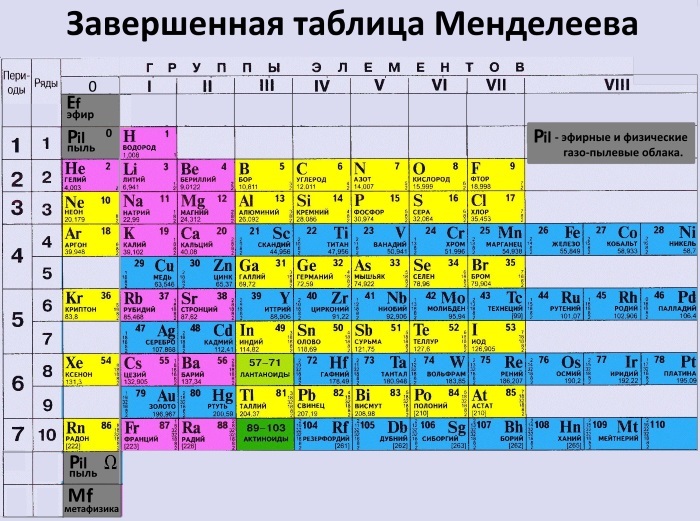 Они назвали его нобелием. В 1958 году американские химики Альберт Гиорсо, Т. Сиккеланд, Дж. Р. Уолтон и Гленн Т. Сиборг из Калифорнийского университета в Беркли сообщили об изотопе 254 как о продукте бомбардировки кюрия (атомный номер 9).6) с ионами углерода (атомный номер 6) в линейном ускорителе тяжелых ионов. В том же году советская научная группа под руководством Георгия Флерова из Объединенного института ядерных исследований в Дубне, Россия, добилась аналогичного результата. Другие эксперименты, проведенные в Советском Союзе (в Институте атомной энергии им. И. В. Курчатова, Москва и в Дубне) и в США (Беркли), не подтвердили стокгольмское открытие. Последующие исследования в следующем десятилетии (в основном в Беркли и Дубне) привели Международный союз теоретической и прикладной химии к выводу, что статьи Дубны, опубликованные в 1966 установил существование изотопа нобелий-254 с периодом полураспада альфа-распада около 51 секунды.
Они назвали его нобелием. В 1958 году американские химики Альберт Гиорсо, Т. Сиккеланд, Дж. Р. Уолтон и Гленн Т. Сиборг из Калифорнийского университета в Беркли сообщили об изотопе 254 как о продукте бомбардировки кюрия (атомный номер 9).6) с ионами углерода (атомный номер 6) в линейном ускорителе тяжелых ионов. В том же году советская научная группа под руководством Георгия Флерова из Объединенного института ядерных исследований в Дубне, Россия, добилась аналогичного результата. Другие эксперименты, проведенные в Советском Союзе (в Институте атомной энергии им. И. В. Курчатова, Москва и в Дубне) и в США (Беркли), не подтвердили стокгольмское открытие. Последующие исследования в следующем десятилетии (в основном в Беркли и Дубне) привели Международный союз теоретической и прикладной химии к выводу, что статьи Дубны, опубликованные в 1966 установил существование изотопа нобелий-254 с периодом полураспада альфа-распада около 51 секунды.
Britannica Викторина
118 Названия и символы периодической таблицы Викторина
Элементарная викторина по фундаментальным вопросам.
Из изотопов нобелия, которые были произведены, нобелий-259 (период полураспада 58 минут) является самым стабильным. Используя следы этого изотопа, радиохимики показали, что нобелий существует в водном растворе как в +2, так и в +3 степени окисления. Катионообменная хроматография и эксперименты по соосаждению убедительно показали, что состояние +2 более стабильно, чем состояние +3, эффект более выражен, чем ожидалось, по сравнению с гомологичным лантаноидным элементом иттербием (атомный номер 70). Таким образом, № 2+ химически несколько похож на щелочноземельные элементы кальций, стронций и барий. Металлический нобелий не был получен, но было предсказано, что его свойства аналогичны свойствам щелочноземельных металлов и европия.
| atomic number | 102 |
|---|---|
| stablest isotope | 255 |
| oxidation states | +2, +3 |
| электронная конфигурация атомного состояния в газообразном состоянии | [Rn]5 f 14 7 s 2 |
В этой статье вы узнаете об атомном номере, его определении, его полезности для классификации элементов и его истории как теории в химии.
- Как читать периодическую таблицу
- Что такое изотоп?
- Ядерные реакции
- Уравновешивание химических уравнений
- Дж. Дж. Томпсон и электронно-лучевая трубка
Что именно отличает один элемент от другого? Почему углерод, водород и кислород считаются разными веществами? На что мы можем конкретно указать, что объясняет различие между этими элементами на самом базовом уровне?
Ответ: атомный номер. Если вы посмотрите на периодическую таблицу, то заметите, что каждый элемент имеет уникальное значение от 1 до 118, которое химики называют «атомным номером». Водород имеет атомный номер 1. Углерод имеет атомный номер 6. Кислород имеет атомный номер 8.
Современная периодическая таблица с атомными номерами, перечисленными выше атомных символов. Источник. На первый взгляд, вы можете предположить, что атомный номер элемента произвольный. Поскольку между атомными номерами от 1 до 118 не существует пробелов, легко предположить, что атомный номер служит только для удобной числовой идентификации. Вы можете даже подумать о некоторых преимуществах организации данных, которые могут предложить такие числовые идентификаторы. Однако атомный номер не является произвольным; это говорит что-то фундаментальное о субатомной структуре каждого элемента.
Поскольку между атомными номерами от 1 до 118 не существует пробелов, легко предположить, что атомный номер служит только для удобной числовой идентификации. Вы можете даже подумать о некоторых преимуществах организации данных, которые могут предложить такие числовые идентификаторы. Однако атомный номер не является произвольным; это говорит что-то фундаментальное о субатомной структуре каждого элемента.
По сути, элемент является разновидностью атома. Атомы сами по себе представляют собой небольшие круглые структуры, состоящие из того, что химики называют субатомными частицами, а именно из протонов, электронов и нейтронов. Различные элементы включают атомы с различным количеством этих субатомных частиц.
Имея это в виду, атомный номер элемента представляет собой количество протонов в одном атоме элемента. Таким образом, атомы водорода имеют 1 протон, атомы углерода имеют 6 протонов и так далее.
Важно отметить, что химики используют атомный номер как определяющую характеристику элемента. Атом может иметь любое количество нейтронов и электронов, но пока у него 6 протонов, химики всегда будут считать его атомом углерода.
Атом может иметь любое количество нейтронов и электронов, но пока у него 6 протонов, химики всегда будут считать его атомом углерода.
Имея в виду конкретно углерод, его атомная структура чаще всего состоит из 6 нейтронов, хотя химикам известны и другие формы углерода с 7, 8 и более нейтронами. Варианты элемента с разным числом нейтронов и, следовательно, разным атомным весом называются «изотопами» элемента. Кроме того, кислород имеет 8 электронов в своей элементарной форме, но также может иметь 10 электронов при определенных условиях. Варианты элемента с разным числом электронов и, следовательно, с разным электрическим зарядом называются «ионами» элемента.
Атомный номер и периодическая таблица Поскольку мы знаем, что атомы могут различаться не только числом протонов, но также числом нейтронов и электронов, почему мы так заботимся о протонах? В конце концов, химики организуют элементы по атомному номеру в периодической таблице, что предполагает некую неотъемлемую важность, связанную с числом протонов атома. Ответ лежит в химии различных элементов.
Ответ лежит в химии различных элементов.
По правде говоря, химики не всегда использовали атомные номера для классификации элементов. Дмитрий Менделеев, архитектор современной таблицы Менделеева, составил свою первую таблицу в 1869 году.вместо этого в соответствии с атомной массой. Поскольку атомная масса по существу равна сумме протонов и нейтронов, она сильно коррелирует с атомным номером. Действительно, в первой периодической таблице Менделеева элементы располагаются в том же порядке, что и в современной таблице.
Периодическая таблица Менделеева 1869 года с элементами, расположенными по атомной массе. Источник. Что не использует атомный вес? Однако, некоторые быстрые наблюдения за таблицей показали, что упорядочение элементов по атомной массе оказалось бесполезным и вводящим в заблуждение. Во-первых, у некоторых элементов нет уникальных атомных масс. Во время составления таблицы химики оценили атомные массы никеля и кобальта примерно равными друг другу. Неуникальные атомные массы предполагали, что таким образом невозможно осмысленно упорядочить элементы.
Неуникальные атомные массы предполагали, что таким образом невозможно осмысленно упорядочить элементы.
Во-вторых, что более тревожно, химическое поведение элементов подорвало массовый порядок. В то время химики понимали, что некоторые элементы с очень разными атомными массами имеют сходные химические характеристики. Фтор, хлор, бром и йод имели двухатомные элементарные формы, а также сильную склонность к ионизации исключительно до заряда -1. Натрий, калий, рубидий и цезий имели невероятно нестабильные нейтральные состояния и, казалось, образовывали ионы с зарядом только +1. Химики также сгруппировали углерод, кремний и селен, а также азот, фосфор и мышьяк по сходному поведению.
Именно расположение этой первой группы, называемой «галогены», вызвало удивление у химиков. Менделеев расположил таблицу так, чтобы эти сходные химические группы располагались в одной строке, включая строку для этих галогенов. Однако он знал, что теллур имеет сходное химическое поведение с кислородной группой элементов. Теллур имеет более тяжелый атомный вес, чем йод, что вынудило Менделеева ошибочно поместить его на один пробел перед йодом, чтобы сохранить химические группы.
Теллур имеет более тяжелый атомный вес, чем йод, что вынудило Менделеева ошибочно поместить его на один пробел перед йодом, чтобы сохранить химические группы.
Вскоре после публикации первой таблицы Менделеева стало ясно, что таблица нуждается в перестановке.
Сила атомного числаБолее полувека химики жили в неудобном пространстве относительно периодической таблицы. С одной стороны, они понимали, что в таблице Менделеева 1869 года есть недостатки, которые требуют новой модели. С другой стороны, лучшей модели не существовало, и таблица атомной массы по-прежнему поддерживала большинство химических группировок.
Изменено в 1911 января, когда Эрнест Резерфорд опубликовал данные своего знаменитого эксперимента с золотой фольгой. Резерфорд предположил, что каждый атом имеет ядро из заряженных частиц внутри облака противоположно заряженных частиц. Важно отметить, что это означало, что ученые теоретически могли измерить этот ядерный заряд. Химики также предположили, что значение заряда данного элемента соответствует количеству частиц, называемых протонами, в ядре. В последующие десятилетия каждый ядерный заряд, называемый «атомным номером», был измерен, что обеспечило альтернативный способ упорядочения элементов.
Химики также предположили, что значение заряда данного элемента соответствует количеству частиц, называемых протонами, в ядре. В последующие десятилетия каждый ядерный заряд, называемый «атомным номером», был измерен, что обеспечило альтернативный способ упорядочения элементов.
Таким образом, была сформулирована современная форма таблицы Менделеева. В отличие от предыдущей таблицы, упорядочение по атомному номеру лучше сохраняет расположение химических групп.
Интерактивная периодическая таблица Chemtalk с элементами, упорядоченными по атомным номерам. Кроме того, эта современная итерация допускает появление трендов по всей таблице. Этими тенденциями являются электроотрицательность, сродство к электрону, атомный радиус и энергия ионизации. Каждый тренд имеет прямую связь с количеством протонов в каждом элементе. Это приводит к увеличению или уменьшению интенсивности каждого тренда при приближении к верхнему правому или нижнему левому углу таблицы. Чтобы увидеть эти тенденции, ознакомьтесь с нашей интерактивной периодической таблицей.
