Таблица Менделеева. История и суть таблицы Менделеева
Он опирался на труды Роберта Бойле и Антуана Лавузье. Первый ученый ратовал за поиск неразложимых химических элементов. 15 из таковых Бойле перечислил еще в 1668-ом году.
Лавузье прибавил к ним еще 13, но спустя век. Поиски растянулись, поскольку не было стройной теории связи между элементами. Наконец, в «игру» вступил Дмитрий Менделеев. Он решил, что есть связь между атомной массой веществ и их местом в системе.
Эта теория позволила ученому открыть десятки элементов, не обнаруживая их на практике, а природе. Это было возложено на плечи потомков. Но, сейчас не о них. Посвятим статью великому русскому ученому и его таблице.
История создания таблицы Менделеева
Таблица Менделеева началась с книги «Соотношение свойств с атомным весом элементов». Труд выпущен в 1870-ых. Тогда же русский ученый выступил перед химическим обществом страны и разослал первый вариант таблицы коллегам из-за рубежа.
До Менделеева разными учеными были открыты 63 элемента. Наш соотечественник начал со сравнения их свойств. В первую очередь, работал с калием и хлором. Потом, взялся за группу металлов щелочной группы.
Химик обзавелся специальным столом и карточками элементов, чтобы раскладывать их, как пасьянс, ища нужные совпадения и комбинации. В итоге, пришло прозрение: — свойства компонентов зависят от массы их атомов. Так, элементы таблицы Менделеева выстроились в ряды.
Находкой маэстро химии стало решение оставить в этих рядах пустоты. Периодичность перепада между атомными массами заставила ученого предположить, что человечеству известны еще не все элементы. Промежутки в весе между некоторыми «соседями» были слишком велики.
Поэтому, периодическая таблица Менделеева стала похожа на шахматное поле, с обилием «белых» клеток. Время показало, что они, действительно, ждали своих «постояльцев». Ими, к примеру, стали инертные газы. Гелий, неон, аргон, криптон, радиоакт и ксенон открыты лишь в 30-ых годах 20-го века.
Теперь о мифах. Распространено мнение, что химическая таблица Менделеева явилась ему во сне. Это происки университетских педагогов, точнее, одного из них – Александра Иностранцева. Это русский геолог, читавший лекции в Петербургском университете горного дела.
Иностранцев был знаком с Менделеевым, бывал у него в гостях. Однажды, изможденный поисками Дмитрий заснул прямо при Александе. Тот дождался, пока химик проснется и увидел, как Менделеев хватается за листок и записывает окончательный вариант таблицы.
По сути, ученый просто не успел сделать это до того, как его захватил Морфей. Однако, Иностранцеву хотелось позабавить своих студентов. На основе виденного геолог придумал байку, которую благодарные слушатели быстро распространили в массы.
Особенности таблицы Менделеева
С момента первой версии 1969-го года порядковая таблица Менделеева не раз дорабатывалась. Так, с открытием в 1930-ых благородных газов удалось вывести новую зависимость элементов, — от их порядковых номеров, а не массы, как заявлял автор системы.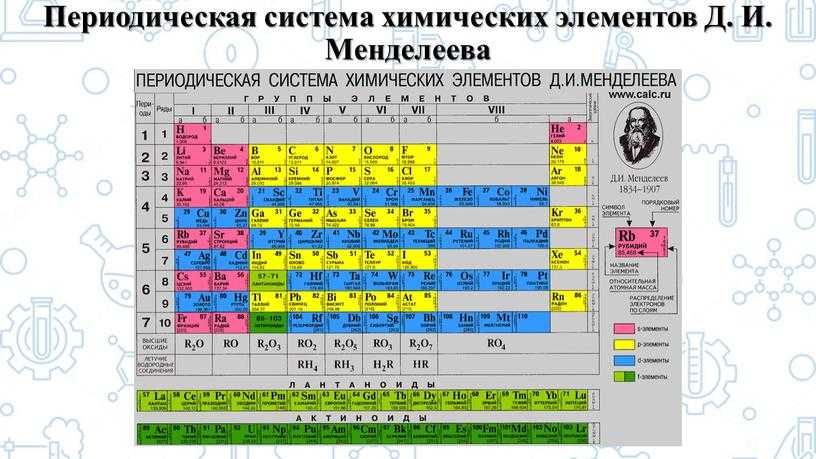
Понятие «атомный вес» заменили на «атомный номер». Удалось изучить число протонов в ядрах атомов. Эта цифра и есть порядковый номер элемента.
Ученые 20-го века изучили и электронное строение атомов. Оно тоже влияет на периодичность элементов и отражено в поздних редакциях таблицы Менделеева. Фото списка демонстрирует, что вещества в нем расставлены по мере роста атомного веса.
Первооснову менять не стали. Масса увеличивается слева направо. При этом, таблица не едина, а поделена на 7 периоды. Отсюда и название списка. Период – горизонтальный ряд. Его начало – типичные металлы, конец – элементы с неметаллическими свойствами. Убывание постепенное.
Есть большие и малые периоды. Первые находятся в начале таблицы, их 3. Открывает список период из 2-х элементов. Следом идут две колонки, в которых по 8 наименований. Оставшиеся 4 периода большие. Наиболее протяжен 6-ой, в нем 32 элемента. В 4-ом и 5-ом их по 18, а в 7-ом – 24.
Можно сосчитать, сколько элементов в таблице Менделеева. Всего 112 наименований. Именно наименований. Клеток же 118, а есть вариации списка и со 126-ю полями. Все еще остаются пустые клетки для неоткрытых элементов, не имеющих имен.
Всего 112 наименований. Именно наименований. Клеток же 118, а есть вариации списка и со 126-ю полями. Все еще остаются пустые клетки для неоткрытых элементов, не имеющих имен.
Не все периоды умещаются в одну строку. Большие периоды состоят из 2-х рядов. Количество металлов в них перевешивает. Поэтому, им полностью посвящены нижние строки. Постепенное убывание от металлов к инертным веществам соблюдается в верхних рядах.
Картинки таблицы Менделеева поделены и вертикально. Это группы в таблице Менделеева, их 8. Вертикально скомпонованы элементы, схожие по химическим свойствам. Они поделены на главную и побочную подгруппы. Последние начинаются только с 4-го периода. В главные подгруппы входят и элементы малых периодов.
Суть таблицы Менделеева
Названия элементов в таблице Менделеева – это 112 позиций. Суть их компоновки в единый список – систематизация первоэлементов. Над этим начали биться еще в античные времена.
Одним из первых понять, из чего составлено все сущее попытался Аристотель. Он взял за основу свойства веществ – холод и тепло. Эмпидокл выделил 4-ре первоосновы по стихиям: воду, землю, огонь и воздух.
Металлы в таблице Менделеева, как и другие элементы, — те самые первоосновы, но с современной точки зрения. Российскому химику удалось открыть большинство составляющих нашего мира и предположить существование еще неизвестных первоэлементов.
Получается, что произношение таблицы Менделеева – озвучивание некой модели нашей реальности, раскладывание ее на составляющие. Однако, выучить их не так-то просто. Попробуем облегчить задачу, описав пару эффективных методов.
Как выучить таблицу Менделеева
Начнем с современного метода. Компьютерщиками разработан ряд флеш-игр, помогающих запомнить список Менделеева. Участникам проекта предлагают находить элементы по разным опциям, например, названию, атомной массе, буквенному обозначению.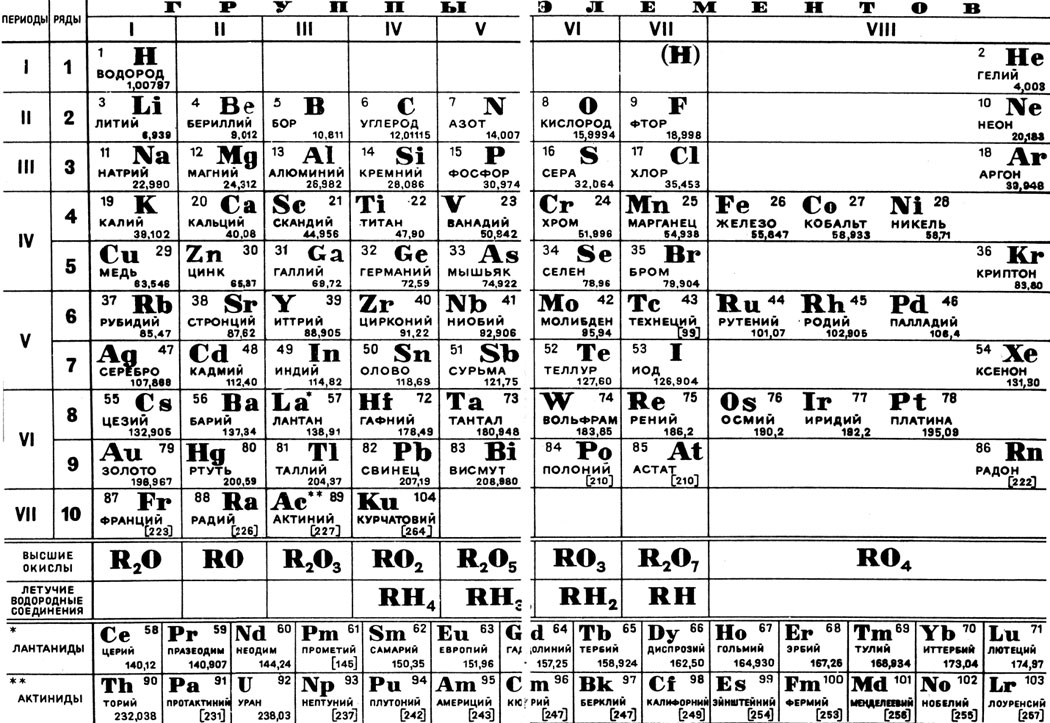
Игрок имеет право выбрать поле деятельности – лишь часть таблицы, или ее всю. В нашей воле, так же, исключить имена элементов, другие параметры. Это усложняет поиск. Для продвинутых предусмотрен и таймер, то есть тренировка ведется на скорость.
Игровые условия делают изучение номеров элементов в таблице Менднлеева не нудным, а занятным. Просыпается азарт, и систематизировать знания в голове становится проще. Те же, кто не приемлет компьютерных флеш-проектов, предлагают более традиционный способ заучивания списка.
Его делят на 8 групп, или 18 (в соответствии с редакцией 1989-го года). Для удобства запоминания, лучше создать несколько отдельных таблиц, а не работать по цельному варианту. Помогают и зрительные образы, подобранные к каждому из элементов. Опираться следует на собственные ассоциации.
Так, железо в мозгу может соотноситься, к примеру, с гвоздем, а ртуть – с градусником. Название элемента незнакомо? Пользуемся методом наводящих ассоциаций. Иридий, например, составим из начал слов «ириска» и «динамик».
Иридий, например, составим из начал слов «ириска» и «динамик».
Характеристика таблицы Менделеева не учиться в один присест. Рекомендованы занятия по 10-20 минут в день. Начинать рекомендована с запоминания лишь основных характеристик: названия элемента, его обозначения, атомной массы и порядкового номера.
Школьники предпочитают вешать таблицу Менделеева над рабочим столом, или на стене, на которую часто смотрят. Метод хорош для людей с преобладанием зрительной памяти. Данные из списка невольно запоминаются даже без зубрежки.
Это учитывают и педагоги. Как правило, они не заставляют заучивать список, разрешают смотреть в него даже на контрольных. Постоянное заглядывание в таблицу равнозначно эффекту распечатки на стене, или написанию шпаргалок до экзаменов.
Приступая к изучению, вспомним, что и Менделеев не сразу запомнил свой список. Однажды, когда ученого спросили, как он открыл таблицу, последовал ответ: — «Я над ней, может, 20 лет думал, а вы считаете: сидел и, вдруг, готово». Периодическая система – кропотливый труд, который не осилить в сжатые сроки.
Периодическая система – кропотливый труд, который не осилить в сжатые сроки.
Наука не терпит спешки, ведь она приводит к заблуждениям и досадным ошибкам. Так, одновременно с Менделеевым таблицу составил и Лотар Мейер. Однако, немец немного недоработал список и не был убедителен при доказательстве своей точки зрения. Поэтому, общественность признала труд русского ученого, а не его коллеги-химика из Германии.
A Game of the Elements) — настольная игра Crowd Games
В 2019 году исполнилось 150 лет со дня открытия периодического закона химических элементов великим русским учёным Д. И. Менделеевым. В связи с этим Генеральная ассамблея ООН объявила 2019 год годом Периодической таблицы химических элементов. Мы не могли пройти мимо такого знаменательного события, а потому издали настольную игру «Таблица Менделеева»!
Издательство Genius Games уже 6 лет занимается созданием игр, в которых сложные физические и химические процессы (например, синтез белка) представлены очень просто, а главное — интересно. Получилось ли у них и в этот раз? Давайте разберёмся.
Получилось ли у них и в этот раз? Давайте разберёмся.
К середине XIX века было открыто 63 химических элемента, и учёные всего мира не раз предпринимали попытки определить закономерности, которые позволили бы создать систему, помогающую расположить химические элементы в удобном и логичном порядке. Удалось это только в 1869 году русскому химику Дмитрию Ивановичу Менделееву.
Суть открытия Менделеева заключается в том, что ему удалось обнаружить взаимосвязь свойств элементов с их атомной массой и их периодичность. Это означает, что после определённого количества разных по свойствам элементов, свойства начинают повторяться. Так, калий похож на натрий, фтор — на хлор, а золото похоже на серебро и медь. Учёный также предсказал открытие нескольких новых химических элементов и описал их химические свойства. В будущем его догадки подтвердились.
Одна из известнейших легенд (помимо, наверное, только байки об изобретении им водки) гласит, что Менделеев открыл таблицу химических элементов во сне.
В коробке с игрой вы обнаружите познавательный буклет, из которого можно узнать много интересного о химии и роли таблицы Менделеева в науке и нашей жизни.
«Таблица Менделеева» — это настольная игра, построенная вокруг периодической таблицы элементов, а также некоторых принципов химии. В ней игроки будут изучать группы химических элементов, перемещаясь для этого по самой таблице. Элементы могут находиться далеко друг от друга, но тем не менее у них обязательно есть что-то общее, в соответствии с реальными химическими законами. В итоге получаем увлекательную гонку, в которой для победы вам придётся эффективно расходовать накопленную энергию и грамотно планировать свой маршрут, чтобы опередить остальных игроков, не забывая о собственных целях, полученных в начале игры.
В итоге получаем увлекательную гонку, в которой для победы вам придётся эффективно расходовать накопленную энергию и грамотно планировать свой маршрут, чтобы опередить остальных игроков, не забывая о собственных целях, полученных в начале игры.
Размер и количество карт: 63 × 88 мм — 20 шт., 110 × 70 мм — 32 шт.
Давайте заглянем в коробку игры вместе с Сергеем Рябухиным:
Подготовка к игре представлена в этом видео:
В свой ход вы выбираете между двумя действиями:
- Вы можете заплатить энергию, чтобы переместить свою фишку колбы по таблице элементов. Первое выбранное вами периодическое свойство стоит одну единицу энергии, а каждое последующее — две единицы энергии.
 Они дают вам возможность переместить вашу фишку колбы в определённом направлении.
Они дают вам возможность переместить вашу фишку колбы в определённом направлении.
- Или вы можете забрать себе всю энергию, которая находится на одном из периодических свойств, и затем активировать его. Это действие позволяет вам совершить только одно перемещение, но собранную энергию вы сможете потратить в следующем ходу.
После каждого перемещения вы получаете возможность «открыть» элемент, на котором вы остановились.
Элементы, доступные для исследования, показаны на картах целей. На каждой из них перечислены элементы, которые имеют что-то общее. Например, все они крайне ядовиты или все очень редко встречаются в природе. На игровом поле эти элементы отмечаются соответствующей фишкой.
Существует три способа получения очков:
- Исследование семейства (вы остановились на нужном элементе).
- Выполнение целей.
- Выполнение карт задач.
Игрок, набравший наибольшее количество очков, считается победителем.
Подробнее с игровым процессом вы можете ознакомится в этом видео:
Авторами игры являются Джон Ковью, основатель издательства Genius Games, и Пол Саломон, учитель математики и заядлый игрок в настольные игры, для которого «Таблица Менделеева» — первый большой проект.
Джон же на данный момент разработал шесть научных игр, и ещё несколько готовятся к выпуску в ближайшем году. Его игры были высоко оценены школьными учителями и родителями учеников, а статьи о них публиковались в таких изданиях, как The Wall Street Journal, Popular Science, Scientific American и Gizmodo, и получили одобрение Национальной ассоциации преподавателей естественных наук США. За достоверностью игр следят не только авторы, но и многочисленные консультанты из академических кругов, а сам Джон имеет степень магистра технических наук в Вашингтонском университете.
«Моя цель — вдохновить следующее поколение на изучение науки, и я надеюсь, что наши игры будут побуждать подростков рассматривать возникающие перед ними трудности как вызовы, которые они могут преодолеть, а не как проблемы, о которых позаботятся другие».
Обычно в этом разделе можно узнать, что думают об этой игре Том Вэсел, Ричард Хэм и другие известные критики, но в этот раз здесь будут отзывы людей, которые оценивали «Таблицу Менделеева» на сайте BoardGameGeek.
Мне нравится подход, который Genius Games использовали в «Таблице Менделеева». Если сформулировать просто, то вы перемещаетесь по игровому полю и собираете элементы, чтобы выполнить карточки целей. Но есть и другие способы получать очки, поэтому вам необходимо следить не только за целями, что делает игровой процесс сложным и увлекательным.
sfarrell, 8/10
Очень забавная игра! Простая в освоении, достаточно сложная, чтобы поддерживать интерес, и настолько веселая, что хочется играть снова и снова!
Kalli4na, 8/10
Ещё один шедевр от одного из моих любимых издателей, всегда приятно видеть на полках магазинов новую игру Genius Games. Весело и познавательно, эта игра прокачает ваше мышление!
Весело и познавательно, эта игра прокачает ваше мышление!
CaptSwissCheese, 10/10
Я оцениваю её исключительно как настольную игру, не за её образовательную ценность. Крепкие механики, интересный игровой процесс. Мне кажется, будто бы кто-то предложил, вот периодическая таблица, что мы можем сделать, чтобы можно было передвигаться по ней и зарабатывать очки?
borisgreggs, 7/10
Правила настольной игры «Таблица Менделеева» и буклет «Научные аспекты игры» на русском языке от Crowd Games.
Страница игры на сайте BoardGameGeek.
Страница игры на сайте «Тесера».
Страница игры на сайте Kickstarter.
9 класс. Химия. Описание элемента по положению в Периодической системе элементов Д.И. Менделеева – Описание элемента по положению в Периодической системе элементов Д.И. Менделеева
Комментарии преподавателя1. Какие характеристики атома меняются в Периодической системе периодически
В 1869 году Д.И.Менделеев на основе данных накопленных о химических элементах сформулировал свой периодический закон. Тогда он звучал так: « Свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величины атомных масс элементов».
Современная формулировка периодического закона: « Свойства простых веществ, также формы и свойства соединений элементов находятся в периодической зависимости от величины заряда ядра атома».
Заряд ядра атома равен числу протонов в ядре. Число протонов уравновешивается числом электронов в атоме. Таким образом, атом электронейтрален.
Заряд ядра атома в Периодической таблице – это порядковый номер элемента.
Номер периода показывает число энергетических уровней, на которых вращаются электроны.
Номер группы показывает число валентных электронов. Для элементов главных подгрупп число валентных электронов равно числу электронов на внешнем энергетическом уровне. Именно валентные электроны отвечают за образование химических связей элемента.
Химические элементы 8 группы – инертные газы имеют на внешней электронной оболочке 8 электронов. Такая электронная оболочка энергетически выгодна. Все атомы стремятся заполнить свою внешнюю электронную оболочку до 8 электронов.
Какие же характеристики атома меняются в Периодической системе периодически?
– Повторяется строение внешнего электронного уровня.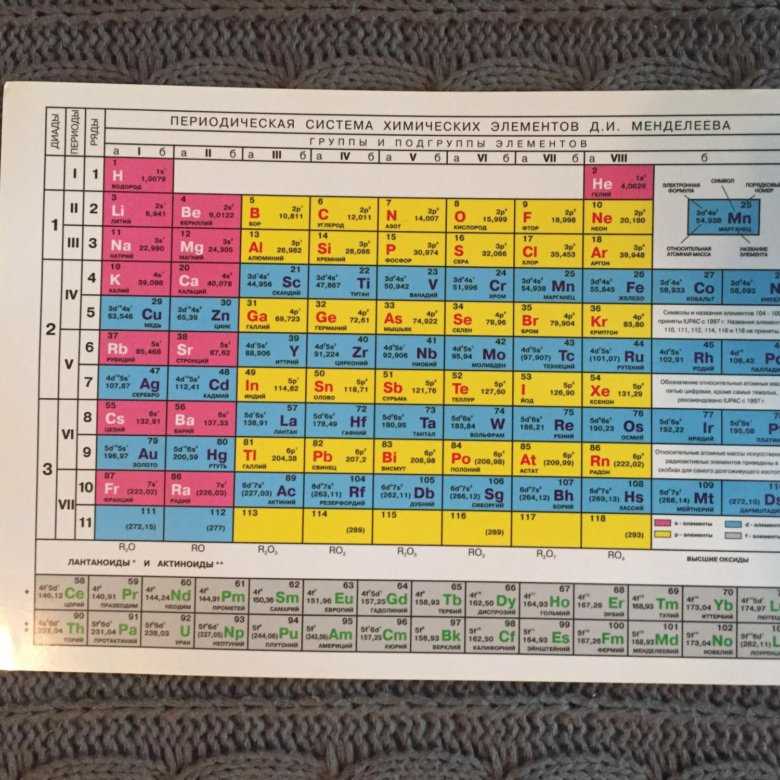
– Периодически меняется радиус атома. В группе радиус увеличивается с увеличением номера периода, так как увеличивается число энергетических уровней. В периоде слева направо будет происходить рост атомного ядра, но притяжение к ядру будет больше и поэтому радиус атома уменьшается.
– Каждый атом стремится завершить последний энергетический уровень У элементов 1 группы на последнем слое 1 электрон. Поэтому им легче его отдать. А элементам 7 группы легче притянуть 1 недостающий до октета электрон. В группе способность отдавать электроны будет увеличиваться сверху вниз, так ка увеличивается радиус атома и притяжение к ядру меньше. В периоде слева направо способность отдавать электроны уменьшается, потому что уменьшается радиус атома.
– Чем легче элемент отдает электроны с внешнего уровня, тем большими металлическими свойствами он обладает, а его оксиды и гидроксиды обладают большими основными свойствами. Значит, металлические свойства в группах увеличиваются сверху вниз, а в периодах справа налево. С неметаллическими свойствами все наоборот.
Значит, металлические свойства в группах увеличиваются сверху вниз, а в периодах справа налево. С неметаллическими свойствами все наоборот.
2. Описание элемента магния, астата, хлора
Рис. 1. Положение магния в таблице
В группе магний соседствует с бериллием и кальцием. Рис.1. Магний стоит ниже, чем бериллий, но выше кальция в группе. У магния больше металлические свойства, чем у бериллия, но меньше чем у кальция. Основные свойства его оксидов и гидроксидов изменяются также. В периоде натрий стоит левее, а алюминий правее магния. Натрий будет проявлять больше металлические свойства, чем магний, а магний больше, чес алюминий. Таким образом, можно сравнить любой элемент с соседями его по группе и периоду.
Кислотные и неметаллические свойства изменяются противоположно основным и металлическим свойствам.
3. Описание элемента хлора
Характеристика хлора по его положению в периодической системе Д.И.Менделеева.
Рис. 4. Положение хлора в таблице
4. Положение хлора в таблице
. Значение порядкового номера 17 показывает число протонов17 и электронов17 в атоме. Рис.4. Атомная масса 35 поможет вычислить число нейтронов (35-17 = 18). Хлор находится в третьем периоде, значит число энергетических уровней в атоме равно 3. Стоит в 7 –А группе, относится к р- элементам. Это неметалл. Сравниваем хлор с его соседями по группе и по периоду. Неметаллические свойства хлора больше чем у серы, но меньше, чем у аргона. Хлор обладает меньшими металлическими свойствами, чем фтор и большими чем бром. Распределим электроны по энергетическим уровням и напишем электронную формулу. Общее распределение электронов будет иметь такой вид. См.Рис. 5
|
|
Рис. 5. Распределение электронов атома хлора по энергетическим уровням
Определяем высшую и низшую степень окисления хлора. Высшая степень окисления равна +7, так как он может отдать с последнего электронного слоя 7 электронов. Низшая степень окисления равна -1, потому что хлору до завершения необходим 1 электрон. Формула высшего оксида Cl2O7 (кислотный оксид), водородного соединения HCl.
Высшая степень окисления равна +7, так как он может отдать с последнего электронного слоя 7 электронов. Низшая степень окисления равна -1, потому что хлору до завершения необходим 1 электрон. Формула высшего оксида Cl2O7 (кислотный оксид), водородного соединения HCl.
4. Степень окисления
В процессе отдачи или присоединения электронов атом приобретает условный заряд. Этот условный заряд называется степенью окисления.
– Простые вещества обладают степенью окисления равной нулю.
– Элементы могут проявлять максимальную степень окисления и минимальную. Максимальную степень окисления элемент проявляет тогда, когда отдает все свои валентные электроны с внешнего электронного уровня. Если число валентных электронов равно номеру группы, то и максимальная степень окисления равна номеру группы.
Рис. 2. Положение мышьяка в таблице
Минимальную степень окисления элемент будет проявлять тогда, когда он примет все возможные электроны для завершения электронного слоя.
Рассмотрим на примере элемента №33 значения степеней окисления.
Это мышьяк As.Он находится в пятой главной подгруппе.Рис.2. На последнем электронном уровне у него пять электронов. Значит, отдавая их, он будет иметь степень окисления +5. До завершения электронного слоя атому As не хватает 3 электрона. Притягивая их, он будет иметь степень окисления -3.
Положение элементов металлов и неметаллов в Периодической системе Д.И. Менделеева.
Рис. 3. Положение металлов и неметаллов в таблице
В побочных подгруппах находятся все металлы. Если мысленно провести диагональ от бора к астату, то выше этой диагонали в главных подгруппах будут все неметаллы, а ниже этой диагонали – все металлы. Рис.3.
Используя Периодическую систему можно очень много сказать об элементе. Можно сравнить его с другими элементами, определить строение его атома, электронной оболочки атома.
Можно сравнить его с другими элементами, определить строение его атома, электронной оболочки атома.
5. План характеристики химического элемента
1. Символ элемента
2. Порядковый номер элемента
3. Значение относительной атомной массы элемента.
4. Число протонов, электронов, нейтронов.
5. Номер периода.
6. Номер и тип группы (тип элемента s -, p -,d -,f – элемент)
7. Металл или неметалл
8. Сравнение свойств элемента (металлических и неметаллических) с соседними элементами по периоду и группе.
9. Написать распределение электронов по атомным орбиталям – квантовую диаграмму.
10. Написать электронную формулу.
11. Зарисовать распределение электронов по энергетическим уровням
12. Определить высшую степень окисления атома и формулу его высшего оксида. Определить характер оксида (основной, кислотный, амфотерный).
13. Определить низшую степень окисления элемента и формулу его водородного соединения (если такое есть).
Подведение итога урока
На этом уроке вы узнали о Периодическом законе Менделеева, который описывает изменение свойств простых тел, а также формы и свойства соединений элементов в зависимости от величины их атомных масс. Рассмотрели, как по положению в Периодической системе можно описать химический элемент.
Источники
http://www.youtube.com/watch?v=1EKDbO-ih2Q
источник презентации – http://ppt4web.ru/khimija/periodicheskaja-sistema-khimicheskikh-ehlementov-di-mendeleeva0.html
Конспект http://interneturok.ru/ru/school/chemistry/9-klass
«Мы приблизились к границам применимости периодического закона»
Интервью Евгении Сидоровой с Юрием Оганесяном
«Природа» №2, 2019
Накануне торжественного открытия Международного года Периодической таблицы химических элементов академик Ю. Ц. Оганесян рассказал редактору «Природы» о выводах, сделанных учеными при исследовании свойств сверхтяжелых элементов, и о своем видении перспектив работы Фабрики сверхтяжелых элементов.
— Юрий Цолакович, почему юбилей открытия периодического закона так важен для всего мира? И что он означает для Вас, для Ваших коллег: это — праздник, подтверждение высокой роли естественно-научного сообщества? Мемориальный год (как его часто называют в печати) поможет решить перспективные научные задачи?
— Мы говорим о событии действительно важном и экстраординарном. Открытие 150-летней давности актуально и сегодня, что случается нечасто. Периодическая таблица химических элементов, которую называют «иконой химиков», в XXI в. ставит задачи на переднем крае науки. Крупнейшие ядерные центры России, США, Германии, Японии, Франции, Китая включают в свои основные программы синтез и исследование новых химических элементов, обсуждают границы Периодической таблицы и пределы применимости периодического закона. На разработку таких тем тратятся значительные средства, создаются новые лаборатории, строятся новые установки, ускорительные комплексы. С этим связаны большие планы разных научных групп, работающих многие годы в тесном международном сотрудничестве. Во всем мире проводятся симпозиумы, конференции, посвященные Периодической системе элементов, которая и спустя полтора века продолжает волновать исследователей всего мира.
Во всем мире проводятся симпозиумы, конференции, посвященные Периодической системе элементов, которая и спустя полтора века продолжает волновать исследователей всего мира.
Все это свидетельство того, что темой Международного года стало явление неординарное. Мы и сегодня ищем ответы на вопросы, которые перед нами ставит Периодическая таблица химических элементов.
— В таком случае «мемориальный» — неподходящее слово. Расскажите, пожалуйста, подробнее об актуальных вопросах, связанных с Периодической таблицей. Речь идет о свойствах новых химических элементов?
— Прежде чем дальше вести нашу беседу, позвольте мне ознакомить читателей журнала с общим положением дел в области, которую мы будем обсуждать.
Из планетарной модели атома Э. Резерфорда (1911) мы знаем, что атом состоит из плотного ядра (в котором сосредоточена практически вся его масса и весь его положительный заряд) и электронов, двигающихся вокруг ядра на большом расстоянии. Ядро, в свою очередь, состоит из протонов и нейтронов, близко расположенных друг к другу. Их связь возникает под действием короткодействующих ядерных сил, нам пока неизвестных. Строгой теории сильных взаимодействий нет. Поэтому описание ядерной материи базируется на различных теоретических моделях. Их области применения ограниченны, и предсказания могут сильно отличаться друг от друга.
Их связь возникает под действием короткодействующих ядерных сил, нам пока неизвестных. Строгой теории сильных взаимодействий нет. Поэтому описание ядерной материи базируется на различных теоретических моделях. Их области применения ограниченны, и предсказания могут сильно отличаться друг от друга.
Наоборот, электромагнитные силы, хотя и в сотни раз слабее ядерных, дальнодействующие, нам хорошо известны. Поэтому описание движения электронов вокруг зарядового центра (ядра атома) базируется на строгой теории — квантовой электродинамике. Свое начало эта наука берет еще от модели атома Н. Бора (1913), уравнения движения электрона в электрическом поле П. Дирака (1925), последующих работ Д. Хартри, В. А. Фока и др. В рамках квантовой электродинамики таблицу Менделеева можно рассчитать в детальных подробностях, что делалось неоднократно в так называемом нерелятивистском приближении, вплоть до элемента с атомным номером 172.
Поэтому ответ на вопросы, сколько может быть элементов в Периодической таблице и как определяются ее границы, мы должны дать с двух позиций — ядерной физики и атомной физики. Попытаемся это сделать.
Попытаемся это сделать.
В первом случае мы скажем: атом (элемент) есть, пока существует ядро с периодом полураспада не менее 10−14 с (время, необходимое для того, чтобы вокруг ядра образовалась соответствующая электронная структура атома). Во втором формулируем так: атом (элемент) существует до тех пор, пока никакие дополнительные (ранее неучтенные) эффекты не изменят предсказаний квантовой электродинамики.
За всю почти 80-летнюю историю искусственного синтеза трансурановых элементов ответ на первый вопрос приходил тогда, когда открывали очередной способ синтеза все более тяжелых ядер. Сначала это были пучки легких частиц — протонов и дейтронов, потом мощные потоки нейтронов (реакторы и даже ядерные взрывы), затем пучки тяжелых ионов с массой до 20 атомных масс, реакции под действием массивных ионов (холодное слияние), наконец, пучки нейтронно-избыточных ионов кальция-48 (48Са). Отметим, что за это время экспериментальные результаты радикально повлияли на теорию. На смену классической модели ядерной заряженной жидкой капли, с пределом существования элементов до Z = 100, пришла микроскопическая модель ядра, предсказывающая существование острова стабильности сверхтяжелых элементов в области Z = 114–120 и N = 184. Элементы, расположенные на этом острове, были недавно синтезированы. Сегодня они замыкают седьмой ряд Периодической таблицы. Исходя из свойств их распада, особенно самых тяжелых — 117-го и 118-го, элементы с атомными номерами 119 и 120 тоже должны существовать. (Далее мы поговорим об этом более подробно.) Данные элементы открывают восьмой период таблицы. Ожидаемые периоды их полураспада будут составлять десятые и сотые доли миллисекунд (громадное время в масштабах микромира, но исключительно малое для работы с ними). Скорее всего, рано или поздно эти элементы будут синтезированы в мировых лабораториях: в Дубне, Токио, в Кане (Франция), Дармштадте (Германия)… По сравнению с 118-м элементом их выход уменьшится, мы меняем пучок ионов кальция-48 (48Са) на пучок ионов титана-50 (50Ti).
На смену классической модели ядерной заряженной жидкой капли, с пределом существования элементов до Z = 100, пришла микроскопическая модель ядра, предсказывающая существование острова стабильности сверхтяжелых элементов в области Z = 114–120 и N = 184. Элементы, расположенные на этом острове, были недавно синтезированы. Сегодня они замыкают седьмой ряд Периодической таблицы. Исходя из свойств их распада, особенно самых тяжелых — 117-го и 118-го, элементы с атомными номерами 119 и 120 тоже должны существовать. (Далее мы поговорим об этом более подробно.) Данные элементы открывают восьмой период таблицы. Ожидаемые периоды их полураспада будут составлять десятые и сотые доли миллисекунд (громадное время в масштабах микромира, но исключительно малое для работы с ними). Скорее всего, рано или поздно эти элементы будут синтезированы в мировых лабораториях: в Дубне, Токио, в Кане (Франция), Дармштадте (Германия)… По сравнению с 118-м элементом их выход уменьшится, мы меняем пучок ионов кальция-48 (48Са) на пучок ионов титана-50 (50Ti). Словом, работа с ними займет много времени.
Словом, работа с ними займет много времени.
В атомных (химических) свойствах сверхтяжелых элементов тоже сюрпризы.
С увеличением атомного номера элемента растет электрическое поле ядра, в котором двигаются электроны. По мере приближения их скорости к скорости света, согласно теории относительности, растет релятивистская масса электрона. Это в первую очередь относится к электронам на внутренних орбитах, ближайших к ядру, двигающихся с максимальной скоростью. Релятивистский эффект приводит к сжатию внутренних орбит (релятивистское сжатие). Эффект должен быть учтен в расчете структуры сверхтяжелого атома, что не было сделано в упомянутых выше нерелятивистских расчетах.
Не менее важны и последствия сжатия внутренних орбит, такие как экранирование поля ядра, электронные корреляции на внешних орбитах, а также другие поправки более высокого порядка. Благо есть строгая теория, которая позволяет повысить точность расчетов на известных атомах и по этому рецепту вести расчеты сверхтяжелых.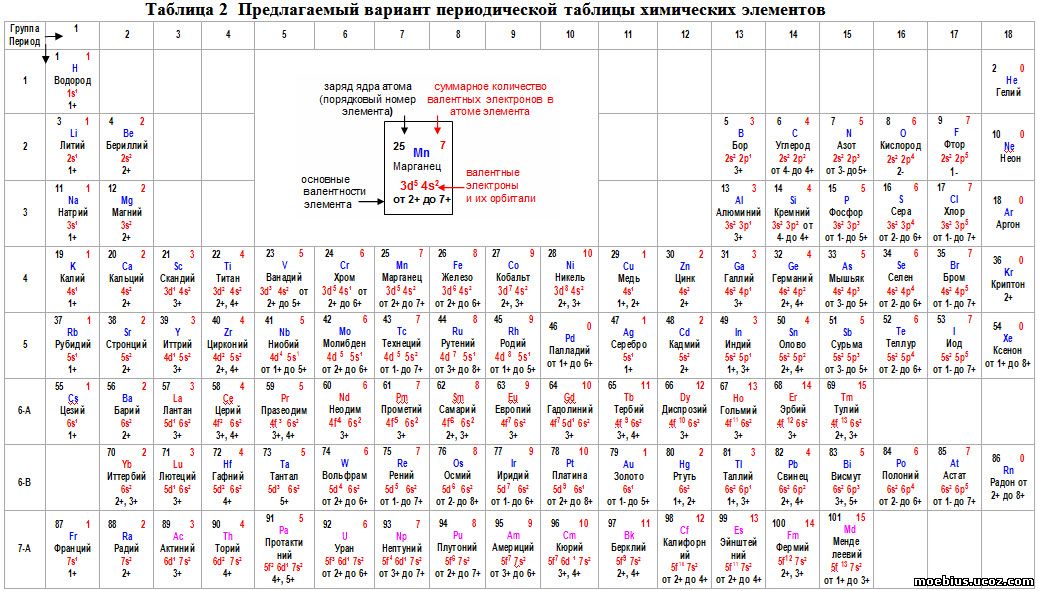 Сейчас физики-теоретики выработали так называемый «золотой стандарт». Они могут рассчитать энергию связи последнего электрона в атоме золота (потенциал ионизации) с беспрецедентной точностью: 0,003 электронвольт, или 0,03%!
Сейчас физики-теоретики выработали так называемый «золотой стандарт». Они могут рассчитать энергию связи последнего электрона в атоме золота (потенциал ионизации) с беспрецедентной точностью: 0,003 электронвольт, или 0,03%!
Первые наблюдения релятивистского эффекта в 12-й группе таблицы Менделеева были проведены в Дубне в 2007 г. с 3,6-секундным изотопом 112-го элемента коперниция (Cn) и его легким гомологом — ртутью (Hg). Последующие измерения для элементов 14-й группы флеровия (Fl) и свинца (Pb) показали сильный рост этого эффекта. Сейчас остается под вопросом, является ли 118-й элемент благородным газом? Думаю, что он еще продемонстрирует принадлежность к 18-й группе, хотя, возможно, и не будет газом при комнатной температуре. Вероятно также, что у 119-го элемента мы обнаружим скачок химических свойств — от характерных для 18-й группы Периодической таблицы до известных у элементов первой группы. Но определенно релятивистский эффект заметно ослабит эти изменения.
Есть основания полагать, что при дальнейшем увеличении атомного номера уже для элементов 121–123 групповые отличия почти исчезнут. По сути, исчезнет периодичность в изменении химических свойств элементов. На смену старой Периодической таблице придет новая, сильно измененная в начале восьмого периода. Выступая на торжественном открытии Международного года Периодической таблицы химических элементов 29 января 2019 г. в штаб-квартире ЮНЕСКО, я говорил о том, что, по-видимому, мы в своих исследованиях уже сегодня близко подошли к границе, за которой исчезают групповые различия химических элементов.
По сути, исчезнет периодичность в изменении химических свойств элементов. На смену старой Периодической таблице придет новая, сильно измененная в начале восьмого периода. Выступая на торжественном открытии Международного года Периодической таблицы химических элементов 29 января 2019 г. в штаб-квартире ЮНЕСКО, я говорил о том, что, по-видимому, мы в своих исследованиях уже сегодня близко подошли к границе, за которой исчезают групповые различия химических элементов.
Как увидеть это в эксперименте, когда атомы живут всего доли миллисекунд? Как получить эти атомы в минимально необходимом количестве? Наконец, можно ли отойти назад и в исследованиях химических свойств уже синтезированных сверхтяжелых элементов увидеть границы применимости периодического закона?
Вы видите, что после открытия сверхтяжелых элементов в нашу действительность, как из ящика Пандоры, выплеснулось много проблем. Некоторые из них пока просто не имеют решения.
— Что это означает и к чему следует готовиться специалистам?
— Для того чтобы продолжить наши рассуждения о Таблице, надо было бы сначала удостовериться, что атомы с такими большими атомными номерами вообще существуют. И конечно, убедиться в том, что столь тяжелые ядра можно синтезировать в тех или иных ядерных реакциях. Я упомянул, что в последние годы были синтезированы тяжелые элементы конца седьмого ряда таблицы Менделеева. Самое тяжелое ядро с массой 294 было получено дважды: как четно-четный изотоп 118-го элемента (содержит 118 протонов и 186 нейтронов) с периодом полураспада около 0,5 мс и нечетно-нечетный изотоп 117-го элемента (117 протонов и 187 нейтронов) с периодом полураспада в 100 раз большим. Это огромные времена в ядерных масштабах (хотя работать с ними очень трудно) — свидетельство того, что и более тяжелые ядра с массой 300 и выше также могут существовать.
И конечно, убедиться в том, что столь тяжелые ядра можно синтезировать в тех или иных ядерных реакциях. Я упомянул, что в последние годы были синтезированы тяжелые элементы конца седьмого ряда таблицы Менделеева. Самое тяжелое ядро с массой 294 было получено дважды: как четно-четный изотоп 118-го элемента (содержит 118 протонов и 186 нейтронов) с периодом полураспада около 0,5 мс и нечетно-нечетный изотоп 117-го элемента (117 протонов и 187 нейтронов) с периодом полураспада в 100 раз большим. Это огромные времена в ядерных масштабах (хотя работать с ними очень трудно) — свидетельство того, что и более тяжелые ядра с массой 300 и выше также могут существовать.
— Кажется, что дело сделано…
— Нет, показана лишь выполнимость необходимого первого условия. Теперь надо эти ядра получить в эксперименте. И тут мы быстро пришли к заключению, что наши средства, которые сыграли решающую роль в синтезе сверхтяжелых элементов (многие из них были лучшими в мировой практике) совершенно непригодны, чтобы двигаться вперед. На новом этапе исследований необходимо существенно поднять чувствительность эксперимента, улучшить аппаратуру, иметь значительно более мощные ускорители, более совершенные методики, освоить новые технологии. Нужно как бы уйти из прошлого и перейти в здание будущего. И совершить переход по возможности быстро. Мы пошли этим путем.
На новом этапе исследований необходимо существенно поднять чувствительность эксперимента, улучшить аппаратуру, иметь значительно более мощные ускорители, более совершенные методики, освоить новые технологии. Нужно как бы уйти из прошлого и перейти в здание будущего. И совершить переход по возможности быстро. Мы пошли этим путем.
С 2012 г. Объединенный институт ядерных исследований в Дубне начал строить новый ускорительный комплекс, по существу новую лабораторию — Фабрику сверхтяжелых элементов. Мы поставили задачу увеличить чувствительность опытов в десятки, а со временем, быть может, в 100 раз. Принять такое решение было нелегко, слишком много нового нужно было делать одновременно, но другого выхода не было.
Прошло семь лет, и 26 декабря 2018 г. в 10 утра новый ускоритель (циклотрон ДЦ-280) в соответствии с графиком сооружения этой установки дал первый пучок ускоренных тяжелых ионов. Для наших конструкторов, инженеров и техников это большой этап проделанной работы, свидетельствующий о том, что все узлы нового изделия работают, как задумано. У руководства института тоже есть чувство завершенности: все вложенные средства правильно и быстро реализованы.
У руководства института тоже есть чувство завершенности: все вложенные средства правильно и быстро реализованы.
Для научных же работников это «первый звонок», надо форсировать подготовку к демонстрационным экспериментам. Мы должны почувствовать, что идеи, лежащие в основе созданного нами научно-экспериментального комплекса, состоятельны, что параметры установок соответствуют нашим ожиданиям. Эти эксперименты для нас будут экзаменом. Я бы не стал серьезно обсуждать и тем более расписывать наше будущее, пока мы не сдадим экзамен.
— Можно задать Вам наивный вопрос: зачем нужно дальше заполнять Периодическую таблицу Менделеева? Какое значение для науки имеет эта работа?
— В конечном счете мы проверяем и тем самым изучаем закон природы, открытый Д. И. Менделеевым 150 лет назад. Заполнять Периодическую таблицу очень важно, потому что мы уже чувствуем, что подошли близко к моменту, когда этот закон начинает меняться, причем меняться быстро. И, несмотря на то что продвижение к все более тяжелым элементам требует огромных усилий, познание любых изменений законов природы — например, периодичности свойств химических элементов — носит фундаментальный характер. Как уже говорилось, с ростом атомного номера элемента релятивистский эффект быстро растет. Еще быстрее меняется электронная структура сверхтяжелого атома и энергия связи его последнего электрона, ответственного за химические свойства элемента. Мы же должны исследовать этот эффект экспериментально. А для того чтобы добраться до этих атомов, надо, как говорится, еще пуд соли съесть. Надо получать в десятки и сотни раз больше атомов, чем мы имели в последние годы. Время существования тяжеловесов в лучшем случае — доли секунды. Как определить химические свойства этих атомов за доли секунды? Да, химические реакции идут значительно быстрее, но нужно придумать, как управляться в эти мгновения. Пока не знаем, но будем, определенно, этим заниматься.
Как уже говорилось, с ростом атомного номера элемента релятивистский эффект быстро растет. Еще быстрее меняется электронная структура сверхтяжелого атома и энергия связи его последнего электрона, ответственного за химические свойства элемента. Мы же должны исследовать этот эффект экспериментально. А для того чтобы добраться до этих атомов, надо, как говорится, еще пуд соли съесть. Надо получать в десятки и сотни раз больше атомов, чем мы имели в последние годы. Время существования тяжеловесов в лучшем случае — доли секунды. Как определить химические свойства этих атомов за доли секунды? Да, химические реакции идут значительно быстрее, но нужно придумать, как управляться в эти мгновения. Пока не знаем, но будем, определенно, этим заниматься.
— Ученые, работающие в вашем исследовательском коллективе — выпускники российских вузов?
— Конечно, большинство наших сотрудников пришли в институт после окончания вузов Москвы, Санкт-Петербурга, Воронежа, Саратова, Твери, Томска, Дальнего Востока. Но мы, Объединенный институт ядерных исследований (ОИЯИ), — международный научный центр 18 стран-участниц. Среди них многие бывшие республики Советского Союза, страны Восточной Европы, Азии (Монголия, Вьетнам), Куба. У института широкое научное сотрудничество и с исследователями Швейцарии, Германии, Италии, Франции, Израиля, США и др. С американскими учеными мы взаимодействуем наиболее плотно уже более 25 лет. Они готовят для наших совместных экспериментов мишенный материал на ядерном реакторе в Национальной лаборатории Ок-Риджа.
Но мы, Объединенный институт ядерных исследований (ОИЯИ), — международный научный центр 18 стран-участниц. Среди них многие бывшие республики Советского Союза, страны Восточной Европы, Азии (Монголия, Вьетнам), Куба. У института широкое научное сотрудничество и с исследователями Швейцарии, Германии, Италии, Франции, Израиля, США и др. С американскими учеными мы взаимодействуем наиболее плотно уже более 25 лет. Они готовят для наших совместных экспериментов мишенный материал на ядерном реакторе в Национальной лаборатории Ок-Риджа.
— Почему так трудно произвести элементы, живущие от микросекунды до нескольких секунд, и идентифицировать их химические свойства? Были ли на протяжении Вашей работы кризисные моменты, когда казалось, что исследования зашли в тупик?
— Потому что образование сверхтяжелого элемента — процесс исключительно редкий, и мы работаем на грани возможностей. Мне кажется, что так было всегда. Все переживания и трудности в ходе работы были связаны часто с тем, что не хватало терпения.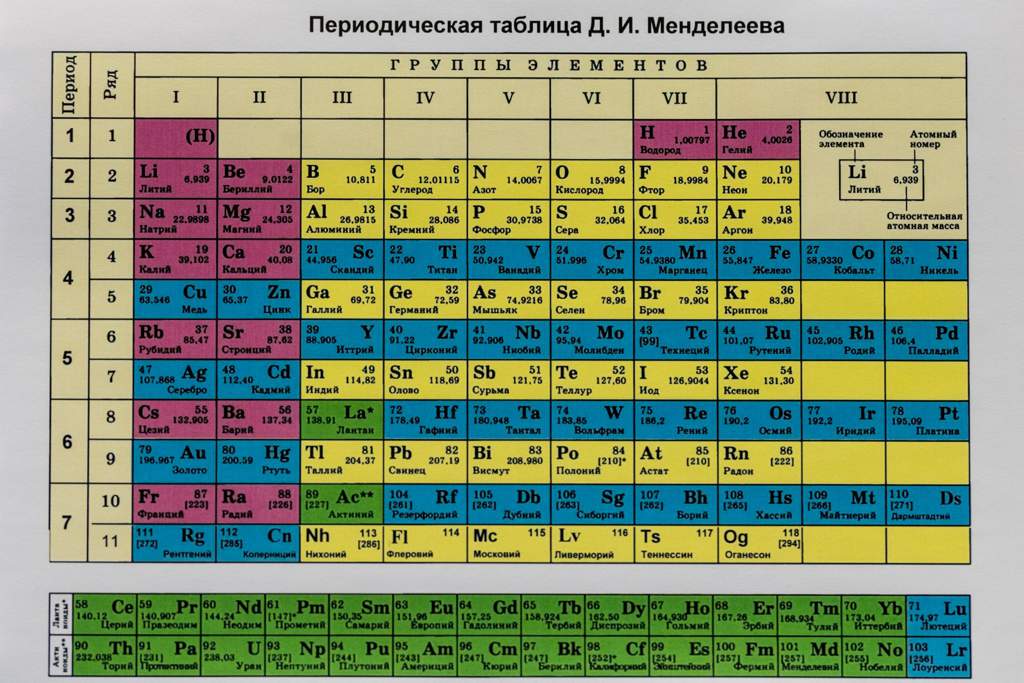 Представьте: на протяжении 12 лет практически непрерывно идет эксперимент. Люди трудятся круглосуточно — посменно, без праздников, суббот и воскресений. Меняется их образ жизни. И в этом режиме, когда, казалось бы, мы должны уже зарегистрировать столь долгожданное событие, его все нет, и непонятна причина. Естественно, закрадываются сомнения: может быть, где-то ошиблись, что-то не доглядели, заранее не проверили. А потом вдруг за неделю сразу два события… В нашей работе это называют статистикой, которую Георгий Николаевич Флёров* справедливо называл «садистикой».
Представьте: на протяжении 12 лет практически непрерывно идет эксперимент. Люди трудятся круглосуточно — посменно, без праздников, суббот и воскресений. Меняется их образ жизни. И в этом режиме, когда, казалось бы, мы должны уже зарегистрировать столь долгожданное событие, его все нет, и непонятна причина. Естественно, закрадываются сомнения: может быть, где-то ошиблись, что-то не доглядели, заранее не проверили. А потом вдруг за неделю сразу два события… В нашей работе это называют статистикой, которую Георгий Николаевич Флёров* справедливо называл «садистикой».
В связи с этими эмоциями я вспомнил, что в 2017 г. был приглашен в Копенгаген на VIII Международную конференцию по ускорителям, ее организаторы решили включить в программу три научных доклада, не связанных непосредственно с тематикой конференции. Меня просили рассказать об открытии сверхтяжелых элементов. А профессор Иоахим Мних, директор по исследованиям Научно-исследовательского центра Deutsches Elektronen-Synchrotron — DESY (Гамбург, Германия) докладывал о будущем проекте Европейского центра ядерных исследований (ЦЕРН, Швейцария). Мне было интересно слушать доклад об открытом в 2012 г. бозоне Хиггса, о котором, как говорил докладчик, мало что известно до сих пор. Из доклада следовало: чтобы исследовать этот знаменитый бозон, надо строить специальный ускорительный комплекс — Хиггс-фабрику (и здесь — фабрика!), так как на Большом адронном коллайдере они рождаются весьма редко. На 10 млрд столкновений — только один бозон Хиггса. «Мне бы такое счастье», — подумал я: у нас ведь в лучшем случае получается один атом сверхтяжелого элемента на триллион столкновений — в 100 раз реже, чем бозон Хиггса! Да еще у этого нуклида надо определить 5–7 поколений его радиоактивного семейства, измерить характеристики распада ядер (энергию и периоды полураспада) в каждом поколении… Когда я сказал об этом Мниху, тот ответил, что знал о наших экспериментах, но не предполагал, что рождение элемента столь редкое явление.
Мне было интересно слушать доклад об открытом в 2012 г. бозоне Хиггса, о котором, как говорил докладчик, мало что известно до сих пор. Из доклада следовало: чтобы исследовать этот знаменитый бозон, надо строить специальный ускорительный комплекс — Хиггс-фабрику (и здесь — фабрика!), так как на Большом адронном коллайдере они рождаются весьма редко. На 10 млрд столкновений — только один бозон Хиггса. «Мне бы такое счастье», — подумал я: у нас ведь в лучшем случае получается один атом сверхтяжелого элемента на триллион столкновений — в 100 раз реже, чем бозон Хиггса! Да еще у этого нуклида надо определить 5–7 поколений его радиоактивного семейства, измерить характеристики распада ядер (энергию и периоды полураспада) в каждом поколении… Когда я сказал об этом Мниху, тот ответил, что знал о наших экспериментах, но не предполагал, что рождение элемента столь редкое явление.
— Как Вам удалось найти оригинальный метод синтеза сверхтяжелых элементов, позволивший обогнать лаборатории ядерных исследований Японии, США?
— Мы действительно использовали новый подход и не делали из этого секрета. Однако и прежний метод синтеза, так называемое холодное слияние ядер, тоже родился в стенах нашей лаборатории в 1974 г. Спустя несколько лет после первых экспериментов нам стало понятно, что к получению долгоживущих сверхтяжелых элементов реакция холодного слияния не приведет, потому что во взаимодействующих ядрах не хватает нейтронов. А для того чтобы получить даже весьма скромный избыток нейтронов, нужно существенно усложнить эксперимент: использовать в качестве мишенного материала не свинец или висмут, как ранее, а нейтронно-избыточные изотопы искусственных элементов, такие как: плутоний-244 (244Pu) или кюрий-248 (248Cm). А в качестве бомбардирующего снаряда надо выбрать уникальное вещество — очень редкий и дорогой кальций-48 (48Ca)** (содержит 20 протонов и 28 нейтронов): в естественной смеси изотопов кальция его в 500 раз меньше основного изотопа — кальция-40 (40Ca). Затем необходимо ускорить ионы 48Ca до скорости, равной примерно 0,1 скорости света, в расчете на редкий процесс слияния ядер — 244Pu + 48Ca, — ведущего к образованию 114-го элемента.
Однако и прежний метод синтеза, так называемое холодное слияние ядер, тоже родился в стенах нашей лаборатории в 1974 г. Спустя несколько лет после первых экспериментов нам стало понятно, что к получению долгоживущих сверхтяжелых элементов реакция холодного слияния не приведет, потому что во взаимодействующих ядрах не хватает нейтронов. А для того чтобы получить даже весьма скромный избыток нейтронов, нужно существенно усложнить эксперимент: использовать в качестве мишенного материала не свинец или висмут, как ранее, а нейтронно-избыточные изотопы искусственных элементов, такие как: плутоний-244 (244Pu) или кюрий-248 (248Cm). А в качестве бомбардирующего снаряда надо выбрать уникальное вещество — очень редкий и дорогой кальций-48 (48Ca)** (содержит 20 протонов и 28 нейтронов): в естественной смеси изотопов кальция его в 500 раз меньше основного изотопа — кальция-40 (40Ca). Затем необходимо ускорить ионы 48Ca до скорости, равной примерно 0,1 скорости света, в расчете на редкий процесс слияния ядер — 244Pu + 48Ca, — ведущего к образованию 114-го элемента.
На Фабрике сверхтяжелых элементов мы не планируем проводить много экспериментов; их будет несколько в год, но более длительных и емких, чем прежние. Наверное, через 15–20 лет наши нововведения вновь устареют, но при трех-четырех экспериментах в год можно будет накопить данные, которые позволят понять структуру и свойства тяжелейших элементов и, конечно, существенно расширят наши знания о границах Таблицы элементов.
— Таким образом, Вы отводите 20 лет для того, чтобы разобраться с вопросами, которые сегодня поставила Периодическая таблица?
— Не могу точно предсказать, но 15–20 лет не столь большой срок. Время летит быстро. Учтем также, что по ходу дела будут возникать вопросы, требующие ответов.
— Можно ли предположить, что где-то в природе (может быть, в космосе) реализуются естественные условия синтеза сверхтяжелых элементов?
— Серьезная проблема, и астрофизики занимаются этим делом основательно. Могут ли сверхтяжелые элементы образоваться в природном синтезе (нуклеосинтезе) подобно всем тяжелым элементам, вплоть до урана? Тот факт, что в космических лучах не обнаружены ядра тяжелее урана, теоретически объясним более коротким временем их жизни по сравнению со временем пролета от источника к детектору. С другой стороны, всегда остается вопрос: способен ли нуклеосинтез во вспышке сверхновой дотянуться до столь тяжелых ядер? А если да, то смогут ли эти элементы выжить в процессе последовательных бета-распадов и лечь на линию бета-стабильности? Я не хочу вводить читателя в частные проблемы, достаточно почувствовать, что процесс определяется многими условиями. Хотел бы только обратить внимание на то, что искусственный синтез элементов далек от того, как он происходит в природе. Мы в лаборатории не в состоянии создать условия вспышки сверхновой, с большими плотностями потока нейтронов, сверхвысокими температурами, с вовлечением огромного количества вещества. Поэтому сталкиваем уже приготовленные природой или наработанные в ядерном реакторе долгоживущие нуклиды, преследуя цель уловить редкий процесс слияния ядер с образованием составного ядра суммарной массы, его быстрое охлаждение не без потерь (выживание) и затем наблюдать его самопроизвольный распад.
С другой стороны, всегда остается вопрос: способен ли нуклеосинтез во вспышке сверхновой дотянуться до столь тяжелых ядер? А если да, то смогут ли эти элементы выжить в процессе последовательных бета-распадов и лечь на линию бета-стабильности? Я не хочу вводить читателя в частные проблемы, достаточно почувствовать, что процесс определяется многими условиями. Хотел бы только обратить внимание на то, что искусственный синтез элементов далек от того, как он происходит в природе. Мы в лаборатории не в состоянии создать условия вспышки сверхновой, с большими плотностями потока нейтронов, сверхвысокими температурами, с вовлечением огромного количества вещества. Поэтому сталкиваем уже приготовленные природой или наработанные в ядерном реакторе долгоживущие нуклиды, преследуя цель уловить редкий процесс слияния ядер с образованием составного ядра суммарной массы, его быстрое охлаждение не без потерь (выживание) и затем наблюдать его самопроизвольный распад.
Результаты, более-менее близкие к природному синтезу, реализуются в малом объеме подземного ядерного взрыва, когда исходным веществом для последующего синтеза более тяжелых элементов служит уран или плутоний. За очень короткий промежуток времени, менее 1 мкс, в цепной реакции возникает поток нейтронов высокой плотности, в котором исходные ядра могут захватить до 20 нейтронов. В последующих после взрыва бета-распадах образуются трансурановые элементы вплоть до 100-го элемента — фермия. Так были впервые синтезированы элементы с Z = 99 и Z = 100. Но для синтеза более тяжелых элементов этих условий явно недостаточно. Напомним, что при вспышке сверхновой синтез длится секунды и в процесс вовлечены массы вещества, превышающие массу Солнца.
За очень короткий промежуток времени, менее 1 мкс, в цепной реакции возникает поток нейтронов высокой плотности, в котором исходные ядра могут захватить до 20 нейтронов. В последующих после взрыва бета-распадах образуются трансурановые элементы вплоть до 100-го элемента — фермия. Так были впервые синтезированы элементы с Z = 99 и Z = 100. Но для синтеза более тяжелых элементов этих условий явно недостаточно. Напомним, что при вспышке сверхновой синтез длится секунды и в процесс вовлечены массы вещества, превышающие массу Солнца.
— Некоторые ученые допускают, что при столкновении черных дыр могут извергаться короткоживущие ядра, которые при распаде образовали бы ядра тяжелее железа. Согласны ли Вы с этим предположением?
— Когда астрофизики говорят о взаимодействии черных дыр или нейтронных звезд, они рассматривают также взрывные процессы нуклеосинтеза, как при вспышке сверхновой. В момент соприкосновения двух нейтронных звезд эти гигантские объекты теряют устойчивость, в результате чего в космическое пространство выплескивается огромное количество вещества, исчисляемое в тысячах сверхновых! Теперь даже принято исчислять подобные катаклизмы в «килоновых». Естественно, при увеличении мощности взрыва на три порядка нуклеосинтез может пройти дальше, к более тяжелым ядрам. Но какие-то иные пути нуклеосинтеза, присущие столкновению нейтронных звезд и отличные от взрыва сверхновых, пока серьезно не рассматриваются. Хотя, конечно, нельзя исключить, что подобные особенности могут стать видны при более глубоком рассмотрении этих сложных процессов.
Естественно, при увеличении мощности взрыва на три порядка нуклеосинтез может пройти дальше, к более тяжелым ядрам. Но какие-то иные пути нуклеосинтеза, присущие столкновению нейтронных звезд и отличные от взрыва сверхновых, пока серьезно не рассматриваются. Хотя, конечно, нельзя исключить, что подобные особенности могут стать видны при более глубоком рассмотрении этих сложных процессов.
— Как бы Вы ответили: какую роль Периодическая таблица играет в Вашей научной работе?
— Я пришел к этой задаче из своих занятий ядерной физикой. Теперь столкнулся с проблемой электронной структуры тяжелейших атомов. Красивая наука — атомная физика, демонстрирующая удивительную гармонию. Она очень притягательна и интересна. Жалею, что не занялся этой наукой немного раньше.
* Г. Н. Флёров (1913–1990) — советский физик-ядерщик, один из отцов-основателей Объединенного института ядерных исследований в Дубне, академик АН СССР.
** Кальций-48 (48Ca) — самый тяжелый изотоп кальция, испытывает двойной бета-распад с периодом полураспада (4,39 ± 0,58) 1019 лет.
115 элемент таблицы Менделеева: краткая характеристика
115 элемент таблицы Менделеева – московий (moscovium) – сверхтяжелый синтетический элемент с символом Mc и атомным номером 115. Он был впервые получен в 2003 году совместной командой российских и американских ученых в Объединенном институте ядерных исследований (ОИЯИ) в Дубне, Россия. В декабре 2015 года признан одним из четырех новых элементов Объединенной рабочей группой международных научных организаций IUPAC/IUPAP. 28 ноября 2016 года он был официально назван в честь Московского региона, в котором находится ОИЯИ.
Характеристика
115 элемент таблицы Менделеева является чрезвычайно радиоактивным веществом: его наиболее стабильный известный изотоп, moscovium-290 имеет период полураспада всего 0,8 секунды. Ученые относят московий к непереходным металлам, по ряду характеристик схожим с висмутом. В периодической таблице относится к трансактинидным элементам p-блока 7-го периода и помещен в группу 15 как самый тяжелый пниктоген (элемент подгруппы азота), хотя и не подтверждено, что он ведет себя, как более тяжелый гомолог висмута.
Согласно расчетам, элемент обладает некоторыми свойствами, схожими с более легкими гомологами: азотом, фосфором, мышьяком, сурьмой и висмутом. При этом демонстрирует несколько существенных отличий от них. На сегодня синтезировано около 100 атомов московия, которые имеют массовые числа от 287 до 290.
Физические свойства
Валентные электроны 115 элемента таблицы Менделеева московия делятся на три подоболочки: 7s (два электрона), 7p1/2 (два электрона) и 7p3/2 (один электрон). Первые два из них релятивистски стабилизируются и, следовательно, ведут себя, как инертные газы, а последние релятивистски дестабилизируются и могут легко участвовать в химических взаимодействиях. Таким образом, первичный потенциал ионизации московия должен составлять около 5,58 эВ. Согласно расчетам, moscovium должен быть плотным металлом из-за его высокого атомного веса с плотностью около 13,5 г/см3.
Предполагаемые расчетные характеристики:
- Фаза: твердая.

- Температура плавления: 400°С (670°К, 750°F).
- Точка кипения: 1100°С (1400°К, 2000°F).
- Удельная теплота плавления: 5,90-5,98 кДж/моль.
- Удельная теплота парообразования и конденсации: 138 кДж/моль.
Химические свойства
115-й элемент таблицы Менделеева стоит третьим в ряду химических элементов 7p и является самым тяжелым членом группы 15 в периодической таблице, располагаясь ниже висмута. Химическое взаимодействие московия в водном растворе обусловлено характеристиками ионов Mc+ и Mc3+. Первые, предположительно, легко гидролизуются и образуют ионную связь с галогенами, цианидами и аммиаком. Гидроксид московия (I) (McOH), карбонат (Mc2CO3), оксалат (Mc2C2O4) и фторид (McF) должны растворяться в воде. Сульфид (Мс2S) должен быть нерастворимым. Хлорид (McCl), бромид (McBr), йодид (McI) и тиоцианат (McSCN) – слаборастворимые соединения.
Фторид московия (III) (McF3) и тиозонид (McS3), предположительно, нерастворимы в воде (аналогично соответствующим соединениям висмута). В то время, как хлорид (III) (McCl3), бромид (McBr3) и иодид (McI3) должны быть легко растворимы и легко гидролизованы с образованием оксогалогенидов, таких как McOCl и McOBr (также аналогично висмуту). Оксиды московия (I) и (III) обладают схожими состояниями окисления, и их относительная стабильность в значительной степени зависит от того, с какими элементами они взаимодействуют.
В то время, как хлорид (III) (McCl3), бромид (McBr3) и иодид (McI3) должны быть легко растворимы и легко гидролизованы с образованием оксогалогенидов, таких как McOCl и McOBr (также аналогично висмуту). Оксиды московия (I) и (III) обладают схожими состояниями окисления, и их относительная стабильность в значительной степени зависит от того, с какими элементами они взаимодействуют.
Неопределенность
Вследствие того, что 115 элемент таблицы Менделеева синтезируется единичными атомами, определить экспериментально его точные характеристики проблематично. Ученым приходится ориентироваться на теоретические расчеты и сравнивать с более стабильными элементами, схожими по свойствам.
В 2011 году были проведены эксперименты по созданию изотопов нихония, флеровия и московия в реакциях между «ускорителями» (кальцием-48) и «мишенями» (америцием-243 и плутонием-244) для исследования их свойств. Однако «мишени» включали примеси свинца и висмута и, следовательно, были получены в реакциях переноса нуклонов некоторые изотопы висмута и полония, что осложнило проведение эксперимента. Между тем, полученные данные помогут в будущем ученым более детально исследовать тяжелые гомологи висмута и полония, такие как moscovium и livermorium.
Между тем, полученные данные помогут в будущем ученым более детально исследовать тяжелые гомологи висмута и полония, такие как moscovium и livermorium.
Открытие
Первым успешным синтезом 115 элемента таблицы Менделеева была совместная работа российских и американских ученых в августе 2003 года в ОИЯИ в Дубне. В команду во главе с физиком-ядерщиком Юрием Оганесяном, помимо отечественных специалистов, вошли коллеги из Ливерморской национальной лаборатории Лоуренса. Исследователи 2 февраля 2004 года опубликовали в издании Physical Review информацию, что они бомбардировали америций-243 ионами кальция-48 на циклотроне У-400 и получили четыре атома нового вещества (одно ядро 287Mc и три ядра 288Mc). Эти атомы затухают (распадаются) за счет эмиссии альфа-частиц до элемента нихония примерно за 100 миллисекунд. Два более тяжелых изотопа московия, 289Mc и 290Mc, были обнаружены в 2009-2010 годах.
Первоначально IUPAC не могла утвердить открытие нового элемента. Требовалось подтверждение из других источников. В течение следующих нескольких лет была проведена еще одна оценка более поздних экспериментов, и еще раз выдвинуто заявление дубненской команды об открытии 115-го элемента.
Требовалось подтверждение из других источников. В течение следующих нескольких лет была проведена еще одна оценка более поздних экспериментов, и еще раз выдвинуто заявление дубненской команды об открытии 115-го элемента.
В августе 2013 года группа исследователей из Университета Лунда и Института тяжелых ионов в Дармштадте (Германия) объявили, что они повторили эксперимент 2004 года, подтвердив результаты, полученные в Дубне. Еще одно подтверждение было опубликовано командой ученых, работавших в Беркли в 2015 году. В декабре 2015 года совместная рабочая группа IUPAC/IUPAP признала обнаружение этого элемента и отдала приоритет в открытии российско-американской команде исследователей.
Название
115 элемент таблицы Менделеева в 1979 году согласно рекомендации IUPAC было решено назвать «унунпентий» и обозначать соответствующим символом UUP. Несмотря на то, что данное название с тех пор широко использовалось в отношении неоткрытого (но теоретически предсказанного) элемента, в сообществе физиков оно не прижилось. Чаще всего вещество так и называли – элемент №115 или E115.
Чаще всего вещество так и называли – элемент №115 или E115.
30 декабря 2015 года обнаружение нового элемента было признано Международным союзом чистой и прикладной химии. Согласно новым правилам, первооткрыватели имеют право предложить собственное название нового вещества. Сначала предполагалось назвать 115 элемент таблицы Менделеева «лангевиний» в честь физика Поля Ланжевена. Позднее команда ученых из Дубны, как вариант, предложила наименование «московий» в честь Московской области, где и было совершено открытие. В июне 2016 года IUPAC одобрил инициативу и 28 ноября 2016 официально утвердил название «moscovium».
Описание проекта | Периодическая таблица химических элементов Д. И. Менделеева с историческими сведениями
Периодическая система химических элементов Д. И. Менделеева, графическим отражением которой является периодическая таблица, является объектом специального изучения в течение всего периода изучения химии в общеобразовательной школе. В традиционном подходе к построению курса химии изучению периодического закона и периодической системы предшествует период накопления знаний об основных законах химии, атомно-молекулярной теории и фактов о веществах и химических реакциях. После изучения периодической системы она становится средством изучения химических элементов и их соединений в основной школе, а затем служит для обобщения, систематизации и углубления знаний в старших классах. С целью усиления мотивации учащихся к изучению химии можно предложить им поучаствовать в проекте по разработке интерактивной периодической таблицы.
После изучения периодической системы она становится средством изучения химических элементов и их соединений в основной школе, а затем служит для обобщения, систематизации и углубления знаний в старших классах. С целью усиления мотивации учащихся к изучению химии можно предложить им поучаствовать в проекте по разработке интерактивной периодической таблицы.
В Интернете можно найти достаточно много интерактивных периодических таблиц, содержащих сведения о химических элементах. Такие таблицы представлены на следующих сайтах:
http://chem.50webs.com/mendeleev/table.html,
http://chemistry.4qp.ru/,
http://chemistry-chemists.com/N3_2012/U3/ChemistryAndChemists_3_2012-U3-…,
http://table-mendeleev.ru/,
http://www.ptable.com/,
http://www.webelements.narod.ru/,
http://www.webmath.ru/poleznoe/table_mendeleev.php и др.
Эти таблицы, по сути, являются электронными справочниками. Их содержание во многих случаях сугубо физико-химическое, представленное сведениями об электронной формуле атомов элемента, относительной электроотрицательности элементов, температурах плавления и кипения, теплопроводности, плотности, цвете простых веществ, образованных элементами, структуре, получении и взаимодействии их с другими веществами. Между тем учащиеся интересуются историей открытия элементов, биографиями отдельных химиков, описанием обстоятельств тех или иных открытий, другими сведениями, выходящими за рамки «сухого» перечисления фактов.
Между тем учащиеся интересуются историей открытия элементов, биографиями отдельных химиков, описанием обстоятельств тех или иных открытий, другими сведениями, выходящими за рамки «сухого» перечисления фактов.
Сведения об учёных-химиках в общеобразовательных школах востребованы в связи с принципом историчности, соблюдение которого свидетельствует о соответствии обучения современным стандартам. О таких известных учёных, как А. Авогадро, С. Аррениус, А. М. Бутлеров, Д. Дальтон, М. В. Ломоносов, Д. И. Менделеев в каждом учебнике содержатся небольшие справки в текстах параграфа или в конце учебника как отдельное приложение. Как правило, это краткая биография учёного и сведения об открытиях, совершённым им, либо описание его вклада в развитие химии. Любые другие сведения, не имеющие отношения к науке, чаще всего не освещаются в школьных учебниках. Учителю для подготовки к уроку также не всегда под силу найти дополнительный материал.
Мы предлагаем проект «Интерактивная периодическая таблица химических элементов», который будет интересен не только учителям химии общеобразовательных школ, но и учащимся, и студентам педагогических вузов, обучающимся по специальности «химия». Учащиеся и студенты не только получат в едином комплексе интересную для них информацию, но и сами могут участвовать в этом проекте, поскольку он является открытым. А учителя химии, помимо участия в проекте, смогут воспользоваться его материалами для разработки своих уроков, самостоятельно определяя объём и структуру содержания, отбирая соответствующие иллюстрации.
Учащиеся и студенты не только получат в едином комплексе интересную для них информацию, но и сами могут участвовать в этом проекте, поскольку он является открытым. А учителя химии, помимо участия в проекте, смогут воспользоваться его материалами для разработки своих уроков, самостоятельно определяя объём и структуру содержания, отбирая соответствующие иллюстрации.
Идея разработки данного интерактивного пособия возникла из желания и необходимости сохранить труд двух известных методистов-химиков – Петра Петровича Чернова и Семёна Васильевича Дьяковича. В 80-е годы прошлого столетия доцент Ферганского педагогического института Чернов разработал периодическую таблицу с историческими сведениями. Свои материалы он передал на кафедру химии Новосибирского государственного педагогического университета(НГПУ), где сведения об элементах были уточнены и дополнены профессором кафедры химии С. В. Дьяковичем. Своими руками он изготовил оригинал таблицы размером 2,5 × 2,2 м, который более 10 лет находился в большой химической аудитории кафедры химии НГПУ. В настоящее время используются уменьшенные копии этой таблицы или отдельные карточки.
В настоящее время используются уменьшенные копии этой таблицы или отдельные карточки.
Новые информационные технологии, реализуемые с помощью компьютера, позволили развить дальше идеи П. П. Чернова и С. В. Дьяковича и разработать интерактивный вариант их таблицы, а именно сайт, размещённый в Интернете.
Это уникальный Интернет-проект (сейчас веб-сайт, а в перспективе, возможно: сайт + мобильное приложение, поэтому можно назвать Интернет-проект) с множеством гиперссылок, написанный на языках веб-программирования (html, php, javascript). Необходимые условия: подключение к интернету, браузер (любой). Желательные условия для корректной работы: браузер IE – от 9 версии, firefox – от 5, chrom – от 5, safari – от 4, opera – от 10, поддержка cookies и javascript. Найти данный продукт можно по ссылке http://mendel.mirapage.ru/.
Основу нашего пособия составляет периодическая таблица химических элементов Д. И. Менделеева. В каждой клетке таблицы имеются все необходимые элементы информации, а именно: порядковый номер, химический знак, русское и латинское названия, происхождение названия, относительная атомная масса элемента, дата и страна открытия, фамилия первооткрывателя, годы его жизни и портрет учёного (рисунок 1).
Каждый элемент информации активен – он является гиперссылкой на соответствующий информационный ресурс. Так, от относительной атомной массы можно перейти в раздел «Строение атома».
Русское название элемента позволяет перейти в раздел «Нахождение элемента в природе», в котором помимо простого вещества, образованного элементом, описываются его минералы и горные породы, в которые он входит.
Рисунок 1 – Карточка элемента с историческими сведениями
Химический знак позволяет раскрыть общую характеристику элемента, а порядковый номер – происхождение названия. Эту же информацию можно получить, переходя на ресурс по гиперссылке от латинского названия.
Под латинским названием указаны год и страна открытия, а также фамилия учёного, открывшего элемент (или иная информация в случае, если неизвестен автор открытия). Все элементы являются активными и отсылают пользователя к краткой истории открытия элемента.
Нажимая на портрет учёного (или иную иконку), можно перейти в раздел, содержащий биографию учёного. Таким образом, основными разделами, связанными с каждым элементом, являются:
Таким образом, основными разделами, связанными с каждым элементом, являются:
- биография учёного, открывшего химический элемент;
- история открытия химического элемента;
- происхождение названия химического элемента;
- нахождение в природе, минералы;
- строение атома;
- характеристика;
- интересные факты.
Существенным отличием нашего электронного продукта является так называемая методическая справка, включающая в себя цели и задачи изучения отдельных тем школьного курса химии, так или иначе связанных в конкретным химическим элементом. Считаем, что эта методическая справка будет полезна не только учителям химии, но и студентам, обучающимся в педагогических вузах по химическим специальностям.
резюме таблицы Менделеева | Британика
- Развлечения и поп-культура
- География и путешествия
- Здоровье и медицина
- Образ жизни и социальные вопросы
- Литература
- Философия и религия
- Политика, право и правительство
- Наука
- Спорт и отдых
- Технология
- Изобразительное искусство
- Всемирная история
- Этот день в истории
- Викторины
- Подкасты
- Словарь
- Биографии
- Резюме
- Популярные вопросы
- Обзор недели
- Инфографика
- Демистификация
- Списки
- #WTFact
- Товарищи
- Галереи изображений
- Прожектор
- Форум
- Один хороший факт
- Развлечения и поп-культура
- География и путешествия
- Здоровье и медицина
- Образ жизни и социальные вопросы
- Литература
- Философия и религия
- Политика, право и правительство
- Наука
- Спорт и отдых
- Технология
- Изобразительное искусство
- Всемирная история
- Britannica Classics
Посмотрите эти ретро-видео из архивов Encyclopedia Britannica.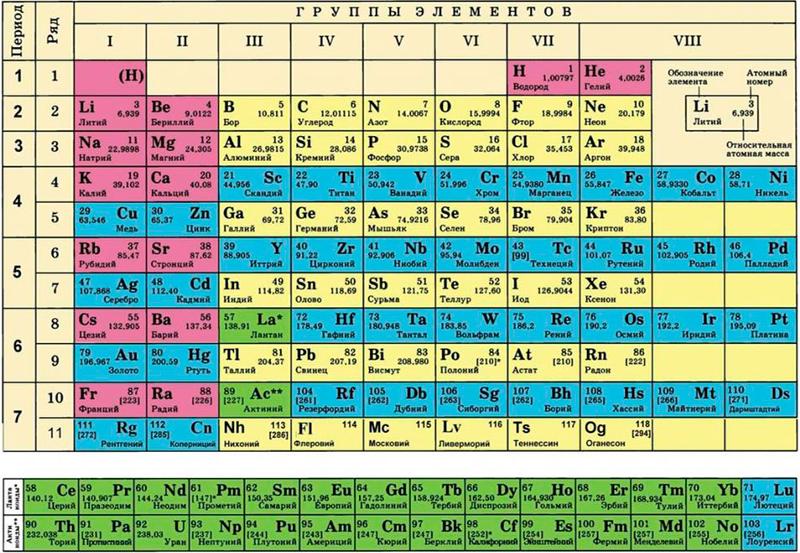
- Britannica объясняет
В этих видеороликах Britannica объясняет различные темы и отвечает на часто задаваемые вопросы. - Demystified Videos
В Demystified у Britannica есть все ответы на ваши животрепещущие вопросы. - #WTFact Видео
В #WTFact Britannica делится некоторыми из самых странных фактов, которые мы можем найти. - На этот раз в истории
В этих видеороликах узнайте, что произошло в этом месяце (или любом другом месяце!) в истории.
- Студенческий портал
Britannica — лучший ресурс для учащихся по ключевым школьным предметам, таким как история, государственное управление, литература и т. д. - Портал COVID-19
Хотя этот глобальный кризис в области здравоохранения продолжает развиваться, может быть полезно обратиться к прошлым пандемиям, чтобы лучше понять, как реагировать сегодня. - 100 женщин
Britannica празднует столетие Девятнадцатой поправки, выделяя суфражисток и политиков, творящих историю.
- Britannica Beyond
Мы создали новое место, где вопросы находятся в центре обучения. Вперед, продолжать. Спросить. Мы не будем возражать. - Спасение Земли
Британника представляет список дел Земли на 21 век. Узнайте об основных экологических проблемах, стоящих перед нашей планетой, и о том, что с ними можно сделать! - SpaceNext50
Britannica представляет SpaceNext50. От полёта на Луну до управления космосом — мы изучаем широкий спектр тем, которые подпитывают наше любопытство к космосу!
- Введение и популярные вопросы
История периодического закона
- Classification of the elements
- The first periodic table
- Other versions of the periodic table
- Predictive value of the periodic law
- Discovery of new elements
- Significance of atomic numbers
- Выяснение периодического закона
- Classification of the elements
Таблица Менделеева
- Периоды
- Группы
- Classification of elements into groups
- Periodic trends in properties
The basis of the periodic system
- Electronic structure
- Periodicity of properties of the elements
Other chemical и физические классификации
Основные факты
- 2-минутное резюме
Популярные вопросы
- Факты и сопутствующий контент
- викторины
Медиа
- Видео
- Картинки
- Интерактивы
Периодическая таблица — элементы, определение, группы, периоды, блоки
Согласно приведенному выше определению и объяснению, полная форма периодической таблицы разделена на три части, такие как левая, правая и средняя части для изучения химии или физики в науке.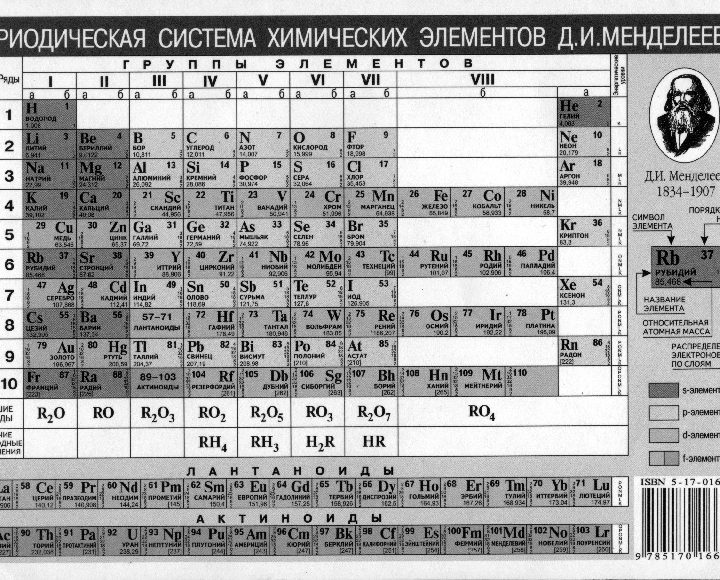 .
.
- В левой части таблицы группы IA и IIA определяют чрезвычайно высокий электроположительный характер, но очень низкую энергию ионизации и всегда показывают положительную степень окисления.
- Правая часть содержит группы IIIA, IVA, VA, VIA, VIIA с высоким сродством к электрону и нереакционноспособные благородные газы, такие как гелий , неон , аргон, криптон, ксенон и радон.
- Организация средней части периодической таблицы представляет собой взаимосвязь между левой и правой частями и содержит список переходных металлов или элементов d-блока и внутренних переходных элементов или элементов f-блока.
Блоки периодической таблицы
Согласно современному периодическому закону, основанному на атомном номере и расположении электронов валентной оболочки элементов, различные типы металлов и неметаллов в химии организованы в формы s, p, d и f- блок в периодической таблице.
Элементы s-блока
Название элемента s-блока в периодической таблице связано с расположением электронов, валентный электрон переходит на ns-орбиталь и постепенно заполняется в соответствии с правилами конфигурации.
Группа 1 (водород, литий, натрий, калий, рубидий, цезий и франций) и группа 2 (бериллий, магний, кальций, стронций, барий и радий) относятся к элементам s-блока. Электронная конфигурация валентной оболочки, ns 1→2 , где n = главное квантовое число или количество периодов.
p-блок Элементы
P-блок в периодической таблице организован за счет постепенно заполняемой p-орбитали в электронной структуре валентной оболочки, но гелий является исключением с электронным расположением 1s 2 .
Группы-3, 4, 5, 6, 7 и благородные газы относятся к р-блочным элементам. Начиная со второго периода p-элементы, такие как бор, углерод, азот, кислород, фтор и аргон, заполнили s-орбитали с электронной конфигурацией валентной оболочки, 2s 2 2p 1→6 , где n = номер периода.
Элементы d-блока и f-блока
Название d-блок (серия переходов) или f-блок (внутренний ряд переходов) в периодической таблице используется из-за наличия постепенно заполняющихся d- или f-орбиталей в периодической таблице.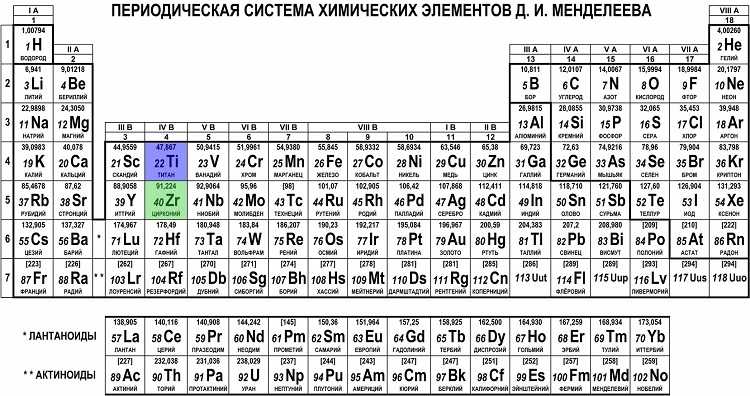 электронная структура валентной оболочки. Переходное или внутреннее переходное семейство образует ионную химическую связь с металлами (s-блок) и ковалентную связь с металлами-неметаллами (p-блок).
электронная структура валентной оболочки. Переходное или внутреннее переходное семейство образует ионную химическую связь с металлами (s-блок) и ковалентную связь с металлами-неметаллами (p-блок).
Таким образом, элементы 3d-блока, такие как скандий, титан, ванадий, хром, железо, кобальт, никель, медь и цинк, помещены в середину таблицы между s- и p-блоком с электронной конфигурацией валентной оболочки, 4s 0→2 3d 1-10 .
F-блок в периодической таблице делится на две серии: 4f или лантаниды и 5f или актиниды, которые содержат много отсутствующих элементов, открытых или синтезированных в результате ядерной реакции радиоактивных изотопов.
Тенденции периодической таблицы
Понимание периодических изменений энергии ионизации, сродства к электрону, электроотрицательности, кислотно-основных свойств и степени окисления в окислительно-восстановительных реакциях химических элементов является очень важными характеристиками для любого обсуждения или информации в химии или науке. При изучении химии мы суммируем физические и химические свойства по группам и периодам.
При изучении химии мы суммируем физические и химические свойства по группам и периодам.
Когда мы движемся вниз в группе, размер и электроположительный характер атомов увеличиваются. Энергия ионизации обычно уменьшается, но во многих случаях увеличивается из-за экранирующих электронов или эффективных зарядов ядер. Нижний член кристаллических твердых металлов, таких как серебро (Ag), золото (Au), кадмий (Cd) и ртуть (Hg), увеличивает энергию ионизации.
Электроотрицательность и сродство к электрону обычно уменьшаются, но иногда наблюдаются некоторые исключения. Тенденция сродства к электрону химического элемента второго ряда в периодической таблице обычно ниже, чем у третьего ряда.
Периодическая таблица с электронной конфигурацией
Пара элементов, расположенных по диагонали друг к другу в таблице Менделеева, описывает простые отношения или химические свойства, такие как электрическая поляризация содержимого в химии. Диагональная пара, такая как бериллий и алюминий, имеет аналогичное отношение изменения к размеру, поскольку размер увеличивается к нижнему периоду, а заряд увеличивается вправо, но это правило не может работать полностью для всех элементов таблицы Менделеева.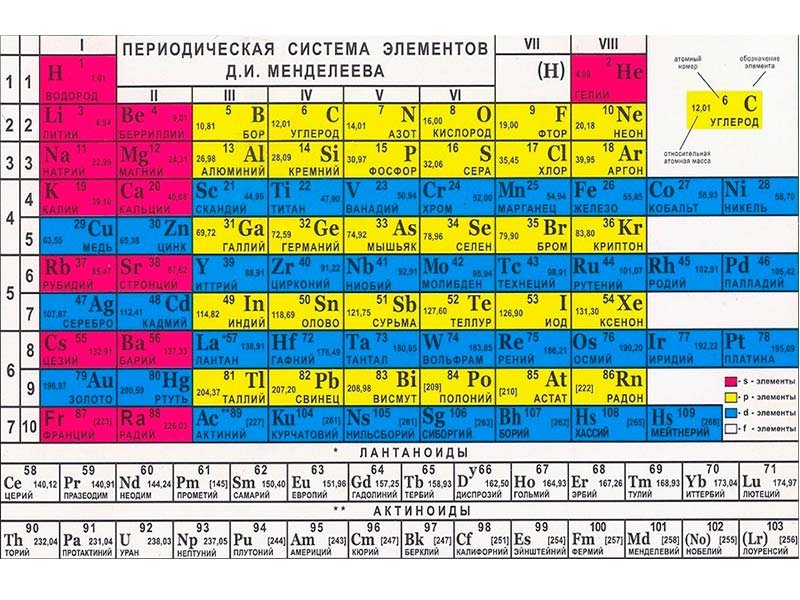
Интересные факты периодической таблицы объясняют общую связь между электронной структурой и периодической аккомодационной способностью химических элементов в краткой форме. Например, на 1s-орбитали может быть только два электрона, следовательно, период один содержит только два элемента.
Период-VI включает 6s, 4f, 5d и 6p орбитали в электронной структуре валентной оболочки с общим количеством (2 + 14 + 10 + 6) = 32 элемента от цезия до радона. Упрощенная научная формула в химии используется для расчета количества химических элементов в каждом периоде периодической таблицы семейств.
Популярные темы
Химическая реакция
Химические соединения
Атомная структура
Периодическая таблица и смысл
[peer-ee-od-ik, peer- ]
/ ˈpɪər iˈɒd ɪk, ˌpɪər- /
Сохранить это слово!
См. синонимы для таблицы Менделеева на Thesaurus.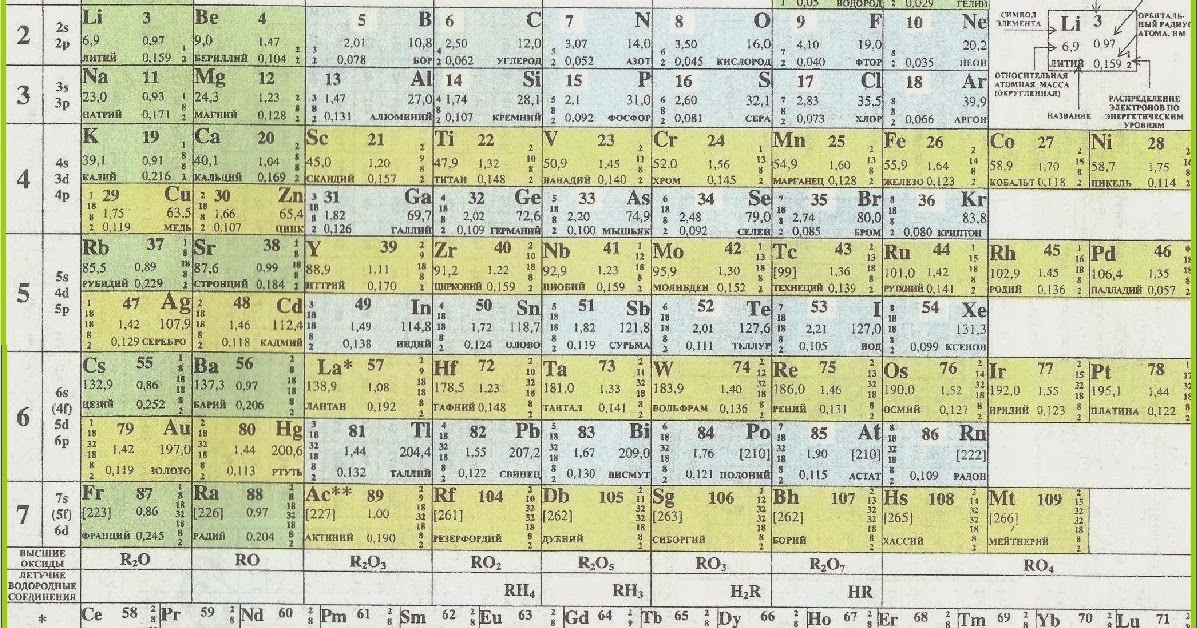 com
com
Показывает уровень обучения в зависимости от сложности слова.
сущ. Химия.
таблица, иллюстрирующая периодическую систему, в которой химические элементы, ранее расположенные в порядке их атомного веса, а теперь в соответствии с их атомными номерами, показаны в связанных группах.
ВИКТОРИНА
Сыграем ли мы в «ДОЛЖЕН» ПРОТИВ. “ДОЛЖЕН” ВЫЗОВ?
Должны ли вы пройти этот тест на «должен» или «должен»? Это должно оказаться быстрым вызовом!
Вопрос 1 из 6
Какая форма используется для указания обязательства или обязанности кого-либо?
Происхождение периодической таблицы
Впервые записано в 1890–1895 гг. , периодизация, отношение период-светимость
Dictionary.com Unabridged Основано на словаре Random House Unabridged Dictionary, © Random House, Inc., 2022 г.
Как использовать периодическую таблицу в предложении
Введите «водородную радугу», систему цветового кодирования для описания множества способов преобразования самого легкого элемента периодической таблицы в энергию.

Путеводитель по «водородной радуге» для начинающих|Purbita Saha|24 августа 2021 г.|Popular-Science
Редкоземельные элементы, также известные как редкоземельные металлы, состоят из 17 металлических элементов периодической таблицы необходимы для многих высокотехнологичных устройств, включая смартфоны, телевизоры, компьютеры и электромобили.
Захват денег за изменение климата|Шон Каллиган|10 апреля 2021|Ози
Затем Сэмс выпалил другие загрязнители угольной золы, которые были обнаружены в ходе испытаний, слова, которые большинство жителей когда-либо слышали только при изучении периодической таблицы на уроках химии учебный класс.
Угольный завод по соседству | Макс Блау для новостей здравоохранения штата Джорджия | 22 марта 2021 г. химические вещества, узнаваемые по периодической таблице, и все они могут медленно проникать в грунтовые воды.
Угольный завод по соседству | Макс Блау для новостей здравоохранения Джорджии | 22 марта 2021 г.
 Франкенштейн и Дмитрий Менделеев открыли периодическую таблицу химических элементов.
Франкенштейн и Дмитрий Менделеев открыли периодическую таблицу химических элементов.Почему стоит поиграть – Выпуск 94: Эволюция|Андреас Вагнер|16 декабря 2020|Наутилус
Он встает, подходит к их столику, представляется и говорит: «Привет, я Оливер Рид.
История улыбки Ли Марвина Liberty Valance Smile|Роберт Уорд|3 января 2015 г.|DAILY BEAST
Джоэл Остин хочет поговорить о том, как отключить звук мобильного телефона за обеденным столом.
Нет богов, нет копов, нет господ|Джеймс Пулос|1 января 2015|DAILY BEAST
На фото в сепии он изображен маленьким мальчиком, с головой в руках, с большой открытой книгой за барным столом.
Бары, которые сделали Америку великой|Нина Строхлик|28 декабря 2014 г.|DAILY BEAST
Это означает, что любой ответ, который может привести к физическому ущербу в Северной Корее, исключен.
Кибервойна в Северной Корее может быть незаконной|Шейн Харрис|23 декабря 2014|DAILY BEAST
Стол, скрипящий под тяжестью рождественского банкета, классического праздника обжорства и выпивки.
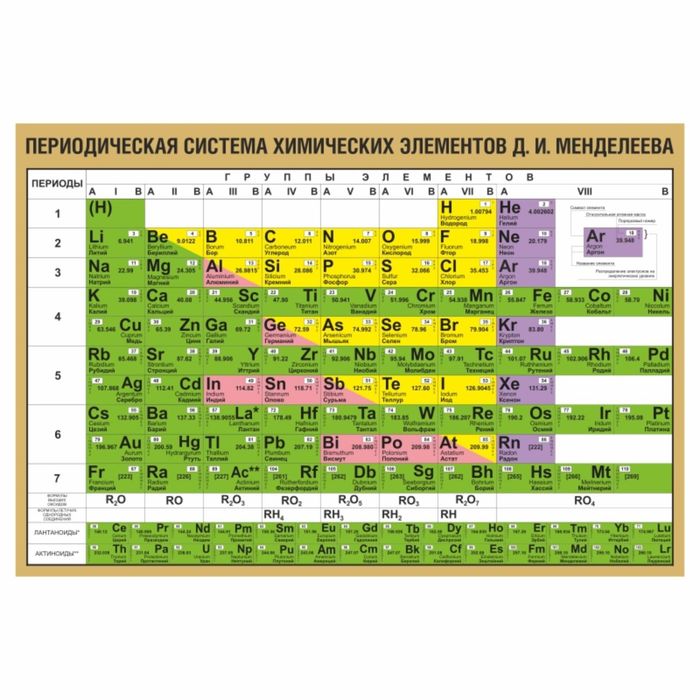
Как Диккенс и Скрудж спасли Рождество|Клайв Ирвинг|22 декабря 2014|DAILY BEAST
Старая миссис Вурзел и пышногрудая, но не слишком симпатичная наследница дома Зерновых сидели во главе стола.
Коронет Пит-Тауна, том I (из 3)|Чарльз Джеймс Уиллс
Маленькая книга в полном фиолетовом переплете лежала наполовину скрытой в пачке тонкой папиросной бумаги на туалетном столике.
Хильда Лессуэйс|Арнольд Беннетт
За большим столом в пасторском доме сидело не менее дюжины дам.
The Pit Town Coronet, Volume I (из 3)|Чарльз Джеймс Уиллс
Мисс Смит тут же встает из-за стола, подставляет свой милый ротик к папочке, чтобы его поцеловали.
Физиология оперы | Джон Х. Сваби (также известный как «Scrici»)
Он вздохнул, кладя бумаги на стол; ибо он думал, что задача будет труднее, чем даже его собственное жертвоприношение.
The Pastor’s Fire-side Vol. 3 of 4|Jane Porter
Определения периодической таблицы в Британском словаре
периодическая таблица
/ (ˌpɪərɪˈɒdɪk) /
существительное
таблица элементов, расположенная в порядке возрастания атомного числа периодический закон. Элементы, имеющие сходные химические свойства и электронное строение, расположены в вертикальных столбцах (группах)
Элементы, имеющие сходные химические свойства и электронное строение, расположены в вертикальных столбцах (группах)
Английский словарь Коллинза – полное и полное цифровое издание 2012 г. © William Collins Sons & Co. Ltd., 1979, 1986 © HarperCollins Publishers 1998, 2000, 2003, 2005, 2006, 2007, 2009, 2012
Медицинские определения для таблицы Менделеева
Таблица Менделеева
n.
Табличное расположение элементов в соответствии с их атомными номерами таким образом, что элементы со сходными химическими свойствами находятся в одном столбце.
Медицинский словарь Стедмана The American Heritage® Авторское право © 2002, 2001, 1995 от компании Houghton Mifflin. Опубликовано компанией Houghton Mifflin.
Научные определения периодической таблицы
Периодическая таблица
Таблица, в которой химические элементы расположены в порядке возрастания атомного номера. Элементы со схожими свойствами располагаются в одном столбце (называемом группой), а элементы с одинаковым числом электронных оболочек располагаются в одном ряду (называемом периодом).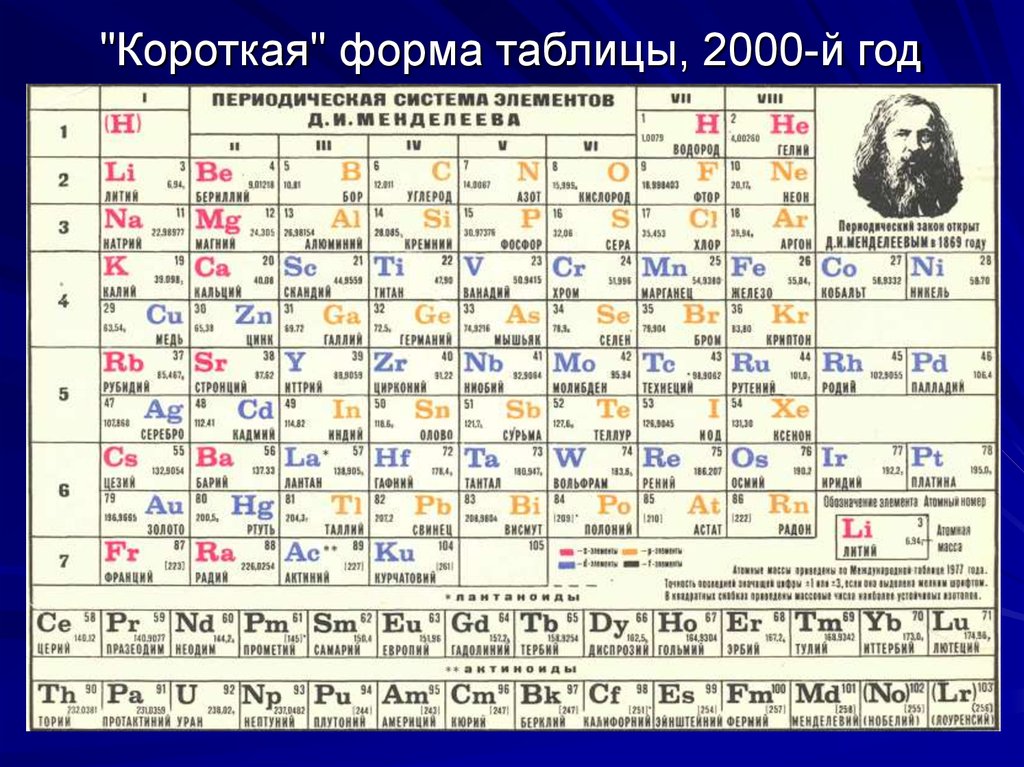
Научный словарь American Heritage® Авторские права © 2011. Опубликовано издательством Houghton Mifflin Harcourt Publishing Company. Все права защищены.
2.S: Элементы, атомы и периодическая таблица (краткое содержание)
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 16179
- Анонимный
- LibreTexts
Чтобы убедиться, что вы понимаете материал этой главы, вам следует просмотреть значения следующих выделенных жирным шрифтом терминов и спросить себя, как они относятся к темам этой главы.
Элемент — это вещество, которое нельзя разложить на более простые химические вещества. Всего известно около 90 встречающихся в природе элементов. Их количество на Земле и в организме различно. Каждый элемент имеет одно- или двухбуквенный химический символ .
Всего известно около 90 встречающихся в природе элементов. Их количество на Земле и в организме различно. Каждый элемент имеет одно- или двухбуквенный химический символ .
современная атомная теория утверждает, что наименьшая часть элемента — это атом . Отдельные атомы чрезвычайно малы, порядка 10 90 248 -10 90 249 м в поперечнике. Большинство элементов существует в чистом виде в виде отдельных атомов, но некоторые существуют в виде двухатомных молекул . Сами атомы состоят из субатомных частиц. Электрон — это крошечная субатомная частица с отрицательным зарядом. Протон имеет положительный заряд и, хотя и мал, намного больше электрона. 9Нейтрон 0231 также намного больше электрона, но не имеет электрического заряда.
Протоны, нейтроны и электроны имеют определенное расположение в атоме. Протоны и нейтроны находятся в центре атома и сгруппированы в ядро . Электроны находятся в нечетких облаках вокруг ядра.
Электроны находятся в нечетких облаках вокруг ядра.
Каждый элемент имеет определенное количество протонов в ядре. Это число протонов атомный номер элемента. Элемент может иметь разное количество нейтронов в ядрах своих атомов; такие атомы называются изотопа . Два изотопа водорода — это дейтерий с протоном и нейтроном в ядре и тритий с протоном и двумя нейтронами в ядре. Сумма числа протонов и нейтронов в ядре называется массовым числом и используется для отличия изотопов друг от друга.
Массы отдельных атомов измеряются в атомных единицах массы . Атомная единица массы равна 1/12 массы одного атома углерода-12. Поскольку разные изотопы элемента имеют разную массу, атомная масса элемента представляет собой средневзвешенное значение масс всех встречающихся в природе изотопов элемента.
Современная теория поведения электрона называется квантовой механикой . Согласно этой теории, электроны в атомах могут иметь только определенные, или , квантованные энергии. Электроны сгруппированы в общие области, называемые оболочками , а внутри них — в более конкретные области, называемые подоболочками . Существует четыре типа подоболочек, и каждый тип может содержать максимальное количество электронов. Распределение электронов по оболочкам и подоболочкам электронная конфигурация атома. Химия обычно возникает из-за взаимодействий между электронами самой внешней оболочки разных атомов, называемых электронами валентной оболочки. Электроны на внутренних оболочках называются остовными электронами.
Согласно этой теории, электроны в атомах могут иметь только определенные, или , квантованные энергии. Электроны сгруппированы в общие области, называемые оболочками , а внутри них — в более конкретные области, называемые подоболочками . Существует четыре типа подоболочек, и каждый тип может содержать максимальное количество электронов. Распределение электронов по оболочкам и подоболочкам электронная конфигурация атома. Химия обычно возникает из-за взаимодействий между электронами самой внешней оболочки разных атомов, называемых электронами валентной оболочки. Электроны на внутренних оболочках называются остовными электронами.
Элементы сгруппированы по сходным химическим свойствам в таблицу, называемую периодической таблицей . Вертикальные столбцы элементов называются группами или семействами . Некоторые из групп элементов имеют названия, такие как щелочные металлы, щелочноземельные металлы, галогены и благородные газы.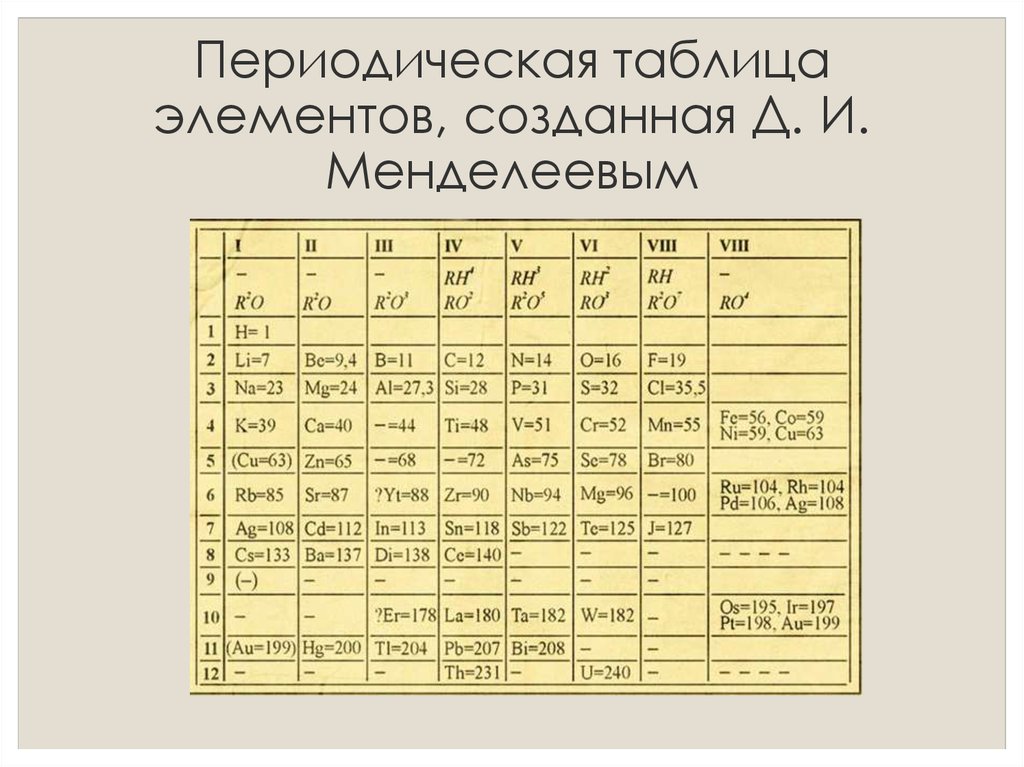 Горизонтальный ряд элементов называется 9.0231 период . Периоды и группы имеют разное количество элементов в них. Периодическая таблица разделяет элементы на металлы , неметаллы и полуметаллы . Периодическая таблица также разделена на элементы основной группы , переходные металлы , лантанидные элементы и актинидные элементы . Лантаноидные и актинидные элементы также называются внутренними элементами из переходных металлов . Форма периодической таблицы отражает последовательное заполнение оболочек и подоболочек в атомах.
Горизонтальный ряд элементов называется 9.0231 период . Периоды и группы имеют разное количество элементов в них. Периодическая таблица разделяет элементы на металлы , неметаллы и полуметаллы . Периодическая таблица также разделена на элементы основной группы , переходные металлы , лантанидные элементы и актинидные элементы . Лантаноидные и актинидные элементы также называются внутренними элементами из переходных металлов . Форма периодической таблицы отражает последовательное заполнение оболочек и подоболочек в атомах.
Периодическая таблица помогает нам понять тенденции в некоторых свойствах атомов. Одним из таких свойств является атомный радиус атомов. Сверху вниз периодической таблицы атомы становятся больше, потому что электроны занимают все большие и большие оболочки. Слева направо по периодической таблице электроны заполняют одну и ту же оболочку, но их притягивает увеличивающийся положительный заряд ядра, и, таким образом, атомы становятся меньше.
Эта страница под названием 2.S: Elements, Atoms, and the Periodic Table (Summary) опубликована в соответствии с лицензией CC BY-NC-SA 3.0 и была создана, изменена и/или курирована Anonymous посредством исходного контента, который был отредактирован к стилю и стандартам платформы LibreTexts; подробная история редактирования доступна по запросу.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или страница
- Автор
- Аноним
- Лицензия
- CC BY-NC-SA
- Версия лицензии
- 3,0
- Программа OER или Publisher
- Издатель, имя которого нельзя называть
- Показать страницу Содержание
- нет на странице
- Метки
- source@https://2012books.
 lardbucket.org/books/introduction-to-chemistry-general-organic-and-biological
lardbucket.org/books/introduction-to-chemistry-general-organic-and-biological
- source@https://2012books.
Периодическая таблица — краткое объяснение основ химии
Главная / Блог Elemental Science
Периодическая таблица наглядно показывает элементы, составляющие все, что мы видим вокруг себя. Это ключевое понятие в химии, которое необходимо преподавать нашим студентам. На самом деле, мы рекомендуем вам знакомить с периодической таблицей в начальных классах.
{Послушайте этот эпизод ниже}
Но это может немного сбивать с толку, потому что кажется, что существует так много разных визуальных вариантов…
Одна таблица Менделеева будет полна цвета, разделив элементы на семейства и дав им имена, как показано ниже.
В одной периодической таблице будет только три цвета, как показано ниже.
Одна периодическая таблица будет иметь четыре разных блока, как показано ниже.
И еще одна периодическая таблица будет иметь столбцы или группы разных цветов, как показано ниже.
И есть еще больше вариантов визуального представления периодической таблицы, чем четыре, которые мы поделились здесь.
Добавьте к этому различия в том, где и как показаны внутренние переходные металлы – лантаноиды и актиноиды. Кроме того, элементы были добавлены и названы на протяжении многих лет, бедный водород, похоже, не знает, к какой группе он принадлежит, а селен иногда является неметаллом, иногда металлоидом!
Все это вызывает простой вопрос – какая таблица Менделеева правильная?
Ну . . . каким-то образом . . . они все есть.
Я знаю – это прозрачно как мутная вода!!
Но помните, что таблица Менделеева — это способ визуально показать отношения между элементами. Подобно нашим человеческим отношениям, эти элементарные отношения можно определить или показать по-разному.
Кроме того, по мере развития технологий растет и наша способность более четко определять эти взаимосвязи. И когда мы экспериментируем с элементами, мы открываем новые вещи, которые помогают формировать периодическую таблицу.
Таким образом, в то время как более новая периодическая таблица может отображать новые элементы, которые мы создали, и более глубокое понимание взаимосвязей между элементами – это не делает старую версию неправильной. Это просто другой снимок нашего понимания элементов.
Принимая во внимание это, можно посмотреть на разные версии и оценить то, чем они могут поделиться с нами. Каждая «картинка» помогает нам узнать больше о том, как элементы связаны друг с другом.
Итак, с этой идеей «моментального снимка» в качестве фона, как мы, педагоги, можем поделиться периодической таблицей со своими учениками?
Давайте начнем с краткого объяснения того, что говорит нам таблица Менделеева…
Как я уже говорил, таблица Менделеева показывает отношения между элементами.
Это систематическое расположение известных и созданных элементов в порядке возрастания атомного номера. И он разработан таким образом, что элементы со схожими свойствами вместе группируются вместе.
Другими словами, вы можете с первого взгляда сказать, какие элементы будут вести себя одинаково, а какие будут сильно отличаться по своей реакции.
Периодическая таблица обычно дает следующую информацию для каждого элемента…
- атомный номер , это количество протонов, которое можно найти в ядре атома.
- Атомная масса , представляющая собой общий вес протонов, нейтронов и электронов в данном атоме. Иногда это может варьироваться, если есть изотопы элемента, поэтому атомная масса, указанная в периодической таблице, является средним значением этих различных весов. ( Примечание. Как правило, эти атомные массы в квадратных скобках означают, что число является оценочным. Элементы в этих скобках очень нестабильны или недавно открыты .)
- химическое вещество s символ , который представляет собой 1- или 2-буквенный код, который ученые используют для элемента.
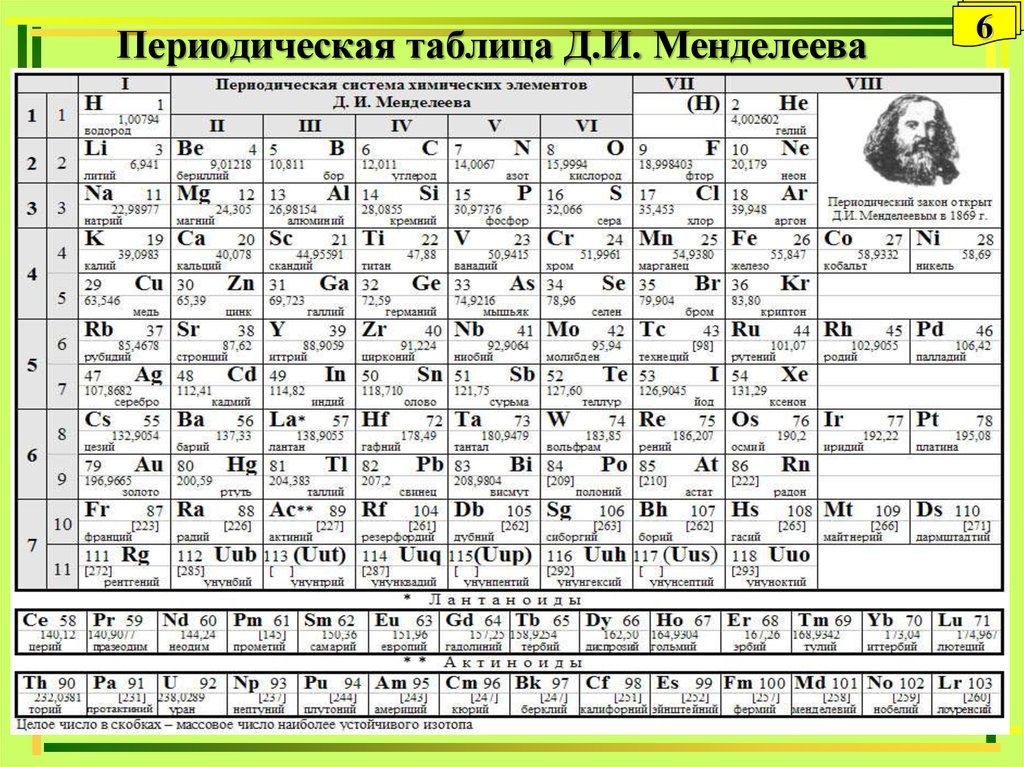 Этот кодекс принят на международном уровне для устранения языковых барьеров при обсуждении химических соединений. Некоторые из них просты, например, O для кислорода; некоторые имеют меньший смысл, например Pb для свинца. Это связано с тем, что символ обычно основан на латинском названии элемента, которое в случае свинца Plumbum . Химики используют символ элемента, когда говорят о нем в соединении или уравнении, поэтому их важно знать.
Этот кодекс принят на международном уровне для устранения языковых барьеров при обсуждении химических соединений. Некоторые из них просты, например, O для кислорода; некоторые имеют меньший смысл, например Pb для свинца. Это связано с тем, что символ обычно основан на латинском названии элемента, которое в случае свинца Plumbum . Химики используют символ элемента, когда говорят о нем в соединении или уравнении, поэтому их важно знать.
При движении слева направо по таблице атомный номер и атомная масса элемента увеличиваются. То же самое верно, когда вы путешествуете по периодической таблице.
Первоначальная таблица Менделеева была создана русским химиком Дмитрием Менделеевым. Он написал ее почти за 30 лет до того, как Томсон открыл электрон, почти за 45 лет до того, как Резерфорд открыл ядро атома, и более чем за 50 лет до того, как ученые определили, что ядро атома составляют протон и нейтрон!
Менделеев предложил примитивную версию современной таблицы Менделеева, когда писал учебник по общей химии.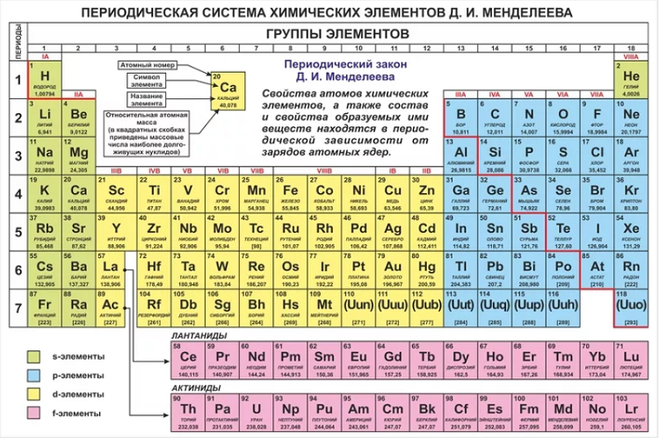 В ходе своих исследований он был поражен тем фактом, что химические свойства элементов меняются в зависимости от атомной массы, поэтому он составил таблицу, чтобы показать эти отношения.
В ходе своих исследований он был поражен тем фактом, что химические свойства элементов меняются в зависимости от атомной массы, поэтому он составил таблицу, чтобы показать эти отношения.
Периодическая таблица Менделеева 1871 года, фото
Гениально, он оставил пробелы для элементов, которые еще не были открыты, и даже зашел так далеко, что предсказал свойства этих отсутствующих элементов. И что удивительно, когда эти элементы были наконец открыты, их свойства оказались очень похожими на то, что предсказывал Менделеев!
Несмотря на то, что наша современная таблица несколько отличается от того, что нарисовал Менделеев, мы все же отдаем ему должное за первоначальную идею периодической таблицы.
Вот как мы делим периодическую таблицу на протяжении многих лет:
- В начальных классах я ввожу идею периодической таблицы вместе с упрощенным представлением о группах.
- В средней школе я учу основным отношениям, которые может показать нам периодическая таблица, наряду с периодами и группами.
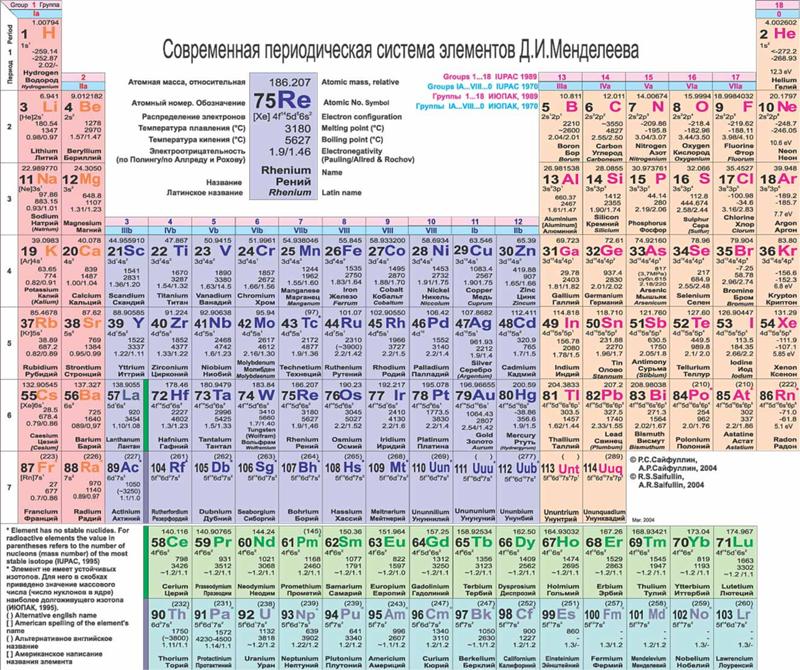
- И, наконец, в старшей школе учащийся может сосредоточиться на изучении химических принципов и математики , которые показывает нам таблица Менделеева.
Преподавание основ химии таким образом позволяет нашим учащимся узнавать об элементах и периодической таблице на том уровне, который они поймут по мере того, как будут строить ее на протяжении многих лет.
Вы можете неформально познакомиться с периодической таблицей с помощью книг, а затем использовать игры, чтобы помочь своим ученикам изучить включенные элементы, или вы можете выбрать более формальное изучение химии, используя заранее запланированную программу. Ниже приведены несколько вариантов, которые мы использовали на пути к домашнему обучению.
Следующие книги являются одними из моих любимых, чтобы узнать больше о периодической таблице:
*( Приведенные выше ссылки являются партнерскими ссылками. Периодическая таблица:
- Сопоставление периодической таблицы {Бесплатная загрузка}
- Periodic Table Battleship {Инструкции по настройке и игре в игре приведены в связанном посте.
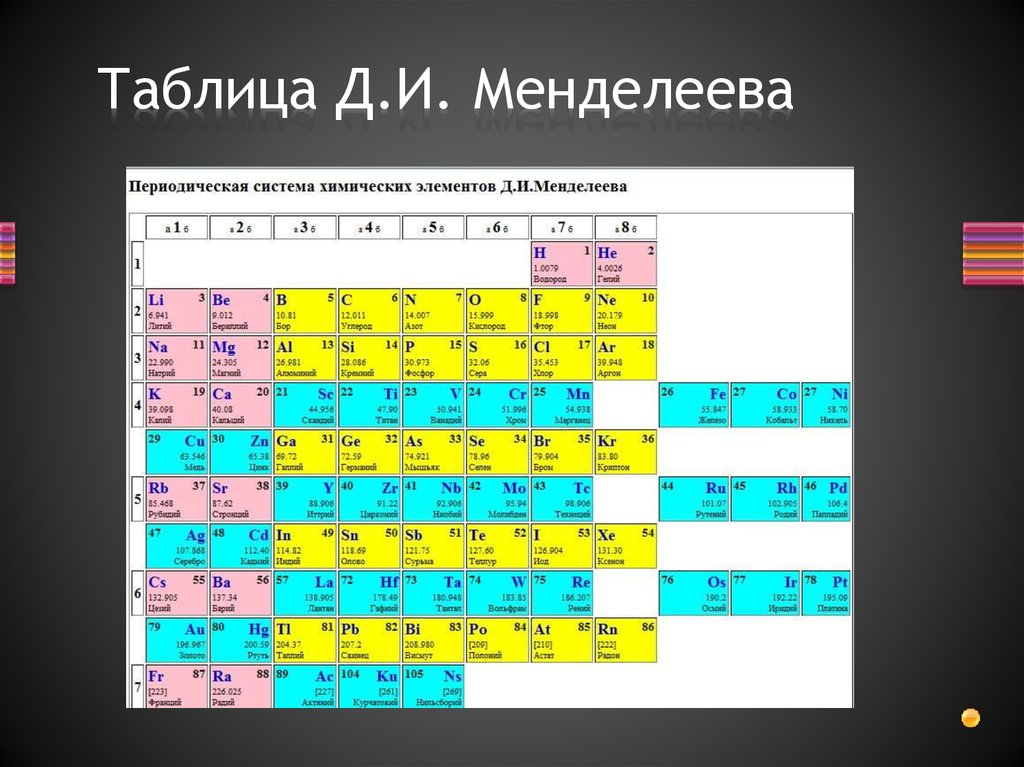 Вот бесплатная таблица Менделеева, которую вы можете использовать в игре.}
Вот бесплатная таблица Менделеева, которую вы можете использовать в игре.}
А чтобы помочь вашим детям запомнить таблицу Менделеева, вот песенка:
- Песня Периодической таблицы {обновлено в 2018 г.}
Наконец, если вы решите использовать программу, чтобы узнать больше о периодической таблице, мы предлагаем следующие программы, чтобы помочь вам:
- Лапбукинг по периодической таблице
- Химия для грамматики
- Химия для логической стадии
- Химия средней школы
Независимо от того, как вы решите поделиться таблицей Менделеева со своими учениками, это поможет им лучше понять химию и глубже понять элементы, из которых состоит мир вокруг нас!
Электронная структура и периодическая таблица – Введение в химию – 1-е канадское издание
Глава 8. Электронная структура
- Свяжите электронные конфигурации элементов с формой таблицы Менделеева.
- Определите ожидаемую электронную конфигурацию элемента по его месту в периодической таблице.

В главе 3 «Атомы, молекулы и ионы» мы представили периодическую таблицу как инструмент для систематизации известных химических элементов. Периодическая таблица показана на рисунке 8.5 «Периодическая таблица». Элементы перечислены по атомному номеру (количеству протонов в ядре), а элементы со схожими химическими свойствами сгруппированы в столбцы.
Рисунок 8.5 «Периодическая таблица». Просмотр доступной периодической таблицы в Интернете.Почему таблица Менделеева имеет такую структуру? Ответ довольно прост, если вы понимаете электронные конфигурации: форма таблицы Менделеева имитирует заполнение подоболочек электронами .
Начнем с H и He. Их электронные конфигурации 1 с 1 и 1 с 2 соответственно; He заполняется оболочка n = 1. Эти два элемента составляют первую строку периодической таблицы (см. рис. 8.6).0515 с Подоболочка»).
Рисунок 8.6 «Подоболочка 1 s ». H и He представляют заполнение подоболочки 1 s .
Следующие два электрона для Li и Be перейдут на подоболочку 2 s . Рисунок 8.7 «Подоболочка 2 s » показывает, что эти два элемента расположены рядом в периодической таблице.
Рисунок 8.7 «Подоболочка 2 с ». В Li и Be заполняется подоболочка 2 s .Для следующих шести элементов 2 p 9Подоболочка 0731 занята электронами. В правой части периодической таблицы эти шесть элементов (от B до Ne) сгруппированы вместе (рис. 8.8 «Подоболочка 2 p »).
Рисунок 8.8 «Подоболочка 2 p ». Для B до Ne занята подоболочка 2 p .Следующей подлежащей заполнению подоболочкой является подоболочка 3 s . Элементы, когда эта подоболочка заполняется, Na и Mg, возвращаются в левую часть таблицы Менделеева (рис. 8.9).0728 с Подоболочка»).
Рисунок 8.9 «Подоболочка 3 s ». Сейчас подоболочка 3 s занята. Затем подоболочка 3 p заполняется следующими шестью элементами (рис. 8.10 «Подоболочка 3 p »).
Вместо заполнения следующей подоболочки 3 d электроны переходят в подоболочку 4 s , состоящую из K и Ca (рис. 8.11 «4 с Подоболочка»).
Рисунок 8.11 «Подоболочка 4 s ». Подоболочка 4 s заполняется перед подоболочкой 3 d . Это отражено в структуре периодической таблицы.После заполнения подоболочки 4 s подоболочка 3 d заполняется до 10 электронами. Это объясняет секцию из 10 элементов в середине таблицы Менделеева, состоящую из Sc и Zn (рис. 8.12 «Подоболочка 3 d »).
Рисунок 8.12 «3 d Подоболочка». Подоболочка 3 d заполнена в средней части периодической таблицы.И так далее. Когда мы просматриваем строки периодической таблицы, общая форма таблицы показывает, как электроны занимают оболочки и подоболочки.
Первые два столбца в левой части таблицы Менделеева занимают подоболочки s . Из-за этого первые два столбца периодической таблицы помечены как . Точно так же – шесть самых правых столбцов периодической таблицы, – 10 средних столбцов периодической таблицы, а – 14-столбцовый раздел, который обычно изображается отделенным от основной части периодической таблицы. Она могла бы быть частью основной части, но тогда таблица Менделеева была бы довольно длинной и громоздкой. На рис. 8.13 «Блоки периодической таблицы» показаны блоки периодической таблицы.
Из-за этого первые два столбца периодической таблицы помечены как . Точно так же – шесть самых правых столбцов периодической таблицы, – 10 средних столбцов периодической таблицы, а – 14-столбцовый раздел, который обычно изображается отделенным от основной части периодической таблицы. Она могла бы быть частью основной части, но тогда таблица Менделеева была бы довольно длинной и громоздкой. На рис. 8.13 «Блоки периодической таблицы» показаны блоки периодической таблицы.
Электроны в оболочке с наибольшим номером плюс любые электроны в последней незаполненной подоболочке называются ; оболочка с наибольшим номером называется . (Внутренние электроны называются остовными электронами .) Валентные электроны в значительной степени контролируют химию атома. Если мы посмотрим только на электронную конфигурацию валентной оболочки, мы обнаружим, что в каждом столбце электронная конфигурация валентной оболочки одинакова. Например, возьмем элементы в первом столбце периодической таблицы: H, Li, Na, K, Rb и Cs. Их электронные конфигурации (сокращенно для более крупных атомов) следующие, с выделенной электронной конфигурацией валентной оболочки:
Например, возьмем элементы в первом столбце периодической таблицы: H, Li, Na, K, Rb и Cs. Их электронные конфигурации (сокращенно для более крупных атомов) следующие, с выделенной электронной конфигурацией валентной оболочки:
| Элемент | Электронная конфигурация |
|---|---|
| Н | 1 с 1 |
| Ли | 1 с 2 2 с 1 |
| Нет данных | [Ne]3 с 1 |
| К | [Ar]4 с 1 |
| Руб | [Кр]5 с 1 |
| Цс | [Хе]6 с 1 |
Все они имеют одинаковую электронную конфигурацию в своих валентных оболочках: один s электрон. Поскольку большая часть химического состава элемента находится под влиянием валентных электронов, мы ожидаем, что эти элементы будут иметь схожий химический состав — , а они . Организация электронов в атомах объясняет не только форму таблицы Менделеева, но и тот факт, что элементы в одном и том же столбце таблицы Менделеева имеют схожий химический состав.
Поскольку большая часть химического состава элемента находится под влиянием валентных электронов, мы ожидаем, что эти элементы будут иметь схожий химический состав — , а они . Организация электронов в атомах объясняет не только форму таблицы Менделеева, но и тот факт, что элементы в одном и том же столбце таблицы Менделеева имеют схожий химический состав.
То же самое относится и к другим столбцам таблицы Менделеева. Элементы в каждом столбце имеют одинаковую конфигурацию электронов валентной оболочки, а также некоторые химические свойства элементов. Это строго верно для всех элементов в блоках s и p . В блоках d и f из-за исключения порядка заполнения подоболочек электронами подобные валентные оболочки в этих блоках не являются абсолютными. Однако в этих блоках действительно существует много общего, поэтому ожидается сходство в химических свойствах.
Сходство электронной конфигурации валентной оболочки означает, что мы можем определить электронную конфигурацию атома исключительно по его положению в периодической таблице. Рассмотрим Se, как показано на рис. 8.14 «Селен в периодической таблице». Он находится в четвертом столбце блока p . Это означает, что его электронная конфигурация должна заканчиваться электронной конфигурацией p 4 . Действительно, электронная конфигурация Se такова: [Ar]4 s 2 3 d 10 4 p 4 , как и ожидалось.
Рассмотрим Se, как показано на рис. 8.14 «Селен в периодической таблице». Он находится в четвертом столбце блока p . Это означает, что его электронная конфигурация должна заканчиваться электронной конфигурацией p 4 . Действительно, электронная конфигурация Se такова: [Ar]4 s 2 3 d 10 4 p 4 , как и ожидалось.
По положению элемента в периодической таблице предскажите конфигурацию электрона валентной оболочки для каждого атома. См. рис. 8.15 «Различные элементы периодической таблицы».
- Ca
- Сн
Solution
- Ca находится во втором столбце блока s . Мы ожидаем, что его электронная конфигурация должна заканчиваться на с 2 . Электронная конфигурация кальция [Ar]4 s 2 .
- Sn расположен во втором столбце блока p , поэтому мы ожидаем, что его электронная конфигурация будет заканчиваться на p 2 .
 Электронная конфигурация олова: [Kr]5 s 2 4 d 10 5 p 2 .
Электронная конфигурация олова: [Kr]5 s 2 4 d 10 5 p 2 .
По положению элемента в периодической таблице предскажите конфигурацию электрона валентной оболочки для каждого атома. См. рисунок 8.15.
- Ти
- Кл
Ответ
- [Ar]4 s 2 3 d 2
- [Ne]3 с 2 3 р 5
Цвет объектов зависит от механизма, отличного от цвета неона и других газоразрядных ламп. Хотя цветные огни производят свои цвета, объекты окрашены, потому что они предпочтительно отражают определенный цвет от падающего на них белого света. Красный помидор, например, ярко-красный, потому что отражает красный свет, поглощая при этом все остальные цвета радуги.
Многие продукты, такие как помидоры, сильно окрашены; на самом деле, распространенное утверждение «сначала вы едите глазами» является имплицитным признанием того, что внешняя привлекательность еды так же важна, как и ее вкус. Но как насчет обработанных пищевых продуктов?
Но как насчет обработанных пищевых продуктов?
Во многие обработанные пищевые продукты добавляются пищевые красители. Пищевые красители бывают двух видов: натуральные и искусственные. Натуральные пищевые красители включают карамелизированный сахар для коричневого цвета; аннато, куркума и шафран для различных оттенков оранжевого или желтого; бетанин из свеклы для фиолетового; и даже кармин, темно-красный краситель, который извлекают из кошенили, небольшого насекомого, паразитирующего на кактусах в Центральной и Южной Америке. (Правильно: возможно, вы едите сок жуков!)
Некоторые красители являются искусственными. В Соединенных Штатах Управление по санитарному надзору за качеством пищевых продуктов и медикаментов в настоящее время утверждает только семь соединений в качестве искусственных красителей в продуктах питания, напитках и косметике:
- FD&C Blue #1: Brilliant Blue FCF
- FD&C Blue #2: индиготин
- FD&C Green #3: Fast Green FCF
- RD&C Red #3: Эритрозин
- FD&C Красный #40: Allura Red AC
- FD&C Желтый #5: Тартразин
- FD&C Желтый #6: Желтый закат FCF
Цвета с меньшими номерами больше не продаются или были удалены по разным причинам.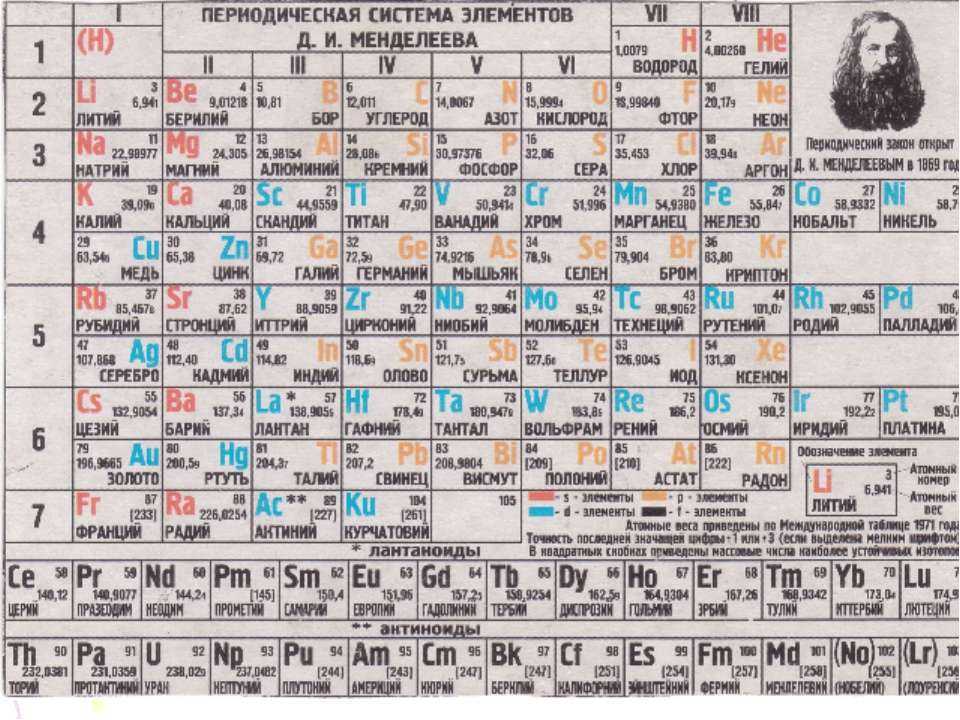 Как правило, эти искусственные красители представляют собой большие молекулы, которые очень сильно поглощают определенные цвета света, что делает их полезными даже при очень низких концентрациях в продуктах питания и косметике. Некоторые критики утверждают, что даже в таких малых количествах небольшая часть населения (особенно дети) чувствительна к искусственным красителям, и призывают сократить или прекратить их использование. Однако формальные исследования искусственных красителей и их влияния на поведение были безрезультатными или противоречивыми. Несмотря на это, большинству людей по-прежнему нравятся обработанные пищевые продукты с искусственными красителями (такие, как показаны на прилагаемом рисунке).
Как правило, эти искусственные красители представляют собой большие молекулы, которые очень сильно поглощают определенные цвета света, что делает их полезными даже при очень низких концентрациях в продуктах питания и косметике. Некоторые критики утверждают, что даже в таких малых количествах небольшая часть населения (особенно дети) чувствительна к искусственным красителям, и призывают сократить или прекратить их использование. Однако формальные исследования искусственных красителей и их влияния на поведение были безрезультатными или противоречивыми. Несмотря на это, большинству людей по-прежнему нравятся обработанные пищевые продукты с искусственными красителями (такие, как показаны на прилагаемом рисунке).
- Расположение электронов в атомах определяет форму таблицы Менделеева.

- Конфигурации электронов можно предсказать по положению атома в периодической таблице.
- Где в периодической таблице s подоболочек заняты электронами?
- Где в периодической таблице находятся d подоболочек, занятых электронами?
- В каком блоке находится Ра?
- В каком блоке находится Br?
- Каковы конфигурации электронов валентной оболочки элементов во втором столбце периодической таблицы?
- Каковы конфигурации электронов валентной оболочки элементов предпоследнего столбца периодической таблицы?
- Каковы электронные конфигурации валентных оболочек элементов в первом столбце блока p ?
- Каковы электронные конфигурации валентных оболочек элементов в последнем столбце блока p ?
- По положению элемента в периодической таблице предскажите электронную конфигурацию каждого из следующих атомов:
- Старший
- С
- По положению элемента в периодической таблице предскажите электронную конфигурацию каждого из следующих атомов:
- Fe
- Ба
- По положению элемента в периодической таблице предскажите электронную конфигурацию каждого из следующих атомов:
- В
- Ар
- По положению элемента в периодической таблице предскажите электронную конфигурацию каждого из следующих атомов:
- Класс
- К
- По положению элемента в периодической таблице предскажите электронную конфигурацию каждого из следующих атомов:
- Ge
- С
- По положению элемента в периодической таблице предскажите электронную конфигурацию каждого из следующих атомов:
- мг
- я
- первые два столбца
- с блок
- нс 2
- нс 2 нп 1
- 1 s 2 2 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 10 4 р 6 5 с 2
- 1 S 2 2 S 2 2 P 6 3 S 2 3 P 40248 40248 40248 40248 40248 40248 40248 40248 40248 40248 40248 40248 402448 402448 402448 4.
 4. 402448 4. 4. 2 3 .
4. 402448 4. 4. 2 3 .
- 1 s 2 2 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 3
- 1 S 2 2 S 2 2 P 6 3 S 2 3 P 40248 40248 40248 40248 40248 40248 4. 2 2 3 .
- 1 с 2 2 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 10 4 p 2
- 1 с 2 2 с 2 2 р 2
Описание рисунка 8. 15: Различные элементы периодической таблицы.
15: Различные элементы периодической таблицы.
Ca (кальций) находится во втором столбце слева и в четвертой строке.
Ti (титан) находится в четвертой колонке слева и четвертой строке.
Cl (хлор) находится во второй колонке справа и второй строке.
Sn (олово) находится в пятой колонке справа и в пятой строке.
[Вернуться к рис. 8.15]
Атрибуция СМИ
- «Периодическая таблица» Дэвида Болла © CC BY-NC-SA (Attribution NonCommercial ShareAlike)
- «Подоболочка 1 s » Дэвида В. Болла © CC BY-NC-SA (Attribution NonCommercial ShareAlike)
- «The 2 s Subshell» Дэвида В. Болла © CC BY-NC-SA (Attribution NonCommercial ShareAlike)
- «The 2 p Subshell» Дэвида В. Болла © CC BY-NC-SA (Attribution NonCommercial ShareAlike)
- «Подоболочка 3 s » Дэвида В. Болла © CC BY-NC-SA (Attribution NonCommercial ShareAlike)
- «The 3 p Subshell» Дэвида В.

