Латинские названия химических элементов – произношение на русском языке
Чтобы понимать, как правильно произносить названия химических элементов таблицы Менделеева, необходимо выучить несколько важных правил:
1. Химические элементы в периодической таблице обозначаемые одной буквой, читаются по первой букве из латинского названия, например, химический элемент “Углерод”, химический знак которого буква “С”, значит и читаться будет по этой букве, а именно “Це”.
Исключением в данном правиле являются химические элементы: Бор (B), Фтор (F), Калий (K) и Йод (I), которые соответствуют названию химического элемента на русском языке.
2. Некоторые химические элементы, обозначаемые двумя буквами, читаются в соответствии с названием химического элемента на латинском языке, например, неорганическое вещество сульфат серебра AgSO4, читается как: “аргентум эс о 4”.
3. Несмотря на огромное количество химических элементов, запомнить правильное произношение не сложно, потому как большинство из них произносятся также, как и пишется на русском языке, за исключением 16 элементов, которые приведены в таблице ниже. Таблицу можно скачать и сохранить как памятку.
Таблица исключений с правильным произношением химических элементов на русском языке
| АТОМНЫЙ НОМЕР |
РУССКОЕ НАЗВАНИЕ ХИМИЧЕСКОГО ЭЛЕМЕНТА
| ХИМИЧЕСКИЙ ЗНАК | ПРОИЗНОШЕНИЕ НА РУССКОМ ЯЗЫКЕ |
| 1 | Водород | H | Аш |
| 6 | Углерод | C | Це |
| 7 | Азот | N | Эн |
| 8 | Кислород | O | О |
| Кремний | Si | Силициум | |
| 15 | Фосфор | P | Пэ |
| 16 | Сера | S | Эс |
| 26 | Железо | Fe | Феррум |
| 29 | Медь | Cu | Купрум |
| 33 | Мышьяк | As | Арсеникум |
| 47 | Серебро | Ag | Аргентум |
| 50 | Олово | Sn | Станум |
| 51 | Сурьма | Sb | Стибиум |
| 79 | Au | Аурум | |
| 80 | Ртуть | Hg | Гидраргирум |
| 82 | Свинец | Pb | Плюмбум |
Примечание: произношение остальных химических элементов соответствует названию элементов на русском языке (пример: аргон произносится как аргон, хром произносится как хром и т.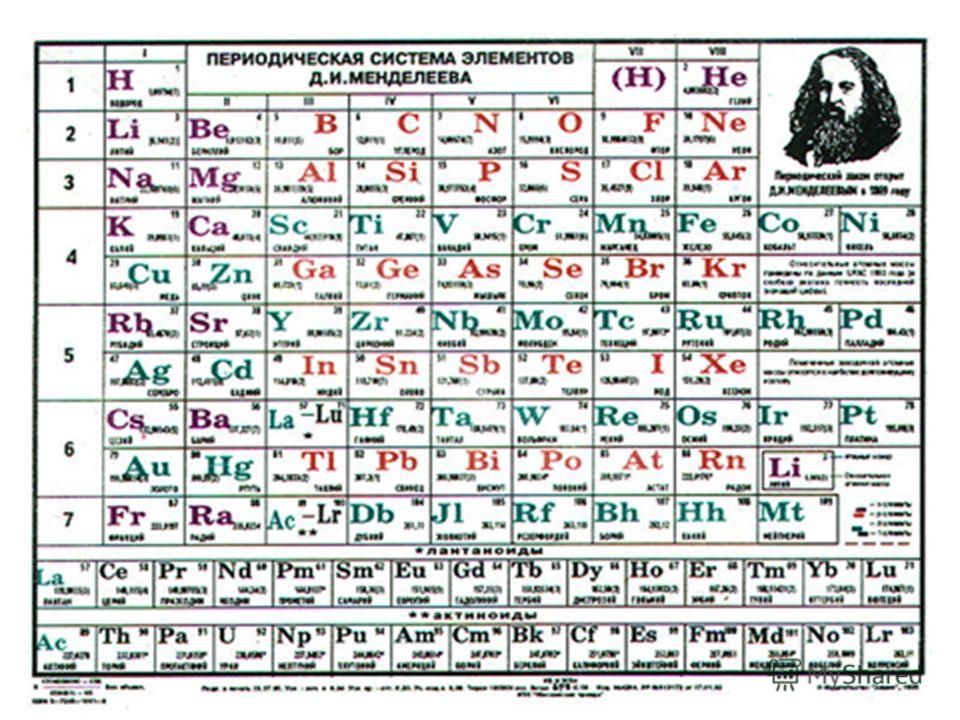 д.) д.) |
|||
Скачать таблицу в хорошем качестве по ссылке: скачать таблицу
В таблице ниже описаны произношения всех известных на данный момент химических элементов.
Полная таблица латинских названий химических элементов с произношением на русском языке
(расположение слоев в порядке заполнения подуровней)
| Атомный номер | Русское название химического элемента | Латинское название химического элемента | Химический знак | Произношение на русском языке |
| 1 | водород | hydrogenium | H | аш |
| 2 | гелий | helium | He | гелий |
| 2 период химических элементов | ||||
| 3 | литий | lithium | Li | литий |
| 4 | бериллий | beryllium | Be | бериллий |
| 5 | бор | B | бор | |
| 6 | углерод | carboneum | C | це |
| 7 | азот | nitrogenium | N | эн |
| 8 | кислород | oxygenium | O | о |
| 9 | фтор | fluorum | F | фтор |
| неон | neon | Ne | неон | |
| 3 период химических элементов | ||||
| 11 | натрий | natrium | Na | натрий |
| 12 | магний | magnesium | Mg | магний |
| 13 | алюминий | aluminium | Al | алюминий |
| кремний | silicium | Si | силициум | |
| 15 | фосфор | phosphorus | P | пэ |
| 16 | сера | sulfur | S | эс |
| 17 | хлор | clorum | Cl | хлор |
| 18 | аргон | argon | Ar | аргон |
| 19 | калий | kalium | K | калий |
| 20 | кальций | calcium | Ca | кальций |
| 21 | скандий | scandium | Sc | скандий |
| 22 | титан | titanium | Ti | титан |
| 23 | ванадий | vanadium | V | ванадий |
| 24 | хром | chromium | Cr | хром |
| 25 | марганец | manganum | Mn | марганец |
| 26 | железо | ferrum | Fe | феррум |
| 27 | кобальт | cobaltum | Co | кобальт |
| 28 | никель | niccolum | Ni | никель |
| 29 | медь | cuprum | Cu | купрум |
| 30 | цинк | zincum | Zn | цинк |
| 31 | галий | gallium | Ga | галий |
| 32 | германий | germanium | Ge | германий |
| 33 | мышьяк | arsenicum | As | арсеникум |
| 34 | селен | selenium | Se | селен |
| 35 | бром | bromum | Br | бром |
| 36 | криптон | krypton | Kr | криптон |
| 5 период химических элементов | ||||
| 37 | рубидий | rubidium | Rb | рубидий |
| 38 | стронций | strontium | Sr | стронций |
| 39 | иттрий | yttrium | Y | иттрий |
| 40 | цирконий | zirconium | Zr | цирконий |
| 41 | ниобий | niobium | Nb | ниобий |
| 42 | молибден | molybdaenum | Mo | молибден |
| 43 | технеций | technetium | Tc | технеций |
| 44 | рутений | ruthenium | Ru | рутений |
| 45 | родий | rhodium | Rh | родий |
| 46 | палладий | palladium | Pd | палладий |
| 47 | серебро | argentum | Ag | аргентум |
| 48 | кадмий | cadmium | Cd | кадмий |
| 49 | индий | indium | In | индий |
| 50 | олово | stannum | Sn | станум |
| 51 | сурьма | stibium | Sb | стибиум |
| 52 | теллур | tellurium | Te | теллур |
| 53 | йод | iodum | I | йод |
| 54 | ксенон | xenon | Xe | ксенон |
| 6 период химических элементов | ||||
| 55 | цезий | ceslum | Cs | цезий |
| 56 | барий | barlum | Ba | барий |
| 57 | лантан | lanthanum | La | лантан |
| 58 | церий | cerium | Ce | церий |
| 59 | празеодим | praseodymium | Pr | празеодим |
| 60 | неодим | neodymium | Nd | неодим |
| 61 | прометий | promethium | Pm | прометий |
| 62 | самарий | samarium | Sm | самарий |
| 63 | европий | europium | Eu | эвропий |
| 64 | гадолиний | gadolinium | Gd | гадолиний |
| 65 | тербий | terbium | Tb | тербий |
| 66 | диспрозий | dysprosium | Dy | диспрозий |
| 67 | гольмий | holmium | Ho | гольмий |
| 68 | эрбий | erbium | Er | эрбий |
| 69 | тулий | thulium | Tm | тулий |
| 70 | иттербий | ytterbium | Yb | иттербий |
| 71 | лютеций | lutetium | Lu | лютеций |
| 72 | гафний | hafnium | Hf | гафний |
| 73 | тантал | tantalum | Ta | тантал |
| 74 | вольфрам | wolframium | W | вольфрам |
| 75 | рений | rhenium | Re | рений |
| 76 | осмий | osmium | Os | осмий |
| 77 | иридий | iridium | Ir | иридий |
| 78 | платина | platinum | Pt | платины |
| 79 | золото | aurum | Au | аурум |
| 80 | ртуть | hydrargyrum | Hg | гидраргирум |
| 81 | таллий | thallium | Tl | таллий |
| 82 | свинец | plumbum | Pb | плюмбум |
| 83 | висмут | bismuthum | Bi | висмут |
| 84 | полоний | polonium | Po | полоний |
| 85 | астат | astatium | At | астата |
| 86 | радон | radon | Rn | радон |
| 7 период химических элементов | ||||
| 87 | франций | francium | Fr | франций |
| 88 | радий | radium | Ra | радий |
| 89 | актиний | actinium | Ac | актиний |
| 90 | торий | thorium | Th | торий |
| 91 | протактиний | protactinium | Pa | протактиний |
| 92 | урана | uranium | U | уран |
| 93 | нептуний | neptunium | Np | нептуний |
| 94 | плутоний | plutonium | Pu | плутоний |
| 95 | америций | americium | Am | америций |
| 96 | кюрий | curium | Cm | кюрий |
| 97 | берклий | berkelium | Bk | берклий |
| 98 | калифорний | californium | Cf | калифорний |
| 99 | эйнштейний | einsteinium | Es | эйнштейний |
| 100 | фермий | fermium | Fm | фермий |
| 101 | менделеевий | mendelevium | Md | менделеевий |
| 102 | нобелий | nobelium | No | нобелий |
| 103 | лоуренсий | lawrencium | Lr | лоуренсий |
| 104 | резерфордий | rutherfordium | Rf | резерфордий |
| 105 | дубний | dubnium | Db | дубний |
| 106 | сиборгий | seaborgium | Sg | сиборгий |
| 107 | борий | bohrium | Bh | борий |
| 108 | хассий | hassium | Hs | хассий |
| 109 | мейтнерий | meitnerium | Mt | мейтнерий |
| 110 | Дармштадтий (Унуннилий) | Darmstadtium (Ununnilium) | Ds (Uun) | дармштадий |
| 111 | Рентгений (Унунуний) | Roentgenium (Unununium) | Rg (Uuu) | рентгений |
| 112 | Коперниций (Унунбий) | Copernicium (Ununbium) | Cn (Uub) | коперниций |
| 113 | Нихоний (Унунтрий) | Nihonium (Ununtrium) | Nt (Unt) | нихоний |
| 114 | Флеровий (Унунквадий) | Flerovium (Ununquadium) | Fl (Uuq) | флеровий |
| 115 | Московий (Унунпентий) | Moscovium (Ununpentium) | Mc (Uup) | московий |
| 116 | Ливерморий (Унунгексий) | Livermorium (Ununhexium) | Lv (Uuh) | ливерморий |
| 117 | Теннессин (Унунсептий) | Tennessine (Ununseptium) | Тc (Uus) | теннессин |
| 118 | Оганесон (Унуноктий) | Oganesson (Ununoctium) | Og (Uuo) | оганесон |
| 8 период химических элементов | ||||
| 119 | унуненний | ununnenium | Uue | |
| 120 | унбинилий | unbinilium | Ubn | |
| 121 | унбиуний | unbiunium | Ubu | |
| 122 | унбибий | unbibium | Ubb | |
| 123 | унбитрий | unbitrium | Ubt | |
| 124 | унбиквадий | unbiquadium | Ubq | |
| 125 | унбипентий | unbipentium | Ubp | |
| 126 | унбигексий | unbihexium | Ubh | |
“РГ” нашла 7 легенд о названиях химических элементов — Российская газета
27 августа 1875 года французский ученый Поль Эмиль Лекок де Буабодран открыл элемент системы Менделеева, который был назван галлием.
Считается, что это наименование дано в честь родины химика – Франции (на латыни – Галлия). Однако есть и другая версия, куда более интересная. Якобы Лекок де Буабодран решил увековечить заодно и свою фамилию – Lecoq. Дело в том, что в переводе с французского le coq означает “петух”, а на латинском это звучит не иначе как gallus.
“РГ” нашла еще семь интересных историй, связанных с названиями химических элементов.
Азот
По наиболее распространенной версии это название предложил основатель современной химии, француз Антуан Лавуазье, который приоритетным свойством азота посчитал то, что этот газ не поддерживает горения и не пригоден для дыхания. И выбрал для его названия древнегреческое слово “безжизненный”, которое очень похоже на современное “азот”. Хотя позже ученые доказали, что азот необходим живым существам и входит в состав любого белка и нуклеиновой кислоты, это наименование сохранилось.
Однако есть мнение, что слово “азот” появилось задолго до Лавуазье. Еще в средневековье алхимики употребляли его, обозначая “первичную материю металлов”. Она считалась началом и концом всего живого. А потому “азот” – не что иное как аббревиатура, составленная из первых и последних букв трех священных языков – латинского, греческого и древнееврейского: “а”, “альфа”, “алеф”, “зет”, “омега” и “тав” (aaazoth).
Еще в средневековье алхимики употребляли его, обозначая “первичную материю металлов”. Она считалась началом и концом всего живого. А потому “азот” – не что иное как аббревиатура, составленная из первых и последних букв трех священных языков – латинского, греческого и древнееврейского: “а”, “альфа”, “алеф”, “зет”, “омега” и “тав” (aaazoth).
Есть ученые, которые говорят и об арабском происхождении слова – “аззат” означает “сущность” или “внутренняя реальность”.
Впрочем, азот азотом называют далеко не везде – это слово устоялось в русском, французском, итальянском, турецком и некоторых других языках. В большинстве же случаев седьмой элемент таблицы Менделеева называют латинским словом nitrogenium (“рождающий селитру”) или производными от него.
Неон
Название “неон” для элемента, открытого шотландским химиком Уильямом Рамзаем и его английским коллегой Морисом Траверсом, придумал сын шотландца, 13-летний Вилли. Он якобы спросил у отца, как тот назовет новый газ.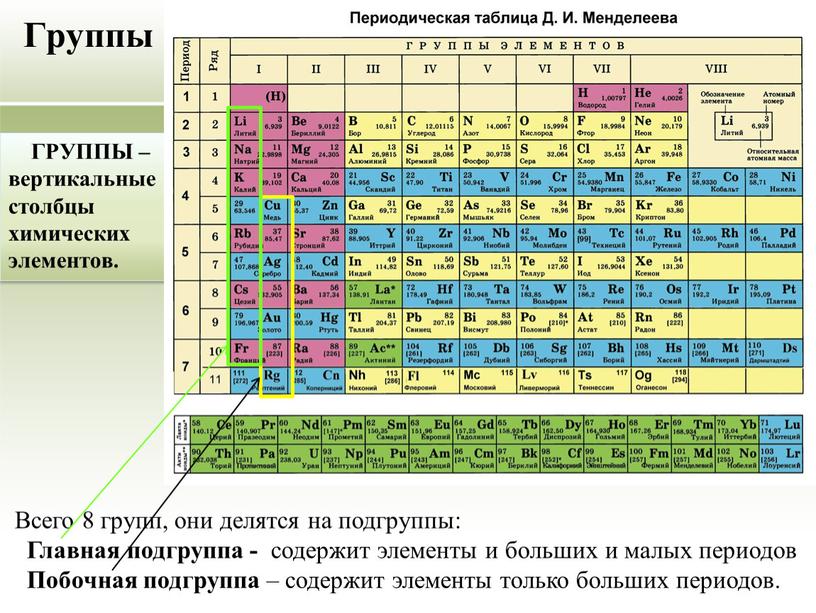 В разговоре всплыло, что если уж вещество действительно новое, то и имя ему подойдет novum (с латыни – “новый”). Отец согласился, но убедил сына, что более красивым будет аналог из греческого языка – neon.
В разговоре всплыло, что если уж вещество действительно новое, то и имя ему подойдет novum (с латыни – “новый”). Отец согласился, но убедил сына, что более красивым будет аналог из греческого языка – neon.
Никель
В средневековье саксонские горняки просто замучились, пытаясь получить из добываемого ими никеля медь – уж больно никелевая руда походила на медную. Но все попытки заканчивались неудачей. Случались порой и отравления мышьяковыми газами, которые выделялись при выплавке. А потому никель в то время применяли только в стекловарении – благодаря ему стекла можно было красить в зеленый цвет.
Отчаявшиеся рудокопы “в отместку” стали называть этот материал Kupfernickel, что можно перевести как “медный дьявол”. Вторая часть слова – nickel – у шахтеров было ругательством и образовалось от слова Nicolaus, которым обозначали двуличных людей, “обманчивых бездельников”.
Кобальт
Похожим образом название получил и этот химический элемент. Правда, тут роль отчаявшихся горняков сыграли не саксонцы, а норвежцы. Они также нередко травились летучим оксидом мышьяка, пытаясь выплавить что-то из добываемой ими руды. В итоге минералам присвоили имя горного духа Кобольда. Хотя в Северной Европе так нередко называли добродушных домовых и эльфов, шахтеры недолюбливали подземных кобольдов за порчу руды.
Они также нередко травились летучим оксидом мышьяка, пытаясь выплавить что-то из добываемой ими руды. В итоге минералам присвоили имя горного духа Кобольда. Хотя в Северной Европе так нередко называли добродушных домовых и эльфов, шахтеры недолюбливали подземных кобольдов за порчу руды.
Тантал
Английский химик Чарлз Хатчет в 1801 году обнаружил в хранившемся в Британском музее черном минерале оксид неизвестного элемента. Ученый назвал его колумбитом, в честь открытой знаменитым путешественником страны, ставшей в последствии США, где и был найден этот камень в 1635 году.
Однако еще через год опытами с тем же минералом занялся швед Андерс Экеберг. Обнаруженный им другой оксид никак не хотел растворяться ни в какой кислоте. Знаменитый соотечественник Экеберга – химик Йене Якоб Берцелиус – высказался за то, чтобы назвать содержащийся в необычном оксиде металл “танталом”. Одноименный древнегреческий герой был наказан жестоким образом – стоя по горло в воде рядом с ветвями, богатыми фруктами, он не был в состоянии ни отведать плодов, ни утолить жажду. Ученому показалось, что налицо аналогия -тантал-металл тоже не мог “насытиться” жидкостью-кислотой.
Ученому показалось, что налицо аналогия -тантал-металл тоже не мог “насытиться” жидкостью-кислотой.
В последствии оказалось, что выявленный Хатчетом колумбий – это смесь тантала и сходного с ним элемента. Его было решено назвать ниобий – производным от имени дочери Тантала Ниобы.
Титан
По официальной версии, этот элемент назван открывшим его немцем Мартином Клапротом в честь одноименных персонажей древнегреческой мифологии, поскольку к концу XVIII века ученый не смог выделить какие-то ключевые характеристики нового вещества по его оксиду.
Между тем, современные химики утверждают, что Клапрот кое-что понимал в свойствах нового элемента, да и интересовался мифами не древнегреческими, а германскими. А потому, подбирая наименование своему титану, имел в виду королеву фей Титанию, поскольку хотел отметить особую “легкость” металла.
Торий
Название “торий”, придуманное в честь древнескандинавского бога Тора, знаменитый шведский химик Йене Якоб Берцелиус посчитал таким удачным, что куда только ни пытался его “пристроить”. Сначала, в 1815 году, он присвоил его элементу, который выявил в минерале из Швеции. Позже сам химик признал свою неточность – это был фосфат иттрия. Но освободившееся название пригодилось ему спустя 13 лет, когда он исследовал редкий норвежский минерал и теперь уже без какой-либо ошибки открыл новый элемент.
Сначала, в 1815 году, он присвоил его элементу, который выявил в минерале из Швеции. Позже сам химик признал свою неточность – это был фосфат иттрия. Но освободившееся название пригодилось ему спустя 13 лет, когда он исследовал редкий норвежский минерал и теперь уже без какой-либо ошибки открыл новый элемент.
Справка “РГ”
Из 118 химических элементов (ученые уверены, что смогут синтезировать еще как минимум 8 и всего их будет 126) четыре до сих пор не имеют постоянных названий. В частности, 115-й элемент именуют “унунпентий” (с латыни буквально “одно-одно-пятый”), а 118-й – “унуноктий” (“одно-одно-восьмой”).
Большинство химических элементов названы в честь географический названий (например, европий, америций, франций, рутений, по латинскому названию России – Ruthenia), фамилий ученых (Борий, Кюрий, Менделевий), выявленных свойств самих элементов (хлор – от греческого “желто-зеленый”, радий и радон – от латинского “испускающий лучи”), способам их открытия (технеций – с греческого “искусственный” – был получен путем синтеза), а также в честь богов и героев мифов.
Химические элементы. Символы химических элементов — урок. Химия, 8–9 класс.
Химический элемент — это определённый вид атомов.
Атомы разных химических элементов отличаются массой, размерами, строением и свойствами.
Каждый химический элемент имеет название и обозначается символом или химическим знаком.
Символ химического элемента состоит из одной или двух букв. Как правило, используются первые буквы его латинского названия.
Название элемента | Символ | Произношение |
| Азот | N | «эн» |
| Алюминий | Al | «алюминий» |
| Барий | Ba | «барий» |
| Бром | Br | «бром» |
| Водород | H | «аш» |
| Гелий | He | «гелий» |
| Железо | Fe | «феррум» |
| Золото | Au | «аурум» |
| Иод | I | «иод» |
| Калий | K | «калий» |
| Кальций | Ca | «кальций» |
| Кислород | O | «о» |
| Кремний | Si | «силициум» |
| Магний | Mg | «магний» |
| Медь | Cu | «купрум» |
| Натрий | Na | «натрий» |
| Сера | S | «эс» |
| Серебро | Ag | «аргентум» |
| Углерод | C | «це» |
| Фосфор | P | «пэ» |
| Фтор | F | «фтор» |
| Хлор | Cl | «хлор» |
| Цинк | Zn | «цинк» |
Названия и символы \(118\) химических элементов приведены в периодической таблице. Более \(20\) элементов получены искусственно с помощью сложных физических методов. Таблица постоянно дополняется новыми элементами.
Более \(20\) элементов получены искусственно с помощью сложных физических методов. Таблица постоянно дополняется новыми элементами.
Атомы химических элементов соединяются друг с другом в разных комбинациях и образуют огромное количество природных и синтетических веществ.
Алфавитный список химических элементов – это… Что такое Алфавитный список химических элементов?
- Алфавитный список химических элементов
Алфавитный список химических элементов.
Wikimedia Foundation. 2010.
- Дрейф
- Круизное судно
Полезное
Смотреть что такое “Алфавитный список химических элементов” в других словарях:
Список химических элементов по символам — См.
 также: Список химических элементов по атомным номерам и Алфавитный список химических элементов Содержание 1 Символы, используемые в данный момент … Википедия
также: Список химических элементов по атомным номерам и Алфавитный список химических элементов Содержание 1 Символы, используемые в данный момент … ВикипедияСписок химических элементов по атомным номерам — См. также: Список химических элементов по символам и Алфавитный список химических элементов Это список химических элементов, упорядоченный в порядке возрастания атомных номеров. В таблице приводятся название элемента, символ, группа и период в… … Википедия
ISO 4217 — (ИСО 4217) Коды для представления валют и фондов Codes for the representation of currencies and funds (англ.) Codes pour la représentation des monnaies et types de fonds (фр.) … Википедия
ЭЛЕМЕНТЫ ХИМИЧЕСКИЕ — простейшая форма материи, которая может быть идентифицирована химическими методами. Это составные части простых и сложных веществ, представляющие собой совокупность атомов с одинаковым зарядом ядра. Заряд ядра атома определяется числом протонов в … Энциклопедия Кольера
Хронология изобретений — Содержание 1 Эпоха палеолита 2 10 е тысячелетие до н.
 э. 3 9 е тысячелетие до н. э … Википедия
э. 3 9 е тысячелетие до н. э … ВикипедияИзобретения человека — Содержание 1 Эпоха палеолита 2 10 е тысячелетие до н. э. 3 9 е тысячелетие до н. э … Википедия
Изобретения — Содержание 1 Эпоха палеолита 2 10 е тысячелетие до н. э. 3 9 е тысячелетие до н. э … Википедия
Русские — У этого термина существуют и другие значения, см. Русские (значения). Русские … Википедия
1: — Терминология 1: : dw Номер дня недели. «1» соответствует понедельнику Определения термина из разных документов: dw DUT Разность между московским и всемирным координированным временем, выраженная целым количеством часов Определения термина из… … Словарь-справочник терминов нормативно-технической документации
Название химических элементов и их произношение таблица. Алфавитный список химических элементов
«Химический элемент – сера» – Природный сросток кристаллов самородной серы. Возможны молекулы с замкнутыми (S4, S6) цепями и открытыми цепями. Серные руды добывают разными способами – в зависимости от условий залегания. Природные минералы серы. Нельзя забывать о возможности ее самовозгорания. Добыча руды открытым способом. Шагающие экскаваторы снимают пласты пород, под которыми залегает руда.
Возможны молекулы с замкнутыми (S4, S6) цепями и открытыми цепями. Серные руды добывают разными способами – в зависимости от условий залегания. Природные минералы серы. Нельзя забывать о возможности ее самовозгорания. Добыча руды открытым способом. Шагающие экскаваторы снимают пласты пород, под которыми залегает руда.
«Вопросы по химическим элементам» – Могут быть стабильными и радиактивными, естественными и искуственными. Связана с изменением числа энергетических уровней в главных подгруппах. 8. Какой элемент не имеет постоянной «прописки» в Периодической системе? Находятся в постоянном движении. Теллур, 2) селен, 3) осмий, 4) германий. Где накапливается мышьяк?
«h3O и h3S» – Cульфат-ион. Y = ? K K2 =1,23 · 10?13 моль/л. Получение: Na2SO3 + S = Na2SO3S (+t, водн.р-р). В водном растворе: +Hcl (эфир). Купоросы MSO4·5(7)h3O (M – Cu, Fe, Ni, Mg …). Серная кислота h3SO4. Строение анионов SO32– и HSO3–. = y. Молекула SO3 – неполярная и диамагнитная. ? . Гидросульфит-ион: таутомерия.
«Периодическая система химических элементов» – 8. Сколько электронов максимально может находиться на третьем энергетическом уровне? Расположить элементы в порядке возрастания металлических свойств. Название страны: «Химический элементарий». Стихи Степана Щипачева. А. 17 Б. 35 В. 35,5 Г. 52 6. Сколько электронов вращается вокруг ядра в атоме фтора?
«Кальций Сa» – Соединения Ca. Химические свойства Ca. Физические свойства Ca. Кальций относится к распространенным элементам. Применение. Получение кальция в промышленности. Кальций Ca. Опишите физические свойства Ca. Нахождение в природе. Задание для повторения. Кальций Ca серебристо белый и довольно твердый металл, легкий.
«Элемент фосфор» – Фосфор занимает 12-е место по распространенности элементов в природе. Взаимодействие с простыми веществами – неметаллами. Взаимодействие с металлами. Для связывания соединений кальция добавляют кварцевый песок. При нагревании белого фосфора в растворе щелочи он диспропорционирует. Фосфор.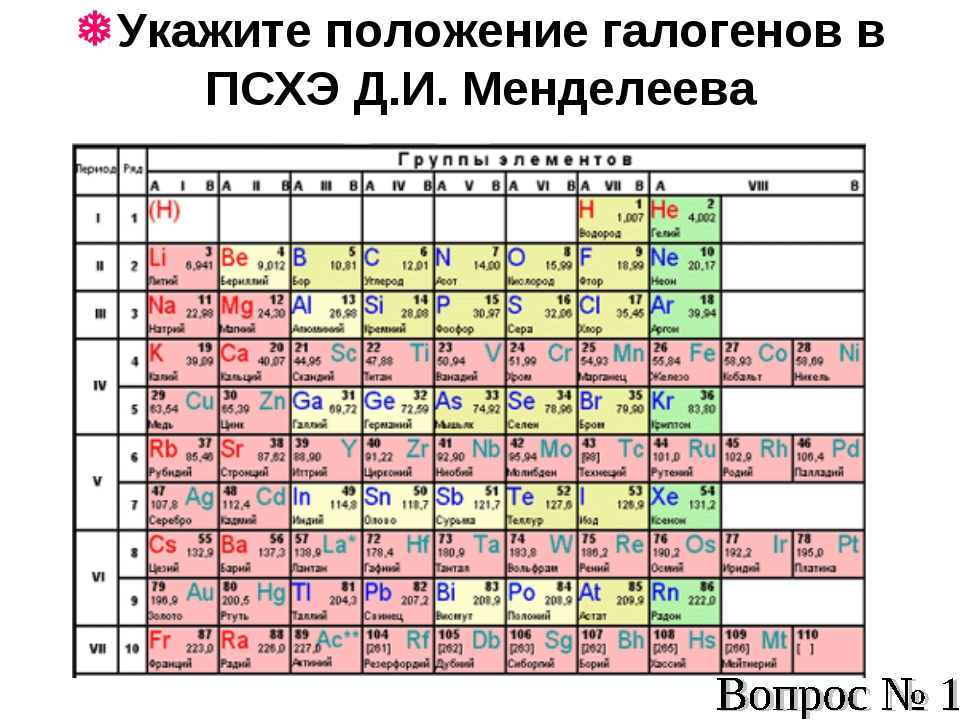 Черный фосфор.
Черный фосфор.
Всего в теме 46 презентаций
Все названия химических элементов происходят из латинского языка. Это необходимо в первую очередь для того, чтобы ученые разных стран могли понимать друг друга.
Химические знаки элементов
Элементы принято обозначать химическими знаками (символами). По предложению шведского химика Берцелиуса (1813 г.) химические элементы обозначают начальной или начальной и одной из последующих букв латинского названия данного элемента; первая буква всегда прописная, вторая строчная. Например, водород (Hydrogenium) обозначается буквой H, кислород (Oxygenium) – буквой O, сера (Sulfur) – буквой S; ртуть (Hydrargyrum) – буквами Hg, алюминий (Aluminium) – Al, железо (Ferrum) – Fe и т. д.
Рис. 1. Таблица химических элементов с названиями на латинском и русском языке.
Русские названия химических элементов зачастую представляют собой латинские названия с видоизмененными окончаниями. Но также существует множество элементов, произношение которых отличается от латинского первоисточника. Это либо коренные русские слова (например, железо), либо слова, которые являются переводом (пример – кислород).
Это либо коренные русские слова (например, железо), либо слова, которые являются переводом (пример – кислород).
Химическая номенклатура
Химическая номенклатура – правильное наименование химических веществ. Латинское слово nomenclatura переводится как «перечень имен, названий»
На ранней стадии развития химии веществам давались произвольные, случайные наименования (тривиальные названия). Легколетучие жидкости назывались спиртами, к ним относились «соляной спирт» – водный раствор соляной кислоты, «силитряный спирт» – азотная кислота, «нашатырный спирт» – водный раствор аммиака. Маслообразные жидкости и твердые вещества назывались маслами, например, концентрированная серная кислота носила название «купоросное масло», хлорид мышьяка – «мышьяковое масло».
Иногда вещества получали название по имени его первооткрывателя, например, «глауберова соль» Na 2 SO 4 *10H 2 O, открытая немецким химиком И. Р. Глаубером в XVII веке.
Рис. 2. Портрет И. Р. Глаубер.
В старинных названиях могли указываться вкус веществ, цвет, запах, внешний вид, медицинское действие. Одно вещество иногда имело несколько наименований.
К концу XVIII века химикам было известно не более 150-200 соединений.
Первую систему научных названий в химии выработала в 1787 г. комиссия химиков во главе с А. Лавуазье. Химическая номенклатура Лавуазье послужила основой для создания национальных химических номенклатур. Для того, чтобы химики разных стран понимали друг друга, номенклатура должна быть единой. В настоящее время построение химических формул и названий неорганических веществ подчиняется системе номенклатурных правил, созданной комиссией Международного союза теоретической и прикладной химии (ИЮПАК). Каждое вещество изображается формулой, в соответствии с ней строится систематическое название соединения.
Рис. 3. А. Лавуазье.
Что мы узнали?
Все химические элементы имеют латинские корни. Латинские названия химических элементов являются общепринятыми.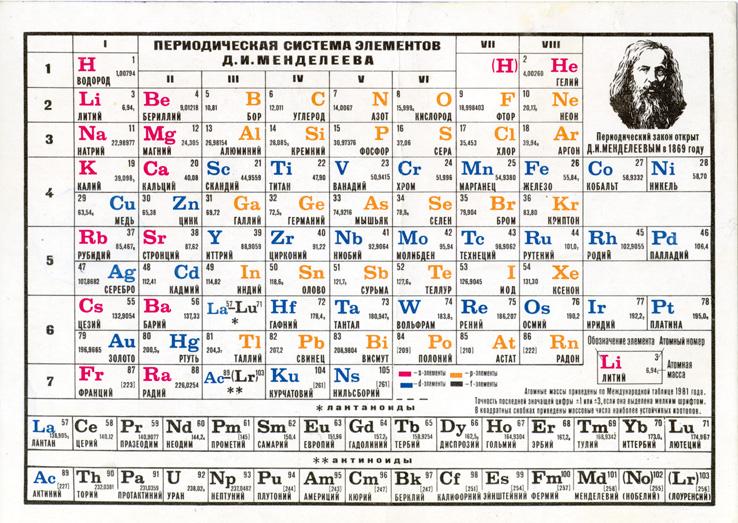 В русский язык они переносятся с помощью калькирования или перевода. однако некоторые слова имеют изначально русское значение, например, медь или железо. Химической номенклатуре подчиняются все химические вещества, состоящие из атомов и молекул. впервые система научных названий была разработана А. Лавуазье.
В русский язык они переносятся с помощью калькирования или перевода. однако некоторые слова имеют изначально русское значение, например, медь или железо. Химической номенклатуре подчиняются все химические вещества, состоящие из атомов и молекул. впервые система научных названий была разработана А. Лавуазье.
Тест по теме
Оценка доклада
Средняя оценка: 4.2 . Всего получено оценок: 768.
Как пользоваться таблицей Менделеева? Для непосвященного человека читать таблицу Менделеева – всё равно, что для гнома смотреть на древние руны эльфов. А таблица Менделеева может рассказать о мире очень многое.
Помимо того, что сослужит вам службу на экзамене, она еще и просто незаменима при решении огромного количества химических и физических задач. Но как ее читать? К счастью, сегодня этому искусству может научиться каждый. В этой статье расскажем, как понять таблицу Менделеева.
Периодическая система химических элементов (таблица Менделеева) – это классификация химических элементов, которая устанавливает зависимость различных свойств элементов от заряда атомного ядра.
История создания Таблицы
Дмитрий Иванович Менделеев был не простым химиком, если кто-то так думает. Это был химик, физик, геолог, метролог, эколог, экономист, нефтяник, воздухоплаватель, приборостроитель и педагог. За свою жизнь ученый успел провести фундаментально много исследований в самых разных областях знаний. Например, широко распространено мнение, что именно Менделеев вычислил идеальную крепость водки – 40 градусов.
Не знаем, как Менделеев относился к водке, но точно известно, что его диссертация на тему «Рассуждение о соединении спирта с водой» не имела к водке никакого отношения и рассматривала концентрации спирта от 70 градусов. При всех заслугах ученого, открытие периодического закона химических элементов – одного их фундаментальных законов природы, принесло ему самую широкую известность.
Существует легенда, согласно которой периодическая система приснилась ученому, после чего ему осталось лишь доработать явившуюся идею. Но, если бы все было так просто. . Данная версия о создании таблицы Менделеева, по-видимому, не более чем легенда. На вопрос о том, как была открыта таблица, сам Дмитрий Иванович отвечал: «Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово»
. Данная версия о создании таблицы Менделеева, по-видимому, не более чем легенда. На вопрос о том, как была открыта таблица, сам Дмитрий Иванович отвечал: «Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово»
В середине девятнадцатого века попытки упорядочить известные химические элементы (известно было 63 элемента) параллельно предпринимались несколькими учеными. Например, в 1862 году Александр Эмиль Шанкуртуа разместил элементы вдоль винтовой линии и отметил циклическое повторение химических свойств.
Химик и музыкант Джон Александр Ньюлендс предложил свой вариант периодической таблицы в 1866 году. Интересен тот факт, что в расположении элементов ученый пытался обнаружить некую мистическую музыкальную гармонию. В числе прочих попыток была и попытка Менделеева, которая увенчалась успехом.
В 1869 году была опубликована первая схема таблицы, а день 1 марта 1869 года считается днем открытия периодического закона. Суть открытия Менделеева состояла в том, что свойства элементов с ростом атомной массы изменяются не монотонно, а периодически.
Первый вариант таблицы содержал всего 63 элемента, но Менделеев предпринял ряд очень нестандартных решений. Так, он догадался оставлять в таблице место для еще неоткрытых элементов, а также изменил атомные массы некоторых элементов. Принципиальная правильность закона, выведенного Менделеевым, подтвердилась очень скоро, после открытия галлия, скандия и германия, существование которых было предсказано ученым.
Современный вид таблицы Менделеева
Ниже приведем саму таблицу
Сегодня для упорядочения элементов вместо атомного веса (атомной массы) используется понятие атомного числа (числа протонов в ядре). В таблице содержится 120 элементов, которые расположены слева направо в порядке возрастания атомного числа (числа протонов)
Столбцы таблицы представляют собой так называемые группы, а строки – периоды. В таблице 18 групп и 8 периодов.
- Металлические свойства элементов при движении вдоль периода слева направо уменьшаются, а в обратном направлении – увеличиваются.

- Размеры атомов при перемещении слева направо вдоль периодов уменьшаются.
- При движении сверху вниз по группе увеличиваются восстановительные металлические свойства.
- Окислительные и неметаллические свойства при движении вдоль периода слева направо увеличиваются.
Что мы узнаем об элементе по таблице? Для примера, возьмем третий элемент в таблице – литий, и рассмотрим его подробно.
Первым делом мы видим сам символ элемента и его название под ним. В верхнем левом углу находится атомный номер элемента, в порядке которого элемент расположен в таблице. Атомный номер, как уже было сказано, равен числу протонов в ядре. Число положительных протонов, как правило, равно числу отрицательных электронов в атоме (за исключением изотопов).
Атомная масса указана под атомным числом (в данном варианте таблицы). Если округлить атомную массу до ближайшего целого, мы получим так называемое массовое число. Разность массового числа и атомного числа дает количество нейтронов в ядре.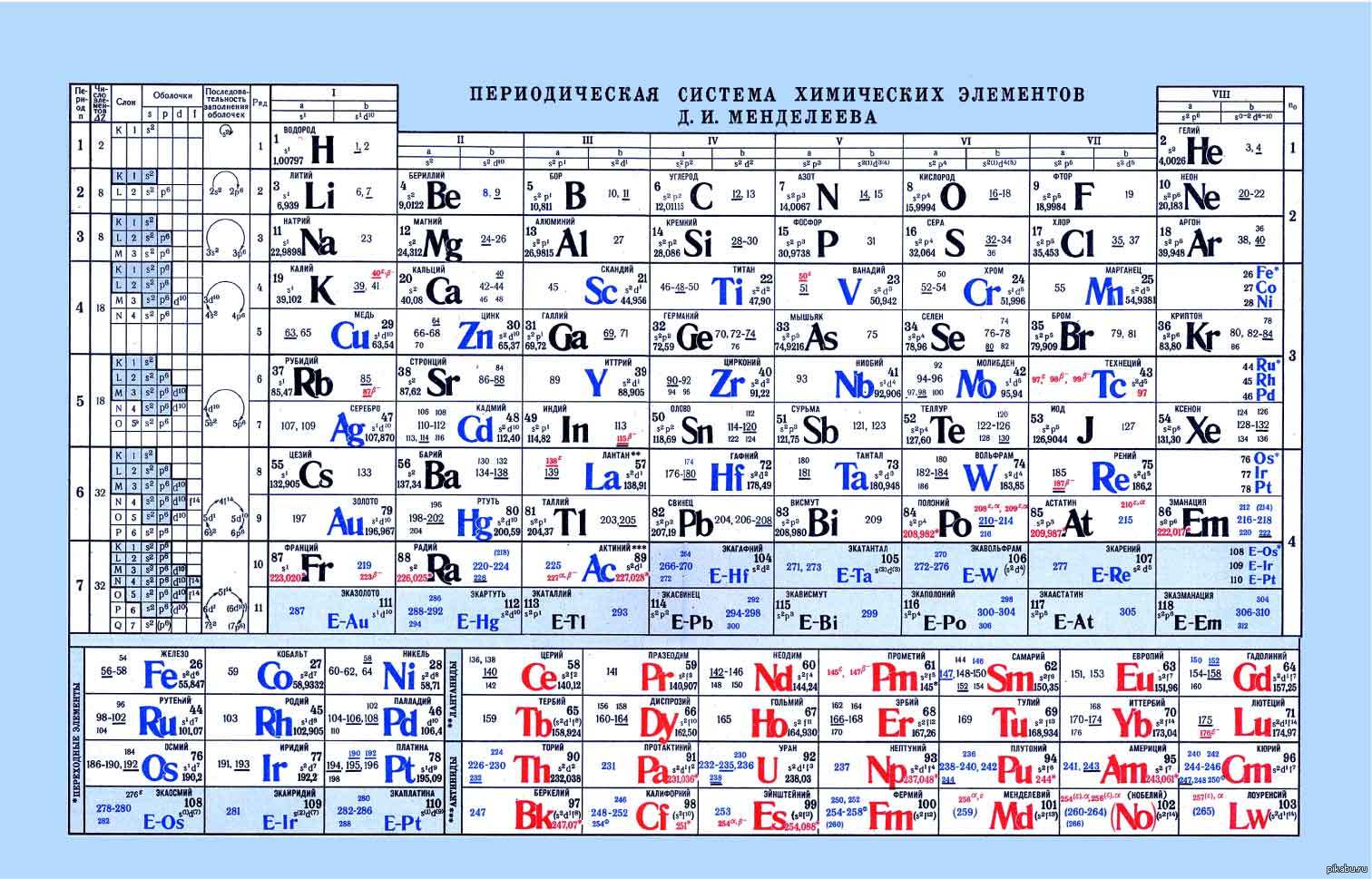 Так, число нейтронов в ядре гелия равно двум, а у лития – четырем.
Так, число нейтронов в ядре гелия равно двум, а у лития – четырем.
Вот и закончился наш курс “Таблица Менделеева для чайников”. В завершение, предлагаем вам посмотреть тематическое видео, и надеемся, что вопрос о том, как пользоваться периодической таблицей Менделеева, стал вам более понятен. Напоминаем, что изучать новый предмет всегда эффективнее не одному, а при помощи опытного наставника. Именно поэтому, никогда не стоит забывать о студенческом сервисе , который с радостью поделится с вами своими знаниями и опытом.
Инструкция
Периодическая система представляет собой многоэтажный «дом», в котором располагается большое количество квартир. Каждый «жилец» или в своей собственной квартире под определенным номером, который является постоянным. Помимо этого элемент имеет «фамилию» или название, например кислород, бор или азот. Кроме этих данных в каждой «квартире» или указана такая информация, как относительная атомная масса, которая может иметь точные или округленные значения.
Как в любом доме, здесь имеются «подъезды», а именно группы. Причем в группах элементы располагаются слева и справа, образуя . В зависимости от того, с какой стороны их больше, та называется главной. Другая подгруппа, соответственно, будет побочной. Также в таблице имеются «этажи» или периоды. Причем периоды могут быть как большими (состоят из двух рядов) так и малыми (имеют только один ряд).
По таблице можно показать строение атома элемента, каждый из которых имеет положительно заряженное ядро, состоящее из протонов и нейтронов, а также вращающихся вокруг него отрицательно заряженных электронов. Число протонов и электронов численно совпадает и определяется в таблице по порядковому номеру элемента. Например, химический элемент сера имеет №16, следовательно, будет иметь 16 протонов и 16 электронов.
Чтобы определить количество нейтронов (нейтральных частиц, также расположенных в ядре) вычтите из относительной атомной массы элемента его порядковый номер. Например, железо имеет относительную атомную массу равную 56 и порядковый номер 26. Следовательно, 56 – 26 = 30 протонов у железа.
Электроны находятся на разном расстоянии от ядра, образуя электронные уровни. Чтобы определить число электронных (или энергетических) уровней, нужно посмотреть на номер периода, в котором располагается элемент. Например, алюминий находится в 3 периоде, следовательно, у него будет 3 уровня.
По номеру группы (но только для главной подгруппы) можно определить высшую валентность. Например, элементы первой группы главной подгруппы (литий, натрий, калий и т.д.) имеют валентность 1. Соответственно, элементы второй группы (бериллий, магний, кальций и т.д.) будут иметь валентность равную 2.
Также по таблице можно проанализировать свойства элементов. Слева направо металлические свойства ослабевают, а неметаллические усиливаются. Это хорошо видно на примере 2 периода: начинается щелочным металлом натрием, затем щелочноземельный металл магний, после него амфотерный элемент алюминий, затем неметаллы кремний, фосфор, сера и заканчивается период газообразными веществами – хлором и аргоном. В следующем периоде наблюдается аналогичная зависимость.
Сверху вниз также наблюдается закономерность – металлические свойства усиливаются, а неметаллические ослабевают. То есть, например, цезий гораздо активнее по сравнению с натрием.
2.1. Химический язык и его части
Человечество использует много разных языков.
Кроме естественных языков (японского,
английского, русского – всего более 2,5 тысяч),
существуют еще и искусственные языки ,
например, эсперанто. Среди искусственных языков
выделяются языки различных наук . Так, в
химии используется свой, химический язык .
Химический язык – система условных
обозначений и понятий, предназначенная для
краткой, ёмкой и наглядной записи и передачи
химической информации.
Сообщение, написанное на большинстве
естественных языков, делится на предложения,
предложения – на слова, а слова – на буквы. Если
предложения, слова и буквы мы назовем частями
языка, то тогда мы сможем выделить аналогичные
части и в химическом языке (таблица 2).
Таблица 2. Части химического языка
Любым языком овладеть сразу невозможно, это относится и к химическому языку. Поэтому пока вы познакомитесь только с основами этого языка: выучите некоторые ” буквы” , научитесь понимать смысл ” слов” и” предложений” . В конце этой главы вы познакомитесь с названиями химических веществ – неотъемлемой частью химического языка. По мере изучения химии ваше знание химического языка будет расширяться и углубляться.
ХИМИЧЕСКИЙ ЯЗЫК.
1.Какие искусственные языки вы знаете (кроме
названных в тексте учебника)?
2.Чем естественные языки отличаются от
искусственных?
3.Как вы думаете, можно ли при описании химических
явлений обходиться без использования
химического языка? Если нет, то почему? Если да, то
в чем будут заключаться преимущества, а в чем
недостатки такого описания?
2.2. Символы химических элементов
Символ химического элемента обозначает сам
элемент или один атом этого элемента.
Каждый такой символ представляет собой
сокращенное латинское название химического
элемента, состоящее из одной или двух букв
латинского алфавита (латинский алфавит см. в
приложении 1). Символ пишется с прописной буквы.
Символы, а также русские и латинские названия
некоторых элементов, приведены в таблице 3. Там же
даны сведения о происхождении латинских
названий. Общего правила произношения символов
не существует, поэтому в таблице 3 приводится и
” чтение” символа, то есть, как этот символ
читается в химической формуле.
Заменять символом название элемента в устной
речи нельзя, а в рукописных или печатных текстах
это допускается, но не рекомендуется.В настоящее
время известно 110 химических элементов, у 109 из
них есть названия и символы, утвержденные
Международным союзом теоретической и прикладной
химии (ИЮПАК).
В таблице 3 приведена информация только о 33
элементах. Это те элементы, которые при изучении
химии вам встретятся в первую очередь. Русские
названия (в алфавитном порядке) и символы всех
элементов приведены в приложении 2.
Таблица 3. Названия и символы некоторых химических элементов
Название | ||||
Латинское | Написание | |||
| – | Написание | Происхождение | – | – |
| Азот | N itrogenium | От греч. ” рождающий селитру” | ” эн” | |
| Алюминий | Al uminium | От лат. ” квасцы” | ” алюминий” | |
| Аргон | Ar gon | От греч. ” недеятельный” | ” аргон” | |
| Барий | Ba rium | От греч. ” тяжелый” | ” барий” | |
| Бор | B orum | От арабск. ” белый минерал” | ” бор” | |
| Бром | Br omum | От греч. ” зловонный” | ” бром” | |
| Водород | H ydrogenium | От греч. ” рождающий воду” | ” аш” | |
| Гелий | He lium | От греч. ” Солнце” | ” гелий” | |
| Железо | Fe rrum | От лат. ” меч” | ” феррум” | |
| Золото | Au rum | От лат. ” горящий” | ” аурум” | |
| Йод | I odum | От греч. ” фиолетовый” | ” йод” | |
| Калий | K alium | От арабск. ” щёлочь” | ” калий” | |
| Кальций | Ca lcium | От лат. ” известняк” | ” кальций” | |
| Кислород | O xygenium | От греч. ” рождающий кислоты” | ” о” | |
| Кремний | Si licium | От лат. ” кремень” | ” силициум” | |
| Криптон | Kr ypton | От греч. ” скрытый” | ” криптон” | |
| Магний | M ag nesium | От назв. полуострова Магнезия | ” магний” | |
| Марганец | M an ganum | От греч. ” очищающий” | ” марганец” | |
| Медь | Cu prum | От греч. назв. о. Кипр | ” купрум” | |
| Натрий | Na trium | От арабск, ” моющее средство” | ” натрий” | |
| Неон | Ne on | От греч. ” новый” | ” неон” | |
| Никель | Ni ccolum | От нем. ” медь святого Николая” | ” никель” | |
| Ртуть | H ydrarg yrum | Лат. ” жидкое серебро” | ” гидраргирум” | |
| Свинец | P lumb um | От лат. названия сплава свинца с оловом. | ” плюмбум” | |
| Сера | S ulfur | От санскриттского ” горючий порошок” | ” эс” | |
| Серебро | A rg entum | От греч. ” светлый” | ” аргентум” | |
| Углерод | C arboneum | От лат. ” уголь” | ” цэ” | |
| Фосфор | P hosphorus | От греч. ” несущий свет” | ” пэ” | |
| Фтор | F luorum | От лат. глагола ” течь” | ” фтор” | |
| Хлор | Cl orum | От греч. ” зеленоватый” | ” хлор” | |
| Хром | C hr omium | От греч. ” краска” | ” хром” | |
| Цезий | C aes ium | От лат. ” небесно-голубой” | ” цезий” | |
| Цинк | Z in cum | От нем. ” олово” | ” цинк” | |
2.3. Химические формулы
Для обозначения химических веществ используют химические формулы .
Для молекулярных веществ химическая формула
может обозначать и одну молекулу этого вещества.
Информация о веществе может быть разной, поэтому
существуют разные типы химических формул .
В зависимости от полноты информации химические
формулы делятся на четыре основных типа: простейшие , молекулярные , структурные и пространственные .
Подстрочные индексы в простейшейформуле не
имеют общего делителя.
Индекс ” 1″ в формулах не ставится.
Примеры простейших формул: вода – Н 2 О,
кислород – О, сера – S, оксид фосфора – P 2 O 5 ,
бутан – C 2 H 5 , фосфорная кислота – H 3 PO 4 ,
хлорид натрия (поваренная соль) – NaCl.
Простейшая формула воды (Н 2 О) показывает,
что в состав воды входит элемент водород (Н) и
элемент кислород (О), причем в любой порции
(порция – часть чего-либо, что может быть
разделено без утраты своих свойств.) воды число
атомов водорода в два раза больше числа атомов
кислорода.
Число частиц , в том числе и число атомов ,
обозначается латинской буквой N . Обозначив
число атомов водорода – N H , а число
атомов кислорода – N O , мы можем
записать, что
Или N H: N O = 2: 1.
Простейшая формула фосфорной кислоты (Н 3 РО 4) показывает, что в состав фосфорной кислоты входят атомы водорода , атомы фосфора и атомы кислорода , причем отношение чисел атомов этих элементов в любой порции фосфорной кислоты равно 3:1:4, то есть
N H: N P: N O = 3: 1: 4.
Простейшая формула может быть составлена для любого индивидуального химического вещества, а для молекулярного вещества, кроме того, может быть составлена молекулярная формула .
Примеры молекулярных формул: вода – H 2 O, кислород – O 2 , сера – S 8 , оксид фосфора – P 4 O 10 , бутан – C 4 H 10 , фосфорная кислота – H 3 PO 4 .
У немолекулярных веществ молекулярных формул нет.
Последовательность записи символов элементов в простейших и молекулярных формулах определяется правилами химического языка, с которыми вы познакомитесь по мере изучения химии. На информацию, передаваемую этими формулами, последовательность символов влияния не оказывает.
Из знаков, отражающих строение веществ, мы будем использовать пока только валентный штрих (” черточку”). Этот знак показывает наличие между атомами так называемой ковалентной связи (что это за тип связи и каковы его особенности, вы скоро узнаете).
В молекуле воды атом кислорода связан простыми (одинарными) связями с двумя атомами водорода, а атомы водорода между собой не связаны. Именно это наглядно показывает структурная формула воды.
Другой пример: молекула серы S 8 . В этой молекуле 8 атомов серы образуют восьмичленный цикл, в котором каждый атом серы связан с двумя другими атомами простыми связями. Сравните структурную формулу серы с объемной моделью ее молекулы, показанной на рис. 3. Обратите внимание на то, что структурная формула серы не передает форму ее молекулы, а показывает только последовательность соединения атомов ковалентными связями.
Структурная формула фосфорной кислоты показывает, что в молекуле этого вещества один из четырех атомов кислорода связан только с атомом фосфора двойной связью, а атом фосфора, в свою очередь, связан еще с тремя атомами кислорода простыми связями. Каждый из этих трех атомов кислорода, кроме того, связан простой связью с одним из трех имеющихся в молекуле атомов водорода./p>
Сравните приведенную ниже объемную модель молекулы метана с его пространственной, структурной и молекулярной формулой:
В пространственной формуле метана клиновидныевалентные штрихи как бы в перспективе показывают, какой из атомов водорода находится ” ближе к нам” , а какой ” дальше от нас” .
Иногда в пространственной формуле указывают длины связей и значения углов между связями в молекуле, как это показано на примере молекулы воды.
Немолекулярные вещества не содержат молекул. Для удобства проведения химических расчетов в немолекулярном веществе выделяют так называемую формульную единицу .
Примеры состава формульных единиц некоторых веществ: 1) диоксид кремния (кварцевый песок, кварц) SiO 2 – формульная единица состоит из одного атома кремния и двух атомов кислорода; 2) хлорид натрия (поваренная соль) NaCl – формульная единица состоит из одного атома натрия и одного атома хлора; 3) железо Fe – формульная единица состоит из одного атома железа.Как и молекула, формульная единица – наименьшая порция вещества, сохраняющая его химические свойства.
Таблица 4
Информация, передаваемая формулами разных типов
Тип формулы | Информация, передаваемая формулой. | |
| Простейшая Молекулярная Структурная Пространственная |
| |
Рассмотрим теперь на примерах, какую информацию дают нам формулы разных типов.
1. Вещество: уксусная кислота . Простейшая формула – СН 2 О, молекулярная формула – C 2 H 4 O 2 , структурная формула
Простейшая формула говорит нам, что
1) в состав уксусной кислоты входит углерод,
водород и кислород;
2) в этом веществе число атомов углерода
относится к числу атомов водорода и к числу
атомов кислорода, как 1:2:1, то есть N H: N C:N O = 1:2:1.
Молекулярная формула добавляет, что
3) в молекуле уксусной кислоты – 2 атома углерода,
4 атома водорода и 2 атома кислорода.
Структурная формула добавляет, что
4, 5) в молекуле два атома углерода связаны между
собой простой связью; один из них, кроме этого,
связан с тремя атомами водорода, с каждым простой
связью, а другой – с двумя атомами кислорода, с
одним – двойной связью, а с другим – простой;
последний атом кислорода связан еще простой
связью с четвертым атомом водорода.
2. Вещество: хлорид натрия . Простейшая формула – NaCl.
1) В состав хлорида натрия входит натрий и хлор.
2) В этом веществе число атомов натрия равно числу
атомов хлора.
3. Вещество: железо . Простейшая
формула – Fe.
1) В состав этого вещества входит только железо,
то есть это простое вещество.
4. Вещество: триметафосфорная кислота . Простейшая формула – HPO 3 , молекулярная формула – H 3 P 3 O 9 , структурная формула
1) В состав триметафосфорной кислоты входит
водород, фосфор и кислород.
2) N H: N P:N O = 1:1:3.
3) Молекула состоит из трех атомов водорода, трех
атомов фосфора и девяти атомов кислорода.
4, 5) Три атома фосфора и три атома кислорода,
чередуясь, образуют шестичленный цикл. Все связи
в цикле простые. Каждый атом фосфора, кроме того,
связан еще с двумя атомами кислорода, причем с
одним – двойной связью, а с другим – простой.
Каждый из трех атомов кислорода, связанных
простыми связямис атомами фосфора, связан еще
простой связью с атомом водорода.
| Фосфорная кислота – H 3 PO 4 (другое название – ортофосфорная кислота) – прозрачное бесцветное кристаллическое вещество молекулярного строения, плавящееся при 42 o С. Это вещество очень хорошо растворяется в воде и даже поглощает пары воды из воздуха (гигроскопично). Фосфорную кислоту производят в больших количествах и используют прежде всего в производстве фосфорных удобрений, а также в химической промышленности, при производстве спичек и даже в строительстве. Кроме того, фосфорная кислота применяется при изготовлении цемента в зубоврачебной технике, входит в состав многих лекарственных средств. Эта кислота достаточно дешева, поэтому в некоторых странах, например в США, очень чистая сильно разбавленная водой фосфорная кислота добавляется в освежающие напитки для замены дорогой лимонной кислоты. |
| Метан – CH 4 . Если у вас дома есть газовая плита, то с этим веществом вы сталкиваетесь ежедневно: природный газ, который горит в конфорках вашей плиты, на 95 % состоит из метана. Метан – газ без цвета и запаха с температурой кипения –161 o С. В смеси с воздухом он взрывоопасен, этим и объясняются происходящие иногда в угольных шахтах взрывы и пожары (другое название метана – рудничный газ). Третье название метана – болотный газ – связано с тем, что пузырьки именно этого газа поднимаются со дна болот, где он образуется в результате деятельности некоторых бактерий. В промышленности метан используется как топливо и сырье для производства других веществ.Метан является простейшим углеводородом . К этому классу веществ относятся также этан (C 2 H 6), пропан (C 3 H 8), этилен (C 2 H 4), ацетилен (C 2 H 2) и многие другие вещества. |
Таблица 5 . Примеры формул разных типов для некоторых веществ –
| | Адрес этой страницы (вложенность) в справочнике dpva.ru: главная страница / / Техническая информация / / Химический справочник / / Таблица Менделеева. Названия. Электронные формулы. Молярные массы. Структурные формулы. Таблицы степеней окисления и валентности. Изотопы. Поделиться:
| ||
| Если Вы не обнаружили себя в списке поставщиков, заметили ошибку, или у Вас есть дополнительные численные данные для коллег по теме, сообщите , пожалуйста. Вложите в письмо ссылку на страницу с ошибкой, пожалуйста. | |||
| Проект является некоммерческим. Информация, представленная на сайте, не является официальной и предоставлена только в целях ознакомления. Владельцы сайта www.dpva.ru не несут никакой ответственности за риски, связанные с использованием информации, полученной с этого интернет-ресурса. Free xml sitemap generator | |||
Элементы 113, 115, 117 и 118: от открытия до признания
07 дек. 2016 г., 12:15
Научный руководитель Лаборатории ядерных реакций ОИЯИ, руководитель работ по синтезу сверхтяжелых элементов в Дубне, академик РАН Юрий Цолакович Оганесян, в честь которого получил название 118-й элемент, рассказал о том, как идет научный поиск в этом направлении, как новые элементы получают свои названия.
Новость о внесении в таблицу Менделеева сразу четырех новых сверхтяжелых элементов вызвала живой интерес людей даже весьма далеких от науки. Но это итог некоего пути от собственно открытия элементов до их официального признания. На основе отчетов научных групп, которым удалось синтезировать элементы с номерами 113, 115, 117 и 118, совместная комиссия международных союзов по физике (ИЮПАП) и по химии (ИЮПАК) присудила приоритеты в открытии.
Согласно пресс-релизу от 30 декабря 2015 года ИЮПАК признал приоритет в открытии элементов: 113 – за японской группой ученых, 115, 117, 118 – за дубненской.
8 июня 2016 года ИЮПАК сообщил, что принял названия, предложенные авторами открытий. После чего в течение пяти месяцев шло обсуждение этих названий в научных сообществах всех стран мира. И 28 ноября 2016 года ИЮПАК принял решение внести в Периодическую таблицу элементы:
Нихоний (Nh) – 113,
Московий (Mc) – 115,
Теннессин (Ts) – 117,
Оганесон (Og) – 118.
Научный руководитель Лаборатории ядерных реакций ОИЯИ, руководитель работ по синтезу сверхтяжелых элементов в Дубне, академик РАН Юрий Цолакович Оганесян, в честь которого получил название 118-й элемент, в начале нынешнего года рассказывал журналистам о том, как идет научный поиск в этом направлении, как новые элементы получают свои названия и т. д.
– Как реагировало научное сообщество на сообщение о признании приоритетов в открытии элементов с номерами 113, 115, 117 и 118?
– Большие дискуссии идут, причем на высоком уровне – все вдруг оживились. Хотели найти границы: насколько может быть большой Периодическая таблица элементов? Наш эксперимент показал: она может быть очень и очень большой. Все ожидали, что этих элементов не будет, а теперь, когда оказалось, что они есть, – граница отодвинулась. Вопрос: сколько вообще может быть элементов – остается открытым. С одной стороны, это говорит о том, что надо дальше работать по этой теме. С другой стороны, это оправдывает то, что мы «фабрику» делаем – для того, чтобы идти дальше.
– Есть ли сегодня представление о том, каким путем продвигаться дальше?
– На четыре новых элемента нами было потрачено 15 лет. Мы первые результаты получили в 2000 году, и за прошедшие 15 лет что-то увидели, что-то поняли. Мы не знали, есть ли вообще там какие-то элементы. Теперь наши знания пополнились. С другой стороны – (идет) научно-технический прогресс. И если бы мы сегодня ставили такой эксперимент: с учетом того, что теперь знаем, и с техникой, которая есть сейчас, – мы могли бы в сто раз быстрее это сделать. Вот потому создается «фабрика»: она воплощает в себе все знания, которые получены здесь (в Лаборатории ядерных реакций), и весь научно-технический прогресс, который был за 15 лет.
Тут вопрос в том, как идти дальше. Надо остановиться в какой-то момент и сказать себе: теперь надо идти по-другому. Академик Л. А. Арцимович, у которого я учился, говорил: если вы хотите какую-то установку усовершенствовать, вы можете каждый из ее узлов улучшить – здесь на 10 %, там на 20 %, где-то на 30% – и получить улучшение результата в 2–3 раза. Но если вы хотите в 10 раз лучше, надо старую установку выбросить и делать новую.
То же самое и здесь (с фабрикой сверхтяжелых элементов): если хотим получить (чувствительность эксперимента) в 100 раз больше, то нужно остановиться и сделать что-то новое – тогда получишь нужный фактор и увидишь то, чего сейчас не видишь. Это, кстати, естественное человеческое отношение к любой вещи: если вы хотите сделать серьезный скачок, надо остановиться и делать дальше по-другому.
– Помогает ли в дальнейшей работе признание новых элементов?
– Нет. Это не только мое мнение, но и всех, кто занимается этим делом. Например, когда вы готовите обед – ждете, что скажут гости, или сами чувствуете, что вкусно получилось? Если ты занимаешься делом каждый день, виден тот момент, когда действительно получается. Может быть, остальные не очень верят, но ты-то это видишь: один, второй раз (новый элемент образуется), потом еще и еще раз получается – вот это первая вещь, которая вселяет уверенность.
Вторая вещь, когда в другой лаборатории другие люди на другой установке повторяют тот же эксперимент «один к одному» – тогда и они верят. Еще признания нет, но уже всё понятно, и на конференциях по-другому звучит. А когда уже официально признали и вписали (новый элемент) в Таблицу, надо понимать, что это (его существование) не сейчас стало ясно, а гораздо раньше.
Например, по 117-му элементу, который наиболее сложно нам было получить, второй эксперимент закончили в 2010 году. За 5 лет, прошедшие с тех пор, в Америке в Беркли его повторили, в Германии в Дармштадте – всё то же самое. Хочу сказать, что это довольно-таки тяжелая работа: малое количество событий (когда синтезируется новый элемент), контроль эксперимента надо делать и т. д. А когда всё подтверждается и признается приоритет – это завершающий этап.
– Как получилось, что несколько сверхтяжелых элементов даже не пытались синтезировать в Лаборатории ядерных реакций?
– В 1974 году мы здесь, в Дубне, предложили и продемонстрировали новый метод синтеза элементов. А тогда строился ускоритель в Дармштадте, коллеги из Германии посмотрели и «ухватились» за него – было такое время, когда ездили каждую неделю к нам сюда. Они построили гигантский ускоритель, сделали замечательный сепаратор и применили наш принцип, чтобы синтезировать новые элементы в Дармштадте. Более 20 лет она работали и этим способом первыми получили элементы 107, 108, 109, 110, 111 и 112. Впрочем, 112-й и мы тоже получили.
Меня часто спрашивают: почему вы сами этим методом не занимались? Во-первых, у нас жизнь тогда была непростая – 90-е годы. Во-вторых, не важно, главное, что они нашим методом это сделали. В-третьих, что самое главное: было ясно, что этот метод более тяжелых элементов не даст – не хватает нейтронов, чтобы подойти к этой горе, к острову стабильности. Он ведет мимо «острова стабильности». Поэтому мы начали кальцием заниматься (облучением пучками изотопов кальция-48 мишеней из трансурановых элементов).
А немецкие коллеги дошли до 112-го, и это (возможности прежнего метода) было исчерпано, тем не менее, японцы начали делать 113-й тем же методом. Они за 9 лет получили 3 события (синтеза 113-го элемента) – я называю это «из кастрюли соскребать со дна». Это неинтересно, так как не имеет выхода дальше, а просто дает еще один элемент. Поэтому мы пошли в область нейтронно-избыточных (ядер). Там получается гораздо больше. У нас был сначала 115-й элемент, затем (как результат его альфа-распада) 113-й, и это примерно одно событие в день – в тысячу раз больше.
– Поэтому присуждение Японии приоритета в открытии 113-го воспринято в научных кругах неоднозначно?
– О том, что мы синтезировали 115-й элемент, а из него (после альфа-распада всегда) получается 113-й, его «дочка», – я доложил на конгрессе ИЮПАК в 2003 году в Казани. А японцы свой первый результат опубликовали через год. То есть мы и по времени раньше, и событий у нас больше, и нашим методом можно к более тяжелым элементам идти, а японский эксперимент даже никто повторять не станет – какой смысл заниматься девять лет ради трех событий, если можно (действуя, как в Дубне) получать 113-й в сотнях штук. Поэтому и физики, и химики будут пользоваться нашим методом, который дает более тяжелый изотоп 113-го.
Может быть, ИЮПАК посчитал, что «слишком много» отдавать все четыре элемента в одни руки. Может, решил отдать должное упорству японцев. Можно разные догадки строить. Плохо то, что это решение ИЮПАК ничем не подтвердил. Они должны были подготовить и опубликовать отчет, потом провести дебаты по этому поводу – а пока (на 21 января 2016 года) отчета нет: как они смогли «дочь» (113-й) от «матери» (115-го) оторвать. Это всё уже номенклатура, но мы-то знаем, что это «наше дитя».
– Как придумывают названия для новых элементов?
– По правилам мы должны предложить названия «своих» элементов, но это не значит, что номенклатурная комиссия ИЮПАК примет то, что мы скажем. Ведь потом названия и двухбуквенные символы элементов будут использоваться в учебниках, в формулах химических соединений – важно, чтобы они звучали приемлемо на всех языках мира. Так, 105-й элемент – дубний, в честь города Дубны, 114-й – флеровий, в честь Лаборатории ядерных реакций и ее основателя Георгия Николаевича Флерова, 116-й – ливерморий, в честь города в Америке (места нахождения национальной лаборатории, совместно с которой проводились эксперименты по синтезу сверхтяжелых).
Обсуждается (для 115-го) название «московий». Важно понимать, что это в честь Московии как исторической русской древней территории. Сейчас на ней находятся Москва и Московская область, но речь не об административных единицах, а о земле Московии – той местности, в которой мы живем.
По двум другим элементам предложений пока не было, но мы должны отдать дань нашим коллегам-американцам, они внесли свой вклад. Знаете, в современном мире вообще так устроено: надо взять всё лучшее, что есть – и тогда можно чего-то достичь. Поэтому мы взяли самый мощный в мире реактор, который работает в Окридже, и самый мощный ускоритель, который работает в Дубне – и это дало такой мощный симбиоз. Вот такое сотрудничество, когда одно без второго не даст ничего, когда обе стороны являются фундаментами, – это и есть настоящее сотрудничество. У нас оно и дальше будет продолжаться. Вот сейчас у нас (в циклотроне) стоит американская мишень, на пучке облучается. И новые элементы – это наш общий результат, хотя эксперименты делаются в Дубне.
Что касается названия третьего из элементов, надо подумать – у нас есть на это время. Но, вообще говоря, мы будем следовать традиции. А по традиции принято называть элементы либо в честь планет (Плутон, Нептун, Уран), либо в честь великих ученых (Кюри, Ферми, Менделеев), либо в честь мест, где произошло их открытие (в честь немецкой земли Гессен получил название 108-й элемент, хассий). Этот вариант мне нравится больше всего, потому что когда пишешь статью по результатам эксперимента, количество авторов ограничено, хотя участвует в нем множество людей. И если элемент назван в честь места, где он открыт, все себя чувствуют упомянутыми в этом названии. Вот когда был объявлен наш приоритет по элементам 114 и 116, я предложил выписать одинаковые премии всем сотрудникам лаборатории – от директора до уборщиц, потому что все участвовали. По большому счету надо вспомнить и всех, кто работал в лаборатории раньше, ведь труд каждого здесь остался. И когда мы называем элемент в честь нашей земли, я считаю такой подход – гуманный и правильный. Не будем отходить от этой традиции.
Источник: http://indubnacity.ru/intervyu/elementy-113-115-117-i-118-ot-otkrytiya-do-priznaniya
элементов таблицы Менделеева по имени Москва, Япония, Теннесси
НЬЮ-ЙОРК. Скоро вы увидите четыре новых имени в периодической таблице элементов, в том числе три имени Москвы, Японии и Теннесси.
Имена входят в число четырех, рекомендованных в среду международной научной группой. Четвертый назван в честь русского ученого.
Международный союз теоретической и прикладной химии, регулирующий названия химических элементов, представил свое предложение на общественное рассмотрение.Имена были представлены первооткрывателями элементов.
Четыре элемента, известные теперь по своим номерам, заполнили седьмую строку периодической таблицы, когда химическая организация проверила их открытия в декабре прошлого года.
Теннесси – второй штат США, получивший статус элемента; Калифорния была первой. Названия элементов могут происходить из мест, мифологии, имен ученых или характеристик элемента. Другие примеры: америций, эйнштейний и титан.
Присоединение к более знакомым названиям элементов, таких как водород, углерод и свинец:
– московий символ Mc для элемента 115 и теннессин, символ Ts, для элемента 117.Команда по открытию представляет собой Объединенный институт ядерных исследований в Дубне, Россия, Национальную лабораторию Ок-Ридж и Университет Вандербильта в Теннесси, а также Ливерморскую национальную лабораторию Лоуренса в Калифорнии.
Профессор физики Вандербильта Джозеф Гамильтон, сыгравший важную роль в открытиях, предложил назвать элемент Теннесси. Он надеялся использовать символ Tn, но он использовался в прошлом и не мог быть переназначен для нового элемента.
– оганессон, символ Ог, для элемента 118.Этим именем признан российский физик Юрий Оганесян.
– нихоний, символ Nh, для элемента 113. Элемент был обнаружен в Японии, и Nihon – это один из способов произнести название страны на японском языке. Это первый элемент, обнаруженный в азиатской стране.
Период общественного обсуждения завершится 8 ноября.
российских ученых предлагают новый способ упорядочения элементов
Периодическая таблица элементов, созданная главным образом русским химиком Дмитрием Менделеевым (1834–1907), в прошлом году отметила свое 150-летие.Трудно переоценить его важность как организующего принципа в химии – все начинающие химики знакомятся с ним с самых ранних этапов своего образования.
Учитывая важность таблицы, можно простить мысль, что порядок элементов больше не является предметом обсуждения. Однако два ученых из Москвы, Россия, недавно опубликовали предложение о новом порядке.
Давайте сначала рассмотрим, как была разработана таблица Менделеева. К концу 18 века химики ясно понимали разницу между элементом и соединением: элементы были химически неделимы (например, водород, кислород), тогда как соединения состояли из двух или более элементов в комбинации, обладающих свойствами, совершенно отличными от составляющих их элементов.К началу 19 века появились хорошие косвенные доказательства существования атомов. А к 1860-м годам стало возможно перечислять известные элементы в порядке их относительной атомной массы – например, водород был равен 1, а кислород 16.
Простые списки, конечно, одномерные по своей природе. Но химики знали, что некоторые элементы имеют довольно похожие химические свойства: например, литий, натрий и калий или хлор, бром и йод. Казалось, что-то повторяется, и, помещая химически похожие элементы рядом друг с другом, можно было построить двухмерную таблицу.Так родилась таблица Менделеева.
Важно отметить, что периодическая таблица Менделеева была получена эмпирическим путем на основе наблюдаемого химического сходства определенных элементов. Только в начале 20 века, после того, как была установлена структура атома и после развития квантовой теории, появилось теоретическое понимание его структуры.
Элементы теперь были упорядочены по атомному номеру (количеству положительно заряженных частиц, называемых протонами в атомном ядре), а не по атомной массе, но также по химическому сходству.Но последнее теперь следовало из расположения электронов, повторяющихся в так называемых «оболочках» через равные промежутки времени. К 1940-м годам в большинстве учебников была периодическая таблица, аналогичная той, что мы видим сегодня, как показано на рисунке ниже.
Сегодняшняя таблица Менделеева.
Можно было бы подумать, что на этом все кончено. Однако это не так. Простой поиск в Интернете покажет всевозможные версии таблицы Менделеева. Есть короткие версии, длинные версии, круглые версии, спиральные версии и даже трехмерные версии.Конечно, многие из них представляют собой просто разные способы передачи одной и той же информации, но по-прежнему существуют разногласия по поводу того, где следует разместить некоторые элементы.
Точное размещение определенных элементов зависит от того, какие именно свойства мы хотим выделить. Таким образом, периодическая таблица, которая отдает приоритет электронной структуре атомов, будет отличаться от таблиц, для которых основными критериями являются определенные химические или физические свойства.
Эти версии не сильно различаются, но есть определенные элементы, например водород, которые можно разместить совершенно по-разному в зависимости от конкретного свойства, которое нужно выделить.В некоторых таблицах водород помещен в группу 1, тогда как в других он находится в верхней части группы 17; некоторые столы даже включают его в отдельную группу.
Более радикально, однако, мы также можем рассмотреть упорядочение элементов совершенно другим способом, который не включает атомный номер и не отражает электронную структуру – возвращаясь к одномерному списку.
Новое предложение
Последняя попытка упорядочить элементы таким образом была недавно опубликована в «Журнале физической химии» учеными Захедом Аллахьяри и Артемом Огановым.Их подход, основанный на более ранней работе других, состоит в том, чтобы присвоить каждому элементу так называемое число Менделеева (MN). Есть несколько способов получить такие числа, но последнее исследование использует комбинацию двух фундаментальных величин, которые можно измерить напрямую: атомного радиуса элемента и свойства, называемого электроотрицательностью, которое описывает, насколько сильно атом притягивает электроны к себе.
Если упорядочить элементы по их MN, неудивительно, что ближайшие соседи имеют довольно похожие MN.Но гораздо полезнее сделать еще один шаг и построить двумерную сетку на основе MN составляющих элементов в так называемых «бинарных соединениях». Это соединения, состоящие из двух элементов, таких как хлорид натрия, NaCl.
В чем преимущество такого подхода? Важно отметить, что это может помочь предсказать свойства бинарных соединений, которые еще не были созданы. Это полезно при поиске новых материалов, которые могут понадобиться как для будущих, так и для существующих технологий.Со временем, без сомнения, это будет распространено на соединения с более чем двумя элементарными компонентами.
Хороший пример важности поиска новых материалов можно оценить, рассматривая периодическую таблицу, показанную на рисунке ниже. Эта таблица иллюстрирует не только относительное количество элементов (чем больше прямоугольник для каждого элемента, тем их больше), но также выделяет потенциальные проблемы с поставками, относящиеся к технологиям, которые стали повсеместными и важными в нашей повседневной жизни.
Периодическая таблица, показывающая относительное содержание элементов. Кредит: Европейское химическое общество, CC BY-SA
.Возьмем, к примеру, мобильные телефоны. Все элементы, используемые при их производстве, обозначены значком телефона, и вы можете видеть, что некоторые необходимые элементы становятся дефицитными – их будущие поставки неизвестны. Если мы собираемся разработать материалы-заменители, которые избегают использования определенных элементов, информация, полученная при упорядочивании элементов их MN, может оказаться ценным в этом поиске.
Спустя 150 лет мы видим, что периодические таблицы – это не просто жизненно важный образовательный инструмент, они остаются полезными для исследователей в их поисках необходимых новых материалов. Но мы не должны думать о новых версиях как о замене более ранних изображений. Наличие множества разных таблиц и списков только помогает нам лучше понять, как ведут себя элементы.
Написано Ником Норманом, профессором химии Бристольского университета.
Первоначально опубликовано в The Conversation.
На столе появилось четыре новых имени элемента | Наука
Страна: Страна * AfghanistanAland IslandsAlbaniaAlgeriaAndorraAngolaAnguillaAntarcticaAntigua и BarbudaArgentinaArmeniaArubaAustraliaAustriaAzerbaijanBahamasBahrainBangladeshBarbadosBelarusBelgiumBelizeBeninBermudaBhutanBolivia, многонациональное государство ofBonaire, Синт-Эстатиус и SabaBosnia и HerzegovinaBotswanaBouvet IslandBrazilBritish Индийский океан TerritoryBrunei DarussalamBulgariaBurkina FasoBurundiCambodiaCameroonCanadaCape VerdeCayman IslandsCentral африканских RepublicChadChileChinaChristmas IslandCocos (Килинг) IslandsColombiaComorosCongoCongo, Демократическая Республика theCook IslandsCosta RicaCote D’IvoireCroatiaCubaCuraçaoCyprusCzech RepublicDenmarkDjiboutiDominicaDominican RepublicEcuadorEgyptEl SalvadorEquatorial GuineaEritreaEstoniaEthiopiaFalkland острова (Мальвинские ) Фарерские острова, Фиджи, Финляндия, Франция, Французская Гвиана, Французская Полинезия, Французские Южные территории, Габон, Гамбия, Грузия, Германия, Гана, Гибралтар, Греция, Гренландия, Гренада, Гваделупа, Гватемала, Гернси, Гвинея, Гвинея-Бисау, Гайана, Гаити, Остров Херд и МакДональда IslandsHoly Престол (Ватикан) HondurasHong KongHungaryIcelandIndiaIndonesiaIran, Исламская Республика ofIraqIrelandIsle из ManIsraelItalyJamaicaJapanJerseyJordanKazakhstanKenyaKiribatiKorea, Корейская Народно-Демократическая Республика ofKorea, Республика ofKuwaitKyrgyzstanLao Народная Демократическая RepublicLatviaLebanonLesothoLiberiaLibyan Арабская JamahiriyaLiechtensteinLithuaniaLuxembourgMacaoMacedonia, бывшая югославская Республика ofMadagascarMalawiMalaysiaMaldivesMaliMaltaMartiniqueMauritaniaMauritiusMayotteMexicoMoldova, Республика ofMonacoMongoliaMontenegroMontserratMoroccoMozambiqueMyanmarNamibiaNauruNepalNetherlandsNew CaledoniaNew ZealandNicaraguaNigerNigeriaNiueNorfolk IslandNorwayOmanPakistanPalestinianPanamaPapua Новый GuineaParaguayPeruPhilippinesPitcairnPolandPortugalQatarReunionRomaniaRussian FederationRWANDASaint BarthélemySaint Елены, Вознесения и Тристан-да-КуньяСент-Китс и НевисСент-ЛюсияСент-Мартен (французская часть) Сен-Пьер и МикелонСент-Винсент и ГренадиныСам oaSan MarinoSao Том и PrincipeSaudi ArabiaSenegalSerbiaSeychellesSierra LeoneSingaporeSint Маартен (Голландская часть) SlovakiaSloveniaSolomon IslandsSomaliaSouth AfricaSouth Джорджия и Южные Сандвичевы IslandsSouth SudanSpainSri LankaSudanSurinameSvalbard и Ян MayenSwazilandSwedenSwitzerlandSyrian Arab RepublicTaiwanTajikistanTanzania, Объединенная Республика ofThailandTimor-LesteTogoTokelauTongaTrinidad и TobagoTunisiaTurkeyTurkmenistanTurks и Кайкос IslandsTuvaluUgandaUkraineUnited арабского EmiratesUnited KingdomUnited StatesUruguayUzbekistanVanuatuVenezuela, Боливарианская Республика ofVietnamVirgin остров, BritishWallis и Футуна Западная Сахара Йемен Замбия Зимбабве
Пожертвовать сейчасПоддержка некоммерческой научной журналистики
Если мы чему-то научились из пандемии COVID-19, так это тому, что мы не можем дождаться реакции кризиса. Science и AAAS неустанно работают над предоставлением достоверной, основанной на фактах информации о последних научных исследованиях и политике с широким бесплатным освещением пандемии. Ваш не подлежащий налогообложению вклад играет решающую роль в поддержании этих усилий.
Раскрытие благотворительной информацииХорошее начало – хороший конец
28 июля 2016 года я получил следующее сообщение от сэра Мартина Полякова, профессора Ноттингемского университета в Великобритании и иностранного члена Российской академии наук, которого я знаю много лет.Он написал:
«Уважаемая Наталья,
, надеюсь, у вас все хорошо. Я понял, что в 2019 году исполняется 150 годов годовщина публикации Менделеевым Периодической таблицы Менделеева. Поэтому мне было интересно, может ли ИЮПАК выступить с просьбой сделать 2019 год Международным годом Периодической таблицы Менделеева. Я чувствую, что это предложение может получить широкую поддержку. Что вы думаете?
С наилучшими пожеланиями
Мартын ».
Это было начало истории со счастливым концом.20 декабря 2017 года Генеральная Ассамблея Организации Объединенных Наций провозгласила 2019 год Международным годом Периодической таблицы химических элементов (IYPT 2019) на своем 74-м пленарном заседании на 72-й сессии. Провозгласив Международный год Периодической таблицы химических элементов и ее приложений, Организация Объединенных Наций признала важность повышения глобальной осведомленности о том, как химия способствует устойчивому развитию и обеспечивает решения глобальных проблем в области энергетики, образования, сельского хозяйства и здравоохранения.Действительно, резолюция была принята как часть более общего пункта повестки дня «Наука и техника в целях развития». Этот Международный год соберет вместе множество различных заинтересованных сторон, включая ЮНЕСКО, научные общества и союзы, образовательные и исследовательские учреждения, технологические платформы, некоммерческие организации и партнеров из частного сектора, чтобы продвигать и отмечать значение Периодической таблицы и ее применения в обществе. в 2019 году.
Поскольку я принимал участие в деятельности Комитета по менеджменту Международного года химии 2011 года, алгоритм процедуры был мне понятен.Ключевым элементом на начальном этапе является определение страны, которая будет готова через свое национальное представительство в ЮНЕСКО продвигать идею МГПО. Именно ЮНЕСКО как орган ООН может рекомендовать Генеральной Ассамблее ООН провозгласить 2019 год МГПЭ. На самом деле, время, которое нам нужно было продвинуть вперед, было довольно коротким. По правилам ООН решение должно быть принято за два года вперед. Мои коллеги из Исполнительного комитета IUPAC поддержали идею IYPT в принципе, хотя и со здоровым скептицизмом, основываясь на воспоминаниях о провозглашении в 2011 году Международного года химии.Россия, как родина Дмитрия Менделеева, была выбрана ведущей инициативой через ЮНЕСКО.
30 сентября 2016 года 3000 участников 20 -го Менделеевского съезда, состоявшегося в Екатеринбурге, Россия, единогласно проголосовали за провозглашение МГИП в 2019 году. Резолюцию поддержали Российское химическое общество имени Менделеева и Российская академия химии. Наук. На основании этого постановления академик Владимир Фортов, в то время президент Российской академии наук, направил министру иностранных дел Российской Федерации Сергею Лаврову письмо с просьбой поддержать инициативу МПОП в ЮНЕСКО.Одновременно в секретариат ИЮПАК было отправлено письмо Российской академии наук (Российской национальной присоединяющейся организации (НАО) ИЮПАК). Российская академия наук предложила ИЮПАК стать ведущим союзом МГИП, поскольку определение ведущего международного научного союза является обязательной частью процедуры ЮНЕСКО. На основании этого запроса 18 декабря 2016 года я направил письмо профессору Ирине Боковой, в то время Генеральному директору ЮНЕСКО. Я написал:
«С большим удовольствием Международный союз теоретической и прикладной химии (ИЮПАК) принимает приглашение Российской академии наук стать основным спонсором заявки в ЮНЕСКО о том, что в 2019 г. Международный год Периодической таблицы химических элементов, посвященный 150-летию Периодической таблицы Менделеева….Таблица Менделеева тесно связана с миссией ИЮПАК. Химические элементы имеют решающее значение для человечества и нашей планеты, а также для промышленности. В то же время важно, чтобы, хотя они использовались для создания добавленной стоимости и продуктов, необходимых для нашей цивилизации, это делалось устойчивым образом. В частности, необходимо осознание устойчивости использования более редких элементов, которые часто либо разбавлены в земной коре, либо доступны только в очень определенных местах. Проведение Международного года Периодической таблицы химических элементов даст возможность привлечь внимание детей и пожилых людей к этим аспектам, которые имеют важное значение для будущего нашей планеты, а также отметить возникновение и развитие Периодической таблицы элементов. последние 150 лет.Другие мероприятия также будут организованы с использованием в полной мере обширной сети членов IUPAC.
Мы очень надеемся, что ЮНЕСКО удовлетворит заявку на проведение Международного года Периодической таблицы химических элементов, и ИЮПАК очень горд и гордится тем, что является основным спонсором заявки ».
Конец 2016 года был богат на события, связанные с Периодической таблицей химических элементов. 28 ноября 2016 года ИЮПАК утвердил названия и символы для четырех новых элементов: названия nihonium (Nh), moscovium (Mc), tennessine (Ts) и oganesson (Og) были официально применены к элементам 113, 115, 117, и 118 соответственно.Это событие широко освещалось в СМИ. В начале 2017 года церемонии открытия прошли в Окриджской национальной лаборатории (ORNL, США), в Объединенном институте ядерных исследований в Дубне и в Москве (Россия) и в Токио (Япония). Во время церемонии открытия в Москве письмо в ЮНЕСКО подписали директор ORNL Томас Мейсон, директор Ливерморской национальной лаборатории Лоуренса (LLNL, США) Уильям Голдштейн и директор Объединенного института ядерных исследований ( Дубна, Россия), академик Виктор Матвеев.В этом письме они поддержали призыв ИЮПАК к ЮНЕСКО об объявлении 2019 года Международным годом Периодической таблицы химических элементов. Писали:
«Уважаемая проф. Бокова,
. Одним из величайших научных достижений ХlX века было открытие Д.л. Менделеева. Он был первым, кто заметил, что свойства химических элементов периодичны по своей природе. В 2019 году мировое научное сообщество отметит 150 годовщину создания Периодической таблицы химических элементов.Сегодня, впервые за всю свою историю, Табие выглядит наиболее комплементарно: все элементы его 7 периодов открыты и получили свои окончательные названия.
За последние 100 лет человечество совершило гигантский скачок в понимании того, как образуются элементы, встречающиеся в природе. Это позволило, среди прочего, провести лабораторный синтез и изучить свойства более 20 трансурановых элементов. За последние 16 лет ученые из Объединенного института ядерных исследований (ОИЯИ, Дубна) в сотрудничестве со своими коллегами из ведущих ядерных центров США: Ливерморской и Окриджской национальных лабораторий Лоуренс, а также Университета Вандербильта и Университета Теннесси. в KnoxviIle стали первыми, кто синтезировал пять сверхтяжелых элементов, завершающих седьмой ряд Periodiс TabIe.
В 2012 году ИЮПАК назвал элемент 114 филейным (Fl), а элемент 116 – ливерморием (Lv). 28 ноября 2016 года ИЮПАК принял окончательное решение присвоить следующие названия элементам 113, 115, 117 и 118: нихоний (Nh) для элемента 113; московий (Mс) для элемента 115; теннессин (Тs) для ЭЛЕМЕНТА 117; и оганессон (Og) для элемента 118.
Периодическая таблица элементов действительно является провинцией всего человечества. Все ведущие страны мира внесли свой неоценимый вклад, пополняя Таблицу новыми элементами, изучая и конкретизируя свойства открытых.2 марта 2016 г. в Москве прошел международный коллоквиум, посвященный названию трех сверхтяжелых элементов с номерами 115, 117 и 118. Участниками коллоквиума стали более 200 делегатов из 112 стран, в том числе представительные делегации ОИЯИ (Дубна). , Россия), ORNL (США), LLNL (США), Университет Вандербильта и Университет Теннесси в Ноксвилле (США), RlKЕН (Япония), GSI (Германия), PSI (Швейцария), GANIL (Франция), IUPAC и IUPAP, и Российской академии наук, а также ведущих ученых, внесших значительный вклад в эту область ядерной медицины.
Мы, нижеподписавшиеся, от имени участников коллоквиума, принимая во внимание полномочия Д.И. Открытие Мендеева поддержало обращение ИЮПАК к ЮНЕСКО о провозглашении 2019 года Международным годом Периодической таблицы элементов ».
В течение следующих нескольких месяцев инициативу IYPT поддержали Международный союз теоретической и прикладной физики (IUPAP), Европейская ассоциация химических и молекулярных наук (EuCheMS), Международный астрономический союз, Международный союз История и философия науки и техники (IUHPS), а также более чем 80 национальными организациями, присоединившимися к IUPAC, академиями наук, химическими обществами и исследовательскими институтами.Колоссальная работа по поддержке инициативы была проделана Секретариатом ИЮПАК во главе с доктором Линн Соби.
24 января 2017 года я имел удовольствие и привилегию представить концепцию IYPT на 10 заседании Научного совета ЮНЕСКО в штаб-квартире ЮНЕСКО в Париже. В соответствии с рекомендациями Международной программы ЮНЕСКО по фундаментальной науке был сформирован Международный руководящий комитет. Тринадцать ученых со всего мира совместно с Рабочей группой Российской академии наук (ученый секретарь и академик РАН, профессор Юлия Горбунова) подготовили 15-страничный проспект МГИП.Многие добровольцы со всего мира помогали своими фотографиями, идеями и комментариями (а иногда и критикой). Проспект и концепция были представлены на Генеральной ассамблее IUPAC 49 th , 7-13 июля 2017 г., в Сан-Паулу, Бразилия. Постоянное представительство России при ЮНЕСКО и Комиссия Российской Федерации по делам ЮНЕСКО работали очень эффективно, чтобы заручиться поддержкой стран-членов ЮНЕСКО, и на своей 39 -й сессии 2 ноября 2017 г. Генеральная конференция ЮНЕСКО приняла резолюцию, в которой рекомендуется .N. Генеральная Ассамблея объявляет 2019 год Международным годом Периодической таблицы химических элементов Организации Объединенных Наций.
И это случилось.
Трудовые отношения сокращаются, Bene factum non abscedet. Чуть более 18 месяцев после того, как сэр Мартин Полякофф написал мне, Международный год Периодической таблицы химических элементов стал реальностью. 28 июля 2016 г. ему исполнилось 98 лет, когда он впервые написал мне. В то время ни мне, ни ему не приходило в голову, что IYPT, вероятно, будет самым необычным подарком на день рождения, который IUPAC когда-либо получал – в 2019 г. Мы не только будем отмечать IYPT, мы также будем отмечать столетие IUPAC.
Online erschienen: 2018-4-30
Erschienen im Druck: 2018-4-1
Битва за последние дополнения таблицы Менделеева
Настроение в замке Бэцкаског на юге Швеции должно было быть оптимистичным, когда в мае 2016 года химики и физики собрались там на симпозиум. Встреча, спонсируемая Нобелевским фондом, дала исследователям возможность подвести итоги глобальных усилий по исследованию границ ядерная наука, и отметить четыре новых элемента, которые они добавили в таблицу Менделеева несколькими месяцами ранее.Названия элементов должны были быть объявлены в течение нескольких дней – огромная честь для исследователей и стран, ответственных за открытия.
Хотя многие участники встречи были в восторге от того, как развивается их область – и заголовков, которые она генерировала, – многие были обеспокоены. Они опасались, что в процессе оценки заявлений о новых элементах были недостатки, и были обеспокоены тем, что обзоры недавних открытий не дали результатов. Некоторые считали, что недостаточно доказательств, чтобы оправдать включение наиболее спорных элементов, номеров 115 и 117.На карту была поставлена научная целостность таблицы Менделеева.
Ближе к концу встречи один ученый попросил поднять руки, должны ли они объявлять названия элементов, как планировалось. Вопрос выявил глубину беспокойства толпы. Большинство исследователей проголосовали за то, чтобы отложить объявление, говорит Уолтер Ловленд, химик-ядерщик из Университета штата Орегон в Корваллисе. И это вызвало замечательную реакцию со стороны некоторых российских ученых, которые предприняли усилия, результатом которых стали три элемента.«Они просто топнули ногами и вышли», – говорит Лавленд. «Я никогда не видел этого на научном собрании».
Несмотря на опасения, названия элементов были объявлены вскоре после этого. Нихоний (атомный номер 113), московий (115), теннессин (117) и оганессон (118) присоединились к 114 ранее открытым элементам как постоянные дополнения к таблице Менделеева. Спустя почти 150 лет после того, как Дмитрий Менделеев мечтал об этой организационной структуре, седьмой ряд таблицы был официально завершен.
Тем не менее, ход событий глубоко расстроил некоторых исследователей. Клас Фахландер, физик-ядерщик из Лундского университета в Швеции, ожидает, что результаты экспериментов в конечном итоге подтвердят утверждения о московии и теннессине. Тем не менее, он утверждает, что утверждать элементы было «преждевременно». «Мы ученые», – говорит он. «Мы не верим – мы хотим видеть доказательства».
Пока мир готовится к празднованию Международного года Периодической таблицы Менделеева в 2019 году, дебаты по поводу четырех дополнений вынудили реформировать процесс проверки других новых элементов в будущем.И это противоречие бросило тень неопределенности на нижний ряд элементов: не исключено, что руководящие органы таблицы могут переоценить некоторые из последних открытий.
Частично разногласия возникли из-за разногласий между некоторыми химиками и физиками по поводу того, кто должен быть законным хранителем таблицы Менделеева. Химики исторически занимали эту роль, потому что они открыли естественные элементы с помощью химических методов на протяжении веков работы.
Однако в течение последних нескольких десятилетий физики-ядерщики вели охоту за новыми элементами, создавая их искусственно, разбивая атомные ядра о мишени (см. «Как создать элемент»).Могут потребоваться годы, чтобы произвести всего один атом этих сверхтяжелых элементов, которые также заведомо нестабильны, расщепляясь в результате радиоактивного распада за доли секунды. Таким образом, по мере того, как группы соперничали за право первыми создавать следующие элементы, становилось все труднее устанавливать доказательства своих открытий.
Соперничество братьев и сестер
Ответственность за одобрение или отклонение новых элементов лежит на двух родственных организациях: Международном союзе чистой и прикладной химии (IUPAC) и Международном союзе чистой и прикладной физики (IUPAP).С 1999 года они полагались на заключение группы экспертов, известной как Объединенная рабочая группа (JWP), под председательством Пола Кароля, химика-ядерщика и почетного профессора Университета Карнеги-Меллона в Питтсбурге, штат Пенсильвания. Периодически восстанавливаемая для оценки заявлений об открытиях по мере их возникновения, последняя версия JWP была собрана в 2012 году и расформирована в 2016 году. Она состояла из Кароля и четырех физиков.
За это время группа присудила открытие элементов 115, 117 и 118 российско-американскому сотрудничеству под руководством опытного физика-ядерщика Юрия Оганесяна из Объединенного института ядерных исследований (ОИЯИ) в Дубне, Россия.И комиссия назначила элемент 113 исследователям из Центра науки на основе ускорителей RIKEN Nishina недалеко от Токио.
Решения JWP были публично объявлены 30 декабря 2015 года, когда IUPAC выпустил пресс-релиз, в котором провозгласил открытие четырех новых элементов (которые еще не получили своих официальных названий). Представители профсоюзов заявили, что они оперативно работали над распространением решений. Фактически, они сделали это объявление до того, как исполнительный комитет профсоюза смог утвердить выводы JWP, как указано в опубликованных правилах профсоюза 1 ; это одобрение пришло в следующем месяце.Более спорно то, что результаты JWP даже не были представлены профсоюзу физиков, IUPAP, который ожидал их увидеть, говорит Брюс МакКеллар из Мельбурнского университета в Австралии, который в то время был президентом IUPAP.
Это упущение усилило существовавшую ранее напряженность между двумя союзами. Сесилия Ярлског, физик из Лундского университета и президент IUPAP до Маккеллара, утверждает, что в течение многих лет химический союз несправедливо доминировал в процессе оценки открытий.(Кароль сообщил Nature , что при подготовке отчетов JWP он поддерживал связь почти исключительно с химическим союзом.) Выделяя свое разочарование на встрече в Швеции в 2016 году, она обвинила IUPAC в попытке привлечь внимание к открытию, объявив об открытии самостоятельно, и утверждала, что только физики «обладают компетенцией» оценивать утверждения, согласно опубликованной версии ее презентации 2 .
В этом случае напряженность в физическом и химическом сообществах усилилась из-за критики по поводу оценки JWP утверждений относительно элементов 115 и 117.JWP поддержал 3 выводы группы, открывшей эти элементы, которая обнаружила, что цепочки радиоактивного распада элементов 115 и 117 совпадают таким образом, что подкрепляет доказательства обоих открытий. Но такого рода анализ «перекрестной бомбардировки», как известно, сложен для нечетных элементов. Фахландер и его коллеги из Лундского университета сообщают 4 , что совпадение маловероятно для 115 и 117 – проблема, доведенная до сведения JWP в феврале 2015 года.
Член комиссии Роберт Барбер, физик-ядерщик из Университета Манитобы в Виннипеге, Канада, говорит, что, хотя он и его коллеги «были очень обеспокоены» перекрестной бомбардировкой, они пришли к выводу, что альтернативы этому типу доказательств нет, и они достигли консенсуса по всем своим решениям. Лавленд также поддерживает общее решение. И даже если последний JWP ошибся в некоторых деталях, говорит он, история показывает, что его решения вряд ли будут отменены.
Однако дубненский физик-ядерщик Владимир Утёнков целится в СПР.Хотя он не согласен с аргументом группы Лунда о перекрестной бомбардировке и уверен, что российско-американское заявление является убедительным, Утёнков утверждает, что группе не хватало экспертов «высокого уровня» по синтезу тяжелых элементов, и говорит, что его проекты отчетов содержали множество ошибки . Кароль защищает работу, которую он и его коллеги проделали в рамках JWP, говоря, что они пытались соблюдать опубликованные критерии, регулирующие процесс оценки. В целом, по его словам, «я считаю, что комитет очень доволен своим отчетом».
Но похоже, что большинство делегатов на встрече 2016 года в Швеции критиковали JWP. Дэвид Хинд, физик-ядерщик из Австралийского национального университета в Канберре, спросил около 50 присутствующих исследователей, считают ли они выводы комиссии «удовлетворительными с научной точки зрения». Он говорит, что получил очень мало положительных ответов на этот вопрос.
Контрольные вопросы
Несмотря на различные опасения, в июне 2016 года IUPAC и IUPAP объявили названия четырех новых элементов.Маккеллар признает, что сомневался в этом, но говорит, что большинство физиков и химиков, с которыми он консультировался, сказали ему, что общие выводы JWP – если не все детали их анализа – вероятно, были правильными.
Ян Ридейк, в то время президент подразделения неорганической химии IUPAC, говорит, что первоначальное объявление было сделано заранее, чтобы избежать утечек в прессе и удовлетворить требования лабораторий-заявителей, которые стремились сообщить новости. Для этого, по его словам, он быстро одобрил выводы JWP в декабре 2015 года от имени своего подразделения, после того как они были рецензированы и приняты для публикации в профсоюзном журнале Pure and Applied Chemistry .«Я отметил, что было проведено надлежащее судейство, поэтому дал свое« да »менее чем за час», – говорит он.
Однако неясно, проводилась ли действительно независимая проверка. По словам исполнительного директора химического союза Линн Соби, работа JWP была проанализирована в два этапа до объявления. Во-первых, его результаты были отправлены в несколько лабораторий, в основном тех, кто занимался последними открытиями, а также еще одному рецензенту, предложенному одной из лабораторий. Затем отчеты JWP были отправлены членам комитета химического союза по терминологии, номенклатуре и символам.
Соби говорит, что работа комитета заключалась в проверке ошибок в формулировках и форматировании, и поэтому сами лаборатории должны были обеспечить научную проверку. Она говорит, что это было уместно, учитывая, что они являются экспертами в этой области. Однако один из этих исследователей, Утенков, полагал, что химический союз нанял 15 независимых экспертов для проведения научной экспертизы. Он предположил, что его и двух дубненских коллег попросили проверить в отчетах только факты и цифры.«Я не знаю, как нас можно считать независимыми судьями», – говорит он.
Оглядываясь назад, Ярлског желает, чтобы она и остальное физическое сообщество уделяли больше внимания тому, как был завершен весь процесс оценки, в частности, рецензированию выводов JWP. «Мне будут сниться кошмары о том, насколько мы небрежны».
Для решения поднятых вопросов оба профсоюза согласовали новые процедуры оценки любых будущих элементов. Согласно измененным правилам, выпущенным в мае (см.nature.com/2ji1gv4), президенты IUPAC и IUPAP теперь получат возможность ознакомиться с выводами JWP, прежде чем вместе объявить о своих выводах. Для этого они проведут независимую экспертную оценку наряду с анализом Pure and Applied Chemistry .
Маккеллар говорит, что изменения будут иметь положительный эффект. « Каждый профсоюз приобрел немало доверительных отношений, работая вместе над этим», – говорит он.
Но эти изменения не удовлетворят некоторых критиков, таких как Ярлског.«Я просто не думаю, что новые правила что-то изменят», – говорит она.
СМОТРИТЕ СВОЙ ЯЗЫК! Многое уходит в именование элемента
Я очень мало знаю о науке, но слышал о Периодической таблице элементов.
Недавно я увидел комикс, в котором один человек показывал другому неожиданный предмет из таблицы Менделеева. Это был «элемент неожиданности», представленный смайликом для изумленного лица.
😲
И по какой-то сумасшедшей причине я задумался, назван ли полоний в честь персонажа Шекспира в «Гамлете» Полония.Он отец Лаэрта и Офелии.
Так я начал интересоваться, как элементы получили свои имена.
Периодическая таблица представляет собой таблицу всех элементов в порядке их атомного номера и массы.
Русский химик Дмитрий Менделеев решил организовать элементы в 1860-х годах.
Усилия были монументальными. Живая наука говорит: «Расположить элементы в каком-либо порядке было бы довольно сложно. В то время было известно менее половины элементов, а для некоторых из них были даны неверные данные.Это было похоже на работу над действительно сложным пазлом, состоящим только из половины частей, а некоторые из них деформированы ». (См. Arkansasonline.com/105live.)
Процесс наименования элемента формальный и жесткий. Международный союз теоретической и прикладной химии, арбитр процесса присвоения имен, говорит просто: «Элементы могут быть названы в честь мифологической концепции, минерала, места или страны, собственности или ученого». Ученые не осмелились бы назвать элемент своим именем.
Ученый может предложить имя, и одно из подразделений международного союза сначала принимает идею, а затем дает возможность общественности высказывать свои замечания в течение пяти месяцев. (Я отправил в отдел по электронной почте, чтобы спросить, какие были некоторые из публичных комментариев. Я не получил ответа.) Окончательный выбор опубликован в журнале Pure and Applied Chemistry.
Несмотря на всю эту церемонию, названия некоторых элементов просто скучны. Железо, латинское название которого обозначает «феррум», означает «серый».
Литий происходит от греческого слова «камень».
Бром, обозначаемый символом Br, происходит от греческого слова «зловоние». Это потому, что пахнет бромидом. (Боюсь, что в тот день ни у кого не было своих мыслящих кепок.)
Точно так же металлический элемент осмий происходит от греческого слова, обозначающего запах. (Опять же, где были креативные намёщики?)
Гелий, который большинству из нас известен как газ, удерживающий воздушные шары в воздухе, был назван в честь греческого слова, обозначающего солнце, гелиос, потому что этот элемент был впервые обнаружен во время изучения Солнца.
УCobalt есть небольшая история.Название металлического элемента происходит от немецкого слова гоблин. Видимо, добытчики серебра когда-то считали, что эти гоблины или озорные эльфы украли серебро и заменили его кобальтом.
Уран, нептуний и плутоний были названы в честь планет Уран, Нептун и Плутон. Время было ключевым для этих названий элементов. Уран только что был открыт, поэтому немецкий ученый, нашедший уран, решил почтить память новой планеты на блоке. Нептуний был назван в честь Нептуна, но также он удобно расположен сразу после урана в периодической таблице.И плутоний, названный в честь Плутона, следует за ураном.
Криптон – это редкий бесцветный газ, поэтому он был назван от греческого слова «скрытый» – криптос. (Склеп, место захоронения, часто находящееся под церковью, происходит от того же корня.) Стыдно сказать, как часто я путаю его с криптонитом, тем воображаемым веществом, которое делает Супермена слабым.
Шведская деревня Иттерби с населением 2 900 человек известна тем, что является источником названий четырех элементов. Иттрий, тербий, эрбий и иттербий были обнаружены на руднике Иттерби.Нигде больше не было обнаружено столько элементов.
Кстати, иттрийпомогает нам получать цветные изображения на экране телевизора.
Никель происходит от немецкого слова “мошенник” или “демон”. Причина в том, что никель имеет обманчивый медный цвет.
Что касается мифических имен, то двое составляют семейное дело. Ниобий назван в честь Ниобы, дочери Тантала.
Тантал назван в честь Тантала. В словаре говорится, что этот элемент получил свое название «из-за его высокой устойчивости к абсорбции кислот, даже при погружении в них.”Король Тантал был обречен стоять в воде, которая истощалась, когда он пытался ее пить, а когда он тянулся за фруктами, они всегда уходили вне досягаемости. Довольно соблазнительно.
Ниобий извлекается из тантала.
Эйнштейний назван в честь Альберта Эйнштейна. Фермий назван в честь Энрико Ферми. В словаре говорится, что оба являются синтетическими трансурановыми металлическими элементами. Я знаю значения синтетического и металлического. Трансурановая означает, что атомный номер больше 92. Что ж, это действительно проясняет мою путаницу.
Четыре последних названных элемента: нихоний (для Японии), московий (для Москвы), теннессин (для Теннесси) и оганессон (для российского физика-ядерщика Юрия Оганесяна). Все эти элементы созданы искусственно. Для меня это звучит как обман.
Полоний, кстати, назван в честь Польши. Мария Кюри, которая отождествляла элемент со своим мужем Пьером, была полькой.
Менделеев, создатель таблицы, носит менделевий в его честь. Оказывается, он тоже трансурановый элемент.
Источники: Словарь американского наследия, Live Science, Международный союз чистой и прикладной химии, Atlas Obscura, BBC.com, Reuters. Добраться до Бернадетт по телефону
[адрес электронной почты защищен]
Четыре новых имени элемента будут добавлены в периодическую таблицу
Джейкоб Арон
Как раз тогда, когда вы думали, что все сделали правильно
Chamussy / SIPA / Rex / Shutterstock
Забудьте о земле, ветре, воде и огне – в городе есть четыре новых элемента.Международный союз теоретической и прикладной химии (IUPAC) объявил, что недавно открытые элементы 113, 115, 117 и 118 теперь будут известны как нихоний, московий, теннессин и оганессон, ожидая публичного рассмотрения.
Четыре элемента, составляющие седьмую строку периодической таблицы, были официально признаны в январе этого года после открытий, сделанных командами из Японии, России и США, которые представили имена руководящему органу ИЮПАК.
Исследователи из RIKEN в Вако, Япония, предложили для своего открытия нихоний (символ Nh), элемент 113, после Нихон, одного из японских слов, обозначающих «Япония».
Московий (Mc) и теннессин (Ts), формально элементы 115 и 117, были предложены группами из Объединенного института ядерных исследований в Дубне, Россия, и Окриджской национальной лаборатории, Университета Вандербильта и Ливерморской национальной лаборатории Лоуренса (LLNL). США, после Москвы и Теннесси.
Наконец, оганессон (Og) был предложен командами Дубны и LLNL после Юрия Оганесяна, российского физика, который помог открыть элемент 114 в 1999 году. Он и элемент 116, теперь известные как флеровий и ливерморий, были последними, которые присоединились к таблице Менделеева. , еще в 2011 году.
IUPAC ограничивает выбор названий элементов мифологическими персонажами, минералами, местами, свойствами элемента или учеными – исключая публичные призывы назвать элемент в честь фронтмена хэви-метал группы Motörhead Лемми, который умер в начале этого года.
Теперь новые имена пройдут пятимесячную публичную проверку на предмет возможных возражений, что означает, что они могут официально присоединиться к периодической таблице к концу этого года. А пока охота за более тяжелыми элементами и первой записью восьмого ряда продолжается.
Статья изменена на 9 июня 2016 г.
