Строение атома 11 класс онлайн-подготовка на Ростелеком Лицей
Строение атома
В переводе с греческого языка, слово «атом» означает «неделимый». Однако, были открыты явления, которые демонстрируют возможность его деления. Это испускание рентгеновских лучей, испускание катодных лучей, явление фотоэффекта, явление радиоактивности. Электроны, протоны и нейтроны – это частицы, из которых состоит атом. Они называются субатомными частицами.
Табл. 1
|
атом |
||
|
ядро |
электроны |
|
|
протоны |
нейтроны |
|
|
p+ |
no |
e– |
|
Масса протона |
Масса нейтрона |
Масса электрона |
|
1,0073 а. |
1,0087 а.е.м. |
0,0005 а.е.м. |
|
Заряд протона |
Заряд нейтрона |
Заряд электрона |
|
+1 |
0 |
-1 |
Кроме протонов, в состав ядра большинства атомов входят
Масса атома (массовое число) равна сумме масс, составляющих его ядро протонов и нейтронов. Массовое число обозначается буквой А. Из названия этой величины видно, что она тесно связана с округленной до целого числа атомной массой элемента.
Массовое число обозначается буквой А. Из названия этой величины видно, что она тесно связана с округленной до целого числа атомной массой элемента.
Здесь A – массовое число атома (сумма протонов и нейтронов), Z – заряд ядра (число протонов в ядре), N – число нейтронов в ядре. Согласно учению об изотопах, понятию «химический элемент» можно дать такое определение:
Химическим элементом называется совокупность атомов с одинаковым зарядом ядра.
Некоторые элементы существуют в виде нескольких изотопов. «Изотопы» означает «занимающий одно и тоже место». Изотопы имеют одинаковое число протонов, но отличаются массой, т. е. числом нейтронов в ядре (числом N). Поскольку нейтроны практически не влияют на химические свойства элементов, все изотопы одного и того же элемента химически неотличимы.
Изотопы
Изотопами называются разновидности атомов одного и того же химического элемента с одинаковым зарядом ядра (то есть с одинаковым числом протонов), но с разным числом нейтронов в ядре.
Изотопы отличаются друг от друга только массовым числом. Это обозначается либо верхним индексом в правом углу, либо в строчку: 12С или С-12. Если элемент содержит несколько природных изотопов, то в периодической таблице Д. И. Менделеева указывается, его средняя атомная масса с учетом распространённости. Например, хлор содержит 2 природных изотопа 35Cl и 37Cl, содержание которых составляет соответственно 75 % и 25 %. Таким образом, атомная масса хлора будет равна:
Аr(Cl) = 0,75 . 35 + 0,25 . 37 = 35,5
Для тяжёлых искусственно-синтезированных атомов приводится одно значение атомной массы в квадратных скобках. Это атомная масса наиболее устойчивого изотопа данного элемента.
Основные модели строения атома
Исторически первой в 1897 году была модель атома Томсона.
Рис. 1. Модель строения атома Дж. Томсона
Английский физик Дж. Дж. Томсон предположил, что атомы состоят из положительно заряженной сферы, в которую вкраплены электроны (рис. 1). Эту модель образно называют «сливовый пудинг», булочка с изюмом (где «изюминки» – это электроны), или «арбуз» с «семечками» – электронами. Однако от этой модели отказались, т. к. были получены экспериментальные данные, противоречащие ей.
Рис. 2. Модель строения атома Э. Резерфорда
В 1910 году английский физик Эрнст Резерфорд со своими учениками Гейгером и Марсденом провели эксперимент, который дал поразительные результаты, необъяснимые с точки зрения модели Томсона. Эрнст Резерфорд доказал на опыте, что в центре атома имеется положительно заряженное ядро (рис. 2), вокруг которого, подобно планетам вокруг Солнца, вращаются электроны. Атом в целом электронейтрален, а электроны удерживаются в атоме за счет сил электростатического притяжения (кулоновских сил). Эта модель имела много противоречий и главное, не объясняла, почему электроны не падают на ядро, а также возможность поглощения и излучения им энергии.
Датский физик Н. Бор в 1913 году, взяв за основу модель атома Резерфорда, предложил модель атома, в которой электроны-частицы вращаются вокруг ядра атома примерно так же, как планеты обращаются вокруг Солнца.
Рис. 3. Планетарная модель Н. Бора
Бор предположил, что электроны в атоме могут устойчиво существовать только на орбитах, удаленных от ядра на строго определенные расстояния. Эти орбиты он назвал стационарными. Вне стационарных орбит электрон существовать не может. Почему это так, Бор в то время объяснить не мог. Но он показал, что такая модель (рис. 3) позволяет объяснить многие экспериментальные факты.
Формы атомных орбиталей
В настоящее время для описания строения атома используется квантовая механика. Это наука, главным аспектом в которой является то, что электрон обладает свойствами частицы и волны одновременно, т. е. корпускулярно-волновым дуализмом. Согласно квантовой механике, область пространства, в которой вероятность нахождения электрона наибольшая, называется орбиталью.
Рис. 4. Формы атомных орбиталей
В электронной оболочке любого атома ровно столько электронов, сколько протонов в его ядре, поэтому атом в целом электронейтрален. Электроны в атоме размещаются так, чтобы их энергия была минимальной. Чем дальше электрон находится от ядра, тем больше орбиталей и тем сложнее они по форме. На каждом уровне и подуровне может помещаться только определенное количество электронов. Подуровни, в свою очередь, состоят из одинаковых по энергии
На первом энергетическом уровне, наиболее близком к ядру, может существовать одна сферическая орбиталь (1s). На втором энергетическом уровне – сферическая орбиталь, большая по размеру и три р-орбитали: 2s2ppp. На третьем уровне: 3s3ppp
На втором энергетическом уровне – сферическая орбиталь, большая по размеру и три р-орбитали: 2s2ppp. На третьем уровне: 3s3ppp
Кроме движения вокруг ядра, электроны обладают еще движением, которое можно представить, как их движение вокруг собственной оси. Это вращение называется спином (в пер. с англ. «веретено»). На одной орбитали могут находиться лишь два электрона, обладающих противоположными (антипараллельными) спинами.
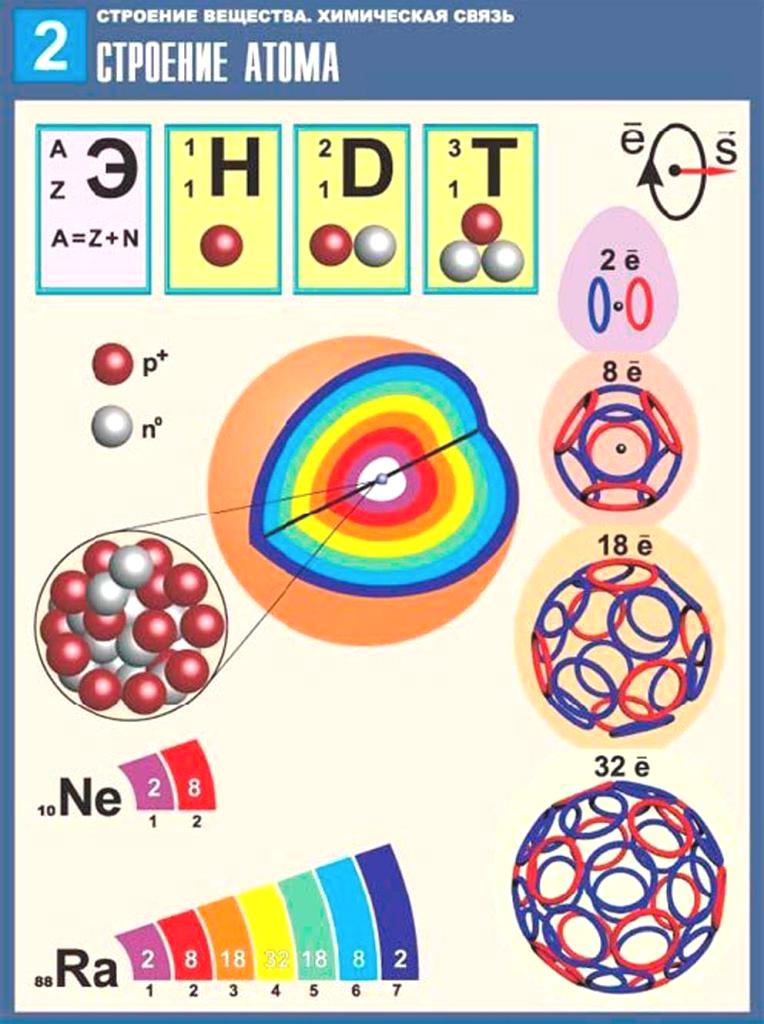
Максимальное число электронов на энергетическом уровне определяется по формуле N = 2n2.
Где n – главное квантовое число (номер энергетического уровня) (см. табл. 2).
Табл. 2
|
Энергетический уровень |
N |
Электронная конфигурация |
|
1-ый |
2 |
1s2 |
|
2-ой |
8 |
2s22p6 |
|
3-ий |
18 |
3s23p63d10 |
|
4-ый |
32 |
4s24p64d104f14 |
В зависимости от того, на какой орбитали находится последний электрон, различают s, p-, d-элементы. Элементы главных подгрупп относятся к s, p-элементам. В побочных подгруппах находятся
Элементы главных подгрупп относятся к s, p-элементам. В побочных подгруппах находятся
Примеры написания электронно-графических формул атомов
Графическая схема строения электронных слоев атомов (электронно-графическая формула).
Для описания расположения электронов на атомных орбиталях используют электронную конфигурацию. Для её написания в строчку пишутся орбитали в условных обозначениях (s-, p-, d-, f-орбитали), а перед ними – числа, обозначающие номер энергетического уровня. Чем больше число, тем дальше электрон находится от ядра. В верхнем регистре, над обозначением орбитали, пишется количество электронов, находящихся на данной орбитали (рис. 5).
Рис. 5
Графически распределение электронов на атомных орбиталях можно представить в виде ячеек. Каждая ячейка соответствует одной орбитали. Для р-орбитали таких ячеек будет три, для d-орбитали – пять, для f-орбитали – семь. В одной ячейке может находиться 1 или 2 электрона. Согласно правилу Гунда, электроны распределяются на одинаковых по энергии орбиталях (например, на трех p-орбиталях) сначала по одному, и лишь когда в каждой такой орбитали уже находится по одному электрону, начинается заполнение этих орбиталей вторыми электронами. Такие электроны называют спаренными. Объясняют это тем, что в соседних ячейках электроны меньше отталкиваются друг от друга, как одноименно заряженные частицы.
Для р-орбитали таких ячеек будет три, для d-орбитали – пять, для f-орбитали – семь. В одной ячейке может находиться 1 или 2 электрона. Согласно правилу Гунда, электроны распределяются на одинаковых по энергии орбиталях (например, на трех p-орбиталях) сначала по одному, и лишь когда в каждой такой орбитали уже находится по одному электрону, начинается заполнение этих орбиталей вторыми электронами. Такие электроны называют спаренными. Объясняют это тем, что в соседних ячейках электроны меньше отталкиваются друг от друга, как одноименно заряженные частицы.
См. рис. 6 для атома 7N.
Рис. 6
Электронная конфигурация атома скандия
21Sc: 1s22s22p63s23p64s23d1
Электроны внешнего энергетического уровня называются валентными.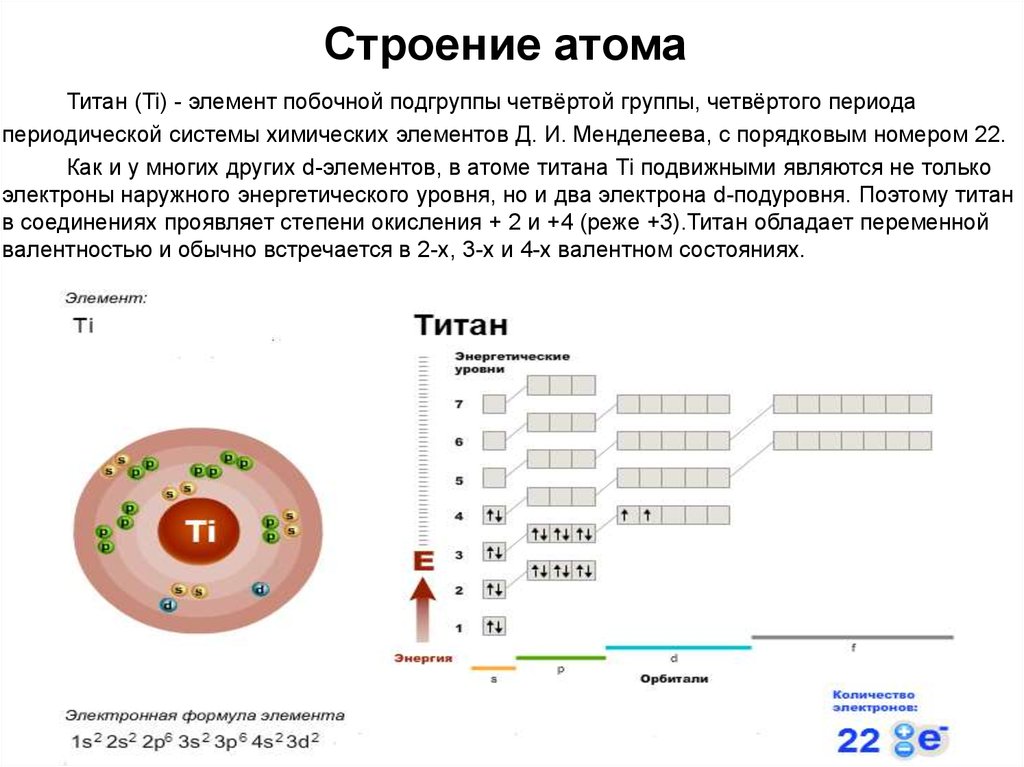 21Sc относится к d-элементам.
21Sc относится к d-элементам.
Подведение итога урока
На уроке было рассмотрено строение атома, состояние электронов в атоме, введено понятие «атомная орбиталь и электронное облако». Учащиеся узнали, что такое форма орбиталей (s-, p-, d-орбитали), каково максимальное число электронов на энергетических уровнях и подуровнях, распределение электронов по энергетическим уровням, что такое s-, p– и d-элементы. Приведена графическая схема строения электронных слоев атомов (электронно-графическая формула).
Список литературы
- Рудзитис Г. Е. Химия. Основы общей химии. 11 класс: учебник для общеобразовательных учреждений: базовый уровень / Г. Е. Рудзитис, Ф. Г. Фельдман. – 14-е изд. – М.: Просвещение, 2012.
- Попель П. П. Химия: 8 кл.: учебник для общеобразовательных учебных заведений / П.
 П. Попель, Л. С. Кривля. – К.: ИЦ «Академия», 2008. – 240 с.: ил.
П. Попель, Л. С. Кривля. – К.: ИЦ «Академия», 2008. – 240 с.: ил. - А. В. Мануйлов, В. И. Родионов. Основы химии. Интернет-учебник.
Дополнительные рекомендованные ссылки на ресурсы сети Интернет
- Интернет-портал «internerurok.ru» (Источник)
- Интернет-портал «hemi.nsu.ru» (Источник)
- Интернет-портал «chemport.ru» (Источник)
- Интернет-портал «Химик» (Источник)
Домашнее задание
- №№ 5-7 (с. 22) Рудзитис Г. Е. Химия. Основы общей химии. 11 класс: учебник для общеобразовательных учреждений: базовый уровень / Г. Е. Рудзитис, Ф. Г. Фельдман. – 14-е изд. – М.: Просвещение, 2012.
- Напишите электронные формулы для следующих элементов: 6C, 12Mg, 16S, 21Sc.
- Элементы имеют следующие электронные формулы: а) 1s22s22p4.б) 1s22s22p63s23p1.
 в) 1s22s22p
в) 1s22s22p
конспект урока на тему “Строение атома”
Тема: Строение атома.
Дата проведения урока:
Тема: Строение атома. 8 класс
Цель:
| Сформировать представление о строении атома.
|
Задачи: | 1.Способствовать формированию представлений о сложности строения атома, составе атомных ядер, физическом смысле атомного номера; формированию умений давать характеристику элементарных частиц (протонов, нейтронов и электронов), определять число протонов
в ядре атома химического элемента. 2. Продолжить развитие умений анализировать, сопоставлять, сравнивать, обобщать, делать выводы, работать самостоятельно, прогнозировать, структурировать и представлять информацию в наглядном виде. 3.Воспитывать умение вести дискуссию, участвовать в коллективном обсуждении вопросов. |
Оборудование:
Тип урока: | Учебник, таблицы, иллюстрирующие сложное строение атома (опыт Резерфорда, строение атома)
Урок усвоения новых знаний.
|
Технологическая карта
Этапы урока | Деятельность учителя | Деятельность учеников. |
1. Организационный момент (2 мин.). | Приветствие, проверка отсутствующих и готовности учеников к уроку. | Приветствуют учителя, называют отсутствующих, демонстрируют готовность к уроку. |
2. Актуализация знаний. ( 13 мин.) 2.1. Проверка домашнего задания.
2.2. Мотивация. |
Фронтальный опрос.
Сообщает тему урока. |
Отвечают на вопросы учителя.
Открывают тетрадь, записывают дату и новую тему. |
3. Формирование новых знаний (20 мин.) 3.1 Модели строения атома.
3.
3.3 Физический смысл атомного номера элемента. |
Формирует представление о моделях строения атома. Обращает внимание на таблицу на доске.
Характеризует параметры атома.
Дает представление о физическом смысле атомного номера элемента. |
Слушают, анализируют, смотрят на доску.
Слушают.
Слушают, конспектируют.
Слушают, конспектируют. |
4. Применение новых знаний и умений. (6 мин.). | Формулирует вопросы для закрепления новой темы. | Отвечают на вопросы. |
5.
Домашнее
задание (2 мин. | Объясняет выполнение домашнего задания. | Записывают домашнее задание в дневник. |
6. Рефлексия (2 мин.). | Организация оценки составление синквейна по теме урока. | Составляют синквейн по теме урока. |
Ход урока.
1. Организационный момент.
Актуализация знаний.
2.1 Проверка домашнего задания.
Фронтальный опрос по теме «Периодическая система химических элементов».
1. Дайте определение понятий: группа, период, А-группа, В-группа.
2. Укажите атомный номер, номер периода и номер группы, в которых находятся химические элементы:
фтор, магний, железо.
3. Укажите химический
элемент, простое вещество которого имеет более выраженные металлические свойства:
натрий или алюминий. Ответ поясните.
Ответ поясните.
4. Укажите химические элементы, которые образуют высший оксид состава Э2O5. Ответ поясните.
2.1 Мотивация.
Сегодня
мы поговорим о строении атома. На всех прошедших уроках мы встречались с этим
понятием. Наш век не случайно называют атомным ( атомные корабли, атомные
электростанции, атомные бомбы ). К атомизму мы привыкаем с детства и не
удивляемся тому, что все окружающие нас тела состоят из мельчайших частичек.
Противоестественно не понимать величия атомистической идеи и не оценивать тех
трудностей, которые удалось преодолеть человеческому уму на длительном пути её
утверждения. Именно поэтому вы, как современные дети, должны знать об
особенностях строения атома, иметь представление об элементарных частицах
атома, познакомиться с ядерной моделью атома. Кроме того, сегодня на уроке мы
ещё раз постараемся доказать, что именно строение атома является главной
характеристикой элемента и вспомним, как определять число протонов, электронов
в атоме любого химического элемента.
3. Формирование новых знаний.
Итак, тема нашего урока – «Строение атома». Тему дети записывают в тетрадь.
До конца XIX в. атом считали неделимой частицей, но последовавшие позже открытия (радиоактивность, фотоэффект) поколебали это убеждение. Сейчас известно, что атом состоит из элементарных частиц, основные из которых – протон, нейтрон, электрон.
Прямым доказательством сложности строения атома явилось и открытие самопроизвольного распада атомов некоторых элементов с испусканием невидимых глазу лучей. Это явление, открытое в 1896 г. французским ученым Анри Беккерелем, получило название радиоактивности. В 1897 г. английский физик Дж. Дж. Томсон установил существование в атоме электронов — отрицательно заряженных частиц.
Эти открытия свидетельствовали о том, что атом имеет сложное строение.
3.1 Модели строения атома.
После
открытия основных элементарных частиц, входящих в состав атома, встал вопрос об
их местонахождении, т. е. о строении атома. В 1911 г. Томсон предложил свою
модель строения атома, которая получила условное название «пудинг с изюмом».
Согласно этой модели атом представляет собой некую субстанцию, в которой
равномерно распределены протоны, нейтроны и электроны. Число протонов равно
числу электронов, поэтому атом в целом электронейтрален.
е. о строении атома. В 1911 г. Томсон предложил свою
модель строения атома, которая получила условное название «пудинг с изюмом».
Согласно этой модели атом представляет собой некую субстанцию, в которой
равномерно распределены протоны, нейтроны и электроны. Число протонов равно
числу электронов, поэтому атом в целом электронейтрален.
В 1913 г. Резерфорд ставит опыт, результаты которого модель Томсона объяснить не может. Это заставляет Резерфорда предложить свою модель строения атома (посмотрите на рисунок №15 на странице 42 учебника), получившую название планетарной. Согласно этой модели атом состоит из ядра, в котором сконцентрирована основная масса атома, поскольку ядро содержит протоны и нейтроны; вокруг ядра на огромной скорости вращаются электроны. Поскольку модель Резерфорда содержала ряд противоречий, Н.Бором были введены постулаты, устраняющие эти противоречия.
1-й
постулат. Электроны
вращаются вокруг ядра не по произвольным, а по строго определенным,
стационарным орбитам.
2-й постулат. При движении по стационарной орбите электрон не излучает и не поглощает энергию. Изменение энергии происходит при переходе электрона с одной стационарной орбиты на другую.
Но теория Резерфорда–Бора дает удовлетворительные результаты только для атома водорода. Современные представления о строении атома подчиняются квантовой модели строения атома.
Из курса химии 7-го класса вы уже знаете одно определение атома как мельчайшей, химически неделимой частицы. Теперь можно дать еще одно, физическое, определение этого понятия. Давайте запишем его в конспект:
Атом — электронейтральная частица, состоящая из положительно за-
ряженного ядра и отрицательно заряженных электронов.
Позже было установлено, что ядро атома также имеет сложное строение.
Оно состоит из частиц двух типов: протонов и нейтронов.
Протон и
нейтрон имеют практически одинаковую массу, равную примерно 1 u, т.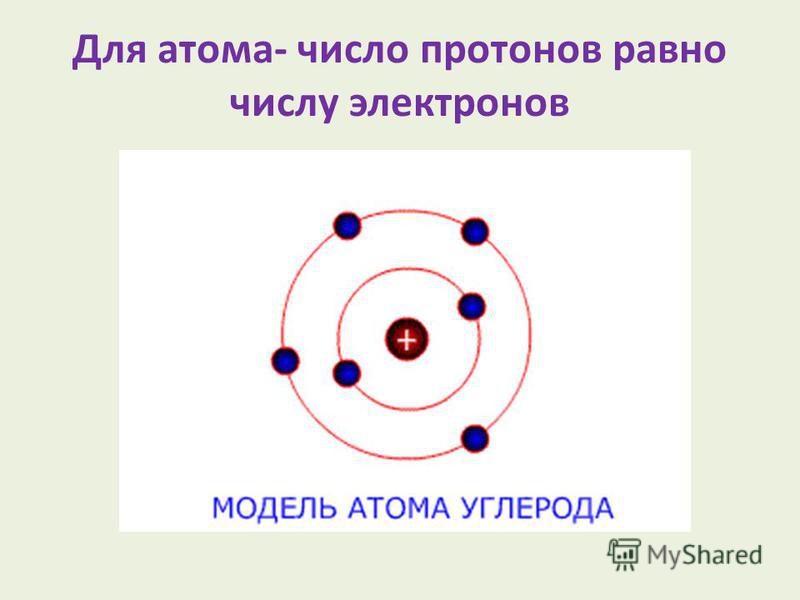 е.
одной атомной единице массы. Протон (его символ р) имеет относительный
заряд 1+, а нейтрон (символ n) электронейтрален.
е.
одной атомной единице массы. Протон (его символ р) имеет относительный
заряд 1+, а нейтрон (символ n) электронейтрален.
Относительный заряд электрона (его символическое обозначение е−
) равен 1−, а масса примерно в 1840 раз меньше массы протона, т. е. равна
1/1840u.
3.2 Параметры для характеристики атомов.
Учащиеся записывают краткую характеристику в конспекты.
Массовое число А – сумма чисел протонов и нейтронов атома.
Заряд ядра Z – число протонов, определяется по порядковому номеру элемента в таблице Д.И.Менделеева. В 1913 г. английским физиком Г.Мозли было установлено, что положительный заряд ядра атома (в условных единицах) равен порядковому номеру элемента в периодической системе Д.И.Менделеева.
Число нейтронов N определяется как разность между массовым числом и зарядом ядра (учитывая, что массой электрона можно пренебречь).
Изотопы – атомы
одного элемента, имеющие одинаковый заряд ядра (следовательно, и количество
электронов), но различное число нейтронов (следовательно, различные массовые числа). Например, элемент водород имеет три изотопа: протий, дейтерий и тритий. Первые
два существуют в природе, тритий получен искусственным путем. Подавляющее
большинство химических элементов имеет разное число природных изотопов с разным
процентным содержанием каждого из них. Относительная атомная масса элемента,
которая приводится в периодической системе, – это средняя величина массовых
чисел природных изотопов данного элемента с учетом процентного содержания
каждого из этих изотопов. Химические свойства всех изотопов одного химического
элемента одинаковы. Следовательно, химические свойства элемента зависят не от
атомной массы, а от заряда ядра.
Например, элемент водород имеет три изотопа: протий, дейтерий и тритий. Первые
два существуют в природе, тритий получен искусственным путем. Подавляющее
большинство химических элементов имеет разное число природных изотопов с разным
процентным содержанием каждого из них. Относительная атомная масса элемента,
которая приводится в периодической системе, – это средняя величина массовых
чисел природных изотопов данного элемента с учетом процентного содержания
каждого из этих изотопов. Химические свойства всех изотопов одного химического
элемента одинаковы. Следовательно, химические свойства элемента зависят не от
атомной массы, а от заряда ядра.
3.3 Физический смысл атомного номера:
В
1913—1916 гг. рядом теоретических и экспериментальных исследований было
установлено, что атомный (порядковый) номер элемента в
периодической системе равен заряду ядра его атомов. Именно в этом
заключается физический смысл атомного номера элемента. (Запишем в конспект)
(Запишем в конспект)
Заряд ядра определяется числом протонов, и, поскольку атом в целом электронейтрален, очевидно, что число протонов в его ядре равно числу электронов.
Увеличение атомного номера элемента связано с возрастанием числа про-
тонов в ядре, т. е. с увеличением положительного заряда ядра.
Таким образом, можно заключить, что заряд ядра является главной характеристикой элемента, определяя его положение в периодической системе, а следовательно, все свойства этого элемента и его соединений.
Поэтому современная формулировка периодического закона звучит так:
свойства атомов химических элементов, а также состав и свойства образуемых ими веществ находятся в периодической зависимости от зарядов атомных ядер.
Периодический
закон дал импульс к изучению внутреннего строения веществ, в том числе и
строения атома. В свою очередь, теория строения атома способствовала
пониманию сущности периодического закона и периодической системы химических элементов,
наполнила их современным содержанием и определила пути дальнейшего развития.
4. Применение новых знаний.
А сейчас, ребята, давайте с вами повторим то, что узнали сегодня на уроке: (учащиеся, совместно с учителем отвечают на вопросы).
Кому принадлежит теория ядерной модели атома? Какое она имеет название?
Предполагаемый ответ: теория ядерной модели атома принадлежит Резерфорду, она называется планетарной.
Каково строения атома? ( кто-нибудь из учащихся рисует модель простейшего атома водорода из электрона, протона, нейтрона ).
Что является главной характеристикой данного химического элемента?
Предполагаемый ответ: главной характеристикой химического элемента является число протонов в ядре атома.
Определите число электронов в атомах химических элементов магния и алюминия.
Предполагаемый ответ: у магния 12 электронов, у алюминия – 13.
Определите
число протонов в атомах химических элементов фосфора и хлора.
Предполагаемый ответ: у фосфора 15 протонов, у хлора – 17, что равно порядковому номеру химического элемента.
Как образуется отрицательный ион?
Предполагаемый ответ: атом приобретает электрон – отрицательно заряженную частицу.
Найдите ряд, в котором правильно указано количество электронов в нейтральных атомах химических элементов Ве, В, С:
а) 3,4,5;
б) 4,5,6;
в) 9,10,12.
Предполагаемый ответ: вариант б – 4,5,6.
Найдите ряд, в котором верно указаны число протонов в атомах химических элементов Аl, Si, P и заряды ядра:
а) 27, 28, 31;
б) +13, +14, +15;
в) 13, 14,15.
Предполагаемый ответ: вариант б – +13, +14, +15.
5. Домашнее задание.
§ 9 учебника, упражнения 3,4 с. 44-45 учебника–длявсех. По выбору учащихся– сообщение, доклад или презентация по выбранной
Теме «Хочу узнать»
(подготовить к уроку обобщения и систематизации знаний «Строение атома и систематизация
элементов»).
6. Рефлексия.
Составить синквейн
к термину «атом».
1. Название синквейна.
2. 2 глагола.
3. 3 прилагательных.
4. Обобщающая фраза.
5. Существительное.
2.2: Структура атома и то, как мы ее представляем
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 217246
Развитие навыков
- Опишите три субатомные частицы, из которых состоят атомы
- Дайте определение изотопам и приведите примеры для нескольких элементов
- Записывать и интерпретировать символы, изображающие атомный номер, массовое число и заряд атома или иона
Учебник по субатомным частицам и атомам
Видео \(\PageIndex{1}\) : Учебник по тому, что такое атом от Fuse School Chemistry.
Развитие современной атомной теории многое открыло о внутренней структуре атомов. Стало известно, что атом содержит очень маленькое ядро, состоящее из положительно заряженных протонов и незаряженных нейтронов, окруженное гораздо большим объемом пространства, содержащим отрицательно заряженные электроны. Ядро содержит большую часть массы атома, потому что протоны и нейтроны намного тяжелее электронов, тогда как электроны занимают почти весь объем атома. Диаметр атома порядка 10 −10 м, тогда как диаметр ядра составляет примерно 10 −15 м — примерно в 100 000 раз меньше. Чтобы получить представление об их относительных размерах, рассмотрим следующее: если бы ядро было размером с чернику, атом был бы размером с футбольный стадион (рис. \(\PageIndex{1}\)).
\(\PageIndex{1}\)).
Рисунок \(\PageIndex{1}\): Если бы атом можно было увеличить до размеров футбольного стадиона, ядро было бы размером с ягоду черники. (в центре кредита: модификация работы «babyknight» / Wikimedia Commons; право на авторство: модификация работы Паксона Вулбера).
Атомы и составляющие их протоны, нейтроны и электроны чрезвычайно малы. Например, атом углерода весит менее 2 \(\times\) 10 −23 г, а электрон имеет заряд менее 2 \(\times\) 10 −19 Кл (кулон). При описании свойств крошечных объектов, таких как атомы, мы используем соответственно малые единицы измерения, такие как атомная единица массы (а.е.м.) и фундаментальная единица заряда (е). Изначально аму определяли по водороду, самому легкому элементу, а затем по кислороду. С 1961, он был определен в отношении наиболее распространенного изотопа углерода, атомам которого приписана масса ровно 12 а.е.м. (Этот изотоп известен как «углерод-12», что будет обсуждаться далее в этом модуле. ) Таким образом, одна а.е.м. точно равна \(1/12\) массы одного атома углерода-12: 1 а.е.м. = 1,6605 \( \раз\) 10 −24 г. (Дальтон (Да) и единая атомная единица массы (u) являются альтернативными единицами, эквивалентными а.е.м.) Фундаментальная единица заряда (также называемая элементарным зарядом) равна величине заряда электрона (е). с e = 1,602 \(\times\) 10 −19 C.
) Таким образом, одна а.е.м. точно равна \(1/12\) массы одного атома углерода-12: 1 а.е.м. = 1,6605 \( \раз\) 10 −24 г. (Дальтон (Да) и единая атомная единица массы (u) являются альтернативными единицами, эквивалентными а.е.м.) Фундаментальная единица заряда (также называемая элементарным зарядом) равна величине заряда электрона (е). с e = 1,602 \(\times\) 10 −19 C.
Протон имеет массу 1,0073 а.е.м. и заряд 1+. Нейтрон — это немного более тяжелая частица с массой 1,0087 а.е.м. и нулевым зарядом; как следует из названия, он нейтрален. Электрон имеет заряд 1– и представляет собой гораздо более легкую частицу с массой около 0,00055 а.е.м. (чтобы сравнять массу одного протона, потребуется около 1800 электронов. Свойства этих фундаментальных частиц приведены в таблице \(\PageIndex {1}\) (Внимательный студент может заметить, что сумма субатомных частиц атома не равна фактической массе атома: общая масса шести протонов, шести нейтронов и шести электронов равна 12,09.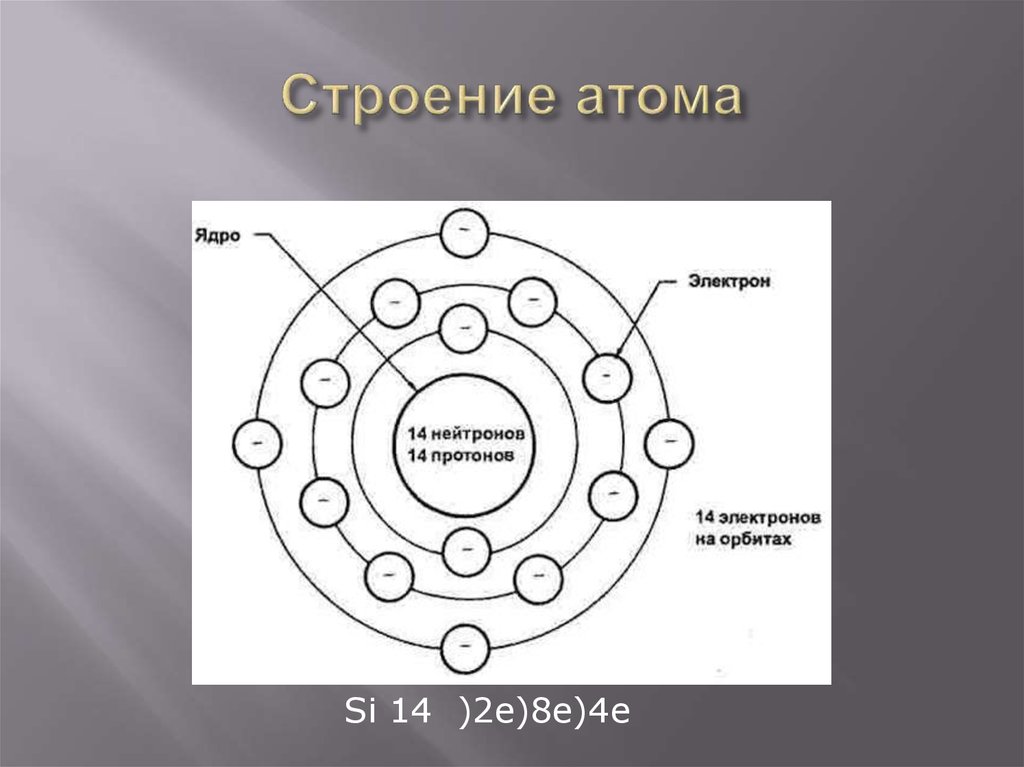 93 а.е.м., что немного больше, чем 12,00 а.е.м. фактического атома углерода-12. Эта «недостающая» масса известна как дефект массы, и вы узнаете об этом в главе о ядерной химии.)
93 а.е.м., что немного больше, чем 12,00 а.е.м. фактического атома углерода-12. Эта «недостающая» масса известна как дефект массы, и вы узнаете об этом в главе о ядерной химии.)
| Имя | Местоположение | Заряд (С) | Плата за единицу | 9{−24}\)
|---|
Количество протонов в ядре атома является его атомным номером (Z). Это определяющая черта элемента: его значение определяет идентичность атома. Например, любой атом, содержащий шесть протонов, является элементом углерода и имеет атомный номер 6, независимо от того, сколько в нем нейтронов или электронов. Нейтральный атом должен содержать одинаковое количество положительных и отрицательных зарядов, поэтому количество протонов равно количеству электронов. Следовательно, атомный номер также указывает на количество электронов в атоме. Суммарное количество протонов и нейтронов в атоме называется его массовым числом (А). Таким образом, количество нейтронов представляет собой разницу между массовым числом и атомным номером: A – Z = количество нейтронов.
Это определяющая черта элемента: его значение определяет идентичность атома. Например, любой атом, содержащий шесть протонов, является элементом углерода и имеет атомный номер 6, независимо от того, сколько в нем нейтронов или электронов. Нейтральный атом должен содержать одинаковое количество положительных и отрицательных зарядов, поэтому количество протонов равно количеству электронов. Следовательно, атомный номер также указывает на количество электронов в атоме. Суммарное количество протонов и нейтронов в атоме называется его массовым числом (А). Таким образом, количество нейтронов представляет собой разницу между массовым числом и атомным номером: A – Z = количество нейтронов.
\[\begin{align*}
\ce{атомный\: число\:(Z)\: &= \:число\: число\: протонов\\
масса\: число\:(A)\: &= \:число\: из\: протонов + число\: из\: нейтронов\\
A-Z\: &= \:число\: из\: нейтронов}
\end{align*}\]
Атомы электрически нейтральны, если они содержат одинаковое количество положительно заряженных протонов и отрицательно заряженных электронов. Когда количество этих субатомных частиц равно , а не , атом электрически заряжен и называется ионом. Заряд атома определяется следующим образом:
Когда количество этих субатомных частиц равно , а не , атом электрически заряжен и называется ионом. Заряд атома определяется следующим образом:
Атомный заряд = количество протонов − количество электронов
Как будет более подробно обсуждаться далее в этой главе, атомы (и молекулы) обычно приобретают заряд, приобретая или теряя электроны. Атом, который получает один или несколько электронов, будет иметь отрицательный заряд и называется анионом. Положительно заряженные атомы, называемые катионами, образуются, когда атом теряет один или несколько электронов. Например, нейтральный атом натрия (Z = 11) имеет 11 электронов. Если этот атом потеряет один электрон, он станет катионом с зарядом 1+ (11 – 10 = 1+). Нейтральный атом кислорода (Z = 8) имеет восемь электронов, и если он получит два электрона, то станет анионом с зарядом 2– (8–10 = 2–).
Пример \(\PageIndex{1}\): Состав атома
Йод является важным микроэлементом в нашем рационе; он необходим для выработки гормона щитовидной железы. Недостаток йода в рационе может привести к развитию зоба, увеличению щитовидной железы (Рисунок \(\PageIndex{2}\)).
Недостаток йода в рационе может привести к развитию зоба, увеличению щитовидной железы (Рисунок \(\PageIndex{2}\)).
Рисунок \(\PageIndex{2}\): (a) Недостаток йода в рационе может вызвать увеличение щитовидной железы, называемое зобом. (b) Добавление небольшого количества йода в соль, предотвращающее образование зоба, помогло устранить эту проблему в США, где потребление соли велико. (кредит а: модификация работы «Алмази»/Wikimedia Commons; кредит б: модификация работы Майка Моцарта)
Добавление небольшого количества йода в поваренную соль (йодированную соль) практически устранило эту проблему для здоровья в Соединенных Штатах, но до 40% населения мира по-прежнему подвержены риску дефицита йода. Атомы йода добавляются в виде анионов, каждый из которых имеет заряд 1- и массовое число 127. Определите количество протонов, нейтронов и электронов в одном из этих анионов йода.
Решение
Атомный номер йода (53) говорит нам о том, что нейтральный атом йода содержит 53 протона в ядре и 53 электрона вне ядра.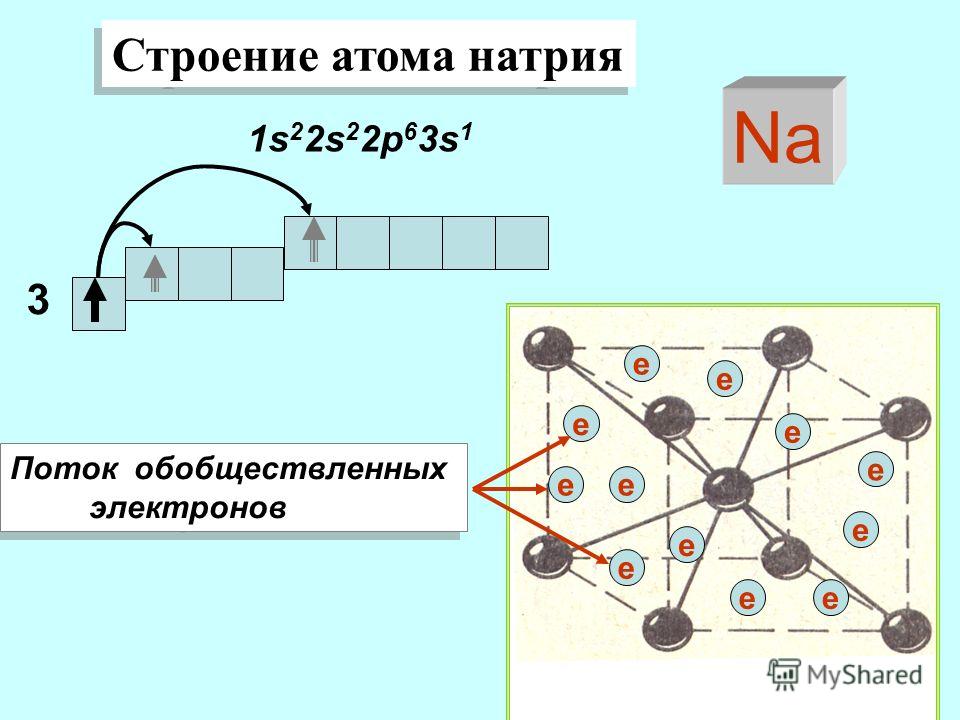 Поскольку сумма количества протонов и нейтронов равна массовому числу 127, количество нейтронов равно 74 (127 – 53 = 74). Поскольку йод добавляется в виде аниона 1–, число электронов равно 54 [53 – (1–) = 54].
Поскольку сумма количества протонов и нейтронов равна массовому числу 127, количество нейтронов равно 74 (127 – 53 = 74). Поскольку йод добавляется в виде аниона 1–, число электронов равно 54 [53 – (1–) = 54].
Упражнение \(\PageIndex{1}\)
Ион платины имеет массовое число 195 и содержит 74 электрона. Сколько протонов и нейтронов он содержит и каков его заряд?
- Ответить
78 протонов; 117 нейтронов; заряд 4+
Химические символы
Химический символ — это аббревиатура, которую мы используем для обозначения элемента или атома элемента. Например, ртуть обозначается как Hg (рис. \(\PageIndex{3}\)). Мы используем один и тот же символ для обозначения одного атома ртути (микроскопический домен) или для обозначения контейнера из многих атомов элемента ртути (макроскопический домен).
Рисунок \(\PageIndex{3}\) : Символ Hg представляет элемент ртуть независимо от количества; он может представлять собой один атом ртути или большое количество ртути. Изображение использовано с разрешения Википедии (пользователь: Materialscientist).
Изображение использовано с разрешения Википедии (пользователь: Materialscientist).
Символы для нескольких распространенных элементов и их атомов перечислены в таблице \(\PageIndex{2}\). Некоторые символы происходят от общего названия элемента; другие являются сокращениями имени на другом языке. Символы состоят из одной или двух букв, например, H для водорода и Cl для хлора. Чтобы избежать путаницы с другими обозначениями, только первая буква символа пишется заглавной. Например, Co — это символ кобальта, а CO — это соединение монооксида углерода, которое содержит атомы углерода (C) и кислорода (O). Все известные элементы и их символы есть в периодической таблице.
| Элемент | Символ | Элемент | Символ |
|---|---|---|---|
| алюминий | Ал | железо | Fe (из железа ) |
| бром | Бр | свинец | Pb (из свинца ) |
| кальций | Са | магний | мг |
| уголь | С | ртуть | Hg (из гидраргирум ) |
| хлор | Кл | азот | Н |
| хром | Кр | кислород | О |
| кобальт | Со | калий | К (из калия ) |
| медь | Cu (из меди ) | кремний | Си |
| фтор | Ф | серебро | Ag (из argentum ) |
| золото | Au (из Aurum ) | натрий | Na (из натрия ) |
| гелий | Он | сера | С |
| водород | Х | олово | Sn (из стали ) |
| йод | я | цинк | Цинк |
Традиционно первооткрыватель (или первооткрыватели) нового элемента дает ему имя. Однако до тех пор, пока название не будет признано Международным союзом теоретической и прикладной химии (IUPAC), рекомендуемое название нового элемента основано на латинском слове (словах) для его атомного номера. Например, элемент 106 назывался уннилгексий (Unh), элемент 107 — уннилсептий (Uns), а элемент 108 — уннилокций (Uno) в течение нескольких лет. Эти элементы теперь названы в честь ученых или мест; например, элемент 106 теперь известен как seaborgium (Sg) в честь Гленна Сиборга, лауреата Нобелевской премии, принимавшего активное участие в открытии нескольких тяжелых элементов.
Однако до тех пор, пока название не будет признано Международным союзом теоретической и прикладной химии (IUPAC), рекомендуемое название нового элемента основано на латинском слове (словах) для его атомного номера. Например, элемент 106 назывался уннилгексий (Unh), элемент 107 — уннилсептий (Uns), а элемент 108 — уннилокций (Uno) в течение нескольких лет. Эти элементы теперь названы в честь ученых или мест; например, элемент 106 теперь известен как seaborgium (Sg) в честь Гленна Сиборга, лауреата Нобелевской премии, принимавшего активное участие в открытии нескольких тяжелых элементов.
IUPAC
Посетите этот сайт, чтобы узнать больше об IUPAC, Международном союзе теоретической и прикладной химии, и изучить его периодическую таблицу.
Авторы
Пол Флауэрс (Университет Северной Каролины, Пембрук), Клаус Теопольд (Университет Делавэра) и Ричард Лэнгли (Государственный университет Стивена Ф. Остина) с соавторами. Контент учебника, созданный OpenStax College, находится под лицензией Creative Commons Attribution License 4.
 0. Скачать бесплатно на http://cnx.org/contents/85abf193-2бд…[email protected]).
0. Скачать бесплатно на http://cnx.org/contents/85abf193-2бд…[email protected]).- Аделаида Кларк, Орегонский технологический институт
- Fuse School, открытый бесплатный образовательный ресурс, в соответствии с лицензией Creative Commons: Attribution-NonCommercial CC BY-NC (см. лицензионный договор: https://creativecommons.org/licenses/by-nc/4.0/)
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или Страница
- Показать страницу TOC
- № на стр.
- Включено
- да
- Теги
- источник[1]-chem-98686
Структура атома — заметки, темы, формулы, книги, часто задаваемые вопросы
Структура атома — очень основная и фундаментальная тема для изучения в химии и современной физике.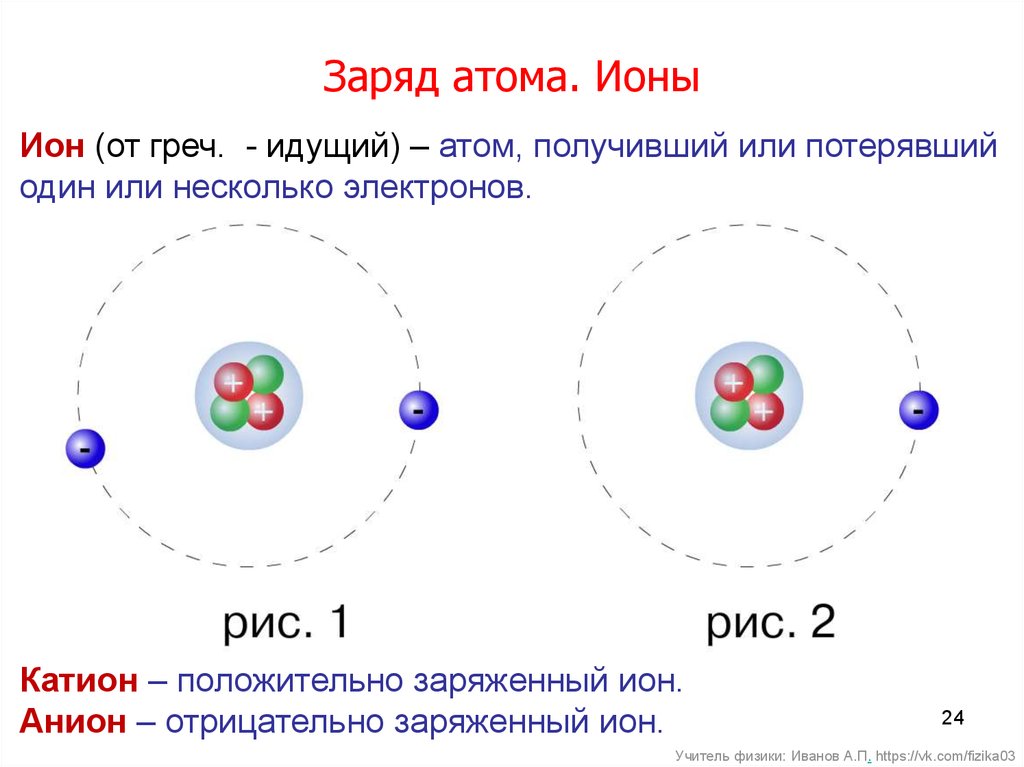 «Как подготовить атомную структуру» — один из запутанных вопросов, который задают многие кандидаты на конкурсных экзаменах. Хорошее понимание темы может дать вам высшую оценку по этой главе. Знание некоторых тем этой главы может решить вашу проблему «Как подготовить атомную структуру»?
«Как подготовить атомную структуру» — один из запутанных вопросов, который задают многие кандидаты на конкурсных экзаменах. Хорошее понимание темы может дать вам высшую оценку по этой главе. Знание некоторых тем этой главы может решить вашу проблему «Как подготовить атомную структуру»?
Атомы — чрезвычайно важные частицы, из которых состоят все материалы на Земле. Атомы присутствуют в наших телах, и они соединяются вместе, образуя молекулы, из которых состоит материя. Все во Вселенной состоит из отдельных атомов различных элементов, которые соединяются вместе, образуя молекулы. Базовая структура атома состоит из ядра, содержащего протоны и нейтроны, и облака электронов, вращающегося вокруг ядра.
Без атомов мир не мог бы существовать. Атомы создают материю, а материя создает все в мире, за некоторыми исключениями. Ниже приведены несколько примеров того, как атомы влияют на мир:
– Атомы кислорода находятся в воздухе и поддерживают нашу жизнь, потому что кислород необходим для дыхания.
– Атомы углекислого газа высвобождаются из нашего тела, и растения поглощают CO 2 , чтобы мог происходить фотосинтез.
– Атомы кислорода и водорода соединяются вместе, образуя молекулу воды (H 2 O). Вода так важна в мире, потому что она имеет множество применений (питьевая, уборка, приготовление пищи, транспортировка). Наше выживание в основном зависит от воды.
– Атомы углерода (C) связываются вместе в определенной структуре, образуя графит, который мы используем в карандаше.
В этой главе претендент изучит некоторые важные и основные термины: электроны, протоны, нейтроны, атомный номер, массовое число, изотопы, изобары, скорость, частота, длина волны, волновое число, орбитали, квантовые числа и т. д.
Примечания для атомная структура:В примечаниях мы шаг за шагом обсудим:
1. Темы, которые будут затронуты в этой главе
2. Обзор главы
Обзор главы
3. Формулы связаны с атомной структурой
Подготовка онлайн к JEE Main/NEET Темы атомной структуры:.
Субатомные частицы.
Атомные модели.
Двойственная природа Материи.
Фотоэлектрический эффект.
Электромагнитное излучение.
Квантово-механическая модель атомов.
Электронная конфигурация.
Из этой главы кандидат прежде всего узнает об атомной теории, предложенной Дальтоном в 1808 году как неделимую частицу атома. иметь значение. В конце девятнадцатого века было доказано, что атомы делимы и состоят из трех элементарных частиц: электронов, протонов и нейтронов. Затем Фарадей открыл электроны, используя эксперимент с электронно-лучевой разрядной трубкой. Нейтроны были открыты Джеймсом Чедвиком путем бомбардировки тонкого листа бериллия частицами. Для объяснения строения атома были предложены различные атомные модели. Претендент будет знать о модели сливового пудинга Томсона, модели атома Резерфорда и модели атома Бора. Модель Бора смогла объяснить спектры атома водорода, говоря о различных спектральных сериях, таких как:
Затем Фарадей открыл электроны, используя эксперимент с электронно-лучевой разрядной трубкой. Нейтроны были открыты Джеймсом Чедвиком путем бомбардировки тонкого листа бериллия частицами. Для объяснения строения атома были предложены различные атомные модели. Претендент будет знать о модели сливового пудинга Томсона, модели атома Резерфорда и модели атома Бора. Модель Бора смогла объяснить спектры атома водорода, говоря о различных спектральных сериях, таких как:
1. Спектр серии Лаймана: Где
Это лежит в ультрафиолетовой области.
2. Спектр серии Balmer: , где
Находится в видимой области.
3. Спектры серии Paschen, Bracket и Pfund:
Они лежат в инфракрасной области.
Претендент также узнает о квантовой теории Планка, в которой вещество поглощает или излучает энергию дискретно в виде небольших пакетов. В этой главе очень интересно узнать о явлении фотоэлектрического эффекта, при котором электрон выбрасывается с поверхности металла, когда на его поверхность падает свет подходящей частоты. После этого стремящийся столкнется с четырьмя квантовыми числами, такими как главное квантовое число, азимутальное квантовое число, магнитное квантовое число и спиновое квантовое число, включая форму и размер различных орбиталей.
После этого стремящийся столкнется с четырьмя квантовыми числами, такими как главное квантовое число, азимутальное квантовое число, магнитное квантовое число и спиновое квантовое число, включая форму и размер различных орбиталей.
Форма s-орбитали: сферическая
Правила заполнения электронами различных орбиталей — очень важная часть, которую следует изучить в этой главе, которая будет полезна в остальной части раздела химии, особенно в неорганическая и органическая химия.
Правила заполнения орбиталей:
Правило 1 – Принцип Ауфбау – Сначала заполняются орбитали с наименьшей энергией. Таким образом, порядок заполнения 1с, 2с, 2п, 3с, 3р, 4с, 3д и т. д.
Правило 2 – Принцип исключения Паули – На одну орбиталь допускается только два электрона, и они должны иметь противоположный спин.
Правило 3- Правило Хунда – Никакое спаривание электронов не начинается ни на одной из вырожденных орбиталей до тех пор, пока все орбитали подоболочки не будут содержать по одному электрону с параллельным спином.
Структурная формула атома:1. Скорость электрона на n-й боровской орбите:
2. Радиус n-й боровской орбитали:
3. Полная энергия электрона на n-й орбите :
4. Кинетическая энергия электрона: -(полная энергия электрона): = – P.E/2
5. Потенциальная энергия электрона:
6. Линейчатый спектр водородоподобных атомов
Где R называется константой Ридберга, где Z = атомный номер.
7. Длина волны Де Бройля
Как подготовить атомную структуру:
Прежде всего кандидат должен прочитать книгу NCERT и тщательно изучить все темы, затронутые в этой главе.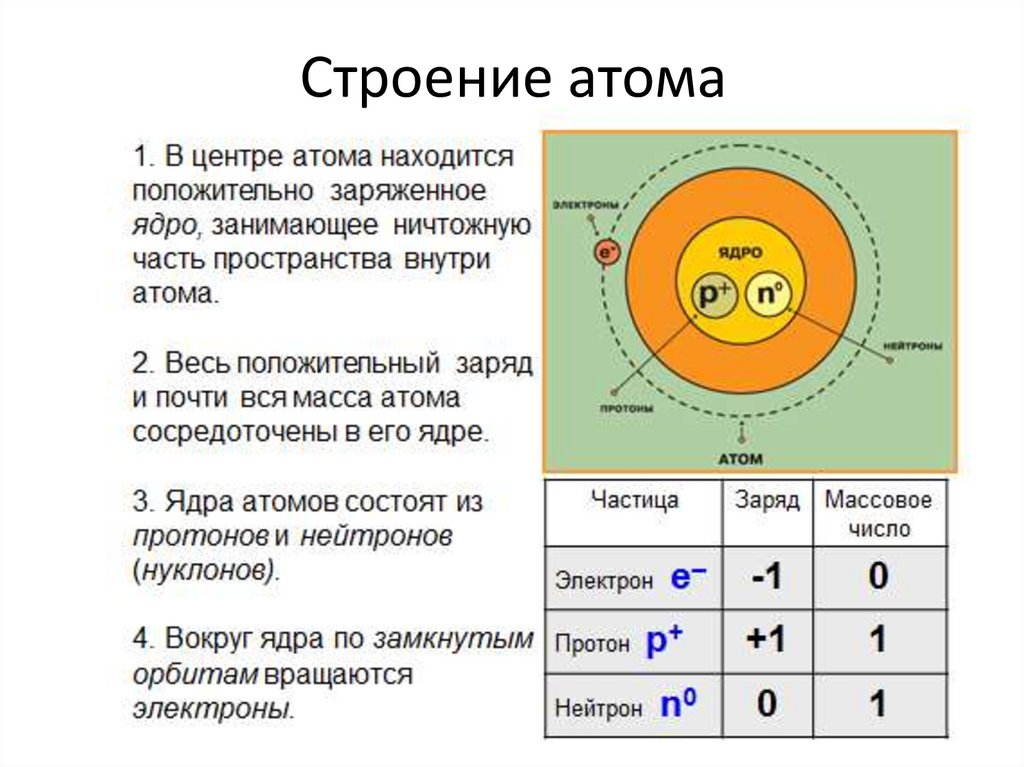 Чтобы избавиться от путаницы «Как подготовиться к атомной структуре», кандидат может также воспользоваться анимацией и видео, которые легко доступны в Интернете, чтобы понять форму орбиталей, фотоэлектрический эффект, модель Бора и другие связанные с этим вопросы. темы. Очень важно иметь четкое представление об экспериментальной установке и наблюдениях в уме кандидата. После того, как аспирант тщательно изучит все концепции главы, он/она должен будет решить числовые задачи. После того, как все вопросы, данные в учебнике NCERT, решены и изучены, соискатель может перейти к другим книгам и попытаться решить больше задач, приведенных в других книгах. Можно изучить такие книги, как Дж. Д. Ли и О. П. Тандон, чтобы получить глубокие знания по главе. Кандидат также должен сосредоточиться на вопросниках предыдущих лет, связанных со структурой атома. На основе анализа установлено, что большинство численных задач приходится на теорию Бора и спектр водорода. Это важные темы с точки зрения экзамена.
Чтобы избавиться от путаницы «Как подготовиться к атомной структуре», кандидат может также воспользоваться анимацией и видео, которые легко доступны в Интернете, чтобы понять форму орбиталей, фотоэлектрический эффект, модель Бора и другие связанные с этим вопросы. темы. Очень важно иметь четкое представление об экспериментальной установке и наблюдениях в уме кандидата. После того, как аспирант тщательно изучит все концепции главы, он/она должен будет решить числовые задачи. После того, как все вопросы, данные в учебнике NCERT, решены и изучены, соискатель может перейти к другим книгам и попытаться решить больше задач, приведенных в других книгах. Можно изучить такие книги, как Дж. Д. Ли и О. П. Тандон, чтобы получить глубокие знания по главе. Кандидат также должен сосредоточиться на вопросниках предыдущих лет, связанных со структурой атома. На основе анализа установлено, что большинство численных задач приходится на теорию Бора и спектр водорода. Это важные темы с точки зрения экзамена.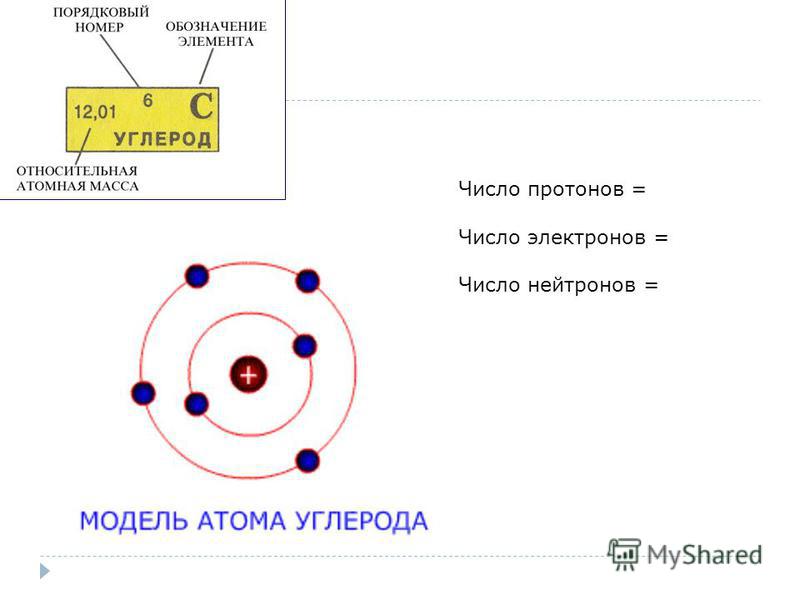

 е.м.
е.м.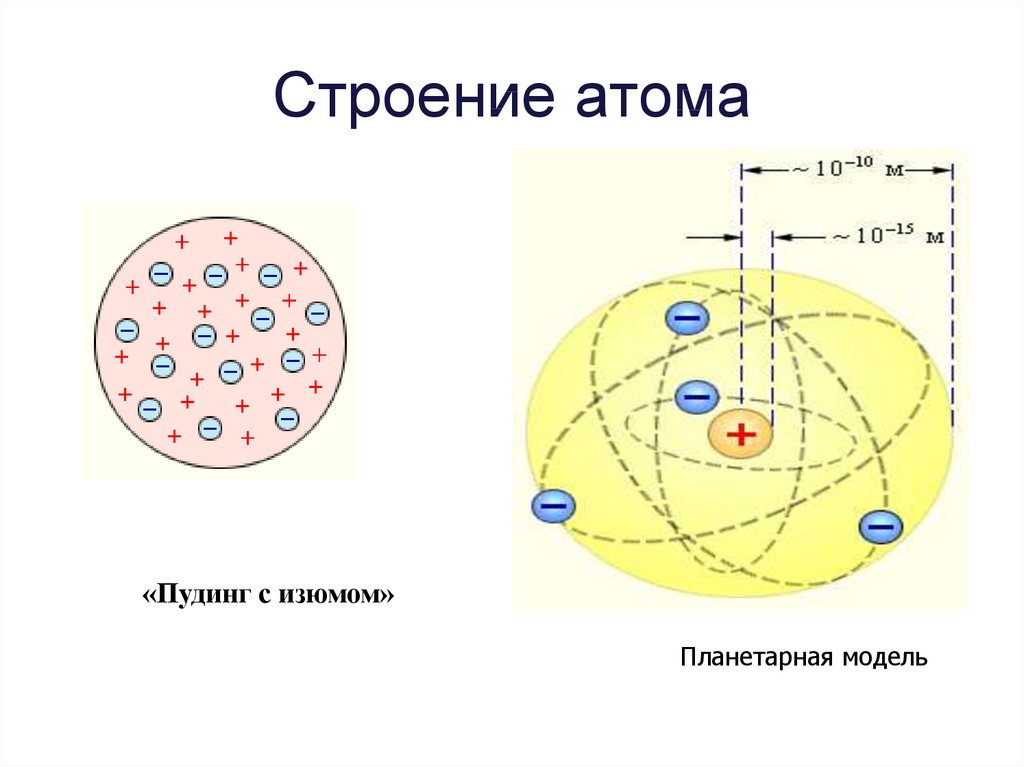

 2 Параметры
для характеристики атомов.
2 Параметры
для характеристики атомов.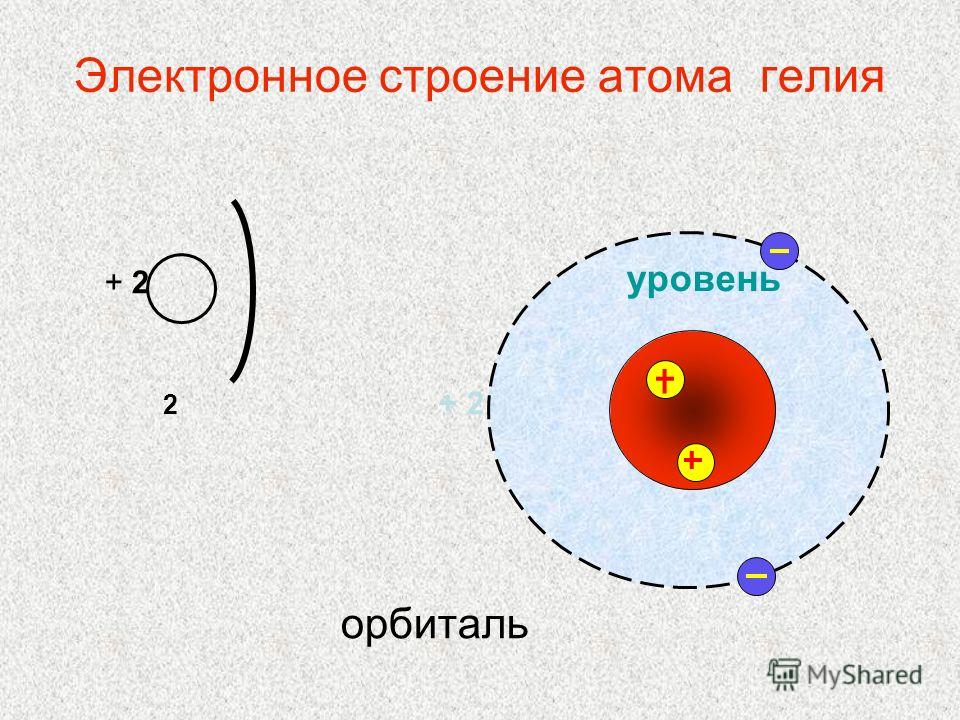 ).
).