Удельная теплота плавления – формула, что называется и как обозначается
4.6
Средняя оценка: 4.6
Всего получено оценок: 216.
4.6
Средняя оценка: 4.6
Всего получено оценок: 216.
Для решения прикладных задач о плавлении тел важно было установить, сколько энергии требует этот процесс. В ходе экспериментов удалось выявить простую эмпирическую зависимость между количество теплоты, массой тела и некой константой, характеризующей вещество с точки зрения процесса плавления, которую назвали удельной теплотой плавления.
Плавление кристаллических тел
У кристаллических тел атомы – кирпичики материи – упорядочены в жесткую структуру, которую называют кристаллической решеткой. Чтобы расплавить такое тело, необходимо разрушить решетку, разорвать прочные связи между атомами. Для этого необходима энергия.
Рис. 1. Структура кристаллического тела и жидкости.Из законов термодинамики известно, что для изменения внутренней энергии необходимо либо совершить работу, либо подвести тепло. Нас интересует второй случай. Когда к кристаллическому телу подводят тепло, его температура растет. Атомы в решетке начинают колебаться чаще и сильнее, внутренняя энергия увеличивается. По достижении необходимой температуры (которую называют температурой плавления) всё подводимое тепло будет уходить на ее поддержание и на разрушение кристаллической решетки твердого вещества.
Нас интересует второй случай. Когда к кристаллическому телу подводят тепло, его температура растет. Атомы в решетке начинают колебаться чаще и сильнее, внутренняя энергия увеличивается. По достижении необходимой температуры (которую называют температурой плавления) всё подводимое тепло будет уходить на ее поддержание и на разрушение кристаллической решетки твердого вещества.
Что такое удельная теплота плавления
Наблюдение за плавлением различных кристаллических тел одинаковой массы позволило сделать вывод, что каждое из них требует различного количества теплоты. При этом те же вещества, но большей массы, требовали большего количества теплоты. Математически эту зависимость выражают так:
$Q=Cm$ (1), где С – некая константа пропорциональности. Ей дали название – удельная теплота плавления (или энтальпия плавления), и ввели для нее специальное обозначение – λ.
 Рис. 3. График плавления тела.
Рис. 3. График плавления тела.Величина удельной теплоты плавления зависит от свойств вещества. Так, например, для льда она равна 340 кДж/кг, а для золота – 66,6 кДж/кг. Из этого следует, что для плавления льда необходимо больше теплоты, чем для плавления золота.
Расчетная формула удельной теплоты плавления выводится из уравнения (1):
$ \lambda= \frac{Q_{плавления}}{m_{вещества}}$ – (2)
Из формулы не трудно понять, в чем измеряется энтальпия плавления. Если теплота – в джоулях, масса – в килограммах, то результат их деления – в Дж/кг.
Задачи
- Какое количество теплоты необходимо подвести к котлу, чтобы расплавить V метров кубических снега плотностью ρ? Удельную теплоту плавления снега принять за λ, удельную теплоемкость за с.
Решение первой задачи
Обозначим за $t_1$ начальную температуру льда, за $t_2$ – температуру плавления.
Тогда на нагрев льда до температуры плавления будет затрачено $Q_1 = cm(t_2-t_1)$ Дж или, выражая массу через объем и плотность, $Q_1 = c \rho V(t_2-t_1)$ Дж.
На плавление льда будет затрачено $Q2 = \rho V \lambda$ Дж.
Тогда общее количество теплоты $Q = Q_1 + Q_2 = \rho V(c(t_2-t_1) + \lambda)$
- 1 литр кипятка вылили на кусок льда массой 2 кг, взятого при температуре 0̊ С. Какая часть льда расплавится?
Решение второй задачи
Из литра кипятка при его остывании выделяется $Q = cm(t_1-t_2) = cmt_1$ Дж, так как $t_2=0$.
Масса льда, которая расплавится данным количеством теплоты, $m_2 = \frac{Q}{λ} = \frac {cmt_1}{λ} = \frac {{4200}\times{100}}{340000} = 1,24$ кг.
Тогда исходную массу разделим на массу расплавленного льда:
$\frac {m_1}{m_2} = \frac {1,24}{2} = 0,62$ или 62% – часть льда, которая расплавится.
Что мы узнали?
В ходе урока мы узнали, что называется удельной теплотой плавления (константа пропорциональности между количеством теплоты и массой вещества в процессе плавления), какой буквой греческого алфавита она обозначается, узнали, как найти ее.
Тест по теме
Доска почёта
Чтобы попасть сюда – пройдите тест.
Sarhan Global
10/10
Оценка доклада
4.6
Средняя оценка: 4.6
Всего получено оценок: 216.
А какая ваша оценка?
как найти удельную, единица измерения, формула, как обозначается
Источник: myslide.ru
Процесс теплопередачи всегда предусматривает переход энергии между телами либо при обмене с внешней средой. Сколько именно энергии потеряло либо приобрело тело, отражает специальный параметр — количество теплоты.
Количество теплоты — что это за параметр в физике
Определение 1Под «количеством теплоты» в физике понимают энергию, которую в результате теплопередачи приобретает либо теряет какое-то тело. В международной СИ введена специальная единица — Джоуль. Вне этой системы для измерения может применяться единица «калория» (килокалория). Переход между этими единицами происходит с учетом, что 1 кал равняется 4,2 Дж.
Переход между этими единицами происходит с учетом, что 1 кал равняется 4,2 Дж.
Для обозначения количества теплоты введено обозначение Q.
Джоуль является также единицей, измеряющей работу. Поэтому справедлива запись:
Q=A=E=1Дж
Тело теряет либо приобретает энергию в ходе какого-либо процесса, в который оно вовлечено. Количественная характеристика определяется способом осуществления этого процесса. Имеет значение также начальная внутренняя энергия этого тела, на которую оказывают влияние внешние силы.
Какой физический параметр определяет количество теплоты
То количество теплоты, которое передается между телами, вызывает их нагревание (вплоть до парообразования и плавления), охлаждение (вплоть до кристаллизации). Возможно также образование конденсата. В то же время не каждое количество теплоты способно вызвать эти процессы. Существует определенная зависимость между количеством теплоты и массой взятого вещества. Эта зависимость выражается формулой:
Q=CMΔT
Определение 2Количество теплоты, необходимое для нагревания тела, есть величина, прямо пропорциональная его массе и разнице его начальной и конечной температур.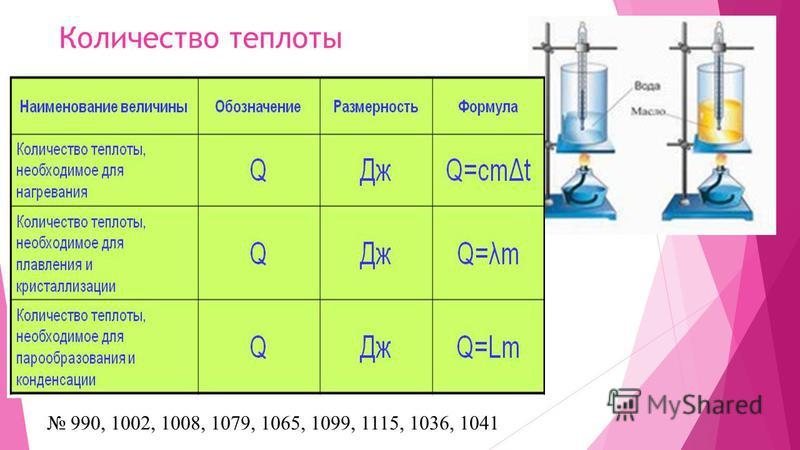
Аналогичным образом формулируются следующие закономерности:
- Величина Q, которое потребуется для перехода жидкости из обычного состояния в парообразное, находится в прямой зависимости от ее массы: Q=Lm, где L — особая величина, именуемая теплотой парообразования.
- Величина Q, которое потребуется для перехода твердого тела в расплавленное состояние либо наоборот, находится в прямой зависимости от его массы: Q=λm, где λ — особая величина, именуемая удельной теплотой плавления.
- Величина Q, которое выделится при сгорании топлива, находится в прямо пропорциональной зависимости от его массы: Q=qm, где q — особая величина, именуемая удельной теплотой сгорания.
Таким образом, мы пришли к физическому понятию «удельная теплоемкость».
Определение 3Удельная теплоемкость характеризует величину количества теплоты, которое потратится в процессе нагревания (либо выделится в процессе охлаждения) тела массой 1 кг на 1 К.
Исходя из определения, чтобы определить, какое количество теплоты будет затрачено на парообразование либо плавление (конденсацию, кристаллизацию), необходимо знать удельную теплоту парообразования, плавления, конденсации, кристаллизации, сгорания. Эти показатели рассчитываются экспериментальным путем и являются величинами постоянными. Для решения соответствующих задач по термодинамике пользуются специальными таблицами.
Эти показатели рассчитываются экспериментальным путем и являются величинами постоянными. Для решения соответствующих задач по термодинамике пользуются специальными таблицами.
Источник: ru.teplowiki.org
Для некоторых жидкостей:
Источник: ru.teplowiki.org
Понятие теплоемкости, как измеряется, график зависимости температуры от времени
Определение 4Под понятием «теплоемкости» подразумевается то количество теплоты, которое поглощается либо выделяется телом при его нагревании (либо охлаждении) на 1 Кельвин. Это физическое понятие, зависящее от соотношения количества теплоты, которое в термодинамической системе поглощается либо выделяется, незначительно изменяя температуру, к данному изменению.
Для обозначения теплоемкости вводится знак C. Формула для ее определения:
C=ΔQ÷ΔT
Становится понятным, что, с увеличением массы тела количества теплоты, необходимое для его нагревания, увеличивается. Другими словами, теплоемкость тела находится в прямо пропорциональной зависимости от количества содержащегося в нем вещества.
С другой стороны, показателем количества вещества является масса либо количество молей. Отсюда вытекает уже знакомое понятие и формула «удельной теплоемкости»:
c=C÷m
и теплоемкости молярной:
Cμ=C÷ν
Существует также понятие «объемной теплоемкости»:
С’=C÷V
Одно и то же вещество, принимая различное агрегатное состояние, определяет теплоемкость.
Например, теплоемкость идеального газа зависит от числа степеней свобод молекул. Теплоемкость твердого тела характеризуется по нескольким теориям:
- Законы Дюлонга — Пти и Джоуля — Коппа;
- Квантовая теория Эйнштейна;
- Квантовая теория теплоёмкостей Дебая.
На рисунке графически изображены характеристики теплоемкости твердого тела согласно теорий Дебая и Эйнштейна.
Источник: ru.wikipedia.org
ПримечаниеПонятие «теплоемкость» отличается от «удельная теплоемкость» тем, что в нем речь идет о сообщении теплоты всему телу, а не единице его массы (1 кг).
Единицей измерения теплоемкости является Дж/К (для системы СИ).
Удельная теплоемкость может иметь различные единицы измерения, поскольку количество вещества имеет несколько выражений (по массе, объему, молям).
Выражая количество теплоты, необходимое для нагревания (либо охлаждения) 1 кг на 1 К, говорят о массовой теплоемкости, которая измеряется в Дж/кг*К.
Если необходимо выразить количество теплоты, которое нужно дать (либо забрать) телу в рассчете на 1 м3, чтобы изменить его температуру на 1К, говорят об объемной темплоемкости, которая измеряется в Дж/м3*К.
Если затрагивается понятие «молярная теплоемкость», то имеют ввиду то количество теплоты, которое необходимо для нагревания (либо охлаждения) 1 моля вещества на 1К. Единицей измерения в таком случае является Дж/моль*К.
Рассчитывать затраты тепла в физике принято, основываясь на законе сохранения энергии, являющегося первым началом термодинамики. Для случаев, когда работа равна нулю, т.е. учитывается только теплообмен, уравнение теплового баланса учитывает для изолированной системы сумму количеств теплоты, которые отдаются телами (при этом их внутренняя энергия снижается) и получаются. При этом количество отданной и полученной энергии равно. Такой энергетический обмен между телами будет происходить до тех пор, пока их температуры уравновесятся, т.е. наступит термодинамическое равновесие.
При этом количество отданной и полученной энергии равно. Такой энергетический обмен между телами будет происходить до тех пор, пока их температуры уравновесятся, т.е. наступит термодинамическое равновесие.
Рассмотрим, как выглядит график зависимости температуры тела от времени его нагревания. В данном примере первоначально тело находилось в твердом состоянии:
Источник: neznaika.info
Как найти удельную теплоёмкость, формулы
Удельная теплоемкость по сути является коэффициентом пропорциональности между изменением температуры тела и его массой. Поэтом рассчитать ее можно по формуле:
Источник: skysmart.ru
Вторым способом ее можно рассчитать, используя теплоемкость:
Источник: skysmart.ru
Количество теплоты, необходимое для нагревания веществ
Если нужно узнать, какое количество теплоты необходимо для нагревания вещества, то нужно произвести действие умножения между его удельной теплоемкостью, массой и разностью конечной и начальной температур:
Q=cm(tкон-tнач)
Поскольку конечная температура тела выше, чем начальная, то Q будет положительным числом.
Количество теплоты, выделяемое при охлаждении веществ
Рассматривая процесс охлаждения, анализируем ситуацию, когда конечная температура тела ниже начальной. Высчитать, какое количество теплоты тело будет выделять, можно по той же формуле, однако Q будет иметь знак минус.
Примеры решения задач
Задача 1Определить вещество, лежащее в основе тела, если при нагревании его с 200 до 600К ему передалось 4,0*106 Дж. Масса тела 40 кг.
Решение
Чтобы решить задачу, необходимо узнать удельную теплоемкость этого вещества, затем — по таблице узнать его название.
C=Q÷mΔT
C=4,0*106÷40*400=0,25*103Дж/кгК
По таблице находим, что такую удельную теплоемкость имеет олово.
Задача 2Масса воды в сосуде 800г, температура 60оС. В эту воду помещают лед с температурой -10оС. Какой массы лед был помещен, если термодинамическое равновесие установилось, когда температура воды стала равной 40оС.
Решение
Из таблиц определяем, что удельная теплоемкость воды равна 4,2*103 Дж/кгК, льда – 2,1*103 Дж/кгК. λ льда (удельная теплота плавления) = 3,33*105Дж/кг.
λ льда (удельная теплота плавления) = 3,33*105Дж/кг.
Для состояния теплового баланса характерно:
с2m2(to-t2)+λm2+c1m2(t3-to)+c1m1(t3-t1)=0
Находим m2:
m2=c1m1(t1-t3)⁄(c2(to-t2)+λ+c1(t3-t0))
Подставляя значения, находим величину массы, равную 0,13 кг.
Задача 3Определить Q, выделившееся при охлаждении 20 л масла, если его температура снизилась с 60оС до 20оС.
Первым делом, для перехода в систему СИ заменяем объем, выраженный в литрах, на единицу м3: 20л=0,02м3.
Q=cmΔT.
В то же время m=ρV/
Найдя в таблице ρ, высчитываем массу масла: m=90*0,02=18 кг
Разница температур составила 40оС.
Q=1800*18*40=1296 (кДж).
Изменение температуры и теплоемкость
Цели обучения
К концу этого раздела вы сможете:
- Наблюдать теплопередачу и изменение температуры и массы.
- Рассчитать конечную температуру после теплопередачи между двумя объектами.
Одним из основных эффектов теплопередачи является изменение температуры: при нагревании температура повышается, а при охлаждении снижается. Мы предполагаем, что фазового перехода нет и что над системой или системой не совершается никакой работы. Опыты показывают, что передаваемое тепло зависит от трех факторов — изменения температуры, массы системы, вещества и фазы вещества.
Мы предполагаем, что фазового перехода нет и что над системой или системой не совершается никакой работы. Опыты показывают, что передаваемое тепло зависит от трех факторов — изменения температуры, массы системы, вещества и фазы вещества.
Рис. 1. Теплота Q , переданная для изменения температуры, зависит от величины изменения температуры, массы системы, а также вовлеченного вещества и фазы. а) Количество переданного тепла прямо пропорционально изменению температуры. Чтобы удвоить изменение температуры массы m, нужно добавить удвоенное количество теплоты. б) Количество переданного тепла также прямо пропорционально массе. Чтобы вызвать эквивалентное изменение температуры в удвоенной массе, нужно добавить в два раза больше тепла. в) Количество переданного тепла зависит от вещества и его фазы. Если требуется сумма 
Зависимость от изменения температуры и массы легко понять. Благодаря тому, что (средняя) кинетическая энергия атома или молекулы пропорциональна абсолютной температуре, внутренняя энергия системы пропорциональна абсолютной температуре и числу атомов или молекул. Благодаря тому, что переданное тепло равно изменению внутренней энергии, теплота пропорциональна массе вещества и изменению температуры. Переносимое тепло также зависит от вещества, так что, например, теплота, необходимая для повышения температуры, для спирта меньше, чем для воды. Для одного и того же вещества передаваемая теплота также зависит от фазы (газовая, жидкая или твердая).
Теплопередача и изменение температуры
Количественная связь между теплопередачей и изменением температуры содержит все три фактора: Q = mc Δ T , где Q — символ теплопередачи, м масса вещества, а Δ T — изменение температуры. Символ c означает удельную теплоемкость и зависит от материала и фазы. Удельная теплоемкость – это количество теплоты, необходимое для изменения температуры 1,00 кг массы на 1,00°С. Удельная теплоемкость c — свойство вещества; его единица СИ – Дж / (кг ⋅ K) или Дж / (кг ⋅ ºC). Напомним, что изменение температуры (Δ T ) одинаково в единицах кельвина и градусах Цельсия. Если теплопередача измеряется в килокалориях, то единицей удельной теплоемкости является ккал/(кг ⋅ ºC).
Удельная теплоемкость – это количество теплоты, необходимое для изменения температуры 1,00 кг массы на 1,00°С. Удельная теплоемкость c — свойство вещества; его единица СИ – Дж / (кг ⋅ K) или Дж / (кг ⋅ ºC). Напомним, что изменение температуры (Δ T ) одинаково в единицах кельвина и градусах Цельсия. Если теплопередача измеряется в килокалориях, то единицей удельной теплоемкости является ккал/(кг ⋅ ºC).
Значения удельной теплоемкости обычно нужно искать в таблицах, потому что нет простого способа их расчета. В общем случае удельная теплоемкость также зависит от температуры. В таблице 1 перечислены репрезентативные значения удельной теплоемкости для различных веществ. За исключением газов, зависимость теплоемкости большинства веществ от температуры и объема слабая. Мы видим из этой таблицы, что удельная теплоемкость воды в пять раз больше, чем у стекла, и в десять раз больше, чем у железа, а это значит, что требуется в пять раз больше теплоты, чтобы поднять температуру воды на ту же величину, что и для стекла, и в десять раз больше, чем для стекла. много тепла, чтобы поднять температуру воды, как для железа. На самом деле вода имеет одну из самых больших удельных теплоемкостей среди всех материалов, что важно для поддержания жизни на Земле.
много тепла, чтобы поднять температуру воды, как для железа. На самом деле вода имеет одну из самых больших удельных теплоемкостей среди всех материалов, что важно для поддержания жизни на Земле.
Пример 1. Расчет необходимого количества тепла: нагрев воды в алюминиевой кастрюле
Алюминиевая кастрюля весом 0,500 кг на плите используется для нагрева 0,250 л воды с 20,0°C до 80,0°C. а) Какое количество тепла потребуется? Какой процент тепла используется для повышения температуры (b) кастрюли и (c) воды?
Стратегия
Посуда и вода всегда имеют одинаковую температуру. Когда вы ставите кастрюлю на плиту, температура воды и сковороды увеличивается на одинаковую величину. Воспользуемся уравнением теплообмена при заданном изменении температуры и массы воды и алюминия. Удельные теплоемкости воды и алюминия приведены в табл. 1.
Решение
Поскольку вода находится в тепловом контакте с алюминием, кастрюля и вода имеют одинаковую температуру.
Рассчитайте разницу температур:
Δ T = T f − T i = 60,0ºC.
Рассчитайте массу воды. Поскольку плотность воды 1000 кг/м 3 , один литр воды имеет массу 1 кг, а масса 0,250 л воды равна м w = 0,250 кг.
Рассчитайте теплоту, переданную воде. Используйте удельное тепло воды в Таблице 1:
Q W = M W C W δ T = (0,250 кг) (4186 J/KGºC) (60,0,016C) (60,0,016C) (60,0,016C) (60,0,016C) (60,0,016C) (60,0,016 = (0,250 кг) (4186 J/кг. = 62,8 кДж.
Рассчитайте тепло, переданное алюминию. Используйте удельную теплоемкость алюминия из таблицы 1:
Q Al = m Al c Al Δ T = (0,500 кг)(900 Дж/кгºC)(60,0ºC) = 27,0 × 10 4 Дж = 27,0 кДж. вода. Сначала найдем общее переданное тепло:
Q Всего = Q w + Q Al = 62,8 кДж + 27,8 кДж + 27,8 кДж + 27,8 кДж + 27,8 кДж
Таким образом, количество тепла, идущее на нагрев сковороды, равно
[латекс]\frac{27. 0\text{ кДж}}{89.8\text{ кДж}}\times100\%=30,1\%\\[/латекс]
0\text{ кДж}}{89.8\text{ кДж}}\times100\%=30,1\%\\[/латекс]
и количество, идущее на нагрев воды, равно
[латекс]\фрак{62,8\текст{ кДж}}{89,8 \text{ кДж}}\times100\%=69,9\%\\[/latex].
Обсуждение
В этом примере тепло, переданное контейнеру, составляет значительную долю от общего количества переданного тепла. Хотя масса кастрюли в два раза больше массы воды, удельная теплоемкость воды более чем в четыре раза больше, чем у алюминия. Следовательно, для достижения заданного изменения температуры воды требуется чуть более чем в два раза больше тепла по сравнению с алюминиевой кастрюлей.
Пример 2. Расчет увеличения температуры по работе, совершаемой над веществом: перегрев тормозов грузовика при движении под уклон
Рис. 2. Дымящиеся тормоза на этом грузовике являются видимым свидетельством механического эквивалента тепла.
Тормоза грузовиков, используемые для контроля скорости на спуске, работают, преобразовывая потенциальную энергию гравитации в повышенную внутреннюю энергию (более высокую температуру) тормозного материала. Это преобразование предотвращает преобразование потенциальной энергии гравитации в кинетическую энергию грузовика. Проблема заключается в том, что масса грузовика велика по сравнению с массой тормозного материала, поглощающего энергию, и повышение температуры может произойти слишком быстро, чтобы достаточное количество тепла передавалось от тормозов в окружающую среду.
Это преобразование предотвращает преобразование потенциальной энергии гравитации в кинетическую энергию грузовика. Проблема заключается в том, что масса грузовика велика по сравнению с массой тормозного материала, поглощающего энергию, и повышение температуры может произойти слишком быстро, чтобы достаточное количество тепла передавалось от тормозов в окружающую среду.
Рассчитайте повышение температуры 100 кг тормозного материала со средней удельной теплоемкостью 800 Дж/кг ⋅ ºC, если материал сохраняет 10 % энергии от 10 000-килограммового грузовика, спускающегося с высоты 75,0 м (при вертикальном перемещении) при постоянном скорость.
Стратегия
Если тормоза не задействованы, гравитационная потенциальная энергия преобразуется в кинетическую энергию. При торможении потенциальная энергия гравитации преобразуется во внутреннюю энергию тормозного материала. Сначала вычислим гравитационную потенциальную энергию ( Mgh ), что весь грузовик теряет при спуске, а затем найти повышение температуры только в тормозном материале.
Решение
- Рассчитайте изменение потенциальной энергии гравитации при движении грузовика под гору
- Рассчитайте температуру по переданному теплу, используя Q = Mgh и [латекс]\Delta{T}=\frac{Q}{mc}\\[/latex], где 9{\ circ} C \\ [/латекс].
Обсуждение
Эта температура близка к температуре кипения воды. Если бы грузовик какое-то время ехал, то непосредственно перед спуском температура тормозов, вероятно, была бы выше температуры окружающей среды. Повышение температуры при спуске, вероятно, повысит температуру тормозного материала выше точки кипения воды, поэтому этот метод нецелесообразен. Однако та же идея лежит в основе новейшей гибридной технологии автомобилей, где механическая энергия (потенциальная энергия гравитации) преобразуется тормозами в электрическую энергию (аккумулятор).
| Таблица 1. Удельная теплоемкость [1] различных веществ | ||
|---|---|---|
| Вещества | Удельная теплоемкость ( c ) | |
| Твердые вещества | Дж/кг ⋅ ºC | ккал/кг ⋅ ºC [2] |
| Алюминий | 900 | 0,215 |
| Асбест | 800 | 0,19 |
| Бетон, гранит (средний) | 840 | 0,20 |
| Медь | 387 | 0,0924 |
| Стекло | 840 | 0,20 |
| Золото | 129 | 0,0308 |
| Тело человека (в среднем при 37 °C) | 3500 | 0,83 |
| Лед (средний, от −50°C до 0°C) | 2090 | 0,50 |
| Железо, сталь | 452 | 0,108 |
| Свинец | 128 | 0,0305 |
| Серебро | 235 | 0,0562 |
| Дерево | 1700 | 0,4 |
| Жидкости | ||
| Бензол | 1740 | 0,415 |
| Этанол | 2450 | 0,586 |
| Глицерин | 2410 | 0,576 |
| Меркурий | 139 | 0,0333 |
| Вода (15,0 °С) | 4186 | 1. 000 000 |
| Газы [3] | ||
| Воздух (сухой) | 721 (1015) | 0,172 (0,242) |
| Аммиак | 1670 (2190) | 0,399 (0,523) |
| Углекислый газ | 638 (833) | 0,152 (0,199) |
| Азот | 739 (1040) | 0,177 (0,248) |
| Кислород | 651 (913) | 0,156 (0,218) |
| Пар (100°C) | 1520 (2020) | 0,363 (0,482) |
Обратите внимание, что пример 2 является иллюстрацией механического эквивалента тепла. В качестве альтернативы, повышение температуры может быть произведено с помощью паяльной лампы вместо механического.
Пример 3. Расчет конечной температуры при передаче тепла между двумя телами: наливание холодной воды на горячую сковороду
Предположим, вы наливаете 0,250 кг воды температурой 20,0ºC (около чашки) в 0,500-килограммовую алюминиевую кастрюлю с температурой 150ºC, снятую с плиты. Предположим, что кастрюля находится на изолированной подушке и что незначительное количество воды выкипает. При какой температуре вода и кастрюля через короткое время достигают теплового равновесия?
Предположим, что кастрюля находится на изолированной подушке и что незначительное количество воды выкипает. При какой температуре вода и кастрюля через короткое время достигают теплового равновесия?
Стратегия
Кастрюля размещена на изолирующей прокладке, чтобы обеспечить небольшой теплообмен с окружающей средой. Первоначально кастрюля и вода не находятся в тепловом равновесии: кастрюля имеет более высокую температуру, чем вода. Затем теплопередача восстанавливает тепловое равновесие, когда вода и кастрюля соприкасаются. Поскольку теплопередача между кастрюлей и водой происходит быстро, масса испаряемой воды пренебрежимо мала, а величина тепла, теряемого кастрюлей, равна теплу, приобретаемому водой. Обмен теплом прекращается, как только достигается тепловое равновесие между чашей и водой. Теплообмен можно записать как | Q горячий |= Q холодный .
Решение
Используйте уравнение теплопередачи Q = mc Δ T , чтобы выразить потери тепла алюминиевой кастрюлей через массу кастрюли, удельную теплоемкость алюминия, начальную температуру сковороде и конечная температура: Q горячий = m Al c Al ( T f − 150ºC).
Выразите тепло, полученное водой, через массу воды, удельную теплоемкость воды, начальную температуру воды и конечную температуру: Q холод = m W c W ( T f – 20,0ºC).
Обратите внимание, что Q горячая <0 и Q холодная >0, и что их сумма должна равняться нулю, поскольку тепло, отдаваемое горячей кастрюлей, должно быть таким же, как тепло, получаемое холодной водой: 9{\circ}\text{C}\end{array}\\[/latex]
Обсуждение
Это типичная задача калориметрии : два тела при разных температурах соприкасаются друг с другом и обмениваются нагревать до достижения общей температуры. Почему конечная температура намного ближе к 20,0ºC, чем к 150ºC? Причина в том, что вода имеет большую удельную теплоемкость, чем большинство обычных веществ, и, таким образом, претерпевает небольшое изменение температуры при данной теплопередаче. Большому водоему, такому как озеро, требуется большое количество тепла, чтобы заметно повысить его температуру. Это объясняет, почему температура озера остается относительно постоянной в течение дня даже при больших изменениях температуры воздуха. Однако температура воды меняется в течение более длительного времени (например, с лета на зиму).
Большому водоему, такому как озеро, требуется большое количество тепла, чтобы заметно повысить его температуру. Это объясняет, почему температура озера остается относительно постоянной в течение дня даже при больших изменениях температуры воздуха. Однако температура воды меняется в течение более длительного времени (например, с лета на зиму).
Самостоятельный эксперимент: изменение температуры земли и воды
Что нагревается быстрее, земля или вода?
Для изучения различий в теплоемкости:
- Поместите равные массы сухого песка (или почвы) и воды одинаковой температуры в два небольших сосуда. (Средняя плотность почвы или песка примерно в 1,6 раза выше, чем у воды, поэтому вы можете получить примерно равные массы, используя на 50% больше воды по объему.)
- Нагревайте оба (используя духовку или нагревательную лампу) в течение одинакового времени.
- Запишите конечную температуру двух масс.
- Теперь доведите обе банки до одинаковой температуры, нагревая их в течение более длительного периода времени.

- Снимите банки с источника тепла и измеряйте их температуру каждые 5 минут в течение примерно 30 минут.
Какой образец остывает быстрее? Эта деятельность воспроизводит явления, ответственные за наземные и морские бризы.
Проверьте свое понимание
Если для повышения температуры блока с 25°C до 30°C необходимо 25 кДж, то какое количество теплоты необходимо для нагрева блока с 45°C до 50°C?
Решение
Теплопередача зависит только от разницы температур. Так как разность температур одинакова в обоих случаях, то и во втором случае необходимы одни и те же 25 кДж.
Резюме секции
- Передача HEAT Q , которая приводит к изменению T в температуре тела с массой M – Q = MC Δ T , где C MC Δ T , где C C Δ T , где C, MC Δ T , C, MC . – удельная теплоемкость материала.
 Это соотношение также можно рассматривать как определение удельной теплоемкости.
Это соотношение также можно рассматривать как определение удельной теплоемкости.
Концептуальные вопросы
- Какие три фактора влияют на теплопередачу, необходимую для изменения температуры объекта?
- Температура тормозов автомобиля повышается на Δ T при остановке автомобиля со скорости v . Насколько больше было бы Δ T , если бы скорость автомобиля изначально была вдвое больше? Вы можете предположить, что автомобиль останавливается достаточно быстро, чтобы тепло от тормозов не отводилось.
Задачи и упражнения
- В жаркий день температура в бассейне объемом 80 000 литров повышается на 1,50ºC. Какова чистая теплопередача при этом нагреве? Игнорируйте любые осложнения, такие как потеря воды в результате испарения.
- Показать, что 1 кал/г · ºC = 1 ккал/кг · ºC.
- Чтобы стерилизовать стеклянную детскую бутылочку весом 50,0 г, мы должны поднять ее температуру с 22,0ºC до 95,0ºC.
 Какая теплопередача требуется?
Какая теплопередача требуется? - Одинаковая передача тепла одинаковым массам различных веществ вызывает различные изменения температуры. Рассчитайте конечную температуру, когда 1,00 ккал теплоты переходит в 1,00 кг следующих веществ при исходной температуре 20,0ºC: (a) вода; (б) бетон; (в) сталь; и d) ртуть.
- Потирание рук согревает их, превращая работу в тепловую энергию. Если женщина потирает руки взад-вперед, совершая в общей сложности 20 движений, на расстоянии 7,50 см за одно движение и со средней силой трения 40,0 Н, на сколько повысится температура? Масса согреваемых тканей составляет всего 0,100 кг, преимущественно в ладонях и пальцах.
- Блок чистого материала массой 0,250 кг нагревается с 20,0ºC до 65,0ºC за счет добавления 4,35 кДж энергии. Рассчитайте его удельную теплоемкость и определите вещество, из которого он, скорее всего, состоит.
- Предположим, что одинаковые количества тепла передаются разным массам меди и воды, вызывая одинаковые изменения температуры.
 Каково отношение массы меди к воде?
Каково отношение массы меди к воде? - (a) Количество килокалорий в пище определяется методами калориметрии, при которых пища сжигается и измеряется количество теплопередачи. Сколько килокалорий на грамм содержится в 5,00 г арахиса, если энергия его сжигания передается 0,500 кг воды, находящейся в алюминиевом стакане весом 0,100 кг, вызывая 54,9ºC повышение температуры? (б) Сравните свой ответ с информацией на этикетке на упаковке арахиса и прокомментируйте, совпадают ли значения.
- После интенсивной физической нагрузки температура тела человека массой 80,0 кг составляет 40,0ºC. С какой скоростью в ваттах человек должен передать тепловую энергию, чтобы снизить температуру тела до 37,0ºC за 30,0 мин, если предположить, что тело продолжает производить энергию мощностью 150 Вт? 1 Вт = 1 Дж/сек или 1 Вт = 1 Дж/сек.
- Даже при остановке после периода нормальной эксплуатации большой коммерческий ядерный реактор передает тепловую энергию со скоростью 150 МВт за счет радиоактивного распада продуктов деления.
 Этот теплообмен вызывает быстрое повышение температуры в случае отказа системы охлаждения (1 Вт = 1 Дж/сек или 1 Вт = 1 Дж/сек и 1 МВт = 1 мегаватт). (a) Рассчитайте скорость повышения температуры в градусах Цельсия в секунду (ºC/с), если масса активной зоны реактора составляет 1,60 × 10 5 кг и имеет среднюю удельную теплоемкость 0,3349 кДж/кг ⋅ ºC. (б) Сколько времени потребуется, чтобы получить повышение температуры на 2000ºC, что может привести к плавлению некоторых металлов, содержащих радиоактивные материалы? (Начальная скорость повышения температуры будет больше рассчитанной здесь, поскольку теплопередача сосредоточена в меньшей массе. Однако позже рост температуры замедлится, поскольку стальная защитная оболочка массой 5 × 10 5 кг также начинают нагреваться.)
Этот теплообмен вызывает быстрое повышение температуры в случае отказа системы охлаждения (1 Вт = 1 Дж/сек или 1 Вт = 1 Дж/сек и 1 МВт = 1 мегаватт). (a) Рассчитайте скорость повышения температуры в градусах Цельсия в секунду (ºC/с), если масса активной зоны реактора составляет 1,60 × 10 5 кг и имеет среднюю удельную теплоемкость 0,3349 кДж/кг ⋅ ºC. (б) Сколько времени потребуется, чтобы получить повышение температуры на 2000ºC, что может привести к плавлению некоторых металлов, содержащих радиоактивные материалы? (Начальная скорость повышения температуры будет больше рассчитанной здесь, поскольку теплопередача сосредоточена в меньшей массе. Однако позже рост температуры замедлится, поскольку стальная защитная оболочка массой 5 × 10 5 кг также начинают нагреваться.)
Рис. 3. Бассейн с радиоактивным отработавшим топливом на атомной электростанции. Отработавшее топливо долго остается горячим. (кредит: Министерство энергетики США)
Глоссарий
удельная теплоемкость: количество теплоты, необходимое для изменения температуры 1,00 кг вещества на 1,00 ºC
Избранные решения задач и упражнений
× 2. 10 8 J
10 8 J
3. 3,07 × 10 3 J
5. 0,171ºC
7. 10,8
9. 617 Вт
- Значения для твердых и жидких веществ даны при постоянном объеме и температуре 25ºC, если не указано иное. ↵
- Эти значения идентичны в единицах кал/г ⋅ ºC. ↵
- c v при постоянном объеме и температуре 20,0ºC, если не указано иное, и среднем давлении 1,00 атм. В скобках указаны значения c p при постоянном давлении 1,00 атм. ↵
Формула теплоты – Вывод, примеры и часто задаваемые вопросы
Теплофизика имеет дело со многими уравнениями и формулами, которые оказываются полезными во всех аспектах науки. Одной из полезных формул в области теплофизики является формула теплопроводности. Мы знаем, что теплота — это еще одна форма энергии, которая передается между двумя веществами, находящимися при разных температурах. Направление потока энергии всегда от вещества, находящегося при более высокой температуре, к веществу, находящемуся при более низкой температуре.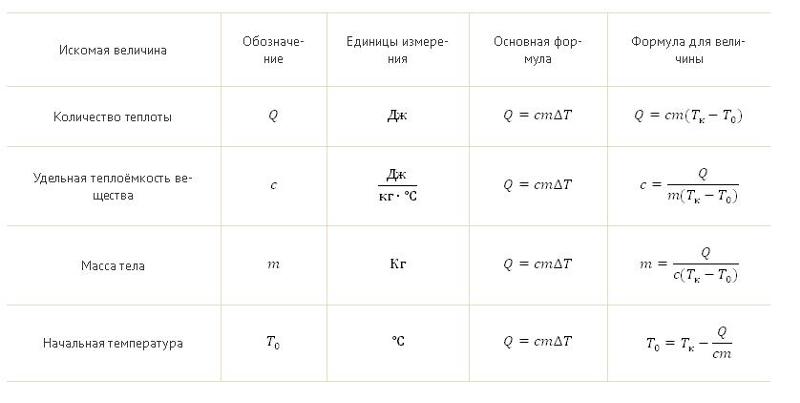 Тепловая энергия также передается от более горячих тел к более низким телам без нарушения закона сохранения энергии.
Тепловая энергия также передается от более горячих тел к более низким телам без нарушения закона сохранения энергии.
Тепло обычно измеряется в виде энергии, поэтому единица измерения тепла такая же, как единица энергии, т. е. калории или джоули. студенты часто путают термины «тепло» и «температура», «тепло» — это эффект температуры, и это не одно и то же. Теплоту и температуру нельзя поменять местами, но это неправильно. Тепло и температура не могут быть заменены местами, потому что температура будет измерять уровень тепла или холода наблюдаемого материала. В этой статье мы обсудим формулу теплоемкости, формулу удельной теплоемкости, формулу удельной теплоемкости, формулу энтальпии с решенными численными задачами.
Формула удельной теплоемкости:
Мы знаем, что термин удельная теплоемкость в термодинамике относится к отношению количества тепла, необходимого для повышения температуры вещества на один градус Цельсия, к количеству тепла, необходимому для повышения температуры эквивалентная масса жидкости (скажем, воды) на один градус Цельсия. В то же время мы используем термин «удельная теплоемкость» по более традиционной причине для определения количества тепла в калориях, которое нам требуется для повышения температуры одного грамма материала на один градус Цельсия.
В то же время мы используем термин «удельная теплоемкость» по более традиционной причине для определения количества тепла в калориях, которое нам требуется для повышения температуры одного грамма материала на один градус Цельсия.
Проще говоря, уравнение удельной теплоемкости или формула удельной теплоемкости представляет собой отношение количества теплоты, необходимого для повышения температуры вещества на один градус Цельсия, к количеству теплоты, необходимому для повышения температуры равного количества воды на один градус Цельсия при комнатной температуре.
Термин удельная теплоемкость обычно используется, когда мы имеем в виду что-то конкретное, например, мы имеем в виду повышение температуры определенного вещества. Сейчас обычно все путаются между удельной теплоемкостью и теплоемкостью.
Удельная теплоемкость Формула:
Теплоемкость — это отношение количества тепла, необходимого для изменения температуры на один градус Цельсия, тогда как удельная теплоемкость — это количество тепла, необходимое для повышения температуры вещества, а не только изменить или изменить температуру материала. Здесь важно отметить один важный момент: когда мы рассматриваем конкретное количество массы, мы склонны использовать слова «удельная теплоемкость» или «удельная теплоемкость». Удельная теплоемкость большинства термодинамических систем непостоянна и зависит от физических величин, таких как давление, объем и температура.
Здесь важно отметить один важный момент: когда мы рассматриваем конкретное количество массы, мы склонны использовать слова «удельная теплоемкость» или «удельная теплоемкость». Удельная теплоемкость большинства термодинамических систем непостоянна и зависит от физических величин, таких как давление, объем и температура.
Вывод:
Теперь давайте посмотрим на формулу удельной теплоемкости или формулу удельной теплоемкости, которая обозначается буквой C. Согласно определению удельной теплоемкости, мы видели, что она прямо пропорциональна изменение температуры (в частности повышение температуры). Мы знаем, что количество требуемой теплоты (Q) прямо пропорционально изменению температуры, поэтому запишем:
⇒ Q ∝ ΔT ……(1)
Где,
ΔT – изменение или повышение температуры
Также мы знаем, что удельная теплоемкость тоже прямо пропорциональна массе рассматриваемого вещества, таким образом получаем:
⇒ Q ∝ м ……. .(2)
.(2)
Где,
м – Масса вещества
Объединяя уравнения (1) и (2), получаем:
⇒ Q ∝ mΔT
⇒ Q = CmΔT
Где,
C – удельная теплоемкость
Таким образом, дано уравнение теплоемкости по:
⇒ C = \[\frac{Q}{m \Delta T }\]
9{0}\]c……..(3)Где,
\[\Delta\]Q – количество полученного или потерянного тепла в джоулях
\[\Delta\]T – изменение или увеличение при температуре в градусах Цельсия
m – Масса вещества в кг
Уравнение (3) известно как формула удельной теплоемкости или формула удельной теплоемкости в физике и используется для решения примеров удельной теплоемкости и оценки удельной теплота вещества в реальной жизни. Удельная теплоемкость вещества будет варьироваться в зависимости от типа вещества.
Формула скрытой теплоты:
Так же, как и формула удельной теплоемкости, можно вывести множество других тепловых формул, таких как формула скрытой теплоты, формула теплопроводности, формула теплопередачи, формула тепловой энергии и т. д., которые можно использовать для расчет различных параметров данной термодинамической системы.
д., которые можно использовать для расчет различных параметров данной термодинамической системы.
Одной из полезных формул в термодинамике является скрытая теплоемкость или формула скрытой теплоты. Скрытую теплоту можно определить как количество теплоты, поглощаемой или выделяемой термодинамической системой при фазовом переходе при постоянной температуре. Или, другими словами, скрытая теплота — это количество тепла, необходимое для преобразования фаз материала, то есть твердого тела в жидкую или паровую фазу, или жидкости в паровую фазу или наоборот. В зависимости от фазового превращения скрытая теплота имеет разные теги. Скрытая теплота также известна как теплота конденсации, теплота парообразования и т. д.
Также определяется как отношение количества поглощенного или выделенного тепла к массе вещества. Обозначается буквой L, а формула скрытой теплоты имеет вид:
⇒ L = \[\frac{Q}{м}\]
Где,
Q – Количество подведенного тепла
м – Масса вещества
Скрытая теплота вещества измеряется в единицах Кал/г. Примерами скрытой теплоты являются скрытая теплота парообразования или скрытая теплота конденсации, когда вещество либо поглощает и испаряется, либо конденсируется с образованием осадка.
Примерами скрытой теплоты являются скрытая теплота парообразования или скрытая теплота конденсации, когда вещество либо поглощает и испаряется, либо конденсируется с образованием осадка.
Примеры:
1. Рассчитайте количество тепла, необходимое для нагревания 4 кг воды с 30⁰C до 70⁰C? (удельная теплоемкость воды = 4,2 x 10³ Дж/кг⁰c)
Сол:
Дано,
Масса воды = m = 6 кг
Изменение температуры = ∆T = T₂ – T₁ = 70 – 30 = 40⁰c
Удельная теплоемкость воды = C = 4,2 x 10³ Дж/кг⁰c
Теперь мы стремимся определить количество тепла, необходимое для повышения температуры 6 кг воды с 40⁰C до 80⁰C. Таким образом, мы знаем, что необходимое количество определяется уравнением:
⇒ Q = Cm∆T
Где,
C – Удельная теплоемкость вещества
∆T – Изменение или повышение температуры
m – Масса вещества
Подставляя, требуемые значения в приведенное выше выражение:
⇒ Q = Cm∆T = (4,2 x 10³)(4)(40)
⇒ Q = 672 x 103 джоулей
⇒ Q = 672 кДж
Следовательно, количество теплоты, необходимое для Поднять 4 кг воды с 30⁰C до 70⁰C составляет 672 кДж.


 Это соотношение также можно рассматривать как определение удельной теплоемкости.
Это соотношение также можно рассматривать как определение удельной теплоемкости. Какая теплопередача требуется?
Какая теплопередача требуется? Каково отношение массы меди к воде?
Каково отношение массы меди к воде? Этот теплообмен вызывает быстрое повышение температуры в случае отказа системы охлаждения (1 Вт = 1 Дж/сек или 1 Вт = 1 Дж/сек и 1 МВт = 1 мегаватт). (a) Рассчитайте скорость повышения температуры в градусах Цельсия в секунду (ºC/с), если масса активной зоны реактора составляет 1,60 × 10 5 кг и имеет среднюю удельную теплоемкость 0,3349 кДж/кг ⋅ ºC. (б) Сколько времени потребуется, чтобы получить повышение температуры на 2000ºC, что может привести к плавлению некоторых металлов, содержащих радиоактивные материалы? (Начальная скорость повышения температуры будет больше рассчитанной здесь, поскольку теплопередача сосредоточена в меньшей массе. Однако позже рост температуры замедлится, поскольку стальная защитная оболочка массой 5 × 10 5 кг также начинают нагреваться.)
Этот теплообмен вызывает быстрое повышение температуры в случае отказа системы охлаждения (1 Вт = 1 Дж/сек или 1 Вт = 1 Дж/сек и 1 МВт = 1 мегаватт). (a) Рассчитайте скорость повышения температуры в градусах Цельсия в секунду (ºC/с), если масса активной зоны реактора составляет 1,60 × 10 5 кг и имеет среднюю удельную теплоемкость 0,3349 кДж/кг ⋅ ºC. (б) Сколько времени потребуется, чтобы получить повышение температуры на 2000ºC, что может привести к плавлению некоторых металлов, содержащих радиоактивные материалы? (Начальная скорость повышения температуры будет больше рассчитанной здесь, поскольку теплопередача сосредоточена в меньшей массе. Однако позже рост температуры замедлится, поскольку стальная защитная оболочка массой 5 × 10 5 кг также начинают нагреваться.)