Посвященная таблице Менделеева акция “Открытая лабораторная” пройдет в РФ и еще 30 странах – Наука
МОСКВА, 9 февраля. /ТАСС/. Научно-популярная акция “Открытая лабораторная”, которая пройдет в России и еще 30 странах в субботу, станет одним из первых российских событий объявленного в 2019 году Международного года периодической таблицы химических элементов. Традиционный тест на научную грамотность будет посвящен жизни и работе ее создателя Дмитрия Менделеева, а также популярным мифам о химии, сообщает пресс-служба автономной некоммерческой организации “Лаборатория просветительских проектов”.
“Открытая лабораторная” начнет Международный год периодической таблицы химических элементов, объявленный ООН и ЮНЕСКО. Участники ответят на вопросы, посвященные жизни и работе Дмитрия Менделеева, а также разберут популярные научные мифы <…> 25 вопросов будут ждать ответов участников “Открытой лабораторной”, пришедших на одну из более чем трехсот площадок акции 9 февраля”, – говорится в сообщении.
В акции могут принять участие все желающие старше 12 лет. После завершения письменной работы ведущие ученые и популяризаторы химии назовут правильные ответы и разберут с аудиторией каждое задание.
Акция впервые будет проходить не только на русском, но и на английском языке. При поддержке Россотрудничества “Открытая лабораторная” пройдет в 30 странах. За рубежом площадками проведения акции станут российские центры науки и культуры. “По предварительной информации, в акции примут участие более 100 тысяч человек по всему миру”, – приводятся в сообщении слова руководителя акции Евгения Насырова.
Участников “Открытой лабораторной” также ждут научные шоу, экскурсии, лекции и научно-популярные фильмы. Акция пройдет в Москве, Петербурге и еще 109 городах России. Жители столицы России смогут принять в ней участие на девяти площадках, среди которых Российский научный фонд, химический факультет МГУ, парк “Зарядье” и другие. Расписание тестирования и регистрация – на сайте openlaba.
Ранее в этом месяце международная акция “Открытая лабораторная” стала лауреатом премии “За верность науке” в номинации “Прорыв года”, которую проводит Министерство науки и высшего образования РФ совместно с Министерством просвещения, Российской академией наук и МГУ имени М. В. Ломоносова.
Памятка участнику репетиционного тестирования (on-line режим) » Республиканский Институт Контроля Знаний
Памятка участнику репетиционного тестирования (on-line режим)
Репетиционное тестирование (РТ) в on-line режиме проводится для проверки знаний по учебным предметам и адаптации абитуриентов к условиям сдачи вступительных испытаний в форме централизованного тестирования.
Для того чтобы пройти РТ в on-line режиме абитуриенту необходимо иметь учетную запись в системе регистрации на репетиционное тестирование на сайте РИКЗ. Если вы зарегистрированы в системе, войдите в свой личный кабинет на сайте РИКЗ.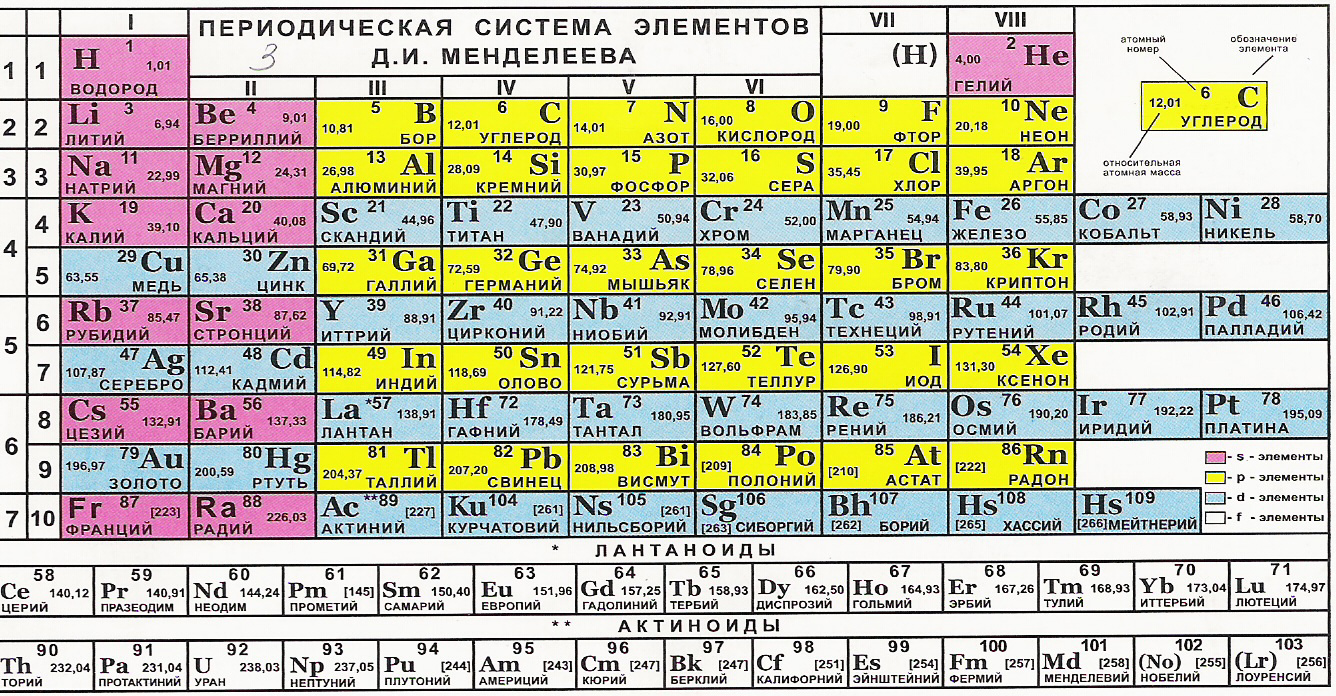 Если вы еще не зарегистрированы в системе, пройдите регистрацию и войдите в свою учетную запись.
Если вы еще не зарегистрированы в системе, пройдите регистрацию и войдите в свою учетную запись.
По аналогии с регистрацией на обычное репетиционное тестирование вам необходимо оформить в своем личном кабинете на сайте РИКЗ заявку на прохождение РТ в on-line режиме. Для этого в области добавления заявок на РТ выберите вкладку «РТ on-line». После этого укажите учебный предмет, язык представления теста и вариант теста. Подтвердите свой выбор.
Оплатите оформленную заявку на тестирование. Для оплаты можно использовать имеющиеся в системе регистрации «свободные оплаты» (образовавшиеся после отмены обычных сеансов РТ) или произвести платеж в системе «Расчет» (ЕРИП).
Подробно о создании учетной записи в системе регистрации РТ, авторизации в системе, оформлении заявки на участие в РТ, а также о том, как оплатить участие в РТ, можно ознакомиться в
После подтверждения факта оплаты вы можете приступить к выполнению теста. Для этого в своем личном кабинете на сайте РИКЗ в таблице регистраций выберите нужный тест и нажмите кнопку «Пройти».
Для этого в своем личном кабинете на сайте РИКЗ в таблице регистраций выберите нужный тест и нажмите кнопку «Пройти».
Для корректной работы сервиса по прохождению РТ в режиме on–line требуется использовать актуальную версию браузера Google Chrome.
Перед началом работы убедитесь, что в браузере отключена блокировка всплывающих окон. Для этого через разделы меню «Настройки» – «Конфиденциальность и безопасность» – «Настройки сайта – Разрешения» – «Всплывающие окна и переадресация» необходимо установить переключатель в положение «Разрешить», после чего кликнуть по кнопке «Добавить» и вставить строку https://reg.rikc.by
Перед началом сеанса тестирования рекомендуем подготовить в необходимом вам количестве черновые листы для записей, ручку. При прохождении тестирования по физике и химии вам может понадобиться калькулятор.
Абитуриенты, желающие распечатать тест, могут сделать это до начала сеанса тестирования (до нажатия на кнопку «Начать тестирование»), нажав в появившемся окне на кнопку «Распечатать тест». Рекомендуем сделать это. Однако обращаем внимание, что ознакомиться с содержанием тестовых заданий необходимо только после начала сеанса тестирования (после нажатия на кнопку «Начать тестирование»).
При нажатии на кнопку «Начать тестирование» начнется отсчет времени, отведенного на выполнение теста по выбранному вами учебному предмету, и вы перейдете на вкладку браузера, содержащую электронный вид бланка ответов РТ, при этом вам также будет доступен для просмотра в электронном виде бланк тестового задания.
При выполнении теста по химии будет доступна периодическая система химических элементов Д. И. Менделеева и таблица растворимости солей, кислот и оснований в воде, электрохимический ряд активности металлов.
При выполнении тестов по иностранным языкам будет доступна инструкция по внесению с клавиатуры букв, не входящих в стандартный набор латиницы.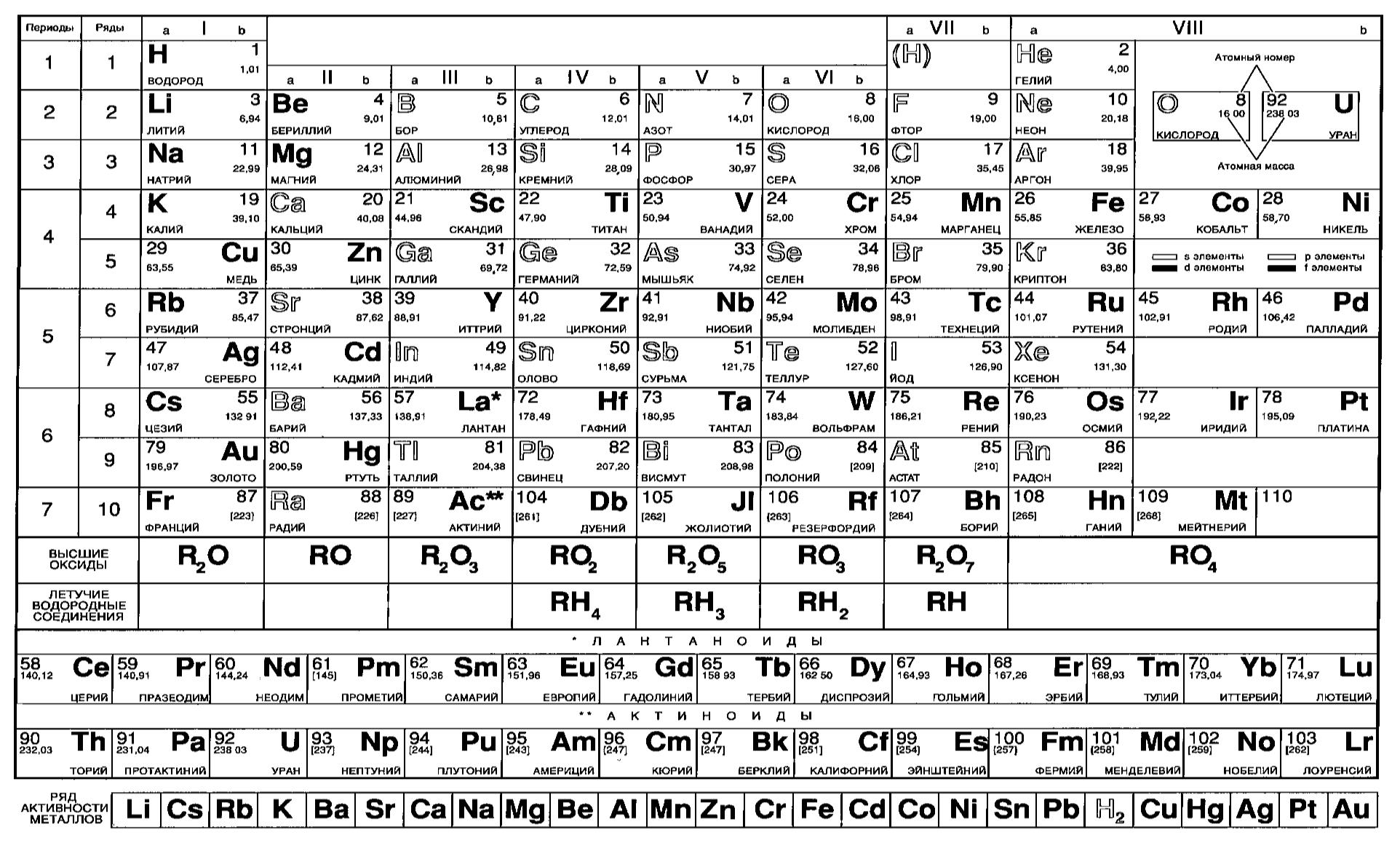
Система предупредит вас за 15 и 5 минут до окончания времени, отведенного на выполнение теста.
Если вы закончили работу с тестом и заполнили бланк ответов до окончания времени, отведенного на выполнение теста (отображается в правом нижнем углу экрана), нажмите на кнопку «Завершить тестирование».
По истечении времени, отведенного на выполнение теста, если вы не нажали на кнопку «Завершить тестирование», система прервет сеанс тестирования, сохранив те ответы, которые вы внесли в электронную форму бланка ответов. В этой связи, как и при прохождении централизованного тестирования, вам необходимо оставить время для заполнения бланка ответов.
Результат выполнения теста отобразится на экране компьютера и будет доступен для просмотра в личном кабинете абитуриента на сайте РИКЗ по аналогии с бланочным РТ.
Как и при прохождении обычного репетиционного тестирования, с определенной даты в личном кабинете абитуриента будет доступна консультация для выполнения работы над ошибками.
В случае прерывания сеанса тестирования (выключение компьютера, случайное закрытие вкладки в браузере и пр.) возобновить работу над тестом можно будет через личный кабинет абитуриента.
Рекомендуем ответственно подойти к выполнению заданий теста и заполнению бланка ответов. Не используйте помощь посторонних лиц,а также вспомогательную справочную литературу. Добросовестная работа позволит вам получить объективный результат.
Напоминаем вам, что тесты репетиционного тестирования охраняются Законом об авторском праве, и вы не должны передавать их содержание третьим лицам и распространять их через сеть Интернет или каким-либо другим образом.
Краткий конспект подготовки к ЗНО по химии №4 Периодический закон и периодическая система химических элементов Д. И. Менделеева
Подготовка к ВНО. Химия.
Конспект 4. Периодический закон и периодическая система химических элементов Д. И. Менделеева
Открытие Периодического закона
Основной закон химии – Периодический закон был открыт Д. И. Менделеевым в 1869 году в то время, когда атом считался неделимым, и о его внутреннем строении ничего не было известно. В основу Периодического закона Д.И. Менделеев положил атомные массы (ранее – атомные веса) и химические свойства элементов. Расположив 63 известных в то время элемента в порядке возрастания их атомных масс, Д. И. Менделеев получил естественный (природный) ряд химических элементов, в котором он обнаружил периодическую повторяемость химических свойств. Например, свойства типичного металла лития повторялись у элементов натрия и калия , свойства типичного неметалла фтора – у элементов хлора , брома , иода .
И. Менделеевым в 1869 году в то время, когда атом считался неделимым, и о его внутреннем строении ничего не было известно. В основу Периодического закона Д.И. Менделеев положил атомные массы (ранее – атомные веса) и химические свойства элементов. Расположив 63 известных в то время элемента в порядке возрастания их атомных масс, Д. И. Менделеев получил естественный (природный) ряд химических элементов, в котором он обнаружил периодическую повторяемость химических свойств. Например, свойства типичного металла лития повторялись у элементов натрия и калия , свойства типичного неметалла фтора – у элементов хлора , брома , иода .

Периодический закон в формулировке Д.И. Менделеева
Свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величины атомных весов элементов.
Периодическая система химических элементов
На основе Периодического закона Д.И. Менделеев создал Периодическую систему химических элементов. Она состоит из 7 периодов и 8 групп (короткопериодный вариант таблицы).
Периоды – это горизонтальные ряды таблицы. Они подразделяются на малые и большие.
В малых периодах находится 2 элемента (1-й период) или 8 элементов (2-й, 3-й периоды), В больших периодах – 18 элементов (4-й, 5-й периоды) или 32 элемента (6-й, 7-й период). Каждый период начинается с типичного металла, а заканчивается благородным газом.
Группы – это вертикальные последовательности элементов, они нумеруется римской цифрой от I до VIII и русскими буквами А и Б. Короткопериодный вариант Периодической системы включает подгруппы элементов (главную и побочную).
Короткопериодный вариант Периодической системы включает подгруппы элементов (главную и побочную).
Подгруппа – это совокупность элементов, являющихся безусловными химическими аналогами; часто элементы подгруппы обладают высшей степенью окисления, отвечающей номеру группы.
В А-группах химические свойства элементов могут меняться в широком диапазоне от неметаллических к металлическим (например, в главной подгруппе V группы азот – неметалл, а висмут – металл).
В Периодической системе типичные металлы расположены в IА группе (),
IIА () и IIIА ().
Неметаллы расположены в группах VIIА (), VIА (), VА (), IVА () и IIIА ().
Некоторые элементы А-групп (бериллий , алюминий , германий , сурьма , полоний и другие), а также многие элементы Б-групп проявляют и металлические, и неметаллические свойства (явление амфотерности).
Некоторые главные подруппы имеют свои особенные названия:
| I-a | Щелочные металлы |
| II-a | Щелочноземельные металлы |
| V-a | Пниктогены |
| VI-a | Халькогены |
| VII-a | Галогены |
| VIII-a | Благородные (инертные) газы |
В каждой ячейке, соответствующей элементу, представлены: химический символ, название, порядковый номер, соответствующий числу протонов в атоме, относительная атомная масса.
Число электронов в атоме соответствует числу протонов. Количество нейтронов в атоме можно найти, по разности меду относительной атомной массой и количеством протонов, т.е. порядкового номера.
У каждой группы есть формула высшего оксида, т.е. оксиды с максимальной степенью окисления элементов. Эта информация написана внизу таблицы.
Например, для элементов V группы, формула высшего оксида: . Это .
По составу высшего оксида элемента можно определить его свойства. Оксиды состава – основные, – чаще всего – амфотерные. Остальные оксиды – кислотные. Чем выше степень окисления элемента , чем ярче выраженными кислотными свойствами обладает его оксид.
Таким образом, кислотность высших оксидов элементов главных подгрупп увеличивается по периоду слева направо.
В таблице отражен состав летучих водородных соединений. Такие соединения образуют элементы IV-VII групп, причем только легких.
Изменение атомного радиуса
В группах: Для элементов главных подгрупп, сверху вниз увеличивается число энергетических уровней. Энергетический уровень – это и есть расстояние, на котором находится электрон от ядра. Значит, по группе вниз атомный радиус увеличивается.
В периодах: По периоду номер энергетического уровня, на котором находятся валентные электроны, остается неизменным, но число валентных электронов увеличивается, а также растет и заряд ядра.
Значит, электроны электростатически сильнее притягиваются к ядру. Поэтому радиус атома уменьшается.
Закономерности изменения периодических свойств
| Параметр | По группе вниз | По периоду вправо |
| Заряд ядра | Увеличивается | Увеличивается |
| Число валентных электронов | Не меняется | Увеличивается |
| Число энергетических уровней | Увеличивается | Не меняется |
| Радиус атома | Увеличивается | Уменьшается |
| Электроотрицательность | Уменьшается | Увеличивается |
| Металлические свойства | Увеличиваются | Уменьшаются |
| Степень окисления в высшем оксиде | Не меняется | Увеличивается |
|
Степень окисления в водородных соединениях (для элементов IV-VII групп) |
Не меняется | Увеличивается |
Современная формулировка закона: свойства химических элементов, простых веществ, также состав и свойства соединений находятся в периодической зависимости от значений зарядов ядер атомов.
Тесты подготовки к ЗНО:
Online-тест подготовки к ЗНО по химии №4 “Периодический закон”
Вводное занятие по химии – Галина Енютина
Привет, дорогой друг!
Хочешь научиться понимать химию и окунуться в волшебный мир веществ, формул, химических превращений? – Тогда ты попал по адресу!
Вводный тест
Для начала пройди вводный тест Пройти тест
Анкета ученика
Теперь заполни анкету Заполнить анкету
Знакомство
А теперь давай познакомимся, ведь нам предстоит вместе работать в течение года!
Давай познакомимсяОпредели свою цельЧто нужно для занятияКак мы работаемЧто делать после занятияОбучающие материалыРекомендации по изучению химииТвой результат после прохождения курса
- Химический знак = приветствие
- Название = имя
- Номер = возраст
- Атомная масса = кто я (статус)
- Группа, период – где я живу
- Свойства = я по характеру
- С кем я реагирую = мое хобби
Давай определим цель занятий
Ответь на 3 простых вопроса:
- Зачем тебе заниматься химией?
- Что ты хочешь получить в результате занятий?
- Что даст тебе этот результат?
Ответил? – А теперь давай разберемся, чем же мы будем заниматься.
а ещё:
- программа Skype
- тетрадь и ручка
- таблица Менделеева
- тишина в комнате
- выключенный звук на телефоне
- всякие вкусняшки (сухофрукты, шоколад, орехи) и стакан воды
Что мы будем делать на занятии?
Длительность занятия 60 минут.
Контроль
- входной контроль
- проверка ДЗ
- выявление имеющихся знаний
Теория
- обсуждение
- презентации
- онлайн-учебник
- конспект занятия
- интеллект-карты
- видео-ролики
Практика
- разбор алгоритмов
- решение задач
- практическое применение знаний
- связь биологии с другими науками
Контроль
- тесты (на бумаге и онлайн)
- задачи
- флеш-тесты
- вопросы
- кейсы
ДЗ
- тесты
- задачи
- практические задания
- творческие задания
- Отдохнуть.

- Подкрепиться.
- Открыть браузер и пройти по ссылке в папку УРОКИ ХИМИИ либо по ссылке на сайт и скачать все материалы для изучения для конкретного урока
- Создать отдельную папку на рабочем столе и складывать там все материалы курса
- Приступить к домашнему заданию: начать с теории, потом выполнять задания
- Выполнить задания из файла Домашнее задание к уроку
- Отправить задание на е-майл или выложить в соответствующую папку на том же Яндекс.Диске
- Всегда держи под рукой таблицу Менделеева и таблицу растворимости.
- Всегда записывай ход решения любого задания, даже если можешь решить его в уме.
- Используй максимальное количество источников информации (не менее 3-х).
- Внимательно читай условие задачи и задание, прежде чем выполнить его. Большинство ошибок возникает именно из-за невнимательности.
- При любых сомнениях в решении задания сразу обращайся сначала к теории, потом обратиться к учителю.
- Перед новым занятием обязательно выполни домашку, она придумана не для учителя, а для тебя, чтобы закрепить материал и пойти дальше к более сложным темам.
- Выполняй задания в три подхода: сразу в день после занятия (хотя бы полчаса),
- Если тебе трудно решить какое-то задание с первого раза, не отчаивайся и попробуй решить его завтра.
Ты получишь
- Базовые знания по химии
- Основы работы с таблицей Менделеева
- Важные навыки для химических расчетов
- Лайфхаки для быстрого решения заданий по химии
- Навыки построения интеллект карт для обучения
- Заряд мотивации и уверенности в своих силах для дальнейшего обучения
Ты будешь знать
- что такое ПСХЭ, РИО, ТЭД, ОВР и ЭО
- как не путать Калий и Кальций, отличать металлы от неметаллов
- что такое моль и почему это не только насекомое
- как выглядят атомы/молекулы/ионы, кислоты и соли, жидкости и газы
- как происходит взаимодействие веществ
- узнаешь много новых терминов и понятий
Ты будешь уметь
- называть и определять химические соединения
- составлять формулы химических веществ и определять их виды
- составлять химические уравнения
- определять состав атома
- писать электронный баланс
- решать основные виды задач по химии
Ну что, поехали? Осталось только обсудить некоторые детали:
Расписание
Мы встречаемся2 раза в неделю
Занимаемся 1 час (60 минут)
Время – согласуем
Оплата
Перевод на карту ТиньковОплата за месяц вперед
(минимум 8 занятий)
Обратная связь
E-mail:galina@enutina. ru
Skype: enyutinagv
ВК: vk.com/enutina_ru
Ученые КФУ нашли на месторождении гипса в Татарстане вещество внеземного происхождения
Ученые КФУ нашли на Камско-Устьинском месторождении гипса вещество внеземного происхождения. Образец с необычайно плотными микровключениями обнаружила студентка КФУ Клавдия Петренко. Научная группа исследовала богатые железом микросферы и микрочастицы, содержащиеся в гипсовой породе, сообщает пресс-служба КФУ.
«Предварительное изучение состава показало, что основным их компонентом является железо. Используя комплекс методов для микроанализа, мы изучили различные возможности их происхождения и пришли к выводу, что микровключения из верхнеказанского подъяруса имеют внеземной генезис», — сообщил доцент кафедры региональной геологии и полезных ископаемых Института геологии и нефтегазовых технологий КФУ Раиль Кадыров.
org/ImageObject” itemprop=”image”>Фото: пресс-служба КФУ
Космическое происхождение находки подтверждается тем, что она имеет сферическую морфологию; размеры 10−150 мкм; дендритные текстуры, имеющие решетчатый или ячеистый вид; большие субсферические полости, где раньше располагались выветрившиеся металлические ядра; нерегулярные сети полостей — везикулы от остаточных захваченных летучих газов; обогащенная железом минералогия, характерная для магнетита.
Обнаруженные микрочастицы и микросферулы за последние 2 млн лет претерпели диагенетические изменения. Основываясь на необычайной концентрации внеземных микросфер и очень близких к ним по составу микрочастиц, сконцентрированных в тонкой доломитовой прослойке исследуемого образца, ученые предположили их происхождение от метеорной абляции — процесса разрушения поверхности метеорного тела при движении в атмосфере.
Ученые предполагают, что метеорное тело подверглось разрушению при движении в атмосфере, произошедшем над исследуемой территорией 272,95 млн лет назад.
Испытания российской вакцины от коронавируса «Бетувакс-Ков-2» могут начаться в сентябре
Испытания российской вакцины от коронавируса «Бетувакс-Ков-2» могут начаться в сентябре
«Компания «Институт стволовых клеток человека» (ИСКЧ, участник рынка НТИ «Хелснет»), ставшая разработчиком российской рекомбинантной вакцины от коронавируса «Бетувакс-Ков-2» совместно с компанией «Бетувакс», готовится к началу клинических исследований в сентябре 2021 года. <…> Сейчас Минздрав РФ рассматривает заявку на клинические испытания вакцины и по стандартной процедуре задает разработчикам дополнительные вопросы», — сказали в Платформе Национальной технологической инициативы (НТИ).
закрытьВакцина «Бетувакс-Ков-2» — рекомбинантная вакцина на основе сферических частиц содержащих поверхностный антиген (белок) коронавируса. Такой тип вакцин относится к субъединичным вакцинам. Они содержат только поверхностные антигены коронавируса, что позволяет уменьшить содержание белка и, следовательно, снизить аллергенность препарата. Субъединичные вакцины реже других дают побочные эффекты, что особенно важно для групп риска и имеют хорошие перспективы при использовании для повторных вакцинаций. Конструкция вакцины «Бетувакс-КоВ-2» также даёт возможность её быстрой оптимизации под новые штаммы коронавируса.
Они содержат только поверхностные антигены коронавируса, что позволяет уменьшить содержание белка и, следовательно, снизить аллергенность препарата. Субъединичные вакцины реже других дают побочные эффекты, что особенно важно для групп риска и имеют хорошие перспективы при использовании для повторных вакцинаций. Конструкция вакцины «Бетувакс-КоВ-2» также даёт возможность её быстрой оптимизации под новые штаммы коронавируса.
Создание вакцины началось летом 2020 года. По результатам доклинических исследований, вакцина «Бетувакс-КоВ-2» показала хороший профиль безопасности и эффективности с формированием высоких титров нейтрализующих антител против коронавируса SARS-CoV-2 на моделях животных. Разработка вакцины была поддержана Фондом развития венчурного инвестирования города Москвы (Moscow Seed Fund).
Поданная в Минздрав заявка предполагает совмещенные 1-2 фазы исследования, в которых в общей сложности примут участие 116 добровольцев от 18 до 60 лет без хронических заболеваний, сообщают разработчики.
Холдинг «Институт стволовых клеток человека», основанный в 2003 году, объединяет несколько компаний в сфере генной терапии, регенеративной медицины, генетической диагностики и консалтинга. Наибольшая доля выручки приходится на компанию Genetico, которая занимается разработкой генетических тестов, решений для онкоскрининга и ряда других направлений. В конце июля 2021 года компания группы ИСКЧ Бетувакс стала резидентом инновационного центра Сколково и вошла в кластер Биомед.
Проверить зрения онлайн. Проверка остроты зрения
Содержание:
Общие тенденции ухудшения зрения
В последние годы врачи отмечают общий уровень падения остроты зрения не только у взрослых и пожилых людей, но и у подростков. Очень важно не проигнорировать первые признаки ухудшения зрения (повышенную утомляемость глаз, покраснение и раздражение век) и вовремя обратиться за консультацией к врачу-офтальмологу. Проверить зрение, как правило, можно в ближайшем салоне оптики. В случае, если такая возможность отсутствует, на помощь придут специальные онлайн-тесты для самостоятельной проверки зрения и материалы, доступные в интернете для каждого.
В случае, если такая возможность отсутствует, на помощь придут специальные онлайн-тесты для самостоятельной проверки зрения и материалы, доступные в интернете для каждого.
Проверка зрения в домашних условиях: о чем нужно знать
Тесты для самостоятельной проверки зрения в домашних условиях ничем не отличаются от тех, которыми пользуются специалисты в салонах оптики, поликлиниках и медицинских центрах. Два главных условия прохождения тестов — достаточно интенсивное освещение комнаты (в идеале естественный дневной свет) и хорошее самочувствие. Проверка зрения при головных болях, повышенной температуре или чрезмерной усталости может показать искаженные результаты. Тусклый искусственный свет в тёмное время суток дополнительно напрягает глаза — результаты такого теста могут быть необъективными.
Этапы самостоятельной проверки зрения:
- Выберите и скачайте из сети подходящий тест. Самыми распространенными и популярными вариантами считаются таблица Сивцева и таблица Орловой, предназначенная для маленьких детей.

- Распечатайте таблицу на лазерном принтере. Бумага для печати должна быть белой без желтизны, масштабирование изображения при печати необходимо отключить, чтобы не искажать размер символов. Скорректируйте высоту расположения таблицы так, чтобы десятая строчка располагалась на уровне глаз.
- Уровень освещения в комнате должен достигать 700 лк: такую яркость может обеспечить одна лампа накаливания мощностью 40 Вт или пара люминесцентных ламп. Свет от источника должен быть направлен прямо на таблицу.
- Проведите проверку, учитывая необходимые для каждого теста условия, согласно информации ниже.
Для самостоятельного вычисления результатов проверки необходимо скачать таблицы с пометками напротив строк. Буквой D слева строки обозначается расстояние в метрах, с которого видит человек, обладающий стопроцентным зрением. V справа — величина, обозначающая остроту зрения.
Недостатки самостоятельной проверки зрения
Плюсы самостоятельной проверки зрения очевидны. Это:
- быстро;
- удобно, если нет возможности обратиться к окулисту или в салоны оптики;
- беззатратно: для прохождения теста не потребуется специальное оборудование.
И всё же те, кто решился проверить зрение без помощи специалистов, рискуют получить недостаточно точный результат.
- Во-первых, неспециалисту легко упустить на первый взгляд незначительные, но фактически важные аспекты вроде яркости освещения.
- Во-вторых, без специального аппарата для проверки зрения (рефрактометра) невозможно определить рефракцию глаза – важнейший показатель при выявлении дефектов зрения.
Поэтому всем, чьё зрение заметно ухудшилось, рекомендуется в обязательном порядке обратиться к врачу-офтальмологу для проведения комплексной профессиональной проверки.
Таблица Сивцева
Самым базовым и распространённым способом проверки зрения остается таблица врача-офтальмолога Д. А. Сивцева (так называемая «ШБ»). Без неё сегодня не обходится ни один кабинет офтальмолога и салон оптики.
Для самостоятельной проверки зрения методом Сивцева распечатайте таблицу и разместите её на уровне глаз. Требуемая дистанция от человека до таблицы — пять метров. Один глаз закройте ладонью или любым непрозрачным предметом (не зажмуривайте!), а другим внимательно читайте каждую строчку. Желательно, чтобы в комнате находился помощник, контролирующий процесс и фиксирующий результаты. Если вы проходите тест в одиночку, удобно записать прохождение теста на диктофон.
Полная таблица Сивцева состоит из рядов со значениями «V» в интервале от 0.1 до 5.0. Острота зрения считается полной, если в рядах с V=0.3–0.6 было допущено не более одной ошибки, а в рядах с V>0.7 — не более двух. На распознавание знака отводится 2-3 секунды. Численное значение остроты вашего зрения равно численному значению V в последней строке, где не было допущено ошибок сверх нормы. Если испытуемый видит более 10 строк — острота зрения выше среднестатистической. Если полученное значение меньше 1.0, желательно проверить рефракцию.
Детская таблица Орловой
Этот тест предназначен для детей дошкольного возраста, ещё не знакомых с алфавитом: он содержит схематические изображения звезд, животных и растений вместо букв. Для начала стоит попросить ребенка перечислить предметы, чтобы удостовериться в его готовности к проверке.
Острота зрения определяется аналогично системе Сивцева. Если ребенок видит десятую строку с расстояния пяти метров одинаково хорошо каждым глазом — зрение считается нормальным. Если символы верхнего ряда с этой дистанции не видны, ребенок должен подойти к таблице еще ближе. Каждые полметра проверяйте, видит ли он знаки — до тех пор, пока не будут названы картинки верхнего ряда.
Решетка Амслера
Изображение решетки с точкой в середине.
При прохождении проверки взгляд фиксируют на центральной точке, боковым зрением наблюдая за линиями таблицы. При нормальном зрении точка остается на месте. В случае искажения сетки есть повод заподозрить макулодистрофию — в такой ситуации не стоит откладывать посещение окулиста.
Звезда Сименса
Звезда Сименса предназначена для проверки зрения на астигматизм — дефект зрения, связанный с нарушением формы хрусталика.
Человеку, страдающему астигматизмом, кажется, будто лучи перекрывают друг друга и сливаются с фоном. Белые лучи при этом видятся черными — и наоборот.
Дуохромный тест
С помощью этого теста возможно определить тип рефракции глаза и без труда выявить дальнозоркость или близорукость.
Проверку проводят при дневном свете с комфортного для глаз расстояния. Основная задача — понять, на каком фоне знаки кажутся чётче. Дальнозоркие люди лучше видят на зеленом, близорукие — на красном фоне. При нормальном зрении символы одинаково хорошо видны вне зависимости от цвета подложки.
Проверка зрения в компании «Мединвест»
Тесты для самостоятельной проверки зрения — простой способ быстро и комфортно продиагностировать остроту зрения прямо у себя дома. Тем не менее, результат самостоятельной проверки в любом случае необходимо закрепить консультацией у специалистов.
Центр «Мединвест» – место, где можно сделать это абсолютно бесплатно. При этом вы будете уверены в точности результатов: прием ведут квалифицированные офтальмологи, а для диагностики используется самое современное оборудование.
Берегите своё зрение — приходите в «Мединвест»!
Периодическая таблица
Вещество, которое не может быть расщеплено на более простые химические вещества, также известно как
.- ? элемент
- ? молекула
- ? ядро
- ? смесь
- ? Дмитрий Менделеев
- ? Владимир Путин
- ? Анна Курникова
- ? Леонид Толстой
Что означает группа в Периодической таблице?
- ? Вертикальный ряд элементов
- ? Горизонтальный ряд элементов
- ? Семейство металлов в Периодической таблице
- ? Семейство неметаллов в Периодической таблице
- ? Восемь
- ? Два
- ? Четыре
- ? 18
- ? C
- ? Cl
- ? Na
- ? Ca
- ? неметаллы
- ? металлы
- ? галогены
- ? жидкие элементы
- ? Гелий, неон и аргон
- ? Литий, кальций и сера
- ? Литий, бор и фтор
- ? Водород, фтор и хлор
- ? Периоды
- ? Группы
- ? Щелочные металлы
- ? Металлы
- ? Натрий
- ? Углерод
- ? Фосфор
- ? Неон
- ? S
- ? Na
- ? Al
- ? Быть
- ? Меркурий
- ? Алюминий
- ? Натрий
- ? Кальций
- ? Натрий
- ? Магний
- ? Медь
- ? Меркурий
Какая из следующих пар свойств являются свойствами щелочных металлов?
- ? Они хорошие проводники тепла и электричества.
- ? Они не вступают в реакцию с водой и имеют низкую плотность.
- ? Они плавают в воде и не вступают в реакцию с воздухом.
- ? Они твердые металлы и не вступают в реакцию с водой.
Какая группа элементов обладает следующими свойствами?
Хорошие проводники электричества, блестящие, обладают высокой реакционной способностью по отношению к воде и хранятся в масле.
- ? Щелочные металлы
- ? Галогены
- ? благородные газы
- ? Щелочноземельные металлы
Элементы группы I обычно не встречаются в природе свободными, потому что
- ? они очень реактивны.
- ? они редкоземельные металлы.
- ? все они созданы людьми.
- ? они очень инертны.
Элементы группы I имеют схожие химические свойства, потому что
- ? все они имеют один электрон на внешней оболочке.
- ? все они металлы.
- ? все они похожи.
- ? все они реагируют с водой.
Какая из следующих реакций происходит при добавлении калия в воду?
- ? Калий загорается и выделяет газообразный водород.
- ? Ничего не происходит, потому что калий не реагирует с водой.
- ? Калий с громким хлопком опускается на дно емкости.
- ? Калий медленно вступает в реакцию с водой с образованием газообразного кислорода.
Какой элемент из приведенного ниже списка имеет свойства, аналогичные калию?
- ? Натрий
- ? Кальций
- ? Гелий
- ? Водород
- ? Рубидий
- ? Натрий
- ? Калий
- ? Литий
Пламя какого цвета образуется при сжигании калия или калиевой соли в пламени Бунзена?
- ? Сирень
- ? Желтый
- ? Зеленый
- ? красный
Что такое элемент?
- ? Вещество, которое не может быть расщеплено химическим путем на более простые вещества.
- ? Самая маленькая частица, которая может существовать независимо.
- ? Отрицательно заряженная частица, вращающаяся вокруг ядра.
- ? Вещество, состоящее из двух или более атомов, химически соединенных.
На химические свойства элемента в основном влияет
- ? количество электронов, окружающих ядро.
- ? количество нейтронов в ядре.
- ? размер ядра.
- ? количество протонов в его ядре.
Элементы в Периодической таблице расположены в порядке возрастания
- ? атомный номер.
- ? массовое число.
- ? объем.
- ? плотность.
- ? Атомный номер элемента
- ? Массовое число элемента
- ? Номер своей группы
- ? Его период
Назовите элементы, имеющие символы: Na и Fe
- ? Натрий и железо
- ? Азот и железо
- ? Натрий и фтор
- ? Неон и фосфор
- ? K
- ? Ли
- ? Ne
- ? п
Как обычно называются элементы в группе I?
- ? Щелочные металлы
- ? Галогены
- ? Щелочноземельные металлы
- ? Неметаллы
К какой группе в Периодической таблице принадлежит нереактивный элемент аргон?
- ? Группа 0
- ? Группа II (2)
- ? Группа VII (7)
- ? Группа I
Какие из следующих элементов являются щелочноземельными металлами?
- ? Магний и бериллий
- ? Натрий и калий
- ? Натрий и кальций
- ? Медь и золото
Что из перечисленного обычно является свойством неметаллов?
- ? Они плохие проводники электричества.
- ? У них блестящий блеск.
- ? Они хорошие проводники тепла.
- ? Они менее плотные, чем вода.
Из следующего списка выберите неметаллы:
медь, хлор, цинк, натрий, углерод.
- ? Хлор и углерод
- ? Медь, цинк и натрий
- ? Хлор
- ? Хлор, натрий и углерод
- ? Ювелирные изделия
- ? Убийство бактерий
- ? Бидоны для безалкогольных напитков
- ? Сварочные горелки
- ? кремний
- ? хлор
- ? серебро
- ? неон
Элементы группы VII (7) известны как
.- ? галогены
- ? щелочные металлы
- ? переходные металлы
- ? благородные газы
- ? Они уменьшаются в порядке реактивности.
- ? Их реактивность по группе не меняется.
- ? По мере снижения группы они становятся более растворимыми в воде.
- ? Они увеличиваются в порядке реактивности.
Почему элементы фтор, хлор и йод помещены в одну группу Периодической таблицы?
- ? У них одинаковое количество электронов на внешней оболочке.
- ? Все они металлы.
- ? Все они легко реагируют с кислородом.
- ? У них одинаковая плотность.
- ? Хлор
- ? Фтор
- ? Бром
- ? Йод
Назовите элемент, который образует желтоватый газ и содержится в зубной пасте для предотвращения разрушения зубов.
- ? Фтор
- ? Хлор
- ? Бром
- ? Йод
Почему элементы в группе 0 неактивны?
- ? У них есть полная внешняя оболочка из электронов.
- ? У каждого из них есть стабильное ядро.
- ? У них на внешней оболочке четное число электронов.
- ? Все они газы.
- ? Неон
- ? Гелий
- ? Аргон
- ? Кислород
Что из следующего является элементом?
- ? Алюминий
- ? Стали
- ? Латунь
- ? Вода
- ? их возрастающие атомные номера.
- ? их плотности.
- ? их количество нейтронов увеличивается.
- ? их возрастающая массовая численность.
- ? Щелочноземельные металлы
- ? Щелочные металлы
- ? Металлы
- ? Галогены
- ? Атомный номер элемента.
- ? Количество нейтронов в ядре атома.
- ? Массовое число элемента.
- ? Его плотность.
Сопоставьте элементы хлор и гелий с их правильными символами
- ? Cl и He соответственно.
- ? C и He соответственно.
- ? Cl и H соответственно.
- ? Ca и Hg соответственно.
Какие газы из следующего списка существуют как отдельные атомы:
водород, гелий, азот, кислород, неон.
- ? Гелий и неон
- ? Гелий и азот
- ? Водород и гелий
- ? Кислород и азот
(i) Они плавают на воде.
(ii) Они легко реагируют с кислородом.
(iii) Они горят в пламени Бунзена характерного цвета.
- ? Щелочные металлы
- ? Щелочноземельные металлы
- ? Галогены
- ? Благородные газы
Калий – это металл, который плавает в воде.Какова основная причина отказа от его использования при производстве кораблей?
- ? Он очень реактивен с водой.
- ? Это мягкий металл.
- ? Это очень дорого.
- ? Это очень редкий металл.
Что общего у элементов группы II (2)?
- ? Подобные химические свойства
- ? Тот же атомный номер
- ? Ничего общего
- ? То же массовое число
Какой из элементов, перечисленных ниже, наиболее вероятно будет обладать следующими свойствами:
Серебристого цвета, хороший проводник электричества и металл низкой плотности
- ? Магний
- ? Углерод
- ? Фтор
- ? Кислород
Какой элемент в группе III (3) является неметаллом?
- ? Бор
- ? Алюминий
- ? Галлий
- ? Скандий
Какой из следующих элементов используется в электропроводке?
- ? Медь
- ? Хлор
- ? Неон
- ? Натрий
Можете ли вы выбрать из приведенного ниже списка неметалл, который существует в виде жидкости при комнатной температуре?
- ? Бром
- ? Азот
- ? Меркурий
- ? Аргон
Какое из следующих утверждений относительно элементов VII (7) группы является правильным?
(i) Они известны как галогены.
(ii) Все они имеют одинаковую температуру плавления.
(iii) Они обладают схожими химическими свойствами.
- ? Заявления (i) и (iii)
- ? Заявления (i) и (ii)
- ? Утверждения (ii) и (iii)
- ? Только заявление (i)
- ? Фтор и хлор
- ? Хлор и бром
- ? Кислород и магний
- ? Кальций и фтор
Только один из следующих наборов элементов принадлежит галогенам.Который из них?
- ? Хлор, бром и фтор
- ? Бериллий, углерод и кислород
- ? Фтор, углерод и бром
- ? Неон, гелий и аргон
Какой из следующих галогенов находится в твердом состоянии при комнатной температуре?
- ? Йод
- ? Хлор
- ? Бром
- ? Фтор
Какая из следующих групп элементов обычно не реагирует?
- ? Благородные газы
- ? Галогены
- ? Щелочные металлы
- ? Переходные металлы
Какое из следующих утверждений верно / относительно благородных газов в группе O?
(i) Они очень реактивные элементы.
(ii) У них есть полные внешние оболочки из электронов.
(iii) Они обладают схожими химическими свойствами.
- ? Утверждения (ii) и (iii)
- ? Заявления (i) и (ii)
- ? Только заявление (i)
- ? Только утверждение (ii)
- ? Поскольку аргон инертен, он не вступает в реакцию с нитью накала.
- ? Аргон заставит лампу светиться ярче.
- ? Производство аргона обходится дешевле, чем производство воздуха.
- ? Аргон более доступен, чем воздух.
Атомный номер элемента – это число __________ в ядре каждого атома этого элемента.
- ? протоны
- ? нейтроны
- ? электроны
- ? протоны и нейтроны
Вещество, состоящее только из одного типа атомов, называется
.- ? элемент
- ? молекула
- ? неметалл
- ? соединение
Сколько здесь природных элементов?
- ? 92
- ? 20
- ? 36
- ? 8
Химический символ – это сокращенный метод записи названия элемента.
Какой химический символ у углерода?
- ? C
- ? Ca
- ? Cu
- ? Cl
Поместите в правильном порядке:
Химические символы для натрия, азота и никеля:
- ? Na, N и Ni
- ? S, Ni и N
- ? Na, N и Nk
- ? S, N и Ni
Каждому элементу периодической таблицы присвоен номер, называемый атомным номером .
Это равно
- ? количество протонов в каждом атоме этого элемента.
- ? количество нейтронов в каждом атоме этого элемента.
- ? количество протонов и нейтронов в каждом атоме этого элемента.
- ? количество протонов плюс количество электронов-электронов в каждом атоме этого элемента.
Ваш учитель мог продемонстрировать реакции, которые происходят между щелочными элементами и водой.Какой из этих элементов наиболее реактивен?
- ? Калий
- ? Литий
- ? Натрий
- ? Гелий
Атом углерода с массовым числом 14 часто называют углерод-14 или C-14 .
Если его атомный номер 6, сколько в нем протонов и нейтронов?
- ? 6 протонов и 8 нейтронов
- ? 8 протонов и 6 нейтронов
- ? 6 протонов и 6 нейтронов
- ? 6 протонов и 14 нейтронов
Что из перечисленного не является общим свойством металлов?
- ? Плохой проводник электричества
- ? Блестящий на вид
- ? Обычно твердое вещество при комнатной температуре
- ? Хороший проводник тепла
Сколько основных групп в Периодической таблице?
- ? 8
- ? 2
- ? 4
- ? 18
| Абилин, Техас
Добро пожаловать в виртуальный класс публичной библиотеки Абилина.Это пространство станет новым местом для молодежи, подростков и взрослых, где они смогут больше узнать о самых разных темах, с регулярным добавлением нового контента.
Для каждого класса мы поделимся справочной информацией, образовательными видео, планами уроков, ресурсами, доступными для продолжения обучения, и многим другим. Кроме того, мы предложим ссылку на тест, который мы будем признательны, если вы его пройдете, чтобы показать, что вы узнали!
| Периодическая таблица элементов |
|---|
| Как элементы получили свои названия 7 | 99 |
|
|---|
| Периодическая таблица Менделеева – интенсивный курс по химии | | | 9 | элементы для идеи периодической таблицы. |
|---|
| Королевское химическое общество – История Периодической таблицы элементов | |
|---|---|
| Королевское общество химии 9062 Интерактивная таблица Менделеева содержит историю, алхимию, подкасты, видео и тенденции данных по периодической таблице.Скопируйте и вставьте следующий URL-адрес в свой браузер, https://www.rsc.org/periodic-table/history, затем щелкните вкладки вверху и изучите каждый раздел. Используйте кнопки, чтобы изменить свой взгляд на таблицу Менделеева. Мюррей Робертсон отвечает за оформление визуальных элементов. Щелкните каждый элемент, чтобы прочитать подробную информацию об истории элемента, включая ученых, которые открыли элемент и когда. |
| Карьера в химии | |
|---|---|
| исследования, которые можно найти в этой области. .Ведущий рассказывает о том, что вам нужно делать в колледже, чтобы приобрести навыки, необходимые в этой области. Он описывает необходимые навыки, работу и карьеру, начальную работу в качестве лаборанта, химика начального уровня, стажировки и аспирантуру. Он также исследует карьеру в химии, которую можно сделать после того, как студент получит ученую степень, различные отрасли, в которых работают химики, построение здорового резюме и создание социальной сети. Докладчик дает советы по поиску работы, исследованиям в бакалавриате и развитию навыков межличностного общения. |
Эта интерактивная периодическая таблица творчески иллюстрирует элементы
Вы боретесь с химией? Эта интерактивная таблица Менделеева дает вам подробную информацию об элементах. Но это не обычные скучные детали вроде атомного веса. Это позволяет вам точно знать, где находится элемент и его использование.
Бесчисленное количество студентов каждый год барахтаются на курсах химии, ломая голову над тем, как запомнить таблицу Менделеева. Эта интерактивная таблица должна сделать этот процесс намного проще и увлекательнее, чем механическое запоминание.
Все мы кое-что знаем об общих элементах, таких как кислород, железо, титан, кальций и калий. Но как насчет менее известных, но не менее важных элементов? Например, кто помнит атомный номер и области применения рубидия? А как насчет иттрия? Осмий или тантал? Если вы не занимаетесь химией, понять элементы может быть сложно.
[Источник изображения: Elements Wlonk]
Кейт Эневольдсен из elements.wlonk разработал эту замечательную таблицу Менделеева. Кроме того, вы можете проверить себя и устроить тренажерный зал для мозга, где бы вы ни находились, распечатав диаграмму, которую вы можете;
Креативный дизайн
Основные поля каждого элемента включают имя, атомные символы, атомный вес и виджеты, которые подробно описывают естественные явления.
Цветовое кодирование также помогает пользователям классифицировать элементы. Маленькие символы содержат дополнительную информацию: твердое вещество / жидкость / газ, цвет элемента и редкость.
Однако слишком много информации не озадачивает детей. Дополнительные информационные панели описывают химическую связь, структуру и радиоактивность.
[Источник изображения: Elements Wlonk]
“Эта диаграмма показывает, из чего состоит Вселенная. На ней показаны все элементарные частицы в стандартной модели (СМ) физики элементарных частиц, а также многие неэлементарные частицы.Все начинается с основ: атом содержит ядра протонов и нейтронов, которые состоят из кварков. В таблице упорядочены все первичные частицы и их классы:
Элементарные фермионы: нейтрино, кварки, электроны и лептоны.
Бозоны: фотоны, глюоны, W- и Z-бозоны, предсказанные гравитоны и Хиггса.
Составные частицы: адроны. , протоны, барионы, мезоны, нейтроны и античастицы.
[Источник изображения: Elements Wlonk]
Атомные орбитали
“Эта цветная диаграмма показывает, как выглядят атомы.На этой диаграмме показаны все основные атомные и электронные орбитали в виде распределений плотности вероятности электронов (нечеткие облака), что очень близко к визуализации того, как на самом деле выглядит атом. Обозначены орбитали. Он описывает другие способы визуализации атомов, а именно орбиты электронов (например, планет) и поверхности с постоянной вероятностью (выпуклые капли). В нем есть небольшая периодическая таблица, показывающая, в каком порядке заполняются электронные оболочки ».
[Источник изображения: Elements Wlonk]
Эневольдсен обновляет таблицу всякий раз, когда новый элемент утверждается IUPAC.Недавно он обновил в конце 2016 года новые названия элементов: 113 Nihonium (Nh), 117 Tennessine (Ts), 115 Moscovium (Mc) и 118 Oganesson (Og).
СМОТРИ ТАКЖЕ: официально добавлены четыре новых элемента
Удачи, исследуя элементы!
Через: Elements Wlonk
Написано Тамар Мелике Тегюн
Редактируемая периодическая таблица – заполнение онлайн, для печати, заполняется, пусто
Комментарии и помощь с заполнением пропусков в таблице Менделеева
Видеоинструкция и помощь по заполнению и заполнению редактируемой таблицы Менделеева
Инструкции и справка о таблице Менделеева для заполнения формы
Да, теперь мы начинаем некоторую химию, последний блок не обязательно был ориентирован на химию, и мы уже сделали большую часть главы об атомной структуре, ясная глава 4 говорит об атоме, а атом имеет ядро, протоны и нейтроны, так что вы продолжаете Чтобы знать такие термины, как этот, вы должны знать массовое число атомный номер, вы можете не записывать все это, я не собираюсь повторять, мне нужно было слишком много, чтобы пройти через изотопы нуклоны, протоны, нейтроны, электроны, масса каждого заряда каждой массы представляет собой массу в атомных единицах массы, которую вы должны будете знать ученых, которые сложили все это вместе, таких как Дж. Дж. Томпсон, Далтон Демокрит, и, более того, есть много новых и старых видеороликов о четвертой и пятой главах. как бы делаю это вместе, как единое целое, хотя я тестирую их по отдельности, я тестировал их как одно устройство, но теперь я тестировал отдельно то, что я хочу начать сегодня, фактически начинается в главе 4, и я хочу поговорить о периодической таблице, которую мы Невозможно игнорировать таблицу Менделеева, это гигантский слон в комнате, другими словами, вы не обязательно можете игнорировать такой ценный инструмент из четвертой главы и изучать химию, которую великие ученые разработали, что очень сложно для понимания. Прежде всего, вы знаете, что такое апериодическая таблица, и вы использовали ее. Прежде чем сколько людей узнают, что такое апериодическая таблица, поднимите руку, сколько людей не знают, сколько людей не совсем здесь, вы знаете в чем ты не веришь? Ты никогда раньше не пользовался апериодической таблицей, у тебя когда-либо был курс естествознания, но он был пропущен из-за этого.Nayar это было с MR. Вы не знаете, что такое периодическая таблица, я даже не хочу туда идти, ладно, так что мы собираемся поговорить о периодической таблице, да, мы собираемся пройти историческое развитие периодической таблицы с Менделеевым и другие ученые, которые помогают составить это, но я хочу нарисовать периодическую таблицу на доске, хорошо, и я хочу, чтобы вы сделали это со мной, вам не нужна линейка, просто сделайте это от руки, и я собираюсь показать вам, как это сделать быстро, ладно, ладно, сейчас периодическая таблица имеет 18 столбцов, ладно, давайте сделаем, давайте, я на вашей бумаге сделаю 18 столбцов примерно равными по всей странице, ладно, поэтому я хочу сделать гигантскую таблицу восемнадцать детенышей хорошо, это будет наша периодическая таблица, хорошо, и что мы собираемся сделать, так это узнать основную структуру периодической таблетки, вот периодическая она прямо на стене, а я на самом деле заказал те, которые являются худшей периодической таблицей, которую я видел, трудно увидеть фактический символ каждого элемента Это не так, а у вас, ребята, прекрасные глаза, я не знаю, о чем они думали, когда разрабатывали эту периодическую таблицу, но в любом случае, эй, если это может быть как девять, прямо сейчас, и тогда вы собираетесь сказать, что 39; с.
