Триумф русской химической науки – Проект «Юбилейный урок»
Содержание
- Предпосылки открытия Периодического закона Д. И. Менделеева
- Рукопись «Опыт системы элементов, основанной на их атомном весе и химическом сходстве»
- Сон Менделеева
- История открытия благородных газов
- Нобелевская премия
- Периодическая система химических элементов
- Альтернативные периодические таблицы
- Интерактивная карта
- Рабочий лист № 1
- Рабочий лист № 2
- Интерактивные задания
- Ссылки
- Авторы-разработчики урока
Периодический закон и Периодическая система химических элементов Д. И. Менделеева — основа современной химии. Они относятся к таким научным закономерностям, которые отражают явления, реально существующие в природе, и поэтому никогда не потеряют своего значения. Их открытие было подготовлено ходом истории развития химии, однако потребовалась гениальность Д.
 И. Менделеева, его дар научного предвидения, чтобы эти закономерности были сформулированы и графически представлены в виде таблицы.
И. Менделеева, его дар научного предвидения, чтобы эти закономерности были сформулированы и графически представлены в виде таблицы.Предпосылки открытия Периодического закона Д. И. Менделеева
«Закон триад»Спираль Шанкуртуа
Таблица Мейера
«Закон октав»
История науки не знает другого подобного триумфа. Открыт новый закон природы. Вместо разрозненных, не связанных между собой веществ встала единая стойкая система, объединившая в одно целое все элементы Вселенной.
Ученый, творец, один из последних энциклопедистов в науке
«Будут появляться и умирать новые теории, блестящие обобщения. Новые представления будут сменять наши уже устаревшие понятия об атоме и электроне. Величайшие открытия и эксперименты будут сводить на нет прошлое и открывать на сегодня невероятные по новизне и широте горизонты, – все это будет приходить и уходить, но Периодический закон Д. И. Менделеева будет всегда жить и руководить исканиями».
И. Менделеева будет всегда жить и руководить исканиями».
А. Е. Ферсман
Д. И. Менделеев. Рукопись «Опыт системы элементов, основанной на их атомном весе и химическом сходстве»
Этот небольшой листок обычной писчей бумаги относится к числу наиболее ценных документов в истории человечества. Ныне он хранится в Музее-архиве Д. И. Менделеева при Санкт-Петербургском университете. Учёный отпечатал в типографии оттиски «Опыта системы…» с заглавиями на русском и французском языках и разослал их своим отечественным и зарубежным коллегам.
Сон Менделеева
Многие слышали историю, что Д. И. Менделееву его таблица приснилась. Эта версия активно распространялась соратником Менделеева А. А. Иностранцевым в качестве забавной истории, которой он развлекал своих студентов. Он говорил, что Дмитрий Иванович лёг спать и во сне отчётливо увидел свою таблицу, в которой все химические элементы были расставлены в нужном порядке. Но реальные предпосылки для истории со сном всё же были: как уже упоминалось, Д. И. Менделеев работал над таблицей без сна и отдыха, и А. А. Иностранцев однажды застал его уставшим и вымотанным. Днём Менделеев решил немного передохнуть, а некоторое время спустя резко проснулся, сразу же взял листок бумаги и изобразил на нём уже готовую таблицу. Но сам учёный опровергал всю эту историю со сном, говоря: «Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово». Так что легенда о сне, может быть, и очень привлекательна, но создание таблицы стало возможным только благодаря упорному труду.
И. Менделеев работал над таблицей без сна и отдыха, и А. А. Иностранцев однажды застал его уставшим и вымотанным. Днём Менделеев решил немного передохнуть, а некоторое время спустя резко проснулся, сразу же взял листок бумаги и изобразил на нём уже готовую таблицу. Но сам учёный опровергал всю эту историю со сном, говоря: «Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово». Так что легенда о сне, может быть, и очень привлекательна, но создание таблицы стало возможным только благодаря упорному труду.
С открытием Периодического закона в химии стало возможным научное предвидение.
Ларс Фредерик Нильсоноткрыл экабор (1875 г.)
Поль Эмиль Лекок де Буабодран
открыл экаалюминий (1879 г.)
Клеменс Александр Винклер
открыл экасилиций (1886 г.)
В 1900 году Д. И. Менделеев и шотландский химик Уильям Рамзай пришли к мнению, что в таблицу должны быть включены и элементы нулевой группы — до 1962 года они назывались инертными (после — благородными газами).
С 1890 года Рамзай начал серьезное изучение газов атмосферы. В 1894 году Уильям Рамзай встретился с Рэлеем для обсуждения проблем, связанных с различиями в массе азота, полученного из атмосферы разными способами. Ученые начали совместные исследования и в апреле 1894 года установили наличие в атмосфере нового газа — аргона. Первое публичное заявление о своём открытии Рамзай и Рэлей сделали 13 августа 1894 года в Оксфорде на заседании Британской ассоциации, однако научное сообщество критически отнеслось к их докладу. В течение полугода ученые дорабатывали и проверяли свои исследования и окончательно объявили об открытии аргона 31 января 1895 года в Лондонском университете на собрании Королевского общества, а 28 марта 1895 года вышла научная публикация «Аргон — новая составная часть атмосферы». Рамзай предсказал существование других инертных газов и вёл активную работу по их поиску и выделению. После блестящих экспериментов 16 марта 1900 г. в Лондоне произошла встреча Менделеева и Рамзая, на которой было официально решено включить в Периодическую систему новую группу химических элементов.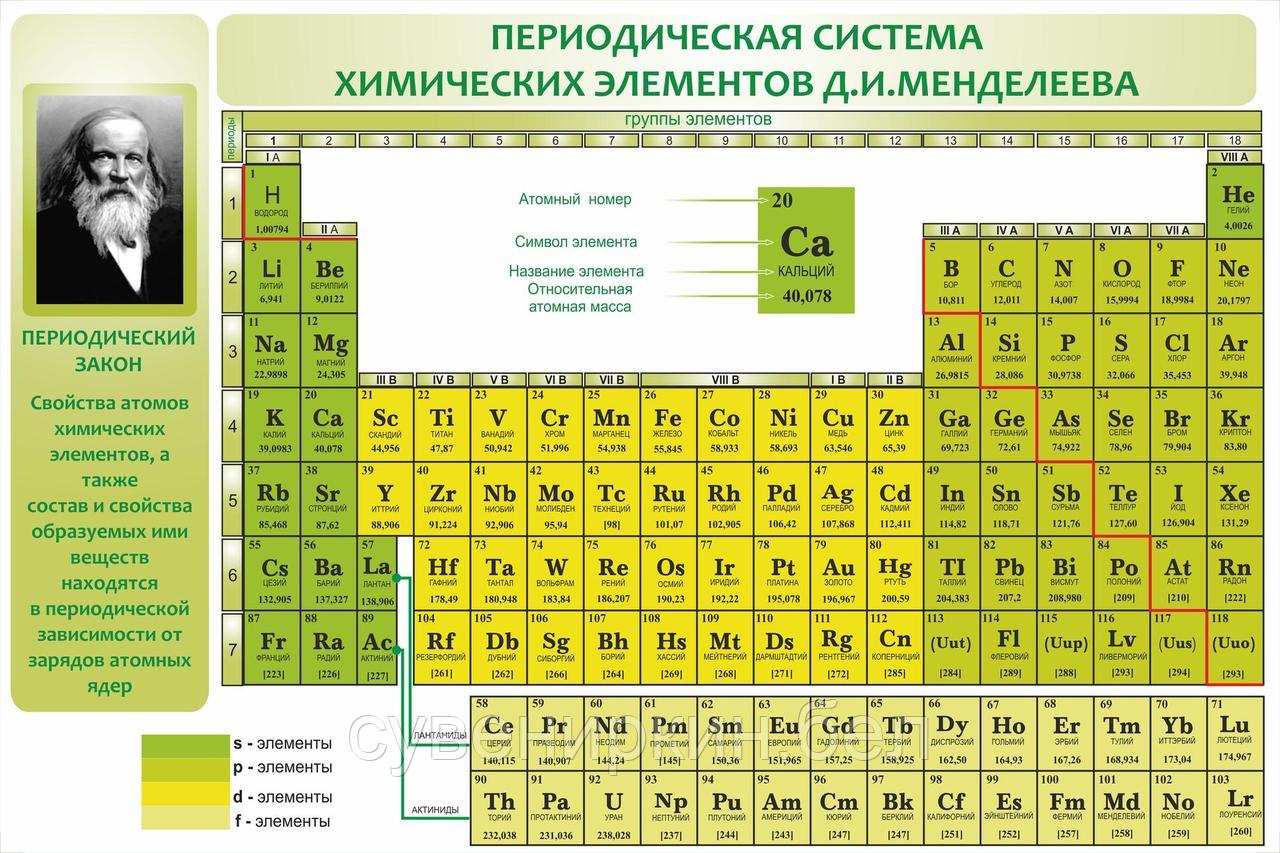
История открытия благородных газов
Нобелевская премия
Существовала вполне объективная составляющая, ограничивавшая возможность выдвижения Д. И. Менделеева на Нобелевскую премию. Дело в том, что одним из главнейших требований в течение первых четырёх десятилетий функционирования нобелевских учреждений была непременная новизна открытия. Это требование, повторенное в уставе, предусмотрел сам Альфред Нобель в своём завещании. И оттого научный прорыв Д. И. Менделеева в создании Периодической системы элементов, датируемый 1869 годом, когда он опубликовал свой «Опыт системы элементов, основанный на их атомном весе и химическом сродстве», никак не укладывался в прокрустово ложе строго выполнявшегося устава. Д. И. Менделеева выдвигали на Нобелевскую премию (которая, напомним, присуждается с 1901 г.) — в 1905, 1906 и 1907 годах. Читать далее
Список лауреатов Нобелевской премии с 1901 по 1907 год:
- 1901 год — Якоб Хендрик Вант-Гофф «В знак признания огромной важности открытия законов химической динамики и осмотического давления в растворах».
- 1902 год — Герман Эмиль Фишер «За эксперименты по синтезу веществ с сахаридными и пуриновыми группами».
- 1903 год — Сванте Август Аррениус «Присуждена премия как факт признания особого значения его теории электролитической диссоциации для развития химии».
- 1904 год — Уильям Рамзай «В знак признания открытия им в атмосфере различных инертных газов и определения их места в периодической системе».
- 1905 год — Адольф фон Байер «За заслуги в развитии органической химии и химической промышленности благодаря работам по органическим красителям и гидроароматическим соединениям».
- 1906 год — Анри Муассан «За получение элемента фтора и введение в лабораторную и промышленную практику электрической печи, названной его именем».
«Считают, что недоброжелателем Менделеева в Шведской королевской академии, повлиявшим на смену правил игры в ходе самой игры, был лауреат Нобелевской премии по химии 1903 года Сванте Аррениус. Менделеев критиковал некоторые положения его теории электролитической диссоциации, и Аррениус воспринял критику очень болезненно.
Периодическая система химических элементов
Наиболее распространёнными являются три формы таблицы Д. И. Менделеева: «короткая» (короткопериодная), «длинная» (длиннопериодная) и «сверхдлинная». В каждой из форм имеются свои преимущества и недостатки. Однако связь природы элемента со структурой электронной оболочки атомов наиболее полно и однозначно раскрывается длинной формой системы.
Альтернативные периодические таблицы
Альтернативные периодические таблицы часто разрабатываются для того, чтобы выделить или подчеркнуть различные химические или физические свойства элементов, которые не очевидны из традиционных периодических таблиц.
Известно свыше 400 вариантов таблиц Периодической системы, различающихся размещением отдельных групп элементов-аналогов, способом отображения Периодического закона. В некоторых из них группа инертных газов размещена в правой части (этими элементами заканчиваются периоды в системе), в других — в левой части (ими начинаются периоды), в третьих — в середине таблицы.
Есть таблицы, где элементы располагаются не в порядке заполнения электронных уровней в атомах, а в порядке последовательного расположения в левой части таблицы групп s- и р-элементов, в правой части — всех групп d-элементов, а затем f-элементов.
Известны варианты, в которых элементы первого периода расположены внизу таблицы, а над ними — элементы последующих периодов, что символизирует постепенное усложнение электронной оболочки атомов. Авторы ряда таблиц делят группы элементов на 3 или 4 подгруппы, внося в эти «дополнительные» подгруппы f-элементы.
Однако большинство этих таблиц, оттеняя периодичность изменения тех или иных свойств элементов и их соединений, ничего принципиально нового не вносят в конструкцию Периодической системы.
Интерактивная карта
Рабочий лист № 1
Рабочий лист № 2
Интерактивные задания
Установите соответствие между автором и предложенной им классификацией химических элементов.
Александр Эмиль Бегуйе де Шанкуртуа
Иоганн Вольфганг Дёберейнер
Джон Ньюлендс
Юлиус Лотар Мейер
Д. И. Менделеев
Таблица из 28 элементов, размещённых согласно их валентностям
«Опыт системы элементов, основанной на их атомном весе и химическом сходстве»
Химические элементы в единой последовательности возрастания их атомных масс в виде спирали
«Закон октав»
«Закон триад»
Многие элементы, известные учёным, скорее всего, отсутствуют в природе — их возможно получить только с помощью синтеза. Знаете, какой элемент стал первым искусственным химическим элементом?
Атомы с зарядами ядра +113, +115, +117 и +118 тоже были получены искусственно, с помощью бомбардировки тяжелых ядер ядрами других атомов.

Установите соответствие между химическим элементом и происхождением его названия.
113-й элемент – Нихоний (Nihonium), символ Nh
115-й элемент – Московий (Moscovium), символ Mc
117-й элемент – Теннессин (Tennessine), символ Ts
118-й элемент – Оганесон (Oganesson), символ Og
Получил свое название в честь американского штата
Получил свое название в честь Юрия Цолаковича Оганесяна, научного руководителя лаборатории ядерных реакций Объединённого института ядерных исследований
Первый из элементов, название которого связано с Японией
Получил свое название в честь Московской области
Расположите работы ученых по классификации химических элементов в хронологическом порядке.
1829
1862
1864
1866
1869
Ссылки
- Голубева Р. М., Раткевич Е. Ю., Мансуров Г. Н. Длиннопериодный вариант таблицы Периодической системы химических элементов Д. И. Менделеева
- Динамическая таблица Д.
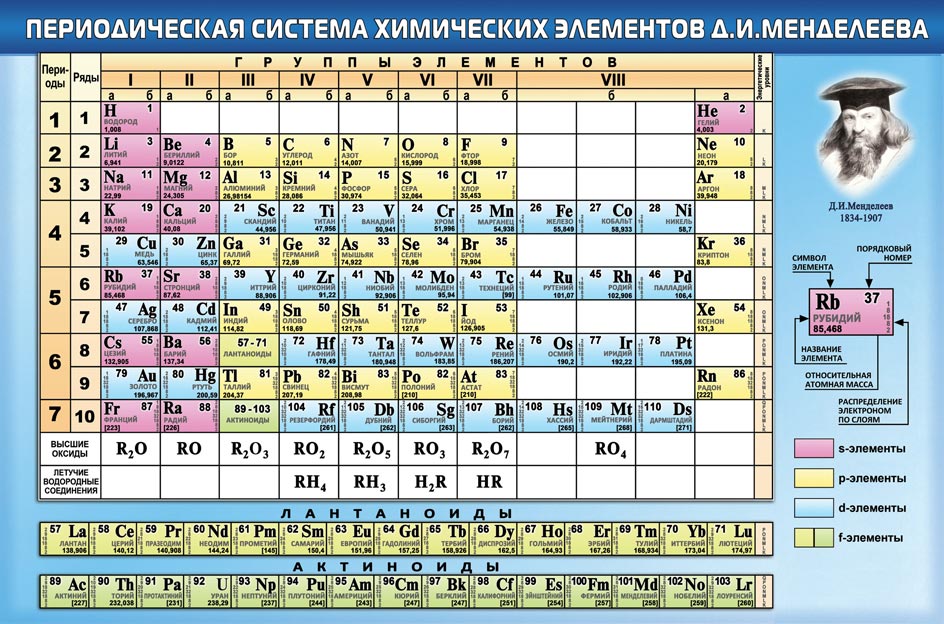 И. Менделеева
И. Менделеева - Интерактивная онлайн-игра «Таблица Менделеева»
- «Нобелиана» Дмитрия Менделеева
Авторы-разработчики урока
Д. В. Болотов, С. В. Наседкина, Н. Е. Савельева.
Техническая поддержка и реализация проекта в сети: сотрудники пресс-центра ГМЦ, г. Москва, 2019 г.
В 1933 году Джон Друри Кларк опубликовал спиральную диаграмму химических элементов. Этот дизайн был использован в 1949 году журналом Life. На обложке этого журнала была представлена красочная система элементов, в которой цвет использовался с целью демонстрации отношений между элементами. Например, фиолетовое окрашивание ячеек и штриховой стрелки использовано для объединения элементов VII-B группы (марганец, технеций, рений) с элементами VII-А группы (фтор, хлор, бром, иод, астат).
В периодической системе Теодора Бенфея (1960) элементы образуют двухмерную спираль, которая, раскручиваясь, опоясывает «острова» с переходными металлами, лантаноидами и актиноидами.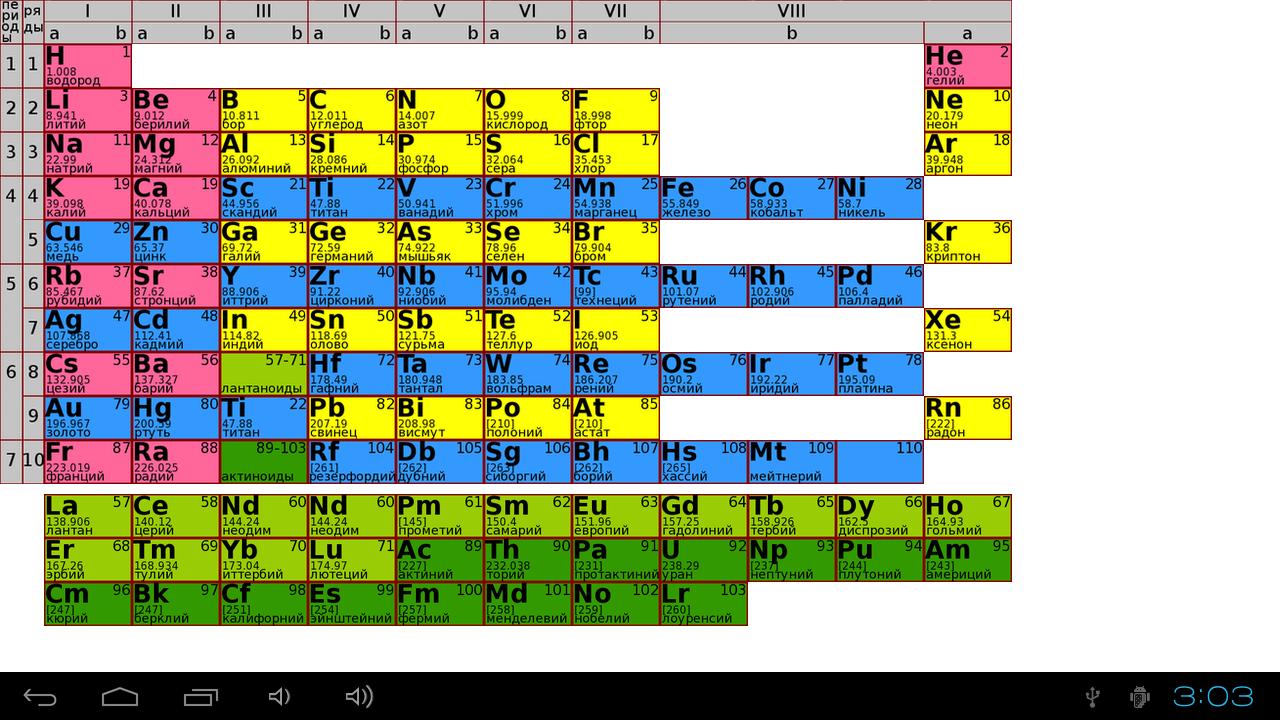 В данной модели появляются ещё не открытые, но предсказанные g-элементы (с атомными числами от 121 до 138).
В данной модели появляются ещё не открытые, но предсказанные g-элементы (с атомными числами от 121 до 138).
Спиральное представление таблицы Менделеева, предложенное профессором химии и дизайнером Филиппом Стюартом, имеет ряд преимуществ перед традиционным. Подложка в виде галактики напоминает о космическом происхождении необходимых для жизни элементов.
Левосторонняя система Жанета (1928) считается наиболее значительной альтернативой традиционному описанию Периодической системы. В ней элементы расположены согласно заполнению атомных орбиталей, и она часто используется физиками. Её современная версия, известная как ADOMAH Periodic Table (2006), удобна для написания электронной конфигурации атомов.
Иоганну Вольфгангу Дёберейнеру удалось установить первые закономерности в изменении свойств элементов. Он заметил, что если расположить три сходных по химическим свойствам элемента в порядке возрастания их атомных весов, то атомный вес второго (среднего) элемента будет равен среднему арифметическому атомных весов первого и третьего.
В 1817 году И. Дёберейнер установил такую закономерность для первой «триады» — щёлочноземельных металлов: кальция, стронция и бария.
В 1829 году, после того как Й. Я. Берцелиус подтвердил его данные, Дёберейнер распространил этот принцип на другие элементы, предложив ещё две триады (литий, натрий, калий и сера, селен, теллур).
В 1840 году Л. Гмелин, расширив список элементов, показал, что характер их классификации по свойствам гораздо сложнее, чем разделение на триады.
Тем не менее закон триад Дёберейнера подготовил почву для систематизации элементов, завершившейся созданием Периодического закона.
Английский учёный Джон Александр Рейна Ньюлендс в 1866 году заметил, что сходство в свойствах проявляется между каждым восьмым элементом.
 Ньюлендс назвал законом октав по аналогии с семью интервалами музыкальной гаммы. В своей таблице он располагал химические элементы в вертикальные группы по семь элементов в каждой и при этом обнаружил, что сходные по химическим свойствам элементы оказываются на одной горизонтальной линии.
Ньюлендс назвал законом октав по аналогии с семью интервалами музыкальной гаммы. В своей таблице он располагал химические элементы в вертикальные группы по семь элементов в каждой и при этом обнаружил, что сходные по химическим свойствам элементы оказываются на одной горизонтальной линии.Однако в одном и том же ряду часто оказывались и элементы совершенно непохожие.
В некоторых ячейках Д. Ньюлендс вынужден был разместить по два элемента.
Юлиус Лотар Мейер внёс значительный вклад в систематизацию химических элементов. В 1864 году он опубликовал таблицу, содержавшую 28 элементов, размещённых в шесть столбцов согласно их валентностям. Ю. Мейер намеренно ограничил число элементов в таблице, чтобы подчеркнуть закономерное (аналогичное триадам Дёберейнера) изменение атомной массы в рядах сходных элементов. В 1870 году он опубликовал ещё одну работу, содержавшую новую таблицу и график зависимости атомного объёма элемента от атомного веса, имеющий характерный пилообразный вид.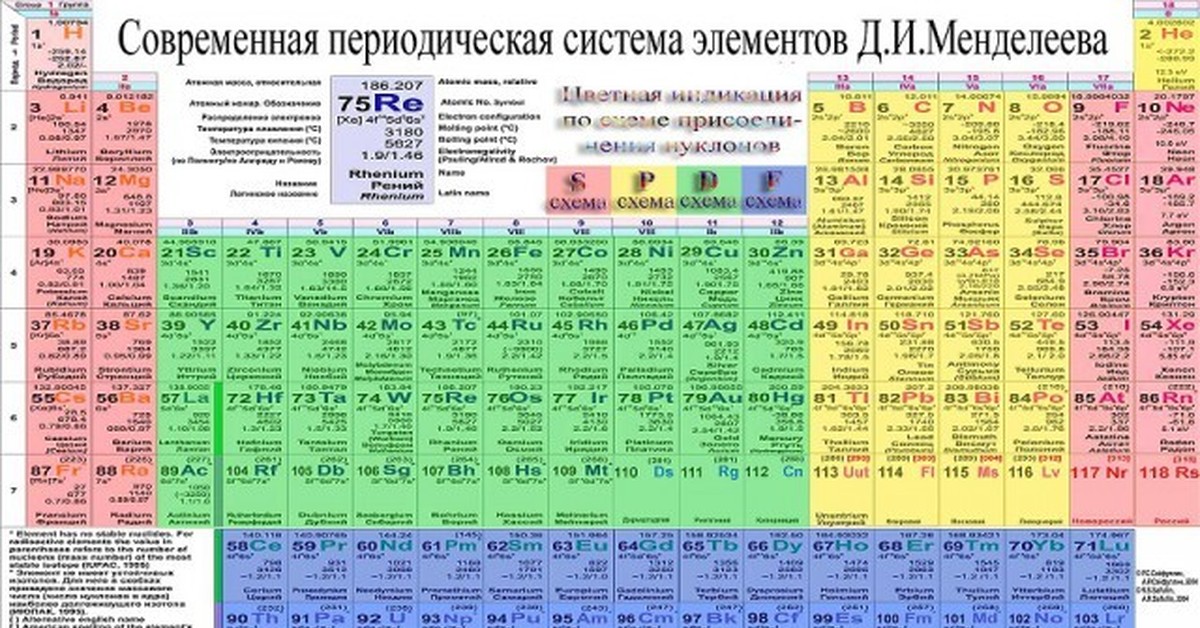
Один из важных шагов к созданию Периодической системы — спираль Шанкуртуа. Она стала первой попыткой упорядочить в виде таблицы известное к тому времени множество химических элементов. Пытаясь, как и другие химики, найти основу для их классификации, французский учёный Александр Эмиль Бегуйе де Шанкуртуа высказал предположение, что «свойства элементов являются функцией чисел». В 1862 году он предложил для систематизации химических элементов оригинальную пространственную схему. Шанкуртуа выдвинул идею спирального расположения элементов в зависимости от их атомных масс.
В своём сочинении «Земная спираль» он сгруппировал элементы по спирали вокруг цилиндра в порядке возрастания их масс. Оказалось, что через 16 единиц атомной массы появляются близкие по химическим свойствам элементы. В спирали Шанкуртуа они находятся на одной вертикальной линии, образующей цилиндр, на который «наворачивается» эта спираль. Однако идея расположения элементов на оси «земного винта» не привлекла внимания его современников. Не знал о ней и Д. И. Менделеев.
Самая примечательная работа Поля Эмиля Лекока де Буабодрана — это открытие галлия.
В 1875 году он получил несколько миллиграммов хлорида галлия, выделив его из образца минеральной руды, и нашёл, что это вещество дает новые спектроскопические линии. Он продолжал эксперименты, переработав несколько сот килограммов цинковой руды из Пиренеев, и в том же году выделил более 1 грамма чистого металла посредством электролиза раствора его гидроксида в гидроксиде калия.
Позже он приготовил 75 граммов галлия, используя более 4 тонн руды. Лекок де Буабодран вычислил атомную массу галлия — 69,86, весьма близкую к ныне принятой массе — 69,723. Существование галлия было предсказано в 1871 г. Д. И. Менделеевым, который назвал его «экаалюминием», и открытие де Буабодрана было подтверждением Периодического закона <br\>Д. И. Менделеева. Лекок де Буабодран внёс большой вклад в развитие Периодической системы элементов, предположив вскоре после открытия аргона, что тот является представителем новой, ранее непредусмотренной серии химических элементов, позже получившей известность как группа благородных газов.
Лекок де Буабодран вычислил атомную массу галлия — 69,86, весьма близкую к ныне принятой массе — 69,723. Существование галлия было предсказано в 1871 г. Д. И. Менделеевым, который назвал его «экаалюминием», и открытие де Буабодрана было подтверждением Периодического закона <br\>Д. И. Менделеева. Лекок де Буабодран внёс большой вклад в развитие Периодической системы элементов, предположив вскоре после открытия аргона, что тот является представителем новой, ранее непредусмотренной серии химических элементов, позже получившей известность как группа благородных газов.
В 1886 году выделил чистый элемент, германий, и опубликовал свои результаты. Триумф предсказательной силы открытия Д. И. Менделеева был настолько велик, что К. Винклер натолкнулся на неприятие со стороны некоторых химиков предложенного им названия «германий». Они стали обвинять К. Винклера в национализме и в присвоении открытия, которое сделал Д. И. Менделеев, уже давший элементу имя «экасилиций». Обескураженный К. Винклер обратился за советом к самому Дмитрию Ивановичу. Тот объяснил, что именно первооткрыватель нового элемента должен дать ему название. Позже Винклер писал: «Едва ли можно найти иное, более поразительное доказательство справедливости учения о периодичности, как во вновь открытом элементе. Это не просто подтверждение смелой теории, здесь мы видим очевидное расширение химического кругозора, мощный шаг в области познания».
Винклер обратился за советом к самому Дмитрию Ивановичу. Тот объяснил, что именно первооткрыватель нового элемента должен дать ему название. Позже Винклер писал: «Едва ли можно найти иное, более поразительное доказательство справедливости учения о периодичности, как во вновь открытом элементе. Это не просто подтверждение смелой теории, здесь мы видим очевидное расширение химического кругозора, мощный шаг в области познания».
В 1869 году в научные учреждения России и других стран поступил первый вариант системы («Опыт системы элементов, основанной на их атомном весе и химическом сходстве»), в котором элементы были расставлены по девятнадцати горизонтальным рядам (рядам сходных элементов, ставших прообразами групп современной системы) и по шести вертикальным столбцам (прообразам будущих периодов).
В 1870 году Д. И. Менделеев в «Основах химии» публикует второй вариант системы («Естественную систему элементов»), имеющий более привычный для нас вид: горизонтальные столбцы элементов-аналогов превратились в восемь вертикально расположенных групп; шесть вертикальных столбцов первого варианта превратились в периоды, начинавшиеся щелочным металлом и заканчивавшиеся галогеном.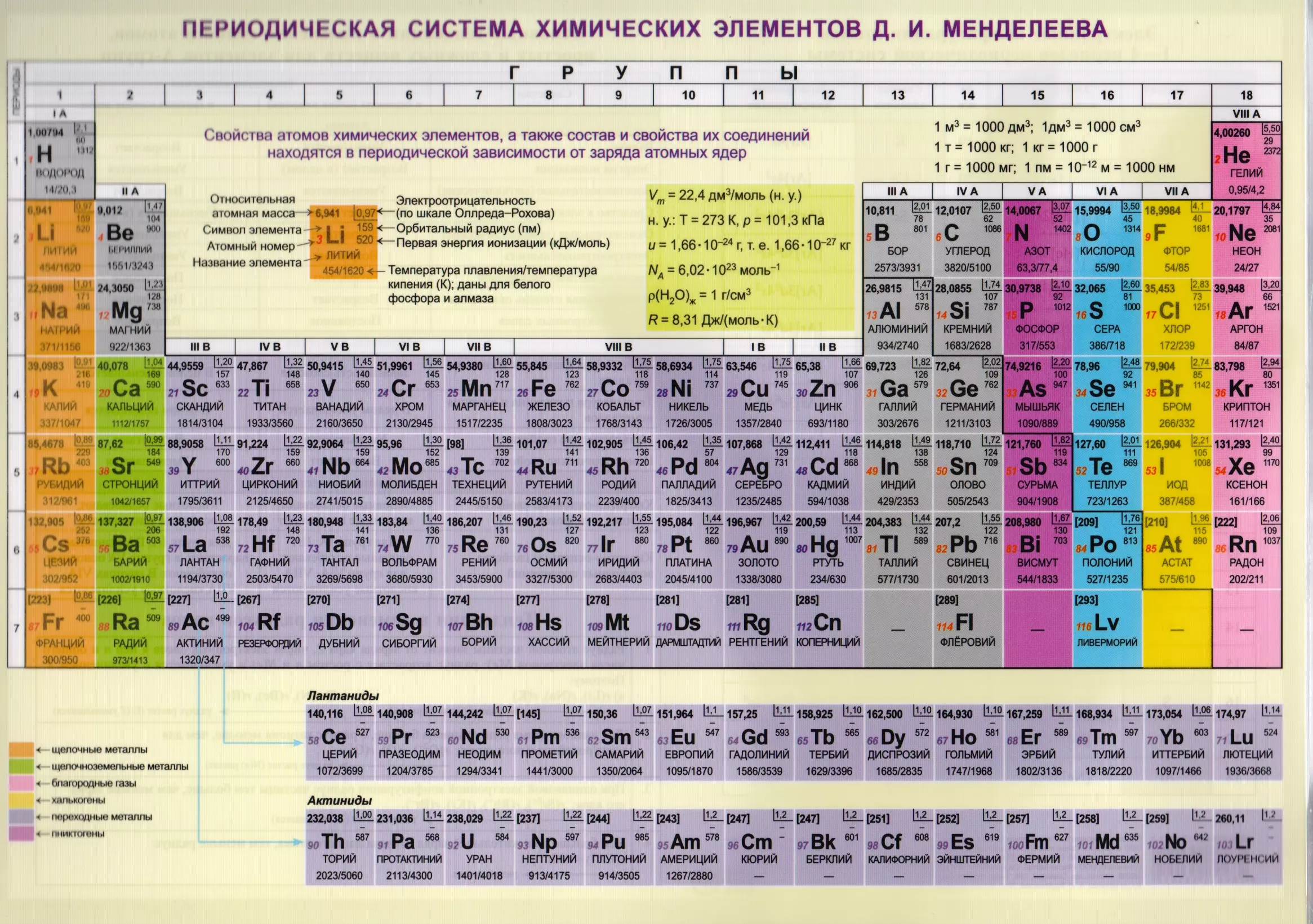 Каждый период был разбит на два ряда; элементы разных вошедших в группу рядов образовали подгруппы.
Каждый период был разбит на два ряда; элементы разных вошедших в группу рядов образовали подгруппы.
Сущность открытия Д. И. Менделеева заключалась в том, что с ростом атомной массы химических элементов их свойства меняются не монотонно, а периодически. После определённого количества разных по свойствам элементов, расположенных по возрастанию атомного веса, свойства начинают повторяться. Например, натрий похож на калий, фтор похож на хлор, а золото похоже на серебро и медь. Разумеется, свойства не повторяются в точности, к ним добавляются и изменения.
Отличием работы Д. И. Менделеева от работ его предшественников было то, что для классификации элементов у Дмитрия Ивановича была не одна, а две основы: атомная масса и химическое сходство. Для того чтобы периодичность полностью соблюдалась, им были предприняты очень смелые шаги: он исправил атомные массы некоторых элементов (например, бериллия, индия, урана, тория, церия, титана, иттрия), несколько элементов разместил в своей системе вопреки принятым в то время представлениям об их сходстве с другими (например, таллий, считавшийся щелочным металлом, он поместил в третью группу согласно его фактической максимальной валентности), оставил в таблице пустые клетки, где должны были разместиться пока не открытые элементы.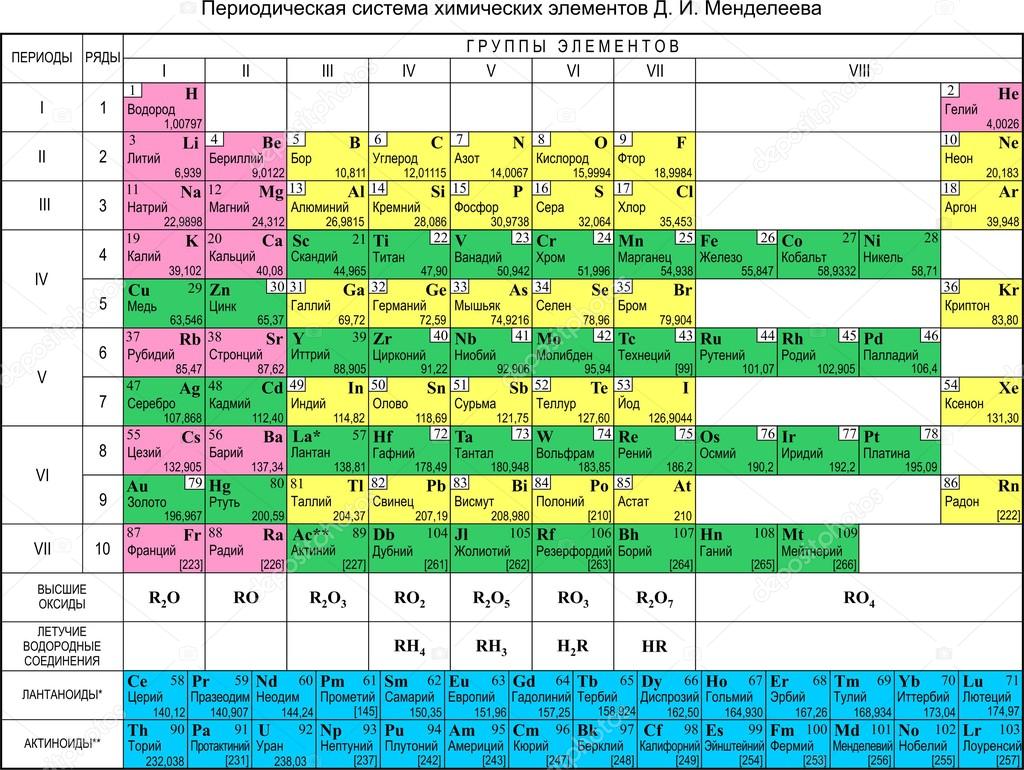
В 1871 году на основе этих работ Д. И. Менделеев сформулировал Периодический закон, форма которого со временем была несколько усовершенствована.
Научная достоверность Периодического закона получила подтверждение очень скоро: в 1875—1886 годах были открыты галлий (экаалюминий), скандий (экабор) и германий (экасилиций), для которых Д. И. Менделеев, пользуясь Периодической системой, предсказал не только возможность их существования, но и — с поразительной точностью — целый ряд физических и химических свойств.
Основные работы Ларса Фредерика Нильсона связаны с изучением редких элементов. В 1879 году он открыл элемент скандий, атомная масса и свойства которого соответствовали предсказанному Д. И. Менделеевым «экабору» (1870). Это открытие, наряду с открытием галлия (П. Э. Лекок де Буабодран, 1875) и германия (К. А. Винклер, 1885), способствовало утверждению Периодического закона, сформулированного в 1869 году Д. И. Менделеевым.
1. Самая большая таблица Менделеева установлена на стенах химического факультета в Университете Мурсии в Испании. В общей сложности инсталляция занимает около 150 кв. м и состоит из 118 металлических квадратов размером 75 × 75 см. В Периодическую систему включены все известные на сегодняшний день химические элементы.
В общей сложности инсталляция занимает около 150 кв. м и состоит из 118 металлических квадратов размером 75 × 75 см. В Периодическую систему включены все известные на сегодняшний день химические элементы.
2. В 2006 году в административном центре города Чикаго из отдельных плакатов была собрана огромная таблица Менделеева, которая простиралась на восемь этажей.
3. В 2016 году в городе Сан-Антонио ученики более 100 школ собрались на стадионе и выложили громадную таблицу Менделеева из отдельных квадратных элементов размером 3,5 × 4,5 м. Общая площадь инсталляции составила 2000 кв. м.
4. В Санкт-Петербурге Периодическая таблица Менделеева была создана в 1935 году по адресу: Московский проспект, дом 19. Памятник представляет собой выполненную мозаикой на стене дома таблицу химических элементов, которая соответствовала её состоянию при жизни Менделеева и была приведена в последнем прижизненном восьмом издании, опубликованном в 1906 году. На ней элементы, открытые при жизни учёного, изображены красным цветом, а элементы, открытые с 1907 по 1934 год, — синим. Выполнен памятник в 1935 году по инициативе Сталина. Ранее, в 1932 году, здесь была установлена скульптура Дмитрия Ивановича Менделеева.
Выполнен памятник в 1935 году по инициативе Сталина. Ранее, в 1932 году, здесь была установлена скульптура Дмитрия Ивановича Менделеева.
5. В городе Верхний Уфалей, расположенном в Челябинской области, есть памятник
Д. И. Менделееву. Ученый заезжал в этот город в 1899 году и, осмотрев здешнее производство и разработки, воскликнул: «Да у вас тут вся моя таблица!». В честь этого в Верхнем Уфалее поставили памятник Менделееву на фоне его таблицы.
6. Памятник Менделееву и его таблице есть в Словакии. Находится он перед химическим факультетом Словацкого технологического университета в Братиславе.
В 2017 году памятник Менделееву украсил бульвар Менделеева в посёлке Мурино Ленинградской области. Памятник «Сон Менделеева» посвящен легенде о знаменитом сне ученого, в котором он увидел периодическую таблицу элементов. Футуристическая скульптура изображает химические элементы, над которыми парит фигура Дмитрия Менделеева.
- ← 250-летию со дня рождения И.
 А. Крылова
А. Крылова - «Если быть, то быть первым» →
Как была создана Периодическая таблица Labmate Online
Сегодня Периодическая таблица украшает стены учебных кабинетов и университетских лабораторий по всему миру. Чего многие люди не знают, так это того, что табличное отображение химических элементов было впервые введено более 150 лет назад Дмитрием Менделеевым, русским химиком, который был одним из первых, кто понял отношения между элементами.
Периодическая таблица в настоящее время содержит 118 подтвержденных элементов, каждый из которых содержит уникальный набор символов и чисел. Эти числовые и символические подписи раскрывают закономерности и связи в свойствах каждого элемента и служат ориентиром для химических исследований.
«Периодическая таблица, — пишет знаменитый английский исследователь из Оксфордского университета Питер Аткинс, — возможно, самое важное понятие в химии».
От нарисованного от руки эскиза к научным знаниям Хотя сегодня Периодическая таблица считается чем-то вроде научной Библии, первоначальная таблица, составленная Менделеевым, была не более чем нарисованным от руки наброском.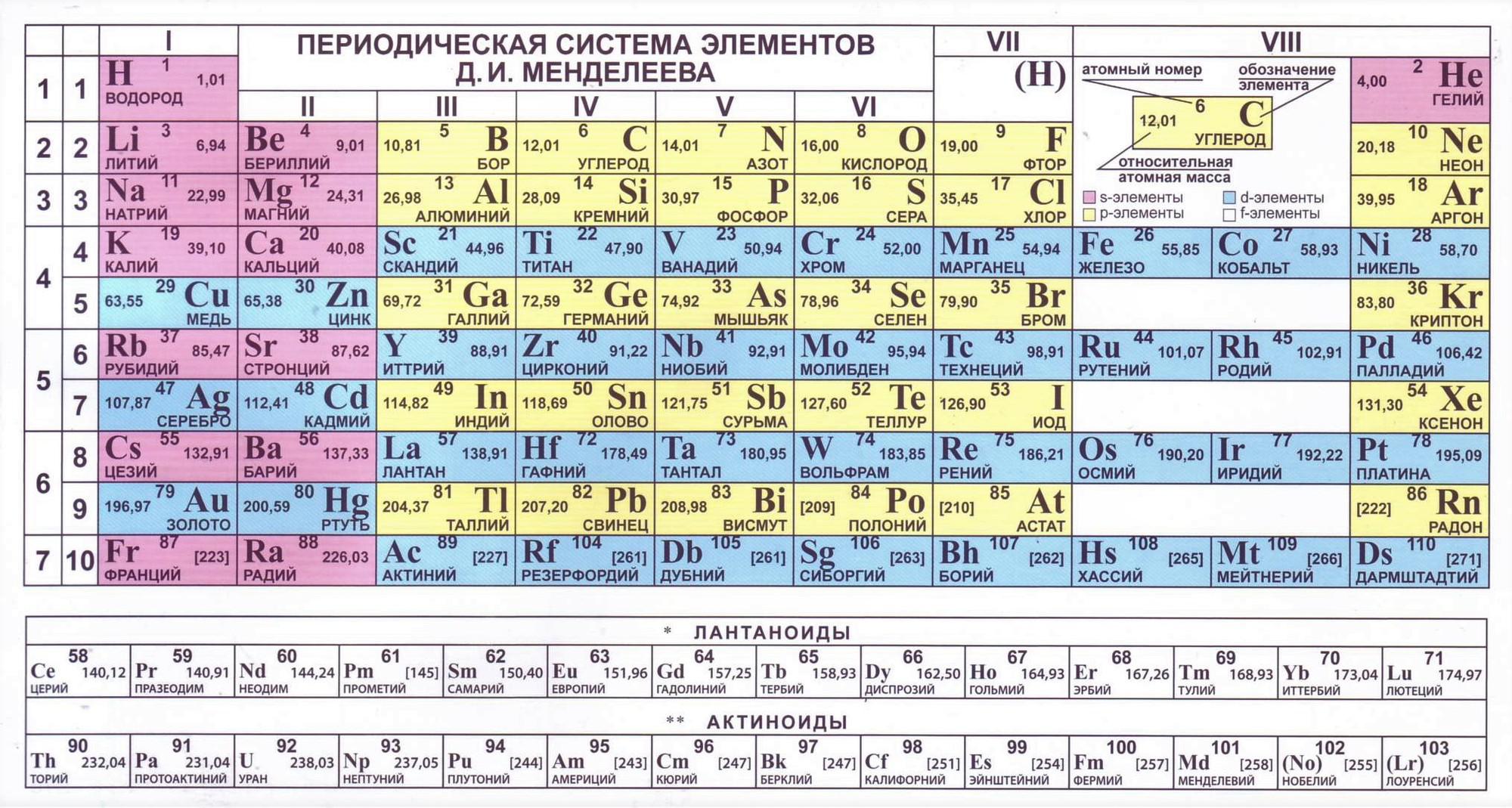 Он реализовал свое видение, чтобы расположить элементы в порядке их атомного веса, и в результате смог точно определить семейные отношения. Эти сходные свойства появлялись через определенные промежутки времени, или периоды, как называл их Менделеев.
Он реализовал свое видение, чтобы расположить элементы в порядке их атомного веса, и в результате смог точно определить семейные отношения. Эти сходные свойства появлялись через определенные промежутки времени, или периоды, как называл их Менделеев.
«Элементы, расположенные в соответствии с величиной их атомного веса, обнаруживают явные периодические свойства, — сказал Менделеев, сформулировавший Периодический закон в 1869 году. определяет природу элементов».
Предсказание новых элементовЭто открытие позволило ему не только уточнить свойства известных элементов, но и предсказать свойства восьми элементов, которые в то время еще не были открыты. В переводе с русского название оригинальной Периодической таблицы, набросанной Менделеевым, звучит так: «Набросок системы элементов: на основе их атомных масс и химических характеристик».
«До обнародования этого закона химические элементы были лишь фрагментарными, случайными фактами в Природе», — сказал Менделеев. «Закон периодичности впервые позволил нам воспринимать неоткрытые элементы на расстоянии, ранее недоступном химическому зрению».
«Закон периодичности впервые позволил нам воспринимать неоткрытые элементы на расстоянии, ранее недоступном химическому зрению».
В то время как Менделеев получил большую часть заслуг в разработке Периодической таблицы, следует также отдать должное немецкому химику Иоганну Вольфгангу Доберейнеру, который исследовал концепцию сгруппированных элементов в начале 1800-е годы. Английский школьный учитель Джон Дальтон также внес свой вклад в ранние исследования, объяснив механику химических реакций в своей «Новой системе химической философии», опубликованной в 1842 г.
На протяжении многих лет Периодическая таблица развивалась, обновлялась и дополнялась. Некоторые из новейших дополнений включают нихоний, московий, теннессин и оганесон, которые были одобрены Международным союзом теоретической и прикладной химии и добавлены в таблицу в 2016 году. Чтобы ознакомиться с последними обновлениями технологий, производимых австрийской компанией Anton Paar, не пропустите «Новое определение цифрового измерения плотности».
Самая старая периодическая таблица в мире найдена в хранилище
Самая старая известная периодическая таблица в мире была обнаружена в Университете Сент-Эндрюс. Датированная 1885 годом, таблица была создана всего через 16 лет после того, как русский химик Дмитрий Менделеев представил эту концепцию в 1869 году.
Исторический документ, обнаруженный профессором химии Аланом Эйкеном в 2014 году, очевидно, был оставлен в хранилище. Эйкен убирал ненужные химикаты и просроченные материалы, когда обнаружил таблицу, которая, по-видимому, находилась там с 19-го века.68. Не сохранив сохранности, которая требовалась бы для старого документа, его свернули и забыли. Неудивительно, что документ был чрезвычайно хрупким и отслаивался при первом обращении.
1860-е годы, когда была создана таблица Менделеева, были захватывающим временем для науки. Каждый год открывали примерно один новый элемент. Ученые разработали ряд способов систематизировать эти новые открытия.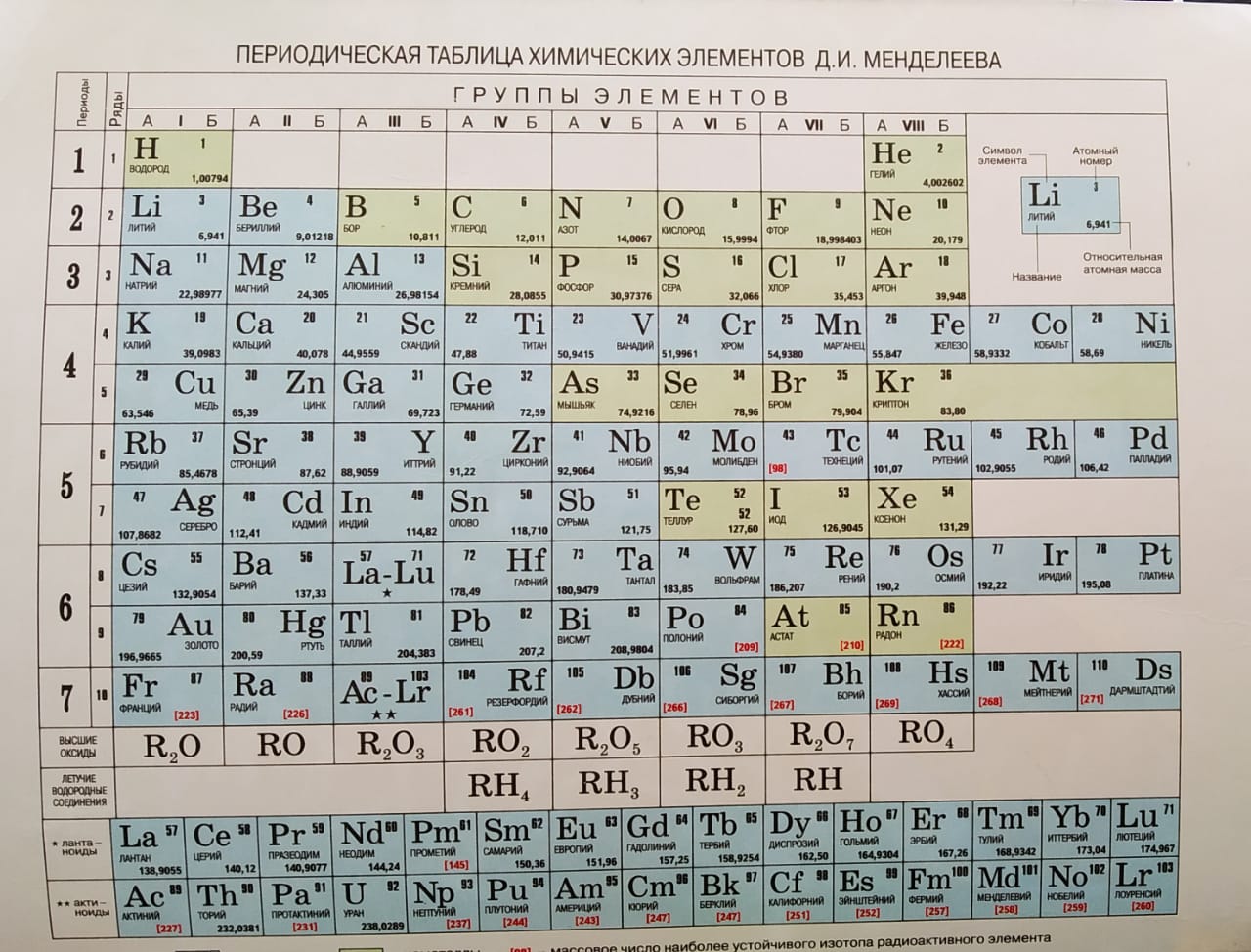 Французский геолог Александр-Эмиль Бегуйе де Шанкуртуа попытался создать трехмерный цилиндр, который работал бы, когда его обернули вокруг шеста, а британский химик Джон Ньюлендс попытался сравнить элементы с музыкальной гаммой.
Французский геолог Александр-Эмиль Бегуйе де Шанкуртуа попытался создать трехмерный цилиндр, который работал бы, когда его обернули вокруг шеста, а британский химик Джон Ньюлендс попытался сравнить элементы с музыкальной гаммой.
Легенда гласит, что Менделеев раскладывал элементы в стиле карточного пасьянса, находя спички и раскладывая их по весу. Правда это или нет, но таблица Менделеева закрепилась в научном сообществе по нескольким причинам, в том числе потому, что она оставляла место для будущих открытий. В его системе также есть чистая визуальная простота, которой не хватало другим до нее.
К 1871 году, когда Менделеев выпустил улучшенную версию своей диаграммы, которая казалась более близкой к современной, она приближалась к положению научного стандарта. График Сент-Эндрюс похож на эту вторую версию с небольшими отличиями. Аннотированный на немецком языке, он гласит: «Verlag v. Lenoir & Forster, Wien» в нижнем левом углу — имя немецкого научного издателя, работавшего в то время в Вене между 1875 и 1888 годами. 0003
0003
Сама таблица также содержит историческое свидетельство того, когда она была изготовлена. По словам Эрика Шерри, эксперта по истории периодической таблицы из Калифорнийского университета в Лос-Анджелесе, эта таблица может быть датирована периодом между 1879 и 1886 годами. Галлий и скандий, например, были обнаружены в 1870-е годы. Отсутствует германий, предсказанный Менделеевым элемент, открытый в 1886 году.
Карта попала в Сент-Эндрюс с вполне предсказуемой миссией: помочь профессору преподавать химию. Архивариусы считают, что профессор Томас Пурди купил диаграмму у своих немецких типографий в 1885 г. за три марки и получил ее в 1888 г.
Теперь, когда стол был обнаружен, ему будет оказана крайне необходимая нежная забота. Он будет промыт в деионизированной воде, доведенной до нейтрального pH с помощью гидроксида кальция, чтобы удалить растворимое обесцвечивание и его кислотность, тщательно очищен щеткой для удаления рыхлого поверхностного мусора, отремонтирован японской бумагой кодзо и в целом получит пятизвездочную обработку документ этого заслуживает историчность.
