Старинный способ решения задач на смеси
Старинный арифметический способ
Автор презентации Софронова Наталия Андреевна,
Учитель математики МОУ «Упшинская ООШ» Оршанского района Республики Марий Эл
Данный тип задач охватывает большой круг ситуаций – смешение товаров разной цены, жидкостей с различным содержанием соли, кислот различной концентрации, сплавление металлов с различным содержанием некоторого металла и пр. Связь различных задач между собою станет яснее, если рассматривать типичные ситуации в общем виде.
При решении задач данного типа используются следующие допущения:
- Всегда выполняется «Закон сохранения объема или массы»: если два раствора (сплава) соединяют в «новый» раствор (сплав), то выполняются равенства:
V = V 1 + V 2 – сохраняется объем;
m = m 1 +

- Данный закон выполняется и для отдельных составляющих частей (компонентов) сплава (раствора).
- При соединении растворов и сплавов не учитываются химические взаимодействия их отдельных компонентов.
Задачи на смеси, растворы и сплавы называют еще задачами на процентное содержание или концентрацию.
Введем основные понятия.
Говоря о смесях, растворах и сплавах, будем употреблять термин «смесь» независимо от ее вида (твердая, жидкая, газообразная, сыпучая и т. д.). Смесь состоит из «чистого вещества» и «примеси».
Долей α чистого вещества в смеси называется отношение количества чистого вещества
Процентным содержанием чистого вещества в смеси с называют его долю, выраженную процентным отношением:
На практике для выражений «отношение массы растворённого вещества к массе раствора» и «отношение объёма растворённого вещества к объёму раствора» применяют термин «концентрация » и говорят о концентрации растворов.
Задача №1. В каких пропорциях нужно смешать раствор 50%-й и 70%-й кислоты, чтобы получить раствор 65%-й кислоты?
1 раствор
Масса раствора
х
2 раствор
Концентрация
Смесь
у
50%
Масса чистой кислоты
0,5х
х+у
70%
0,7у
65%
0,65(х+у)
Ответ: 1:3
В каких пропорциях нужно смешать раствор 50%-й и 70%-й кислоты, чтобы получить раствор 65%-й кислоты?
Арифметический (старинный) способ .
50
70-65
65
65-50
70
х : у = (70 – 65) : (65 – 50) = 1 : 3
Обоснование старинного способа решения:
Пусть требуется смешать растворы кислоты различной концентрации – n% -й и m %-й, чтобы получить р%-й раствор
Масса раствора
1 раствор
х
2 раствор
Концентрация
Смесь
у
n %
Масса чистой кислоты
х+у
m %
p %
Схема решения
m-p
n
p
m
p-n
х : у = ( m – p ) : ( p – n
Задача № 2 Смешали 30%-й раствор соляной кислоты с 10%-ым и получили 600 г 15%-го раствора. Сколько граммов каждого раствора было взято?
Сколько граммов каждого раствора было взято?
30
5
15
15
10
Ответ: 150 г первого раствора и 450 г второго раствора
Задача №3. В лаборатории имеется 2 кг раствора кислоты одной концентрации и 6 кг раствора этой же кислоты другой концентрации. Если эти растворы смешать, то получится раствор, концентрация которого составляет 36%. Если же смешать равные массы этих растворов, то получится раствор, содержащий 32% кислоты. Какова концентрация каждого из двух имеющихся растворов?
m-36
n
m-32
n
32
36
36-n
32-n
m
m
x : x = (m-32) : (32-n)
2 : 6 = (m-36) : (36-n)
Ответ: 20% и 24%
Задача №4. Имеются два сосуда, содержащие 30 кг и 20 кг раствора кислоты различной концентрации. Если их слить вместе, то получим раствор, содержащий 81% кислоты. Если же слить равные массы этих растворов, то полученный раствор будет содержать 83% кислоты. Сколько килограммов кислоты содержится во втором растворе?
Если их слить вместе, то получим раствор, содержащий 81% кислоты. Если же слить равные массы этих растворов, то полученный раствор будет содержать 83% кислоты. Сколько килограммов кислоты содержится во втором растворе?
n % – концентрация 1 раствора, m % – концентрация 2 раствора
m- 83
n
m- 81
n
81
83
83 -n
m
81 -n
m
x : x = (m- 83 ) : ( 83 -n)
30 : 20 = (m- 81 ) : ( 81 -n)
Концентрация второго раствора – 93%
Второй раствор содержит 0,93∙20=18,6 кг
Ответ: 18,6 кг
Задача №5. При смешивании первого раствора кислоты, концентрация которого 20%, и второго раствора этой же кислоты, концентрация которого 50%, получили раствор, содержащий 30% кислоты. В каком отношении были взяты первый и второй раствор?
х – масса 20%-го раствора,
у – масса – 50%-го раствора
2 0
20
30
10
5 0
Ответ: 2 : 1
Задача №6. На аукционе одна картина была продана с прибылью 20%, а другая – с прибылью 50%. Общая прибыль от продажи двух картин составила 30%. У какой картины первоначальная цена была выше и во сколько раз?
На аукционе одна картина была продана с прибылью 20%, а другая – с прибылью 50%. Общая прибыль от продажи двух картин составила 30%. У какой картины первоначальная цена была выше и во сколько раз?
х руб – первоначальная стоимость первой картины
у руб – первоначальная стоимость второй картины
2 0
20
30
10
5 0
Ответ: У первой картины стоимость была выше в 2 раза
Задачи на смеси и сплавы .
Задачи на смеси, сплавы и растворы.
1. Подход к решению задач на смеси.
Человеку часто приходится смешивать различные жидкости, порошки, или твердые вещества, или разбавлять что-либо водой.
Задачи на смеси имеют практическую направленность. Например,
мы пьём чай и кладем в чашку столько сахара, чтобы не пересластить (создаём
нужную нам концентрацию), а если пересластили, то добавляем воды.
Летом мы ходим за грибами, затем их сушим. И мы понимаем, что чем дольше их сушить, тем меньше в них остается воды, при этом масса сухого вещества не меняется.
Врач выписывает рецепт, и мы покупаем мази, микстуры с определенной концентрацией лекарственных веществ. Решая задачи данного типа, нам нужно будет выделить компоненты, которые изменяются, и те, что остаются неизменными.
Говоря о смесях, растворах и сплавах будем употреблять термин «смесь» независимо от её вида (твердая, жидкая, сыпучая, газообразная). Смесь состоит из основного вещества и примеси. Что такое основное вещество, в каждой задаче определяется отдельно.
Текстовые задачи на смеси, сплавы и растворы входят в различные сборники заданий по математике и химии ОГЭ и ЕГЭ.
При решении любых задач, прежде всего, нужно грамотно прочитать условие, последовательно остановиться на каждой строчке, и попытаться выразить условие в качестве какого-то уравнения.
. Что же отличает задачи на
смеси? Уравнение трудно составить, если не знать основную формулу для всех
задач на смеси.
В «Занимательной алгебре» Я.И. Перельмана есть любопытная задача под названием: «В парикмахерской»:
Задача:
-Не поможете ли нам разрешить задачу, с которой мы никак не справимся?
– Уж сколько раствора испортили из-за этого!- добавил другой
– В чем задача?
– У нас имеется два раствора перекиси водорода: 30%- ыйи 3 % -ый. Нужно их смешать так, чтобы составился 12% -ый раствор. Не можем подыскать правильной пропорции.
Мне дали бумажку, и требуемая пропорция была найдена.
Она оказалась очень простой. Какой именно?
Решение: Пусть для составления 12%-ной смеси требуется взять
В результате получается (x + y) граммов раствора, в котором чистой перекиси должно быть 0,12 (x + y)
Имеем уравнение: 0,03x + 0,3y=0,12 (x + y)
Из
этого уравнения находим x =2y, т. е. 3%-ного
раствора надо взять вдвое больше.
е. 3%-ного
раствора надо взять вдвое больше.
Задача, описанная Перельманом, встречается не только в парикмахерских.
Например, для зарядки аккумуляторов бывает необходимо приготовить электролит, который должен содержать 24% серной кислоты из двух растворов с содержанием 92% и 10% серной кислоты.
2. Теоретические основы решения задач на смеси и сплавы.
Задачи на смеси, растворы и сплавы называют еще задачами на процентное содержание или концентрацию. Данный тип задач охватывает большой круг ситуаций – смешение товаров разной цены, жидкостей с различным содержанием соли, кислот различной концентрации, сплавление металлов с различным содержанием некоторого металла и пр. При решении задач данного типа используются следующие допущения:
1. Все получающиеся смеси и сплавы однородны;
2.Всегда выполняется «Закон сохранения объема или массы»:
если два раствора (сплава) соединяют в «новый» раствор (сплав), то выполняются равенства:
V = V1+V2 –сохраняется объем;
m = m1 + m2 – сохраняется масса.
3 Данный закон выполняется и для отдельных составляющих частей (компонентов)сплава (раствора).
Определение. Процентным содержанием (концентрацией или массовой долей) вещества в смеси называется отношение его массы к общей массе всей смеси. Это отношение может быть выражено либо в дробях, либо в процентах.
3.Задачи на смешение растворов разных концентраций.
Решим типовую задачу в общем виде и выведем формулу.
Задача:Имеются два куска сплава меди с цинком. Процентное содержание меди в них p1% иp2 % соответственно. В каком отношении нужно взять массы этих сплавов, чтобы, переплавив взятые куски вместе, получить сплав, содержащий p%меди?
Решение.Понаблюдаем за содержанием меди.
Исследуем
уравнение (*) при условии, что будем брать ненулевые массы сплавов.
I случай. Если p1 ,p2 и p попарно не равны, то получим формулу
m1 (p1 – p) =m2(p – p2) (*)
II случай. Возьмём два
сплава с одинаковым процентным содержанием меди, т.е. p1=p2 . Решая
уравнение (*), получим, что p1=p2=p, т. к. ни большей, ни меньшей концентрации сплав просто не
получится, если исходные материалы имеют одинаковую процентную концентрацию
меди, каковы бы ни были массы исходных сплавов.
к. ни большей, ни меньшей концентрации сплав просто не
получится, если исходные материалы имеют одинаковую процентную концентрацию
меди, каковы бы ни были массы исходных сплавов.
III случай. Если p2 =p, или p1= p ,то вывод тот же.
Если взять два сплава, массы которых одинаковы, т.е. m1 = m2 , то
то есть процентное содержание нового сплава станет равно среднему арифметическому процентных концентраций исходных сплавов. А теперь рассмотрим однотипные задачи, решение которых очень удобно по этой формуле:
| ||||||
Смешали
некоторое количество 11%-го раствора некоторого вещества с таким же
количеством 19%-го раствора этого же вещества.
|
|
11% |
|
19% |
| Или т. к. массы исходных растворов равны, то |
Сколько килограммов 20%-го раствора соли нужно добавить к 1 кг 10%-го раствора, чтобы получить 12%-ый раствор соли?
|
|
20% |
1кг |
10% |
12% |
|
В сосуд,
содержащий 13л 18%-го водного раствора некоторого вещества, добавили 5л воды. |
13л |
18% |
5л |
0% |
% |
|
Старинный способ решения задач на смешивание двух веществ.
Предположим, что смешиваются два вещества
– первое стоимостью а гривен за фунт и второе стоимостью b гривен за фунт. Желательно получить вещество стоимостью с гривен за
фунт. Будем считать, что а<b( если с>b или c<a
, то задача неразрешима, ибо, смешивая дешевые вещества, дорогое не получишь). Поэтому можно считать, что a<c<b.
Смешиваем один фунт первого вещества и q фунт второго. В результате получится 1+q фунтов вещества стоимостью a+bq гривен.
Один фунт смеси должен стоить с гривен. Значит должно выполняться
равенство
Поэтому можно считать, что a<c<b.
Смешиваем один фунт первого вещества и q фунт второго. В результате получится 1+q фунтов вещества стоимостью a+bq гривен.
Один фунт смеси должен стоить с гривен. Значит должно выполняться
равенство
a+bq=c*(1+q). Отсюда находим q=(c-a)/(b-c) или (b-c):(c-a).
Это соотношение дает старинный способ.
«Правило креста»
При решении задач на смешивание растворов разных концентраций используется «правило креста». В точке пересечения двух прямых обозначают концентрацию смеси. У концов этих прямых слева от точки пересечения указывают концентрации составных частей смеси, а справа – разности концентраций смеси и ее составных частей:
Для приготовления 30 г
80%-го раствора кислоты требуется взять 20 г 90%-го и 10 г 60%-го растворов
кислоты.
Задача:У некоторого человека были на продажу масла двух сортов: одно ценою 10 гривен за ведро, другое же 6 гривен за ведро. Захотелось ему сделать из этих двух масел, смешав их, масло ценою 7 гривен за ведро. Какие части этих двух масел нужно взять, чтобы получить ведро масла ценою 7 гривен?
Из схемы делаем заключение, что дешевого масла нужно взять втрое больше, чем дорогого, т.е. для получения одного ведра ценою 7 гривен нужно взять дорогого масла 1/4 ведра, а дешевого масла 3/4.
Способ Л.Ф.Магницкого для трех веществ
Указанный Л. Ф. Магницким способ
состоит в следующем. Надо дважды применить способ записи исходных данных и
необходимых количеств веществ, причем в первый раз взять вещества с большей и
меньшей стоимостью, а во второй раз с наименьшей и средней стоимостью.
Повторив действие вычитания и соответствующей записи разности, получим доли, в
которых нужно смешивать вещества наибольшей и средней стоимости (на
соответствующих строках). Сложив доли дешевого вещества, найденные в первый и
во второй раз, получим долю дешевого вещества в общей смеси.
Сложив доли дешевого вещества, найденные в первый и
во второй раз, получим долю дешевого вещества в общей смеси.
Задача: Некто имеет чай трех сортов – цейлонский по 5 гривен за фунт, индийский по 8 гривен за фунт и китайский по 12 гривен за фунт. В каких долях нужно смешать эти сорта, чтобы получить чай стоимостью 6 гривен за фунт?
Взять 6+2=8 частей чая ценой по 5 гривен и по одной части ценой 8 гривен и 12 гривен за один фунт.
Возьмем 8/10 фунта чая ценой по 5 гривен за фунт и по1/10 фунта чая ценой 8 и 12 гривен за фунт, то получим 1 фунт чая ценой 8/10*5 + 1/10*8 + 1/10*12 = 6 гривен
Ответ: 100 т и 40 т.
4. Задачи на многократные переливания.
Рассмотрим задачи, при решении которых можно выявить общую закономерность изменения концентрации раствора в результате многократно повторяющейся операции.
Решим в общем виде такую задачу:
В
сосуде, объём которого равен V0 литров, содержится раствор соли концентрации С0.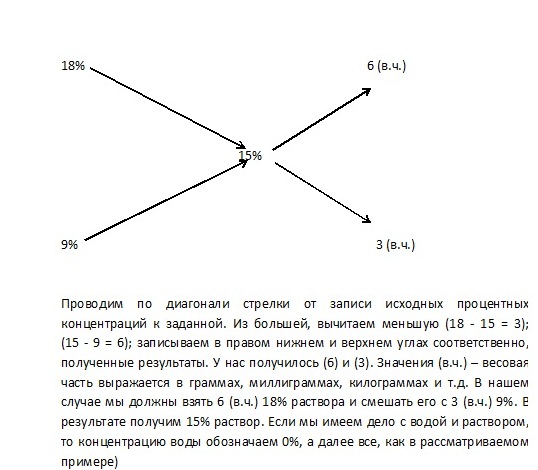 Из сосуда
выливается a литров смеси и доливается a литров воды, после чего
раствор тщательно перемешивается. Эта процедура повторяется n раз. Какова станет концентрация соли в растворе после n таких процедур?
Из сосуда
выливается a литров смеси и доливается a литров воды, после чего
раствор тщательно перемешивается. Эта процедура повторяется n раз. Какова станет концентрация соли в растворе после n таких процедур?
Если в задаче n раз отливают некоторое количество раствора и затем столько же раз приливают такое же количество воды или другого однородного вещества, то для решения задачи пригодится формула:
Где n– количество шагов, V0– начальный объём, который сохраняют неизменным при каждом шаге Сn– конечная концентрация,C0– начальная концентрация,
a – объём отливаемой каждый раз смеси
Докажем эту формулу:
Последовательность С0, С1, С2, Сn-1, Сn представляет собой убывающую
геометрическую
прогрессию концентраций раствора.
Выражение Сn* V0соответствует количеству соли после проведения n-ой процедуры.
Но эта же соль присутствовала в (V0 – a) л предыдущего раствора
в количестве Сn-1 (V0 –a)л Составим уравнение: Сn* V0 = Сn-1 (V0 –a) и разделим обе части на V0 , откуда получаем .
Однотипные задачи, которые
уже легко решить с помощью данной формулы.
| С0 | V0 | a | n | Cn |
|
В сосуде имелось 1250 л 80%-го р-ра к-ты. Из него три раза отливали некоторое кол-во р-ра, добавляя такое же кол-во воды. В результате в сос. осталось 125л чистой к-ты. Какое кол-во р-ра брали изсосуда каждый раз? Ответ:625 л. |
|
|
|
|
| С3=С0(1-a/1250)3 0,1=0,8(1-a/1250)3 0,125=(1-a/1250)3 0,5=1-a/1250 a/1250=0,5 a=625 |
Сколько литров чистого спирта останется в сосуде, если из 50л 80%-ного раствора 20 раз отливать по 1л раствора, каждый раз добавляя по 1 л воды? Ответ:26,7 л. |
|
|
|
|
| С20=0,8(1-1/50)20 С20=0,534 0,534*50=26,7(л) |
Существуют задачи, внешне похожие на применение формулы Сn, но при внимательном чтении оказывается, что цикл переливаний не закончен. В таких случаях надо быть очень внимательным.
Задача:Из сосуда, наполненного кислотой, вылили несколько литров и долили водой; потом опять вылили столько же литров смеси; тогда в сосуде осталось 24 л чистой кислоты. Ёмкость сосуда 54 л. Сколько кислоты вылили в первый раз и второй раз?
Решение: Будем иметь в виду, что на втором шаге воду не доливали.
По
условию задачи объём сосуда, наполненного кислотой, 54 л. Её
концентрация 100%. Пусть вылили х литров смеси, тогда в сосуде осталось (54-х) литров 100%-ной кислоты. В сосуд доливают хл воды. По
определению концентрации надо массу кислоты разделить на массу раствора: (54-х)/54.
Её
концентрация 100%. Пусть вылили х литров смеси, тогда в сосуде осталось (54-х) литров 100%-ной кислоты. В сосуд доливают хл воды. По
определению концентрации надо массу кислоты разделить на массу раствора: (54-х)/54.
Опять выливают х литров смеси, в сосуде остаётся (54-х) л смеси с массовой долей кислоты (54-х)/54.
Чтобы найти массу кислоты в этой оставшейся смеси, надо массу раствора умножить на концентрацию кислоты в этом растворе. По условию масса чистой кислоты в этом растворе стала 24л.
Составим и решим уравнение:
(54-х)* ((54-х)/54) = 24,
(54-х)2= 1296,
зная, что х<54, получим единственное решение: х = 18.
В первый раз вылили 18 литров чистой кислоты. Но во второй раз выливали 18 литров смеси, в ней чистой кислоты было
18* (54-18)/5 =12 (л)
Ответ: 18 л; 12л
Задача: Имеются сплавы золота и серебра. В одном эти металлы находятся
в отношении 2: 3, а в другом в отношении 3: 7. Сколько нужно взять от каждого
сплава, чтобы получить 1 кг нового, в котором золото и серебро находились бы в
отношении 5: 11?
В одном эти металлы находятся
в отношении 2: 3, а в другом в отношении 3: 7. Сколько нужно взять от каждого
сплава, чтобы получить 1 кг нового, в котором золото и серебро находились бы в
отношении 5: 11?
По этой схеме уравнение х + у =1 показывает массу нового сплава.
Определяем массу золота в каждом сплаве и получаем уравнение
Аналогично определяем массу серебра и получаем уравнение
Записываем одну из систем:
Решая ее, получаем х = 0,125 и у = 0,875
Ответ: 125 г и 875 г.
Есть очень легкий, быстрый и «хитрый» способ решения подобных задач, предложенный американским физиком ( русского происхождения) Алексеем Султановым:
= ==
Использованная
литература.
1. Алгебра-7:учебник автор: Ю.Н. Макарычев, Н.Г. Миндюк, К.Н. Нешков,
С.Б. Суворова, Просвещение, 2010
- Прокопенко Н. И.Задачи на смеси и сплавы. – М.: Чистые пруды, 2010.
3. Под редакцией М.И. Сканави. Сборник задач по математике. Москва, 2002г.
4. И.Н. Сергеев ,С. Н. Олехник. Примени математику. Москва «Наука»,1990 г.
5. Сборник задач по математике. Под редакцией А. И. Прилепко.
Москва «Высшая школа», 1998 г.
6. О. А.Городнова Статья «Учимся решать задачи на«смеси и сплавы»,
г-та«Математика»№36 за 2004 г.
7. А.В. Шевкин Школьные математические олимпиады,
изд-во «Русское слово», 2002г.
8.« Занимательной алгебры» авт. Я.И. Перельман.
Как рассчитать конечную концентрацию раствора с различными концентрациями
••• Comstock/Comstock/Getty Images
Обновлено 10 июля 2019 г.
Клэр Гиллеспи , конечное решение не просто соответствует комбинированным уровням концентрации исходных ингредиентов. Характер эксперимента определяет используемые ингредиенты, включая их индивидуальные уровни концентрации. Уровни концентрации обычно представляют собой процент от исходного ингредиента по объему контейнера, поскольку не существует установленных единиц концентрации.
Характер эксперимента определяет используемые ингредиенты, включая их индивидуальные уровни концентрации. Уровни концентрации обычно представляют собой процент от исходного ингредиента по объему контейнера, поскольку не существует установленных единиц концентрации.
Например, если смешать 100 мл 10-процентной концентрации соединения А с 250 мл 20-процентной концентрации того же соединения, математическая формула, включающая начальные концентрации двух растворов, а также объем конечного раствора, позволяет рассчитать конечную концентрацию в процентах от объема нового объединенного раствора.
Вы можете использовать любые единицы для значений концентрации и объемов, если вы используете одни и те же единицы для каждого из двух растворов. Концентрация также может быть выражена процентным составом по массе, мольной доле, молярности, моляльности или нормальности.

Например, вычислите процентный состав по массе 100 г солевого раствора, содержащего 20 г соли, путем деления массы концентрации на общую массу растворенного вещества, а затем умножения на 100. Формула: (20 г ÷ 100 г) х 100, что составляет 20 процентов.
Если вы не знаете концентрации исходных растворов, рассчитайте молярность, разделив количество молей растворенного вещества на объем раствора в литрах. Например, молярность 0,6 моля NaCl, растворенного в 0,45 л, составляет 1,33 М (0,6 моль ÷ 0,45 л). Сделайте это для обоих веществ, чтобы рассчитать конечную концентрацию раствора. (Помните, что 1,33 М означает 1,33 моль/л, а не 1,3 моль.)
Определите объем каждого концентрированного вещества, использованного в эксперименте, путем преобразования процента концентрации в десятичную дробь (т. е. деления на 100) и последующего умножения на общий объем раствора. Расчет объема соединения А в первой концентрации составляет (10 ÷ 100) х 100 мл, что составляет 10 мл. Расчет объема соединения А во второй концентрации составляет (20 ÷ 100) х 250 мл, что составляет 50 мл.
Сложите эти количества вместе, чтобы найти общее количество соединения А в конечной смеси: 10 мл + 50 мл = 60 мл.
Сложите два объема вместе, чтобы определить общий объем конечной смеси: 100 мл + 250 мл = 350 мл.
Используйте формулу x = ( c ÷ V ) × 100 для преобразования концентрации ( c ) и объема ( V процентов) конечного раствора в проценты.
В примере c = 60 мл и В = 350 мл. Решите приведенную выше формулу для x , что является процентной концентрацией конечного раствора. В этом случае х = (60 мл ÷ 350 мл) х 100, поэтому х = 17,14 процента, что означает, что конечная концентрация раствора составляет 17,14 процента.
Related Articles
References
- UCLA Chemistry and Biochemistry: Aqueous Solutions – Molarity
- University of Kent: Mixing Concentrations
About the Author
Claire is a writer and editor with 18 years’ experience. Она пишет о науке и здоровье для ряда цифровых изданий, включая Reader’s Digest, HealthCentral, Vice и Zocdoc.
Фото Кредиты
Comstock/Comstock/Getty Images
Как рассчитать концентрацию растворов и смесей
Revolutionized поддерживается читателями. Когда вы покупаете по ссылкам на нашем сайте, мы можем получать партнерскую комиссию. Узнайте больше здесь.
Химия может показаться сложной отраслью науки, но большая часть исследований в этой области направлена на смешивание разных вещей и наблюдение за тем, что происходит дальше. Одним из занятий химиков является создание растворов и смесей для проведения экспериментов. Что такое решения? Что такое смеси? Как химики используют каждую формулу концентрации, и можете ли вы воспроизвести этот процесс дома?
Давайте подробнее рассмотрим эти вопросы и посмотрим, что мы можем узнать об этом основном арендаторе химии.
Что такое решения?
Когда вы смешиваете ложку сахара в стакане теплой воды, что происходит? Покрутите ложку несколько раз, и сахар растворится в воде, создавая что-то сладкое для глотка. Поздравляем — вы сделали свое первое решение. Каковы другие примеры решений?
Поздравляем — вы сделали свое первое решение. Каковы другие примеры решений?
Химики определяют растворы как любую смесь двух или более веществ, когда они становятся гомогенными или полностью смешиваются и не могут быть разделены механическими средствами. Например, вы не можете получить сахар из сахарной воды, пропуская ее через сито или фильтр. Растворы состоят из двух частей — растворителя и растворенного вещества. В нашем примере с сахаром и водой вода является растворителем, а сахар — растворенным веществом.
Решения не ограничиваются химической лабораторией. Есть много, которые вы можете найти лежащими вокруг вашего дома. Например, газировка и другие газированные напитки шипят из-за растворенного в жидкости углекислого газа. Бытовой отбеливатель представляет собой раствор воды, растворителя, и гипохлорита натрия, растворенного вещества.
Ваша утренняя чашка кофе представляет собой раствор, созданный путем полного растворения кофейной гущи или частиц в воде. Проверьте эту идею, разбавив кофе водой — смесь будет прозрачной, а не мутной. Майонез, который вы намазываете на бутерброды, также представляет собой раствор, известный как эмульсия. Это гомогенная смесь яиц и масла, в которой и растворитель, и растворенное вещество являются жидкими.
Проверьте эту идею, разбавив кофе водой — смесь будет прозрачной, а не мутной. Майонез, который вы намазываете на бутерброды, также представляет собой раствор, известный как эмульсия. Это гомогенная смесь яиц и масла, в которой и растворитель, и растворенное вещество являются жидкими.
Теперь, когда у вас есть общее представление о том, что такое решение, давайте перейдем к следующему персонажу нашей истории — смеси.
Что такое смеси?
Помните, что растворы нельзя разделить механически? Смеси — полная противоположность. Это два разных материала, но они не становятся однородными, поэтому их можно разделить путем фильтрации или просеивания.
Все, что вы смешиваете и можете снова разделить, считается смесью. Когда дело доходит до примеров смесей, рассмотрим простую идею о камнях в банке с водой. Свойства камней и воды остаются прежними, и вы можете удалить камни и отфильтровать любые мелкие частицы, которые могут остаться.
Где в вашем домашнем хозяйстве вы можете найти другие смеси? Поищите в холодильнике заправку для салата в стиле винегрет. Масло и уксус смешать, если встряхнуть, чтобы получилась вкусная заправка для салата. Однако, если вы оставите их на некоторое время, два компонента разделятся. Говоря о салатах, ассортимент разных овощей представляет собой смесь.
Масло и уксус смешать, если встряхнуть, чтобы получилась вкусная заправка для салата. Однако, если вы оставите их на некоторое время, два компонента разделятся. Говоря о салатах, ассортимент разных овощей представляет собой смесь.
У тебя во дворе грязь? У вас смесь воды и грязи. Оба кажутся однородными, но ни один из них не изменяется другим. Если вы испытываете волну тепла, вода высыхает, и грязь снова становится грязью. Дым, поднимающийся от гриля, также представляет собой смесь твердых частиц, выделяющихся из огня.
Теперь, когда вы хорошо представляете себе, что такое растворы и смеси, как можно рассчитать концентрацию каждого из них?
Формула концентрации, о которой следует помнить
Существует несколько способов расчета концентрации раствора. Первым шагом является определение растворителя и растворенного вещества в растворе. Для этого примера мы вернемся к той аналогии сахара и воды, которая использовалась ранее, где наш растворитель — это вода, а наше растворенное вещество — сахар. Теперь у нас есть несколько различных формул концентрации на выбор:
Теперь у нас есть несколько различных формул концентрации на выбор:
- Частей на миллион/миллиард (ppm/ppb): Этот расчет применим только к очень разбавленным растворам. Если бы у вас был 1 миллион частей воды и 50 частей из них были бы сахаром, у вас было бы измерение 50 частей на миллион.
- Граммы на литр (г/л): Простое измерение, идеально подходящее для домашних химиков. Если у вас есть 50 граммов сахара и 1 литр воды, ваш результат будет 50 г/л.
- Состав в процентах по массе: Для этого расчета разделите массу растворенного вещества — в данном случае сахара — на массу растворителя. Если весь ваш раствор весит 100 граммов, и вы добавили 50 граммов сахара, у вас есть 50%-й раствор сахара.
- Объемный процент: Для этой формулы разделите объем раствора на объем растворенного вещества и умножьте его на 100%. Алкогольные напитки являются отличным примером этого, так как на этикетках указано процентное содержание этанола — может быть, от 12 до 15%.
 Это означает, что на каждые 100 мл жидкости приходится от 12 до 15 мл этанола.
Это означает, что на каждые 100 мл жидкости приходится от 12 до 15 мл этанола.
Когда вы смотрите на решения, есть также понятие моля, молярности и моляльности. Моли — это отдельные частицы растворенного вещества, а молярность — это количество молей в растворе. Чтобы определить молярную массу растворенного вещества, необходимо знать молярную массу каждого элемента в растворенном веществе. Это то, что вы часто можете найти в периодической таблице.
Расчет концентрации смесей
Формула концентрации для смесей, а не для гомогенных растворов проста в тех случаях, когда можно отделить растворенное вещество от растворителя. Если у вас есть смесь камней и воды, отфильтруйте камни и измерьте каждый компонент отдельно.
Если вы смешиваете жидкости, такие как масло и уксус, вы можете использовать упомянутую выше смесь объемных процентов. Большинство винегретов состоят из одной части уксуса и двух частей масла, а также других дополнительных ингредиентов для придания вкуса.
Если ваши компоненты трудно разделить, используйте метод молярной концентрации. Шаги для расчета концентрации смеси почти такие же, как и для расчета концентрации раствора.
Ваше будущее в химии
Когда дело доходит до химии, смеси и растворы являются неотъемлемой частью науки, но это не означает, что они ограничены лабораторией. Загляните на свою кухню или в свой дом. Какие еще решения и смеси вы можете обнаружить?
Если вы хотите иметь будущее в области химии, крайне важно знать, как использовать каждую формулу концентрации. Вы можете использовать свои знания, чтобы преуспеть в нескольких областях науки, таких как неорганическая химия. Прежде чем вы это узнаете, вы сможете сразиться с такими экспертами, как Уильям Липскомб, который получил Нобелевскую премию по химии в 2976 году за исследование боранов с помощью рентгеновских методов.
Revolutionized поддерживается считывателями. Когда вы покупаете по ссылкам на нашем сайте, мы можем получать партнерскую комиссию.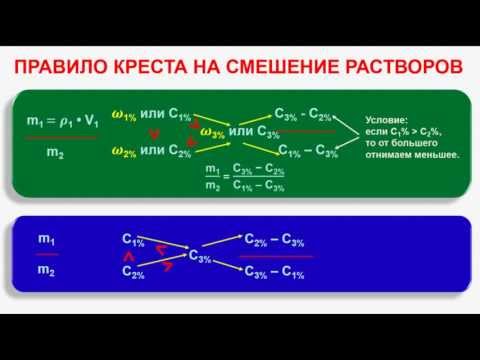

 Найдите концентрацию
раствора.
Найдите концентрацию
раствора. Найти концентрацию получившегося раствора.
Найти концентрацию получившегося раствора.