Константа кислотности – это… Что такое Константа кислотности?
- Константа кислотности
Константа диссоциации кислоты (Ka) — константа равновесия реакции диссоциации кислоты на ион водорода и анион кислотного остатка. Для многоосновных кислот, диссоциация которых проходит в несколько стадий, оперируют отдельными константами для разных стадий диссоциации, обозначая их как Ka1, Ka2 и т. д.
Примеры расчета
(A — условное обозначение аниона кислоты, [HA] — равновесная концентрация в растворе частицы НА):
Одноосновная кислота
HA = H + + A −
Двухосновная кислота
H2A = H + + HA −
HA − = H + + A2 −
Следует понимать, что фигурирующая в выражениях концентрация HA — это равновесная концентрация недиссоциировавшей кислоты, а не изначальная концентрация кислоты до её диссоциации.
Величина pK
Чаще вместо самой константы диссоциации K используют величину pK, которая определяется как отрицательный десятичный логарифм самой константы: pK = -lg K.
См. также
Wikimedia Foundation. 2010.
- Константа в программировании
- Константа фон Клитцинга
Смотреть что такое “Константа кислотности” в других словарях:
константа кислотности — (константа диссоциации кислоты) – константа равновесия Ка, характеризующая степень переноса протона от кислоты к воде как к растворителю. Общая химия : учебник / А. В. Жолнин [1] … Химические термины
константа кислотности — rūgštingumo konstanta statusas T sritis Standartizacija ir metrologija apibrėžtis Rūgšties protolizės pusiausvyros konstanta. atitikmenys: angl. acidity constant vok. Aziditätskonstante, f rus. константа кислотности, f pranc. constante d’acidité … Penkiakalbis aiškinamasis metrologijos terminų žodynas
константа кислотности — rūgštingumo konstanta statusas T sritis chemija apibrėžtis Rūgšties protolizės pusiausvyros konstanta. atitikmenys: angl. acidity constant rus. константа кислотности … Chemijos terminų aiškinamasis žodynas
Уровень кислотности — Водородный показатель, pH (произносится «пэ аш»), это мера активности (в случае разбавленных растворов отражает концентрацию) ионов водорода в растворе, количественно выражающая его кислотность, вычисляется как отрицательный (взятый с обратным… … Википедия
ФУНКЦИИ КИСЛОТНОСТИ — определяют протонирую щую способность р ров к т. Если протонируется нейтральная молекула В, Ф. к. обозначают H0, если анион или катион H или … Химическая энциклопедия
Угольная кислота — Угольная кислота … Википедия
КИСЛОТЫ И ОСНОВАНИЯ — Термины кислоты и основания вполне сформировались в 17 в. Их содержание неоднократно пересматривалось и дополнялось. Этот процесс происходил и происходит в острых столкновениях представителей разных взглядов на природу К. и о. Развитие взглядов… … Химическая энциклопедия
Десорбционные методы ионизации в масс-спектрометрии — Десорбционные методы ионизации в масс спектрометрии группа методов ионизации в масс спектрометрии, для которых процессы десорбции твердого анализируемого вещества и его ионизации практически неотделимы во времени. Наиболее полное развитие… … Википедия
Уравнение Бренстеда — Уравнение Бренстеда уравнение, количественно описывающее зависимость скорости катализируемых кислотами или основаниями реакций от природы кислоты. Впервые предложено в 1924 г. Бренстедом и Педерсеном. Для кислотного катализа уравнение… … Википедия
dic.academic.ru
| α-Аминопропионовая (α-Аланин) | K1 | CH3CH(NH2)COOH | 1.35·10−10 | 9.87 | [1, c.249] |
| β-Аминопропионовая (β-Аланин) | K1 | NH2 | 5.89·10−11 | 10.23 | [1, c.249] |
| 8-Оксихинолин | K1 | C9H7ON | 1.26·10−10 | 9.90 | [1, c.249] |
| Адипиновая | K1 | HOOC(CH2)4COOH | 5.5·10−5 | 4.26 | [1, c.249] |
| K2 | 5.01·10−6 | 5.30 | |||
| Азотистая | K1 | HNO2 | 5.13·10−4 | 3.29 | [1, c.249] |
| K1 | HN3 | 1.91·10−5 | 4.72 | [1, c.249] | |
| Азотноватистая | K1 | H2N2O2 | 6.17·10−8 | 7.21 | [1, c.249] |
| K2 | 2.88·10−12 | 11.54 | |||
| Акриловая | K1 | CH2=CHCOOH | 5.5·10−5 | 4.26 | [1, c.249] |
| Аминоуксусная (Глицин) | K1 | NH2CH2COOH | 1.66·10−10 | 9.78 | [1, c.249] |
| Аскорбиновая | K1 | CH2(OH)CH(OH)CHC(OH)=C(OH)COO | 9.12·10−5 | 4.04 | [1, c.249] |
| K2 | 4.57·10−12 | 11.34 | |||
| Бензойная | K1 | C6H5COOH | 6.17·10−5 | 4.21 | [1, c.249] |
| Борная (орто-) К1 | K1 | H3BO3 | 5.75·10−10 | 9.24 | |
| Борная (тетра-) | K1 | H2B4O7 | 1.82·10−4 | 3.74 | [1, c.249] |
| K2 | 2·10−8 | 7.70 | |||
| Бромноватистая | K1 | HBrO | 2.51·10−9 | 8.60 | [1, c.249] |
| Валериановая (изо-) | K1 | (CH3)2CHCH2COOH | 1.66·10−5 | 4.78 | [1, c.249] |
| Валериановая (норм.) | K | CH3(CH2)3COOH | 1.38·10−5 | 4.86 | [1, c.249] |
| Ванадиевая (орто-) (К2, К3) | K2 | H3VO4 | 1.12·10−9 | 8.95 | [1, c.249] |
| K3 | 3.98·10−15 | 14.40 | |||
| Виннная | K1 | HOOCCH(OH)CH(OH)COOH | 9.12·10−4 | 3.04 | [1, c.249] |
| K2 | 4.27·10−5 | 4.37 | |||
| Вольфрамовая | K1 | H2WO4 | 6.31·10−5 | 4.20 | [1, c.249] |
| Галловая | K1 | C6H2(OH)3COOH | 3.89·10−5 | 4.41 | [1, c.249] |
| Германиевая | K1 | H4GeO4 | 1.66·10−9 | 8.78 | [1, c.249] |
| K2 | 2·10−13 | 12.70 | |||
| Гидросернистая (дитионистая) (К2) | K2 | H2S2O4 | 2.45 | [1, c.249] | |
| Гидрохинон | K1 | 1,4-C6H4(OH)2 | 1.1·10−10 | 9.96 | [1, c.249] |
| Гликолевая | K1 | CH2(OH)COOH | 1.32·10−4 | 3.88 | [1, c.249] |
| Глицериновая | K1 | CH2(OH)CH(OH)COOH | 3.02·10−4 | 3.52 | [1, c.249] |
| Глутаминовая | K1 | HOOC(CH2)2CH(NH2)COOH | 4.68·10−5 | 4.33 | [1, c.249] |
| K2 | 1.2·10−10 | 9.92 | |||
| Глутаровая | K1 | HOOC(CH2)3COOH | 4.57·10−5 | 4.34 | [1, c.249] |
| K2 | 5.37·10−6 | 5.27 | |||
| Глюконовая | K1 | CH2OH(CHOH)4COOH | 1.38·10−4 | 3.86 | [1, c.249] |
| Двумолибденовая | K1 | H2Mo2O7 | 9.55·10−6 | 5.02 | [1, c.249] |
| Двухромовая (К2) | K2 | H2Cr2O7 | 2.29·10−2 | 1.64 | [1, c.249] |
| Дитионовая | K1 | H2S2O6 | 1.58·10−0 | 0.20 | [1, c.249] |
| K2 | 3.98·10−4 | 3.40 | |||
| Дихлоруксусная | K1 | CHCl2COOH | 5.01·10−2 | 1.30 | [1, c.249] |
| Железистосинеродистая (К3, К4) | K3 | H4Fe(CN)6 | 2.69·10−3 | 2.57 | [1, c.249] |
| K4 | 4.47·10−5 | 4.35 | |||
| Иодная | K1 | HIO4; H5IO6 | 2.82·10−2 | 1.55 | [1, c.249] |
| K2 | 5.37·10−9 | 8.27 | |||
| K3 | 1.05·10−15 | 14.98 | |||
| Иодноватая | K1 | HIO3 | 6.17·10−0 | 0.79 | [1, c.249] |
| Иодноватистая | K1 | HIO | 2.29·10−11 | 10.64 | [1, c.249] |
| Кислотный хром черный специальный | K1 | 5.01·10−7 | 6.30 | [1, c.249] | |
| K2 | 2.82·10−12 | 11.55 | |||
| Коричная (транс-) | K1 | C6H5CH=CHCOOH | 3.72·10−5 | 4.43 | [1, c.249] |
| Коричная (цис-) | K1 | C6H5CH=CHCOOH | 1.32·10−4 | 3.88 | [1, c.249] |
| Кремневая (орто ) | K1 | H4SiO4 | 1.26·10−10 | 9.90 | [1, c.249] |
| K2 | 1.58·10−12 | 11.80 | |||
| K3 | 2·10−14 | 13.70 | |||
| Лимонная | K1 | HOOCCH2C(OH)(COOH)CH2COOH | 7.41·10−4 | 3.13 | [1, c.249] |
| K2 | 1.74·10−5 | 4.76 | |||
| K3 | 3.98·10−7 | 6.40 | |||
| м-Крезол | K1 | CH3C6H4OH | 9.77·10−11 | 10.01 | [1, c.249] |
| м-Нитробензойная | K1 | NO2C6H4COOH | 3.55·10−4 | 3.45 | [1, c.249] |
| м-Фталевая | K1 | C6H4(COOH)2 | 2·10−4 | 3.70 | [1, c.249] |
| K2 | 2.51·10−5 | 4.60 | |||
| Малеиновая | K1 | HOOCCH=CHCOOH | 1.2·10−2 | 1.92 | [1, c.249] |
| K2 | 5.89·10−7 | 6.23 | |||
| Малоновая | K1 | HOOCCH2COOH | 1.41·10−3 | 2.85 | [1, c.249] |
| K2 | 2·10−6 | 5.70 | |||
| Марганцовистая | K1 | H2MnO4 | 10·10−0 | 1.00 | [1, c.249] |
| K2 | 7.08·10−11 | 10.15 | |||
| Масляная (изо) | K1 | (CH3)2CHCOOH | 1.38·10−5 | 4.86 | [1, c.249] |
| Масляная (норм.) | K1 | CH3CH2CH2COOH | 1.51·10−5 | 4.82 | [1, c.249] |
| Миндальная | K1 | C6H6CH(OH)COOH | 3.89·10−4 | 3.41 | [1, c.249] |
| Молибденовая | K1 | H2MoO4 | 2.88·10−3 | 2.54 | [1, c.249] |
| K2 | 1.38·10−4 | 3.86 | |||
| Молочная | K1 | CH3CH(OH)COOH | 1.38·10−4 | 3.86 | [1, c.249] |
| Муравьиная | K1 | HCOOH | 1.78·10−4 | 3.75 | [1, c.249] |
| Мышьяковая | K1 | H3AsO4 | 6.03·10−3 | 2.22 | [1, c.249] |
| K2 | 1.05·10−7 | 6.98 | |||
| K3 | 2.95·10−12 | 11.53 | |||
| Мышьяковистая | K1 | H3AsO3 | 5.13·10−10 | 9.29 | [1, c.249] |
| Надперекись водорода | K1 | HO2 | 6.31·10−3 | 2.20 | [1, c.249] |
| о-Крезол | K1 | CH3C6H4OH | 6.31·10−11 | 10.20 | [1, c.249] |
| о-Нитробензойная | K1 | NO2C6H4COOH | 6.76·10−3 | 2.17 | [1, c.249] |
| о-Фталевая | K1 | C6H4(COOH)2 | 1.12·10−3 | 2.95 | [1, c.249] |
| K2 | 3.98·10−6 | 5.40 | |||
| п-Крезол | K1 | CH3C6H4OH | 6.76·10−11 | 10.17 | [1, c.249] |
| п-Нитробензойная | K1 | NO2C6H4COOH | 3.63·10−4 | 3.44 | [1, c.249] |
| п-Фталевая | K1 | C6H4(COOH)2 | 2.88·10−4 | 3.54 | [1, c.249] |
| K2 | 3.47·10−5 | 4.46 | |||
| Перикись водорода | K1 | H2O2 | 2·10−12 | 11.70 | [1, c.249] |
| Пикриновая (тринитрофенол) | K1 | HOC6H2(NO2)3 | 1.95·10−0 | 0.29 | [1, c.249] |
| Пирокатехин (К1) | K1 | 1,2-C6H4(OH)2 | 3.55·10−10 | 9.45 | [1, c.249] |
| Пропионовая | K1 | CH3CH2COOH | 1.35·10−5 | 4.87 | [1, c.249] |
| Резорцин | K1 | 1,3-C8H4(OH)2 | 3.63·10−10 | 9.44 | [1, c.249] |
| Роданистоводородная | K1 | HSCN | 7.08·10−0 | 0.85 | [1, c.249] |
| Салициловая | K1 | C6H4(OH)COOH | 1.07·10−3 | 2.97 | [1, c.249] |
| Себациновая | K1 | HOOC(CH2)8COOH | 3.98·10−5 | 4.40 | [1, c.249] |
| K2 | 6.03·10−6 | 5.22 | |||
| Селенистая | K1 | H2SeO3 | 2.4·10−3 | 2.62 | [1, c.249] |
| K2 | 4.79·10−9 | 8.32 | |||
| Селенистоводородная | K1 | H2Se | 1.29·10−4 | 3.89 | [1, c.249] |
| K2 | 1·10−11 | 11.00 | |||
| Селеновая (К2) | K2 | H2SeO4 | 1.32·10−2 | 1.88 | [1, c.249] |
| Серная (K2) | K2 | H2SO4 | 1.15·10−2 | 1.94 | [1, c.249] |
| Сернистая | K1 | H2SO3 | 1.74·10−2 | 1.76 | [1, c.249] |
| K2 | 6.31·10−8 | 7.20 | |||
| Сероводородная | K1 | H2S | 1.02·10−7 | 6.99 | [1, c.249] |
| K2 | 1.29·10−13 | 12.89 | |||
| Синильная | K1 | HCN | 6.17·10−10 | 9.21 | [1, c.249] |
| Сульфаминовая | K1 | H2NSO3H | 9.55·10−0 | 0.98 | [1, c.249] |
| Сульфаниловая | K1 | H2NC6H4SO3H | 6.31·10−4 | 3.20 | [1, c.249] |
| Сульфосалициловая (К2, К3) | K2 | C6H3(OH)(COOH)SO3H | 1.38·10−3 | 2.86 | [1, c.249] |
| K3 | 1.82·10−12 | 11.74 | |||
| Сурьмяная | K1 | H[Sb(OH)6] | 3.98·10−5 | 4.40 | [1, c.249] |
| Теллуристая | K1 | H2TeO3 | 2.69·10−3 | 2.57 | [1, c.249] |
| K2 | 1.82·10−8 | 7.74 | |||
| Теллуристоводородная | K1 | H2Te | 2.29·10−3 | 2.64 | [1, c.249] |
| K2 | 1·10−11 | 11.00 | |||
| Теллуровая | K1 | H6TeO6 | 2·10−8 | 7.70 | [1, c.249] |
| K2 | 1.12·10−11 | 10.95 | |||
| K3 | 1·10−15 | 15.00 | |||
| Тиосерная | K1 | H2S2O3 | 3.98·10−0 | 0.60 | [1, c.249] |
| K2 | 1.91·10−2 | 1.72 | |||
| Трихлоруксусная | K1 | CCl3COOH | 5.01·10−0 | 0.70 | [1, c.249] |
| Угольная | K1 | CO2(aq.)+H2O | 4.47·10−7 | 6.35 | [1, c.249] |
| K2 | 4.79·10−11 | 10.32 | |||
| Уксусная | K1 | CH3COOH | 1.74·10−5 | 4.76 | [1, c.249] |
| Фенол | K1 | C6H5OH | 1·10−10 | 10.00 | [1, c.249] |
| Фосфористая | K1 | H3PO3 | 1.58·10−2 | 1.80 | [1, c.249] |
| K2 | 2·10−7 | 6.70 | |||
| Фосфорная (орто) | K1 | H3PO4 | 7.59·10−3 | 2.12 | [1, c.249] |
| K2 | 6.17·10−8 | 7.21 | |||
| K3 | 4.17·10−13 | 12.38 | |||
| Фосфорная (пиро) | K1 | H4P2O7 | 3.02·10−2 | 1.52 | [1, c.249] |
| K2 | 2.29·10−3 | 2.64 | |||
| K3 | 2·10−7 | 6.70 | |||
| K4 | 4.27·10−10 | 9.37 | |||
| Фосфорноватая | K1 | H4P2O6 | 6.31·10−3 | 2.20 | [1, c.249] |
| K2 | 1.55·10−3 | 2.81 | |||
| K3 | 5.37·10−8 | 7.27 | |||
| K4 | 9.33·10−11 | 10.03 | |||
| Фосфорноватистая | K1 | H3PO2 | 5.89·10−2 | 1.23 | [1, c.249] |
| Фтористоводородная | K1 | HF | 6.76·10−4 | 3.17 | [1, c.249] |
| Фторофосфорная | K1 | H2[PO3F] | 3.55·10−0 | 0.55 | [1, c.249] |
| K2 | 1.58·10−5 | 4.80 | |||
| Фумаровая | K1 | HOOCHC=CHCOOH | 9.33·10−4 | 3.03 | [1, c.249] |
| K2 | 4.17·10−5 | 4.38 | |||
| Хлористая | K1 | HClO2 | 1.07·10−2 | 1.97 | [1, c.249] |
| Хлорноватистая | K1 | HClO | 5.01·10−8 | 7.30 | [1, c.249] |
| Хлоруксусная | K1 | CH2ClCOOH | 1.38·10−3 | 2.86 | [1, c.249] |
| Хромовая | K1 | H2CrO4 | 9.55·10−0 | 0.98 | [1, c.249] |
| K2 | 3.16·10−7 | 6.50 | |||
| Хромотроповая | K1 | C10H6(OH)2(SO3H)2 | 4.37·10−6 | 5.36 | [1, c.249] |
| K2 | 2.51·10−16 | 15.60 | |||
| Циановая | K1 | HCNO | 3.47·10−4 | 3.46 | [1, c.249] |
| Щавелевая | K1 | H2C2O4 | 5.62·10−2 | 1.25 | [1, c.249] |
| K2 | 5.37·10−5 | 4.27 | |||
| Этилендиаминтетрауксусная | K1 | (HOOCCH2)2NCH2-CH2N(CH2COOH)2 | 1.02·10−2 | 1.99 | [1, c.249] |
| K2 | 2.14·10−3 | 2.67 | |||
| K3 | 5.37·10−7 | 6.27 | |||
| K4 | 1.12·10−11 | 10.95 | |||
| Яблочная | K1 | HOOCCH(OH)CH2COOH | 3.47·10−4 | 3.46 | [1, c.249] |
| K2 | 8.91·10−6 | 5.05 | |||
| Янтарная | K1 | HOOCCH2CH2COOH | 6.17·10−5 | 4.21 | [1, c.249] |
| K2 | 2.34·10−6 | 5.63 |
chemequ.ru
Константы диссоциации кислот и оснований неорганических (Таблица)
Справочная таблица константы диссоциации кислот и оснований по общей и неорганической химии содержит следующую информацию: название и формула гидрооксида и кислоты и соответствующие им константы диссоциации . Таблица содержит справочный материал, необходимый для решения задач по общей и неорганической химии. Предназначено для школьников и студентов.
К – константа диссоциации кислот и оснований
pK – величина, которая определяется как отрицательный десятичный логарифм константы диссоциации (часто используется вместо константы).
Смотрите также таблицу “константы кислотности сопряженных пар”.
Константы диссоциации неорганических оснований (таблица)
Гидроксид | Формула вещества | Константы диссоциации, Кв | рКв |
Алюминия | Al(OH)3 | 1,38 · 10-9 | 8,86 |
Аммония | NH4OH | 1,79 · 10-5 | 4,75 |
Бария | Ba(OH)2 | 2,30 · 10-1 | 0,64 |
Галлия | Ga(OH)3 | 1,60 · 10-11 (2) | 10,8 |
Железа (2) | Fe(OH)2 | 1,30 · 10-4 | 3,89 |
Железа (3)
| Fe(OH)3
| 1,82 · 10-11 (2) | 10,74 |
1,35 · 10-12 (3) | 11,87 | ||
Кадмия | Cd(OH)2 | 5,00 · 10-3 (2) | 2,30 |
Кальция | Ca(OH)2 | 4,30 · 10-2 (2) | 1,37 |
Кобальта (2) | Co(OH)2 | 4,00 · 10-5 (2) | 4,40 |
Лантана | La(OH)2 | 5,20 · 10-4 (3) | 3,30 |
Лития | LiOH | 6,75 · 10-1 | 0,17 |
Магния | Mg(OH)2 | 2,50 · 10-3 (2) | 2,60 |
Марганца (2) | Mn(OH)2 | 5,00 · 10-4 (2) | 3,30 |
Меди (2) | Cu(OH)2 | 3,40 · 10-7 (2) | 6,47 |
Натрия | NaOH | 5,90 | -0,77 |
Никеля | Ni(OH)2 | 2,50 · 10-5 (2) | 4,60 |
Свинца | Pb(OH)2 | 9,60 · 10-4 (1) | 3,02 |
Стронция | Sr(OH)2 | 1,50 · 10-1 (2) | 0,82 |
Хрома (3) | Cr(OH)3 | 1,02 · 10-10 (3) | 9,90 |
Цинка | Zn(OH)2 | 4,00 · 10-5 (2) | 4,40 |
Константы диссоциации неорганических кислот (таблица)
Кислота | Формула вещества | Константа диссоциации, Ка | рКа |
Азотистая | HNO2 | 4,00 · 10-4 | 3,4 |
Азотистоводородная | HN3 | 2,60 · 10-5 |
|
Азотная | HNO3 | 4,36 · 10 | -1,64 |
Алюминиевая (мета) | HAlO2 | 4,00 · 10-13 | 12,4 |
Борная (мета) | HBO2 | 7,50 · 10-10 | 9,12 |
Борная (орто)
| H3BO3
| 5,80 · 10-10(1) | 9,24 |
1,80 · 10-13(2) | 12,74 | ||
1,60 · 10-14(3) | 13,80 | ||
Борная (тетра)
| H2B4O7
| ~10-4(1) | ~4 |
~10-9(2) | ~9 | ||
Бромоводородная | HBr | 1,00 · 109 | -9 |
Бромноватая | HBrO3 | 2,00 · 10-1 | 0,7 |
Бромноватистая | HBrO | 2,06 · 10-9 | 8,7 |
Вода | Н2О | 1,8 · 10-16 |
|
Водорода пероксид | H2O2 | 2,63 · 10-12(1) | 11,58 |
Галлиевая
| H3GaO3
| 5,00 · 10-11(2) | 10,3 |
2,00 · 10-12(3) | 11,7 | ||
Германиевая | H2GeO3 | 1,70 · 10-9(1) | 8,77 |
Иодоводородная | HI | 1,00 · Ю11 | -11 |
Иодная (мета) | HIO4 | 2,30 · 10-2 | 1,64 |
Иодная (орто)
| H5IO6
| 3,09 · 10-2(1) | 1,51 |
7,08 · 10-9(2) | 8.15 | ||
2,50 · 10-13(3) | 12,60 | ||
Иодноватая | HIO3 | 1,70 · 10-1 | 0,77 |
Кремневая (мета) | H2SiO3 | 2,20 · 10-10(1) | 9,66 |
Кремневая (орто)
| H4SiO4
| 2,00 · 10-10(1) | 9,7 |
2,00 · 10-12(2) | 11,7 | ||
1,00 · 10-12(3) | 12,0 | ||
1,00 · 10-12(4) | 12,0 | ||
Марганцовая | HMnO4 | 2,00 · 102 | -2,3 |
Молибденовая | H2MoO4 | 1,00 · 10-6(2) | 6,0 |
Мышьяковая (орто)
| H3ASO4
| 5,89 · 10-3(1) | 2,22 |
1,05 · 10-7(2) | 6,98 | ||
3,89 · 10-12(3) | 11,41 | ||
Мышьяковистая (мета) | HASO2 | 6,00 · 10-10 | 9,2 |
Мышьяковистая (орто)
| H3ASO3
| 6,00 · 10-10(1) | 9,2 |
1,70 · 10-14(2) | 13,77 | ||
Оловянистая | H2SnO2 | 6,00 · 10-18 | 17,2 |
Оловянная | H2SnO3 | 4,00 · 10-10 | 9,4 |
Роданистоводородная | HCNS | 1,40 · 10-1 |
|
Свинцовистая | H2PbO2 | 2,00 · 10-16 | 15,7 |
Селенистая
| H2SeO3
| 3,50 · 10-3(1) | 2,46 |
5,00 · 10-8(2) | 7,3 | ||
Селеновая
| H2SeO4
| 1,00 · 103(1) | -3 |
1,20 · 10-2(2) | 1,9 | ||
Селеноводородная
| H2Se
| 1,70 · 10-4(1) | 3,77 |
1,00 · 10-11(2) | 11,0 | ||
Серная
| H2SO4
| 1,00 · 103(1) | -3 |
1,20 · 10-2(2) | 1,9 | ||
Сернистая
| H2SO3
| 1,58 · 10-2(1) | 1,8 |
6,31 · 10-8(2) | 7,2 | ||
Сероводородная
| H2S | 6,00 · 10-8(1) | 7,2 |
1,00 · 10-14(2) | 14 | ||
Сурьмяная(орто) | H3SbO4 | 4,00 · 10-5 | 4,4 |
Сурьмянистая (мета) | HSbO2 | 1,00 · 10-11 | 11 |
Теллуристая
| H2TeO3
| 3,00 · 10-3(1) | 2,5 |
2,00 · 10-8(2) | 7,7 | ||
Теллуровая
| H2TeO4
| 2,29 · 10-8(1) | 7,64 |
6,46 · 10-12(2) | 11,19 | ||
Теллуроводородная | H2Te | 1,00 · 10-3 | 3,0 |
Тиосерная
| H2S2O3
| 2,20 · 10-1(1) | 0,66 |
2,80 · 10-2(2) | 1,56 | ||
Угольная
| H2CO3
| 4,45 · 10-7(1) | 6,35 |
4,69 · 10-11(2) | 10,33 | ||
Фосфористая (орто)
| H3PO3
| 1,60 · 10-3(1) | 1,8 |
6,30 · 10-7(2) | 6,2 | ||
Фосфорная (орто)
| H3PO4
| 7,52 · 10-3(1) | 2,12 |
6,31 · 10-8(2) | 7,20 | ||
1,26 · 10-12(3) | 11,9 | ||
Фосфорная (пиро)
| H4P2O7
| 1,40 · 10-1(1) | 0,85 |
1,10 · 10-2(2) | 1,95 | ||
2,10 · 10-7(3) | 6,68 | ||
Фтороводородная | HF | 6,61 · 10-4 | 3,18 |
Хлороводородная | HCl | 1 · 107 | -7 |
Хлорноватистая | HClO | 5,01 · 10-8 | 7,3 |
Хромовая
| H2CrO4
| 1 · 10 (1) | -1 |
3,16 · 10-7 | 6,5 | ||
Циановодородная | HCN | 7,90 · 10-10 | 9,1 |
_______________
Источник информации: Справочные таблицы по общей и неорганической химии / Учебное пособие. Новосибирск, 2008
infotables.ru
3.5. Общие принципы расчёта состава равновесных систем
Для удобства многие константы равновесия разных типов имеют свои обозначения, например, Ka – константа кислотности, KSH – константа автопротолиза растворителя, KS – произведение растворимости.
Некоторые из равновесий, используемые в аналитической химии (протолитические равновесия с участием многоосновных кислот и многокислотных оснований, процессы комплексообразования), протекают ступенчато. Константы равновесия, характеризующие каждую ступень, называются ступенчатыми. Произведение ступенчатых констант называетсяобщей константой равновесия. Общая константа не описывает реально существующего равновесия, но более удобна для расчётов. Например:
1 ступень Ag+ + Nh4 î [Ag(Nh4)]+
2 ступень [Ag(Nh4)]+ + Nh4 î [Ag(Nh4)2]+
K1 | = | [Ag(Nh4 )+ ] |
|
| K 2 | = |
| [Ag(Nh4 )2 | + ] | ||||
|
|
|
|
|
|
|
|
|
| ||||
[Ag+ ][Nh4 ] |
| [Ag(Nh4 )+ ][Nh4 ] | |||||||||||
|
|
|
|
|
| ||||||||
|
|
| β2= K1K 2 | = |
| [Ag(Nh4 )2 | + ] |
|
| ||||
|
|
| [Ag+ ][Nh4 | ]2 |
|
| |||||||
|
|
|
|
|
|
|
| ||||||
Часто вместо значений констант равновесия используют их десятичные логарифмы (если константа очень большая) или отрицательные десятичные логарифмы (если она, наоборот, значительно меньше единицы). Отрицательный десятичный логарифм константы равновесия называется показателем даннойконстанты (рК).
Для определения состава равновесной смеси при определённых условиях используют концентрационные константы равновесия, а также уравнения материального баланса и электронейтральности.
Уравнение материального баланса основано на том, что чис-
ло атомов определённого элемента (или групп атомов определённого вида) в изолированной системе остаётся неизменным.
Например, для раствора, содержащего частицы Ag+, Nh4, Nh5+, Ag(Nh4)+ и Ag(Nh4)2+:
CAg =[Ag+ ]+[Ag(Nh4 )+ ]+[Ag(Nh4 )+2 ]
studfiles.net
Константы диссоциации Кa и константы кислотности pКa=-lg(Кa) неорганических кислот в водных растворах
Источник: Новый справочник химика и технолога. Химическое равновесие. Свойства растворов. — СПб.: АНО НПО «Профессионал», 2004. — 998 с. |
tehtab.ru
Органическая химия (конспект лекций): Учебное пособие, страница 7
Силу кислоты выражают количественно через константу кислотности:
Ka = | Kp[H2O] = | [A–][H3O+] |
[AH] |
где: Ka – константа кислотности; Kp – константа равновесия.
Кислота там сильнее, чем больше константа кислотности. Часто пользуются значениями рКа. Чем меньше величина рКа, тем сильнее кислота.
рКа = –lgКа
Например, рКа фенола = 10, рКа этанола = 16. Это означает, что фенол на шесть порядков (в миллион раз) более сильная кислота, чем этиловый спирт.
Основность может быть выражена через рКb.
рКb = 14 – рКa
Важно помнить, что рКа воды = 15,7. Все вещества, которые имеют рКа больше, чем вода, не способны проявлять кислые свойства в водных растворах. Вода, как более сильная кислота, подавляет диссоциацию более слабых кислот. Так как у большинства органических соединений кислотные свойства выражены во много раз слабее, чем у воды, разработан полярографический подход к оценке их кислотности (И.П. Белецкая и др.). Он позволяет оценивать кислотность до рКа = 50, хотя для очень слабых кислот значения рКа можно оценить только очень приблизительные.
Чрезвычайно важна качественная оценка кислотности как в рядах близких по строению веществ, так и для соединений различных классов. Способность кислоты отдавать протон связана со стабильностью образующегося аниона. Чем стабильнее образующийся анион, тем меньше его стремление захватить протон обратно и превратиться в нейтральную молекулу. При оценке относительной стабильности аниона надо учитывать несколько факторов.
Природа атома, отдающего протон. Атом тем легче теряет протон, чем выше его электроотрицательность и поляризуемость. Поэтому в ряду кислот способность к диссоциации уменьшается следующим образом:
S-H > O-H > –N-H > C-H
Этот ряд прекрасно соответствует свойствам атомов, известным из периодической таблицы.
Влияние окружения. Если сравниваются близкие по строению вещества, оценка проводится сравнением электронной плотности на атоме, отдавшем протон. Все структурные факторы, способствующие уменьшению заряду, стабилизирует анион, а увеличению заряда – дестабилизируют. Таким образом, все акцепторы увеличивают кислотность, все доноры – уменьшают.
Это происходит независимо от того, за счет какого эффекта передачи электронов (индуктивного или мезомерного) происходит перераспределение электронной плотности.
Сольватационный эффект. Сольватация (взаимодействие с молекулами растворителя) повышает стабильность аниона за счет перераспределения избытка электронной плотности между анионом и молекулами растворителя. В общем случае закономерность следующая:
· чем полярнее растворитель, тем сильнее сольватация;
· чем меньше ион, тем лучше он сольватируется.
Основность по Брёнстеду – способность вещества предоставить свою пару электронов для взаимодействия с протоном. Как правило, это вещества, содержащие в молекуле атомы азота, кислорода и серы.
Чем слабее основный центр удерживает пару электронов, тем выше основность. В ряду
R3–N > R2O > R2S
основность уменьшается. Эту последовательность легко запомнить, используя мнемоническое правило “NOS”.
Среди оснований Брёнстеда существует зависимость: анионы более сильные основания, чем соответствующие нейтральные молекулы. Например, гидроксид-анион (–ОН) более сильное основание, чем вода (Н2О). При взаимодействии основания с протоном могут образовываться ониевые катионы:
· R3О+ – оксониевый катион;
· NR4+ – аммониевый катион;
· R3S+ – сульфониевый катион.
Качественная оценка основности у близких по строению веществ проводится с использованием той же логики, что и оценка кислотности, но с обратным знаком.
Поэтому все акцепторные заместители основностьи уменьшают, все донорные – увеличивают.
Кислоты и основания по Льюису
Основания по Льюису – доноры электронной пары, как и основания по Брёнстеду.
Определение Льюиса для кислот заметно отличается от привычного (по Брёнстеду). Кислотой по Льюису считается любая молекула или ион, имеющая свободную орбиталь, которая может быть в результате взаимодействия заполнена электронной парой. Если по Брёнстеду кислота – донор протона, то по Льюису сам протон (Н+) – кислота, поскольку его орбиталь пуста. Кислот Льюиса очень много: Na+, Mg2+, SnCl4, SbCl5, AlCl3, BF3, FeBr3 и т.д. Теория Льюиса позволяет описать многие реакции как кислотно-основные взаимодействия. Например:
Часто в реакциях с кислотами Льюиса в качестве оснований участвуют органические соединения, являющиеся донорами пары p-электронов:
В органической химии принято следующее:
· если используется термин «кислота» – подразумевается кислота по Брёнстеду;
· если используют термин «кислота» в льюисовском понимании – говорят «кислота Льюиса».
Лекция № 5
Углеводороды
Алканы
· Гомологический ряд, номенклатура, изомерия, алкильные радикалы. Электронное строение молекул алканов, sp3-гибридизация, s-связь. Длины C-C и C-H связей, валентные углы, энергии связей. Пространственная изомерия органических веществ. Способы изображения пространственного строения молекул с sp3-гибридизованными атомами углерода. Спектральные характеристики алканов. Физические свойства алканов и закономерности их изменения в гомологическом ряду.
Алканы (насыщенные ациклические соединения, парафины)
Алканы – углеводороды с открытой цепью атомов, отвечающие формуле СnH2n+2, где атомы углерода связаны между собой только σ-связями.
Термин «насыщенный» означает, что каждый углерод в молекуле такого вещества связан с максимально возможным числом атомов (с четырьмя атомами).
Строение метана подробно изложено в лекции № 2.
Изомерия, номенклатура
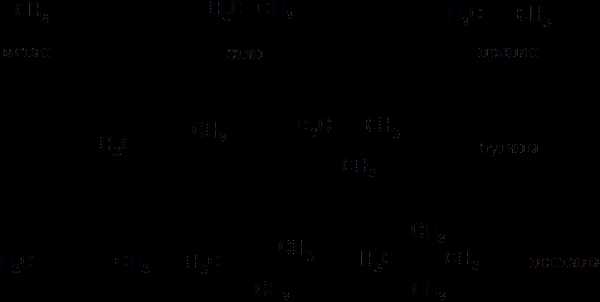
Три первых члена гомологического ряда (метан, этан и пропан) существуют в виде одного структурного изомера. Начиная с бутана число изомеров стремительно растет: у пентана три изомера, а у декана (С10Н22) их уже 75.
Конформационная изомерия
vunivere.ru
Константа кислотности — Циклопедия
Расчет реальной константы кислотности. Разбор задачи по аналитической химии для студентов 1 курса биофака МГУКонстанта кислотности — константа равновесия реакции диссоциации кислоты на ион водорода и анион кислотного остатка.
Константу кислотности можно определить экспериментально по измерению электрической проводимости раствора. Многоосновные кислоты ионизируются ступенчато, и каждая ступень кислотности характеризуется своим значением константы кислотности.
Обычно вместо самой константы кислотности К используют величину pK, которая определяется как отрицательный десятичный логарифм самой константы:
- [math]pK_a = {−\lg K_a}[/math].
Для слабых кислот значения рК положительны, и чем слабее кислота, тем больше рК. Для сильных кислот рК отрицательны.
Очевидно, что чем сильнее кислота, тем меньше константа кислотности. Так, HbrO (очень слабая кислота) имеет рК 8,7, H2SO4 как очень сильная кислота имеет рК −3, HMnO4 имеет рК −2,3.
[править] Сила кислородсодержащих кислот
Сила кислородсодержащих кислот зависит от строения молекулы. Формулу кислородсодержащих кислот в общем виде можно записать ЭОm(ОН)n. Сила кислот практически не зависит от числа групп ОН, но возрастает с увеличением m, так как увеличивается степень окисления центрального атома Э. В этом проявляется общая закономерность: с увеличением степени окисления элемента в ряду его гидроксидов основные свойства ослабевают, а кислотные — усиливаются.
Для оснований имеется аналогичная константа основности.
cyclowiki.org
