Вопрос 22. Современные представления о строении атома
Атом – это мельчайшая, химически неделимая частица. В настоящее время известно более 110 химических элементов (видов атомов). Согласно современным представлениям атомы имеют сложное строение. Они состоят из ядра и электронов. Ядро почти в 2000 раз тяжелее атома. Но при этом оно примерно в 50000 раз меньше атома. Если мысленно увеличить масштаб и представить, что ядро атома имеет диаметр 2 см, тогда радиус атома составил бы приблизительно 500 м. Как выяснили ученые, ядро тоже имеет сложное строение. Оно состоит, главным образом, из двух видов частиц протонов и нейтронов.
Планетарная модель атома Бора-Резерфорда. В 1911 году Эрнест Резерфорд, проделав ряд экспериментов, пришёл к выводу, что атом представляет собой подобие планетной системы, в которой электроны движутся по орбитам вокруг расположенного в центре атома тяжёлого положительно заряженного ядра («модель атома Резерфорда»). Однако такое описание атома вошло в противоречие с классической электродинамикой. Дело в том, что, согласно классической электродинамике, электрон при движении с центростремительным ускорением должен излучать электромагнитные волны, а, следовательно, терять энергию. Расчёты показывали, что время, за которое электрон в таком атоме упадёт на ядро, совершенно ничтожно. Для объяснения стабильности атомов Нильсу Бору пришлось ввести постулаты, которые сводились к тому, что электрон в атоме, находясь в некоторых специальных энергетических состояниях, не излучает энергию («модель атома Бора-Резерфорда»). Постулаты Бора показали, что для описания атома классическая механика неприменима. Дальнейшее изучение излучения атома привело к созданию квантовой механики, которая позволила объяснить подавляющее большинство наблюдаемых фактов. Современная модель атома является развитием планетарной модели. Согласно этой модели, ядро атома состоит из положительно заряженных протонов и не имеющих заряда нейтронов и окружено отрицательно заряженными электронами. Однако представления квантовой механики не позволяют считать, что электроны движутся вокруг ядра по сколько-нибудь определённым траекториям (неопределённость координаты электрона в атоме может быть сравнима с размерами самого атома).
Химические свойства атомов определяются конфигурацией электронной оболочки и описываются квантовой механикой. Положение атома в таблице Менделеева определяется электрическим зарядом его ядра (то есть количеством протонов), в то время как количество нейтронов принципиально не влияет на химические свойства; при этом нейтронов в ядре, как правило, больше, чем протонов (см.: атомное ядро). Если атом находится в нейтральном состоянии, то количество электронов в нём равно количеству протонов. Основная масса атома сосредоточена в ядре, а массовая доля электронов в общей массе атома незначительна (несколько сотых процента массы ядра). Хотя слово атом в первоначальном значении обозначало частицу, которая не делится на меньшие части, согласно научным представлениям он состоит из более мелких частиц, называемых субатомными частицами. Атом состоит из электронов, протонов, все атомы, кроме водорода-1, содержат также нейтроны. Электрон является самой лёгкой из составляющих атом частиц с массой 9,11×10−31 кг, отрицательным зарядом и размером, слишком малым для измерения современными методами. Протоны обладают положительным зарядом и в 1836 раз тяжелее электрона (1,6726×10−27 кг). Нейтроны не обладают электрическим зарядом и в 1839 раз тяжелее электрона (1,6929×10−27 кг). При этом масса ядра меньше суммы масс составляющих её протонов и нейтронов из-за эффекта дефекта массы. Нейтроны и протоны имеют сравнимый размер, около 2,5×10−15 м, хотя размеры этих частиц определены плохо. В стандартной модели элементарных частиц как протоны, так и нейтроны состоят из элементарных частиц, называемых кварками. Наряду с лептонами, кварки являются одной из основных составляющих материи. И первые и вторые являются фермионами. Существует шесть типов кварков, каждый из которых имеет дробный электрический заряд, равный +2⁄3 или −1⁄3 элементарного. Протоны состоят из двух u-кварков и одного d-кварка, а нейтрон — из одного u-кварка и двух d-кварков. Это различие объясняет разницу в массах и зарядах протона и нейтрона. Кварки связаны между собой сильными ядерными взаимодействиями, которые передаются глюонами. При описании электронов в атоме в рамках квантовой механики, обычно рассматривают распределение вероятности в 3n-мерном пространстве для системы n электронов. Электроны в атоме притягиваются к ядру, между электронами также действует кулоновское взаимодействие. Эти же силы удерживают электроны внутри потенциального барьера, окружающего ядро. Для того, чтобы электрон смог преодолеть притяжение ядра, ему необходимо получить энергию от внешнего источника. Чем ближе электрон находится к ядру, тем больше энергии для этого необходимо.
Электронам, как и другим частицам, свойственен корпускулярно-волновой дуализм. Иногда говорят, что электрон движется по орбитали, что неверно. Состояние электронов описывается волновой функцией, квадрат модуля которой характеризует плотность вероятности нахождения частиц в данной точке пространства в данный момент времени, или, в общем случае, оператором плотности. Существует дискретный набор атомных орбиталей, которым соответствуют стационарные чистые состояния электронов в атоме. Каждой орбитали соответствует свой уровень энергии. Электрон может перейти на уровень с большей энергией, поглотив фотон. При этом он окажется в новом квантовом состоянии с большей энергией. Аналогично, он может перейти на уровень с меньшей энергией, излучив фотон. Энергия фотона при этом будет равна разности энергий электрона на этих уровнях
studfiles.net
8 Современные представления о строении атома
Атомы классифицируются по количеству протонов и нейтронов в ядре: количество протонов определяет принадлежность атома некоторому химическому элементу, а число нейтронов — изотопу этого элемента.
Принцип Паули
Принцип
Паули можно сформулировать следующим
образом: в пределах одной квантовой
системы в данном квантовом состоянии
может находиться только одна частица,
состояние другой должно отличаться
хотя бы одним
Гипотеза де Бройля
Луи де Бройль выдвинул гипотезу, что дуализм не является особенностью только оптических явлений, а имеет универсальный характер. Частицы вещества также обладают волновыми свойствами.
Волны, связанные с любыми микрочастицами и отражающие их волновую природу.
Принцип Бора
Принцип дополнительности — один из важнейших принципов квантовой механики, сформулированный в 1927 году Нильсом Бором. Согласно этому принципу, для полного описания квантовомеханических явлений необходимо применять два взаимоисключающих («дополнительных») набора классических понятий, совокупность которых даёт исчерпывающую информацию об этих явлениях как о целостных. Например, дополнительными в квантовой механике являются пространственно-временная и энергетически-импульсная картины.
9 Материя не может существовать вне движения, она всегда находится в состоянии движения, изменения и развития. При уничтожении движения объект прекращает свое существование, переходит в другие объекты, которым характерно движение покоя – состояния движений, обеспечивающих стабильность предмета, сохраняя его качества. Покой относителен, а движение абсолютно – это неотъемлемое свойство материи.
Материя не существует без движения, так же как движение не существует без материи.
Движение материи – постоянное ее взаимодействие, а также изменения состояния объектов, вызванные этими взаимодействиями. Формы движения материи различны. Пример формы движения материи: нагревание и охлаждение тел, излучение света, электрический ток, химические и физические превращения, жизненные процессы. Классификация форм движения материи :
1) неживая природа;
2) живая природа;
3) общество.
10 Механика. Законы движения Ньютона. Абсолютное пространство и время
МЕХАНИКА – область физики, изучающая движение материальных тел и взаимодействие между ними. Движением в механике называют изменение во времени взаимного положения тел или их частей в пространстве.
Законы движения Ньютона
1, Закон инерции.( Инерция — это явление сохранения телом скорости движения (и по величине, и по направлению), когда на тело не действуют никакие силы. Чтобы изменить скорость движения тела, на него необходимо подействовать с некоторой силой. Естественно, результат действия одинаковых по величине сил на различные тела будет различным. Таким образом, говорят, что тела обладают инертностью. Инертность — это свойство тел сопротивляться изменению их текущего состояния. Величина инертности характеризуется массой тела.)
2. Дифференциальный закон движения. (дифференциальный закон движения, описывающий взаимосвязь между приложенной к материальной точке силой и получающимся от этого ускорением этой точки. Фактически, второй закон Ньютона вводит массу как меру проявления инертности материальной точки в выбранной инерциальной системе отсчёта.
где — ускорение материальной точки; — сила, приложенная к материальной точке; — масса материальной точки.
Или в более известном виде:
)
3, Взаимодействие 2-х тел. (Этот закон объясняет, что происходит с двумя взаимодействующими телами. Возьмём для примера замкнутую систему, состоящую из двух тел. Первое тело может действовать на второе с некоторой силой , а второе — на первое с силой . Как соотносятся силы? Третий закон Ньютона утверждает: сила действия равна по модулю и противоположна по направлению силе противодействия. Подчеркнём, что эти силы приложены к разным телам, а потому вовсе не компенсируются.)
Абсолютное пространство и время
– Абсолютное пространство по своей сущности, безотносительно к чему бы то ни было внешнему, остается всегда одинаковым и неподвижным. Относительное пространство есть мера или какая-либо ограниченная подвижная часть, которая определяется нашими чувствами по положению его относительно некоторых тел и которое в обыденной жизни принимается за пространство неподвижное.
– Время понималось абсолютным, однородным, равномерно текущим. Оно идет сразу и везде во всей Вселенной “единообразно и синхронно” и выступает как независимых материальных объектов процесс длительности, Фактически классическая механика сводила время к длительности, фиксируя определяющее свойство времени “показывать чродссти-тельность события”. Значение указаний времени в класс иче ской механике считалось абсолютным, не зависяицш от со стояния движения тела отсчета.
11 Законы Сохранения, физические законы, согласно которым некоторое свойство замкнутой системы остается неизменным при каких-либо изменениях в системе. Самыми важными являются законы сохранения вещества и энергии. Закон сохранения вещества утверждает, что вещество не создается и не разрушается; при химических превращениях общая масса остается неизменной. Общее количество энергии в системе также остается неизменным; энергия только преобразуется из одной формы в другую. Оба эти закона верны лишь приблизительно. Масса и энергия могут превращаться одна в другую согласно уравнению Е = тс2. Неизменным остается лишь общее количество массы и эквивалентной ей энергии. Еще один закон сохранения касается электрического заряда: его также нельзя создать и нельзя уничтожить. В применении к ядерным процессам закон сохранения выражается в том, что общая величина заряда, спин и другие КВАНТОВЫЕ ЧИСЛА взаимодействующих частиц должны остаться такими же у частиц, возникших в результате взаимодействия. При сильных взаимодействиях все квантовые числа сохраняются. При слабых взаимодействиях некоторые из требований этого закона нарушаются, особенно в отношении ЧЕТНОСТИ.
Закон сохранения энергии можно объяснить на примере падения шара весом 1 кг с вы соты 100 м. Начальная общая энергия шара — это ею потенциальная энергия. Когда он падаег, погенциальная энергия постепенно убывает а кинетическая нарастает, но общее копичество энергии остается неизменным Таким образом, имеет место сохранение энергии. А — кинетическая энергия возрастает от 0 до максимума: В -— потенциальная энергия уменьшается от максимума до нуля; С -— общее количество энергии, которое равно сумме кинетическом и потен Закон сохранения вещества, утверждает, что в ходе химических реакций вещество не создается и не исчезает. Это явление можно продемонстрировать при помощи класси ческого опыта, при котором производится взвешивание свечи, горящей под стеклянным колпаком (А). В конце опыта вес колпака и его содержимого остаегся таким же, каким был в начале, хотя свеча, вещество которой состоит в основном из углерода и водорода, «исчезла», поскольку из нее выделились летучие продукты реакции (вода и углекислый газ). Только после того, как в конце XVIII в ученые признали принцип сохранения вещества, стал возможен количественных подход к химии.
12 Теория относительности — научная теория, объясняющая устройство нашего мира на макроуровне, объединяющая механику, электродинамику и гравитацию. Собственно термин «Теория относительности» ввёл немецкий физик Макс Планк. Внедрена в научные круги расовым немецким евреем Альбертом «E=mc²» Эйнштейном. Делится на две части: Специальную и Общую.
Специальная теория относительности
Большинство парадоксальных и противоречащих интуитивным представлениям о мире эффектов, возникающих при движении со скоростью, близкой к скорости света, предсказывается именно специальной теорией относительности. Самый известный из них — эффект замедления хода часов, или эффект замедления времени. Часы, движущиеся относительно наблюдателя, идут для него медленнее, чем точно такие же часы у него в руках.
Общая теория относительности
Общая теория относительности применяется уже ко всем системам отсчета (а не только к движущимися с постоянной скоростью друг относительно друга) и выглядит математически гораздо сложнее, чем специальная (чем и объясняется разрыв в одиннадцать лет между их публикацией). Она включает в себя как частный случай специальную теорию относительности (и, следовательно, законы Ньютона). При этом общая теория относительности идёт значительно дальше всех своих предшественниц. В частности, она дает новую интерпретацию гравитации.
Общая теория относительности делает мир четырехмерным: к трем пространственным измерениям добавляется время. Все четыре измерения неразрывны, поэтому речь идет уже не о пространственном расстоянии между двумя объектами, как это имеет место в трехмерном мире, а о пространственно-временных интервалах между событиями, которые объединяют их удаленность друг от друга — как по времени, так и в пространстве. То есть пространство и время рассматриваются как четырехмерный пространственно-временной континуум или, попросту, пространство-время. В этом континууме наблюдатели, движущиеся друг относительно друга, могут расходиться даже во мнении о том, произошли ли два события одновременно — или одно предшествовало другому. К счастью для нашего бедного разума, до нарушения причинно-следственных связей дело не доходит — то есть существования систем координат, в которых два события происходят не одновременно и в разной последовательности, даже общая теория относительности не допускает.
Закон всемирного тяготения Ньютона говорит нам, что между любыми двумя телами во Вселенной существует сила взаимного притяжения. С этой точки зрения Земля вращается вокруг Солнца, поскольку между ними действуют силы взаимного притяжения. Общая теория относительности, однако, заставляет нас взглянуть на это явление иначе.
Под релятивистскими эффектами понимаются проявления при высоких скоростях действия принципа относительности. В классической физике предполагается, что все наблюдатели, где бы во вселенной они не находились, получают одинаковые результаты измерений протяженности в пространстве и во времени. Принцип относительности подразумевает, что разные наблюдатели получают различные результаты измерений.
РЕЛЯТИВИСТСКИЕ ЭФФЕКТЫ – физ. явления, наблюдаемые при скоростях тел (частиц) v, сравнимых со скоростью света с. К ним относятся: релятивистское сокращение продольных (в направлении движения тела) длин, релятивистские замедление времени, увеличение массы тела с ростом его энергии и т. п., рассматриваемые в частной (специальной) относительности теории. Для квантовых систем частиц (атомов, атомных ядер и др.), в к-рых относит. движение частиц происходит со скоростями , Р. э. дают поправки к уровням энергии, пропорц. степеням отношения . Релятивистскими наз. также эффекты общей теории относительности (релятивистской теории тяготения), напр. эффект замедления течения времени в сильном грави-тац. Поле.
Простра́нство-вре́мя (простра́нственно-временно́й конти́нуум) — физическая модель, дополняющая пространстворавноправным временны́м измерением и, таким образом, создающая теоретико-физическую конструкцию, которая называется пространственно-временным континуумом.
В соответствии с теорией относительности, Вселенная имеет три пространственных измерения и одно временное измерение, и все четыре измерения органически связаны в единое целое, являясь почти равноправными и в определенных рамках (см. примечания ниже) способными переходить друг в друга при смене наблюдателем системы отсчёта.
В рамках общей теории относительности пространство-время имеет и единую динамическую природу, а его взаимодействие со всеми остальными физическими объектами (телами, полями) — и есть гравитация. Таким образом, теория гравитации в рамках ОТО и другихметрических теорий гравитации есть теория пространства-времени, полагаемого не плоским, а способным динамически менять своюкривизну.
studfiles.net
Современные представления о строении атома
Поиск ЛекцийИ.В.ТРИГУБЧАК
Пособие-репетитор по химии
ЗАНЯТИЕ 3
10-й класс (первый год обучения)
Продолжение. Начало см. в № 22,/2005; 1/2006
Современные представления о строении атома
До конца XIX в. атом считали неделимой частицей, но последовавшие позже открытия (радиоактивность, фотоэффект) поколебали это убеждение. Сейчас известно, что атом состоит из элементарных частиц, основные из которых – протон, нейтрон, электрон.
| Частица | Обозначение | Заряд | Относительная атомная масса |
| Протон | p | + | |
| Нейтрон | n | ||
| Электрон | e | – | 1/1840 |
После открытия основных элементарных частиц, входящих в состав атома, встал вопрос об их местонахождении, т.е. о строении атома. В 1911 г. Томсон предложил свою модель строения атома, которая получила условное название «пудинг с изюмом». Согласно этой модели атом представляет собой некую субстанцию, в которой равномерно распределены протоны, нейтроны и электроны. Число протонов равно числу электронов, поэтому атом в целом электронейтрален.
В 1913 г. Резерфорд ставит опыт, результаты которого модель Томсона объяснить не может (рис.).Это заставляет Резерфорда предложить свою модель строения атома, получившую название планетарной. Согласно этой модели атом состоит из ядра, в котором сконцентрирована основная масса атома, поскольку ядро содержит протоны и нейтроны; вокруг ядра на огромной скорости вращаются электроны. Поскольку модель Резерфорда содержала ряд противоречий, Н.Бором были введены постулаты, устраняющие эти противоречия.
| Рис. Схема установки в опыте Резерфорда: 1 – источник -излучения; 2 – золотая фольга; 3 – экран с покрытием из сульфида цинка |
1-й постулат. Электроны вращаются вокруг ядра не по произвольным, а по строго определенным, стационарным орбитам.
2-й постулат. При движении по стационарной орбите электрон не излучает и не поглощает энергию. Изменение энергии происходит при переходе электрона с одной стационарной орбиты на другую.
Но теория Резерфорда–Бора дает удовлетворительные результаты только для атома водорода. Современные представления о строении атома подчиняются квантовой модели строения атома, которая учитывает волновые свойства элементарных частиц. Приведем ее основные положения.
| Э.Резерфорд (1871–1937) |
• Электрон имеет двойственную (корпускулярно-волновую) природу, т.е. ведет себя и как частица, и как волна. Как частица, электрон обладает массой и зарядом; как волна, он обладает способностью к дифракции.
| Н.Бор (1885–1962) |
• Для электрона невозможно одновременно точно измерить координату и скорость.
• Электрон в атоме не движется по определенным траекториям, а может находиться в любой части околоядерного пространства, однако вероятность его нахождения в разных частях этого пространства неодинакова. Область пространства, где вероятнее всего находится электрон, называется орбиталью*.
• Ядра атомов состоят из протонов и нейтронов, имеющих общее название – нуклоны.
Параметры для характеристики атомов
Массовое число А – сумма чисел протонов и нейтронов атома.
Заряд ядра Z – число протонов, определяется по порядковому номеру элемента в таблице Д.И.Менделеева. В 1913 г. английским физиком Г.Мозли было установлено, что положительный заряд ядра атома (в условных единицах) равен порядковому номеру элемента в периодической системе Д.И.Менделеева.
Число нейтронов N определяется как разность между массовым числом и зарядом ядра (учитывая, что массой электрона можно пренебречь).
Изотопы – атомы одного элемента, имеющие одинаковый заряд ядра (следовательно, и количество электронов), но различное число нейтронов (следовательно, различные массовые числа). Например, элемент водород имеет три изотопа: протий, дейтерий и тритий. Первые два существуют в природе, тритий получен искусственным путем. Подавляющее большинство химических элементов имеет разное число природных изотопов с разным процентным содержанием каждого из них. Относительная атомная масса элемента, которая приводится в периодической системе, – это средняя величина массовых чисел природных изотопов данного элемента с учетом процентного содержания каждого из этих изотопов. Химические свойства всех изотопов одного химического элемента одинаковы. Следовательно, химические свойства элемента зависят не от атомной массы, а от заряда ядра.
Помимо изотопов существуют изобары – атомы разных химических элементов, которые имеют одинаковые массовые числа, и изотоны – атомы разных химических элементов, которые имеют одинаковое число нейтронов.
Радиоактивность. Ядерные реакции
Радиоактивностью называют самопроизвольное превращение неустойчивого изотопа одного химического элемента в изотоп другого элемента, сопровождающееся испусканием элементарных частиц или ядер.
Периодом полураспада (Т1/2) называется время, за которое распадается половина исходного количества радиоактивного изотопа.
где m0 – начальная масса вещества, mост – масса остатка, t – время процесса, Т1/2 – период полураспада.
К основным видам радиоактивного распада относятся:
–распад ( -частица – ядро атома 42He). При испускании -частицы ядро теряет два протона и два нейтрона, например:
––распад ( –-частица – электрон). При испускании электрона заряд ядра увеличивается на 1, а массовое число не изменяется, например:
Позитронный ( +) распад ( +-частица – позитрон, обладает массой электрона и положительным зарядом). Число протонов в ядре при позитронном распаде уменьшается на 1, а массовое число не изменяется, например:
Электронный захват. При захвате ядром электрона заряд ядра уменьшается на 1, а массовое число остается прежним, например:
Уравнения ядерных реакций должны удовлетворять правилу равенства сумм индексов:
а) сумма массовых чисел частиц, вступающих в реакцию, равна сумме массовых чисел частиц – продуктов реакции;
б) сумма зарядов частиц, вступающих в реакцию, и сумма зарядов образовавшихся частиц – продуктов реакции – равны между собой.
Тест по теме
«Современные представления о строении атома»
1. Число протонов в атоме элемента, который находится в четвертом периоде и в главной подгруппе
V группы периодической системы Д.И.Мендлеева, равно:
а) 75; б) 42; в) 33; г) 23.
2. Изотопы – это частицы, имеющие одинаковое число:
а) протонов; б) нейтронов;
в) нуклонов; г) электронов.
3. Что одинаковое в атомах 126С и 146С?
а) Массовое число; б) число протонов;
в) число электронов; г) радиоактивные свойства.
4. Чему равен заряд ядра атома натрия?
а) 0; б) +1; в) +11; г) +23.
5. Чему равен заряд ядра атома азота?
а) 0; б) +7; в) +14; г) –1.
6. Выберите атомы, в которых число протонов равно числу нейтронов:
а) 2H; б) 11B; в) 16O; г) 38K.
7. Cколько протонов и электронов содержит нитрит-ион?
а) 46р, 46е; б) 23р, 24е; в) 23р, 23е; г) 46р, 47е.
8. В результате серии последовательных радиоактивных распадов изотоп 22888Ra превращается в устойчивый изотоп 20882Pb. Сколько – и -распадов включает эта серия ядерных превращений?
а) 10 , 6 ; б) 10 , 5 ; в) 5 , 4 ; г) 5 , 6 .
9. В природе существуют два стабильных изотопа водорода и три изотопа кислорода. Сколько разных стабильных молекул воды существует в природе?
а) 5; б) 6; в) 8; г) 9.
10. Число элементов, образующих следующие вещества: легкая вода, тяжелая вода, сверхтяжелая вода, пероксид водорода, кислород, озон, – равно:
а) 6; б) 5; в) 3; г) 2.
Ключ к тексту
| в | б | б, в | в | а | а, в, г | б | в | г | г |
Задачи на определение
элементного состава вещества
и вывод формулы сложного вещества
по известному элементному составу
Уровень А
1. Вычислить, в каком из оксидов железа больше массовая доля металла.
Ответ. (Fe) в FeO – 77,8%.
2. Сколько граммов кальция содержится в 250 г известняка?
Ответ. 100 г.
3. Рассчитать массу сернистого газа, в которой содержится 8 г серы.
Ответ. 16 г.
4. Рассчитать массу питьевой соды, содержащую 30 г углерода.
Ответ. 210 г.
5. Технический хлорид алюминия содержит 98% чистого вещества, остальное составляют примеси, не содержащие хлора. Вычислить процентное содержание хлора в этом химическом продукте.
Ответ. 78,5%.
6. Железные руды относятся к богатым, если содержание железа в них более 50% по массе. Определить, относится ли к богатым рудам карбонат железа(II).
Решение
Для FeCO3 массовая доля железа:
Ответ. FeCO3 не относится к богатым рудам.
7. Образец соединения фосфора и брома массой 81,3 г содержит 9,3 г фосфора. Определить формулу этого соединения.
Ответ. PBr3.
8. Органическое вещество содержит 82,76% углерода и 17,24% водорода; 2,74 г этого вещества при температуре 37 °С и давлении 0,5 атм занимают объем 2,4 л. Определить молекулярную формулу вещества.
Ответ. C4H10.
9. Органическое вещество содержит 40% углерода, 53,3% кислорода, 6,7% водорода; 15 г этого вещества при температуре 18 °С и давлении 610 мм рт. ст. занимают объем 14,9 л. Определить молекулярную формулу вещества.
Ответ. CH2O.
10. Найти отношения масс элементов в гидроксиде магния и в пропане.
Ответ. m(Mg) : m(O) : m(H) = 12 : 16 : 1,
m(C) : m(Н) = 9 : 2.
11. Вычислить массу нитрата серебра, содержащего столько же серебра, сколько его содержится в 696 г оксида серебра.
Ответ. 1020 г.
12. Определить простейшую формулу вещества, содержащего (мол. %) 7,69% серебра, 23,08% азота, 46,15% водорода, 23,08% кислорода.
Ответ. AgN3H6O3.
13. В молекулах двух веществ соотношение чисел атомов С : Н : О = 1 : 2 : 1. Масса 100 мл паров первого из них при н.у. составляет 0,402 г. Молекулярная масса у второго вещества в два раза больше, чем у первого. Определить вещества.
Ответ. С3Н6О3, С6Н12О6.
14. Вывести молекулярную формулу вещества, имеющего состав (массовая доля в процентах):
а) натрия – 36,51, серы – 25,39, кислорода – 38,1;
б) натрия – 29,11, серы – 40,51, кислорода – 30,38;
в) калия – 26,53, хрома – 35,37, кислорода – 38,1;
г) водорода – 4,17, кремния – 29,17, кислорода – 66,67;
д) калия – 28,16, хлора – 25,63, кислорода – 46,21.
Решение (14б)
Представим искомую формулу в виде NaxSyOz. Запишем массовые доли элементов (Э) и их относительные атомные массы Ar(Э) в виде таблицы.
| Элемент | Ar | |
| Na | 29,11% | |
| S | 40,51% | |
| O | 30,38% |
Разделим все три числа соотношения на наименьшее (1,266), получим простое соотношение: 1 : 1: 1,5. Умножим все три числа на 2, получим: 2 : 2 : 3. Отсюда формула вещества – Na2S2O3.
Ответ. а – Na2SO3, б – Na2S2O3, в – K2Cr2O7, г – H4SiO4, д – KClO4.
Уровень Б
1. Определить формулу вещества, состоящего из кислорода, азота, фосфора и водорода, если известно, что оно содержит 48,5% кислорода; количество атомов азота в нем в 2 раза больше количества атомов фосфора, а количество атомов водорода – в 2,25 раза больше количества атомов кислорода. Молярная масса вещества меньше 200 г/моль.
Ответ. Гидрофосфат аммония (NH4)2HPO4.
2. Неизвестная соль содержит элемент X, а также водород, азот и кислород в следующем массовом соотношении: 12 : 5 : 14 : 48 (в порядке перечисления). Определить формулу соли.
Ответ. Гидрокарбонат аммония NH4HCO3.
3. Написать формулу углеводорода, в котором масса углерода равна массе водорода.
Ответ. CT4, где T – 31H, тритий.
4. В порции кристаллогидрата ацетата калия содержится 3,612•1023 атомов углерода и 1,084•1024 атомов водорода. Установить формулу кристаллогидрата.
Ответ. 2СН3СООК•3Н2О.
* При более строгом определении орбиталь – это функция, описывающая плотность электронного облака в каждой точке пространства.
poisk-ru.ru
§ 45 Современные представления о строении атома
§ 45 Современные представления о строении атома
Строение ядра.
Термин «атом» сохранился в современной науке, несмотря на то что уже давно стало понятно, что эта частица не является собственно «атомом», т. е. «неделимым». В настоящее время известно, что атом состоит из ядра и окружающей его электронной оболочки, которую также называют электронным облаком. Ядро обладает положительным электрическим зарядом, а электроны – отрицательным, поэтому они удерживаются около атомного ядра за счёт силы электростатического притяжения. В то же время между электронами действует сила электрического отталкивания. Совокупность этих взаимодействий определяет устойчивость атома. Положительный электрический заряд ядра атома всегда равен по абсолютной величине сумме отрицательных зарядов электронов, окружающих ядро. Поэтому суммарный заряд атома равен нулю, т. е. атом является электрически нейтральным. Если под воздействием внешней энергии один или несколько электронов покидают атом, тот приобретает положительный заряд и становится положительно заряженным ионом.
Атомное ядро по размеру составляет менее одной стотысячной части всего атома, однако масса ядра примерно в 4000 раз больше, чем масса всех входящих в него электронов. Так как электронное облако не имеет резкой границы, размеры атомов определяют по расстоянию между их ядрами в молекулах. Радиус самого маленького атома (гелия) составляет тридцать две миллиардных миллиметра, а самого большого (цезия) – приблизительно в семь раз больше. Эти размеры в тысячи раз меньше, чем длина волны видимого света, поэтому атомы невозможно увидеть в обычный световой микроскоп. Отдельные атомы можно наблюдать только с помощью современных микроскопов, использующих квантовые эффекты. Для того чтобы получить представление о размере атомов, надо представить себе, что яблоко увеличилось до размеров Земли. Тогда размеры атомов будут равны размеру первоначального яблока.
Масса атома определяется главным образом массой его ядра, которое состоит из двух видов частиц, называемых нуклонами (от лат. nucleus – ядро), имеющих почти одинаковую массу. Нуклоны бывают двух видов: положительно заряженные протоны и нейтральные нейтроны.
Вид атома с определённым зарядом ядра называют химическим элементом. Атом каждого элемента отличается от других числом протонов в атомном ядре, которое соответствует его порядковому номеру в Периодической системе элементов Д. И. Менделеева и числу электронов в электронной оболочке. Кроме того, число протонов определяет электрический заряд ядра, так как электрически нейтральные нейтроны не вносят в него вклада. Поэтому число протонов в ядре какого-либо атома называют его зарядовым числом. Самое простое строение имеет атом водорода. Он состоит всего из одного протона и одного электрона. Другие элементы обязательно имеют в составе своего ядра нейтроны. Так, ядро атома гелия состоит из двух протонов и двух нейтронов.
Масса ядра определяется суммой масс составляющих его протонов и нейтронов и называется атомной массой. Поскольку масса атомов очень мала, её неудобно измерять непосредственно в граммах. Поэтому в практических целях используют величину, называемую массовым числом, которая равна числу всех входящих в ядро нуклонов. Масса одного протона или нейтрона, таким образом, принимается за единицу.
Изотопы
Может показаться, что каждый химический элемент должен всегда иметь определённое зарядовое число и определённую атомную массу. Однако это утверждение верно только в отношении зарядового числа. Ещё в начале XX в. было обнаружено, что некоторые элементы, проявляющие одинаковые свойства в химических реакциях, состоят из атомов, имеющих различную атомную массу. Атомы одного и того же элемента, имеющие различную массу, были названы изотопами. Встречающиеся в природе элементы чаще всего являются смесью нескольких изотопов, один из которых является преобладающим. Атомы всех изотопов одного элемента имеют одинаковый заряд ядра и, соответственно, занимают одно и то же место в периодической системе химических элементов. Различие между ними заключается в числе содержащихся в ядре нейтронов.
Ядро атома гелия чаще всего содержит два нейтрона, но встречаются изотопы, число нейтронов в ядре которых равно одному или трём. Кислород в природе может существовать в виде трёх изотопов с восемью, девятью или десятью нейтронами. При этом число протонов в ядре атома кислорода и, следовательно, его зарядовое число и атомный номер всегда равны восьми. Водород является первым элементом периодической системы элементов. Ядро его атома содержит всего один протон и чаще всего вообще не содержит нейтронов. Такой изотоп водорода называют протий. Однако в природном водороде содержится почти 0,02 % изотопа, называемого дейтерием и содержащего один нейтрон (рис. 115, А). Соответственно, атомная масса дейтерия равна двум.
Рассмотренные изотопы гелия, кислорода и водорода называют стабильными, так как они устойчивы и не подвергаются самопроизвольному распаду. К настоящему времени в природе обнаружено 270 стабильных изотопов. Кроме них существуют и нестабильные изотопы, ядро которых неустойчиво и подвержено постоянному распаду. Эти изотопы чаще всего встречаются у тяжёлых элементов, т. е. элементов с большой атомной массой. Нестабильные изотопы часто получают искусственно при помощи ядерных реакций. Таким способом можно получить, например, нестабильный изотоп водорода, в ядре которого находятся два нейтрона. Этот изотоп водорода называется тритием из-за того, что его атомная масса равна трём (один протон плюс два нейтрона) (см. рис. 115, А).
Рис. 115. Состав атомных ядер: А – водорода; Б – углерода (красные шарики – протоны, голубые – нейтроны)
Большинство природных химических элементов существуют в виде нескольких устойчивых изотопов (рис. 115, Б). Например, железо имеет четыре стабильных изотопа, ртуть – семь, а олово – десять. Поэтому атомная масса элементов выражается дробным числом. Так, хлор, встречающийся в природе, на 76,5 % состоит из изотопа с атомной массой, равной 35, и на 24,5 % – из изотопа с массой 37. Поэтому средняя атомная масса хлора равна приблизительно 35,5.
Как следует из самого названия, нестабильные изотопы не могут существовать в течение неограниченного периода времени и постоянно распадаются. Скорость распада ядер этих изотопов измеряется их периодом полураспада – временем, за которое первоначальное количество частиц уменьшается вдвое. У большинства нестабильных изотопов этот период составляет не более нескольких секунд, хотя известны изотопы с периодом полураспада в миллионы лет. Во время распада ядра таких атомов испускают радиоактивное излучение. Таким образом, можно сказать, что все неустойчивые изотопы обладают радиоактивностью (рис. 116).
Химические свойства элементов, т. е. их способность вступать в химические реакции, не зависят от числа нейтронов в ядре атома, а связаны со строением его электронной оболочки. Поэтому в химическом отношении все изотопы одного элемента являются абсолютно одинаковыми. Эту особенность используют во многих областях науки, техники и медицины. Таким образом можно, например, судить о превращениях какого-либо химического вещества в организме и о местах его включения в клетки и ткани. Можно синтезировать биологически активное вещество, включив в него неустойчивый радиоактивный изотоп какого-либо атома, например углерода или азота. В химическом и биологическом отношении это вещество ничем не будет отличаться от такого же вещества, не содержащего радиоактивного изотопа. В какие бы другие соединения это вещество ни превращалось, как бы ни изменялось строение его молекулы, радиоактивное излучение нестабильного атома всегда будет сохраняться. Если затем ввести это вещество в кровь, то, измеряя испускаемое этим изотопом слабое, безопасное для организма, радиоактивное излучение в различных участках человеческого тела, можно судить о том, где и в каких количествах накапливается в организме это вещество или продукты его обмена. Постепенно эти продукты или само вещество будут выводиться из организма, и по уменьшению радиоактивности можно определить скорость их выведения. Такой метод получил название исследования с применением «меченых атомов».
Рис. 116. Радиоактивный металл кюрий светится в темноте, испуская большое количество ядер гелия
Сильное и слабое взаимодействие.
При знакомстве со строением атомного ядра возникает естественный вопрос: с помощью каких сил нуклоны удерживаются друг около друга? Мы знаем, что протоны и электроны, будучи противоположно заряженными, взаимно притягиваются, и именно это электрическое поле определяет устойчивость атома в целом. Но поскольку все протоны заряжены одинаково положительно, они должны отталкиваться друг от друга и ядро должно немедленно разрушиться. Нейтральные нейтроны не могут вмешиваться в этот процесс, а сила гравитации настолько мала по сравнению с электромагнитной, что никак не может препятствовать этому распаду. Почему же ядро может существовать в неизменном виде миллиарды лет?
Оказывается, что в природе, помимо двух уже известных нам фундаментальных взаимодействий – гравитационного и электромагнитного, существуют ещё два типа взаимодействий, называемых сильным и слабым. Первое из них удерживает нуклоны внутри атомного ядра, а второе обнаруживается при превращениях элементарных частиц. Главной особенностью сильного взаимодействия, отличающей его от гравитационного и электромагнитного взаимодействий, является то, что оно действует только на очень малых расстояниях, соизмеримых с размером нуклонов. Эти расстояния составляют около 1015 м. На таких расстояниях эта сила становится столь огромной, что по сравнению с ней можно пренебречь всеми электромагнитными, не говоря уже о гравитационных, взаимодействиями между нуклонами. Слабое взаимодействие тоже распространяется только на очень малые расстояния, но превышает оно только силу гравитации.
Проверьте свои знания
1. Что происходит с атомом, если он теряет один или несколько электронов?
2. Почему атомы невозможно увидеть с помощью светового микроскопа?
3. Какими частицами определяется масса атомного ядра, а какими – его заряд?
4. Что такое период полураспада атомного ядра?
5. Какие виды взаимодействия осуществляются внутри атомного ядра и элементарных частиц?
Задания
Подберите эпиграф к данному параграфу.
librolife.ru
Современные представления о строении атомов — реферат
Введение:
определение атома
Основная
часть: современные представления
о строении атома
Заключение:
немного об ученых
Определение
атома
А́том
(от др.-греч. ἄτομος — неделимый) —
наименьшая химически неделимая
часть химического элемента, являющаяся
носителем его свойств. Атом состоит из
атомного ядра и электронов. Ядро атома
состоит из положительно заряженных протонов
и незаряженных нейтронов. Если число
протонов в ядре совпадает с числом электронов,
то атом в целом оказывается электрически
нейтральным. В противном случае он обладает
некоторым положительным или отрицательным
зарядом и называется ионом. Атомы классифицируются
по количеству протонов и нейтронов в
ядре: количество протонов определяет
принадлежность атома некоторому химическому
элементу, а число нейтронов — изотопу
этого элемента.
История
представлений о строении
атома
Впервые
понятие “атом” (неделимый) было введено
греческим философом Демокритом
в V веке до нашей эры. Он утверждал,
что атомы существуют вечно; они
настолько малы, что их размеры не поддаются
измерению; все атомы одинаковы, но они
различаются внешне (атомы воды, например,
гладкие, они способны перекатываться,
и поэтому жидкости свойственна текучесть;
атомы железа имеют зубчики, которыми
они зацепляются друг за друга, что придает
железу свойства твердого тела). Представления
Демокрита были умозрительными и мало
полезными.
В начале
нглийский химик и физик Д. Дальтон вновь
предположил, что вещества состоят из
мельчайших частиц – атомов. Он установил,
что атомы одного и того же химического
элемента имеют одинаковые свойства, а
разным элементам соответствуют разные
атомы. Введена важнейшая характеристика
атома – атомная масса. Атом также считался
неделимой частицей.
Однако
со временем эпериментальные доказательства
сложной структуры атома: фотоэффект (явление,
когда при освещении некоторых металлов
с их поверхности испускаются носители
электрического заряда), катодные лучи
(поток отрицательно заряженных частиц
– электронов из катода в вакуумированной
трубке, содержащей катод и анод), рентгеновские
лучи (электромагнитное излучение, подобное
видимому свету, но с гораздо более высокой
частотой, испускаемое веществами при
сильном воздействии на них катодных лучей),
радиоактивность (явление самопроизвольного
превращения одного химического элемента
в другой, сопровождающееся испусканием
электронов, положительно заряженных
частиц, других элементарных частиц и
рентгеновского излучения).
Таким
образом, было установлено, что атомы
состоят из отрицательно и положительно
заряженных частиц, сильно взаимодействующих
между собой. Возник вопрос, как же устроен
атом?
Современные
представления о
строении атома.
Подтверждённая
экспериментально в 1927 г. двойственная
природа электрона, обладающего
свойствами не только частицы, но и волны,
побудила учёных к созданию новой теории
строения атома, учитывающей оба этих
свойства. Современная теория строения
атома опирается на квантовую механику.
Двойственность свойств электрона проявляется в том, что он, с одной стороны, обладает свойствами частицы (имеет определённую массу покоя), а с другой — его движение напоминает волну и может быть описано определённой амплитудой, длиной волны, частотой кол***ий и др. Поэтому нельзя говорить о какой-либо определённой траектории движения электрона — можно лишь судить о той или иной степени вероятности его нахождения в данной точке пространства.
Cледовательно,
под электронной орбитой
По современным представлениям состояние элетрона в атоме описывается четырьмя квантовыми числами. Главное квантовое число n характеризует величину энергии электрона и может принимать только положительные целочисленные значения: 1, 2, 3 и т. д. С увеличением главного квантового числа энергия электрона возрастает. Состояние электрона, отвечающее определённому значению главного квантового числа, называют энергетическим уровнем электрона в атоме. Помимо энергии электрона главное квантовое число определяет размеры электронного облака: чем выше значение главного квантового числа, тем больше электронное облако. Электроны, характеризующиеся одним и тем же квантовым числом, имеют электронные облака приблизительно одинаковых размеров. Поэтому говорят о существовании в атоме электронных слоёв. Электронные слои обозначают большими буквами латинского алфавита K, L, M, N, O, причём K-слой является первым от ядра атома, ему соответствует главное квантовое число n = 1, L-слой — вторым, M-слой — третьим и т. д. Электроны, образующие данный слой, могут обладать несколько отличающейся друг от друга энергией и иметь орбитали различных форм. Из квантовомеханической теории следует, что с увеличением главного квантового числа n изменяются число и характер электронных орбиталей в пределах данного электронного слоя. Количество орбиталей для каждого значения n равно квадрату главного квантового числа (n2).
Второе квантовое число l, описывающее форму электронного облака, называется орбитальным квантовым числом. При данном главном вантовом числе n орбитальное квантовое число l может принимать любые целочисленные значения от 0 до n–1. Соответствующие орбитали обозначаются строчными буквами латинского алфавита: s (l = 0), p (l = 1), d (l = 2), f (l = 3). Орбитальное квантовое число отображает энергию электрона на подуровне. Электроны с различными орбитальными квантовыми числами несколько отличаются друг от друга: их энергия тем выше, чем больше число l. Число возможных подуровней в каждом энергетическом уровне совпадает с порядковым номером электронного слоя, но фактически ни один энергетический уровень не содержит больше четырёх подуровней. Это справедливо для стационарного состояния атомов всех элементов. Так, первому энергетическому уровню соответствует s-подуровень; второму уровню — два подуровня: s и p; третьему уровню — три подуровня: s, p и d; четвёртому и следующим уровням —четыре подуровня: s, p, d и f.
Ориентацию орбиталей в пространстве определяет третье квантовое число, называемое магнитным квантовым числом и обозначаемое m. При данном орбитальном квантовом числе l магнитное квантовое число m может принимать любые целочисленные значения от –l до +l, в том числе нулевое значение. Оно определяет число орбиталей в одном и том же электронном слое: одна s-орбиталь (m = 0), три p-орбитали (m равно –1, 0, +1), пять d-орбиталей (m равно –3, –2, –1, 0, +1, +2, +3). Орбитали с различными магнитными квантовыми числами, но с одинаковым главным и орбитальным квантовыми числами характеризуются одной и той же энергией. Магнитное квантовое число есть вектор, следовательно, ему соответствует не только определённое числовое значение, но и определённое направление, что выражается в знаках “+” и “–”.
Четвёртое
квантовое число, называемое спином
и обозначаемое ms, раньше связывали
с вращением электрона вокруг
своей оси, но теперь ему не придают
какого-либо наглядного образа и считают
чисто квантовомеханической величиной.
Спин электрона может иметь два
значения: +1/2 и –1/2.
Строение
атомного ядра. Субатомные
частицы. Элементы. Изотопы.
Атом
состоит из ядра и окружающего
его электронного “облака”. Находящиеся
в электронном облаке электроны
несут отрицательный
В любом атоме число протонов в ядре в точности равно числу электронов в электронном облаке, поэтому атом в целом – нейтральная частица, не несущая заряда.
Атом может потерять один или несколько электронов или наоборот – захватить чужые электроны. В этом случае атом приобретает положительный или отрицательный заряд и называется ионом.
Практически вся масса атома сосредоточена в его ядре, так как масса электрона составляет всего лишь 1/1836 часть массы протона. Плотность вещества в ядре фантастически велика – порядка 1013 – 1014 г/см3. Спичечный коробок, наполненный веществом такой плотности, весил бы 2,5 миллиарда тонн!
Внешние размеры атома – это размеры гораздо менее плотного электронного облака, которое примерно в 100000 раз больше диаметра ядра.
Кроме протонов, в состав ядра большинства атомов входят нейтроны, не несущие никакого заряда. Масса нейтрона практически не отличается от массы протона. Вместе протоны и нейтроны называются нуклонами (от латинского nucleus – ядро).
Электроны, протоны и нейтроны являются главными “строительными деталями” атомов и называются субатомными частицами. Их заряды и массы в кг и в специальных “атомных” единицах массы (а.е.м.) показаны в таблице 1.
Таблица 1. Субатомные частицы.
| ||||||||||||||||||||
Частица
Заряд
Масса:
кг
а.е.м.
Протон
+1
1,67·10-27
1,00728
Нейтрон
0
1,67·10-27
1,00867
Электрон
-1
9,11·10-31
0,000549
Из таблицы 1 видно, что массы субатомных частиц чрезвычайно малы. Показатель степени (например, десять в минус двадцать седьмой степени) показывает, сколько нулей после запятой нужно записать, чтобы получилась десятичная дробь, выражающая массу субатомной частицы в килограммах. Это ничтожнейшая часть килограмма, поэтому массу субатомных частиц удобнее выражать в атомных единицах массы (сокращенно – а.е.м.). За атомную единицу массы принята ровно 1/12 часть массы атома углерода, в ядре которого содержится 6 протонов и 6 нейтронов. Схематическое изображение такого “эталонного” атома углерода приведено на рис. 2 . Атомную единицу массы можно выразить и в граммах: 1 а.е.м. = 1,660540·10-24 г.
<>
Рис. 2. Атомы состоят из положительно заряженного ядра и электронного облака. а) В состав ядра атома водорода входит только 1 протон, а электронное облако заполняется одним электроном. б) В ядре атома углерода 6 протонов и 6 нейтронов, а в электронном облаке – 6 электронов. в) Существует также изотопный углерод, ядре которого на 1 нейтрон больше. Содержание этого изотопа в природном углероде составляет чуть более 1% (об изотопах см. ниже). Линейные размеры атомов очень малы: их радиусы составляют от 0,3 до 2,6 ангстрема (1 ангстрем = 10–8 см). Радиус ядра около 10–5 ангстрема, то есть 10–13 см. Это в 100000 раз меньше размеров электронной оболочки. Поэтому правильно показать относительные пропорции ядер и электронных оболочек на рисунке невозможно. Если бы атом увеличился до размеров Земли, то ядро имело бы всего около 60 м в диаметре и могло бы поместиться на футбольном поле.
Масса атома, выраженная в килограммах или граммах, называется абсолютной атомной массой. Чаще пользуются относительной атомной массой, которая выражается в атомных единицах массы (а.е.м.). Относительная атомная масса представляет собой отношение массы какого-нибудь атома к массе 1/12 части атома углерода. Иногда говорят более коротко: атомный вес. Последний термин вовсе не устаревший, как иногда пишут в учебниках – он широко используются в современной научной литературе, поэтому мы тоже будем его применять. Относительная атомная масса и атомный вес, фактически, безразмерные величины (масса какого-либо атома делится на массу части атома углерода), поэтому обозначение “а.е.м.” после численного значения обычно опускают (но можно и написать, в этом не будет ошибки). Термины “относительная атомная масса”, “атомная масса”, “атомный вес” в научном химическом языке обычно используются равноправно и между ними просто не делают различий. В Международном союзе химиков (IUPAC) существует Комиссия по относительной распространенности изотопов и атомным весам (Commission on Isotopic Abundances and Atomic Weights или сокращенно – CIAAW), но не “Комиссия по относительным атомным массам”. Однако все химики прекрасно понимают, что речь идет об одном и том же.
student.zoomru.ru
Сайт преподавателя Коноваловой Лидии – Занятие № 2
Занятие №2. Строение атома. Периодическая система химических элементов.
Описание свойств элементов по положение в ПСХЭ.
Лекция
Полный текст лекции можно скачать здесь
Современные представления о строении атома
До конца XIX в. атом считали неделимой частицей, но последовавшие позже открытия (радиоактивность, фотоэффект) поколебали это убеждение. Сейчас известно, что атом состоит из элементарных частиц, основные из которых – протон, нейтрон, электрон.
Частица | Обозначение | Заряд | Относительная атомная масса |
Протон | p | + | 1 |
Нейтрон | n | 0 | 1 |
Электрон | e | – | 1/1840 |
После открытия основных элементарных частиц, входящих в состав атома, встал вопрос об их местонахождении, т.е. о строении атома. В 1911 г. Томсон предложил свою модель строения атома, которая получила условное название «пудинг с изюмом». Согласно этой модели атом представляет собой некую субстанцию, в которой равномерно распределены протоны, нейтроны и электроны. Число протонов равно числу электронов, поэтому атом в целом электронейтрален.
В 1913 г. Резерфорд ставит опыт, результаты которого модель Томсона объяснить не может.Это заставляет Резерфорда предложить свою модель строения атома, получившую название планетарной. Согласно этой модели атом состоит из ядра, в котором сконцентрирована основная масса атома, поскольку ядро содержит протоны и нейтроны; вокруг ядра на огромной скорости вращаются электроны. Поскольку модель Резерфорда содержала ряд противоречий, Н.Бором были введены постулаты, устраняющие эти противоречия.
1-й постулат. Электроны вращаются вокруг ядра не по произвольным, а по строго определенным, стационарным орбитам.
2-й постулат. При движении по стационарной орбите электрон не излучает и не поглощает энергию. Изменение энергии происходит при переходе электрона с одной стационарной орбиты на другую.
Но теория Резерфорда–Бора дает удовлетворительные результаты только для атома водорода. Современные представления о строении атома подчиняются квантовой модели строения атома, которая учитывает волновые свойства элементарных частиц. Приведем ее основные положения.
• Электрон имеет двойственную (корпускулярно-волновую) природу, т.е. ведет себя и как частица, и как волна. Как частица, электрон обладает массой и зарядом; как волна, он обладает способностью к дифракции.
• Для электрона невозможно одновременно точно измерить координату и скорость.
• Электрон в атоме не движется по определенным траекториям, а может находиться в любой части околоядерного пространства, однако вероятность его нахождения в разных частях этого пространства неодинакова. Область пространства, где вероятнее всего находится электрон, называется орбиталью*.
• Ядра атомов состоят из протонов и нейтронов, имеющих общее название – нуклоны.
Параметры для характеристики атомов
Массовое число А – сумма чисел протонов и нейтронов атома.
Заряд ядра Z – число протонов, определяется по порядковому номеру элемента в таблице Д.И.Менделеева. В 1913 г. английским физиком Г.Мозли было установлено, что положительный заряд ядра атома (в условных единицах) равен порядковому номеру элемента в периодической системе Д.И.Менделеева.
Число нейтронов N определяется как разность между массовым числом и зарядом ядра (учитывая, что массой электрона можно пренебречь).
Изотопы – атомы одного элемента, имеющие одинаковый заряд ядра (следовательно, и количество электронов), но различное число нейтронов (следовательно, различные массовые числа). Например, элемент водород имеет три изотопа: протий, дейтерий и тритий. Первые два существуют в природе, тритий получен искусственным путем. Подавляющее большинство химических элементов имеет разное число природных изотопов с разным процентным содержанием каждого из них. Относительная атомная масса элемента, которая приводится в периодической системе, – это средняя величина массовых чисел природных изотопов данного элемента с учетом процентного содержания каждого из этих изотопов. Химические свойства всех изотопов одного химического элемента одинаковы. Следовательно, химические свойства элемента зависят не от атомной массы, а от заряда ядра.
Посмотреть учебный фильм о строении атома
Строение электронной оболочки атома
Атом состоит из ядра и электронной оболочки. Электронная оболочка атома – это совокупность всех электронов в данном атоме. От строения электронной оболочки атома напрямую зависят химические свойства данного химического элемента. Согласно квантовой теории каждый электрон в атоме занимает определенную орбиталь и образует электронное облако, которое является совокупностью различных положений быстро движущегося электрона.
Для характеристики орбиталей и электронов используют квантовые числа.
Главное квантовое число n характеризует энергию и размеры орбитали и электронного облака, принимает значения целых чисел – от 1 до бесконечности (n = 1, 2, 3, 4, 5, 6…). Орбитали, имеющие одинаковые значения n, близки между собой по энергии и по размерам, они образуют один энергетический уровень.
Энергетический уровень – это совокупность орбиталей, имеющих одинаковое значение главного квантового числа. Энергетические уровни обозначают либо цифрами, либо большими буквами латинского алфавита (1 – K, 2 – L, 3 – M, 4 – N, 5 – O, 6 – P, 7 – Q). С увеличением порядкового номера энергия орбиталей увеличивается.
Электронный слой – это совокупность электронов, находящихся на одном энергетическом уровне.На одном энергетическом уровне могут находиться электронные облака, имеющие различные геометрические формы.
Побочное (орбитальное) квантовое число l характеризует формы орбиталей и облаков, принимает значения целых чисел от 0 до n – 1.
Энергетический | Значения главного | Значения побочного |
K | 1 | 0 (s) |
L | 2 | 0, 1 (s, p) |
M | 3 | 0, 1, 2 (s, p, d) |
N | 4 | 0, 1, 2, 3 (s, p, d, f) |
Орбитали, для которых l = 0, имеют форму сферы и называются s–орбиталями. Они содержатся на всех энергетических уровнях, причем на К-уровне есть только s-орбиталь.
Орбитали, для которых l = 1, имеют форму вытянутой восьмерки и называются р–орбиталями. Они содержатся на всех энергетических уровнях, кроме первого (К).
Орбитали, для которых l = 2, называются d–орбиталями. Их заполнение электронами начинается с третьего энергетического уровня.
Заполнение f–орбиталей, для которых l = 3, начинается с четвертого энергетического уровня.
Энергия орбиталей, находящихся на одном энергетическом уровне, но имеющих разную форму, неодинакова: Es < Ep < Ed < Ef, поэтому на одном уровне выделяют разные энергетические подуровни.
Энергетический подуровень – это совокупность орбиталей, которые находятся на одном энергетическом уровне и имеют одинаковую форму. Орбитали одного подуровня имеют одинаковые значения главного и побочного квантовых чисел, но отличаются направлением (ориентацией) в пространстве.
Магнитное квантовое число ml характеризует ориентацию орбиталей (электронных облаков) в пространстве и принимает значения целых чисел от –l через 0 до +l. Число значений mlопределяет число орбиталей на подуровне, например:
s-подуровень: l = 0, ml = 0 – одна орбиталь;
p-подуровень: l = 1, ml = –1, 0, +1 – три орбитали;
d-подуровень: l = 2, ml = –2, –1, 0, +1, +2 – пять орбиталей.
Таким образом, число орбиталей на подуровне равно 2l + 1. Общее число орбиталей на одном энергетическом уровне – n2. Общее число электронов на одном энергетическом уровне – 2n2. Графически любая орбиталь изображается в виде клетки (квантовой ячейки).
Итак, каждая орбиталь и электрон, находящийся на этой орбитали, характеризуются тремя квантовыми числами: главным, побочным и магнитным. Электрон характеризуется еще одним квантовым числом – спином.
Спиновое квантовое число ms, спин (от англ. spin – кружение, вращение) – характеризует вращение электрона вокруг своей оси и принимает только два значения: +1/2 и –1/2.
Заполнение электронной оболочки атома подчиняется следующим законам.
П р и н ц и п П а у л и. В атоме не может быть двух электронов с одинаковым набором всех четырех квантовых чисел.
П р и н ц и п н а и м е н ь ш е й э н е р г и и. Основное (устойчивое) состояние атома характеризуется минимальной энергией. Поэтому электроны заполняют орбитали в порядке увеличения их энергии.
П р а в и л о К л е ч к о в с к о г о. Электроны заполняют энергетические подуровни в порядке увеличения их энергии. Этот порядок определяется значением суммы главного и побочного квантовых чисел (n + l): 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, 5d, 6p, 7s, 5f, 6d.
П р а в и л о Г у н д а. На одном подуровне электроны располагаются так, чтобы абсолютное значение суммы спиновых квантовых чисел (суммарного спина) было максимальным. Это соответствует устойчивому состоянию атома.
Например, электронные формулы магния, железа и теллура имеют вид:
Mg(+12) 1s22s22p63s2;
Fe(+26) 1s22s22p63s23p64s23d6;
Te(+52) 1s22s22p63s23p64s23d104p65s24d105p4.
Исключения в четвертом периоде составляют атомы хрома и меди, в которых происходит проскок (переход) одного электрона с 4s-подуровня на 3d-подуровень, что объясняется большой устойчивостью образующихся при этом электронных конфигураций 3d5 и 3d10. Таким образом, электронные формулы атомов хрома и меди имеют вид:
Cr(+24) 1s22s22p63s23p64s13d5;
Cu(+29) 1s22s22p63s23p64s13d10.
Тренажёр для закрепления знаний о строении атома
Периодический закон и система химических элементов Д.И.Менделеева
Видеолекция ПЗ и ПСХЭ
1 марта 1869 г. считается датой открытия одного из важнейших законов химии – периодического закона. В середине XIX в. было известно 63 химических элемента, и возникла потребность в их классификации. Попытки такой классификации предпринимали многие ученые (У.Одлинг и Дж.А.Р.Ньюлендс, Ж.Б.А.Дюма и А.Э.Шанкуртуа, И.В.Деберейнер и Л.Ю.Мейер), но лишь Д.И.Менделееву удалось увидеть определенную закономерность, расположив элементы в порядке возрастания их атомных масс. Эта закономерность имеет периодический характер, поэтому Менделеев сформулировал открытый им закон следующим образом: свойства элементов, а также формы и свойства их соединений находятся в периодической зависимости от величины атомной массы элемента.
В системе химических элементов, предложенной Менделеевым, был ряд противоречий, которые сам автор периодического закона устранить не смог (аргон–калий, теллур–йод, кобальт–никель). Лишь в начале XX в., после открытия строения атома, был объяснен физический смысл периодического закона и появилась его современная формулировка: свойства элементов, а также формы и свойства их соединений находятся в периодической зависимости от величины заряда ядер их атомов.
Такую формулировку подтверждает и наличие изотопов, химические свойства которых одинаковы, хотя атомные массы различны.
Периодический закон – один из основных законов природы и важнейший закон химии. С открытия этого закона начинается современный этап развития химической науки. Хотя физический смысл периодического закона стал понятен только после создания теории строения атома, сама эта теория развивалась на основе периодического закона и системы химических элементов. Закон помогает ученым создавать новые химические элементы и новые соединения элементов, получать вещества с нужными свойствами. Сам Менделеев предсказал существование 12 элементов, которые в то время еще не были открыты, и определил их положение в периодической системе. Свойства трех из этих элементов он подробно описал, и при жизни ученого эти элементы были открыты («экабор» – галлий, «экаалюминий» – скандий, «экасилиций» – германий). Кроме того, периодический закон имеет большое философское значение, подтверждая наиболее общие законы развития природы.
Графическим отражением периодического закона является периодическая система химических элементов Менделеева. Существует несколько форм периодической системы (короткая, длинная, лестничная (предложена Н.Бором), спиралеобразная). В России наибольшее распространение получила короткая форма. Современная периодическая система содержит 110 открытых на сегодняшний день химических элементов, каждый из которых занимает определенное место, имеет свой порядковый номер и название. В таблице выделяют горизонтальные ряды – периоды (1–3 – малые, состоят из одного ряда; 4–6 – большие, состоят из двух рядов; 7-й период – незавершенный). Кроме периодов выделяют вертикальные ряды – группы, каждая из которых подразделяется на две подгруппы (главную – а и побочную – б). Побочные подгруппы содержат элементы только больших периодов, все они проявляют металлические свойства. Элементы одной подгруппы имеют одинаковое строение внешних электронных оболочек, что обусловливает их схожие химические свойства.
Период – это последовательность элементов (от щелочного металла до инертного газа), атомы которых имеют одинаковое число энергетических уровней, равное номеру периода.
Главная подгруппа – это вертикальный ряд элементов, атомы которых имеют одинаковое число электронов на внешнем энергетическом уровне. Это число равно номеру группы (кроме водорода и гелия).
Все элементы в периодической системе разделяются на 4 электронных семейства (s-, p-, d-, f-элементы) в зависимости от того, какой подуровень в атоме элемента заполняется последним.
Побочная подгруппа – это вертикальный ряд d-элементов, имеющих одинаковое суммарное число электронов на d-подуровне предвнешнего слоя и s-подуровне внешнего слоя. Это число обычно равно номеру группы.
Важнейшими свойствами химических элементов являются металличность и неметалличность.
Металличность – это способность атомов химического элемента отдавать электроны. Количественной характеристикой металличности является энергия ионизации.
Энергия ионизации атома – это количество энергии, которое необходимо для отрыва электрона от атома элемента, т. е. для превращения атома в катион. Чем меньше энергия ионизации, тем легче атом отдает электрон, тем сильнее металлические свойства элемента.
Неметалличность – это способность атомов химического элемента присоединять электроны. Количественной характеристикой неметалличности является сродство к электрону.
Сродство к электрону – это энергия, которая выделяется при присоединении электрона к нейтральному атому, т. е. при превращении атома в анион. Чем больше сродство к электрону, тем легче атом присоединяет электрон, тем сильнее неметаллические свойства элемента.
Универсальной характеристикой металличности и неметалличности является электроотрицательность (ЭО) элемента. ЭО элемента характеризует способность его атомов притягивать к себе электроны, которые участвуют в образовании химических связей с другими атомами в молекуле. Чем больше металличность, тем меньше ЭО. Чем больше неметалличность, тем больше ЭО.
Коротко самое главное из лекции в виде таблиц можно посмотреть и скачать здесь
Вопросы к лекции (потренироваться отвечать): ответы на первые 10 вопросов оцениваются в 1 балл (основной уровень) остальные вопросы повышенного уровня (оцениваются в 2 балла)
Проверочный тест “Строение атома” (каждый правильный ответ – 1 балл)
Дополнительное количество баллов можно набрать решив любой вариант данного теста “Периодический закон и ПСХЭ”
Задание по выбору не обязательное, на дополнительную оценку (оценивается от 5 до15 баллов):
А) составьте кроссворд
Б) составьте тест (не менее 10 вопросов)
В) выполните презентацию (не менее 10 слайдов)
Г) сделайте сообщение (на 3 – 4 минуты выступления)
Примерные темы сообщений: строение атома, значение Периодического закона, применение изотопов в медицине.
Занятие № 3
lidijavk.ucoz.ru
Современные представления о строении атома — КиберПедия
Представление о мельчайших неделимых частицах материи – «кирпичиках» мироздания возникло в глубокой древности. Впервые понятие об атоме как последней и неделимой частице тела («атомос» – неделимый, неразложимый) сформулировано в античной Греции в рамках натурфилософского учения. Идея атомизма оказалась весьма продуктивной для объяснения эмпирических законов для процессов в идеальных газах, теплового расширения тел и различных химических законов. Однако к началу XX в. выяснилось, что атом не является неделимым, были экспериментально обнаружены частицы его составляющие – электрон (Дж. Томсон, 1897), протон (Э. Резерфорд, 1919), нейтрон (Д. Чедвик, 1932).
Одной из первых попыток создания на основе накопленных экспериментальных данных модели атома принадлежит Дж. Дж. Томсону (1903). Согласно модели Томсона атом представляет собой равномерно заряженный положительный шар радиусом порядка 10-10 м, внутри которого около положений равновесия колеблются электроны. Суммарный отрицательный заряд электронов равен положительному заряду шара. Модель атома Томсона оказалась несостоятельной и сейчас представляет только исторический интерес.
Большую роль в развитии представлений о строении атома сыграли опыты Э.Резерфорда по рассеянию α-частиц в веществе. Резерфорд предложил ядерную (планетарную) модель атома (1911). Согласно этой модели, вокруг положительно заряженного ядра с зарядом Ze (Z – порядковый номер химического элемента в системе Менделеева, e – элементарный заряд) по замкнутым орбитам движутся Z электронов. Вся масса атома практически сосредоточена в ядре, линейные размеры которого составляют величину порядка 10-15 м. Линейные размеры электронной оболочки атома по порядку величины равны 10-10 м. Заряд ядра равен суммарному заряду электронов; атомы нейтральны.
Модель атома Резерфорда основана на классической электродинамике, согласно которой электрический заряд, движущийся по криволинейной траектории (с ускорением) должен излучать электромагнитные волны и непрерывно терять энергию. Поэтому такая система будет неустойчивой, что противоречит действительности.
Таким образом, построить модель атома в рамках классической физики оказалось невозможным. Попытка построения качественно новой – квантовой – теории атома была предпринята Н. Бором (1913). Бор сформулировал знаменитые постулаты, с помощью которых сумел во многом объяснить закономерности в линейчатых спектрах атома водорода и водородоподобных систем. Однако, будучи внутренне противоречивой (применяя как законы классической физики, так и квантовые постулаты) теория Бора не смогла описать атом гелия – один из простейших атомов, следующий в Периодической системе химических элементов непосредственно за атомом водорода.
Последовательная теория атомных явлений появилась только после создания квантовой механики, описывающей законы движения и взаимодействия микрочастиц с учетом их волновых свойств.
По современным представлениям атом состоит из положительно заряженного ядра, состоящего из протонов и нейтронов, и отрицательно заряженных электронов. Электроны располагаются вокруг ядра в виде электронного облака. Заряд ядра равен суммарному заряду электронов, поэтому атом электрически нейтрален.
Для описания атома в квантовой механике решается уравнение Шредингера, позволяющее найти соответствующие собственные волновые функции и собственные значения энергии. Согласно этому решению, энергия электронов, их орбитальный момент импульса, проекция момента импульса на выделенное направление в пространстве дискретны или квантованы.
Опытные данные свидетельствуют о том, что электрон (и ряд других элементарных частиц) обладают собственным механическим моментом импульса (спином), не связанным с их движением в пространстве. Проекцию момента импульса электрона на выделенное направление в пространстве также оказывается квантованной.
Состояние электрона в атоме описывается набором четырех квантовых чисел: n, l, m и s.
n называется главным квантовым числом и характеризует энергию электрона в атоме.
Орбитальное число l характеризует момент импульса электрона в атоме.
Магнитное число m определяет проекцию момента импульса на выделенное направление в пространстве (например, на направление магнитного поля).
Квантовые числа n и l характеризуют размер и форму электронного облака, а квантовое число m характеризует ориентацию электронного облака в пространстве. На рисунке 14 представлены формы и ориентации электронных облаков различных электронов. Электроны, для которых орбитальное число l=0, называются s-электронами. Для этих электронов электронное облако имеет форму шара. Электронное облако p-электронов (l=1) имеет форму гантели и три возможных ориентации в выбранной системе координат. Электроны, для которых орбитальное число l=2, называются d-электронами; электронное облако d-электронов имеет 5 возможных ориентаций в выбранной системе координат.
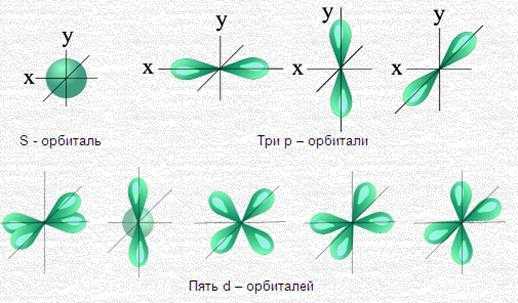
Рисунок 14 – Формы и ориентация в пространстве
различных электронных облаков (орбиталей)
Спиновое число sхарактеризует проекцию момента импульса электрона на выделенное направление в пространстве.
Большое значение в квантовой механике имеет принцип Паули. Применительно к атому этот принцип утверждает, что в атоме не может быть двух электронов, обладающих одинаковым набором всех четырех квантовых чисел. Принцип Паули лежит в основе систематики заполнения электронных состояний в атомах и позволяет объяснить Периодическую систему элементов Д.И. Менделеева.
Исследования спектров излучения разреженных газов (т.е. отдельных атомов) показали, каждому газу присущ вполне определенный линейчатый спектр, состоящий из отдельных спектральных линий и групп близко расположенных линий. На рисунке 15 представлены энергетический спектр и спектральные серии излучения атома водорода. Квантовая механика позволила описать излучение (и поглощение) энергии атомом и, соответственно, объяснить линейчатый спектр. При переходе с одного энергетического уровня (Em) на другой (En) атом испускает или поглощает квант энергии электромагнитного поля (фотон)
hn=Em – En. (5.1)
В зависимости от величины кванта энергии спектральная линия попадает в ультрафиолетовую (УФ), инфракрасную (ИК) области или в область видимого излучения.
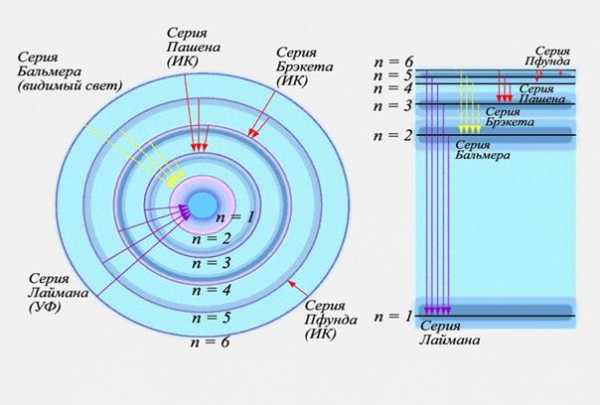
Рисунок 15 – Энергетические уровни атома водорода
Строение атомного ядра
Атомное ядро состоит из элементарных частиц – протонов и нейтронов.Протон (p) имеет положительный заряд, численно равный заряду электрона, и массу покоя, превышающую массу покоя электрона в 1836 раз. Нейтральная частица нейтрон (n) имеет массу, превышающую массу электрона в 1839 раз. Протоны и нейтроны называются нуклонами(от лат. nucleus – ядро), общее число нуклонов в ядре называется массовым числом А. Заряд ядра определяется числом протонов Z, которое называется зарядовым числом. Зарядовое число совпадает с порядковым номером химического элемента в Периодической системе элементов. В настоящее время известно более 100 химических элементов и около 1500 ядер, отличающихся либо А, либо Z, либо тем и другим. Примерно 20 % этих ядер устойчивы, остальные нестабильны (радиоактивны). Ядра с одинаковым зарядовым числом А (одинаковым числом протонов), но разным массовым числом Z(разным числом нейтронов) называются изотопами. Большинство химических элементов имеет по несколько изотопов: кислород имеет три стабильных изотопа (16О, 17О, 18О), у олова 10 изотопов и т.д. Водород имеет три изотопа: стабильные протий 1Н и дейтерий 2Н и радиоактивный тритий 3Н.
Радиус ядра пропорционален массовому числу А и составляет (1,3-1,7)×10-15 м. Плотность ядерного вещества примерно одинакова для всех ядер (1017 кг/м3).
Опыт показывает, что масса ядра меньше суммы масс составляющих нуклонов на величину Dm, называемую дефектом массыядра. Энергия, которую необходимо затратить, чтобы расщепить ядро на отдельные нуклоны, называется энергией связи ядра Wсв. Энергия связи ядра связана с его дефектом массы Dm соотношением Wсв.=Dmc2.
| Важной характеристикой ядра является его удельная энергия связи Wсв/A – энергия связи, отнесенная к одному нуклону. Эта энергия в миллион раз меньше, чем энергия связи электронов в атомах. Из рисунка 16 следует, что наиболее устойчивыми с энергетической точки зрения являются ядра средней части таблицы Менделеева. Тяжелые и легкие ядра менее устойчивы. Это означает, что энергетически выгодны процессы деления тяжелых ядер на более легкие и слияние легких ядер в более тяжелые. |
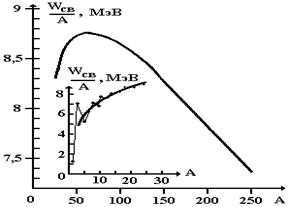 Рисунок 16 – Зависимость удельной энергии связи ядра от числа нуклонов
Рисунок 16 – Зависимость удельной энергии связи ядра от числа нуклонов
|
При обоих процессах выделяется огромное количество энергии; эти процессы в настоящее время осуществлены практически (реакции деления и термоядерного синтеза)
Между составляющими ядро нуклонами действуют особые силы, значительно превышающие кулоновские силы отталкивания между протонами. Эти силы называются ядерными. Отличительные особенности ядерных сил состоят, в частности, в следующем:
Ядерные силы являются короткодействующими. Радиус действия ядерных сил составляет 10-15 м; на расстояниях, больших 10-15 м, ядерное притяжение протонов сменяется их кулоновским отталкиванием.
Ядерные силы обладают зарядовой независимостью. Взаимодействие протона с протоном, протона с нейтроном и нейтрона с нейтроном имеет одинаковую величину.
Ядерные силы обладают свойством насыщения. Каждый нуклон взаимодействует с ограниченным числом нуклонов.
Единая последовательная теория атомного ядра до настоящего времени не разработана. Среди моделей, описывающих свойства ядра, наиболее известны капельная и оболочечная модели. Капельная модель (Н. Бор, Я.И. Френкель, 1936) основана на аналогии между поведением нуклонов в ядре и поведением молекул в капле жидкости. Оболочечная модель (М. Гепперт-Майер, Х. Иенсен, 1950) предполагает распределение нуклонов в ядре по дискретным энергетическим уровням (оболочкам), заполняемым нуклонами согласно принципу Паули. Устойчивость ядер в этой модели связана с заполнением этих оболочек. Наиболее устойчивыми (магическими) оказываются ядра с полностью заполненными оболочками (4Не, 16О, 40Са, 48Са, 208Pb).
cyberpedia.su
