Модели строения атома
Модели строения атома
ВВЕДЕНИЕ
Открытие сложного строения атома – важнейший этап становления современной физики. Первые сведения о строении атома были получены при изучении процессов прохождения электрического тока через жидкости. В тридцатых годах XIX в. опыты выдающегося физика М. Фарадея навели на мысль о том, что электричество существует в виде отдельных единичных зарядов. Открытие самопроизвольного распада атомов некоторых элементов, названное радиоактивностью, стало прямым доказательством сложности строения атома. В 1902 году английские учёные Эрнест Резерфорд и Фредерик Содди доказали, что при радиоактивном распаде атом урана превращается в два атома – атом тория и атом гелия. Это означало, что атомы не являются неизменными, неразрушимыми частицами.
Цель реферата: отразить процесс эволюции представлений о строении атомов на примере моделей Эрнеста Резерфорда и Нильса Бора.
Задачи реферата: изучить, проанализировать, обобщить представления о строении атомов, высказанные Э. Резерфордом и Н. Бором, сделать выводы о наиболее верном, с точки зрения современной физики, предположении.
Практическая значимость реферата заключается в том, чтобы познакомить студентов на лекциях по КСЕ с современными представлениями о строении атома и с вкладом Резерфорда и Бора в изучение этого вопроса.
В процессе работы были использованы различные виды источников: учебники С. Х. Карпенкова и Т.И. Трофимовой, предназначенные для высшей школы. В них доступным языком рассказывается об истории возникновения и развития знаний о строения атома; Интернет – ресурсы. использованные для изучения данной темы с точки зрения современной науки. Данный подход обусловлен стремлением изучить проблему во всей многогранности.
Глава 1. Модели строения атома Томсона и Резерфорда
Представление об атомах как неделимых мельчайших частицах веществ возникло еще в античные времена (Демокрит, Эпикур, Лукреций). В средние века учение об атомах, будучи материалистическим, не получило признания. К началу XVIII в. атомистическая теория приобретает все большую популярность. К этому времени работами французского химика А. Лавуазье (1743-1794), великого русского ученого М.В. Ломоносова и английского химика и физика Д. Дальтона (1766-1844) была доказана реальность существования атомов. Однако в это время вопрос о внутреннем строении атомов даже не возникал, так как атомы считались неделимыми.
Большую роль в развитии атомистической теории сыграл выдающийся русский химик Д.И. Менделеев, разработавший в 1869 г. периодическую систему элементов, в которой впервые на научной основе был поставлен вопрос о единой природе атомов. Во второй половине XIX в. было экспериментально доказано, что электрон является одной из основных частей любого вещества. Эти выводы, а также многочисленные экспериментальные данные привели к тому, что в начале XX в. серьезно встал вопрос о строении атома. Существование закономерной связи между всеми химическими элементами, ярко выраженное в периодической системе Менделеева, наталкивает на мысль о том, что в основе строения всех атомов лежит общее свойство: все они находятся в близком родстве друг с другом.
Первые косвенные подтверждения о сложной структуре атомов были получены при изучении катодных лучей, возникающих при электрическом разряде в сильно разреженных газах. Изучение свойств этих лучей привело к заключению, что они представляют собой поток мельчайших частиц, несущих отрицательный электрический заряд и летящих со скоростью, близкой к скорости света. Кроме того, катодные частицы известны только в заряженном состоянии и не могут быть лишены своих зарядов и превращены в электронейтральные частицы: электрический заряд составляет сущность их природы. Эти частицы, получившие название электронов, были открыты в 1897 г. английским физиком Дж. Томсоном. Ему же принадлежит первая попытка создания на основе накопленных экспериментальных данных модели атома в 1903г. «Согласно этой модели, атом представляет собой непрерывно заряженный положительным зарядом шар, радиусом порядка 10-10 м, внутри которого около своих положений равновесия колеблются электроны; суммарный отрицательный заряд электронов равен положительному заряду шара, поэтому атом в целом нейтрален». [2, с. 334]
Положительно заряженных частиц внутри атома модель атома Томсона (Приложение А) не предполагала. Но как же тогда объяснить испускание положительно заряженных альфа-частиц радиоактивными веществами? Модель атома Томсона не давала ответа и на некоторые другие вопросы.
В 1911 г. английским физиком Эрнестом Резерфордом при исследовании движения альфа-частиц в газах и других веществах была обнаружена положительно заряженная часть атома. Дальнейшие более тщательные исследования показали, что при прохождении пучка параллельных лучей сквозь слои газа или тонкую металлическую пластинку выходят уже не параллельные лучи, а несколько расходящиеся: происходит рассеяние альфа-частиц, т. е. отклонение их от первоначального пути. Углы отклонения невелики, но всегда имеется небольшое число частиц (примерно одна из нескольких тысяч), которые отклоняются очень сильно. Некоторые частицы отбрасываются назад, как если бы на пути встретилась непроницаемая преграда. Это не электроны – их масса гораздо меньше массы альфа-частиц. Отклонение может происходить при столкновении с положительными частицами, масса которых того же порядка, что и масса альфа-частиц. Исходя из этих соображений, Резерфорд предложил ядерную (планетарную) модель строения атома. (Приложение Б)
«В центре атома находится положительно заряженное ядро, вокруг которого по разным орбитам вращаются электроны. Возникающая при их вращении центробежная сила уравновешивается притяжением между ядром и электронами, вследствие чего они остаются на определенных расстояниях от ядра. Поскольку масса электрона ничтожна мала, то почти вся масса атома сосредоточена в его ядре. На долю ядра и электронов, число которых сравнительно невелико, приходится лишь ничтожная часть всего пространства, занятого атомной системой». [1, с. 88]
Предложенная Резерфордом схема строения атома или, как обыкновенно говорят, ядерная модель атома, легко объясняет явления отклонения альфа-частиц. Действительно, размеры ядра и электронов чрезвычайно малы по сравнению с размерами всего атома, которые определяются орбитами наиболее удаленных от ядра электронов, поэтому большинство альфа-частиц пролетает через атомы без заметного отклонения. Только в тех случаях, когда альфа-частица очень близко подходит к ядру, электрическое отталкивание вызывает резкое отклонение ее от первоначального пути. Таким образом, изучение рассеяния альфа-частиц положило начало ядерной теории атома. Но, несмотря на последовательные рассуждения, модель Резерфорда не смогла объяснить все свойства атомов. Так, согласно законам классической физики атом из положительно заряженного ядра и электронов, обращающимся по круговым орбитам, должен излучать электромагнитные волны. «Излучение электромагнитных волн должно приводить к уменьшению запаса потенциальной энергии в системе ядро – электрон, к постепенному уменьшению радиуса орбиты электрона и падению электрона на ядро. Однако атомы обычно не излучают электромагнитные волны, электроны не падают на атомные ядра, то есть атомы устойчивы». Попытки построить модель атома в рамках классической физики не привели к успеху: модель Томсона была опровергнута опытами Резерфорда, ядерная же модель оказалась неустойчивой электродинамически и противоречила опытным данным. Преодоление возникших трудностей потребовало создания качественно новой теории атома.
Глава 2. Модель строения атома Бора.
.1 Постулаты Бора
Первая попытка построить качественно новую – квантовую теорию атома была предпринята в 1913г. датским физиком Нильсом Бором. Он поставил перед собой цель связать в единое целое эмпирические закономерности линейчатых спектров, ядерную модель атома Резерфорда и квантовый характер излучения и поглощения света. В основу своей теории Бор положил ядерную модель Резерфорда. Он предположил, что электроны движутся вокруг ядра по круговым орбитам. Движение по окружности даже с постоянной скоростью обладает ускорением. Такое ускоренное движение заряда эквивалентно переменному току, который создает в пространстве переменное электромагнитное поле. На создание этого поля расходуется энергия. Энергия поля может создаваться за счет энергии кулоновского взаимодействия электрона с ядром. В результате электрон должен двигаться по спирали и упасть на ядро. Однако опыт показывает, что атомы – очень устойчивые образования. Отсюда следует вывод, что результаты классической электродинамики, основанной на уравнениях Максвелла, неприменимы к внутриатомным процессам. Необходимо найти новые закономерности. В основу своей теории Бор положил два постулата.
Первый постулат Бора (постулат стационарных состояний): «в атоме существуют стационарные (не изменяющиеся со временем) состояния, в которых он не излучает энергии. Стационарным состояниям атома соответствуют стационарные орбиты, по которым движутся электроны. Движение электронов по стационарным орбитам не сопровождается излучением электромагнитных волн. В стационарном состоянии атома электрон, двигаясь по круговой орбите должен иметь дискретные квантовые значения момента импульса, удовлетворяющие условию:
mevrn = n? (n = 1, 2, 3,…)
где, me – масса электрона, v – его скорость по n-й орбите радиуса rn, ? = h/(2?)». [2, с. 336]
Второй постулат Бора (правило частот): «при переходе электрона с одной стационарной орбиты на другую излучается (поглощается) один фотон с энергией
= En – Em
равной разности энергий соответствующих стационарных состояний (En и Em – соответственно энергии стационарных состояний атома до и после излучения и поглощения). При En > Em происходит излучение фотона (переход атома из состояния с большей энергией в состояние с меньшей энергией, т.е. переход электрона с более удаленной от ядра орбиты на более близлежащую), при En < Em – его поглощение (переход атома в состояние с большей энергией, т.е. переход атома на более отдалённую от ядра орбиту)».
Теория Бора блестяще объяснила экспериментально наблюдаемый линейчатый спектр водорода. Но успехи теории атома водорода были получены ценой отказа от фундаментальных положений классической механики, которая на протяжении более 200 лет остается безусловно справедливой. Поэтому большое значение имело прямое экспериментальное доказательство справедливости постулатов Бора, особенно первого – о существовании стационарных состояний. Второй постулат можно рассматривать как следствие закона сохранения энергии и гипотезы о существовании фотонов. [1, с.89]
Немецкие физики Д. Франк и Г. Герц, изучая методом задерживающего потенциала столкновение электронов с атомами газов (1913г.), экспериментально подтвердили существование стационарных состояний и дискретность значений энергии атомов.
Несмотря на несомненный успех концепции Бора применительно к атому водорода, для которого оказалось возможным построить количественную теорию спектра, создать подобную теорию для следующего за водородом атома гелия на основе представлений Бора не удалось. Относительно атома гелия и более сложных атомов теория Бора позволила делать лишь качественные (хотя и очень важные) заключения. Представление об определенных орбитах, по которым движется электрон в атоме Бора, оказалось весьма условным. На самом деле движение электронов в атоме имеет мало общего с движением планет по орбитам.
В настоящее время с помощью квантовой механики можно ответить на многие вопросы, касающиеся строения и свойств атомов любых элементов.
2.2. Стационарные орбиты и энергетические уровни
На основании постулатов Бора можно наглядно представить стационарные состояния атома следующим образом.
Центростремительное ускорение ? при движении электрона по окружности создается кулоновской силой Fэ. Следовательно,
= v2/r = Fэ/m
В атоме водорода заряд ядра равен заряду e электрона, поэтому для атома водорода получим:
/r = e2/4??0mr2
откуда
v2 = e2/4??0mr
Двигаясь по каждой из разреженных стационарных круговых орбит, электрон обладает определенным запасом кинетической энергии, а также и потенциальной энергией в электрическом поле атомного ядра. Обозначим через En сумму кинетической энергии электрона на стационарной орбите с номером n и потенциальной энергии взаимодействия электрона с атомным ядром. Тогда каждой разрешенной стационарной орбите электрона в атоме можно поставить соответствие в значение энергии атома в стационарном состоянии. Для наглядного представления возможных энергетических состояний атомов используются энергетические диаграммы. (Приложение В)
На энергетической диаграмме каждое стационарное состояние атома отмечается горизонтальной линией, называемой энергетическим уровнем. Ниже всех остальных на диаграмме располагается энергетический уровень, соответствующий энергии E1 основного состояния атома, энергетические уровни возбужденных состояний располагаются над основным уровнем на расстояниях, пропорциональных разности энергий возбужденного и основного состояний. Переходы атома из одного состояния в другое изображаются вертикальными линиями между соответствующими уровнями на энергетической диаграмме, направление перехода указывается стрелкой.
Переходу электрона со стационарной орбиты под номером m на стационарную орбиту под номером n соответствует переход атома из состояния с энергией Em в состояние с энергией En. Этот переход на диаграмме энергетических уровней обозначается вертикальной стрелкой от уровня Em к уровню En. (Приложение Г)
2.3 Объяснение происхождения линейчатых спектров
Постулаты Бора позволяют объяснить происхождение линейчатых спектров излучения и поглощения, связывая их существование с наличием дискретного ряда энергетических состояний атомов.
Все атомы одного химического элемента обладают одинаковым зарядом атомного ядра. При одинаковом заряде ядра атомы обладают одинаковым строением электронных оболочек и потому имеют одинаковый набор возможных энергетических состояний и переходов между ними. Излучение и поглощение фотонов происходит при переходах атомов из одного разрешенного стационарного состояния в другое. Энергия фотона, поглощаемого атомом при переходе из нормального состояния с энергией E1 в возбужденное состояние с энергией En, в точности равна энергии фотона, излучаемого атомом при обратном переходе, так как и в том, и в другом случае она равна разности энергий атома в этих двух состояниях:
= En – E1
2.4 Достоинства и недостатки теории Бора
. Достоинства теории Бора.
Теория Бора подошла к объяснению внутриатомных процессов с принципиально новых позиций, стала первой полуквантовой теорией атома. Она объяснила дискретность энергетических состояний водородоподобных атомов. Эвристическое значение теории Бора состоит в смелом предположении о существовании стационарных состояний и скачкообразных переходов между ними. Эти положения позднее были распространены и на другие микросистемы. Теория объясняет границу таблицы Менделеева. «Последний атом, способный существовать физически, имеет порядковый номер 137, так как начиная со 138-го элемента 1s-электрон должен двигаться со сверхсветовой скоростью, что противоречит специальной теории относительности». [4]
. Недостатки теории Бора
Теория Бора логически противоречива: не является ни классической, ни квантовой. В системе двух уравнений, лежащих в её основе, одно – уравнение движения электрона – классическое, другое – уравнение квантования орбит – квантовое. Также, она не смогла объяснить интенсивность спектральных линий. Даная теория справедлива только для водородоподобных атомов и не работает для атомов, следующих за ним в таблице Менделеева без экспериментальных данных (энергии ионизации или других). Теория Бора являлась недостаточно последовательной и общей. Поэтому она в дальнейшем была заменена современной квантовой механикой, основанной на более общих и непротиворечивых исходных положениях. Сейчас известно, что постулаты Бора являются следствиями более общих квантовых законов. Но правила квантования широко используются и в наши дни как приближенные соотношения: их точность часто бывает очень высокой.
Итак, теория Бора – это крупный шаг в развитии атомной физики. Она является важным этапом в создании квантовой механики. Однако эта теория обладает многими противоречиями (с одной стороны, применяет законы классической физики, а с другой – основывается на квантовых постулатах). Она рассмотрела спектры атома водорода и водородоподобных систем и вычислила частоты спектральных линий, однако не смогла объяснить их интенсивности и ответить на вопрос: почему совершаются те или иные переходы? Серьезным недостатком теории Бора была невозможность описания с ее помощью спектра – атома гелия – одного из простейших атомов, непосредственно следующего за атомом водорода.
орбита излучение бор энергетический
Заключение
В ХХ веке некоторые положения теории Н. Бора были дополнены и переосмыслены. Наиболее значительным изменением стало введение понятия об электронном облаке, которое сменило понятие об электроне только как частице. Позже теорию Бора сменила квантовая теория Альберта Эйнштейна, которая учитывает волновые свойства электрона и других элементарных частиц, образующих атом.
Основой современной теории строения атома является планетарная модель, дополненная и усовершенствованная. Согласно данной теории, ядро атома состоит из протонов (положительно заряженных частиц) и нейронов (не имеющих заряда частиц). А вокруг ядра по неопределённым траекториям движутся электроны (отрицательно заряженные частицы).
В ходе данного исследования был отражен процесс эволюции представлений о строении атомов на примере моделей Эрнеста Резерфорда и Нильса Бора. Полностью изучены, проанализированы и обобщены представления о строении атомов, высказанные Резерфордом и Бором. С точки зрения современной физики, наиболее верное предположение о строении атома было сделано датским ученым – Нильсом Бором.
На одной из лекций по КСЕ студенты будут ознакомлены с современными представлениями о строении атома и с вкладом Резерфорда и Бора в изучение этого вопроса.
Библиографический список
1. Карпенков, С. Х. Концепции современного естествознания: Практикум: учебное пособие / С. Х. Карпенков. – М.: Культура и спорт, 1998. – 237с.
. Трофимова, Т.И. Курс физики: учебное пособие / Т. И. Трофимова – М.: Высшая школа, 1990. – 478с.
ПРИЛОЖЕНИЯ
ПРИЛОЖЕНИЕ А
П. 1.1. Модель строения атома Томсона («кекс с изюмом»)
ПРИЛОЖЕНИЕ Б
П. 2.1 Модель строения атома Резерфорда (ядерная)
ПРИЛОЖЕНИЕ В
П. 3.1. Энергетическая диаграмма Бора
ПРИЛОЖЕНИЕ Г
П. 4.1 Модель строения атома Бора (планетарная)
Теги: Модели строения атома Реферат Физика
Просмотров: 9507
Найти в Wikkipedia статьи с фразой: Модели строения атома
diplomba.ru
Строение атома Первая попытка создания модели атома
 Строение атома
Строение атома
 Первая попытка создания модели атома принадлежит Дж. Томсону (1903 г. ). Он считал, что атом представляет собой электронейтральную систему шарообразной формы радиусом примерно равным 1010 м. Положительный заряд атома равномерно распределен по всему объему шара, а отрицательно заряженные электроны находятся 2
Первая попытка создания модели атома принадлежит Дж. Томсону (1903 г. ). Он считал, что атом представляет собой электронейтральную систему шарообразной формы радиусом примерно равным 1010 м. Положительный заряд атома равномерно распределен по всему объему шара, а отрицательно заряженные электроны находятся 2
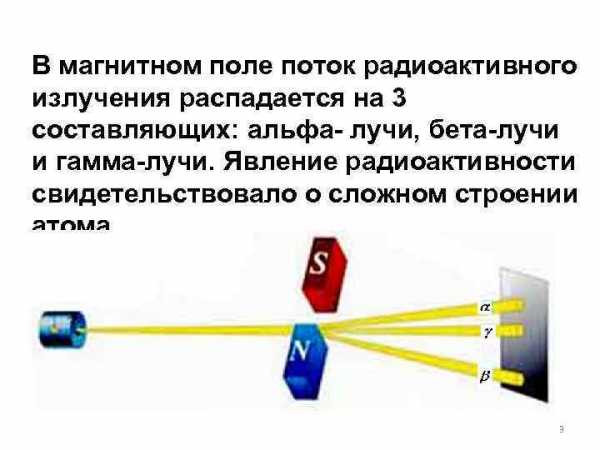 В магнитном поле поток радиоактивного излучения распадается на 3 составляющих: альфа- лучи, бета-лучи и гамма-лучи. Явление радиоактивности свидетельствовало о сложном строении атома. 3
В магнитном поле поток радиоактивного излучения распадается на 3 составляющих: альфа- лучи, бета-лучи и гамма-лучи. Явление радиоактивности свидетельствовало о сложном строении атома. 3
 Первые прямые эксперименты по исследованию внутренней структуры атомов были выполнены Э. Резерфордом и его сотрудниками Э. Марсденом и Х. Гейгером в 1909– 1911 годах. Резерфорд предложил применить зондирование атома с помощью αчастиц, которые возникают при радиоактивном распаде радия и некоторых других элементов. 4
Первые прямые эксперименты по исследованию внутренней структуры атомов были выполнены Э. Резерфордом и его сотрудниками Э. Марсденом и Х. Гейгером в 1909– 1911 годах. Резерфорд предложил применить зондирование атома с помощью αчастиц, которые возникают при радиоактивном распаде радия и некоторых других элементов. 4
 Эрне ст Ре зерфорд (Ernest Rutherford; 1871 – 1937, Спринг Грув ) — британский физик и новозеландского происхождения. Создал планетарную модель атома. Лауреат Нобелевской премии по химии 1908 г. Открыл альфа- и бета-излучение и множество изотопов. Открыл и объяснил радиоактивное превращение химических элементов, создал теорию радиоактивного распада, Доказал, что расщепил атом азота, обнаружил протон. альфа-частица — ядро гелия. Первым открыл образование новых химических элементов при распаде тяжелых химических радиоактивных элементов. Уточнил на 30 % отношение заряда к массе электрона. 12 учеников Резерфорда стали лауреатами Нобелевской премии по физике и химии. 5
Эрне ст Ре зерфорд (Ernest Rutherford; 1871 – 1937, Спринг Грув ) — британский физик и новозеландского происхождения. Создал планетарную модель атома. Лауреат Нобелевской премии по химии 1908 г. Открыл альфа- и бета-излучение и множество изотопов. Открыл и объяснил радиоактивное превращение химических элементов, создал теорию радиоактивного распада, Доказал, что расщепил атом азота, обнаружил протон. альфа-частица — ядро гелия. Первым открыл образование новых химических элементов при распаде тяжелых химических радиоактивных элементов. Уточнил на 30 % отношение заряда к массе электрона. 12 учеников Резерфорда стали лауреатами Нобелевской премии по физике и химии. 5
 Масса α-частиц приблизительно в 7300 раз больше массы электрона, а положительный заряд равен удвоенному элементарному заряду. В своих опытах Резерфорд использовал α-частицы с кинетической энергией около 5 Мэ. В (скорость таких частиц очень велика – порядка 107 м/с, но она все же значительно меньше скорости света). α-частицы – это 6
Масса α-частиц приблизительно в 7300 раз больше массы электрона, а положительный заряд равен удвоенному элементарному заряду. В своих опытах Резерфорд использовал α-частицы с кинетической энергией около 5 Мэ. В (скорость таких частиц очень велика – порядка 107 м/с, но она все же значительно меньше скорости света). α-частицы – это 6
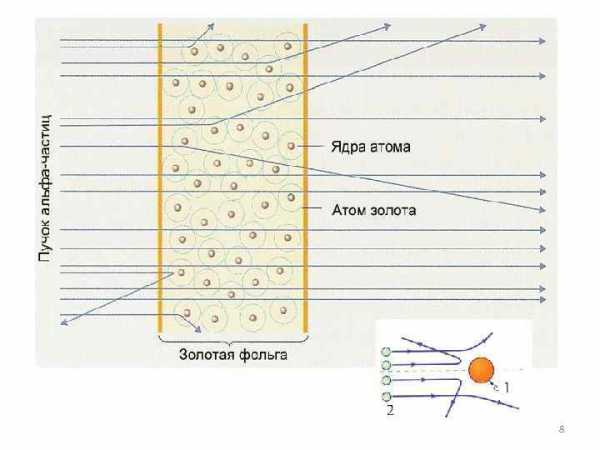
 Пучок aльфа-частиц пропускался через тонкую золотую фольгу. Золото было выбрано как очень пластичный материал, из которого можно получить фольгу толщиной практически в один атомный слой. Некоторые альфа-частицы проходили сквозь фольгу, образуя на экране размытое пятно, а следы от других альфа-частиц были зафиксированы на боковых 7
Пучок aльфа-частиц пропускался через тонкую золотую фольгу. Золото было выбрано как очень пластичный материал, из которого можно получить фольгу толщиной практически в один атомный слой. Некоторые альфа-частицы проходили сквозь фольгу, образуя на экране размытое пятно, а следы от других альфа-частиц были зафиксированы на боковых 7
 8
8
 Опыты Резерфорда и его сотрудников привели к выводу, что в центре атома находится плотное положительно заряженное ядро, диаметр которого не превышает 10– 14– 10– 15 м. Это ядро занимает только 10– 12 часть полного объема атома, но содержит весь положительный заряд и не менее 99, 95 % его массы. Веществу, составляющему ядро атома, следовало приписать плотность порядка ρ ≈ 1015 г/см 3. Заряд ядра должен быть равен суммарному заряду всех электронов, 9
Опыты Резерфорда и его сотрудников привели к выводу, что в центре атома находится плотное положительно заряженное ядро, диаметр которого не превышает 10– 14– 10– 15 м. Это ядро занимает только 10– 12 часть полного объема атома, но содержит весь положительный заряд и не менее 99, 95 % его массы. Веществу, составляющему ядро атома, следовало приписать плотность порядка ρ ≈ 1015 г/см 3. Заряд ядра должен быть равен суммарному заряду всех электронов, 9
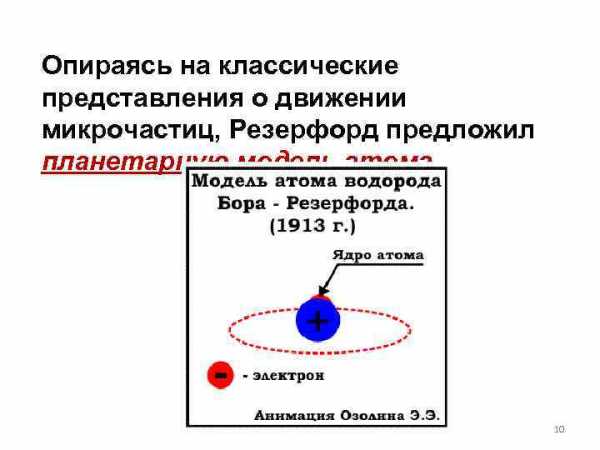 Опираясь на классические представления о движении микрочастиц, Резерфорд предложил планетарную модель атома. 10
Опираясь на классические представления о движении микрочастиц, Резерфорд предложил планетарную модель атома. 10
 Следующий шаг в развитии представлений об устройстве атома сделал в 1913 году датский физик Н. Бор. Первый постулат Бора (постулат стационарных состояний) гласит: атомная система может находится только в особых стационарных или квантовых состояниях, каждому из которых соответствует определенная энергия En. В стационарных состояниях атом не 11
Следующий шаг в развитии представлений об устройстве атома сделал в 1913 году датский физик Н. Бор. Первый постулат Бора (постулат стационарных состояний) гласит: атомная система может находится только в особых стационарных или квантовых состояниях, каждому из которых соответствует определенная энергия En. В стационарных состояниях атом не 11
 Второй постулат Бора (правило частот) формулируется следующим образом: при переходе атома из одного стационарного состояния с энергией En в другое стационарное состояние с энергией Em излучается или поглощается квант, энергия которого равна h – разности энергий постоянная стационарных состояний: Планка, равная 6. 626 10 -34 Дж с 12
Второй постулат Бора (правило частот) формулируется следующим образом: при переходе атома из одного стационарного состояния с энергией En в другое стационарное состояние с энергией Em излучается или поглощается квант, энергия которого равна h – разности энергий постоянная стационарных состояний: Планка, равная 6. 626 10 -34 Дж с 12
 Третий постулат (Правило квантования). Бор предположил, что из всех возможных орбит электрона осуществляются только те для которых момент импульса равен целому кратному постоянной планка h, деленной на 2π: Число n – называется квантовым числом. главным 13
Третий постулат (Правило квантования). Бор предположил, что из всех возможных орбит электрона осуществляются только те для которых момент импульса равен целому кратному постоянной планка h, деленной на 2π: Число n – называется квантовым числом. главным 13
 n принимает значения от 1 до ∞. Чем меньше n, тем больше энергия взаимодействия электрона с ядром. При n = 1 атом водорода находится в основном состоянии, при n > 1 – в возбужденном. В многоэлектронных атомах электроны с одинаковыми значениями n образуют слой или оболочку, обозначаемый буквами K, L, M, N, O, P и Q. Буква K соответствует первому уровню, L – второму и т. д. 14
n принимает значения от 1 до ∞. Чем меньше n, тем больше энергия взаимодействия электрона с ядром. При n = 1 атом водорода находится в основном состоянии, при n > 1 – в возбужденном. В многоэлектронных атомах электроны с одинаковыми значениями n образуют слой или оболочку, обозначаемый буквами K, L, M, N, O, P и Q. Буква K соответствует первому уровню, L – второму и т. д. 14
 Нильс Хе нрик Дави д Бор (Niels Henrik David Bohr 1885 – 1962 , Копенгаген) — датский физик-теоретик и общественный деятель, один из создателей современной физики. Лауреат нобелевской премии по физике (1922) Бор известен как создатель активный участник разработки основ квантовой первой квантовой теории механики. Также он внёс значительный вклад в атома и развитие теории атомного ядра и ядерных реакций, процессов взаимодействия элементарных частиц со средой. 15
Нильс Хе нрик Дави д Бор (Niels Henrik David Bohr 1885 – 1962 , Копенгаген) — датский физик-теоретик и общественный деятель, один из создателей современной физики. Лауреат нобелевской премии по физике (1922) Бор известен как создатель активный участник разработки основ квантовой первой квантовой теории механики. Также он внёс значительный вклад в атома и развитие теории атомного ядра и ядерных реакций, процессов взаимодействия элементарных частиц со средой. 15
 Применим полуклассический подход Бора к описанию движения электрона в поле ядра с зарядом Ze. При Z=1 такая система соответствует атому водорода. Произведение массы электрона на его центростремительное ускорение должно равняться силе Кулона, действующей на электрон: 16
Применим полуклассический подход Бора к описанию движения электрона в поле ядра с зарядом Ze. При Z=1 такая система соответствует атому водорода. Произведение массы электрона на его центростремительное ускорение должно равняться силе Кулона, действующей на электрон: 16
 Радиус может принимать только дискретные значения. Внутренняя энергия атома складывается из энергии взаимодействия электрона с ядром и кинетической электрона: Кинетическую энергию находим следующим образом: 17
Радиус может принимать только дискретные значения. Внутренняя энергия атома складывается из энергии взаимодействия электрона с ядром и кинетической электрона: Кинетическую энергию находим следующим образом: 17
 Тогда внутренняя энергия атома Окончательно 18
Тогда внутренняя энергия атома Окончательно 18
 При переходе атома водорода (Z=1) из состояния n в состояние m излучается квант Частота испущенного свет равна: 19
При переходе атома водорода (Z=1) из состояния n в состояние m излучается квант Частота испущенного свет равна: 19
 Спектры атомов – линейчатые, спектры молекул – полосчатые, спектры твердого тела – сплошные 20
Спектры атомов – линейчатые, спектры молекул – полосчатые, спектры твердого тела – сплошные 20
 Элементы квантовой теории
Элементы квантовой теории
 В 1923 году французский физик Л. де Бройль выдвинул гипотезу об универсальности корпускулярно-волнового дуализма: не только фотоны, но и электроны и любые другие частицы материи наряду с корпускулярными обладают также и волновыми свойствами. Согласно де Бройлю, с каждым микрообъектом связаны, с одной стороны, корпускулярные характеристики – энергия E и импульс p, а с другой стороны, 22
В 1923 году французский физик Л. де Бройль выдвинул гипотезу об универсальности корпускулярно-волнового дуализма: не только фотоны, но и электроны и любые другие частицы материи наряду с корпускулярными обладают также и волновыми свойствами. Согласно де Бройлю, с каждым микрообъектом связаны, с одной стороны, корпускулярные характеристики – энергия E и импульс p, а с другой стороны, 22
 Луи де Бройль ( 1892 -1987) — французский физик-теоретик, один из основоположников квантовой механики, лауреат Нобелевской премии по физике за 1929 год. Ему принадлежит гипотеза о свойствах материальных частиц, положившая волновых начало развитию волновой механики. Он предложил оригинальную интерпретацию квантовой механики, развивал релятивистскую теорию частиц, занимался вопросами радиофизики, классической и квантовой теориями поля, и других разделов физики.
Луи де Бройль ( 1892 -1987) — французский физик-теоретик, один из основоположников квантовой механики, лауреат Нобелевской премии по физике за 1929 год. Ему принадлежит гипотеза о свойствах материальных частиц, положившая волновых начало развитию волновой механики. Он предложил оригинальную интерпретацию квантовой механики, развивал релятивистскую теорию частиц, занимался вопросами радиофизики, классической и квантовой теориями поля, и других разделов физики.
 Корпускулярные и волновые характеристики микрообъектов связаны такими же количественными соотношениями, как и у фотона: 24
Корпускулярные и волновые характеристики микрообъектов связаны такими же количественными соотношениями, как и у фотона: 24
 Любой частице, обладающей импульсом, сопоставлялся волновой процесс с длиной волны λ = h / p. Для частиц, имеющих массу, 25
Любой частице, обладающей импульсом, сопоставлялся волновой процесс с длиной волны λ = h / p. Для частиц, имеющих массу, 25
 Электрону, движущемуся со скоростью 1000000 м/с = 106 м/с, соответствует волна де Бройля 10 -9 м Пылинке массой 1 мг = 10 -6 кг, движущейся со скоростью 1 м/с. соответствует волна де Бройля 10 -28 м
Электрону, движущемуся со скоростью 1000000 м/с = 106 м/с, соответствует волна де Бройля 10 -9 м Пылинке массой 1 мг = 10 -6 кг, движущейся со скоростью 1 м/с. соответствует волна де Бройля 10 -28 м
 Подтверждением квантовой природы света является эффект Комптона. В 1923 году американский физик Артур Комптон наблюдал рассеяние рентгеновских волн с длиной волны легкими веществами (парафин). 27
Подтверждением квантовой природы света является эффект Комптона. В 1923 году американский физик Артур Комптон наблюдал рассеяние рентгеновских волн с длиной волны легкими веществами (парафин). 27
 Первое экспериментальное подтверждение гипотезы де Бройля было получено в 1927 году американскими физиками К. Девиссоном и Л. Джермером. Они обнаружили, что пучок электронов, рассеивающийся на кристалле никеля, дает отчетливую дифракционную картину, подобную той, которая возникает при рассеянии на кристалле коротковолнового рентгеновского излучения. В этих экспериментах кристалл играл роль естественной дифракционной решетки. По положению дифракционных максимумов была определена длина волны электронного 28
Первое экспериментальное подтверждение гипотезы де Бройля было получено в 1927 году американскими физиками К. Девиссоном и Л. Джермером. Они обнаружили, что пучок электронов, рассеивающийся на кристалле никеля, дает отчетливую дифракционную картину, подобную той, которая возникает при рассеянии на кристалле коротковолнового рентгеновского излучения. В этих экспериментах кристалл играл роль естественной дифракционной решетки. По положению дифракционных максимумов была определена длина волны электронного 28
 29
29
 В 1928 году английский физик Дж. Томсон получил новое подтверждение гипотезы де Бройля. Томсон наблюдал дифракционную картину, возникающую при прохождении пучка электронов через тонкую поликристаллическую фольгу из золота. На фотопластинке отчетливо наблюдались концентрические светлые и темные кольца, радиусы которых изменялись с изменением скорости 30
В 1928 году английский физик Дж. Томсон получил новое подтверждение гипотезы де Бройля. Томсон наблюдал дифракционную картину, возникающую при прохождении пучка электронов через тонкую поликристаллическую фольгу из золота. На фотопластинке отчетливо наблюдались концентрические светлые и темные кольца, радиусы которых изменялись с изменением скорости 30
 Микрочастица – это образование особого рода: частица+волна. Все это привело к необходимости построения непротиворечивой теории, объясняющей процессы, происходящие в микромире. За короткий период с июня 1925 го года и по июнь 1926 -го года, были опубликованы сразу три оригинальных и независимо сделанных варианта полной квантовой теории. Первая – матричная квантовая механика – Вернером Гейзенбергом (1901 -76). Вторая – волновая механика – Эрвином Шредингером (1887 -1961). Третья – квантовая алгебра – Паулем Дираком (1902 – 1984). 31
Микрочастица – это образование особого рода: частица+волна. Все это привело к необходимости построения непротиворечивой теории, объясняющей процессы, происходящие в микромире. За короткий период с июня 1925 го года и по июнь 1926 -го года, были опубликованы сразу три оригинальных и независимо сделанных варианта полной квантовой теории. Первая – матричная квантовая механика – Вернером Гейзенбергом (1901 -76). Вторая – волновая механика – Эрвином Шредингером (1887 -1961). Третья – квантовая алгебра – Паулем Дираком (1902 – 1984). 31
 Состояние микрочастицы описывается в квантовой механике волновой функцией Ψ. Она является функцией координат и времени и может быть найдена путем решения уравнения: Это уравнение было установлено Шредингером в 1926 г. И называется общим уравнением Шредингера. i – мнимая единица, m – масса частицы, – оператор Лапласа, U – потенциальная 32
Состояние микрочастицы описывается в квантовой механике волновой функцией Ψ. Она является функцией координат и времени и может быть найдена путем решения уравнения: Это уравнение было установлено Шредингером в 1926 г. И называется общим уравнением Шредингера. i – мнимая единица, m – масса частицы, – оператор Лапласа, U – потенциальная 32
 – оператор Лаплас Это соотношение называется уравнением Шредингера для стационарных состояний. 33
– оператор Лаплас Это соотношение называется уравнением Шредингера для стационарных состояний. 33
 Физический смысл Ψ функции состоит в следующем: квадрат модуля Ψ определяет вероятность d. P того, что частица будет обнаружена в пределах объема d. V: Волновые функции должны всегда быть нормированы таким образом, чтобы: 34
Физический смысл Ψ функции состоит в следующем: квадрат модуля Ψ определяет вероятность d. P того, что частица будет обнаружена в пределах объема d. V: Волновые функции должны всегда быть нормированы таким образом, чтобы: 34
 Волновые функции, получаемые из решений уравнения Шредингера должны удовлетворять следующим условиям: 1) однозначность; 2) конечность; 3) непрерывность. Эти условия должны выполняться во всей области изменения переменных x, y, z. Они являются следствием того факта, что волновая функция по своему физическому смыслу 35
Волновые функции, получаемые из решений уравнения Шредингера должны удовлетворять следующим условиям: 1) однозначность; 2) конечность; 3) непрерывность. Эти условия должны выполняться во всей области изменения переменных x, y, z. Они являются следствием того факта, что волновая функция по своему физическому смыслу 35
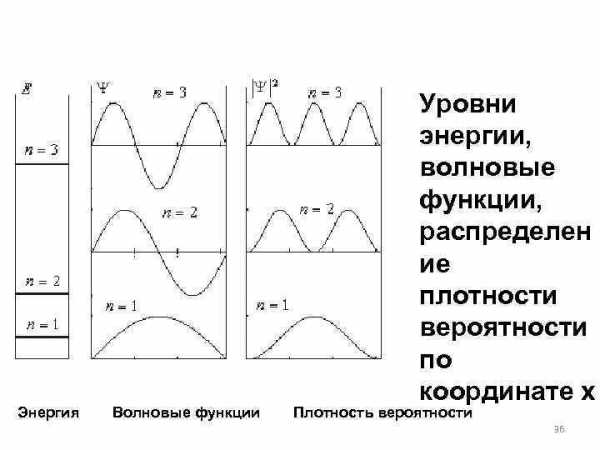 Уровни энергии, волновые функции, распределен ие плотности вероятности по координате х Энергия Волновые функции Плотность вероятности 36
Уровни энергии, волновые функции, распределен ие плотности вероятности по координате х Энергия Волновые функции Плотность вероятности 36
 Соотношения неопределенностей, установлены В. Гейзенбергом. Первое из них ограничивает точности одновременного измерения координат и соответствующих проекций импульса частицы. Для проекции, например на ось Х оно выглядит следующим образом: Второе соотношение устанавливает неопределенность измерения энергии, ΔЕ, за данный промежуток времени Δt: 37
Соотношения неопределенностей, установлены В. Гейзенбергом. Первое из них ограничивает точности одновременного измерения координат и соответствующих проекций импульса частицы. Для проекции, например на ось Х оно выглядит следующим образом: Второе соотношение устанавливает неопределенность измерения энергии, ΔЕ, за данный промежуток времени Δt: 37
 Многоэлектронные атомы В многоэлектронных атомах электроны с одинаковыми значениями n (n – главное квантовое число)образуют слой или оболочку, обозначаемый буквами K, L, M, N, O, P и Q. Буква K соответствует первому уровню, L – второму и т. д. 38
Многоэлектронные атомы В многоэлектронных атомах электроны с одинаковыми значениями n (n – главное квантовое число)образуют слой или оболочку, обозначаемый буквами K, L, M, N, O, P и Q. Буква K соответствует первому уровню, L – второму и т. д. 38
 39
39
 Орбитальное (азимутальное) квантовое число — в квантовой физике квантовое число ℓ, определяющее форму электронного облака. Определяет подуровень энергетического уровня, задаваемого главным квантовым числом n и может принимать значения. l = 0, 1, 2, …; n-1 40
Орбитальное (азимутальное) квантовое число — в квантовой физике квантовое число ℓ, определяющее форму электронного облака. Определяет подуровень энергетического уровня, задаваемого главным квантовым числом n и может принимать значения. l = 0, 1, 2, …; n-1 40
 Кроме числовых ℓ имеет буквенные обозначения. Электроны с одинаковым значением ℓ образуют подуровень. Квантовое число ℓ определяет квантование орбитального момента количества движения электрона в сферически симметричном кулоновском поле ядра. ℓ = 0 1 2 3 4 … ℓ = s p d f g … 41
Кроме числовых ℓ имеет буквенные обозначения. Электроны с одинаковым значением ℓ образуют подуровень. Квантовое число ℓ определяет квантование орбитального момента количества движения электрона в сферически симметричном кулоновском поле ядра. ℓ = 0 1 2 3 4 … ℓ = s p d f g … 41
 42
42
 Орбитальное квантовое число Магнитное квантовое число ℓ Число орбиталей с данным значением l 2ℓ + 1 0 (s) 0 1 1 (p) – 1, 0, +1 3 2 (d) 3 (f) – 2, – 1, 0, +1, +2 – 3, – 2, – 1, 0, 5 7 43
Орбитальное квантовое число Магнитное квантовое число ℓ Число орбиталей с данным значением l 2ℓ + 1 0 (s) 0 1 1 (p) – 1, 0, +1 3 2 (d) 3 (f) – 2, – 1, 0, +1, +2 – 3, – 2, – 1, 0, 5 7 43
 44
44
 1907) – русский химик, педагог, разносторонний ученый. Оставил свыше 500 печатных трудов, среди которых классические “Основы химии” — первое стройное изложение неорганической химии. Автор фундаментальных исследований по химии, химической технологии, физике, метеорологии, воздухоплаванию, сельскому 6 марта 1869 хозяйству, народному просвещению и года на заседании Русского физикохимического общества профессор Н. А. Меншуткин др. прочитал доклад Менделеева “Опыт системы элементов, основанной на их атомном весе и химическом сродстве”. Это была самая первая формулировка всемирно известного Периодического закона, окончательная редакция которого вышла в 1869 -1870 годах и является одним из фундаментальных 45
1907) – русский химик, педагог, разносторонний ученый. Оставил свыше 500 печатных трудов, среди которых классические “Основы химии” — первое стройное изложение неорганической химии. Автор фундаментальных исследований по химии, химической технологии, физике, метеорологии, воздухоплаванию, сельскому 6 марта 1869 хозяйству, народному просвещению и года на заседании Русского физикохимического общества профессор Н. А. Меншуткин др. прочитал доклад Менделеева “Опыт системы элементов, основанной на их атомном весе и химическом сродстве”. Это была самая первая формулировка всемирно известного Периодического закона, окончательная редакция которого вышла в 1869 -1870 годах и является одним из фундаментальных 45
 Периодическая система химических элементов (таблица Менделеева) — классификация химических элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра. Система является графическим выражением периодического закона, установленного русским химиком Д. И. Менделеевым в 1869 году. В современном варианте системы предполагается сведение элементов в двумерную таблицу, в которой каждый столбец (группа) определяет основные физико -химические свойства, а строки представляют 46 собой периоды, в определённой мере
Периодическая система химических элементов (таблица Менделеева) — классификация химических элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра. Система является графическим выражением периодического закона, установленного русским химиком Д. И. Менделеевым в 1869 году. В современном варианте системы предполагается сведение элементов в двумерную таблицу, в которой каждый столбец (группа) определяет основные физико -химические свойства, а строки представляют 46 собой периоды, в определённой мере
 47
47
 Контрольные вопросы 1. Модели атома 2. Опыт Резерфорда по строению атома 3. Постулаты Бора 4. Квантовые числа 5. Волна де Бройля и ее корпускулярные и волновые характеристики 6. Стационарное уравнение Шредингера
Контрольные вопросы 1. Модели атома 2. Опыт Резерфорда по строению атома 3. Постулаты Бора 4. Квантовые числа 5. Волна де Бройля и ее корпускулярные и волновые характеристики 6. Стационарное уравнение Шредингера
present5.com
Первые модели строения атома – Справочник химика 21
Атом давно перестал быть неделимым. После открытия естественной радиоактивности, катодных лучей и электронов были предложены первые модели строения атомов. Согласно модели первооткрывателя электрона Томсона (1904) атом представляет собой сферу положительного электричества одинаковой плотности пО всему объему диаметром порядка 0,1 нм. Электроны как бы плавают в этой сфере, нейтрализуя положительный заряд. Колебательное движение электронов возбуждает в пространстве электромагнитные волны. Экспериментальную проверку этих наглядных представлений предпринял английский физик Эрнест Резерфорд в-своих знаменитых опытах по рассеянию а-частиц (ядра атома гелия). Схема установки Резерфорда (1907) приведена на рис. 8. Радиоактивный препарат Р излучает а-частицы ( снаряды ) в виде узкого пучка, на пути движения которого ставится тонкая золотая фольга Ф. Регистрация а-частиц, прошедших через фольгу, производится микроскопом М на люминесцирующем экране Э по вспышке световых точек сцинтилляция). Если модель атома Томсона верна, а-частицы не могут пройти даже через очень тонкую фоль- [c.31]В 1910 г. датский ученый Н.Бор, используя модель Резерфорда и теорию Планка, предложил модель строения атома водорода, согласно которой электроны двигаются вокруг ядра не по любым, а лишь по разрешенным орбитам, на которых электрон обладает определенными энергиями. При переходе электрона с одной орбиты на другую атом поглощает или испускает энергию в виде квантов. Каждая орбита имеет номер и (1, 2, 3, 4,. ..), который назвали главным квантовым числом. Бор вычислил радиусы орбит. Радиус первой орбиты был 5,29-10 м, радиус других орбит был равен [c.19]
Ядерная модель атома. Одна из первых моделей строения атома была предложена английским физиком Э. Резерфордом. В опытах по рассеянию а-частиц было показано, что почти вся масса атома сосредоточена в очень малом объеме — положительно заряженном ядре. Согласно модели Резерфорда, вокруг ядра на относительно большом расстоянии непрерывно движутся электроны, причем их количество таково, что в целом атом электрически нейтрален. Позднее наличие в атоме тяжелого ядра, окруженного электронами, было подтверждено другими учеными. [c.10]
Магнитные свойства ферромагнитных материалов определяются магнитными свойствами многоэлектронного атома. Однако далеко не все материалы с многоэлектронными атомами обладают ферромагнитными свойствами. Строение атомов ферромагнитных материалов имеет ряд особенностей. Атом состоит из положительно заряженного ядра, вокруг которого вращаются электроны, образующие электронные слои и оболочки. Число электронных слоев определяют главным квантовым числом, которое принимает целые значения 1, 2, 3,. .., п. Число оболочек в слое выражают орбитальным квантовым числом I и обозначают их буквами 8, р, планетарная модель атома железа, из которого видно, что в атоме содержится четыре электронных слоя. В первом слое находится одна электронная оболочка 18 с двумя электронами во втором слое содержатся оболочки 28 с двумя электронами, 2р с шестью электронами в третьем слое – оболочка Зз с двумя электронами, оболочка Зр с шестью электронами и оболочка 3(1 с шестью [c.238]
Одну из первых моделей строения атома предложил английский-физик Дж. Дж. Томсон (1904 г.). Он предположил, что атом представляет собой положительно заряженную сферическую частицу, внутри которой распределены электроны, компенсирующие положительный заряд этой частицы. Электроны распределены равномерно и колеблются относительно своих равновесных положений, при химических реакциях электроны могут переходить от одних атомов-к другим с образованием заряженных частиц — ионов. Эта первая модель строения атома получила впоследствии название пудинга Томсона (электроны, вставленные в положительно заряженную сферу, выглядели наподобие изюминок в пудинге ). [c.32]
Н. Бор в 1913 г. впервые четко сформулировал вывод, что классическая электродинамика недостаточна для описания систем атомного размера [42]. Этот вывод привел его к разработке квантовой теории строения атома водорода в качестве первого шага и далее — к построению формальных моделей атомов всех элементов периодической системы. Применив к атомной теории постоянную Планка, Бор сформулировал два основных постулата 1) атом может существовать, не излучая, в определенных стационарных состояниях, характеризующихся определенными [c.247]
Первым основополагающим достижением в области изучения внутреннего строения вещества было создание модели атома английским физиком Резерфордом (1911 г.). По Резерфорду атом состоит из ядра, окруженного электронной оболочкой. Выдающийся датский физик теоретик Вор использовал представления Резерфорда и созданную немецким физиком Плаиком (1900 г.) квантовую теорию для разработки в 1913 г. теории водородоподобного атома и первой квантовой модели атома модель атома Бора, см. 4.5). Приняв, что электроны — это частицы, он описал атом как ядро, вокруг которого на разных расстояниях движутся по круговым орбитам электроны. Б 1916 г. модель атома Бора была усовершёиствована немецким физиком Зоммерфель-дом, который объединил квантовую теорию Планка и теорию относительности Эйнштейна (1905 г.), создав квантовую теорию атомных орбит, которые по Зоммерфельду, могут быть не только круговыми, но и эллиптическими. [c.77]
Атом элемента представляет собой одну из важнейших микрочастиц. Первые исследователи ее строения (Н.Бор, А. Зоммерфельд, 1912, 1913) положили в основу внутриатомной энергетики представления теории квант. Электромагнитное поле атомного ядра квантовано, т. е. имеет дискретное строение в самой природе структуры атома заложены определенные энергетические уровни. В соответствии с ними электрон, рассматриваемый как частица, согласно теории Бора, движется вокруг ядра по круговым или эллиптическим орбитам, напоминая движение планет вокруг Солнца. Так возникла планетарная модель атома. Форма траекторий-орбит и их расстояние от ядра рассматривались как фактор, определяющий энергетическое состояние электрона. Энергетические уровни обозначались как главные кванто- [c.31]
Преимущество метода МО над методом валентных связей состоит очевидно в том, что в основе первого лежит модель, которая в известной степени правильно передает внутреннее строение химических соединений. Клементи следующим образом характеризует преимущества метода МО он использует расчетную методику, которая может быть апробирована на примерах атомов. Электронная теория молекул принципиально и практически должна быть применима к предельному случаю — атому. Электроны не меняют своей природы при переходе от атомов к молекулам И для описания различных [c.90]
Открытие субатомных частиц и первые модели атома. В 1897 г. Дж. Томсон (Англия) открыл электрон, а в 1909 г. Р. Малликен определил его заряд, который равен 1,6-10 Кл. Масса электрона составляет 9,1 М0 г. В 1904 г. Дж. Томсон предложил модель строения атома, согласно которой атом можно представить в виде положительно заряженной сферы с вкрапленными электронами. [c.17]
Говоря о первоначальных атомных моделях, мы должны отметить весьма любопытное обстоятельство, на которое мало обращали внимание историки учения о строении вещества. Именно, еще в 1901 г. Ж. Перреп опубликовал работу Ядерно-планетарная структура атома [20]. Согласно Перрену, атом должен состоять из положительно заряженного ядра, окруженного отрицательными электронами, которые двигаются по определенным орбитам , со скоростями, соответствующими частотам световых волн . Иными словами, Перрен предвосхитил основные структурные моменты будущей резерфордовской модели атома. Однако идея Перрена оказалась явно не своевременной, она не нашла, да и не могла вызвать никакого резонанса. Во-первых, потому, что был совершенно неясен вопрос о носителе положительного заряда в атоме (никаких прямых или косвенных экспериментальных данных на сей счет не существовало) во-вторых, модель Перрена противоречила представлениям классической электродинамики (это противоречие имело место и в резерфордовской модели, но оно было своевременно преодолено Н. Бором, применившим к строению атомов планковскую гипотезу о квантах). [c.237]
Для достаточно полного обзора экспериментального материала по конформациям органических молекул, по-видимому, не хватит объема даже большой книги. Поэтому имеет смысл обсудить лишь обш,ие принципы и основные закономерности, характеризующие конформационные особенности молекул различных классов. Рассмотренная в предыдущей главе механическая модель обладает достаточной общностью, чтобы на ее основе можно было бы понять конформации молекул самого разного химического строения. Но как бы ни было построено изложение, пропуск большого числа экспериментальных данных неизбежен. Во-первых, не во всех молекулах геометрия определяется взаимодействиями, описываемыми атом-атом потенциалами в металлоорганических соединениях, например, большую роль играют слабые взаимодействия типа координационных связей. Во-вторых, если включить в рассмотрение все молекулы, к которым приложимы общие принципы конформационного анализа, то изложение могло бы вырасти до непомерных размеров. Поэтому за пределами нашего внимания остаются такие интересные органические системы, как стероиды, биологически активные молекулы типа ацетилхолина, никотина и некоторые другие. [c.146]
Строение хлорангидридов фосфиновых кислот (ЬХХХУП) доказано химическими и физическими способами [109, 706, 1035]. На основании данных хроматографии и спектров ПМР показано, что реакция этинилвиниловых эфиров, и тиоэфиров с пятихлористым фосфором в описанных условиях протекает стереоспецифично и приводит к образованию аддуктов, у которых атомы водорода при первом и втором атомах углерода находятся в транс-расположении. Ввиду того, что исходные этинилвиниловые эфиры и тиоэфиры имеют г г/с-конфигурацию, допускается, что цис — тракс-изомеризация происходит в ходе реакции присоединения пятихлористого фосфора [109]. Возможно, что реакция осуществляется путем электрофильной атаки РС14 [1037] на тройную связь с последующим переходом аниона хлора к третьему атому углерода внутри образовавшегося катиона. Последний стабилизован показанными на схеме электронными сдвигами и поэтому утратил геометрическую конфигурацию исходного бутенина. Атом хлора вступает в наиболее выгодное стерическое положение, что приводит к т >акс-расположению водородных атомов при 1,2-двойной связи. Высказанные соображения подтверждаются при построении атомной модели Бриглеба — Стюарда исследованных соединений, причем наиболее благоприятным является трйнс-размещение атома хлора и фосфонильной группы [c.308]
Одна из первых моделей строения атома была предложена Дж. Томсоном в 1903 г. Атом представлялся как море положительного электричества с колеблющимися в нем электронами. Суммарный отрицательный заряд электронов электронейтрального атома приравнивался его суммарному положительному за-рядз. [c.38]
Томсон в 1904 г. математически разработал аналогичную модель атома. Его статья имеет очень выразительное заглавие О строении атома исследование устойчивости и периодов колебания совокупности корпускул, расположенных с равными интервалами по окружности круга с применением результатов к теории атомного строения [2]. Согласно Томсону, положительный заряд атома распределен равномерно по всему его объему, тогда как корпускулы (так Томсон называет электроны) занимают внутри атома некоторое определенное положение. Томсон показывает расчетом, что такая модель атома может быть устойчива лишь при расположении корпускул либо в серии концентрических колец (если корпускулы вынуждены двигаться в одной плоскости), либо в ряде концентрических сфер (если допустить, что они могут двигаться во всех направлениях). Стабильность кольца (или сферы) достигается только при определенном числе корпускул в них в этом случае атом не способен удерживать дополнительно ни положительный, ни отрицательный заряд. Распределив все атомы в ряд (следуя порядку увеличения числа корпускул), мы получим сначала систему, которая ведет себя подобно атому одновалентного электроположительного элемента следующая система ведет себя подобно атому двухвалентного электроположительного элемента, в то время как на другом конце ряда у нас имеется система, которая ведет себя подобно нульвалентному атому ей непосредственно предшествует система, которая ведет себя подобно атому одновалентного электроотрицательного элемента, тогда как ей в свою очередь предшествует система, ведущая себя подобно атому двухвалентного электроотрицательного элемента [там же, стр. 262]. С глубокой проницательностью Томсон проводит далее аналогию между таким накоплением корпускул и свойствами элементов в двух первых периодах от гелия до неона и от неона до аргона. [c.29]
До 1912 г. выдвигались модели строения атома, которые были лишь частично удовлетворительными. Томсоновская модель, согласно которой атом должен быть похож на арбуз, представляла собой первую попытку как-то описать положение электронов в атоме, но эта модель не позволяла объяснить многие свойства атомов. Резерфорд выдвинул модель атома, предполагающую вращение электронов вокруг ядра по орбитам (рис. 5.2). Если обозначить заряд электрона q , а заряд протона (ядра атома водорода) массу электрона т и радиус орбиты г, то выполняется условие [c.68]
Как же расположены все эти частицы внутри атома Представляет ли атом беспорядочную смесь частиц или же строение его строго определенное Первая попытка ответить на этот вопрос была сделана Дж. Томсоном. Он предположил, что атом представляет собой миниатюрный шар, внутри которого равномерно распределено положительное электричество, а также расположены электроны. Эта модель, получившая название пудинга с изюмом , продержалась очень короткое время. [c.226]
Модель атома водорода, предложенная Н. Бором (1913 г.), является первой попыткой количественного изображения строения и внутреннего механизма атома, поясняющая все экспериментальные данные, главным образом частоты линий испускаемых спектров. Атом водорода изображен в виде солнечной системы в миниатюре, в которой солнде представлено протоном с элементарным зарядом -fe, а планета — электроном с элементарным зарядом —е, вращающимся вокруг протона по круговой орбите радиуса г. Согласно закону Кулона, между этими двумя частицами развивается сила притяжения В своем дви- [c.57]
В общем, энергия деформации валентного угла столь незначительна, что отклонения порядка 0° могут быть вызваны уже тепловой энергией. Это означает, что даже столь высокосимметричные молекулы, как метан, постоянно обнаруживают относительно большие отклонения от симметричного положения равновесия. Однако это не может служить поводом для отказа от тетраэдрической модели атома углерода . Свойственное атому углерода стремление к регулярно-тетраэдрическому расположению при использовании его четырех связей, 5р -гибридизацию, следует рассматривать как основной принцип пространственного строения всех соединений углерода. Важнейшим и исторически первым доказательством этого служит явление оптической активности, изложению которой посвящен следуюищй раздел. [c.83]
Модель атома водорода, предложенная Н. Бором (1913 г.), является первой попыткой количественного изображения строения и внутреннего механизма атома, поясняющая все экспериментальные данные, главным образом частоты линий испускаемых спектров. Атом водорода изображен в виде солнечной системы в миниатюре, в которой солнце представлено протоном с элементарным зарядом – -е, а планета — электроном с элементарным зарядом —е, вращающимся вокруг протона по круговой орбите радиуса г. Согласно закону Кулона, между этими двумя частицами развивается сила притяжения е 1г . В своем движении по орбите электрон остается в равновесии благодаря центробежной силе, которая долнша равняться силе притяжения между частицами, следовательно, [c.57]
chem21.info
Строение атома. Атомная физика :: Класс!ная физика
СТРОЕНИЕ АТОМА
Модель атома Томсона
1897 г.- Дж. Томсоном выдвинута модель строения атома.
Атом имеет форму шара. По всему объему атома с постоянной плотностью распределен положительный заряд. Внутри (как изюм в кексе) расположены электроны.
В целом атом электрически нейтрален.
Когда электроны колеблются относительно центра сферы, атом излучает свет.
Опыт Резерфорда по рассеянию альфа-частиц
1906 г. – Э. Резерфорд проводит опыты для проверки состоятельности модели атома Томсона:
В вакууме в свинцовом стакане располагался источник радиоактивного излучения (альфа-частиц) – полоний(Ро).
Тонкая золотая фольга бомбардировалась положительно заряженными альфа-частицами, скорость которых около 20 ООО км /с.
На экране регистрировались вспышки от попадания на него альфа-частиц.
Кроме основного экрана следы от альфа-частиц были зафиксированы и на боковых экранах.
Зная о том, как взаимодействуют одноименно заряженные частицы, а они отталкиваются друг от друга, можно объяснить результаты опыта Резерфорда:
– частицы, которые отклонялись, пролетали недалеко от ядра
– частицы, которые отражались, попадали точно в ядро
– частицы, которые не испытывали отклонений, пролетали далеко от ядра
Понимание причин отклонения альфа-частиц позволило Э.Резерфорду выдвинуть собственную планетарную (иначе ядерную) модель строения атома.
Атом по Резерфорду
– это положительно заряженное ядро в центре атома и электроны на орбитах вокруг ядра
– характер движения электронов определяется действием кулоновских сил со стороны ядра
– диаметр ядра в 100000 раз меньше диаметра атома
– масса ядра составляет 99,4% от массы всего атома
– заряд ядра составляет 99,4% от заряда всего атома
– заряд ядра по модулю равен сумме зарядов электронов, поэтому атом в целом нейтрален.
Однако, возникли противоречия между законами классической механики и электродинамики и предложенной Резерфордом моделью атома:
1. Согласно классической механике по модели атома Резерфорда атомы должны быть неустойчивы, т.к.:
электроны движутся по орбитам с ускорением, поэтому должны излучать электромагнитные волны
излучая, должны терять энергию
в результате должны упасть на ядро
тогда атом должен прекратить свое существование.
Однако, реальные атомы устойчивы и в невозбужденном состоянии могут существовать неограниченно долго, не излучая электромагнитные волны.
2. По законам классической электродинамики, электрон, приближаясь к ядру, должен двигаться все быстрее, излучая все более короткие электромагнитные волны, поэтому спектр излучения атома должен быть сплошным.
Однако, у реальных атомов спектр излучения является линейчатым.
Вспомни тему “Атомная физика” за 9 класс:
Радиоактивность.
Радиоактивные превращения.
Состав атомного ядра. Ядерные силы.
Энергия связи. Дефект масс.
Деление ядер урана.
Ядерная цепная реакция.
Ядерный реактор.
Термоядерная реакция.
Другие страницы по теме “Атомная физика” за 10-11 класс:
Строение атома
Квантовые постулаты Бора
Методы регистрации частиц
Естественная радиоактивность
Радиоактивный распад
Закон радиоактаивного распада
Ядерные силы
Открытие электрона
Открытие протона
Открытие нейтрона
Строение ядра атома
Изотопы
Энергия связи ядра
Ядерные реакции
Деление ядер урана. Цепная реакция
Ядерный реактор. Атомная бомба
Термоядерная реакция
Водородная бомба
Топливные ресурсы. Ядерная энергетика
А ЗНАЕТЕ ЛИ ВЫ?
Атом – именно это понятие было введено древнегреческим ученым Левкиппом для обозначения мельчайших единиц бытия.
____
Демокрит – один из основателей античной атомистики считал, что атомы – это неделимые материальные геометрические тела, вечные, неразрушимые, непроницаемые, различаются формой, положением в пустоте, величиной. По Демокриту атомы неделимы физически, но мысленно в них можно выделить части – точки, которые нельзя отторгнуть, они не имеют своего веса, но они тоже являются протяженными. Это минимальная величина, дальше неделимая, мысленная часть атома – “амера” (бесчастная). В самом мелком атоме, по мнению Демокрита, было семь амер: верх, низ, левое, правое, переднее, заднее, середина.
____
В 1903 году английский физик Джозеф Джон Томсон разработал “модель атома”, согласно которой атом – “сфера однородной положительной электризации”, в которую вкраплено определенное количество электронов, нейтрализующих положительный заряд. Эту модель сравнили с одним из традиционных атрибутов Англии – с пудингом. Электроны подобны изюминкам в пудинге.
____
Английский физик Э. Резерфорд в 1911 году уже знал это, но на Сольвеевском конгрессе в Брюсселе промолчал, так как это свидетельствовало о катастрофе. Через два года он получил пакет от датского физика Нильса Бора из Копенгагена, который подтвердил правильность его открытия. Их современник, оценивая сложившуюся ситуацию, писал: “Это было так, точно из-под ног ушла земля, и нигде не было видно твердой почвы, на которой можно было строить…”.
Речь идет о планетарной модели атома Э. Резерфорда и об открытиях Н. Бора, все это свидетельствовало о катастрофе классической физики!
___
Нильс Бор писал: «Перед нами – безумная теория. Вопрос в том, достаточно ли она безумна, чтобы быть верной?»
class-fizika.narod.ru
