Натрий. Строение атома натрия
Разнообразен и интересен мир металлов. Их свойства издавна изучались человеком, и нашу жизнь просто невозможно представить без таких элементов, как железо, алюминий, хром. В нашей статье речь пойдет о натрии.
Строение атома натрия, расположение электронов по энергетическим уровням определяют его главные характеристики. К ним, например, относятся такие показатели, как высокая химическая активность, пластичность, способность проводить тепло и электрический ток.
Но особое внимание стоит уделить рассмотрению строения элементарной частицы химического элемента натрия – его атома.
Самые активные и агрессивные
Щелочные металлы, к которым относится натрий, в химии по праву считаются самыми реакционно-способными. Именно поэтому ни один из них, в том числе и натрий, не встречается в природе как самородок, а находится в ионном виде в составе горных пород и минералов.
К ним относится поваренная соль, сильвинит и карналлит. Чем же можно это объяснить?
Ответ лежит в особенностях строения атома натрия. Элемент, как и его собратья по подгруппе щелочных металлов, имеет большой радиус атома. Кроме того, его единственный электрон, расположенный на последнем энергетическом уровне, слабо связан с положительно заряженным ядром. Поэтому он легко отрывается от самого атома и захватывается частицами других химических элементов. Эта способность – легко отдавать собственные электроны – и определяет все главные свойства металлических элементов.

Электронное строение атома натрия
Полная формула, показывающая распределение электронов по энергетическим уровням в атоме, имеет следующий вид: 1s22s22p63s1.
Последний неспаренный электрон, при вращении образующий облако в виде сферы, находится на значительном удалении от собственного ядра. Он участвует в возникновении такого типа связи, как ионное взаимодействие, и называется валентным.
Радиус самого атома составляет около 0,189 нм, а энергия его ионизации равна 5,14 эВ. Благодаря такому строению атома элемента натрия, его простое вещество проявляет хорошо выраженные восстановительные свойства, то есть в реакциях с атомами других элементов всегда отдает свой единственный электрон, расположенный на последнем энергетическом уровне (третий).
При этом электронейтральная частица натрия превращается в положительно заряженный ион – катион. Ярко выраженные восстановительные свойства металла и его химическая активность предъявляют особые требования к условиям его хранения. Чтобы металл не окислялся кислородом воздуха, его сберегают под слоем технического масла или керосина. Электронная схема атома натрия имеет следующий вид (см. фото ниже).
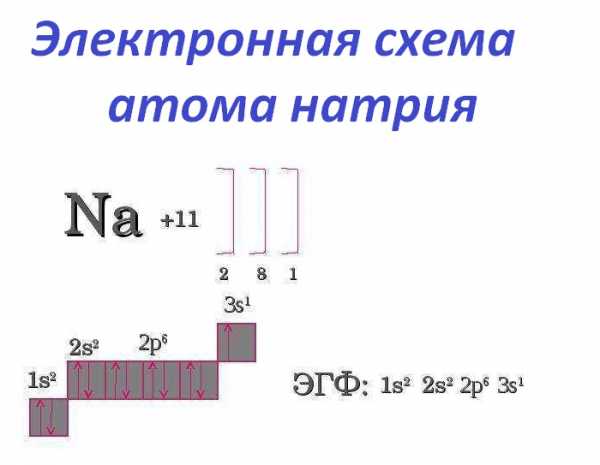
Физические свойства
Какова же зависимость между электронной формулой и физическими свойствами натрия? Строение атома натрия раскрывает эту взаимосвязь.
Природный Na состоит только из одного изотопа. Он представляет собой очень мягкий серебристо-белый металл, который можно резать ножом. Его плотность составляет всего 0,97 г/см.
Как и другие металлы, натрий хорошо проводит электрический ток и тепло. Поскольку в подгруппе щелочных металлов радиусы атомов и их свойства как восстановителей с увеличением заряда ядра увеличиваются, то температуры кипения и плавления будут уменьшаться.
Как строение атома влияет на химические свойства элемента?
Продолжим изучение строения атома натрия. Натрий содержит на третьем энергетическом уровне один электрон, электронное облако которого имеет форму сферы. Поэтому металл относят к s-элементам, а они, как известно, легко вступают в химическое взаимодействие с неметаллами, например с кислородом, водородом, серой, азотом и т. д. Реагируя с водой, натрий быстро растворяется в ней, образуя раствор щелочи.

Высокая активность щелочного металла натрия выражается в особенностях его взаимодействия с кислотами, которая сопровождается взрывом. Поэтому такую реакцию в лабораторных условиях проводить запрещено. Еще одна особенность металлического натрия заключается в том, что он не реагирует с растворами солей и щелочей, так как сам начинает активно взаимодействовать с растворителем – водой.
Так что, как можно видеть, строение атома натрия, а также его взаимосвязь с физическими и химическими свойствами элемента, действительно представляют собой научный интерес.
fb.ru
Схема электронного строения атома натрия
Схема электронного строения атома натрия имеет вид:
Гидриды щелочных металлов разлагаются на элементы до плавления. Все они кристаллизуются в структуре NaCl и являются сильными восстановителями. При непосредственном взаимодействии компонентов в вакууме образуются сульфиды . Они представляют собой бесцветные кристаллы, хорошо растворимые в воде и спирте. В водном растворе они, как и сульфид лития, подвергаются гидролизу с образованием гидроксидов и гидросульфидов щелочных металлов. Под действием кислорода воздуха медленно окисляется до тиосульфата:
Кроме того, щлочные металлы образуют полисульфиды. Селениды и туллуриды щелочных металлов получают сплавлением компонентов в вакууме. В воде они разлагаются с выделением селена и теллура, например
Нитриды щелочных металлов образуются при взаимодействии паров металлов с возбужденными атомами азота (тлеющий разряд). Они гигроскопичны и энергично взаимодействуют с водой:
ru.solverbook.com
Строение электронных оболочек атома
Быть может, эти электроны –
Миры, где пять материков,
Искусство, знания, войны, троны
И память сорока веков.
Вспомним, из чего состоит атом. Помните планетарную модель строения атома, согласно которой, в центре атома расположено положительно заряженное ядро, вокруг которого вращаются отрицательно заряженные электроны, подобно тому, как вращаются планеты вокруг Солнца.
Строение атома
Электроны, двигаясь вокруг ядра, в совокупности образуют электронную оболочку атома. Число электронов в атоме равно числу протонов в ядре и соответствует порядковому номеру элемента.
Электроны двигаются в определённом порядке и различаются своей энергией. Электроны с маленьким запасом энергии расположены ближе к ядру, они связаны крепко с ядром и их тяжелее вырвать из электронной оболочки. А вот электроны с большим запасом энергии, напротив, находятся дальше от ядра, слабо с ним связаны, поэтому их легче оторвать.
Несмотря на это, в атоме находятся электроны, которые имеют близкие значения энергии. Эти электроны образуют
Чтобы определить число энергетических уровней, достаточно знать номер периода, в котором находится данный элемент. Например, у азота семь электронов в атоме, и два энергетических уровня. Теперь распределим эти семь электронов по уровням. Получается на первом их 2, а на втором – оставшиеся 5.
Максимальное число электронов на энергетическом уровне определяется по формуле: 2n2, где n – номер периода.
Если подставить значения первых трех периодов, то получится, что
Число электронов на внешнем энергетическом уровне для элементов главных подгрупп равно номеру группы.
Рассмотрим это на примере атома натрия.
Ядро атома натрия имеет заряд +11, т.е. и электронов в атоме тоже 11. Натрий находится в третьем периоде, значит, у него три энергетических уровня, которые мы будем изображать в виде скобки «)». Это записывают с помощью электронной формулы следующим образом: 11Na 2ē, 8ē, 1ē.
И так, на первом уровне 2 электрона (это максимально), на втором – 8 (больше быть не может), а на третий остается один электрон. Вот этот электрон и будет электроном внешнего энергетического уровня. Натрий –
Двигаясь, электроны образуют своеобразный рисунок, так называемое электронное облако, которое можно ещё назвать орбиталью. Электронное облако, или орбиталь, – пространство вокруг ядра, где наиболее вероятно нахождение данного электрона.
На всех энергетических уровнях есть s-орбитали, они сферической формы, и она только одна, на втором уровне уже появляются
Для того, чтобы записать электронную формулу атома, для обозначения уровня используют арабские цифры, орбитали соответственно буквами s и р, а число электронов данной орбитали – арабской цифрой сверху справа над буквой орбитали.
Например, азот будет иметь электронную формулу 1s22s22p3.
Если элементы имеют одинаковое число электронов на внешнем уровне, значит, у них будут схожие свойства. Вспомните, благородные газы – инертны, не вступают в химические реакции, ведь у них, кроме гелия, восемь электронов на внешнем уровне, который считается завершенным. Вот почему они все инертны.
videouroki.net
Строение атома азота (N), схема и примеры
Общие сведения о строении атома азота
Порядковый номер равен 7. Заряд ядра равен +7. Атомный вес – 14,007а.е.м. В природе встречаются два изотопа азота: 14N — 99,635 % и
Электронное строение атома азота
Атом азота имеет две оболочки, как и все элементы, расположенные во втором периоде. Номер группы –V – свидетельствует о том, что на внешнем электронном уровне атома азота находится 5 валентных электронов.

Рис. 1. Схематичное строение атома азота.
Электронная конфигурация основного состояния записывается следующим образом:
1s22s22p3.
Азот – элемент p-семейства. Энергетическая диаграмма для валентных электронов в невозбужденном состоянии выглядит следующим образом:
Возбужденного состояния нет. По числу неспаренных электронов можно сказать, что азот в соединениях проявляет валентность III. Однако, валентность так же определяется по номеру группы (V), следовательно, азот может проявлять две валентности – III и V.

Рис. 2. Пространственное изображение строения атома азота.
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |||
ru.solverbook.com
